Изобретение относится к медицине, в частности фармакологии, и может быть использовано в клинической практике для лечения злокачественных новообразований.
Современная медицина располагает достаточно обширным арсеналом лекарственных препаратов для химиотерапии опухолей. В основном химиотерапевтические средства представлены группой цитостатических препаратов, среди которых наиболее распространенными и эффективными являются алкилирующие цитостатики типа циклофосфана, хлорбутина и сарколизина. Из-за более низкой цитостатической, антипролиферативной активности в меньшей степени применяются препараты из группы антиметаболитов (азатиоприн, фторурацил и др.). Природные противоопухолевые препараты растительного (колхицин и др.) и бактериального (рубромицин и др.) происхождения имеют также ограниченное применение из-за высокой токсичности и узкого терапевтического спектра действия (лечение некоторых разновидностей опухолей, преимущественно с экзофитным ростом). В настоящее время на фармацевтическом рынке противоопухолевых препаратов отсутствуют лекарственные средства, обладающие комплексным фармакологическим действием, а именно обладающие собственной противоопухолевой активностью в сочетании с радиопротекторным и антитоксическим действием при проведении комплексной химиотерапии, преимущественно с использованием алкилирующих цитостатиков и рентгенотерапии опухолей.
Известно использование алкилирующих цитостатиков типа циклофосфана, имеющих широкий терапевтический спектр для терапии наиболее распространенных злокачественных новообразований: рака легкого, рака молочной железы, сарком, рака яичников и др. (М.Д.Машковский Лекарственные средства, ч.II, М., Медицина, 1993, с.498-499; с.501-502). Недостатком данных препаратов является их высокая токсичность и угнетающее влияние на лейкопоэз. Развитие лейкопении является опасным осложнением в терапии злокачественных новообразований цитостатиками, так как создает угрозу развития кровотечений, снижения иммунологической резистентности и распространения суперинфекции. Практически любая инфекция на фоне проведения цитостатической терапии, например циклофосфаном или сарколизином, может вызвать септические осложнения, которые практически не поддаются лечению современными антибактериальными препаратами, так как отсутствуют клеточные и гуморальные механизмы естественной резистентности из-за подавления цитостатиками.
В настоящее время наиболее эффективным способом при лечении солидных опухолей является рентгенотерапия (Е.Браунвальд, Внутренние болезни, 2 т., М., Медицина, 1993, с.501-505), однако она обладает также значительным процентом осложнений, прежде всего связанных с иммуносупрессией, подавлением белого ростка крови и развитием суперинфекции.
Наиболее близким к заявляемому препарату - прототипом является препарат “Дезоксинат”, представляющий собой натриевую соль двухспиральной дезоксирибонуклеиновой кислоты, получаемую из молок осетровых рыб и частично деполимеризованную с помощью ультразвука до молекулярной массы 2,7-4,0×105 дальтон. Содержание ДНК в препарате более 90%, в качестве примесей в препарате присутствуют РНК (от 3 до 5%) и белки негистонового типа, связанные с ДНК (ФС 42-3922-00). Препарат обладает антитоксическим и радиопротекторным действием и используется в качестве стимулятора лейкопоэза при химиолучевой терапии, проводимой онкологическим больным. Препарат выпускается в виде 0,5% раствора и предназначен для подкожного и внутримышечного введения из расчета 75 мг активного вещества независимо от возраста больного.
Недостатками “Дезоксината” являются
- содержащаяся в “Дезоксинате” ДНК не имеет видовой специфичности, гетерологична и поэтому может вызывать аллергические и пирогенные реакции, которые проявляются в виде повышения температуры. По этой причине препарат не может быть введен внутривенно, ввиду возможного развития анафилактического шока, часто наблюдающегося при внутривенных инфузиях видонеспецифичных биологических субстанций.
- “Дезоксинат” не обладает собственной противоопухолевой активностью и поэтому применяется лишь в качестве вспомогательного лейкостимулирующего препарата для профилактики миелодепрессий при химиолучевой терапии онкологических больных. При этом лейкостимулирующий эффект развивается медленно и стойкие изменения наблюдаются через 4-10 дней. Радиопротекторный эффект “Дезоксината” носит непрямой характер и направлен на коррекцию лейкопении и стимуляцию иммунитета, развивающиеся при острой лучевой болезни II-III степени тяжести.
Технической задачей настоящего изобретения является создание препарата из видоспецифичного сырья, обладающего противоопухолевым, антитоксическим и радиопротекторным действием.
Поставленная техническая задача достигается предлагаемым препаратом на основе фрагментированного до 200-2000 пар нуклеотидов нуклеопротеидного комплекса, выделенного из плаценты человека, содержащего, мас.%:
двухспиральную ДНК 60-80
белки ядерного матрикса 20-40
Заявляемый препарат получают следующим образом.
Плаценту от здоровых рожениц, проверенную на гепатит, ВИЧ-инфекцию и сифилис, замораживают и хранят при -20°С в отдельном стерильном полиэтиленовом пакете, сопровождаемом санитарно-гигиеническим паспортом, до момента получения препарата (условное название “Панаген”), но не более 1 года с момента заготовки.
После накопления требуемого количества, плаценту размораживают в течение 5-6 часов, промывают, гомогенизируют в 10 мМ трис-НСl буфере (рН 7,5), содержащем 1 мМ ЭДТА. В полученный гомогенат добавляют додецилсульфат натрия до конечной концентрации 2% и инкубируют при 65°С в течение 6-24 часов. К полученному лизату добавляют хлорид натрия до конечной концентрации 2 М и инкубируют в течение 3-12 часов при 65°С. После инкубации лизат центрифугируют при 9000 g в течение 10 минут. К полученному супернатанту добавляют равный объем ацетона, охлажденного до +10°С, для осаждения нуклеопротеидного комплекса (НПК). Полученный НПК трижды промывают охлажденным ацетоном и 96° этиловым спиртом для удаления несвязанных с ДНК низкомолекулярных белков и пептидов. Очищенный НПК растворяют при 65°С в 10 мМ трис-НСl буфере (рН 7,5), содержащем 1 мМ ЭДТА, затем раствор центрифугируют при 9000 g в течение 10 минут, супернатант фильтруют через стеклянный фильтр с диаметром пор 120 мкм и воздействуют на него ультразвуком с частотой 11-44 кГц для фрагментации НПК. Выход целевого продукта составляет 0,3-0,5% от исходного сырья, содержание основного вещества (нуклеопротеидного комплекса) составляет 95,0-99,5%. Молекулярная масса нуклеопротеидного комплекса 1,5х106 дальтон. Глубину фрагментации контролируют с помощью электрофореза и по достижении необходимого диапазона в пределах 200-2000 пар нуклеотидов процесс воздействия ультразвуком останавливают. Раствор фрагментированного НПК центрифугируют при 9000 g в течение 10 минут, затем добавляют двукратный объем охлажденного 96° этилового спирта. Осажденный НПК промывают 70° этиловым спиртом и после его высушивания получают заявляемый препарат.
Перед использованием препарат растворяют в фармацевтически приемлемом растворителе до содержания основного вещества 0,5-4,0%. В качестве фармацевтически приемлемого растворителя используют преимущественно фосфатную или трис-HCL буферную смесь, физиологический раствор.
Определяющими существенными отличиями заявляемого препарата от препарата-прототипа являются
- заявляемый препарат содержит нативный, видоспецифичный фрагментированный нуклеопротеидный комплекс, состоящий из д.с. ДНК и связанных с ней белков ядерного матрикса, при соотношении: д.с. ДНК 40-80%, белки 20-60%, что позволяет расширить спектр терапевтической активности препарата: последний обладает собственной противоопухолевой активностью в сочетании с прямым радиопротекторным и антитоксическим действием (лейкостимулирующим);
- за счет определенной глубины фрагментации нуклеопротеидного комплекса (200-2000 пар нуклеотидов), заявляемый препарат можно отнести к нативным препаратам, содержащим полный набор фрагментов генома человека и, соответственно, при терапии онкологических заболеваний у человека препарат обладает заместительной, рецепторно-опросредованной, генно-репаративной функцией, а также анаболической и трофической. В прототипе степень фрагментации выше (молекулярно массовое распределение находится в интервале 2,7-4,0×105 дальтон), что делает препарат более удаленным от нативных препаратов, содержащих фрагменты генома, к тому же биологическое сырье невидоспецифично, гетерологично и, соответственно, при терапии онкологических заболеваний у человека функция препарата будет лишь анаболической или трофической;
- заявляемый препарат ввиду видоспецифичности и гомологичности биологического материала (плацента человека) может вводиться внутривенно, благодаря чему лейкостимулирующий эффект при сочетании с химиотерапией цитостатиками развивается быстрее и более выражен.
Известны препараты из плаценты человека, применяемые для стимуляции процессов регенерации раневых поверхностей различной этиологии, а также используемые для лечения язвенной болезни желудка, преимущественно в виде экстрактов для внутримышечных и подкожных инъекций (Машковский М.Д. Лекарственные средства. Ч.I, Ч.II. - 12-е изд., перераб., испр. и доп. - М., 1996). Однако из доступных источников не обнаружено сведений о препарате, аналогичном заявляемому, обладающему вышеназванной комплексной фармакологической активностью.
Противоопухолевая активность заявляемого препарата исследована на модели in vivo. Линейно-специфическую опухоль ГА-1, поддерживаемую в асцитной форме на мышах линии A/Sn трансплантировали внутримышечно (10 опухолевых клеток) сингенным мышам A/Sn. Через 6 дней этим же мышам в течение 11 дней вводили внутрибрюшинно заявляемый препарат, полученный из плаценты человека и НПК, полученный из печени мышей линии СВА, контролем служил физиологический раствор. Экспериментальные животные были разделены на группы:
1-я группа. Контрольные мыши, введение физиологического раствора.
2-я группа. Экспериментальные мыши, введение НПК из плаценты человека (доза 0,5 мг на мышь ежедневно).
3-я группа. Экспериментальные мыши, введение НПК из печени мышей линии СВА (доза 0,5 мг на мышь ежедневно).
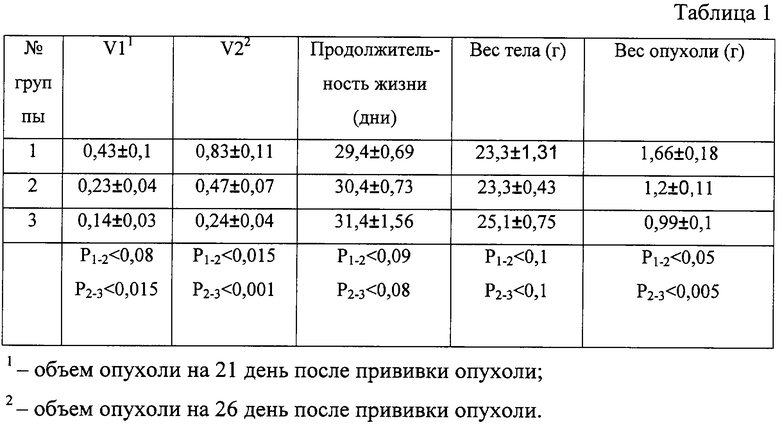
Как видно из представленных данных, заявляемый препарат из плаценты человека и НПК из печени мышей обладают противоопухолевым действием, однако противоопухолевое действие заявляемого препарата имеет видоспецифичность и более выражено.
Радиопротекторная активность заявляемого препарата исследована на модели in vivo. 4-х месячных самок мышей СВА облучали на гамма-установке дозой облучения 980 рад. 4 группы мышей облучали одновременно в одном контейнере. Каждая группа состояла из 10 животных:
1. 1-я группа. Контрольные мыши.
2. 2-я группа. Мыши, которым за 30 минут до облучения внутрибрюшинно вводили по 1 мг НПК, полученного из печени мышей линии СВА.
3. 3-я группа. Мыши, которым через 30 минут после облучения внутрибрюшинно вводили по 1 мг НПК, полученного из печени мышей линии СВА, а на второй и третий день после облучения - в дозе 0,5 мг.
4. 4-я группа. Мыши, которым через 30 минут после облучения внутрибрюшинно ввеодили по 1 мг НПК, полученного из плаценты человека (заявляемая композиция), а на второй и третий день после облучения - в дозе 0,5 мг.
Полученные результаты представлены в таблице 2.
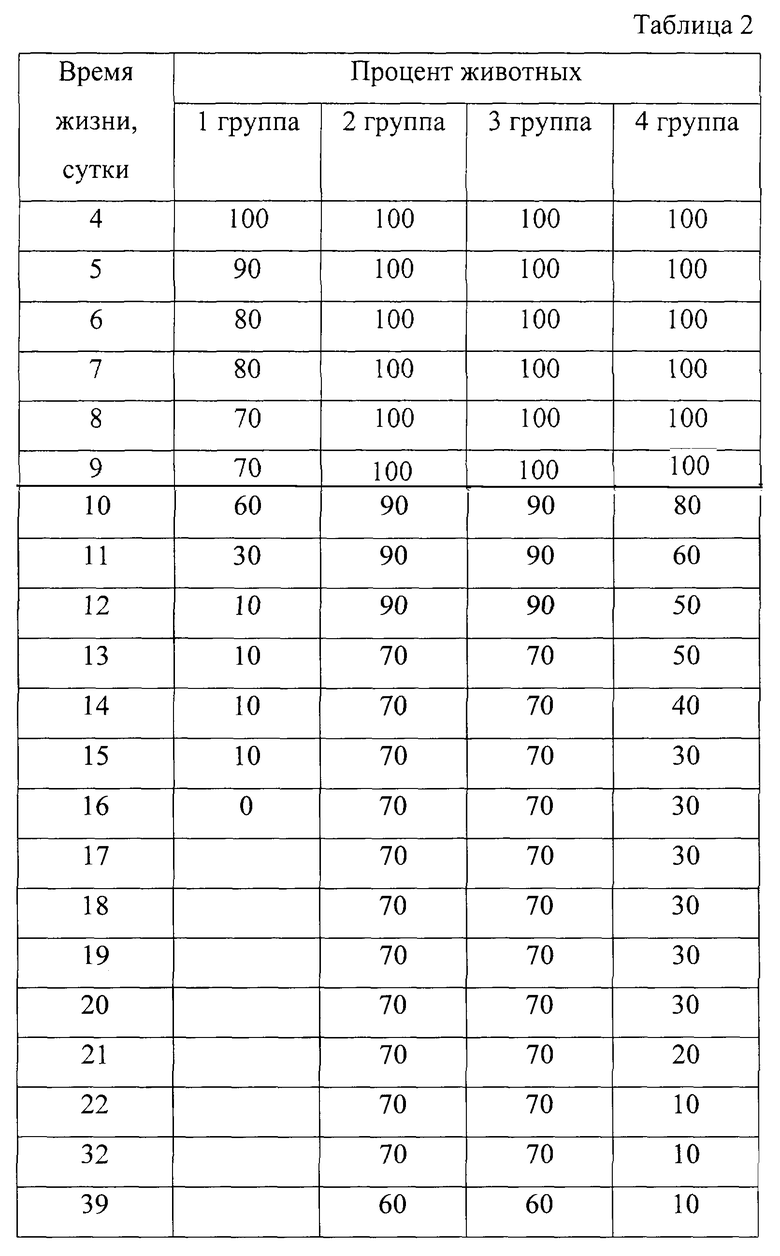
Из табл.2 видно, что заявляемый препарат обладает лечебным радиопротекторным действием, направленным на снижение пострадиационных биологических эффектов (введение препарата после облучения). Радиопротекторные свойства заявляемого препарата зависят от видовой специфичности НПК и максимальны при использовании для его выделения гомологичного биологического сырья.
Антитоксические свойства заявляемого препарата исследованы на модели восстановления количества лейкоцитов, получавших цитостатикцик-лофосфан.
Методика
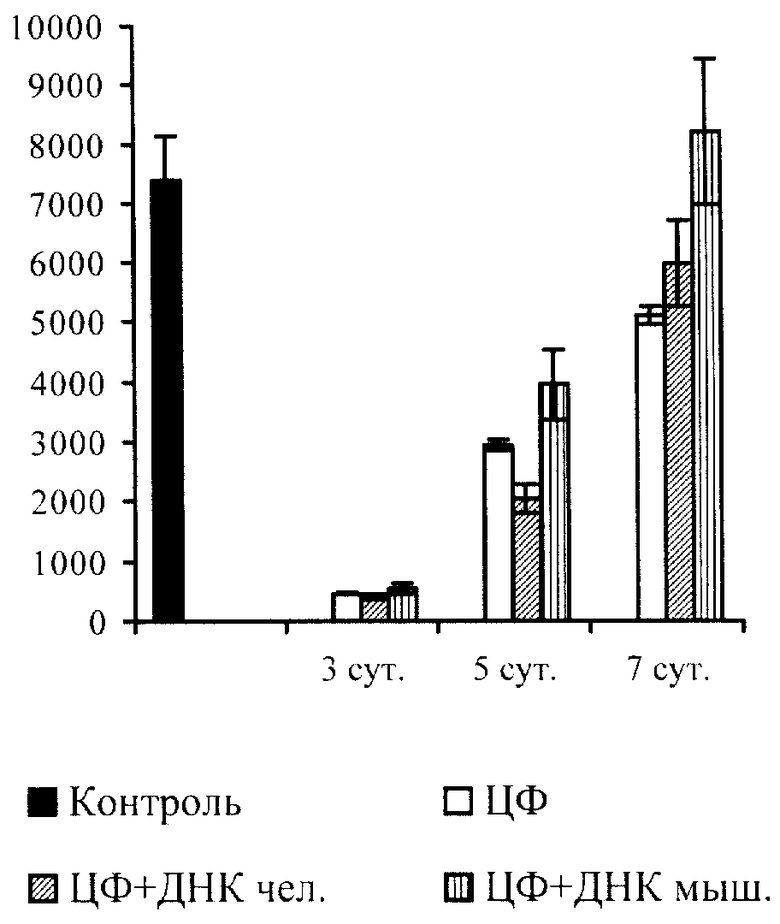
Мышам-самцам линии A/Sn внутрибрюшинно однократно вводили циклофосфан (ЦФ) в дозе 200 мг/кг. Двум группам мышей (по 12 в каждой) за сутки до ЦФ и после него ежедневно внутрибрюшинно вводили растворы НПК из плаценты человека и НПК из печени мышей линии A/Sn по 50 мкг на мышь. На 3, 5 и 7 сутки после введения ЦФ по 4 мыши из каждой группы умерщвляли декапитацией, забирали кровь и подсчитывали количество лейкоцитов в камере Горяева. Контролем (исходное количество лейкоцитов) служили интактные мыши того же пола и возраста.
Результаты
2 мыши из 12, получавших только ЦФ пали на 5-й день после введения ЦФ. В группах мышей, получавших помимо ЦФ нуклепротеидные комплексы, гибели не было.
На чертеже видно, что на 3 сут. после введения ЦФ количество лейкоцитов в крови животных было резко сниженным и составляло около 6% от количества лейкоцитов у интактных мышей. При этом введение НПК не препятствовало снижению количества лейкоцитов, то есть не препятствовало действию цитостатика. Однако их восстановление существенно ускорилось на фоне введения НПК из печени мышей: количество лейкоцитов на 7 сутки уже превышало средние значения интактного контроля, тогда как у мышей, не получавших НПК, оно составляло около 70% от исходного. НПК из плацеты человека обладал несколько меньшим эффектом, однако значительно превышал показатели у контрольных животных, не получавших заявляемый препарат.
Таким образом, заявляемый препарат обладает антитоксическим действием, а именно стимулируюет лейкопоэз после его подавления цитостатиками. Антитоксические свойства заявляемого препарата также зависят от видовой специфичности и максимальны при использовании для выделения НПК гомологичного биологического сырья.
Изобретение иллюстрируется следующими конкретными примерами получения заявляемого препарата.
Пример 1
Плаценту (250 г) размораживают в течение 5 часов, затем гомогенизируют в гомогенизаторе с 250 мл 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА. В полученный гомогенат добавляют додецилсульфат натрия до конечной концентрации 2% по массе и инкубируют при 65°С в течение 24 часов. К полученному лизату добавляют хлорид натрия до конечной концентрации 2 М и инкубируют 12 часов при 65°С. После инкубации лизат центрифугируют при 9000 g в течение 10 минут. К полученному супернатанту добавляют равный объем ацетона, охлажденного до +10°С, для осаждения нуклеопротеидного комплекса (НПК). Полученный НПК трижды промывают охлажденным ацетоном и 96° этиловым спиртом для удаления несвязанных с ДНК низкомолекулярных белков и пептидов. Очищенный НПК растворяют при 65°С в 1 л 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА, затем раствор центрифугируют при 9000 g в течение 10 минут, супернатант фильтруют через стеклянный фильтр с диаметром пор 120 мкм и воздействуют на него ультразвуком в режиме 11 кГц для фрагментации НПК. Раствор фрагментированного НПК центрифугируют при 9000 g в течение 10 минут, затем добавляют двукратный объем охлажденного 96° этилового спирта. Осажденный НПК промывают 70° этиловым спиртом и после его высушивания получают заявляемый препарат на основе нуклеопротеидного комплекса со степенью фрагментации 200 пар нуклеотидов следующего состава, мас.%:
ДНК 80
белки ядерного матрикса 20
Выход целевого продукта составляет 0,37%, содержание основного вещества 98,5%.
Пример 2
Плаценту (250 г) размораживают в течение 6 часов, затем гомогенизируют в гомогенизаторе с 250 мл 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА. В полученный гомогенат добавляют додецилсульфат натрия до конечной концентрации 2% по массе и инкубируют при 65°С в течение 6 часов. К полученному лизату добавляют хлорид натрия до конечной концентрации 2 М и инкубируют 3 часа при 65°С. После инкубации лизат центрифугируют при 9000 g в течение 10 минут. К полученному супернатанту добавляют равный объем ацетона, охлажденного до +10°С, для осаждения НПК. Полученный НПК трижды промывается охлажденным ацетоном и 96° этиловым спиртом для удаления несвязанных с ДНК низкомолекулярных белков и пептидов. Очищенный НПК растворяют при 65°С в 1 л 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА, затем раствор центрифугируют при 9000 g в течение 10 минут, супернатант фильтруют через стеклянный фильтр с диаметром пор 120 мкм и воздействуют на него ультразвуком в режиме 44 кГц для фрагментации НПК. Раствор фрагментированного НПК центрифугируют при 9000 g в течение 10 минут, затем добавляют двукратный объем охлажденного 96° этилового спирта. Осажденный НПК промывают 70° этиловым спиртом и после его высушивания получают заявляемый препарат на основе НПК со степенью фрагментации 2000 пар нуклеотидов, содержащий, мас.%:
ДНК 40
белки ядерного матрикса 60
Выход целевого продукта составляет 0,3%, содержание основного вещества 95%.
Пример 3
Плаценту (250 г) размораживают в течение 5часов, затем гомогенизируют в гомогенизаторе с 250 мл 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА. В полученный гомогенат добавляют додецилсульфат натрия до конечной концентрации 2% по массе и инкубируют при 65°С в течение 12 часов. К полученному лизату добавляют хлорид натрия до конечной концентрации 2 М и инкубируют 6 часов при 65°С. После инкубации лизат центрифугируют при 9000 g в течение 10 минут. К полученному супернатанту добавляют равный объем ацетона, охлажденного до +10°С, для осаждения НПК. Полученный НПК трижды промывают охлажденным ацетоном и 96° этиловым спиртом для удаления несвязанных с ДНК низкомолекулярных белков и пептидов. Очищенный НПК растворяют при 65°С в 1 л 10 мМ трис-НСl буфера (рН 7,5), содержащего 1 мМ ЭДТА, затем раствор центрифугируют при 9000 g в течение 10 минут, супернатант фильтруют через стеклянный фильтр с диаметром пор 120 мкм и воздействуют на него ультразвуком в режиме 22 кГц для фрагментации НПК. Раствор фрагментированного НПК центрифугируют при 9000 g в течение 10 минут, затем добавляют двукратный объем охлажденного 96° этилового спирта. Осажденный НПК промывают 70° этиловым спиртом и после его высушивания получают заявляемый препарат на основе НПК со степенью фрагментации 1000 пар нуклеотидов следующего состава, мас.%:
ДНК 60
белки ядерного матрикса 40
Выход целевого продукта составляет 0,5%, содержание основного вещества 99,5%.
Использование предлагаемого препарата позволит, по сравнению с прототипом, расширить спектр фармацевтической активности, так как заявляемый препарат обладает собственной противоопухолевой активностью, а также снизить побочные осложнения химиолучевой терапии при сочетанием применении, за счет антитоксических и радиопротекторных свойств заявляемого препарата.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2008 |
|
RU2387456C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2490028C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2429019C2 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2489169C2 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2675233C1 |
| СПОСОБ ЛЕЧЕНИЯ АСЦИТНОЙ ФОРМЫ РАКА | 2015 |
|
RU2595864C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2345792C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2322264C1 |
| СПОСОБ ЭРАДИКАЦИИ СТВОЛОВЫХ ИНИЦИИРУЮЩИХ РАКОВЫХ КЛЕТОК | 2013 |
|
RU2542410C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТИМУЛИРОВАННЫХ ДЕНДРИТНЫХ КЛЕТОК ДЛЯ ИНДУКЦИИ ИММУННОГО ОТВЕТА ПРОТИВ ТУБЕРКУЛЕЗА ЧЕЛОВЕКА | 2009 |
|
RU2401664C1 |
Изобретение относится к медицине, точнее к химико-фармацевтической промышленности, и может быть использовано в клинической практике для лечения онкологических заболеваний. Разработан аллогенный препарат из плаценты человека на основе фрагментированного до 200-2000 пар нуклеотидов нуклеопротеидного комплекса, содержащего, мас.%: д.с. ДНК 60-80; белки ядерного матрикса 20-40. Преимущество изобретения заключается в том, что препарат обладает комплексной фармацевтической активностью и обеспечивает противоопухолевое, антитоксическое и радиопротекторное действие. 2 з.п.ф-лы, 2 табл., 1 ил.
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| СПОСОБ СТИМУЛЯЦИИ ЛЕЙКОПОЭЗА | 1993 |
|
RU2078581C1 |
| СПОСОБ КОРРЕКЦИИ ПОБОЧНЫХ ЭФФЕКТОВ ХИМИОЛУЧЕВОЙ ТЕРАПИИ | 1995 |
|
RU2110995C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 5470577 А, 28.11.1995. | |||
Авторы
Даты
2004-08-20—Публикация
2003-05-27—Подача