Изобретение относится к биотехнологии, в частности к генетической инженерии, и может быть использовано в сельском хозяйстве, ветеринарии, медицинской, микробиологической и пищевой промышленности для получения микроорганизмов с заданными свойствами, в том числе для создания пробиотиков и заквасок - препаратов на основе живых культур микроорганизмов.
В настоящее время используется много способов гетерологичной экспрессии генов, однако все они разработаны для ограниченного круга микроорганизмов.
В качестве ближайшего аналога может быть рассмотрен способ получения трансформированных молочнокислых бактерий (Международная заявка WO 89/01970; Michiels F., Delcour J., Mahillon J., Transformed lactic acid bacteria). При этом для экспрессии клонированных бактериальных генов используются их природные промоторы, которые проявляют активность в реципиентных штаммах молочнокислых бактерий. Однако свойствами обеспечивать экспрессию генов в достаточно широком круге клеток обладают далеко не все природные промоторы.
Между тем нередко возникает задача экспрессировать некоторую последовательность в штамме микроорганизма, для которого специальных экспрессионных систем не разрабатывалось, или в различных штаммах микроорганизмов, что требует разработки достаточно универсального способа экспрессии.
Целью изобретения является создание молекул ДНК для клонирования генов, введения клонированных генов в молочнокислые бактерии и другие виды микроорганизмов и экспрессии клонированных генов в реципиентных клетках.
Поставленная цель большей универсальности экспрессии клонированного целевого гена по сравнению с аналогами достигается способом конструирования, заключающемся в соединении в один транскриптон под универсальным промотором как репликативных генов вектора, так и подлежащих экспрессии последовательностей. Этот способ конструирования обеспечивает экспрессию клонированных генов во всех видах реципиентов, поддерживающих репликацию выбранного репликона.
Изобретение реализовано в виде семейства плазмид, состоящего из плазмид широкого круга хозяев pLF21, pLF22, pLF-SL1, pLF-SL2. В состав всех этих плазмид входит репликон криптической плазмиды pLF 1311, исходно происходящей из Lactobacillus fermentum BKM 1311. Для их репликации строго необходимо присутствие в клетках продукта гена герВ, транскрипция которого происходит с идентифицированнго промотора вектора (Aleshin V.V. et al., FEMS Microbiol. Lett., 1999, 178, 47-53). Круг бактериальных штаммов-хозяев, в которых происходит репликация однорепликонных плазмид семейства pLF1311, и, соответственно, экспрессия гена герВ, был определен (Aleshin V. V. et al., FEMS Microbiol. Lett., 1999, 178, 47-53). Он оказался очень широким и включает несколько штаммов, применяемых в качестве пробиотиков.
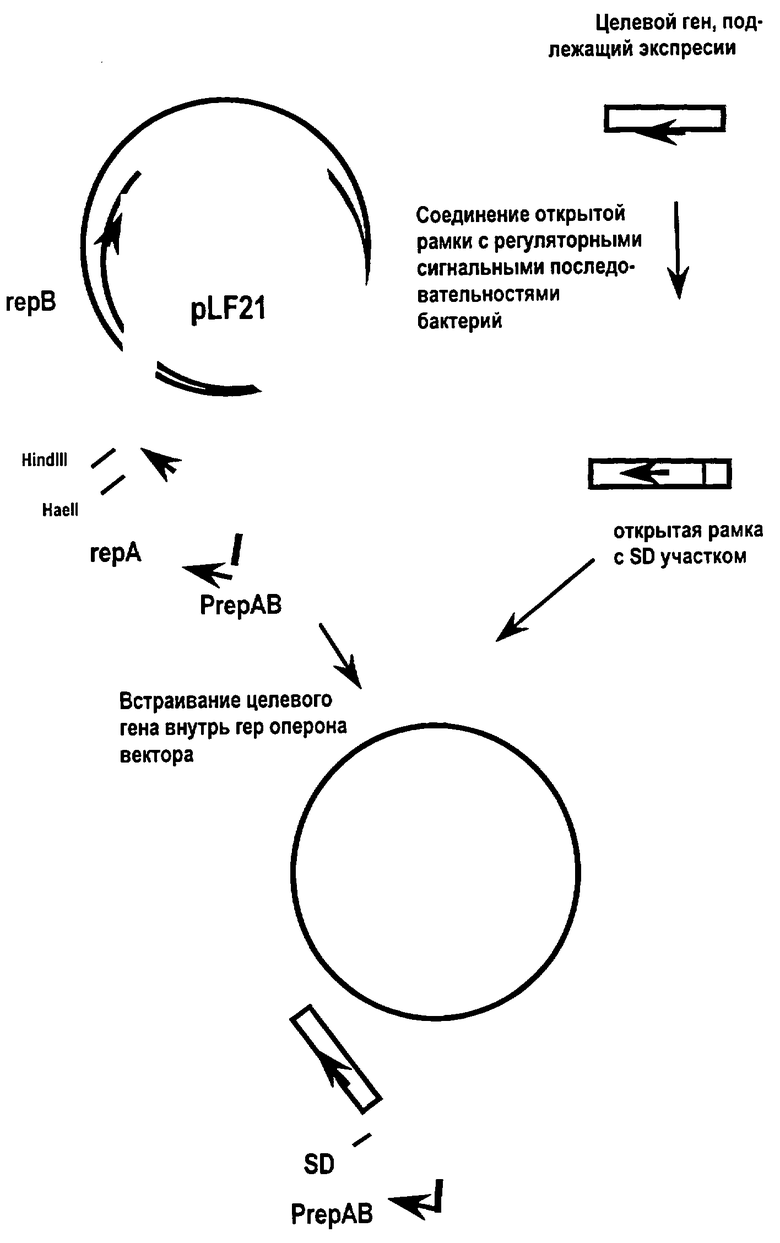
Сущность патентуемого генно-инженерного решения поясняется чертежом, где показана схема конструирования гибридной плазмиды pLF-SL2.
Для создания экспрессионного вектора pLF21 используют плазмиду pLF20, нуклеотидная последовательность которой полностью известна. В состав плазмиды pLF20 входит репликативная область pLF 1311, включая гены rерА и rерВ с промотором, локусы ori+, ori-; ген cat из плазмиды рС194 (Horinouchi S., Weisblum В. J. Bacteriol., 1982, 150, 815-825), направляющий синтез хлорамфениколацетилтрансферазы; nic сайт из плазмиды RP4 (Simon R., Mol. Gen. Genet. 1984, 196, 413-420; Pansegrau W., Ziegelin G., Lanka E., Biochim. Biophys. Acta, 1988, 951, 365-374). ДНК плазмиды pLF20 гидролизуют рестриктазами Асc 161 и Bmel42I, затем проводят лигирование и трансформацию в соответствии с известными методами ("Методы молекулярной генетики и генной инженерии", Новосибирск, "Наука", СО, 1990, с.7-10, 39-44). После лигирования и трансформации отбирают колонии, содержащие плазмиду pLF21, которая отличается от pLF20 тем, что не содержит балластного фрагмента между сайтами рестриктаз Асс 161 и Bme 142I, в пределах которого локализуется один из двух сайтов НаеII плазмиды. В полученной плазмиде pLF21 имеются уникальные сайты HindIII и НаеII в спейсере между генами герА и герВ репликативного оперона, позволяющие клонировать и экспрессировать чужеродный генетический материал.
Еще одним существенным преимуществом патентуемого способа конструирования является повышенная структурная стабильность полученных генетических конструкций. Известно, что структурная стабильность рекомбинантных молекул в клетках микроорганизма-хозяина представляет серьезную проблему для биотехнологии. В случае конструкций, полученных патентуемым способом, структурная стабильность рекомбинантных молекул в клетках обеспечивается локализацией клонированных генов в межгенном спейсере в составе rep оперона. Любые протяженные делеции, захватывающие фланкирующие последовательности клонированного гена, приведут к нарушению функции rep генов и нарушению репликации таких мутантных плазмид, против которых будет таким образом происходить естественный отбор в живых клетках без участия человека.
Экологическая безопасность, в частности предотвращение диссеминации рекомбинантной плазмиды в природе, обеспечивается неконъюгативностью и потребностью для мобилизации в специфических плазмидах-помощниках, не способных к репликации в грамположительных реципиентах. Ранее было показано, что происхождение плазмиды pLF1311 связано с делецией природных mob-сайтов, характерных для большинства родственных плазмид, но отсутствующих в pLF1311 (Алешин В.В., Дорошенко В.Г., Тараканов Б.В., Молекулярная биология, 1998, 32, 415-419).
Изобретение иллюстрируется примерами, которые характеризуют экспрессию клонированных последовательностей с промотора репликативных генов.
Пример 1. Экспрессия α-пептида β-галактозидазы с промотора репликативных генов векторной плазмиды.
Для тестирования экспрессии чужеродной ДНК с промотора репликативных генов вектора в промежуток между уникальными сайтами HindIII и HaeII в спейсере генов герА и герВ репликативного оперона был клонирован фрагмент плазмиды pTZ19 (Mead D.A., Szczesna-Skorupa E., Kemper В. Protein Eng., 1986, 1, 67-74), содержащий ген lacZ’. Последовательность lucZ’ клонирована в направлении транскрипции генов герА и герВ, так что конец векторной ДНК, образованный после гидролиза рестриктазой HindIII и затупления с помощью достраивания 3’-выступающего конца с помощью фрагмента Кленова ДНК-полимеразы I Escherichia coli, соединен с концом фрагмента lacZ, образованным гидролизом ДНК плазмиды pTZ19 рестриктазой BsrBI в области оператора lacZ.
Для отбора нужной конструкции лигазной смесью были трансформированы клетки Escherichia coli штамма TG1 Δ(1ас, pro), supE, thi, hsdD5/F’ traD36, proA+B+, ladq и высеяны на селективные чашки со средой LB, содержащей хлорамфеникол в концентрации 15 мкг/мл, хромогенный субстрат 5-бром-4-хлор-3-индолил-β-D-галактопиранозид (X-gal) в концентрации 50 мкг/мл, но не содержащей индуктора лактозного оперона изопропил-β-D-тиогалактозида (ИПТГ). В результате на вторые сутки инкубации при 37oС были отобраны колонии, окрашенные в светло-голубой цвет. Они содержат плазмиду pLF22 и экспрессируют работающую β-галактозидазу без добавления в среду индуктора ИПТГ.
Пример 2. Клонирование синтетического гена соматолиберина в состав репликативного оперона плазмиды pLF21.
Клонирование синтетического гена соматолиберина в состав репликативного оперона плазмиды pLF21 осуществляют в два этапа. На первом этапе решается задача амплификации структурной части синтетичнеского гена соматолиберина и соединение ее с регуляторной последовательностью для трансляции в прокариотическом хозяине, в частности, соединением с последовательностью SD для связывания соответствующей мРНК бактериальной рибосомой и инициации трансляции. Эта цель достигается использованием метода амплификации фрагментов ДНК в системе in vitro под контролем термостабильной ДНК-полимеразы Taq (полимеразная цепная реакция, ПЦР). Для этого используют олигонуклеотидный праймер M1 из 32 нуклеотидных остатков, имеющий последовательность д(5’ГААГГАТАААТТТАТГТАЦГЦТЦАЦГЦТАТЦТ3’), в котором 19 остатков, составляющих 3’- конец олигонуклеотида, комплементарны последовательности плазмиды pMTGRF1 (Brenig В., Brem G. Chimica OGGI - Chemistry today, 1993, 11 (1-2), 33-42), несущей синтетическую последовательность структурной части гена соматолиберина под управлением эвкариотических регуляторных элементов. Этот сегмент M1 имеет следующую последовательность: 5’-...АТГТАЦГЦТЦАЦГЦТАТЦТ-3’,5’-концевой сегмент праймера Ml не комплементарен матрице pMTGRF1, этот сегмент содержит последовательность 5’-ГААГТА...3’, соответствующую консенсусу SD бактериальных генов, и канонический спейсерный участок между SD и инициаторным кодовом ATG, обогащенный остатками аденозина и тимидина. Для облегчения манипуляций в спейсерную последовательность между SD и инициаторным кодоном введена последовательность узнавания рестриктазы Apol. Парный праймер МП имеет структуру д(5’-ТЦЦАТАТТГГТЦГАЦТАТТАА-3’). Амплификацию осуществляют в следующем режиме: 93°С-1 мин, 50oС-1 мин, 72°С-2 мин, всего 25 циклов на автоматическом термоциклере Techne-3 (Англия). Состав реакционной смеси: 10 мМ трис-НСl (рН 9,0 при 25°С), 50 мМ КС1, 0,1% тритон Х-100, 2 мМ MgCl2, по 0,2 мМ каждого из дезоксинуклеотидтрифосфатов: дГТФ, дАТФ, дТТФ, дЦТФ, по 5 пМ олигонуклеотидов MI и MII, 1 нг ДНК pMTGRFl и 1 ед. Taq-полимеры производства Силекс (Москва), объем реакционной смеси 50 мкл под слоем минерального масла. По окончании процесса амплифицированный фрагмент ДНК клонируют по известным методикам в векторной плазмиде pBluescriptKS(+) (Stratagene), предварительно линнеаризованной эндонуклеазой Есо32I. Бактерии Е.coli TG1, содержащие плазмиду с геном соматолиберина, образуют на индикаторных чашках Петри на среде LB с ампициллином, хромогенным субстратом X-gal и индуктором ИПТГ в концентрации 50 мкг/мл, колонии белого или светло-голубого цвета в зависимости от ориентации вставки, в отличие от колоний, образованных клетками с векторной плазмидой pBluescriptKS(+), окрашенных в интенсивный синий цвет. Среди светло-голубых колоний отбирают колонию, содержащую плазмиду pSLD2 с тандемной дупликацией последовательности соматолиберина в той же ориентации, что и lacZα вектора. В плазмиде pSLD2 происходит сквозная транскрипция соматолиберин+lacZα мРНК с бактериального лактозного промотора кишечной палочки, и экспрессия соматолиберина может быть индуцирована ИПТГ. В полученной конструкции ген соматолиберина находится также под промотором бактериофага Т3 и может быть экспрессирован в системах in vitro или in vivo в различных модификациях.
Последовательности соматолиберина в составе плазмиды pSLD2 не содержат терминаторов транскрипции, так же как и фрагмент lacZα. Причем асимметричное расположение сайтов HindIII и НаеII в pSLD2 обеспечивает клонирование целевого фрагмента в требуемой ориентации. На втором этапе ДНК плазмид pSLD2 и pLF21 в количестве 0,5 мкг гидролизуют последовательно рестриктазами НаеII и HindIII, очищают от продуктов реакции, лигируют и лигазную смесь используют для трансформации Е.coli TG1. Трасформанты высевают на селективные чашки Петри со средой LB с добавкой хлорамфеникола с концентрации 15 мкг/мл и хромогенного субстрата X-gal в концентрации 50 мкг/мл. После инкубации чашек при 37°С в течение 20 ч их переносят в холодильник с температурой 12°С и инкубируют 5 суток. По окончании инкубации отбирают светло-голубую колонию с фенотипом CmrAps, клетки которой содержат плазмиду pLF-SL2. Последовательности структурной области гена соматолиберина и lacZα помещены внутрь rep оперона вектора и транскрибируются независимо от ИПТТ.
Плазмидную pLF-SL2 вводят в штамм Lactobacillus ps. 8РА3 обработкой суспензии клеток в растворе ДНК pLF-SL2 в концентрации 0,1 мкг на 50 мкл клеточной суспензии с помощью устройства для обработки суспензии клеток импульсным электрическим током для генетических исследований (Тюрин М.В., Лившиц В.А., Биол. мембраны, 1994, 11, 117-139). К суспензии клеток, находящейся в ледяной бане, прикладывают одиночный прямоугольный импульс положительной полярности длительностью 2,6 мс и напряженностью электрического поля 17 кВ/см. Немедленно после приложения импульса образец разводят охлажденной питательной средой и выдерживают в ледяной бане 10 мин, затем 1 ч при 37°С, после чего высевают на селективную среду MRS.
Штамм Lactobacillus ps. ВРАЗ (pLF-SL2) депонирован во Всероссийской коллекции промышленных микроорганизмов под регистрационным номером В-7495.
Полученный штамм характеризуется следующими культурально-морфологическими признаками. Грамположительные короткие палочки, расположенные беспорядочными скоплениями или короткими цепочками по 3-5 клеток. На агаризованной среде МРС-1 и Рогозы образуют беловатые, выпуклые, непрозрачные колонии.
Штамм отличается следующими физиолого-биохимическими свойствами. Оптимальная температура для роста 37°С, толерантен к присутствию кислорода. Расщепляет глюкозу без образования газа. Сбраживает сахарозу, мальтозу, лактозу, галактозу, целлобиозу, мелецитозу, маннозу, сорбитол, маннитол, салицин. Не ферментирует тагатозу и рамнозу.
Находящаяся в штамме Lactobacillus ps. 8РАЗ (pLF-SL2) плазмида pLF-SL2 содержит двойную дозу гена соматолиберина, перед каждой из дуплицированных кодирующих областей соматолиберина имеется бактериальный сигнал трансляции. Транскрибция клонированных генов соматолиберина происходит с универсального репликативного промотора, она конститутивная и регулируется в основном через копийность плазмиды в клетке.
Изобретение относится к биотехнологии, в частности к генетической инженерии. Способ конструирования рекомбинантных штаммов микроорганизмов обеспечивает экспрессию целевого прокариотического или эукариотического гена в любом штамме микроорганизма, поддерживающем репликацию векторной ДНК. На основе мультикопийной плазмиды pLF1311 сконструирован вектор, позволяющий легко отбирать клонированные последовательности по фенотипическому признаку несущих его бактерий и экспрессировать их. С его помощью сконструирован пробиотический штамм Lactobacillus sp. ВРАЗ (pLF-SL2), который экспрессирует эукариотический ген соматолиберина. Данное изобретение используется для создания пробиотиков и заквасок - препаратов на основе живых культур микроорганизмов. 1 ил.
| WO 8901970, 12.04.1989 | |||
| СПОСОБ ПОЛУЧЕНИЯ АТТЕНУИРОВАННОГО ШТАММА БАКТЕРИЙ SALMONELLA И ВАКЦИНА | 1992 |
|
RU2126447C1 |
| РЕКОМБИНАТНАЯ ПЛАЗМИДНАЯ ДНК PECO29KI, ОПРЕДЕЛЯЮЩАЯ СИНТЕЗ ЭНДОНУКЛЕАЗЫ РЕСТРИКЦИИ ECO29KI И ШТАММ ESCHERICHIA COLI - ПРОДУЦЕНТ ЭНДОНУКЛЕАЗЫ РЕСТРИКЦИИ ECO29KI | 1992 |
|
RU2054037C1 |
| НЕГЛИКОЗИЛИРОВАННЫЙ ПОЛИПЕПТИД СО СВОЙСТВАМИ ПРОУРОКИНАЗЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК ДЛЯ ЭКСПРЕССИИ ПОЛИПЕПТИДА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1992 |
|
RU2108387C1 |
Авторы
Даты
2004-09-20—Публикация
2002-04-30—Подача