Область техники, к которой относится изобретение
Настоящее изобретение относится к новому терапевтическому составу. В частности данный состав содержит N-(4-Нитро-2-Феноксифенил)метансульфонамид (нимесулид) с 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитолом и вводится в форме внутривенных и внутримышечных инъекций, а также в жидкой форме для приема через рот и для местного применения, а также к способу приготовления таких составов.
Ниже приводится химическая формула нимесулида, химическое название которого N-(4-нитро-2-феноксифенил)метансульфонамид (нимесулид):
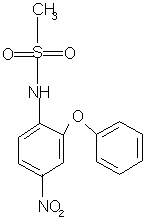
Предпосылки создания изобретения
Препараты на основе нимесулида используются в качестве болеутоляющих в форме таблеток, взвеси, мазей и внутримышечных препаратов.
Плохая растворимость нимесулида в водной среде ограничивает его применение в болеутоляющих составах в форме инъекций или для приготовления составов с различными ингредиентами для применения через рот или местно. Использование в таких рецептурах масла приводит к возникновению различных проблем, например составы для инъекции не поддаются фильтрации и при внутримышечном введении вызывают боль и образуют закупорки и поэтому не пригодны и для внутривенного применения. Различные производные касторового масла при применении внутрь могут привести к анафилактической реакции и не обеспечивают быстрой помощи.
В патенте США №5688829 описано приготовление нимесулида для терапевтического применения в форме внутримышечных инъекций. В патенте описано применение целого ряда средств доставки препарата типа диметилацетамида, бензилбензоната, бензилового спирта и этилолеата в различных пропорциях, что говорит о применении более чем одного ингредиента, что, в свою очередь, требует проверок качества отдельных ингредиентов и стабилизирующих средств. Применение таких растворов для внутривенного введения ограничено определенными параметрами продукта.
Соль нимесулида, как таковая, используется нечасто, так как ее водный раствор обладает очень высокой щелочностью, характеризуемой величиной рН, и с точки зрения гомеостаза не подходит для введения в виде инъекций.
В документе WО 95/34533 описан препарат для инъекций на основе нимесулида в комплексной форме, образованной с использованием L-лизина. Применение этого препарата также имеет ограничения, поскольку, например, для достижения высокого терапевтического эффекта необходимо внутримышечно вводить большие количества или дозы этого состава, что соответствует субтерапевтическому уровню, если сравнивать с обычным внутримышечным способом введения.
Недостатки нимесулида не позволяют вводить его внутривенно, а также в форме прозрачных препаратов типа сиропов и капель.
Таким образом, существует необходимость в устойчивом анальгетике, противоспалительном, жаропонижающем препарате или растворе, который может быть отфильтрован, стерилизован обычным образом и не имеет недостатков, присущих препаратам на основе масла и его составляющих.
Описание изобретения
Авторы изобретения обнаружили, что состав в форме, приемлемой для инъекций, в жидкой форме для приема через рот (а именно, сиропов и капель), лосьонов, кремов и мазей может быть получен при растворении N-(4-нитро-2-феноксифенил)метансульфонамида (нимесулида) в 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоле.
Этот раствор в форме, приемлемой для инъекций, может традиционно вводиться внутривенно и по необходимости разными дозами в зависимости от назначений пациенту.
Этот препарат представляет собой прозрачный раствор, который устойчив, безопасен и так же эффективен, как и состав, предлагаемый в настоящее время на рынке.
Авторы изобретения также раскрыли более дешевый способ приготовления нового состава. Способ по настоящему изобретению так же прост.
В другом случае состав может быть получен при растворении N-(4-нитро-2-феноксифенил)метансульфонамида (нимесулида) в смеси 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитола с водой.
В другом варианте настоящего изобретения составы могут содержать средства доставки и вспомогательные лекарственные средства типа средств разбавления, подслащивающих средств, буферов, ароматизаторов, стабилизирующих агентов и т.п.
Изобретение также относится к способу приготовления указанного терапевтического состава, который включает
- смешивание N-(4-нитро-2-феноксифенил)метансульфонамида (нимесулида) с 2,5-ди-О-метил-1, 4:3,6-диангидро-D-глюцитолом при помешивании и нагреве;
- охлаждение смеси и извлечение раствора.
Растворы нимесулида можно вводить либо внутривенно, либо внутримышечно. Болеутоляющий эффект максимален в случае достаточно равномерного распределения лекарственного средства в тканях пациента, что и обуславливает терапевтический эффект после его усвоения при внутривенном или внутримышечном введении препарата. Дозировка может быть разной с различными концентрациями от 25 до 100 мг/мл, что не токсично. В соответствии с рекомендациями врачей препарат может вводиться один раз или много раз.
Состав по настоящему изобретению также подходит для применения через рот и местно. Используемый растворитель хорошо растворяется в воде, универсален и нетоксичен при соответствующем применении. Он также снижает стоимость и повышает эффективность при применении через рот.
Более того, побочные эффекты типа желудочного раздражения, которое может возникать при приеме препарата через рот, могут быть уменьшены, если состав по настоящему изобретению вводится в форме инъекции или детских капель или в жидкой форме для приема через рот с использованием соответствующих разбавителей.
Состав может быть приготовлен в виде инъекций с растворителем, готовым к применению, в ампуле с одноразовой или многоразовой дозой специально для гериатрических и педиатрических пациентов. Однако это не ограничивает его применения только для этих категорий пациентов и может назначаться любым пациентам для получения немедленного эффекта с высоким терапевтическим показателем без каких-либо ограничений к применению через рот или суппозитарно. Доза для применения людьми через рот составляет 100 мг, которая назначается дважды в день или 5 мг на 1 кг массы тела пациента в день за 2-3 приема с началом действия в течение 30-60 минут и продолжительностью действия 8-10 часов. Для местного применения изготавливается гель, содержащий карбопол и 1% спирта.
В соответствии с настоящим изобретением готовятся растворы концентрацией 25 или 100 мг/мл с антиоксидантом или без него, которые вводятся внутримышечно или внутривенно или в жидкой форме для приема через рот с максимальным пороговым уровнем снижения боли, что обеспечивает наилучшее болеутоляющее, жаропонижающее и противовоспалительное действие. Преимуществом является быстродействие препарата в тех случаях, когда время является определяющим фактором для обезболивания, снижения температуры и т.п.
Примеры даются в качестве иллюстрации изобретения и не исчерпывают всех его возможностей; на основе данного изобретения с использованием этого универсального и первоклассного растворителя могут быть приготовлены производные формы нимесулида. Растворитель легко смешивается с водой. Дозы до 100 мг/мл нимесулида и его аналогов могу быть приготовлены в 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоле. Этот же растворитель можно использовать для приготовления 1% геля.
Ниже для иллюстрации настоящего изобретения приводятся примеры, показывающие приготовление нимесулида в смеси растворителя-носителя в виде 2, 5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля с водой, которая обеспечивает получение безопасного, эффективного, экономичного, простого в приготовлении раствора для внутримышечного или внутривенного применения и для применения через рот в воде капель и сиропов.
ПРИМЕРЫ
Пример I
В колбу, содержащую 50 мл 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля, вводится нимесулид в количестве 8,10872 ммоль. Раствор непрерывно перемешивается, и его температура поддерживается на уровне 40°С в течение 1 ч в среде азота. Температура реакционной смеси понижается до 25°С и с помощью 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля объем препарата доводится до 100 мл. Этот раствор фильтруется с соблюдением условий асептики через миллипористый фильтр с ячейкой размером 0,2 мкм, заливается в ампулу из янтарного стекла и закупоривается в ней для приготовления состава для инъекции. Прозрачный раствор может применяться для приготовления жидких форм для приема через рот и педиатрических капель путем добавления разбавителей, подслащивающих составов, буферов, ароматизаторов и стабилизирующих агентов.
Пример II
В колбу, содержащую 50 мл 2,5-ди-O-метил-1,4:3,6-диангидро-D-глюцитоля, вводится нимесулид в количестве 32,43 ммоль. Раствор непрерывно перемешивается и промывается азотом. Смесь перемешивается при 40°С в течение 45 минут. Затем смесь охлаждается до 25°С и объем полученного препарата доводится до 100 мл. Этот раствор фильтруется через миллипористый фильтр с ячейкой размером 0,2 мкм, заливается в ампулу из янтарного стекла и закупоривается в ней для приготовления состава для инъекции. Раствор может применяться для приготовления жидких форм для приема через рот и капель путем добавления необходимых средств доставки и вспомогательных лекарственных средств типа разбавителей, подслащивающих составов, буферов, ароматизаторов и стабилизирующих агентов.
Пример III
В колбу, содержащую 50 мл 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля, вводится нимесулид в количестве 8,1072 ммоль. Температура раствора поддерживается на уровне 60°С. При непрерывном перемешивании добавляется 15 мл воды двойной перегонки, пригодной для инъекций, перемешивание продолжается. При непрерывном перемешивании до полного растворения добавляется 0,7 ммоль хлорокрезола и температура раствора доводится до комнатной. С помощью 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля объем готового препарата доводится до 100 мл. С помощью потенциометра и с использованием стеклокаломелевых электродов измеряется уровень рН раствора, величина которого составляет около 6. Раствор фильтруется с соблюдением условий асептики через миллипористый фильтр с ячейкой размером 0,2 мкм, заливается в ампулу из янтарного стекла и закупоривается в ней в среде азота.
Хлорокрезол не добавляется, и путем введения необходимых разбавителей типа сахара, буферов и ароматизаторов можно приготовить педиатрические капли и жидкости для приема через рот.
Пример IV
В колбу, содержащую 50 мл 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля, при непрерывном перемешивании вводится нимесулид в количестве 16,21 ммоль. Раствор перемешивается в течение 45 минут при 60°С и затем к раствору добавляется 15 мл воды двойной перегонки. При непрерывном перемешивании до полного растворения добавляется 0,7 ммоль хлорокрезола и после полного растворения температура раствора доводится до комнатной и с помощью 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоля объем готового препарата доводится до 100 мл. Раствор фильтруется с соблюдением условий асептики через миллипористый фильтр с ячейкой размером 0,2 мкм, заливается в ампулу из янтарного стекла и закупоривается в ней.
Хлорокрезол не добавляется, и путем введения необходимых разбавителей типа сахара, буферов и ароматизаторов можно приготовить педиатрические капли и жидкости для приема через рот.
Испытания раствора нимесулида в 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитоле на устойчивость показали, что он устойчив при комнатной температуре, а также при температуре до 40°С в течение 6 месяцев.
Периодические исследования устойчивости препарата приведены в табл.1
Название продукта: нимесулид
Условия хранения: 25±2°С при относительной влажности 60±5%
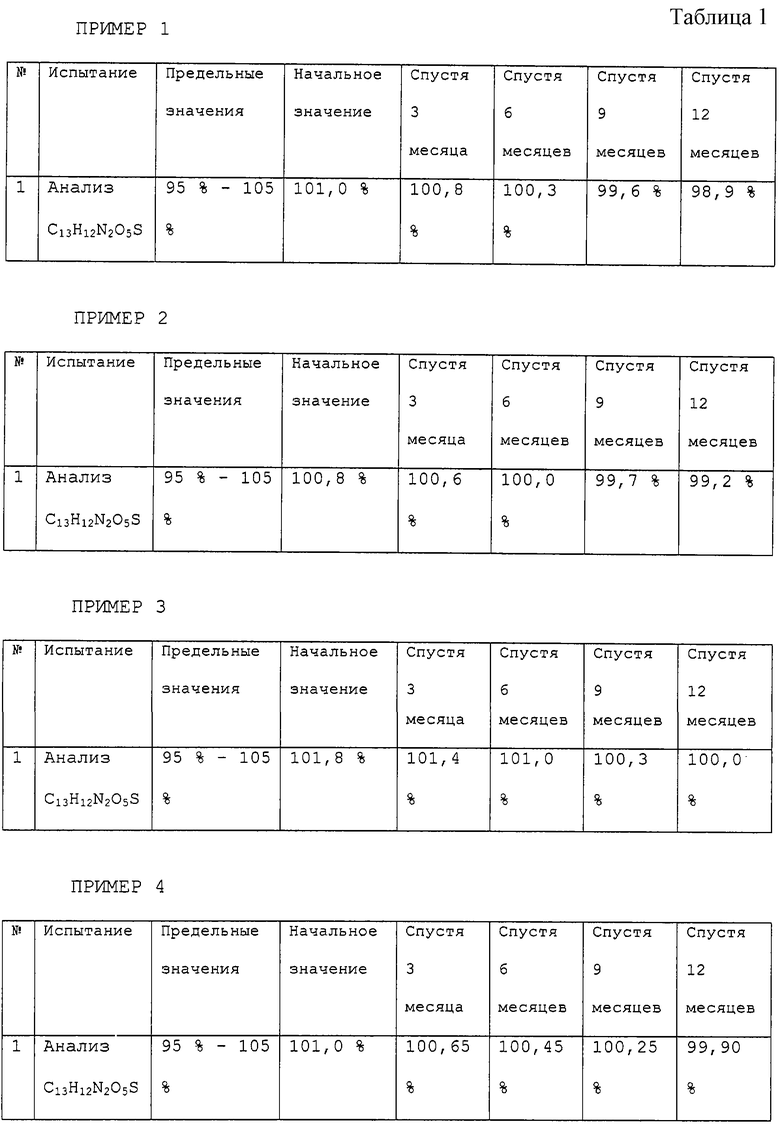
Ускоренные исследования устойчивости препарата приведены в табл.2
Название продукта: нимесулид
Условия хранения: 40±2°С при относительной влажности 75±5%
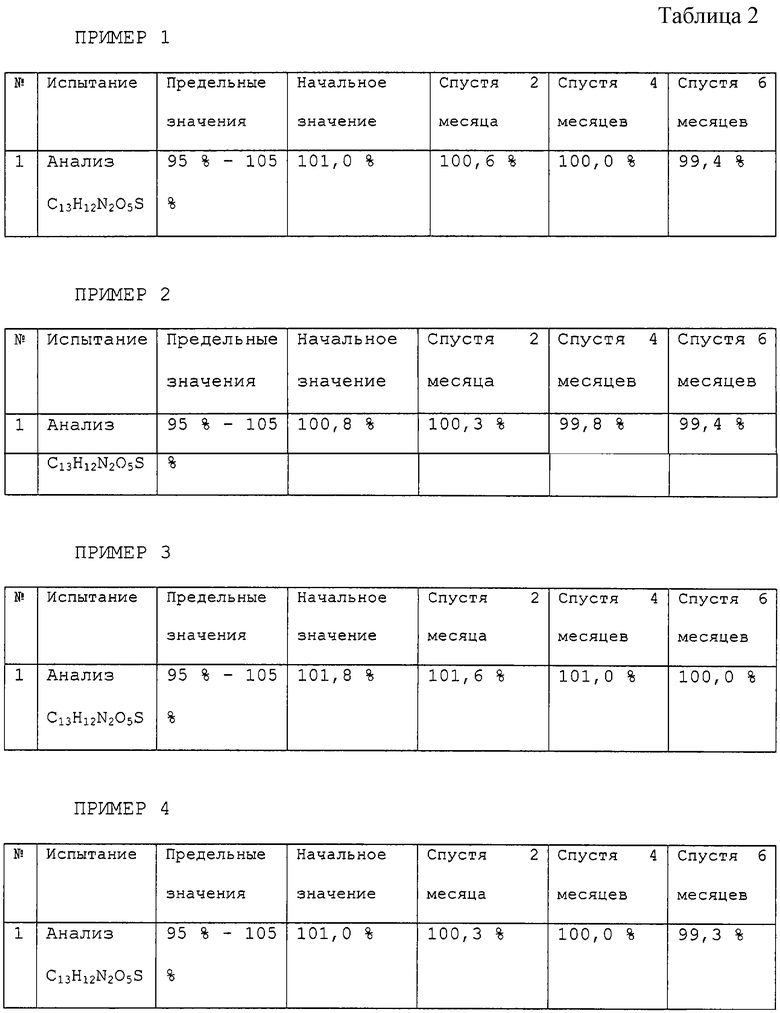
Таким образом, из приведенных примеров ясно, что растворы, приготовленные в различных концентрациях 25, 50 и 100 мг/мл, которые назначаются либо как разовые, либо как многоразовые инъекции или в виде жидкого раствора для приема через рот, очень устойчивы. Можно применять различные разбавители типа воды для получения растворов объемной концентрацией до 15%. Проверка устойчивости осуществлялась спектроскопическим способом.
Действенность препаратов на основе данного раствора испытывалась на животных, и оказалось, что эти препараты действуют гораздо быстрее, чем препараты нимесулида, принимаемые через рот.
Сранительный анализ противовоспалительного действия нового состава в форме инъекций
Описание эксперимента
В состав групп А и В входили по 6 разнополых мышей. Воспаление вводилось в лапы мышей с помощью 0,025 мл раствора, содержащего 0,05% каррагена, приготовленного в растворе с концентрацией соли 0,085%. Спустя примерно 18 ч в правой лапе наблюдались отеки. Данные получали после 18 ч исследований с помощью плетизмографии. Животным группы А внутримышечно вводили натриевую соль диклофенака из расчета 5 мг на 1 кг массы тела животного, а животным группы В вводили новый состав нимесулида из расчета 8 мг на 1 кг массы тела животного. Спустя 21 ч с помощью плетизмографии измеряли объем лап.
В табл.I приводятся данные измерений.
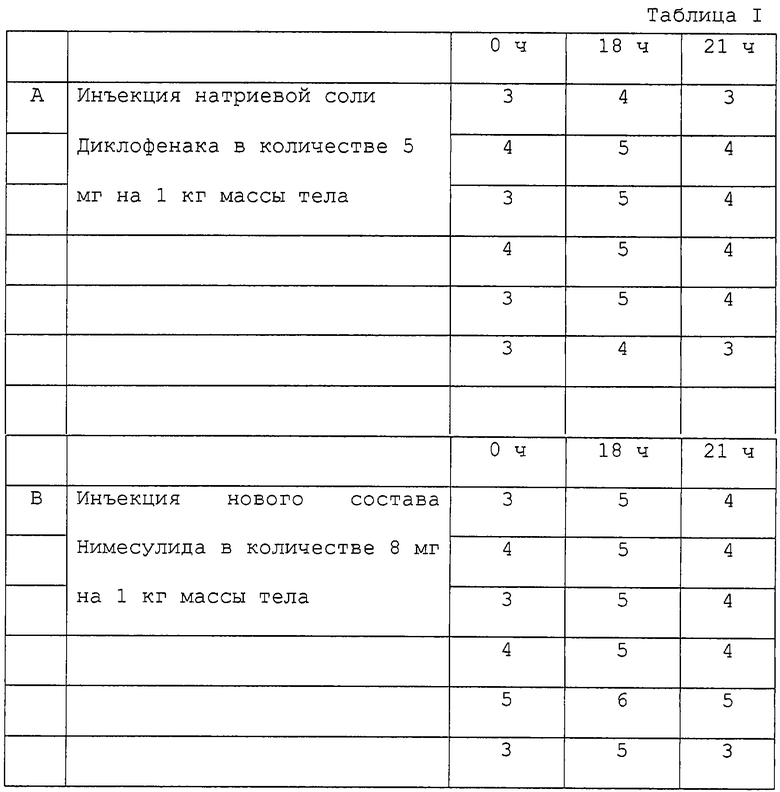
Заключение: из рассмотренного выше эксперимента видно, что болеутоляющее действие нового состава не уступает, а в некоторых случаях даже превосходит болеутоляющее действие, оказываемое натриевой солью диклофенака.
Сранительный анализ противовоспалительного действия нового состава в форме геля
Состав А) Гель нимесулида (10 мг/г)
Состав В) нимесулид (10 мг/г) + метилсалицилат + ментол + капсацин
Описание эксперимента
Эксперимент проводился на разнополых крысах и морских свинках. Отеки вызывали с помощью каррагена. Животных подвергали анестезии с помощью пентобарбитона и местно за 30 минут до заражения каррагеном на правую лапу наносился состав А (гель нового состава) и состав В (гель, доступный на рынке) (100 мг на животное). Острый отек на правых задних лапах крыс вызывался путем инъекции 0,1 мл свежеприготовленного раствора, содержащего 1% каррагена. В левые контрольные лапы вводился 0,1 мл солевого раствора. Объем лап измерялся с помощью плетизмографии через 30, 60, 120, 180 и 240 минут после заражения каррагеном. Величина воспаления выражалась в виде относительных изменений объема лапы.
Результаты противовоспалительной активности приведены в табл.II
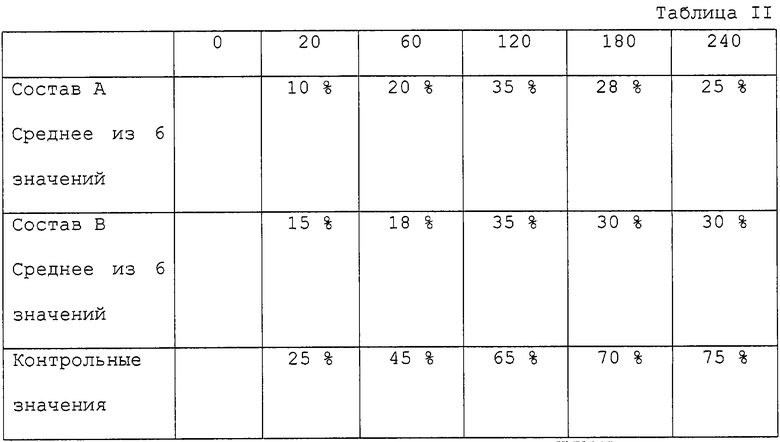
Карраген вызывает значительное увеличение объема лап контрольной группы. Применение составов А и В приводило к значительному уменьшению объема лап в сравнении со значениями этого показателя в контрольной группе.
Как явствует из результатов эксперимента, противовоспалительное действие обоих составов сравнимо при отеках, вызванных введением каррагена, однако в отличие от группы А (новый состав) в группе В (состав капсиацина) наблюдалось раздражение, эритема и отек. Эксперименты, выполненные на добровольцах, показали такой же эффект, характеризующийся раздражением и эритемой в группе, обрабатываемой составом В в отличие от группы, на которой испытывался состав А (новый препарат), применение которого не вызывало никаких эффектов.
Исследования раздражения кожи
На спинках морских свинок сбривались волосы на площади 4 см2 и дважды в день в течение 7 дней на это место накладывался гель из препаратов А и В. Ниже показана бальная шкала чувствительности и реакции.
0 - нет реакции;
0,5 - слабая, бляшечная эритема;
1 - слабая, но сливная или умеренная, но бляшечная эритема;
2 - умеренная эритема;
3 - сильная эритема с отеком или без него.
Влияние нового состава и состава, доступного на рынке, на раздражение кожи приведены в табл.III
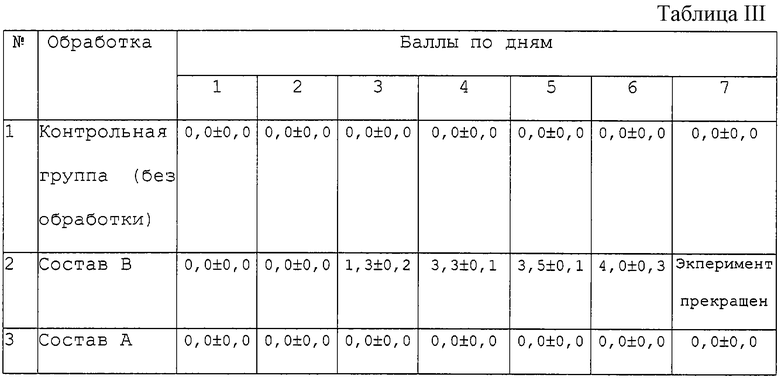
Результаты
У животных группы В наблюдалось раздражение со стороны нанесения препарата, содержащего капсациан, в то время как у животных группы А, на которых испытывался новый состав, раздражения не наблюдалось. Применение состава В вызывало сильное покраснение и эритему. Из-за такой реакции эксперимент был прекращен на 6-й день.
Клиничекие исследования
На тыльной стороне руки десяти мужчин-добровольцев испытывалось действие препаратов А и В, которое оценивалось по величине раздражения и покраснения.
Результаты
Все полученные в результате экспериментов данные указывают на очевидное преимущество состава по настоящему изобретению в сравнении с применяемыми в настоящее время составами.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ БОЛЕУТОЛЯЮЩЕГО СРЕДСТВА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2141845C1 |
| СПОСОБЫ РОТОГРАВЮРНОЙ ПЕЧАТИ ДЛЯ ПОЛУЧЕНИЯ ОПТИЧЕСКИ ИЗМЕНЯЮЩИХСЯ ПРИЗНАКОВ ЗАЩИТЫ | 2014 |
|
RU2640269C2 |
| ПРОИЗВОДНЫЕ 5-АРИЛ-1Н-1,2,4-ТРИАЗОЛА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2249588C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ПАРЕНТЕРАЛЬНОГО ПРИМЕНЕНИЯ | 2001 |
|
RU2182004C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ТЕРАПЕВТИЧЕСКОГО АНТИВОСПАЛИТЕЛЬНОГО И БОЛЕУТОЛЯЮЩЕГО СРЕДСТВА ДЛЯ МЕСТНОГО НАНЕСЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2157689C2 |
| ИНГИБИТОРЫ РЕПЛИКАЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2019 |
|
RU2812128C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ НИТРОЗИЛИРОВАННЫХ ПРОПАНДИОЛОВ, КОМПОЗИЦИЙ, СОДЕРЖАЩИХ ТАКИЕ СОЕДИНЕНИЯ, И ИХ КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2830610C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ N-(4-НИТРО-2-ФЕНОКСИФЕНИЛ)-МЕТАНСУЛЬФОНАМИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2013 |
|
RU2537121C1 |
| ПРИМЕНЕНИЕ 9-ОКСОАКРИДИН-10-УКСУСНОЙ КИСЛОТЫ И/ИЛИ ЕЕ СОЛИ В КОМБИНАЦИИ С АНТИЭСТРОГЕНОМ И/ИЛИ ПРОГЕСТИНОМ ДЛЯ ЛЕЧЕНИЯ ЭСТРОГЕНЗАВИСИМЫХ ОПУХОЛЕЙ, СПОСОБ ЛЕЧЕНИЯ И НАБОРЫ | 2007 |
|
RU2346691C2 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА | 2005 |
|
RU2414468C2 |
Фармацевтический состав противовоспалительного, жаропонижающего и болеутоляющего действия содержит N-(4-нитро-2-феноксифенил)метансульфонамид (нимесулид) и 2,5-ди-О-метил-1,4:3,6-диангидро-D-глюцитол и вводится в форме внутривенных и внутримышечных инъекций, а также в жидкой форме через рот или наносится на кожу в виде кремов и мазей. Новый состав нимесулида с глюцитолом устойчив при хранении, безопасен и не имеет недостатков, присущих препаратам на основе масла. 3 с. и 13 з.п. ф-лы, 5 табл.
| US 5688829 А, 18.11.1997 | |||
| WO 9801124 А, 15.01.1998 | |||
| WO 9837879 А, 03.09.1998 | |||
| Способ получения сферических двухслойных гранул | 1977 |
|
SU782855A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ БОЛЕУТОЛЯЮЩЕГО СРЕДСТВА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2141845C1 |
Авторы
Даты
2004-10-20—Публикация
1999-09-14—Подача