Изобретение относится к области химии почв и может быть использовано для количественного определения аморфных+слабокристаллизованных соединений железа Feoкc, растворимых реактивом Тамма.
В прототипе (Воробьева Л.А., Химический анализ почв. - Изд-во МГУ, 1998, 272 с.) количество Feокс определяют следующим образом. Образец почвы обрабатывают реактивом Тамма (0.14 М С2Н2О4+0.2 М C2H8N2O4) при соотношении почва: раствор=1: 100 или 1: 50. Колба встряхивается на ротаторе. Через 1 час содержимое колбы фильтруется или центрифугируется, а раствор сливают в колбу-премник. Затем к почве снова приливают раствор Тамма и взбалтывают еще 1 час. После этого операции повторяются и новая порция раствора сливается в колбу-приемник. Единственное определение Feокс в растворе выполняют атомно-абсорбционным или фотометрическим методами.
Целью изобретения является повышение точности определения величины Feoкc и повышения воспроизводимости анализа за счет снижения погрешности, обусловленной различной неконтролируемой температурой, при который проводится определение. Изобретение позволяет результаты анализа привести к стандартной комнатной температуре Т=298К.
Способ осуществляют следующим образом. Предварительно берут два образца почвы. У первого образца почвы определяют содержание всех свободных соединений Feдит путем обработки почвы дитионит-цитрат-бикарбонатом.
Вторую образец обрабатывают реактивом Тамма при соотношении почва: раствор=1: 100 или 1: 50. Определяют температуру почвенной суспензии. Колба встряхивается на ротаторе. Через 20; 60 и 120 мин после начала опыта отбирается по 3 мл раствора, который фильтруется. Затем отбираются аликвоты объемом 0.5 мл и определяется содержание железа (Feокс) атомно-абсорбционным или фотометрическим методом.
Затем по уравнению (1): lnln [Feдит/(Feдит-Feокс)]=ln К + α ln t, где t выражено в мин, а константа ln К=α ln kопыт, определяется логарифм константы скорости растворения соединений железа ln koпыт при данной температуре почвенной суспензии.
Для того чтобы от логарифма константы растворения при данной температуре ln kопыт перейти к логарифму константы скорости при стандартной температуре Т=298К, то есть к ln k298, необходимо получить калибровочную зависимость, связывающую энергию активации Е с константой скорости ln kопыт. Для этого были выполнены кинетические эксперименты с эталонными минералами железа: гематитом α Fe2О3 и ферригидритом FeOOH 2Fe2O3·2.6H2O, а также с 3 образцами дерново-подзолистой почвы из Пермской обл. Эти кинетические эксперименты проводили при 3-х разных температурах: 288; 293 и 299К. В результате получены 15 значений логарифма констант скорости растворения ln koпыт и энергии активации Е. Между ними выявлена отрицательная корреляционная зависимость, которая описывается следующим уравнением регрессии:
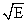 -4.75-0.44 ln kопыт.
-4.75-0.44 ln kопыт.
Коэффициент корреляции между параметрами уравнения высокий: r=0.97, достоверный при вероятности Р 99.9.
По этой калибровочной зависимости определяется энергия активации Е растворения соединений железа реактивом Тамма.
После этого по уравнению Аррениуса: ln (k298/kопыт)=Е· (Т298 - Топыт) / R· Топыт·Т298, где R - газовая постоянная (R - 8.31 Дж/моль· К), а индексы “опыт” и “298” означают температуру, при которой проводили опыт и Т=298К, подсчитывается величина логарифма константы скорости растворения минералов железа при стандартной температуре опыта: ln k298.
Используя величину логарифма константы скорости ln k298, а также - величины α и ln t (t=120 мин), из уравнения (1) определяется искомая стандартизованная величина Feокс(станд).
Пример. В дерново-подзолистой почве из Пермской обл. из гор. В1 экстракция Fe по Тамму ведется при температуре в лаборатории Топыт=288К. Необходимо установить, сколько железа из этой почвы перейдет в раствор Тамма при стандартной температуре Т298=298К, то есть - определить стандартизованную величину Fокс(станд).
Вначале берется два образца почвы. У первого образца почвы определяется содержание свободных соединений железа путем обработки дитионит-цитат-бикарбонатом по Мера-Джексону: Feдит=1.225%. Эта характеристика используется в дальнейшем при определении логарифма константы скорости растворения соединений железа ln kопыт.
Затем у второго образца почвы определяется кинетика выхода Feокс(опыт) в раствор Тамма. В табл.1 внесены исходные и преобразованные данные по кинетике выхода железа в раствор. По уравнению (1) определяется величина логарифма константы скорости растворения минералов железа ln k288.
Полученные значения ln t, обозначенные через х, и ln ln [Feдит / (Feдит – Feокс)], обозначенные через у, используются для определения коэффициентов уравнения прямой. Расчет этих коэффициентов ведется либо графоаналитическим, либо аналитическим методом, в последнем случае удобно использовать компьютер. В результате расчета получаем, что тангенс угла наклона прямой а=0.46, а отрезок на оси ординат, отсекаемый прямой In К=-3.91, следовательно, ln k=ln К: α =-3.91: 0.46=-8.5.
Теперь по калибровочной зависимости: 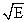 =4.75 - 0.44 ln k определяем величину энергии активации, которая равна Е=72.08 кДж/моль=72080 Дж/моль. Для подсчета логарифма новой константы скорости растворения In k298 используем уравнение Аррениуса:
=4.75 - 0.44 ln k определяем величину энергии активации, которая равна Е=72.08 кДж/моль=72080 Дж/моль. Для подсчета логарифма новой константы скорости растворения In k298 используем уравнение Аррениуса:
ln k298 - ln kопыт=Е· (Т298-Т288)/R· Т288·t298.
Следовательно,
ln k298=Е (Т298 - Т288) / R· T288·Т298 + ln kопыт=
72080(298-288) / 8.31 288· 298-8.5=-7.49.
Определяем ln К из выражения
ln К=ln k· α =- 7.49· 0.46=-3.44.
Затем подсчитываем величину ln ln [Feдит / (Feдит – Feокс)] из уравнения
ln ln [Feдит / (Feдит – Feокс)]=ln К +
α · ln t=-3.44 + 0.46· 4.79=-1.24.
Дважды потенцируя значение -1.24, получаем величину [Feдит / (Feдит – Feокс)], которая равна 1.336. Теперь определяем искомую стандартизованную величину Feокс(станд):
Feокс(станд)=Feдит (1-1/1.336)=1.225 (1-1/1.341)=0.308%.
Сравним эту величину с найденной экспериментально при Т=298К:
Feокс(298)=0.328%. Ошибка предлагаемого способа составляет m=0.328 - 0.308=0.020% или 6 отн.%. Неучет температуры в лаборатории при использовании прототипа дает гораздо более высокую ошибку: m=0.328 - 0.207=0.121% или 37 отн.%.
Как видно из табл.2, ошибка в определении Feокс в почвах и гематите α Fe2О3 по прототипу составляет 34-46 отн. %, тогда как по предлагаемому способу - всего 6-15 отн. %.
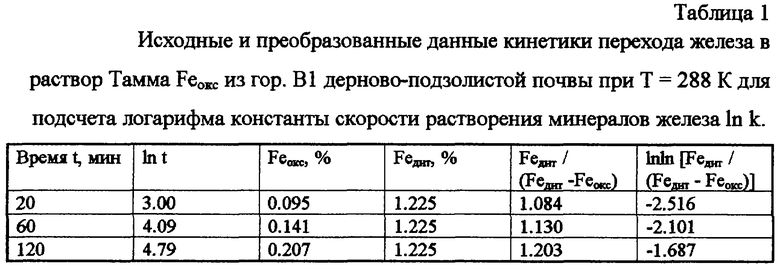
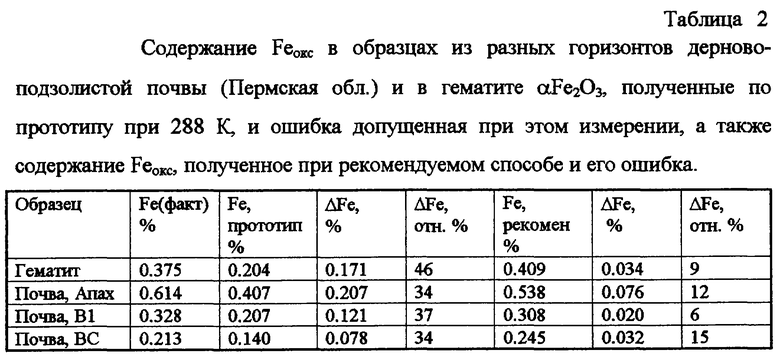
Изобретение относится к области химии почв и может быть использовано для количественного определения аморфных и слабокристаллизованных соединений железа. Способ включает обработку почв реактивом Тамма в течение 2-х часов и определение содержания железа Feокс(опыт). При определении Feокс(опыт) учитывают кинетику выхода железа в раствор и температуру почвенной суспензии. При этом дополнительно берут образец той же почвы и определяют содержание всех свободных соединений железа Feдит путем обработки почвы дитионит-цитрат-бикарбонатом. Затем подсчитывают логарифм константы скорости растворения соединений железа ln kопыт с учетом содержания в почве всех свободных соединений железа Feдит. По калибровочной зависимости 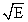 =4.75-0.44 ln kопыт определяют энергию активации Е растворения соединений железа. Далее, используя уравнение Аррениуса, определяют величину ln k298 и количество экстрагированного железа Feокс(станд) при стандартной комнатной температуре 298К. Способ позволяет повысить точность определения Feокс, снижая ошибку, связанную с неучетом температуры почвенной суспензии. 2 табл.
=4.75-0.44 ln kопыт определяют энергию активации Е растворения соединений железа. Далее, используя уравнение Аррениуса, определяют величину ln k298 и количество экстрагированного железа Feокс(станд) при стандартной комнатной температуре 298К. Способ позволяет повысить точность определения Feокс, снижая ошибку, связанную с неучетом температуры почвенной суспензии. 2 табл.
Способ определения в почве железа, включающий обработку почв реактивом Тамма в течение 2 ч и определение содержания железа Fеокс(опыт), отличающийся тем, что при определении Fеокс(опыт) учитывают кинетику выхода железа в раствор и температуру почвенной суспензии, при этом дополнительно берут образец той же почвы и определяют содержание всех свободных соединений железа Fедит путем обработки почвы дитионит-цитрат-бикарбонатом, затем подсчитывают логарифм константы скорости растворения соединений железа ln kопыт с учетом содержания в почве всех свободных соединений железа Fедит, по калибровочной зависимости 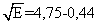 ln kопыт определяют энергию активации Е растворения соединений железа, и, наконец, используя уравнение Аррениуса, определяют величину ln k298 и количество экстрагированного железа Fеокс(станд) при стандартной комнатной температуре 298 К.
ln kопыт определяют энергию активации Е растворения соединений железа, и, наконец, используя уравнение Аррениуса, определяют величину ln k298 и количество экстрагированного железа Fеокс(станд) при стандартной комнатной температуре 298 К.
| ВОРОБЬЕВА Л.А | |||
| Химический анализ почв | |||
| Изд-во МГУ, 1998, с.55 | |||
| Способ определения железа | 1989 |
|
SU1737317A1 |
| Способ определения железа | 1989 |
|
SU1732224A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕХНОГЕННОЙ ЗАГРЯЗНЕННОСТИ ПОЧВЕННОГО ПОКРОВА ТЯЖЕЛЫМИ МЕТАЛЛАМИ ГРУППЫ ЖЕЛЕЗА (ЖЕЛЕЗО, КОБАЛЬТ, НИКЕЛЬ) | 1998 |
|
RU2133487C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) И АЛЮМИНИЯ (III) В КИСЛЫХ РАСТВОРАХ | 1993 |
|
RU2043629C1 |
| DE 3225374, 12.01.1984. | |||
Авторы
Даты
2004-11-10—Публикация
2002-12-17—Подача