Изобретение относится к области медицины, конкретно к экспериментальной медицине, и касается способа моделирования энцефалопатии и связанных с ней нарушений в системе крови.
Известны способы моделирования разнообразных гапоксических состояний [1], известны физиологические нарушения и изменения в системе крови, вызванные гипоксическим воздействием, однако по своим проявлениям они являются непосредственным следствием гипоксического воздействия и носят адапативный характер [2].
Наиболее близким способом моделирования постгипоксической энцефалопатии (прототип) является способ моделирования постгипоксической энцефалопатии, получаемой путем однократного помещения животных в гермокамеру до начала агонального судорожного припадка или остановки дыхания [3].
Однако при данном способе моделирования посгипоксической энцефалопатии достоверно наблюдаются лишь отсроченные нарушения когнитивных функций без развития явлений дизадаптации и нарушения регуляции физиологических функций, характерных для энцефалопатии, наблюдаемой в клинической практике. Со стороны системы крови при этом способе отмечаются компенсаторно-приспособительные реакции, носящие явно адаптивный характер. Способы моделирования постгипоксической энцефалопатии с явлениями дизадаптации не известны и связанные с ней нарушения в системе кроветворения не описаны.
Задачей, решаемой данным изобретением, является максимальное приближение экспериментальной модели постгипоксической энцефалопатии к энцефалопатии человека.
Поставленная задача достигается тем, что лабораторные животные (мыши или крысы) подвергаются двукратному гипоксическому воздействию в условиях гипоксии гермобъема до появления агонального судорожного припадка или остановки дыхания с интервалом между двумя гипоксическими воздействиями в 5-60 минут.
Новым в предлагаемом изобретении является то, что постгипоксическая энцефалопатия моделируется путем двукратного нанесения гипоксического воздействия в условиях гипоксии гермобъема до наступления агонального судорожного припадка или остановки дыхания с интервалом между воздействиями в 5-60 минут.
Авторами не найдено в проанализированной литературе способа моделирования постгипоксической энцефалопатии путем двукратного нанесения гипоксического воздействия в условиях гипоксии гермобъема до наступления агонального судорожного припадка или остановки дыхания с интервалом между воздействиями в 5-60 минут.
Сравнение предлагаемого изобретения с существующими способами моделирования гипоксических состояний (однократным гипоксическим воздействием) показало, что впервые предложено моделировать постгипоксическую энцефалопатию с вызываемыми ей нарушениями кроветворной функции путем двукратного гипоксического воздействия в условиях гипоксии гермобъема до агонального судорожного припадка или остановки дыхания с интервалами между воздействиями в 5 -60 минут. Не смотря на то, что в литературе известно создание постгипоксической энцефалопатии путем однократного воздействия, фактор двукратного воздействия с получением желаемого результата, для специалиста не является очевидным. Эксперимент показал непредсказуемые результаты.
Таким образом, заявленное изобретение соответствует критериям изобретения “Новизна” и “Изобретательский уровень”, так как оно явным образом не следует для специалиста из уровня техники. Предлагаемое изобретение соответствует критерию “Промышленно применимо”, так как оно с успехом может использоваться в экспериментальной медицине (физиологии, патологической физиологии, фармакологии) для моделирования патологических состояний человека и животных.
Гипоксия, как типовой патологический процесс, сопровождает практически все известные заболевания. Проблеме повреждающего воздействия недостатка кислорода посвящено множество работ, однако, до сих пор, остаются не изучеными многие аспекты патогенеза состояний, проявляющихся после аноксии. Выраженное энергетическое голодание, как следствие окислительной недостаточности, приводит к накоплению в мозге лактата, ионов аммония, ацетил-коэнзима А и др., в частности нейромедиаторов, перераспределению ряда ионов (калий, натрий, кальций, хлор) и воды между вне и внутриклеточными секторами, появлению свободных радикалов и веществ, способных усилить образование свободных радикалов в период реоксигенации. Существенным структурно-функциональным изменениям при гипоксии сопутствует нарушение деятельности интегративных систем (в первую очередь ЦНС) и формирование качественно нового паттерна их взаимодействия. При тяжелом гипоксическом воздействии формируется длительно существующая декомпенсация механизмов адаптации, что предопределяет патогенное влияние вновь сложившегося функционального континиума внутренней среды на другие органы. Данное обстоятельство является одним из основных факторов развития различных нарушений жизнедеятельности организма, перенесшего гипоксическую травму.
Способ осуществляют следующим образом.
Животное помещают в гермокамеру, закрывают крышкой и оставляют до появления агонального судорожного припадка или остановки дыхания, затем извлекают животное из гермокамеры и после восстановления самостоятельного дыхания через 5-60 минут животное вновь помещают в гермокамеру до наступления агонального судорожного припадка или остановки дыхания.
Предлагаемый способ был изучен в экспериментах на животных мышах-самцах линии CBA/CaLac в количестве 540 штук, массой 18-20 г. Животные 1 категории, конвенциональные линейные мыши, получены из питомника отдела экспериментального биомедицинского моделирования НИИ фармакологии ТНЦ СО РАМН (сертификат имеется).
Пример 1
Способ осуществлялся следующим образом. Гипоксическое воздействие моделировалось с помощью гермокамеры объемом 500 мл. Мыши помещались в гермокамеру, крышка закрывалась и мыши оставались там до агонального судорожного припадка или остановки дыхания, определяемой визуально, в течение 10-15 секунд. После извлечения из гермокамеры и восстановления самостоятельного дыхания, через 5-60 минут, мыши вновь помещались в гермокамеру также до наступления агонального состояния (генерализованного судорожного припадка или остановки дыхания).
Пример 2
Способ прототип. Гипоксическое воздействие моделировалось также с помощью гермокамеры объемом 500 мл. По способу прототипу мыши подвергались однократному гипоксическому воздействию.
Оценка состояния центральной нервной системы животных производилась по условно-рефлекторной деятельности и ориентировочно-исследовательскому поведению в открытом поле. Состояние висцеральных систем оценивалось на примере системы крови.
Через 3 часа после извлечения из гермокамеры (при исследовании по заявляемому способу - после повторного извлечения из гермокамеры) у мышей вырабатывался условный рефлекс пассивного избегания [4] проверка сохранности рефлекса осуществлялась через 24 часа, на 14, 21 сутки после выработки. На 1, 3, 7, 14 и 21 сутки после гипоксической травмы производилась регистрация ориентировочно-исследовательского поведения в открытом поле [5]. Для подтверждения наличия висцеральных нарушений у мышей, подвергнутых гипоксии по способу-прототипу и предлагаемому способу, на 1-10, 14, 21 сутки определяли показатели периферической крови, костно-мозгового кроветворения, осмотическую резистентнось эритроцитов, с 1-х по 10-е сутки содержание клеток-предшественников в костном мозге, их пролиферативную активность и интенсивность дифференцировки, а также продукцию гуморальных гемопоэтических факторов отдельными фракциями гемопоэзиндуцирующего микроокружения и структурно-функциональную организацию костного мозга [6]. Обработку результатов проводили методом вариационной статистики с использованием t-критерия Стьюдента и непараметрического U-критерия Вилкоксона-Манна-Уитни [7].
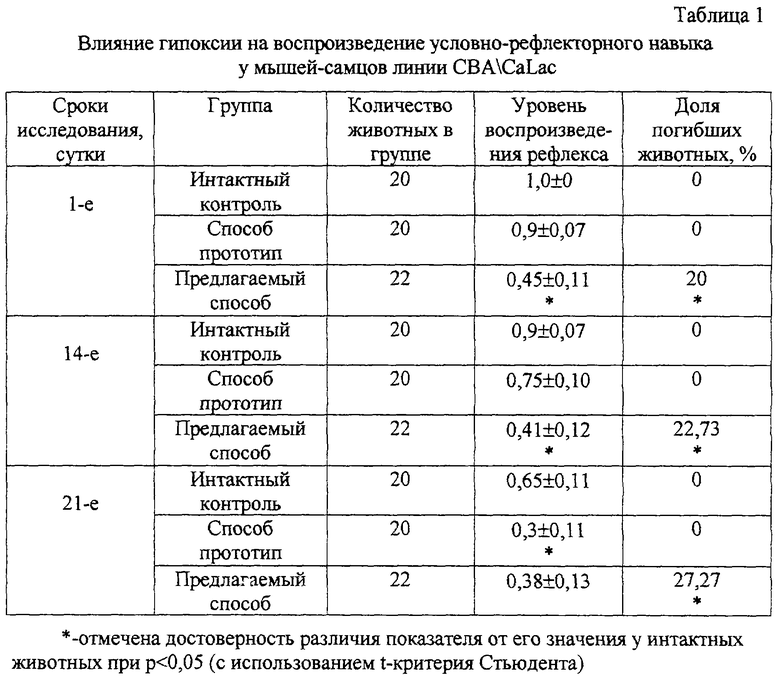
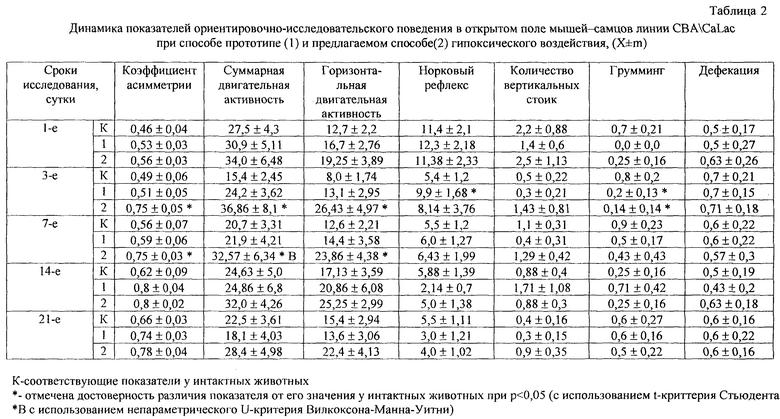
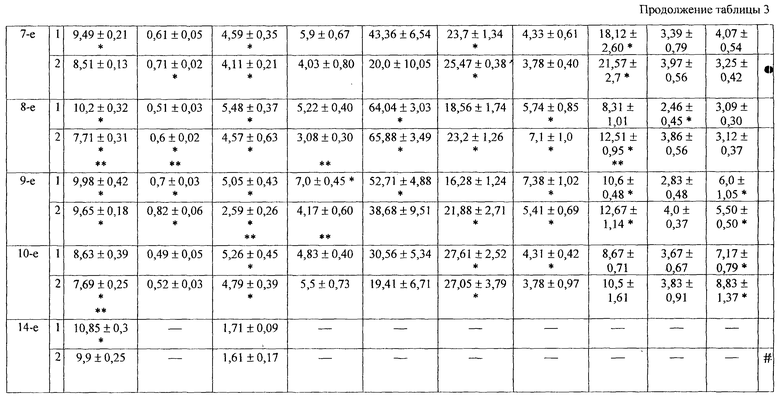
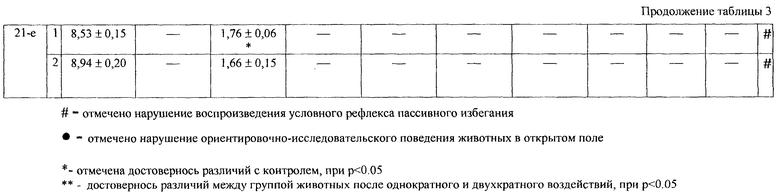
Результаты исследования. В случае использования способа прототипа (однократное воздействие) не регистрировалось достоверных изменений психоневрологического статуса (таблица 1, 2). Предлагаемый способ (двукратное помещение мышей в камеру с промежутком в 5-60 минут) с первых суток приводил к формированию энцефалопатии, которую регистрировали по развитию амнезии при воспроизведении условного рефлекса пассивного избегания и нарушению ориентировочно-исследовательского поведения в открытом поле (таблица 1, 2).
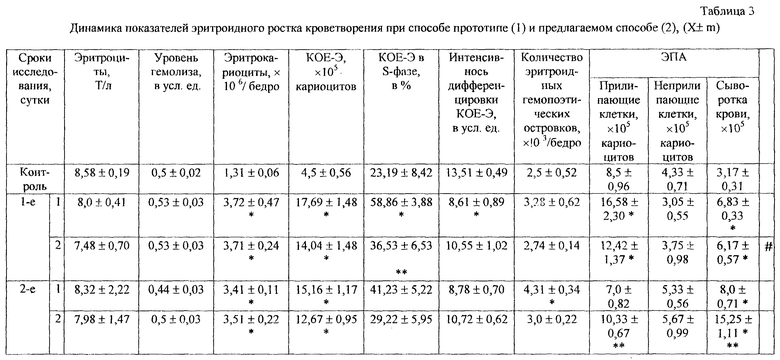
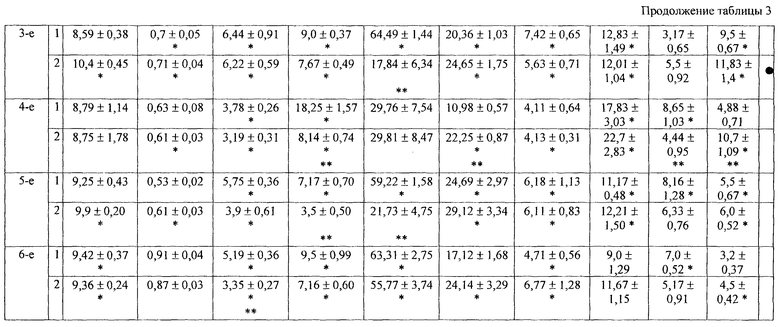
В ходе эксперимента гипоксия гермообъема, вызванная по способу-прототипу приводила к гиперплазии костно-мозгового кроветворения. Так, отмечалось увеличение содержания эритрокариоцитов, в гемопоэтической ткани, количество ретикуло-, эритро-кариоцитов в периферической крови. Этому предшествовало усиление выхода КОЕ-Э, увеличение пролиферативной активности и интенсивности дифференцировки прекурсоров в результате повышения поступления продуктов распада эритроцитов, секреции ЭПА клеточными компонентами ГИМ и возрастания способности макрофагальных элементов формировать эритроидные ГО (таблица 3).
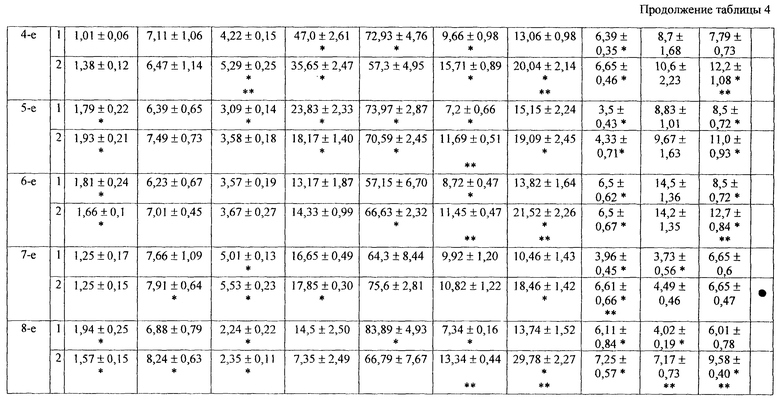
Реакция грануломоноцитарного ростка была не столь однозначной. Наблюдалось накопление незрелых нейтрофильных гранулоцитов в костном мозге, повышение числа КОЕ-ГМ и возрастание темпа их деления под влиянием возрастания уровней КСА в кондиционных средах прилипающих клеток и сыворотки крови при нарушении реализации дифференцировочных потенции КОЕ-ГМ и сохранении числа зрелых форм нейтрофильных гранулоцитов в кроветворной ткани на уровне не превышающем исходных значений и снижение числа сегментоядерных нейтрофилов в периферической крови (таблица 4).
Таким образом, однократное воздействие (способ прототип) приводило к активации локальных и дистантных механизмов гемопоэза и стимуляции преимущественно эритроидного ростка кроветворения. Описанные изменения носят ярко выраженный адаптивный характер.
Развитие постгипоксической энцефалопатии, полученной предлагаемым способом сопровождалось снижением числа костно-мозговых КОЕ-Э, их пролиферативной активности и падению количества эритрокариоцитов в костном мозге, несмотря на увеличение ЭПА в биологических жидкостях и ускорения дифференцировки клеток-предшественников, а также развитием гемолитической анемии в поздние сроки исследования (таблица 3). Кроме того, регистрировалось повышение индекса созревания КОЕ-ГМ за счет увеличения концентрации КСА в сыворотке крови и кондиционных средах миелокариоцитов и образования клеточных ассоциаций гранулоцитарного типа, что, в свою очередь, сопровождалось накоплением зрелых нейтрофильных гранулоцитов в костном мозге и нейтрофильным лейкоцитозом в периферической крови (таблица 4).
Таким образом, гипоксия, полученная по заявляемому способу, предопределяет развитие значительных расстройств высшей нервной деятельности, которое оказывается тесно связанным с нарушениями адаптивных реакций гемопоэза, выражающимися в повреждении кроветворных прекурсоров при сохранении функциональной активности относительно резистентных стромальных компонентов ГИМ, расширении плацдарма костно-мозгового грануломоноцитопоэза и снижении образования полноценных эритроцитов.
Предлагаемый способ позволяет максимально приблизить модели экспериментальной энцефалопатии к клинической картине, наблюдаемой при энцефалопатии у человека.
Литература
1. Методические рекомендации по скринигу и доклиническому испытанию антигипоксических средств./Ю.Г.Бобков, А.С.Лосев и др. М., 1989,-20 с.
2. Ястребов А.П., Юшков Б.Г., Большаков В.Н. Регуляция гемопоэза при воздействии на организм экстремальных факторов. -Свердловск, 1988,-153 с.
3. Першина О.В., Суслов Н.И., Провалова Н.В., Скурихин Е.Г., Зюзьков Г.Н., Минакова М.Ю. Влияние препаратов природного происхождения на систему крови и когнитивные функции при гипоксическом воздействии.//Бюллетень экспериментальной биологии и медицины. –2002,-приложение 1,-с. 27-30.
4. Буреш Я., Бурешова О., Хьюстон Дж. П. Методики и основные эксперименты по изучению мозга и поведения./пер. с англ. Под ред проф. А.С. Батуева).-М.: Высшая школа, 1991,-398 с.
5. Walsh R.N., Cummins R.A. The open-field test: a critical review. // Psychol. Bull.-1976, V.83.-P. 482-504.
6. Гольдберг Е.Д., Дыгай A.M., Шахов В.П. Методы культуры ткани в гематологии. –Томск, 1992.-272 С.
7. Лакин Г.Ф. Биометрия. -М.: Высшая школа, 1973,-215 с.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ЭРИТРОПОЭЗА ПРИ ЭКСПЕРИМЕНТАЛЬНОЙ ЭНЦЕФАЛОПАТИИ | 2005 |
|
RU2302664C2 |
| СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ЭРИТРОПОЭЗА ПРИ ЭКСПЕРИМЕНТАЛЬНОЙ ГИПОКСИИ | 2005 |
|
RU2285300C1 |
| СПОСОБ ЭКСПЕРИМЕНТАЛЬНОЙ ТЕРАПИИ ЭНЦЕФАЛОПАТИИ | 2004 |
|
RU2284060C1 |
| СПОСОБ УСИЛЕНИЯ МОБИЛИЗАЦИИ СТВОЛОВЫХ КЛЕТОК | 2006 |
|
RU2330674C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГЕМОСТИМУЛИРУЮЩИМ, АНТИМУТАГЕННЫМ, ПРОТИВООПУХОЛЕВЫМ, ЦЕРЕБРОПРОТЕКТОРНЫМ, АНТИГИПОКСИЧЕСКИМ, НООТРОПНЫМ, АНКСИОЛИТИЧЕСКИМ И ПРОТИВОНЕВРОТИЧЕСКИМ ДЕЙСТВИЕМ | 2010 |
|
RU2438691C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦЕРЕБРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2501562C1 |
| ЦЕРЕБРОПРОТЕКТОРНОЕ СРЕДСТВО | 2013 |
|
RU2517282C1 |
| АНТИГИПОКСИЧЕСКОЕ СРЕДСТВО | 1996 |
|
RU2121357C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ И АДАПТОГЕННЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2136292C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГИПОКСИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ | 2003 |
|
RU2253152C2 |
Изобретение относится к области медицины, конкретно к экспериментальной медицине, и касается способа моделирования энцефалопатии и связанных с ней нарушений в системе крови. Лабораторным животным наносят дважды с интервалом между воздействиями 5-60 минут гипоксическое воздействие с помощью гермокамеры до появления агонального судорожного припадка или остановки дыхания. Способ позволяет приблизить экспериментальную модель постгипоксической энцефалопатии к энцефалопатии человека. 4 табл.
Способ моделирования постгипоксической энцефалопатии и связанных с ней нарушений в системе крови, включающий нанесение гипоксического воздействия с помощью гермокамеры до появления агонального судорожного припадка или остановки дыхания, отличающийся тем, что гипоксическое воздействие наносят двукратно с интервалом между воздействиями 5-60 мин.
| ПЕРШИНА О.В | |||
| и др | |||
| Влияние препаратов природного происхождения на систему крови и когнитивные функции при гипоксическом воздействии | |||
| Бюллетень экспериментальной биологии и медицины, 2002, 1, с.27-30 | |||
| Способ моделирования энцефалопатии | 1978 |
|
SU767820A1 |
| СПОСОБ ЭКСТРАКОРПОРАЛЬНОЙ РЕГЕНЕРАЦИИ ПЛАЗМЫ ПОСЛЕ ПЛАЗМАФЕРЕЗА | 1993 |
|
RU2033190C1 |
Авторы
Даты
2004-11-20—Публикация
2003-02-27—Подача