Изобретение относится к химии стероидов, касается новых химических соединений - 3-OR-ди-(2-хлорэтил)аминосодержащих 11-альфа-ацил(гидр)оксистероидов, обладающих противоопухолевой активностью.
Область применения - медицина с использованием предмета изобретения в качестве потенциальных препаратов - гормоноцитостатиков для лечения гормонозависимых опухолей, а также биология и биохимия, где заявляемые соединения могут быть использованы как химические реагенты на нуклеиновые кислоты [Кнорре Д.Г, Власов В.В. // Биоорг. Хим. 1992. Т. 18. С. 1330-1340].
Известно использование стероидных гормонов, содержащих цитотоксическую группировку (гормоноцитостатики) в онкологии для лечения гормонозависимых опухолей [Sof''ina Z.P., Lagova N.D. // Sov. Med. Rev. Oncol. 1992. V. 4. Р. 1-55] . Наиболее широко в качестве гормоноцитостатиков применяются производные стероидных гормонов, содержащие группировку ди-(2-хлорэтил)амина. Такого рода соединения (аналоги изобретения) известны во всех важнейших рядах стероидных гормонов - андрогенов, эстрогенов, гестагенов и кортикостероидов [Nilsson Т. , Jonsson G. // Cancer Chemother.Rep. 1975. V. 59. Р. 229-232. Пат. 55-89299 (1980). Япония. РЖХим. 1982. 50188П].
Известны препараты на основе эфиров природного гормона эстрадиола с ди-(2-хлорэтил)аминомуравьиной кислотой ЭСТРАЦИТ, ЭСТРАМУСТИН, БУСТРАМУСТИН [Kubota Т.К., Yamada Y., Oka S., Enomoto K. // Jap.J.Cancer Res. 1988. V.79. Р. 1224-1229; Cytotoxic Estrogens in Hormone Receptive Tumors. Ed. J.Raus. London, New York. 1980. P. 245-269]. При этом одним из наиболее эффективных средств при лечении рака предстательной железы считается противоопухолевый препарат ЭСТРАЦИТ, обладающий эстрогенной активностью.
Гормоноцитостатики, цитированные в примерах аналогов и прототипа - эстрацита, получены на основе природных гормонов, что обусловливает гормональную активность гормоноцитостатиков. Это их свойство, особенно для половых гормонов, является нежелательным при клиническом применении. Известно, что на основе природных стероидов невозможно создание гормоноцитостатиков с антигормональным действием. Между тем, учитывая противоопухолевое действие антигормонов (антиэстрогенов, антиандрогенов) [Машковский М.Д. // Лекарственные средства. Москва. Медицина. Т.2. С. 549-552. Namer М. // J. Steroid Biochem. 1988. V. 31. Р. 719-730], можно рассчитывать, что такого рода соединения будут обладать высокой противоопухолевой активностью в результате сочетания цитотоксического эффекта с антигормональным.
С целью создания противоопухолевых стероидов, необладающих гормональной активностью, а также проявляющих антигормональное действие, предлагаются 3-OR-ди-(2-хлорэтил)аминосодержащие стероиды общей формулы I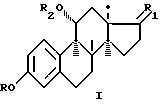
где R = COCH2C6H4N(CH2CH2Cl)2;
R2 = H(а), COH (б,г), COCH3 (в).
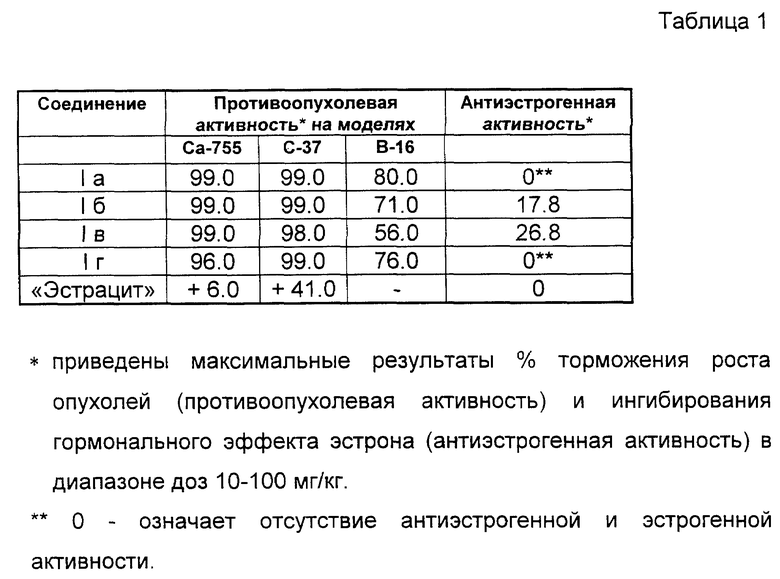
Заявляемые соединения обладают противоопухолевой активностью. При этом соединения (I б, в) проявляют антиэстрогенный эффект и обладают наиболее выраженным противоопухолевым действием. Соединения (I а,г) гормонально не активны. В таблице 1 приведены данные изучения противоопухолевого действия соединений (I а-г) на трех моделях опухолей мышей: аденокарциноме молочной железы Ca-755, саркоме C-37 и меланоме B-16.
Как следует из таблицы 1, заявляемые вещества обладают широким диапазоном действия и проявляют высокую противоопухолевую активность на всех трех видах опухолей. На аденокарциноме Ca-755 и саркоме C-37 заявляемые вещества тормозят рост опухолей на 98-99% (C-37) и 96-99% (Ca-755). Взятый для сравнения препарат "эстрацит" оказался неэффективным, более того его введение стимулировало рост опухолей C-37 и Ca-755 (знак + означает стимуляцию роста опухоли).
Существенно, что соединения (I б) и (I в) на аденокарциноме вызывают излечение подопытных животных в 28,5% и 12,5% случаев, соответственно.
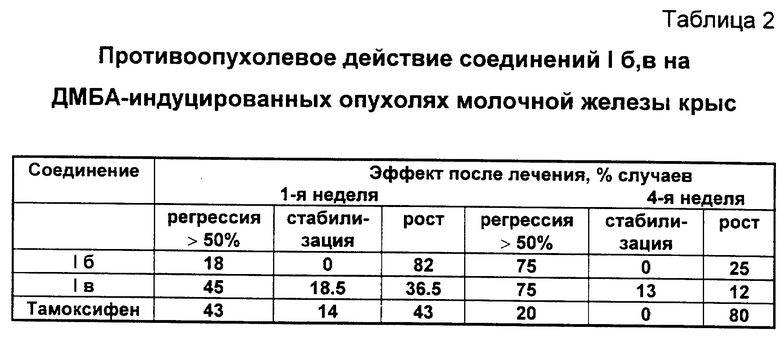
В таблице 2 представлены данные противоопухолевой активности соединений (I б, в) на ДМБА-индуцированных опухолях молочной железы крыс в сравнении с известным противоопухолевым препаратом антиэстрогенного действия "тамоксифеном", что обусловило его применение в качестве "препарата сравнения".
Соединение (I в) после 30-дневного введения вызывает регрессию опухолей в 45% случаев, то есть на уровне тамоксифена. Однако, в отличие от него, это вещество обладает выраженным пролонгированным действием. По терапевтическому эффекту через 4 недели (I в) превосходит тамоксифен в 3,75 раза. Соединение (I б) по длительности действия также превосходит тамоксифен.
Таким образом, из сравнения заявляемых веществ с прототипом - эстрацитом и аналогами можно констатировать, что впервые реализованное в структуре заявляемых веществ объединение ди-хлорэтиламиносодержащего заместителя и 11α-гидр(ацил)окси группы определяет положительный эффект и соответствует критерию "существенное отличие". Заявляемые вещества отвечают критерию "новизны" как впервые синтезированные.
Исследование токсичности заявляемых веществ на мышах BDF показало их сильное различие. Наиболее активные противоопухолевые стероиды (I б, в) не проявляют токсических свойств в суммарных дозах 500 мг/кг и 125 мг/кг, соответственно. Соединение (I г) также нетоксично в дозе 125 мг/кг, тогда как соединение (I а) проявляет токсичность в суммарной дозе 75 мг/кг. При пересчете на человека ежедневная доза соединения (I а) составляет 88 мг, что в 2 раза превосходит терапевтическую дозу тамоксифена.
Заявляемые соединения могут быть получены из синтезированных известным способом [Ржезников В. М. // А.С. 1395639 (1988). СССР. Б.И. 1988. N. 18] 11α-гидроксистероидов формулы (II) и их соответствующих 11-ацильных производных (где R1 и R2 аналогичны заместителям для формулы I), реакцией с п-[ди- (2-хлорэтил)]аминофенилуксусной кислотой (ХАФК) в присутствии дициклогексилкарбодиимида (ДЦК) и 4-диметиламинопиридина (ДМА).
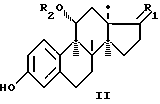
где 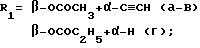
R2 = H(а), COH (б,г), COCH3 (в).
Примеры конкретных решений
Общий метод получения 3-п-[ди-(2-хлорэтил)]аминофенилацетоксистероидов формулы (I):
Смесь 1,0 ммоля стероида (II) в CH2Cl2 перемешивают при 20oC с 1,5 ммол (ХАФК), 1,6 ммол (ДЦК) и 1,7 ммол (ДМА) в течение 1,5 - 20 ч (контроль с помощью ТСХ). Желтый раствор после отделения дициклогексилмочевины промывают последовательно 4 н. HCl и 1 н. NaHCO3, сушат Na2SO4. Остаток после удаления растворителя хроматографируют на SiO2, выделяя продукт смесью бензол-этилацетат 10:1.
Пример 1. 3-п-[ди-(2-хлорэтил)] аминофенилацетокси-11α- гидрокси-17β-ацетокси-17α-этинилэстра-1,3,5(10)-триен (Ia)
1,55 г Стероида (IIа) в 50 мл CH2Cl2 обрабатывают ХАФК, ДЦК и ДМА 6 ч, как описано выше, и хроматографируют на 15 г SiO2. Получают 1,22 г (45,5%) соединения (I а) в виде бесцветной пены. [α]D -70o (с 0,92, CHCl3), УФ-спектр λмакс, нм (Ig E): 260,5 (4,47), 298 (3,42). ИК-спектр, KBr. см-1: 3450-3470 (ОН); 3295 (C≡CH); 1740, 1230-1240 (OAc, OCyt); 1485, 1515, 1615 (ар. ). ПМР-спектр, CDCl3, м.д.: 0,87 (с, 3Н, 18-CH3); 2,04 (с, 3Н, OAc); 2,63 (с, 1Н, C≡CH); 4,2 (м, 1Н, J = 10 и 5 Гц, 11-Н); 3,66 и 3,72 (уш.с, 10H, N(C2H4Cl)2 и COCH2Ph); 6,60 - 8,06 (м, 7Н, Hар). Найдено, %: C 66,90; H 6,82; Cl 11,57. C34H39NO5Cl2. Вычислено, %: C 66,65; H 6,41; Cl 11,59.
В реакции образуется также 23% диэфира I [R=R2=COCH2C6H4N(C2H4Cl)2].
Пример 2. Ацетат (I в).
0,32 г Стероида (I а) ацетилируют 2 мл смеси уксусный ангидрид-пиридин (1: 1) при 20oC, 16 ч. Выделенный обычной обработкой продукт очищают фильтрованием бензольного раствора через SiO2, получают 0,27 г (79% на I а; 36% на II а) ацетата (I в) в виде бесцветного порошка. Аналитический образец: т. пл. 148-150oC (эфиp). [α]D -80,1o, (c 0,89, CHCl3). УФ-спектр*: 261 (4,34). ИК-спектр*, CCl4, см-1: 3320 (C≡CH); 1740-1750, 1235-1240; 1495, 1520, 1618. ПМР-спектр±: 0,935 (с, 3Н); 2,04 (с, 3Н); 2,08 (с, 3Н, 11-ОАс); 2,66 (с, 1Н); 3,67 и 3,75 (уш.с., 10Н); 5,40(м, 1Н, J = 10 и 5 Гц, 11-Н); 6,67-7,26 (м, 7Н). Найдено, %: C 65,84; H 6,20; Cl 10,63. C36H41NO6Cl2. Вычислено, %: C 66,04; H 6,30; Cl 10,84.
Пример 3. Формиат (I б).
0,38 г Формиата (II б) в 25 мл CH2Cl2 обрабатывают ХАФК, ДЦК и ДМА, как описано выше, 6 ч и получают 0,35 г (55,5%) бесцветных кристаллов соединения (I б). Аналитический образец: т. пл. 130-131,5oC (эфир). [α]D -88,1o; (с 0,70, CHCl3). УФ-спектр*: 260,5 (4,38); 297 (перегиб) (3,39). ИК-спектр*: 3285; 1730-1750, 1240; 1496, 1525, 1620. ПМР-спектр+: 0,94 (с, 3Н); 2,04 (с, 3Н); 2,65 (с, 1Н); 3,67 и 3,73 (уш.с, 10Н); 5,5 (м, 1Н, J = 10 и 5 Гц); 6,66 - 7,25 (м, 7Н); 8,14 (с, 1Н, OCOH). Найдено, %: C 65,58; H 6,43; Cl 11,15. C35H39NO6Cl2. Вычислено, %: C 65,62; H 6,13; N 11,08.
Пример 4. 3-[ди-(2-хлорэтил)]аминофенилацетокси-11α- формилокси-17β-пропионилоксиэстра-1,3,5(10)-триен (I г).
0,37 г Формиата (II г) в 20 мл CH2Cl2 обрабатывают ХАФК, ДЦК и ДМА 24 ч и получают 0,52 г (82,5%) формиата (I г) в виде бесцветной пены. [α]D - 65,5o (с 0,61, CHCl3); УФ-спектр*: 261 (4,55). ИК-спектр*: 1720-1740, 1240, 1185, 1497, 1525, 1620. ПМР-спектр*: 0,84 (с, 3Н); 1,13 (т., 3Н, J = 7,7 Гц, OCOCH2CH3); 3,66 и 3,72 (уш.с., 10Н); 4,76 (т, 7Н, J = 8,0 Гц, 17-Н); 5,54 (м, 7Н, J = 10 и 5 Гц, 11-Н); 6,60-7,35 (м, 7Н); 8,09 (с, 1Н). Найдено, %: C 64,91; H 7,05; Cl 11,35. C34H41NO6Cl2. Вычислено, %: C 64,75; H 6,55; Cl 11,26.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ НЕОПЕРАБЕЛЬНЫХ БОЛЬНЫХ ПЛОСКОКЛЕТОЧНЫМ РАКОМ ЛЕГКОГО | 2000 |
|
RU2185206C2 |
| СТЕРОИДНЫЕ ЭФИРЫ N-ДИ(2-ХЛОР-ЭТИЛ)-АМИНОФЕНИЛ-N-АЦЕТИЛАЛАНИНА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ, АНДРОГЕННОЙ И АНАБОЛИЧЕСКОЙ АКТИВНОСТЬЮ | 1984 |
|
SU1266111A1 |
| Сложные моноэфиры 5 @ -андростандиола-3 @ ,17 @ ,проявляющие противоопухолевую и гормональную активность | 1983 |
|
SU1361152A1 |
| СПОСОБ ФОРМИРОВАНИЯ КУЛЬТИ БРОНХА | 1994 |
|
RU2076642C1 |
| СПОСОБ КАЧЕСТВЕННОГО И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ В СЛОЖНЫХ СМЕСЯХ И ЭКСТРАКТАХ НИТРОПРОИЗВОДНЫХ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ, ИМЕЮЩИХ ФОСФОРЕСЦЕНЦИЮ В ЗАМОРОЖЕННЫХ РАСТВОРАХ | 1997 |
|
RU2122199C1 |
| 11-Дезокси-17 @ -окси-21- @ п-ди(2-хлорэтил)аминофенилацетат @ кортикостерон,проявляющий противоопухолевую активность | 1979 |
|
SU1249022A1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 1998 |
|
RU2128042C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ЗАПУЩЕННЫМ И РЕЦИДИВНЫМ РАКОМ ПРЯМОЙ КИШКИ | 2000 |
|
RU2185208C2 |
| СПОСОБ ПОЛУЧЕНИЯ N (2-ХЛОРЭТИЛ)- N НИТРОЗО-L-ГОМОЦИТРУЛЛИНА ИЛИ N (2-ХЛОРЭТИЛ)- N НИТРОЗО-2-ГОМОЦИТРУЛЛИНА ДЛЯ ИНЪЕКЦИЙ | 1995 |
|
RU2111742C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2292209C2 |
Изобретение относится к химии стероидов и касается конкретно 3-OR-ди-(2-хлорэтил)аминосодержащих 11α-ацил(гидр)оксиcтероидов, обладающих противоопухолевой активностью общей формулы (I), где R = COCH2C6H4N(CH2CH2Cl)2; R1 = β-OCOCH3 + α-C≡CH; β-OCOC2H5 + α-H; R2 = H, OCOH, COCH3. Заявляемые вещества представляют интерес для медицины. Описываются новые типы противоопухолевых соединений, обладающих цитотоксическим и антиэстрогенным действием, а также цитотоксические соединения, не проявляющие побочного эстрогенного действия. 2 табл.
3-OR-ди-(2-Хлорэтил)аминосодержащие 11α-ацил(гидр)оксистероиды общей формулы I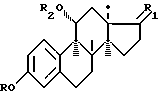
где R = COCH2C6H4N(CH2CH2Cl)2;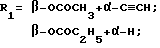
R2 = H, OCOH, COCH3,
обладающие противоопухолевой активностью.
Авторы
Даты
1999-10-10—Публикация
1998-04-07—Подача