Изобретение относится к молекулярной биологии, биотехнологии и касается сухой амплификационной смеси реагентов для полимеразной цепной реакции (ПЦР) и способа проведения ПЦР-анализа и может быть использовано в ветеринарии, медицине, пищевой промышленности и других областях, связанных с исследованием ДНК.
ПЦР представляет собой многократно повторяющиеся в условиях in vitro циклы синтеза определенной области ДНК (амплификацию), приводящие к экспоненциальному увеличению количества фрагмента ДНК, ограниченного двумя олигонуклеотидными праймерами. Для проведения ПЦР готовят амплификационную реакционную смесь, в которую добавляют анализируемую ДНК для ее амплификации, с последующей визуализацией амплифицированных нуклеотидных последовательностей.
Амплификационная смесь включает: ДНК-полимеразу, раствор дезоксинуклеозидтрифосфатов (dNTP), праймеры и буферный раствор, содержащий Tris-HCl для поддержания рН среды (около 8,0), KCl и (NH4)2SO4 для стабилизации ДНК-полимеразы и dNTP, и MgCl2 для активирования ДНК-полимеразы.
Смесь готовят непосредственно перед проведением ПЦР путем смешивания компонентов, которые хранят в виде водных растворов при низкой температуре (-20°С). Длительное хранение, а также многократное замораживание и оттаивание часто приводят к потере активности реагентов, а при смешивании компонентов смеси появляется вероятность попадания экзогенной ДНК и, как следствие, ложноположительных результатов.
Для сохранения реакционной активности реагентов для ПЦР и увеличения срока хранения при температурах выше 0°С применяют лиофилизацию. Лиофильно высушивают либо отдельные реагенты, например dNTP (US 5763157, С 07 Н 021/00, 1995), либо смесь реагентов (US 6153412, С 12 Р 19/34, 2000), используя при этом специальные вещества - стабилизаторы. Так для стабилизации растворов ДНК-полимеразы и dNTP применяют желатин, бычий сывороточный альбумин (BSA), (NH4)2SO4, тезит, полиэтиленгликоль-8000 (PEG-8000), полиолы, а также неионные детергенты NP40, TritonX-100 и Tween20 (Science, 239:487-491, 1988). Для сохранения реакционной активности смеси в нее перед лиофилизацией добавляют глюцитол, глюкозу, фиколл, сахарозу (US 5861251, С 12 Р 19/34, 1999; US 6153412, С 12 Р 19/34, 2000).
При использовании трегалозы высушенная смесь для ПЦР сохраняет свойства до 1 года при температуре хранения +4°С и +20°С (J. Clin. Microbiol., 1998, V.36(6), p.1798-1800).
Высокая специфичность и чувствительность позволяют использовать ПЦР для анализа нуклеотидных последовательностей и секвенировании генов, для генотипирования и ДНК-маркирования, для диагностики наследственных и инфекционных заболеваний, для определения пола человека и идентификации личности, для обнаружения генетически модифицированных организмов и чужеродного генетического материала в продуктах питания.
Для каждого вида исследования используют специфичные олигонуклеотидные праймеры, которые ограничивают амплифицируемый участок ДНК. Как правило, готовые амплификационные смеси содержат специфичные праймеры, необходимые для каждого вида анализа (J. Clin. Microbiol., 1998, V.36(6), p.1798-1800). Так при тестировании организмов-возбудителей, относящихся к разным систематическим группам, необходимо иметь готовые ПЦР-смеси на каждый вид возбудителя, которые будут различаться только по входящим в них специфичным праймерам. Это повышает стоимость единичного анализа, затрудняет проведение серийных исследований и ограничивает использование готовых сухих ПЦР-смесей.
В качестве ближайшего аналога выбрана амплификационная смесь, описанная в патенте US 6153412, С 12 Р 19/34, 2000, представляющая собой лиофильно высушенную смесь водных растворов реагентов для ПЦР. В ее состав входят: 10 mM Tris-HCl (pH 8,3), 40 mM KCl, 1,5 mM MgCl2, ДНК-полимераза, смесь дезоксинуклеозидтрифосфатов (dATP, dTTP, dGTP, dCTP no 250 mM каждого), 0,01% водорастворимого красителя (выбранного из группы бромфеноловый синий; ксиленцианол; бромкрезол красный; крезол красный), 1 mM DTT, 50 mg/ml BSA, 100 mM фиколла или сахарозы в качестве стабилизирующих агентов и олигонуклеотидные праймеры (по 50 рМ Р1 5/-cgccacgacgatgaacagac-3/ и Р2 5/-ccacgggtaaagttgggc-3/). Смесь готовят путем смешивания водных растворов реагентов, дальнейшего быстрого замораживания при -70°С и высушивания при низкой температуре. Смесь сохраняет активность при +55°С в течение 136 и 115 часов. Для проведения ПЦР-анализа смесь растворяют деионизованной водой.
Сухие ПЦР-смеси, подобные описанной, обладают высокой гигроскопичностью и в результате поглощения влаги при длительном хранении при положительной температуре могут терять реакционную активность. Присутствующие в смеси ионы Mg2+ могут приводить к началу неспецифичной реакции. Наличие праймеров в готовых сухих ПЦР-смесях ограничивает использование таких смесей для широкого круга исследований.
Задачи изобретения - сухая амплификационная смесь реагентов для полимеразной цепной реакции, сохраняющая реакционную активность в течение длительного времени хранения при положительной температуре и позволяющая проводить специфичную ПЦР и имеющая многоцелевое назначение, а также способ проведения ПЦР-анализа.
Поставленные задачи решаются тем, что сухая амплификационная смесь реагентов для ПЦР содержит ДНК-полимеразу, дезоксинуклеозидтрифосфаты, буферные компоненты, водорастворимый краситель для электрофореза и композицию веществ-стабилизаторов (D-глюкозу, инулин и D-маннитол). Способ проведения ПЦР-анализа включает растворение сухой амплификационной смеси реагентов для полимеразной цепной реакции буферным раствором, содержащим ионы магния, с последующим добавлением специфичных праймеров и анализируемой ДНК.
Композиция D-глюкозы, инулина и D-маннитола в предлагаемой амплификационной смеси выполняет не только функцию стабилизаторов при лиофилизации, но и позволяет одновременно проводить лиофилизацию при более мягких условиях, что уменьшает гигроскопичность сухой ПЦР-смеси. Готовая смесь может храниться длительное время (от года и более) в широком диапазоне температур (от -20°С до +30°С), не теряя реакционной активности. Наличие ионов Mg2+ в буфере-растворителе, а не в составе самой смеси, позволяет контролировать начало реакции, избежать появления неспецифических продуктов и ложноположительных результатов при проведении ПЦР-анализа с использованием предлагаемой амплификационной смеси. Предлагаемая амплификационная смесь работает с любыми системами праймеров для геномной, плазмидной, митохондриальной, рекомбинантной (генетически модифицированной) ДНК и может быть использована для ПЦР-анализа ДНК любых многоклеточных и одноклеточных организмов, вирусов, продуктов питания или их компонентов, а также для количественного определения содержания ДНК в исследуемых образцах.
Предлагаемая смесь содержит ДНК-полимеразу (0,1 U/μ1), смесь дезоксинуклеозидтрифосфатов (по 500 mM каждого), 80 тМ Tris-HCl (pH 8,0), 0,1% Triton X-100, 24 mM (NH4)2SO4, 0,5 mМ EDTA, D-глюкозу (0,16%), инулин (1,6%), D-маннитол (8%) и водорастворимый краситель для проведения электрофореза, например ксиленцианол (0,04%).
Предлагаемую ПЦР-смесь реагентов готовят путем смешивания водных растворов входящих компонентов, которую затем разливают по 10 мкл по пробиркам для амплификации и лиофильно высушивают при -20°С в течение 4-х часов. Лиофильно высушенную смесь используют для проведения ПЦР-анализа. Для этого смесь растворяют при помощи 10 мкл буферного раствора (буфера-растворителя), содержащего 5 mM MgCl2, 10 mM Tris-HCl (pH 8,0), 0,1% Triton X-100, 5% глицерина, и добавляют олигонуклеотидные праймеры (5 мкл) и раствор анализируемой ДНК (5 мкл).
Для приготовления предлагаемой сухой ПЦР-смеси использовали следующие реагенты: в качестве ДНК-полимеразы - OligoTaq; Pfu; Vent - фирмы Promega, США; dNTP, Tris-HCl, Triton X-100, (NH4)2SO4 EDTA, D-глюкозу, инулин, D -маннитол, краситель для электрофореза - фирмы Sigma, США. В качестве красителя для электрофореза использовали водорастворимый краситель, который был выбран из группы бромфеноловый синий, ксиленцианол, бромкрезол красный, крезол красный. Изобретение осуществимо и с другими препаратами используемых реагентов. В качестве олигонуклеотидных праймеров использовали готовые препараты или праймеры, синтезированные в зависимости от целей исследования. ДНК из исследуемых образцов выделяли общепринятыми методиками.
Изобретение иллюстрируют следующие примеры.
Пример 1. Приготовление сухой смеси реагентов для ПЦР.
Из стандартных водных растворов готовят амплификационную смесь следующего состава: 80 mM Tris-HCl (рН 8,0; 0,1% Triton X-100, 24 mM (NH4)2SO4, 0,5 mM EDTA, дезоксинуклеозидтрифосфаты dATP, dTTP, dGTP, dCTP по 500 mM каждого, OligoTaq ДНК-полимераза 0,1 U/μ1, 0,04% водорастворимого красителя для электрофореза ксиленцианола, 0,16% D-глюкозы, 1,6% инулина, 8% D-маннитола. Приготовленную жидкую смесь разливают по 10 мкл по пробиркам и лиофильно высушивают при температуре -20°С в течение 4-х часов. Хранят при +4°С в течение года и более.
Пример 2. ПЦР-анализ возбудителей инфекционных заболеваний.
Для анализа использовали биологический материал, инфицированный патогенной бактерией Chlamydia pneumonia, патогенным грибом Candida albicans, патогенным простейшим Toxoplasma gondii, ДНК-содержащим вирусом Bovine leukemia virus.
В пробирки с лиофильно высушенной амплификационной смесью по примеру 1 добавляют по 10 мкл буфера-растворителя, содержащего 5 mM MgCl2, 10 тМ Tris-HCl (рН 8,0), 0,1% Triton X-100, 5% глицерина. Затем в каждую пробирку добавляют по 5 мкл смеси олигонуклеотидных праймеров по 10 рМ каждого (для определения ДНК Chlamydia pneumonia - (F) 5'-gtggagccttatgggaatgcggttgtg-3' и (R) 5'-tagctgttgctacgccagcgtctgttg-3', для определения ДНК Candida albicans - (F)5'-gcaatccccaagacaatcacctaat-3' и (R) 5'-gactggcatcatccgacaaataaga-3', для определения ДНК Toxoplasma gondii -(F) 5'-ctccacacttcattgtgtggagt-3' и (R) 5'-gatacaagaacacgaagttcctga-3', для определения ДНК Bovine leukemia virus - (F) 5'-ggaggtggaaagatgcgaactatt-3' и (R) 5'- gtccgctctactaaccctgaactt -3'). После перемешивания в пробирки с готовой к проведению ПЦР-смесью добавляют по 5 мкл пробы ДНК из исследуемых образцов. В качестве отрицательного контроля используют буфер ТЕ, положительного контроля - геномную ДНК соответствующего возбудителя. После повторного перемешивания пробирки помещают в амплификатор и осуществляют амплификацию в следующем режиме: 1. 94°С - 60 с, 62°С - 40 с, 72°С - 90 с (1 цикл), 2. 94°С - 30 с, 60°С - 30 с, 72°С - 60 с (1 цикл), 3. 94°С - 20 с, 58°С - 20 с, 72°С - 40 с (43 цикла), 4. 72°С - 60 с. Продукты ПЦР анализируют при помощи электрофореза в 1,5% агарозном геле, окрашенном бромистым этидием при напряжении 100 В.
На фиг.1 приведена электрофореграмма продуктов амплификации ДНК бактериального возбудителя Chlamydia pneumonia, которая показывает наличие специфической зоны размером 183 н.п., которая соответствует ожидаемой в положительном контроле и исследуемых образцах, и отсутствие таковой в отрицательном контроле.
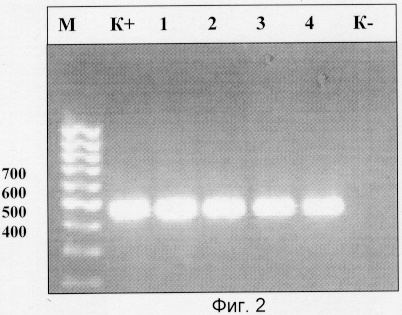
На фиг.2 приведена электрофореграмма продуктов амплификации ДНК патогенного гриба Candida albicans, которая показывает наличие специфической зоны размером 490 н.п., которая соответствует ожидаемой в положительном контроле и исследуемых образцах, и отсутствие таковой в отрицательном контроле.
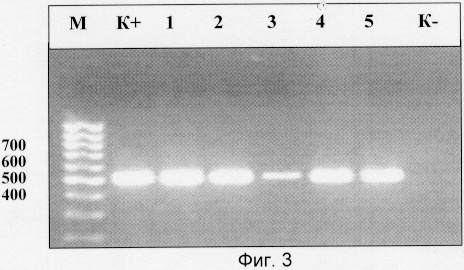
На фиг.3 приведена электрофореграмма продуктов амплификации ДНК патогенного простейшего Toxoplasma gondii, которая показывает наличие специфической зоны размером 523 н.п., которая соответствует ожидаемой в положительном контроле и исследуемых образцах, и отсутствие таковой в отрицательном контроле.
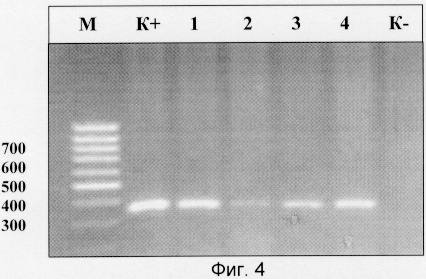
На фиг.4 приведена электрофореграмма продуктов амплификации ДНК вируса Bovine leukemia virus, которая показывает наличие специфической зоны размером 347 н.п., которая соответствует ожидаемой в положительном контроле и исследуемых образцах, и отсутствие таковой в отрицательном контроле.
Пример 3. ПЦР-анализ геномной ДНК растения (ДНК-маркирование)
Исследования проводили на различных сортах и гибридах капусты белокачанной Brassica oleracea L. var. capitata. Использовали амплификационную смесь по примеру 1, но содержащую в качестве ДНК-полимеразы Pfu.
Геномную ДНК выделяют из 14-дневных проростков по общепринятой методике. В пробирки с лиофильно высушенной амплификационной смесью по примеру 1 добавляют буфер-растворитель, как описано в примере 2. Затем добавляют 5 мкл (20 рМ) олигонуклеотидного праймера (например, PawS16, комплиментарного концевым повторам ретротранспозона семейства R173 - Ds-элемента R173 состава 5'-acctctgcgcttggaggc-3). Далее подготовку к амплификации проводят, как описано в примере 2. В качестве отрицательного контроля используют стерильную дистиллированную воду. Амплификацию осуществляют в следующем режиме: 1. 94°С - 3 мин, 2. 94°С - 45 с, 55°С - 45 с, 72°С - 100 с (35 циклов), 3. 72°С - 3 мин. Продукты ПЦР анализируют, как описано в примере 2.
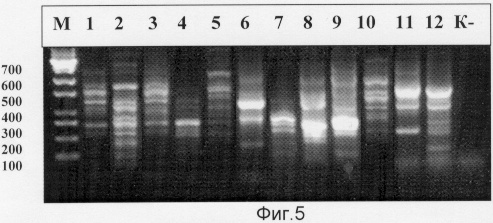
На фиг.5 приведена электрофореграмма, показывающая наличие в каждом исследуемом образце спектров уникальных фрагментов размером от 100 до 700 н.п. и отсутствие таковых в отрицательном контроле, что свидетельствует об отличимости геномов различных сортов и гибридов капусты белокачанной.
Пример 4. ПЦР-анализ генетически модифицированной ДНК в продуктах питания и пищевом сырье.
ДНК для анализа выделяли из соевой муки и продуктов, содержащих сою.
В пробирки с лиофильно высушенной амплификационной смесью по примеру 1 добавляют буфер-растворитель, как описано в примере 2. Затем добавляют 5 мкл смеси олигонуклеотидных праймеров (например, комплиментарных нуклеотидной последовательности 35S промотора вируса мозаики цветной капусты (ВМЦК) следующего состава: (F) 5'-ggctatcgttcaagatgcctctgc-3', (R) 5'-ggattgtgcgtcatcccttacgtc-3' по 10 рМ каждого). Далее в готовую к амплификации смесь добавляют по 5 мкл выделенного образца ДНК. В качестве отрицательного контроля используют буфер ТЕ, а положительного контроля - ДНК трансгенной сои линии 40-3-2, устойчивой к глифосату (Монсанто, США). Амплификацию осуществляют в следующем режиме: 1. 94°С - 3 мин, 2. 94°С - 45 с, 72°С - 30 с, 72°С - 40 с (35 циклов), 3. 72°С - 4 мин. Продукты ПЦР анализируют по примеру 2.
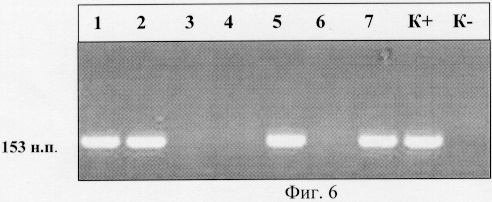
На фиг.6 приведена электрофореграмма, которая показывает наличие специфической зоны размером 153 н.п. в положительном контроле и исследуемых образцах, что свидетельствует о наличии в исследуемых образцах генетически модифицированной ДНК.
Пример 5. Количественный ПЦР-анализ генетически модифицированной ДНК.
ПЦР-анализ для определения количества генетически модифицированной ДНК в соевой муке, содержащей сою генетически модифицированной линии 40-3-2 (Монсанто, США), проводили с использованием амплификационной смеси по примеру 1. Для количественного определения ДНК в анализируемой пробе использовали прибор для проведения ПЦР в реальном времени Smart CyclerII (Cefeid, США). Определение проводили с использованием технологии TaqMan (Heid C.A., Stevens J., Livak K.J. and Williams P.M. Real time quantitative PCR. Genome Res. 6, 986-994, 1996).
В пробирки с лиофильно высушенной амплификационной смесью добавляют буфер-растворитель, как описано в примере 2. Затем в пробирки добавляют 5 мкл смеси олигонуклеотидных праймеров и зондов (олигонуклеотидов, меченных флуоресцентными агентами ROX и FAM). В качестве праймеров используют олигонуклеотиды комплиментарные нуклеотидной последовательности гена ср4 устойчивости к гербициду глифосат состава (F) 5'- gtggtcccaaagaacct-3', (R) 5'-cccttgagccatgaacc-3' и комплиментарные нуклеотидной последовательности гена лектина сои lec (F) 5'-accagcaaggcaatgaa-3', (R) 5'-cgagaaagaaggcatct-3' по 10 рМ каждого. В качестве зондов - флуоресцентно меченные олигонуклеотиды состава 5'-(FAM)agcacgtaagggatgacgca(BHQ1)-3' и 5'-(ROX)ttactggaacaagttcgtgc(BHQ2)-3', комплиментарные нуклеотидным последовательностям генов ср4 и lec соответственно по 6 рМ каждого. Далее в готовую к амплификации смесь добавляют 10 мкл выделенной ДНК (концентрация 10 нг/мкл). В качестве отрицательного контроля используют ДНК, выделенную из пшеничной муки. Для проведения амплификации и детекции результатов пробирки с готовой к реакции смесью и ДНК помещают в прибор для проведения ПЦР в режиме реального времени. 7
Амплификацию осуществляют в следующем режиме: 1. 94°С - 3 мин; 2. 94°С - 20 с, 57°С - 30 с, 72°С - 30 с (45 циклов).
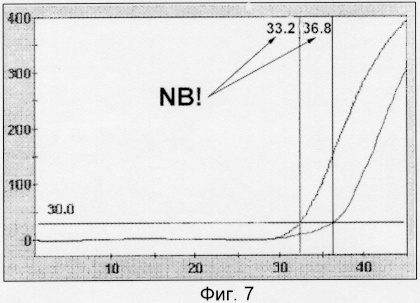
На фиг.7 приведен график с кривыми флуоресценции, полученными в результате ПЦР в реальном времени. На нем указано время достижения определенного порогового значения флуоресценции, выраженное в количестве циклов амплификации. Значение 33,2 пропорционально суммарной концентрации ДНК сои (рекомбинантной и нативной) в исследуемом материале при амплификации фрагмента гена lee соевого лектина (детекция по ROX). Значение 36,8 - концентрации рекомбинантной ДНК при амплификации фрагмента гена ср4 устойчивости к гербициду глифосат (детекция по FAM). Исходя из отношения этих величин (33,2/36,8) по калибровочной кривой определяют долю рекомбинантной ДНК, которая в анализируемом образце соответствует 5%.
Пример 6. ПЦР-анализ геномной ДНК человека
Для анализа генома человека (например, с цепью определение пола плода) при помощи ПЦР использовали амплификационную смесь по примеру 1, но содержащую в качестве ДНК-полимеразы Vent.
Геномную ДНК выделяют из фетальных клеток плода, находящихся в крови матери. В пробирки с лиофильно высушенной амплификационной смесью добавляют буфер-растворитель, как описано в примере 2. Затем в каждую пробирку добавляют по 5 мкл смеси олигонуклеотидных праймеров (например, комплиментарных уникальным нуклеотидным последовательностям гена amelogenin в Х- и Y-хромосомах человека состава: 5'-gatggttggcctcaagcctgtg-3' и 5'- accttgctcatattatacttgaca-3'). Далее к готовой амплификационной смеси добавляют 5 мкл выделенной ДНК. В качестве отрицательного контроля используют буфер ТЕ, в качестве положительного - векторные конструкции, содержащие нуклеотидные последовательности, идентичные определяемым. Амплификацию осуществляют в следующем режиме: 1. 94°С - 60 с, 62°С - 40 с, 72°С - 90 с (1 цикл), 2. 94°С - 30 с, 60°С - 30 с, 72°С - 60 с (1 цикл), 3. 94°С - 20 с, 58°С - 20 с, 72°С - 40 с (43 цикла), 4. 72°С - 60 с. Продукты ПЦР анализируют, как описано в примере 2.
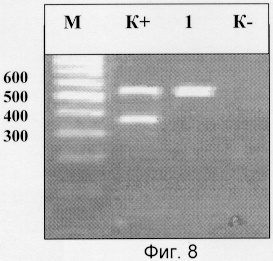
На фиг.8 приведена электрофореграмма, которая показывает наличие зоны размером 533 н.п., характерной для Х-хромосомы в исследуемом образце, и отсутствие зоны размером 348 н.п., характерной для Y-хромосомы, а также отсутствие зон в отрицательном контроле, что позволяет определить пол плода как женский.
Пример 7. Влияние лиофилизации на стабильность реакционной активности смеси реагентов для ПЦР
Смесь (I) готовят, лиофильно высушивают и хранят, как описано в примере 1. Смесь (II) готовят из водных растворов входящих компонентов. Смесь содержит 10 mM Tris-HCl (pH 8,0), 24 mM (NH4)2SO4, 1,5 mM MgCl2, ДНК-полимеразу, смесь дезоксинуклеозидтрифосфатов (dATP, dTTP, dGTP, dCTP no 250 mM каждого), 0,1% Triton X-100, 5% глицерина, 0,01% водорастворимого красителя для электрофореза (например, ксиленцианола), 0,16% D-глюкозы, 1,6% инулина, 8% D-маннитола в качестве стабилизирующих агентов. Смесь (II) хранят при -20°С. Смесь (I) и смесь (II) используют для ПЦР-анализа с целью обнаружения в исследуемых образцах генетически модифицированной ДНК из трансгенной сои линии 40-3-2 (Монсанто, США).
Выделение ДНК для ПЦР-анализа проводят по общепринятой методике.
Для проведения анализа смесь (I) растворяют буфером-растворителем, как описано в примере 2, и добавляют по 5 мкл олигонуклеотидных праймеров для определения 35S промотора ВМЦК по примеру 6. К смеси (II) добавляют по 5 мкл тех же олигонуклеотидных праймеров. Содержимое обеих пробирок перемешивают и в каждую добавляют по 5 мкл ДНК трансгенной сои линии 40-3-2. Амплификацию и детекцию осуществляют, как описано в примере 6. Анализ повторяют в течение 12 месяцев с регулярностью 1 раз в месяц.
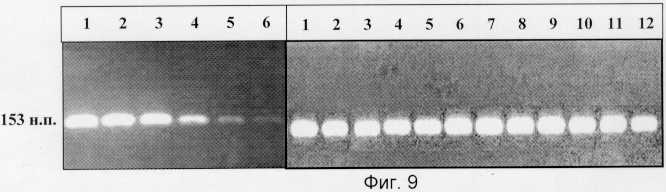
На фиг.9 приведена электрофореграмма, которая показывает снижение реакционной активности смеси (II) на 5 месяце хранения при -20°С. Реакционная активность смеси (I) не изменяется в течение 12-ти месяцев хранения при +4°С.
Изобретение относится к области молекулярной биологии и биотехнологии и может быть использовано в ветеринарии, медицине и пищевой промышленности. Сухую смесь реагентов для полимеразной цепной реакции получают путем лиофильного высушивания водного раствора, содержащего ДНК-полимеразу, дезоксинуклеозидтрифосфаты, буферные компоненты, краситель для электрофореза, D-глюкозу, инулин и D-маннитол. Для проведения ПЦР-анализа указанную смесь растворяют в буферном растворе, содержащем ионы магния, добавляют в полученный раствор специфические праймеры и анализируемую ДНК и осуществляют амплификацию нуклеиновой кислоты в условиях полимеразной цепной реакции. Применение изобретения позволяет сохранить реакционную активность реагентов для полимеразной цепной реакции при длительном хранении и упрощает проведение ПЦР-анализа. 9 ил.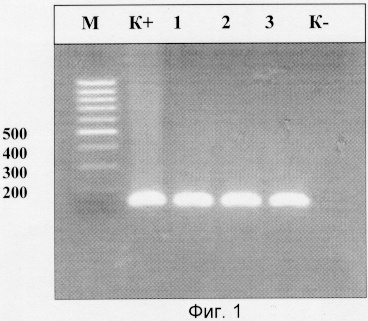
| US 6153412, 19.01.1999 | |||
| US 5861251, 19.01.1999 | |||
| СПОСОБ СКАНИРОВАНИЯ ЦВЕТНОГО ИЗОБРАЖЕНИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2158486C1 |
| US 5643764 01.07.1997 | |||
| ГАСИТЕЛЬ ПУЛЬСАЦИЙ | 2004 |
|
RU2277198C1 |
Авторы
Даты
2005-08-27—Публикация
2004-04-27—Подача