Известен способ оценки профилактики иммунодефицита путем проведения ультразвукового воздействия на область иммунокомпетентных органов, например, тимуса у животных, например, мышей, с последующим на 1-2 день после окончания воздействия острым внешним гамма-облучением и исследованием на 5-й или 12-й день после облучения уровня лейкоцитов в капиллярной крови, клеточности тимуса и массы селезенки, отличающийся тем, что оценку профилактического действия физического фактора производят путем вычисления произведения уровней лейкоцитов и клеточности тимуса, деленного на массу селезенки, и при его значениях на 5-й день, больших 3,3 определяют наличие раннего профилактического эффекта, а на 12-й день - больших 10,9 - наличие профилактического эффекта в фазе разгара лучевых проявлений ("Способ оценки профилактики нарушений иммунного статуса при воздействии ионизирующей радиации" - описание к патенту РФ №2106634; авторы Ю.М.Гринзайд, Н.И.Демешко, А.В.Щелкунов).
Данный способ рассчитан на определение профилактического эффекта ультразвука в отношении действия ионизирующей радиации при остром внешнем облучении и не может быть применен при оценке профилактики нарушений иммунного статуса с помощью других физических факторов в условиях других иммуносупрессорных воздействий в силу принципиальной разницы патогенеза двух указанных моделей. Мы попытались проверить информативность этого коэффициента при воздействии ультразвука или низкочастотного электрического тока на модели циклофосфанового иммунодефицита. В первом случае КПуз=3,70±0,43, во втором - КПнэт=4,34±0,67, практически не отличаясь от КПмодели=4,78±0,63. Следовательно, при работе с моделью иммунодефицита медикаментозного генеза способ прототипа неинформативен.
Предлагаемый способ лишен указанных недостатков. Для его осуществления вначале проводят курс воздействия низкочастотной электротерапии (НЭТ) на область тимуса подопытных животных, например, крыс, при частоте 50 Гц, напряжении - 20 В, разовой экспозиции - 60 секунд, числе процедур 6 - через 1-2 дня. Результаты сравнивают у животных основной и контрольной (без пресанации НЭТ) групп, у которых моделируется иммунодефицит медикаментозного генеза путем внутрибрюшинного введения в течение 3 недель 2% раствора циклофосфана в суммарной дозе 42 мг препарата (1 инъекция в 3 дня). На 26-й день после начала введения препарата животных забивают и проводят исследование масс селезенки (МС) и тимуса (МТ), содержания антителообразующих клеток в селезенке (АОК) по методу локального гемолиза (Иммунологические методы//Под ред. Г.Фримеля. Перевод с немецкого. - М.: Медицина, 1987. - С.57-63) и фагоцитарной активности лейкоцитов в крови - ФАЛ (Иванов А.И., Чухловин Б.А. К методике определения поглотительной и переваривающей способности нейтрофилов. - Лаб. дело. - 1967. - №10. - С.610-613). Вычисляют индекс профилактики (ИП) по формуле:
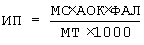
где МС - масса селезенки, АОК - число антителообразующих клеток селезенки - в кл/чП, ФАЛ - фагоцитарная активность лейкоцитов в %, МТ - масса тимуса.
При значениях ИП, больших 8,0, определяют наличие профилактического эффекта. Способ осуществляют следующим образом. Группе животных, например, крыс, воздействуют на область тимуса низкочастотным электрическим током (НЭТ) при частоте 50 Гц, напряжении - 20 В при разовой экспозиции - 60 секунд, числе процедур 6 - через 1-2 дня. Результаты сравнивают у животных основной и контрольной (без пресанации НЭТ) групп, у которых моделируется иммунодефицит медикаментозного генеза путем внутрибрюшинного введения 1 раз в 3 дня по 0,3 мл в течение 3 недель 2% раствора циклофосфана (суммарная доза - 42 мг препарата). На 26-й день после начала введения препарата животных забивают и проводят исследование иммунокомпетентных органов - тимуса и селезенки. Определяют массу селезенки и массу тимуса (в мг), содержание АОК в селезенке (в клетках на чашку Петри), фагоцитарную активность лейкоцитов (в %). Профилактическое действие физического фактора оценивают путем вычисления индекса профилактики. Для этого определяют частное от деления произведений массы селезенки на АОК и на ФАЛ на массу тимуса. Полученное число делят на 103. При значениях ИП, превышающих 8,0, констатируют наличие профилактического эффекта.
Примеры осуществления способа.
1. Интактная крыса-самец линии Вистар №15, масса тела - 360 г. Дополнительных воздействий не получала. Исследование животного осуществлено одновременно с животными опытной группы (на 26-й день после первой инъекции). Масса селезенки - 1280 мг, тимуса - 402 мг, содержание АОК в селезенке - 168 кл/чП, фагоцитарная активность лейкоцитов - 46%, индекс профилактики - 16.3.
2. Крыса-самец линии Вистар №35, масса тела - 310 г. Низкочастотный электрический ток не назначался. Осуществлено воспроизведение циклофосфановой модели иммунодефицита: 1 раз в 3 дня по 0,3 мл в течение 3 недель производилось внутрибрюшинное введение 2% раствора циклофосфана. На 26-й день после первой инъекции проведено исследование животного. Масса селезенки - 604 мг, тимуса - 340 мг, содержание АОК в селезенке - 136 кл/чП, фагоцитарная активность лейкоцитов - 30%, индекс профилактики - 7.2. Профилактический эффект отсутствует.
3. Крыса-самец линии Вистар №3, масса тела - 340 г. Предварительные процедуры низкочастотной электротерапии (НЭТ) на область тимуса и при частоте - 50 Гц, напряжении - 20 В, разовой экспозиции - 60 секунд, числе процедур 6 - через 1-2 дня. Через 2 дня после окончания процедур НЭТ проведено воспроизведение циклофосфановой модели иммунодефицита: 1 раз в 3 дня по 0,3 мл в течение 3 недель производилось внутрибрюшинное введение 2% раствора циклофосфана. На 26-й день после первой инъекции осуществлено исследование животного. Масса селезенки - 688 мг, тимуса - 151 мг, содержание АОК в селезенке - 248 кл/чП, фагоцитарная активность лейкоцитов - 22%, индекс профилактики - 24,9. Наблюдается профилактический эффект.
4. Крыса-самец линии Вистар №8, масса тела - 250 г. Предварительные процедуры низкочастотной электротерапии (НЭТ) на область тимуса и при частоте - 50 Гц, напряжении - 20 В, разовой экспозиции - 60 секунд, числе процедур 6 - через 1-2 дня. Через 2 дня после окончания процедур НЭТ проведено воспроизведение циклофосфановой модели иммунодефицита: 1 раз в 3 дня по 0,3 мл в течение 3 недель производилось внутрибрюшинное введение 2% раствора циклофосфана. На 26-й день после первой инъекции осуществлено исследование животного. Масса селезенки - 640 мг, тимуса - 145 мг, содержание АОК в селезенке - 224 кл/чП, фагоцитарная активность лейкоцитов - 25%, индекс профилактики - 24,7 ед. Наблюдается профилактический эффект.
Способ был апробирован в условиях отдела изучения механизмов действия физических факторов Пятигорского государственного НИИ курортологии. Объектом исследования послужили 25 крыс-самцов линии Вистар, разделенные на 3 группы (см. таблицу).
9 животных 1 группы (интактные) воздействиям физического фактора и медикамента не подвергались. На 40-й день после начала эксперимента осуществлено исследование животных. Масса селезенки составила 1217±110 мг, масса тимуса - 417±28,7 мг, число АОК в селезенке - 186±22,6 кл/чП, ФАЛ - 31,1±2,77%, ИП=17,0±2,71 ед.
У 6 животных 2 группы (модель) в течение недели животным внутрибрюшинно ежедневно вводилось по 0,3 мл 2% раствора циклофосфана (курсовая доза - 42 мг). На 26-й день после первой инъекции осуществлено исследование животных. Масса селезенки составила 630±22,1 мг, масса тимуса - 347±34,1 мг, число АОК в селезенке - 155±11,6 кл/чП, ФАЛ - 26,0±1,55%, ИП=7,33±0,28 ед.
10 животных 3 группы (опыт) вначале приняли курс процедур НЭТ на область тимуса по описанной выше методике, через 1-2 дня после чего крысам этой группы в течение недели внутрибрюшинно ежедневно вводилось по 0,3 мл 2% раствора циклофосфана (курсовая доза - 42 мг). На 26-й день после первой инъекции осуществлено исследование животных. Масса селезенки составила 878±75,0 мг, масса тимуса - 223±19,5 мг, число АОК в селезенке -190,4±24,3 кл/чП, ФАЛ - 27,0±1,24%, ИП=21,1±3,30 ед.
Приведенные в таблице данные свидетельствуют о том, что верхняя граница диапазона ИП, рассчитанная, как М+σ (Л.С.Каминский, 1959), при циклофосфановой модели без профилактики НЭТ составляет на 26 день после начала введения препарата 8,0 ед. Поэтому значения, превышающие указанные, свидетельствуют о наличии профилактического эффекта.
При этом разница отдельных показателей может быть недостаточно существенной, тогда как разница в уровне интегрального показателя достоверна (соответственно 7,33±0,28 и 21,1±3,30 ед.; Р<0,003). Следовательно, предлагаемый способ является более информативным, чем традиционные.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ПОСТМЕДИКАМЕНТОЗНОГО ИММУНОДЕФИЦИТА | 2008 |
|
RU2393480C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОСТМЕДИКАМЕНТОЗНОГО ИММУНОДЕФИЦИТА | 2007 |
|
RU2351019C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИММУНОДЕФИЦИТОВ В ЭКСПЕРИМЕНТЕ | 2002 |
|
RU2243794C2 |
| СПОСОБ ОЦЕНКИ ИММУНОПРОФИЛАКТИЧЕСКОГО ЭФФЕКТА УЛЬТРАЗВУКА В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2445713C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ОЗОНОТЕРАПИИ | 2008 |
|
RU2374700C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТА ЭЛЕКТРОМАГНИТНЫХ ВОЛН МИЛЛИМЕТРОВОГО ДИАПАЗОНА (КВЧ) В ЭКСПЕРИМЕНТЕ | 2012 |
|
RU2529694C2 |
| СПОСОБ ОЦЕНКИ ПРОФИЛАКТИКИ ПОСТСТРЕССОРНОЙ ИММУНОПАТОЛОГИИ В ЭКСПЕРИМЕНТЕ | 2005 |
|
RU2303260C2 |
| СПОСОБ ОЦЕНКИ КАЧЕСТВА ИММУНОМОДУЛЯЦИИ В ЭКСПЕРИМЕНТЕ | 1998 |
|
RU2145085C1 |
| СПОСОБ ОЦЕНКИ БАЗАЛЬНОЙ ИММУНОМОДУЛЯЦИИ В ЭКСПЕРИМЕНТЕ | 1997 |
|
RU2128342C1 |
| СПОСОБ ОЦЕНКИ ПРОФИЛАКТИКИ НАРУШЕНИЙ ИММУННОГО СТАТУСА ПРИ ВОЗДЕЙСТВИИ ИОНИЗИРУЮЩЕЙ РАДИАЦИИ | 1995 |
|
RU2106634C1 |
Изобретение относится к экспериментальной медицине. Способ осуществляют путем проведения воздействия низкочастотным электрическим током на область иммунокомпетентных органов, например, у группы животных, например, крыс в течение 2 недель. Через 2 дня после окончания курса у животных моделируется иммунодефицит медикаментозного генеза путем внутрибрюшинного введения 2% раствора циклофосфана 1 раз в 3 дня по 0,3 мл в течение 3 недель (суммарная доза - 42 мг препарата). На 26-й день после начала введения препарата определяют массы селезенки и тимуса, содержание АОК в селезенке, фагоцитарную активность лейкоцитов. Профилактическое действие физического фактора оценивают путем вычисления индекса профилактики. Для этого определяют частное от деления произведений массы селезенки на АОК и на ФАЛ на массу тимуса. Полученное число делят на 103. При значениях ИП, превышающих 8,0, констатируют наличие профилактического эффекта. Способ позволяет повысить точность и информативность оценки профилактики постмедикаментозных нарушений иммунного статуса. 1 табл.
Способ оценки профилактики иммунодефицита путем физического воздействия на область тимуса подопытных животных с последующим моделированием иммунодефицита и определением массы иммунокомпетентных органов, клеток селезенки и крови, отличающийся тем, что проводят воздействие низкочастотным электрическим током (НЭТ) на область тимуса крыс через 1-2 дня в течение 2 недель, затем спустя 2 дня животным проводят 3-недельный курс инъекции циклофосфана для моделирования иммунодефицита медикаментозного генеза, на 26-й день от начала введения препарата животных забивают, исследуют массу селезенки и тимуса, содержание антителообразующих клеток (АОК) в селезенке и фагоцитарную активность лейкоцитов (ФАЛ) крови, а оценку профилактического действия НЭТ проводят путем вычисления произведения массы селезенки на АОК и ФАЛ, деленного на массу тимуса и на 103, и при его значениях, превышающих 8,0, определяют наличие профилактического эффекта.
| СПОСОБ ОЦЕНКИ ПРОФИЛАКТИКИ НАРУШЕНИЙ ИММУННОГО СТАТУСА ПРИ ВОЗДЕЙСТВИИ ИОНИЗИРУЮЩЕЙ РАДИАЦИИ | 1995 |
|
RU2106634C1 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ОРГАНИЗМА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2194490C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОВРЕЖДЕНИЙ ПЕЧЕНИ, ВЫЗЫВАЕМЫХ ЭФИРНЫМ НАРКОЗОМ В ЭКСПЕРИМЕНТЕ | 1997 |
|
RU2153904C2 |
Авторы
Даты
2005-10-20—Публикация
2003-08-25—Подача