Изобретение относится к области биологическиактивных веществ, в частности к 6-алкил-5-(2-изоникотиноилсульфогидразоил)урацилгидрохлоридам, которые обладают антимикобактериальной и иммунотропной активностью и могут быть использованы в качестве иммуномодулятора и антимикобактериальных средств, а также к фармацевтической композиции на их основе.
Известны щелочные соли N-(6-алкил-2,4-диоксо-1,2,3,4-тетрагидро-5-пиримидинсульфон)-N'-изоникотиноилгидразида формулы (А) (Изодинафон)
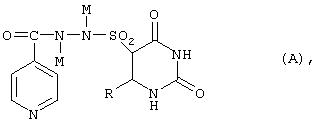
где R является алкилом с 1-4 атомами углерода и М является щелочным металлом, обладающие аналогичной активностью с токсичностью 7000 мг/кг (см. международную заявку на патент WO 01/32650). Однако их активность не достаточно высока (см. нижеследующие таблицы).
Известен также N-(6-метил-2.4-диоксо-1.2.3.4-тетрагидро-5-пиримидинсульфон)-N-изоникотиноилгидразид гидрат (В), обладающий антимикобактериальной и иммуномодулирующей активностями (патент RU 2141322). Однако данное соединение (В) не растворяется в воде, физрастворе и других растворителях, имеет плохую растворимость в биологических жидкостях, что свидетельствуют о его низкой биологической активности, невысокой биодоступности.
В основу изобретения положена задача - изыскание новых близких по структуре соединений, обладающих более высокой активностью.
Задача решается предложенными 6-алкил-5-(2-изоникотиноилсульфо-гидразоил)урацилгидрохлоридами общей формулы (I)
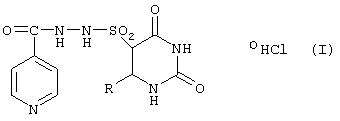
где R является алкилом с 1-4 атомами углерода.
6-Метил-5-(2-изоникотиноилсульфогидразоил)урацилгидрохлорид формулы (I) представляют собой мелкокристаллический порошок от белого до кремового цвета с температурой плавления Тпл= 253-254°С.
Предложенные соединения получают путем взаимодействия гидразида изоникотиновой кислоты с 6-метилурацил-5-сульфохлоридом в растворителе.
Соединения формулы (I) обладают антимикобактериальной и иммунотропной активностью.
Задача также решается предложенной фармацевтической композицией, обладающей антимикобактериальной и иммунотропной активностью, включающей активное вещество и целевые добавки, отличие которой состоит в том, что в качестве активного вещества она содержит 6-алкил-5-(2-изоникотиноилсульфогидразоил)урацилгидрохлорид общей формулы (I) в эффективном количестве.
Дозировка зависит от возраста, состояния и веса пациента, а также от вида введения. Согласно изобретению, предлагаемая фармацевтическая композиция содержит активного вещества в количестве от 0,1 до 4 г.
Токсичность предложенных соединений была определена на белых беспородных мышах весом 18-20 г в остром опыте по методу Литчфильда-Уилкоксона и составила более 7000 мг/кг.
Заявленные соединения были испытаны в экспериментах на животных.
Определение иммунотропной активности предложенного гидрохлорида
а) Влияние на гуморальный иммунитет изучали с помощью метода локального гемолиза в геле. Мышей гибридов F1 (СВА × С57BI6) иммунизировали эритроцитами барана в дозе 5×106 и сразу после этого вводили изучаемые вещества как перорально в крахмальной суспензии, так и парентерально. На 5-е сутки подсчитывали количество антителообразующих клеток (АОК) в селезенке мышей и определяли индекс стимуляции иммунного ответа по отношению число АОК в опытной группе к числу АОК в контрольной группе.
Данные представлены в таблице 1.
Влияние исследуемых соединений на накопление антителообразующих клеток (АОК) в селезенке мышей (различие достоверно (р меньше 0,01) по отношению к норме).
Индексы стимуляции иммунного ответа гидрохлорида и изодинафона при введении препаратов внутрь достоверно неразличимы между собой. Это говорит о том, что исследуемые препараты обладают близким действием на гуморальный иммунитет, тестируемый в реакции накопления АОК в селезенке мышей.
б) Влияние исследуемых препаратов на пролиферацию Т-лимфоцитов изучали на модели in vitro. Для этого проводили предварительную 3-х часовую инкубацию мононуклеарных клеток человека в присутствии различных концентраций каждого исследуемого вещества. Изучали широкий диапазон концентраций каждого исследуемого вещества: от 0,01 до 5 мкг/л. В качестве негативного контроля добавляли физиологический раствор 0,9% NaCI.
Результаты влияния новых соединений на интенсивность пролиферации Т-лимфоцитов человека в культуре клеток in vitro представлены в таблице 2.
Влияние гидрохлорида на пролиферацию Т-лимфоцитов в культуре in vitro.
Таким образом, предлагаемый гидрохлорид также как и изодинафон обладает как собственной митогенной активностью, так и в ответ на фитогемагглютинин, но проявляет эту активность при добавлении в меньшей дозе.
в) Влияние исследуемых препаратов на фагоцитарную активность макрофагов изучали по клиренсу туши в крови, взятой из ретроорбитального синуса мышей, получавших препараты перорально. Результаты оценивали по фагоцитарному индексу (таблица 3).
Влияние исследуемых препаратов на фагоцитарную активность макрофагов (различие достоверно (р меньше 0,01) по отношению к норме).
Результаты, приведенные в таблице, говорят о том, что гидрохлорид стимулирует фагоцитарную активность макрофагов в большей степени, чем изодинафон при любом способе введения.
г) Иммунокорригирующая способность гидрохлорида была определена на модели иммунодефицита, вызванного облучением мышей F1 (СВА х С57BI6) в дозе 4 Грэя.
Показано, что облучение мышей в дозе 4 Грэя уменьшает иммунный ответ в 15-20 раз, его восстановление начинается на 6-8 сутки и заканчивается к 30 суткам (Ярилин А.А., Полушкина Э.Ф., Филатов П.П. Действие ионизирующей радиации на соотношение популяций лимфоидных клеток у мышей, Радиобиология, 1976 г., т. 16, №3, стр. 451-454). При использовании этой модели подопытным животным вводили испытуемые препараты в дозах 500 мкг/мышь перорально в 0,5 мл крахмальной суспензии и 100 мкг/мышь парентерально в 0,2 мл физраствора. Препараты вводили трижды на 6,7,8 сутки после облучения. Контрольная группа животных получала 0,5 мл крахмальной суспензии или 0,2 мл физраствора. На 15 сутки у этих животных определяли количество АОК в селезенке методом локального гемолиза в геле.
Полученные данные представлены в таблице 4.
Влияние гидрохлорида на восстановление процесса формирования антителообразующих клеток селезенки у облученных животных.
На основании полученных данных по восстановлению иммунного ответа после облучения можно сделать вывод, что гидрохлорид проявляет большую иммунокорригирующую активность чем у препаратов сравнения.
Определение противотуберкулезной активности гидрохлорида.
Активность проверялась в сравнении с изодинафоном. Для заражения использовались лабораторные штаммы микобактерий туберкулеза Н37RV обычный и тубазидоустойчивый до 100 мг. 230 мышей линии СВА заражали внутривенно 0,25 мг культуры микробактерий туберкулеза в 0,5 мл физраствора. Опыт продолжался 2 месяца. Под наблюдением находилось 20 групп животных по 15 мышей в каждой группе, все животные содержались в одинаковых условиях вивария на стандартном рационе. Контрольные группы получали в течение всего опыта через зонд 5 раз в неделю 0,5 мл крахмальной суспензии или 0,2 мл физраствора парентерально. Опытные группы животных получали препараты перорально в различных дозах в 0,5 мл крахмальной суспензии или в 0,2 мл физраствора парентерально. Все животные, как павшие, так и забитые, по окончании опыта взвешивались, также взвешивались их внутренние органы, определялась степень поражения внутренних органов, оцениваемая в «+», кроме этого о действии препарата судили по средней продолжительности жизни (СПЖ).
Результаты экспериментов приведены в таблице 5.
Влияние исследуемых веществ на противотуберкулезную активность.
Вышеизложенные результаты показывают, гидрохлорид обладает выраженным противотуберкулезным действием как на микобактерии, чувствительные к большинству противотуберкулезных препаратов, так и на микобактерии, резистентные к тубазиду. Судя по индексу поражения легких, зараженных животных, противотуберкулезная активность гидрохлорида проявляется в большей степени, чем у препаратов сравнения.
Определение противолепрозной активности гидрохлорида в сравнении с изодинафоном.
Противолепрозная активность гидрохлорида в сравнении с изодинафоном изучалась на мышах самцах линии СВА, зараженных лабораторным штаммом Кур-4 микобактерии лепры, взятыми в количестве 5000 и введенными интраплантарно по методу Шепарда. Опыт продолжался 6 месяцев. Под наблюдением находилось 5 групп по 20 мышей в каждой группе. Все мыши содержались в одинаковых условиях вивария на стандартном рационе.
Первая группа - контрольная: в течение 6 месяцев мыши этой группы получали через зонд 5 раз в неделю 0,5 мл крахмальной суспензии. В другой серии опытов контрольным животным парентерально в исследуемые сроки вводили 0,2 мл физраствора, а опытным - препараты, разведенные в физрастворе.
Через 6 месяцев животные были забиты цервикальным смещением позвоночника, органы были подвергнуты бактериоскопическому исследованию, никаких патологических отклонений, характерных для какой-либо группы, не обнаружено. При бактериоскопическом исследовании места заражения (лапку) растирали в 2 мл 0,1% раствора альбумина, из 0,01 мл суспензии делали мазок, окрашивали по Цилю-Нильсену и подсчитывали количество микобактерий на 1 мышь в каждой группе.
Результаты исследований представлены в таблице 6.
Влияние исследуемых веществ на противолепрозную активность (различие достоверно (р меньше 0,01) по отношению к норме).
Как следует из приведенных данных, гидрохлорид во всех исследуемых дозах и способах применения проявляет выраженную противолепрозную активность так же, как и изодинафон в дозе 25 мкг/мышь.
Изучение антимикробного действия гидрохлорида
Антимикробное действие гидрохлорида в сравнении с изодинафоном исследовалось на культурах Bacillus cereus и Staphylococcus aureus. Для определения антимикробного действия препаратов на В. cereus брали по 100 мг каждого препарата, разводили в 10 мл фосфатного буфера (рН 7,0) и добавляли по 1 мл в пробирки, содержащие 1 мл расплавленной среды №1 (Государственная Фармакопея СССР, изд-е XI, вып.1, т.2, стр.200) и 1 мл суточной бульонной культуры В. cereus, разведенной в 1000 раз физ-раствором. Содержимое пробирки сразу выливали на чашку Петри, содержащую 15 мл застывшей среды №1, чашки ставили в термостат при температуре от 30 до 35°С.
Для определения антимикробного действия препаратов на St. aureus брали по 100 мг каждого препарата, разводили в среде №8 (Государственная Фармакопея СССР, изд.XI, вып.1, т.2, стр.208) и добавляли по 1 мл в пробирки, содержащие по 4 мл расплавленной среды №10 (Государственная Фармакопея СССР, изд.XI, вып.1, т.2, стр.208) и 1 мл суточной бульонной культуры Staphylococcus aureus, разведенной физраствором в 1000 раз. Содержимое пробки сразу же выливали в чашки Петри, содержащие 15 мл застывшей среды №10, чашки ставили в термостат с температурой от 30 до 35°С. Эксперимент длился 5 суток.
В случае отсутствия роста тест-штаммов на соответствующих питательных средах отмечают антимикробное действие препаратов. Результаты эксперимента представлены в таблице 7.
Антимикробное действие гидрохлорида в сравнении с изоди-нафоном.
+ - наличие роста микроорганизмов
- - отсутствие роста микроорганизмов
± - незначительный рост микроорганизмов
Как показывают результаты проведенных экспериментов, гидрохлорид обладает бактерицидным действием на микроорганизмы В. cereus и выраженным бактериостатическим действием на St. aureus.
Способ получения предложенных соединений формулы (I) иллюстрируется следующим примером.
Пример
Смешивают 1,26 г (0,01 моль) гидразида изоникотиновой кислоты и 2,245 г (0,01 моль) 6-метилурацил-5-сульфохлорида в ацетонитриле при температуре кипения растворителя в течение 5 часов.
Фильтруют, выпавший в осадок гидрохлорид и очищают в несколько стадий следующим образом: 0,5 г гидрохлорида кипятят в 15 мл спирта в течение 10 минут, далее фильтруют, промывают осадок 6 мл спирта, сушат на воздухе. Так повторяют еще один или два раз до момента, когда останутся только следовые количества примесей.
Получают 3,115 г 6-метил-5-(2-изоникотиноилсульфогидразоил)урацил-гидрохлорида (примерно выход 90%), который представляет собой мелкокристаллический порошок от белого до кремового цвета. Тпл= 253-254°С
Примеры рецептур фармацевтических композиций
Капсулы
Гидрохлорид в желатиновых капсулах по 0,1 г и по 0,2 г получают фасованием ручным способом в капсулы №1 и №0 с помощью капсульниц с запорным устройством. Состав: гидрохлорид - 0,1 г и 0,2 г без наполнителей и консервантов.
Навеску гидрохлорида 10,0 г помещают на пластину капсульницы, распределяют по поверхности пластины и далее в соответствии с описанием процесса работы с капсульницей.
Желатиновые капсулы состоят из: хинолина эпу - 0,05%, титана диоксида-1,0%, желатина - до 100%. Входящие в состав капсул вещества разрешены к медицинскому применению в России.
Таблетки
Активное вещество - соединение формулы (I) в количестве 100 мг, 200 мг - массовая часть 40%. Целевые добавки (лактоза, аэросил, стеарат кальция) - массовая часть 60%.
Смешивают основное и вспомогательные вещества в соотношениях, указанных в таблице 8 (расчет на массу таблетки):
Диаметр шаров - 5 мм. Масса шаров на 100г готовой формы - 500 г.
Прессование таблеток осуществляют на прессе РТМ-12. На таблетки наносят покрытие на основе ацетилфталилцеллюлозы (АФЦ) на аппарате "Strea-1". Состав покрытия (массовые части): ацетон - 56,4; этиловый спирт 96% - 37,6; касторовое масло - 1,0; АФЦ - 5,0; тропеолин - добавляют до светло-коричневой окраски раствора. Расход покрытия: количество покрытия (мл) = 50% от массы таблеток (г).
Раствор для инъекции
Гидрохлорид для инъекций представляет собой рассыпку порошка лекарственного средства, включающее активное вещество и его фармацевтически приемлемые соли в дозировке 0,1-0,5 г.
Конкретные составы указаны в таблице 9.
Эксперимент на животных (кроликах) показал, что около 50% этого соединения в неизменном видеобнаруживается в продуктах их жизнедеятельности. Биологические же испытания гидрохлорида (I) показали, что его действие на гуморральный иммунитет при приеме перорально незначительно выше, чем у соединения (В), тогда как при парентеральном введении одинаковый эффект достигается при введении в 8 раз меньших доз гидрохлорида.
Гидрохлорид по сравнению с вышеуказанным соединением (В) показал антимикробную активность, в случае с В. cereus - бактерицидную, а в случае с St. aureus - бактериостатическую, о чем свидетельствуют данные таблицы 10.

| название | год | авторы | номер документа |
|---|---|---|---|
| ДИНАТРИЕВАЯ СОЛЬ N-(6-МЕТИЛ-2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРО-5H-ПИРИМИДИНСУЛЬФОН)-N'- ИЗОНИКОТИНОИЛГИДРАЗИДА, ПРОЯВЛЯЮЩАЯ АНТИМИКРОБНУЮ И ИММУНОТРОПНУЮ АКТИВНОСТЬ, И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕЕ ОСНОВЕ | 1999 |
|
RU2191015C2 |
| ОРОТАТ ГИДРАЗИДА ИЗОНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ АНТИМИКОБАКТЕРИАЛЬНОЙ И ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1990 |
|
RU2044728C1 |
| N,N'-(СУЛЬФОНИЛДИ-1,4-ФЕНИЛЕН)БИС(N'',N''- ДИМЕТИЛФОРМАМИДИН)1,2,3,4-ТЕТРАГИДРО-6-МЕТИЛ-2,4- ДИОКСО-5-ПИРИМИДИНСУЛЬФОНАТ, СТИМУЛИРУЮЩИЙ КЛЕТОЧНЫЙ МЕТАБОЛИЗМ И ОБЛАДАЮЩИЙ ИММУНОТРОПНОЙ И АНТИМИКОБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2136668C1 |
| N-(6-МЕТИЛ-2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОПИРИМИДИНИЛ-5-СУЛЬФОНИЛ) ПИРАЗИН-2-КАРБОКСАМИД, ОБЛАДАЮЩИЙ ПРОТИВОЛЕПРОЗНОЙ, ПРОТИВОТУБЕРКУЛЕЗНОЙ И ИММУНОТРОПНОЙ АКТИВНОСТЬЮ, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2102390C1 |
| 4,4'-СУЛЬФОНИЛБИС-(N,N'-ДИМЕТИЛАММОНИОМЕТИЛЕНАНИЛИН)-ХЛОРИД, 6-МЕТИЛ-2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОПИРИМИДИН-5-СУЛЬФОНАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2004 |
|
RU2275356C2 |
| ТРИАЗИНЫ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2431633C1 |
| ПРОИЗВОДНЫЕ β-КАРБОЛИНА, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ, ИХ ПРИМЕНЕНИЯ ДЛЯ ПРОИЗВОДСТВА ЛЕКАРСТВЕННОГО СРЕДСТВА, СПОСОБ ИХ СИНТЕЗА, А ТАКЖЕ НОВЫЕ МЕТОДЫ ЛЕЧЕНИЯ С ИХ ИСПОЛЬЗОВАНИЕМ | 2010 |
|
RU2419431C1 |
| ОРОТАТ N,N'-ДИАМИНОДИФЕНИЛСУЛЬФОНА, ПРОЯВЛЯЮЩИЙ АНТИЛЕПРОЗНУЮ И ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1995 |
|
RU2074856C1 |
| ПРОТИВОТУБЕРКУЛЕЗНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ 4-ТИОУРЕИДОИМИНОМЕТИЛПИРИДИНИЯ ПЕРХЛОРАТА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2010 |
|
RU2423977C1 |
| Противотуберкулёзное средство на основе (Z)-3-(3,3-Диметил-2-оксобутилиден)-3,4-дигидро-2H-1,4-бензоксазин-2-она и способ его синтеза | 2020 |
|
RU2748748C1 |
Изобретение относится к новым 6-алкил-5-(2-изоникотиноилсульфогидразоил)урацил гидрохлоридам общей формулы (I), где R является алкилом с 1-4 атомами углерода, которые обладают антимикобактериальной и иммунотропной активностью и могут быть использованы в качестве иммуномодулятора и антимикобактериальных средств. Изобретение также относится к фармацевтической композиции на их основе. 3 н. и 1 з.п. ф-лы, 10 табл.
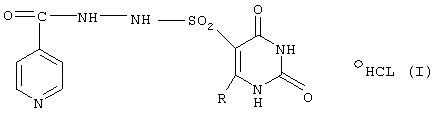
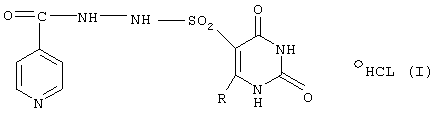
где R является алкилом с 1-4 атомами углерода.
| ИММУНОМОДУЛЯТОР С АНТИМИКОБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ "ИЗОФОН", СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 1997 |
|
RU2141322C1 |
Авторы
Даты
2005-11-20—Публикация
2003-07-11—Подача