Штамм "Краснодонский" вируса трансмиссивного гастроэнтерита свиней для изготовления диагностических и вакцинных препаратов.
Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при изготовлении средств диагностики и профилактики трансмиссивного гастроэнтерита свиней (ТГЭС).
Трансмиссивный гастроэнтерит свиней (инфекционный гастроэнтерит свиней, болезнь Дойла и Хатчингса) - инфекционная высококонтагиозная болезнь, главным образом поросят до 3-месячного возраста, характеризующаяся катарально-геморрагическим гастроэнтеритом, рвотой, профузной диареей, дегидратацией организма и сопровождающаяся атрофией ворсинок верхнего отдела тонкого кишечника и высокой смертностью (часто до 100%) среди поросят до 2-недельного возраста.
Заболевание широко распространено в большинстве стран мира с развитым свиноводством, в том числе в государствах СНГ, и наносит весьма значительный экономический ущерб. Он складывается из высокой смертности новорожденных поросят, низкой эффективности профилактики и лечения, а также сложности предупреждения заноса инфекции.
Возбудитель ТГЭС имеет вирусную этиологию. Его вирусную этиологию подтвердили американские исследователи Дойл и Хатчингс (1946), когда они описали фильтруемость этиологического агента ТГЭС. Вирус ТГЭС впервые выделил и описал японский исследователь Тайама (1970). Вирус ТГЭС относится к семейству Coronaviridae, роду Coronavirus.
К настоящему времени в различных регионах мира выделено большое количество изолятов вируса ТГЭС, которые не имеют серотипических различий, и по результатам реакции нейтрализации (РН) отнесены к одному серотипу. Выделенные изоляты вызывают сходную клиническую картину при заражении восприимчивых поросят 1-10-дневного возраста, полученных от неиммунных к вирусу ТГЭС свиноматок.
Выделенные изоляты вируса ТГЭС используют для изготовления вакцин, действие которых основано на том, что вируснейтрализующие колостральные антитела, вырабатываемые организмом свиноматок в ответ на введение им вакцинного вируса, обеспечивают защиту подсосных поросят от заражения вирулентным вирусом ТГЭС.
Для профилактики ТГЭС в России и за рубежом получили распространение живые и инактивированные вакцины из аттенуированного или убитого вируса ТГЭС различных штаммов (1).
Известен штамм V-52 вируса ТГЭС для изготовления вакцинных препаратов (2).
Известен штамм "№5 ВГНКИ" вируса ТГЭС для изготовления вакцинных препаратов (3).
Известен штамм "МК-25" вируса ТГЭС для изготовления вакцинных препаратов (4).
Известен штамм "ЛУК" респираторного коронавируса свиней (РКВС) для изготовления вакцинных препаратов против ТГЭС (5).
Известен штамм CAPM-V355 РКВС для изготовления вакцинных препаратов против ТГЭС (6).
Наиболее близким предлагаемому изобретению по совокупности существенных признаков является штамм "№1941 ВНИИВВиМ" вируса ТГЭС для изготовления вакцинных препаратов (7).
Недостатки известных штаммов, в том числе и штамма-прототипа, состоят:
1) в их остаточной вирулентности и низкой иммуногенной активности;
2) в непригодности для изготовления инактивированных вакцин.
В задачу создания настоящего изобретения входило получение нового производственного штамма вируса ТГЭС, обладающего высокой биологической, антигенной и иммуногенной активностью в нативном виде и после инактивации и обеспечивающего изготовление высокоспецифичных и чувствительных диагностикумов и высокоиммуногенных и безвредных инактивированных вакцинных препаратов.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала производственных штаммов вируса ТГЭС, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления высокоспецифичных и чувствительных диагностикумов и высокоиммуногенных и безвредных инактивированных вакцинных препаратов.
Указанный технический результат достигнут получением штамма "Краснодонский" вируса ТГЭС (авторское наименование).
Штамм "Краснодонский" выделен в 1998 году из тонкого отдела кишечника больных поросят-сосунов, принадлежащих ЗАО "Краснодонское" Волгоградской области серийными пассажами на первичной культуре клеток почки свиньи (СП) и адаптирован на 28 пассаже к перевиваемой монослойной культуре клеток почки эмбриона свиньи (СПЭВ) с титром, по меньшей мере, 7,5 Ig ТЦД50/см3. Вирус штамма "Краснодонский" является авирулентным для свиней.
Полученный штамм депонирован во Всероссийской государственной коллекции штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ВГНКИ) МСХ РФ 27 апреля 2001 года под регистрационным наименованием "аттенуированный эпителиотропный культуральный штамм "Краснодонский - ВНИИЗЖ-ДЕП" вируса ТГЭС.
По сравнению с прототипом штамм "Краснодонский-ВНИИЗЖ-ДЕП" вируса ТГЭС обладает более высокой биологической, антигенной и иммуногенной активностью в нативном виде и после инактивации. Экспериментально подтверждена возможность его использования для изготовления диагностических препаратов и инактивированной вакцины против ТГЭС, обеспечивающей защиту восприимчивых животных против возбудителя заболевания, циркулирующего на территории России.
Штамм "Краснодонский ВНИИЗЖ-ДЕП" вируса ТГЭС характеризуется следующими признаками и свойствами.
Морфологические свойства
При электронно-микроскопическом исследовании вируссодержащего материала установлено, что вирус штамма "Краснодонский-ВНИИЗЖ-ДЕП" является оболочечным, плеоморфным, диаметром 80-150 нм, имеет один слой булавообразных отростков на поверхности проекции длиной 12-25 нм, т.е. штамм морфологически тождественен представителям сем. Coronaviridae, рода Coronavirus.
Антигенные свойства
Штамм "Краснодонский-ВНИИЗЖ-ДЕП" вируса ТГЭС индуцирует синтез вируснейтрализующих и преципитирующих антител к вирусу ТГЭС в организме свиней и кроликов. Его антигенное родство изучали в перекрестной реакции микронейтрализации (РМН). Вирус не проявляет гемагглютинирующей активности (ГА-активности).
Биотехнологические характеристики
Штамм "Краснодонский-ВНИИЗЖ-ДЕП" является аттенуированным, эпителиотропным, культуральным. Наиболее эффективно размножается в перевиваемой культуре клеток СПЭВ с выраженным ЦПД, проявляющемся в округлении и гибели клеток с последующей деструкцией монослоя через 24-30 часов после его заражения.
Оптимальными условиями выращивания вируса ТГЭС в культуре клеток СПЭВ являются заражение 3-4-суточного монослоя, полученного на роллерных сосудах, в дозе 0,1 ТЦД50/кл и снятие урожая через 24-30 часов после инфицирования.
Титр вируса в указанной культуре клеток достигает 7,5 Ig ТЦД50/см3. При титровании вирусной суспензии обнаружилось, что при 70-80% ЦПД титр вируса на 0,5-1,25 Ig ТЦД50/см3 выше, чем при 90-100% поражения монослоя. Результаты адаптации предлагаемого штамма к перевиваемым культурам клеток, изучения динамики накопления вируса в клеточной культуре СПЭВ в зависимости от возраста монослоя, времени культивирования и дозы заражения культуры клеток вирусом приведены в таблицах 1, 2, 3 и 4.
Хемо- и генотаксономическая характеристика
Штамм "Краснодонский-ВНИИЗЖ-ДЕП" является РНК-содержащим вирусом. Вирус содержит одну большую полиаденилированную плюс РНК (>23 кДа). РНК, экстрагированная из вирионов, обладает инфекционностью. Вирус был исследован методом ПЦР, и в пробе подтверждено наличие только геномной РНК.
В процессе репликации вируса синтезируется 5-7 субгеномных мРНК с общими 3'-концами для продукции вирусных белков. Определена нуклеотидная последовательность по 3'-концу генома, соответствующая мРНК. Плавучая плотность вирионов в градиенте сахарозы составляет 1,18-1,20 г/см3. Фосфо- и гликолипиды, инкорпорированные в оболочку, имеют клеточное происхождение, т.е. оболочка вириона является клеточно-зависимой. Вирус содержит 3 главных структурных белка: нуклеокапсидный белок (N), мелкий оболочечный гликопротеин (М) и большой гликопротеин пепломеров (S).
В зрелом вирионе N-протеин "вплетен" в вирусную РНК, образуя рибонуклеопротеидный комплекс.
Гетерофильный N-конец гликопротеина М выступает из вириона, имеет единственный доступный гликопротеиновый сайт и обеспечивает индукцию комплементсвязывающих и вируснейтрализующих антител, а также интерферона. Гликопротеин S (или пепломерный белок) мол.массы 195-220 кДа смотрится на электронограммах как корона вируса. Он отвечает за прикрепление вируса к клетке, расплавление мембраны и индукцию комплементнезависимых вируснейтрализующих антител. Очищенный S-гликопротеин индуцирует образование вируснейтрализующих антител, которые нейтрализуют репликацию вируса на всех стадиях. Определен 3' участок генома вируса. Этот участок содержит 3 главных структурных гена с согласованностью коронавирусной ориентации 5'-S-M-N-3' и 4 больших открытых рамки считывания, которые кодируют потенциальные вирусные протеины.
5' часть генома кодирует вирусную репликазу/транскриптазу.
Вирулентные свойства
Штамм "Краснодонский-ВНИИЗЖ-ДЕП" является авирулентным для свиней.
Иммуногенные свойства
При введении лабораторным животных (кролики, морские свинки) и поросятам-сосунам вызывает образование специфических антител и устойчивость поросят-сосунов к прямому заражению вирулентными штаммами вируса ТГЭС.
Устойчивость к внешним факторам
Вирус штамма "Краснодонский-ВНИИЗЖ-ДЕП" чувствителен к эфиру, хлороформу и дезоксихолату натрия, устойчив к трипсину. Не подавляется ДНК ингибиторами. Инактивируется 0,03% раствором формалина, 1% Lysovet (смесь фенола и альдегида), 0,01% раствором β-пропиолактона, гипохлорита натрия, едкого натра, йода. Вирус устойчив к замораживанию. В замороженном виде вируссодержащий материал сохраняется 5-8 недель, при -18°С до 18 месяцев, при -20, -40 или -80°С - не менее 365 дней. При нагревании до 56°С и н активируется за 30 минут и до 50°С в присутствии 1 М MgCl2 - за 1 час. При 37°С полная потеря инфекционности наступила через 4 дня. Устойчив к рН (4-9). Амантадин и пуромицин тормозят репродукцию вируса. Вирус стабилен в желчи поросят при рН 3,0, сохраняющей его инфекционность в тонком кишечнике.
Условия хранения
Штамм хранится в нативном состоянии при температуре -70°С, рН среды 7,2-7,4. Допустимая длительность хранения без освежения 18 месяцев.
Стабильность основных свойств штамма
В течение 18 месяцев хранения не снижает титр инфекционной активности, сохраняет антигенную (в РМН) и иммуногенную активность, а также стабильность генетических свойств как в период хранения, так и в пассажах на СПЭВ (9-10 пассажей).
Дополнительные сведения о штамме
Свободен от контаминации бактериями, микоплазмами, грибами и другими вирусами.
На основании полученных данных можно утверждать, что штамм "Краснодонский-ВНИИЗЖ-ДЕП" по антигенному и иммуногенному спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным изолятом вируса ТГЭС.
По мнению заявителя предлагаемый штамм соответствует установленным Патентным законом России условиям патентоспособности "новизна" и "изобретательский уровень".
Сущность предлагаемого изобретения пояснена примерами его использования.
Пример 1.
Исходный вирус для получения штамма "Краснодонский-ВНИИЗЖ-ДЕП" выделен в 1998 году из тонкого отдела кишечника больных поросят-сосунов, принадлежащих ЗАО "Краснодонское" Волгоградской области, серийными пассажами на первичной культуре клеток СП.
Вакцинный штамм получен в ФГУ ВНИИЗЖ путем адаптации к перевиваемой культуре клеток СПЭВ. Штамм является авирулентным для свиней.
Результаты исследований по адаптации вируса ТГЭС штамма "Краснодонский-ВНИИЗЖ-ДЕП" к перевиваемым культурам клеток представлены в таблице 1.
Полученный вирус был подвергнут всестороннему контролю в соответствии с руководством МЭБ по стандартным диагностическим методам и вакцинам (1996) и на уровне 28 пассажа в культуре клеток СПЭВ заложен на хранение в качестве матровой расплодки. Вирус матровой расплодки с титром инфекционной активности 7,5 Ig ТЦД50/см3 представлен в виде нативной суспензии культуральной жидкости и пораженного монослоя, хранится при температуре -70°С.
Полученному штамму вируса ТГЭС присвоено авторское наименование "Краснодонский". Штамм депонирован в коллекции микроорганизмов ВГНКИ под регистрационным наименованием "аттенуированный эпителиотропный культуральный штамм "Краснодонский-ВНИИЗЖ-ДЕП" вируса ТГЭС.
Пример 2.
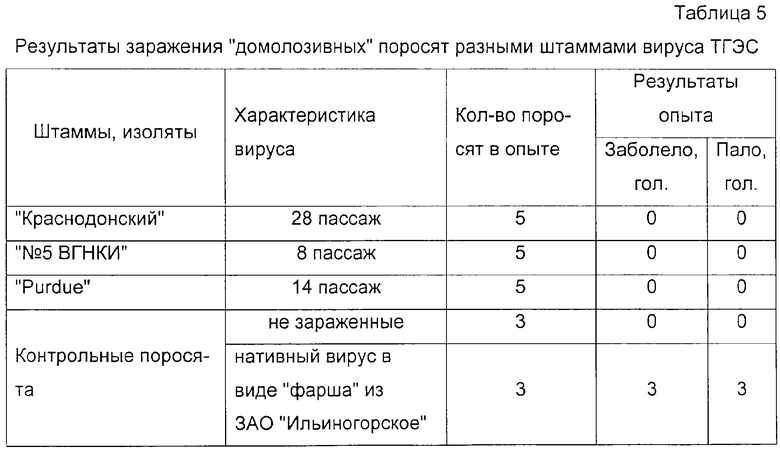
Вирулентные свойства штамма "Краснодонский-ВНИИЗЖ-ДЕП" изучены на "домолозивных" поросятах.
Для сравнения в опытах использовали также суспензию из "фарша", используемого в хозяйствах для изготовления "тканевой" вакцины для иммунизации свиноматок против ТГЭС, и аттенуированные штаммы "Purdue" (эталонный) и "№5 ВГНКИ". Последний используется для производства вирусвакцины на Омском биокомбинате.
Каждую зараженную и контрольную группу животных содержали изолированно. Клинические наблюдения вели в течение 48 часов. Результаты этих опытов приведены в таблице 5.
Согласно данным таблицы 5 штамм "Краснодонский-ВНИИЗЖ-ДЕП", а также штаммы "Purdue" и "№5 ВГНКИ" являются авирулентными, так как все зараженные поросята за период наблюдения оставались клинически здоровыми. Все поросята, зараженные суспензией из "фарша", заболели через 18 часов с характерной клинической картиной ТГЭС. Контрольные, т.е. незараженные поросята оставались клинически здоровыми в течение 48 часов (срок наблюдения).
Пример 3.
Проведены сравнительные испытания антигенных свойств штаммов "Краснодонский-ВНИИЗЖ-ДЕП" и "Purdue" вируса ТГЭС. Для этого на них были получены гипериммунные сыворотки от взрослых кроликов. В опытах использовали очищенные антигены с инфекционной активностью, по меньшей мере, 7,5 Ig ТЦД50/см3, которые смешивали с масляным адъювантом Montanide ISA-70 в соотношении 1:1,5, получая водно-масляную эмульсию. Полученные препараты вводили кроликам внутримышечно в объеме 2,0 см3 двукратно с интервалом в 14 дней. Пробы крови от кроликов отбирали до и через 14-30 дней после иммунизации и сыворотки исследовали в РМН на наличие антител против эталонного штамма "Miller" вируса ТГЭС. Результаты исследований представлены в таблице 6.
Из данных, представленных в таблице 6, видно, что на 14 день после иммунизации против испытуемых штаммов в сыворотках крови кроликов образовались специфические вируснейтрализующие антитела. После повторной иммунизации уровень антител во всех группах повысился, при этом средний уровень антител в группе животных, иммунизированных эмульсионным препаратом из штамма "Краснодонский-ВНИИЗЖ-ДЕП", составил 5,25±0,25 log2, который оказался несколько ниже среднего уровня антител в 6,66±0,31 log2 в группе животных, иммунизированных эмульсионным препаратом из штамма "Purdue".
Таким образом, в результате проведенных исследований установлено, что предлагаемый штамм обладает высокой антигенной активностью и пригоден для изготовления диагностических препаратов.
Пример 4.
Инактивированную эмульсионную вакцину против ТГЭС из штамма "Краснодонский-ВНИИЗЖ-ДЕП" получают следующим образом.
Для изготовления вакцины используют выращенную в роллерных сосудах культуру клеток СПЭВ с хорошим монослоем 3-4-суточного возраста. В качестве ростовой используют среду ПСП с добавлением сыворотки. Для изготовления 20 литров вируссодержащей суспензии вируса ТГЭС берут от 90 до 100 роллерных сосудов с культурой клеток емкостью 3,0 дм3 каждый. После слива ростовой среды клеточный монослой промывают раствором Хенкса или фосфатно-буферным раствором с рН 7,2-7,4, затем в роллерные сосуды вносят по 3-5 см3 вируса ТГЭС матриксной серии. После 40-60 минут инкубирования при температуре 37±2°С в роллерные сосуды вносят по 250-300 см3 поддерживающей среды (без сыворотки КРС).
Зараженные роллерные сосуды помещают в термальную комнату на вращающиеся роллерные установки для культивирования при 37±2°C.
Срок культивирования от 24 до 28 часов. Для контроля незараженными оставляют 2 роллерных сосуда, в которых ростовую среду меняют на 300 см3 поддерживающей среды. Начиная с 18 часа инкубирования, инфицированные и контрольные роллерные сосуды периодически микроскопируют. Роллерные сосуды, в которых наблюдаются цитопатические изменения с поражением до 70% клеточного монослоя (обычно через 24-28 часов) собирают и 3-кратно замораживают при температуре -20°С и оттаивают. После этого содержимое роллерных сосудов сливают в одну емкость и охлажденную вируссодержащую суспензию, соблюдая стерильные условия, освобождают от клеточного детрита центрифугированием при 3000 об/мин в течение 20 мин. Очищенная от детрита суспензия имеет вид прозрачной жидкости розовато-вишневого цвета. В очищенную суспензию вносят гентамицин (50 мкг/см3) и перемешивают 20 мин. Затем из емкости отбирают пробу для лабораторно-производственного контроля на стерильность и инфекционную активность вируса. Производственная серия ТГЭС должна иметь инфекционную активность, по меньшей мере, 6,5 Ig ТЦД50/см3. Полученный вирус подвергают инактивации. Для этого в вируссодержащую суспензию, нагретую до 26-28°С, вносят при постоянном перемешивании 25-32% раствор аминоэтилэтиленимина (АЭЭИ) до конечной концентрации 0,008% и устанавливают значение рН 7,2-7,6. Инактивацию ведут при 37±2°С в течение 22-24 часов с периодическим перемешиванием. По окончании инактивации суспензию охлаждают до 4-6°С, поддерживая рН на уровне 7,2-7,6. Затем отбирают пробы антигенного материала для проверки его на стерильность и авирулентность.
Антиген из культурального вируса ТГЭС считают пригодным для составления вакцины, если:
- грибково-бактериальная микрофлора отсутствует;
- антиген ТГЭС на СПЭВ не вызывает ЦПД.
Эмульсионную вакцину готовят путем диспергирования смеси антигенного материала с масляным адъювантом Montanide ISA-70 (фирма Seppic, Франция). Для этого 2 части антигена и 3 части масляного адъюванта пропускают через коллоидные мельницы в течение 5-10 минут и готовую инактивированную эмульсионную вакцину собирают в одну стерильную емкость. Вакцину расфасовывают по 10, 50, 100 и 200 см3 в стерильные стеклянные флаконы, которые закрывают стерильными резиновыми пробками и закатывают алюминиевыми колпачками.
Готовая вакцина представляет собой эмульсию бело-розового цвета. При хранении вакцины возможно образование белого или бело-розового неплотного осадка, устраняющегося при встряхивании.
Полученную вакцину подвергают контролю на содержание водородных ионов (рН) в пределах 7,3±0,3, стерильность, стабильность, вязкость (55±20 мм2/с), полноту инактивации, безвредность и иммуногенную активность.
Вакцина предназначена для профилактической иммунизации свиней против ТГЭС.
Пример 5.
Проведены испытания иммуногенной активности инактивированной эмульсионной вакцины против ТГЭС из штамма "Краснодонский-ВНИИЗЖ-ДЕП", изготовленной так, как описано в примере 1.
Оценку проводили по результатам исследования в РМН против штамма "№5 ВНГКИ" вируса ТГЭС сывороток крови и молозива от вакцинированных свиноматок и поросят, полученных от них. Результаты этих исследований приведены в таблице 7.
В таблице 7 представлены убедительные доказательства того, что предлагаемый штамм обладает высокой иммуногенной активностью, безвредностью и пригоден для изготовления вакцинных препаратов.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемого изобретения следующей совокупности условий:
- штамм "Краснодонский-ВНИИЗЖ-ДЕП", воплощающий предлагаемое изобретение, предназначен для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии;
- для предлагаемого изобретения в том виде, как оно охарактеризовано в независимом пункте формулы изобретения, подтверждена возможность его осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- штамм "Краснодонский-ВНИИЗЖ-ДЕП", полученный в соответствии с предлагаемым изобретением, обладает высокой биологической, антигенной и иммуногенной активностью, пригоден для изготовления высокоспецифичных и чувствительных диагностикумов и высокоиммуногенных и безвредных вакцинных препаратов и расширяет арсенал новых производственных штаммов вируса ТГЭС.
Следовательно, предлагаемый штамм соответствует условию патентоспособности "промышленная применимость".
Источники информации
1. Сюрин В.Н., Самуйленко А.Я., Соловьев Б.В. и др. Вирусные болезни животных. - М.: ВНИТИБП, 1998. - С.165-183.
2. Патент США №4046875, 424-89, 1977.
3. Авт.свид. СССР №734279; С 12 N 7/00, 5/00; 15.05.80.
4. Авт.свид. СССР №1238294, А 61 К 39/225, 20.10.95.
5. Сергеев В.А., Рухадзе Г.Г. и Алипер Т.И. Респираторный коронавирус свиней. Вестник с.-х. науки, 1989, 8 (396). - С.96-100.
6. Авт.свид. СССР №1731812, С 12 N 7/00; 07.05.92.
7. Патент РФ №2140982; С 12 N 7/00, А 61 К 39/255; 10.11.99 (прототип).
12
7,0±0,15
8,75±0,25
10,2±0,3
<2,0
8,25±0,5
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ "ЛЕНИНГРАДСКИЙ" ВИРУСА ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2004 |
|
RU2266326C1 |
| ШТАММ "ИЛЬИНОГОРСКИЙ" ВИРУСА ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2004 |
|
RU2266328C1 |
| ШТАММ "ВН-96" ВИРУСА ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРОИЗВОДСТВА ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2009 |
|
RU2399668C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА И ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 2004 |
|
RU2269361C2 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ВИРУСНОЙ ДИАРЕИ, РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2515058C1 |
| ВАКЦИНА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ | 2002 |
|
RU2236253C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ЭМУЛЬСИОННОЙ ВАКЦИНЫ ПРОТИВ ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 2002 |
|
RU2214275C1 |
| ШТАММ "АС-21/07" ВИРУСА АУЕСКИ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2010 |
|
RU2439150C1 |
| ШТАММ "NADL-ВНИИЗЖ" ВИРУСА ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА DIARRHEA VIRUS BOVINUM ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТОВ ДЛЯ ДИАГНОСТИКИ, СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА | 2010 |
|
RU2449013C2 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2504400C1 |
Изобретение относится к ветеринарной вирусологии и биотехнологии. Штамм выделен и получен последовательными пассажами на культурах клеток СП и СПЭВ. Штамм депонирован в Коллекции микроорганизмов ВГНКИ под регистрационным наименованием «Краснодонский-ВНИИЗЖ-ДЕП». Вирус штамма «Краснодонский» наиболее эффективно размножается в 3-4-суточном монослое клеток СПЭВ, полученном на роллерных сосудах, достигая через 24-30 часов культивирования уровня инфекционной активности 7,5 Ig ТЦД50/см3. Сохраняет исходные характеристики в течение 18 месяцев хранения и в течение 9-10 пассажей на культуре клеток СПЭВ (срок наблюдения). Технический результат: изобретение расширяет арсенал производственных штаммов вируса ТГЭС, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления высокоспецифичных и чувствительных диагностикумов и высокоиммуногенных и безвредных инактивированных вакцинных препаратов. 7 табл.
Штамм вируса «Краснодонский» трансмиссивного гастроэнтерита свиней, семейства Coronaviridae, рода Coronavirus, коллекция ВГНКИ, «Краснодонский - ВНИИЗЖ-ДЕП», для изготовления диагностических и вакцинных препаратов.
| АТТЕНУИРОВАННЫЙ ШТАММ ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ (TRANSMISSIVE GASTROENTERITIS VIRUS) | 1998 |
|
RU2140982C1 |
| Штамм респираторного коронавируса свиней для изготовления вакцины против трансмиссивного гастроэнтерита свиней | 1990 |
|
SU1731812A1 |
Авторы
Даты
2005-12-20—Публикация
2004-03-09—Подача