Изобретение относится к новым способам получения 2-аминометилпиридинов (особенно 2-аминометил-3-хлор-5-трифторметилпиридина), а также получения 2-цианопиридинов, используемых для их приготовления, т.е. соединений, которые полезны в качестве промежуточных продуктов при получении пестицидов.
Известно каталитическое восстановление цианопиридинов с целью получения аминометилпиридинов. Однако когда соединение цианопиридина содержит дополнительный(е) атом(ы) галогена, восстановление может осложняться протеканием параллельной реакции дегалогенирования. В работе P.N.Rylander, Hydrogenation Methods (Best Synthetic Series, Academic Press), (1985), p.148 указывается, что обычно выбирают палладий, когда хотят осуществить реакцию дегалогенирования, и что платина и родий являются относительно неэффективными и следовательно часто используются в реакциях гидрирования, где необходимо сохранить галоген.
В отличие от вышеописанного предшествующего уровня техники заявители обнаружили, что использование палладиевого катализатора дает особенно хорошие результаты при восстановлении цианопиридинов, которые содержат дополнительный(е) атом(ы) галогена. Заявители разработали новый способ получения 2-аминометилпиридинов, которые содержат дополнительный(е) атом(ы) галогена, при котором происходит минимальное дегалогенирование и который подходит для процессов промышленного масштаба.
Был опубликован ряд методик введения цианогруппы в 2-положение пиридинового компонента. Типично они включают замещение галогена, в частности брома или фтора, в полярном растворителе, например в диметилсульфоксиде или диметилформамиде. Кроме того, существуют многочисленные методы, где в качестве исходных материалов используют активированную N-окись пиридина или N-алкилпиридин. Многие из данных путей цианирования используют реагенты на основе тяжелых металлов, содержащие медь или никель. Например, ЕР0034917 описывает получение 2-циано-3-хлор-5-трифторметилпиридина из аналога, содержащего бром в 2-положении, реакцией с цианидом одновалентной меди в диметилформамиде при 120°С.
Однако многие из данных способов предшествующего уровня техники страдают от одного или нескольких недостатков, включающих низкие выходы, использование тяжелых металлов, которые дают токсичные потоки отходов, или полярных растворителей, которые трудно регенерировать. Кроме того, методы, которые включают образование N-оксида пиридина или N-алкилпиридина, включают несколько стадий. Указанные недостатки становятся критичными при увеличении масштаба производства до промышленного.
Публикация патента GB номер 117970 описывает цианирование соединений 2-галогенпиридина активирующим реагентом и источником цианида в полярном растворителе и, таким образом, избегает многих описанных выше недостатков. Однако при проведении данной процедуры все еще остается необходимость рециркуляции активирующего реагента и апротонного растворителя для сведения к минимуму стоимости процесса промышленного масштаба.
Заявители разработали альтернативный и улучшенный способ получения 2-цианопиридинов, который можно использовать для процессов промышленного масштаба.
Согласно первому аспекту настоящего изобретения предлагается способ (А) получения соединения общей формулы (I):
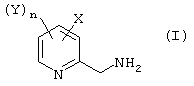
или его соли, включающий каталитическое гидрирование соединения общей формулы (II):
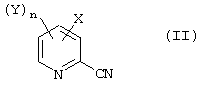
или его соли,
где Х представляет галоген; каждый из Y могут быть одинаковы или различны и представляют галоген, галогеналкил, алкоксикарбонил или алкилсульфонил; и n равно от 0 до 3.
В данном изобретении галоген означает атом фтора, хлора или брома. Предпочтительным атомом галогена является хлор.
Галогенированный алкил обычно означает алкильную группу C1-С6, замещенную одним или несколькими атомами галогена. Например, алкильная группа C1-C6 может представлять метил, этил, н-пропил или изопропил, предпочтительно метил. Алкильная группа C1-C6, предпочтительно, замещена одним или несколькими атомами хлора или фтора. Более предпочтительной галогеналкильной группой является трифторметил.
Алкоксикарбонильная группа обычно представляет C1-C6 алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, н-пропоксикарбонил или изо-пропоксикарбонил.
Алкилсульфонильная группа обычно представляет C1-C6 алкилсульфонил, где группа C1-C6 является такой, как определено выше.
Предпочтительно, Х является хлором.
Предпочтительно, Y является галогеном или галогеналкилом (более предпочтительно, трифторметилом).
Соединение (II) предпочтительно представляет собой 3-хлор-2-циано-5-трифторметилпиридин.
Как правило, катализатор включает металл, выбранный из палладия, платины, рутения, никеля или кобальта. Количество металла в используемом катализаторе (который обычно нанесен, например, на древесный уголь), как правило, составляет 0,05-0,7% по массе относительно количества соединения формулы (II), предпочтительно, 0,05-0,3%, более предпочтительно, 0,1-0,2%. Предпочтительный катализатор содержит палладий, например, тонко дисперсный палладий на инертном носителе, таком как древесный уголь. Было обнаружено, что это обеспечивает как подходящую скорость реакции, так и минимум побочных реакций. Таким образом, когда соединением формулы (II) является 3-хлор-2-циано-5-трифторметилпиридин, имеет место минимальное дехлорирование при использовании способа по изобретению. Другие примеры подходящих катализаторов включают катализаторы, содержащие оксиды и другие соединения вышеуказанных металлов.
Обычно способ проводят в присутствии растворителя, такого как спирт, например метанола, этанола, пропанола или бутанола, или такого как сложный эфир, например этилацетата, или такого как эфир, например тетрагидрофурана. Спиртовые растворители являются предпочтительными (метанол является наиболее предпочтительным). Предпочтительно, способ осуществляют в присутствии сильной кислоты, такой как хлористоводородная кислота, бромистоводородная кислота, серная кислота или фосфорная кислота (предпочтительно, хлористоводородной кислоты). Присутствие кислоты помогает предотвратить отравление катализатора аминогруппой продукта формулы (I), а также предотвращает взаимодействие промежуточных аминосоединений, которое, как известно, в противном случае происходит в ходе каталитического гидрирования нитрилов.
Условия реакции обычно включают объединение всех реагентов в подходящем реакционном сосуде и перемешивание, например, при температуре от 0 до 60°С, предпочтительно от 20 до 30°С. Дополнительное преимущество способа заключается в том, что используют низкое давление, причем, как правило, применяют давление водорода, составляющее от 1 до 4 атмосфер (предпочтительно, способ проводят при 1 атмосфере).
Необязательно реакцию проводят в присутствии ингибитора катализатора, который может привести к дополнительному улучшению селективности реакции, уменьшая степень дегалогенирования, которое может происходить в виде побочной реакции. Такие ингибиторы катализатора известны из уровня техники, например, как описывается в P.N.Rylander, Hydrogenation Methods (Best Synthetic Series, Academic Press), (1985), p.125-126, и включают бромиды или йодиды щелочных металлов, такие как бромид калия или йодид калия; или бромид аммония или йодид аммония; или бромистый водород или йодистый водород; или соединения фосфора, такие как трифенилфосфит, фосфорноватистая кислота, фосфористая кислота или алкилфосфиновые кислоты; или тиодигликоль (2,2'-тиодиэтанол); или тиомочевину; или серу. Предпочтительно, ингибитор катализатора выбран из бромида или йодида щелочных металлов, бромида или йодида аммония и йодистого водорода.
Таким образом, настоящее изобретение предлагает обеспечивающий высокую производительность селективный и удобный способ получения 2-аминометилпиридинов.
Также удобно получать соединение формулы (I) в форме соли, также хлористоводородной соли. При использовании в качестве промежуточного продукта при производстве пестицида соль может подаваться непосредственно на следующую стадию реакции без предварительного выделения соответствующего свободного амина. Следовательно, получение соли и ее последующую реакцию можно легко осуществить в одном сосуде. Особенно предпочтительной солью является 2-аминометил-3-хлор-5-трифторметилпиридина гидрохлорид.
Согласно следующему аспекту настоящего изобретения предлагается способ (В) получения соединения общей формулы (II), как определено выше, который включает обработку соединения общей формулы (III):
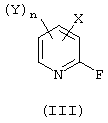
источником цианида и катализатором в водном растворителе или в отсутствии растворителя,
где X, Y и n являются такими, как определено выше; и где источником цианида является цианистый водород, цианид щелочного металла, цианид щелочноземельного металла или цианид необязательно замещенного аммония.
Катализатор, как правило, является межфазным катализатором, таким как соль тетраалкиламмония, например хлоридом бензилтриметиламмония, хлоридом трикаприлилметиламмония, хлоридом тетраметиламмония, бромидом тетра-н-пропиламмония, хлоридом н-додецилтриметиламмония, хлоридом тетра-н-бутиламмония, бромидом тетра-н-бутиламмония, бромидом тетра-н-октиламмония или бромидом н-тетрадецилтриметиламмония; или соль тетраалкилфосфония, например, бромидом тетра-н-бутилфосфония или бромидом тетрафенилфосфония; или краун-эфир или его ациклический аналог, например TDA-1 (трис[2-(2-метоксиэтокси)этил]амин); или амин, такой как 4-диметиламинопиридин.
Предпочтительно катализатор выбран из хлорида трикаприлилметиламмония и бромида тетра-н-октиламмония.
Количество используемого катализатора, обычно, составляет примерно от 0,01 до 10 мольн.%, предпочтительно примерно от 0,1 до 5 мольн.%, более предпочтительно примерно от 1 до 5 мольн.%.
Соединение (III) предпочтительно представляет собой 3-хлор-2-фтор-5-трифторметилпиридин.
Вышеуказанный способ (В) по изобретению является способом получения 2-цианопиридинов, обеспечивающим высокий выход, который является простым для осуществления, работает при умеренных температурах и не страдает от недостатков многих способов предшествующего уровня техники. В частности, способ по изобретению не требует цианидов тяжелых металлов, таких как цианид меди или цианид никеля, которые при использовании в промышленном масштабе приводят к образованию токсичных эффлюентных потоков и трудны для регенерации. Способ (В) по изобретению дает потоки отходов, которые легко перерабатывать.
Кроме того, способ не требует получения активированного N-оксида пиридина или N-алкил пиридина для высоких степеней превращения, что необходимо для многих способов предшествующего уровня техники. Способ (В) по изобретению не требует активирующего агента, такого как 4-диметиламинопиридин и, следовательно, исключает необходимость дополнительных стадий регенерации и рециркуляции. Следующее преимущество способа (В) по изобретению заключается в том, что в реакции не используются органические растворители, таким образом, исключается необходимость рециркуляции дорогостоящих растворителей, таких как диметилсульфоксид.
Предпочтительно, источником цианида является цианид натрия или цианид калия, предпочтительно цианид калия. Количество используемого источника цианида, как правило, составляет примерно от 1,0 до 2,0 молярных эквивалентов (однако, если желательно, можно использовать большее количество), предпочтительно, от 1,0 до 1,5 молярных эквивалентов, более предпочтительно, от 1,0 до 1,1 молярных эквивалентов.
Как правило, и предпочтительно реакцию проводят с использованием воды в качестве растворителя, однако ее можно также провести в отсутствие растворителя.
Условия реакции обычно включают объединение всех реагентов в подходящем реакционном сосуде и перемешивание при температуре от 10 до 60°С, предпочтительно от 20 до 40°С.
Таким образом, настоящее изобретение предлагает способ (В) получения 2-цианопиридинов, обеспечивающий высокий выход. Поскольку реакция использует умеренные температуры реакции, все что необходимо это простые и недорогие реакторы и расположенное за ними технологическое оборудование для отвода продуктов реакции. Более того, поскольку реагенты легко доступны, способ является недорогим в эксплуатации. Кроме того, настоящий способ дает потоки отходов, которые легко перерабатывать.
Согласно дальнейшему аспекту изобретения способы (В) и (А) можно объединить с целью получения соединения формулы (I) из соединения формулы (III).
Согласно следующему аспекту изобретения за способом (А), или объединенными способами (В) и (А) следует дополнительная стадия способа (С), которая включает ацилирование указанного соединения (I) соединением бензоила формулы (IV):
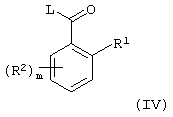
где L представляет уходящую группу; R1 и R2 каждый представляют галоген, одинаковые или различные; и m равно 0, 1 или 2, с целью получения соединения формулы (V):
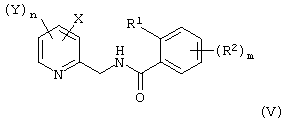
Предпочтительно L представляет хлор.
Соединения формулы (V) являются ценными пестицидными активными ингредиентами, описанными, например, в публикации международного патента номер WO 99/42447.
Предпочтительными соединениями формулы (V) являются:
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2,6-дихлорбензамид;
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2,6-дифторбензамид;
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2-хлор-6-фторбензамид;
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2,3-дифторбензамид;
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2,4,6-трифторбензамид
или
N-[(3-хлор-5-трифторметил-2-пиридил)метил]-2-бром-6-хлорбензамид.
Стадия способа (С) описывается в публикации международного патента номер WO 99/42447.
Согласно следующему аспекту изобретения способ (В) или объединенные способы (В) и (А), или (В), (А) и (С) можно объединить с более ранней стадией способа (D), которая включает фторирование соединения формулы (VI):
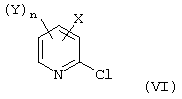
где X, Y и n являются такими, как описано выше.
Стадию способа (D) обычно осуществляют с использованием соответствующего фторирующего агента, такого как фторид щелочного металла, предпочтительно фторида калия или фторида натрия, в апротонном растворителе, таком как диметилсульфоксид или сульфолан, при температуре от 50°С до 150°С.
Соединения формул (I) и (II), полученные указанными выше способами по изобретению, особенно полезны до получения фунгицидно активных производных 2-пиридилметиламина формулы (V) по следующей ниже схеме реакции:
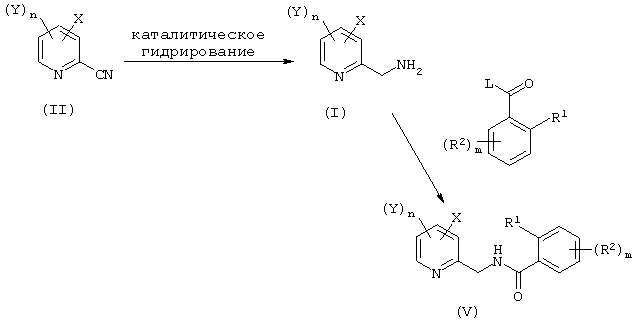
Далее настоящее изобретение иллюстрируется следующими примерами получения.
Пример 1 (стадия способа А)
Смесь 3-хлор-2-циано-5-трифторметилпиридина (5,1 г) и 5% палладия на древесном угле (5,1 мг по металлическому палладию) перемешивают при 20°C с метанолом и концентрированной хлористо-водородной кислотой (2,5 мл) в атмосфере водорода под давлением в 1 атмосферу. На основе данных ВЭЖХ полагают, что после 4 часов реакция завершается. Смесь фильтруют через Celatom, промывают метанолом и водой и выпаривают, получая 2-аминометил-3-хлор-5-трифторметилпиридина гидрохлорид с выходом 95-97%, ЯМР (в D2O) 4,6 (с, 2Н), 8,35 (с, 1Н), 8,9 (с, 1Н).
Пример 2 (стадия способа В)
К перемешанной смеси 3-хлор-2-фтор-5-трифторметилпиридина (199,5 г) и Aliquat 336 (хлорид трикаприлилметиламмония, 12,1 г) при 30°С в течение 1 часа добавляют раствор цианида калия (71,6 г) в воде (215 г). Перемешивание при данной температуре продолжают в течение 4 часов, после чего количество исходного фторида составляет менее 1% по данным ВЭЖХ. Нижнюю органическую фазу отделяют, промывают водным раствором хлорида натрия и перегоняют, получая 3-хлор-2-циано-5-трифторметилпиридин (185,8 г, выход 90%) Ткип=90°С при 15 мбар. Чистота данного продукта составляет 98%.
Пример 3 (стадия способа В)
К перемешанной смеси 3-хлор-2-фтор-5-трифторметилпиридина (0,8 г) и бромида тетрабутиламмония (0,06 г) при 20-25°С добавляют твердый цианид натрия (0,29 г) и перемешивают в течение 23 часов, получая 3-хлор-2-циано-5-трифторметилпиридин (0,68 г, выход 82% по ВЭЖХ).
Пример стадии способа D
К перемешанной смеси безводного фторида калия (320 г) и безводного диметилсульфоксида при 110°С добавляют 2,3-дихлор-5-трифторметилпиридин (800 г), затем нагревают при 120°С в течение 2 часов и подвергают фракционной перегонке при пониженном давлении, получая 3-хлор-2-фтор-5-трифторметилпиридин (685 г) с выходом 92% (чистота 98%).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-ЦИАНОПИРИДИНОВ | 2000 |
|
RU2222530C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ТРИФТОРМЕТИЛИЗОНИКОТИНОВОЙ КИСЛОТЫ И ЕЕ ЭФИРОВ | 2013 |
|
RU2654486C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ-1-ЦИАНОЦИКЛОБУТАНА | 1996 |
|
RU2179168C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИНИТРИЛОВ | 1994 |
|
RU2127724C1 |
| Способ получения 2-/2',2',2'-тригалогенэтил/-4-галогенциклобутан-1-онов | 1978 |
|
SU917695A3 |
| СПОСОБ ГИДРОЦИАНИРОВАНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С НЕНАСЫЩЕННОЙ ЭТИЛЕНОВОЙ СВЯЗЬЮ | 1996 |
|
RU2186058C2 |
| 2-АМИНО-5,5-ДИФТОР-5,6-ДИГИДРО-4Н-ОКСАЗИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ВАСЕ 1 И(ИЛИ) ВАСЕ 2 | 2010 |
|
RU2515221C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИЛЬНЫХ СОЕДИНЕНИЙ ИЗ ЭТИЛЕННЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ | 2009 |
|
RU2503656C2 |
| СПОСОБ ГИДРОЦИАНИРОВАНИЯ ОРГАНИЧЕСКИХ ЭТИЛЕННЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ | 2001 |
|
RU2250896C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИЛЬНЫХ СОЕДИНЕНИЙ ИЗ ЭТИЛЕННЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ | 2009 |
|
RU2509075C2 |
Изобретение относится к усовершенствованным способам получения соединений формул (I) и (II)
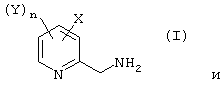
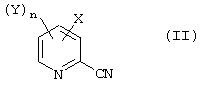
или их солей, где Х представляет галоген; Y представляет галоген, галогеналкил, алкоксикарбонил или алкилсульфонил; n равно от 0 до 3. Способ получения (I) заключается в каталическом гидрировании соединения (II) в присутствии катализатора, такого как палладий, в среде растворителя при температуре от 0 до 60°С. Способ позволяет получать целевые продукты с высоким выходом (95-97%) и высокой степени чистоты за счет сведения до минимума побочной реакции дегалогенирования исходных реагентов. Способ получения (II) заключается в обработке соответствующего 2-фторпроизводного источником цианида в присутствии катализатора, такого как соль тетраалкиламмония в водном растворителе или без растворителя при температуре от 10 до 60°С. Способ позволяет получать целевые продукты с высоким выходом (80-90%), высокой степени чистоты (98%) при умеренных температурах. 2 н. и 21 з.п. ф-лы.
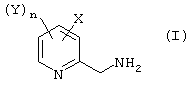
или его соли, включающий каталитическое гидрирование соединения общей формулы (II)
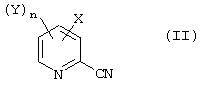
или его соли,
где Х представляет галоген; каждый из Y, которые могут быть одинаковы или различны, представляют собой галоген, галогеналкил, алкоксикарбонил или алкилсульфонил и n равно от 0 до 3; в присутствии катализатора, такого как палладий, причем процесс проводят в растворителе при температуре от 0 до 60°С.
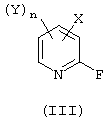
источником цианида в присутствии катализатора, представляющего собой соль тетраалкиламмония в водном растворителе или без растворителя,
где X, Y и n являются такими, как определено в п.1, и где источником цианида является цианистый водород, цианид щелочного металла, цианид щелочноземельного металла или необязательно замещенный цианид аммония.
Приоритет по пунктам:
| СПОСОБ ПОЛУЧЕНИЯ ПИРИДИЛМЕТИЛАМИНОВ | 1972 |
|
SU427008A1 |
| ПНЕВМАТИЧЕСКАЯ ТРАМБОВКА | 0 |
|
SU369208A1 |
| US 4851539 А, 25.07.1989 | |||
| Станок для сортировки листов бумаги и т.п. материала | 1930 |
|
SU34917A1 |
Авторы
Даты
2005-12-27—Публикация
2001-08-21—Подача