Изобретение относится к области технической физики, а именно к исследованию материалов с помощью анализа оптических сред, и может быть использовано для неразрушающего контроля молекулярного состава и структуры биологических препаратов, содержащих ароматические соединения, например, для контроля качественного и количественного состава лекарственных препаратов, для мониторинга веществ, загрязняющих окружающую среду, для выявления в биологических жидкостях токсических веществ и др.
Известен способ количественного определения состава многокомпонентных лекарственных препаратов жаропонижающего, анальгезирующего, противопростудного действия (RU 2267115 C2, 23.06.2003). Данный способ одновременного количественного определения состава многокомпонентных лекарственных препаратов методом обращенно-фазовой высокоэффективной жидкостной хроматографии с помощью ультрафиолетового детектора, характеризующийся тем, что анализ препаратов жаропонижающего, анальгезирующего, противопростудного действия, содержащих парацетамол, пропифеназон, кофеин, фенобарбитал, кодеина фосфат, или парацетамол, аскорбиновую кислоту, кодеина фосфат, фенилэфедрина гидрохлорид, хлорфениламина малеат, или парацетамол, теофиллин, кофеин, фенобарбитал, эфедрина гидрохлорид, или кодеина фосфат, нипагин, нипазол, проводят в одну стадию в режиме линейного градиента, наклон и продолжительность которого определяют свойствами компонентов анализируемого препарата, при этом состав подвижной фазы изменяется от фосфатного буферного раствора с pH 3,0 до смеси ацетонитрила с этим же фосфатным буферным раствором в объемном соотношении
1:1. При анализе лекарственных препаратов, содержащих анальгин или неидентифицированные компоненты растительного сырья, на начальном этапе градиента вводится подвижная фаза, содержащая только ацетонитрил и воду, а фосфатный буферный раствор вводится в подвижную фазу после выхода всех пиков, кроме кодеина.
Данный способ обладает рядом недостатков, таких как:
1) ограниченность, поскольку не для всех компонентов, входящих в состав препарата, возможно установить количественные характеристики;
2) недостоверность: качественный состав препарата не может быть установлен;
3) сложная и трудоемкая методика исследования;
4) затратность, поскольку для исследования необходимо использовать сторонние реагенты.
Наиболее близким к заявленному способу является способ анализа жидкой биологической среды в процессе мониторинга (RU 2212029 C1, 03.12.2001). Он основан на регистрации и последующем анализе электронных спектров поглощения в ультрафиолетовой области спектра. Способ анализа включает: мониторинг исследуемой среды, в ходе которого берут пробы исследуемой среды, определяют концентрацию присутствующих в среде компонентов в каждой пробе, одновременно измеряют спектры поглощения каждой пробы, после чего определяют границы информативной области спектра, в пределах которой наблюдается изменение спектра поглощения взятых проб, после чего измеряют спектры поглощения каждого из присутствующих в среде компонентов в ультрафиолетовой области спектра, выделяют компоненты, полосы собственного поглощения которых приходятся на информативную область, и определяют зависимости спектрального коэффициента экстинкции от концентрации для выделенных компонентов в этой области в диапазоне концентраций проб с учетом взаимного влияния компонентов, затем проводят мониторинг аналогичного процесса, в ходе которого через установленные интервалы времени измеряют спектры поглощения исследуемой среды в информативной области и для каждого спектра вычисляют концентрации тех компонентов, для которых получены спектральные характеристики коэффициента экстинкции.
К недостаткам данного способа можно отнести:
1) трудоемкость методики исследования;
2) необходимость использования большого объема исследуемого образца;
3) длительное проведение эксперимента и сложная обработка результатов.
Задачи, которые решены изобретением, состоят в обеспечении неразрушающего контроля высокой степени достоверности молекулярного состава и структуры биологических препаратов с минимизацией временных затрат на исследование.
Поставленная задача решена следующим образом. Способ неразрушающего контроля молекулярного состава и структуры биологических препаратов, содержащих ароматические соединения, характеризующийся тем, что для регистрации спектров флуоресценции образец облучают коротковолновым (266 нм) электромагнитным излучением ультрафиолетового диапазона с высоким (0,1 мм) пространственным разрешением, в этих веществах из-за наличия ароматических колец происходит фундаментальное электронное поглощение этих соединений в среднем ультрафиолетовом диапазоне, регистрируемые спектры флуоресценции преобразуют в корреляционные спектры флуоресценции, которые позволяют устанавливать различия в качественном и количественном составе образца даже при близости вида их спектров флуоресценции.
Для возбуждения и регистрации спектров флуоресценции использовалась известная волоконно-оптическая методика [1], в которой в качестве источника электромагнитного излучения ультрафиолетового диапазона используется четвертая гармоника (266 нм) лазера на алюмоиттриевом гранате, генерирующего импульсно-периодическое излучение с длиной волны 1064 нм. Высокое пространственное разрешение лазерных методов обеспечивается тем, что зондирующее излучение лазера с помощью кварцевого световода с внутренним диаметром 0,1 мм подводится к поверхности исследуемого образца.
Для установления количественного отличия спектров, полученных от различных биологических образцов, строят корреляционные функции 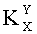
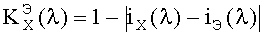
где iX(λ), iЭ(λ) - нормированные спектры флуоресценции анализируемого образца (X) и эталонного (Э).
Коэффициенты корреляции 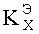
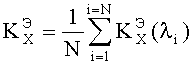
где N - количество диапазонов разбиения.
Пример.
Рассмотрим возможность применения заявленного способа для контроля качественного и количественного состава фармацевтических препаратов, таких как цитрамон, анальгин, аспирин, парацетамол.
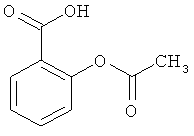
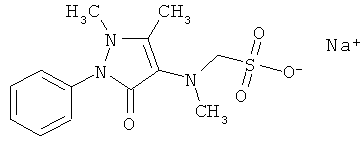

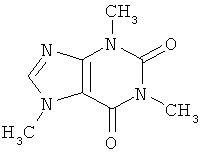
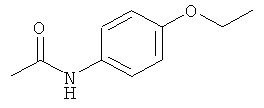
Из таблицы 1 видно, что в структуре всех исследуемых веществ присутствуют ароматические кольца, что приводит к фундаментальному электронному поглощению этих соединений в среднем ультрафиолетовом диапазоне. Соответственно, в этих веществах наблюдается флуоресценция в фиолетово-красном диапазоне при возбуждении флуоресценции коротковолновым (266 нм) электромагнитным излучением.
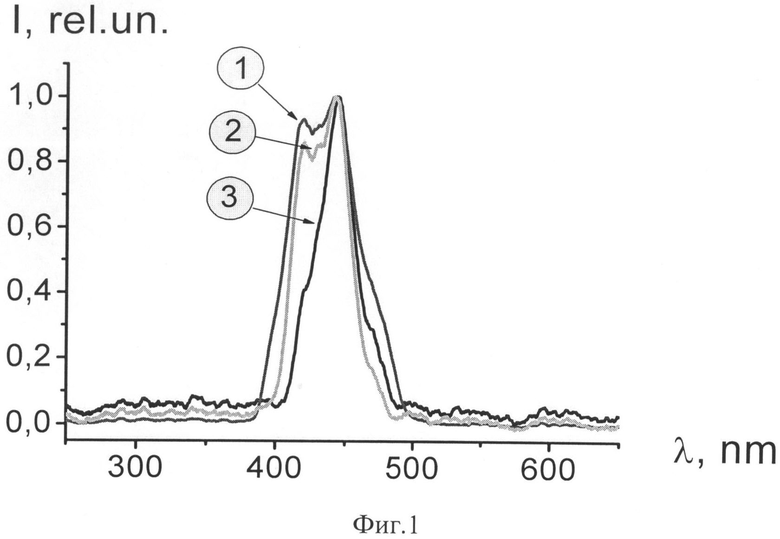
На основе зарегистрированных спектров флуоресценции фармацевтических препаратов были построены нормированные спектры флуоресценции. Фиг.1 иллюстрирует вид спектров флуоресценции таблетки цитрамона от нескольких точек на поверхности образца, отстоящих друг от друга на расстоянии 3-4 мм. Молекулярный состав анализируемой таблетки цитрамона оказывается различным для областей поверхности, представленных кривыми на Фиг.1: 1 - вид спектров флуоресценции таблетки цитрамона, на расстоянии 3 мм от левого края образца; 2 - вид спектров флуоресценции таблетки цитрамона, на расстоянии 6 мм от левого края образца; 3 - вид спектров флуоресценции таблетки цитрамона, на расстоянии 9 мм от левого края образца. Это свидетельствует о неоднородности молекулярного состава анализируемой пробы.
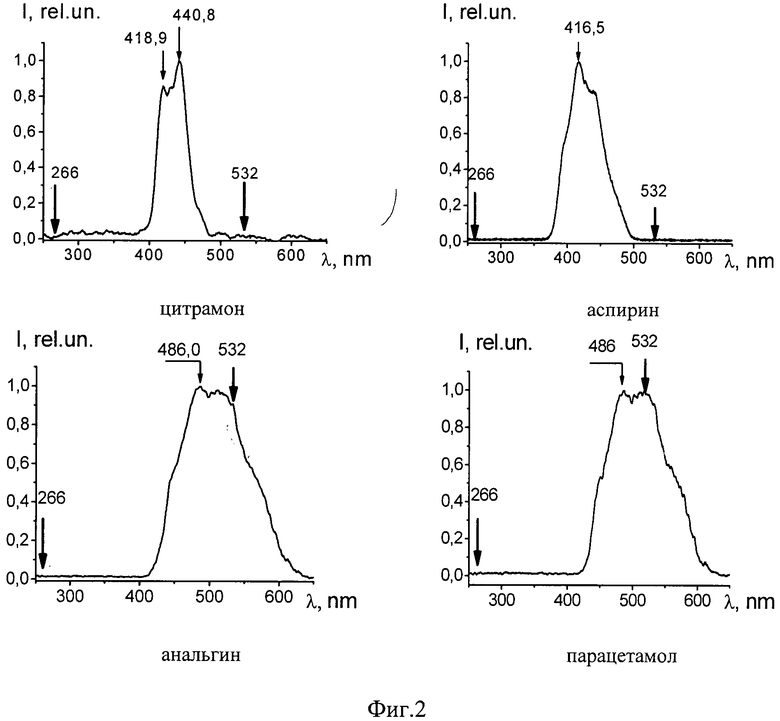
На Фиг.2 приводятся спектры флуоресценции всех четырех изучаемых препаратов. У всех анализируемых фармацевтических препаратов наблюдаются структурированные полосы флуоресценции в фиолетово-красной области спектра, форма которых несущественно отличается, по крайней мере, для цитрамона и аспирина, а также для анальгина и парацетамола. Для установления количественного отличия спектров, полученных от различных фармацевтических препаратов, нами были построены корреляционные функции с использованием следующего соотношения:
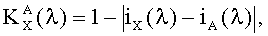
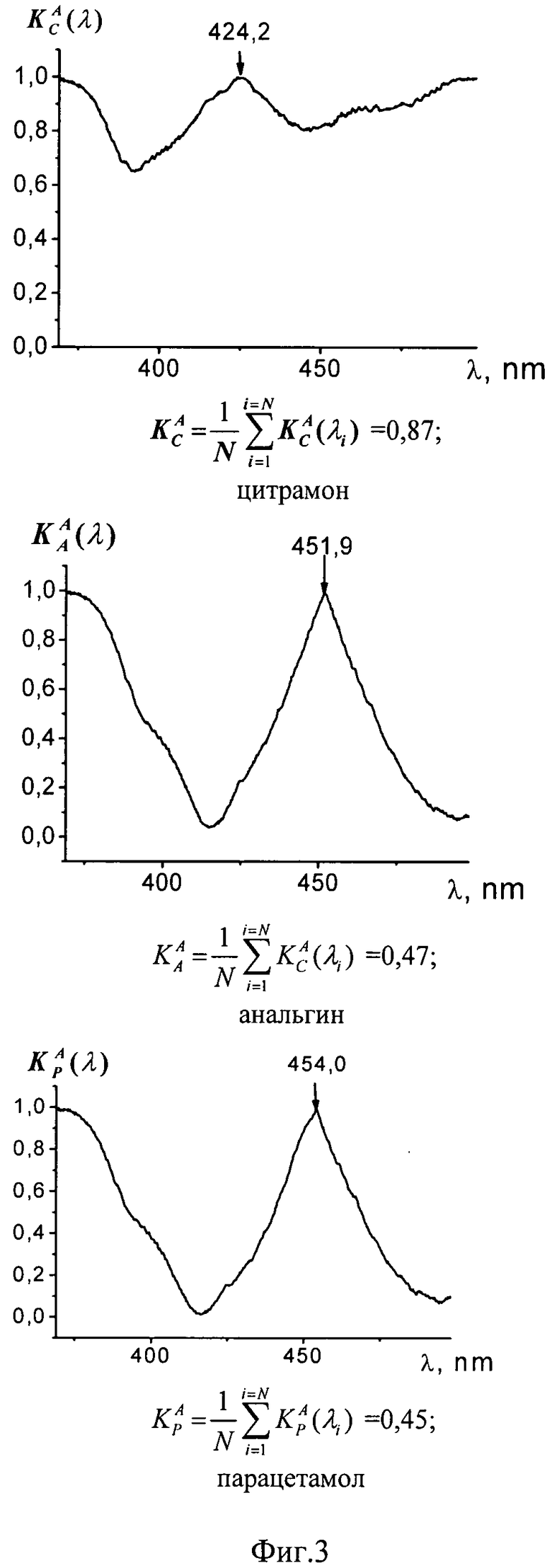
где iX(λ), iА(λ) - нормированные спектры флуоресценции анализируемого образца (X) и аспирина (А), соответствующие спектры приведены на Фиг.3. Корреляционные спектры строились в диапазоне длин волн Δλ=369-468 нм с интервалом разбиения Δλi=0.26 нм. Кроме того, были вычислены соответствующие коэффициенты корреляции анализируемых препаратов по отношению к аспирину по формуле:
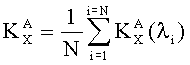
Близость вида спектров флуоресценции цитрамона и аспирина обусловлена присутствием в них одного и того же компонента. В то же время различия в спектрах флуоресценции от различных областей поверхности цитрамона обусловлена неравномерным распределением в нем компонентов (кофеина и фенацетина). Уширение полосы флуоресценции анальгина по сравнению со спектром парацетамола можно объяснить более сложной молекулярной структурой анальгина.
Литература
1. V.S.Gorelik, Yu.P.Voinov, V.D.Zvorykin, et al., Laser implantation of sodium nitrite ferroelectric into pores of synthetic opal / Journal of Russian Laser Research. 31(1), p.80 (2010).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОСТАВА МНОГОКОМПОНЕНТНОГО ЛЕКАРСТВЕННОГО ПРЕПАРАТА ЖАРОПОНИЖАЮЩЕГО, АНАЛГЕЗИРУЮЩЕГО, ПРОТИВОПРОСТУДНОГО ДЕЙСТВИЯ | 2005 |
|
RU2332663C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОСТАВА ТАБЛЕТОК "ПЕНТАЛГИН ФС" | 2005 |
|
RU2332662C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СОСТАВА МНОГОКОМПОНЕНТНЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ЖАРОПОНИЖАЮЩЕГО, АНАЛГЕЗИРУЮЩЕГО, ПРОТИВОПРОСТУДНОГО ДЕЙСТВИЯ | 2003 |
|
RU2267115C2 |
| Способ определения ацетилсалициловой кислоты | 1985 |
|
SU1269006A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ ПРИМЕСИ 4-МЕТИЛАМИНОАНТИПИРИНА В МНОГОКОМПОНЕНТНЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ ЖАРОПОНИЖАЮЩЕГО, АНАЛГЕЗИРУЮЩЕГО, ПРОТИВОПРОСТУДНОГО ДЕЙСТВИЯ | 2007 |
|
RU2338189C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОСТАВА МНОГОКОМПОНЕНТНОГО ЛЕКАРСТВЕННОГО ПРЕПАРАТА ПРОТИВОПРОСТУДНОГО, АНТИАЛЛЕРГИЧЕСКОГО ДЕЙСТВИЯ | 2007 |
|
RU2330281C1 |
| Способ количественного определения доксорубицина в биологических образцах | 2024 |
|
RU2839330C1 |
| СПОСОБ СПЕКТРАЛЬНОГО АНАЛИЗА ХИМИЧЕСКОГО СОСТАВА ВЕЩЕСТВА | 2006 |
|
RU2319137C1 |
| Способ определения парацетамола | 1982 |
|
SU1065347A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОГО ЗАГРЯЗНЕНИЯ ВОЗДУХА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2007 |
|
RU2337349C1 |
Изобретение относится к исследованию материалов с помощью анализа оптических сред и может быть использовано для неразрушающего контроля молекулярного состава и структуры различных веществ. Способ характеризуется тем, что для регистрации спектров флуоресценции образец облучают коротковолновым (266 нм) электромагнитным излучением ультрафиолетового диапазона с высоким (0,1 мм) пространственным разрешением. В этих веществах из-за наличия ароматических колец происходит фундаментальное электронное поглощение этих соединений в среднем ультрафиолетовом диапазоне, регистрируемые спектры флуоресценции преобразуют в корреляционные спектры флуоресценции, которые позволяют устанавливать различия в качественном и количественном составе образца даже при близости вида их спектров флуоресценции. Изобретение обеспечивает неразрушающий контроль высокой степени достоверности молекулярного состава и структуры биологических препаратов с минимизацией временных затрат на исследование. 2 з.п. ф-лы, 3 ил.
1. Способ анализа биологических препаратов по электронным спектрам поглощения в ультрафиолетовой области спектра, основанный на абсорбционном методе, отличающийся тем, что для регистрации спектров флуоресценции образец облучают коротковолновым (266 нм) электромагнитным излучением ультрафиолетового диапазона с высоким (0,1 мм) пространственным разрешением, в веществах из-за наличия ароматических колец происходит фундаментальное электронное поглощение этих соединений в среднем ультрафиолетовом диапазоне, причем регистрируют спектры флуоресценции, строят нормированные спектры анализируемого и эталонного образцов, используя которые, получают корреляционные функции с коэффициентами корреляции и строят корреляционные спектры, которые позволяют устанавливать различия в качественном и количественном составах образца даже при близости вида их спектров флуоресценции.
2. Способ по п.1, отличающийся тем, что для установления количественного отличия спектров, полученных от различных биологических образцов, строят корреляционные функции с использованием следующего соотношения:
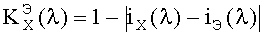
где iX(λ), iЭ(λ) - нормированные спектры флуоресценции анализируемого образца (X) и эталонного (Э).
3. Способ по п.1, отличающийся тем, что коэффициент корреляции 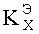
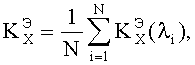
где N - количество диапазонов разбиения.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ МИКРОБОВ И СЛОЖНЫХ АМИНОКИСЛОТ | 2007 |
|
RU2362145C2 |
| СПОСОБ КОНТРОЛЯ КАЧЕСТВА НЕФТЕПРОДУКТОВ И ГОРЮЧЕ-СМАЗОЧНЫХ МАТЕРИАЛОВ | 2001 |
|
RU2187092C1 |
| Карусельная машина для отопки стеклянных изделий | 1950 |
|
SU93990A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СПОСОБ (ВАРИАНТЫ) И УСТРОЙСТВО ДЛЯ АНАЛИЗА СВОЙСТВ ФЛЮИДА ЭМУЛЬСИЙ С ИСПОЛЬЗОВАНИЕМ ФЛУОРЕСЦЕНТНОЙ СПЕКТРОСКОПИИ | 2007 |
|
RU2373523C2 |
| СПОСОБ АНАЛИЗА ЖИДКОЙ БИОЛОГИЧЕСКОЙ СРЕДЫ В ПРОЦЕССЕ МОНИТОРИНГА | 2001 |
|
RU2212029C1 |
Авторы
Даты
2013-07-20—Публикация
2011-11-22—Подача