Настоящее изобретение относится к применению производных бензазепин-N-уксусной кислоты, которые в α-положении относительно атома азота содержат оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой, и их солей и биолабильных эфиров, прежде всего для профилактики и/или лечения нарушений сердечной деятельности у крупных млекопитающих, прежде всего у человека, которые обусловлены введением доз лекарственных средств или химических соединений, приводящих к окислительно-токсическому, прежде всего кардиотоксическому действию, а также относится к получению лекарственных средств, предназначенных для такой профилактики и/или лечения. Изобретение относится также в целом к применению указанных производных бензазепин-N-уксусной кислоты для вспомогательного лечения в рамках терапевтических методов лечения, при которых используется лекарственное средство, обладающее окислительно-токсическими и прежде всего кардиотоксическими побочными действиями. Изобретение предпочтительно относится к профилактике и лечению нарушений сердечной деятельности, прежде всего заболеваний миокарда, которые могут возникать при цитостатической химиотерапии.
Известно, что цитостатические лекарственные средства, применяемые при химиотерапии злокачественных опухолей, могут оказывать нежелательные побочные кардиотоксические действия. Так, например, при цитостатической терапии применяют некоторые антибиотики, которые из-за их общего токсического действия не могут применяться для лечения бактериальных инфекций. К ним относятся, например, антрациклины, которые выделены из различных видов Streptomyces и которые причисляют к имеющим наиболее важное значение достижениям в области цитостатиков. Однако клиническое применение антрациклинов ограничено из-за их более или менее выраженной кардиотоксичности. При этом кардиотоксичность кореллирует с величиной вводимой общей дозы и часто является необратимой. Предположительно нарушение сердечной деятельности, а также цитотоксическое действие, вызываемое этими антибиотиками, по крайней мере частично обусловлено их воздействием на мембрану, в результате чего при связывании антибиотика с компонентами клеточной мембраны повышается текучесть и проницаемость мембраны. Кроме того, следует учитывать, что еще одной причиной может являться окислительное повреждение.
Типичными применяемыми при цитостатической терапии антибиотиками являются такие антрациклины, как даунорубицин и его пролекарство зорубицин, доксорубицин (адриамицин) и эпирубицин, а также синтетический антибиотик митоксантрон.
Производные бензазепин-N-уксусной кислоты, которые в α-положений относительно атома азота содержат оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой, и их соли и биолабильные эфиры подпадают под объем охраны описанных в заявке DE 19510566 производных бензазепин-, бензоксазепин- и бензотиазепин-N-уксусной кислоты, которые в α-положении относительно атома азота содержат оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой и которые обладают NEP-ингибирующим действием на сердце. Производные бензазепин-N-уксусной кислоты, применяемые согласно настоящему изобретению, можно получать согласно методу, описанному в DE 19510566.
Ближайшим аналогом является патент US 5677297, в котором описаны соединения формулы I, обладающие NEP/ECE-ингибирующим действием на сердце, где нарушение сердечной деятельности вызвано активностью нейтральной эндопептидазы (NEP).
В основу изобретения положена задача разработать новые фармацевтические композиции, которые могут быть применены для профилактики и/или лечения нарушений сердечной деятельности, которые возникают при использовании обладающих кардиотоксическим действием доз лекарственных средств или химических соединений.
Таким образом, согласно изобретению соединения общей формулы I
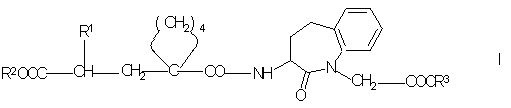
где
R1 обозначает фенил(низш.)алкильную группу, которая необязательно может быть замещена в фенильном кольце (низш.)алкилом, (низш.)алкоксигруппой или галогеном, или нафтил(низш.)алкильную группу,
R2 обозначает водород или группу, образующую биолабильный эфир, и
R3 обозначает водород или группу, образующую биолабильный эфир,
и физиологически приемлемые соли кислот формулы I применяют для приготовления фармацевтических композиций, предназначенных для профилактики и/или лечения у крупных млекопитающих и человека нарушений сердечной деятельности, прежде всего заболеваний миокарда, индуцируемых кардиотоксическими дозами лекарственных средств, прежде всего цитостатических средств, предпочтительно обладающих цитостатическим действием антибиотиков, или химических соединений.
Кроме того, соединения приведенной выше общей формулы I и физиологически приемлемые соли кислот формулы I можно применять для приготовления фармацевтических композиций, предназначенных для вспомогательного лечения крупных млекопитающих и человека в рамках терапии, при которой используют лекарственное средство, обладающее окислительно-цитотоксическими и прежде всего окислительно-кардиотоксическими побочными действиями.
Если в соединениях формулы I заместители представляют собой или содержат (низш.)алкильные или алкоксигруппы, то они могут иметь прямую или разветвленную цепь и содержать, в частности, от 1 до 4, предпочтительно от 1 до 2 атомов углерода и предпочтительно представляют собой метил или метоксигруппу. Если заместители содержат галоген, то он представляет собой прежде всего фтор, хлор или бром, предпочтительно фтор или хлор.
В радикале R1 (низш.)алкиленовая цепь может содержать от 1 до 4, предпочтительно от 1 до 2 атомов углерода. R1 представляет собой прежде всего необязательно замещенную фенетильную группу, которая необязательно может быть одно- или многократно замещена галогеном, (низш.)алкоксигруппой или (низш.)алкилом, или нафтилэтильную группу.
Соединения формулы I представляют собой необязательно этерифицированные производные карбоновых кислот. В зависимости от формы применения предпочтительны биолабильные моноэфиры, прежде всего соединения, где R2 обозначает группу, образующую биолабильный эфир, а R3 обозначает водород, или дикарбоновые кислоты, при этом последние наиболее предпочтительны для внутривенного введения.
В качестве групп R2 и R3, образующих биолабильный эфир, могут использоваться (низш.)алкильные группы, фенильные или фенил(низш.)алкильные группы, необязательно замещенные в фенильном кольце (низш.)алкилом или (низш.)алкиленовой цепью, связанной с двумя соседними атомами углерода, диоксоланилметильные группы, необязательно замещенные в диоксолановом кольце (низш.)алкилом, или С2-С6алканоилоксилметильные группы, необязательно замещенные у оксиметильной группы (низш.)алкилом. Если образующая биолабильный эфир группа R2 или R3 обозначает (низш.)алкил, то он предпочтительно может представлять собой неразветвленную алкильную группу, содержащую 1-4, предпочтительно 2 атома углерода. Если образующая биолабильный эфир группа представляет собой необязательно замещенную фенил(низш.)алкильную группу, то ее алкиленовая цепь может содержать 1-3, предпочтительно 1 атом углерода. Если фенильное кольцо замещено (низш.)алкиленовой цепью, то она может содержать 3-4, прежде всего 3 атома углерода. В качестве содержащих фенил заместителей R2 и/или R3 прежде всего можно использовать фенил, бензил или инданил. Если R2 и/или R3 представляют собой необязательно замещенную алканоилоксиметильную группу, то ее алканоилоксигруппа может содержать 2-6, предпочтительно 3-5 атомов углерода и предпочтительно является разветвленной и может представлять собой, например, пивалоилоксиметильную группу (т.е. трет-бутилкарбонилоксиметильную группу).
В качестве физиологически приемлемых солей дикарбоновых кислот или моноэфиров формулы I можно использовать их соли щелочных металлов, щелочно-земельных металлов или аммонийные соли, например, натриевые или кальциевые соли или соли физиологически приемлемых фармакологически нейтральных органических аминов, таких как диэтиламин или трет-бутиламин.
Соединения формулы I содержат два хиральных атома углерода, а именно: несущий боковую амидную цепь атом углерода в положении 3 кольцевого каркаса и несущий радикал R1 атом углерода боковой амидной цепи. Таким образом, соединения могут существовать в нескольких оптически активных стереоизомерных формах или в виде рацематов. Согласно настоящему изобретению можно применять как рацемические смеси, так и соединения формулы I в виде чистых изомеров.
При создании изобретения неожиданно было установлено, что применяемая согласно изобретению группа соединений формулы I и их физиологически приемлемые кислотно-аддитивные соли помимо наличия у них установленной ранее NEP-ингибирующей активности обладают также способностью противодействовать нарушениям сердечной деятельности, вызываемым кардиотоксическими соединениями (действующими веществами, химическими соединениями), прежде всего процессам разложения и перестройки (ремоделирования), например гипертрофии и фиброзу миокарда, защищая тем самым сердце от таких кардиотоксичесих веществ. Таким образом, соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли обладают профилактическим или снижающим опасность появления указанных нарушений действием, а тем самым и антикардиотоксическим действием в отношении нарушений сердечной деятельности, вызываемых кардиотоксическими соединениями, у человека и крупных млекопитающих. Вследствие этого соединения формулы I, включая их кислотно-аддитивные соли и их биолабильные эфиры, можно применять для профилактики и/или лечения нарушений сердечной деятельности, прежде всего заболеваний миокарда, вызываемых кардиотоксическими дозами лекарственных средств или химических соединений различного типа. Каузальные субстанции, вызывающие нарушения сердечной деятельности, например лекарственные средства, могут представлять собой вещества различного типа, например, применяемые при химиотерапии злокачественных опухолей цитостатические средства, прежде всего обладающие цитостатическим действием антибиотики. Кроме того, в этой связи было установлено, что применяемая согласно изобретению группа соединений формулы I в целом обладает также антиоксидантными свойствами. Эти свойства могут обусловливать эффективное цитозащитное и прежде всего кардиозащитное действие, благодаря чему применяемые согласно изобретению соединения можно использовать для вспомогательного лечения крупных млекопитающих и человека при терапевтическом лечении, при котором используются лекарственные средства, обладающие окислительно-цитотоксическими и прежде всего окислительно-кардиотоксическими побочными действиями.
Антикардиотоксическое действие, т.е. профилактическое действие или действие, снижающие опасность нарушений сердечной деятельности действие, обусловленных кардиотоксическими соединениями, а также антиоксидантное действие применяемых согласно изобретению соединений формулы I оценивали в фармакологических опытах in vivo на кроликах и крысах, страдающих вызванной адриамицином кардиомиопатией. Исследование проводили на кроликах, оценивая воздействие вещества на ингибирование, соответственно уменьшение индуцируемых адриамицином процессов разложения и перестройки (ремоделирования) в сердце, а также оценивания на крысах антиоксидантную активность соединений.
Описание методов тестирования
А) Опыты проводили на кроликах обоего пола, вес которых в начале опыта составлял 2,1±0,2 кг. Животных разделяли на 3 группы:
1) животные, которых не подвергали обработке (контрольные животные, n=20);
2) животные, которых подвергали обработке адриамицином (+плацебо вместо тестируемого соединения, n=8);
3) животные, которых подвергали обработке адриамицином и тестируемым соединением (n=8).
В качестве тестируемого соединения использовали (3S,2R')-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту, являющуюся репрезентативным представителем применяемых согласно изобретению соединений формулы I.
Животным из групп 2 и 3 в течение 4 недель дважды в неделю вводили внутривенно (в.в.) 1 мг/кг адриамицина. Кроликам из группы 3 с индуцированной адриамицином кардиомиопатией ежедневно, начиная с первого дня после обработки адриамицином, в течение 4 недель вместе с кормом перорально вводили тестируемое соединение (в дозе 30 мг/кг веса тела). По истечении 4 недель выделяли сердца и взвешивали. После этого их фиксировали с помощью формалина для последующих биохимических исследований (содержание гидроксипролина в тканях сердца измеряли путем анализа аминокислот с помощью ЖХВР согласно методу, описанному у Blankenship D.T. и др., Aunal. Biochem. 178,227-232, 1989 и у Schuster R., J. Chromatogr., 431,271-284, 1989). Увеличение относительной массы сердца по сравнению с массой тела, а также увеличение содержания гидроксипролина в тканях сердца по сравнению с нормальными тканями, свидетельствуют о протекавших в сердце процессах разложения и перестройки (ремоделирования). Результаты опытов приведены ниже в таблице I.
животные, обработанные адриамицином +тестируемым соединением, n=8 (Х±С.К.О.)
Примечания:
С.К.О означает среднеквадратичное отклонение,
***р<0,001 при сравнении с необработанными животными (группа 1),
+p<0,01 при сравнении с животными, обработанными адриамицином,
+плацебо (группа 2).
При оценке этим методом было установлено, что обработка тестируемым соединением приводит к статистически достоверному уменьшению соотношения масса сердца/масса тела по сравнению с контрольными животными, обработанными адриамицином. В результате обработки адриамицином (группа 2) соотношение масса сердца/масса тела (измеренное в г/кг) по сравнению с необработанной контрольной группой (группа 1) увеличивалось приблизительно на 69% (что было определено с высокой степенью статистической достоверности). Если наряду с адриамицином дополнительно вводили тестируемое соединение (группа 3), то индуцируемое адриамицином увеличение соотношения масса сердца/масса тела статистически достоверно уменьшалось приблизительно на 18% по сравнению с группой животных, обработанных плацебо (группа 2).
Концентрация гидроксипролина в левом желудочке, характеризующая степень сердечного фиброза, у животных, обработанных тестируемым соединением (группа 3), была ниже, чем у контрольных животных, обработанных адриамицином (группа 2). Обработка адриамицином повышала содержание гидроксипролина (измеренное в мкг/нг) в миокарде по сравнению с необработанной контрольной группой (группа 1) приблизительно на 60% (что было определено с высокой степенью статистической достоверности). Если наряду с адриамицином вводили также тестируемое соединение (группа 3), то индуцируемое адриамицином увеличение содержания гидроксипролина было приблизительно на 13% меньше по сравнению с группой животных, обработанных плацебо (группа 2). Результаты опытов позволяют сделать вывод о том, что при введении тестируемого соединения процесс перестройки внеклеточного миокардиального матрикса существенно замедляется.
Б) Опыты проводили на самцах крыс линии Wistar с начальным весом тела от 229 до 277 г. Животных разделяли на 4 группы:
1. необработанные животные (контрольные животные, n=19);
2. животные, которых обрабатывали адриамицином (+плацебо вместо тестируемого соединения, n=14);
3. животные, которых обрабатывали тестируемым соединением (n=11);
4. животные, которых обрабатывали адриамицином и тестируемым соединением (n=14).
В качестве тестируемого соединения использовали (3S,2R')-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту, являющуюся репрезентативным представителем применяемых согласно изобретению соединений формулы I.
Животным из групп 2 и 4 вводили внутрибрюшинно по 15 мг/кг адриамицина в течение 2 недель. Животные из группы 4, начиная с первого дня после обработки адриамицином, ежедневно в течение 2 недель получали вместе с кормом по 30 мг/кг тестируемого соединения. Животные из группы 3 также получали вместе с кормом ежедневно в течение 2 недель по 30 мг/кг тестируемого соединения (но без адриамицина).
По истечении 2-недельного периода обработки животных подвергали анестезии с помощью пентобарбитала (50 мг/кг, внутрибрюшинно) и отбирали образцы венозной крови, из которых получали плазму. Концентрацию пероксидов липидов и ферроксидазную активность в плазме оценивали с помощью методов, описанных у Wong S.H.Y. и др., Clin. Chem., 33, 214-220, 1987, соответственно у Johnson D.A. и др., Clin. Chem., 13, 142-150, 1967. Кроме того, концентрацию α-токоферола в плазме измеряли с помощью метода, описанного у Catignani G.L. и Bieri J.G., Clin. Chem., 29, 708-712, 1983. Результаты исследований представлены в приведенной ниже таблице II.
крысах
С.К.0 означает среднеквадратичное отклонение,
*р<0,05 при сравнении с необработанной группой (группа 1),
***р<0,001 при сравнении с необработанной группой (группа 1),
+р<0,05 при сравнении с группой, обработанной адриамицином+плацебо (группа 2),
+++р<0,001 при сравнении с группой, обработанной адриамицином+плацебо (группа 2).
Тестируемое соединение непосредственно обладало антиоксидантным действием (например, оно повышало уровень α-токоферола в плазме у обработанных им животных по сравнению с контрольными животными и животными, обработанными адриамицином) и ингибировало прооксидантное действие адриамицина, что проявлялось в значительном снижении липидного окисления и ферроксидазной активности в плазме по сравнению с крысами, обработанными адриамицином. В результате введения тестируемого соединения содержание α-токоферола (витамина Е, измеренное в мкг/дл) в плазме опытных животных из группы 3 повышалось приблизительно на 95% по сравнению с контрольными животными (группа 1) (что было определено с высокой степенью статистической достоверности). У животных, обработанных адриамицином и тестируемым соединением (группа 4), по сравнению с животными из группы 2 (обработка адриамицином+плацебо) также было выявлено выраженное увеличение содержания α-токоферола в плазме приблизительно на 21%. Концентрация пероксидов липидов в плазме крыс (которую оценивали по уровню аддукта малондиальдегида и тиобарбитуровой кислоты) повышалась у обработанных адриамицином животных (группа 2) приблизительно на 131% (что было определено с высоким уровнем статистической достоверности) по сравнению с контрольной группой (группа 1). Если наряду с адриамицином дополнительно вводили тестируемое соединение (группа 4), то это позволяло приблизительно на 32% (что было определено с высоким уровнем статистической достоверности) понижать индуцируемое адриамицином повышение концентрации пероксидов липидов в плазме по сравнению с группой 2 (обработка адриамицином+плацебо). Общая ферроксидазная активность (измеряемая в МЕ/л) в плазме крыс в группе животных, обработанных адриамицином (группа 2), статистически достоверно превышала приблизительно на 22% активность в контрольной группе (группа 1). Если наряду с адриамицином дополнительно вводили тестируемое соединение (группа 4), то это статистически достоверно снижало ферроксидазную активность на 23% по сравнению с таковой в группе 2 (обработка адриамицином+плацебо), и в этом случае она оказывалась близкой к ферроксидазной активности, выявленной в контрольной группе (группа 1).
На основе результатов этих опытов можно сделать вывод о том, что прооксидантное действие адриамицина в определенной степени обусловливает кардиотоксичность, которой обладает это соединение, и что тестируемое соединение благодаря своим антиоксидантным свойствам оказывает положительное влияние на эту карднотоксичность.
Соединения формулы I благодаря их описанному выше действию могут применяться в качестве лекарственных средств для профилактики и/или лечения у крупных млекопитающих и прежде всего человека нарушений сердечной деятельности, вызванных кардиотоксическими дозами лекарственных средств и других химических соединений, прежде всего процессов разложения и перестройки (ремоделирования) в сердце, таких как гипертрофия или фиброз миокарда. При этом соединения общей формулы I обладают эффективным антиоксидантным действием. В результате этого снижаются вредные окислительные воздействия других лекарственных средств, например цитостатических средств. Таким образом, соединения формулы I могут применяться в качестве вспомогательных лекарственных средств при терапевтическом лечении, при котором используются лекарственные средства, обладающие окислительно-токсическими и прежде всего кардиотоксическими побочными действиями. Для этого дикарбоновые кислоты формулы I и их соли целесообразно применять в виде лекарственных форм, пригодных для парентерального, прежде всего внутривенного введения, а моно- или диэфиры соединений формулы I целесообразно применять в виде лекарственных форм, пригодных для перорального введения. Вводимые дозы могут быть различными для различных пациентов, и они варьируются в зависимости от типа состояния, подлежащего лечению, применяемого соединения и методики введения. Так, например, композиции для парентерального введения в целом содержат меньшее количество действующего вещества, чем препараты, предназначенные для перорального введения. В целом для введения крупным млекопитающим и прежде всего человеку можно использовать лекарственные формы, в которых содержание действующего вещества на разовую дозу составляет от 1 до 200 мг.
Соединения формулы I, применяемые в качестве лечебного средства, можно включать наряду с обычными фармацевтическими вспомогательными веществами в состав галеновых композиций, например таблеток, капсул, суппозиториев или растворов. Такие галеновы композиции можно приготавливать известными методами с использованием обычных твердых или жидких носителей, таких как лактоза, крахмал или тальк либо жидкие парафины, и/или с использованием обычных фармацевтических вспомогательных веществ, например разрыхлителей для таблеток, веществ, способствующих растворению, или консервантов.
Изобретение относится также к продуктам, содержащим обладающее кардиотоксическими побочными действиями или окислительно-цитотоксическими либо окислительно-кардиотоксическими побочными действиями лекарственное средство, прежде всего обладающий кардиотоксическими побочными действиями цитостатик, и соединение приведенной выше формулы I или физиологически приемлемую кислотно-аддитивную соль соединения формулы I и пригодным в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при терапевтическом лечении с использованием обладающего кардиотоксическими побочными действиями лекарственного средства. Такие продукты содержат прежде всего в качестве цитостатического средства антибиотик, обладающий цитостатическим действием, и соединение формулы I или физиологически приемлемую кислотно-аддитивную соль соединения формулы I в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при цитостатической химиотерапии. Такие продукты могут, например, содержать в качестве антибиотика обладающий цитостатическим действием антибиотик из группы антрациклинов, митоксантрон или их пролекарство. В качестве антрациклинового соединения можно использовать, в частности, даунорубицин, доксорубицин (адриамицин) или эпирубицин или их пролекарство, предпочтительно доксорубицин (адриамицин) или его пролекарство.
Ниже изобретение более подробно поясняется на примерах, которые никоим образом не ограничивают его объем.
В приведенных ниже примерах 1 и 2 описаны фармацевтические композиции по изобретению, содержащие действующее вещество формулы I, a также способ приготовления таких фармацевтических композиций. Применяемые согласно изобретению соединения формулы I можно получать согласно методу, описанному в указанной выше заявке DE 19510566.
Пример 1
Таблетки, содержащие (3S,2'К)-3-{1-[2'-(этоксикарбонил)- 4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту
Приготавливают таблетки, имеющие следующий состав из расчета на одну таблетку:
Действующее вещество, кукурузный крахмал и лактозу концентрируют с 10%-ным раствором желатина. Пасту измельчают и полученный гранулят вносят в соответствующий поддон и сушат при 45°С. Высушенный гранулят пропускают через измельчающую машину и смешивают в смесителе со следующими вспомогательными веществами:
и затем прессуют в таблетки массой по 240 мг каждая.
Пример 2
Раствор для инъекций, содержащий (3S,2'R)-3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту
Приготавливают раствор для инъекций, имеющий следующий состав из расчета на 5 мл:
Твердые вещества растворяют в воде, раствор стерилизуют и порциями по 5 мл заполняют ампулы.
Пример 3
Предпочтительными соединениями формулы I, которые можно применять согласно изобретению для приготовления лекарственных средств, предназначенных для профилактики и/или лечения нарушений сердечной деятельности, вызываемых окислительно-токсическими и прежде всего кардиотоксическими дозами лекарственных средств, главным образом для вспомогательного лечения в рамках терапевтического лечения с использованием указанных лекарственных средств, например в рамках цитостатической химиотерапии, являются, например, следующие соединения (включая их кислотно-аддитивные соли):
трет-бутиловый эфир 3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
трет-бутиловый эфир (3S,2'R)-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
(3S,2'R)-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
трет-бутиловый эфир 3-{1-[2'-(трет-бутоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
бензиловый эфир 3-{1-[2'-(трет-бутоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
бензиловый эфир 3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
бензиловый эфир 3-{1-[2'-(трет-бутилкарбонилоксиметоксикарбонил)-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-{1-[2'-(пивалоилоксиметоксикарбонил)-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1H-1-бензазепин-1-уксусная кислота.
Изобретение относится к химико-фармацевтической промышленности и касается применения соединений формулы I для приготовления фармацевтических композиций, предназначенных для профилактики и/или лечения нарушений сердечной деятельности, индуцируемых кардиотоксическими дозами лекарственных средств, предпочтительно обладающих цитостатическим действием антибиотиков, или химических соединений. Соединения формулы I обладают высокой активностью при лечении нарушений сердечной деятельности и высокой биодоступностью. 4 н. и 8 з.п. ф-лы, 2 табл.


где
R1 обозначает фенил(ннзш.)алкильную группу, которая необязательно может быть замещена в фенильном кольце (низш.)алкилом, (низш.)алкоксигруппой или галогеном, или нафтил(низш.)алкильную группу,
R2 обозначает водород или группу, образующую биолабильный эфир, и
R3 обозначает водород или группу, образующую биолабильный эфир,
и физиологически приемлемых кислотно-аддитивных солей соединений формулы I для приготовления фармацевтических композиций, предназначенных для профилактики и/или лечения нарушений сердечной деятельности, индуцируемых кардиотоксическими дозами лекарственных средств, прежде всего цитостатических средств, предпочтительно обладающих цитостатическим действием антибиотиков, или химических соединений.
| US 5677297 А, 14.10.1997 | |||
| Автореферат АБД Medline | |||
| Jaenke RS | |||
| Cardiotoxicity and comparative pharmacokinetics of six anthracyclines in the rabbit | |||
| Cancer Res | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Способ получения аминопропанолпроизводных 6-окси-2,3,4,5-тетрагидро-1н-1-бензазепин-2-она или их солей | 1979 |
|
SU900808A3 |
| КОНДЕНСИРОВАННОЕ ПРОИЗВОДНОЕ БЕНЗАЗЕПИНА, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ ДЛЯ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2129123C1 |
Авторы
Даты
2006-01-27—Публикация
2000-07-10—Подача