Настоящее изобретение относится к применению производных бензазепин-N-уксусной кислоты, которые в α-положении на атоме азота несут оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой, и к их солям и биолабильным сложным эфирам, которые предназначены для лечения гипертензии, прежде всего определенных форм вторичной (симптоматической) гипертензии у крупных млекопитающих, прежде всего у людей, и для приготовления лекарственных средств, пригодных для такого лечения. При этом причина возникновения подлежащей лечению гипертензии может иметь самый различный генез. Изобретение прежде всего относится к лечению таких форм симптоматической гипертензии, которые могут возникать вследствие различных болезней, не относящихся к сердечным заболеваниям.
Производные бензазепин-N-уксусной кислоты, которые в α-положении на атоме азота несут оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой, и их соли и биолабильные сложные эфиры подпадают под объем описанных в немецкой заявке на патент DE 19510566 производных бензазепин-, бензоксазепин- и бензотиазепин-N-уксусной кислоты, которые в α-положении на атоме азота несут оксогруппу и в положении 3 замещены 1-(карбоксиалкил)циклопентилкарбониламиногруппой и которые оказывают NEP-ингибирующие воздействия на сердце. Применяемые в рамках настоящего изобретения производные бензазепин-N-уксусной кислоты могут быть получены согласно методу, описанному в DE 19510566.
Задачей изобретения является разработка новых фармацевтических композиций для лечения гипертензии, прежде всего определенных форм симптоматической гипертензии. Наиболее важной задачей изобретения является разработка новых фармацевтических композиций для лечения таких форм симптоматической гипертензии, которые могут возникать вследствие различных болезней, не относящихся к сердечным заболеваниям.
Таким образом, согласно изобретению соединения общей формулы I
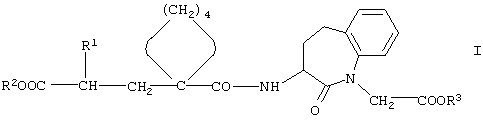
где
R1 обозначает фенил (низш.)алкильную группу, которая при необходимости может быть замещена на фенильном кольце (низш.)алкилом, (низш.)алкоксигруппой, или галогеном, или нафтил(низш.)алькильную группу,
R2 обозначает водород или группу, образующую биолабильный сложный эфир, и
R3 обозначает водород или группу, образующую биолабильный сложный
эфир,
и физиологически переносимые соли кислот формулы I применяют для приготовления фармацевтических композиций, предназначенных для лечения гипертензии, прежде всего определенных форм симптоматической гипертензии, у крупных млекопитающих и у людей.
Если заместители в соединениях формулы I обозначают или содержат (низш.)алкильные или алкоксигруппы, то они могут иметь прямую или разветвленную цепь и содержать прежде всего 1-4, предпочтительно 1-2 атома углерода, и предпочтительно они представляют собой метил или метоксигруппу. Если заместители содержат галоген, то он обозначает прежде всего фтор, хлор или бром, предпочтительно фтор или хлор.
В радикале R1 (низш.)алкиленовая цепь может содержать 1-4, предпочтительно 1-2 атома углерода. Радикал R1 прежде всего обозначает при необходимости замещенную фенэтильную группу, которая при необходимости может иметь один или несколько заместителей, представляющих собой галоген, (низш.)алкоксигруппу или (низш.)алкил, или представляет собой нафтилэтильную группу.
Соединения формулы I представляют собой производные дикарбоновой кислоты необязательно в форме сложного эфира. В зависимости от формы применения предпочтительными являются биолабильные сложные моноэфиры, прежде всего соединения, в которых R2 обозначает группу, образующую биолабильный сложный эфир, и R3 обозначает водород, или дикарбоновые кислоты, причем последние прежде всего могут применяться для внутривенного введения.
В качестве групп R2 и R3, образующих биолабильный сложный эфир, пригодны (низш.)алкильные группы, фенил- или фенил (низш.)алкильные, группы, при необходимости замещенные на фенильном кольце (низш.)алкилом или (низш.)алкиленовой цепью, связывающей два соседних атома углерода, диоксоланилметильные группы, при необходимости замещенные на диоксолановом кольце (низш.)алкилом, или С2-С6алканоилоксиметильные группы, при необходимости замещенные на оксиметильной группе (низш.)алкилом. Если группа R2 или R3, образующая биолабильный сложный эфир, обозначает (низш.)алкил, то предпочтительно он представляет собой неразветвленную алкильную группу, имеющую 1-4, предпочтительно 2 атома углерода. Если группа, образующая биолабильный сложный эфир, обозначает при необходимости замещенную фенил(низш.)алкильную группу, то ее алкиленовая цепь может содержать 1-3, предпочтительно 1 атом углерода. Если фенильное кольцо замещено (низш.)алкиленовой цепью, то она может иметь 3-4, прежде всего 3 атома углерода. В качестве фенилсодержащих заместителей R2 и/или R3 пригодны прежде всего фенил, бензил или инданил. Если R2 и/или R3 обозначают при необходимости замещенную алканоилоксиметильную группу, то ее алканоилоксигруппа может содержать 2-6, предпочтительно 3-5 атомов углерода, и предпочтительно она имеет разветвленную цепь, она может представлять собой, например, пивалоилоксиметильный фрагмент (трет-бутилкарбонилоксиметильный фрагмент).
В качестве физиологически переносимых солей дикарбоновых кислот или сложных моноэфиров формулы I могут применяться соли щелочных металлов, щелочно-земельных металлов или соли аммония, например, соли натрия или кальция или соли с физиологически приемлемыми нейтральными органическими аминами, такими как, например, диэтиламин или трет-бутиламин.
Соединения формулы I имеют два хиральных атома водорода, а именно атом водорода в положении 3 скелета кольца, несущий боковую амидную цепь, и атом водорода боковой амидной цепи, несущий остаток R1. Вследствие этого соединения могут находиться в различных оптически активных стереоизомерных формах или в форме рацемата. Согласно настоящему изобретению могут применяться как рацемические смеси, так и соединения формулы I в форме чистых изомеров.
При создании изобретения неожиданно было установлено, что применяемая согласно изобретению группа соединений формулы I обладает гипотензивным действием на людей и крупных млекопитающих, прежде всего в отношении определенных симптоматических форм гипертензии. Таким образом, соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли и их биолабильные сложные эфиры могут применяться для лечения гипертензии, прежде всего определенных форм симптоматической гипертензии, причем подлежащая лечению гипертензия может иметь различный генез. При этом соединения формулы I, включая их кислотно-аддитивные соли и их биолабильные сложные эфиры, предпочтительно следует применять для лечения таких форм симптоматической гипертензии, которые могут возникать вследствие различных болезней, не относящихся к сердечным заболеваниям.
Под повышенным кровяным давлением (гипертензией) понимают превышающее нормальный уровень кровяное давление, которое проявляется прежде всего в виде повышенного артериального давления. С точки зрения причин возникновения гипертензии различают две основные формы, а именно, с одной стороны, эссенциальную или первичную гипертензию и, с другой стороны, различные формы симптоматической гипертензии. Эссенциальная гипертензия, как правило, обусловлена повышенным сопротивлением потоку крови сначала вследствие чисто функционального, а затем вследствие имеющего органическое происхождение сужения артериального кровеносного русла. Вторичная гипертензия, также называемая симптоматической гипертензией, напротив, представляет собой связанную с органом, т.е. вызываемую заболеванием органа гипертензию, которая может проявляться среди прочего, например, в виде эндокринной, почечной, легочной или сердечно-сосудистой гипертензии. Исходные, обусловливающие возникновение симптоматической гипертензии заболевания, могут иметь разнообразный характер, например, они могут представлять собой хронические обструктивные заболевания легких и дыхательных путей или хроническую астму. Так, в нормальном состоянии циркуляция крови в легких взрослых людей происходит при низком давлении и при малом сопротивлении. Однако продолжающаяся хроническая гипоксия, которая может возникнуть, например, при хронических обструктивных заболеваниях дыхательных путей, приводит к легочной артериальной гипертензии и к перестройке артериол в легких (усиленный рост клеток мышечной ткани сосудов) и правого желудочка (усиленный рост клеток мышечной ткани сердца).
Соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли и их биолабильные сложные эфиры особенно предпочтительно следует применять для лечения легочной гипертензии, прежде всего не вызванной сердечными заболеваниями. При этом легочная гипертензия может представлять собой как первичную форму (неизвестного происхождения), так и симптоматическую легочную гипертензию, и для ее лечения могут применяться соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли и их биолабильные сложные эфиры.
Под (симптоматической) легочной гипертензией (гипертензия малого круга кровообращения) понимают постоянное повышение среднего давления в системе легочных артерий в состоянии покоя на величину > 22 мм рт.ст. Такое повышение среднего давления может наступать, например, вследствие обусловленного нарушенной деятельностью сердца застоя в малом круге кровообращения (например, при митральном пороке сердца, недостаточности левого желудочка сердца), спазмом сосудов перед капиллярной областью (например, в результате гипоксии при нахождении на большой высоте, обструктивной эмфиземы легкого, после операций, связанных с резекцией легкого), вторичной атрофией сосудов (при фиброзе легкого, разрушительной эмфиземе легкого), обильным кровотечением, т.е. гиперциркуляцией в легочном круге кровообращения с последующим заболеванием, приводящим к уменьшению просвета сосудов (например, при пороке сердца с большим шунтом "слева направо"), рецидивом эмболии легкого, в результате побочного действия при приеме определенных средств, подавляющих аппетит (например, аминорекса), или также вследствие первичных сужений сосудов легкого (т.е. вследствие идиопатической, т.е. первичной сосудистой легочной гипертензии).
Для лечения гипертензии согласно изобретению соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли и их биолабильные сложные эфиры могут вводиться перорально, внутривенно или также трансдермально в виде обычных фармацевтических композиций.
Соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли и их биолабильные сложные эфиры в эффективном в отношении снижения кровяного давления количестве в сочетании с обычными фармацевтическими вспомогательными веществами и/или носителями могут быть включены в состав твердых или жидких фармацевтических композиций. В качестве примеров твердых форм можно отметить препараты для перорального введения, такие как таблетки, драже, капсулы, порошок или гранулы, а также суппозитории или пластыри (трансдермальная терапевтическая система). Такие твердые препараты могут содержать обычные фармацевтические неорганические и/или органические носители, такие как, например, лактоза, тальк или крахмал, в сочетании с обычными фармацевтическими вспомогательными веществами, например, веществами, улучшающими скольжение, или разрыхлителями для таблеток. Жидкие препараты, такие как растворы, суспензии или эмульсии действующего вещества, могут содержать обычные разбавители, такие как вода, масло и/или суспендирующий агент, такой как полиэтиленгликоль и т.п. Могут быть дополнительно введены другие вспомогательные вещества, такие как, например, консервант, корригенты и т.п.
Действующие вещества могут быть смешаны известным методом с фармацевтическими вспомогательными веществами и/или носителями и включены в фармацевтические композиции. Для приготовления твердых лекарственных форм действующие вещества могут быть, например, смешаны общепринятым методом с вспомогательными веществами и/или носителями и подвергнуты влажной или сухой грануляции. Гранулы или порошок могут быть непосредственно внесены в капсулы или общепринятым методом спрессованы в ядра таблеток. Они при необходимости могут быть подвергнуты дражированию общепринятым методом. Жидкие композиции могут быть получены в форме растворов или суспензий путем растворения или диспергирования действующих веществ и при необходимости других вспомогательных веществ в пригодном жидком носителе.
Снижающее кровяное давление действие применяемых согласно изобретению соединений формулы I может быть установлено в фармакологических тестах in vivo на страдающих хронической гипоксией крысах путем оценки действия веществ в отношении соответствующих фармакологических характеристик, например, путем измерения легочного артериального давления и массы правого желудочка, а также путем исследования перестройки легочных сосудов у страдающих гипоксией крыс.
Описание методов тестирования и результатов
В качестве тестируемого соединения использовали (3S,2R')-[1-(2'-(карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту, являющуюся характерным представителем применяемых согласно изобретению соединений формулы I. Вводимая доза соединения составляла 40 мг/кг в день (эта доза достаточна для подавления обратного действия давления на Big-эндотелин).
В качестве подопытных животных использовали крыс линии Sprague-Dawley (весом 260-310 г; по 6-10 особей (n=6-10) в тестируемой группе). Для того, чтобы вызвать легочную гипертензию, животных помещали в камеру высокого давления, где создавали условия острой гипоксии. Для сравнения одну контрольную группу содержали в нормальной атмосфере и еще одну контрольную группу содержали в условиях гипоксии.
Опыты проводили следующим образом:
Подопытных животных обрабатывали с помощью осмотического мини-насоса действующим веществом или одним носителем. Осмотические мини-насосы имплантировали животным внутрибрюшинно за 24 ч до того, как животных на 2 недели помещали в камеру высокого давления. Там животных содержали при нормальном атмосферном давлении либо в условиях гипоксии (10% O2), либо в нормальной атмосфере. Через 2 недели животных подготавливали для гемодинамических исследований и проводили измерения.
Гемодинамические исследования
Животных анестезировали и затем в легочную артерию общепринятым методом вводили заранее подготовленную канюлю через правую яремную вену, предсердие и желудочек сердца. В левую яремную вену вводили катетер для того, чтобы вводить действующее вещество. В левую сонную артерию также вводили канюлю для измерения системного давления крови. После окончания действия наркоза у животных регистрировали легочное артериальное давление (ЛАД). Затем крыс помещали на 10 мин в мини-камеру, где снова создавали условия гипоксии (10% O2) и измеряли и регистрировали повышение легочного артериального давления. Влияние тестируемого соединения на ЛАД в условиях нормальной атмосферы и в условиях гипоксии в сравнении с результатами контрольных опытов приведены в таблице 1. Приведенные данные представляют собой средние значения±стандартные отклонения и их подвергали статистической обработке с использованием метода дисперсионного анализа (ANOVA).
Оценка антигипертрофного действия
После окончания гемодинамических исследований животных умерщвляли и сердца выделяли для исследования. Определяли массы правого и левого желудочков и их отношения к массе всего тела. Влияние тестируемого соединения на массу сердца в условиях нормальной атмосферы и в условиях гипоксии в сравнении с результатами контрольных опытов приведены в таблице 1. Приведенные данные представляют собой средние значения ± стандартные отклонения, и их подвергали статистической обработке с использованием метода дисперсионного анализа (ANOVA).
Исследование влияния на перестройку легочно-артериальной системы
После умерщвления крыс помимо сердец выделяли также и легкие. Легкие подвергали гистологическому исследованию, а именно после окрашивания по методу ван Гизона оценивали с помощью микроскопа с 400-кратным увеличением степень разрастания дистальной мышечной ткани (мускуляризации) сосудов легкого. Влияние тестируемого соединения на перестройку легочно-артериальной системы (т.е. на мускуларизацию сосудов легкого) при 2-недельной гипоксии представлено в таблице 2 в сравнении с контрольными опытами для условий гипоксии. Приведенные данные представляют собой средние значения±стандартные отклонения, и их подвергали статистической обработке с использованием метода дисперсионного анализа (ANOVA).
Результаты
С помощью описанного метода тестирования установлено, что обработка подвергнутых гипоксии животных тестируемым соединением приводит к статистически достоверному понижению легочного артериального давления (ЛАД) по сравнению с подвергнутыми гипоксии контрольными животными (таблица 1). При этом не выявлено воздействия на нормальное системное кровяное давление, т.е. не установлено гипотензивное действие. Это является важным преимуществом, так как при этом не следует опасаться понижения кровяного давления ниже нормального уровня у нормотензивных пациентов с легочной гипертензией.
Влияние применяемого согласно изобретению соединения (40 мг/кг/день в течение 14 дней) на легочное артериальное давление и массы правого и левого желудочков крыс после 14-дневного нахождения в условиях нормальной атмосферы и в условиях гипоксии.
В таблице условные обозначения имеют следующие значения:
* - статистически достоверное различие по сравнению с контрольными опытами, проведенными в условиях нормальной атмосферы (р<0,05);
# - статистически достоверное различие по сравнению с контрольными опытами, проведенными в условиях гипоксии (р<0,05);
ЛАД - легочное артериальное давление;
RtHWt - масса правого желудочка (мг);
Rt/LtHWt - отношение массы правого желудочка к массе левого желудочка;
RtHWt/BW - отношение массы правого желудочка к массе тела.
Снижение легочного артериального давления в результате применения тестируемого соединения приводило к статистически достоверному уменьшению массы правого желудочка крыс (антигипертрофное действие) по сравнению с результатами, полученными в контрольных опытах в условиях гипоксии (таблица 1). Также можно отметить тенденцию к уменьшению отношения массы правого желудочка к массе левого желудочка и массы правого желудочка к массе тела (таблица 1).
Кроме того, тестируемое соединение вызывало статистически достоверное уменьшение мускуларизации дистальных сосудов легкого крыс (таблица 2). Такая более слабая перестройка легочно-артериальной системы также является следствием статистически достоверного уменьшения легочной гипертензии.
Влияние применяемого согласно изобретению соединения (40 мг/кг/день в течение 14 дней) на мускуларизацию дистальных сосудов легкого крыс после 14-дневного нахождения в условиях гипоксии по сравнению с контрольными опытами в условиях гипоксии.
*- статистически достоверное различие при сравнении с результатами контрольных опытов, проведенных в условиях гипоксии (р<0,05).
Благодаря описанному выше действию соединения формулы I и их соли и их биолабильные сложные эфиры могут применяться в качестве лекарственного средства для лечения гипертензии, прежде всего определенных форм симптоматической гипертензии, у крупных млекопитающих и людей. При этом применяемые согласно изобретению соединения особенно эффективны для лечения таких форм симптоматической гипертензии, которые могут возникать вследствие различных болезней, не относящихся к сердечным заболеваниям, например, для лечения легочной гипертензии, не обусловленной сердечной деятельностью. Таким образом, применяемые согласно изобретению соединения представляют собой эффективное средство для лечения и/или профилактики прежде всего обусловленной гипоксией легочной гипертензии и связаных с ней осложнений, при этом они не не оказывают вредного воздействия на нормальное системное кровяное давление.
Для этой цели дикарбоновые кислоты формулы I и их соли целесообразно применять в виде лекарственных форм, пригодных для парентерального, прежде всего внутривенного введения, а сложный моно- или диэфир формулы I целесообразно применять в виде лекарственных форм для перорального введения. Применяемые дозы могут различаться в каждом конкретном случае и варьироваться в зависимости от типа состояния, подлежащего лечению, применяемого соединения и пути введения. Например, композиции для парентерального введения в целом содержат меньшее количество действующего вещества, чем препараты для перорального введения. Однако, как правило, для введения крупным млекопитающим, прежде всего людям, пригодны лекарственные формы, содержащие от 1 до 200 мг действующего вещества на одну дозу. При этом соединения формулы I, включая их кислотно-аддитивные соли и их биолабильные сложные эфиры, могут применяться в виде фармацевтических композиций, предназначенных как для немедленного, так и для пролонгированного, контролируемого и/или регулируемого высвобождения действующего вещества.
Приведенные ниже примеры служат для более подробного пояснения изобретения, но они никоим образом не ограничивают его объем.
В приведенных ниже примерах 1 и 2 описаны фармацевтические композиции по изобретению, содержащие действующее вещество формулы I, a также приготовление таких фармацевтических композиций. Применяемые согласно изобретению соединения формулы I могут быть получены согласно методам, описанным в уже упомянутой немецкой заявке на патент DE 19510566. В примере 3 приведены предпочтительные соединения, предназначенные для применения согласно изобретению.
Пример 1:
Таблетки, содержащие (3S,2'R)-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту.
Изготавливали таблетки, имеющие следующий состав (на одну таблетку):
Действующее вещество, кукурузный крахмал и лактозу концентрировали с 10%-ным раствором желатина. Пасту измельчали и образовавшийся гранулят выкладывали на соответствующий поддон и сушили при 45°С. Высушенный гранулят пропускали через измельчающую машину и смешивали в смесителе со следующими вспомогательными веществами:
и после этого спрессовывали в таблетки массой по 240 мг.
Пример 2:
Раствор для инъекций, содержащий (3S,2'R)-3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусную кислоту.
Изготавливали раствор для инъекций, имеющий следующий состав (на 5 мл):
Твердые вещества растворяли в воде, раствор стерилизовали и вносили в ампулы порциями по 5 мл каждая.
Пример 3:
Предпочтительными соединениями формулы I, которые могут применяться согласно изобретению для изготовления лекарственного средства для лечения гипертензии, прежде всего таких форм симптоматической гипертензии, как, например, легочная гипертензия, являются, например, следующие соединения (включая кислотно-аддитивные соли):
трет-бутиловый эфир 3-[1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
трет-бутиловый эфир (3S,2'R)-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
(3S,2'R)-3-[1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
(3S,2'R)-3-[1-[2'-(карбокси-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
трет-бутиловый эфир 3-[1-[2'-(трет-бутоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота;
бензиловый эфир 3-{1-[2'-(трет-бутоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
бензиловый эфир 3-[1-(2'-карбокси-4'-фенилбутил)циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
бензиловый эфир 3-[1-[2'(трет-бутилкарбонилоксиметоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты;
3-{1-[2'(пивалоилоксиметоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусная кислота.
Изобретение относится к химико-фармацевтической промышленности и касается применения соединений формулы I для приготовления лекарственного средства для лечения легочной гипертензии. Заявляемые лекарственные средства обладают низкой токсичностью и повышенной биодоступностью. 4 з.п. ф-лы, 2 табл.
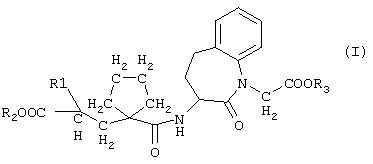

где
R1 обозначает фенил (С1-С4)алкильную группу, которая при необходимости может быть замещена на фенильном кольце (С1-С4)алкилом, (С1-С4)алкоксигруппой или галогеном, или нафтил(С1-С4)алькильную группу,
R2 обозначает водород или группу, образующую биолабильный сложный эфир,
R3 обозначает водород или группу, образующую биолабильный сложный эфир,
и физиологически приемлемых солей кислот формулы I для приготовления фармацевтических композиций, предназначенных для лечения легочной гипертензии.
| DE 19638020 A1, 19.03.1998 | |||
| DE 19510566 A1, 26.09.1996 | |||
| US 5087702 А, 11.02.1992 | |||
| Д.А.Харкевич | |||
| Фармакология | |||
| - М.: Медицина, 1987, с.47-48 | |||
| СПОСОБ ПОЛУЧЕНИЯ ИЗНОСОСТОЙКОГО ПОЛИТЕТРАФТОРЭТИЛЕНА | 2000 |
|
RU2207351C2 |
Авторы
Даты
2006-02-27—Публикация
2000-02-10—Подача