Изобретение относится к новому применению известных бензазепина, бензоксазепина, бензотриазепин-N-уксусной кислоты и фосфонозамещенных производных бензазепинона, обладающих ингибирующей активностью в отношении нейтральной эндопептидазы (NEP) и/или растворимой эндопептидазы человека (hSEP). Соединения по изобретению применимы для получения фармацевтических композиций для профилактики и лечения нейродегенеративных расстройств.
Изобретение относится к применению соединения, раскрываемому в данной заявке, для изготовления лекарственного средства, обладающего полезным эффектом. Полезный эффект раскрывается в данной заявке или очевиден специалисту в данной области из описания изобретения и общедоступных сведений в данной области. Изобретение также относится к применению соединения по изобретению для изготовления лекарственного средства для лечения или профилактики заболевания или состояния. Более конкретно, изобретение относится к новому применению для лечения заболевания или состояния, раскрываемому в данной заявке или очевидному специалисту в данной области из описания изобретения и общедоступных сведений в данной области. В вариантах осуществления изобретения конкретные соединения, раскрываемые в данной заявке, используются для изготовления лекарственного средства.
В патентной заявке США 20030045449 описано, что ингибиторы матричной металлопротеазы применимы для лечения нейродегенеративных расстройств. Проблемы, связанные с указанным изобретением, состоят в том, что, во-первых, ингибиторы матричной металлопротеазы включают большую группу ингибиторов протеаз и, во-вторых, в соответствии с указанным применением металлопротеазы должны использоваться в фармацевтической композиции, содержащей также и ингибитор N-NOS.
Цель настоящего изобретения состояла в том, чтобы идентифицировать конкретные ингибиторы металлопротеазы, которые обладают лечебным действием при введении в качестве монотерапии.
В настоящее время неожиданно обнаружено, что бензазепин, бензоксазепин, бензотиазепин-N-уксусная кислота и фосфонозамещенные производных бензазепинона, проявляющие ингибирующую активность в отношении нейтральной эндопептидазы (NEP) и/или растворимой эндопептидазы человека (hSEP), обладают протективным действием в модели черепно-мозговой травмы на животных. Указанное свойство делает их полезными для получения фармацевтических композиций для профилактики и лечения нейродегенеративных расстройств.
Соединения по изобретению известны из европейских патентов EP 0 733 642, EP 0 916 679 и EP 1 468 010, в которых подробно описаны их синтезы, указанные соединения могут быть представлены общей формулой (1):

где
R1 обозначает группу формулы (2) или (3):
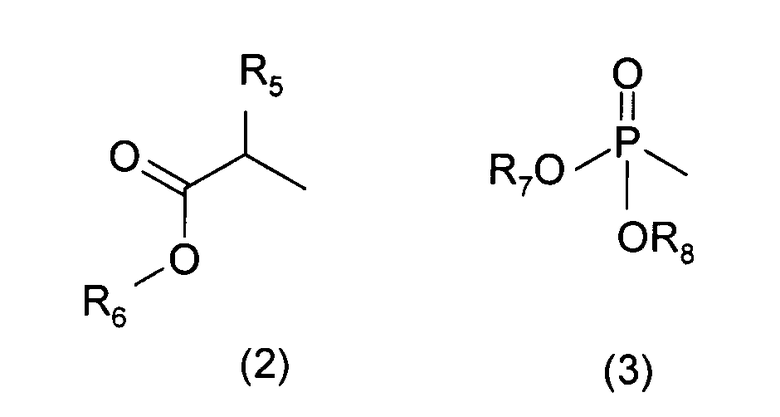
А обозначает СH2, О или S,
R2 и R3 независимо обозначают водород или галоген,
R4 и R6 независимо обозначают водород или группу, образующую биолабильный сложный эфир карбоновой кислоты;
R5 выбран из группы, состоящей из (C1-C6)алкокси(C1-C6)алкила, который может быть замещен (C1-C6)алкокси, фенил(C1-C6)алкилом и фенокси(C1-C6)алкилом, в которых фенильная группа может быть замещена (C1-C6)алкилом, (C1-C6)алкокси или галогеном и нафтил(C1-C6)алкилом,
R7 и R8 независимо обозначают водород или группу, образующую биолабильный сложный эфир фосфоновой кислоты;
К изобретению относятся все соединения формулы (1), их рацематы, смеси диастереоизомеров и индивидуальные стереоизомеры, а также все их фармакологически приемлемые соли. Следовательно, к изобретению относятся соединения, в которых заместители на потенциально асимметрических атомах углерода находятся или в R-конфигурации или в S-конфигурации.
Пролекарствами являются терапевтические средства, которые сами по себе не являются активными, но трансформируются в один или несколько активных метаболитов. Пролекарства представляют собой биообратимые производные молекул лекарств, используемые для преодоления некоторых барьеров для применения молекулы исходного лекарства. Указанные барьеры включают, но не ограничиваются ими, растворимость, проницаемость, стабильность предсистемный метаболизм и целевые ограничения (Medicinal Chemistry: Principles and Practice, 1994, ISBN 0-85186-494-5, Ed.: F.D. King, p. 215; J. Stella, "Prodrugs as therapeutics", Expert Opin. Ther. Patents, 14(3), 277-280, 2004; P.Ettmayer et al., "Lessons learned from marketed and investigational prodrugs", J. Med. Chem., 47, 2393-2404, 2004). К изобретению относятся пролекарства, т.е. соединения, которые при введении человеку любым известным способом, метаболизируют и дают соединения формулы (1). Конкретно, это относится к соединениям с гидроксильными группами. Такие соединения можно подвергать взаимодействию с органическими кислотами и получать соединения формулы (1) с дополнительной группой, которая легко удаляется после введения, например, амидина, енамина, основания Манниха, гидроксилметиленового производного, производного О-(ацилоксиметиленкарбамат), карбамата, сложного эфира, амида или енаминона, но не ограничивается перечисленными примерами.
Фармацевтически приемлемые соли можно получить по стандартным методикам, хорошо известным в данной области техники, например, путем смешивания соединения по настоящему изобретению с подходящим катионом металла или органическим основанием, например, амином.
Указанная цель может быть достигнута получением солей металлов соединений общей формулы (1), как отмечалось выше, в которых ион металла представляет собой ион лития или ион двухвалентного металла. Предпочтительными солями двухвалентных металлов являются соли кальция, магния и цинка. Наиболее предпочтительной является кальциевая соль.
Конкретно, изобретение относится к соединениям общей формулы (4):

где символы имеют такие значения, как указано выше.
Более конкретно, изобретение относится к соединениям общей формулы (5):

где символы имеют такие значения, как указано выше.
Наиболее предпочтительными активными веществами по настоящему изобретению являются:
(2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}-4-фенилбутановая кислота (6):

(2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}-4-(1-нафтил)бутановая кислота (7):

трет-бутил-((3S)-3-{[(1-{[(бензилокси)(этокси)фосфорил]метил}циклопентил)карбонил]амино}-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-1-ил)ацетат (8):

ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Соединения по изобретению можно применять в формах, пригодных для введения обычными способами, используя вспомогательные вещества, такие как жидкие или твердые носители. Фармацевтические композиции по изобретению можно вводить энтерально, парентерально, внутримышечно или внутривенно, ректально или локально (местно). Их можно вводить в виде растворов, порошков, таблеток, капсул (в том числе микрокапсул), мазей (кремов или геля) или суппозиториев. Подходящими наполнителями для таких рецептур являются общеупотребительные фармацевтические жидкие или твердые наполнители и заменители (добавки), растворители, эмульгаторы, вещества для скольжения, вещества, придающие вкус и цвет, и/или буферные вещества. Часто используемыми вспомогательными веществами, которые могут быть упомянуты, являются карбонат магния, диоксид титана, лактоза, маннит и другие сахара, тальк, лактопротеин, желатин, крахмал, целлюлоза и ее производные, животные и растительные масла, такие как рыбий жир, подсолнечное масло, арахисовое или кунжутное масло, полиэтиленгликоль и растворители, такие как, например, стерилизованная вода и одно- или многоатомные спирты, такие как глицерин.
Соединения по настоящему изобретению обычно вводят в виде фармацевтических композиций. Типы фармацевтических композиций, которые можно использовать, включают таблетки, жевательные таблетки, капсулы, растворы, растворы для парантерального введения, суппозитории, суспензии и другие типы, описанные здесь или очевидные для специалиста в данной области из описания изобретения и общедоступных сведений в данной области.
В вариантах осуществления изобретения предоставляется пакет или набор, включающий один или несколько контейнеров, заполненных одним или несколькими ингредиентами фармацевтической композиции по изобретению. В таком контейнере(ах) могут находиться и печатные материалы, такие, как инструкции по применению или уведомление государственного органа, регулирующего производство, применение или продажу фармацевтических продуктов, в котором отмечается, что продукт получил одобрение указанного органа для лечения людей или применения в ветеринарной практике. Конкретные рецептуры, пригодные для соединений по изобретению, описаны в патентных заявках WO 03/068266 и WO 04/062692.
Подразумевается, что конкретные соединения, описанные выше, дополнительно иллюстрируют изобретение в деталях и, следовательно, считается, что они не ограничивают объем изобретения каким-либо образом. Другие варианты осуществления изобретения должны быть очевидны специалистам в данной области при рассмотрении описания и практики изобретения, описанных здесь. Таким образом, подразумевается, что описание и примеры рассматриваются только как типичные, причем действительные объем и сущность изобретения указаны в формуле изобретения.
ЧЕРЕПНО-МОЗГОВАЯ ТРАВМА: ОТСРОЧЕННАЯ ГИБЕЛЬ НЕРВНЫХ КЛЕТОК
Методы
Аппарат для моделирования ушиба. Аппарат для моделирования ушиба, состоящий из трубки из нержавеющей стали длиной 40 см, с отверстиями, сделанными с интервалами 1 см для предотвращения сжатия воздуха в трубке. Крыс линии Вистар (массой 230-270 г) подвергают анестезии хлоральгидратом, 400 мг/кг (внутрибрюшинно, i.p.), делают краниотомию правого полушария, аппарат, с помощью которого подводят падающий груз, к опорной поверхности твердой мозговой оболочки (пахименинкса), помещают перпендикулярно к поверхности черепа и для ушиба головного мозга выбирают усилие 380 г × см, создаваемое грузом весом 20 г. Вмятина на поверхности мозга допустима максимум глубиной 2,5 мм, чтобы избежать механического ранения твердой мозговой оболочки. Центр опорной поверхности позиционируют стереотаксически 1,5 мм позади темени и на 2,5 мм в стороне от темени. Крыс подвергают перфузионной фиксации через 3 дня после повреждения мозга раствором, содержащим 4% параформальдегида в фосфатном буфере.
Интрацеребровентрикулярные (i.c.v.) инъекции: Соединения вводят интрацеребровентрикулярно с помощью шприца Гамильтона объемом 5-15 мкл. Инъекции осуществляют через 5 мин, 15 мин - 8 ч после травмы, используя следующие стереотаксические координаты: AP=-0,5 мм, L=-2 мм и V =-5,5 по отношению к темени (Swanson, L. W. (1992) Brain Maps: Structure of the Rat Brain, Elsevier, Amsterdam).
Внутривенные инъекции: Соединения вводят внутривенно с помощью шприца объемом 1 мл с иглой (26 gauge). Иглу вводят в левую бедренную вену после небольшого надреза на коже. Соединения вводят в объеме 1 мл/кг массы тела в течение 30 сек.
Морфометрический анализ в гиппокампе. Повреждение подобласти CA3 гиппокампа определяют стереологически при 5 различных рострокаудальных уровнях от 10,21 до 11,21 мм (Swanson, L. W. (1992) Brain Maps: Structure of the Rat Brain, Elsevier, Amsterdam) и по всей медиолатеральной оси через три дня после травмы. Для количественной оценки потери нейронов в гиппокампе, методику стереологического диссектора (Cruz-Orive, L. M. & Weibel, E. R. (1990) Am. J. Physiol. 258, L148-L156) используют для определения плотности (NV) пирамидальных нейронов. Для отбора проб используют несмещенную рамку (0,05 мм × 0,05 мм; высота диссектора 0,01 мм) и светосильный объектив (×40). Нормальные нейроны идентифицируют по наличию типичных ядер с прозрачной нуклеоплазмой и отчетливых ядрышек, окруженных цитоплазмой, содержащей вещество Ниссля. Границу между подобластями CA2 и CA3 рассматривают как точку, где рыхлое расположение больших пирамидальных клеток переходит в плотно упакованные пирамидальные подобласти CA3. Произвольно проведенная линия, соединяющая боковые концы дентатных гранул слоев клеток, рассматривается как соединение подобластей CA3 и CA4.
Соединения по изобретению применимы для профилактики и лечения нейродегенеративных расстройств, таких, например, как ишемический инсульт, черепно-мозговая травма, острый рассеянный энцефаломиелит, боковой амиотрифический склероз (ALS), пигментная дегенерация сетчатки, слабое ухудшение когнитивной способности, болезнь Альцгеймера, болезнь Пика, старческая деменция, прогрессирующий супрануклеарный паралич, субкортикальная деменция, болезнь Вильсона, множественный инфаркт, артериосклеротическая деменция, деменция, связанная со СПИД, мозжечковая дегенерация, синдромы спиноцеребеллярной дегенерации, наследственная атаксия Фридрейха, атаксия-телеангиэктазия, эпилепсия, связанная с повреждением мозга, повреждение спинного мозга, синдром усталых ног, болезнь Гентингтона и болезнь Паркинсона, стриатонигральная дегенерация, церебральный васкулит, митохондриальные энцефаломиопатии, нейрональный цероид-липофусциноз, спинальные мышечные атрофии, лизосомные болезни накопления с участием центральной нервной системы, лейкодистрофии, расстройства, связанные с дефектами цикла образования мочевины, гепатические энцефалопатии, почечные энцефалопатии, метаболические энцефалопатии, порфириновая болезнь, бактериальный или вирусный менингит или менингоэнцефалит, заболевания приона, отравления нейротоксичными соединениями, синдром Гийена-Барре, хронические воспалительные невропатии, полимиозит, дерматомиозит и поражение головного мозга, вызванное облучением.
Доза, которую целесообразно вводить, составляет 0,001-1000 мг/кг, предпочтительно 0,1-100 мг/кг массы тела пациента.
РЕЗУЛЬТАТЫ ФАРМАКОЛОГИЧЕСКИХ ИСПЫТАНИЙ
В вышеописанной модели черепно-мозговой травмы для соединений формул 6 и 7 выявлены нейропротективные эффекты, зависимые от дозы. Указанные эффекты все еще очевидны, когда соединения формул 6 и 7 вводят интрацеребровентрикулярно (i.c.v.) через 8 часов после травмы.
Доза-ответ для нейропротективного действия испытываемых соединений
Измеряют зависимость доза-ответ для нейропротективного действия испытываемых соединений формул 6 и 7 при введении интрацеребровентрикулярно (i.c.v.) через 15 мин после травмы взрослым крысам линии Вистар. Определяют нейрональные плотности в CA3 подобласти гиппокампа, как описано в разделе методы. Измеряют плотности CA3 нейронов ± стандартное отклонение (=SED) в 6 стереотактических уровнях в левой нетравмированной стороне крыс, которым вводили носитель, и крыс, которым вводили соединения формулы 6 и 7, и результаты приведены в таблице 1, представленной ниже. Во всех последующих таблицах обозначения (“n”) указывают на число крыс в группе, где их использовали.
(n=8)
(n=8)
(N=8)
(N=8)
Инъекция носителя в правый желудочек головного мозга крыс с травмой головы приводит в результате к уменьшению плотности нейронов в подобласти CA3 гиппокампа до 48% от контрольных величин, тогда как инъекция 10 мкг или соединения формулы 6 или соединения формулы 7 частично предотвращает потерю нейронов в гиппокампе. Анализ дисперсии ("ANOVA") показал, что имеется значительный протективный эффект лечения на нейрональную потерю в подобласти CA3 гиппокампа для обоих испытываемых соединений.
Активность после внутривенного (i.v.) введения
Инъекции носителя приводят к уменьшению нейрональных плотностей в подобласти CA3 гиппокампа до 53% от контрольных величин, тогда как инъекция 30 или 300 мг/кг испытываемого соединения формулы (7) частично предотвращает потерю нейронов в гиппокампе, причем доза 300 мг/кг является наиболее эффективной. Анализ дисперсии ("ANOVA") показал, что имеется значительный протективный эффект лечения на нейрональную потерю в подобласти CA3 гиппокампа для обеих испытанных доз испытываемых соединений. (P<0,001; n=8 на группу). ANOVA также показывает, что доза 300 мг/кг дает значительно лучший нейропротективный эффект, чем дозы 30 мг/кг.
(n=8)
(n=8)
300 мг/кг (N=8)
30 мг/кг (N=8)
Изобретение относится к области медицины и фармацевтики и касается применения (2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}-4-фенилбутановой кислоты или (2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}-4-(1-нафтил)бутановой кислоты для получения фармацевтических композиций для профилактики и лечения черепно-мозговой травмы и повреждения спинного мозга. Изобретение обеспечивает высокую эффективность лечения. 1 з.п. ф-лы, 2 табл.
1. Применение (2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}-4-фенилбутановой кислоты, имеющей формулу (6):
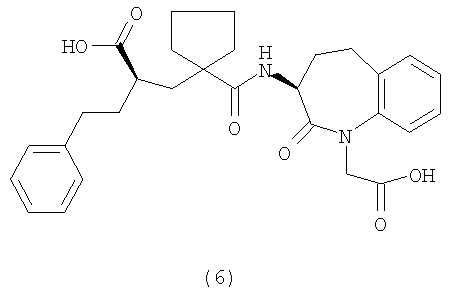
или (2R)-2-{[1-({[(3S)-1-(карбоксиметил)-2-оксо-2,3,4,5-тетрагидро-1H-1-бензазепин-3-ил]амино}карбонил)циклопентил]метил}4-(1-нафтил)бутановой кислоты, имеющей формулу (7):
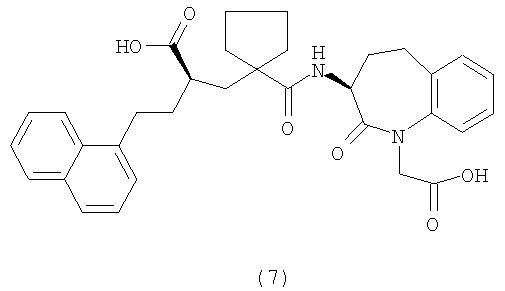
всех его стереоизомеров, а также его фармакологически приемлемых солей и пролекарств, для получения фармацевтических композиций для профилактики и лечения черепно-мозговой травмы и повреждения спинного мозга.
2. Применение по п.1, где фармакологически приемлемую соль выбирают из группы, состоящей из литиевой соли, кальциевой соли, магниевой соли и цинковой соли, и фармакологически приемлемой солью предпочтительно является кальциевая соль.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ПРОИЗВОДНЫЕ БЕНЗАЗЕПИН-, БЕНЗОКСАЗЕПИН- ИЛИ БЕНЗОТИАЗЕПИН-N-УКСУСНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО, ИХ СОДЕРЖАЩЕЕ | 1996 |
|
RU2159768C2 |
| Устройство для сигнализации о неправильной работе нумераторов на типографских машинах | 1928 |
|
SU16679A1 |
Авторы
Даты
2009-07-27—Публикация
2005-01-10—Подача