ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к общей области экспрессии рекомбинантных белков, к диагностике HCV (вирус гепатита С) инфекции, к лечению или профилактике HCV инфекции и к прогнозированию/мониторингу клинической эффективности лечения индивида с хроническим гепатитом или прогнозированию/мониторингу естественной болезни.
Более конкретно настоящее изобретение относится к экспрессии оболочечных белков вируса гепатита С в дрожжах, штаммам дрожжей для экспрессии кор-гликозилированных оболочечных вирусных белков HCV и к применению оболочечных белков HCV по настоящему изобретению в диагностике, профилактике или лечении.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Инфекция вирусом гепатита С (HCV) является серьезной проблемой для здоровья как в развитых, так и развивающихся странах. Установлено, что примерно от 1 до 5% мирового населения поражено этим вирусом. HCV инфекция оказывается самой главной причиной гепатита, связанного с переливанием крови, и часто прогрессирует в хроническое повреждение печени. Более того, существуют свидетельства участия HCV в индукции гепатоцеллюлярной карциномы. Следовательно, потребность в надежных диагностических методах и эффективных терапевтических агентах высока. Кроме того, нужны чувствительные и специфичные способы скрининга кровепродуктов, зараженных HCV, и улучшенные способы культивирования HCV.
HCV представляет собой вирус, содержащий положительную цепь РНК размером приблизительно 9600 оснований, которая кодирует единственный полипротеин-предшественник, состоящий примерно из 3000 аминокислот. Показано, что протеолитическое расщепление этого предшественника, сопряженное с ко- и пост-трансляционными модификациями, приводит по меньшей мере к трем структурным и шести неструктурным белкам. На основании гомологии последовательностей структурные белки можно в функциональном отношении определить как один коровый белок и два оболочечных гликопротеина: Е1 и Е2. Белок Е1 состоит из 192 аминокислот и содержит от 4 до 5 сайтов N-гликозилирования, в зависимости от генотипа HCV. Белок Е2 состоит из 363-370 аминокислот и содержит от 9 до 11 сайтов N-гликозилирования, в зависимости от генотипа HCV (обзоры см. в: Major and Feinstone, 1997; Maertens and Stuyver, 1997). Белок Е1 содержит различные вариабельные домены (Maertens and Stuyver, 1997). Белок Е2 содержит три сверхвариабельных домена, из которых главный домен локализован на N-конце этого белка (Maertens and Stuyver, 1997). Гликопротеины HCV локализуются главным образом в ЭР, где они модифицируются и собираются в олигомерные комплексы.
У эукариотов остатки сахара обычно присоединены к четырем разным аминокислотным остаткам. Эти аминокислотные остатки классифицируются как O-связанные (серии, треонин и гидроксилизин) и N-связанные (аспарагин). O-связанные сахара синтезируются в аппарате Гольджи или шероховатом эндоплазматическом ретикулюме (ЭР) из нуклеотидных сахаров. N-связанные сахара синтезируются из общего предшественника и затем подвергаются процессингу. Считают, что оболочечные белки HCV N-гликозилированы. Из уровня техники известно, что добавление N-связанных углеводных цепей важно для стабилизации складчатых интермедиатов и, таким образом, для эффективной укладки, предотвращения неправильной укладки и деградации в эндоплазматическом ретикулюме, олигомеризации, биологической активности и транспорта гликопротеинов (см. обзоры Rose et al., 1988; Doms et al., 1993; Helenius, 1994). Консенсусными сайтами для присоединения N-связанных олигосахаридов являются трипептидные последовательности Asn-X-Ser и Asn-X-Thr (где Х может быть любой аминокислотой) в составе полипептидов. После добавления N-связанного олигосахарида к полипептиду этот олигосахарид подвергается дальнейшему процессингу в сложный тип (содержащий N-ацетилглюкозамин, маннозу, фукозу, галактозу и сиаловую кислоту) или высокоманнозный тип (содержащий N-ацетилглюкозамин и маннозу). Считается, что оболочечные белки HCV относятся к высокоманнозному типу. Процессинг N-связанных олигосахаридов в дрожжах сильно отличается от процессинга в аппарате Гольджи млекопитающих. В дрожжах олигосахаридные цепи удлиняются в аппарате Гольджи поэтапным добавлением маннозы, что приводит к сложным высокоманнозным структурам и называется гипергликозилированием. В отличие от этого белки, экспрессируемые в прокариотах, никогда не гликозилируются.
Типы гликозилирования белков или пептидов высокоманнозного типа определены для множества разных эукариотических клеток. В клетках млекопитающих в среднем от 5 до 9 маннозных единиц связаны с двумя N-ацетилглюкозаминовыми группировками в олигосахариде с гликозилированием корового типа (структура кратко представлена как Man(5-9)GlcNAc(2)). Kop-гликозилирование относится к структуре, похожей на структуры, обведенные рамками на Фиг.3 в Herscovics and Orleans (1993).
Имеются сообщения, что метилотрофные дрожжи Pichia pastoris присоединяют в среднем от 8 до 14 маннозных единиц, то есть Man(8-14)GlcNAc(2), на каждый сайт гликозилирования (Tschopp в ЕР 0256421), и что приблизительно 85% N-связанных олигосахаридов находятся в диапазоне размеров Man(8-14)GlcNAc(2) (Grinna and Tschopp 1989). Другие исследователи опубликовали несколько отличные олигосахаридные структуры, присоединенные к гетерологичным белкам, экспрессируемым в Р.pastoris: Man(8-9)GlcNAc(2) (Montesino et al. 1989), Man(9-14)GlcNAc(2) или Man(9-15)GlcNAc(2) (Kalidas et al. 2001) и Man(8-18)GlcNAc(2) с преобладанием Man(9-12)GlcNAc(2), причем основным олисахаридом в целом является Man(10)GlcNAc(2) (Miele et al. 1998). Trimble et al. (1991) сообщили, что примерно в 75% N-связанных олигосахаридов имеется примерно поровну Man(8)GlcNAc(2) и Man(9)GlcNAc(2), причем дополнительно 17% сайтов гликозилирования занимает Man(10)GlcNAc(2), а остальные 8% сайтов - Man(11)GtcNAc(2). О гипергликозилировании белков, экспрессируемых в Р.pastoris, сообщают редко (Scorer et al. 1993).
Aspergillus niger добавляет к сайтам гликозилирования Man(5-10)GlcNAc(2) (Panchal and Wodzinski 1998).
Дефектный по гликозилированию мутант mnn9 Saccharomyces cerevisiae отличается от S.cerevisiae дикого типа тем, что клетки mnn9 продуцируют гликозилированные белки с модифицированным олигосахаридом, состоящим из Man(9-13)GlcNAc(2), вместо гипергликозилированных белков (Mackay et al., в US 5135854 и Kniskern et al. в WO 94/01132). О другом мутанте S.cerevisiae, och1mnn9, сообщали, что к сайтам гликозилирования в белках он добавляет Man(8)GlcNAc(2) (Yoshifumi et al., JP 06277086).
Для коровых олигосахаридов S.cerevisiae (дикий тип и мутант mnn9) характерно присутствие концевых α1,3-связанных маннозных остатков (Montesino et al., 1998). Олигосахариды, присоединенные к сайтам гликозилирования белков, экспрессируемых в Р.pastoris или в S.cerevisiae och1mnn1, лишены таких концевых α1,3-связанных манноз (Gellissen et al. 2000). Концевые α1,3-связанные маннозы считаются аллергенными (Jenkins et al. 1996). Поэтому белки, несущие на своих олигосахаридах концевые остатки α1,3-связанной маннозы, не пригодны для диагностических или терапевтических целей.
Тип гликозилирования белков, экспрессируемых в метилотрофных дрожжах Hansenula polymorpha, несмотря на использование этих дрожжей для продуцирования значительного числа гетерологичных белков (см. Табл.3 в Gellisen et al. 2000), не был исследован в деталях. Эксперименты Janowicz et al. (1991) и Diminskiy et al. (1997) создают впечатление, что Н.polymorpha не гликозилирует или очень слабо гликозилирует большой или малый поверхностный антиген вируса гепатита В (HBsAg). Наиболее вероятно это происходит из-за того, что HBsAg экспрессировался без сигнального пептида, что предотвращало поступление продуцированного HBsAg в просвет эндоплазматического ретикулюма (ЭР) и гликозилирование. Есть сообщение об ограниченном добавлении моно- и дигексоз к G-CSF (гранулоцитарный колониестимулирующий фактор), продуцируемому в Н.polymorpha (Fischer et al. в WO 00/40727). С другой стороны, наблюдали гипергликозилирование гетерологичной α-галактозидазы, экспрессируемой в клетках Н.polymorpha (Fellinger et al. 1991).
В настоящее время доказано, что вакцинация против болезни является одним из самых экономически эффективных и действенных способов контроля болезней. Однако, несмотря на многообещающие результаты, усилия по разработке эффективной вакцины против HVC были спряжены с трудностями. Непременным условием для вакцин является индукция иммунного ответа у пациентов. Следовательно, надо идентифицировать антигенные детерминанты HVC и в надлежащих условиях вводить их пациентам. Антигенные детерминанты можно разделить по меньшей мере на две формы, а именно, линейные и конформационные эпитопы. Конформационные эпитопы являются результатом складывания молекулы в трехмерном пространстве, что включает в себя ко- и пост-трансляционные модификации, такие как гликозилирование. В общем, считают, что реализацией самых эффективных вакцин будут конформационные эпитопы, поскольку они представляют собой эпитопы, которые напоминают подобные нативным эпитопы HVC и которые могут быть сохранены лучше, чем действительные линейные аминокислотные последовательности. Следовательно, первоочередную важность для генерирования анигенных детерминант HVC, подобных нативным, имеет окончательная степень гликозилирования оболочечных белков HVC. Однако есть кажущиеся непреодолимыми проблемы с культивированием HVC, которые приводят ко всего лишь ничтожным количествам вирионов. Кроме того, имеются обширные проблемы с экспрессией и очисткой рекомбинантных белков, приводящие как к малым количествам белков, так и к гипергликозилированным белкам или белкам, которые не гликозилированы.
Оболочечные белки HCV были получены рекомбинантными методами в Escherichia coli, клетках насекомых, клетках дрожжей и клетках млекопитающих. Однако у высших эукариот экспрессия характеризуется трудностями в получении больших количеств антигенов для получения, в конечном счете, вакцины. Результатом экспрессия в прокариотах, таких как Е.coli, являются оболочечные белки HCV, которые не гликозилированы. Результатом экспрессии оболочечных белков HCV в дрожжах является гипергликозилирование. Как уже продемонстрировали Maertens et al. в WO 96/04385, экспрессия оболочечного белка Е2 HCV в Saccharomyces cerevisiae приводит к белкам, которые сильно гликозилированы. Это гипергликозилирование приводит к экранированию эпитопов белка. Хотя Mustilli et al. (1999) утверждают, что результатом экспрессии белка Е2 HCV в S.cerevisiae является кор-гликозилирование, результаты внутриклеточной экспрессии этого материала показывают, что по меньшей мере его часть гипергликозилирована, тогда как корректный процессинг остальной части этого материала не продемонстрирован. Более того, гипергликозилирование, которое наблюдали Mustilli et al. (1999), могло быть предотвращено только присутствием туникамицина, инигибитора гликозилирования, и это, таким образом, не отражает гликозилирование, происходящее в нормальных, естественных условиях роста. Потребность в оболочечных белках HCV, происходящих из внутриклеточного источника, вполне признана (Maertens et al. в WO 96/04385, Heile et al., 2000). Еще одним примером этой потребности является плохая реакционная способность секретируемого Е2, происходящего из дрожжей, с сыворотками шимпанзе, иммунизированных белком Е2, происходящим из культуры клеток млекопитающего, как засвидетельствовано на Фиг.5 в Mustilli et al (1999). Это далее документируют Rosa et al. (1996), которые показывают, что иммунизация оболочечными белками HCV дрожжевого происхождения не может защитить от контрольного инфицирования.
Следовательно, существует потребность в эффективных системах экспрессии, результатом которых являются большие и экономически эффективные количества белков, имеющих в то же время тип гликозилирования, подобный нативному, с отсутствием концевой α1,3-связанной маннозы. В частности, такие системы необходимы для продукции оболочечных белков HCV.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Первый аспект настоящего изобретения относится к выделенному оболочечному белку HCV или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он является продуктом экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что в среднем вплоть до 80% сайтов N-гликозилирования кор-гликозилированы. В частности, более 70% указанных кор-гликозилированных сайтов гликозилированы олигоманнозой со структурой, определяемой как Man(8-10)-GlcNAc(2). Более того, соотношение олигоманнозы, имеющей структуру Man(7)-GlcNAc(2) и олигоманнозы, имеющей структуру Man(8)-GlcNAc(2), меньше или равно 0,45. Более конкретно, указанные олигоманнозы содержат менее 10% концевой α1,3-маннозы. Эукариотической клеткой, экспрессирующей указанный выделенный оболочечный белок HCV или его часть, может быть дрожжевая клетка, такая как клетка Hansenula.
Еще один аспект настоящего изобретения относится к выделенному оболочечному белку HCV или его части согласно изобретению, который(ая) получен(а) из белка, содержащего лидерный пептид птичьего лизоцима или его функциональный вариант, присоединенный к указанному оболочечному белку HCV или его фрагменту. Более конкретно, указанный выделенный оболочечный белок HCV или его часть получен(а) из белка, характеризуемого структурой
CL-[(A1)a-(PS1)b-(A2)c]-HCVENV-[(A3)d-(PS2)e-(A4)f]
где:
CL является лидерным пептидом птичьего лизоцима или его функциональным эквивалентом,
А1, А2, A3 и А4 являются адаптерными пептидами, которые могут быть одинаковыми или разными,
PS1 и PS2 являются сайтами процессинга, которые могут быть одинаковыми или разными,
HCVENV является оболочечным белком HCV или его частью,
а, b, с, d, e и f равны 0 или 1, и
где, возможно, А1 и/или А2 представляют собой часть PS1, и/или где A3 и/или А4 представляют собой часть PS2.
Другой аспект этого изобретения охватывает выделенный оболочечный белок HCV или его фрагмент согласно изобретению, который содержится в структуре, выбранной из группы, состоящей из мономеров, гомодимеров, гетеродимеров, гомо-олигомеров и гетеро-олигомеров. Альтернативно указанный выделенный оболочечный белок HCV или его фрагмент согласно изобретению содержится в вирусоподобной частице. Более конкретно, любой выделенный оболочечный белок HCV или его фрагмент согласно изобретению может содержать цистеины, у которых цистеиновые тиольные группы модифицированы химическим путем.
Конкретные аспекты этого изобретения относятся к выделенным оболочечным белкам HCV или их фрагменту согласно изобретению, которые являются антигенными или иммуногенными и/или которые содержат эпитоп, стимулирующий Т-клетки.
Дальнейший аспект относится к композиции, содержащей выделенный оболочечный белок HCV или его фрагмент согласно изобретению. Указанная композиция может дополнительно содержать фармацевтически приемлемый носитель и может быть лекарством или вакциной.
Это изобретение также относится к способу получения выделенного оболочечного белка HCV или его фрагмента согласно изобретению.
Другой способ по этому изобретению представляет собой способ обнаружения присутствия анти-HCV антител в образце, подозреваемом в том, что он содержит анти-HCV антитела, при котором:
1) оболочечный белок HCV или его часть по любому из пп.1-15 формулы изобретения приводят в контакт с указанным образцом в условиях, допускающих образование комплекса указанного оболочечного белка HCV или его части с указанными анти-HCV антителами,
2) выявляют комплекс, образованный на стадии (1),
3) на основании результатов стадии (2) делают вывод о присутствии указанных анти-HCV антител в указанном образце.
Более конкретно, указанный способ может включать в себя стадию (1), на которой указанное приведение в контакт происходит к конкурентных условиях. В частности, в указанных способах может быть использована твердая подложка, к которой присоединен указанный оболочечный белок HCV или его часть.
Далее это изобретение относится к диагностическому набору для обнаружения присутствия анти-HCV антител в образце, подозреваемом в том, что он содержит анти-HCV антитела, содержащему оболочечный белок HCV или его часть согласно изобретению. Более конкретно, указанный набор содержит указанный оболочечный белок HCV или его часть, присоединенный(ую) к твердой подложке.
Это изобретение также относится к лекарству или вакцине, которые содержат оболочечный белок HCV или его часть согласно изобретению.
Также это изобретение охватывает фармацевтическую композицию для индукции у млекопитающего HCV-специфичного иммунного ответа, содержащую эффективное количество оболочечного белка HCV или его части согласно изобретению и, возможно, фармацевтически приемлемый адъювант. Указанная фармацевтическая композиция может альтернативно быть способна индуцировать у млекопитающего HCV-специфичные антитела и/или индуцировать у млекопитающего Т-клеточную функцию. Более того, указанная фармацевтическая комсайт может быть профилактической композицией или терапевтической композицией. В частности, указанное млекопитающее является человеком.
ПОЯСНЕНИЯ К ФИГУРАМ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг.1. Схематическая карта вектора pGEMT-E1sH6RB, который имеет последовательность, определенную в SEQ ID NO:6.
Фиг.2. Схематическая карта вектора pCHH-Hir, который имеет последовательность, определенную в SEQ ID NO:9.
Фиг.3. Схематическая карта вектора pFPMT121, который имеет последовательность, определенную в SEQ ID NO:12.
Фиг.4. Схематическая карта вектора pFPMT-CHH-Е1-Н6, который имеет последовательность, определенную в SEQ ID NO:13.
Фиг.5. Схематическая карта вектора pFPMT-MFa-E1-H6, который имеет последовательность, определенную в SEQ ID NO:16.
Фиг.6. Схематическая карта вектора pUC18-FMD-MFa-E1-H6, который имеет последовательность, определенную в SEQ ID NO:17.
Фиг.7. Схематическая карта вектора pUC18-FMD-CL-E1-H6, который имеет последовательность, определенную в SEQ ID NO:20.
Фиг.8. Схематическая карта вектора pFPMT-CL-E1-Н6, который имеет последовательность, определенную в SEQ ID NO:21.
Фиг.9. Схематическая карта вектора pSР72Е2Н6, который имеет последовательность, определенную в SEQ ID NO:22.
Фиг.10. Схематическая карта вектора рМРТ121, который имеет последовательность, определенную в SEQ ID NO:23.
Фиг.11. Схематическая карта вектора pFPMT-MFa-E2-H6, который имеет последовательность, определенную в SEQ ID NO:24.
Фиг.12. Схематическая карта вектора pMPT-MFa-E2-H6, который имеет последовательность, определенную в SEQ ID NO:25.
Фиг.13. Схематическая карта вектора pMF30, который имеет последовательность, определенную в SEQ ID NO:28.
Фиг.14. Схематическая карта вектора pFPMT-CL-E2-H6, который имеет последовательность, определенную в SEQ ID NO:32.
Фиг.15. Схематическая карта вектора pUC18-FMD-CL-E1, который имеет последовательность, определенную в SEQ ID NO:35.
Фиг.16. Схематическая карта вектора pFPMT-CL-E1, который имеет последовательность, определенную в SEQ ID NO:36.
Фиг.17. Схематическая карта вектора pUC18-FMD-CL-H6-E1-K-H6, который имеет последовательность, определенную в SEQ ID NO:39.
Фиг.18. Схематическая карта вектора pFPMT-CL-H6-K-E1, который имеет последовательность, определенную в SEQ ID NO:40.
Фиг.19. Схематическая карта вектора pYIG5, который имеет последовательность, определенную в SEQ ID NO:41.
Фиг.20. Схематическая карта вектора pYIG5E1H6, который имеет последовательность, определенную в SEQ ID NO:42.
Фиг.21. Схематическая карта вектора pSY1, который имеет последовательность, определенную в SEQ ID NO:43.
Фиг.22. Схематическая карта вектора pSY1aMFE1sH6a, который имеет последовательность, определенную в SEQ ID NO:44.
Фиг.23. Схематическая карта вектора pBSK-E2sH6, который имеет последовательность, определенную в SEQ ID NO:45.
Фиг.24. Схематическая карта вектора pYIG5HCCL-22aH6, который имеет последовательность, определенную в SEQ ID NO:46.
Фиг.25. Схематическая карта вектора pYYIGSE2H6, который имеет последовательность, определенную в SEQ ID NO:47.
Фиг.26. Схематическая карта вектора pYIG7, который имеет последовательность, определенную в SEQ ID NO:48.
Фиг.27. Схематическая карта вектора pYIG7E1, который имеет последовательность, определенную в SEQ ID NO:49.
Фиг.28. Схематическая карта вектора pSY1YIG7E1s, который имеет последовательность, определенную в SEQ ID NO:50.
Фиг.29. Схематическая карта вектора pPICZalphaA, который имеет последовательность, определенную в SEQ ID NO:51.
Фиг.30. Схематическая карта вектора pPICZalphaD', который имеет последовательность, определенную в SEQ ID NO:52.
Фиг.31. Схематическая карта вектора pPICZalphaE', который имеет последовательность, определенную в SEQ ID NO:53.
Фиг.32. Схематическая карта вектора pPICZalphaD'E1sH6, который имеет последовательность, определенную в SEQ ID NO:58.
Фиг.33. Схематическая карта вектора pPICZalphaE'E1sH6, который имеет последовательность, определенную в SEQ ID NO:59.
Фиг.34. Схематическая карта вектора pPICZalphaD'E2sH6, который имеет последовательность, определенную в SEQ ID NO:60.
Фиг.35. Схематическая карта вектора pPICZalphaE'E2sH6, который имеет последовательность, определенную в SEQ ID NO:61.
Фиг.36. Схематическая карта вектора pUC18MFa, который имеет последовательность, определенную в SEQ ID NO:62.
Фиг.37. Профиль элюции хроматографии с вытеснением по размеру частиц белка Е2-Н6, очищенного с помощью IMAC, экспрессированного в MFa-Е2-Н6-экспрессирующей Hansenula polymorpha (см. Пример 15). На оси Х показан объем элюции (в мл). Вертикальные линии через профиль элюции показывают собранные фракции. "Р1"=объединенные фракции 4-9, "Р2"=объединенные фракции 30-35, "Р3"=объединенные фракции 37-44. Ось Y показывает спектральную поглощательную способность, приведенную в мЕА (милли единицы абсорбции). На оси Х показан объем элюции в мл.
Фиг.38. Различные пулы и фракции, собранные после хроматографии с вытеснением по размеру частиц (см. Фиг.37), были проанализированы с помощью электрофореза в полиакриламидном геле с додецилсульфатом натрия в невосстанавливающих условиях (Na-ДДС-ПААГ электрофорез) с последующим окрашиванием полиакриламидного геля серебром. Проанализированные пулы ("Р1", "Р2" и "Р3") и фракции (с 16 по 26) указаны в верхней части изображения геля, окрашенного серебром. Слева (дорожка "М") указаны размеры маркеров молекулярной массы.
Фиг.39. Фракции 17-23 после стадии хроматографии с вытеснением по размеру частиц как показано на Фиг.37, были объединены и проалкилированы. После этого белковый материал был подвергнут обработке посредством Endo H для дегликозилирования. Необработанный и обработанный посредством Endo H материал был разделен на Na-ДДС-ПААГ геле и подвергнут блоттингу на мембране PVDF (поливинилдифторид). Блот был окрашен красителем амидо черный.
Дорожка 1: алкилированный Е2-Н2 до обработки посредством Endo H.
Дорожка 2: алкилированный Е2-Н2 после обработки посредством Endo H.
Фиг.40. Вестерн-блот-анализ клеточных лизатов Е1, экспрессированного в Saccharomyces cerevisiae.
Вестерн-блот обрабатывали с использованием El-специфичного моноклонального антитела IGH 201.
Дорожки 1-4: продукт экспрессии после 2, 3, 5 или 7 дней экспрессии, соответственно, в клоне Saccharomyces, трансформированном pSY1Y1G7E1s (SEQ ID NO:50, Фиг.28), содержащей нуклеотидную последовательность, которая кодирует лидерный пептид куриного лизоцима, присоединенный к Е1-Н6.
Дорожки 5-7: продукт экспрессии через 2, 3 или 5 дней экспрессии, соответственно, в клоне Saccharomyces, трансформированном pSY1aMFE1sH6aYIG1 (SEQ ID NO:44, Фиг.22), содержащей нуклеотидную последовательность, которая кодирует лидерный пептид α-фактора спаривания, присоединенный к Е1-Н6.
Дорожка 8: маркеры молекулярной массы, как указано.
Дорожка 9: очищенный E1s, продуцируемый клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы.
Фиг.41. Анализ белка Е2-Е6, экспрессированного и процессированного из CL-E2-H6 до Е2-Н6 в Н.polymorpha, который был очищен афинной хроматографией с иммобилизованными ионами металлов (IMAC) (см. Пример 17). Белки из разных промывочных фракций (дорожки 2-4) и элюированных фракций (дорожки 5-7) были проанализированы с помощью Na-ДДС-ПААГ электрофореза в восстанавливающих условиях с последующим окрашиванием геля серебром (А, верхнее изображение) или посредством вестерн-блоттинга с использованием специфического моноклонального антитела, направленного против Е2 (В, нижнее изображение). Размеры маркеров молекулярной массы указаны слева.
Фиг.42. Профиль элюции первого этапа IMAC-хроматографии на колонке Ni-IDA (хелатирующая Sepharose FF, нагруженная Ni2+, Pharmacia) для очистки сульфонированного белка Н6-К-Е1, продуцированного Н.polymorpha (см. Пример 18). Колонку уравновешивали буфером А (50 мМ фосфат, 6М GuHCl, 1% Empigen ВВ (об./об.), рН 7,2), обогащенным 20 мМ имидазола. После нанесения образца колонку последовательно промывали буфером А, содержащим 20 мМ и 50 мМ имидазола, соответственно (как показано на хроматограмме). Следующий этап промывки и элюции His-меченых продуктов выполнялся последовательным нанесением буфера В (забуференный фосфатами физиологический раствор (PBS), 1% empigen ВВ, рН 7,2), обогащенного 50 мМ имидазола и 200 мМ имидазола, соответственно (как указано на хроматограмме). Были объединены следующие фракции: пул промывки 1 (фракции 8-11, промывка с 50 мМ имидазола). Элюированный материал собирали отдельными фракциями от 63-й до 72-й или объединяли в пул элюции (фракции 63-69). На оси Y показано поглощение в мЕА (милли единицы абсорбции). На оси Х показан объем элюции в мл.
Фиг.43. Анализ очищенного посредством IMAC белка Н6-К-Е1 (см. Фиг.42), экспрессированного и процессированного из CL-H6-K-E1 до Н6-К-Е1 в Н.polymorpha. Белки в пуле промывки 1 (дорожка 12) и фракциях элюции от 63 до 72 (дорожки 2-11) были проанализированы посредством Na-ДДС-ПААГ электрофореза в восстанавливающих условиях с последующим окрашиванием геля серебром (А, верхнее изображение). Белки, присутствовавшие в образце перед IMAC (дорожка 2), в проходном пуле (дорожка 4), в промывочном пуле 1 (дорожка 5) и в пуле элюции (дорожка 6), были проанализированы вестерн-блоттингом с использованием специфического моноклонального антитела, направленного против Е1 (В, нижнее изображение, на дорожку 3 образец не наносили). Размеры маркеров молекулярной массы (дорожка М) указаны слева.
Фиг.44. Профиль элюции второго этапа IMAC-хроматографии на колонке Ni-IDA (хелатирующая Sepharose PF, нагруженная Mi2+, Pharmacia) для очистки Е1, являющегося результатом процессинга Н6-К-Е1 in vitro (очистка: см. Фиг.42) посредством Endo Lys-C. Поток собирали в разные фракции (1-40), которые были подвергнуты скринингу на присутствие Els-продуктов. Фракции (7-28), содержавшие интактный Е1, процессированный из Н6-К-Е1, объединяли. На оси Y показана спектральная поглощательная способность, приведенная в мЕА (миллиединицы абсорбции). На оси Х показан объем элюции в мл.
Фиг.45. Вестерн-блот-анализ, демонстрирующий специфические полосы белка E1s, прореагировавшие с биотинилированным гепарином (см. также Пример 19). Были проанализированы препараты E1s, очищенные из культуры клеток млекопитающего, инфицированных HCV-рекомбинантным вирусом коровьей оспы, или экспрессируемые Н.polymorpha. Панель справа от вертикальной линии показывает вестерн-блот, проявленный моноклональным биотинилированным E1-специфичным IGH 200. Панель слева от вертикальной линии показывает вестерн-блот, проявленный биотинилированным гепарином. Из этих результатов сделан вывод, что высокую аффинность к гепарину имеет главным образом E1s с низким уровнем гликозилирования.
Дорожки М: маркер молекулярной массы (молекулярные массы указаны слева).
Дорожки 1: E1s из клеток млекопитающего, алкилированный в ходе выделения.
Дорожки 2: E1s-H6, экспрессируемый Н.polymorpha и сульфонированный в ходе выделения.
Дорожки 3: E1s-H6, экспрессируемый Н.polymorpha и алкилированный в ходе выделения.
Дорожки 4: тот же материал, что был загружен на дорожку 2, но обработанный дитиортреитолом для превращения сульфонированных Cys-тиольных группы в Cys-тиольные.
Фиг.46. Профиль хроматографии с вытеснением по размеру частиц (SEC, size exclusion chromatography) очищенного белка Е2-Н6, экспрессированного в Н.polymorpha, в его сульфонированной форме, который прогнали в PBS, 3% бетаина для того, чтобы вызвать образование вирусоподобных частиц (VLP) заменой Empigen BB на бетаин. Объединенные фракции, содержащие VLPs, которые были использованы в дальнейшем исследовании, указаны знаком "↔". Ось Y показывает абсорбцию, приведенную в мЕА (миллиединицы абсорбции). На оси Х показан объем элюции в мл. См. также Пример 20.
Фиг.47. Профиль хроматографии с вытеснением по размеру частиц (SEC, size exclusion chromatography) очищенного белка Е2-Н6, экспрессированного в Н.polymorpha, в его алкилированной форме, который прогнали в PBS, 3% бетаина для того, чтобы вызвать образование вирусоподобных частиц (VLP) заменой Empigen BB на бетаин. Объединенные фракции, содержащие VLPs, указаны знаком "↔". Ось Y показывает абсорбцию, приведенную в мЕА (миллиединицы абсорбции). На оси Х показан объем элюции в мл. См. также Пример 20.
Фиг.48. Профиль хроматографии с вытеснением по размеру частиц (SEC, size exclusion chromatography) очищенного белка Е1, экспрессированного в Н.polymorpha, в его сульфонированной форме, который прогнали в PBS, 3% бетаина для того, чтобы вызвать образование вирусоподобных частиц (VLP) заменой Empigen BB на бетаин. Объединенные фракции, содержащие VLPs, указаны знаком "↔". Ось Y показывает абсорбцию, приведенную в мЕА (миллиединицы абсорбции). На оси Х показан объем элюции в мл. См. также Пример 20.
Фиг.49. Профиль хроматографии с вытеснением по размеру частиц (SEC, size exclusion chromatography) очищенного белка Е1, экспрессированного в Н.polymorpha, в его алкилированной форме, который прогнали в PBS, 3% бетаина для того, чтобы вызвать образование вирусоподобных частиц (VLP) заменой Empigen BB на бетаин. Объединенные фракции, содержащие VLPs, указаны знаком "↔". Ось Y показывает абсорбцию, приведенную в мЕА (миллиединицы абсорбции). На оси Х показан объем элюции в мл. См. также Пример 20.
Фиг.50. Na-ДДС-ПААГ (в восстанавливающих условиях) и анализ вестерн-блоттингом вирусоподобных частиц, выделенных после хроматографии с вытеснением по размеру частиц, как описано для Фиг.48 и 49. Левая панель: окрашенный серебром Na-ДДС-ПААГ гель. Правая панель: вестерн-блот с использованием специфических моноклональных антител против белка Е1 (IGH201). Дорожки 1: маркеры молекулярной массы (молекулярные массы указаны слева); дорожки 2: пул VLPs, содержащих сульфонированный Е1 (Фиг.48); дорожки 3: пул VLPs, содержащих алкилированный Е1 (Фиг.49). См. также Пример 20.
Фиг.51. Е1, продуцированный в клетках млекопитающего ("М"), или Е1, продуцируемый в Hansenula ("H"), были нанесены на твердую подложку для твердофазного иммуноферментного анализа (ELISA), чтобы определить конечную точку титрования антител, присутствующих в сыворотках после вакцинации мышей белком Е1, продуцированным в клетках млекопитающего (верхняя панель), или после вакцинации мышей белком Е1, продуцируемым в Hansenula (нижняя панель). Горизонтальная полоса представляет средний титр антител. Конечные титры (кратности разведения) указаны на оси Y. См. также Пример 22.
Фиг.52. Е1, продуцированный в Hansenula, был алкилирован ("А") или сульфонирован ("S") и нанесен на твердую подложку для твердофазного иммуноферментного анализа (ELISA), чтобы определить конечную точку титрования антител, присутствующих в сыворотках после вакцинации мышей белком Е1, продуцируемым в Hansenula, который был алкилирован (верхняя панель) или после вакцинации мышей белком Е1, продуцируемым в Hansenuta, который был сульфонирован (нижняя панель). Горизонтальная полоса представляет средний титр антител. Конечные титры (кратности разведения) указаны на оси Y. См. также Пример 23.
Фиг.53. HCV E1, продуцированный клетками млекопитающего, которые были инфицированы HCV-рекомбинантным вирусом коровьей оспы, и HCV E1, продуцированный Н.polymorpha, были нанесены непосредственно на планшеты для ELISA. Были определены титры в конечных точках для антител в сыворотках от шимпанзе, вакцинированных белком E1, который был продуцирован клетками млекопитающего (верхняя панель), или мышиных моноклональных антител, наработанных против белка E1, продуцированного клетками млекопитающего (нижняя панель). Шимпанзе Yoran и Marti получили профилактические вакцинации. Шимпанзе Ton, Phil, Marcel, Peggy и Femma получили терапевтические вакцинации. Черные сплошные столбики: планшет для ELISA, покрытый белком E1, продуцированным клетками млекопитающих. Незакрашенные столбики: планшет для ELISA, покрытый белком E1, продуцированным Hansenula. Титры в конечных точках (кратности разведения) указаны на оси Y. См. также Пример 24.
Фиг.54. Проведенный с применением флуорофоров углеводный гель-электрофорез олигосахаридов, высвобождаемых из белка E1, продуцированного клетками млекопитающего, которые были инфицированы HCV-рекомбинантным вирусом коровьей оспы, и из белка Е1-Н6, продуцированного Hansenula.
Дорожка 1: Многоступенчатый глюкозный стандарт, слева указано количество моносахаридов (от 3 до 10, обозначенные как G3-G10).
Дорожка 2: 25 мкг N-связанных олигосахаридов, высвобожденных из (алкилированного) белка E1, продуцированного клетками млекопитающего.
Дорожка 3: 25 мкг N-связанных олигосахаридов, высвобожденных из (алкилированного) белка E1, продуцированного Hansenula.
Дорожка 4: 100 пмоль мальтотетраозы.
См. также Пример 25.
Фиг.55. На данном рисунке представлены упрощенные структуры эталонных олигоманноз Man-9 (Фиг.55.А), Man-8 (Фиг.55.В), Man-7 (Фиг.55.С), Man-6 (Фиг.55.D) и Man-5 (Фиг.55.Е). "Man"=манноза; "GlcNAc"=N-ацетилглюкозамин; "α"=α-связь между двумя маннозами; "β"=β-связь между двумя маннозами; "(1-3)", "(1-4)" и "(1-6)"=связи (1-3), (1-4) и (1-6), соответственно, между двумя маннозами. Скобки на Фиг.55.В и 55.С показывают, что 2 и 1, соответственно, маннозных остатка слева от скобок связаны связью α(1-2) с 2 и 1, соответственно, из 3 маннозных остатков справа от скобок. См. также Пример 26.
Фиг.56. На этом рисунке представлена высшая олигоманноза, состоящая из 10 маннозных группировок, присоединенных к хитобиозе. Каждый концевой маннозный остаток связан α(1-3)-связью с неконцевым маннозным остатком. Тонкая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α(1-2)-маннозидазой (таковых в данной олигоманнозе нет), толстая направленная вверх или влево указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой после удаления α(1-2)-связанных манноз (не применимо к данной олигоманнозе), а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.57. На этом рисунке представлена высшая олигоманноза, состоящая из 9 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе один концевой маннозный остаток связан α(1-2)-связью с неконцевым маннозным остатком. Тонкая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α(1-2)-маннозидазой, толстая направленная вверх или влево указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой после удаления α(1-2)-связанных манноз, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.58. На этом рисунке представлена эталонная высшая олигоманноза Man-9, состоящую из 9 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе все концевые маннозные остатки связаны α(1-2)-связью с неконцевым маннозным остатком. Тонкая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α(1-2)-маннозидазой, толстая направленная вверх или влево указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой после удаления α(1-2)-связанных манноз, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.59. На этом рисунке представлена высшая олигоманноза Man-8, состоящая из 8 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе все концевые маннозные остатки связаны α(1-3)-связью или α(1-6)-связью с неконцевым маннозным остатком, что делает эту структуру полностью устойчивой к расщеплению α(1-2)-маннозидазой. Толстая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.60. На этом рисунке представлена высшая олигоманноза Man-7, состоящая из 7 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе все концевые маннозные остатки связаны α(1-3)-связью с неконцевым маннозным остатком, что делает эту структуру полностью устойчивой к расщеплению α(1-2)-маннозидазой. Толстая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.61. На этом рисунке представлена высшая олигоманноза, состоящая из 9 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе один концевой маннозный остаток связан α(1-2)-связью с неконцевым маннозным остатком. Тонкая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α(1-2)-маннозидазой, толстая направленная вверх или влево указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой после удаления α(1-2)-связанных манноз, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. См. также Пример 26.
Фиг.62. На этом рисунке представлен предполагаемый содержащий глюкозу олигосахарид, состоящий из одной или двух глюкозных группировок и восьми маннозных группировок, присоединенных к хитобиозе. В этом олигосахариде каждый из концевых α(1-2)-связанных маннозных остатков А- или В-ветви ("А→" и "В→" на рисунке) несет один или два глюкозных остатка, как указано обозначением (Glc)Glc слева от скобки. Тонкая направленная вверх указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α(1-2)-маннозидазой при условии, что к концевому маннозному остатку не присоединена глюкоза. Толстая направленная вверх или влево указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению α-маннозидазой после удаления α(1-2)-связанных манноз, а незакрашенная направленная вниз указательная стрелка показывает связи олигосахарида, которые подвержены расщеплению β-маннозидазой после удаления α-связанных манноз. Общий обзор возможных продуктов реакций содержится в Таблице 10 Примера 26.
Фиг.63. Реакционные продукты Man-9 после инкубации в течение ночи с экзогликозидазами или без них были разделены на колонке TSK gel-Amide-80 (0,46×25 см, Tosoh Biosep), присоединенной к установке ВЭЖХ Waters Alliance. Разделение олигосахаридов проводили при температуре окружающей среды при 1,0 мл/мин. Растворитель А состоял из 0,1% уксусной кислоты в ацетонитриле, а растворитель В состоял из 0,2% уксусной кислоты и 0,2% триэтиламина в воде. Разделение меченных 2-аминобензамидом (2-АВ) олигосахаридов проводили с использованием 28% В, изократического для 5 объемов колонки, с последующи линейным возрастанием до 45% В еще для 15 объемов колонки. Состав растворителя для элюции указан на правой оси Y как % растворителя В в растворителе А (об./об.). Время элюции указано в минутах на оси X. Левая ось Y показывает флуоресценцию элюируемых меченых 2-аминобензамидом (2-АВ) олигосахаридов. Длина волны возбуждения 2-аминобензамида равна 330 нм, а длина волны испускания равна 420 нм.
Кривая 1 ("1") хроматограммы показывает элюцию Man-9, инкубированного в течение ночи без экзогликозидазы. Кривая 2 ("2") показывает элюцию смеси Man-5 и Man-6 после инкубации Man-9 в течение ночи с α(1-2)-маннозидазой. Кривые 3 и 4 ("3" и "4") показывают элюцию 4'-β-маннозилхитобиозы после инкубации Man-9 с α-маннозидазой в течение 1 часа и в течение ночи, соответственно. Кривая 5 ("5") показывает элюцию хитобиозы после инкубации Man-9 с α- и β-маннозидазой в течение ночи. Кривые 1-5 представлены как наложенные друг на друга, и у них, как у таковых, не все соответствующие базовые линии находятся на нулевом уровне. Кривая 6 ("6") показывает использованный градиент растворителей.
Пики, если они есть, указанные латинскими буквами от А до К в верхней части рисунка, представляют собой: А, хитобоза; В, 4'-β-маннозилхитобиоза; С, Man-2; D, Man-3; Е, Man-4; F, Man-5; G, Man-6; Н, Man-7; I, Man-7; J, Man-8; К, Man-10. См. также Пример 26.
Фиг.64. Реакционные продукты олигосахаридов, полученных из E1s, продуцируемого Saccharomyces, после инкубации в течение ночи с экзогликозидазами или без них были разделены на колонке TSK gel-Amide-80 (0,46×25 см, Tosoh Biosep), присоединенной к установке ВЭЖХ Waters Alliance. Разделение олигосахаридов проводили при температуре окружающей среды при 1,0 мл/мин. Растворитель А состоял из 0,1% уксусной кислоты в ацетонитриле, а растворитель В состоял из 0,2% уксусной кислоты и 0,2% триэтиламина в воде. Разделение меченых 2-аминобензамидом олигосахаридов проводили с использованием 28% В, изократического для 5 объемов колонки, с последующим линейным возрастанием до 45% В еще для 15 объемов колонки. Состав растворителя для элюции указан на правой оси Y как % растворителя В в растворе А (об./об.). Время элюции указано в минутах на оси X. Левая ось Y показывает флуоресценцию элюируемых меченных 2-аминобензамидом олигосахаридов. Длина волны возбуждения 2-аминобензамида равна 330 нм, а длина волны испускания равна 420 нм.
Кривая 1 ("1") хроматограммы показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Saccharomyces, после инкубации в течение ночи без экзогликозидаз. Кривая 2 ("2") показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Saccharomyces, после инкубации Man-9 в течение ночи с α(1-2)-маннозидазой. Кривые 3 и 4 ("3" и "4") показывают элюцию олигосахаридов, полученных из E1s, продуцируемого Saccharomyces, после инкубации с α-маннозидазой в течение 1 часа и в течение ночи, соответственно. Кривая 5 "5" показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Saccharomyces, после инкубации с α- и β-маннозидазой в течение ночи. Кривые 1-5 представлены как наложенные друг на друга, и у них, как у таковых, не все соответствующие базовые линии находятся на нулевом уровне. Кривая 6 ("6") показывает использованный градиент растворителей.
Пики, если они есть, указанные латинскими буквами от А до К в верхней части рисунка, представляют собой: А, хитобоза; В, 4'-β-маннозилхитобиоза; С, Man-2; D, Man-3; Е, Man-4; F, Man-5; G, Man-6; H, Man-7; I, Man-7; J, Man-8; К, Man-10. См. также Пример 26.
Фиг.65. Реакционные продукты олигосахаридов, полученных из E1s, продуцируемого клетками млекопитающего, трансфицированными вирусом коровьей оспы, после инкубации в течение ночи с экзогликозидазами или без них были разделены на колонке TSK gel-Amide-80 (0,46×25 см, Tosoh Biosep), присоединенной к установке ВЭЖХ Waters Alliance. Разделение олигосахаридов проводили при температуре окружающей среды при 1,0 мл/мин. Растворитель А состоял из 0,1% уксусной кислоты в ацетонитриле, а растворитель В состоял из 0,2% уксусной кислоты и 0,2% триэтиламина в воде. Разделение меченых 2-аминобензамидом олигосахаридов проводили с использованием 28% В, изократического для 5 объемов колонки, с последующим линейным возрастанием до 45% В еще для 15 объемов колонки. Состав растворителя для элюции указан на правой оси Y как % растворителя В в растворе А (об./об.). Время элюции указано в минутах на оси X. Левая ось Y показывает флуоресценцию элюируемых меченных 2-аминобензамидом олигосахаридов. Длина волны возбуждения 2-аминобензамида равна 330 нм, а длина волны испускания равна 420 нм.
Кривая 1 ("1") хроматограммы показывает элюцию олигосахаридов, полученных из E1s, продуцируемого клетками млекопитающего, трансфицированными вирусом коровьей оспы, после инкубации в течение ночи без экзогликозидаз. Кривая 2 ("2") показывает элюцию олигосахаридов, полученных из E1s, продуцируемого клетками млекопитающего, трансфицированными вирусом коровьей оспы, после инкубации Man-9 в течение ночи с α(1-2)-маннозидазой. Кривые 3 и 4 ("3" и "4") показывают элюцию олигосахаридов, полученных из E1s, продуцируемого клетками млекопитающего, трансфицированными вирусом коровьей оспы, после инкубации с α-маннозидазой в течение 1 часа и в течение ночи, соответственно. Кривая 5 "5" показывает элюцию олигосахаридов, полученных из E1s, продуцируемого клетками млекопитающего, трансфицированными вирусом коровьей оспы, после инкубации с α- и β-маннозидазой в течение ночи. Кривые 1-5 представлены как наложенные друг на друга, и у них, как у таковых, не все соответствующие базовые линии находятся на нулевом уровне. Кривая 6 ("6") показывает использованный градиент растворителей.
Пики, если они есть, указанные латинскими буквами от А до К в верхней части рисунка, представляют собой: А, хитобоза; В, 4'-β-маннозилхитобиоза; С, Man-2; D, Man-3; Е, Man-4; F, Man-5; G, Man-6; H, Man-7; I, Man-7; J, Man-8; К, Man-10. См. также Пример 26.
Фиг.66. Реакционные продукты олигосахаридов, полученных из E1s, продуцируемого Hansenula, после инкубации в течение ночи с экзогликозидазами или без них были разделены на колонке TSK gel-Amide-80 (0,46×25 см, Tosoh Biosep), присоединенной к установке ВЭЖХ Waters Alliance. Разделение олигосахаридов проводили при температуре окружающей среды при 1,0 мл/мин. Растворитель А состоял из 0,1% уксусной кислоты в ацетонитриле, а растворитель В состоял из 0,2% уксусной кислоты и 0,2% триэтиламина в воде. Разделение меченых 2-аминобензамидом олигосахаридов проводили с использованием 28% В, изократического для 5 объемов колонки, с последующим линейным возрастанием до 45% В еще для 15 объемов колонки. Состав растворителя для элюции указан на правой оси Y как % растворителя В в растворе А (об./об.). Время элюции указано в минутах на оси X. Левая ось Y показывает флуоресценцию элюируемых меченных 2-аминобензамидом олигосахаридов. Длина волны возбуждения 2-аминобензамида равна 330 нм, а длина волны испускания равна 420 нм.
Кривая 1 ("1") хроматограммы показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Hansenula, после инкубации в течение ночи без экзогликозидаз. Кривая 2 ("2") показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Hansenula, после инкубации Man-9 в течение ночи с α(1-2)-маннозидазой. Кривые 3 и 4 ("3" и "4") показывают элюцию олигосахаридов, полученных из E1s, продуцируемого Hansenula, после инкубации с α-маннозидазой в течение ночи. Кривая 5 "5" показывает элюцию олигосахаридов, полученных из E1s, продуцируемого Hansenula, после инкубации с α- и β-маннозидазой в течение ночи. Кривые 1-5 представлены как наложенные друг на друга, и у них, как у таковых, не все соответствующие базовые линии находятся на нулевом уровне. Кривая 6 ("6") показывает использованный градиент растворителей.
Пики, если они есть, указанные латинскими буквами от А до К в верхней части рисунка, представляют собой: А, хитобоза; В, 4'-β-маннозилхитобиоза; С, Man-2; D, Man-3; Е, Man-4; F, Man-5; G, Man-6; H, Man-7; I, Man-7; J, Man-8; К, Man-10. См. также Пример 26.
Фиг.67. Анализ белков Е1, продуцируемых Hansenula и клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, посредством Na-ДДС-ПААГ и окрашивания Кумасси бриллиантовым синим.
Дорожка 1: маркеры молекулярной массы с молекулярными массами, указанными слева; дорожка 2: алкилированный E1s, продуцируемый Hansenula polymorpha (10 мкг); дорожка 3: алкилированный E1s, продуцируемый Hansenula polymorpha (5 мкг); дорожка 4: алкилированный E1s, продуцируемый Hansenula polymorpha (2,5 мкг); дорожка 5: алкилированный E1s, продуцируемый клетками vero, инфицированными HCV-рекомбинантным вирусом коровьей оспы (10 мкг); дорожка 6: алкилированный E1s, продуцируемый клетками vero, инфицированными HCV-рекомбинантным вирусом коровьей оспы (5 мкг); дорожка 7: алкилированный E1s, продуцируемый клетками vero, инфицированными HCV-рекомбинантным вирусом коровьей оспы (2,5 мкг). См. также Пример 27.
Фиг.68. Последовательность белка HCV E2-H6 (SEQ ID NO:5) с указанием трипсиновых фрагментов (последовательности в прямоугольных рамках) дегликозилированного белка. Гликозилированные Asn-остатки превращены в Asp-остатки ферментом PNGase F и указаны знаком "*" под последовательностью. Asn-остатки подвержены протеолитическому расщеплению Asp-N-эндопептидазой. Возможными сайтами N-гликозилирования в E2-H6 (SEC ID NO:5) являются N417, N423, N430, N448, N478, N532, N540, N556, N576, N623 и N645 согласно нумерации в полипротеине HCV; на данном рисунке эти сайты пронумерованы как N34, N40, N47, N65, N95, N149, N157, N173, N193, N240 и N262. См. также Пример 28.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В работе, которая привела к этому изобретению, было замечено, что экспрессия гликозилированных оболочечных белков HCV в Saccharomyces cerevisiae, Pichia pastoris и Hansenula polymorpha была возможна путем экспрессии указанных оболочечных белков HCV в виде белков, содержащих сигнальную пептидную последовательность, присоединенную к указанным оболочечным белкам HCV. Однако типы гликозилирования оболочечных белков HCV, экспрессировавшихся в этих трех видах дрожжей, были очень разными (см. Примеры 6, 10, 13 и 25). Более конкретно, оболочечные белки HCV из S.cerevisiae (мутант с дефектом гликозилирования) и Н.polymorpha были гликозилированы до некоторой степени схожим с кор-гликозилированием образом. Оболочечные белки HCV, экспрессировавшиеся в Pichia pastoris, были гипергликозилированы, несмотря на ранние сообщения о том, что белки, экспрессируемые в этих дрожжах, обычно не являются гипергликозилированными (Gellisen et al. 2000, Surgue et al. 1997).
При дальнейшем анализе типов гликозилирования белков HCV, продуцированных S.cerevisiae (штамм с дефектом гликозилирования), Н.polymorpha и клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, было неожиданно обнаружено, что оболочечные белки HCV, продуцируемые Hansenula, демонстрировали тип гликозилирования, который весьма благоприятен для диагностических, профилактических и терапевтических применений этих оболочечных белков HCV (см. Примеры 21-24 и 26-29). Это неожиданное открытие отражено в разных аспектах и воплощениях настоящего изобретения, как это представлено ниже.
Первый аспект этого изобретения относится к выделенному оболочечному белку HCV или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он представляет собой продукт экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что в среднем до 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79% и 80% N-гликозилированных сайтов являются кор-гликозилированными. Более конкретно, более чем 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% и 95% этих N-гликозилированных сайтов гликозилированы олигоманнозой со структурой, определяемой как Man(8-10)-GlcNAc(2). Более конкретно для любой из вышеуказанных особенностей N-гликозилирования, соотношение сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(7)-GlcNAc(2), и сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(8)-GlcNAc(2), меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно для любой из вышеуказанных особенностей N-гликозилирования, указанные олигоманнозы содержат менее 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
Выражение "N-гликозилированные сайты, гликозилированные олигоманнозой, имеющей структуру, определяемую как Man(8-10)-GlcNAc(2)" означает, что указанные N-гликозилированные сайты гликозилированы любой из Man(8)-GlcNAc(2), Man(9)-GlcNAc(2) или Man(10)-GlcNAc(2).
Должно быть ясно, что один и тот же сайт N-гликозилирования в двух белках может быть занят разными олигоманнозами.
Термин "белок" относится к полимеру аминокислот и не касается конкретной длины этого продукта; таким образом, в это определение белка включены пептиды, олигопептиды и полипептиды. Также этот термин не касается пост-экспрессионных модификаций белка, например, гликозилирований, ацетилирований, фосфорилирований и тому подобного, и не исключает их. В это определение включены, например, полипептиды, содержащие один или более чем один аналог аминокислоты (включая, например, неприродные аминокислоты, PNA и так далее), полипептиды с замещенными связями, а также другие модификации, известные в данной области, как встречающиеся, так и не встречающиеся в природе.
Под "пре-про-белком" или "пре-белком" при использовании здесь подразумевается, соответственно, белок, содержащий пре-про-последовательность, присоединенную к белку, представляющему интерес, или белок, содержащий про-последовательность, присоединенную к белку, представляющему интерес. В качестве альтернатив "пре-последовательности" используют термины " сигнальная последовательность", "сигнальный пептид", "лидерный пептид" или "лидерная поледовательность"; все они относятся к аминокислотной последовательности, которая направляет пре-белок в шероховатый эндоплазматический ретикулюм (ЭР), что является предпосылкой N-гликозилирования. "Сигнальная последовательность", "сигнальный пептид", "лидерный пептид" или "лидерная последовательность" отщепляется, то есть «отделяется» от белка, содержащего эту сигнальную последовательность, присоединенную к белку, представляющему интерес, в просветном участке этого ЭР специфическими протеазами хозяина, именуемым сигнальными пептидазами. Аналогично, пре-про-белок превращается в про-белок при перемещении в просвет ЭР. В зависимости от природы "про"-аминокислотной последовательности, она может или не может быть удалена клеткой-хозяином, экспрессирующей пре-про-белок. Хорошо известной пре-про-аминокислотной последовательностью является пре-про-последовательность α-фактора спаривания у α-фактора спаривания S.cerevisiae.
Под "оболочечным белком HCV" подразумевается оболочечный белок Е1 HCV или Е2 HCV или его часть, посредством которой указанные белки могут быть получены из штамма HCV любого генотипа. Более конкретно, HCVENV выбирают из группы аминокислотных последовательностей, состоящей из аминокислотных последовательностей SEQ ID NOs:85-98, из аминокислотных последовательностей, которые по меньшей мере на 90% идентичны аминокислотным последовательностям SEQ ID NOs:85-98, и из фрагментов любой из них. "Идентичными" аминокислотами считаются группы консервативных аминокислот, как описано выше, а именно, группа, состоящая из Met, Ile, Ley и Val; группа, состоящая из Arg, Lys и His; группа, состоящая из Phe, Trp и Tyr; группа, состоящая из Asp и Glu; группа, состоящая из Asn и Gln; группа, состоящая из Cys, Ser и Thr; и группа, состоящая из Ala и Gly.
Более конкретно, термин "оболочечные белки HCV" относится к полипептиду или его аналогу (например, мимотопам), содержащему аминокислотную последовательность (и/или аналоги аминокислот), определяющую по меньшей мере один эпитоп HCV из области Е1 или Е2 в дополнение к сайту гликозилирования. Эти оболочечные белки могут быть как мономерными, гетеро-олигомерными, так и гомо-олигомерными формами рекомбинантно экспрессируемых оболочечных белков. В типичных случаях последовательности, определяющие эпитоп, соответствуют аминокислотным последовательностям либо участка Е1, либо участка Е2 из HCV (идентично либо посредством замен аналогами нативного аминокислотного остатка, которые не нарушают эпитоп).
Должно быть понятно, что эпитоп HCV может быть локализован совместно с сайтом гликозилирования.
В общем последовательность, определяющая эпитоп, должна быть длиной в 3 или 4 аминокислоты, более типично длиной в 5, 6 или 7 аминокислот, более типично длиной в 8 или 9 аминокислот и еще более типично длиной в 10 или более чем 10 аминокислот. Что касается конформационных эпитопов, то длина последовательности, определяющей эпитоп, может быть подвержена большим вариациям, поскольку считают, что эти эпитопы формируются трехмерной структурой антигена (например, укладкой). Так, аминокислоты, определяющие эпитоп, могут быть относительно немногочисленными, но широко разбросанными по длине молекулы и приводимыми в правильную конформацию эпитопа путем укладки. Участки антигена между остатками, определяющими эпитоп, могут не быть критичными для конформационной структуры эпитопа. Например, делеция или замена этих промежуточных последовательностей может не влиять на конформационный эпитоп при условии, что сохраняются последовательности, которые критичны для эпитопа (например, цистеины, вовлеченные в образование дисульфидных связей, сайты гликозилирования и так далее). Конформационный эпитоп может быть также образован двумя или более чем двумя существенными участками субъединиц гомо-олигомера или гетеро-олигомера.
Эпитоп определенного полипептида при использовании здесь обозначает эпитопы, у которых аминокислотная последовательность такая же, как у эпитопа этого определенного полипептида, и их иммунологические эквиваленты. Такие эквиваленты также включают в себя варианты, специфичные для штамма, субтипа (=генотипа) или типа (группы), например для известных в настоящее время последовательностей или штаммов, относящихся к генотипам 1а, 1b, 1с, 1d, 1e, 1f, 2a, 2b, 2c, 2d, 2e, 2f, 2g, 2h, 2i, 3а, 3b, 3с, 3d, 3е, 3f, 3g, 4а, 4b, 4c, 4d, 4e, 4f, 4g, 4h, 4i, 4j, 4k, 4l, 5a, 5b, 6a, 6b, 6с, 7a, 7b, 8a, 8b, 9a, 9b, 10a, 11 (и его субтипам), 12 (и его субтипам) или 13 (и его подтипам), или любым другим вновь определенным (суб)типам HCV. Следует понимать, что аминокислоты, составляющие эпитоп, не обязательно должны быть частью линейной последовательности, но могут быть разделены любым количеством аминокислот, тем самым образуя конформационный эпитоп.
Антигены HCV по настоящему изобретению включают в себя эпитопы из (оболочечных) доменов Е1 и/или Е2 из HCV. Домен Е1, который считают соответствующим вирусному оболочечному белку, по современным оценкам простирается в промежутке аминокислот 192-383 полипротеина HCV (Hijikata et al., 1991). Считают, что при экспрессии в системе млекопитающего (будучи гликозилированным) он имеет молекулярную массу около 35 кДа при определении посредством Na-ДДС-ПААГ электрофореза. Считают, что белок Е2, который прежде называли NS1, простирается в промежутке аминокислот 384-809 или 384-746 (Grakoui et al., 1993) полипротеина HCV и также является оболочечным белком. Считают, что при экспрессии в системе вируса коровьей оспы (будучи гликозилированным) он имеет кажущуюся по определению в геле молекулярную массу около 72 кДа. Понятно, что эти конечные параметры белка являются приблизительными (например, карбокси-терминальный конец Е2 может находиться где-то в районе аминокислот 730-820, например, оканчиваться аминокислотой 730, 735, 740, 742, 745, предпочтительно 746, 747, 748, 750, 760, 770, 780, 790, 800, 809, 810, 820). Белок Е2 может также экспрессироваться вместе с белком Е1 и/или кором (аминокислоты 1-191), и/или Р7 (аминокислоты 747-809), и/или NS2 (аминокислоты 810-1026), и/или NS3 (аминокислоты 1027-1657), и/или NS4A (аминокислоты 1658-1711), и/или NS4B (аминокислоты 1712-1972), и/или NS5A (аминокислоты 1973-2420), и/или NS5B (аминокислоты 2421-3011), и/или любой частью этих белков HCV, отличных от Е2. Аналогично, белок Е1 может также экспрессироваться вместе с Е2, и/или кором (аминокислотами 1-191), и/или Р7 (аминокислоты 747-809), и/или NS2 (аминокислоты 810-1026), и/или NS3 (аминокислоты 1027-1657), и/или NS4A (аминокислоты 1658-1711), и/или NS4B (аминокислоты 1712-1972), и/или NS5A (аминокислоты 1973-2420), и/или NS5B (аминокислоты 2421-3011), и/или любой частью этих HCV белков, отличных от Е1. Экспрессия вместе с этими другими белками HCV может быть важной для достижения правильной укладки белка.
Термин "Е1" при использовании здесь также включает в себя аналоги и усеченные формы, которые являются иммунологически перекрестно-реактивными с природным Е1 и включают в себя белки Е1 генотипов 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 или любого другого вновь идентифицированного типа или субтипа HCV. Термин "Е2" при использовании здесь также включает в себя аналоги и усеченные формы, которые являются иммунологически перекрестно-реактивными с природным Е2 и включают в себя белки Е2 генотипов 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 или любого другого вновь идентифицированного типа или субтипа HCV. Например, Kato et al. (1992) сообщают о вставках множественных кодонов между кодоном 383 и кодоном 384, а также о делециях аминокислот 384-387. Таким образом, понятно также, что изоляты, использованные в разделе примеров настоящего изобретения, не предназначены для того, чтобы ограничить объем этого изобретения, и что любой изолят HCV, относящийся к типу 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 или любому новому генотипу HCV, является подходящим источником последовательности Е1 и/или Е2 для практики по настоящему изобретению. Аналогично, как описано выше, белки HCV, которые экспрессируются совместно с оболочечными белками HCV по настоящему изобретению, могут быть получены из HCV любого типа, также из того же типа, что и оболочечные белки HCV по настоящему изобретению.
"Е1/Е2" при использовании здесь относится к олигомерной форме оболочечных белков, содержащих по меньшей мере один Е1 компонент и по меньшей мере один Е2 компонент.
Термин "специфические олигомерные" оболочечные белки Е1 и/или Е2, и/или Е1/Е2 относится ко всем возможным олигомерным формам рекомбинантно экспрессируемых оболочечных белков Е1 и/или Е2, которые не являются агрегатами. Специфические олигомерные оболочечные белки Е1 и/или Е2 также называются гомо-олигомерными оболочечными белками Е1 или Е2 (см. ниже). Термин "единичные или специфические олигомерные" оболочечные белки Е1 и/или Е2, и/или Е1/Е2 относится к отдельным мономерным белкам Е1 или Е2 (отдельным в строгом смысле этого слова), а также к рекомбинантно экспрессируемым специфическим олигомерным белкам Е1 и/или Е2, и/или Е1/Е2. Эти отдельные или специфические олигомерные оболочечные белки по настоящему изобретению можно далее определить следующей формулой: (Е1)х(Е2)у, где х может быть числом между 0 и 100, а у может быть числом между 0 и 100, при условии, что х и у оба не равны 0. При х=1 и у=0 указанные оболочечные белки включают в себя мономерный Е1.
Термин "гомо-олигомер" при использовании здесь относится к комплексу Е1 или Е2, содержащему более чем один мономер Е1 или Е2, например, димеры Е1/Е1, тримеры Е1/Е1/Е1 или тетрамеры Е1/Е1/Е1/Е1 и димеры Е2/Е2, тримеры Е2/Е2/Е2 или тетрамеры Е2/Е2/Е2/Е2, Е1 пентамеры и гексамеры, Е2 пентамеры и гексамеры, или любые гомо-олигомеры Е1 или Е2 высшего порядка, - все они в объеме этого определения являются "гомо-олигомерами". Эти олигомеры могут содержать один, два или несколько разных мономеров Е1 или Е2, полученных из разных типов или субтипов вируса гепатита С, включая, например, те, что описали Maertens et al. в WO94/25601 и WO96/13590, в обоих случаях настоящих заявителей. Такие смешанные олигомеры все равно в объеме этого изобретения являются гомо-олигомерами и могут обеспечить возможность более универсальной диагностики, профилактики или лечения HCV.
Антигены Е1 и Е2, использованные в настоящем изобретении, могут быть полноразмерными вирусными белками, их по существу полноразмерными версиями или их функциональными фрагментами (например, фрагментами, содержащими по меньшей мере один эпитоп и/или сайт гликозилирования). Более того, антигены HCV по настоящему изобретению могут также включать в себя другие последовательности, которые не блокируют или не предотвращают образование конформационного эпитопа, представляющего интерес. Наличие или отсутствие конформационного эпитопа можно легко определить путем скрининга антигена, представляющего интерес, с помощью антитела (поликлональной или моноклональной сыворотки к конформационному эпитопу) и сравнением его реактивности с реактивностью денатурированной версии этого антигена, которая сохраняет только линейные эпитопы (если они есть). В таком скрининге с использованием поликлональных антител может быть полезно сначала адсорбировать поликлональную сыворотку денатурированным антигеном и посмотреть, сохранит ли она антитела к антигену, представляющему интерес.
Белки HCV по настоящему изобретению могут быть гликозилированы. Под гликозилированными белками подразумевают белки, которые содержат одну или более чем одну углеводную группу, в частности группы сахаров. В общем, все эукариотические клетки способны гликозилировать белки. После выравнивания последовательностей оболочечных белков разных генотипов HCV можно сделать вывод, что для правильной укладки и реактивности требуются не все 6 сайтов гликозилирования в белке Е1 HCV. Далее известно, что сайт гликозилирования в положении 325 не модифицируется путем N-гликозилирования (Fournillier-Jacob et al. 1996, Meunier et al. 1999). Более того, белок Е1 субтипа 1b HCV содержит 6 сайтов гликозилирования, но некоторые из этих сайтов гликозилирования у определенных (суб)типов отсутствуют. Четвертый углеводный мотив (на Asn250), имеющийся у типов 1b, 6а, 7, 8 и 9, отсутствует у всех остальных типов, известных на данное время. Этот мотив присоединения сахара может быть мутирован с образованием белка Е1 типа 1b с улучшенной реактивностью. Кроме того, последовательности типа 2b демонстрируют сайт экстра-гликозилирования в области V5 (на Asn299). У изолята S83, относящегося к генотипу 2с, первый углеводный мотив в области V1 (на Asn) даже отсутствует, тогда как он имеется у всех остальных изолятов (Stuyver et al., 1994). Однако даже у полностью консервативных мотивов присоединения сахаров присутствие углевода может не требоваться для укладки, но может играть определенную роль в ускользании от иммунологического надзора. Таким образом, идентификацию роли гликозилирования можно проверить далее мутагенезом мотивов гликозилирования. Мутагенез мотива гликозилирования (последовательностей NXS или NXT) может быть осуществлен либо мутированием кодонов для N, S или Т таким образом, чтобы эти кодоны кодировали аминокислоты, отличные от N в случае N, и/или аминокислоты, отличные от S или Т в случае S или в случае Т. Альтернативно, позицию Х можно мутировать в Р, поскольку известно, что NPS или NPT не часто модифицируются углеводами. После установления того, какие мотивы присоединения сахаров требуются для укладки и/или реактивности, а какие не требуются, можно производить комбинации таких мутаций. Такие эксперименты подробно описали Maertens et al. в Примере 8 из WO96/04385, которая конкретно включена сюда путем ссылки.
Термин «гликозилирование» при использовании в настоящем изобретении относится к N-гликозилированию, если не оговорено иначе.
В частности, настоящее изобретение относится к оболочечным белкам HCV или их частям, которые являются кор-гликозилированными. В этом отношении термин "кор-гликозилирование" относится к структуре, "сходной" со структурой, которая представлена обведенной рамкой структурой на Фиг.3 в Herscovics and Orlean (1993). Таким образом, указанная углеводная структура содержит 10-11 моносахаридов. Важно, что указанное описание включено сюда ссылкой на него. Термин "сходный" подразумевает, что к этой структуре добавлено не более четырех дополнительных моносахаридов или что не более трех моносахаридов удалено из этой структуры. Следовательно, углеводная структура кор-гликозилирования, о которой идет речь в настоящем изобретении, состоит минимум из 7 и максимум из 15 моносахаридов и может состоять из 8, 9, 10, 11, 12, 13 или 14 моносахаридов. Подразумеваемые моносахариды предпочтительно представляют собой глюкозу, маннозу или N-ацетилглюкозамин.
Альтернативный аспект настоящего изобретения относится к выделенному оболочечному белку HCV или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он является продуктом экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что более чем 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% или 95% сайтов N-гликозилирования гликозилированы олигоманнозой со структурой, определяемой как Man(8-10)-GlcNAc(2). Более конкретно для вышеприведенной характеристики N-гликозилирования, соотношение сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(7)-GlcNAc(2), и сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(8)-GlcNAc(2), меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно для любой из вышеуказанных характеристик N-гликозилирования, указанные олигоманнозы содержат менее 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
Еще один альтернативный аспект настоящего изобретения относится к выделенному оболочечному белку HCV или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он является продуктом экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что сайты N-гликозилирования заняты олигоманнозами, причем соотношение олигоманноз со структурой Man(7)-GlcNAc(2) и олигоманноз со структурой Man(8)-GlcNAc(2) меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно для вышеуказанных характеристик N-гликозилирования, указанные олигоманнозы содержат менее чем 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
Другой альтернативный аспект настоящего изобретения охватывает выделенный оболочечный белок HCV или его фрагмент, содержащий по меньшей мере один сайт N-гликозилирования, отличающийся тем, что он является продуктом экспрессии в эукариотической клетке не-млекопитающего, и дополнительно отличающийся тем, что число сайтов N-гликозилирования по меньшей мере на 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13% или 15% меньше, чем число сайтов N-гликозилирования у того же белка или его фрагмента, экспрессируемого из вируса коровьей оспы в эукариотической клетке, подверженной инфицированию или инфицированной указанным вирусом коровьей оспы. Более конкретно в отношении вышеприведенной характеристики N-гликозилирования, вплоть до 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79% и 80% сайтов N-гликозилирования являются кор-гликозилированными. Более конкретно, более чем 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% и 95% сайтов N-гликозилирования гликозилированы олигоманнозой со структурой, определяемой как Man(8-10)-GlcNAc(2). Более конкретно в отношении любой из вышеуказанных характеристик N-гликозилирования, соотношение сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(7)-GlcNAc(2), и сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(8)-GlcNAc(2), меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно в отношении любой из вышеуказанных характеристик N-гликозилирования, указанные олигоманнозы содержат менее 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
В другом аспекте этого изобретения выделенный оболочечный белок HCV или его часть согласно изобретению является продуктом экспрессии в дрожжевой клетке. Более конкретно, выделенный оболочечный белок HCV или его часть согласно изобретению является продуктом экспрессии в клетке штаммов Saccharomyces, таких как Saccharomyces cerevisiae, Saccharomyces kluyveri или Saccharomyces uvarum, Schizosaccharomyces, таких как Schizosaccharomyces pombe, Kluyveromyces, таких как Kluyveromyces lactis, Yarrowia, таких как Yarrowia lipolytica, Hansenula, таких как Hansenula polymorpha, Pichia, таких как Pichia pastoris, видов Aspergillus species, Neurospora, таких как Neurospora crassa, или Schwanniomyces, таких как Schwanniomyces occidentalis, или в мутантных клетках, полученных из любых из них. Более конкретно, выделенный оболочечный белок HCV или его часть согласно изобретению является продуктом экспрессии в клетке Hansenula. Еще более конкретно, выделенный оболочечный белок HCV или его часть согласно изобретению является продуктом экспрессии в дрожжевой клетке, например клетке Hansenula, в отсутствие ингибиторов гликозилирования, таких как туникамицин.
В другом аспекте этого изобретения выделенный оболочечный белок HCV или его часть по изобретению получены из белка, содержащего лидерный пептид птичьего лизоцима или его функциональный вариант, присоединенный к указанному оболочечному белку HCV или его фрагменту. Более конкретно, выделенный оболочечный белок HCV или его часть согласно изобретению получены из белка, который характеризуется следующей структурой
CL-[(A1)a-(PS1)b-(A2)c]-HCVENV-[(A3)d-(PS2)e-(А4)f]
где:
CL является лидерным пептидом птичьего лизоцима или его функциональным эквивалентом,
А1, А2, A3 и А4 являются адаптерными пептидами, которые могут быть одинаковыми или разными,
PS1 и PS2 являются сайтами процессинга, которые могут быть одинаковыми или разными,
HCVENV является оболочечным белком HCV или его частью,
а, b, с, d, e и f равны 0 или 1, и
где, возможно, А1 и/или А2 представляют собой часть PS1, и/или где A3 и/или А4 представляют собой часть PS2.
Под "лидерным пептидом птичьего лизоцима или его функциональным эквивалентом, присоединенным к оболочечному белку HCV или его части" подразумевается, что С-концевая аминокислота указанного лидерного пептида ковалентно связана пептидной связью с N-концевой аминокислотой указанного оболочечного белка HCV или его части. Альтернативно, С-концевая аминокислота указанного лидерного пептида отделена от N-концевой аминокислоты указанного оболочечного белка HCV или его части пептидом или белком. Указанный пептид или белок может иметь структуру [(А1)а-(PS1)b-(А2)с] как определено выше.
Образование представляющего интерес оболочечного белка HCV из белка, содержащего лидерный пептид птичьего лизоцима или его функциональный эквивалент, который присоединен к оболочечному белку HCV или его части, или из белка, характеризующегося структурой CL-[(A1)a-(PS1)b-(A2)c]-HCVENV-[(A3)d-(PS2)e-(A4)f], можно осуществить in vivo посредством протеолитических комплексов клеток, в которых экспрессируется этот пре-белок. Более конкретно, стадию, заключающуюся в удалении птичьего лидерного пептида, предпочтительно осуществляют in vivo протеолитическими комплексами клеток, в которых экспрессируется этот пре-белок. Образование можно, однако, осуществлять исключительно in vitro после и/или во время выделения и/или очистки пре-белка и/или белка из клеток, экспрессирующих этот пре-белок, и/или из культуральной жидкости, в которой выращивают клетки, экспрессирующие этот пре-белок. Альтернативно указанное образование in vivo осуществляют в комбинации с указанным образованием in vitro. Образование этого представляющего интерес белка HCV из рекомбинантно экспрессируемого пре-белка может дополнительно включать в себя применение протеолитического(их) фермента(ов) на стадии «полирования», когда все примесные белки, присутствующие вместе с белком, представляющим интерес, или их большая часть подвергается разложению, и когда белок, представляющий интерес, является устойчивым к «полирующему(щим)» протеолитическим(ому) ферментам(у). Образование и «полировка» не являются взаимно исключающими процессами и могут быть осуществлены применением одного и того же отдельного протеолитического фермента. В качестве примера здесь приведен белок E1s HCV генотипа 1b (SEC ID NO:2), который лишен Lys-остатков. При расщеплении белкового экстракта, содержащего указанные белки Е1 из HCV, эндопротеиназой Lys-C (endo-lys С) белки Е1 расщепляться не будут, тогда как загрязняющие белки, содержащие одни или более чем один Lys-остаток, разлагаются. Такой процесс может значительно упростить или улучшить выделение и/или очистку белков Е1 HCV. Более того, включением дополнительного Lys-остатка в пре-белок, например, между лидерным пептидом и белком Е1 HCV, можно получить дополнительную полезную возможность корректировать in vitro отделение лидерного пептида от пре-белка Е1 HCV. Другие белки Е1 HCV могут содержать Lys-остаток по одному или более чем одному из положений 4, 40, 42, 44, 61, 65 или 179 (причем положение 1 является первой N-концевой природной аминокислотой белка Е1, то есть положением 192 полипротеина HCV). Для того, чтобы сделать возможным применение endo-lys С как описано выше, указанные Lys-остатки можно мутировать в другой аминокислотный остаток, предпочтительно в Arg-остаток.
Под "корректно удаленным" лидерным пептидом подразумевается, что указанный лидерный пептид удаляют из белка, содержащего эту сигнальную последовательность, присоединенную к белку, представляющему интерес, с высокой эффективностью, то есть большое число пре-(про-)белков превращают в (про-)белки, и с высокой точностью, то есть удаляют только пре-аминокислотную последовательность, но не какие-либо аминокислоты белка, представляющего интерес, присоединенного к указанной пре-аминокислотной последовательности. Под "удалением лидерного пептида с высокой эффективностью" подразумевается, что по меньшей мере около 40%, но более предпочтительно около 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или даже 99% пре-белков превращают в белок, из которого удалена эта пре-последовательность. Альтернативно, если существенная часть экспрессируемых пре-белков не превращена в белок, из которого удалена пре-последовательность, эти пре-белки все равно можно очистить или удалить во время очистки.
Под "функциональным эквивалентом лидерного пептида птичьего лизоцима (CL)" подразумевается лидерный пептид CL, в котором одна или более чем одна аминокислота заменена другой аминокислотой, причем указанная замена является консервативной аминокислотной заменой. Под "консервативной аминокислотной заменой" подразумевается замена аминокислоты, принадлежащей к группе консервативных аминокислот, другой аминокислотой, принадлежащей к той же группе консервативных аминокислот. В качестве групп консервативных аминокислот рассматривают: группу, состоящую из Met, Ile, Leu и Val; группу, состоящую из Arg, Lys и His; группу, состоящую из Phe, Trp и Tyr; группу, состоящую из Asp и Glu; группу, состоящую из Asn и Gln; группу, состоящую из Cys, Ser и Thr; и группу, состоящую из Ala и Gly. Примером консервативной аминокислотной замены в лидерном пептиде CL является природная вариация в положении 6, причем аминокислота в этом положении представляет собой либо Val, либо Ile; другая вариация случается в положении 17, причем аминокислота в этом положении представляет собой, среди прочего, Leu или Pro (см. SEQ ID NO:1). Получающиеся лидерные пептиды CL следует, таким образом, считать функциональными эквивалентами. Другие функциональные эквиваленты лидерных пепитидов CL включают в себя те лидерные пептиды, которые воспроизводят те же технические аспекты лидерных пептидов CL, что описаны во всем настоящем изобретении, в том числе варианты с делениями и варианты со вставками.
Под "А" или "адаптерным пептидом" подразумевается пептид (например, от 1 до 30 аминокислот) или белок, который может служить линкером между, например, лидерным пептидом и сайтом процессинга (PS), лидерным пептидом и белком, представляющим интерес, PS и белком, представляющим интерес, и/или белком, представляющим интерес и PS; и/или может служить линкером N- и С-конца, например, лидерного пептида, PS или белка, представляющего интерес. Адаптерный пептид "А" может иметь определенную трехмерную структуру, например, α-спиральную или β-складчатую или их комбинацию. Или же трехмерная структура А не является хорошо определенной, например, структура, представляющая собой свернутый клубок. Адаптер А может быть частью, например, пре-последовательности, про-последовательности, последовательности белка, представляющего интерес, или сайта процессинга. Адаптер А может служить меткой, улучшающей или делающей возможным обнаружение и/или очистку, и/или процессинг белка, частью которого является А. Одним из примеров пептида А является пептид Hn, представляющий собой гистидиновую метку (НННННН; SEQ ID NO:63), причем n обычно равно шести, но может быть 7, 8, 9, 10, 11 или 12. Другие примеры А-пептидов включают в себя пептиды EEGEPK (Kjeldsen et al. в WO98/28429; SEQ ID NO:64) или EEAEPK (Kjeldsen et al. в WO97/22706; SEQ ID NO:65), о которых сообщают, что они, когда присутствуют на N-конце белка, представляющего интерес, усиливают выход ферментации, а также защищают N-конец белка, представляющего интерес, от процессинга дипептидиламинопептидазой, что имеет результатом гомогенность N-конца полипептида. В то же время, созревание белка, представляющего интерес, in vitro, то есть, удаление указанных пептидов EEGEPK (SEQ ID NO:64) и EEAEPK (SEQ ID NO:65) из белка, представляющего интерес, может быть осуществлено применением, например, endo-lys С, которая отщепляет С-конец Lys-остатка указанных пептидов. Указанные пептиды, таким образом, выполняют функцию адаптерного пептида (А), а также сайта процессинга (см. ниже). Адаптерные пептиды приведены в SEQ ID NOs:63-65, 70-72 и 74-82. Другим примером адаптерного белка является иммуно-молчащий линкер G4S. Другие примеры адаптерных белков перечислены в Табл.2 в Stevens (Stevens et al. 2000).
Под "PS" или «сайтом процессинга» подразумевается специфический сайт процессинга белка или процессируемый сайт. Указанный процессинг может происходить ферментативным или химическим путем. Примеры сайтов процессинга, предрасположенных к специфическому ферментативному процессингу, включают в себя IEGR↓X (SEQ ID NO:66), IDGR↓X (SEQ ID NO:67), AEGR↓X (SEQ ID NO:68), все из которых распознаются и расщепляются между остатками Arg и Xaa (любая аминокислота), как указано знаком "↓", протеазой, представляющей собой бычий фактор Ха (Nagai, R. and Thogersen, H.C. 1984). Другим примером сайта PS является двухосновный сайт, например Arg-Arg, Lys-Lys, Arg-Lys или Lys-Arg, расщепляемый дрожжевой протеазой Кех2 (Julius, D. et al. 1984). Сайт PS может быть также одноосновным Lys-сайтом. Указанный одноосновный Lys-PS-сайт может также быть включен в С-конец пептида А. Примерами адаптерных пептидов А, содержащих С-концевой одноосновный Lys-PS-сайт, являются пептиды, представленные SEQ ID NOs:64-65 и 74-76. Экзопротеолитическое удаление гистидиновой метки (His-tag) (HHHHHH, SEQ ID NO:63) возможно применением дипептидиламинопептидазы I (DAPазы) в отдельности или в комбинации с глутаминциклотрансферазой (Q-циклазой) и пироглутаматаминопептидазой (pGAPазой) (Pedersen, J. et al. 1999). Указанные экзопептидазы, содержащие рекомбинантную His-tag (позволяющую удалить пептидазу из реакционной смеси аффинной хроматографией с использованием иммобилизованного металла, IMAC), имеются в продаже, например, TAGZyme System от Unizyme Laboratories (Hørsholm, DK). Таким образом, под "процессингом" в общем подразумевается любой способ или процедура, посредством которой белок специфически расщепляется или может быть расщеплен по меньшей мере в одном сайте процессинга, когда указанный сайт процессинга присутствует в указанном белке. PS может быть предрасположен к эндопротеолитическому расщеплению или может быть предрасположен к экзопротеолитическому расщеплению, в любом случае это расщепление является специфичным, то есть не распространяется на сайты, отличные от сайтов, распознаваемых протеолитическим ферментом процессинга. Множество сайтов PS приведено в SEQ ID NOs:66-68 и 83-84.
Универсальность структуры [(A1/3)a/d-(PS1/2)b/e-(A2/4)c/f)], как отмечено выше, демонстрируют некоторые примеры. В первом примере указанная структура присутствует на С-терминальном конце белка, представляющего интерес, содержащегося в пре-белке, причем A3 является пептидом "VIEGR" (SEQ ID NO:69), который перекрывается с сайтом фактора Ха "IEGRX" (SEQ ID NO:66), а Х=А4 является гистидиновой меткой (SEQ ID NO:63) (таким образом, d, е, и f, d в этом случае все равны 1). Белок HCV, представляющий интерес, может быть (возможно) очищен посредством IMAC. После процессинга фактором Ха этот (возможно очищенный) белок HCV, представляющий интерес, должен иметь на своем С-конце процессированный сайт PS, который представляет собой "IEGR" (SEQ ID NO:70). Вариантом процессированного фактором Ха сайта процессинга может быть IDGR (SEQ ID NO:71) или AEGR (SEQ ID NO:72). В еще одном примере структура [(A1/3)a/d-(PS1/2)b/e-(A2/4)c/f)] присутствует на N-конце представляющего интерес белка HCV. Более того, А1 является гистидиновой меткой (SEQ ID NO:63), PS является сайтом распознавания фактором Ха (любая из SEQ ID NOs:66-68), причем Х является белком, представляющим интерес, а=b=1 и с=0. При корректном удалении лидерного пептида, например, клеткой-хозяином, получающийся белок HCV, представляющий интерес, может быть (возможно) очищен посредством IMAC. После процессинга фактором Ха этот белок, представляющий интерес, будет лишен структуры [(А1)а-(PS1)b-(А2)с)].
Далее должно быть ясно, что любой из А1, А2, A3, А4, PS1 и PS2, если он присутствует, может присутствовать в повторяющейся структуре. Такую повторяющуюся структуру, если она присутствует, в этом контексте все равно считают за 1, то есть, а, с, d, d, e или f равны 1, даже если, например, А1 имеется, например, как два повтора (А1-А1).
Еще один аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, в котором тиольные группы цистеина модифицированы химическим путем.
Еще один аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, который является антигенным.
Еще один аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, который является иммуногенным.
Еще один аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, который содержит эпитоп, стимулирующий Т-клетки.
Другой аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, который содержится в структуре, выбранной из группы, состоящей из мономеров, гомодимеров, гетеродимеров, гомо-олигомеров и гетеро-олигомеров.
Еще один аспект настоящего изобретения относится к любому выделенному оболочечному белку HCV или его фрагменту по этому изобретению, который содержится в вирусоподобной частице.
В описанных здесь оболочечных белках HCV или их частях, содержащих по меньшей мере один остаток цистеина, но предпочтительно 2 или более чем два остатка цистеина, цистеиновые тиольные группы можно необратимо защитить химическими или ферментативными средствами. В частности, "необратимая защита" или "необратимое блокирование" химическими средствами относится к алкилированию, предпочтительно алкилированию оболочечных белков HCV алкилирующими агентами, такими как, например, активные галогены, этиленимин или N-(йодэтил)-трифторацетамид. В этом отношении следует понимать, что алкилирование цистеиновых тиольных групп относится к замене тиольного водорода структурой (CH2)nR, где n означает 0, 1, 2, 3 или 4, a R=Н, СООН, NH2, CONH2, фенил или любое их производное. Алкилирование можно проводить любым способом, известным в данной области, например, активными галогенами X(CH2)nR, где Х представляет собой галоген, такой как I, Br, Cl, или F. Примерами активных галогенов являются метилйодид, йодоуксусная кислота, йодацетамид и 2-бромэтиламин. В других способах алкилирования применяют NEM (N-этилмалеимид) или биотин-NEM, их смесь или этиленимин или N-(йодоэтил)-трифторацетамид, причем оба приводят к замене Н- на -CH2-CH2-NH2 (Hermanson, G.Т. 1996). Термин "алкилирующие агенты" при использовании здесь относится к соединениям, которые способны производить алкилирование, как здесь описано. Результатом таких алкилирований в конечном счете является модифицированный цистеин, который может имитировать другие аминокислоты. Результатом алкилирования этиленимином является структура, похожая на лизин таким образом, что вводит новые сайты расщепления для трипсина (Hermanson, G.Т. 1996). Сходным образом, результатом применения метилйодида является аминокислота, схожая с метионином, тогда как результатом применения йодацетата и йодацетамида являются аминокислоты, схожие с глутаминовой кислотой и глутамином, соответственно. По аналогии, эти аминокислоты предпочтительно применяют в прямом мутировании цистеина. Поэтому настоящее изобретение касается описанных здесь оболочечных белков HCV, у которых по меньшей мере один цистеиновый остаток описанного здесь оболочечного белка HCV мутирован в природную аминокислоту, предпочтительно в метионин, глутаминовую кислоту, глутамин или лизин. Термин "мутирован" относится к сайт-направленному мутагенезу нуклеиновых кислот, кодирующих эти аминокислоты, то есть к способам, хорошо известным в данной области, таким как, например, сайт-направленный мутагенез посредством ПЦР или опосредованный олигонуклеотидами мутаганез, как описано в (Samrock, J. et al. 1989). Следует понимать, что в разделе «Примеры» настоящего изобретения алкилирование относится к применению йодацетамида в качестве алкилирующего агента, если не указано иначе.
Следует также понимать, что в процедуре очистки цистеиновые тиольные группы белков HCV или их частей по настоящему изобретению можно защищать обратимо. Цель обратимой защиты состоит в том, чтобы стабилизировать белок HCV или его часть. В частности, серусодержащая функциональная группа (например, тиолы и дисульфиды) остается после проведения обратимой защиты в нереактивном состоянии. Таким образом, серусодержащая функциональная группа не способна реагировать с другими соединениями, например, теряет склонность образовывать или обменивать дисульфидные связи, как например,
Описанные реакции между тиольными и/или дисульфидными остатками не ограничены межмолекулярными процессами, но могут происходить внутримолекулярным образом.
Термин "обратимая защита" или "обратимое блокирование" при использовании здесь подразумевает ковалентное связывание модифицирующих агентов с цистеиновыми тиольными группами, а также такое манипулирование окружением белка HCV, при котором окислительно-восстановительное состояние цистеиновых тиольных групп остается незатронутым в ходе последующих стадий процедуры очистки (экранирование). Обратимую защиту цистеиновых тиольных групп можно осуществлять химическими или ферментативными средствами.
Термин "обратимая защита ферментативными средствами" при использовании здесь подразумевает обратимую защиту, опосредованную ферментами, такими как, например, ацил-трансферазы, в частности ацил-трансферазы, которые вовлечены в катализирование тио-этерификации, такие как пальмитоилацилтрансфераза (см. ниже).
Термин "обратимая защита химическими средствами" при использовании здесь подразумевает обратимую защиту:
1. Модифицирующими агентами, которые обратимо модифицируют цистеинилы, как например сульфонирование и тио-этерификация.
Сульфонирование является реакцией, в которой тиол или цистеины, участвующие в дисульфидных мостиках, модифицируются в S-сульфонат: RSH→RS-SO3 - (Darbre, A. 1986) или RS-SR→2RS-SO3 - (сульфитолизис; (Kumar, N. et al. 1986)). Реактивами для сульфонирования являются, например, Na2SO3 или тетратионат натрия. Применяют указанные реактивы для сульфонирования в концентрации 10-200 мМ, более предпочтительно в концентрации 50-200 мМ. Сульфонирование возможно может быть проведено в присутствии катализатора, такого как, например, Cu2+ (100 мкС - 1 мМ) или цистеин (1-10 мМ).
Эту реакцию можно проводить в условиях, которые денатурируют белок, так же как в условиях, которые оставляют белок нативным (Kumar, N. et al. 1985, Kumar, N. et al. 1986).
Образование тиоэфирной связи или тио-этерификация описывается реакцией:
RSH+R'COX→RS-COR',
где Х в соединении R'CO-X предпочтительно является галогенидом.
2. Модифицирующими агентами, которые обратимо модифицируют цистеинилы настоящего изобретения, такими как, например, тяжелые металлы, в частности Zn2+, Cd2+, моно-, дитио- и дисульфид-соединениями (например, арил- и алкил-метантиосульфонат, дитиопиридин, дитиоморфолин, дигидролипоамид, реагент Элмана, aldrothiol™ (Aldrich) (Rein, A. et al. 1996), дитиокарбаматы), или тиолирующими агентами (например, глутатион, N-ацетилцистеин, цистеинамин). Дитиокарбамат включает в себя обширный класс молекул, имеющих функциональную группу R1R2NC(S)SR3, которая придает им способность реагировать с сульфгидрильными группами. Используют тиол-содержащие соединения предпочтительно в концентрации 0,1-50 мМ, более предпочтительно в концентрации 1-50 мМ и даже еще более предпочтительно в концентрации 10-50 мМ.
3. В присутствии модифицирующих агентов, которые сохраняют (стабилизируют) состояние тиола, в частности антиоксидантов, таких как, например, дитиотреитол (DTT), дигидроаскорбат, витамины и производные, маннит, аминокислоты, пептиды и производные (например, гистидин, эрготионеин, карнозин, метионин), галлаты, гидроксианизол, гидрокситолуол, гидрохинон, гидроксиметилфенол и их производные, в диапазоне концентраций 10 мкм - 10 мМ, более предпочтительно в концентрации 1-10 мМ.
4. Использованием условий, стабилизирующих тиол, таких как, например, (1) кофакторы, такие как ионы металлов (Zn2+, Mg2+), АТФ, (2) контроль рН (например, для белков в большинстве случаев рН≈5, либо рН предпочтительно соответствует тиольному рКа-2, например, для пептидов, очищенных хроматографией с обращенной фазой при рН≈2).
Результатом комбинаций обратимой защиты, описанной в (1), (2), (3) и 4, могут быть сходным образом чистые и претерпевшие повторную укладку белки HCV. Поэтому можно использовать соединения, представляющие собой комбинации, например Z103 (Zn-карнозин), предпочтительно в концентрации 1-10 мМ. Должно быть ясно, что обратимая защита также относится, помимо вышеописанной модификации групп или экранирования, к любому способу защиты цистеинила, который может быть обращен ферментативно или химически без разрушения пептидного скелета. В этом отношении настоящее изобретение конкретно относится к пептидам, полученным классическим химическим синтезом (см. выше), в котором, например, тиоэфирные связи расщепляются тиоэстеразой, щелочными буферными условиями (Beckman, N.J. et al., 1997) или обработкой гидроксиламином (Vingerhoeds, M.H. et al., 1996).
Тиол-содержащие белки HCV можно очистить, например, на смолах для афинной хроматографии, которые содержат (1) отщепляемое соединительное звено, содержащее дисульфидную связь (например, иммобилизованная 5,5'-дитиобис(2-нитробензойная кислота) (Jayabaskaran, С. et al. 1987) и ковалентной хроматографией на активированной тиол-сефарозе 4В (Pharmacia) или (2) аминогексаноил-4-аминофениларсин в качестве иммобилизованного лиганда. Последнюю аффинную матрицу применяли для очистки белков, которые подвержены окислительно-восстановительному регулированию, и дитиольных белков, которые являются мишенями окислительного стресса (Kalef, E. et al. 1993).
Обратимую защиту можно также применять для увеличения солюбилизации и экстракции пептидов (Pomroy, N.C. and Deber, C.N. 1998).
Соединения для обратимой защиты и стабилизации тиолов могут иметь мономерную, полимерную и липосомную форму.
Снятие состояния обратимой защиты цистеиновых остатков можно осуществлять химическими или ферментативными средствами, например:
- восстановителем, в частности, дитиотреитолом, DTE, 2-меркаптоэтанолом, дитионитом, SnCl2, боргидридом натрия, гидроксиламином, ТСЕР, в частности в концентрации 1-200 мМ, более предпочтительно в концентрации 50-200 мМ;
- удалением условий или агентов, стабилизирующих тиол, например, повышением рН;
- ферментами, в частности тиоэстеразами, глутаредоксином, тиоредоксином, в частности, в концентрации 0,01-5 мкМ, еще более предпочтительно в диапазоне концентраций 0,1-5 мкМ;
- комбинациями вышеописанных химических и/или ферментативных условий.
Снятие состояния обратимой защиты цистеиновых остатков можно осуществлять in vitro или in vivo, например в клетке или в индивиде.
Должно быть понятно, что в процедуре очистки цистеиновые остатки можно подвергать или не подвергать необратимому блокированию или замещению с помощью любого агента обратимой модификации из перечисленных выше.
Восстановителем по настоящему изобретению является любой агент, который достигает восстановления серы в цистеиновых остатках, например, дисульфидных "S-S"-мостиков, десульфонирования цистеинового остатка (RS-SO3 -→RSH). Антиоксидантом является любой реагент, который сохраняет состояние тиола и/или минимизирует образование или обмена "S-S". Восстановление дисульфидных мостиков "S-S" представляет собой химическую реакцию, посредством которой дисульфиды восстанавливаются до тиола (-SH). Тем самым в настоящее описание включены ссылкой на них агенты и способы разрушения дисульфидрых мостиков, которые описали Maertens et al. в WO 96/04385. Восстановления "S-S" можно достичь (1) последовательностями ферментативных каскадов или (2) восстанавливающими соединениями. Известно, что ферменты, подобные тиоредоксину, глутаредоксину, вовлечены в восстановлении дисульфидов in vivo, и показано, что они эффективны в восстановлении "S-S"-мостиков in vitro. Дисульфидные связи быстро расщепляются восстановленным тиоредоксином при рН 7,0 с кажущейся скоростью второго порядка, которая примерно в 104 раз больше, чем соответствующая константа скорости для реакции с дитиотреитолом. Кинетику восстановления можно сильно улучшить предварительной инкубацией раствора белка с 1 мМ дитиотреитола или дигидролипоамида (Holmgren, A. 1979). Тиольными соединениями, способными восстанавливать дисульфидные мостики белков, являются, например, дитиотреитол (DTT), дитиоэритритол (DTE), β-меркаптоэтанол, тиокарбаматы, бис(2-меркаптоэтил)сульфон и N,N'-бис(меркаптоацетил)гидразин и дитионит натрия. Восстанавливающие агенты без тиольных групп, например, аскорбат или хлорид олова (SnCl2), для которых показано, что они очень полезны в восстановлении дисульфидных мостиков в моноклональных антителах (Thakur, M.L. et al. 1991), можно также применять для восстановления белков HCV. Кроме того, на окислительно-восстановительный статус белков HCV могут влиять изменения значений рН. Было показано, что обработка борогидридом натрия эффективна для восстановления дисульфидных мостиков в пептидах (Gailit, J. 1993). Трис-(2-карбоксиэтил)фосфин (ТСЕР) способен восстанавливать дисульфиды при низких рН (Burns, J. et al. 1991). Селенол катализирует восстановление дисульфидов до тиолов, когда в качестве восстановителя применяют DTT или борогидрид натрия. В качестве предшественника этого катализатора применяли имеющийся в продаже диселенид селеноцистеамин (Singh, R. and Kats.L. 1995).
Термин "иммуногенный" относится к способности белка или вещества вызывать иммунный ответ. Иммунный ответ представляет собой тотальный ответ организма на введение антигена и включает в себя образование антител, клеточный иммунитет, гиперчувствительность или иммунологическую толерантность. Клеточный иммунитет относится к ответу Т-хелперных клеток или CTL-клеток.
Термин «антигенный» относится к способности белка или вещества вызывать образование антитела или элисировать клеточный ответ.
Выражение "эпитоп, стимулирующий Т-клетки" согласно настоящему изобретению относится к эпитопу, способному стимулировать Т-клетки или CTL-клетки, соответственно. Эпитоп, стимулирующий Т-хелперные клетки, можно выбрать мониторингом лимфопролиферативного ответа на полипептиды, содержащие в своих аминокислотных последовательностях (предполагаемый) эпитоп, стимулирующий Т-клетки. Указанный лимфопролиферативный ответ можно измерять либо Т-хелперным анализом, при котором стимулируют in vitro мононуклеарные клетки периферической крови (PMBCs, peripheral blood mononuclear cells) из сывороток пациентов варьирующими концентрациями пептидов, подлежащих тестированию на активность, стимулирующую Т-клетки, и подсчитывают количество поглощения меченого радиоактивной меткой тимидина. Эпитоп, стимулирующий CTL, можно выбрать посредством анализа цитотоксичеких Т-кпеток (CTL), измеряющего литическую активность цитотоксических клеток с использованием высвобождения 51Cr. Пролиферацию считают положительной, когда индекс стимуляции (среднее значение числа импульсов в минуту в культурах, стимулированных антигеном/среднее значение числа импульсов в минуту в контрольных культурах) превышает 1, предпочтительно превышает 2, наиболее предпочтительно превышает 3.
Другой аспект этого изобретения относится к композиции, содержащей выделенный оболочечный белок HCV или его фрагмент по настоящему изобретению. Указанная композиция может дополнительно содержать фармацевтически приемлемый носитель и может представлять собой лекарство или вакцину.
Еще один аспект этого изобретения охватывает лекарство или вакцину, содержащие выделенный оболочечный белок HCV или его фрагмент по настоящему изобретению.
Еще один аспект этого изобретения включает в себя фармацевтическую композицию для индуцирования HCV-специфичного иммунного ответа у млекопитающего, содержащую эффективное количество оболочечного белка HCV или его части по изобретению и, возможно, фармацевтически приемлемый адъювант. Указанная фармацевтическая композиция, содержащая эффективное количество оболочечного белка HCV или его части согласно изобретению, может также быть способна индуцировать HCV-специфичные антитела у млекопитающего или может быть способна индуцировать Т-клеточную функцию у млекопитающего. Указанная фармацевтическая композиция, содержащая эффективное количество оболочечного белка HCV или его части согласно изобретению, может быть профилактической композицией или терапевтической композицией. В специфическом воплощении указанное млекопитающее является человеком.
"Млекопитающее" следует понимать как любого члена класса Mammalia высших позвоночных, включая людей, который характеризуется живорождением, волосяным покровом, млечными железами у самок, вырабатывающими молоко для вскармливания детенышей. Таким образом, млекопитающие включают в себя приматов, не являющихся людьми, и мышей trimera (Zauberman et al. 1999).
"Вакцина" или "лекарство" представляет собой композицию, способную элисировать защиту против заболевания, причем защита может быть частичной либо полной, а заболевание может быть либо в острой фазе, либо хронической, и в этом случае вакцина или лекарство являются профилактическими вакциной или лекарством. Вакцина или лекарство могут быть пригодны для лечения уже больного индивида, и в этом случае они называются терапевтическими вакциной или лекарством. Подобным же образом фармацевтическую композицию можно применять для целей как профилактических, так и/или терапевтических, и в этих случаях это будет профилактическая и/или терапевтическая композиция, соответственно.
Оболочечные белки HCV по настоящему изобретению можно применять как таковые, в биотинилированной форме (как раскрыто в WO 93/18054) и/или в виде комплекса с Neutralite Avidin (Molecular Probes Inc., Eugene, OR, USA), авидином или стрептавидином. Следует отметить, что "вакцина" или "лекарство" могут содержать в дополнение к активному началу "фармацевтически приемлемый носитель" или "фармацевтически приемлемый адъювант", который может быть подходящим эксципиентом, разбавителем, носителем или адъювантом, которые, сами по себе, не индуцируют продукцию антител, вредных для индивида, получающего эту композицию, а также не элисируют защиту. Типичные носители обычно представляют собой крупные медленно метаболизируемые макромолекулы, такие как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот и неактивные вирусные частицы. Такие носители хорошо известны специалистам. Предпочтительные адъюванты для усиления эффективности композиции включают в себя следующие: гидроксид алюминия, алюминий в комбинации с 3-O-деацилированным монофосфориллипидом А, как описано в WO 93/19780, фосфат алюминия, как описано в WO 93/24148, N-ацетил-мурамил-L-треонил-D-изоглутамин, как описано в патенте США №4606918, N-ацетил-нормурамил-L-аланил-D-изоглутамин, N-ацетилмурамил-L-аланил-D-изоглутамил-L-аланин-2-(1',2'-дипальмитоил-sn-глицеро-3-гидроксифосфорилокси)-этиламин, RIBI (ImmunoChem Research Inc., Hamilton, MT, USA), который содержит монофосфориллипид А, дезинтоксицированный эндотоксин, трегалоза-6,6-димиколат и скелет клеточной стенки (MPL+TDM+CWS) в 2%-ной эмульсии сквален/твин 80. Любой из этих трех компонентов, MPL, TDM или CWS, можно также применять по-отдельности или в комбинации 2 на 2. MPL можно также заменить его синтетическим аналогом, который обозначают как RC-529. Кроме того, можно применять такие адъюванты, как Stimulon (Cambridge Bioscience, Worcester, MA, USA), SAF-1 (Syntex) или бактериальные адъюванты на основе ДНК, такие как ISS (Dynavax) или CpG (Coley Pharmaceuticals), а также такие адъюванты, как комбинации между QS21 и 3-дез-O-ацетилированным монофосфориллипидом А (WO 94/001153) или MF-59 (Chiron), или адъюванты на основе поли[ди(карбоксилатофенокси)фосфазин]а (Virus Research Institute), или адъюванты на основе блок-сополимеров, такие как Optivax (Vaxcel, Cythx), или адъюванты на основе инулина, такие как Algammulin и Gammalnulin (Anutech), неполный адъювант Фрейнда (IFA) или препараты Gerbu (Gerbu Biotechnik), но не ограничиваются ими. Надо понимать, что полный адъювант Фрейнда (CFA) можно использовать для применений на субъектах, не являющихся людьми, а также для исследовательских целей. "Вакцинная композиция" может дополнительно содержать эксципиенты и разбавители, которые по своей сути являются нетоксичными и не терапевтическими, такие как вода, физиологический раствор, глицерин, этанол, увлажняющие и эмульгирующие агенты, вещества, забуферивающие рН, консерванты и тому подобное. В типичном случае вакцинную композицию готовят как инъецируемую в виде водного раствора или суспензии. Инъекция может быть подкожной, внутримышечной, внутривенной, внутрибрюшинной, внутриоболочечной, внутрикожной. Другие типы введения включают в себя имплантацию, суппозитории, пероральный прием внутрь, введение в тонкий кишечник, ингаляцию, аэрозоли или назальные спреи или капли. Также могут быть приготовлены твердые формы, пригодные для растворения или суспендирования в жидких носителях перед инъекцией. Эти препараты можно также эмульгировать или инкапсулировать в липосомы для усиления адъювантного эффекта. Полипептиды можно также включать в иммуностимулирующие комплексы вместе с сапонинами, например Quil A (ISCOMS). Вакцинные композиции содержат эффективное количество активного вещества, а также любой из вышеупомянутых компонентов. "Эффективное количество" активного вещества означает, что введение этого количества индивиду, как в виде разовой дозы, так и частью серии, эффективно для предотвращения или лечения заболевания или для индукции желаемого эффекта. Это количество варьирует в зависимости от здоровья и физического состояния индивида, подлежащего лечению, таксономической группы индивида, подлежащего лечению (например, человек, примат кроме человека, примат и т.д.), способности иммунной системы индивида давать эффективный иммунный ответ, желаемой степени защиты, препарата вакцины, оценки лечащим врачом, штамма инфекционного патогена и других уместных факторов. Предполагается, что это количество должно попасть в относительно широкий диапазон, который можно определить обычными испытаниями. Обычно это количество варьирует от 0,01 до 1000 мкг/дозу, более конкретно от 0,1 до 100 мкг/дозу. Режим дозирования может представлять собой схему разовых доз или схему множественных доз. Вакцину можно вводить в сочетании с другими иммунорегуляторными агентами.
Другой аспект данного изобретения относится к способу получения выделенного оболочечного белка HCV или его фрагмента согласно изобретению.
Указанный способ получения выделенного оболочечного белка HCV или его части включает в себя, например, трансформацию клетки-хозяина рекомбинантной нуклеиновой кислотой или вектором, содержащими открытую рамку считывания, которая кодирует указанный оболочечный белок HCV или часть этого белка, причем указанная клетка-хозяин способна экспрессировать указанный оболочечный белок HCV или его часть. Указанный способ может дополнительно включать в себя культивирование указанных клеток-хозяев в подходящей среде для того, чтобы осуществить экспрессию указанного белка и выделить экспрессируемый белок из культуры указанных клеток-хозяев или из указанных клеток-хозяев. Указанное выделение может включать в себя одно или более чем одно из следующего: (1) лизис указанных клеток-хозяев в присутствии агента, вызывающего диссоциацию комплексов, (2) химическая модификация цистеиновых тиольных групп в выделенных белках, причем указанная химическая модификация может быть обратимой или необратимой, и (3) аффинная хроматография с использованием гепарина.
Примерами "агентов, вызывающих диссоциацию комплексов" являются хлорид гуанидиния и мочевина. В общем, агент, вызывающий диссоциацию комплексов, представляет собой химический продукт, который может разрушать структуру водородных связей воды. В концентрированных растворах они могут денатурировать белки, поскольку они снижают гидрофобный эффект.
Под "рекомбинантной нуклеиновой кислотой" подразумевается нуклеиновая кислота природного или синтетического происхождения, которая была подвергнута по меньшей мере одной манипуляции техники рекомбинантных ДНК, такой как расщепление ферментом рестрикции, ПЦР (полимеразная цепная реакция), лигирование, дефосфорилирование, фосфорилирование, мутагенез, адаптация кодонов для экспрессии в гетерологичной клетке и т.д. В общем, рекомбинантная нуклеиновая кислота представляет собой фрагмент природной нуклеиновой кислоты или содержит по меньшей мере два фрагмента нуклеиновой кислоты, которые не связаны между собой в природе, или является полностью синтетической нуклеиновой кислотой.
Термины "полинуклеотид", "полинуклеиновая кислота", "последовательность нуклеиновой кислоты" "нуклеотидная последовательность", "молекула нуклеиновой кислоты", "олигонуклеотид", "зонд" или "праймер" при использовании здесь относятся к нуклеотидам, как рибонуклетидам, так и дезоксирибонуклеотидам, пептидным нуклеотидам или замкнутым нуклеотидам, или к их комбинации, в полимерной форме любой длины или любой формы (например, разветвленная ДНК). Указанные термины дополнительно включают в себя двунитевые (ds) и однонитевые (ss) полинуклеотиды, а также трехнитевые полинуклеотиды. Указанные термины также включают в себя известные модификации нуклеотидов, такие как метилирование, циклизация, и "кэпы", а также замены одного или более чем одного природного нуклеотида аналогом, таким как инозин, или неамплифицируемыми мономерами, таким как HEG (гексетиленгликоль). Рибонуклеотиды обозначаются как NTPs, дезоксирибонуклеотиды - как dNTPs, а дидезоксирибонуклеотиды - как ddNTPs.
Нуклеотиды, как правило, можно метить радиоактивными метками, хемилюминесцентным способом, флуоресцентным способом, фосфоресцентным способом или инфракрасными красителями, либо меткой усиленного поверхностью комбинационного рассеяния или плазмено-резонансной частицей (PRP, plasmon resonant particle).
Указанные термины "полинуклеотид", "полинуклеиновая кислота", "последовательность нуклеиновой кислоты", "нуклеотидная последовательность", "молекула нуклеиновой кислоты", "олигонуклеотид", "зонд" или "праймер" также охватывают пептидонуклеиновые кислоты (PNAs, peptide nucleic acids), которые представляют собой аналог ДНК, в котором скелет представляет собой псевдопептид, состоящий из N-(2-аминоэтил)-глициновых единиц вместо сахара. PNAs имитируют поведение ДНК и связывают комплиментарные нити нуклеиновой кислоты. Результатом нейтрального скелета PNA является более сильное связывание и более высокая специфичность, чем достигаемая нормальным путем. Кроме того, уникальные химические, физические и биологические свойства PNA были использованы для того, чтобы получать мощные биомолекулярные инструменты, антисмысловые и антигенные агенты, молекулярные зонды и биосенсоры. PNA-зонды обычно могут быть более короткими, чем ДНК-зонды и обычно имеют от 6 до 20 оснований в длину или, более оптимально, от 12 до 18 оснований в длину (Nielsen, P.E. 2001). Указанные термины далее охватывают замкнутые нуклеиновые кислоты (LNAs, locked nucleic acids), которые представляют собой производные РНК, в которых рибозное кольцо скреплено метиленовой связью между 2'-кислородом и 4'-углеродом. LNAs проявляют беспрецедентное сродство связывания с целевыми последовательностями ДНК или РНК. LNA нуклеотиды могут быть олигомеризованы и могут быть включены в химерные или миксомерные молекулы LNA/ДНК или LNA/PHK. Похоже, что LNA нетоксичны для культивируемых клеток (Orum, H. and Wengel, J. 2001, Wahlenstedt, С. et al., 2000). В общем, принимают в рассмотрение химеры или миксомеры любой ДНК, РНК, PNA или LNA, а также любые из них, в которых тимин заменен на урацил.
Из вышесказанного ясно, что настоящее изобретение также относится к применению кор-гликозилированных оболочечных белков HCV согласно изобретению или композиции согласно изобретению в изготовлении вакцинной HCV композиции. В частности, настоящее изобретение относится к применению кор-гликозилированного оболочечного белка HCV согласно изобретению для индукции иммунитета против HCV у хронических носителей HCV. Более конкретно, настоящее изобретение относится к применению определенного здесь кор-гликозилированного оболочечного белка HCV для индукции иммунитета против HCV у хронических носителей HCV до, одновременно или после любой другой терапии, такой как, например, хорошо известная интерфероновая терапия одна или в сочетании с введением малых лекарств для лечения HCV-инфекции, таких как, например, рибавирин. Такую композицию можно также применять до или после трансплантации печени или после предполагаемого инфицирования, такого как, например, травма иглой.
Другой аспект этого изобретения относится к способу обнаружения присутствия анти-HCV антител в образце, подозреваемом в том, что он содержит анти-HCV антитела, при котором:
(1) оболочечный белок HCV или его часть согласно изобретению приводят в контакт с указанным образцом в условиях, допускающих образование комплекса указанного оболочечного белка HCV или его части с указанными анти-HCV антителами,
(2) выявляют комплекс, образованный на стадии (1),
(3) из результатов стадии (2) делают вывод о присутствии указанных анти-HCV антител в указанном образце.
В конкретном воплощении стадия приведения в контакт (1) указанного способа осуществляется к конкурентных условиях. В другом конкретном воплощении указанного способа указанный оболочечный белок HCV или его часть присоединены к твердой подложке. В дополнительном воплощении указанный образец, подозреваемый в том, что он содержит анти-HCV антитела, является биологическим образцом.
Другой аспект этого изобретения относится к диагностическому набору для обнаружения присутствия анти-HCV антител в образце, подозреваемом в том, что он содержит анти-HCV антитела, содержащему оболочечный белок HCV или его часть согласно изобретению. В конкретном воплощении указанный оболочечный белок HCV или его часть присоединены к твердой подложке. В дополнительном воплощении указанный образец, подозреваемый в том, что он содержит анти-HCV антитела, является биологическим образцом.
Термин "биологический образец" при использовании здесь относится к образцу ткани или жидкости, выделенной из индивида, включая, например, сыворотку, плазму, лимфатическую жидкость, наружные отделы кожи, респираторный, кишечный или мочеполовой тракт, ооциты, слезы, слюну, молоко, клетки крови, опухоли, органы, продукты кишечной секреции, слизь, спинно-мозговую жидкость, наружные секреты, такие как, например, экскременты, моча, сперма и тому подобное, но не ограничиваясь ими.
Оболочечные белки HCV по настоящему изобретению или их части особенно подходят для включения в такие способы, как способы иммунного анализа, для обнаружения HCV и/или генотипирования HCV, для прогнозирования/мониторинга HCV заболевания, либо в качестве терапевтического агента.
Эти способы, такие как способы иммунного анализа, по настоящему изобретению задействуют оболочечные белки HCV по настоящему изобретению, которые сохраняют линейные (в случае пептидов) и конформационные эпитопы, распознаваемые антителами в сыворотках от HCV-инфицированных индивидов. Антигены Е1 и Е2 из HCV по настоящему изобретению можно применять практически в любом формате анализа, который использует известный антиген для обнаружения антител. Конечно, следует избегать или адаптировать формат, который денатурирует конформационный эпитоп HCV. Общим свойством всех этих анализов является то, что антиген приводят в контакт с компонентом организма, подозреваемым в том, что он содержит HCV антитела, в условиях, которые позволяют антигену связаться с любым таким антителом, присутствующим в этом компоненте. Такими условиями в типичном случае являются физиологическая температура, рН и ионная сила при использовании избытка антигена. За инкубацией этого антигена с пробой следует выявление иммунных комплексов, содержащих этот антиген.
Схемы иммунных анализов допускают широкое варьирование, и в данной области известно много форматов. Протоколы могут, например, использовать твердые подложки или иммунопреципитацию. Большинство анализов предусматривает применение меченого антитела или полипептида, причем метки могут быть, например, ферментными, флуоресцентными, хемилюминесцентными, радиоактивными, или представлять собой молекулы красителей. Известны также анализы, которые усиливают сигналы от иммунного комплекса, примерами каковых могут быть анализы, которые используют биотин и авидин или стрептавидин, и иммунные анализы с ферментами в качестве меток или медиаторов, такие как твердофазный иммуноферментный анализ (ELISA) и радиоиммуноанализ (RIA).
Иммунный анализ может быть, без ограничений, в гетерогенном или гомогенном формате и стандартного или конкурентного типа. В гетерогенном формате полипептид в типичном случае связан с твердой матрицей или подложкой для того, чтобы способствовать отделению образца от полипептида после инкубации. Примерами твердых подложек, которые можно применять, являются нитроцеллюлоза (например, в форме мембраны или лунки для микротитрования), поливинилхлорид (например, в форме листов или лунок для микротитрования), полистирольный латекс (например, в форме шариков или планшетов для микротитрования), поливинилидинфторид (известный как Immunolon™), диазотированная бумага, нейлоновые мембраны, активированные шарики и гранулы белка A (Protein А). Например, в гетерогенном формате можно применять планшеты для микротитрования Dynatech Immunolon™ 1 или Immunolon™ 2. Твердую подожку, содержащую антигенные полипептиды, в типичном случае промывают после отделения ее от анализируемого образца и перед выявлением связанных антител. В данной области известны как стандартный, так и конкурентный формат.
В гомогенном формате анализируемый образец инкубируют с комбинацией антигенов в растворе. Например, это может происходить в условиях, при которых будут преципитировать любые образовавшиеся комплексы антиген-антитело. В данной области известны как стандартный, так и конкурентный формат.
В стандартном формате количество антител, таких как анти-HCV-антитела, в комплексах антиген-антитело определяют прямым путем. Это можно осуществить путем определения того, будут ли меченые анти-ксеногенные (например, анти-человеческие) антитела, которые распознают эпитоп на указанных антителах, таких как анти-HCV антитела, связываться благодаря образованию комплекса. В конкурентном формате вывод о количестве указанных антител, таких как анти-HCV антитела, в образце делают на основании определения конкурентного эффекта в отношении связывания известного количества (меченого) антитела (или другого конкурирующего лиганда) или антигена в комплексе.
Комплексы антиген-антитело можно выявлять с помощью любой методики из числа известных в зависимости от формата. Например, немеченые антитела, такие как анти-HCV антитела, можно выявлять с использованием конъюгата анти-ксеногенного lg в комплексе с меткой (например, меткой, которая представляет собой фермент).
В формате анализа, представляющем собой иммунопреципитацию или агглютинацию, реакция между антигеном и антителом образует белковый кластер, который преципитирует из раствора или суспензии и образует видимый слой или пленку преципитата. Если в анализируемой пробе или образце нет антитела, преципитат не образуется.
Оболочечные белки HCV или их специфические части по настоящему изобретению, состоящие из конформационных эпитопов, в типичном случае должны быть упакованы в форме набора для применения в этих иммунных анализах. Этот набор в норме должен содержать в отдельных контейнерах нативный антиген HCV, препараты для контроля антител (позитивные и/или негативные), меченое антитело, когда этого требует формат анализа, реагенты, генерирующие сигнал (например, ферментный субстрат), если метка не генерирует сигнал непосредственно. Нативный антиген HCV может быть уже связан с твердой матрицей или отделен вместе с реагентами для его связывания с этой матрицей. В набор должны быть включены инструкции (например, письменные, на магнитофонной ленте, на CD-ROM и т.д.) по проведению анализа.
Выбранная твердая фаза может включать в себя полимерные или стеклянные шарики, нитроцеллюлозу, микрочастицы, микролунки реакционного планшета, пробирки для анализа или магнитные шарики. Вещество, генерирующее сигнал, может включать в себя фермент, люминесцентное соединение, хромоген, радиоактивный элемент и хемилюминесцентное соединение. Примеры ферментов включают в себя щелочные фосфатазы, пероксидазу хрена и бета-галактозидазу. Примеры соединений-усилителей включают в себя биотин, антибиотин и авидин. Примеры компонентов, связывающих соединения-усилители, включают в себя биотин, антибиотин и авидин. Для того чтобы блокировать эффекты субстанций, подобных ревматоидным факторам, анализируемый образец помещают в условия, обеспечивающие блокирование эффектов субстанций, подобных ревматоидным факторам. Эти условия включают в себя приведение анализируемого образца в контакт с некоторым количеством античеловеческого IgG для образования смеси и инкубацию этой смеси в течение некоторого времени в условиях, достаточных для образования продукта реакционной смеси, существенно свободного от субстанций, подобных ревматоидным факторам.
В частности, настоящее изобретение относится к применению оболочечного белка HCV или его части по настоящему изобретению для изготовления диагностического набора.
Поскольку кор-гликозилированные оболочечные белки HCV по настоящему изобретению высоко иммуногенны и стимулируют как гуморальный, так и клеточный иммунный ответ, то настоящее изобретение далее относится к набору для обнаружения связанного с HCV Т-клеточного ответа, содержащему олигомерные частицы или отдельный очищенный оболочечный белок HCV по данному изобретению. Т-клеточный ответ на HCV можно измерять, например, так, как описано Leroux-Roels et al. в WO 95/12677.
Дальнейший аспект этого изобретения относится к способу индуцирования HCV-специфичного иммунного ответа у млекопитающего, при котором указанному млекопитающему вводят эффективное количество оболочечного белка HCV или его части согласно изобретению, возможно содержащего фармацевтически приемлемый адъювант. Указанный способ, при котором указанному млекопитающему вводят эффективное количество оболочечного белка HCV или его части согласно изобретению, можно также применять для индукции HCV-специфичных антител у млекопитающего или для индукции специфичной Т-клеточной функции у млекопитающего. В указанных способах указанное введение может осуществляться для профилактических целей, то есть являться профилактическим введением, или для терапевтических целей, то есть являться терапевтическим введением.
Еще один аспект этого изобретения относится к способу иммунизации млекопитающего, при котором указанному млекопитающему вводят эффективное количество оболочечного белка HCV или его части согласно изобретению, возможно содержащего фармацевтически приемлемый адъювант.
Настоящее изобретение также относится к способу лечения млекопитающего, инфицированного HCV, при котором указанному млекопитающему вводят эффективное количество оболочечного белка HCV или его части согласно изобретению, возможно содержащего фармацевтически приемлемый адъювант.
Любые из вышеописанных аспектов этого изобретения или воплощений, специфичных для указанных аспектов, также применимы вообще к белкам, представляющим интерес, которые представляют собой продукт экспрессии в эукариотических клетках и которые дополнительно характеризуются теми же свойствами гликозилирования, какие описаны выше для двух разных оболочечных белков HCV.
Таким образом, более конкретно это изобретение относится к выделенному белку, представляющему интерес, или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он является продуктом экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что в среднем до 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79% и 80% сайтов N-гликозилирования являются кор-гликозилированными. Более конкретно, более чем 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% и 95% сайтов N-гликозилирования гликозилированы олигоманнозой со структурой, определяемой как Man(8-10)-GlcNAc(2). Более конкретно для любой из вышеуказанных особенностей N-гликозилирования, соотношение сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(7)-GlcNAc(2), и сайтов, кор-гликозилированных олигоманнозой, имеющей структуру Man(8)-GlcNAc(2), меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно для любой из вышеуказанных особенностей N-гликозилирования, указанные олигоманнозы содержат менее чем 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
Другой альтернативный аспект этого изобретения относится к выделенному белку, представляющему интерес, или его фрагменту, содержащему по меньшей мере один сайт N-гликозилирования, отличающемуся тем, что он является продуктом экспрессии в эукариотической клетке, и дополнительно отличающемуся тем, что сайты N-гликозилирования заняты олигоманнозами, причем соотношение олигоманноз, имеющих структуру Man(7)-GlcNAc(2), и олигоманноз, имеющих структуру Man(8)-GlcNAc(2), меньше или равно 0,15; 0,2; 0,25; 0,30; 0,35; 0,40; 0,44; 0,45 или 0,50. Еще более конкретно для любой из вышеуказанных особенностей N-гликозилирования, указанные олигоманнозы содержат менее 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6% или 5% концевой α1,3-маннозы.
В частности, указанный выделенный белок, представляющий интерес, или его фрагмент является продуктом эспрессии в дрожжевой клетке, такой как клетка Hansenula. Указанный выделенный белок, представляющий интерес, или его фрагмент может быть, например, вирусным оболочечным белком или его фрагментом, таким как оболочечный белок HCV или оболочечный белок HBV (вирус гепатита В), или их фрагмент. Другие служащие примерами вирусные оболочечные белки включают в себя оболочечный белок gp120 из HIV (вирус иммунодефицита человека) и вирусный оболочечный белок вируса, принадлежащего к Flavirideae. В общем, указанным выделенным белком, представляющим интерес, или его фрагментом может быть любой белок, требующий особенностей N-гликозилирования по настоящему изобретению.
Под "HCV-рекомбинантным вирусом коровьей оспы" подразумевается вирус коровьей оспы, содержащий последовательность нуклеиновой кислоты, кодирующую белок HCV или его часть.
Термины "частицы, подобные вирусу HCV, образованные оболочечным белком HCV" и "олигомерные частицы, образованные оболочечными белками HCV" определены здесь как структуры специфической природы и формы, содержащие несколько основных единиц оболочечных белков Е1 и/или Е2 из HCV, которые сами по себе считаются состоящими из одного или двух мономеров Е1 и/или Е2, соответственно. Должно быть ясно, что частицы по настоящему изобретению определены как лишенные инфекционных РНКовых геномов HCV. Частицы по настоящему изобретению могут быть частицами высшего порядка сферической природы, которые могут быть пустыми, состоящими из остова из оболочечных белков, в которые можно инкорпорировать липиды, детергенты, коровый белок HCV или молекулы адъюванта. Эти частицы могут быть также инкапсулированы липосомами или аполипопротеинами, таким как, например, аполипопротеин В или липопротеины низкой плотности, или любыми другими средствами нацеливания указанных частиц на конкретный орган или ткань. В этом случае такие пустые сферические частицы часто называют "вирусоподобными частицами" или VLPs (virus-like particles). Альтернативно, эти частицы высшего порядка могут быть твердыми сферическими структурами, в которых вся сфера, состоит из олигомеров оболочечных белков Е1 и Е2 из HCV, в которые можно дополнительно инкорпорировать липиды, детергенты, коровый белок HCV или молекулы адъюванта и которые в свою очередь сами могут быть инкапсулированы липосомами и/или аполипопротеинами, такими как, например, аполипопротеин В или липопротеины низкой плотности, или любыми другими средствами нацеливания указанных частиц на конкретный орган или ткань, например, асиалогликопротеинами. Эти частицы могут также состоять из более мелких структур (в сравнении с вышеуказанными пустыми или твердыми сферическими структурами), обычно круглой (см. дальше) формы, которые обычно не содержат более одного слоя оболочечных белков HCV. Типичным примером таких более мелких частиц являются розеткоподобные структуры, которые состоят из меньшего числа оболочечных белков HCV, обычно от 4 до 16. Специфический пример последних включает в себя более мелкие частицы, получаемые из белка Е1 в 0,2%-ном CHAPS как показано здесь в примере, которые, судя по всему, содержат 8-10 мономеров E1s. Такие розеткоподобные структуры обычно организованы в плоскости и имеют округлую форму, то есть, форму колеса. Опять же можно дополнительно инкорпорировать липиды, детергенты, коровый белок HCV или молекулы адъювантов, или же эти более мелкие частицы могут быть инкапсулированы липосомами или аполипопротеинами, такими как, например, аполипопротеин В или липопротеины низкой плотности, или любыми другими средствами нацеливания указанных частиц на конкретный орган или ткань. Более мелкие частицы могут также формировать мелкие сферические или глобулярные структуры, состоящие из сходного меньшего числа оболочечных белков Е1 или Е2 из HCV, в которые можно дополнительно инкорпорировать липиды, детергенты, коровый белок HCV или молекулы адъювантов, или же эти более мелкие частицы могут быть в свою очередь инкапсулированы липосомами или аполипопротеинами, такими как, например, аполипопротеин В или липопротеины низкой плотности, или любыми другими средствами нацеливания указанных частиц на конкретный орган или ткань. Размер (то есть диаметр) определенных выше частиц при измерении хорошо известной в данной области методикой динамического светорассеяния (см. дальше в. разделе Примеры) обычно составляет от 1 до 100 нм, более предпочтительно от 2 до 70 нм, даже еще более предпочтительно от 2 до 40 нм, от 3 до 20 нм, от 5 до 16 нм, от 7 до 14 нм или от 8 до 12 нм.
В частности, настоящее изобретение относится к способу очистки кор-гликозилированных оболочечных белков вируса гепатита С (HCV) или любой их части, подходящей для применения в иммуноанализе или вакцине, при котором:
(1) выращивают неспособные к гликозилированию штаммы Hansenula или Saccharomyces, трансформированные оболочечным геном, кодирующим белок HCV E1 и/или HCV E2 или любую их часть, в подходящей культуральной среде;
(2) вызывают экспрессию указанного гена, кодирующего HCV E1 и/или HCV E2 или любую их часть, и
(3) очищают указанный кор-гликозилированный белок HCV E1 и/или HCV E2 или любую их часть из указанной культуры клеток.
Это изобретение далее относится к способу очистки кор-гликозилированных оболочечных белков вируса гепатита С (HCV) или любой их части, подходящей для применения в иммуноанализе или вакцине, при котором:
(1) выращивают неспособные к гликозилированию штаммы Hansenula или Saccharomyces, трансформированные оболочечным геном, кодирующим белок HCV E1 и/или HCV E2 или любую их часть, в подходящей культуральной среде;
(2) вызывают экспрессию указанного гена, кодирующего HCV E1 и/или HCV E2 или любую их часть, и
(3) очищают указанный экспрессируемый внутриклеточно кор-гликозилированный белок HCV E1 и/или HCV E2 или любую их часть при лизировании трансформированной клетки-хозяина.
Это изобретение далее относится к способу очистки кор-гликозилированных оболочечных белков вируса гепатита С (HCV) или любой их части, подходящих для применения в иммуноанализе или вакцине, при котором:
(1) выращивают неспособные к гликозилированию штаммы Hansenula или Saccharomyces, трансформированные оболочечным геном, кодирующим белок HCV E1 и/или HCV E2 или любую их часть, в подходящей культуральной среде, причем указанный белок HCV E1 и/или HCV E2 или любая их часть содержит по меньшей мере две Cys-аминокислоты;
(2) вызывают экспрессию указанного гена, кодирующего HCV E1 и/или HCV E2 или любую их часть, и
(3) очищают указанный кор-гликозилированный белок HCV E1 и/или HCV E2 или любую их часть, в которых указанные Cys-аминокислоты обратимо защищены химическими и/или ферментативными средствами, из указанной культуры.
Это изобретение далее относится к способу очистки кор-гликозилированных оболочечных белков вируса гепатита С (HCV) или любой их части, подходящей для применения в иммуноанализе или вакцине, при котором:
(1) выращивают неспособные к гликозилированию штаммы Hansenuta или Saccharomyces, трансформированные оболочечным геном, кодирующим белок HCV E1 и/или HCV E2 или любую их часть, в подходящей культуральной среде, причем указанный белок HCV E1 и/или HCV Е2 или любая их часть содержит по меньшей мере две Cys-аминокислоты;
(2) вызывают экспрессию указанного гена, кодирующего HCV E1 и/или HCV E2 или любую их часть, и
(3) очищают указанный экспрессируемый внутриклеточно кор-гликозилированный белок HCV E1 и/или HCV E2 или любую их часть при лизировании трансфомированной клетки-хозяина, причем указанные Cys-аминокислоты обратимо защищены химическими и/или ферментативными средствами.
Настоящее изобретение специфически относится к способу очистки рекомбинантных кор-гликозилированных дрожжевых белков HCV или любой их части, как описано здесь, при котором указанная очистка включает в себя аффинную хроматографию с гепарином.
Следовательно, настоящее изобретение относится к способу очистки рекомбинантных кор-гликозилированных дрожжевых белков HCV или любой их части, как описано здесь, при котором указанным химическим средством является сульфонирование.
Следовательно, настоящее изобретение также относится к способу очистки рекомбинантных кор-гликозилированных дрожжевых белков HCV или любой их части, как описано здесь, при котором указанную обратимую защиту Cys-аминокислот заменяют на необратимую защиту химическими и/или ферментативными средствами.
Следовательно, настоящее изобретение также относится к способу очистки рекомбинантных кор-гликозилированных дрожжевых белков HCV или любой их части, как описано здесь, при котором указанная защита химическим средством представляет собой йодацетамид.
Следовательно, настоящее изобретение относится также к способу очистки рекомбинантных кор-гликозилированных дрожжевых белков HCV или любой их части, как описано здесь, при котором указанная необратимая защита химическими средствами представляет собой NEM или биотин-NEM или их смесь.
Настоящее изобретение относится также к композиции, как определено выше, которая также содержит HCV кор, Е1, Е2, Р7, NS2, NS3, NS4A, NS4B, NS5A и/или NS5B белок или их части. Кор-гликозилированные белки Е1, Е2 и/или Е1/Е2 по настоящему изобретению можно, например, комбинировать с другими антигенами HCV, такими как, например, кор, Р7, NS3, NS4A, NS4B, NS5A и/или NS5B. Очистка этих белков NS3 должна предпочтительно включать в себя обратимую модификацию цистеиновых остатков и даже более предпочтительно сульфонирование цистеинов. Способы осуществления такой обратимой модификации, включая сульфонирование, были описаны для белков NS3 в Maertens et al. (PCT/EP99/02547). Следует подчеркнуть, что все содержание последнего документа, включающее в себя все определения, включено в настоящую заявку ссылкой.
Также настоящее изобретение относится к применению описанного здесь кор-гликозилированного оболочечного белка для индуции иммунитета против вируса HCV, отличающемуся тем, что указанный кор-гликозилированный оболочечный белок применяют как часть серии времени и соединений. В этом отношении следует понимать, что термин "серия времени и соединений" относится к введению индивиду соединений, которые применяют для элисирования иммунного ответа, через определенные интервалы времени. Эти соединения могут включать в себя любой из следующих компонентов: кор-гликозилированный оболочечный белок, HCV ДНК вакцинную композицию, полипептиды HCV. В этом смысле серия включает в себя любое введение из числа следующих:
(1) антиген HCV, такой как, например, кор-гликозилированный оболочечный белок, через определенные интервалы времени;
(2) антиген HCV, такой как, например, кор-гликозилированный оболочечный белок, в комбинации с HCV ДНК вакцинной композицией, причем указанные олигомерные частицы кор-гликозилированного оболочечного белка и указанную HCV ДНК вакцинную композицию можно водить одновременно или через разные интервалы времени, в том числе переменные интервалы времени; или
(3) (1) или (2), возможно в комбинации с другими HCV пептидами, через определенные интервалы времени.
В этом отношении должно быть ясно, что HCV ДНК вакцинная композиция содержит нуклеиновые кислоты, кодирующие оболочечный пептид HCV, включая пептиды Е1, Е2, Е1/Е2, пептид NS3, другие пептиды HCV или части указанных пептидов. Более того, надо понимать, что указанные пептиды HCV включают в себя оболочечные пептиды HCV, в том числе пептиды Е1, Е2, Е1/Е2, другие пептиды HCV или их части. Термин "другие пептиды HCV" относится к любому пептиду HCV или его фрагменту. В пункте (1) вышеприведенной схемы HCV ДНК вакцинная композиция содержит предпочтительно нуклеиновые кислоты, кодирующие оболочечные пептиды HCV. В пункте (2) вышеприведенной схемы HCV ДНК вакцинная композиция состоит еще более предпочтительно из нуклеиновых кислот, кодирующих оболочечные пептиды HCV, возможно в комбинации с HCV NS3 ДНК вакцинной композицией. В этом отношении должно быть ясно, что HCV ДНК вакцинная композиция содержит плазмидный вектор, содержащий полинуклеотидную последовательность, кодирующую пептид HCV, как описано выше, функциональным образом соединенную с элементами регуляции транскрипции. При использовании здесь "плазмидный вектор" относится к молекуле нуклеиновой кислоты, способной транспортировать другую нуклеиновую кислоту, с которой она соединена. Предпочтительными векторами являются те, которые способны к автономной репликации и/или экспрессии нуклеиновых кислот, с которыми они соединены. В целом плазмидные векторы представляют собой кольцевые двунитевые ДНК-вые петли, которые в их векторной форме не связаны с хромосомой, но не ограничиваются этим. При использовании здесь "полинукпеотидная последовательность" относится к полинуклеотидам, таким как дезоксирибонуклеиновая кислота (ДНК) и, если уместно, рибонуклеиновая кислота (РНК). Этот термин следует понимать как включающий в себя в качестве эквивалентов аналоги РНК или ДНК, полученные из аналогов нуклеотидов, и одно-(смысловые и антисмысловые) и двунитевые полинуклеотиды. При использовании здесь термин "элемент регуляции транскрипции" относится к нуклеотидной последовательности, которая содержит необходимые регуляторные элементы так, что при введении в живую клетку позвоночного способны направлять клеточные механизмы на продуцирование продуктов трансляции, кодируемых этим полинуклеотидом. Термин "функциональным образом" относится к непосредственному соединению, где все компоненты сконфигурированы так, чтобы выполнять их обычную функцию. Таким образом, элементы регуляции транскрипции, функциональным образом присоединенные к нукпеотидной последовательности, способны запускать экспрессию указанной нуклеотидной последовательности.
Специалисты могут понять, что с успехом можно применять разные транскрипционные промоторы, терминаторы, векторы-носители или специфические генные последовательности.
Альтернативно ДНК вакцину можно доставлять с помощью живого вектора, такого как аденовирус, поксвирус канареек, MVA и тому подобное.
Настоящее изобретение проиллюстрировано Примерами, изложенными ниже. Эти примеры являются всего лишь иллюстративными, и нельзя считать, что они как-либо ограничивают или лимитируют это изобретение.
ПРИМЕРЫ
ПРИМЕР 1
КОНСТРУИРОВАНИЕ ЧЕЛНОЧНОГО ВЕКТОРА pFPMT-MFα-E1-Н6
Конструировали плазмиды для трансформации Hasenula polymorpha следующим образом. Челночный вектор pFPMT-MFα-E1-H6 конструировали в многостадийной процедуре. Исходно клонировали последовательность нуклеиновой кислоты, кодирующую белок HCV E1s (SEQ ID NO:2) вслед за лидерной последовательностью СНН (СНН=гипергликемический гормон из Carcinus maenas), которую затем заменяли на лидерную последовательность MFα (MFα=α-фактор спаривания Saccharomyces cerevisiae).
Сначала методом «бесшовного» клонирования (Pargett, K.A. and Sorge, J.A. 1996) конструировали производное плазмиды pUC18, несущее блок СНН-Е1-Н6 в виде EcoR1/BamH1-фрагмента. Для этого посредством ПЦР как описано ниже получали фрагмент ДНК, кодирующий E1s-H6, и акцепторную плазмиду, производную от плазмиды pCHH-Hir.
Получение фрагмента ДНК, кодирующего E1s-H6
Фрагмент ДНК, кодирующий Е1-Н6 (кодирующий белок E1s из HCV типа 1b, состоящий из аминокислот 192-326 из E1s и удлиненный шестью His-остатками; SEQ ID NO:5) выделяли способом ПЦР из плазмиды pGEMTE1sH6 (SEQ ID NO:6, Фиг.1). Для этого использовали следующие праймеры:
-CHHE1-F:
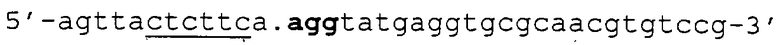
(SEQ ID NO:7);
Eam1104I сайт подчеркнут, точка означает сайт расщепления. Основания, напечатанные жирным шрифтом, комплементарны основаниям праймера CHH-links. Неотмеченные основания гибридизуются в пределах стартового участка Е1 (192-326) в смысловом направлении; и
- CHHE1-R:
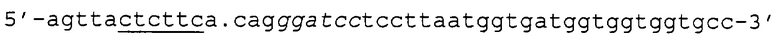
(SEQ ID NO:8);
Eam1104I сайт подчеркнут, точка означает сайт расщепления. Основания, напечатанные жирным шрифтом, комплементарны основаниям праймера MF30-rechts. Основания, образующие BаmН1 сайт, полезный для последующей процедуры клонирования, выделены курсивом. Неотмеченные основания гибридизуются в антисмысловом направлении в пределах конца блока Е1-Н6, который включат в себя стоп-кодон и три дополнительных основания между стоп-кодоном и SamH1 сайтом.
Реакционную смесь составляли следующим образом: общий объем 50 мкл, содержащий 20 нг Eco31I-линеаризованной pGEMTE1sH6, по 0,2 мкМ каждого из праймеров CHHE1-F и CHHE1-R, по 0,2 мкМ каждого из dNTP's, однократный буфер 2 (Expand Long Template PCR System, Boehringer, Cat No 1681 834), 2,5 ед. полимеразной смеси (Expand Long Template PCR System, Boehringer, Cat No 1681 834).
Использовали программу 1, причем указанная программа состоит из следующих этапов:
1. денатурация: 5 мин при 95°С;
2. 10 циклов по 30 сек денатурации при 95°С, 30 сек отжига при 65°С и 130 сек элонгации при 68°С;
3. терминация при 4°С.
Затем к образцу, полученному в программе 1, добавляли 5 мл 10× буфера 2 (Expand Long Template PCR System, Boehringer, Cat No 1681 834), 40 мкл H2O и 5 мкл [dATP, dGTP и dTTP (по 2 мМ каждого); 10 мМ 5-метил-dCTP] и проводили дальнейшую амплификацию по программе 2, состоящей из следующих этапов:
1. денатурация: 5 мин при 95°С;
2. 5 циклов по 45 сек денатурации при 95°С, 30 сек отжига при 65°С и 130 сек при 68°С;
3. терминация при 4°С.
Получение акцепторной плазмиды, производной от pCHH-Hir
Акцепторный фрагмент был получен посредством ПЦР из плазмиды pCHH-Hir (SEQ ID NO:9; Фиг.2) и состоял почти полностью из плазмиды pCHH-Hir за исключением того, что в этом продукте ПЦР не присутствует последовательность, кодирующая Hir. Для этой ПЦР использовали следующие праймеры:
1. CHH-links:
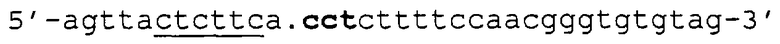
(SEQ ID NO:10)
Eam1104I сайт подчеркнут, точка обозначает сайт расщепления. Основания, напечатанные жирным шрифтом, комплементарны основаниям праймера CHHE1-F. Неотмеченные основания гибридизуются в пределах конца последовательности СНН в антисмысловом направлении; и
2. MF30-rechts:
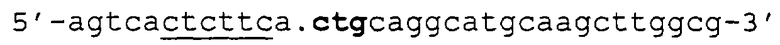
(SEQ ID NO:11)
Eam1104I сайт подчеркнут, точка обозначает сайт расщепления. Основания, напечатанные жирным шрифтом, комплементарны основаниям праймера CHHE1-R. Неотмеченные основания гибридизуются в пределах последовательностей pUC18 за клонированной CHH-Hirudin HL20 плазмиды pCHH-Hir в направлении от вставки.
Реакционную смесь составляли следующим образом: общий объем 50 мкл, содержащий 20 нг Asр718I-линеаризованной pCHH-Hir, по 0,2 мкМ каждого из праймеров, CHH-links и MF30-rechts, по 0,2 мкМ каждого из dNTP's, 1× буфер 2 (Expand Long Template PCR System, Boehringer, Cat No 1681 834), 2,5 ед. полимеразной смеси (Expand Long Template PCR System, Boehringer, Cat No 1681 834).
Использовали программу 1, как описано выше.
Затем к образцу, полученному в программе 1, добавляли 5 мкл 10× буфера 2 (Expand Long Template PCR System, Boehringer, Cat No 1681 834), 40 мкл Н2O и 5 мкл [dATP, dGTP и dTTP (no 2 мМ каждого); 10 мМ 5-метил-dCTP] и проводили дальнейшую амплификацию по программе 2, как описано выше.
Получение вектора рСННЕ1
Фрагмент ДНК, кодирующий E1s-H6, и акцепторную плазмиду, полученную из pCHH-Hir способом ПЦР как описано выше, очищали с использованием набора для очистки продуктов ПЦР (Qiagen) в соответствии со спецификациями поставщика. Затем расщепляли очищенные фрагменты по отдельности рестриктазой Еаm1104I. Затем фрагмент ДНК E1s-H6 лигировали в акцепторную плазмиду, полученную из pCHH-Hir, используя лигазу Т4 (Boehringer) в соответствии со спецификациями поставщика.
Смесью, полученной после лигирования, трансформировали клетки Е.coli XL-Gold и анализировали плазмидную ДНК нескольких устойчивых к ампициллину колоний путем обработки рестриктазами EcoR1 и BamH1. Выбирали позитивный клон и обозначали его как рСННЕ1.
Получение вектора pFPMT-CHH-E1H6
EcoR1/BamH1-фрагмент из рСННЕ1 лигировали с вектором pFPMT121 (SEQ ID NO:12; Фиг.3), обработанным рестриктазами EcoR1 и BamH1. Использовали лигазу Т4 (Boehringer) в соответствии с инструкциями поставщика. Смесь, полученную после лигирования, использовали для трансформации клеток Е.coli DH5αF'. Анализировали несколько трансформантов по рестрикционному паттерну плазмидной ДНК и оставляли позитивный клон, который обозначали как pFPMT-CHH-E1H6 (SEQ ID NO:13; Фиг.4).
Получение pFPMT-MFα-E1-H6
Наконец, получали челночный вектор pFPMT-MFα-E1-H6 лигированием трех фрагментов, представлявших собой:
1. 6,961 т.н. фрагмент pFPMT121, обработанный EcoR1/BamH1 (SEQ ID NO:12; Фиг.3),
2. 0,245 т.н. EcoR1/HindIII-фрагмент pUC18-MFa (SEQ ID NO:62; Фиг.36) и
3. 0,442 т.н. HindIII/BamH1-фрагмент 0,454 т.н. продукта ПЦР, полученный из pFPMT-CHH-E1H6.
0,454 т.н. продукт ПЦР, дающий фрагмент №3, получали посредством ПЦР, используя следующие праймеры:
1. праймер MFα-E1 f-Hi:
5'-aggggtaagcttggataaaaggtatgaggtgcgcaacgtgtccgggatgt-3'
(SEQ ID NO:14)
2. праймер Е1 back-Bam:
5'-agttacggatccttaatggtgatggtggtggtgccagttcat-3'
(SEQ ID NO:15).
Реакционную смесь составляли следующим образом: объем реакционной смеси 50 мкл, pFPMT-CHH-E1-H6 (EcoR1-линеаризованная; 15 нг/мкл), 0,5 мкл; праймер MFa-E1 f-Hi (50 мкМ), 0,25 мкл; праймер Е1 back-Barn (50 мкМ), 0,25 мкл; dNTP's (все по 2 мМ), 5 мкл; ДМСО (диметилсульфоксид), 5 мкл; Н2O, 33,5 мкл; Буфер 2 (сконцентрированный 10×) набора Expand Long Template PCR System (Boehringer Mannheim; Cat. No 1681 834), 5 мкл; полимеразная смесь Expand Long Template PCR System (1 ед./мкл), 0,5 мкл.
Применяли программу ПЦР, состоящую из следующих этапов:
1. денатурация: 5 мин при 95°С,
2. 29 циклов по 45 сек денатурации при 95°С, 45 сек отжига при 55°С и 40 сек элонгации при 68°С,
3. терминация при 4°С,
На основании использованных праймеров, полученный 0,454 т.н. продукт ПЦР, содержал кодоны Е1 (192-326), за которыми следовали шесть кодонов гистидина и стоп-кодон "taa", фланкированные «вверх по течению» 22 3'-терминальными парами оснований пре-про-последовательности MFα (включая существенный для клонирования HindIII сайт плюс избыточные шесть пар оснований) и фланкированные «вниз по течению» (существенный для клонирования) BamHI сайтом и избыточными шестью парами оснований.
Для реакции лигирования применяли ДНК-лигазу Т4 (Boehringer Mannheim) в соответствии с условиями поставщика (объем образца 20 мкл).
Смесью, полученной после лигирования, трансформировали клетки Е.coli HB101 и оставляли позитивные клоны после рестрикционного анализа плазмид, выделенных из нескольких трансформантов. Отбирали позитивную плазмиду и обозначали как pFPMT-MFα-E1-E6 (SEQ ID NO:16; Фиг.5).
ПРИМЕР 2
КОНСТРУИРОВАНИЕ ЧЕЛНОЧНОГО ВЕКТОРА pFPMT-CL-E1-H6
Плазмиды для трансформации Hansesula polymorpha конструировали следующим образом. Челночный вектор pFPMT-CL-E1-H6 конструировали в три этапа, начиная с pFPMT-MFα-E1-H6 (SEQ ID NO:16; Фиг.5).
На первом этапе рамку считывания MFα-E1-H6 плазмиды pFPMT-MFα-E1-Н6 субклонировали в вектор pUC18. Для этого 1,798 т.н. Sa/I/BamH1 фрагмент плазмиды pFPMT-MFα-E1-H6 (содержащий промотор FMD плюс MFα-E1-H6) лигировали с Sa/I/BamH1 векторным фрагментом плазмиды pUC18 с помощью лигазы Т4 (Boehringer) в соответствии со спецификациями поставщика. Результатом этого была плазмида, которая изображена на Фиг.6 (SEQ ID NO:17) и далее обозначена как рМа12-1 (pUC18-FMD-MFα-E1-H6). Смесь, полученную при лигировании, использовали для трансформации клеток Е.coli DH5αF'. Отбирали несколько устойчивых к ампициллину колоний и анализировали расщеплением плазмидной ДНК, выделенной из отобранных клонов, ферментами рестрикции. Позитивный клон анализировали далее определением последовательности ДНК в последовательности, кодирующей MFα-E1-H6. Корректный клон использовали для ПЦР направленного мутагенеза для замены пре-про-последовательности MFα кодонами пре-последовательности птичьего лизоцима ("CL", что соответствует аминокислотам 1-18 птичьего лизоцима; SEQ ID NO:1). Принцип примененного ПЦР-направленного мутагенеза основан на амплификации всей плазмиды с желательными изменениями, локализованными на 5'-концах праймеров. На последующих этапах модифицируют концы линейного ПЦР продукта перед самолигированием, приводящим к желаемой измененной плазмиде.
Для реакции ПЦР использовали следующие праймеры:
1. праймер CL hin:
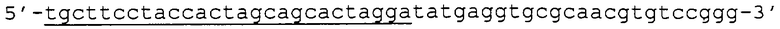
(SEQ ID NO:18);
2. праймер CL her neu:
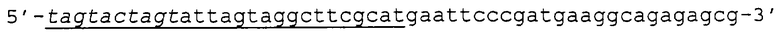
(SEQ ID NO:19).
Подчеркнутые 5'-участки праймеров содержат кодоны, соответствующие приблизительно половине пре-последовательности птичьего лизоцима. Праймер CL her neu включает в себя рестрикционный сайт для SpeI (курсив). Неподчеркнутые участки праймеров гибридизуются с кодонами для аминокислотных остатков 192-199 из Е1 (CL hin) или со стартовым кодоном "atg" над EcoR1 сайтом вплоть до положения -19 (считая от EcoR1 сайта) промотора FMD. Эти праймеры предназначены для амплификации полной рМа12-1, посредством чего заменяют кодоны пре-про-последовательности MFα кодонами пре-последовательности птичьего лизоцима.
Реакционную смесь составляли следующим образом: pUC18-FMD-Mfα-Е1-Н6 (рМа12-1; 1,3 нг/мкл), 1 мкл; праймер CL hin (100 мкМ), 2 мкл; праймер CL her neu (100 мкМ), 2 мкл; dNTP's (все по 2,5 мМ), 8 мкл; H2O, 76 мкл; буфер 2 (сконцентрированный 10×) Expand Long Template PCR System (Boehringer; Cat. No 1681834), 10 мкл; полимеразная смесь Expand Long Template PCR System (1 ед./мкл), 0,75 мкл.
Применяли программу ПЦР, состоящую из следующих этапов:
1. денатурация: 15 мин при 95°С
2. 35 циклов по 30 сек денатурации при 95°С, 1 мин отжига при 60°С и 1 мин элонгации при 72°С
3. терминация при 4°С.
Полученный ПЦР продукт проверяли на правильность размера электрофорезом в агарозном геле (3,5 тысяч нуклеотидов (т.н.)). После этого из продукта ПЦР удаляли 3'-А избыточности Т4-полимеразной реакцией, приводящей к тупым концам с 3'- и 5'-ОН-группами. Для этого ПЦР продукт обрабатывали полимеразой Т4 (Boehringer; 1 ед./мкл): к оставшимся 95 мкл реакционной смеси ПЦР добавляли 1 мкл полимеразы Т4 и 4 мкл dNTP's (все по 2,5 мМ). Образец инкубировали в течение 20 мин при 37°С. Затем ДНК осаждали этанолом и собирали в 16 мкл Н2O.
Затем киназной реакцией к ПЦР продукту с тупыми концами добавляли 5'-фосфаты. Для этого к 16 мкл ПЦР продукта с тупыми концами добавляли 1 мкл полинуклеотидкиназы Т4 (Boehringer, 1 ед./мкл), 2 мкл концентрированного в 10 раз буфера для Т4-полинукпеотидкиназной реакции (Boehringer) и 1 мкл АТР (10 мМ). Образец инкубировали в течение 30 мин при 37°С.
Затем ДНК наносили на 1%-ный агарозный гель и выделяли полосу корректного продукта с помощью набора для гелевой экстракции (Qiagen) в соответствии с условиями поставщика. Затем пятьдесят (50) нг очищенного продукта подвергали самолигированию с применением лигазы Т4 (Boehringer) в соответствии с условиями поставщика. После 72 ч инкубации при 16°С ДНК в смеси для лигирования осаждали этанолом и растворяли в 20 мкл воды.
Затем трансформировали клетки Е.coli DH5α-F' десятью микролитрами образца после лигирования. Плазмидную ДНК нескольких клонов, устойчивых к ампициллину, проверяли путем расщепления ферментами рестрикции. Отбирали позитивный клон и обозначали его как p27d-3 (pUC18-FMD-CL-E1-H6, SEQ ID NO:20, Фиг.7). Затем проверяли рамку считывания CL-E1-H6 секвенированием ДНК.
На последнем этапе конструировали челночный вектор pFPMT-CL-E1-H6 как описано ниже. 0,486 т.н. EcoR1/BamH1-фрагмент плазмиды p27d-3 (содержащий CL-E1(192-326)-H6) лигировали с EcoRI/fiamHt-обработанной плазмидой pFPMT121 (SEQ ID NO:12, Фиг.3). Для этой реакции использовали лигазу Т4 (Boehringer) в соответствии с рекомендациями поставщика. ДНК в образце для лигирования осаждали этанолом и растворяли в 10 мкл Н2O. Трансформировали клетки Е.coli DH5αF' десятью микролитрами образца после лигирования и анализировали ДНК нескольких клонов, устойчивых к ампициллину, обраработкой рестриктазами EcoR1 и ВаmН1. Плазмидный клон р37-5 (pFPMT-CL-E1-H6; SEQ ID NO:21, Фиг.8) демонстрировал желаемые размеры фрагментов, а именно, 0,486 т.н. и 6,961 т.н. Корректную последовательность CL-E1-H6 из р37-5 подтверждали секвенированием.
ПРИМЕР 3
КОНСТРУИРОВАНИЕ ЧЕЛНОЧНЫХ ВЕКТОРОВ
pFPMT-MFα-E2-H6 и pMPT-MFα-E2-H6
Плазмиды для трансформации Hansenula polymorpha конструировали следующим образом. Последовательность ДНК, кодирующую MFα-E2s (аминокислоты 384-673 HCV E2)-VIEGR-His6 (SEQ ID NO:5), выделяли в виде 1,331 т.н. EcoR1/Bg/II-фрагмента из плазмиды pSP72E2H6 (SEQ ID NO:22; Фиг.9). Этот фрагмент лигировали с подвергнутыми рестрикции посредством EcoR1/Bg/II векторами pFPMT121 (SEQ ID NO:12, Фиг.С+2) или рМРТ121 (SEQ ID NO:23; Фиг.10), используя ДНК-лигазу Т4 (Boehringer Mannheim) в соответствии с рекомендациями поставщика. После трансформации Е.coli и проверки плазмидной ДНК, выделенной из разных трансформантов, путем обработки ферментами рестрикции сохраняли позитивные клоны и обозначали полученные челночные векторы как pFPMT-MFα-Н6 (SEQ ID NO:22, Фиг.11) и pMPT-MFα-E2-H6 (SEQ ID NO:23, Фиг.12), соответственно.
ПРИМЕР 4
КОНСТРУИРОВАНИЕ ЧЕЛНОЧНОГО ВЕКТОРА pFPMT-CL-E2-H6
Челночный вектор pFPMT-CL-E2-H6 собирали в трехэтапной процедуре. Готовили промежуточный конструкт, в котором последовательность, кодирующую белок Е2, клонировали вслед за сигнальной последовательностью α-амилазы из Schwanniomyces accidentalis. Это осуществляли способом «бесшовного» клонирования (Padgett, K.A. and Sorge, J.A. 1996).
Получение фрагмента ДНК, кодирующего E2s-H6
Сначала амплифицировали последовательность ДНК, кодирующую Е2-Н6 (аминокислоты 384-673 из HCV E2, удлиненные линкерным пептидом "VEIGR" и шестью остатками His, SEQ ID NO:5) из плазмиды pSP72E2H6 (SEQ ID NO:24, Фиг.11) посредством ПЦР. Использованные праймеры обозначены как MF30E2/F и MF30E2/R и имеют следующие последовательности:
- праймер MF30E2/F:
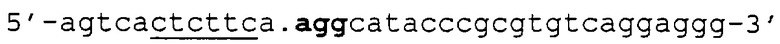
(SEQ ID NO:26);
сайт Eam1104I подчеркнут, точка обозначает сайт расщепления этим ферементом, последний кодон сигнальной последовательности из S.occidentalis напечатан жирным шрифтом, непомеченные основания гибридизуются с кодонами Е2 (аминокислоты 384-390 HCV E2);
- праймер MF30E2/R:
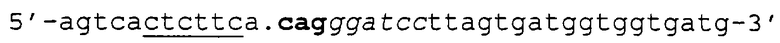
(SEQ ID NO:27);
сайт Eam1104I подчеркнут; точка обозначает сайт расщепления этим ферментом; основания, напечатанные жирным шрифтом, комплементарны основаниям праймера MF30-Rrechts (см. ниже), напечатанным жирным шрифтом; сайт BamHI, подлежащая введению в конструкт, напечатана курсивом; непомеченная последовательность гибридизуется со стоп-кодоном и шестью концевыми His кодонами E2 (384-673)-VIEGR-H6 (SEQ ID NO:5).
Реакционную смесь составляли следующим образом: общий объем 50 мкл, содержащий 20 нг 1,33 т.н. EcoR1/Bg/II-фрагмента из pSP72E2H6, по 2 мкМ праймеров MF30E2/F и MF30E2/R, dNTP's (каждого по 2 мкМ), 1× буфер 2 (Expand Long Template PCR System, Boehringer, Cat. No 1681834), 2,5 ед. полимеразной смеси (Expand Long Template PCR System, Boehringer, Cat. No 1681834)
Для ПЦР применяли программу 3, состоящую из следующих этапов:
1. денатурация: 5 мин при 95°С;
2. 10 циклов по 30 сек денатурации при 95°С, 30 сек отжига при 65°С и 1 мин элонгации при 68°С
3. терминация при 4°С.
Затем к образцу, произведенному в программе 3 для ПЦР, добавляли 10 мкл 10× буфера 2 (Expand Long Template PCR System, Boehringer, Cat. No 1681834), 40 мкл Н2O и 5 мкл [dATP, dGTP и dTTP (каждого по 2 мМ), 10 мМ 5-метил-dCTP], и продолжали по программе 4 для ПЦР, состоящей из следующих этапов:
1. денатурация 5 мин при 95°С
2. 5 циклов по 45 сек денатурации при 95°С, 30 сек отжига при 65°С и 1 мин элонгации при 68°С.
3. терминация при 4°С.
Получение акцепторной плазмиды, производной от pMF30
Второй фрагмент происходил из плазмиды pMF30 (SEQ ID NO:28, Фиг.13); ампликон почти полностью представлял собой плазмиду pMF30 за исключением кодонов зрелой α-амилазы из S.occidentalis; модификации, нужные для клонирования, были введены путем соответствующих праймеров. Применяли следующие наборы праймеров:
- праймер MF30-Links:
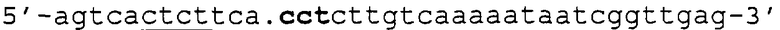
(SEQ ID NO:29; сайт Eam1104I подчеркнут; точка обозначает сайт расщепления этим ферментом; "cct", напечатанные жирным шрифтом, комплементарны напечатанным жирным шрифтом "agg" праймера MF30E2/F (см. выше); непомеченные основания и напечатанные жирным шрифтом гибридизуются с 26-ю концевыми основаниями кодонов α-амилазы из S.accidentalis в pMF30);
- праймер MF30-Rechts:
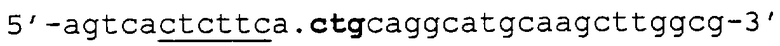
(SEQ ID NO:11; сайт Eam1104I подчеркнут; точка обозначает сайт расщепления этим ферментом; "ctg", напечатанные жирным шрифтом, комплементарны напечатанным жирным шрифтом "cag" праймера MF30E2/R (см. выше); непомеченные основания гибридизуются с последовательностями плазмиды pUC18 «вниз по течению» от стоп-кодона α-амилазы из S.occidentalis в pMF30).
Реакционную смесь составляли следующим образом: общий объем 50 мкл, содержащий 20 нг Bg/II-линеаризованной pMF30, по 0,2 мкМ каждого из праймеров MF30-Links и MF30-Rechts, dNTP's (по 0,2 мкМ каждого), 1× буфер 1 (Expand Long Template PCR System, Boehringer, Cat. No 1681834), 2,5 ед. полимеразной смеси (Expand Long Template PCR System, Boehringer, Cat. No 1681834). Применяли те же программы ПЦР (программы 3 и 4), какие были описаны выше, за исключением того, что в обеих программах периоды элонгации были продлены от 1 мин до 4 мин.
Получение вектора pAMY-E2
Фрагмент ДНК, кодирующий белок E2s-H6, и акцепторную-плазмиду, производную от pMF30, которую получали способом ПЦР, контролировали по их соответствующим размерам электрофорезом в 1%-ном агарозном геле. ПЦР продукты очищали с помощью набора для очистки ПЦР продуктов (Quigen) в соответствии с инструкциями поставщика. Затем обрабатывали очищенные фрагменты по отдельности рестриктазой Еаm11004I. Лигирование этого фрагмента E2s-H6 с акцепторной плазмидой, производной от pMF30, выполняли с использованием лигазы Т4 (Boehringer) в соответствии с рекомендациями поставщика. Смесь, полученную лигированием, применяли для трансформации клеток Е.coli DH5αF', и плазмидные ДНК нескольких клонов анализировали путем рестрикции EcoRI/BamHI. Выбирали позитивный клон, далее обозначали его плазмиду как pAMY-E2 и использовали ее для дальнейшей модификации как описано ниже.
Получение вектора pUC18-CL-E2-H6
pAMY-E2 подвергали ПЦР-направляемому мутагенезу для того, чтобы заменить кодоны сигнальной последовательности α-амилазы кодонами пре-последовательности птичьего лизоцима. Далее он обозначен как "CL" в соответствии с первыми 18-ю аминокислотами ORF (открытая рамка считывания) птичьего лизоцима (SEQ ID NO:1). Для этого мутаганеза применяли следующие праймеры:
- праймер CL2 hin:
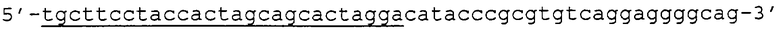
(SEQ ID NO:30) и
- праймер CL2 her:
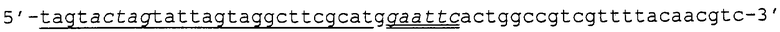
(SEQ ID NO:31).
Подчеркнутые 5'-участки праймеров содержат последовательности ДНК, соответствующие примерно половине пре-последовательности птичьего лизоцима. Праймер CL2 her включает в себя сайты рестрикции SpeI (курсив) и EcoRI (дважды подчеркнутый курсив). Неподчеркнутые участки праймеров гибридизуются с кодонами аминокислотных остатков 384-392 из Е2 (CL2 hin) или со стартовым кодоном "atg" около EcoRI сайта вплоть до положения -19 (при отсчете от сайта EcoRI) промотора FMD. Эти праймеры предназначены для амплификации полного вектора pAMY-E2, посредством чего происходит замена кодонов сигнальной последовательности α-амилазы кодонами пре-последовательности птичьего лизоцима.
Реакцию ПЦР проводили в соответствии со следующей программой:
1. денатурация: 15 мин при 95°С
2. 35 циклов по 30 сек денатурации при 95°С, 1 мин отжига при 60°С и 1 мин элонгации при 72°С
3. терминация при 4°С.
Использовали следующую реакционную смесь: pAMY-E2 (1 нг/мкл), 1 мкл; праймер CL2 hin (100 мкМ), 2 мкл; праймер CL2 her (100 мкМ), 2 мкл; dNTP's (no 2,5 мМ каждого), 8 мкл; H2O, 76 мкл; 10× буфер 2 набора Expand Long Template PCR System (Boehringer, Cat. No 1681834), 10 мкл, полимеразная смесь набора Expand Long Template PCR System (1 ед./мкл), 0,75 мкл.
Получившийся ПЦР продукт проверяли гель-электрофорезом в 1%-ном агарозном геле. ПЦР фрагмент перед лигированием модифицировали следующим образом. 3'-А концевые избыточности удаляли полимеразой Т4, результатом чего были тупые концы с 3'- и 5'-ОН-группами. Для этого к оставшимся 95 мкл реакционной смеси ПЦР добавляли 1 мкл полимеразы Т4 (Boehringer, 1 ед./мкл) вместе с 4 мкл dNTP's (по 2,5 мМ каждого). Образец инкубировали в течение 20 мин при 37°С. Затем ДНК осаждали этанолом и растворяли в 16 мкл деионизированной воды. За этим следовала обработка киназой для добавления 5'-фосфатов к ПЦР продукту с тупыми концами. К 16 мкл растворенного ПЦР продукта с тупыми концами добавляли 1 мкл полинуклеотидкиназы Т4 (Boehringer, 1 ед./мкл), 2 мкл концентрированного в 10 раз буфера для Т4-полинуклеотидкиназной реакции (Boehringer) и 1 мкл АТР (10 мМ). Образец инкубировали в течение 30 мин при 37°С.
Затем обработанный киназой образец разделяли в 1%-ном агарозном геле. Полосу продукта отделяли. ДНК экстрагировали из фрагмента агарозы с помощью набора для гелевой экстракции (Gel Extraction kit, Qiagen) в соответствии с рекомендациями поставщика. Затем пятьдесят (50) нг очищенного продукта подвергали самолигированию с помощью лигазы Т4 (Boehringer) в соответствии с инструкциями поставщика. После 16 часов инкубации при 16°С ДНК в смеси для лигирования осаждали этанолом и растворяли в 20 мкл H2O (образец после лигирования).
Клетки Е.coli DH5αF' трансформировали 10 мкл образца после лигирования. Далее несколько клонов, устойчивых к ампициллину, характеризовали рестрикционным анализом выделенной плазмидной ДНК. Позитивный клон обозначали как pUC18-CL-E2-H6 и использовали для дальнейших модификаций как описано ниже.
Получение челночного вектора pFPMT-CL-E2-H6
EcoRI/BamHI-фрагмент длиной 0,966 т.н. выделяли из pUC18-CL-E2-H6 (содержащей CL-E2(384-673)-VIEGR-H6) и лигировали в подвергнутую EcoRI/BamHI-рестрикциН pFPMT121 (SEQ ID NO:12, Фиг.3). Для этой реакции использовали лигазу Т (Boehringer) в соответствии с условиями поставщика. Образец лигирования осаждали этанолом и растворяли в 10 мкл воды и использовали для трансформации клеток Е.coli DH5αF'. После рестрикционного анализа отбирали позитивный клон и соответствующую плазмиду обозначали как pFPMT-CL-E2-H6 (SEQ ID NO:32, Фиг.14).
ПРИМЕР 5
КОНСТРУИРОВАНИЕ ЧЕЛНОЧНОГО ВЕКТОРА pFPMT-CL-K-H6-E1
Конструирование этого челночного вектора состояло из двух этапов.
На первом этапе посредством сайт-направленного мутагенеза создавали конструкт pUC18-FMD-CL-H6-K-E1-H6. В качестве матрицы использовали pUC18-FMD-CL-E1 (SEQ ID NO:20, Фиг.7). Применяли следующие праймеры:
- Праймер Н6К hin neu:
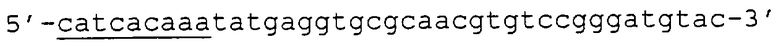
(SEQ ID NO:37).
- Праймер H6KRK her neu:
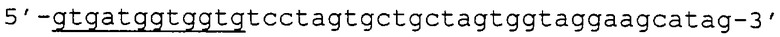
(SEQ ID NO:38).
(Основания, обеспечивающие дополнительные кодоны, подчеркнуты).
Реакционную смесь для ПЦР составляли следующим образом: pUC18-FMD-CL-E1-H6 (2 нг/мкл), 1 мкп; праймер Н6К hin neu (100 мкМ), 2 мкл; праймер H6KRK her neu (100 мкМ), 2 мкл; dNTP's (по 2,5 мМ каждого), 8 мкл; H2O, 76 мкл; концентрированный в 10 раз буфер 2 набора Expand Long Template PCR System (Boehringer, Cat. No 1681834), 10 мкл; полимеразная смесь набора Expand Long Template PCR System (1 ед./мкл), 0,75 мкл.
Примененная программа ПЦР состояла из следующих этапов:
- этап денатурации: 15 мин при 95°С
- 35 циклов по 30 сек денатурации при 95°С, 1 мин отжига при 60°С и 5 мин элонгации при 72°С
- терминация при 4°С.
Аликвоту образца ПЦР анализировали в 1%-ном агарозном геле для проверки ее размера, который был корректным (примерно 4,2 т.н.).
После этого у ПЦР продукта удаляли 3'-А концевые избыточности полимеразой Т4, результатом чего были тупые концы с 3'- и 5'-ОН-группами. Для этого к оставшимся 95 мкл реакционной смеси ПЦР добавляли 1 мкл полимеразы Т4 (Boeringer, 1 ед./мл) и 4 мкл dNTP's (по 2,5 мМ каждого). Образец инкубировали в течение 20 мин при 37°С. Затем ДНК в образце осаждали этанолом и растворяли в 16 мкл воды.
Затем к ПЦР продукту с тупыми концами добавляли 5'-фосфаты киназной реакцией. Для этого к 16 мкл растворенного ПЦР продукта с тупыми концами добавляли 1 мкл полинуклеотидкиназы Т4 (Boehringer, 1 ед./мкл), 2 мкл сконцентрированного в 10 раз буфера для Т4-полинуклеотидкиназной реакции (Boehringer) и 1 мкл АТР (10 мМ). Образец инкубировали в течение 30 мин при 37°С.
Затем образец наносили на 1%-ный агарозный гель и выделяли полосу соответствующего продукта с помощью набора для гелевой экстракции (Qiagen) в соответствии с условиями поставщика. Затем пятьдесят (50) нг очищенного продукта подвергали самолигированию лигазой Т4 (Boehringer) в соответствии с рекомендациями поставщика. После 72 ч инкубации при 16°С ДНК в смеси для лигирования осаждали этанолом и растворяли в 10 мкл воды.
Затем 5 мкл образца лигирования трансформировали клетки Е.coli DH5αF'. Плазмидную ДНК нескольких клонов, устойчивых к ампициллину, анализировали обработкой ферментами рестрикции, отбирали позитивный клон и обозначали соответствующую плазмиду как pUC18-FMD-CL-H6-E1-K-H6 (SEQ ID NO:39, Фиг.17).
На втором этапе конструировали вектор переноса лигированием двух фрагментов. В нижеследующем конструировании участвовали фрагменты с Bc/I-липкими концами. Поскольку Bc/I может расщеплять свой сайт только по неметилированной ДНК, применяемыми плазмидами pUC18-FMD-CL-H6-K-E1-Н6 (SEQ ID NO:39, Фиг.17) и pFPMT-CL-EI (SEQ ID NO:36, Фиг.16) трансформировали штамм Е.coli dam-. После каждой трансформации отбирали колонию, устойчивую к ампициллину, выращивали в жидкой культуре и для последующего применения получали неметилированную плазмидную ДНК. Получали 1,273 т.н. Bc/I/HindIII-фрагмент неметилированной плазмиды pUC18-FMD-CL-H6-K-E1-H6 (содержащий промотор FMD, кодоны блока CL-H6-К и начало Е1) и 6,075 т.н. Bc/I/HindIII-фрагмент плазмиды pFPMT-CL-E1 (содержащий недостающую часть рамки считывания Е1, начиная с сайта Bc/I, без С-концевой гистидиновой метки, а также элементы, локализованные в pFPMT121, за исключением промотора FMD) и лигировали вместе в течение 72 часов при 16°С с использованием лигазы Т4 (Boehringer) в общем объеме 20 мкл в соответствии со спецификациями поставщика. Затем для обессоливания смеси лигирования ее помещали на кусок нитроцеллюлозной мембраны, плавающий на стерильной деионизированной воде (инкубация в течение 30 мин при комнатной температуре). Способом электропорации трасформировали клетки Е.coli TOP10 пятью микролитрами обессоленного образца. Плазмидную ДНК нескольких полученных колоний, устойчивых к ампициллину, анализировали обработкой рестрикционными ферментами. Позитивный клон отбирали и обозначали как pFPMT-CL-H6-K-E1 (SEQ ID NO:40, Фиг.18).
ПРИМЕР 6
ТРАНСФОРМАЦИЯ HANSENULA POLYMORPHA И СЕЛЕКЦИЯ ТРАНСФОРМАНТОВ
Штамм RB11 Н.polymorpha трансформировали (протокол PEG(полиэтиленгликоль)-опосредованного захвата ДНК по существу как описано Klebe, J.R. et al. 1983 с модификацией по Roggenkamp, R. et al. 1986) разными исходными челночными векторами как описано в Примерах 1-5. Для каждой трансформации отбирали 72 колоний, прототрофных по урацилу, и использовали для получения штаммов в нижеследующей процедуре. Каждой колонией инокулировали 2 мл жидкой культуры и выращивали в опытных пробирках в течение 48 часов (37°С, 160 об/мин, угол 45°) в селективной среде (YNB/глюкоза, Difco). Этот этап определен как этап первого пассажа. Аликвоту 150 мкл культур этапа первого пассажа использовали для инокуляции 2 мл свежей среды YNB/глюкоза. Инкубировали культуры снова как описано выше (этап второго пассажа). В целом проводили восемь таких этапов пассирования. Аликвоты культур после этапов третьего и восьмого пассажа использовали для инокуляции 2 мл неселективной среды YPD (Difco). После 48 часов инкубации при 37°С(160 об/мин, угол 45°, так называемый первый этап стабилизации) аликвоты по 150 мкл этих YPD-культур использовали для инокуляции свежих 2 мл YPD-культур, которые инкубировали как описано выше (второй этап стабилизации). Аликвоты культур второго этапа стабилизации высевали штрихом на чашки, содержащие селективный YNB/агар. Инкубировали эти чашки в течение четырех дней, пока не становились видимыми макроскопические колонии. Хорошо определяемую отдельную колонию каждой сепарации определяли как штамм и использовали для дальнейшего анализа экспрессии.
Анализ экспрессии проводили в культурах в малых качалочных колбах. Из вышеупомянутой чашки с YNB/агаром отбирали колонию и инокулировали в 2 мл YPD и инкубировали в течение 48 часов как упомянуто выше. Эту аликвоту объемом 2 мл использовали как посевную культуру для культуры в качалочной колбе на 20 мл. В качестве среды использовали YP-глицерин (1%), а качалочную колбу инкубировали на роторном шейкере (200 об/мин, 37°С). После 48 часов роста в культуру добавляли 1% МеОН для индукции экспрессионной кассеты. Через разные интервалы времени собирали осадок клеток из аликвот по 1 мл и хранили при -20°С до дальнейшего анализа. Экспрессию специфических белков анализировали с помощью комбинации электрофореза в Na-ДДС ПААГ и вестерн-блоттинга. Для этого солюбилизировали осадки клеток в буфере для образцов (Трис-HCl-Ма-ДДС) и инкубировали более 15 минут при 95°С. Разделяли белки в 15%-ном полиакриламидном геле и проводили блоттинг (влажный блот, бикарбонатный буфер) на нитроцеллюлозных мембранах. Проявляли блоты с использованием специфических мышиных анти-Е1 (IGH 201) или мышиных анти-Е2 (IGH 216, описаны Maertens et al. в WO 96/04385) в качестве первых антител, а в качестве второго антитела использовали кроличий антимышиный АР. Окрашивание проводили посредством NBT-BCIP. Для дальнейшего анализа отбирали позитивные штаммы.
Пять из этих позитивных клонов использовали для эксперимента по экспрессии в качалочной колбе. Из чашки с YNB отбирали колонию соответствующего штамма и использовали ее для инокуляции 2 мл YPD. Инкубировали эти культуры как описано выше. Эту клеточную суспензию использовали для инокуляции второй посевной культуры в 100 мл среды YPD в качалочной колбе на 500 мл. Эту качалочную колбу инкубировали на роторном шейкере в течение 48 часов при 37°С и 200 об/мин. Аликвоту этой посевной культуры объемом 25 мл использовали для инокуляции 250 миллилитров среды YP-глицерин (1%) и инкубировали в качалочной колбе с отбойными перегородками на 2 л в вышеописанных условиях. Через 48 часов после инокуляции добавляли 1% МеОН (индукция промотора) и качалочные колбы инкубировали дальше в вышеописанных условиях. Через 24 часа после индукции останавливали эксперимент и собирали осадки клеток центрифугированием. Уровень экспрессии пяти разных клонов анализировали комбинацией Na-ДДС-ПААГ-электрофореза и вестерн-блоттинга (условия как и выше). На гель наносили титрационную серию каждого клона и отбирали самый продуктивный штамм для дальнейших испытаний ферментацией и очисткой.
Неожиданно оказалось, что Н.polymorpha, представляющая собой дрожжевой штамм, близкородственный Pichia pastoris (Gellissen, G. 2000), способна экспрессировать белки HCV по существу без гипергликозилирования и, таким образом, с группировками сахаров, которые сравнимы по размеру с оболочечными белками HCV, экспрессируемыми клетками млекопитающего, которые инфицированы HCV-рекомбинантным вирусом коровьей оспы.
Штамм RB11 Hansenula polymorpha был депонирован 19 апреля 2002 года в соответствии с условиями Будапештского договора в Mycotheque de I'UCL (MUCL), Universite Catholique de Louvain, Laboratoire de mycologie, Place Croix du Sud 3 bte 6, B-1348 Louvain-la-Neuve, Belgium) и имеет MUCL депозитарный номер MUCL43805.
ПРИМЕР 7
КОНСТРУИРОВАНИЕ ВЕКТОРА pSY1aMFE1sH6a
Экспрессионную плазмиду для S.cerevisiae конструировали следующим образом. Последовательность, кодирующую Е1, выделяли как Ns/1/Eco52I-фрагмент из pGEMT-E1sH6 (SEQ ID NO:6, Фиг.1), у которой делали тупые концы (с помощью ДНК-полимеразы Т4), и клонировали в вектор pYIG5 (SEQ ID NO:41, Фиг.19) с использованием ДНК-лигазы Т4 (Boehringer) в соответствии со спецификациями поставщика. Кпонирование было таким, что фрагмент, кодирующий E1s-H6, был присоединен прямым образом и в рамке с последовательностью, кодирующей αMF. Смесью лигирования трансформировали клетки Е.coli DH5αF'. Затем анализировали плазмидную ДНК нескольких клонов, устойчивых к ампициллину, рестрикционным расщеплением, отбирали позитивный клон и обозначали его как pYIG5E1H6 (ICCG3470; SEQ ID NO:42, Фиг.20).
Экспрессионную кассету (содержащую αMF-последовательность и E1s-кодирующий участок с гистидиновой меткой) переносили в виде BamHI-фрагмента(2790 п.н.) плазмиды pYIG6E1H6 в челночный вектор pSY1 для E.coli/S.cerevisiae (SEQ ID NO:21, Фиг.43), расщепленный рестриктазой BamHI. Лигирование осуществляли ДНК-лигазой Т4 (Boehringer) в соответствии с условиями поставщика. Трансфомировали смесью лигирования клетки Е.coli DH5αF' и анализировали плазмидную ДНК нескольких колоний, устойчивых к ампициллину, расщеплением рестрикционными ферментами. Позитивный клон отбирали и обозначали как pSY1aMFE1sH6a (ICCG3479; SEQ ID NO:44, Фиг.22).
ПРИМЕР 8
КОНСТРУИРОВАНИЕ ВЕКТОРА pSYYIGSE2H6
Экспрессионную плазмиду pSYYIGSE2H6 для S.cerevisiae конструировали следующим образом. Последовательность, кодирующую Е2, выделяли как Sa/I/KpnI-фрагмент из плазмиды pBSK-E2sH6 (SEQ ID NO:45, Фиг.23) с тупыми концами (с помощью ДНК-полимеразы Е4) и затем клонировали в вектор pYIG5 (SEQ ID NO:41, Фиг.19) с использованием ДНК-лигазы Т4 (Boehringer) в соответствии со спецификациями поставщика. Клонирование было таким, что фрагмент, кодирующий Е2-Н6, был присоединен прямым образом и в рамке последовательности, кодирующей αMF. Трансформировали смесью лигирования клетки Е.coli DH5αF', анализировали плазмидную ДНК нескольких клонов, устойчивых к ампициллину, рестрикционным расщеплением, отбирали позитивный клон и обозначали его как pYIG5HCCL-22аН6 (ICCG2424; SEQ ID NO:46, Фиг.24).
Экспрессионную кассету (содержащую αMF-последовательность и Е2(384-673)-кодирующий участок с гистидиновой меткой) переносили в виде BamHI-фрагмента (3281 п.н.) плазмиды pYIG5HCCL-22aH6 в челночный вектор pSY1 для Е.coli/S.cerevisiae (SEQ ID NO:43, Фиг.21), раскрытый рестриктазой ВаmН1. Лигирование осуществляли ДНК-лигазой Т4 (Boehringer) в соответствии с условиями поставщика. Трансформировали смесью лигирования клетки Е.coli DH5αF' и анализировали плазмидную ДНК нескольких колоний, устойчивых к ампициллину, расщеплением рестрикционными ферментами. Позитивный по рестрикции клон отбирали и обозначали как pSYYIGSE2H6 (ICCG2466; SEQ ID NO:47, Фиг.25).
ПРИМЕР 9
КОНСТРУИРОВАНИЕ ВЕКТОРА pSY1YIG7E1s
Экспрессионную плазмиду pSY1YIG7E1s для S.cerevisiae конструировали следующим образом. Последовательность, кодирующую Е1, выделяли как NS/1/Есо52I-фрагмент из плазмиды pGEMT-E1s (SEQ ID NO:6, Фиг.1) с тупыми концами и клонировали в вектор pYIG7 (SEQ ID NO:48, Фиг.26) с использованием ДНК-лигазы Т4 (Boehringer) в соответствии со спецификациями поставщика. Кпонирование было таким, что фрагмент, кодирующий Е1, был присоединен прямым образом и в рамке с последовательностью, кодирующей αMF. Трансформировали смесью лигирования клетки Е.coli DH5αF', анализировали плазмидную ДНК нескольких клонов, устойчивых к ампициллину, рестрикционным расщеплением, отбирали позитивный клон и обозначали его как pYIG7E1 (SEQ ID NO:49, Фиг.27).
Экспрессионную кассету (содержащую лидерную последовательность CL и Е1(192-326)-кодирующий участок) переносили в виде BamHI-фрагмента (2790 п.н.) плазмиды pYIG7E1 в BamHI-расщепленный челночный вектор pSY1 для Е.coli/S.cerevisiae (SEQ ID NO:43, Фиг.21). Лигирование осуществляли ДНК-лигазой Т4 (Boehringer) в соответствии с условиями поставщика. Трансформировали смесью лигирования клетки Е.coli DH5αF' и анализировали плазмидную ДНК нескольких колоний, устойчивых к ампициллину, расщеплением рестрикционными ферментами. Позитивный клон отбирали и обозначали как pSY1YIG7E1s (SEQ ID NO:50, Фиг.28).
ПРИМЕР 10
ТРАНСФОРМАЦИЯ SACCHAROMYCES CEREVISIAE И СЕЛЕКЦИЯ ТРАНСФОРМАНТОВ
Для преодоления проблем гипергликозилирования, о которых часто сообщают в случае белков, сверхэкспрессируемых в Saccharomyces cerevisiae, осуществили скрининг мутантов. Этот скрининг был основан на методе Баллу (Ballou, L. et al. 1991), и с его помощью были отобраны спонтанные рецессивные мутанты, устойчивые к ортованадату. Исходную селекцию штаммов выполняли на основании типа гликозилирования инвертазы, наблюдаемого после нативного гель-электрофореза. Штамм со сниженной способностью к гликозилированию отобрали для последующих экспериментов по экспрессии рекомбинантных белков и обозначили как штамм IYCC155. Природу мутации далее не исследовали.
Указанный дефектный по гликозилированию штамм IYCC155 трансформировали плазмидами как описано в Примерах 7-9 по существу литий-ацетатным способом, как описано Elble, R. 1992. Несколько Ura-дополненных штаммов отобрали с селективной чашки YNB+2%-ный агар (Difco) и использовали для инокуляции 2 мл среды YNB+2% глюкозы. Инкубировали эти культуры в течение 72 часов при 37°С и 200 об/мин на орбитальном шейкере и анализирвали супернатант культур и внутриклеточные фракции на экспрессию Е1 вестерн-блоттингом с проявкой E1-специфичным мышиным моноклональным антителом (IGH 201). Высокопродуцирующий клон был отобран для дальнейших экспериментов.
В использованном здесь дефектном по гликозилированию мутанте S.cerevisiae экспрессии белков препятствуют субоптимальные характеристики роста таких штаммов, что ведет к более низкому выходу биомассы и, таким образом, более низкому выходу желаемых белков в сравнении со штаммами S.cerevisiae дикого типа. Выход желаемых белков был все равно значительно выше, чем в клетках млекопитающего.
ПРИМЕР 11
КОНСТРУИРОВАНИЕ ВЕКТОРОВ pPICZalphaD'E1sH6 и pPICZalphaE'E1sH6
Челночный вектор pPICZalphaE'E1sH6 конструировали, начиная с вектора pPICZalphaA (Invitrogen; SEQ ID NO:51, Фиг.29). На первом этапе указанный вектор адаптировали, чтобы сделать возможным клонирование E1-кодирующей последовательности непосредственно за сайтом расщепления протеазами процессинга КЕХ2 или STE13, соответственно. Для этого расщепляли pPICZalphaA рестриктазами Xhol и Notl. Продукт расщепления разделяли на 1%-ном агарозном геле и фрагмент длиной 3519 т.н. (основная часть вектора) выделяли и очищали с помощью набора для гелевой экстракции (Qiagen). Затем этот фрагмент лигировали с использованием полимеразы Т4 (Boeringer) в соответствии с условиями поставщика в присутствии специфических олигонуклеотидов с получением pPICZalphaD' (SEQ ID NO:52, Фиг.30) или pPICZalphaE' (SEQ ID NO:53, Фиг.31).
Использовали следующие олигонуклеотиды:
- для конструирования pPICZalphaD':
8822: 5'-TCGAGAAAAGGGGCCCGAATTCGCATGC-3' (SEQ ID NO:54) и
8823: 5'-GGCCGCATGCGAATTCGGGCCCCTTTTC-3' (SEQ ID NO:55),
которые дают после гибридизации линкерный олигонуклеотид:
TCGAGAAAAGGGGCCCGAATTCGCATGC (SEQ ID NO:54)
CTTTTCCCCGGGCTTAAGCGTACGCCGG (SEQ ID NO:55)
- для конструирования pPICZalphaE':
8649: 5'-TCGAGAAAAGAGAGGCTGAAGCCTGCAGCATATGC-3' (SEQ ID NO:56)
8650: 5'-GGCCGCATATGCTGCAGGCTTCAGCCTCTCTTTTC-3' (SEQ ID NO:57)
которые дают после гибридизации линкерный олигонуклеотид:
TCGAGAAAAGAGAGGCTGAAGCCTGCAGCATATGC (SEQ ID NO:56)
CTTTTCTCTCCGACTTCGGACGTCGTATACGCCGG (SEQ ID NO:57)
Эти челночные векторы pPICZalphaD' и pPICZalphaE' имеют нововведенные сайты клонирования непосредственно за сайтом расщепления соответствующих протеаз процессинга, КЕХ2 и STE13.
Последовательность, кодирующую Е1-Н6, выделяли в виде Ns/1/Eco52I-фрагмента из pGEMT-E1sH6 (SEQ ID NO:6, Фиг.1). Этот фрагмент очищали с использованием набора для гелевой экстракции (Qiagen) после разделения перевара в 1%-ном агарозном геле. Концы полученнного фрагмента делали тупыми (с использованием ДНК-полимеразы Т4) и лигировали либо в pPICZalphaD', либо в pPICZalphaE' прямо за соответствующим сайтом расщепления протеазы процессинга.
Трансформировали смесями лигирования клетки Е.coli TOP10F' и анализировали плазмидные ДНК нескольких колоний, устойчивых к зеоцину, расщеплением ферментами рестрикции. Отбирали позитивные клоны и обозначали их как pPICZalphaD'E1sH6 (ICCG3694; SEQ ID NO:58, Фиг.32) и pPICZalphaE'E1sH6 (ICCG3475; SEQ ID NO:59, Фиг.33), соответственно.
ПРИМЕР 12
КОНСТРУИРОВАНИЕ ВЕКТОРОВ pPICZalphaD'E2sH6 и pPICZalphaE'E2sH6
Конструировали челночные векторы pPICZalphaD' и pPICZalphaE' как описано в Примере 11.
Последовательность, кодирующую Е2-Н6, выделяли как Sa/I/KpnI-фрагмент из pBSK-E2sH6 (SEQ ID NO:45, Фиг.23). Этот фрагмент очищали с помощью набора для гелевой экстракции (Qiagen) после разделения перевара в 1%-ном агарозном геле. Концы полученного фрагмента делали тупыми (с использованием ДНК-полимеразы Т4) и лигировали либо в pPICZaIphaD', либо в pPICZalphaE' прямо за соответствующим сайтом расщепления протеазой процессинга.
Трансформировали смесью лигирования клетки Е.coli TOP10F' и анализировали плазмидные ДНК нескольких колоний, устойчивых к зеоцину, расщеплением ферментами рестрикции. Отбирали позитивные клоны и обозначали их как pPICZalphaD'E2sH6 (ICCG3692; SEQ ID NO:60, Фиг.34) и pPICZalphaE'E2sH6 (ICGG3476; SEQ ID NO:61, Фиг.35), соответственно.
ПРИМЕР 13
ТРАНСФОРМАЦИЯ PICHIA PASTORIS И СЕЛЕКЦИЯ ТРАНСФОРМАНТОВ
Векторными плазмидами Р.pastoris, как описано в Примерах 11 и 12, трансформировали клетки Р.pastoris в соответствии с условиями поставщика (Invitrogen). Отбирали линии, продуцирующие Е1 и Е2, для дальнейшей характеристики.
Экспрессировали оболочечные белки HCV в Р.pastoris, штамме дрожжей, хорошо известному благодаря тому факту, что гипергликозилирование у него в норме отсутствует (Gellissen, G. 2000), и ранее использовавшемуся для экспрессии белка Е вируса денге в GST-слитом виде (Sugrue, R.G. et al. 1997). Примечательно, что результирующие экспрессируемые в Р.pastoris оболочечные белки HCV проявляли гликозилирование, сходное с тем, которое наблюдают в штаммах Saccharomyces дикого типа. Более конкретно, оболочечные белки HCV, продуцируемые Р.pastoris, гипергликозилированы (на основании молекулярной массы продуктов экспрессии, выявляемых в вестерн-блотах белков, выделенных из трансформированных клеток Р.pastoris).
ПРИМЕР 14
УСЛОВИЯ КУЛЬТИВИРОВАНИЯ ДЛЯ SACCHAROMYCES CEREVISIAE, HANSENULA POLYMORPHA И PICHIA PASTORIS
Saccharomyces cerevisiae
Создание банка клеток
Из выбранного рекомбинантного клона готовили основной банк клеток и рабочий банк клеток.
Из культуры в середине экспоненциальной фазы роста в качалочной колбе (условия инкубации как для ферментационных посевных культур) готовили крио-ампулы. В качестве криопротектора добавляли глицерин (конечная концентрация 50%).
Ферментация
Начинали посевные культуры с крио-сохраняемой ампулы рабочего банка клеток и выращивали в 500 мл среды (YBN, обогащенная 2% сахарозы, Difco) в качалочных колбах Эрленмейера на 2 л при 37°С и 200 об/мин в течение 48 часов.
Ферментацию в типичных случаях проводили в ферментаторах Biostat С с рабочим объемом 15 л (В.Braun Int., Melsungen, Germany). Ферментационная среда содержала 1% дрожжевого экстракта, 2% пептона и 2% сахарозы в качестве источника углерода. В качестве пеногасителя применяли полиэтиленгликоль.
В типичных случаях во время ферментации контролировали температуру, рН и растворенный кислород, применимые установки этих параметров суммированы в Табл.1. Растворенный кислород контролировали каскадным способом путем перемешивания/аэрации. рН контролировали добавлением NaOH (0,5 М) или Н3РО4 (8,5%).
Типичные установки параметров для ферментации S.cerevisia
Ферментацию начинали добавлением 10% посевной культуры. Во время фазы роста концентрацию сахарозы независимо отслеживали с помощью ВЭЖХ (высокоэффективная жидкостная хроматография) анализа (колонка Polysphere OAKC Merck).
Во время фазы роста растворенный кислород контролировали каскадным контролем (перемешивание/аэрация). После полного метаболизирования сахарозы продукцию гетерологичных белков запускал эндогенно продуцируемый этанол, причем для удержания его концентрации около 0,5% (независимый ВЭЖХ анализ, колонка Polysphere OAKC) по порциям добавляли EtOH. Во время этой фазы индукции растворенный кислород поддерживали ниже 5% насыщения воздухом подгонкой тока воздуха и скорости перемешивания вручную.
В типичном случае ферментацию завершали через 48-72 часа после индукции, концентрируя клетки фильтрацией в тангенциальном потоке с последующим центрифугированием концентрированной суспензии клеток с получением осадка клеток. Если не выполняли анализ немедленно, хранили осадки клеток при -70°С.
Hansenula polymorpha
Создание банка клеток
Из выбранного рекомбинантного клона готовили основной банк клеток и рабочий банк клеток.
Из культуры в середине экспоненциальной фазы роста в качалочной колбе (условия инкубации как для ферментационных посевных культур) готовили криоампулы. В качестве криопротектора добавляли глицерин (конечная концентрация 50%).
Ферментация
Начинали посевные культуры с криосохраняемой (-70°С) ампулы рабочего банка клеток и выращивали в 500 мл среды (YBN, Difco) в качалочных колбах Эрленмейера на 2 л при 37°С и 200 об/мин в течение 48 часов.
В типичных случаях проводили ферментации в ферментаторах Biostat С с рабочим объемом 15 л (В.Braun Int., Melsungen, Germany). Ферментационная среда содержала 1% дрожжевого экстракта, 2% пептона и 1% глицерина в качестве источника углерода. В качестве пеногасителя применяли полиэтиленгликоль.
В типичных случаях во время ферментации контролировали температуру, рН и растворенный кислород, применимые установки этих параметров суммированы в Табл.2. Растворенный кислород контролировали путем перемешивания. рН контролировали добавлением раствора NaOH (0,5 М) или Н3РО4 (8,5%).
Типичные установки для параметров ферментации Н.polymorpha
Ферментацию начинали добавлением 10% посевной культуры. Во время фазы роста концентрацию глицерина отслеживали независимо с помощью ВЭЖХ анализа (колонка Polysphere OAKC Merck) и через 24 часа после полного потребления глицерина добавляли 1% метанола для того, чтобы индуцировать экспрессию гетерологичных белков. Ферментацию завершали через 24 часа после индукции, концентрируя клетки фильтрацией в тангенциальном потоке с последующим центрифугированием концентрированной суспензии клеток с получением осадка клеток. Если не выполняли анализ немедленно, хранили осадки клеток при -70°С.
Pichia pastoris
Эксперименты по мелкомасштабному продуцированию белков рекомбинантным Pichia pastoris были поставлены на культурах в качалочных колбах. Выращивали посевные культуры в течение ночи в среде YPD (Difco). Исходный рН среды корректировали до 4,5. Инкубировали качалочные колбы на роторном шейкере при 200-250 об/мин и 37°С.
Мелкомасштабное продуцирование в типичных случаях осуществляли в объеме 500 мл в качалочных колбах на 500 мл и начинали 10%-ной инокуляцией в экспрессионную среду, содержащую 1% дрожжевого экстракта, 2% пептона (оба продукта от Difco) и 2% глицерина в качестве источника углерода. Условия инкубации были такими же, как для посевной культуры. Примерно через 72 часа после инокуляции начинали индукцию добавлением 1% МеОН. Через 24 часа после индукции собирали клетки центрифугированием. Если не выполняли анализ немедленно, хранили осадки клеток при -70°С.
ПРИМЕР 15
УДАЛЕНИЕ ЛИДЕРНОГО ПЕПТИДА ИЗ БЕЛКОВ MFα-E1-H6 И MFα-E2-H6, ЭКСПРЕССИРУЕМЫХ В ВЫБРАННЫХ ДРОЖЖЕВЫХ КЛЕТКАХ
Далее анализировали продукты экспрессии белковых конструктов Е1 и Е2 HCV с лидерной последовательностью α-фактора спаривания дрожжей (αMF) S.cerevisiae в Hansenula polymorpha и в штамме Saccharomyces cerevisia, дефектном по гликозилированию. Поскольку оба генотипа 1b HCV E1s (аминокислоты 192-326) и HCV E2s (аминокислоты 383-637, удлиненные последовательностью VIEGR (SEQ ID NO:69)) экспрессировались как белки с С-концевой гистидиновой меткой (Н6, НННННН, SEQ ID NO:63, далее в этом примере указанные белки HCV обозначены как αMF-E1-H6 И αMF-E2-H6), быструю и эффективную очистку экспрессируемых продуктов после солюбилизации клеток дрожжей хлоридом гуанидиния (GuHCl) осуществляли на Ni-IDA (Ni-иминодиуксусная кислота). Вкратце, ресуспензировали клеточные осадки в среде, состоящей из 50 мМ фосфата, 6 М GuHCl, рН 7,4 (9 объемов на 1 г клеток). Сульфонировали белки в течение ночи при комнатной температуре (КТ) в присутствии 320 мМ (4% масс./об.) сульфита натрия и 65 мМ (2% масс./об.) тетратионата натрия. Осветляли лизат после цикла замораживания-оттаивания центрифугированием (10000 g, 30 мин, 4°С) и добавляли к супернатанту Empigen (Albright & Wilson, UK) и имидазол до конечной концентрации 1% (масс./об.) и 20 мМ, соответственно. Образец фильтровали (0,22 мкМ) и наносили на колонку с Ni-IDA Sepharose FF, которую уравновешивали 50 мМ фосфатом, 6М GuHCl, 1% Empigen (буфер А), обогащенным 20 мМ имидазола. Колонку промывали последовательно буфером А, содержащим 20 мМ и 50 мМ имидазола, соответственно, до тех пор, пока поглощение при 280 нм не достигало базового уровня. Элюировали продукты с гистидиновой меткой нанесением буфера D, 50 мМ фосфат, 6 М GuHCl, 0,2% (для Е1) или 1% (для Е2) Empigen, 200 мМ имидазол. Анализировали элюированный материал Na-ДДС-ППАГ-электрофорезом и вестерн-блоттингом с использованием специфических моноклональных антител против Е1 (IGH201) или Е2 (IGH212).
Немедленно анализировали E1-продукты расщеплением по Эдману.
Поскольку на этой стадии Na-ДДС-ПААГ-электрофорез уже выявлял очень сложную картину белковых полос для HCV E2, проводили дальнейшую фракционализацию вытеснительной хроматографией. Ni-IDA элюат концентрировали ультрафильтрацией (MWCO 10 kDa, centriplus, Amicon, Millipore) и наносили на Superdex G200 (10/30 или 16/60, Pharmacia) в PBS (забуференный фосфатом физиологический раствор), 1% Empigen или PBS, 3% Empigen. Собирали и алкилировали (инкубация с 10 мМ DTT (дитиотрейтол) в течение 3 часов при комнатной температуре с последующей инкубацией с 3 мМ йодоацетамида в течение 3 часов при КГ) элюированные фракции, содержащие Е2-продукты с молекулярной массой между примерно 80 кДа и примерно 45 кДа, то есть фракции 17-23 профиля элюции на Фиг.37 на основании миграции при Na-ДДС-ПААГ электрофорезе (Фиг.38). Образцы для амино-терминального секвенирования обрабатывали Endo H (Roche Biochemical) или оставляли их необработанными. Для амино-концевого секвенирования гликозилированные или дегликозилированные Е2-продукты подвергали блоттингу на PVDF-мембранах. Блот гликозилированного и дегликозилированного Е2, окрашенный красителем амидо черным, показан на Фиг.39.
Секвенирование очищенных продуктов Е1 и Е2 приводит к разочаровывающему наблюдению, состоящему в том, что удаление сигнальной последовательности из оболочечных белков HCV происходит только частично (см. Таблицу 3). Кроме того, большинство побочных продуктов (продукты деградации и продукты, все еще содержащие лидерную последовательность или ее часть) гликозилировано. Это гликозилирование отчасти свойственно даже нерасщепленному фрагменту сигнальной последовательности, который содержит еще и сайт N-гликозилирования. Эти сайты можно мутировать, чтобы добиться меньшего гликозилирования побочных продуктов. Однако даже еще более проблематично то наблюдение, что некоторые альтернативно расщепленные продукты при сравнении с желаемым интактным оболочечным белком имеют отличие только в 1-4 аминокислоты. Следовательно, очистка корректно процессированного продукта практически невозможна из-за отсутствия биохимических характеристик, в достаточной степени дифференцирующих различные продукты экспрессии. Несколько продуктов деградации могут быть результатом Кех-2-подобного расщепления (например, расщепление, наблюдаемое после аминокислоты 196 из Е1, которое является расщеплением после аргинина), которое требуется также для отщепления лидера α-фактора спаривания и которое, таким образом, нельзя блокировать без нарушения этого необходимого процесса.
Клон с высокой продукцией Е1, полученный трансформацией S.cerevisiae IYCC155 плазмидой pSY1YIGE1s (SEQ ID NO:50, Фиг.28), сравнили с высокопродуктивным клоном, полученным трансформацией S.cerevisiae IYCC155 плазмидой pSY1aMFE1sH6aYIG1E1s (SEQ ID NO:44, Фиг.22). Внутриклеточную экспрессию белка Е1 оценивали спустя 2-7 дней после индукции посредством вестерн-блоттинга с использованием моноклональных антител, специфичных к Е1 (IGH 201). Как можно судить по Фиг.40, максимальную экспрессию у обоих штаммов наблюдали через 2 дня, но паттерны экспрессии у обоих штаммов совершенно разные. Экспрессия с лидером α-фактора спаривания приводит к очень сложной картине полос, что является следствием того факта, что процессинг лидера неэффективен. Это приводит к нескольким продуктам экспрессии с разными амино-концами, среди которых некоторые модифицированы 1-5 N-гликозилированиями. Однако для Е1, экспрессируемого с лидером CL, видно ограниченное число отдельных полос, что отражает высокий уровень корректного удаления лидера CL и тот факт, что только этот корректно процессированный материал может быть модифицирован N-гликозилированием (от 1 до 5 цепей), как видно в случае белка Е1, полученного из Hansenula и экспрессируемого с тем же лидером CL (см. Пример 16).
Гибридомная клеточная линия, продуцирующая монокональное антитело, направленное против Е1 (IGH201), было депонировано 12 марта 1998 г. согласно условиям Будапештского договора в Европейской коллекции клеточных культур, Center for Applied Microbiology & Research, Salisbury, Wiltshire SP4 0JG, UK, и получила депозитарный номер ЕСАСС 98031216. Maertens et al. в WO 96/04385 описали моноклональное антитело, направленное против Е2 (IGH212) как антитело 12D11F2 в примере 7.4.
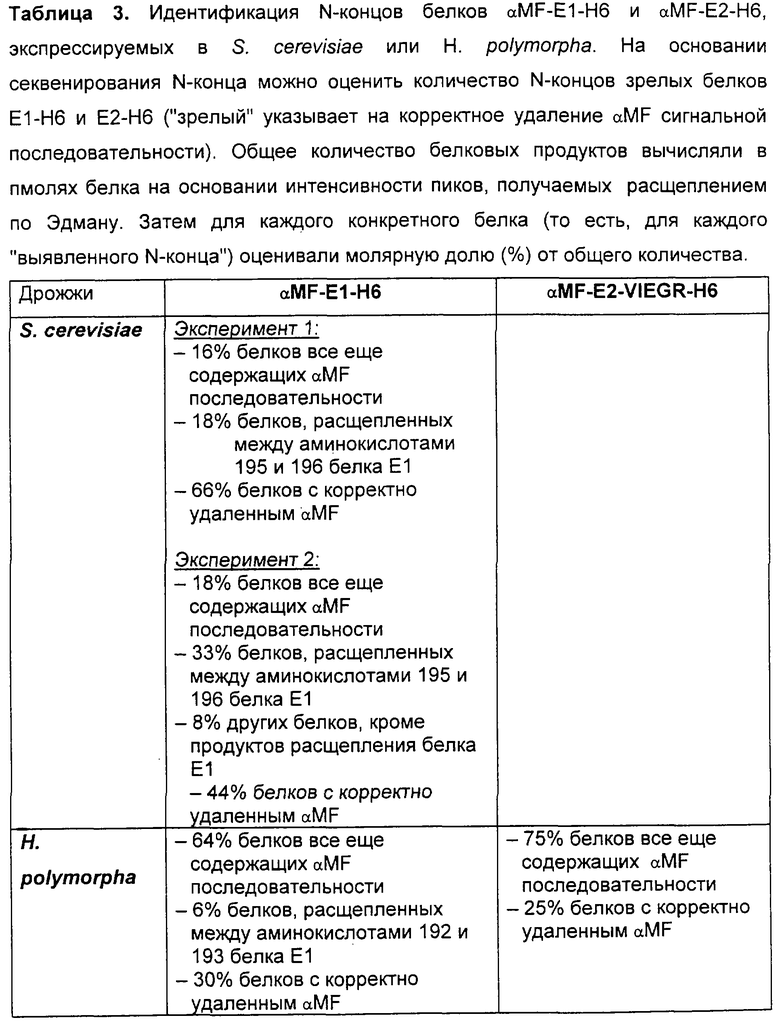
ПРИМЕР 16
ЭКСПРЕССИЯ Е1 КОНСТРУКТА В ДРОЖЖАХ, ПРИГОДНЫХ ДЛЯ КРУПНОМАСШТАБНОГО ПРОДУЦИРОВАНИЯ И ОЧИСТКИ
Для замены лидерного пептида белка αMF S.cerevisiae использовали несколько других лидерных последовательностей, включая СНН (лидерная последовательность гипергликемического гормона из Carcinus maenas), Amy1 (лидерная последовательность амилазы из S.occidentalis), Gam1 (лидерная последовательность глюкоамилазы из S.occidentalis), Phy5 (лидерная последовательность грибковой фитазы), pho1 (лидерная последовательность кислой фосфатазы из Pichia pastoris) и CL (лидерная последовательность птичьего лизоцима С, 1,4-бета-N-ацетилмурамидазы С) и соединяли с Е1-Н6 (то есть с С-концевой гистидиновой меткой). Экспрессировали все конструкты в Hansenula polymorpha и подвергали каждый из получавшихся клеточных лизатов анализу вестерн-блоттингом. Это сразу позволило сделать вывод, что степень удаления лидерной или сигнальной последовательности или пептида была очень низкой, за исключением случая, когда в качестве лидерного пептида в конструкте использован CL. Это было подтверждено для конструкта СНН-Е1-Н6 расщеплением по Эдману материала, очищенного на Ni-IDA: корректно расщепленный продукт не был выявлен, хотя было получено несколько разных последовательностей (см. Таблицу 4).
Идентификация N-концов белков СНН-Е1-Н6, экспрессируемых в Н.polymorpha, на основании секвенирования N-концевых аминокислот разных белковых полос после разделения Na-ДДС-ПААГ электрофорезом и блоттинга на PVDF-мембране
- частично начинается с аминокислоты 9 лидера СНН=продукт альтернативной трансляции, начинающейся со второго колона AUG
- частично начинается с аминокислоты 9 лидера СНН=продукт альтернативной трансляции, начиная со второго колона AUG
Как уже отмечено, вестерн-блоты клеточных лизатов выявили паттерн белковых полос, специфических для Е1, который указывает на более высокий уровень корректного удаления лидерного пептида CL. Это удивительно, поскольку этот лидер не происходит из дрожжей. Секвенирование аминокислот расщеплением по Эдману материала, солюбилизированного гидрохлоридом гуанидиния и очищенного на Ni-IDA, действительно подтвердило, что 84% белков Е1 расщеплено корректно и этот материал по существу свободен от продуктов деградации. Все же 16% непроцессированного материала присутствует, но, поскольку этот материал не гликозилирован, его можно легко удалить из смеси, что позволяет провести специфическое обогащение корректно отщепленного и гликозилированного Е1. Таким способом обогащения может быть аффинная хроматография на лектинах, в Примере 19 даны и другие альтернативы. Альтернативно, более высокогидрофобный характер негликозилированного материала можно использовать для выбора и оптимизации других процедур обогащения. Корректное удаление лидерного пептида CL из белка CL-E1-H6 было далее подтверждено масс-спектрометрией, которая также подтвердила то, что занятыми могут быть до 4 из 5 сайтов гликозилирования генотипа 1b E1s, вследствие чего последовательность NNSS (аминокислоты 233-236; SEQ ID NO:73) считают единственным сайтом N-гликозилирования.
ПРИМЕР 17
ОЧИСТКА И БИОХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА БЕЛКА HCV E2, ЭКСПРЕССИРУЕМОГО В HANSENULA POLYMORPHA ИЗ КОНСТРУКТА, КОДИРУЮЩЕГО CL-E2-H6
Анализировали эффективность удаления лидерного пептида CL из белка CL-E2-VIEGR-H6 (далее в этом Примере обозначаемого как "CL-E2-H6"), экспрессируемого в Hansenula polymorpha. Поскольку HCV E2s (аминокислоты 383-673) экспрессировался как белок с гистидиновой меткой, быструю и эффективную очистку экспрессируемого белка после GuHCI-солюбилизации собранных клеток осуществляли на NI-IDA. Вкратце, ресуспензировали клеточные осадки в 30 мМ фосфата, 6 М GuHCl, pH 7,2 (9 мл буфера/г клеток). Белок сульфонировали в течение ночи при комнатной температуре (КТ) в присутствии 320 мМ (4% масс./об.) сульфита натрия и 65 мМ (2% масс./об.) тетратионата натрия. Осветляли лизат после цикла замораживания-оттаивания центрифугированием (10000 g, 30 мин, 4°С). Добавляли Empigen BB (Albright & Wilson) и имидазол до конечной концентрации 1% (масс./об.) и 20 мМ, соответственно. Выполняли все дальнейшие хроматографические этапы на установке Åkta FPLC (быстрая жидкостная хроматография белков) (Pharmacia). Образец фильтровали через мембрану (ацетат целлюлозы) с порами размером 0,22 мкм и наносили на Ni-IDA-колонку (хелатирующая Sepharose FF, нагруженная Ni2+, Pharmacia), которую уравновешивали 50 мМ фосфата, 6М GuHCl, 1% Empigen BB, pH 7,2 (буфер А), обогащенным 20 мМ имидазола. Колонку промывали последовательно буфером А, содержащим 20 мМ и 50 мМ имидазола, соответственно, до тех пор, пока поглощение при 280 нм не достигало базового уровня. Элюировали продукты с гистидиновой меткой нанесением буфера D, 50 мМ фосфата, 6 М GuHCl, 0,2% Empigen BB (pH 7,2), 200 мМ имидазола. Очищенный материал анализировали Na-ДДС-ПААГ-электрофорезоми и вестерн-блоттингом с использованием специфического моноклонального антитела против E2 (IGH212) (Фиг.41). Очищенный с помощью IMAC белок Е2-Н6 подвергали также N-концевому секвенированию расщеплением по Эдману. С этой целью обрабатывали белки N-гликозидазой F (Roche) (0,2 ед./мкг Е2, инкубация в течение 1 часа при 37°С в забуференном фосфатами физиологическом растворе с 3% Empigen BB) или оставляли их необработанными. Гликозилированные и негликозилированные белки Е2-Н6 подвергали Na-ДДС-ПААГ электрофорезу и проводили блоттинг на PVDF-мембране для секвенирования аминокислот (анализ проводили на секвенаторе белков PROCISE™ 492, Applied Biosystems). Поскольку на этой стадии Na-ДДС-ПААГ выявлял некоторые продукты деградации, выполняли дальнейшее фракционирование вытеснительной хроматографией. Для этого Ni-IDA элюат концентрировали ультрафильтрацией (MWCO 10 кДа, centriplus, Amicon, Millipore) и наносили на Superdex G200 (Pharmacia) в PBS, 1% Empigen BB. Объединяли элюированные фракции, содержащие главным образом продукты, относящиеся к интактному Е2, с относительной молекулярной массой между примерно 30 кДа и примерно 70 кДа на основании миграции в Na-ДДС-ПААГ и в конце концов алкилировали их (инкубация с 5 мМ DTT в течение 30 мин при 37°С с последующей инкубацией с 20 мМ йодоацетамида в течение 30 мин при 37°С). Возможное присутствие продуктов деградации после IMAC-очистки можно, таким образом, устранить дальнейшим фракционированием интактного продукта вытеснительной хроматографией. Был получен неожиданно хороший результат. На основании N-концевого секвенирования можно оценить количество Е2 продукта, у которого удален лидерный пептид CL. Общее количество белковых продуктов рассчитывают в пмолях белка на основании интенсивности пиков, получаемых при расщеплении по Эдману. Затем для каждого конкретного белка (то есть, для каждого "выявленного N-конца") оценивают мольн.% относительно общего количества. В данном эксперименте выявляли только правильный N-конец Е2-Н6, а другие варианты Е2-Н6, не имеющие аминокислот белка Е2 или содержащие N-концевые аминокислоты, не содержащиеся в белке Е2, отсутствовали. Следовательно, белок Е2-Н6, экспрессируемый Н.polymorpha как белок CL-E2-H6, был выделен без какого-либо дальнейшего процессирования in vitro как белок, более чем на 95% расщепленный правильно. Это резко контрастирует с точностью удаления лидерного пептида у Н.polymorpha для белка αMF-E2-H6 с образованием белка Е2-Н6, оцениваемым как происходящее у 25% выделенных белков (см. Таблицу 3).
ПРИМЕР 18
ОЧИСТКА И БИОХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА БЕЛКА HCV E1, ЭКСПРЕССИРУЕМОГО В HANSENULA POLYMORPHA ИЗ КОНСТРУКТА, КОДИРУЮЩЕГО CL-H6-K-E1, И ПРОЦЕССИНГ Н6-СОДЕРЖАЩИХ БЕЛКОВ IN VITRO
Анализировали эффективность удаления лидерного пептида CL из белка CL-H6-K-E1, экспрессируемого в Н.polymorpha, а также эффективность последующего процессинга in vitro с целью удаления адаптерного пептида Н6 с гистидиновой меткой (Н6 (his-tag)), а также Endo Lys-C сайта процессинга. Поскольку HCV E1s (аминокислоты 192-326) экспрессировался как белок CL-H6-K-E1 с N-концевой His-K-меткой, быструю и эффективную очистку можно осуществить так, как описано в Примере 17. Профиль элюции IMAC-хроматографической очистки белков Н6-К-Е1 (и возможно остаточного CL-H6-K-E1) показан на Фиг.42. После Na-ДДС-ПААГ электрофореза с окрашиванием геля серебром и анализа вестерн-блоттингом с использованием специфического моноклонального антитела, направленного против E1 (IGH201) (Фиг.43), объединяли в пул элюированные фракции 63-69, содержащие рекомбинантные E1s продукты («IMAC-пул») и подвергали их обработке эндопротеиназой Lyc-C (Roche) в течение ночи (соотношение фермент/субстрат 1/50 (масс./масс.), 37°С) для удаления Н6-К-слитого хвоста. Удаление непроцессированного слитого продукта осуществляли на этапе негативной IMAC-хроматографии на Ni-IDA-колонке, в результате чего собирали Endo-Lys-C-процессированные белки в проходящей фракции. Для этого образец белка, расщепленного эндопротеиназой Lys-C, после 10-кратного разведения смесью 10 мМ NaH2PO4·3H2O, 1% (об./об.) Empigen В, рН 7,2 (буфер В), наносили на Ni-IDA-колонку с последующим промыванием буфером В до тех пор, пока поглощение при 280 нм не достигало базового уровня. Проходящий поток собирали в разные фракции (1-40), которые подвергали скринингу на присутствие E1s-продуктов (Фиг.44). Объединяли фракции 7-28, содержащие интактный Е1, у которого N-концевой Н6-К (и возможно остаточный CL-H6-K) хвост был удален (с относительной молекулярной массой между примерно 15 кДа и примерно 30 кДа на основании миграции в Na-ДДС-ПААГ с последующим окрашиванием серебром или анализа вестерн-блоттингом с использованием специфического моноклонального антитела, направленного против Е1 (IGH201)) и в конце концов алкилировали их (инкубация с 5 мМ DTT в течение 30 мин при 37°С с последующей инкубацией с 20 мМ йодоацетамида в течение 30 мин при 37С).
Этот материал подвергали N-концевому секвенированию (расщепление по Эдману). С этой целью обрабатывали образцы белков N-гликозидазой F (Roche) (0,2 ед./мкг Е2, инкубация в течение 1 часа при 37°С в PBS/3% Empigen ВВ) или оставляли их необработанными. Гликозилированные и негликозилированные белки Е1 разделяли Na-ДДС-электрофорезом в ПААГ и проводили блоттинг на PVDF-мембране для дальнейшего анализа расщеплением по Эдману (анализ проводили на секвенаторе белков PROCISE™ 492, Applied Biosystems). На основании N-концевого секвенирования можно оценить количество правильно процессированного Е1 продукта (процессинг включает в себя правильное отщепление Н6-К-последовательонсти). Общее количество белковых продуктов рассчитывают в пмолях белка на основании интенсивности пиков, получаемых при расщеплении по Эдману. Затем для каждого конкретного белка (то есть для каждого "выявленного N-конца") оценивают мольн.% относительно общего количества. В данном эксперименте выявили только правильный N-конец белка Е1, yj не N-концы других процессированных вариантов Н6-К-Е1. На этом основании было установлено, что in vitro процессинг эндопротеиназой Lys-C (Endo Lys-C) белка Е1, представляющего собой Н6-К-Е1 (и возможно остаточного CL-H6-K-E1) до белка Е1 происходит с точностью более 95%.
ПРИМЕР 19
СПЕЦИФИЧЕСКОЕ УДАЛЕНИЕ НИЗКОГЛИКОЗИЛИРОВАННЫХ ФОРМ HCV E1 ГЕПАРИНОМ
Для выявления специфических этапов очистки для оболочечных белков HCV из дрожжевых клеток оценили связывание с гепарином. Известно, что гепарин связывается с несколькими вирусами и, соответственно, уже было высказано предположение о связывании с оболочкой HCV (Garson, J. A. et al. 1999). Для того, чтобы проанализировать это потенциальное связывание, биотилировали гепарин и анализировали взаимодействие с HCV E1 в титрационных микропланшетах, покрытых либо сульфонированным HCV E1 из Н.polymorpha, либо алкилированным HCV E1 из Н.polymorpha (оба получены как описано в Примере 16), либо алкилированным HCV E1 из культуры клеток млекопитающего, трансфицированных вектором экспрессии на основе вируса коровьей оспы. Неожиданно наблюдали сильное связывание только с сульфонированным HCV E1 из Н.polymorpha, тогда как связывание с HCV E1 из культуры клеток млекопитающего полностью отсутствовало. Посредством вестерн-блоттинга авторам удалось показать, что это связывание было специфичным для полос смеси белка HCV E1 с низкой молекулярной массой (Фиг.45), соответствующих низкогликозилированным зрелым HCV E1s. Из фиг.45 также видно, что сульфонирование не является необходимым для связывания гепарина, поскольку при ликвидации такого сульфонирования связывание по прежнему наблюдается для E1, имеющего низкую молекулярную массу (дорожка 4). Алкилирование, напротив, существенно снижает это связывание, однако это может быть вызвано специфическим агентом алкилирования (йодоацетамидом), использованным в этом примере. Это связывание продемонстрировало еще и промышленную применимость CL-HVC-оболочечных экспрессионных кассет для дрожжей, поскольку можно специфически обогатить препараты HCV E1 для получения препарата с белками HCV E1, имеющими более высокую степень гликозилирования (то есть, у них оккупировано больше сайтов гликозилирования).
ПРИМЕР 20
ФОРМИРОВАНИЕ И АНАЛИЗ ВИРУСОПОДОБНЫХ ЧАСТИЦ (VLPS)
Превращение оболочечных белков HCV E1 и Е2, экспрессируемых в Н.polymorpha (Примеры 16-18) в VLPs, осуществляли по существу так, как описано Depla et al. в WO 99/67285 и Bosman et al. в WO 01/30815. Вкратце, после культивирования трансформированных клеток Н.polymorpha, во время которого экспрессировались оболочечные белки HCV, собирали клетки, лизировали их в GuHCl и сульфонировали как описано в Примере 17. Затем очищали содержащие гистидиновую метку белки IMAC-хроматографией и концентрировали ультрафильтрацией как описано в Примере 17.
ФОРМИРОВАНИЕ VLP ИЗ ОБОЛОЧЕЧНЫХ БЕЛКОВ HCV С СУЛЬФОНИРОВАННЫМИ CYS-ТИОЛЬНЫМИ ГРУППАМИ
Концентрированные оболочечные белки HCV, сульфонированные во время процедуры выделения, не подвергали восстанавливающей обработке и наносили их на колонку для хроматографии с вытеснением по размеру частиц (Superdex G200, Pharmacia), уравновешенную PBS, 1% (об./об.) Empigen. Анализировали элюированные фракции Na-ДДС-ПААГ электрофорезом и вестерн-блоттингом. Объединяли фракции с относительной молекулярной массой от примерно 29 до примерно 15 кДа (на основании миграции на Na-ДДС-ПААГ), концентрировали их и наносили на Superdex G200, уравновешенную PBS, 3% (масс./об.) бетаина, для того, чтобы вызвать образование вирусоподобных частиц (VLP). Объединяли фракции, концентрировали и обессоливали до PBS, 0,5% (масс./об.) бетаина.
ФОРМИРОВАНИЕ VLP ИЗ ОБОЛОЧЕЧНЫХ БЕЛКОВ HCV С НЕОБРАТИМО МОДИФИЦИРОВАННЫМИ CYS-ТИОЛЬНЫМИ ГРУППАМИ
Для того, чтобы превратить сульфонированные Cys-тиольные группы в свободные Cys-тиольные группы, концентрированные оболочечные белки HCV, сульфонированные во время процедуры выделения, подвергали восстанавливающей обработке (инкубация в присутствии 5 мМ DTT в PBS). Необратимую модификацию Cys-тиольных групп осуществляли (1) инкубацией в течение 30 мин в присутствии 20 мМ йодацетамида, или (2) инкубацией в течение 30 мин в присутствии 5 мМ N-этилмалеимида (NEM) и 15 мМ биотин-N-этилмалеимида. Затем наносили белки на колонку для хроматографии с вытеснением по размеру частиц (Superdex G200, Pharmacia), уравновешенную PBS, 1% (об./об.) Empigen в случае блокирования йодоацетамидом, или PBS, 0,2% CHAPS в случае блокирования посредством NEM и биотин-NEM. Анализировали элюированные фракции Na-ДДС-ПААГ-электрофорезом и вестерн-блоттингом. Объединяли фракции с относительной молекулярной массой от примерно 29 до примерно 15 кДа (на основании миграции в Na-ДДС-ПААГ), концентрировали их и наносили на колонку Superdex G200, уравновешенную PBS, 3% (масс./об.) бетаина, для того, чтобы вызвать образование вирусоподобных частиц. Фракции объединяли, концентрировали и обессоливали до PBS, 0,5% (масс./об.) бетаина в случае блокирования йодоацетамидом, или PBS, 0,05% CHAPS в случае блокирования с помощью NEM и биотин-NEM.
ФОРМИРОВАНИЕ VLP ИЗ ОБОЛОЧЕЧНЫХ БЕЛКОВ HCV С ОБРАТИМО МОДИФИЦИРОВАННЫМИ CYS-ТИОЛЬНЫМИ ГРУППАМИ
Для того, чтобы превратить сульфонированные Cys-тиольные группы в свободные Cys-тиольные группы, сконцентрированные оболочечные белки HCV, сульфонированные во время процедуры выделения, подвергали восстанавливающей обработке (инкубация в присутствии 5 мМ DTT в PBS). Необратимую модификацию Cys-тиольных групп осуществляли инкубацией в течение 30 мин в присутствии дитиодипиридина (DTDP), дитиокарбамата (DTC) или цистеина. Затем наносили белки на колонку для хроматографии с вытеснением по размеру частиц (Superdex G200, Pharmacia), уравновешенную PBS, 1% (об./об.) Empigen. Элюированные фракции анализировали Na-ДДС-ПААГ-электрофорезом и вестерн-блоттингом. Объединяли фракции с относительной молекулярной массой от примерно 29 до примерно 15 кДа (на основании миграции в Na-ДДС-ПААГ), концентрировали их и наносили на Superdex G200, уравновешенный PBS, 3% (масс./об.) бетаина, для того, чтобы вызвать образование вирусоподобных частиц (VLP). Объединяли фракции, концентрировали и обессаливали до PBS, 0,5% (масс./об.) бетаина.
Профили элюции хроматографии с вытеснением по размерам частиц в PBS, 3% (масс./об.) бетаина для получения VLPs из Е2-Н6, экспрессированного в Н. polymorpha, показаны на Фиг.46 (сульфонированный) и Фиг.47 (алкилированный йодоацетамидом).
Профили элюции хроматографии с вытеснением по размерам частиц в PBS, 3% (масс./об.) бетаина для получения VLPs из Е1, экспрессированного в Н.polymorpha, показаны на Фиг.48 (сульфонированный) и Фиг.49 (алкилированный йодоацетамидом). Полученные VLPs были проанализированы Na-ДДС-ПААГ-электрофорезом и вестерн-блоттингом как показано на Фиг.50.
АНАЛИЗ РАЗМЕРОВ VLPS, ОБРАЗОВАННЫХ ОБОЛОЧЕЧНЫМИ БЕЛКАМИ HCV, ЭКСПРЕССИРОВАННЫМИ В Н.polymorpha
Размер частиц VLP определяли динамическим светорассеяньем. Для экспериментов по светорассеянью применяли анализатор размеров частиц (Model Zetasizer 100 HS, Malvern Instruments Ltd., Malvern, Worcester, UK), который управлялся с помощью программного обеспечения для фотоно-корреляционной спектроскопии (PCS). Фотоно-корреляционная спектроскопия или динамическое светорассеянье (DLS) представляет собой оптический способ измерения броуновского движения и его соотнесения с размером частиц. Свет от непрерывного видимого лазерного луча направляют через совокупность макромолекул или частиц в суспензии, движущихся в результате броуновского движения. Некоторая часть лазерного света рассеивается частицами, и этот рассеянный свет измеряют фотоумножителем. Флуктуации интенсивности рассеянного света превращают в электрические импульсы и подают их на коррелятор. Это генерирует функцию автокорреляции, направляемую в компьютер, который производит соответствующий анализ данных. Использованным лазером был монохроматический когерентный He-Ne лазер мощностью 10 мВт с фиксированной длиной волны 633 нм. Для каждого образца делали 6 последовательных измерений. Результаты этих экспериментов суммированы в Таблице 5.
Результаты анализа динамического светорассеяния указанных VLP-композиций оболочечных белков HCV, экспрессированных в Н.polymorpha. Размеры VLP частиц приведены как их средний диаметр.
То наблюдение, что сульфонированный HCV E1, полученный из Н.polymorpha, образует частицы с размерами в том же диапазоне, что и алкилированный HCV E1 из Hansenula, является удивительным. Такого эффекта не ожидали, поскольку сильное (до 8 Cys-тиольных групп может быть модифицировано на HCV E1) общее увеличение отрицательных зарядов вследствие сульфонирования должно вызвать ионное отталкивание между субъединицами. Другие протестированные агенты, обратимо модифицирующие цистеин, также делали возможным формирование частиц, однако получаемые таким путем HCV E1 оказались менее стабильными, чем сульфонированный материал, приводящий к агрегации HCV E1 на основе дисульфидов. Для применения этих других обратимых блокаторов нужна дальнейшая оптимизация условий.
ПРИМЕР 21
АНТИГЕННАЯ ЭКВИВАЛЕНТНОСТЬ ПРОДУЦИРУЕМОГО HANSENULA HCV Е1-Н6 И HCV E1, ПРОДУЦИРУЕМОГО КЛЕТКАМИ МЛЕКОПИТАЮЩЕГО, ИНФИЦИРОВАННЫМИ ВИРУСОМ КОРОВЬЕЙ ОСПЫ
Реактивность продуцируемого Hansenula HCV E1-H6 с сыворотками от хронических носителей HCV сравнили с реактивностью HCV E1, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, как описано Depla et al. в WO 99/67285. Оба протестированных препарата HCV-E1 состояли из VLP's, в которых белки HCV E1 были алкилированы N-этилмалеимидом и биотин-N-этилмалеимидом. Реактивности обоих VLP-препаратов HCV E1 с сыворотками от хронических носителей HCV определяли твердофазным иммуноферментным анализом (ELISA). Результаты суммированы в Таблице 6. Как можно заключить из Таблицы 6, между HCV E1, экспрессированным в клетках млекопитающего, инфицированных HCV-рекомбинантным вирусом коровьей оспы, и HCV E1, экспрессированным в Н.polymorpha, не было различий по реактивности.
Антигенность Е1, продуцируемого в культуре клеток млекопитающего или продуцируемого в Н.polymorpha оценивали на панели сывороток от людей, являющихся хроническими носителями HCV. Для этой цели биотинилированный Е1 связывали с планшетами для ELISA, покрытыми стрептавидином. После этого добавляли человеческие сыворотки в разведении 1/20 и связанные иммуноглобулины из сывороток, связавшихся с Е1, выявляли с помощью специфичного вторичного кроличьего антитела против IgG-Fc человека, меченного пероксидазой. Результаты выражены как значения оптической плотности (ОП). Усредненные значения являются средними значениями оптических плотностей всех тестированных образцов сыворотки.
ПРИМЕР 22
ИММУНОГЕННАЯ ЭКВИВАЛЕНТНОСТЬ HCV E1-H6, ПРОДУЦИРУЕМОГО HANSENULA, И HCV Е1, ПРОДУЦИРУЕМОГО КЛЕТКАМИ МЛЕКОПИТАЮЩЕГО, ИНФИЦИРОВАННЫМИ ВИРУСОМ КОРОВЬЕЙ ОСПЫ
Иммуногенность HCV E1-H6, продуцируемого Hansenula, сравнивали с иммуногенностью HCV E1, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, как описано Depla et al. в WO 99/67285. Оба протестированных препарата HCV E1 состояли из VLP's, в которых белки HCV E1 были алкилированы иодоацетоамидом. В состав обоих препаратов VLP вводили квасцы и инъецировали оба препарата мышам Balb/c (3 внутримышечной/подкожной инъекции с интервалом в 3 недели, причем каждая инъекция состояла из 5 мкг E1 в 125 мкл, содержащих 0,13% Alhydrogel, Superfos, Дания). У мышей брали кровь через десять дней после третьей иммунизации.
Результаты этих экспериментов показаны на Фиг.51. Для верхней части Фиг.51 определяли антитела, выработанные после иммунизации VLPs из E1, продуцированного в клетках млекопитающего. Титры антител определяли способом ELISA (см. Пример 21), при котором E1, продуцированным в клетках, млекопитающего (М), или E1, продуцированным в Hansenula (H), покрывали непосредственно ELISA твердую подложку, после чего блокировали планшеты для ELISA казеином. Для нижней части Фиг.51 определяли антитела, выработанные после иммунизации VLPs из E1, продуцированного в Hansenula. Титры антител определяли способом ELISA (см. Пример 21), при котором E1, продуцированным в клетках млекопитающего (М), или E1, продуцированным в Hansenula (H), покрывали непосредственно ELISA твердую подложку, после чего блокировали планшеты для ELISA казеином.
Определяемые титры антител были титрами, представляющими собой конечные точки. Титр, представляющий собой конечную точку, определяют как разведение сыворотки, приводящее к оптической плотности (определяемой способом ELISA), равное двукратному среднему базовому уровню в данном анализе.
Фиг.51 показывает, что между иммуногенными свойствами обоих E1-композиций не было существенных различий и что определяемые титры антител не зависят от антигена, использованного в ELISA для титрования до конечной точки.
HCV E1 дрожжевого происхождения при вакцинации индуцировал защитный ответ, сходный с защитным ответом, полученным при вакцинации аликилированым HCV E1, полученным из культуры клеток млекопитающего. Этот последний ответ был способен предотвращать хроническое развитие HCV после острой инфекции.
ПРИМЕР 23
АНТИГЕННЫЙ И ИММУНОГЕННЫЙ ПРОФИЛЬ ПРОДУЦИРУЕМОГО HANSENULA HCV E1-H6, КОТОРЫЙ ЯВЛЯЕТСЯ СУЛЬФОНИРОВАННЫМ
Реактивность продуцируемого Hansenula HCV E1-H6 с сыворотками от хронических носителей HCV сравнивали с реактивностью HCV E1, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, как описано Depla et al. в WO 99/67285. Оба протестированных препарата HCV-E1 состояли из VLP's, в которых продуцированные Hansenula белки HCV E1 были сульфонированы, а продуцированные клетками млекопитающего HCV E1 были алкилированы. Результаты даны в Таблице 7. Хотя общая (средняя) реактивность была идентичной, в индивидуальных сыворотках были замечены некоторые значительные. различия. Это значит, что сульфонированный материал представляет по меньшей мере некоторые из своих эпитопов способом, отличным от алкилированных HCV E1.
Иммуногенность продуцируемого Hansenula HCV E1-H6, который был сульфонирован, сравнивали с иммуногенностью продуцируемого Hansenula HCV E1-H6, который был алкилирован. Оба тестированных препарата HCV-E1 состояли из VLP's. Оба VLP препарата были составлены с квасцами и инъецированы мышам Balb/c (3 внутримышечные/подкожные инъекции с трехнедельными интервалами между каждыми, причем каждая состояла из 5 мкг E1 в 125 мкл, содержащих 0,13% Alhydrogel, Superfos, Denmark). У мышей брали кровь через 10 дней после третьей иммунизации.
Определяли титры антител подобно тому, что описано в Примере 22. Неожиданно оказалось, что иммунизация сульфонированным материалом приводила к более высоким титрам антител, независимо от антигена, использованного в ELISA для оценки этих титров (Фиг.51, верхняя панель: титрование антител, вырабатываемых против алкилированного E1; нижняя панель: титрование антител, вырабатываемых против сульфонированного E1; "А": алкилированный E1, нанесенный на планшет для ELISA; "S": сульфонированный Е1, нанесенный на планшет для ELISA). Однако в этом эксперименте индивидуальные титры различны в зависимости от антигена, использованного для анализа, что подтверждает наблюдение, отмеченное с сыворотками HCV пациентов. Следовательно, HCV E1, у которого цистеиновые тиольные группы модифицированы обратимым образом, может быть более иммуногенным и, таким образом, иметь более высокую активность в качестве вакцины, защищающей от HCV (хронической инфекции). В добавление к этому, менее вероятна индукция ответа на нео-эпитопы, индуцированные необратимым блокированием.
Антигенность алкилированного Е1 (продуцируемого в культуре клеток млекопитающего) или сульфонированного Е1-Н6 (продуцируемого в Н.polymorpha) оценивали на панели сывороток от людей, являющихся хроническими носителями HCV («сыворотки пациентов») и на панели контрольных сывороток («сыворотки доноров крови»). Для этой цели связывали Е1 с планшетами для ELISA, после чего планшеты далее насыщали казеином. Добавляли человеческие сыворотки в разведении 1/20 и выявляли связанные иммуноглобулины с помощью вторичных специфических кроличьих антител против человеческого IgG-Fc, меченных пероксидазой. Результаты выражены как значения оптической плотности (ОП). Усредненные значения являются средними значениями оптических плотностей всех тестированных проб
сыворотки.
ПРИМЕР 24
ИДЕНТИЧНЫЕ АНТИГЕННЫЕ РЕАКТИВНОСТИ HCV E1-H6, ПРОДУЦИРУЕМОГО HANSENULA, И HCV E1, ПРОДУЦИРУЕМОГО КЛЕТКАМИ МЛЕКОПИТАЮЩЕГО, ИНФИЦИРОВАННЫМИ ВИРУСОМ КОРОВЬЕЙ ОСПЫ, С СЫВОРОТКАМИ ОТ ВАКЦИНИРОВАННЫХ ШИМПАНЗЕ
Сравнивали реактивности E1, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, и E1-H6, продуцируемого Hansenula (оба алкилированы), с сыворотками от вакцинированных шимпанзе и с моноклональными антителами. Для этого наносили указанные белки E1 прямо на планшеты для ELISA с последующим насыщением этих планшетов казеином. Определяли конечные титры антител, связывающих белки E1, нанесенные на планшеты для ELISA, для сывороток шимпанзе и для специфичных мышиных моноклональных антител, которые были получены от животных, иммунизированных белком E1, продуцируемым клетками млекопитающего. Определение конечного титра выполняли так, как описано в Примере 22. Использованными мышиными моноклональными антителами были IGH201 (см. Пример 15), IGH198 (IGH198=23С12 в Maertens et al. в WO 96/04385), IGH203 (IGH203=15G6 в Maertens et al. в WO 96/04385) и IGH202 (IGH202=3F3 в Maertens et al. в WO 99/50301).
Как можно заключить из Фиг.53, при тестировании белка E1, продуцированного как Hansenula, так и клеткам млекопитающего, реактивности семи разных шимпанзе идентичны. Реактивности моноклональных антител против белка HCV E1 также почти равны. Два из шимпанзе (Yoran и Marti) были включены в исследовании профилактической вакцины и были способны избежать острой инфекции при инфицировании, тогда как контрольное животное не избежало этой инфекции. Пять других шимпанзе (Ton, Phil, Marcel, Femma) были включены в исследования терапевтической вакцинации и при иммунизациях HCV E1 продемонстрировали уменьшение поражения печени согласно результатам определения ALT (аланинаминотрансфераза) в сыворотке и/или гистологическому индексу активности при биопсии печени.
Результаты, полученные в этом эксперименте, явно отличаются от того, что было обнаружено Mustilli и соавторы (Mustili, A.C. et al. 1999), которые экспрессировали белок HCV E2 как в Saccharomyces cerevisiae, так и в Kluyveromyces lactis. Очищенный белок E2, продуцируемый дрожжами, отличался от HCV E2, продуцированного клетками млекопитающего (СНО, клетки яичника китайского хомячка) в том, что с сыворотками от шимпанзе, иммунизированных HCV E2, продуцированным клетками млекопитающего, наблюдали более низкую активность, тогда как реактивность с моноклональными антителами была более высокой для продуцируемого дрожжами белка HCV E2.
ПРИМЕР 25
ГЛИКОПРОФИЛИРОВАНИЕ HCV E1 УГЛЕВОДНЫМ ЭЛЕКТРОФОРЕЗОМ С ИСПОЛЬЗОВАНИЕМ ФЛУОРОФОРА (FACE)
Сравнивали профили гликозилирования HCV E1, продуцируемого Hansenula, и HCV E1, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы, как описано Depla et al. в WO 99/67285. Это осушествляли углеводным электрофорезом с использованием флуорофора (FACE). Для этого из E1s, продуцированного клетками млекопитающего или Hansenula, с помощью пептид-N-гликозидазы (PNGase F) высвобождали олигосахариды и метили ANTS (перед обработкой пептид-N-гликозидазой белки E1 алкилировали йодоацетамидом). Разделяли ANTS-меченые олигосахариды электрофорезом в ПААГ в 21%-ном полиакриламидном геле при силе тока 15 мА при 4°С в течение 2-3 часов. Из Фиг.54 сделали вывод, что олигосахариды на белке E1, продуцированном клетками млекопитающего, и на белке Е1-Н6, продуцированном Hansenula, мигрируют подобно олигомальтозе со степенью полимеризации от 7 до 11 моносахиридов. Это свидетельствует о том, что экспрессионная система Hansenula удивительным образом приводит к белку E1, который не гипергликозилирован и имеет цепи сахаров с длиной, сходной с цепями сахаров, добавляемых к белкам E1, продуцируемым в клетках млекопитающего.
ПРИМЕР 26
СЕКВЕНИРОВАНИЕ N-СВЯЗАННОГО ОЛИГОСАХАРИДА, ПОЛУЧЕННОГО ИЗ E1s, ПРОДУЦИРУЕМОГО SACCHAROMYCES И HANSENULA, И ИЗ E1s, ПРОДУЦИРУЕМОГО КЛЕТКАМИ МЛЕКОПИТАЮЩЕГО, ИНФИЦИРОВАННЫМИ HCV-РЕКОМБИНАНТНЫМ ВИРУСОМ КОРОВЬЕЙ ОСПЫ
Белок E1s (225 мкг), очищенный из культуры Saccharomyces или Hansenula (см. Примеры 15-16) или из культуры клеток RK13, инфицированных HCV-рекомбинантным вирусом коровьей оспы (см. Maertens et at. в WO 96/04385) и представленный в PBS, 0,5% бетаина, разбавляли инкубационным буфером для дегликозилирования (50 мМ Na2HPO4, 0,75% Nonidet P-40) до конечной концентрации 140 мкг/мл. Концентрированной Н3РО4 доводили рН этого раствора до рН 5,5. К этому раствору добавляли 2 ед. PNGase F (пептид-N4-ацетил-бета-глюкозаминил)-аспарагинамидаза из Flavobacterium meningosepticum; EC 3.5.1.52, получена от Roche) и инкубировали этот образец в течение ночи при 37°С. После инкубации в течение ночи доводили рН этого раствора до рН 5,5 концентрированной Н3РО4. Затем осаждали белки и олигосахариды добавлением 4-х объемов ацетона (при -20°С) и инкубировали эти смеси при -20°С в течение 15 мин. Центрифугировали образцы при 4°С в течение 5 мин при 13000 об/мин. Отбрасывали ацетоновый супернатант и после добавления 150 мкл ледяного 60%-ного метанола инкубировали осадок при -20°С в течение 1 часа. Собирали этот метанольный супернатант, содержащий высвобожденные олигосахариды, и сушили роторным выпариванием (SpeedVac).
Растворяли высушенные гликаны белка E1s, а также эталонные олигосахариды (все от Glyco, Bicester, UK; см. Фиг.55) Man-9 (11 моносахаридных единиц), Man-8 (10 моносахаридных единиц), Man-7 (9 моносахаридных единиц), Man-6 (8 моносахаридных единиц) и Man-5 (7 моносахаридных единиц) в 5 мкл 2-аминобензамидного (2-АВ) метящего реагента (±0,35М 2-АВ + ±1М NaCNBH3 в 30% НОАс/70% DMSO) с получением конечной концентрации гликанов между 5 и 100 мкМ. Затем инкубировали этот раствор гликанов в течение 2 часов при 65°С. Через 30 мин перемешивали образцы на вортексе. Избыток 2-аминобензамида после конъюгации удаляли следующим образом. Образец разводили в 16 мкл очищенной воды (MilliQ) и наносили на колонку с Sephadex G-10 (диаметр 1 см, высота 1,2 см, Amersham Biosciences, присоединена к системе VacElut, Varian) после того, как колонку продували досуха.
Элюировали меченые олигосахариды нанесением двух порций по 100 мкл очищенной воды (MilliQ) на колонку. Высушивали элюаты эталонных углеводов (Man-9, Man-8, Man-7 и Man-6) и хранили их при -70°С до анализа способом ВЭЖХ. Распределяли элюаты образцов белка E1s, а также эталонного гликана Man-9 по 4-м пронумерованным пробиркам для ПЦР и высушивали. Проводили реакции, как указано в Табл.8, причем всем реакциям давали проходить в течение ночи при 37°С, кроме реакции в пробирке 3, которую останавливали через 1 час. Конечными концентрациями использованных экзогликозидазных ферментов (все получены от Glyko, Bicester, UK) были: для α1-2-маннозидазы (из Aspergillus saitoi) - 2 миллиединицы/мл; для α-маннозидазы (Jack Bean) - 50 ед./мл; для β-маннозидазы (Helix pomatia) - 4 ед./мл.
Сводка по реакционным смесям для секвенирования олигосахаридов
На Фиг.56 показана высшая олигоманноза, состоящая из 10 маннозных группировок, присоединенных к хитобиозе. Каждый терминальный маннозный остаток связан α(1-3)-связью с неконцевым маннозным остатком. Олигоманноза на Фиг.56 полностью устойчива к расщеплению экзогликозидазой α-(1-2)-маннозидазой. Длительная (в течение ночи) инкубация олигоманнозы по Фиг.56 с экзогликозидазой α-маннозидазой приводит к расщеплению всех α-связей, а именно, α-(1-2), α-(1-3), α-(1-6), но не β-связей. Получившимся олигосахаридом, таким образом, должна быть 4'-β-маннозилхитобиоза. Эту 4'-β-маннозилхитобиозную группировку можно превратить в маннозу и хитобиозу действием экзогликозидазы β-маннозидазы. В соответствии со спецификациями поставщика (Glyko), α-маннозидаза полностью превращает эталонный олигосахарид Man-6 (см. Фиг.55 D) в 4'-маннозилхитобиозу, и сообщается, что ее дальнейшее превращение в маннозу и хитобиозу тоже является полным.
На Фиг.57 показана высшая олигоманноза, состоящая из 9 маннозных группировок, присоединенных к хитобиозе. В этой олигоманнозе один концевой маннозный остаток связан α(1-2)-связью с неконцевым маннозным остатком. При действии экзогликозидазы α-(1-2)-маннозидазы указанная α-(1-2)-связанная манноза удаляется. При последующем действии α-маннозидазы и β-маннозидазы получаются продукты реакции, описанные для олигоманнозы согласно Фиг.56. В соответствии со спецификациями поставщика (Glyko), α-(1-2)-маннозидаза способна превращать эталонные олигосахариды Man-9 и Man-6 в Man-5 (см. Фиг.55) с эффективностью более 90%.
На Фиг.58 показана эталонная высшая олигоманноза Man-9, состоящая из 9 маннозных группировок, присоединенных к хитобиозе. В этой олигоманозе концевой маннозный остаток связан α(1-2)-связью с неконцевым маннозным остатком. При действии экзогликозидазы α-(1-2)-маннозидазы Man-9 превратится, таким образом, в Man-5, в соответствии со спецификацией поставщика, более чем на 90%. Последующее расщепление α-маннозидазой превращает Man-5 в 4'-β-маннозилхитобиозу.
Содержимое разных реакционных пробирок, как указано в Табл.8, высушивали на центрифужном вакуумном испарителе или в лиофилизаторе и хранили при -70°С до анализа способом ВЭЖХ. Перед нанесением на колонку каждый образец (белок E1s и эталон) растворяли в 25 мкл воды и наносили на колонку TSK gel-Amide-80 (0,46×25 см, Tosoh Biosep), подсоединенную к установке ВЭЖХ Waters Alliance.
Разделение олигосохаридов осуществляли при температуре окружающей среды при 1,0 мл/мин. Растворитель А состоял из 0,1% уксусной кислоты в ацетонитриле, растворитель В состоял из 0,2% уксусной кислоты и 0,2% триэтиламина в воде. Разделение олигосахаридов, меченных 2-аминобинзамидом, осуществляли с использованием 28% В, изократического для 5 объемов колонки, за которым следовало линейное увеличение до 45% В для пятнадцати объемов колонки.
Эталонный олигосахарид Man-6 элюируется при 53±1 мин, Man-7 элюируется при 59±1 мин, Man-8 при 67±2 мин, а Man-9 при 70±1 мин; 4'-β-маннозилхитобиоза элюируется при 10±1 мин, а хитобиоза при 6±1 мин (не показано). Пример приведен для реакционного продукта Man-9 после инкубации в течение ночи без экзогликозидаз (кривая 1 хроматограммы на Фиг.63; только Man-9), после инкубации в течение ночи с α-(1-2)-маннозидазой (кривая 2 хроматограммы на Фиг.63; смесь Man-5 и Man-6), после инкубации с α-маннозидазой в течение 1 часа или ночи (кривые 3 и 4, соответственно, хроматограммы на Фиг.63; только 4'-β-маннозилхитобиоза) и после инкубации в течение ночи с α-и β-маннозидазой (кривая 5 хроматограммы на Фиг.63; только хитобиоза). Кривая 6 хроматограммы на Фиг.63 показывает примененный градиент растворителя.
Продуктами реакции олигосахаридов белка E1s, продуцируемого Saccharomyces (получено после обработки PNGaseF), без экзогликозидаз были главным образом четыре присутствующих углевода, элюируемые при 59±1 мин (15%), 67±1 мин (45%), 70±1 мин (25%) и 75±1 мин (15%). Общее содержание Man(8)-GlcNAc(2) и Man(9)-GlcNAc(2) в белке E1s, продуцируемом Saccharomyces, составляло около 65%. В реакции с α-1-2-маннозидазой исчезли только углеводы со временем удерживания 70±1 мин. Интенсивность углевода со временем удерживания 75±1 мин осталась той же, а интенсивность углевода со временем удерживания 67±1 мин увеличилась. Это значит, что не все концевые маннозные единицы имеют α-(1-2)-конфигурацию. После инкубации в течение ночи с α-маннозидазой все углеводные цепи были восстановлены до 4'-β-маннозилхитобиозной группировки. Это значит, что углевод является высшей маннозой и все маннозные остатки, кроме одного, имеют α-конфигурацию. Восстановление этой 4'-β-маннозилхитобиозной группировки до хитобиозы обнаружилось после инкубации в течение ночи с β-маннозидазой. Полученные хроматограммы изображены на Фиг.64 и были получены при тех же условиях, что описаны для хроматограммы на Фиг.63. Результаты суммированы в Табл.9.
Неожиданно такие же эксперименты, повторенные с E1s, продуцированным клетками, инфицированными вирусом коровьей оспы, показали совершено другую картину. В реакционной смеси без ферментов присутствовала сложная смесь углеводов (см. Фиг.65 и Таблицу 9). Общее содержание моносахарид(8)-GlcNAc(2) и моносахарид(9)-GlcNAc(2) составляло 37%. После реакции с α-1-2-маннозидазой исчезли углеводы с величинами времени удерживания 70±1 мин и 59±1 мин. После инкубации в течение ночи с α-маннозидазой осталось значительное количество моносахарид(6)-GlcNAc(2) в дополнение к продукту, представляющему собой 4'-β-маннозилхитобиозу. Это указывает на то, что одна из олигосахаридных цепей устойчива к разложению α-маннозидазой. Это можно объяснить присутствием одного или двух глюкозных остатков, присоединенных к Manα(1-2)-терминированной цепи N-связанного олигосахарида. Предполагаемая структура такого олигосахарида, содержащего глюкозу, представлена на Фиг.62. Возможные реакционные продукты олигосахаридов, содержащих глюкозу, приведены в Таблице 10. Поскольку после α-1-2-маннозидазной реакции не остаются Man-7-эквивалентные олигосахариды (то есть олигосахариды, состоящие из 9 моносахаридов), эти глюкозные остатки скорее всего связаны с В-цепью олигосахаридной структуры, приведенной на Фиг.62. Однако нельзя исключить, что обе цепи, А и В, олигосахарида на Фиг.62 частично терминированы глюкозой.
Восстановление этой 4'-β-маннозилхитобиозной группировки до хитобиозы обнаружилось после инкубации в течение ночи с β-маннозидазой. Полученные хроматограммы изображены на Фиг.65 и были получены при тех же условиях, что описаны для хроматограмм на Фиг.63-64. Полученные результаты суммированы в Табл.9.
Такие же эксперименты были повторены с белком E1s, продуцированым Hasenula, и неожиданно они показали совершенно другую картину. В реакции без ферментов присутствовали главным образом два углевода с временем удерживания 67±2 мин и 70±1 мин, что соответствует Man-8 и Man-9, соответственно. Общее содержание Man(8)-GlcNAc(2) и Man(9)-GlcNAc(2) в белке E1s, который продуцирован Hasenula, составляло около 90%. После реакции с α-(1-2)-маннозидазой углеводы были восстановлены главным образом до Man-5 со временем удерживания 45±1 мин и Man-6 со временем удерживания 53±1 мин. После инкубации в течение ночи с α-маннозидазой все углеводные цепи были восстановлены до 4'-β-маннозилхитобиозной группировки. Это значит, что углевод является высокоманнозным и все маннозные остатки, кроме одного, имеют α-конфигурацию. Восстановление этой 4'-β-маннозилхитобиозной группировки до хитобиозы стало очевидным после инкубации в течение ночи с β-маннозидазой. Полученные хроматограммы изображены на Фиг.66 и они были получены при тех же условиях, что описаны для хроматограмм на Фиг.63-65.
Полученные результаты суммированы в Табл.9.
Олигоманнозы, получающиеся при расщеплении олигоманноз, полученных из E1s, продуцируемых Saccharomyces ("Sc") и Hansenula ("Hp"), a также из E1s, продуцируемого клетками млекопитающего, инфицированными HCV-рекомбинантным вирусом коровьей оспы ("Vac"). Указаны разные олигоманнозы и значения их хроматографического времени удерживания ("Rt" в минутах), а процентное содержание данной олигоманнозы относительно общего содержания олигоманноз (верхний ряд), а также наиболее вероятная структура для каждой наблюдаемой олигоманнозы указаны с отсылкой к любому из Фиг.55-62. Олигоманнозы с концевыми α-(1-3)-маннозами отмечены зонком "°". Олигоманнозы с концевыми глюкозами отмечены знаком "*", для некоторых сделана отсылка "из 62*", означающая, что данную структуру можно получить из структуры, приведенной на Фиг.62. "1" означает реакцию без экзогликозидаз, "2" означает реакцию с α-(1-2)-маннозидазой. Олигоманноза со временем удерживания 45±1 мин предположительно является олигоманнозой, содержащей 5 маннозных остатков, связанных с хитобиозой. Олигоманноза со временем удерживания 75±1 мин предположительно является олигоманнозой, содержащей 10 маннозных остатков, связанных с хитобиозой.
55.D
59°
57°
61°
56°
55.Е
60°
59°
57°
61°
56°
55.Е
55.Е
из 62* и Табл.10
55.D
55.С
55.В
55.Е
55.D
Продукты, содержащие глюкозу N-связанных олигосахаридов после реакции с α-(1-2)-маннозидазой или α-(1-2)-маннозидазой и α-маннозидазой
ПРИМЕР 27
ОККУПАЦИЯ САЙТОВ N-ГЛИКОЗИЛИРОВАНИЯ В РЕКОМБИНАНТНОМ HCV E1
В зависимости от количества оккупированных сайтов N-гликозилирования, E1s демонстрирует разное миграционное поведение при анализе посредством Na-ДДС-ПААГ-электрофореза. На основании этого свойства можно оценить среднее количество оккупированных сайтов N-гликозилирования в E1 продукте. Для этого образцы очищенного E1-продукта подвергали Na-ДДС-электрофорезу в ПААГ и окрашиванию красителем кумасси бриллиантовым синим (Coomassie Brilliant Blue) (Фиг.67) и анализировали далее с помощью пакета программного обеспечения ImageMaster 1D Prime (Pharmacia). Вкратце, сканировали гель и для каждого конкретного белка оценивали полосу и % присутствия (ее интенсивность относительно суммарной интенсивности разных полос, вследствие чего сумма всех полос составляет 100%) (Табл.11). Следует отметить, что каждая конкретная полоса белка представляет E1s-молекулы с одним и тем же числом оккупированных сайтов N-гликозилирования.
Полученные результаты показали, что основная часть (>90%) E1-продукта, продуцируемого Hansenula, имеет число оккупированных сайтов N-гликозилирования, которое на один или более чем один сайт меньше, чем имеет белок E1s, полученный из экспрессионной системы на основе вируса коровьей оспы (как описали Maertens et al. в WO 96/04385). Если допустить, что в E1 продукте, полученном из вируса коровьей оспы, оккупированы все сайты N-гликозилирования (в которых последовательность "NNSS" (SEQ ID NO:73) в положении 233-236 в Е1 рассматривается как один сайт N-гликозилирования), вполне можно заключить, что среднее число оккупированных сайтов N-гликозилирования в белке Е1, экспрессируемом Hansenuta, не превосходит 80% от всех доступных сайтов N-гликозилирования.
Оценка среднего числа оккупированных сайтов N-гликозилирования в белках Е1, полученных из Hansenula polymorpha и экспрессионных систем коровья оспа/vero, Na-ДДС-электрофорезом в ПААГ и анализом интенсивности окрашивания красителем Кумасси бриллиантовый синий. Белковые полосы указаны по молекулярной массе. См. Фиг.67.
ПРИМЕР 28
ОККУПАЦИЯ САЙТОВ N-ГЛИКОЗИЛИРОВАНИЯ В РЕКОМБИНАНТНОМ HCV E2
Дегликозилировали ферментом PNGase F двести (200) мкг белка Е2-Н6, продуцированного Hansenula. Дегликозилированный E2s-H6 наносили на мини-гель (10 мкг/дорожка). Полосы белка обрабатывали трипсином и endoAsp-N. Определяли массы получившихся белков масс-спектрометрией Maldi-MS (метод высушенной капли и тонкого слоя).
Этот метод можно использовать для определения степени N-гликозилирования: во время дегликозилирования фермент PNGase F отщепляет полную цепь сахара и в то же время аспарагин (N) гидролизуется до аспарагиновой кислоты (D). Разница по массе между этими двумя аминокислотами составляет 1 Да, что можно определить масс-спектрометрией. Кроме того, гидролиз N до D создает новые сайта расщепления для фермента Asp-N.
Возможными сайтами гликозилирования в E2s являются N417, N423, N430, N448, N532, N540, N556, N576, N623 и N645 (см. Фиг.68). Анализ Maldi-MS показал для каждого из этих сайтов гликозилирования, что N-гликозилирование не полное, потому что после дегликозилирования посредством PNGase F были найдены пептиды либо с N, либо с D в сайте гликозилирования (разница по массе составляет 1 Да). Отношение числа D-остатков к числу N-остатков дает показатель средней оккупации одной сайта N-гликозилирования цепью сахара по всем белкам E2, экспрессируемым Hansenula и присутствующим в анализируемом образце. Эти результаты суммированы в Табл.12-14.
Из этих результатов рассчитали, что в среднем каждый сайт гликозилирования был гликозилирован примерно на 54%.
Процент гликозилирования, определенный по пептидам, являющимся продуктами действия трипсина, содержащими один сайт N-гликозилирования
Процент гликозилирования, определенный по пептидам, являющимся продуктами действия трипсина, содержащими два сайта N-гликозилирования
Процент гликозилирования, определенный для N478, в переваре Asp-N
ПРИМЕР 29
РЕАКТИВНОСТЬ СЫВОРОТОК ОТ ДОНОРОВ КРОВИ С HCV Е1, ПРОДУЦИРУЕМЫМ SACCHAROMYCES ИЛИ HANSENULA
Оба белка, E1s-H6, продуцируемый Saccharomyces (эспрессируемый с α-MF лидером), и E1s-H6, продуцируемый Hansenula (экспрессируемый с CL лидером), очищали, как описано в Примерах 15 и 16 и в заключении подвергали их алкилированию и процедуре образования VLP как описано в Примере 20. Адсорбировали оба белка прямо на титрационный микропланшет при 0,5 мкг/мл (1 час, 37°С) и после блокирования планшета (PBS-0,1% казеин, 1 час, 37°С) инкубировали сыворотки от прошедших скрининг на HCV негативных доноров крови в разведении 1/20 (PBS-0,5% казеин, 10% (масс//об/) сахароза, 0,2% (об//об.) Тритон Х-705, 1 час, 37°С). В заключении определяли связывание, используя вторичную кроличью анти-человеческий IgG-Fc специфическую антисыворотку, конъюгированную с пероксидазой (Dako, Denmark) в разведении 1/50000 (PBS-0,1% казеин, 1 час, комнатная температура), с последующим развитием окраски. Между всеми этапами трижды промывали планшеты PBS-0,05% (масс//об.) Твин-20. Для сравнения также анализировали эти сыворотки идентичным образом на E1s, полученном из клеток млекопитающего и продуцированном и очищенном как описали Depla et al. в WO 99/67285.
Уровень отсечки для этого анализа способом ELISA установили в двукратное среднее фона (то есть реактивность всех сывороток в тех же самых условиях, но со стрептавидином, адсорбированном на лунках).
По Табл.15 можно судить, что реактивность выше указанного уровня отсечки с Saccharomyces-продуцированным Е1 проявили многие (75%) сыворотки, тогда как некоторую реактивность выше указанного уровня отсечки с Hansenula-продуцированным Е1 проявили только немногие сыворотки (6%). Эту разницу в реактивности приписали присутствию концевых α(1-3)-манноз, связанных с α(1-2)-маннозами Saccharomyces-продуцированного Е1, как свидетельствует Пример 26. Young и соавторы (1998) ранее уже показали, что этот тип манноз также ответственен за реактивность человеческих сывороток с маннаном из Saccharomyces. Для дальнейшего подтверждения того, что реактивность с Saccharomyces-продуцированным Е1 можно приписать этому типу маннозных остатков, повторили ELISA с Saccharomyces-продуцированным Е1, причем разведенные сыворотки доноров крови предварительно инкубировали (1 час при 37°С) с 1 или 5 мг/мл маннана (Sigma), добавленным к буферу для разведения. Как можно судить по Табл.16, предварительная инкубация с маннаном снижала реактивность этого белка Е1 с сыворотками доноров крови зависимым от концентрации образом до фоновых уровней у всех анализированных сывороток, кроме одной (F556). (Средняя оптическая плотность снижалась от 0,24 без конкуренции со стороны маннана до 0,06 с использованием 5 мг маннана/мл.)
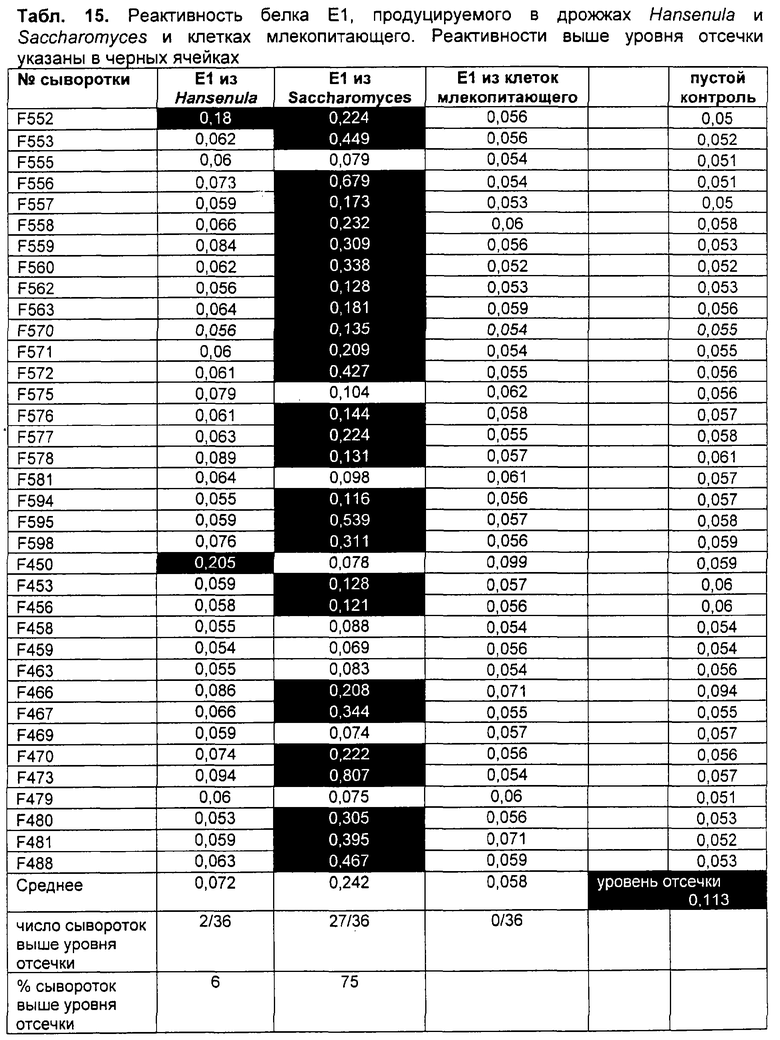
Реактивность белка Е1, продуцируемого в клетках Saccharomyces, как в Табл.15, но в присутствии 5 мг маннана/ мл. Реактивности выше уровня отсечки указаны в черных ячейках
Источники информации








































































































































































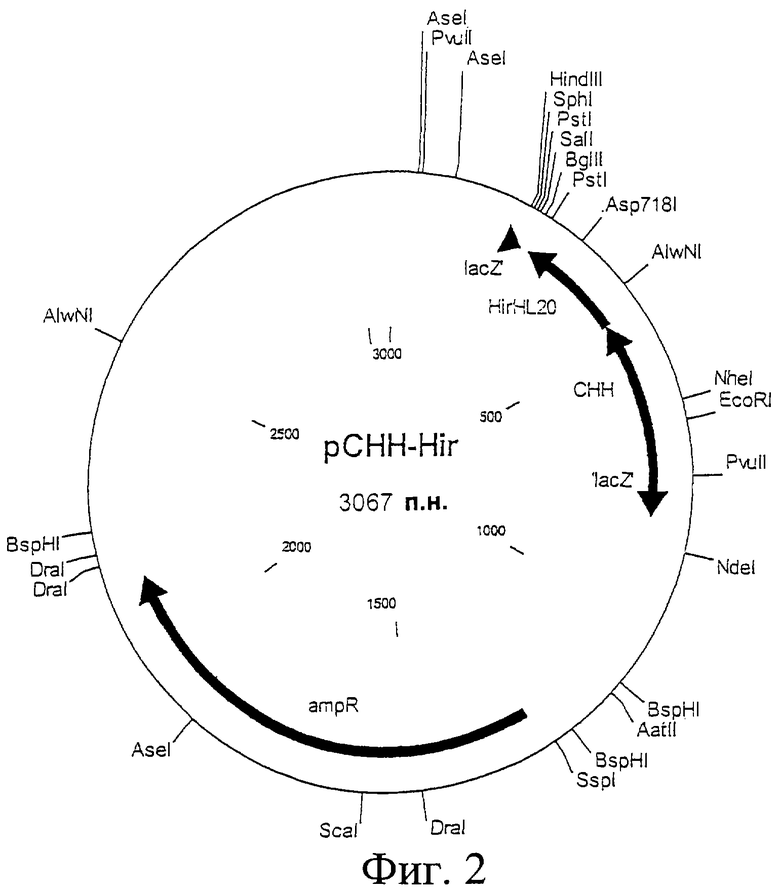
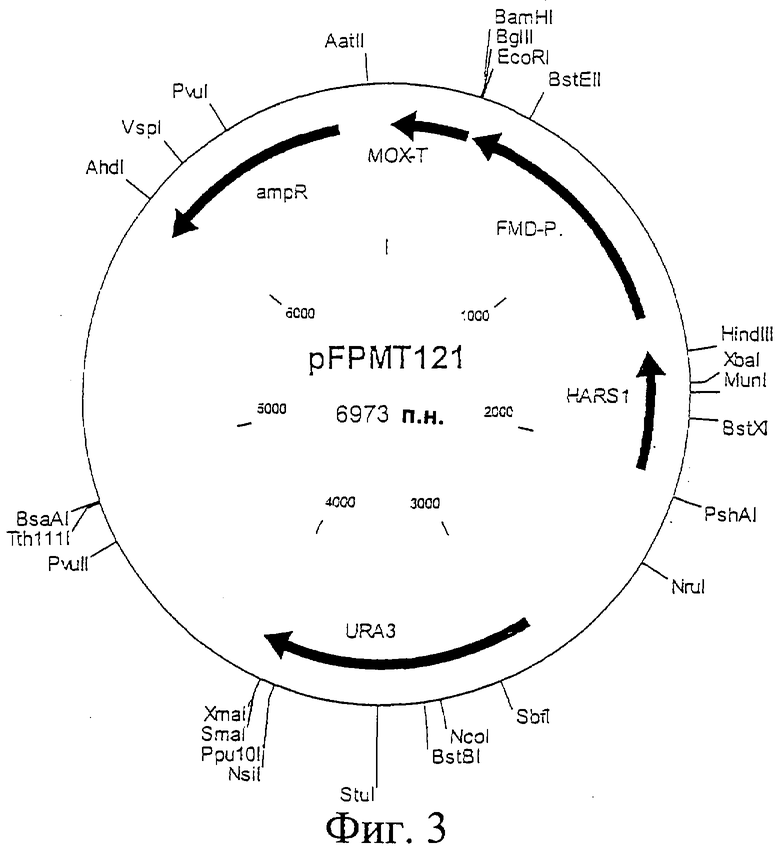
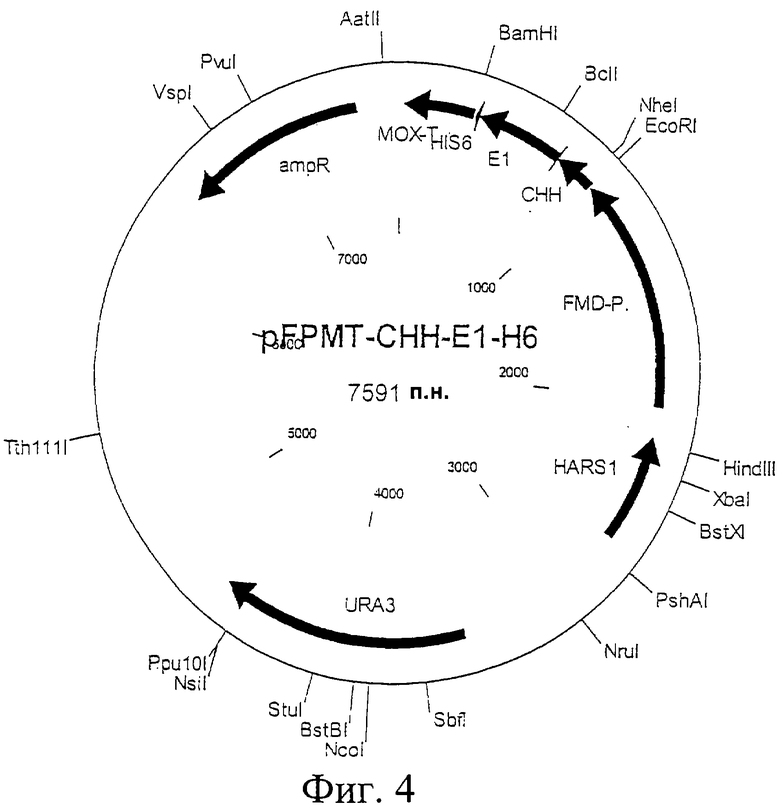
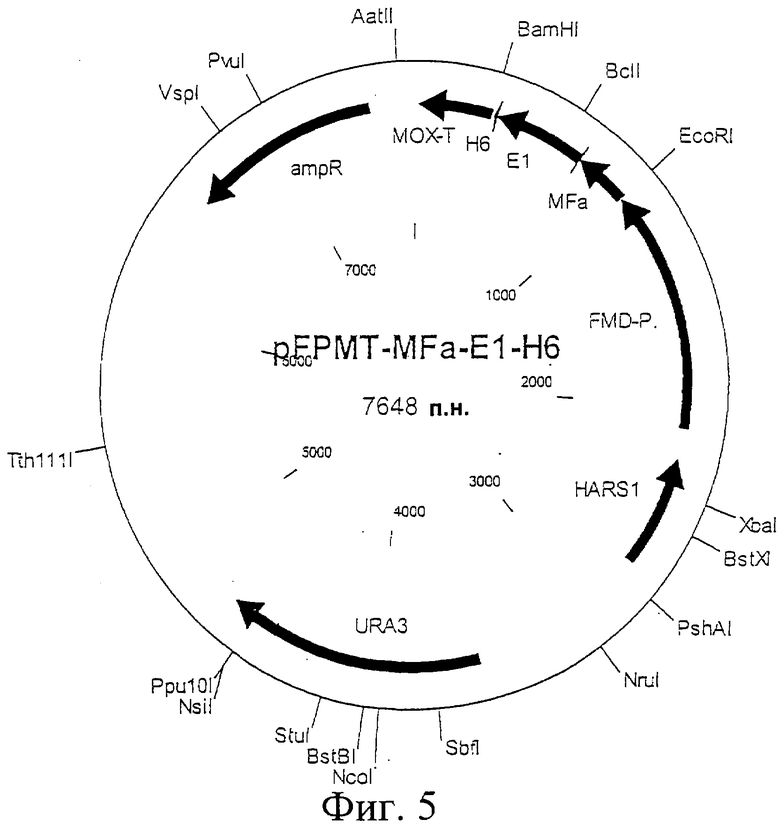
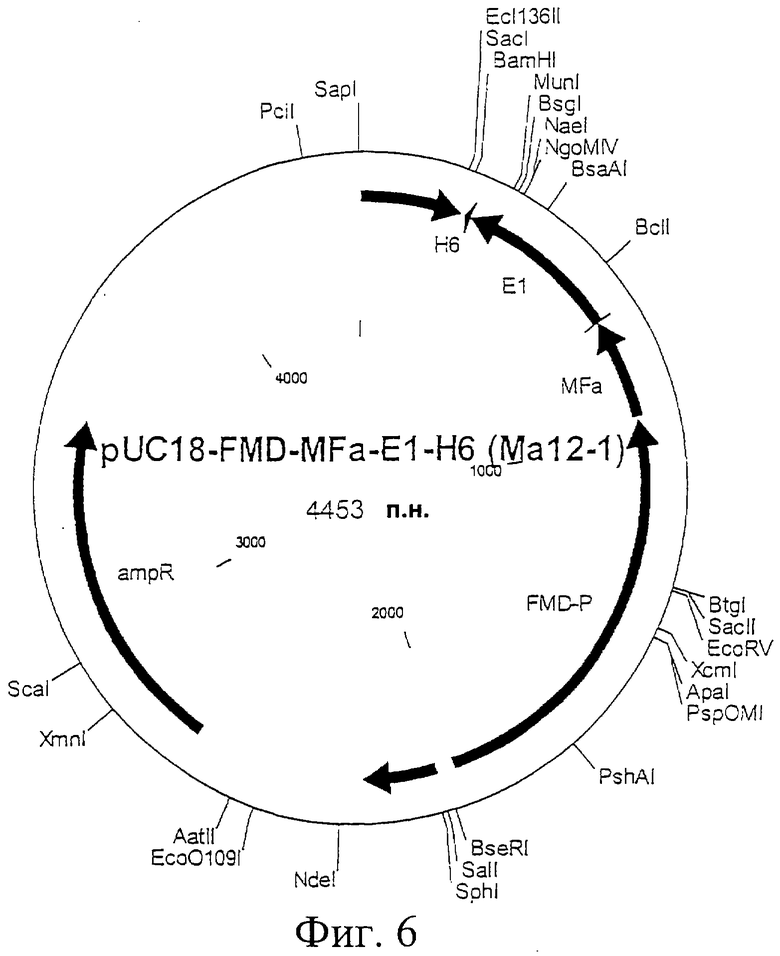
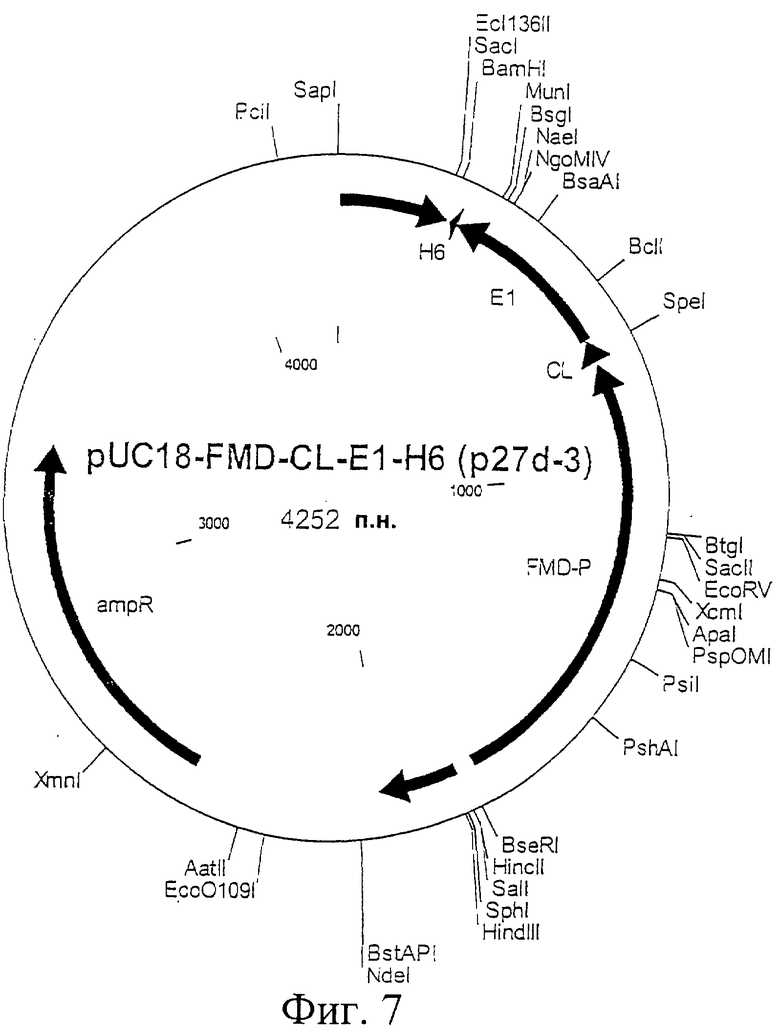
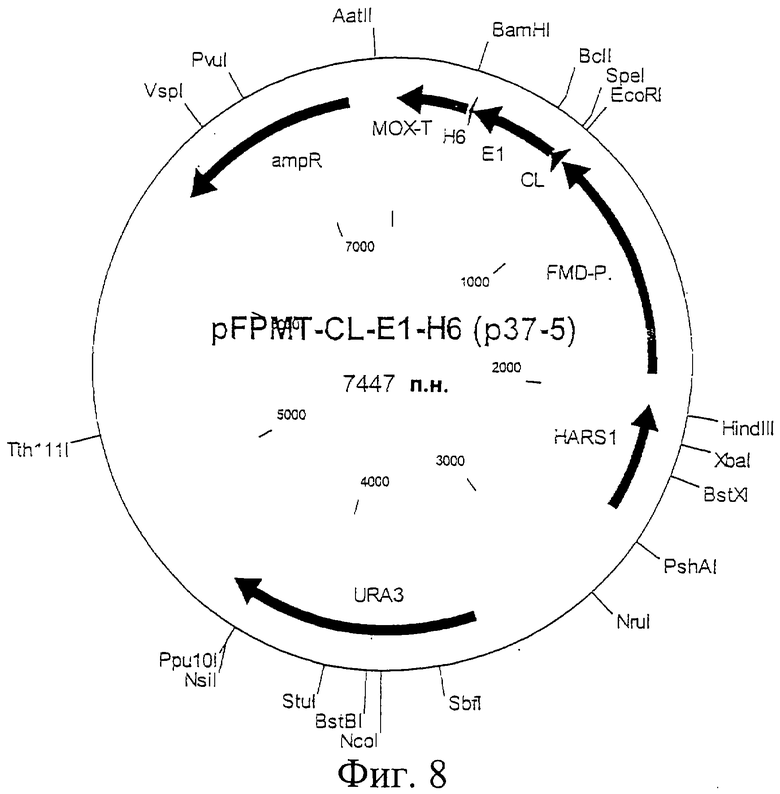
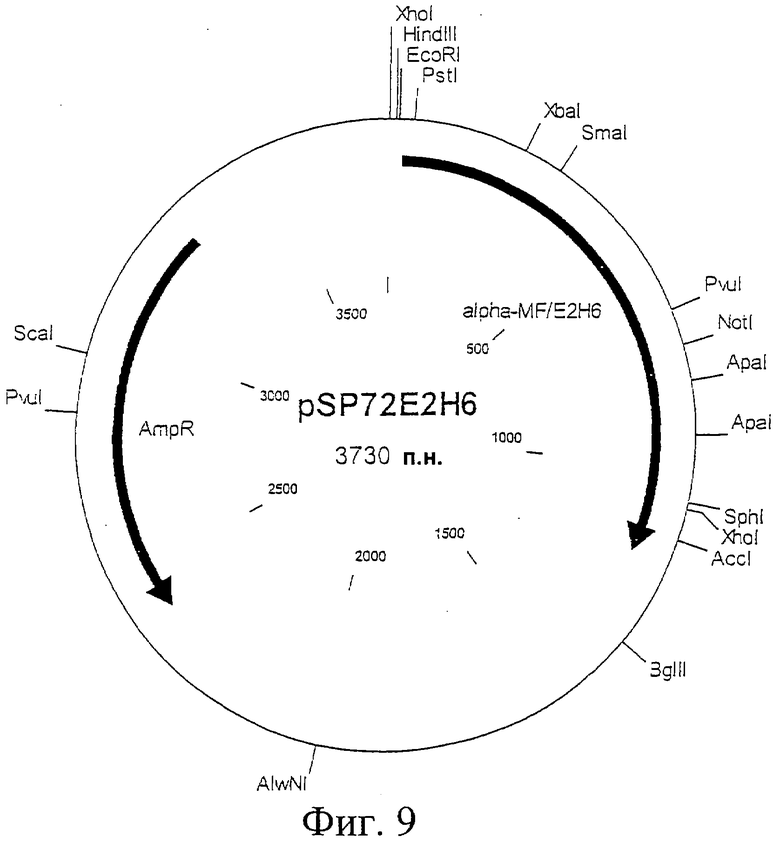
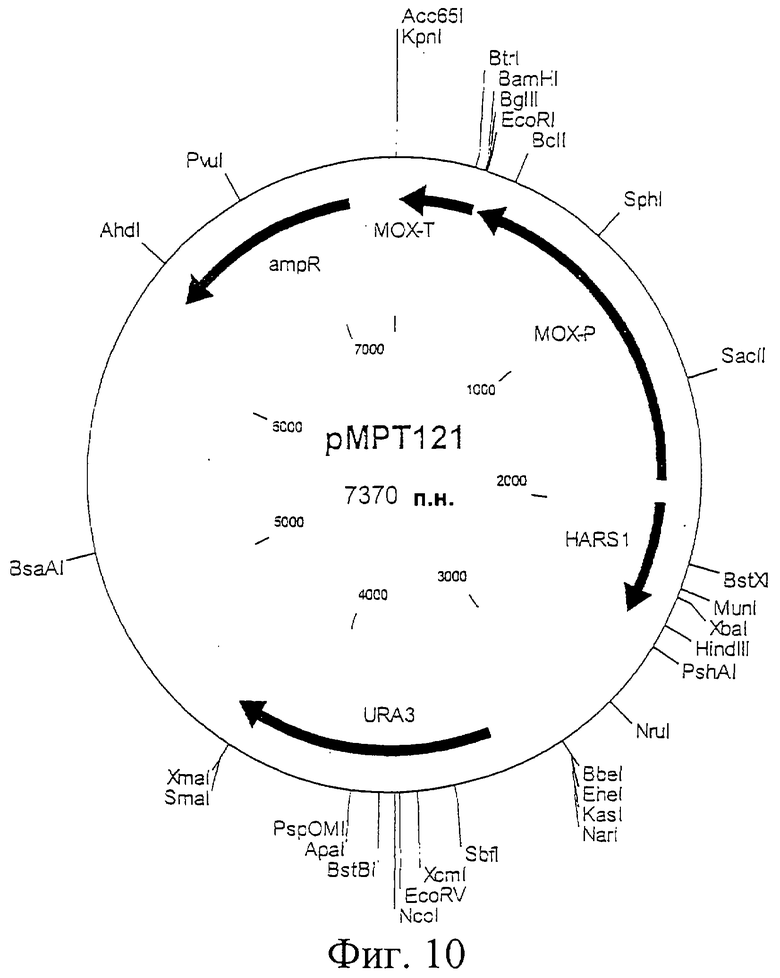
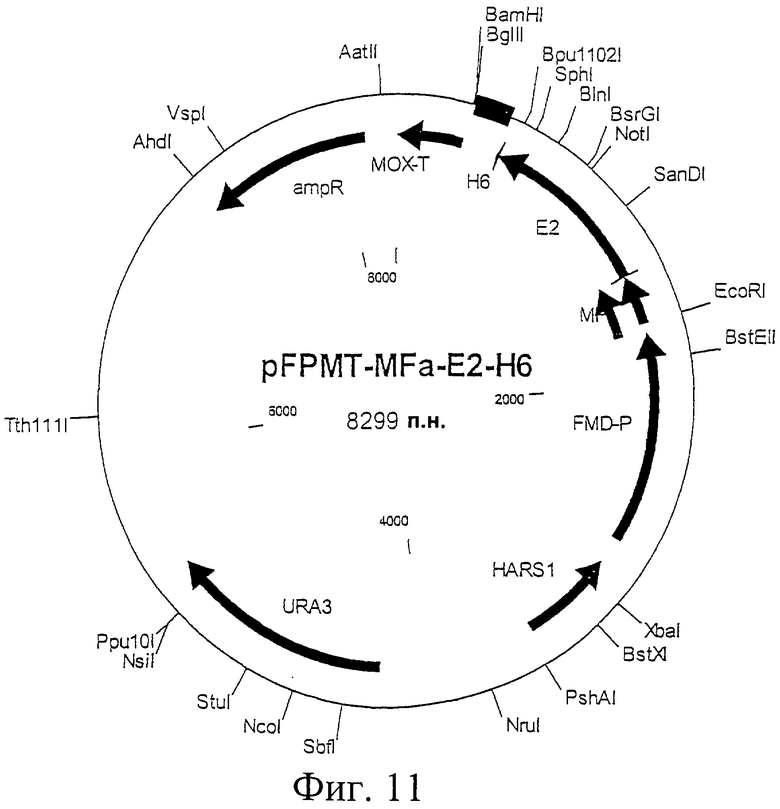
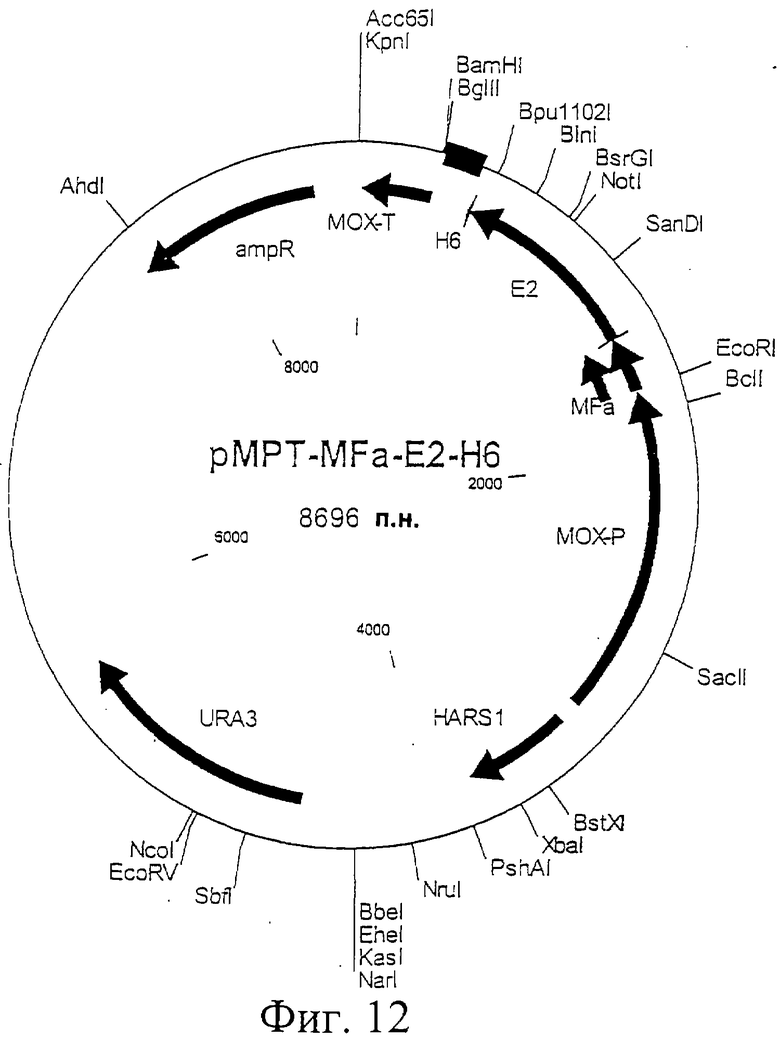
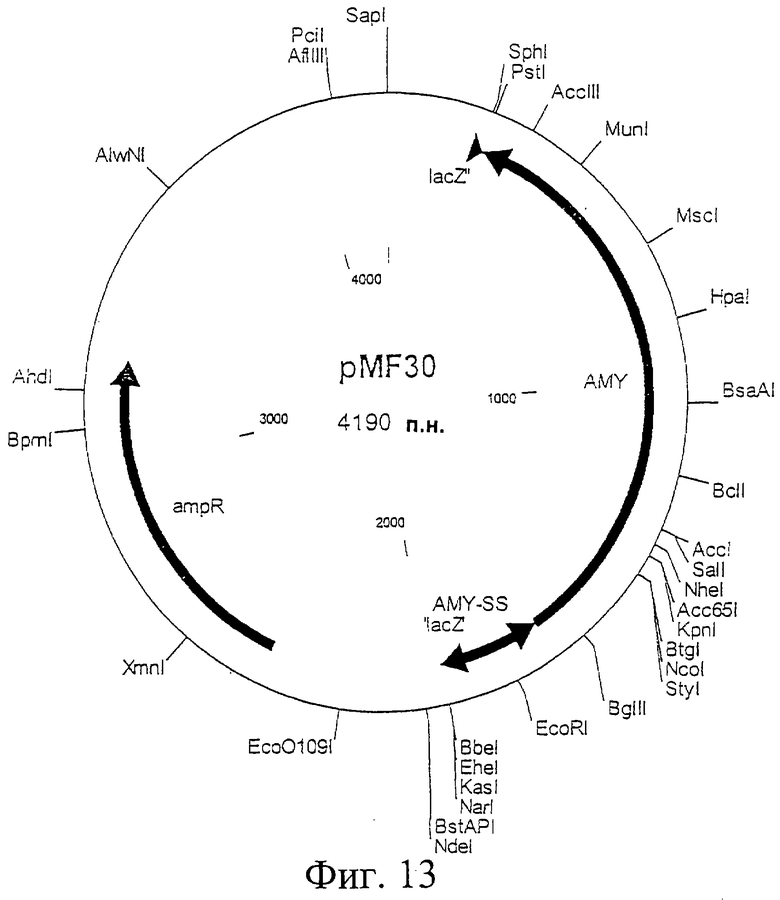
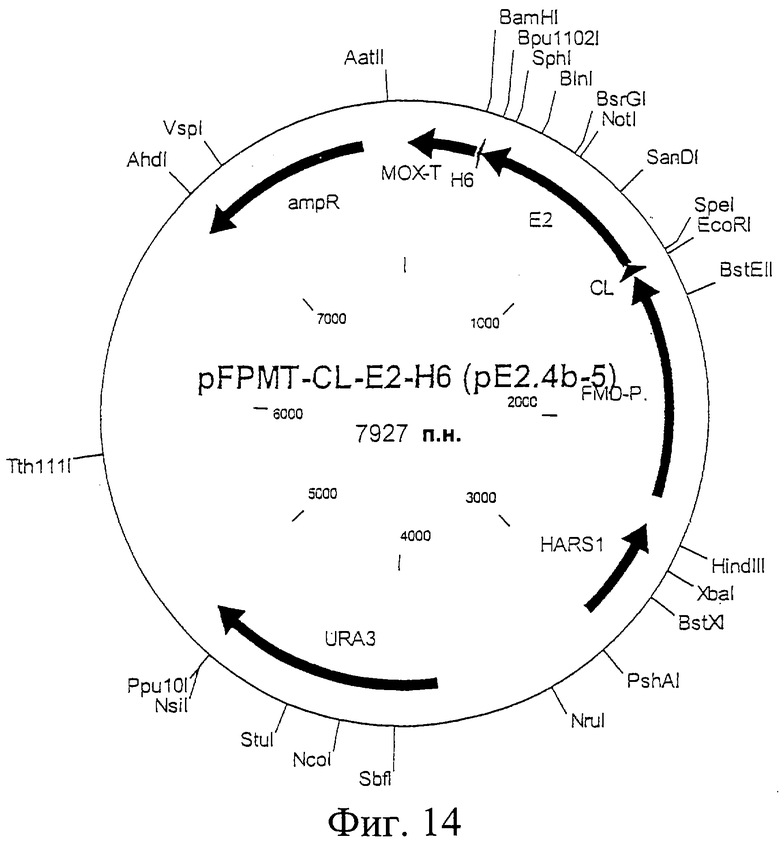
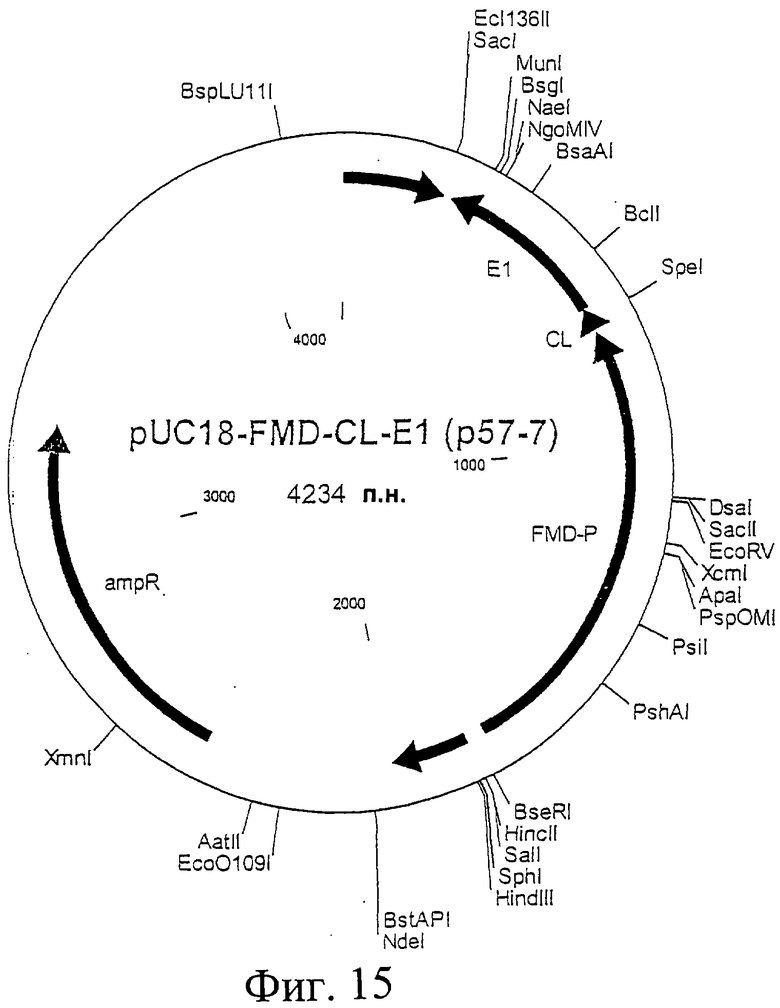
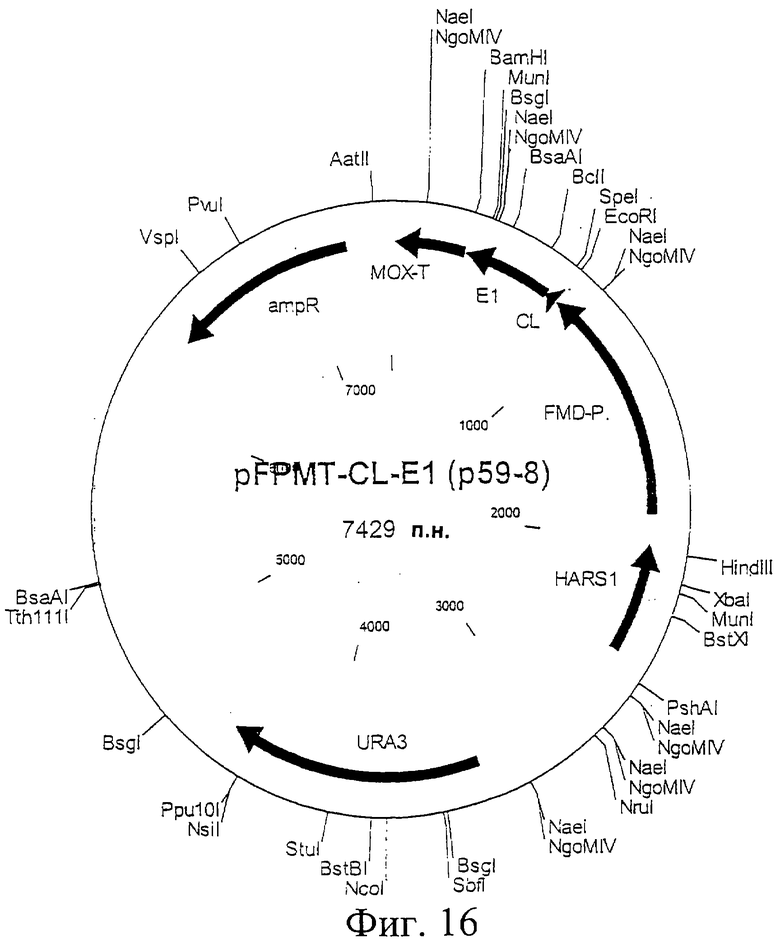
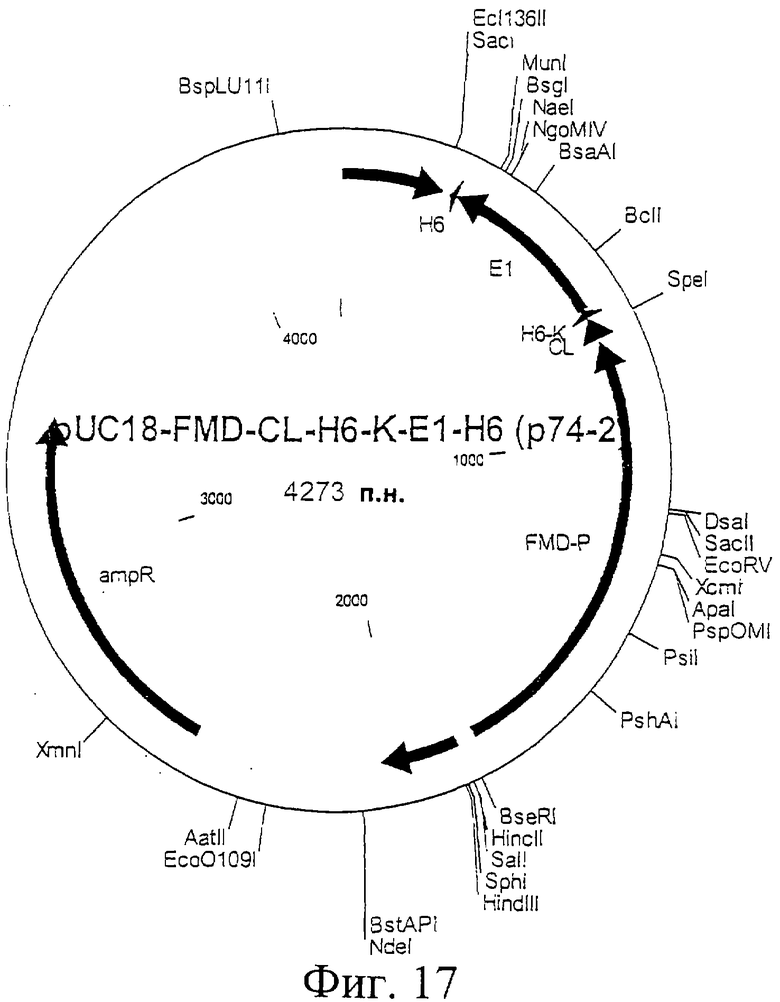
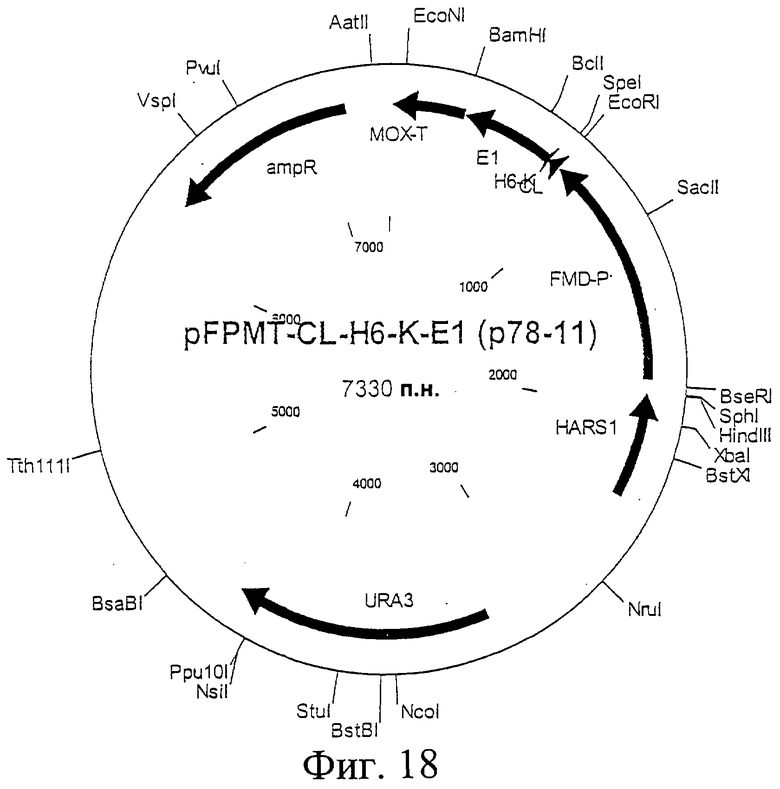
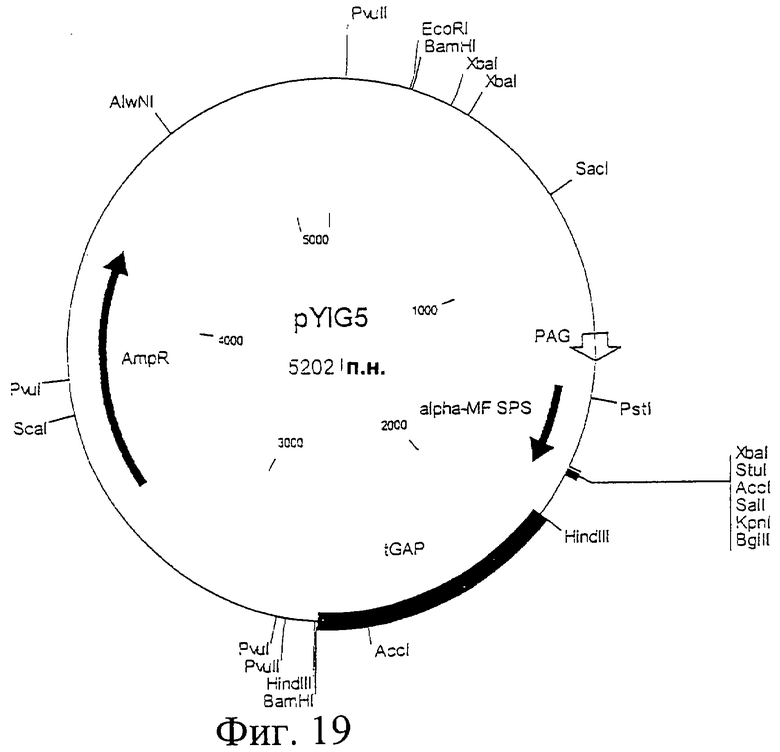
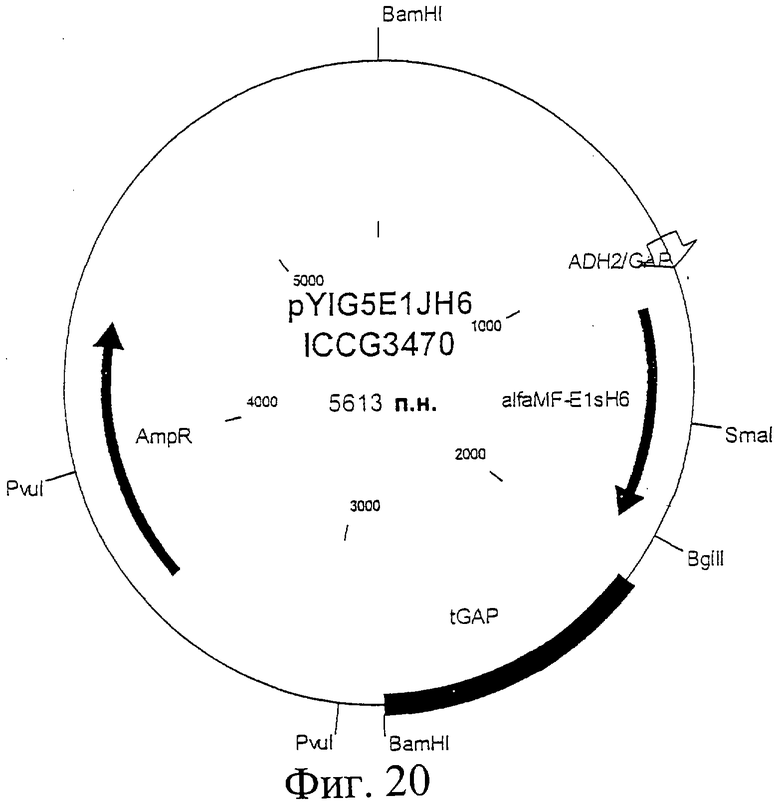
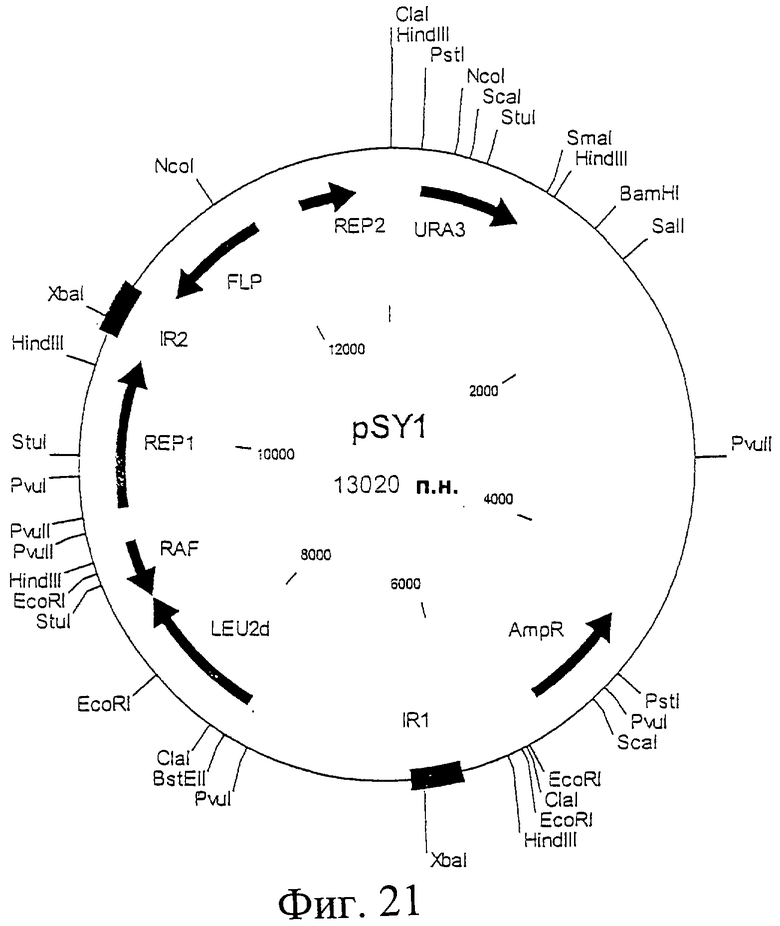
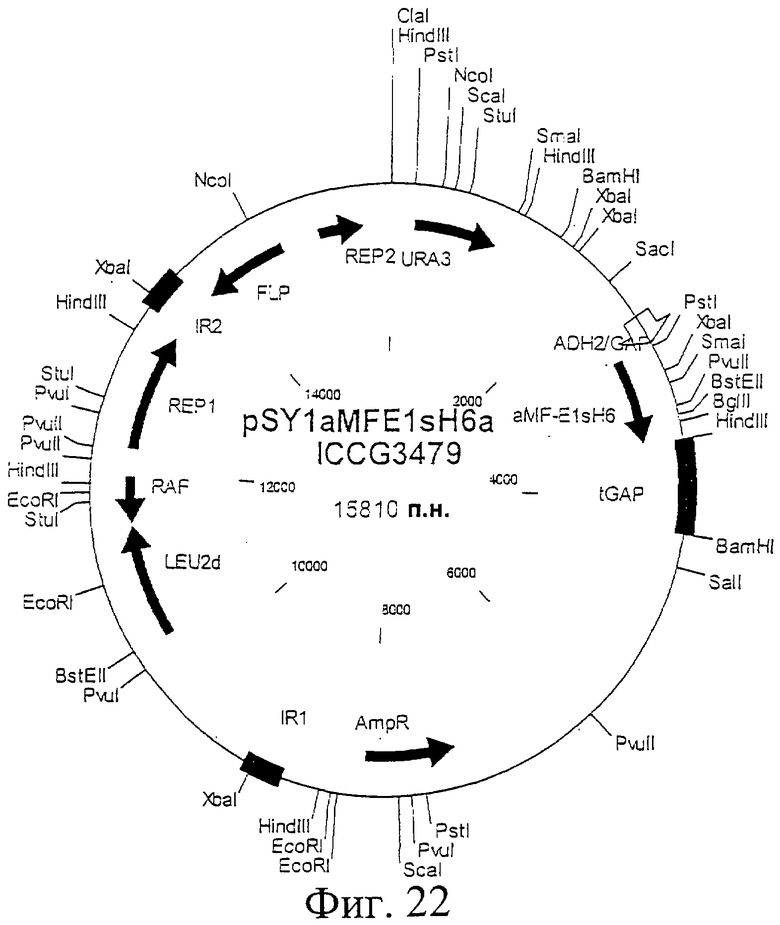
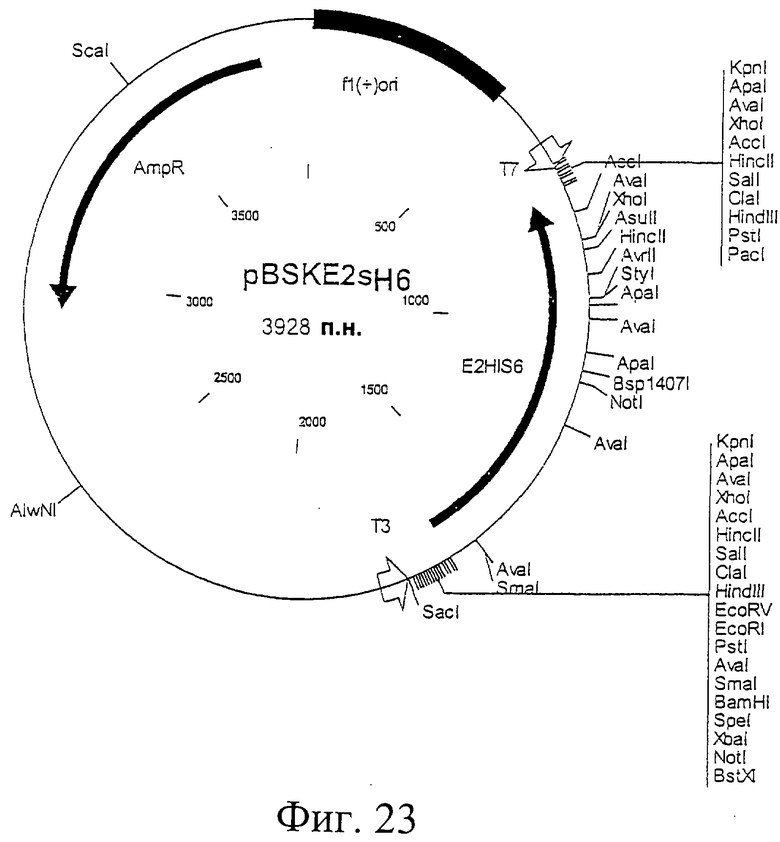
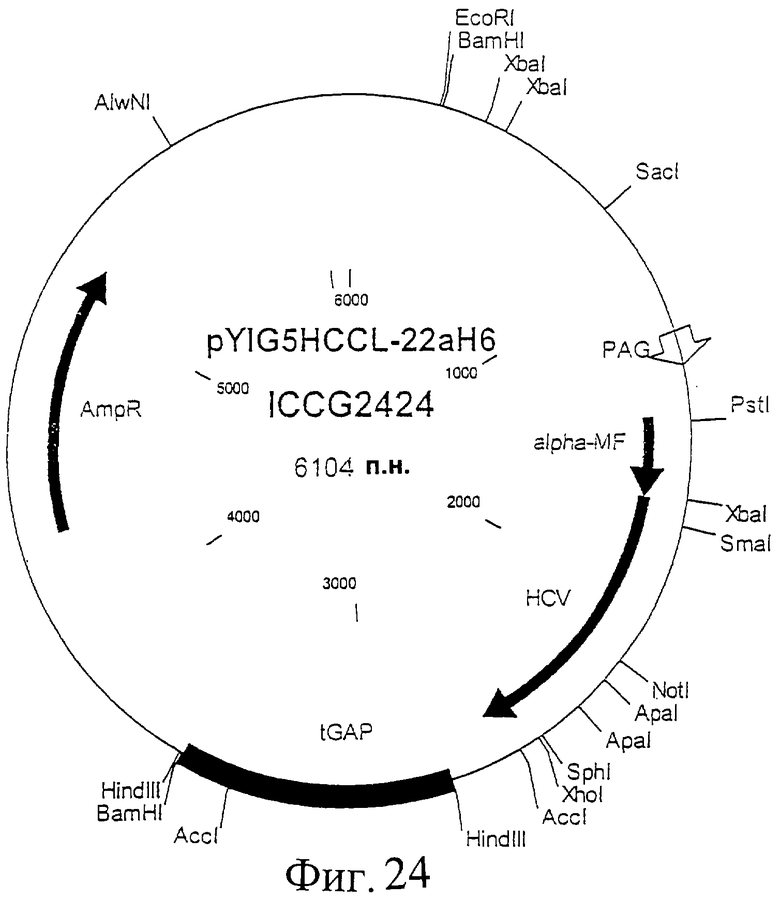
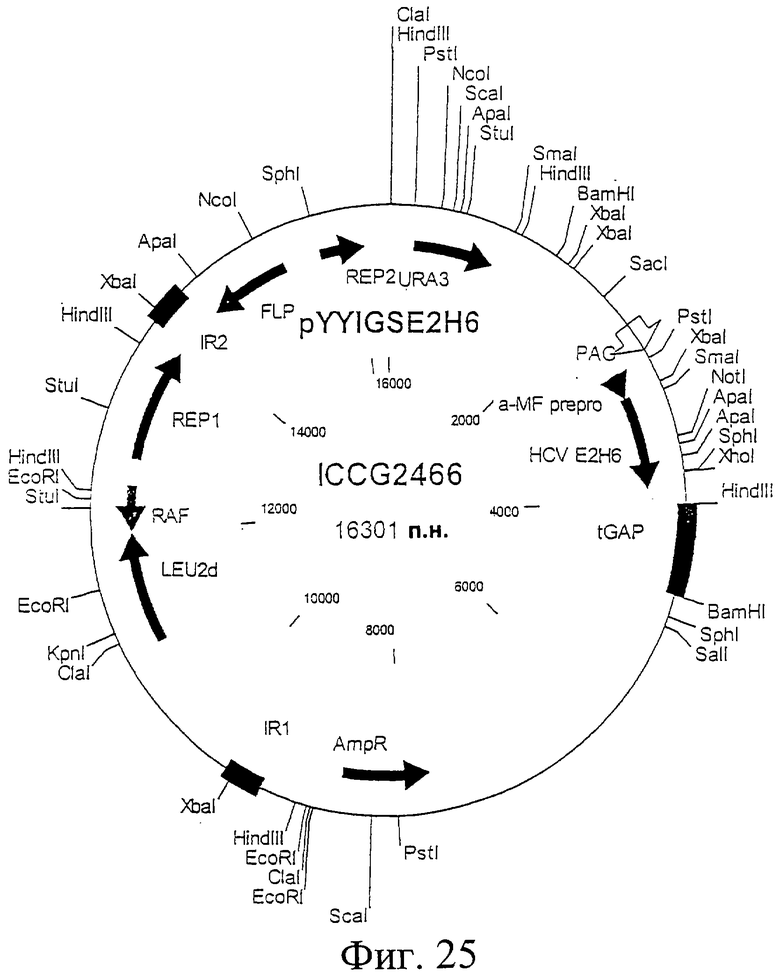
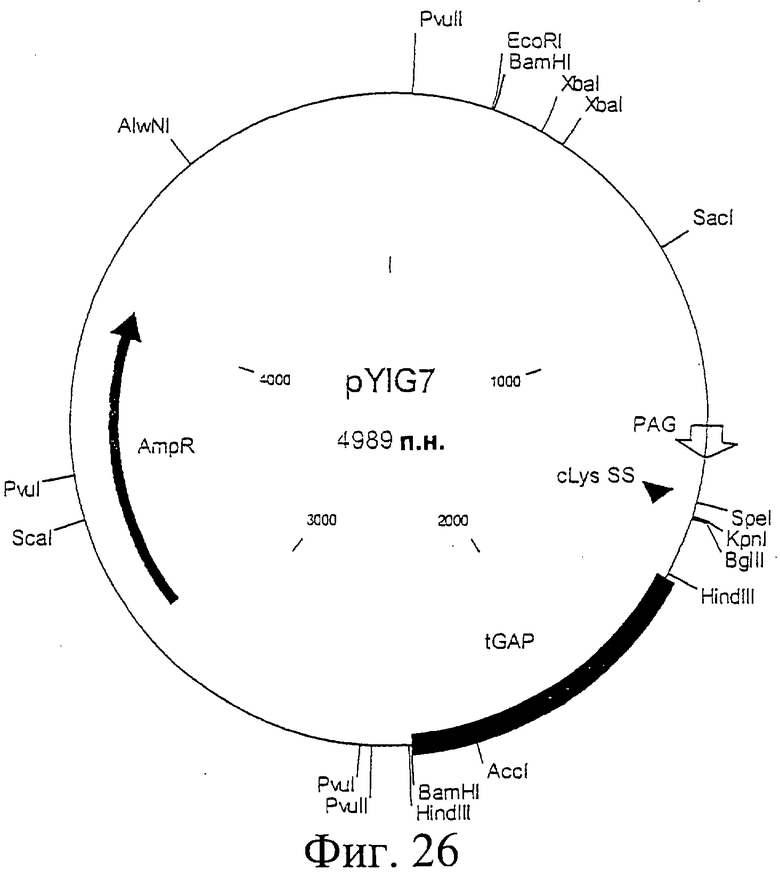
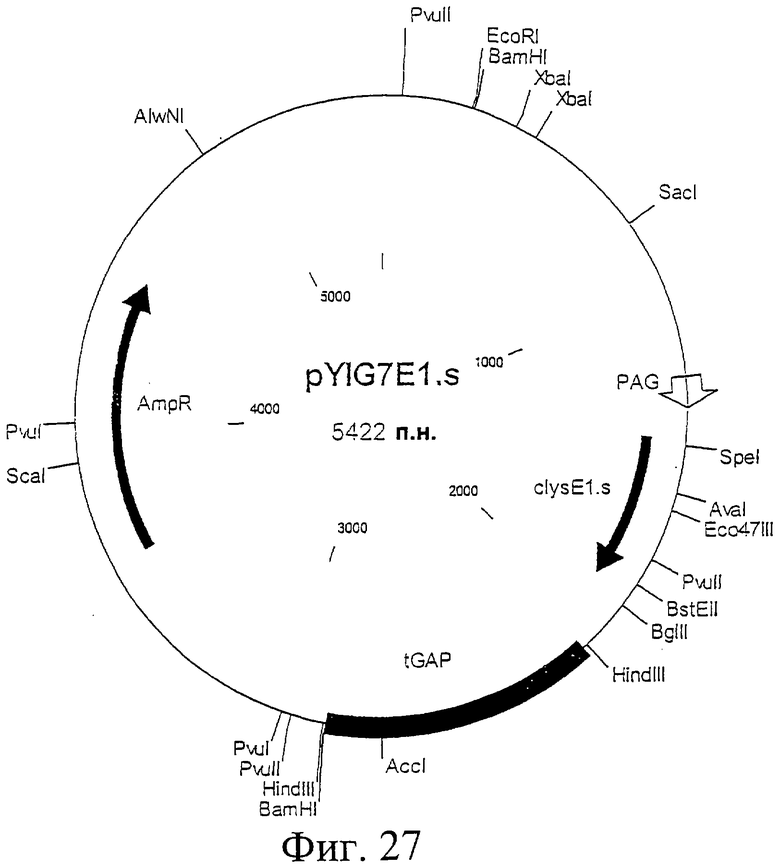
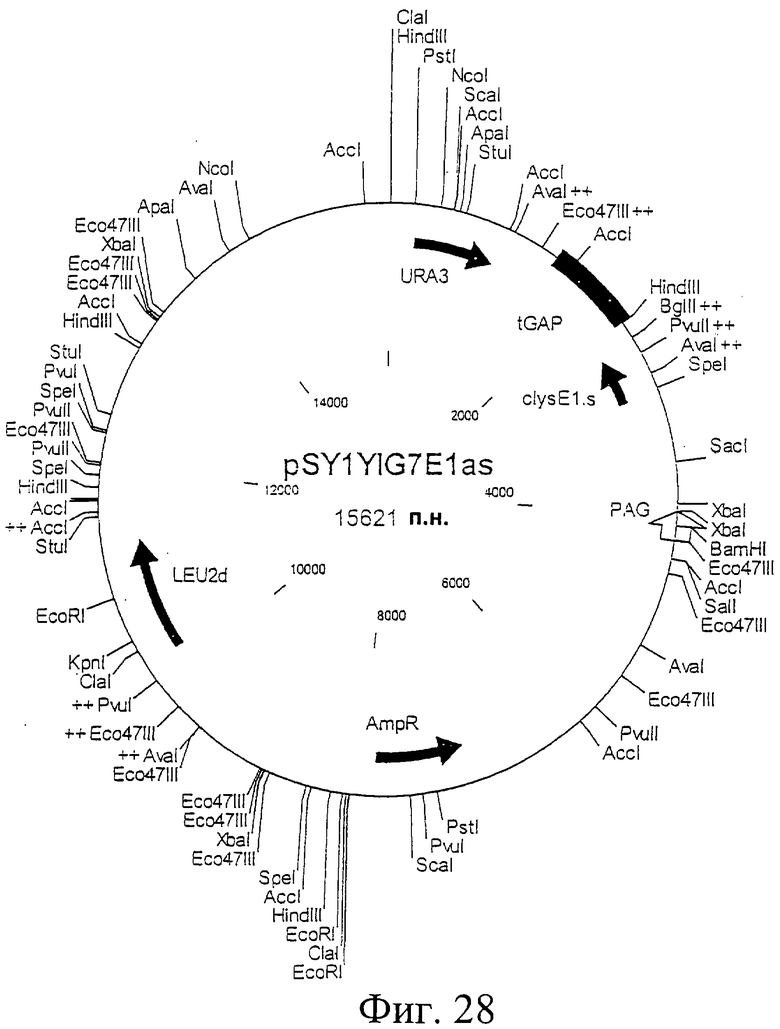
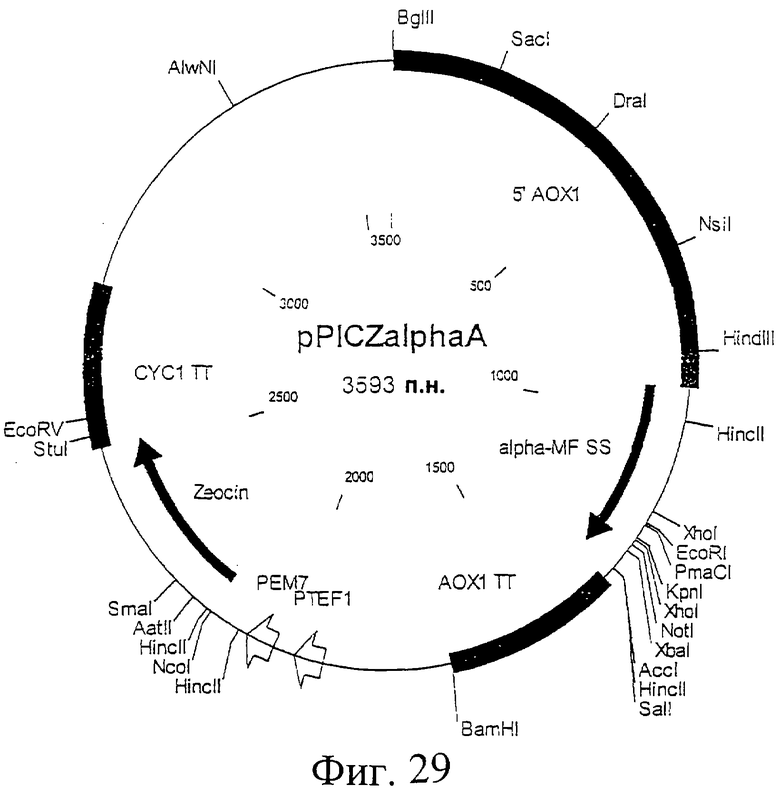
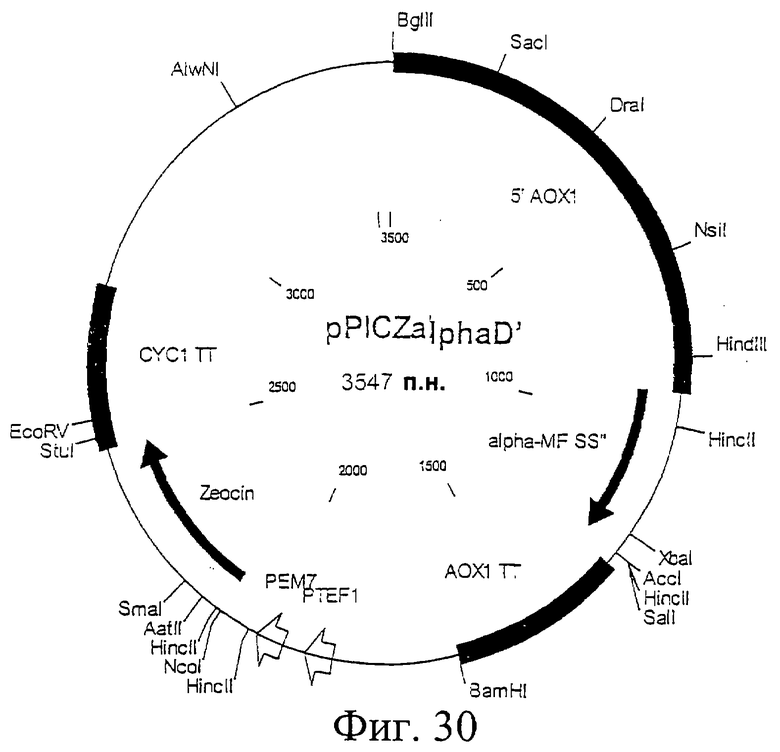
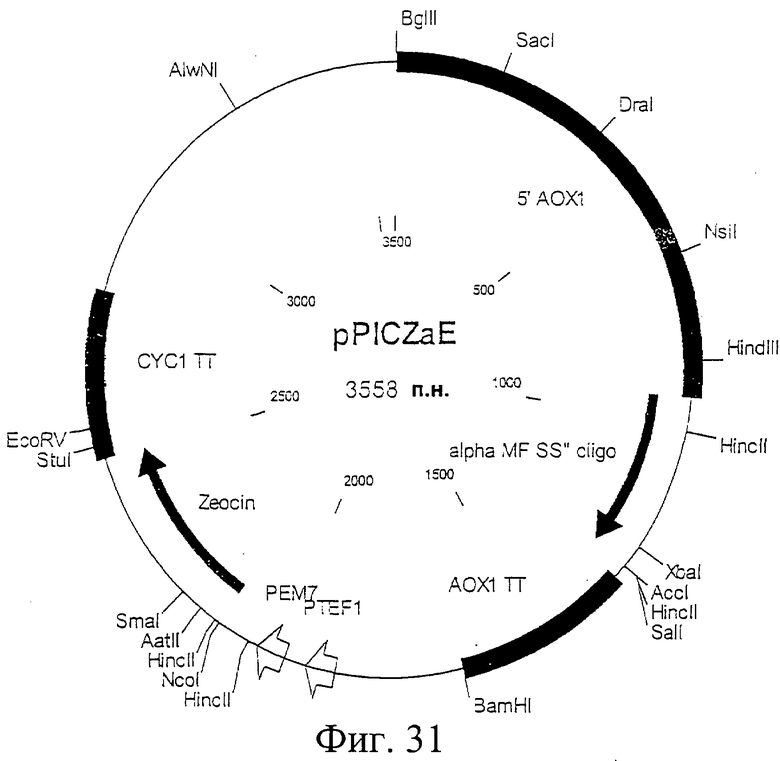
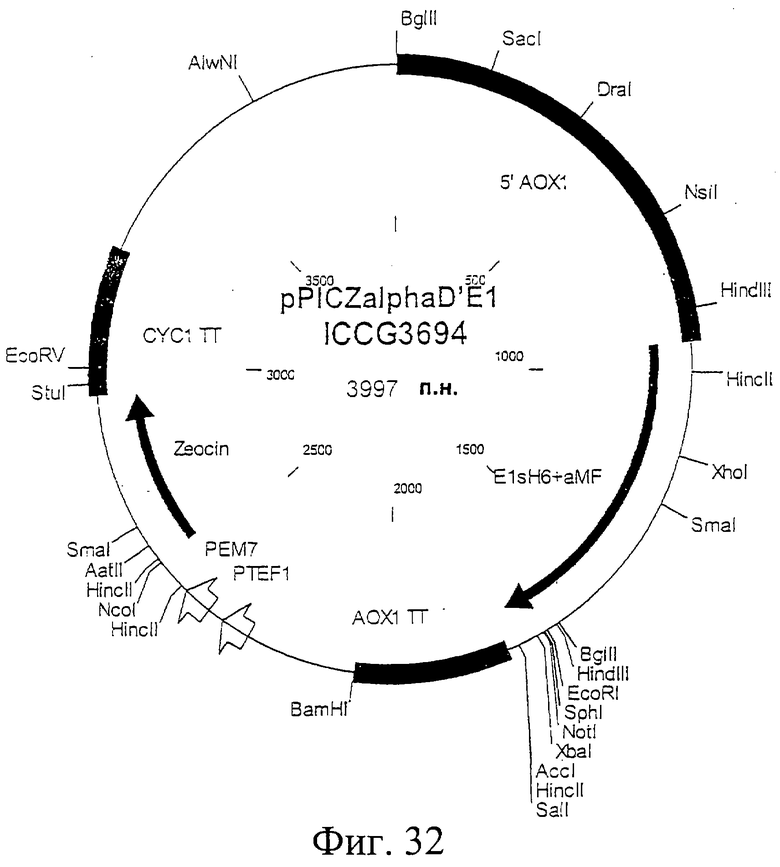
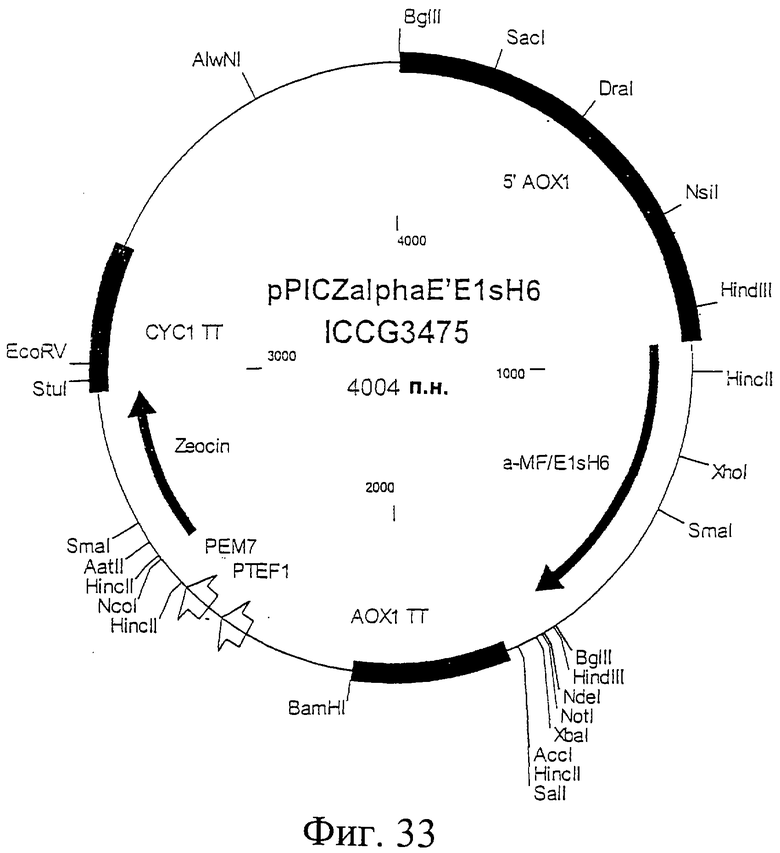
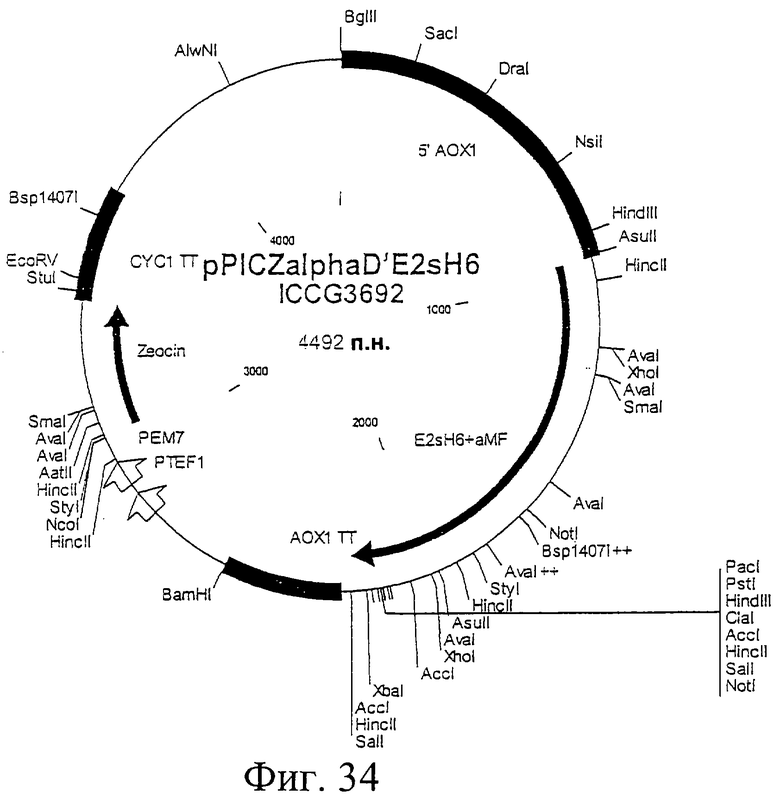
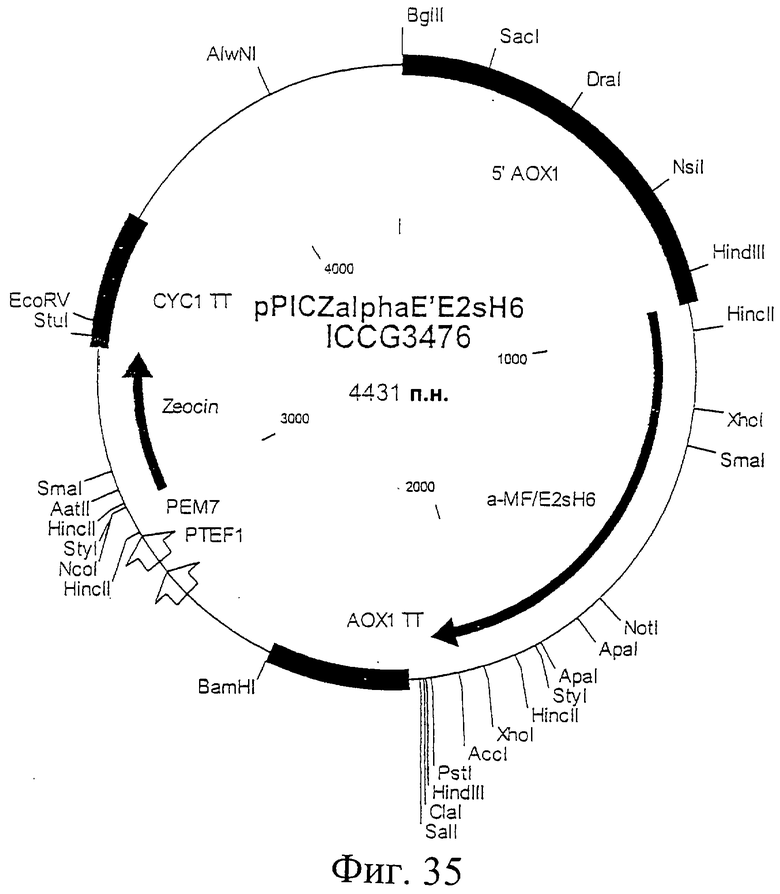
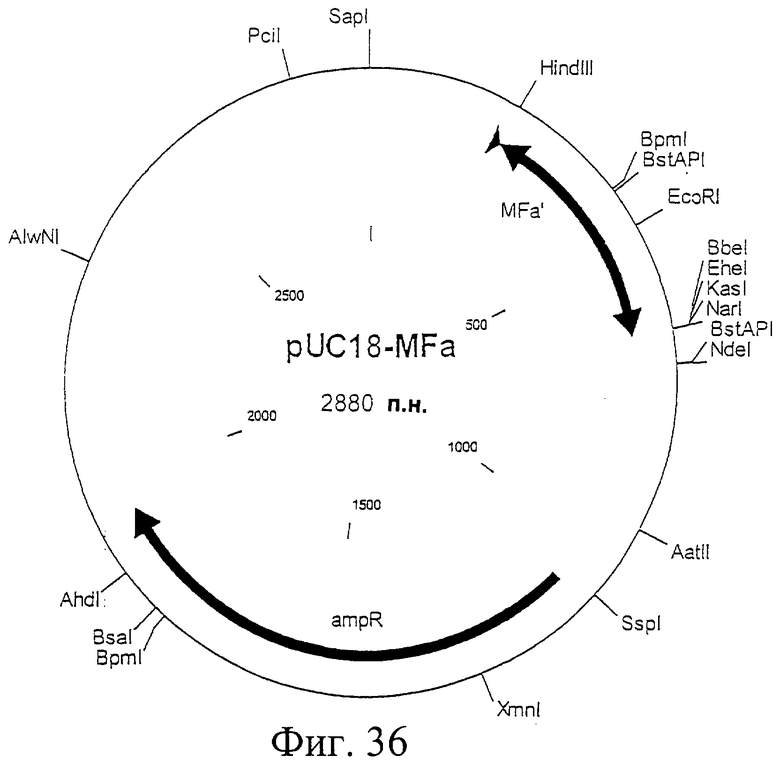
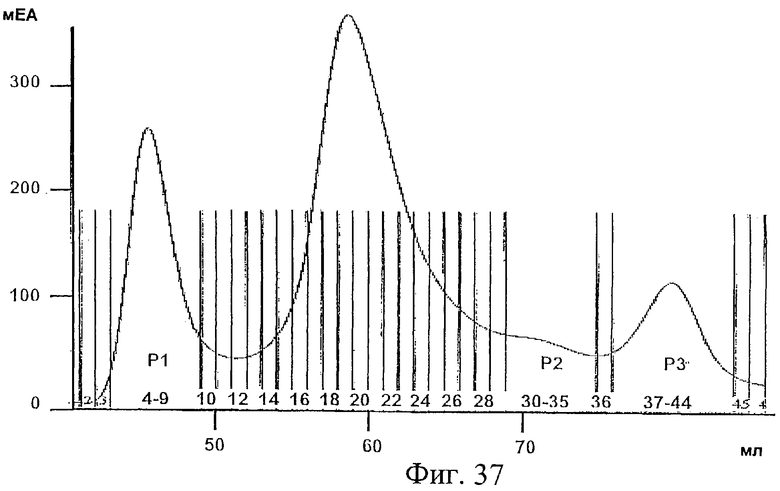
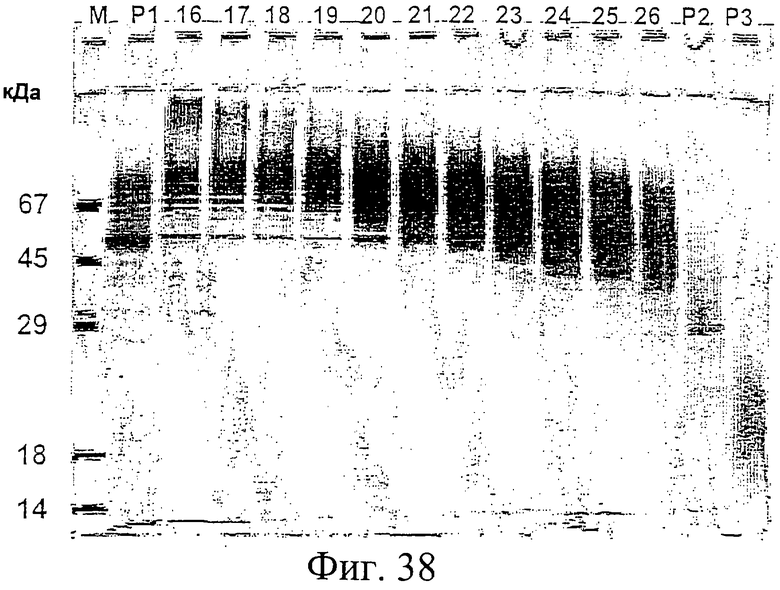
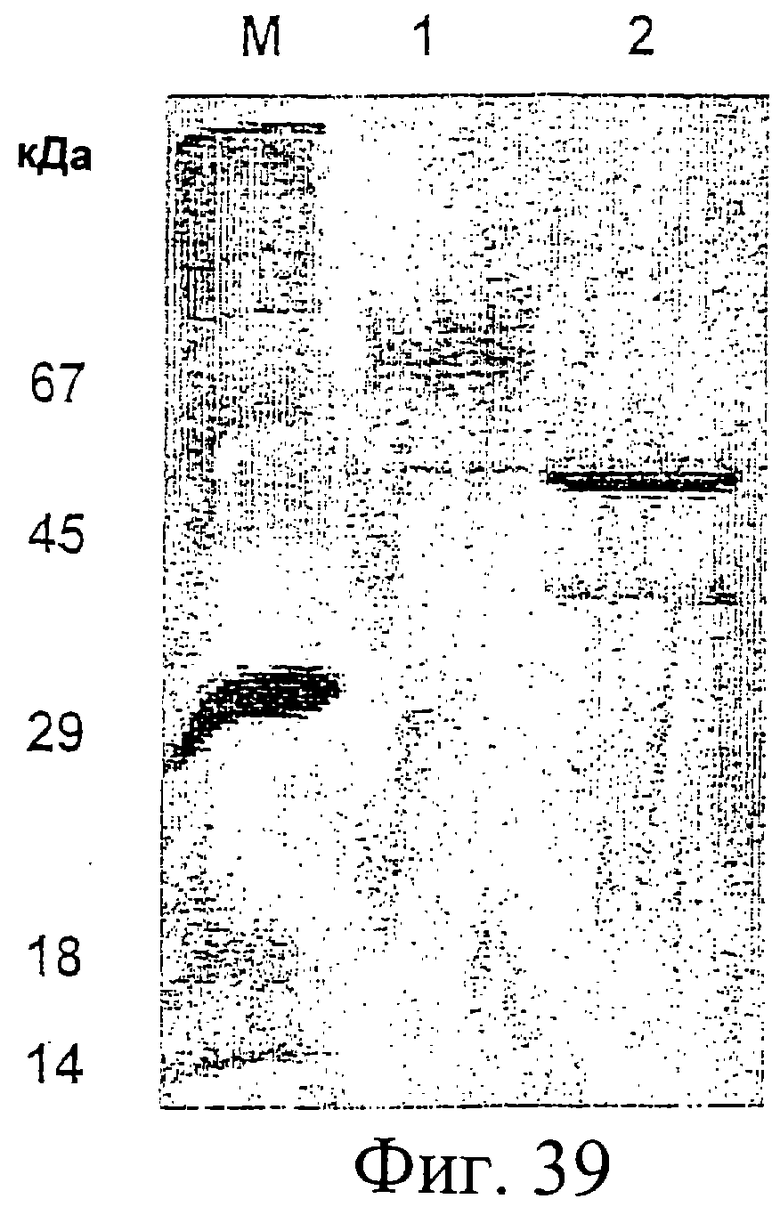
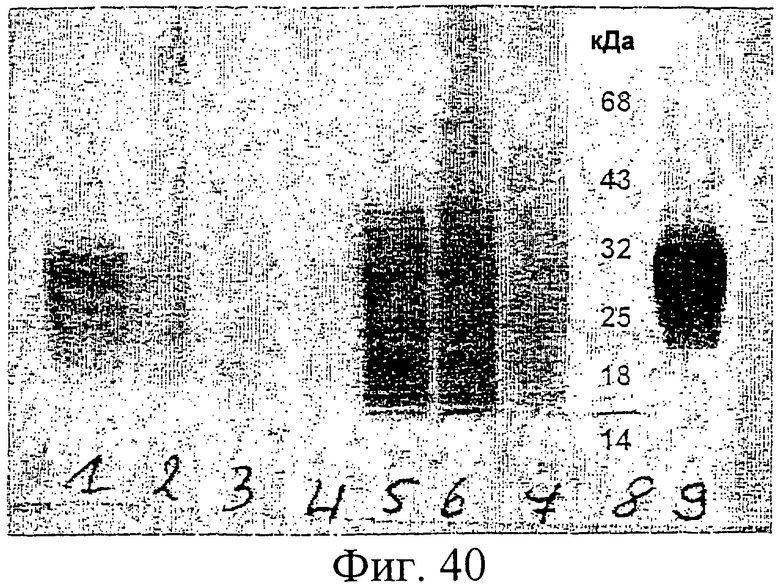
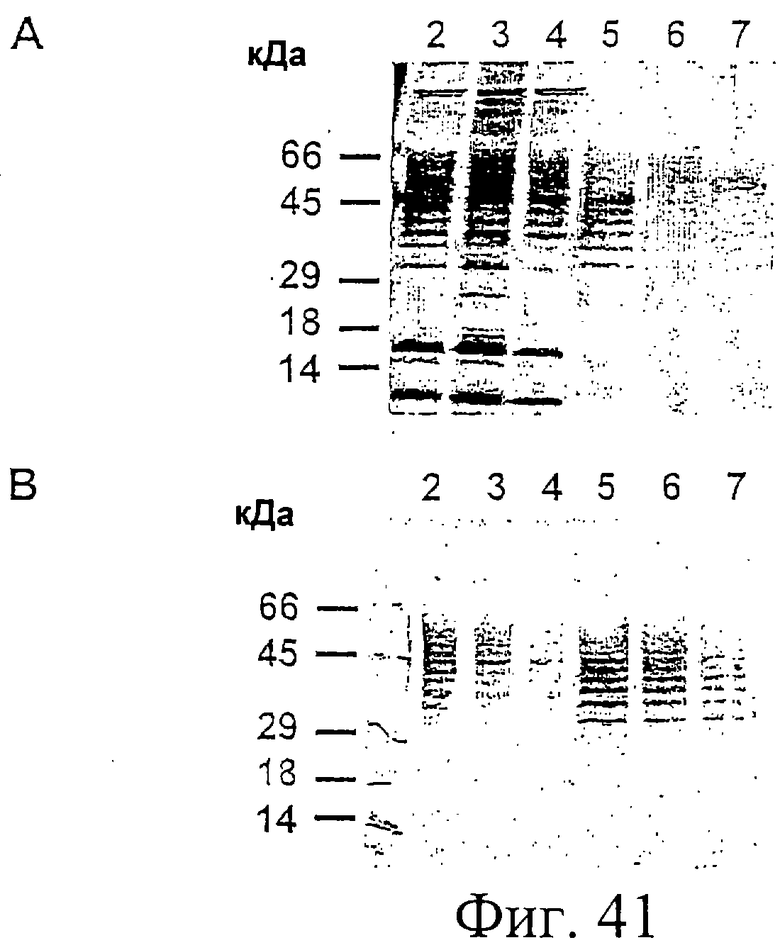
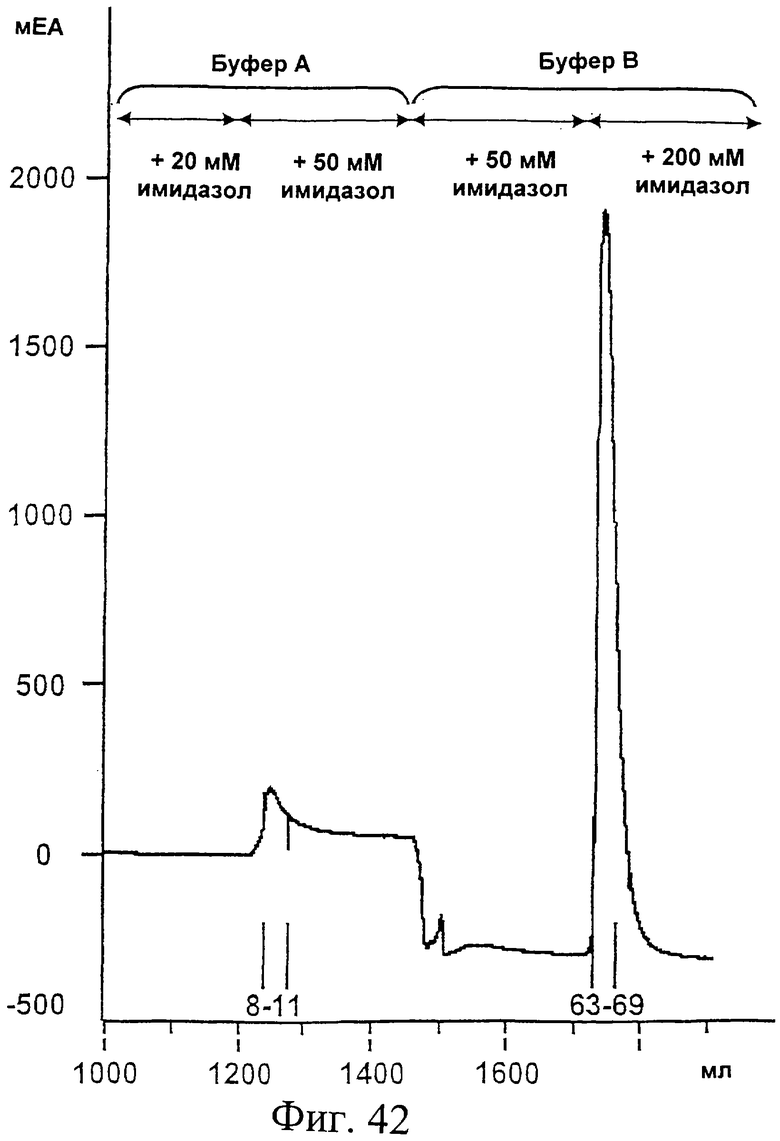
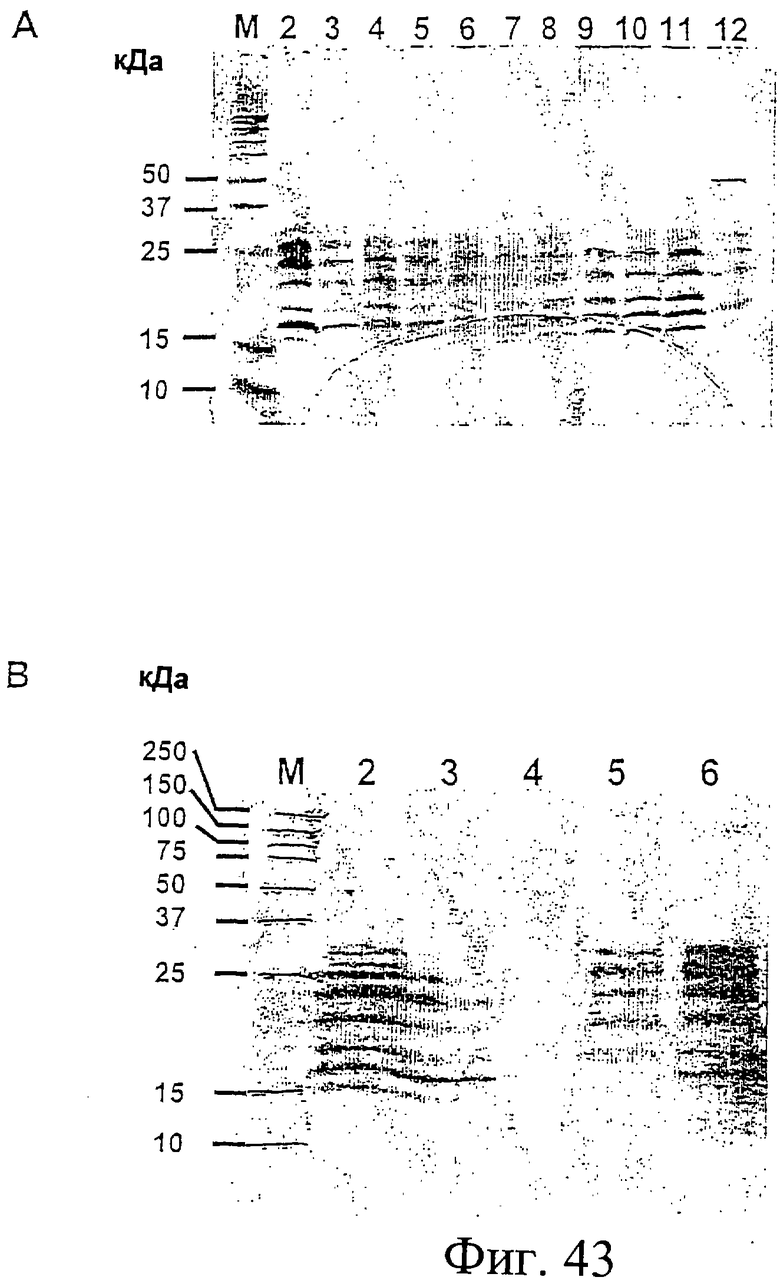
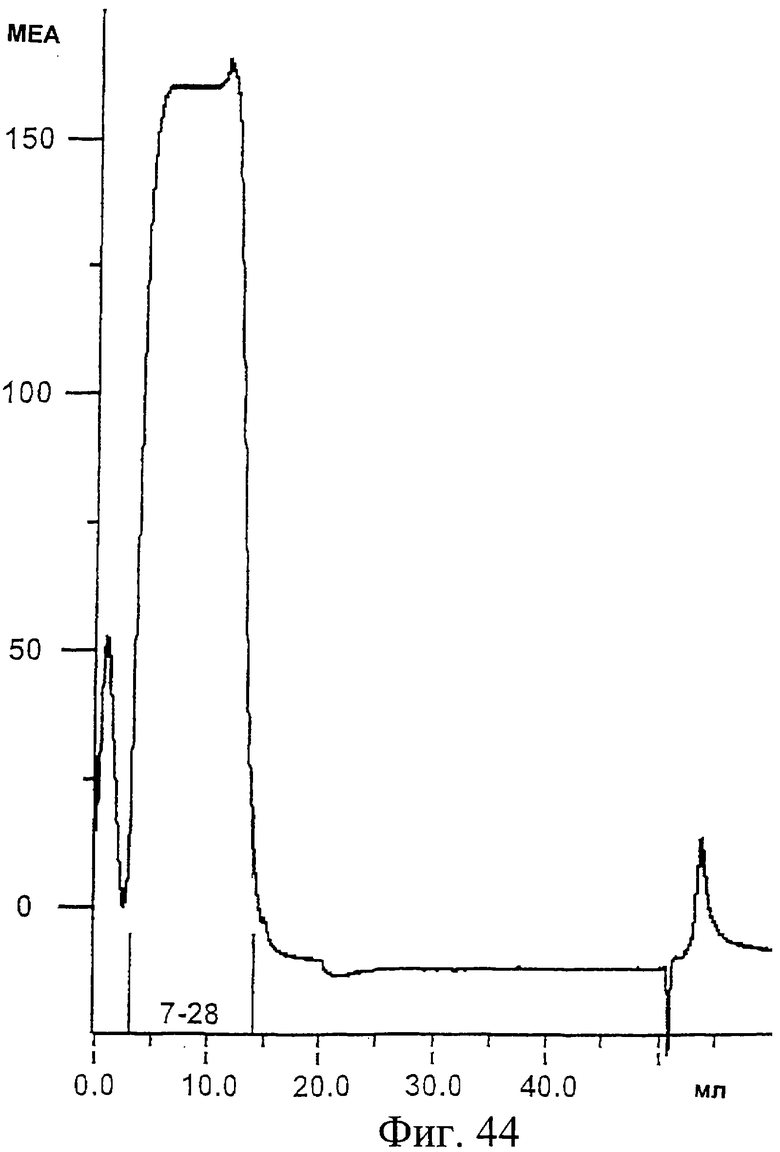
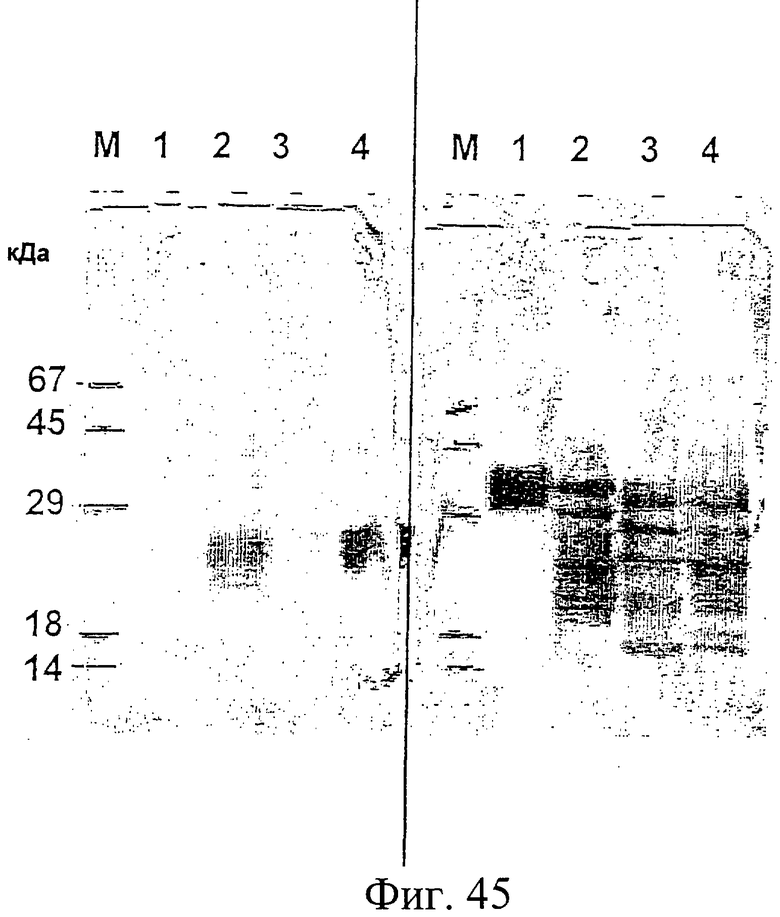
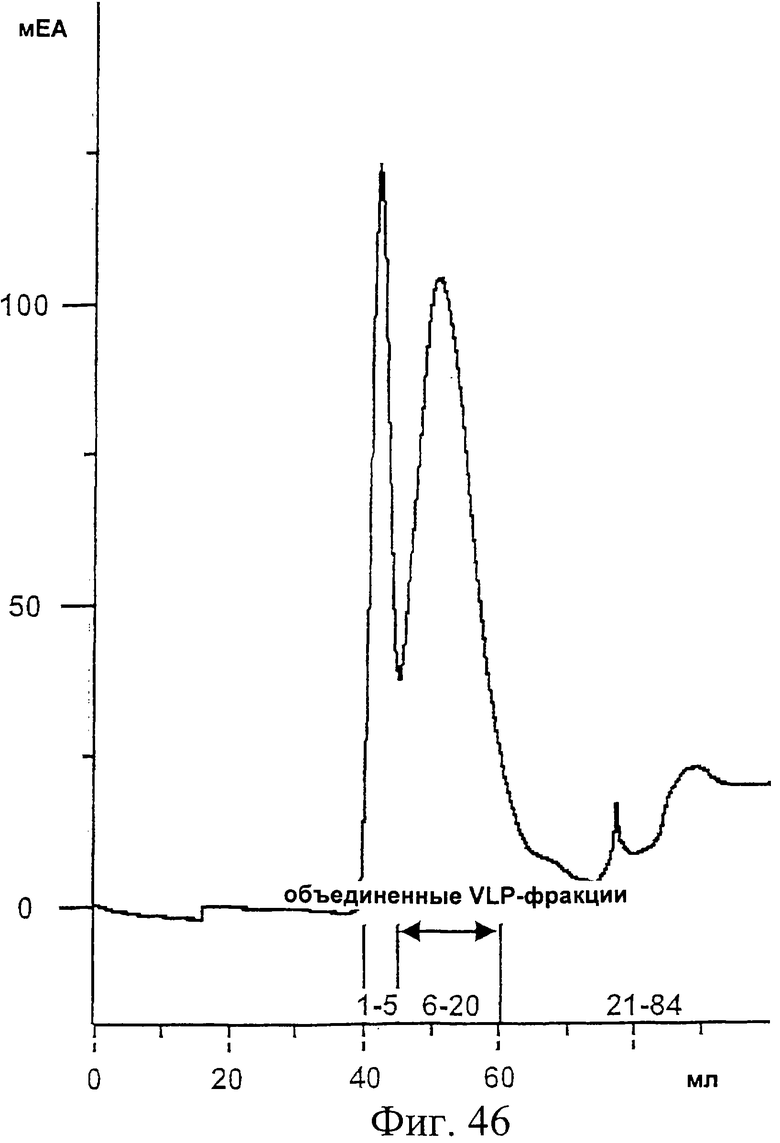
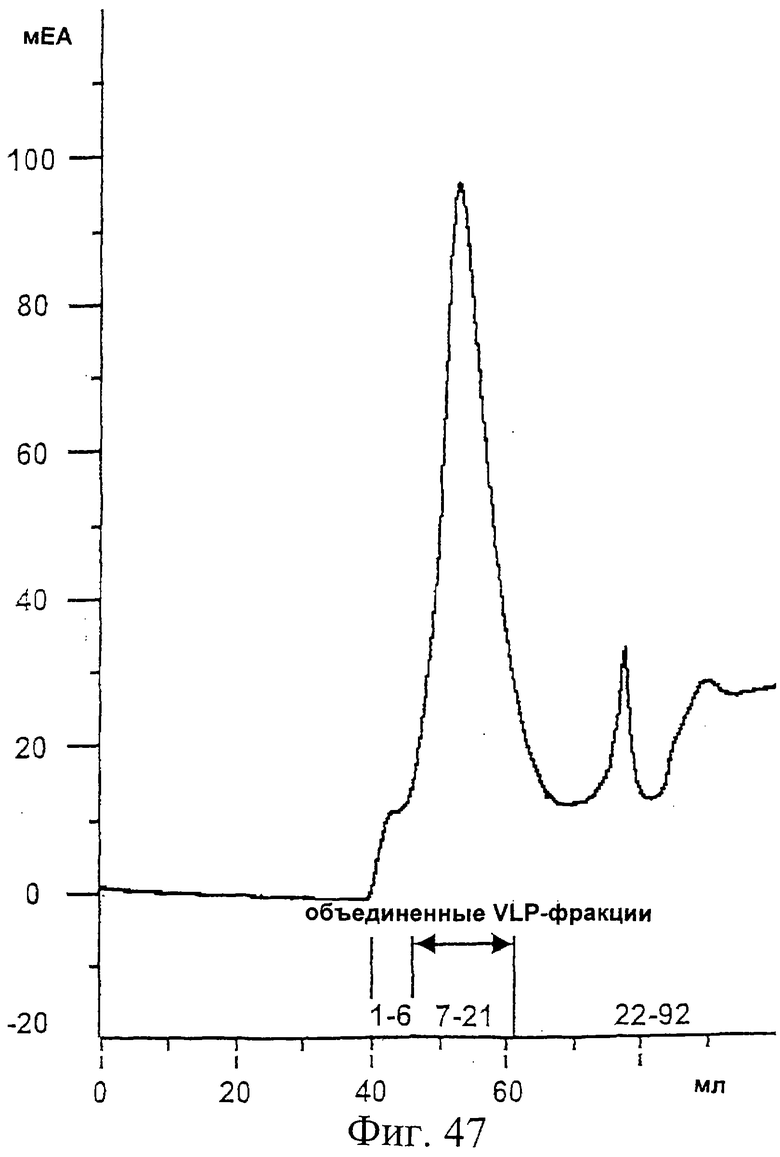


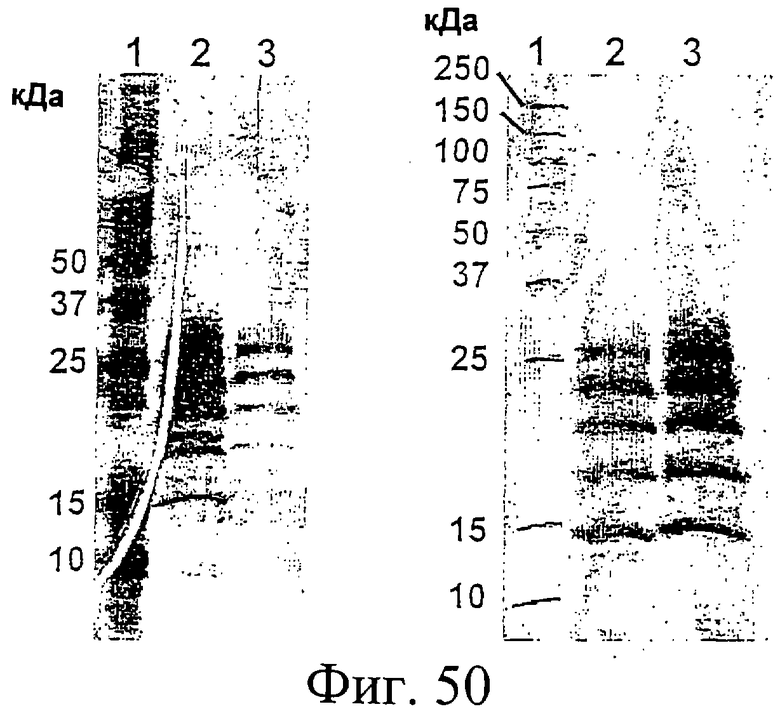
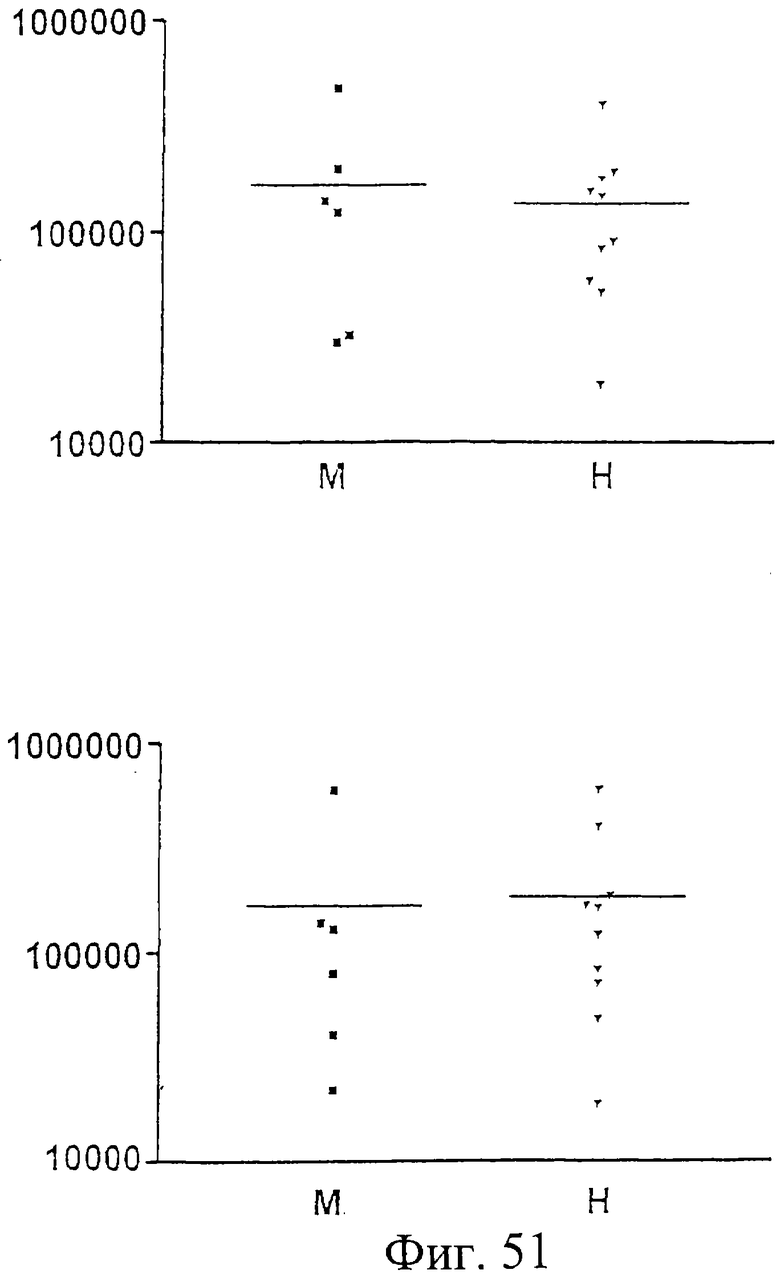
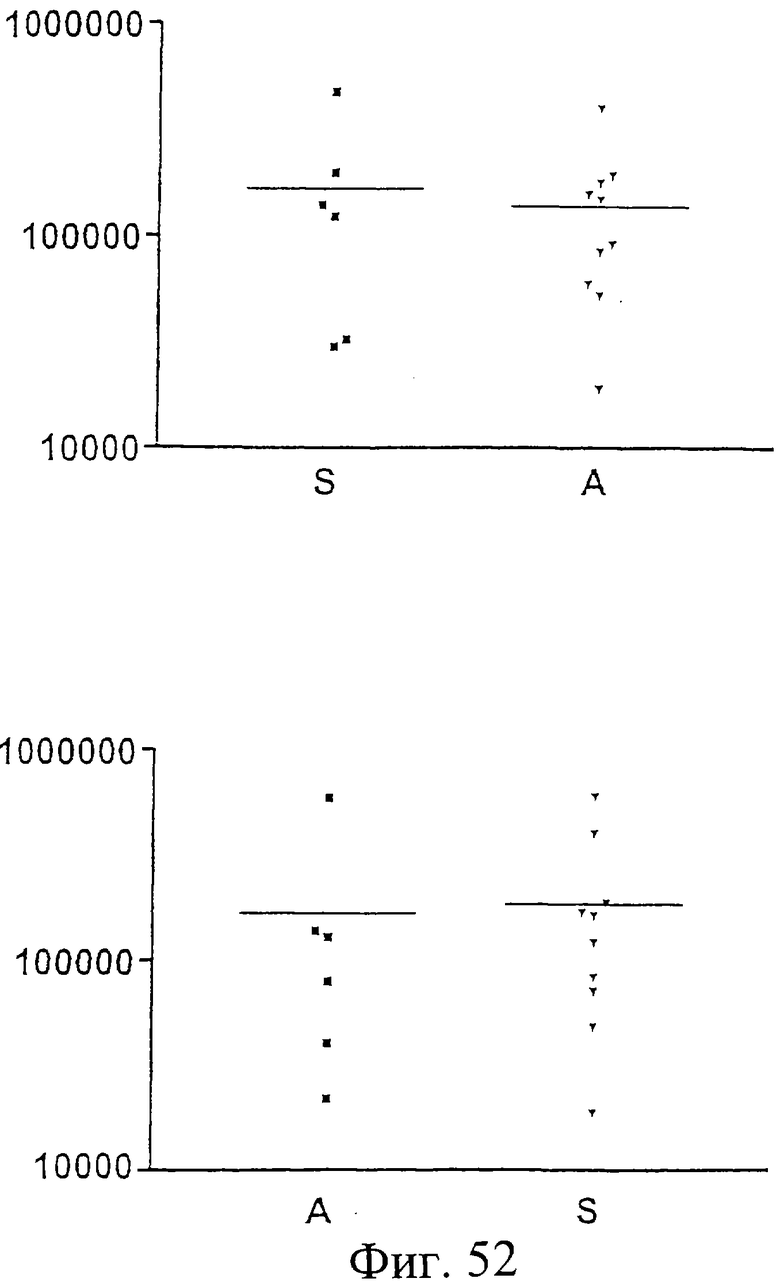
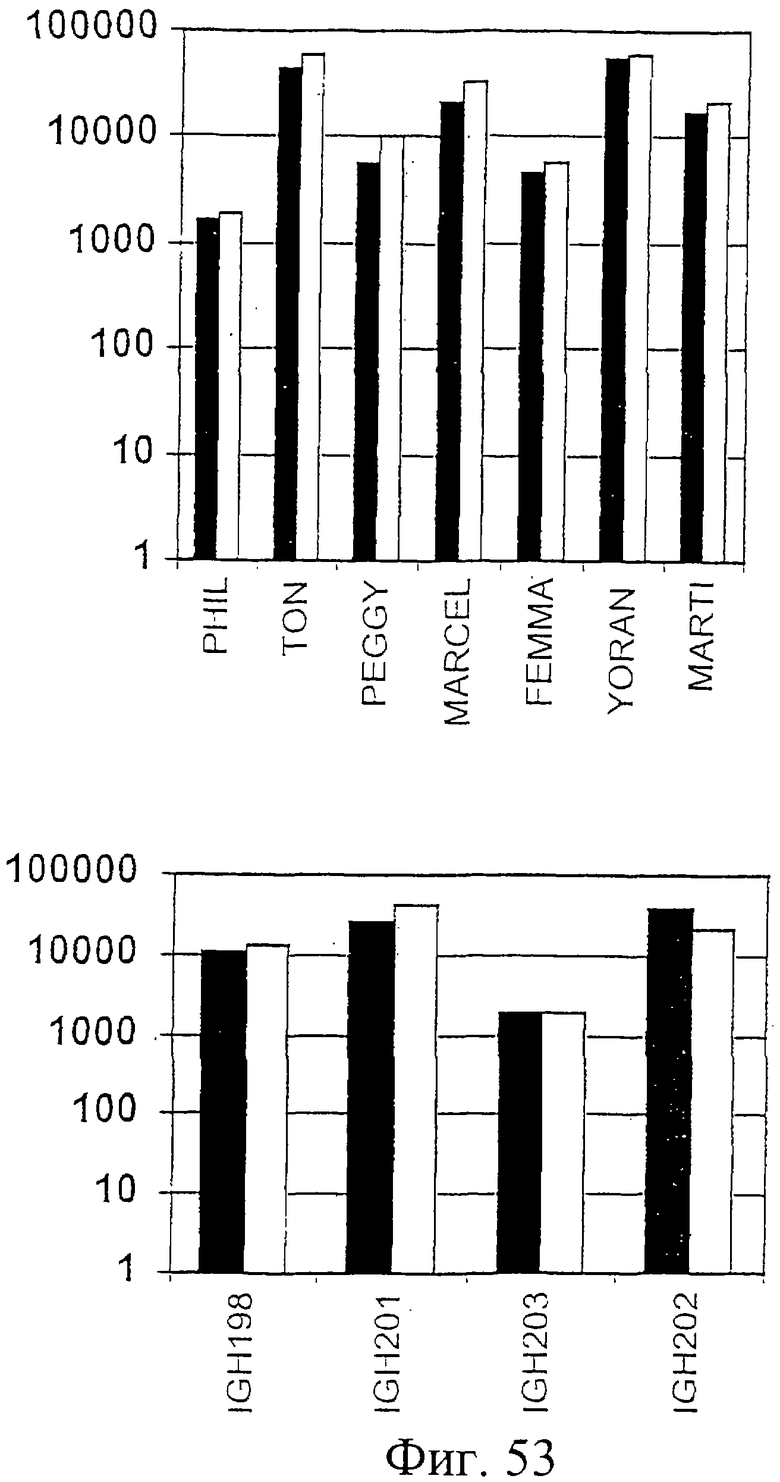
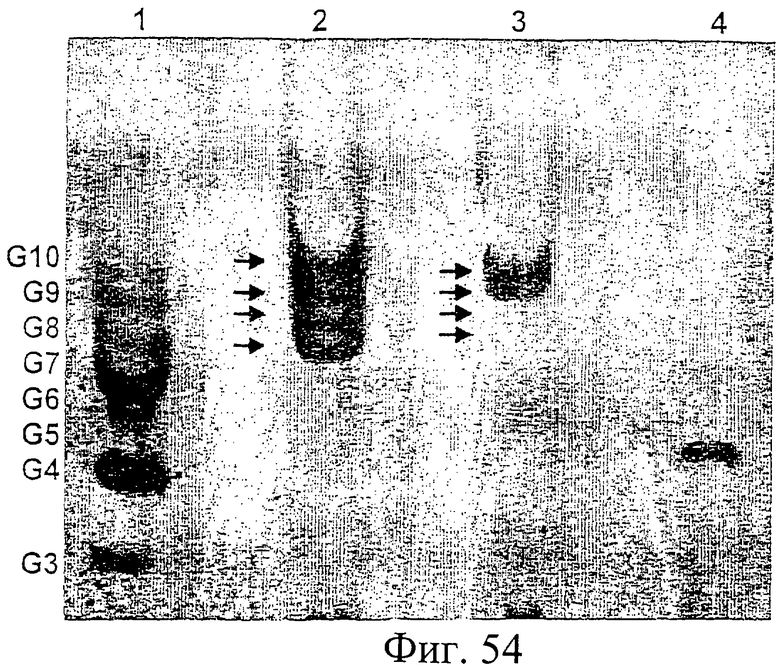
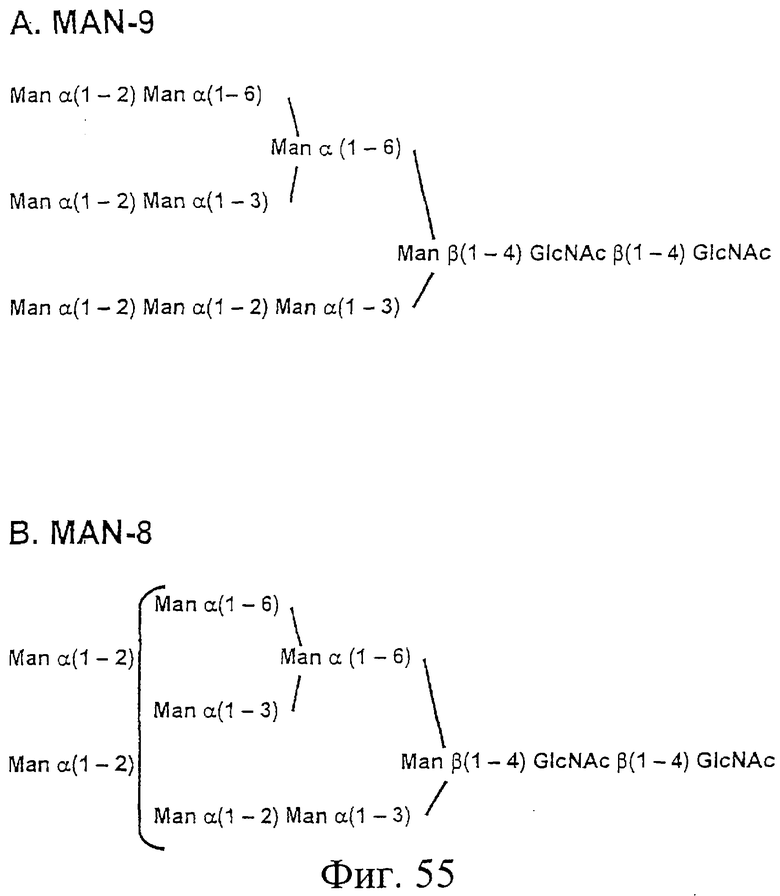
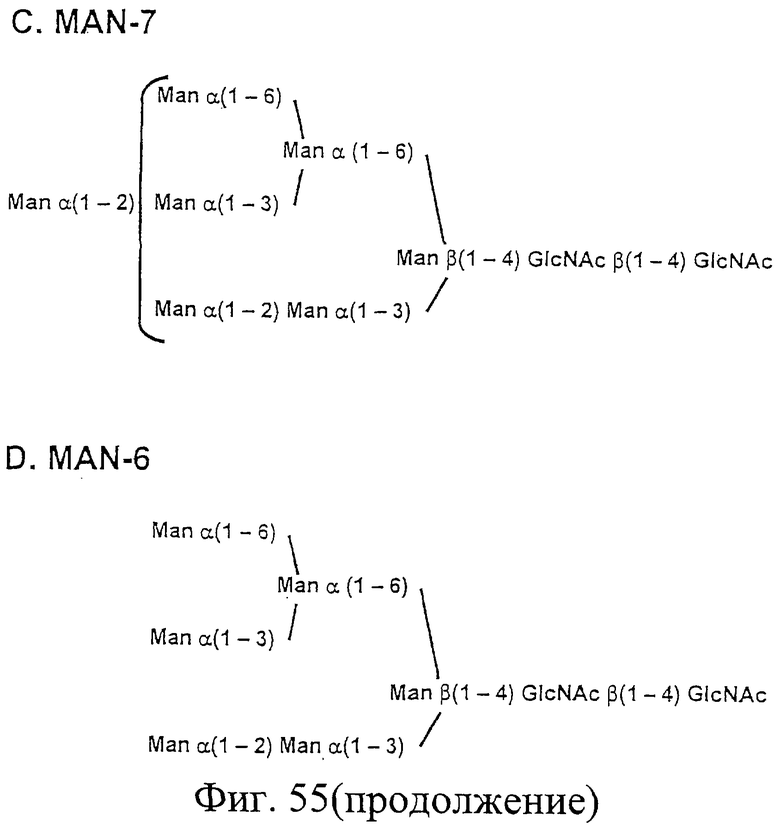

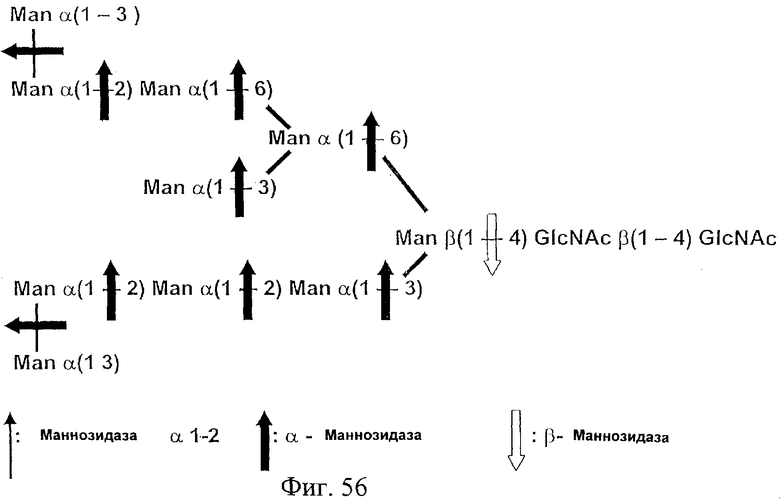
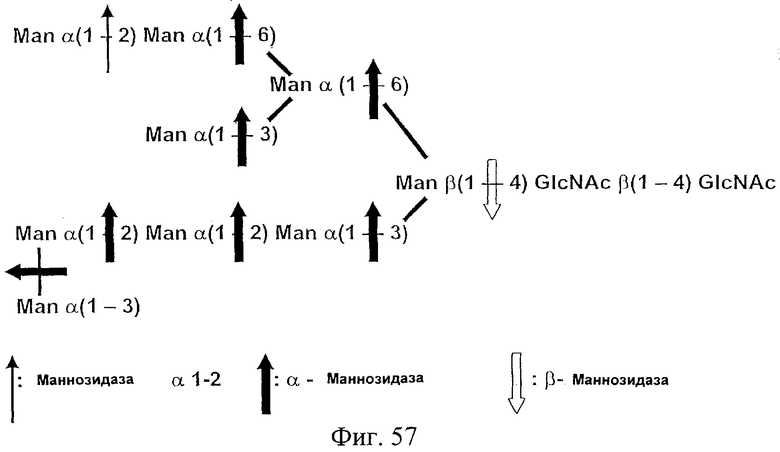
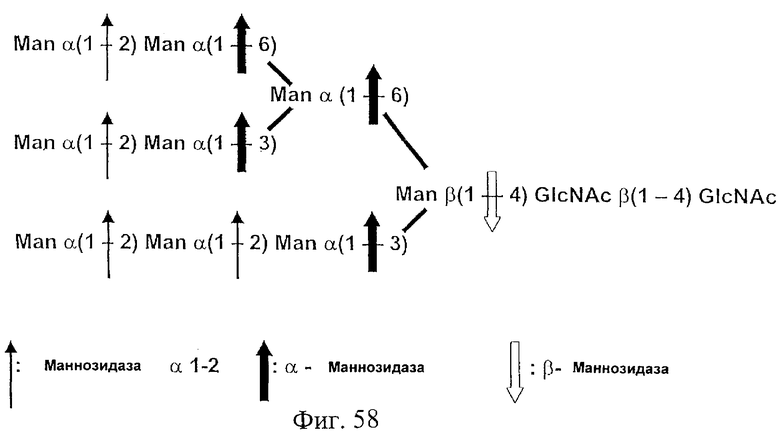
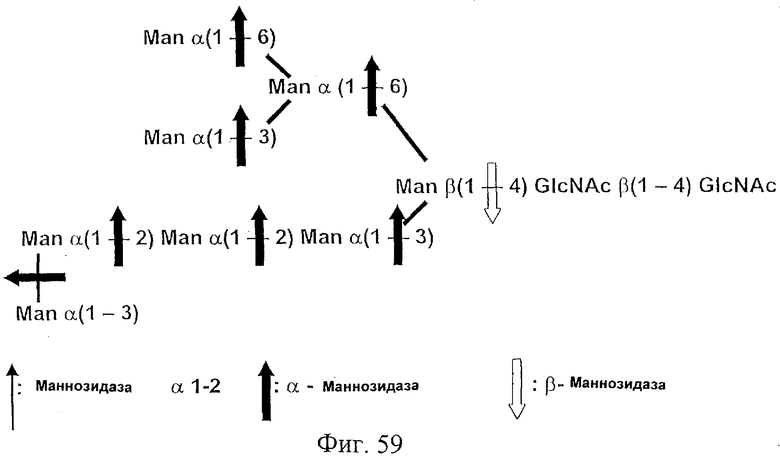
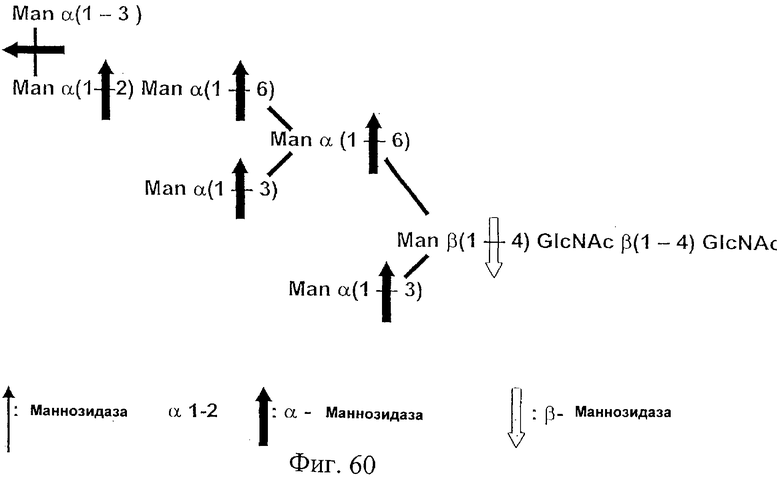
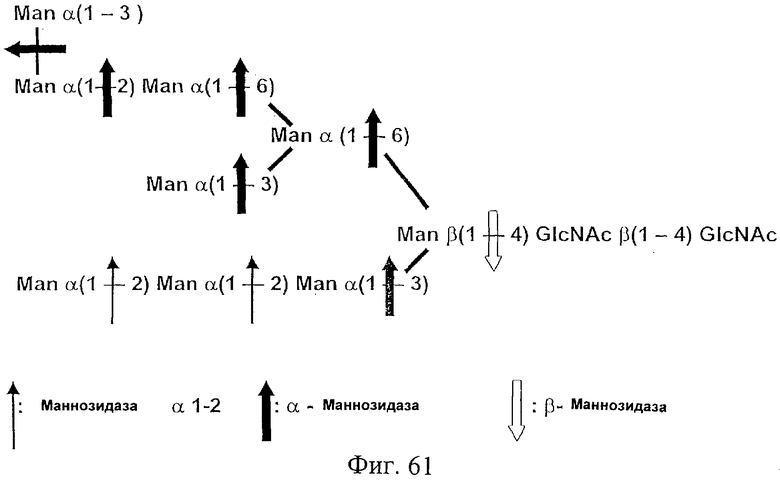

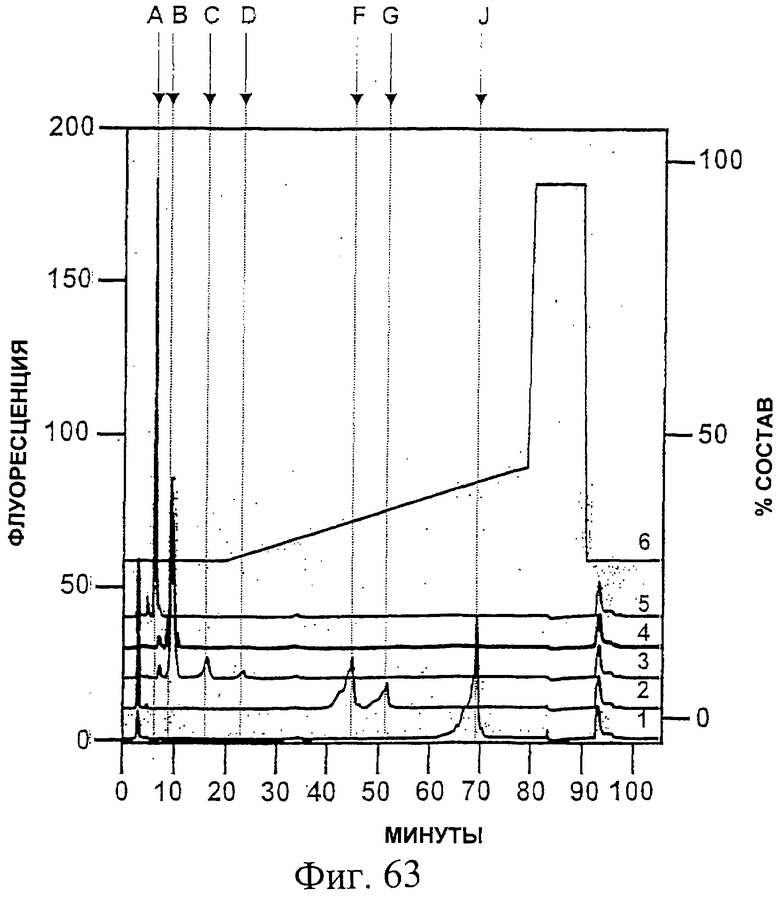
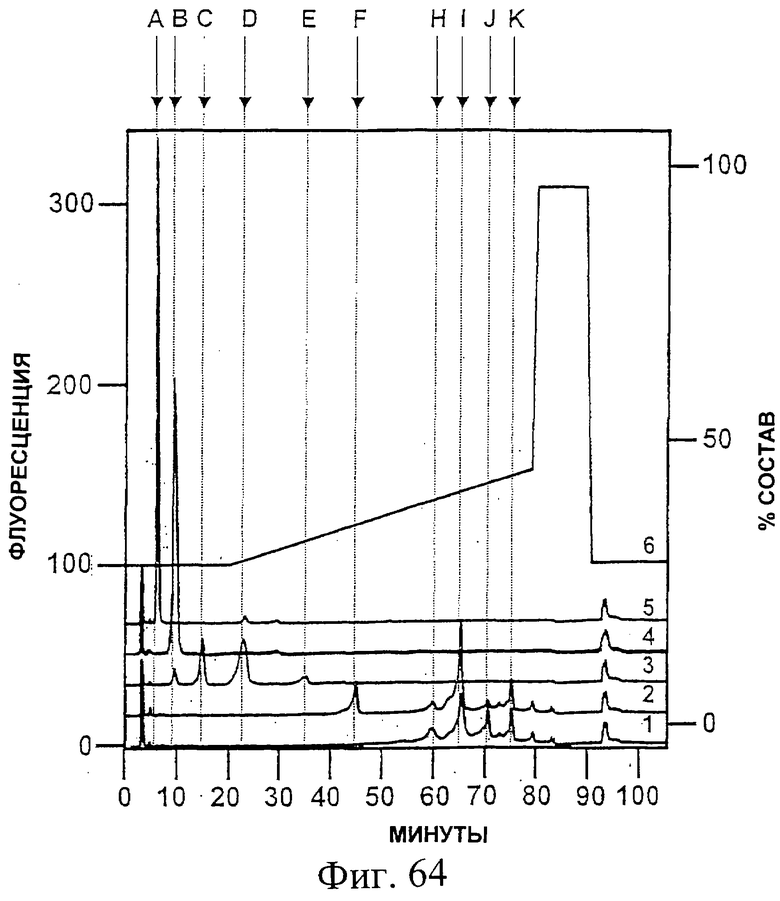
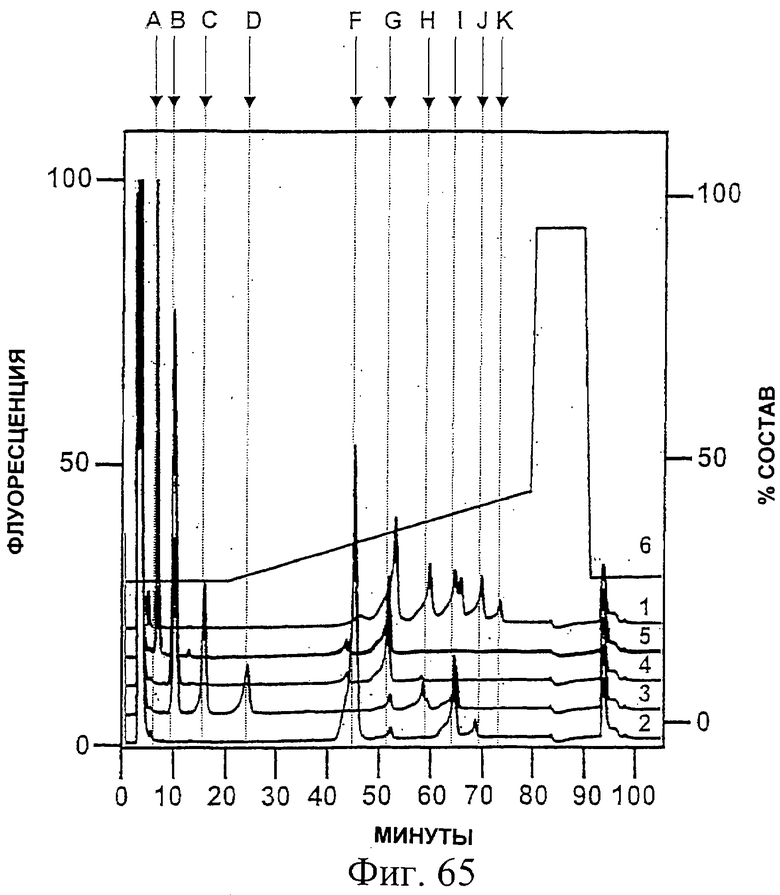
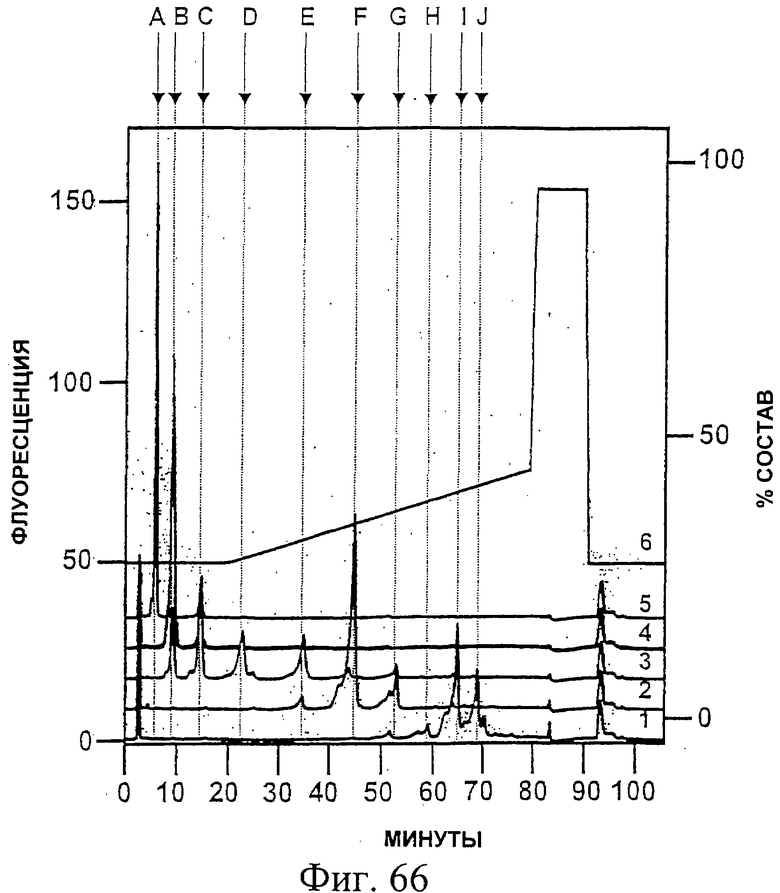
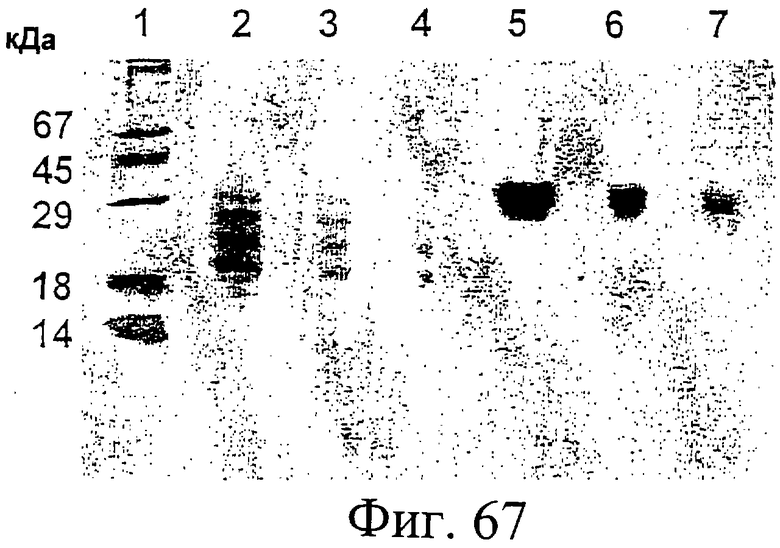

Изобретение относится к области вирусологии и биотехнологии. Предложен оболочечный белок HCV (вирус гепатита С). Белок характеризуется тем, что 80% его сайтов гликозилирования являются кор-гликозилированными. Такой белок является более предпочтительным для его диагностического, профилактического и терапевтического применения. Предложен также способ получения такого белка, а также лекарство, вакцина и различные фармацевтические композиции, содержащие такой белок. Предложенная группа изобретения может быть использована в медицине для диагностики, лечения и профилактики HCV инфекции, а также к прогнозированию клинической эффективности лечения. 12 н. и 25 з.п. ф-лы, 68 ил., 16 табл.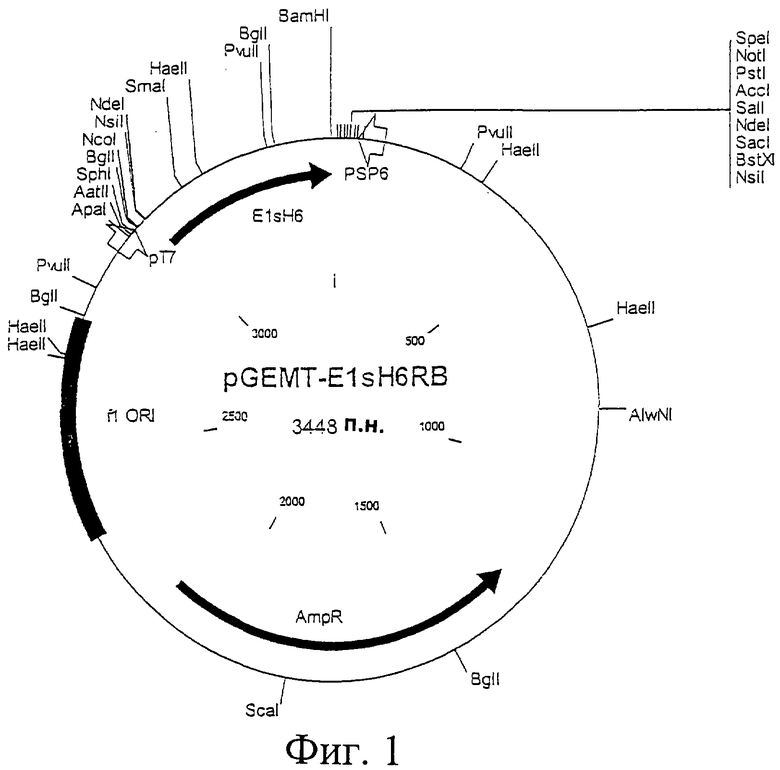
CL-[(Al)a-(PS1)b-(A2)c]-HCVENV-[(A3)d-(PS2)e-(A4)f],
где CL представляет собой лидерный пептид птичьего лизоцима или его функциональный эквивалент;
А1, А2, A3 и А4 являются адаптерными пептидами, которые могут быть одинаковыми или разными;
PS1 и PS2 являются сайтами процессинга, которые могут быть одинаковыми или разными;
HCVENV представляет собой оболочечный белок HCV или его часть;
а, b, с, d, e и f обозначают 0 или 1, и
где, возможно, A1 и/или А2 являются частью PS1, и/или A3 и/или А4 являются частью PS2.
1) оболочечный белок HCV или его часть по любому из пп.1-16 приводят в контакт с указанным образцом в условиях, допускающих образование комплекса указанного оболочечного белка HCV или его части с указанными анти-HCV антителами,
2) выявляют комплекс, образовавшийся на стадии (1), и
3) из результатов стадии (2) делают вывод о присутствии указанных анти-HCV антител в указанном образце.
| WO 9604385, 15.02.1996 | |||
| WO 9967285, 29.12.1999. |
Авторы
Даты
2006-04-20—Публикация
2002-04-24—Подача