Изобретение относится к способу получения 5-амино-1,2,3-тиадиазола, известного в качестве полупродукта для получения фармацевтических препаратов и химических средств защиты растений (DE Off №2506690).
Известен способ получения 5-амино-1,2,3-тиадиазола взаимодействием диазометана с фенилизоцианатом с последующим превращением образующегося 5-анилино-1,2,3-тиадиазола в целевой продукт (Гетероциклические соединения./Под редакцией Р.Эльдерфильда, М.: Мир, 1965, т.7, стр.416). Недостатком этого способа является использование взрывоопасного и ядовитого диазометана.
Известен также способ получения 5-амино-1,2,3-тиадиазола аминированием 5-хлор-1,2,3-тиадиазола, который в свою очередь получают реакцией галоидацетальдегида или его ацеталя с производным гидразина с последующей обработкой образовавшегося ацилгидразона тионилхлоридом (DE Off №2636994, Патент СССР №673171). Недостатком этого способа является низкий выход целевого продукта. Кроме того, 5-хлор-1,2,3-тиадиазол представляет собой термически нестабильное вещество, которое разлагается со взрывом (Termochimica Acta, Vol.47, №1, р.85-94).
Известен также способ получения 5-амино-1,2,3-тиадиазола взаимодействием диазоацетонитрила с сероводородом в среде органического растворителя и в присутствии третичного амина, например, триэтиламина или пиридина. Исходный диазоацетонитрил в свою очередь получают диазотированием аминоацетонитрила в среде органического растворителя действием на него водного раствора нитрита натрия (Авт. свидетельство СССР №956476, опубл. 07.09.1982 г.; J. Chem. Soc., 1956, р.2028). Процесс можно вести как с выделением, так и без выделения диазоацетонитрила.
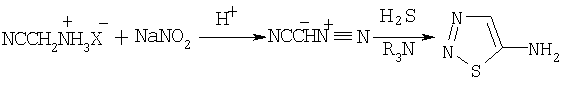
Наиболее близким к заявленному способу является способ получения 5-амино-1,2,3-тиадиазола взаимодействием сульфата аминоацетонитрила в растворе, смеси равных по объему количеств, дихлорметана и четыреххлористого углерода с нитритом натрия в присутствии фосфорной кислоты с последующей реакцией полученного раствора диазоацетонитрила с сероводородом при -10°С (прототип) [Heterocycles Vol.44, №1, 1997, р.197-201]. Недостатком является сложность и связанная с этим длительность процедуры проведения реакции диазотирования, а также недостаточно высокий выход целевого продукта (˜61%, считая на аминоацетонитрил).
Сущность настоящего изобретения состоит в усовершенствовании вышеприведенного способа, а именно в нахождении таких параметров проведения процесса диазотирования аминоацетонитрила, соблюдение которых позволило существенно упростить процесс и вместе с тем получить целевой продукт высокой степени чистоты с выходом более 72%, считая на аминоацетонитрил.
В соответствии с известным способом, описанным в J. Chem. Soc., 1956, р.2026-2029 и его модификацией, описанной в Heterocycles Vol.44, №1, 1997, p.197-201, необходимые для реакции количества нитрита натрия и кислоты, серной или фосфорной, добавляют к раствору аминоацетонитрила не сразу, а ступенчато, то есть отдельными порциями. Когда очередные порции нитрита натрия и кислоты вступят в реакцию, органический слой отделяют, а водный экстрагируют растворителем, затем добавляют новую порцию нитрита натрия и кислоты. Процедуру повторяют до полного завершения реакции. Процесс проводят при температуре 15°С и ниже. Количество нитрита натрия и кислоты, находящихся в реакционной смеси, восстанавливается от начала до конца реакции за счет добавления новых порций реагентов. Такая многоступенчатость операций делает процесс сложным и продолжительным, что создает неблагоприятные условия для устойчивости образующегося диазоацетонитрила и для получения высокого выхода целевого продукта.
В соответствии с настоящим изобретением процесс диазотирования аминоацетонитрила проводят при температуре, не превышающей 0°С, точнее от -5 до 0°С. Нитрит натрия и ортофосфорную кислоту при этой температуре добавляют последовательно к раствору аминоацетонитрила в смеси равных по объему количеств дихлорметана и четыреххлористого углерода, после чего реакционную смесь перемешивают при этой температуре в течение 30-60 минут, предпочтительно 50-60 минут. Органический слой отделяют, водный экстрагируют растворителем. Объединенные растворы охлаждают до -10 - -12°С, добавляют триэтиламин и пропускают в реакционную смесь сероводород в количестве, незначительно превышающем 1 моль на 1 моль содержащегося в растворе диазоацетонитрила. Выпавший в осадок 5-амино-1,2,3-тиадиазол отфильтровывают. Растворитель регенерируют и используют повторно. На стадии диазотирования кислотность среды поддерживают на уровне рН 1-2.
По сравнению с прототипом количество операций и продолжительность процесса сокращаются, а выход целевого продукта, пригодного для дальнейшего использования без дополнительной очистки, возрастает более чем на 10%.
Пример 1
К раствору 5,67 г (0,054 моль) сульфата аминоацетонитрила в 7 мл воды добавляют 100 мл смеси равных объемов хлористого метилена и четыреххлористого углерода. Реакционную смесь охлаждают до -5°С и при перемешивании по каплям прибавляют раствор 5,25 г (0,076 моль нитрита натрия в 10 мл воды (избыток 40%), поддерживая температуру реакционной смеси не выше 0°С. Далее к реакционной смеси при температуре от -5 до 0°С прибавляют 6,5 мл 4 н. раствора ортофосфорной кислоты и при той же температуре продолжают перемешивание в течение 50-60 минут (рН среды 1-2). Органический слой отделяют, а водный трижды экстрагируют смесью равных по объему количеств хлористого метилена и четыреххлористого углерода (2×30 мл и 1×25 мл). Объединенные органические фазы промывают 4,65 мл 2 н. раствора углекислого натрия и 9,25 мл воды, сушат 1 час над сульфатом натрия и охлаждают до -12- -10°С. К охлажденному раствору медленно прибавляют 3,58 мл (0,0257 моль) триэтиламина и пропускают 2,00 г (0,059 моль) сероводорода. Реакционную массу перемешивают при -10°С 15 минут. Выпавший осадок отфильтровывают, промывают небольшим количеством гексана. Растворитель регенерируют. Получают 3,95 г 5-амино-1,2,3-тиадиазола, tплавл=146-147°С. Выход 72,5%. В ПМР-спектре, снятом в d-DMCO присутствовали синглеты в области 7,60 млн. д. (1Н, С4-Н) и в области 6,85 млн. д. (2Н, NH2), в ИК-спектре наблюдали поглощение NH2-группы в области 3335 и 3277 см -1.
Пример 2. Процесс проводят в условиях примера 1, но время перемешивания после прибавления ортофосфорной кислоты составляет 1,5 часа. Получают 3,93 г 5-амино-1,2,3-тиадиазола, tплавл=146-147°С. Выход 72,1%.
Пример 3. Процесс проводят в условиях примера 1, но время перемешивания составляет 30 минут. Получают 3,75 г 5-амино-1,2,3-тиадиазола, tплавл=145-146°С. Выход 68,8%.
Пример 4. Процесс проводят в условиях примера 2, но полученный раствор диазоацетонитрила используют для дальнейшей реакции без высушивания над сульфатом натрия. Получают 3,81 г 5-амино-1,2,3-тиадиазола, tплавл=142-143°С. Выход 69,9%.
Пример 5. Процесс проводят в условиях примера 1, но в реакцию вводят 4,84 г (0,070 моль), т.е. 30%-ный избыток нитрита натрия. Получают 3,84 г 5-амино-1,2,3-тиадиазола, tплавл=145-146°С. Выход 70,5%.
Пример 6. Процесс проводят в условиях примера 1, но в реакцию вводят 5,4 г (0,078 моль), т.е. 45%-ный избыток нитрита натрия. Получают 3,9 г 5-амино-1,2,3-тиадиазола, tплавл=145-146°С. Выход 71,4%.
Пример 7. Процесс проводят в условиях примера 2, но в реакцию вводят 4,5 г (0,065 моль), т.е. 20%-ный избыток нитрита натрия. Получают 3,65 г 5-амино-1,2,3-тиадиазола, tплавл=145-146°С. Выход 67%.
Пример 8. Процесс проводят в условиях примера 1 с использованием на стадии диазотирования 70 мл смеси равных по объему количеств хлористого метилена и четыреххлористого углерода. Получают 3,74 г 5-амино-1,2,3-тиадиазола, tплавл=143-144°С. Выход 68,4%.
Пример 9. Процесс проводят в условиях примера 1 с использованием на стадии диазотирования 50 мл смеси равных по объему количеств хлористого метилена и четыреххлористого углерода. Получают 3,60 г 5-амино-1,2,3-тиадиазола. Выход 66,1%, tплавл=143-144°С.
Пример 10. Процесс проводят в условиях примера 1, но ортофосфорную кислоту добавляют в эквимолярном с учетом основности количестве по отношению к нитриту натрия, то есть 2,96 г 85%-ной кислоты (объем 6,5 мл). Получают 2,55 г 5-амино-1,2,3-тиадиазола, tплавл=142-143°С. Выход 46,8%.
Таким образом, опытным путем установлено, что при соблюдении температурного режима от - 5 до 0°С и одновременном добавлении к раствору аминоацетонитрила раствора нитрита натрия в количестве, превышающем эквимолярное на 30-40%, и поддержании кислотности среды на уровне рН 1-2 за счет прибавления рассчитанного количества ортофосфорной кислоты процесс диазотирования аминоацетонитрила завершается в течение 30-60 минут. Дальнейшее перемешивание до 1,5 часа не вносит никаких изменений в конечный результат. Процесс становится более простым и компактным. Образовавшийся диазоацетонитрил пригоден для получения 5-амино-1,2,3-тиадиазола без какой-либо дополнительной обработки или очистки. Выход целевого продукта при сохранении качества значительно (на 10%) повышается по сравнению с прототипом.
Показано также, что полученный новым способом раствор диазоацетонитрила можно вводить в реакцию с сероводородом без освобождения его от содержащейся в нем воды. При этом не наблюдается существенного снижения выхода и ухудшения качества продукта.
Уменьшение количества растворителя допустимо только в определенных пределах. Как показали опыты, дальнейшее уменьшение количества растворителя приводит к снижению выхода целевого продукта из-за достаточно высокой растворимости диазоацетонитрила в воде.
Также показано, что увеличение количества ортофосфорной кислоты на стадии диазотирования аминоацетонитрила не приводит к увеличению выхода конечного продукта. Наоборот, наблюдается его снижение, т.е. используемое количество ортофосфорной кислоты является оптимальным для представленного процесса.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 5-амино-1,2,3-тиадиазола | 1980 |
|
SU956476A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-АМИНО-2-МЕРКАПТОБЕНЗОЙНОЙ КИСЛОТЫ (ВАРИАНТЫ), ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2176241C2 |
| Способ получения 5-меркапто-1,2,3-триазолов | 1979 |
|
SU961559A3 |
| Способ получения 1,2,3-тиадиазол-5-ил-мочевин | 1979 |
|
SU921466A3 |
| ПРОИЗВОДНОЕ 2-ЗАМЕЩЕННОГО САХАРИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ ИНГИБИТОРНУЮ АКТИВНОСТЬ ПРОТИВ ЭЛАСТАЗЫ | 1992 |
|
RU2101281C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЛЕСКО-СТРУКТУРООБРАЗУЮЩЕЙ ДОБАВКИ ДЛЯ ЭЛЕКТРОЛИТА СЕРНОКИСЛОГО МЕДНЕНИЯ | 1991 |
|
RU2027703C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОАЗОКРАСИТЕЛЕЙ | 1970 |
|
SU288201A1 |
| СПОСОБ ПОЛУЧЕНИЯ М-ГАЛОИДФЕНОЛОВ | 2000 |
|
RU2177932C1 |
| МЕТИЛОВЫЙ ЭФИР 4-ЙОД-2-[N-(N-АЛКИЛАМИНОКАРБОНИЛ)АМИНОСУЛЬФОНИЛ]-БЕНЗОЙНОЙ КИСЛОТЫ, ЕГО ПРОИЗВОДНЫЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2309948C2 |
| Способ получения производных 1,2,3-тиадиазол-5-илмочевины | 1979 |
|
SU927114A3 |
Изобретение относится к области органической химии, в частности к способу получения 5-амино-1,2,3-тиадиазола, который может быть использован в качестве промежуточного продукта для получения фармацевтических препаратов и химических средств защиты растений. Описывается способ получения 5-амино-1,2,3-тиадиазола диазотированием аминоацетонитрила с последующей реакцией образовавшегося диазоацетонитрила в растворе смеси равных по объему количеств дихлорметана и четыреххлористого углерода с сероводородом в присутствии триэтиламина при температуре (-) 10°С, причем получение диазоацетонитрила в растворе смеси равных по объему количеств дихлорметана и четыреххлористого углерода осуществляют путем последовательного прибавления к исходному раствору аминоацетонитрила при температуре от (-) 5°С до 0°С водных растворов нитрита натрия в количестве, превышающем эквимолярное по отношению к аминоацетонитрилу на 30-40%, и ортофосфорной кислоты до достижения рН 1-2, перемешивания реакционной смеси при этой температуре в течение 30-60 минут с последующим превращением полученного диазоацетонитрила в целевой продукт известным способом. Предложенный способ позволяет упростить технологический процесс и получить целевой продукт, пригодный для использования без дополнительной очистки, с выходом 72,5%.
Способ получения 5-амино-1,2,3-тиадиазола взаимодействием сульфата аминоацетонитрила в растворе смеси равных по объему количеств дихлорметана и четыреххлористого углерода с нитритом натрия в присутствии фосфорной кислоты при охлаждении с последующей реакцией образовавшегося диазоацетонитрила в растворе смеси равных по объему количеств дихлорметана и четыреххлористого углерода с сероводородом в присутствии триэтиламина при температуре (-) 10°С, отличающийся тем, что получение диазоацетонитрила в растворе смеси равных по объему количеств дихлорметана и четыреххлористого углерода осуществляют путем последовательного прибавления к исходному раствору аминоацетонитрила при температуре от (-) 5°С до 0°С водных растворов нитрита натрия в количестве, превышающем эквимолярное по отношению к аминоацетонитрилу на 30-40%, и ортофосфорной кислоты до достижения рН 1-2, перемешивания реакционной смеси при этой температуре в течение 30-60 мин с последующим превращением полученного диазоацетонитрила в целевой продукт известным способом.
| HARADA, KATSUMASA et al | |||
| Heterocycles | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Способ получения 5-амино-1,2,3-тиадиазола | 1980 |
|
SU956476A1 |
| Приспособление для регулирования давления пара в котле | 1931 |
|
SU31548A1 |
| US 4269982 A, 26.05.1981 | |||
| US 5075427 A, 24.12.1991 | |||
| JP 52068181 A, 06.06.1977 | |||
| P.C.БЕЛЕНЬКАЯ и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Химия гетероциклических соединений | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ формования из композитного материала пустотелых аэродинамических поверхностей - 2 | 2016 |
|
RU2636994C1 |
Авторы
Даты
2006-05-10—Публикация
2004-11-22—Подача