Область изобретения
Данное изобретение относится к использованию замещенных пиразолов для лечения аллергического заболевания.
Предпосылки создания изобретения
Атопическая аллергия поражает по крайней мере 20% населения в развитых странах и включает широкий диапазон IgE-опосредованных заболеваний, таких как сенная лихорадка, астма, атопический дерматит и пищевые аллергии. Воздействие на субъекта, подверженного аллергии, соответствующих аллергенов приводит к поперечному связыванию аллерген-специфической IgE связи с тучными клетками, инициируя дегрануляцию и высвобождение провоспалительных медиаторов, таких как гистамин и эйкозаноиды, которые вызывают ответную реакцию благополучие-и-сигнал в кожном тесте. Обычно, за такой ранней ответной реакцией следует продолжительная поздняя реакция, в которой воспалительные клетки, в частности эозинофилы и активированные ТН-2 CD4 T-клетки, привлекаются в место аллергического воздействия. Воспалительные цитокины, такие как IL-4 и IL-5, оба продуцируемые ТН-2 клетками, важны для продуцирования IgE В-клетками и для эозинофилии соответственно. Было показано, что иммунотерапия, нацеленная на CD4 Т-клетки, является эффективной для снижения продуцирования IgE, активации провоспалительных клеток и высвобождения воспалительных медиаторов.
Лечение аллергии в настоящее время, нацеленное на CD4 Т-клетки, имеет смешанный успех. Уменьшение чувствительности с использованием аллергеновых экстрактов или вакцин является эффективным в случае многих аллергенов, таких как укусы насекомых Hymenoptera, которые могут вызывать угрожающие жизни аллергические реакции. Механизм может представлять собой либо индуцирование толерантности Т-клеток, либо превращение ТН-2 в ТН-1. Однако такое лечение требует продолжительного режима лечения, частых визитов лечащего врача и предварительную стабилизацию с использованием других лекарственных средств и связано с некоторой долей болезненности и редкими смертями. Альтернативно, иммуноподавляющие лекарственные средства, такие как стероиды, которые эффективно стабилизируют начинающиеся аллергические ответные реакции, часто связаны с серьезными побочными действиями.
Активация CD4 Т-клеток является основным фактором в инициировании и сохранении аллергической ответной реакции. Аллергены поглощаются специализированными антиген-представляющими клетками (APCs), такими как дендритные клетки и В-клетки. Белковые аллергены проходят через эндосомальную и лизосомальную системы, где они разрушаются различными протеазами. Такие пептидные фрагменты связываются молекулами МНС класса II, которые на клеточной поверхности представляют собой гетеротримерные комплексы, состоящие из двух трансмембранных гликопротеиновых цепей (α и β), которые образуют связывающую поддержку для третьего компонента, пептида из 11-20 аминокислот. Комплекс антиген-молекула МНС класса II распознается CD4 Т-клетками и приводит к активации Т-клетки. Активированные Т-клетки, в свою очередь, активируют несколько других компонентов иммунной системы, таких как В-клетки и макрофаги, которые являются ключевыми для ответной реакции тела на патогены, но также приводят к симптомам аллергии.
Молекулы класса II, как и другие трансмембранные белки, перемещаются в эндоплазматическую сеть (ER) после синтеза, где они связываются с третьим белком, инвариантной цепью (Ii). Инвариантная цепная молекула представляет собой трансмембранный белок типа II, который служит в качестве класс II-специфического компаньона, промотирующего выход комплексов класс II-Ii из ER и не допускающего связывания молекул класса II с пептидами и развернутыми белками в ER и секреторном пути. Целенаправляющий мотив в цитоплазматическом хвосте Ii направляет комплексы класс II-Ii из секреторного пути в эндосомальную систему.
Прежде чем молекулы МНС класса II смогут представлять собой антиген, Ii должен быть удален рядом протеаз, которые отщепляют Ii. Конечные Ii пептидные фрагменты, называемые класса II-связанные инвариантные цепные пептиды (CLIP), занимают место пептидного связывания молекулы класса II и в большинстве случаев самопроизвольно не высвобождаются. CLIP защищает связывающую зону класса II от свертывания как во время внутриклеточного транспорта, так и после Ii разрушения в эндосомальной системе. Связывание антигенных пептидов, генерированных из эндоцитозных белков, требует свободного и уже открытого сайта связывания. Следовательно, CLIP должен высвобождаться во время, когда открытый сайт связывания стабилизирован, чтобы давать возможность связывания с другими пептидами. Лейкоцитный антиген человека -DM («HLA-DM») опосредует обе такие функции, промотируя таким образом связывание антигенных пептидов. После связывания пептидов молекулы класса II транспортируются к клеточной поверхности через пути, которые большей частью не известны.
Принимая вышеизложенное во внимание, ингибирование протеолиза инвариантной цепи будет предотвращать удаление Ii из связывающей зоны класса II, что, в свою очередь, будет специфически блокировать связывание антигена с молекулой МНС класса II.
Катепсин S (CatS) представляет собой цистеинпротеазу, экспрессируемую в лимфатических тканях. CatS опосредует протеолиз инвариантной цепи, что является предпосылкой пептидного нагружения молекул класса II (Riese et al. (1996) Immunity 4:357). CatS имеет 50-60% гомологию с катепсинами L и К, но отличается от них тем, что имеет широкий оптимум рН, который расширен в щелочную область рН. CatS модулирует антигенную демонстрацию на животных моделях, и ингибиторы являются эффективными на модели астмы (Riese et al. (1998) J.Clin.Invest. 101:2351). Катепсин S-дефицитные мыши обладают ослабленной способностью представлять экзогенные белки с помощью профессиональных антиген-представляющих клеток (Nakagawa et al (1999) Immunity 10:207; Shi et al. (1999) Immunity 10:197).
Предполагается, что соединения, которые ингибируют протеолитическую активность катепсина S человека, могут найти применение для лечения хронических аутоиммунных заболеваний, включая, но не ограничиваясь ими, волчанку и ревматоидный артрит; и имеют потенциальную полезность для модулирования иммунного ответа на трансплантацию тканей. Способы модулирования аутоиммунитета с помощью агента, который модулирует активность катепсина S, например, протеолиз Ii цепи, а также способы лечения субъекта, имеющего аутоиммунное заболевание, способы оценки лечения на его способность модулировать иммунный ответ описаны в WO 99/58153.
Соединения, некоторым образом подобные соединениям настоящего изобретения, описаны в следующих ссылках.
Winters и др. ((Winters G., Sala A., Barone D., Baldoli E. J.Med.Chem., 1985, 28, 934-940; Singh P., Sharma R.C., Quant. Struct. -Act. Relat. 1990, 9, 29-32; Winters G., Sala A., Barone D. в патенте США 4500525 (1985)) описали бициклические пиразолы показанного ниже типа. Заместитель R никогда не содержит гетероциклическое кольцо, и данным молекулам не предписывается никакой ингибирующей активности в отношении протеазы; они описаны в качестве модуляторов α1-адренергических рецепторов.
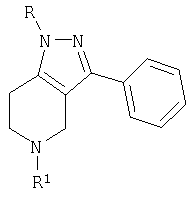
Shutske и др. описали представленные ниже бициклические пиразолы. В их системе пиридиновое кольцо является ароматическим (Shutske G.M., Kapples K.J., Tomer J.D. Патент США 5264576 (1993)). Другая ссылка относится к R, являющемуся линкером для гетероцикла, формула изобретения указывает только R=водород. Соединения упоминаются в качестве ингибиторов обратного захвата серотонина.

Соединение 2-[4-[4-(3-метил-5-фенил-1Н-пиразол-1-ил)бутил]-1-пиперазинил]пиримидин известно из ЕР-382637, где описаны пиримидины, обладающие анксиолитическими свойствами. Данное соединение и его аналоги дополнительно описаны в ЕР-502786 в качестве сердечно-сосудистых агентов и агентов в отношении центральной нервной системы. Фармацевтические препараты с такими соединениями описаны в ЕР-655248 для применения при лечении желудочной секреции и в качестве противоязвенных агентов. В WO 9721439 описаны лекарственные средства с такими соединениями для лечения обцессивно-компульсивных нарушений, апноэ (отдышка) во сне, половых расстройств, рвоты и морской болезни.
Соединения 5-метил-3-фенил-1-[4-(4-фенил-1-пиперазинил)бутил]-1Н-индазол и 5-бром-3-(2-хлорфенил)-1-[4-(4-фенил-1-пиперазинил)бутил]-1Н-индазол, в частности их гидрохлоридные соли, известны из WO-9853940 и СА122:314528, где данные и подобные им соединения описаны в качестве ингибиторов киназы в первой ссылке и как обладающие сродством к бензодиазепиновым рецепторам в последней ссылке.
Краткое изложение сущности изобретения
Объектом настоящего изобретения является применение ингибиторов катепсина S для лечения аллергических заболеваний, включая, но не ограничиваясь этим, атопические аллергии. Примеры аллергического заболевания включают сенную лихорадку, астму, атопический дерматит и пищевые аллергии. Аллергены включают пыль, пыльцу, плесень и аллергию на домашних животных или шерсть домашних животных.
В одном аспекте настоящее изобретение относится к способу лечения субъекта, страдающего от аллергического заболевания, в частности от атопического аллергического заболевания, который включает введение указанному субъекту терапевтически эффективного количества фармацевтической композиции, включающей ингибитор катепсина S.
В другом аспекте настоящее изобретение относится к способу лечения субъекта, страдающего от IgE-опосредованного аллергического заболевания, в частности от атопического аллергического болезненного состояния, который включает введение указанному субъекту терапевтически эффективного количества фармацевтической композиции, включающей ингибитор катепсина S.
В третьем аспекте изобретение относится к применению или применению для получения лекарственного средства ингибитора катепсина S для лечения аллергического заболевания, более конкретно для лечения IgE-опосредованных аллергических заболеваний, еще более конкретно для лечения сенной лихорадки, астмы, атопических дерматитов или пищевых аллергий. Изобретение также относится к противоаллергическим фармацевтическим композициям, включающим в качестве активного ингредиента эффективное количество ингибитора катепсина S и фармацевтически приемлемый носитель. Активный ингредиент может быть введен в состав лекарственного средства любым способом, подходящим для конкретного аллергического заболевания, включая аэрозоль, пероральные и местные препараты и препараты замедленного высвобождения.
Настоящее изобретение касается лечения аллергического заболевания с использованием одного или нескольких соединений, которые могут быть представлены формулой (I):
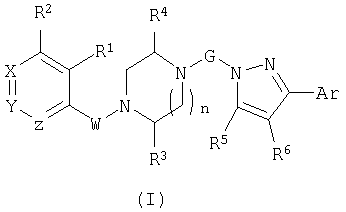
где
R1 представляет собой водород, азидо, галоген, С1-5 алкокси, гидрокси, С1-5 алкил, С2-5 алкенил, циано, нитро, R7R8N, С2-8 ацил, R9OC=O, R10R11NC=O или R10R11NSO2, или R1 взят вместе с W, как описано ниже;
R2 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, С2-5 алкенил, С1-5 галогеналкил, циано или R48R49N;
альтернативно, R1 и R2 могут быть взяты вместе с образованием необязательно замещенного 5-7-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим;
каждый R3 и R4 независимо представляет собой водород или С1-5 алкил;
каждый R5 и R6 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, С1-5 алкокси, С1-5 алкилтио, галоген или 4-7-членный карбоциклил или гетероциклил;
альтернативно, R5 и R6 могут быть взяты вместе с образованием необязательно замещенного 5-7-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим, и необязательно может быть замещено одним-тремя заместителями, независимо выбранными из галогена, циано, амино, нитро, R40, R40O-, R40S-, R40O(C1-5 алкилен)-, R40O(C=O)-, R40(C=O)-, R40(C=S)-, R40(C=O)O-, R40O(C=O)(C=O)-, R40SO2, NHR62(C=NH)-, NHR62SO2- и NHR62(C=O)-;
R40 представляет собой Н, С1-5 алкил, С2-5 алкенил, фенил, бензил, фенэтил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен, амино или моно- или ди(С1-5 алкил)амино, или R58OR59-, где R58 представляет собой Н, С1-5 алкил, С2-5 алкенил, фенил, бензил, фенэтил, С1-5 гетероциклил или (С1-5 гетероциклил)С1-6 алкилен, и R59 представляет собой С1-5 алкилен, фенилен или двухвалентный С1-5 гетероциклил; и
R62 может представлять собой Н в дополнение к значениям для R40;
R7 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R27OC=O, R28R29NC=O, R27SO, R27SO2 или R28R29NSO2;
R8 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R7 и R8 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
R9 представляет собой С1-5 алкил, фенил, нафтил или С1-5 гетероциклил;
R21 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R30OC=O, R31R32NC=O, R30SO, R30SO2 или R31R32NSO2;
R22 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R21 и R22 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R23, R26, R27, R30, R33, R44, R45 и R50 представляет собой С1-5 алкил, фенил, нафтил или С1-5 гетероциклил;
R24 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R33OC=O, R34R35NC=O, R33SO, R33SO2 или R34R35NSO2;
R25 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R24 и R25 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R10 и R11 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R10 и R11 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R28, R29, R31, R32, R34, R35, R46, R51 и R52 независимо представляет собой водород, С1-5 алкил, фенил или С1-5 гетероциклил;
альтернативно, R28 и R29, R31 и R32,R34 и R35, R46 и R47, илиR51 и R52 независимомогут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
n равно 1 или 2;
G представляет собой С3-6 алкендиил или С3-6 алкандиил, необязательно замещенный гидрокси, галогеном, С1-5 алкилом, С1-5 алкокси, оксо, гидроксиимино, CO2R60, R60R61NCO2, (L)-C1-4 алкиленом, (L)-C1-5 алкокси, N3 или [(L)-C1-5алкилен]амино;
каждый R60 и R61 независимо представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил, фенэтил или С1-5 гетероциклил;
альтернативно, R60 и R61 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
L представляет собой амино, моно- или ди-С1-5 алкиламино, пирролидинил, морфолинил, пиперидинил, гомопиперидинил или пиперазинил, где доступные кольцевые атомы азота могут быть необязательно замещены С1-5 алкилом, бензилом, С2-5 ацилом, С1-5 алкилсульфонилом или С1-5 алкоксикарбонилом;
Х представляет собой азот или R12C;
Y представляет собой азот или R13C;
Z представляет собой азот или R14C;
R12 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R21R22N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен, R23OC=O, R23O(C=O)NH-, R23SO, R22NHCO-,, R22NH(C=O)NH-, R23(C1-4 алкилен)NHCO-, R23SO2 или R23SO2NH-;
R13 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R42R43N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен R44OC=O, R44O(C=O)NH-, R44SO, R43NHCO-, R43NH(C=O)NH-, R44(C1-4 алкилен)NHCO-, R44SO2 или R44SO2NH-;
R14 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R24R25N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен R26OC=O, R26O(C=O)NH-, R26SO, R25NHCO-, R25NH(C=O)NH-, R26(C1-4 алкилен)NHCO-, R26SO2 или R26SO2NH-;
альтернативно, R12 и R13 или R12 и R2, илиR13 и R14 могут быть взяты вместе с образованием необязательно замещенного 5-6-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим;
Ar представляет собой моноциклическое или бициклическое арильное или гетероарильное кольцо, необязательно замещенное 1-3 заместителями, выбранными из галогена, С1-5 алкокси, С1-5 алкила, С2-5 алкенила, циано, азидо, нитро, R15R16N, R17SO2, R17S, R17SO, R17O(C=O), R15R16NC=O, С1-5 галогеналкила, С1-5 галогеналкокси, С1-5 галогеналкилтио и С1-5 алкилтио;
R15 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил, С1-5 гетероциклил, С2-8 ацил, ароил, R53OC=O, R54R55NC=O, R53S, R53SO, R53SO2 или R54R55NSO2;
R16 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил или С1-5 гетероциклил;
альтернативно, R15 и R16 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R17 и R53 представляет собой С1-5 алкил, фенил или С1-5 гетероциклил;
каждый R54 и R55 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, фенил, бензил или С1-5 гетероциклил;
альтернативно, R54 и R55 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
W представляет собой SO2, C=O, CHR20 или ковалентную связь; или W и R1, взятые вместе с 6-членным кольцом, к которому оба из них присоединены, образуют одну из двух следующих формул:

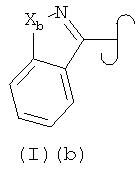
где Ха представляет собой О, S или N; и Хb представляет собой О, S или SO2;
R20 представляет собой водород, С1-5 алкил, фенил, бензил, нафтил или С1-5 гетероциклил;
R42 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R45OC=O, R46R47NC=O, R45SO, R45SO2 или R46R47NSO2;
R43 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R42 и R43 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
R44 представляет собой С1-5 алкил, С2-5 алкенил, фенил, нафтил или С1-5 гетероциклил;
R48 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R50OC=O, R51R52NC=O, R50SO, R50SO2 или R51R52NSO2;
R49 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R48 и R49 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим; и
где каждая из вышеуказанных углеводородных или гетероуглеродных групп, если не указано иначе, и, в дополнение к любым определенным заместителям, необязательно и независимо замещена 1-3 заместителями, выбранными из метила, галогенметила, гидроксиметила, галогена, гидрокси, амино, нитро, циано, С1-5 алкила, С1-5 алкокси, -СООН, С2-6 ацила, [ди(С1-4 алкил)амино]С2-5алкилена, [ди(С1-4 алкил)амино]С2-5алкил-NH-CO- и С1-5 галогеналкокси;
или его фармацевтически приемлемой соли, амида или сложного эфира, включая их стереоизомерную форму.
Описанные соединения представляют собой ингибиторы протеолитической активности катепсина S человека с высоким сродством связывания. Для применения в медицине может оказаться желательным получение фармацевтически приемлемых солей соединений формулы (I).
Некоторые соединения настоящего изобретения могут иметь один стереогенный атом и могут существовать в виде двух энантиомеров. Некоторые соединения настоящего изобретения могут иметь два или несколько стереогенных атомов и, дополнительно, могут существовать в виде диастереомеров. Специалистам в данной области следует понимать, что все такие стереоизомеры и их смеси в любом соотношении включены в объем настоящего изобретения.
Другой аспект настоящего изобретения относится к фармацевтическим противоаллергическим композициям, включающим соединение формулы (I) и фармацевтически приемлемый носитель. Дополнительный вариант осуществления изобретения представляет собой способ получения противоаллергической фармацевтической композиции, включающий смешивание указанного соединения, описанного выше, с подходящим фармацевтически приемлемым носителем.
В изобретении также рассматриваются фармацевтические композиции, включающие более одного соединения формулы (I) и композиции, включающие соединение формулы (I) и другой фармацевтически активный агент.
Еще одним объектом изобретения является способ лечения аллергического заболевания или болезненного состояния, опосредованного ферментом катепсином S, у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества любого из соединений или фармацевтических композиций, описанных выше. При введении более одного активного агента терапевтически эффективное количество может представлять собой совместное эффективное количество. Описанные здесь соединения ингибируют протеазную активность катепсина S человека, фермента, вовлеченного в иммунную ответную реакцию. В предпочтительных вариантах осуществления ингибирование катепсина S является селективным. Как таковые описанные соединения и композиции могут использоваться для профилактики, ингибирования или лечения аллергических заболеваний, в частности атопических аллергических заболеваний.
Дополнительные отличительные признаки и преимущества изобретения будут очевидны из приведенных ниже подробного описания и примеров и прилагаемой формулы изобретения.
Краткое описание чертежей
На фиг.1 показано ингибирование пролиферативных ответных реакций Т-клеток человека на два вида пылевых клещей, Der p и Der f. Верхняя диаграмма, фиг.1А: Кривая разведения для очищенного РВМС от аллергического донора при культивировании с титрованными дозами аллергенных экстрактов, приготовленных из Der p и Der f, в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования. Нижняя диаграмма, фиг.1В: Действие титрованных доз LHVS на пролиферативные ответные реакции Т-клеток на экстракты пылевых клещей.
На фиг.2 показано ингибирование пролиферативных ответных реакций Т-клеток человека на амброзию, но не ConA, с использованием LHVS. Верхняя диаграмма, фиг.2А: Кривая разведения для очищенного РВМС от аллергического донора при культивировании с титрованными дозами аллергенных экстрактов, приготовленных из Амброзии короткой и Амброзии гигантской в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования. Нижняя диаграмма, фиг.2В: Действие титрованных доз LHVS на пролиферативные ответные реакции Т-клеток на экстракты амброзии.
На фиг.3 показано ингибирование пролиферативных ответных реакций Т-клеток человека на Der f, но не Con A, двумя ингибиторами катепсина S, соединениями примера 11 (фиг.3А) и примера 36 (фиг.3В). Очищенный РВМС от аллергического донора культивировали с экстрактами аллергенов, приготовленных из Der f в присутствии титрованных доз указанных соединений в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования.
Подробное описание изобретения
Цель настоящего изобретения заключалась в определении, воздействует ли ингибирование катепсина S на присутствие определенных антигенов в системе человека. Согласно изобретению, в настоящее время установлено, что ингибиторы катепсина S блокируют присутствие нескольких неочищенных аллергеновых экстрактов у человека в анализе ex vivo, подтверждая, таким образом, полезность ингибиторов катепсина S для лечения таких аллергических заболеваний.
Блокирование Ii разложения должно снизить присутствие антигена в CD4 Т клетках и прервать нормальный иммунный ответ. Ингибитор катепсина S должен специфически воздействовать на активацию CD4 T клеток, таким образом, ограничивая степень сопутствующего иммуноподавления, нежелательного побочного действия при кортикостероидной терапии.
При использовании ингибиторов катепсина S в соответствии со способами настоящего изобретения иммунологический компонент аллергической реакции может быть блокирован в различной степени, обладая преимуществом по сравнению с современной терапией, заключающимся в большей селективности, наличии незначительных или сниженных побочных действий или тем и другим. Настоящее изобретение частично основано на обнаружении того факта, что ингибиторы катепсина S могут блокировать присутствие неочищенных аллергеновых экстрактов у человека в анализе ex vivo. Такая ex vivo система близко имитирует процесс, который происходит во всем теле, когда антигены входят в систему кровообращения и представлены с помощью антиген-представляющих клеток, которые, в свою очередь, активируют CD4 T клетки. В случае лечения субъекта ингибитор или его метаболит также будут присутствовать в крови, как и в анализе ex vivo.
Объектом изобретения является лечение аллергического заболевания с использованием соединений пиразола формулы (I).
А. Термины
Следующие термины, используемые в описании, определены ниже.
«Алкил» включает необязательно замещенные линейные или разветвленные углеводороды, имеющие по крайней мере один удаленный водород с образованием радикальной группы. Алкильные группы включают метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, 1-метилпропил, пентил, изопентил, втор-пентил, гексил, гептил, октил и подобные. Алкил включает циклоалкил, такой как циклопропил, циклобутил, циклопентил и циклогексил.
«Алкенил» включает необязательно замещенные линейные и разветвленные углеводородные радикалы, как указано выше, имеющие, по крайней мере, одну углерод-углеродную двойную связь (sp2). Алкенилы включают этенил (или винил), проп-1-енил, проп-2-енил (или аллил), изопропенил (или 1-метилвинил), бут-1-енил, бут-2-енил, бутадиенилы, пентенилы, гекса-2,4-диенил и подобные. Углеводородные радикалы, имеющие сочетание двойных связей и тройных связей, такие как 2-пентен-4-инил, включены в данном описании в определения алкинилов. Алкенил включает циклоалкенил. Цис- и транс- или (Е)- и (Z)-формы включены в данное изобретение.
«Алкинил» включает необязательно замещенные линейные и разветвленные углеводородные радикалы, как указано выше, имеющие, по крайней мере, одну углерод-углеродную тройную связь (sp). Алкинилы включают этинил, пропинилы, бутинилы и пентинилы. Углеводородные радикалы, имеющие сочетание двойных связей и тройных связей, такие как 2-пентен-4-инил, включены в данном описании в определения алкинилов. Алкинил не включает циклоалкинил.
«Алкокси» включает необязательно замещенную линейную или разветвленную алкильную группу с концевым кислородом, связывающим алкильную группу с остатком молекулы. Алкокси включает метокси, этокси, пропокси, изопропокси, бутокси, трет-бутокси, пентокси и подобные. «Аминоалкил», «тиоалкил» и сульфонилалкил» аналогичны алкоксильной группе, при этом концевой атом кислорода в алкокси заменен соответственно на NH (или NR), S и SO2. Гетероалкил включает алкокси, аминоалкил, тиоалкил и подобные.
«Арил» включает фенил, нафтил, бифенилил, тетрагидронафтил и подобные, каждый из которых необязательно может быть замещенным. Арил также включает арилалкильные группы, такие как бензил, фенэтил и фенилпропил. Арил включает кольцевую систему, содержащую необязательно замещенное 6-членное карбоциклическое ароматическое кольцо, указанная система может быть бициклической, мостиковой и/или конденсированной. Система может включать кольца, которые являются ароматическими или частично или полностью насыщенными. Примеры кольцевых систем включают инденил, пенталенил, 1,4-дигидронафтил, инданил, бензимидазолил, бензотиофенил, индолил, бензофуранил, изохинолинил и подобные.
«Гетероциклил» включает необязательно замещенные ароматические и неароматические кольца, имеющие атомы углерода и, по крайней мере, один гетероатом (О, S, N) или гетероатомный фрагмент (SO2, CO, CONH, COO) в кольце. Если не указано иначе, гетероциклический радикал может иметь валентность, связывающую его с остатком молекулы через атом углерода, например, 3-фурил или 2-имидазолил, или через гетероатом, например, N-пиперидил или 1-пиразолил. Предпочтительно моноциклический гетероциклил содержит от 4 до 7 кольцевых атомов или от 5 до 6 кольцевых атомов; в кольце может быть от 1 до 5 гетероатомов или гетероатомных фрагментов и предпочтительно от 1 до 3. Гетероциклил может быть насыщенным, ненасыщенным, ароматическим (например, гетероарил), неароматическим или конденсированным.
Гетероциклил также включает конденсированные, например бициклические, кольца, такие как необязательно конденсированные с необязательно замещенным карбоциклическим или гетероциклическим пяти- или шестичленным ароматическим кольцом. Например, «гетероарил» включает необязательно замещенное шестичленное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота, конденсированное с необязательно замещенным пяти- или шестичленным карбоциклическим или гетероциклическим ароматическим кольцом. Указанное гетероциклическое пяти- или шестичленное ароматическое кольцо, конденсированное с указанным пяти- или шестичленным ароматическим кольцом, может содержать 1, 2 или 3 атома азота, когда это шестичленное кольцо, или 1, 2 или 3 гетероатома, выбранных из кислорода, азота и серы, когда это пятичленное кольцо.
Примеры гетероциклилов включают тиазолил, фурил, пиранил, изобензофуранил, пирролил, имидазолил, пиразолил, изотиазолил, изоксазолил, пиридил, пиразинил, пиримидинил, пиридазинил, индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолил, фуразанил, пирролидинил, пирролинил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперидил, пиперазинил, индолинил и морфолинил. Например, предпочтительные гетероциклилы или гетероциклические радикалы включают морфолинил, пиперазинил, пирролидинил, пиридил, циклогексилимино, циклогептилимино и, более предпочтительно, пиперидил.
Примерами, иллюстрирующими гетероарил, являются тиенил, фуранил, пирролил, имидазолил, оксазолил, тиазолил, бензотиенил, бензофуранил, бензимидазолил, бензоксазолил, бензотиазолил.
«Ацил» относится к карбонильной части, связанной или с атомом водорода (то есть формильная группа) или с необязательно замещенной алкильной или алкенильной цепью, или гетероциклилом.
«Гало» или «галоген» включает фтор, хлор, бром и иод, и предпочтительны в качестве заместителя хлор или бром.
«Алкандиил» или «алкилен» представляет собой линейный или разветвленный необязательно замещенный двухвалентный алкановый радикал такой как, например, метилен, этилен, пропилен, бутилен, пентилен или гексилен.
«Алкендиил» представляет собой, аналогично описанному выше, линейный или разветвленный необязательно замещенный двухвалентный алкеновый радикал, такой как, например, пропенилен, бутенилен, пентенилен или гексенилен. В таких радикалах атом углерода, связывающий азот, предпочтительно не должен быть ненасыщенным.
«Ароил» относится к карбонильной группе, связанной с необязательно замещенной арильной или гетероарильной группой, где арил или гетероарил имеют представленные выше значения. В частности, бензоил представляет собой фенилкарбонил.
Как определено в данном описании, два радикала вместе с атомом(ами), к которому они присоединены, могут образовывать необязательно замещенное 4-7-, 5-7- или 5-6-членное карбоциклическое или гетероциклическое кольцо, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим. Указанные кольца могут быть такими, как определено выше в разделе «Краткое изложение сущности изобретения». Конкретные примеры таких колец такие, как указано в следующем разделе.
«Фармацевтически приемлемые соли, сложные эфиры и амиды» включают карбоксилатные соли (например, С1-8 алкил, циклоалкил, арил, гетероарил или неароматические гетероциклические), аминокислотно-аддитивные соли, сложные эфиры и амиды, которые обладают подходящим соотношением польза/риск, являются фармакологически эффективными и подходящими для контакта с тканями пациентов без чрезмерной токсичности, раздражения или ответной аллергической реакции. Примеры солей включают гидробромид, гидрохлорид, сульфат, бисульфат, нитрат, ацетат, оксалат, валерат, олеат, пальмитат, стеарат, лаурат, борат, бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептонат, лактиобионат и лаурилсульфонат. Они могут включать катионы щелочного металла и щелочноземельного металла, такие как натрий, калий, кальций и магний, а также нетоксичные катионы аммония, четвертичного аммония и амина, такие как тетраметиламмоний, метиламин, триметиламин и этиламин. Смотри, например, публикацию S.M.Berge et al., "Pharmaceutical Salts (Фармацевтические соли)", J.Pharm.Sci., 1977, 66:1-19, включенную в данное описание в качестве ссылки. Примеры фармацевтически приемлемых амидов по изобретению включают амиды, которые получены из аммиака, первичных С1-6 алкиламинов и вторичных ди(С1-6 алкил)аминов. Вторичные амины включают 5- или 6-членные гетероциклические или гетероароматические кольцевые группы, содержащие по крайней мере один атом азота и необязательно от 1 до 2 дополнительных гетероатомов. Предпочтительные амиды получают из аммиака, С1-3 алкил первичных аминов или ди(С1-2 алкил)аминов. Примеры фармацевтически приемлемых сложных эфиров по изобретению включают С1-7 алкиловые, С5-7 циклоалкиловые, фениловые и фенил(С1-6)алкиловые сложные эфиры. Предпочтительные сложные эфиры включают метиловые эфиры.
«Пациент» или «субъект» включает млекопитающих, таких как люди и животные (собаки, кошки, лошади, крысы, кролики, мыши, приматы, не являющиеся людьми), нуждающихся в наблюдении, эксперименте, лечении или профилактике в связи с подходящим заболеванием или болезненным состоянием. Предпочтительно, пациент или субъект является человеком.
«Композиция» включает продукт, содержащий определенные ингредиенты в определенных количествах, а также любой продукт, который получен непосредственно или косвенно при комбинации определенных ингредиентов в определенных количествах.
«Терапевтически эффективное количество» или «эффективное количество» означает такое количество активного соединения или фармацевтического агента, которое вызывает биологическую или медицинскую ответную реакцию в системе тканей, у животного или человека, требуемую для исследователя, ветеринара, лечащего врача или другого клинициста, которая включает облегчение симптомов заболевания или нарушения, подвергаемого лечению.
Касаясь различных радикалов в данном описании и формуле изобретения, следует сделать три общих замечания. Первое замечание касается валентности. Для всех углеводородных радикалов, являются ли они насыщенными, ненасыщенными или ароматическими, и являются они или не являются циклическими, линейными или разветвленными, а также аналогично в отношении всех гетероциклических радикалов, каждый радикал включает замещенные радикалы такого типа и одновалентные, двухвалентные и поливалентные радикалы, как указано в формуле изобретения. Контекст будет указывать, что заместитель является алкиленом или углеводородным радикалом, у которого удалены, по крайней мере, два атома водорода (двухвалентный) или удалено большее число атомов водорода (поливалентный). Примером двухвалентного радикала, связывающего две части молекулы, является G в формуле (I), которое связывает два кольца.
Во-вторых, следует понимать, что радикалы или структурные фрагменты, как определено в данном описании, включают замещенные радикалы или структурные фрагменты. Углеводороды включают одновалентные радикалы, содержащие углерод и водород, такие как алкил, алкенил, алкинил, циклоалкил и циклоалкенил (либо ароматический, либо ненасыщенный), а также соответствующие двухвалентные радикалы, такие как алкилен, алкенилен, фенилен и подобные. Гетероуглероды включают одновалентные и двухвалентные радикалы, содержащие углерод, водород и, по крайней мере, один гетероатом. Примеры одновалентных гетероуглеродов включают ацил, ацилокси, алкоксиацил, гетероциклил, гетероарил, ароил, бензоил, диалкиламино, гидроксиалкил и подобные. Используя «алкил» в качестве примера, следует понимать, что «алкил» включает замещенный алкил, имеющий один или несколько заместителей, как, например, от 1 до 5, от 1 до 3, от 2 до 4 заместителей. Заместители могут быть одинаковыми (дигидрокси, диметил), подобными (хлорфтор) или различными (хлорбензил- или аминометилзамещенный). Примеры замещенного алкила включают галогеналкил (такой как фторметил, хлорметил, дифторметил, перхлорметил, 2-бромэтил, перфторметил и 3-иодциклопентил), гидроксиалкил (такой как гидроксиметил, гидроксиэтил, 2-гидроксипропил), аминоалкил (такой как аминометил, 2-аминоэтил, 3-аминопропил и 2-аминопропил), нитроалкил, алкилалкил и подобные. Ди(С1-6 алкил)амино группа включает независимо выбранные алкильные группы с образованием, например, метилпропиламино и изопропилметиламино, в дополнение к диалкиламино группам, имеющим две одинаковые алкильные группы, таким как диметиламино или диэтиламино.
Третье, подразумеваются только стабильные соединения. Например, когда имеется NR'R" группа, и R может представлять собой алкенильную группу, двойная связь удалена, по крайней мере, на один углерод от атома азота, чтобы исключить образование енамина. Аналогично, когда пунктирная линия представляет собой необязательную sp2 связь, если она отсутствует, то включен(ы) соответствующий атом(ы) водорода.
Предпочтительные заместители для Ar включают метил, метокси, фторметил, дифторметил, перфторметил (трифторметил), 1-фторэтил, 2-фторэтил, этокси, фтор, хлор и бром и особенно метил, бром, хлор, перфторметил, перфторметокси, метокси и фтор. Предпочтительными примерами замещенного Ar или Ar1 являются 4-замещенный и 3,4-дизамещенный фенил. Соединения по изобретению дополнительно описаны в следующем разделе.
В. Соединения
Объектом изобретения является применение соединений формулы (I), как описано выше в разделе «Краткое изложение сущности изобретения» для лечения аллергического заболевания.
Предпочтительные соединения включают те, в которых:
(а) R1 представляет собой водород, галоген, С1-5 алкокси, гидрокси, С1-5 алкил, циано, нитро, R7R8N, С2-8 ацил или R10R11NSO2;
(b) R1 представляет собой галоген, циано, нитро, R7R8N или R10R11NSO2;
(c) R2 представляет собой водород;
(d) каждый R3 и R4 независимо представляет собой водород или С1-3 алкил;
(е) один R3 и R4 представляет собой водород;
(f) каждый R3 и R4 представляет собой водород;
(g) один из R5 и R6 представляет собой водород, а другой представляет собой 5-7-членный карбоциклил или гетероциклил, необязательно замещенный;
(h) R5 и R6, взятые вместе, образуют шестичленный гетероциклил;
(i) R5 и R6, взятые вместе, образуют пиридинил, пиримидинил или пиперазинил, необязательно N-замещенный группой R40O(C=O)(C=O)-, R40SO2, R40NHCO2, R40(C=O)- или R40N(C=O)-;
(j) каждый R7, R8, R21, R22, R24, R25 независимо представляет собой водород или С1-5 алкил; или, независимо, каждый из R7 и R8, R21 и R22 иR24 и R25 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
(k) по крайней мере, один из R7 и R8, R21 и R22 иR24 и R25, взятые вместе, представляет морфолинил, пиперидинил или пирролидинил;
(l) каждый R9, R23, R26 и R27 независимо представляет собой водород или С1-5 алкил;
(m) G представляет собой С3-4 алкандиил, необязательно замещенный гидрокси, (L)-C1-5 алкилокси- или [(L)-C1-5 алкилен]амино-;
(n) G представляет собой С3 алкандиил, необязательно замещенный гидрокси, (L)-C1-5 алкилокси- или [(L)-C1-5 алкилен]амино-;
(о) Х представляет собой азот;
(р) Y представляет собой CR13;
(q) Z представляет собой CR14;
(r) X представляет собой СН;
(s) R12 представляет собой водород, R22O(C=O)NH-, R22NH(C=O)NH-, R22SO2NH-; R23SO или R23SO2, и R13 представляет собой водород, R43O(C=O)NH-, R43NH(C=O)NH-, R43SO2NH-, R44SO или R44SO2;
(t) R14 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, циано, нитро, R25O(C=O)NH-, R25NH(C=O)NH-, R25SO2NH- или R24R25N;
(u) R14 представляет собой галоген, R25O(C=O)NH-, R25NH(C=O)NH-, R25SO2NH- или R24R25N; Ar представляет собой моноциклическое кольцо, необязательно замещенное 1-2 заместителями, выбранными независимо из галогена, С1-5 алкила, циано, нитро R15R16N, CF3 и OCF3;
(v) Ar представляет собой шестичленное кольцо, замещенное 1-2 заместителями, выбранными независимо из галогена, CF3 и OCF3, указанный заместитель или заместители находятся в 4-положении или в 3- и 4-положениях соответственно;
(w) W представляет собой SO2, C=O или CHR20;
(x) W представляет собой ковалентную связь;
(y) W и R1, взятые вместе, имеют формулу (I)(a);
(z) W и R1, взятые вместе, имеют формулу (I)(b);
(aa) один из R3 и R4 представляет собой водород; Ar представляет собой моноциклическое кольцо, необязательно замещенное 1-2 заместителями, выбранными независимо из галогена, С1-5 алкила, циано, нитро R15R16N, CF3 и OCF3; R12 представляет собой водород, R23SO или R23SO2; R13 представляет собой водород, R44SO или R44SO2; R14 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, циано, нитро или R24R25N; и G представляет собой С3-4 алкандиил, необязательно замещенный гидрокси, С1-3 алкил, (L)-C1-5 алкилокси или [(L)-C1-5 алкилен]амино-;
(bb) каждый R3 и R4 представляет собой водород; Ar представляет собой шестичленное кольцо, необязательно замещенное 1-2 заместителями, выбранными независимо из галогена, С1-5 алкила, циано, нитро, R15R16N, CF3 и OCF3; R12 представляет собой водород, R23SO или R23SO2; R13 представляет собой водород, R44SO или R44SO2; R14 представляет собой водород, галоген, С1-5алкокси, С1-5 алкил, циано, нитро или R24R25N; и G представляет собой С3 алкандиил, необязательно замещенный гидрокси, (L)-C1-5 алкилокси- или [(L)-C1-5 алкиламино-;
(сс) Ar представляет собой фенил;
(dd) комбинации вышеуказанных значений.
Особенно предпочтительные соединения включают приведенные в данном описании в примерах, такие как
1-[4-(2-амино-6-хлорфенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол; 1-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]-3-метилмочевина; 1-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]-3-метилмочевина; метиловый эфир 3-амино-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензойной кислоты; 3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фениламин; 1-[2-(4-{3-[3-(4-бромфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)-3-хлорфенил]-3-метилмочевина; амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты; метиловый эфир [3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]карбаминовой кислоты; амид 1-[3-(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)пропил]-3-(4-бромфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты; метиловый эфир 2-(4-{3-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил]пиперазин-1-ил)-3-нитробензойной кислоты; 1-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол; 2-(4-{2-гидрокси-3-[3-(4-иодфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрил; амид 3-(4-бромфенил)-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты; 2-(4-{3-[5-ацетил-3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил; 2-(4-{3-[3-(4-хлор-3-метилфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил; 1-(3-(4-хлор-3-метилфенил)-1-{3-[4-(2,4-диметилфенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон; 1-{3-[4-(3,5-дихлорпиридин-4-ил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1Н-пиразоло[4,3-c]пиридин; 2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло-[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрил; N-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]метансульфонамид; амид 3-(3,4-дихлорфенил)-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты; и амид 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты.
Кроме того, предпочтительные соединения включают те, в которых Ar выбирают из 4-трифторметилфенила, 4-бромфенила, 4-хлорфенила, 4-хлор-3-метилфенила и 3,4-дихлорфенила.
Более предпочтительные соединения включают соединения, описанные в примерах 19, 27 и 33.
Родственные соединения
Изобретение относится к описанным соединениям и близко родственным фармацевтически приемлемым формам описанных соединений, таким как их соли, сложные эфиры, амиды, кислоты, гидратные или сольватные формы; скрытые или защищенные формы и рацемические смеси или энантиомерно или оптически чистые формы. Родственные соединения также включают соединения по изобретению, которые были модифицированы для обнаружения, например, помечены изотопом 18F для использования в качестве зонда в позитронной эмиссионной томографии (РЕТ) или однофотонной эмиссионной компьютерной томографии (SPECT).
Изобретение также включает описанные соединения, имеющие одну или несколько функциональных групп (например, гидроксил, амино или карбоксил), скрытых защитными группами. Смотри, например, Greene and Wuts, Protective Groups in Organic Synthesis, 3rd ed., (1999), John Wiley & Sons, NY. Некоторые из таких скрытых или защищенных соединений являются фармацевтически приемлемыми; другие полезны в качестве промежуточных соединений. Раскрытые в описании синтетические промежуточные продукты и способы и их незначительные модификации также входят в объем изобретения.
Защитные группы для гидрокси
Защита гидроксильной группы включает метиловые простые эфиры, замещенные метиловые простые эфиры, замещенные этиловые простые эфиры, замещенные бензиловые простые эфиры и силиловые простые эфиры.
Замещенные простые метиловые эфиры
Примеры замещенных простых метиловых эфиров включают метилоксиметиловый, метилтиометиловый, трет-бутилтиометиловый, (фенилдиметилсилил)метоксиметиловый, бензилоксиметиловый, п-метоксибензилоксиметиловый, (4-метоксифенокси)метиловый, гвиаколметиловый, трет-бутоксиметиловый, 4-пентенилоксиметиловый, силоксиметиловый, 2-метоксиэтоксиметиловый, 2,2,2-трихлорэтоксиметиловый, бис(2-хлорэтокси)метиловый, 2-(триметилсилил)этоксиметиловый, тетрагидропираниловый, 3-бромтетрагидропираниловый, тетрагидротиопираниловый, 1-метоксициклогексиловый, 4-метокситетрагидропираниловый, 4-метокситетрагидротиопираниловый, S,S-диоксидо 4-метокситетрагидротиопираниловый, 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-иловый, 1,4-диоксан-2-иловый, тетрагидрофураниловый, тетрагидротиофураниловый и 2,3,3а,4,5,6,7,7а-октагидро-7,8,8-триметил-4,7-метанобензофуран-2-иловый.
Замещенные простые этиловые эфиры
Примеры замещенных простых этиловых эфиров включают 1-этоксиэтиловый, 1-(2-хлорэтокси)этиловый, 1-метил-1-метоксиэтиловый, 1-метил-1-бензилоксиэтиловый, 1-метил-1-бензилокси-2-фторэтиловый, 2,2,2-трихлорэтиловый, 2-триметилсилилэтиловый, 2-(фенилселенил)этиловый, трет-бутиловый, аллиловый, п-хлорфениловый, п-метоксифениловый, 2,4-динитрофениловый и бензиловый.
Замещенные простые бензиловые эфиры
Примеры замещенных простых бензиловых эфиров включают п-метоксибензиловый, 3,4-диметоксибензиловый, о-нитробензиловый, п-нитробензиловый, п-галогенбензиловый, 2,6-дихлорбензиловый, п-цианобензиловый, п-фенилбензиловый, 2- и 4-пиколиловые, N-оксид 3-метил-2-пиколиловый, дифенилметиловый, п,п'-динитробензгидриловый, 5-дибензосубериловый, трифенилметиловый, α-нафтилдифенилметиловый, п-метоксифенилдифенилметиловый, ди(п-метоксифенил)фенилметиловый, три(п-метоксифенил)метиловый, 4-(4'-бромфенацилокси)фенилдифенилметиловый, 4,4'4''-трис(4,5-дихлорфталимидофенил)метиловый, 4,4',4''-трис(левулиноилоксифенил)метиловый, 4,4'4''-трис(бензоилоксифенил)метиловый, 3-(имидазол-1-илметил)бис(4,4''-диметоксифенил)метиловый, 1,1-бис(4-метоксифенил)-1'-пиренилметиловый, 9-антриловый, 9-(9-фенил)ксантениловый, 9-(9-фенил-10-оксо)антриловый, 1,3-бензодитиолан-2-иловый и S,S-диоксидо бензизотиазолиловый.
Силиловые простые эфиры
Примеры силиловых простых эфиров включают триметилсилиловый, триэтилсилиловый, триизопропилсилиловый, диметилизопропилсилиловый, диэтилизопропилсилиловый, диметилгексилсилиловый, трет-бутилдиметилсилиловый, трет-бутилдифенилсилиловый, трибензилсилиловый, три-п-ксилилсилиловый, трифенилсилиловый, дифенилметилсилиловый и трет-бутилметоксифенилсилиловый.
Сложные эфиры
В дополнение к простым эфирам гидроксильная группа может быть защищена в виде сложного эфира. Примеры сложных эфиров включают формиат, бензоилформиат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, п-хлорфеноксиацетат, п-Р-фенилацетат, 3-фенилпропионат, 4-оксопентаноат (левулинат), 4,4-(этилендитио)пентаноат, пивалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, п-фенилбензоат, 2,4,6-триметилбензоат (мезитоат).
Карбонаты
Примеры карбонатных защитных групп включают метил, 9-флуоренилметил, этил, 2,2,2-трихлорэтил, 2-(триметилсилил)-этил, 2-(фенилсульфонил)этил, 2-(трифенилфосфонио)этил, изобутил, винил, аллил, п-нитрофенил, бензил, п-метоксибензил, 3,4-диметоксибензил, о-нитробензил, п-нитробензил, S-бензилтиокарбонат, 4-этокси-1-нафтил и метилдитиокарбонат.
Группы вспомогательного отщепления
Примеры групп вспомогательного отщепления включают 2-иодбензоат, 4-азидобутират, 4-нитро-4-метилпентаноат, о-(дибромметил)бензоат, 2-формилбензолсульфонат, 2-(метилтиометокси)этилкарбонат, 4-(метилтиометокси)бутират и 2-(метилтиометоксиметил)бензоат.
Смешанные сложные эфиры
Примеры смешанных сложных эфиров включают 2,6-дихлор-4-метилфеноксиацетат, 2,6-дихлор-4-(1,1,3,3-тетраметилбутил)феноксиацетат, 2,4-бис(1,1-диметилпропил)феноксиацетат, хлордифенилацетат, изобутират, моносукциноат, (Е)-2-метил-2-бутеноат (тиглоат), о-(метоксикарбонил)бензоат, п-Р-бензоат, α-нафтоат, нитрат, алкил N,N,N',N'-тетраметилфосфордиамидат, N-фенилкарбамат, борат, диметилфосфинотиоил и 2,4-динитрофенилсульфенат.
Сульфонаты
Примеры сульфонатов включают сульфат, метансульфонат (мезилат), бензилсульфонат и тозилат.
Защитные группы для амино
Защитные группы для аминогруппы включают карбаматы, амиды и специальные -NH защитные группы.
Примеры карбаматов включают метил- и этилкарбаматы, замещенные этилкарбаматы, карбаматы вспомогательного расщепления, карбаматы протолитического расщепления, производные типа мочевины и смешанные карбаматы.
Карбаматы
Примеры метил- и этилкарбаматов включают метил и этил, 9-флуоренилметил, 9-(2-сульфо)флуоренилметил, 9-(2,7-дибром)флуоренилметил,2,7-ди-трет-бутил-[9-(10,10-диоксо-10,10,10,10-тетрагидротиоксантил)]метил и 4-метоксифенацил.
Замещенный этил
Примеры замещенных этилкарбаматов включают 2,2,2-трихлорэтил, 2-триметилсилилэтил, 2-фенилэтил, 1-(1-адамантил)-1-метилэтил, 1,1-диметил-2-галогенэтил, 1,1-диметил-2,2-дибромэтил, 1,1-диметил-2,2,2-трихлорэтил, 1-метил-1-(4-бифенилил)этил, 1-(3,5-ди-трет-бутилфенил)-1-метилэтил, 2-(2'- и 4'-пиридил)этил, 2-(N,N-дициклогексилкарбоксамидо)этил, трет-бутил, 1-адамантил, винил, аллил, 1-изопропилаллил, циннамил, 4-нитроциннамил, 8-хинолил, N-гидроксипиперидинил, алкилдитио, бензил, п-метоксибензил, п-нитробензил, п-бромбензил, п-хлорбензил, 2,4-дихлорбензил, 4-метилсульфинилбензил, 9-антрилметил и дифенилметил.
Группы вспомогательного отщепления
Примеры групп вспомогательного отщепления включают 2-метилтиоэтил, 2-метилсульфонилэтил, 2-(п-толуолсульфонил)этил, [2-(1,3-дитианил)]метил, 4-метилтиофенил, 2,4-диметилтиофенил, 2-фосфониоэтил, 2-трифенилфосфониоизопропил, 1,1-диметил-2-цианоэтил, м-хлор-п-ацилоксибензил, п-(дигидроксиборил)бензил, 5-бензизоксазолилметил и 2-(трифторметил)-6-хромонилметил.
Группы протолитического отщепления
Примеры групп протолитического отщепления включают м-нитрофенил, 3,5-диметоксибензил, о-нитробензил, 3,4-диметокси-6-нитробензил и фенил(о-нитрофенил)метил.
Производные типа мочевины
Примеры производных типа мочевины включают фенотиазинил-(10)-карбонил производное, N'-п-толуолсульфониламинокарбонил и N'-фениламинотиокарбонил.
Смешанные карбаматы
Примеры смешанных карбаматов включают трет-амил, S-бензилтиокарбамат, п-цианобензил, циклобутил, циклогексил, циклопентил, циклопропилметил, п-децилоксибензил, диизопропилметил, 2,2-диметоксикарбонилвинил, о-(N,N-диметилкарбоксамидо)бензил, 1,1-диметил-3-(N,N-диметилкарбоксамидо)пропил, 1,1-диметилпропинил, ди(2-пиридил)метил, 2-фуранилметил, 2-иодэтил, изоборнил, изобутил, изоникотинил, п-(п'-метоксифенилазо)бензил, 1-метилциклобутил, 1-метилциклогексил, 1-метил-1-циклопропилметил, 1-метил-1-(3,5-диметоксифенил)этил, 1-метил-1-(п-фенилазофенил)этил, 1-метил-1-фенилэтил, 1-метил-1-(4-пиридил)этил, фенил, п-(фенилазо)бензил, 2,4,6-три-трет-бутилфенил, 4-(триметиламмоний)бензил и 2,4,6-триметилбензил.
Примеры амидов включают:
Амиды
N-формил, N-ацетил, N-хлорацетил, N-трихлорацетил, N-трифторацетил, N-фенилацетил, N-3-фенилпропионил, N-пиколиноил, N-3-пиридилкарбоксамид, N-бензоилфенилаланиновое производное, N-бензоил, N-п-фенилбензоил.
Группы вспомогательного отщепления
N-о-нитрофенилацетил, N-о-нитрофеноксиацетил, N-ацетоацетил, (N'-дитиобензилоксикарбониламино)ацетил, N-3-(п-гидроксифенил)пропионил, N-3-(о-нитрофенил)пропионил, N-2-метил-2-(о-нитрофенокси)пропионил, N-2-метил-2-(о-фенилазофенокси)пропионил, N-4-хлорбутирил, N-3-метил-3-нитробутирил, N-о-нитроциннамоил, N-ацетилметиониновое производное, N-о-нитробензоил, N-о-(бензоилоксиметил)бензоил и 4,5-дифенил-3-оксазолин-2-он.
Циклические имидные производные
N-фталимид, N-дитиасукциноил, N-2,3-дифенилмалеоил, N-2,5-диметилпирролил, N-1,1,4,4-тетраметилдисилилазациклопентановый аддукт, 5-замещенный 1,3-диметил-1,3,5-триазациклогексан-2-он, 5-замещенный 1,3-дибензил-1,3,5-триазациклогексан-2-он и 1-замещенный 3,5-динитро-4-пиридонил.
Специальные NH-защитные группы
Примеры специальных NH-защитных групп включают
N-алкил и N-арил амины,
N-метил, N-аллил, N-[2-(триметилсилил)этокси]метил, N-3-ацетоксипропил, N-(1-изопропил-4-нитро-2-оксо-3-пирролин-3-ил), четвертичные соли аммония, N-бензил, N-ди(4-метоксифенил)метил, N-5-дибензосуберил, N-трифенилметил, N-(4-метоксифенил)дифенилметил, N-9-фенилфлуоренил, N-2,7-дихлор-9-флуоренилметилен, N-ферроценилметил и N-2-пиколиламин N'-оксид.
Иминопроизводные
N-1,1-диметилтиометилен, N-бензилиден, N-п-метоксибензилиден, N-дифенилметилен, N-[(2-пиридил)мезитил]метилен и N-(N',N'-диметиламинометилен).
Защита для карбонильной группы
Ациклические ацетали и кетали
Примеры ациклических ацеталей и кеталей включают диметил, бис(2,2,2-трихлорэтил), дибензил, бис(2-нитробензил) и диацетил.
Циклические ацетали и кетали
Примеры циклических ацеталей и кеталей включают 1,3-диоксаны, 5-метилен-1,3-диоксан, 5,5-дибром-1,3-диоксан, 5-(2-пиридил)-1,3-диоксан, 1,3-диоксоланы, 4-бромметил-1,3-диоксолан, 4-(3-бутенил)-1,3-диоксолан, 4-фенил-1,3-диоксолан, 4-(2-нитрофенил)-1,3-диоксолан, 4,5-диметоксиметил-1,3-диоксолан, О,О'-фенилендиокси и 1,5-дигидро-3Н-2,4-бензо-диоксепин.
Ациклические дитиоацетали и кетали
Примеры ациклических дитиоацеталей и кеталей включают S,S'-диметил, S,S'-диэтил, S,S'-дипропил, S,S'-дибутил, S,S'-дипентил, S,S'-дифенил, S,S'-дибензил и S,S'-диацетил.
Циклические дитиоацетали и кетали
Примеры циклических дитиоацеталей и кеталей включают 1,3-дитиан, 1,3-дитиолан и 1,5-дигидро-3Н-2,4-бензодитиепин
Ациклические монотиоацетали и кетали
Примеры ациклических монотиоацеталей и кеталей включают О-триметилсилил-S-алкил, О-метил-S-алкил или -S-фенил и О-метил-S-2-(метилтио)этил.
Циклические монотиоацетали и кетали
Примеры циклических монотиоацеталей и кеталей включают 1,3-оксатиоланы.
Смешанные производные
О-замещенные циангидрины
Примеры О-замещенных циангидринов включают О-ацетил, О-триметилсилил, О-1-этоксиэтил и О-тетрагидропиранил.
Замещенные гидразоны
Примеры замещенных гидразонов включают N,N-диметил и 2,4-динитрофенил.
Оксимные производные
Примеры оксимных производных включают О-метил, О-бензил и О-фенилтиометил.
Имины
Замещенные метиленовые производные, циклические производные.
Примеры замещенных метиленовых и циклических производных включают оксазолидины, 1-метил-2-(1'-гидроксиалкил)имидазолы, N,N'-диметилимидазолидины, 2,3-дигидро-1,3-бензотиазолы, аддукты диэтиламина и комплекс бис(2,6-ди-трет-бутил-4-метоксифеноксида) метилалюминия (MAD).
Защита для карбоксильной группы
Сложные эфиры
Замещенные метиловые сложные эфиры
Примеры замещенных метиловых сложных эфиров включают 9-флуоренилметиловый, метоксиметиловый, метилтиометиловый, тетрагидропираниловый, тетрагидрофураниловый, метоксиэтоксиметиловый, 2-(триметилсилил)этоксиметиловый, бензилоксиметиловый, фенациловый, п-бромфенациловый, α-метилфенациловый, п-метоксифенациловый, карбоксамидометиловый и N-фталимидометиловый.
2-Замещенные этиловые сложные эфиры
Примеры 2-замещенных этиловых сложных эфиров включают 2,2,2-трихлорэтиловый, 2-галогенэтиловый, ω-хлоралкиловый, 2-(триметилсилил)этиловый, 2-метилтиоэтиловый, 1,3-дитианил-2-метиловый, 2-(п-нитрофенилсульфенил)этиловый, 2-(п-толуолсульфонил)этиловый, 2-(2'-пиридил)этиловый, 2-(дифенилфосфино)этиловый, 1-метил-1-фенилэтиловый, трет-бутиловый, циклопентиловый, циклогексиловый, аллиловый, 3-бутен-1-иловый, 4-(триметилсилил)-2-бутен-1-иловый, циннамиловый, α-метилциннамиловый, фениловый, п-(метилмеркапто)фениловый и бензиловый.
Замещенные бензиловые сложные эфиры
Примеры замещенных бензиловых сложных эфиров включают трифенилметиловый, дифенилметиловый, бис(о-нитрофенил)метиловый, 9-антрилметиловый, 2-(9,10-диоксо)антрилметиловый, 5-дибензосубериловый, 1-пиренилметиловый, 2-(трифторметил)-6-хромилметиловый, 2,4,6-триметилбензиловый, п-бромбензиловый, о-нитробензиловый, п-нитробензиловый, п-метоксибензиловый, 2,6-диметоксибензиловый, 4-(метилсульфинил)бензиловый, 4-сульфобензиловый, пиперониловый, 4-пиколиловый и п-Р-бензиловый.
Силиловые сложные эфиры
Примеры силиловых сложных эфиров включают триметилсилиловый, триэтилсилиловый, трет-бутилдиметилсилиловый, изо-пропилдиметилсилиловый, фенилдиметилсилиловый и ди-трет-бутилметилсилиловый.
Активированные сложные эфиры
Примеры активированных сложных эфиров включают тиолы.
Смешанные производные
Примеры смешанных производных включают оксазолы, 2-алкил-1,3-оксазолины, 4-алкил-5-оксо-1,3-оксазолидины, 5-алкил-4-оксо-1,3-диоксоланы, сложные орто-эфиры, фенильную группу и комплекс пентааминокобальта(III).
Станниловые сложные эфиры
Примеры станниловых сложных эфиров включают триэтилстаннил и три-н-бутилстаннил.
Амиды и гидразиды
Амиды
Примеры амидов включают N,N-диметил, пирролидинил, пиперидинил, 5,6-дигидропентантридинил, о-нитроанилиды, N-7-нитроиндолил, N-8-нитро-1,2,3,4-тетрагидрохинолил и п-Р-бензолсульфонамиды.
Гидразиды
Примеры гидразидов включают N-фенил и N,N'-диизопропил гидразиды.
С. Синтез
Соединения настоящего изобретения могут быть получены с использованием обычной синтетической органической химии и с использованием матричных или комбинаторных способов в соответствии с приведенными далее схемами 1-11 и иллюстрациями, подробно описанными в примерах 1-24. Обычный специалист в данной области сможет модифицировать и адаптировать приведенные в данном описании методики для получения описанных соединений.
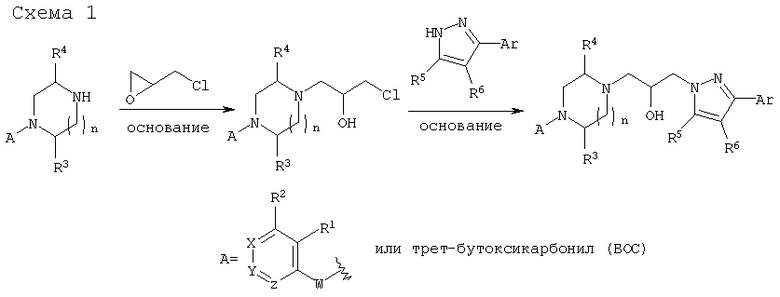

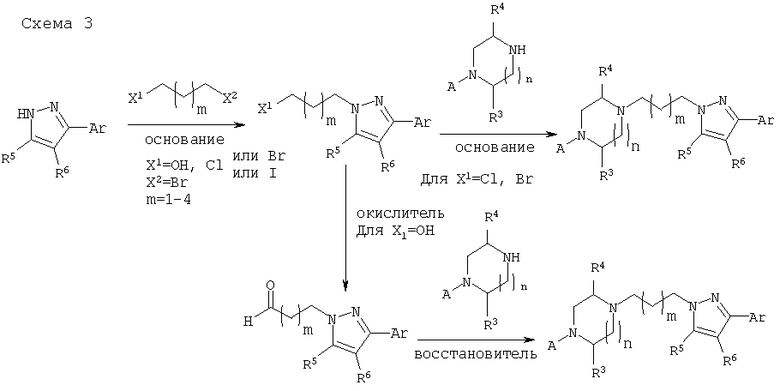
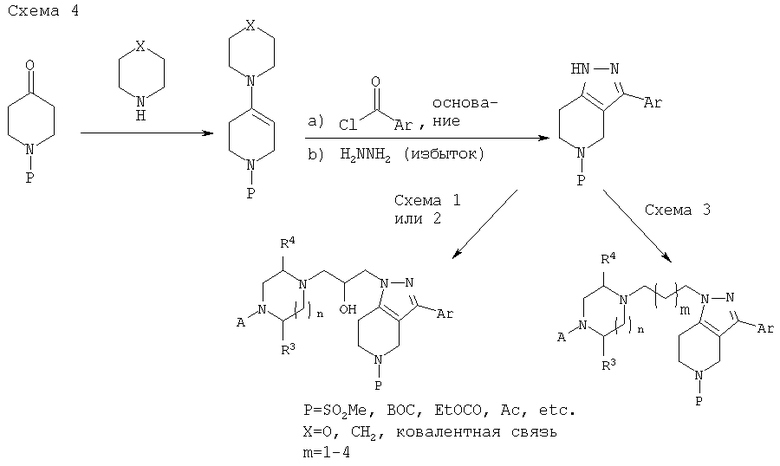



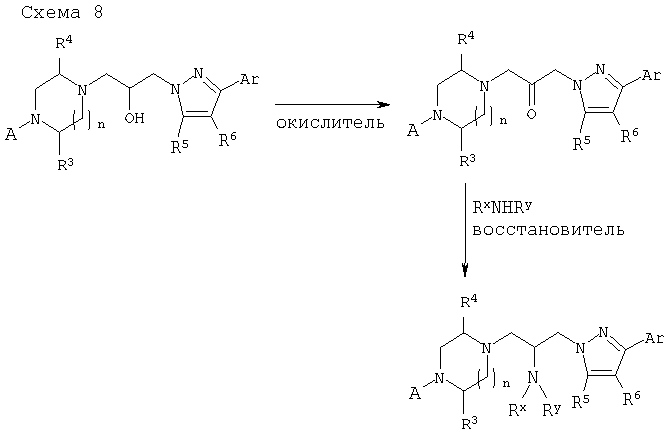

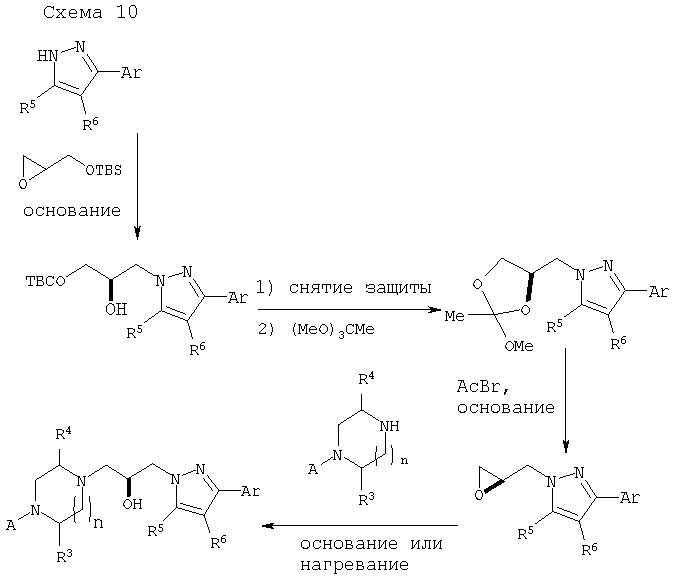
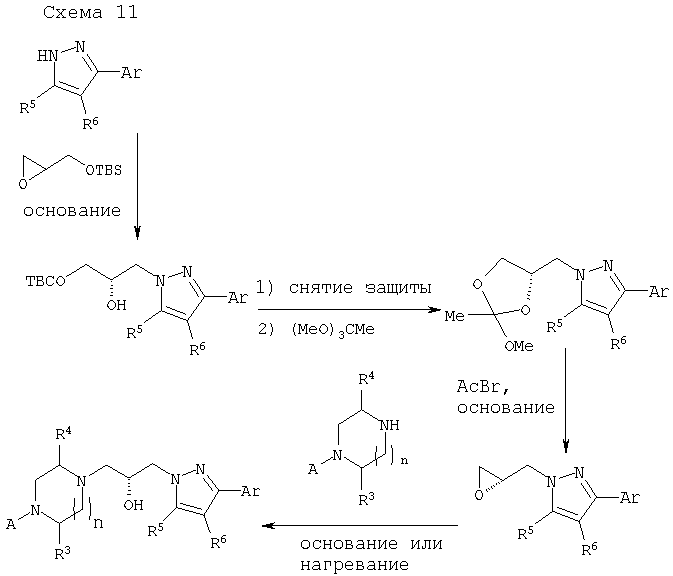
D. Препаративная форма и введение
Настоящие соединения ингибируют протеолитическую активность катепсина S человека и поэтому полезны в качестве лекарственного средства, особенно в способах лечения пациентов, страдающих от аллергических заболеваний или состояний, которые модулируются или регулируются ингибированием активности катепсина S.
Объектом изобретения является способ лечения субъекта с аллергическим заболеванием, опосредованным катепсином S, который включает введение субъекту терапевтически эффективного количества фармацевтической композиции, включающей соединение изобретения. Изобретение также относится к способу ингибирования активности катепсина S у субъекта, который включает введение субъекту терапевтически эффективного количества фармацевтической композиции, включающей соединение изобретения.
Принимая во внимание ингибирующее действие в отношении протеолитической активности катепсина S человека, соединения по настоящему изобретению могут быть сформулированы в виде различных фармацевтических форм для целей введения. Для получения таких фармацевтических композиций эффективное количество конкретного соединения в форме основания или кислотно-аддитивной соли в качестве активного ингредиента тщательно смешивают с фармацевтически приемлемым носителем.
Носитель может иметь широкий диапазон форм в зависимости от формы препарата, желательного для введения. Такие фармацевтические композиции предпочтительны в виде стандартной лекарственной формы, подходящей предпочтительно для перорального введения или парентеральной инъекции. Например, при получении композиций в виде пероральной препаративной лекарственной формы можно использовать любую из обычных фармацевтических сред. Они включают воду, гликоли, масла, спирты и подобные в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазывающие агенты, связывающие агенты, разрыхляющие агенты и подобные в случае порошков, пилюль, капсул и таблеток. Принимая во внимание легкость их введения, таблетки и капсулы представляют собой предпочтительную пероральную стандартную лекарственную форму, и в таком случае обычно используют твердые фармацевтические носители. Для парентеральных композиций носитель обычно будет включать стерильную воду, по крайней мере большей частью, хотя могут быть включены другие ингредиенты, например, способствующие растворимости. Например, могут быть получены растворы для инъекций, в которых носитель включает физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также могут быть получены суспензии для инъекций, в таком случае можно использовать подходящие жидкие носители, суспендирующие агенты и подобные. В композициях, подходящих для подкожного введения, носитель необязательно включает агент, усиливающий проницаемость, и/или подходящий смачивающий агент, необязательно в сочетании с подходящими добавками любой природы в незначительных количествах, при этом указанные добавки не вызывают значительного вредного влияния на кожу. Такие добавки могут облегчать введение в кожу и/или могут быть полезными для получения желаемых композиций. Такие композиции могут вводиться различными путями, например, в виде чрескожного пластыря, путем нанесения пятна, в виде мази. Кислотно-аддитивные соли соединений формулы I благодаря их повышенной растворимости в воде по сравнению с соответствующей основной формой являются более подходящими для получения водных композиций.
Особенно предпочтительно формулировать вышеуказанные фармацевтические композиции в виде стандартной лекарственной формы для легкости введения и однородности дозирования. Стандартная лекарственная форма, как использовано в данном описании, относится к физически дискретным единицам, подходящим в качестве единичных доз, каждая единица содержит предварительно определенное количество активного ингредиента, рассчитанное для оказания желательного терапевтического действия, вместе с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с насечкой или покрытые оболочкой), капсулы, пилюли, саше, облатки, растворы для инъекций или суспензии, чайные мерные ложки, столовые мерные ложки и подобные и отдельные их составляющие.
Фармацевтически приемлемые кислотно-аддитивные соли включают терапевтически активные нетоксичные кислотно-аддитивные солевые формы, которые способны образовывать описанные соединения. Последние обычно могут быть получены обработкой основной формы подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например хлористоводородная или бромистоводородная кислота; серная, азотная, фосфорная и подобные; или органические кислоты, такие как, например уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, пальмовая и подобные. Термин «аддитивная соль» также включает сольваты, которые описанные соединения, а также их соли способны образовывать. Такие сольваты, например, представляют собой гидраты, алкоголяты и подобные. Наоборот, солевая форма может быть превращена при обработке щелочью в форму свободного основания.
Стереоизомерные формы включают все возможные изомерные формы, которые могут иметь соединения формулы (I). Если не отмечено или не указано другого, химическое обозначение соединений означает смесь всех возможных стереохимически изомерных форм, указанные смеси включают все диастереомеры и энантиомеры основной молекулярной структуры. Более конкретно стереогенные центры могут иметь (R)- или (S)-конфигурацию; заместители при двухвалентных циклических насыщенных радикалах могут иметь или цис- или транс-конфигурацию. Изобретение включает стереохимически изомерные формы описанных соединений, включая диастереоизомеры, а также их смеси в любом соотношении. Описанные соединения также могут существовать в виде таутомерных форм. Подразумевается, что хотя такие формы ясно не указаны в вышеуказанных и следующих далее формулах, они включены в объем настоящего изобретения.
Специалисты в области лечения заболеваний или состояний, опосредованных ферментом катепсином S, легко определят эффективное суточное количество из представленных далее результатов испытаний и другой информации. Обычно предполагается, что терапевтически эффективная доза будет составлять от 0,001 мг/кг до 5 мг/кг веса тела, более предпочтительно от 0,01 мг/кг до 0,5 мг/кг веса тела. Может оказаться подходящим осуществлять введение терапевтически эффективной дозы в виде двух, трех, четырех или более поддоз через подходящие промежутки времени в течение дня. Указанные поддозы могут быть получены в виде стандартных лекарственных форм, например, содержащих от 0,05 мг до 250 мг, и, в частности, от 0,5 до 50 мг активного ингредиента на стандартную лекарственную форму. Примеры включают 2 мг, 4 мг, 7 мг, 10 мг, 15 мг, 25 мг и 35 мг лекарственные формы. Соединения по изобретению также могут быть получены в виде составов с замедленным высвобождением или составов для подкожного введения или чрескожных пластырей. Описанные соединения также могут быть сформулированы в виде спрея или других составов для ингаляции или местного введения.
Точная доза и частота введения зависит от конкретного использованного соединения формулы (I), конкретного заболевания, подвергаемого лечению, тяжести заболевания, подвергаемого лечению, возраста, веса и общего физического состояния конкретного пациента, а также от других лекарственных средств, которые может принимать пациент, как хорошо известно специалистам в данной области. Кроме того, очевидно, что указанное эффективное суточное количество может быть снижено или увеличено в зависимости от ответной реакции пациента, подвергаемого лечению, и/или в зависимости от оценки лечащего врача, назначающего соединения по настоящему изобретению. Диапазоны эффективного суточного количества, отмеченные в данном описании, приведены, следовательно, только в качестве указания.
Следующий раздел включает подробную информацию, относящуюся к получению, характеристикам и применению описанных соединений.
Е. Примеры
ПРИМЕР 1
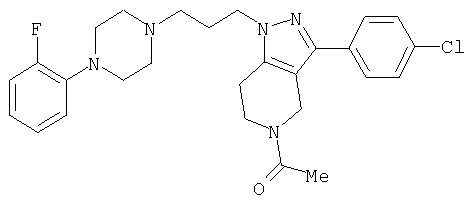
1-(3-(4-Хлорфенил)-1-{3-[4-(2-фторфенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон
A. 1-[3-(4-Хлорфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
К перемешиваемому раствору 50 г (0,35 моль) N-ацетил-4-пиперидона и 31 г (0,35 моль) морфолина в бензоле (350 мл) добавляли каталитическое количество (˜0,25 г) п-толуолсульфоновой кислоты. Смесь кипятили с обратным холодильником в течение 10 часов с ловушкой Дина-Старка. Растворитель удаляли при пониженном давлении, получая коричневое масло. Неочищенный продукт разбавляли CH2Cl2 (175 мл) и добавляли 50,0 мл (0,35 моль) Et3N. Смесь охлаждали до 0°C и медленно добавляли в течение 1 часа через капельную воронку раствор 45,0 мл (0,35 моль) 4-хлорбензоил хлорида в CH2Cl2 (50 мл). Смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь затем разбавляли 1н. HCl (150 мл) и перемешивали интенсивно в течение 3 часов. Водный слой экстрагировали CH2Cl2 (3×250 мл) и объединенные экстракты сушили над Na2SO4 и растворитель удаляли при пониженном давлении. Неочищенное масло разбавляли EtOH (350 мл) и охлаждали до 0°C. К данному перемешиваемому раствору медленно добавляли 33,0 мл (1,06 моль) гидразина и смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи, за это время образовывался белый осадок. Объем реакционной смеси уменьшали до ˜150 мл и добавляли к смеси EtOAc (750 мл). Суспензию интенсивно перемешивали в течение 2 часов и фильтровали, затем промывали EtOAc (2×200 мл) и сушили в вакууме, получая 41,4 г (42% по 3 стадиям) бледно-желтого твердого вещества. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление), m/z вычислено для C14H14ClN3O [M+H]+ 276,08, найдено 276,0, 1H ЯМР (400 МГц, CDCl3, смесь амидных ротамеров): 7,65 (д, J=8,4 Гц, 2H), 7,64 (д, J=9,3 Гц, 2H), 7,58 (д; J=10,5 Гц, 2H), 7,55 (д, J=8,5 Гц, 2H), 4,94 (с, 2H), 4,78 (с, 2H), 4,08 (т, J=5,9 Гц, 2H), 3,90 (т, J=5,8 Гц, 2H), 3,02 (т, J=5,8 Гц, 2H), 2,96 (т, J=5,9 Гц, 2H), 2,36 (с, 3H), 2,31 (с, 3H).
B. 1-[3-(4-Хлорфенил)-1-(3-хлорпропил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Cs2CO3 (2,66 г, 8,2 ммоль) добавляли к раствору 1-[3-(4-хлор-фенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (1,0 г, 5,4 ммоль) в ДМФ (10 мл) и перемешивали в течение 15 минут. Добавляли 1-бром-3-хлорпропан (1,28 г, 8,2 ммоль) и перемешивали в атмосфере N2 при комнатной температуре в течение 36 часов. К реакционной смеси добавляли воду (50 мл) и перемешивали в течение 5 минут. Продукт выпадал в осадок. Водную часть декантировали и добавляли к остатку воду и опять декантировали. Полутвердое вещество помещали в CH2Cl2 и пропускали через короткий слой SiO2 (5% MeOH/EtOAc), получая 1,06 г (83%) бледно-желтого полутвердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C17H19Cl2N3O, 351,09; m/z найдено, 352,0 [M+H]+. 1H ЯМР (500 МГц, CDCl3, смесь 1:1 ротамеров): 7,60 (д, J=8,3 Гц, 1H), 7,53 (д, J=8,3 Гц, 1H), 7,40 (д, J=8,3 Гц, 1H), 7,36 (д, J=8,3 Гц, 1H), 4,77 (с, 1H), 4,61 (с, 1H), 4,20 (т, J=6,2 Гц, 2H), 3,94 (т, J=5,8 Гц, 1H), 3,76 (т, J=5,8 Гц, 1H), 3,52 (кв, J=6,1 Гц, 2H), 2,84 (т, J=5,5 Гц, 1H), 2,77 (т, J=5,6 Гц, 1H), 2,37 (секстет, J=6,1 Гц, 2 H), 2,21 (с, 1,5 H), 2,16 (с, 1,5 H).
C. 1-(3-(4-Хлорфенил)-1-{3-[4-(2-фторфенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон
1-[3-(4-Хлорфенил)-1-(3-хлорпропил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон (0,053 г, 0,15 ммоль) растворяли в CH3CN (0,5 мл) и добавляли раствор 1-(2-фторфенил)пиперазина (0,053 г, 0,30 ммоль) в CH3CN (0,5 мл) с последующим добавлением K2CO3 (0,031 г, 0,22 ммоль) и Bu4NI (0,018 г, 0,05 ммоль). Смесь перемешивали при комнатной температуре в течение 7 дней. Препаративная ТСХ (диоксид кремния, 5% MeOH/EtOAc) давала 30 мг (41%) указанного в заголовке соединения. Масс-спектр (электрораспыление): точная масса вычислено для C27H31ClFN5O 495,22; m/z найдено, 496,3 [M+H]+. 1H ЯМР (500 МГц, CDCl3, смесь 1:1 ротамеров): 7,60 (д, J=8,3 Гц, 1H), 7,54 (д, J=8,3 Гц, 1H), 7,39 (д, J=8,3 Гц, 1H), 7,35 (д, J=8,3 Гц, 1H), 7,06-6,90 (м, 4H), 4,77 (с, 1H), 4,60 (с, 1H), 4,10 (т, J=6,8 Гц, 2H), 3,92 (т, J=5,7 Гц, 1H), 3,74 (т, J=5,7 Гц, 1H), 3,08 (ушир. с, 4H), 2,83 (т, J=5,6 Гц, 1H), 2,77 (т, J=5,7 Гц, 1H), 2,58 (ушир. с, 4H), 2,41-2,38 (м, 2H), 2,19 (с, 1,5H), 2,13 (с, 1,5H), 2,10-2,07 (м, 2H).
ПРИМЕР 2
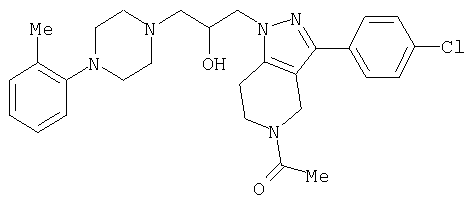
1-{3-(4-Хлорфенил)-1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон
A. 1-[3-(4-Хлорфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
К перемешиваемому раствору 1,00 г (3,63 ммоль) 1-[3-(4-хлорфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона и 2,85 мл (36,3 ммоль) эпихлоргидрина добавляли 1,30 г (3,99 ммоль) твердого Cs2CO3, Реакционную смесь перемешивали в течение 48 часов и растворитель удаляли при пониженном давлении. Остаток затем разбавляли H2O (50 мл) и EtOAc (50 мл). Слои отделяли и органический слой промывали H2О (25 мл) и насыщенным раствором соли (25 мл), сушили над Na2SO4 и растворитель удаляли при пониженном давлении. Очистка флэш-хроматографией (диоксид кремния, 0-15% ацетон/CH2Cl2) давала 0,72 г (60%) белого твердого вещества. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,5. Масс-спектр (электрораспыление): m/z вычислено для C17H18ClN3O2 [M+H]+, 332,11, найдено 332,0, 1H ЯМР (400 МГц, CDCl3, смесь амидных ротамеров): 7,60 (д, J=8,6 Гц, 2H), 7,54 (д, J=8,4 Гц, 2H), 7,40 (д, J=8,6 Гц, 2H), 7,36 (д, J=8,4 Гц, 2H), 4,80 и 4,73 (A и B AB квартета, Jab=15,8 Гц, 2H), 4,60 (с, 2H), 4,47 (дд, J=15,3, 2,5 Гц, 1H), 4,42 (дд, J=15,0, 2,7 Гц, 1H), 4,11 (дд, J=5,3, 2,5 Гц, 1H), 4,08 (дд, J=5,1, 3,3 Гц, 1H), 3,99-3,85 (м, 2H), 3,73 (дт, J=5,9, 1,8 Гц, 2H), 3,37 (м, 2H), 2,87-2,80 (м, 3H), 2,80-2,69 (м, 3H), 2,53 (дд, J=4,7, 2,5 Гц, 1H), 2,48 (дд, J=4,6, 2,6, 1H), 2,19 (с, 3H), 2,15 (с, 3H).
B. 1-{3-(4-Хлорфенил)-1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон
Раствор 1-[3-(4-хлорфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]-этанона (0,8 г, 2,42 ммоль) в CH2Cl2 (12 мл) обрабатывали трифлатом иттербия(III) (0,15 г, 0,24 ммоль) и 1-(0-толил)-пиперазином (0,51 г, 2,90 ммоль) при 25°C. Реакционную смесь перемешивали в течение 24 часов и разбавляли EtOAc (100 мл) и H2O (50 мл). Органический слой отделяли, промывали H2O (2×50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 5% MeOH/CH2Cl2) давала 1,08 г (88%) целевого соединения, белый порошок. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,38. Масс-спектр (электрораспыление): m/z 508,3 ([M+H]+, C28H34ClN5O2 вычислено 507,2). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,60 и 7,37 (AB система, Jab=8,8 Гц, 2H), 7,54 и 7,40 (AB система, Jab=8,8 Гц, 2H), 7,18-7,14 (м, 2H), 7,00-6,97 (м, 2H), 4,85 и 4,73 (АВ система, Jab=15,5 Гц, 1H), 4,62 (с, 1H), 4,20-4,11 (м, 2H), 4,06-4,01 (м, 1H), 3,88-3,70 (м, 2H), 2,97-2,87 (м, 6H), 2,85-2,75 (м, 2H), 2,65-2,55 (м, 2H), 2,51-2,48 (м, 2H), 2,29 (с, 3H), 2,21 (с, 1,5H), 2,17 (с, 1,5H).
ПРИМЕР 3

1-{3-(4-Хлорфенил)-1-[2-метокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон
Перемешиваемый раствор 1-{3-(4-хлорфенил)-1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанона (25 мг, 0,05 ммоль) в ТГФ (0,2 мл) обрабатывали NaH (1,42 мг, 0,06 ммоль) при 25°C. Через 20 минут добавляли иодистый метил (3,7 мл, 0,06 ммоль) и реакционную смесь перемешивали дополнительно в течение 2 часов. Препаративная ТСХ (диоксид кремния, 5% MeOH/CH2Cl2) давала 14,6 мг (56%) бесцветной пленки. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,38. Масс-спектр (электрораспыление): m/z 522,2 ([M+H]+, C29Н36CIN5О2 вычислено 521,3). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,62 и 7,37 (АВ система, Jab=8,8 Гц, 2H), 7,55 и 7,40 (АВ система, Jab=8,8 Гц, 2H), 7,18-7,14 (м, 2H), 7,02-6,95 (м, 2H), 4,82 и 4,75 (АВ система, Jab=15,5 Гц, 1H), 4,62 (с, 1H), 4,30-4,25 (м, 1H), 4,09-3,73 (м, 4H), 3,29 (с, 1,5H), 3,27 (с, 1,5H), 2,93-2,55 (м, 12H), 2,30 (с, 3H), 2,21 (с, 1,5H), 2,16 (с, 1,5H).
ПРИМЕР 4
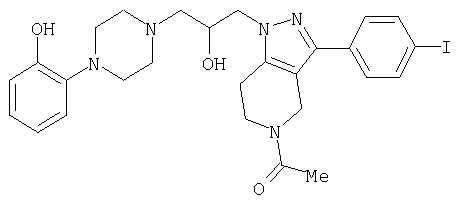
1-[1-{2-Гидрокси-3-[4-(2-гидроксифенил)пиперазин-1-ил]пропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
A. 1-[3-(4-Иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
В колбу, оборудованную ловушкой Дина-Старка, загружали N-ацетил-4-пиперидон (27,29 г, 137 ммоль), пиперидин (16,5 мл, 129 ммоль), п-толуолсульфоновую кислоту (0,5 г) и бензол (150 мл). Смесь нагревали до 125°C. Через 8 часов смесь оставляли охлаждаться и концентрировали в вакууме, получая соответствующий енамин (35 г). В течение 2 часов добавляли по каплям к раствору енамина (11,0 г, примерно 41 ммоль) в CH2Cl2 (80 мл) при 0°C раствор п-иодбензоилхлорида (9,28 г, 34,8 ммоль) в CH2Cl2 (40 мл). Смесь затем оставляли нагреваться до комнатной температуры и перемешивали дополнительно в течение 17 часов. Раствор обрабатывали 1н. HCl (200 мл) и перемешивали интенсивно в течение 5 часов. Слои отделяли и водный слой экстрагировали CH2Cl2 (3×150 мл). Объединенные экстракты сушили над Na2SO4 и концентрировали. Остаток растворяли в EtOH (200 мл) и обрабатывали NH2NH2 (16,0 мл, 51 ммоль). Смесь перемешивали в течение 17 часов и добавляли H2O (300 мл). Образовавшийся осадок собирали фильтрованием и сушили на воздухе, получая 8,82 г (59%) 1-[3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона, подходящего для использования без дополнительной очистки. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): m/z вычислено для C14H15IN3O [M+H]+ 368,03, найдено 368,0. 1H ЯМР (CD3OD/CDCl3, 500 МГц, смесь амидных ротамеров): 7,72 (д, J=8,2 Гц, 2H), 7,69 (д, J=8,3 Гц, 2H), 7,24 (д, J=8,2 Гц, 2H), 7,20 (д, J=8,3 Гц, 2H), 4,69 (с, 2H), 4,56 (с, 2H), 3,83 (т, J=6,0 Гц, 2H), 3,69 (т, J=5,8 Гц, 2H), 2,79 (т, J=5,7 Гц, 2H), 2,72 (т, J=5,8 Гц, 2H), 2,13 (с, 3H), 2,08 (с, 3H).
B. 1-[3-(4-Иодфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Cs2CO3 (1,30 г, 4,01 ммоль) добавляли к раствору 1-[3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (1,34 г, 3,65 ммоль) и эпихлоргидрина (2,85 мл, 36,4 ммоль) в ДМФ (10,0 мл). Смесь перемешивали в течение 17 часов, затем распределяли между EtOAc (400 мл) и насыщенным раствором NaHCO3 (150 мл). Содержащий NaHCO3 слой экстрагировали EtOAc (2×150 мл). Объединенные экстракты промывали H2O (2×150 мл), насыщенным раствором соли (150 мл), сушили над Na2SO4 и концентрировали. Остаток очищали колоночной хроматографией (диоксид кремния, 10-25% ацетон/CH2Cl2), получая 890 мг (58%) указанного в заголовке соединения. ВЭЖХ, tR=5,53 мин. (Условия обращенной фазы: HP 1100 LCMS, Phenomenex luna 2,1×150 мм колонка, 60% MeOH/H2O (0,5% AcOH) до 90%MeOH/H2O (0,5% AcOH), выдерживание при первоначальных условиях в течение 2 минут, затем доводили до конечных условий в течение 5 минут). Масс-спектр (электрораспыление), m/z вычислено для C17H18IN3O2Na [M+Na]+ 445,04, найдено 445,95, 1H ЯМР (CDCl3, 500 МГц, смесь амидных ротамеров): 7,76 (д, J=8,3 Гц, 2H), 7,75 (д, J=8,3 Гц, 2H), 7,42 (д, J=8,2 Гц, 2H), 7,35 (д, J=8,2 Гц, 2H), 4,80 и 4,73 (A и B AB квартета, Jab=15,6 Гц, 2H), 4,60 (с, 2H), 4,84 (дд, J=15,1, 2,1 Гц, 1H), 4,42 (дд, J=15,0, 2,1 Гц, 1H), 4,11 (т, J=5,0, Гц, 1H), 4,08 (т, J=5,0 Гц, 1H), 3,98-3,87 (м, 2H), 3,74 (м, 2H), 3,34 (м, 2H), 2,87-2,72 (м, 6H), 2,52 (дд, J=4,6, 2,6 Гц, 1H), 2,48 (дд, J=4,5, 2,6, 1H), 2,20 (с, 3H), 2,14 (с, 3H).
C. 1-[1-{2-Гидрокси-3-[4-(2-гидроксифенил)пиперазин-1-ил]-пропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
1-[3-(4-Иодфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон (62 мг, 0,15 ммоль) и 4-(2-гидроксифенил)пиперазин (34 мг, 0,19 ммоль) объединяли в CH2Cl2 (0,5 мл) и раствор обрабатывали Yb(OTf)3·H2O (44 мг, 0,071 ммоль). Смесь встряхивали в течение 72 часов, затем разбавляли CH2Cl2 (1 мл). Очистка препаративной ТСХ (диоксид кремния, 10% MeOH/CH2Cl2) давала 45 мг (51%) не совсем белого порошка. ТСХ (диоксид кремния, 8% MeOH/CH2Cl2): Rf=0,2. Масс-спектр (электрораспыление): m/z вычислено для C27H33IN5O3 [M+H]+ 602,15, найдено 602,2. 1H ЯМР (CDCl3, 500 МГц, смесь амидных ротамеров): 7,76 (д, J=8,6 Гц, 1H), 7,72 (д, J=8,6 Гц, 1H), 7,42 (д, J=8,5 Гц, 1H), 7,34 (д, J=8,5 Гц, 1H), 7,14 (м, 1H), 7,80 (т, J=7,7 Гц, 1H), 6,94 (д, J=8,1 Гц, 1H), 6,86 (т, J=7,7 Гц, 1H), 4,83 и 4,72 (A и B AB квартета, Jab=15,6 Гц, 1H), 4,61 (с, 1H), 4,22-4,15 (м, 2H), 4,02 (м, 2H), 3,88 (м, 1H), 3,76 (м, 3H), 3,00-2,49 (м, 11H), 2,20 (с, 1,5H), 2,15 (с, 1,5H).
ПРИМЕР 5
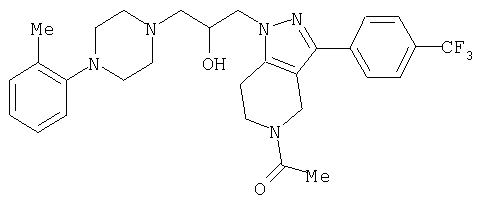
1-[1-[2-Гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
A. 1-[3-(4-Трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Раствор N-ацетил-4-пиперидона (2,82 г, 20 ммоль), морфолина (1,93 мл, 22 ммоль) и п-толуолсульфоновой кислоты (5 мг) в бензоле (8,5 мл) кипятили с обратным холодильником в течение 8 часов с устройством Дина-Старка. Растворитель удаляли и остаток растворяли в CH2Cl2 (20 мл). Добавляли триэтиламин (3,1 мл) и п-трифторметилбензоилхлорид (3,27 мл, 22 ммоль) в CH2Cl2 (4 мл) добавляли по каплям в раствор при 0°C. Реакционную смесь перемешивали при 25°C в течение 24 часов и разбавляли водной HCl (5%, 25 мл). После перемешивания еще в течение 30 минут, органический слой отделяли, промывали H2O (20 мл), сушили (Na2SO4) и концентрировали. Остаток растворяли в EtOH (95%, 18 мл) и обрабатывали при 0°C гидразином (2,9 мл, 60 ммоль). Смесь перемешивали при 25°C в течение 3 часов и добавляли H2O (4 мл). Большинство летучих компонентов удаляли и остаток экстрагировали CH2Cl2 (50 мл). Органический слой отделяли, промывали H2O (20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 5% MeOH/CH2Cl2) давала 5,1 г (83%) белого порошка. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,30. Масс-спектр (электрораспыление): m/z 332,0 ([M+Na]+, C15H14F3N3O вычислено 309,1). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,73-7,67 (м, 4H), 4,85 (с, 1,2H), 4,68 (с, 0,8H), 3,96 (т, J=4,5 Гц, 0,8H), 3,78 (т, J=4,5 Гц, 1,2H), 2,89 (т, J=4,5 Гц, 1,2H), 2,83 (т, J=4,5 Гц, 0,8H), 2,23 (с, 1,8H), 2,18 (с, 1,2H).
B. 1-[1-Оксиранилметил-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Раствор 1-[3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (2,4 г, 7,77 ммоль) в ДМФ (15 мл) обрабатывали карбонатом цезия (5,05 г, 15,5 ммоль) и эпихлоргидрином (6,1 мл, 77,7 ммоль) при 25°C и перемешивали в течение 24 часов перед разбавлением EtOAc (100 мл) и H2O (50 мл). Органический слой отделяли, промывали H2O (2×50 мл), насыщенным раствором соли (50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10% ацетон/CH2Cl2) давала 2,30 г (81%) белого порошка. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,35. Масс-спектр (электрораспыление): m/z 388,0 ([M+Na]+, C18H18F3N3O2 вычислено 365,1. 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,77 и 7,63 (АВ система, Jab=8,2 Гц, 2H), 7,71 и 7,67 (AB система, Jab=8,4 Гц, 2H), 4,82 и 4,76 (АВ система, Jab=15,5 Гц, 1,2H), 4,58 (с, 0,8H), 4,45-4,35 (м, 1H), 4,08-4,02 (м, 1H), 3,92-3,80 (м, 1H), 3,70-3,63 (м, 1H), 3,30 (м, 1H), 2,80-2,67 (м, 3H), 2,48-2,42 (м, 1H), 2,13 (с, 1,3H), 2,08(с, 1,7H).
C. 1-[1-[2-Гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон.
Раствор 1-[1-оксиранилметил-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (1,16 г, 3,20 ммоль) в CH2Cl2 (15 мл) обрабатывали трифлатом иттербия(III) (0,40 г, 0,64 ммоль) и 1-(O-толил)пиперазином (0,84 г, 4,77 ммоль) при 25°C и перемешивали в течение 48 часов перед разбавлением CH2Cl2 (100 мл) и H2O (50 мл). Органический слой отделяли, промывали H2O (2×50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 5% MeOH/CH2Cl2) давала 1,54 г (89%) белого порошка. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,35. Масс-спектр (электрораспыление): m/z 542,3 ([M+H]+, C29H34F3N5O2 вычислено 541,3). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,82 и 7,65 (АВ система, Jab=8,2 Гц, 2H), 7,72 и 7,68 (АВ система, Jab=8,4 Гц, 2H), 7,18-6,97 (м, 4H), 4,88 и 4,76 (АВ система, Jab=16 Гц, 0,9H), 4,65 (с, 1,1H), 4,23-4,12 (м, 2H), 4,08-4,00 (м, 2H), 3,88-3,70 (м, 2H), 3,02-2,85 (м, 6H), 2,85-2,75 (м, 2H), 2,65-2,55 (м, 2H), 2,53-2,45 (м, 2H), 2,29 (с, 3H), 2,21 (с, 1,8H), 2,17 (с, 1,2H).
ПРИМЕР 6
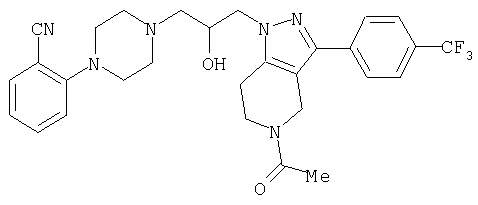
2-(4-{3-[5-Ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил
Раствор 1-[1-оксиранилметил-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (0,84 г, 2,30 ммоль) в CH2Cl2 (10 мл) обрабатывали трифлатом иттербия(III) (0,29 г, 0,46 ммоль) и 1-(2-цианофенил)пиперазином (0,75 г, 3,5 ммоль) при 25°C и перемешивали в течение 48 часов перед разбавлением CH2Cl2 (100 мл) и H2O (50 мл). Органический слой отделяли, промывали H2O (2×50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 5% MeOH/CH2Cl2) давала 1,15 г (90%) светло-желтых кристаллов. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,30. Масс-спектр (электрораспыление): m/z 553,3 ([M+H]+, C29H31F3N6O2 вычислено 552,3). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,82 и 7,68 (АВ система, Jab=8,2 Гц, 2H), 7,76 и 7,72 (АВ система, Jab=8,4 Гц, 2H), 7,60-7,48 (м, 2H), 7,05-7,00 (м, 2H), 4,90 и 4,78 (АВ система, Jab=16 Гц, 1H), 4,69 (с, 1H), 4,30-3,71 (м, 6H), 3,25 (м, 4H), 3,02-2,75 (м, 4H), 2,70-2,65 (м, 2H), 2,60-2,53 (м, 2H), 2,23 (с, 1,5 H), 2,18 (с, 1,5H).
ПРИМЕР 7
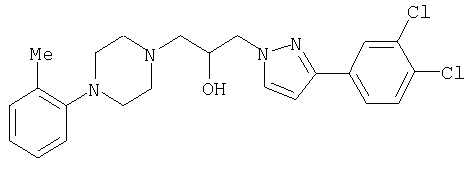
1-[3-(3,4-Дихлорфенил)пиразол-1-ил]-3-(4-o-толилпиперазин-1-ил)пропан-2-ол.
A. 3-(3,4-Дихлорфенил)-1-оксиранилметил-1H-пиразол
Перемешиваемый раствор 3-(3,4-дихлорфенил)пиразола (300 мг, 1,4 ммоль) в ДМФ (5 мл) обрабатывали карбонатом цезия (550 мг, 1,69 ммоль) и эпихлоргидрином (1,1 мл, 14,0 ммоль) при комнатной температуре в течение 18 часов. Неочищенную реакционную смесь затем распределяли между EtOAc (50 мл) и водой (35 мл). Водную фазу дополнительно экстрагировали (2×50 мл) и объединенные органические слои промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали при пониженном давлении, получая неочищенный продукт. Очистка колоночной хроматографией (диоксид кремния, 25% EtOAc/гексаны) давала 308 мг (82%) указанного в заголовке соединения. 1ЯМР (400 МГц, CDCl3): 7,83 (д, J=2 Гц, 1H), 7,54 (дд, J=2,8 Гц, 1H), 7,44 (д, J=2 Гц, 1H), 7,38 (д, J=8 Гц, 1H), 6,48 (д, J=2 Гц, 1H), 4,45 (дд, J=3, 9,7 Гц, 1H), 4,12 (дд, J=6, 15 Гц, 1H), 3,31 (м, 1H), 2,81 (дд, J=4,0, 4,6 Гц, 1H), 2,47 (дд, J=2,6, 4,7 Гц, 1H).
В. 1-[3-(3,4-Дихлорфенил)пиразол-1-ил]-3-(4-o-толилпиперазин-1-ил)пропан-2-ол
Раствор 3-(3,4-дихлорфенил)-1-оксиранилметил-1H-пиразола (30 мг, 0,11 ммоль) и 1-(2-метилфенил)пиперазина (22 мг, 0,12 ммоль) в EtOH (1 мл) нагревали при 80°C в течение ночи. Удаление растворителя и очистка колоночной хроматографией (диоксид кремния, 0-5% ацетон/CH2Cl2) давала 35 мг (70%) указанного в заголовке соединения. 1H ЯМР (400 МГц, CDCl3): 7,89 (д, J=2 Гц, 1H), 7,61 (дд, J=2, 8,7 Гц, 1H), 7,57 (д, J=2 Гц, 1H), 7,45 (д, J=8,4 Гц, 1H), 7,16 (м, 2H), 6,99 (м, 2H), 6,54 (д, J=2,3 Гц, 1H), 4,31 (м, 1H), 4,18 (м, 2H), 2,93 (м, 4H), 2,60 (м, 2H), 2,47 (м, 3H), 2,88 (с, 3H).
ПРИМЕР 8

1-[1-[2-(2-Пиперазин-1-ил-этиламино)-3-(4-o-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
A. 1-[5-Ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-3-(4-o-толилпиперазин-1-ил)пропан-2-он
Раствор ДМСО (3,55 мл, 50 ммоль) в CH2Cl2 (7 мл) обрабатывали оксалилхлоридом (2,90 мл, 33 ммоль) при -78°C и перемешивали в течение 30 минут. Затем медленно добавляли раствор 1-[1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (1,8 г, 3,3 ммоль) в CH2Cl2 (7 мл) и реакционную смесь перемешивали дополнительно в течение 30 минут перед гашением с помощью триэтиламина (18,4 мл, 132 ммоль). Реакционную смесь медленно нагревали до 25°C и разбавляли EtOAc (50 мл) и насыщенным NaHCO3 (30 мл). Органический слой отделяли, промывали H2O (2×50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 2-5% MeOH/CH2Cl2) давала 1,50 г (83%) светло-желтого порошка. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,35. Масс-спектр (электрораспыление): m/z 540,3 ([M+H]+, C29H32F3N5O2 вычислено 539,3). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,78 и 7,62 (АВ система, Jab=8,2 Гц, 2H), 7,70 и 7,64 (АВ система, Jab=8,4 Гц, 2H), 7,18-6,95 (м, 4H), 5,10 (с, 1H), 5,07 (с, 1H), 4,84 (с, 1H), 4,68 (с, 1H), 3,96 (т, J=4,4 Гц, 1H), 3,78 (т, J=4,4 Гц, 1H), 3,47 (с, 4H), 3,34 (с, 2H), 2,74-2,65 (м, 6H), 2,29 (с, 3H), 2,20 (с, 1,5H), 2,17 (с, 1,5H).
B. 1-[1-[2-(2-Пиперазин-1-илэтиламино-3-(4-o-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон.
Раствор 1-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-3-(4-o-толилпиперазин-1-ил)пропан-2-она (54 мг, 0,1 ммоль) в 1,2-дихлорэтане (0,5 мл) обрабатывали 1-(2-аминоэтил)пиперазином (26 мкл, 0,2 ммоль) и ледяной уксусной кислотой (34 мкл, 0,6 ммоль) при 25°C и перемешивали в течение 30 минут. Добавляли триацетоксиборгидрид натрия (63,6 мг, 0,3 ммоль) и реакционную смесь перемешивали дополнительно в течение 4 часов, после чего гасили CH2Cl2 (5 мл) и насыщенным NaHCO3 (5 мл). Органический слой отделяли, промывали H2O (2×5 мл), сушили над Na2SO4 и концентрировали. Препаративная ТСХ (диоксид кремния, 10% MeOH/CH2Cl2 давала 22 мг (35%) светло-желтой пленки. ТСХ (10% MeOH/CH2Cl2): Rf=0,2. Масс-спектр (электрораспыление): m/z 653,3 ([M+H]+, C35H47F3N8O вычислено 652,4). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,78-7,60 (м, 4H), 7,18-6,82 (м, 4H), 4,88-4,30 (м, 2H), 4,23-3,90 (м, 2H), 3,85-3,70 (м, 2H), 3,22-2,85 (м, 10H), 2,85-2,30 (м, 15H), 2,30 (с, 3H), 2,21 (с, 1,5H), 2,17 (с, 1,5H).
ПРИМЕР 9

трет-Бутиловый эфир 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил)-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
A. трет-Бутиловый эфир 3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
п-Толуолсульфоновую кислоту (0,055 г, 0,29 ммоль) и морфолин (4,76 мл, 54 ммоль) добавляли к раствору трет-бутил 4-оксо-1-пиперидинкарбоксилата (10,3 г, 52 ммоль) в бензоле (22 мл). Реакционную смесь нагревали в колбе, оборудованной обратным холодильником и ловушкой Дина-Старка при кипячении с обратным холодильником в течение 20 часов. Реакционную смесь охлаждали и концентрировали в вакууме, получая енамин, который использовали без дополнительной очистки. Енамин растворяли в CH2Cl2 (60 мл) и охлаждали до 0°C. Добавляли триэтиламин (8,67 мл, 62 ммоль) с последующим добавлением по каплям 4-иодбензоил хлорида (13,8 г, 52 ммоль), растворенного в CH2Cl2 (10 мл). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 72 часов. Реакционную смесь выливали в воду (200 мл) и CH2Cl2 слой отделяли, сушили (Na2SO4) и концентрировали. Полученное масло помещали в EtOH (200 мл) и обрабатывали гидразином (4,88 мл, 155 ммоль) при 0°C. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 17 часов. Смесь концентрировали и полученное вещество растирали с EtOAc, получая 9,52 г (43%) белого твердого вещества. ТСХ (диоксид кремния, 10% ацетон/CH2Cl2): Rf=0,18. Масс-спектр (электрораспыление): m/z 426,0 (426,1 вычислено для C17H20IN3O2 [M+H]+). 1H ЯМР (400 МГц, CDCl3): 7,74 (ушир. с, 2H), 7,31 (ушир. д, J=8,0 Гц, 2H), 4,63 (ушир. с, 2H), 3,73 (ушир. с, 2H), 2,77 (ушир. с, 2H), 1,49 (с, 9H).
B. трет-Бутиловый эфир 3-(4-иодфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
Карбонат цезия (1,84 г, 5,65 ммоль) добавляли к раствору эпихлоргидрина (3,68 мл, 47,05 ммоль) и трет-бутилового эфира 3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (2,0 г, 4,71 ммоль) в ДМФ (10 мл). Реакционную смесь оставляли перемешиваться в течение 24 часов, затем распределяли между водным NaHCO3 и EtOAc. Водный слой экстрагировали EtOAc и объединенные органические слои промывали водой и насыщенным раствором соли, сушили (Na2SO4) и концентрировали. Очистка колоночной хроматографией (диоксид кремния, 0-10% ацетон/CH2Cl2) давала 2,26 г (69%) белого вспененного вещества. ТСХ (диоксид кремния, 10% ацетон/CH2Cl2): Rf=0,44. Масс-спектр (электрораспыление): m/z 482,0 (482,1 вычислено для C20H24IN3O3, [M+H]+). 1H ЯМР (400 МГц, CDCl3): 7,60 (ушир. с, 2H), 7,28 (ушир. д, J=8,2 Гц, 2H), 4,48 (ушир. с, 2H), 4,32 (ушир. д, J=14,8 Гц, 1H), 3,99 (дд, J=15,0, 5,4 Гц, 1H), 3,61 (ушир. с, 1H), 3,26-3,20 (м, 1H), 2,72 (т, J=4,4 Гц, 1H), 2,65-2,58 (м, 2H), 2,40 (ушир. с, 1H), 1,36 (с, 9H).
C. трет-Бутиловый эфир 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты.
Гидрат трифторметансульфоната иттербия (III) (0,193 г, 0,311 ммоль) и 1-(2-цианофенил)пиперазин (0,292 г, 1,56 ммоль) растворяли в CH2Cl2 (2 мл) и добавляли к раствору трет-бутилового эфира 3-(4-иодфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты в CH2Cl2 (5 мл). Реакционную смесь оставляли перемешиваться в течение 48 часов при 25°C. Очистка флэш-хроматографией (диоксид кремния, 0-15% ацетон/CH2Cl2) давала 392 мг (56%) белого вспененного вещества. ТСХ (диоксид кремния, 10% ацетон/CH2Cl2): Rf=0,41. Масс-спектр (электрораспыление): m/z 669,2 (669,2 вычислено для C31H37IN6O3 [M+H]+). 1H ЯМР (400 МГц, CDCl3): 7,73 (ушир. с, 2H), 7,58-7,56 (м, 1H), 7,52-7,48 (м, 1H), 7,39 (ушир. д, J=7,1 Гц, 2H), 7,04-7,00 (м, 2H), 4,60 (ушир. с, 2H), 4,06-4,04 (м, 2H), 4,06-4,04 (м, 1H), 3,76-3,70 (м, 2H), 3,26 (ушир. с, 4H), 2,84-2,38 (м, 7H), 1,56-1,53 (м, 2H), 1,48(с,9H).
ПРИМЕР 10

Амид 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
A. 2-(4-{2-Гидрокси-3-[3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрил.
Трифторуксусную кислоту (3 мл) добавляли к раствору трет-бутилового эфира 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (0,402 г, 0,601 ммоль) в CH2Cl2 (3 мл) и реакционную смесь перемешивали в течение 2 часов. Смесь концентрировали, затем разбавляли EtOAc. Органический слой промывали водным NaHCO3 и насыщенным раствором соли, сушили (Na2SO4) и концентрировали, получая амин (0,342 г, 100%) в виде желтоватого вспененного вещества. ТСХ (диоксид кремния, 10% ацетон/CH2Cl2): Rf=0,14. Масс-спектр (электрораспыление): m/z 569,2 (569,1, вычислено для C26Н29IN6O, [M+H]+). 1H ЯМР (400 МГц, CDCl3:CD3OD(6:1)): 7,73 (д, J=8,6 Гц, 2H), 7,56 (дд, J=7,6, 1,8 Гц, 1H), 7,52 (т, J=8,0 Гц, 1H), 7,25 (д, J=8,6 Гц, 2H), 7,09 (т, J=7,6 Гц, 1H), 7,02 (дд, J=8,4 Гц, 1H), 4,43-4,36 (м, 1H), 4,31 (с, 2H), 4,21 (дд, J=14,1, 4,5 Гц, 1H), 4,11 (дд, J=14,5, 6,3 Гц, 1H), 3,54-3,49 (м, 2H), 3,40-3,24 (м, 8H), 3,18-3,06 (м, 3H), 3,03-2,95 (м, 3H).
B. Амид 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты.
Диизопропилэтиламин (0,531 мл, 3,05 ммоль), DMAP (5 мг) и триметилсилилизоцианат (0,413 мл, 3,05 ммоль) добавляли к раствору 2-(4-{2-гидрокси-3-[3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрила в пиридине (3 мл) и CH2Cl2 (6 мл). Реакционную смесь перемешивали в течение 20 часов, затем распределяли между водным NaHCO3 и CH2Cl2. Содержащий CH2Cl2 слой промывали насыщенным раствором соли, сушили (Na2SO4) и концентрировали. Полученный продукт растворяли в CH2Cl2 (5 мл) и обрабатывали 21 вес.% этоксидом натрия в EtOH (0,5 мл) в течение 3 часов. Реакционную смесь промывали насыщенным раствором соли, сушили (Na2SO4) и концентрировали. Очистка колоночной хроматографией (диоксид кремния, 0-10% MeOH/CH2Cl2) давала 290 мг (78%) указанного в заголовке соединения. ВЭЖХ (условия обращенной фазы), tR=4,21 мин. Масс-спектр (электрораспыление): m/z 612,2 (612,5, вычислено для C27Н30IN7О2, M++H). 1H ЯМР (400 МГц, CDCl3): 7,73 (д, J=8,6 Гц, 2H), 7,57 (дд, J=7,6, 1,6 Гц, 1H), 7,50 (т, J=7,8 Гц, 1H), 7,36 (д, J=8,6 Гц, 2H), 7,05 (т, J=7,6 Гц, 1H), 7,00 (д, J=8,4 Гц, 1H), 4,64 (ушир. с, 2H), 4,57 (ушир. с, 2H), 4,30 (ушир. с, 1H), 4,20 (дд, J=14,1, 3,3 Гц, 1H), 4,06 (дд, J=14,1, 6,3 Гц, 1H), 3,82-3,65 (м, 2H), 3,29-3,20 (м, 4H), 3,04-2,80 (м, 6H), 2,68 (ушир. с, 2H).
ПРИМЕР 11
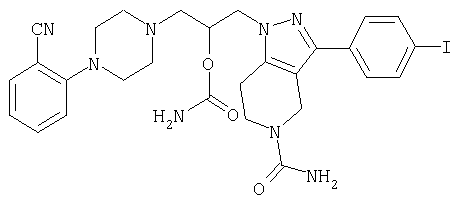
1-[5-Карбамоил-3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-илметил]-2-[4-(2-цианофенил)пиперазин-1-ил]этиловый эфир карбаминовой кислоты
Указанное в заголовке соединение (13 мг, 3%) получали вместе с 1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислотой, как описано в примере 10. Масс-спектр (электрораспыление): m/z 655,2 (655,2, вычислено для C28Н31IN8О3, [M+H]+). ВЭЖХ (условия обращенной фазы): tR=6,29 мин. 1H ЯМР (400 МГц, CDCl3): 7,69 (д, J=8,1 Гц, 2H), 7,50 (д, J=7,52, 1H), 7,43 (т, J=8,1 Гц, 1H), 7,31 (д, J=8,1 Гц, 2H), 6,96 (т, J=9,0 Гц, 2H), 4,64 (ушир. с, 2H), 4,08 (д, J=16,8 Гц, 2H), 3,96 (дд, J=14,0, 6,6 Гц, 1H), 3,80-3,69 (м, 2H), 3,10-2,80 (м, 4H), 2,66 (ушир. с, 2H), 2,50 (ушир. с, 2H).
ПРИМЕР 12
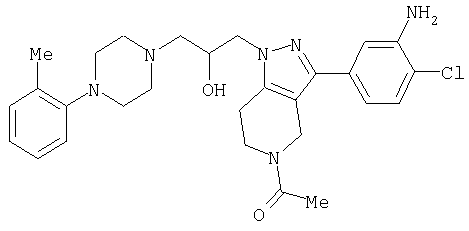
1-{3-(3-Амино-4-хлорфенил)-1-[2-гидрокси-3-(4-o-толил-пиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон
A. 1-[3-(4-Хлор-3-нитрофенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
В колбу, оборудованную ловушкой Дина-Старка, загружали N-ацетил-4-пиперидон (27,29 г, 137 ммоль), пиперидин (16,5 мл, 129 ммоль), п-толуолсульфоновую кислоту (0,5 г) и бензол (150 мл). Смесь нагревали до 125°C. Через 8 часов смесь оставляли охлаждаться и концентрировали в вакууме, получая соответствующий енамин (35 г). Раствор енамина (3,87 г, 20,0 ммоль) в дихлорметане (24 мл) обрабатывали триэтиламином (3,07 мл, 22,0 ммоль) и 4-хлор-3-нитробензоил хлоридом (4,84 г, 22,0 ммоль). Реакционную смесь перемешивали при 0°C в течение 1 часа и затем при комнатной температуре в течение 16 часов. К реакционной смеси добавляли гидразин (1,88 мл, 60 ммоль). Данный раствор перемешивали при комнатной температуре дополнительно в течение 16 часов. Растворители удаляли при пониженном давлении. К остатку для образования суспензии добавляли этилацетат (100 мл). Данную суспензию фильтровали и сушили, получая 6,4 г (100%) желтого твердого вещества. Масс-спектр (электрораспыление): m/z 321,0 (321,0, вычислено для C14H13ClN4O3, [M+H]+). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 8,10-8,00 (м, 3H), 4,90 (с, 0,8H), 4,85 (с, 1,2H), 3,96 (м, 2H), 2,95 (м, 2H), 2,20 (с,3H).
B. 1-[3-(4-Хлор-3-нитрофенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон.
Раствор 1-[3-(4-хлор-3-нитрофенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (6,4 г, 20,0 ммоль) в ДМФ (60 мл) обрабатывали карбонатом цезия (13,0 г, 40 ммоль) и эпихлоргидрином (15,6 мл, 200,0 ммоль) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре дополнительно в течение 24 часов перед разбавлением этилацетатом (350 мл) и водой (50 мл). Органический слой отделяли, промывали водой (2×50 мл), насыщенным раствором соли (50 мл), сушили над сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией (диоксид кремния, 10% ацетон/CH2Cl2), получая 7,5 г (83%) светло-желтого порошка. Масс-спектр (электрораспыление): m/z 377,0 (377,0, вычислено для C17H17ClN4O4, [M+H]+). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 8,15-8,05 (м, 1H), 7,75-7,65 (м, 1H), 7,55-7,45 (м, 1H), 4,80-4,65 (м, 1,2H), 4,60 (с, 0,8H), 4,45-4,35 (м, 1H), 4,08-4,02 (м, 1H), 3,92-3,80 (м, 1H), 3,70-3,63 (м, 1H), 3,30-3,20 (м, 1H), 2,90-2,67 (м, 3H), 2,55-2,48 (м, 1H), 2,15 (с, 1,7H), 2,10 (с, 1,3H).
C. 1-{3-(4-Хлор-3-нитрофенил)-1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон
Раствор 1-[3-(4-хлор-3-нитрофенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (0,754 г, 2,0 ммоль) в дихлорметане (10 мл) обрабатывали трифлатом иттербия(III) (0,25 г, 0,40 ммоль) и 1-(2-метилфенил)пиперазином (0,705 г, 4,0 ммоль) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 16 часов и разбавляли дихлорметаном (100 мл) и водой (50 мл). Органический слой отделяли, промывали водой (2×50 мл), сушили над сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией (диоксид кремния, 5% MeOH/CH2Cl2), получая 0,98 г (90%) целевого продукта в виде светло-желтого твердого вещества. Масс-спектр (электрораспыление): m/z 553,2 (553,2, вычислено для C28Н33ClN6O4, [M+H]+). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 8,25-8,15 (м, 1H), 7,75-7,70 (м, 1H), 7,63-7,55 (м, 1H), 7,20-7,10(м, 2H), 7,05-6,95 (м, 2H), 4,90-4,70 (м, 1H), 4,65 (с, 1H), 4,30-4,15 (м, 2H), 4,10-3,70 (м, 4H), 3,00-2,40 (м, 12H), 2,20(с, 3H), 2,15 (с, 1,5H), 2,10 (с, 1,5H).
D. 1-{3-[3-Амино-4-хлорфенил)-1-[2-гидрокси-3-(4-o-толилпиперизин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон.
К раствору гидросульфита натрия (1,28 г, 7,3 ммоль) в 30 мл воды добавляли 1-{3-(4-хлор-3-нитрофенил)-1-[2-гидрокси-3-(4-o-толилпиперазин-1-ил)пропил]-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил}этанон (810 мг, 1,5 ммоль) в 15 мл ТГФ. Реакционную смесь перемешивали при комнатной температуре в течение 5 минут. Цвет раствора изменялся от светло-желтого до бесцветного. Раствор хлористого водорода (1н., 10 мл) добавляли к реакционной смеси. Этот раствор перемешивали при комнатной температуре в течение 30 минут и обрабатывали насыщенным раствором бикарбоната натрия до тех пор, пока рН раствора не достигало величины от 7 до 8. Продукт экстрагировали дихлорметаном (3×80 мл). Органические фазы объединяли, сушили над сульфатом натрия и концентрировали при пониженном давлении, получая остаток. Этот остаток очищали колоночной хроматографией (диоксид кремния, 5-20% MeOH/CH2Cl2), получая 644 мг (84,1%) указанного в заголовке соединения. Масс-спектр (электрораспыление): m/z 523,3 (523,3, вычислено для C28H35ClN6O2, [M+H]+). 1H ЯМР (CDCl3, 400 МГц, смесь двух ротамеров): 7,30-6,70 (м, 7H), 4,80-4,60 (м, 1H), 4,55 (с, 1H), 4,20-4,05 (м, 4H), 3,95-3,90 (м, 2H), 3,80-3,60 (м, 2H), 2,90-2,30 (м, 9H), 2,20 (с, 3H), 2,15 (с, 1,5H), 2,10 (с, 1,5H).
ПРИМЕР 13

(R)-1-(3-(4-Бромфенил)-1-{3-[4-(5-хлор-2-метилфенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон.
A. (2S)-1-трет-Бутилдиметилсилилглицидол.
К охлажденному до 0°C раствору R-(+)-глицидола (3,88 г, 52,4 ммоль) в CH2Cl2 (100 мл) добавляли трет-бутилхлордиметилсилан (9,41 г, 62,4 ммоль), после чего Et3N (13,5 мл, 96,8 ммоль). Раствор оставляли нагреваться до 23°C, при перемешивании в течение 17 часов. Полученный розовый раствор разбавляли Et2O (250 мл) и перемешивали дополнительно в течение 30 минут. Раствор распределяли между Et2O (800 мл) и насыщенным водным раствором NaHCO3 (200 мл). Содержащий Et2O слой промывали насыщенным водным раствором NaHCO3 (250 мл), H2O (3 × 200 мл), насыщенным раствором соли (100 мл), сушили над Na2SO4 и концентрировали. Очистка остатка колоночной хроматографией (диоксид кремния, 5-10% Et2O/гексаны) давало 8,21 г (84%) указанного в заголовке соединения. ТСХ (диоксид кремния, 10% Et2О/гексаны): Rf=0,5. 1H ЯМР (CDCl3, 400 МГц): 3,85 (дд, J=11,9, 3,2 Гц, 1H), 3,66 (дд, J=11,9, 4,8 Гц, 1H), 3,09 (м, 1H), 2,77 (дд, J=5,0, 4,2 Гц, 1H), 2,64 (дд, J=5,2, 2,7 Гц, 1H), 0,90 (с, 9H), 0,08 (с, 3H), 0,07 (с, 3H).
B. 1-[3-(4-Бромфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
В колбу, оборудованную ловушкой Дина-Старка, загружали N-ацетил-4-пиперидон (100,1 г, 709 ммоль), пиперидин (68 мл, 779 ммоль), п-TsOH (3,7 г) и бензол (500 мл). Смесь нагревали до 125°C. Через 17 часов смесь оставляли охлаждаться и делили на две порции. К охлажденному до 0°C раствору енамина (примерно 355 ммоль) в CH2Cl2 (320 мл) в течение 15 часов добавляли по каплям раствор п-бромбензоил хлорида (70,0 г, 319 ммоль) в CH2Cl2 (400 мл). Смесь затем оставляли нагреваться до 23°C и перемешивали дополнительно в течение 5 ч. Раствор обрабатывали 1н. HCl (500 мл) и интенсивно перемешивали в течение 1,5 часов. Слои отделяли и водный слой экстрагировали CH2Cl2 (2×300 мл). Объединенные экстракты промывали насыщенным водным раствором NaHCO3 (300 мл), H2O (300 мл), насыщенным раствором соли (300 мл), сушили над Na2SO4 и концентрировали. Остаток растворяли в MeOH (300 мл) и обрабатывали NH2NH2 (50,0 мл, 1,59 моль). Смесь перемешивали в течение 17 часов, после чего образовавшийся осадок собирали фильтрованием и сушили на воздухе, получая 52 г (50%) указанного в заголовке соединения, которое подходило для использования без дополнительной очистки. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): m/z вычислено для C14H16 79BrN3O [M+H]+, 320,04, найдено 320. 1H ЯМР (CD3OD/CDCl3, 400 МГц, смесь амидных ротамеров): 7,53 и 7,35 (A и B системы AA'BB', J=8,5 Гц, 2H), 7,51 и 7,39 (A и B системы AA'BB', J=8,6 Гц, 2H), 4,72 (с, 2H), 4,58 (с, 2H), 3,85 (т, J=5,9 Гц, 2H), 3,71 (т, J=5,8 Гц, 2H), 2,81 (т, J=5,8 Гц, 2H), 2,74 (т, J=5,8 Гц, 2H), 2,16 (с, 3H), 2,11 (с, 3H).
C. (S)-1-[3-(4-Бромфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Раствор KHMDS в толуоле (0,5 M, 3,7 мл, 1,85 ммоль) добавляли к 0°C раствору 1-[3-бромфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона (492 мг, 1,54 ммоль) в ДМФ (4,0 мл). Смесь перемешивали в течение 1 часа, после чего добавляли шприцом (2S)-1-трет-бутилдиметилсилилглицидол (870 мг, 4,62 ммоль). Смесь перемешивали дополнительно в течение 48 часов и распределяли между EtOAc (300 мл) и насыщенным водным NaHCO3 (100 мл). Водный слой экстрагировали EtOAc (2×100 мл). Объединенные экстракты промывали H2O (2×100 мл), насыщенным раствором соли (100 мл), сушили над Na2SO4 и концентрировали. Остаток растворяли в MeOH (50 мл) и обрабатывали CSA (97 мг). Смесь перемешивали в течение 17 часов и концентрировали досуха. Остаток суспендировали в MeC(OMe)3 (50 мл) и перемешивали дополнительно в течение 17 часов. Смесь разбавляли EtOAc (400 мл) и промывали насыщенным водным раствором NaHCO3 (50 мл), H2O (2×50 мл), насыщенным раствором соли (50 мл), сушили над Na2SO4 и концентрировали. Неочищенный сложный ортоэфир растворяли в CH2Cl2 (5 мл), охлаждали до 0°C и обрабатывали AcBr (0,18 мл, 2,4 ммоль). Смесь оставляли нагреваться при перемешивании в течение 4 часов перед обработкой, как описано выше. Неочищенный полученный ацетилбромид растворяли в MeOH (50 мл), обрабатывали K2CO3 (207 мг, 1,50 ммоль) и перемешивали в течение 4 часов. Реакционную смесь разбавляли EtOAc (400 мл) и промывали насыщенным водным раствором NH4Cl (100 мл). Содержащий EtOAc слой промывали H2O (2×100 мл), насыщенным раствором соли (100 мл), сушили над Na2SO4 и концентрировали. Неочищенный продукт очищали колоночной хроматографией (диоксид кремния, 10-40% ацетон/CH2Cl2), получая 158 мг (27%) указанного в заголовке соединения. Анализ хиральной ВЭЖХ (Daicel OD, 0,5% Et2NH/MeOH) показал >95% оптической чистоты. ВЭЖХ (условия обращенной фазы): tR=4,90 мин. Масс-спектр (электрораспыление): m/z вычислено для C17H19 79BrN3O2 [M++H], 376,07, найдено 376,0. 1H ЯМР (CDCl3, 400 МГц, смесь амидных ротамеров): 7,47 (д с небольшим расщеплением (частично нечеткий), J=8,5 Гц, 2H), 7,44 (м, 4H), 7,38 (д с небольшим расщеплением, J=8,5 Гц, 2H), 4,71 и 4,64 (A и B AB-квартета, Jab=15,7 Гц, 2H), 4,51 (с, 2H), 4,39 (дд, J=15,1, 2,5 Гц, 1H), 4,34 (дд, J=15,0, 2,9 Гц, 1H), 4,02 (дд, J=5,2, 3,9 Гц, 1H), 3,98 (дд, J=5,3, 3,7 Гц, 1H), 3,83 (м, 2H), 3,64 (м, 2H), 3,25 (ушир. м, 2H), 2,80-2,60 (м, 6H), 2,46 (дд, J=4,6, 2,6 Гц, 1H), 2,38 (дд, J=4,6, 2,6 Гц, 1H), 2,10 (с, 3H), 2,06 (с, 3H).
D. (R)-1-(3-(4-Бромфенил)-1-{3-[4-(5-хлор-2-метилфенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон.
(S)-1-[3-(4-Бромфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон (37 мг, 0,98 ммоль) и 4-(2-метил-5-хлорфенил)пиперазин (36 мг, 0,17 ммоль) объединяли в EtOH (0,4 мл) и нагревали до 70°C. Через 18 часов смесь оставляли охлаждаться, разбавляли CH2Cl2 и очищали препаративной ТСХ (диоксид кремния, 8% MeOH/CH2Cl2), получая 35 мг (61%) указанного в заголовке соединения. ВЭЖХ (условия обращенной фазы): tR=4,41 мин. Масс-спектр (электрораспыление): m/z вычислено для C28H34 35Cl79BrN6O2 [M++H], 586,16, найдено 586,2, 1H ЯМР (CDCl3, 400 МГц, смесь амидных ротамеров): 7,56 (д (частично нечеткий), J=8,5 Гц, 2H), 7,53 (с, 4H), 7,48 (д, J=8,5 Гц, 2H), 7,08 (ушир. д, J=8,5 Гц, 1H), 6,95 (м, 2H), 4,85 и 4,73 (A и B AB квартета, Jab=15,6 Гц, 1H), 4,62 (с, 1H), 4,20 (м, 2H), 4,04 (м, 2H), 3,90-3,71 (м, 2H), 2,92-2,53 (м, 11H), 2,21 (с, 1,5H), 2,16 (с, 1,5H).
ПРИМЕР 14
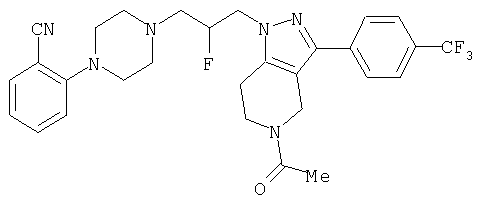
2-(4-{3-[5-Ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-фторпропил}пиперазин-1-ил)бензонитрил.
Раствор 2-(4-{3-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрила (150 мг, 0,27 ммоль) в CH2Cl2 (1 мл) обрабатывали DAST (Et2NSF3, 7 мкл, 0,60 ммоль) при -78°C. Реакционную смесь медленно нагревали до 25°C в течение 1 часа и затем до 60°C в течение дополнительных 2 часов. Препаративная ТСХ (диоксид кремния, 5% MeOH/CH2Cl2) давала 75 мг (50%) указанного в заголовке соединения в виде светло-желтого порошка. ТСХ (5% MeOH/CH2Cl2): Rf=0,28. Масс-спектр (электрораспыление): m/z 555,2 ([M+H]+, C29H30F4N6O вычислено 554,2). 1H ЯМР(CDCl3, 400 МГц, смесь двух ротамеров): 7,71 и 7,59 (АВ система, Jab=8,2 Гц, 2H), 7,66 и 7,62 (АВ система, Jab=8,4 Гц, 2H), 7,50-7,38 (м, 2H), 6,96-6,92 (м, 2H), 5,01 (дп, J=49,0, 3,0 Гц, 1H), 4,77 и 4,73 (АВ система, Jab=15,7 Гц, 1,1H), 4,59 (с, 0,9H), 4,41-4,18 (м, 2H), 3,95-3,80 (м, 1H), 3,69 (дд, J=5,5, 5,5 Гц, 1H), 3,18 (м, 4H), 2,83-2,65 (м, 8H), 2,14 (с, 1,6H), 2,10 (с, 1,4H).
ПРИМЕР 15
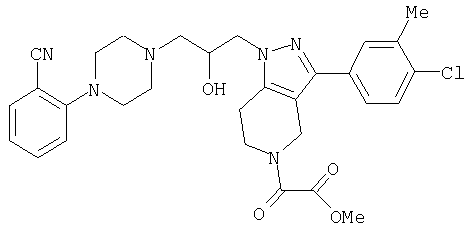
Метиловый эфир (3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)оксоуксусной кислоты
A. 4-Хлор-3-метилбензоилхлорид
К суспензии 52,55 г (0,31 моль) 4-хлор-3-метилбензойной кислоты в CH2Cl2 (1,2 л) с ДМФ (1 мл) при 0°C в атмосфере N2 с газовым выводом, барботируемым через 2,5н. раствор гидроксида натрия, добавляли 29,56 мл (0,339 моль) оксалилхлорида. Смесь оставляли нагреваться до комнатной температуры в течение 3 часов. Реакционную смесь концентрировали и использовали далее в неочищенном виде.
В. трет-Бутиловый эфир 3-(4-хлор-3-метилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
К перемешиваемому раствору 55,8 г (0,28 моль) трет-бутилового эфира 4-оксопиперидин-1-карбоновой кислоты и 25,7 г (0,29 моль) морфолина в бензоле (125 мл) добавляли каталитическое количество (˜0,25 г) п-толуолсульфоновой кислоты. Смесь кипятили с обратным холодильником в течение 10 часов с ловушкой Дина-Старка. Растворитель удаляли при пониженном давлении, получая коричневое масло. Неочищенный продукт разбавляли CH2Cl2 (400 мл) и добавляли 46,83 мл (0,34 моль) Et3N. Смесь охлаждали до 0°C и медленно добавляли через капельную воронку в течение 2 часов раствор 4-хлор-3-метилбензоилхлорида (0,35 моль) в CH2Cl2 (200 мл). Реакционную смесь выливали в воду (400 мл) и CH2Cl2 слой отделяли, сушили (Na2SO4) и концентрировали. Полученное масло помещали в EtOH (400 мл) и обрабатывали 35 мл гидразина при 0°C. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 17 часов, в течение данного времени происходило образование белого осадка. Объем реакционной смеси уменьшали до ˜150 мл и добавляли Et2O (750 мл). Суспензию интенсивно перемешивали в течение 2 часов и фильтровали, затем промывали Et2O (2×200 мл) и сушили в вакууме, получая 50,74 г (52% по 3 стадиям) трет-бутилового эфира 3-(4-хлор-3-метилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты в виде бледно-оранжевого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C18Н22ClN3О2, 347,1; m/z найдено, 348,1 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,26-7,43 (м, 4H), 4,65 (ушир. с, 2H), 3,73 (ушир. с, 2H), 2,77 (ушир. с, 2H), 2,34 (с, 3H), 1,49 (с, 9H).
C. трет-Бутиловый эфир 3-(4-хлор-3-метилфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
К раствору трет-бутилового эфира 3-(4-хлор-3-метилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (18,26 г, 53 ммоль) и эпихлоргидрина (41,12 мл, 526 ммоль) в ДМФ (100 мл) добавляли карбонат цезия (20,56 г, 63 ммоль). Реакционную смесь оставляли перемешиваться в течение 72 часов, разбавляли EtOAc (200 мл) и промывали насыщенным раствором NaHCO3 и насыщенным раствором соли. Органический слой сушили над Na2SO4, концентрировали и очищали колоночной хроматографией (диоксид кремния, 20% ацетон/CH2Cl2), получая трет-бутиловый эфир 3-(4-хлор-3-метилфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (12,0 г, 57%). ТСХ (диоксид кремния, 20% ацетон/CH2Cl2): Rf=0,68. Масс-спектр (электрораспыление) m/z 491,2 (491,2, вычислено для C27Н31ClN6O, [M+H]+). 1H ЯМР (400 МГц, CDCl3): 7,55 (с, 1H), 7,36 (м, 2H), 4,61 (м, 2H), 4,38-4,47 (м, 1H), 4,11 (дд, J=14,3, 5,7 Гц, 1H), 3,67-3,79 (м, 2H), 3,34 (м, 1H), 2,83 (т, J=4,5 Гц, 1H), 2,75 (м, 2H), 2,51 (м, 1H), 2,41 (с, 3H), 1,48 (с, 9H).
D. трет-Бутиловый эфир 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
трет-Бутиловый эфир 3-(4-хлор-3-метилфенил)-1-оксиранилметил-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (5,33 г, 13,2 ммоль) и 1-(2-цианофенил)пиперазин (2,97 г, 15,86 ммоль) частично растворяли в EtOH (50 мл) и триэтиламине (2 мл). Реакционную смесь нагревали при 80°C в течение 18 часов. Смесь концентрировали и очищали колоночной хроматографией (диоксид кремния, 20% ацетон/CH2Cl2), получая трет-бутиловый эфир 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (6,51 г, 83%) в виде желтого твердого вещества. ТСХ (диоксид кремния, 20% ацетон/CH2Cl2): Rf=0,35. Масс-спектр (электрораспыление): m/z 591.3 (591,3, вычислено для C32H39ClN6O3, [M+H]+).
E. 2-(4-{3-[3-(4-Хлор-3-метилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил
трет-Бутиловый эфир 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (1,26 г, 2,13 ммоль) растворяли в трифторуксусной кислоте (3 мл) и CH2Cl2 (3 мл) и оставляли перемешиваться в течение 2 часов. Реакционную смесь концентрировали, помещали в EtOAc (50 мл) и промывали водным раствором NaHCO3 (2×25 мл). Содержащий EtOAc слой сушили над Na2SO4 и концентрировали, получая 2-(4-{3-[3-(4-хлор-3-метилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил (1,05 г, 99%) в виде желтого вспененного вещества. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,27. Масс-спектр (электрораспыление): m/z 491,2 (491,2, вычислено для C27H31ClN6O, [M+H]+). 1H ЯМР (400 МГц, CDCl3): 9,8 (ушир. с, 1H), 7,55 (д, J=7,6 Гц, 1H), 7,50 (т, J=8,2 Гц, 1H), 7,38 (с, 1H), 7,31 (д, J=8,2 Гц, 1H), 7,20 (д, J=8,2 Гц, 1H), 7,11 (т, J=8,2 Гц, 1H), 6,98 (д, J=8,2 Гц, 1H), 4,56 (ушир. с, 1H), 4,12-4,32 (м, 4H), 2,98-3,51 (м, 13 H), 2,35 (с, 3H).
F. Метиловый эфир (3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)оксоуксусной кислоты
2-(4-{3-[3-(4-Хлор-3-метилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил)пиперазин-1-ил)бензонитрил (58 мг, 0,118 ммоль) растворяли в CH2Cl2 (0,59 мл) и обрабатывали метилхлороксоацетатом (16 мг, 0,129 ммоль). Реакционную смесь оставляли перемешиваться в течение 18 часов при комнатной температуре. Колоночная хроматография (диоксид кремния, 2-10% MeOH/CH2Cl2) давала метиловый эфир (3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)оксоуксусной кислоты (54 мг, 79%) в виде белого твердого вещества. Масс-спектр (электрораспыление): m/z 577,3 (577,2, вычислено для С30H33ClN6О4, [M+H]+). 1H ЯМР (400 МГц, CDCl3): 7,32-7,62 (м, 5H), 7,14 (т, J=7,6 Гц, 1H), 7,05 (д, J=8,2 Гц, 1H), 4,59-4,80 (м, 3H), 4,12-4,28 (м, 2H), 3,92 (с, 3H), 3,78-3,86 (м, 2H), 3,44-3,60 (м, 5H), 3,15-3,40 (м, 4H), 2,83-3,05 (м, 2H), 2,41 (с, 3H).
ПРИМЕР 16
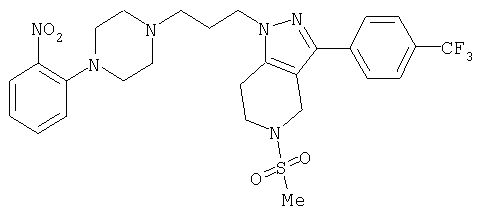
5-Метансульфонил-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
A. 1-Метансульфонилпиперидин-4-он
Карбонат калия (324 г, 2340 ммоль) добавляли к раствору моногидрата гидрохлорида 4-пиперидона (90 г, 586 ммоль) в хлороформе (300 мл) и воде (300 мл). Суспензию охлаждали до 0°C и обрабатывали метилсульфонилхлоридом (136 мл, 1760 моль), добавляя по каплям в течение 1 часа (наблюдали выделение газа). Реакционную смесь оставляли встряхиваться в течение 72 часов и распределяли между CH2Cl2 (500 мл) и насыщенным водным раствором NaHCO3 (500 мл). Водный слой экстрагировали CH2Cl2 (3×200 мл). Органический слой промывали 1% KHSO4 (250 мл), сушили (Na2SO4) и концентрировали, получая 90,5 г (87%) белого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C6H11NO3S, 177,1; m/z найдено, 178,1 [M+H]+. ВЭЖХ (условия обращенной фазы): tR=2,19 мин. 1H ЯМР (400 МГц, CDCl3): 3,60 (т, J=6,5 Гц, 4H), 2,89 (с, 3H), 2,59 (т, J=6,3 Гц, 4H).
B. 5-Метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
п-Толуолсульфоновую кислоту (1,34 г, 7,0 ммоль) и морфолин (25,83 мл, 296 ммоль) добавляли к раствору 1-метансульфонил-пиперидин-4-она (50,0 г, 282 ммоль) в бензоле (282 мл). Реакционную смесь нагревали в колбе, оборудованной обратным холодильником и ловушкой Дина-Старка, при кипячении с обратным холодильником в течение 15 часов. Реакционную смесь охлаждали и концентрировали в вакууме, получая енамин, который использовали без дополнительной очистки. Енамин растворяли в CH2Cl2 (200 мл) и охлаждали до 0°C. К нему добавляли триэтиламин (47,2 мл, 339 ммоль) с последующим добавлением по каплям 4-трифторметилбензоилхлорида (42,3 мл, 285 ммоль), растворенного в CH2Cl2 (82 мл). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 20 часов. Реакционную смесь промывали 1н. водной HCl (250 мл) и содержащий CH2Cl2 слой отделяли, сушили (Na2SO4) и концентрировали. Полученное масло помещали в EtOH (300 мл) и обрабатывали гидразином (44,3 мл, 1,41 моль) при 0°C. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 24 часов. Смесь концентрировали и полученное твердое вещество фильтровали, промывая EtOH, и сушили в вакууме, получая 70 г (72%) 5-метансульфонил-3-(4-трифторметилфенил-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин в виде белого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C14H14F3N3O2S, 345,0; m/z найдено, 346,0 [M+H]+. ВЭЖХ (условия обращенной фазы): tR=6,33 мин. 1H ЯМР (400 МГц, CDCl3): 7,72 (с, 4H), 4,58 (с, 2H), 3,69 (т, J=5,7 Гц, 2H), 2,99 (т, J=5,7 Гц, 2H), 2,92 (с, 3H).
C. 3-[5-Метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-1-ол
Cs2CO3 (33,74 г, 103,5 ммоль) добавляли к раствору 5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридина (29,8 г, 86,3 ммоль) в безводном ДМФ (70 мл) и перемешивали в течение 25 минут. Добавляли 3-бром-1-пропанол (8,6 мл, 13,2 г, 94,9 ммоль) и перемешивали в атмосфере N2 при комнатной температуре в течение 18 часов. К реакционной смеси добавляли воду (500 мл) и перемешивали в течение 5 минут. Выпавшее в осадок вещество отфильтровывали и промывали водой (4×100 мл) и сушили с помощью сушки вымораживанием. Неочищенное вещество (31,0 г) помещали в безводный ДМФ (65 мл), добавляли Cs2CO3 (33,74 г, 103,5 ммоль) и перемешивали в течение 10 минут. Добавляли 3-бром-1-пропанол (8,6 мл, 13,2 г, 94,9 ммоль) и MeOH (6,0 мл, 4,75 г, 148 ммоль) и перемешивание продолжали в атмосфере N2 при комнатной температуре в течение 15 часов. К реакционной смеси добавляли воду (500 мл) и перемешивали в течение 10 минут. Выпавшее в осадок вещество отфильтровывали и промывали водой (3×100 мл). Осадок на фильтре растворяли в CH2Cl2 (200 мл) и промывали насыщенным раствором соли (50 мл), сушили (Na2SO4) и концентрировали. Твердое вещество растирали с Et2O (200 мл), отфильтровывали, промывали Et2O и сушили, получая 16,0 г целевого соединения. Маточный раствор хроматографировали (диоксид кремния, 0-10% ацетон/EtOAc), получая дополнительно 3,0 г указанного в заголовке соединения. Суммарный выход составлял 54,6%. Масс-спектр (электрораспыление): вычислено для C17H20F3N3О3S, 403,12; m/z найдено, 404,0 [M+H]+, 426,0 [M+Na]+. 1H ЯМР (400 МГц, CDCl3): 7,71 (д, J=8,2 Гц, 2H), 7,66 (д, J=8,5 Гц, 2H), 4,55 (с, 2H), 4,23 (т, J=6,5 Гц, 2H), 3,70-3,63 (м, 4H), 2,90 (с, 3H), 2,90 (т, J=5,1 Гц, 2H), 2,62 (т, J=5,9 Гц, 1H), 2,06 (кв, J=6,1 Гц, 2H).
D. 3-[5-Метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропиональдегид.
Периодинан Десса-Мартина (Dess-Martin) (3,45 г, 8,2 ммоль) добавляли к раствору 3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-1-ола (3,0 г, 7,4 ммоль) в CH2Cl2 (20 мл) при 0°C в атмосфере N2. Через 15 минут реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали еще в течение 1,5 часов. Реакционную смесь разбавляли Et2O (60 мл) и медленно добавляли 20% водного NaHCO3 (35 мл). Затем добавляли Na2S2O3 и перемешивали при комнатной температуре в течение 30 минут. Слои отделяли и водную часть экстрагировали Et2O (2×30 мл). Объединенные органические экстракты промывали насыщенным раствором соли, сушили (Na2SO4) и концентрировали. Жидкостная хроматография среднего давления (СДЖХ) (1-10% MeOH/CH2Cl2) давала 2,53 г целевого альдегида с 85% выходом. Масс-спектр (электрораспыление): вычислено для C17H18F3N3O3S, 401,11; m/z найдено, 402,1 [M+H], 434,1 [M+MeOH+H]. 1H ЯМР (400 МГц, CDCl3): 9,82 (с, 1H), 7,63 (д, J=8,4 Гц, 2H), 7,58 (д, J=8,4 Гц, 2H), 4,68 (с, 2H), 4,25 (т, J=6,1 Гц, 2H), 3,63 (т, J=5,8 Гц, 4H), 3,14 (т, J=6,1 Гц, 2H), 2,92 (т, J=5,8 Гц, 2H), 2,81 (с, 3H).
E. 5-Метансульфонил-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
К перемешиваемому раствору 3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропиональдегида (0,060 г, 0,15 ммоль) и 1-(2-нитрофенил)пиперазина (0,032 г, 0,157 ммоль) в CH2Cl2 (0,5 мл), добавляли ледяную AcOH (8,5 мкл, 0,15 ммоль) и перемешивали в течение 15 минут при комнатной температуре. Добавляли NaBH(OAc)3 (0,041 г, 0,19 ммоль) и перемешивали в атмосфере азота в течение ночи. Затем добавляли насыщенный раствор NaHCO3 (0,5 мл) и перемешивали в течение 15 минут. Слои разделяли и водный слой экстрагировали CH2Cl2 (0,5 мл). СДЖХ-очистка (диоксид кремния, 2-15% MeOH/CH2Cl2) давала целевой продукт в виде белого твердого вещества (0,063 г, 71%). ТСХ (диоксид кремния, 12% MeOH/CH2Cl2): Rf=0,67. Масс-спектр (электрораспыление): точная масса, вычисленная для C27H31F3N6O4S, 592,21; m/z найдено, 593,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,80 (дд, J=1,6, 8,2 Гц, 1H), 7,77 (д, J=8,3 Гц, 2H), 7,70 (д, J=8,3 Гц, 2H), 7,52 (ддд, J=1,6, 7,3, 8,3 Гц, 1H), 7,19 (дд, J=1,2, 8,3 Гц, 1H), 7,09 (м, 1H), 4,59 (с, 2H), 4,17 (т, J=6,9 Гц, 2H), 3,71 (т, J=5,8 Гц, 2H), 3,13 (ушир. т, J=4,8 Гц, 4H), 2,96 (т, J=5,6 Гц, 2H), 2,95 (с, 3H), 2,66 (ушир. т, J=4,4 Гц, 4H), 2,51 (т, J=7,0 Гц, 2H), 2,17 (кв, J=6,9 Гц, 2H).
ПРИМЕР 17
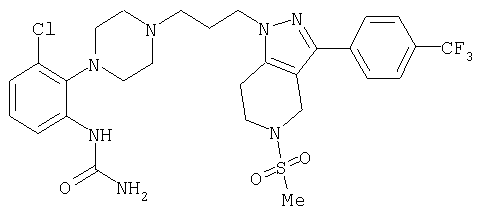
1-[3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]мочевина
A. трет-Бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 1,2-дихлор-3-нитробензола (0,96 г, 5,0 ммоль) и трет-бутилового эфира пиперазин-1-карбоновой кислоты (0,93 г, 5,0 ммоль) в ацетонитриле (5 мл) добавляли K2CO3 (1,38 г, 10 ммоль). Смесь кипятили с обратным холодильником в течение 48 часов. Растворитель удаляли при пониженном давлении. Неочищенное вещество распределяли между EtOAc (100 мл) и H2O (20 мл). Органический слой промывали H2O (2×20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-20% EtOAc/гексаны) давала трет-бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты (1,2 г, 70%). ТСХ (диоксид кремния, 20% EtOAc/гексаны): Rf=0,45. Масс-спектр (электрораспыление): точная масса, вычисленная для C15H20ClN3O4, 341,1; m/z найдено, 364,1 [M+Na]+. 1H ЯМР (400 МГц, CDCl3): 7,56 (дд, J=8,2, 1,4 Гц, 1H), 7,50 (дд, J=8,2, 1,4 Гц, 1H), 7,13 (т, J=8,2 Гц, 1H), 3,38-3,56 (м, 4H), 3,06 (м, 4H), 1,48 (с, 9H).
B. 1-(2-хлор-6-нитрофенил)пиперазин
трет-Бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты (1,87 г, 5,47 ммоль) растворяли в трифторуксусной кислоте (5,0 мл) и CH2Cl2 (5,0 мл) и оставляли перемешиваться в течение 2 часов. Реакционную смесь концентрировали, разбавляли EtOAc и промывали насыщенным водным раствором NaHCO3. Органический слой сушили над Na2SO4, концентрировали и очищали колоночной хроматографией (диоксид кремния, 100% CH2Cl2), получая 1-(2-хлор-6-нитрофенил)пиперазин (1,26 г, 95%). Масс-спектр (электрораспыление): точная масса, вычисленная для C10H12ClN3O2, 241,1; m/z найдено, 242,1 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,54 (дд, J=8,2, 1,6 Гц, 1H), 7,49 (дд, J=8,2, 1,6 Гц, 1H), 7,10 (т, J=8,2 Гц, 1H), 3,08 (ушир. с, 4H), 2,99 (ушир. с, 4H), 2,07-2,12 (м, 1H).
C. 1-{3-[4-(2-Хлор-6-нитрофенил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
К перемешиваемому раствору 3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропиональдегида (0,5 г, 1,25 ммоль) и 1-(2-хлор-6-нитрофенил)пиперазина (0,301 г, 1,25 ммоль) в CH2Cl2 (6 мл) добавляли сульфат натрия (0,354 г, 2,50 ммоль) и триацетоксиборгидрид натрия (0,396 г, 1,87 ммоль). Смесь оставляли перемешиваться при комнатной температуре в течение ночи. Смесь разбавляли CH2Cl2 и промывали водой. Содержащий CH2Cl2 слой сушили над Na2SO4 и растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией (диоксид кремния, 10% ацетон/CH2Cl2), получая 1-{3-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-1,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин (0,380 г, 49%). Масс-спектр (электрораспыление): точная масса, вычисленная для C27H30ClF3N6O4S, 626,2; m/z найдено, 627,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,73 (д, J=8,2 Гц, 2H), 7,66 (д, J=8,2 Гц, 2H), 7,54 (дд, J=8,2, 1,2 Гц, 1H), 7,49 (дд, J=8,2, 1,2 Гц, 1H), 7,10 (т, J=8,2 Гц, 1H), 4,58 (с, 2H), 4,13 (т, J=6,5 Гц, 2H), 3,71 (т, J=5,9 Гц, 2H), 3,01-3,11 (м, 4H), 2,95 (т, J=5,9 Гц, 2H), 2,92 (с, 3H), 2,42-2,53 (м, 4H), 2,40 (т, J=6,5 Гц, 2H), 2,12 (кв, J=6,5 Гц, 2H).
D. 3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фениламин
К перемешиваемому раствору 1-{3-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридина (0,153 г, 0,244 ммоль) в EtOH (2,44 мл) добавляли цинковую пыль (0,80 мг, 1,22 ммоль) и медленно добавляли уксусную кислоту (0,70 мл). Через 15 минут желтый раствор становился бесцветным и избыток цинковой пыли отфильтровывали через слой целита. Фильтрат концентрировали и остаток очищали колоночной хроматографией (диоксид кремния, 0-10% MeOH/CH2Cl2), получая 3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фениламин (0,146 г, 100%). Масс-спектр (электрораспыление): точная масса, вычисленная для C27H32ClF3N6О2S 596,2; m/z найдено, 597,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,73 (д, J=8,2 Гц, 2H), 7,66 (д, J=8,2 Гц, 2H), 6,88 (т, J=8,2 Гц, 1H). 6,63 (т, J=7,6 Гц, 2H), 4,55 (с, 2H), 4,36 (с, 2H), 4,15 (т, J=6,5 Гц, 2H), 3,60-3,70 (м, 4H), 2,97 (т, J=5,3 Гц, 2H), 2,90 (с, 3H), 2,83 (д, J=10,8 Гц, 2H), 2,74 (д, J=11,5 Гц, 2H), 2,37 (т, J=6,6 Гц, 2H), 2,11-2,20 (м, 4H).
E. 1-[3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]мочевина
К перемешиваемому раствору 3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фениламина (0,062 г, 0,104 ммоль) в CH2Cl2 (0,52 мл) добавляли триметилсилилизоцианат (0,017 мл, 0,125 ммоль). Реакционную смесь оставляли перемешиваться в течение 48 часов при комнатной температуре. Реакция не завершилась, поэтому дополнительно добавляли 0,017 мл (0,125 ммоль) триметилсилилизоцианата и реакционную смесь нагревали при 45°C в течение 10 часов. Колоночная хроматография (диоксид кремния, 3-10% MeOH/CH2Cl2) давала 1-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]мочевину (0,015 г, 22%). Масс-спектр (электрораспыление): точная масса, вычисленная для C28H33ClF3N7O3S, 639,2; m/z найдено, 640,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 8,26 (ушир. с, 1H), 8,05 (д, J=8,2 Гц, 1H), 7,73 (д, J=8,2 Гц, 2H), 7,66 (д, J=8,2 Гц, 2H), 7,09 (т, J=8,2 Гц, 1H), 6,92 (д, J=8,2 Гц, 1H), 4,65 (с, 2H), 4,55 (с, 2H), 4,15 (т, J=6,7 Гц, 2H), 3,65-3,73 (м, 4H), 2,96 (т, J=5,6 Гц, 2H), 2,87-2,92 (м, 2H), 2,91 (с, 3H), 2,70 (д, J=11,4 Гц, 2H), 2,40 (т, J=6,7 Гц, 2H), 2,09-2,22 (м, 4H).
ПРИМЕР 18
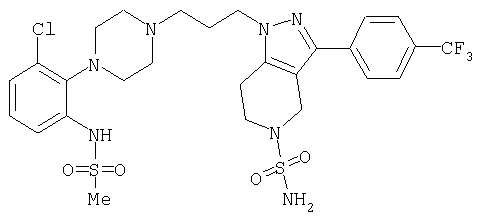
Амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-сульфоновой кислоты
A. трет-Бутиловый эфир 3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
К перемешиваемому раствору 500 г (2,51 моль) трет-бутоксикарбонил-4-пиперидона и 87,1 г (2,76 моль) морфолина в бензоле (1,25 л) добавляли каталитическое количество (˜0,25 г) п-TsOH. Смесь кипятили с обратным холодильником в течение 36 часов с ловушкой Дина-Старка. Половину растворителя удаляли при пониженном давлении и полученный раствор охлаждали и фильтровали. Затем фильтрат концентрировали, получая 630 г (94%) оранжево-красного масла. Енамин делили и 320 г (1,19 моль) разбавляли CH2Cl2 (1,0 л) и добавляли 165,0 мл (1,19 моль) Et3N. Смесь охлаждали до 0°C и медленно добавляли с использованием капельной воронки в течение 1 часа раствор 225 г (1,08 моль) 4-трифторметилбензоилхлорида в CH2Cl2 (0,5 л). Смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь затем разбавляли 1н. HCl (450 мл) и перемешивали интенсивно в течение 3 часов. Водный слой экстрагировали CH2Cl2 (3×500 мл) и объединенные экстракты сушили над Na2SO4 и растворитель удаляли при пониженном давлении. Неочищенное масло разбавляли EtOH (1 л) и охлаждали до 0°C. К данному перемешиваемому раствору медленно добавляли 115 г (3,57 моль) гидразина и смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи, за это время образовывался белый осадок. Объем реакционной смеси уменьшали до ˜500 мл и охлаждали. Осадок собирали, получая 285 г (72% из енамина) белого твердого вещества. 1H ЯМР (400 МГц, CDCl3): 7,63-7,55 (м, 4H), 4,58 (ушир. с, 2H), 3,69-3,62 (ушир. м, 2H), 2,74-2,68 (ушир. м, 2H), 1,47 (с, 9H).
B. трет-Бутиловый эфир 1-(2-метоксикарбонилэтил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
трет-Бутиловый эфир 3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (1,85 г, 5,04 ммоль) и метилакрилат (0,50 мл, 5,6 ммоль) объединяли в толуоле (30 мл) и нагревали до 75°C. Полученную смесь обрабатывали t-BuONa (100 мг) и нагревание продолжали в течение 48 часов. Смесь оставляли охлаждаться и распределяли между EtOAc (300 мл) и NaHCO3 (75 мл). Водный слой экстрагировали EtOAc (3×75 мл). Объединенные экстракты сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 30-60% EtOAc/гексаны) давала 343 мг (15%) указанного в заголовке соединения. ТСХ (диоксид кремния, 50% EtOAc/гексаны): Rf=0,4. Масс-спектр (электрораспыление): m/z вычислено для C22H27F3N3O4 [M++H] 454,20, найдено 454,1, 1H ЯМР (CDCl3, 400 МГц): 7,75 (ушир. д, J=8,1 Гц, 2H), 7,64 (ушир. с, 2H), 4,63 (ушир. с, 2H), 4,30 (т, J=6,6 Гц, 2H), 3,75 (ушир. с, 2H), 3,68 (с, 3H), 2,98 (т, J=6,6 Гц, 2H), 2,79 (ушир. т, J=5,6 Гц, 2H), 1,48 (с, 9H).
C. трет-Бутиловый эфир 1-(3-гидроксипропил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
Раствор LiBH4 (26 мг, 1,2 ммоль) в ТГФ (0,5 мл) добавляли к охлажденному до 0°C раствору трет-бутилового эфира 1-(2-метоксикарбонилэтил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (317 мг, 0,70 ммоль) в ТГФ (4,0 мл). Смесь перемешивали в течение 5 минут, затем дополнительно добавляли LiBH4 (15 мг) и перемешивание продолжали в течение 17 часов. Смесь распределяли между EtOAc (80 мл) и насыщенным водным раствором NaHCO3 (20 мл). Водный слой экстрагировали EtOAc (2×20 мл). Объединенные экстракты сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 0-8% MeOH/CH2Cl2) давала 268 мг (95%) указанного в заголовке соединения. ВЭЖХ (условия обращенной фазы), tR=6,82 мин. Масс-спектр (электрораспыление): m/z вычислено для C21H26F3N3O3 [M++Na] 448,18, найдено 448,10, 1H ЯМР (CDCl3, 400 МГц): 7,73 (ушир. д, J=8,2 Гц, 2H), 7,65 (ушир. с, 2H), 4,64 (ушир. с, 2H), 4,21 (т, J=6,4 Гц, 2H), 3,76 (ушир. с, 2H), 3,66 (т, J=5,7 Гц, 2H), 2,73 (ушир. т, J=5,4 Гц, 2H), 2,04 (кв, J=6,1, 2H), 1,48 (с, 9H).
D. трет-Бутиловый эфир 1-(3-оксопропил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
Периодинан Десса-Мартина (1,43 г, 3,36 ммоль) добавляли порциями к перемешиваемому раствору трет-бутилового эфира 1-(3-гидроксипропил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (1,30 г, 3,05 ммоль) в CH2Cl2 (15 мл) при 0°C в атмосфере N2. Затем реакционную смесь перемешивали при 0°C в течение 15 минут и оставляли нагреваться до комнатной температуры. После перемешивания при комнатной температуре в течение 1,5 часов реакционную смесь разбавляли Et2O (50 мл) и медленно добавляли насыщенный раствор NaHCO3 (15 мл) (Осторожно! Выделение газа). Затем добавляли Na2S2O3 .5H2O (5,31 г, 21,4 ммоль) и перемешивали в течение 30 минут. Слои отделяли и водный слой экстрагировали Et2O (2×30 мл). Объединенные экстракты промывали насыщенным раствором соли, сушили (Na2SO4) и концентрировали. СДЖХ (1-10% MeOH/CH2Cl2) давала альдегид с выходом 79% (1,02 г). ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,67. Масс-спектр (электрораспыление) вычислено для C21H24F3N3O3, 424,2 ([M+H]+), m/z найдено, 424,2, 1H ЯМР (400 МГц, CDCl3): 9,82 (с, 1H), 7,65 (ушир. д, J=8,0 Гц, 2H), 7,54 (ушир. с, 2H), 4,53 (с, 2H), 4,21 (т, J=6,2 Гц, 2H), 3,68 (ушир. с, 2H), 3,04 (т, J=6,2 Гц, 2H), 2,70 (т, J=5,6 Гц, 2H), 1,39(с, 9H).
E. трет-Бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 0,96 г (5,0 ммоль) 1,2-дихлор-3-нитробензола и 0,93 г (5,0 ммоль, 1 эквив.) 1-трет-бутилоксикарбонилпиперазина в ацетонитриле (5 мл) добавляли 1,38 г (10 ммоль, 2 эквив.) K2CO3. Смесь кипятили с обратным холодильником в течение 48 часов. Растворитель удаляли при пониженном давлении. Неочищенный продукт распределяли между EtOAc (100 мл) и 20 мл H2O. Органический слой промывали H2O (2×20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-20% EtOAc/гексаны) давала 1,2 г (70%) трет-бутилового эфира 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты. ТСХ (диоксид кремния, 20% EtOAc/гексаны): Rf=0,45. 1H ЯМР (400 МГц, CDCl3): 7,56 (дд, J=8,2, 1,4 Гц, 1H), 7,50 (дд, J=8,2, 1,4 Гц, 1H), 7,13 (т, J=8,2 Гц, 1H), 3,56-3,38 (м, 4H), 3,10-3,00 (м, 4H), 1,48 (с, 9H).
F. трет-Бутиловый эфир 1-{3-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
трет-Бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты (940 мг, 2,75 ммоль) в 10 мл CH2Cl2 обрабатывали 5 мл трифторуксусной кислоты и перемешивали при 25°C в течение 1 часа. Летучие компоненты затем удаляли. Остаток помещали в CH2Cl2 (60 мл) и KOH (4н., 20 мл). Органический слой отделяли, сушили над Na2SO4 и концентрировали. Желтое масло растворяли в CH2Cl2 и добавляли к 996 мг (2,35 ммоль) трет-бутилового эфира 1-(3-оксопропил)-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты. Желтый раствор обрабатывали ледяной уксусной кислотой (0,8 мл, 6 экв.) и перемешивали при 25°C в течение 1 часа. Добавляли NaBH(OAc)3 (1,5 г, 7,05 ммоль) и перемешивали в атмосфере азота в течение 2 часов. Затем добавляли насыщенный раствор NaHCO3 (20 мл), перемешивали в течение 30 минут и слои отделяли. Органический экстракт промывали насыщенным раствором соли, сушили над Na2SO4 и концентрировали при пониженном давлении. Колоночная хроматография (диоксид кремния, 2-5% MeOH/CH2Cl2) давала трет-бутиловый эфир 1-{3-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты в виде белого твердого вещества (1,40 г, 92%). ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): точная масса, вычисленная для C31H36ClF3N6О4, 648,24; m/z найдено 649,3 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,69 (д, J=8,2 Гц, 1H), 7,60-7,50 (м, 1H), 7,45-7,37 (м, 4H), 7,02 (т, J=8,2 Гц, 1H), 4,58 (ушир. с, 2H), 4,04 (т, J=6,7 Гц, 2H), 3,73-3,65 (м, 2H), 3,05-2,95 (м, 4H), 2,71 (т, J=5,6 Гц, 2H), 2,50-2,35 (м, 4H), 2,30 (т, J=6,8 Гц, 2H), 2,05-1,95 (м,2H), 1,41 (с, 9H).
G. 1-{3-[4-(2-Амино-6-хлорфенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
Раствор 360 мг (0,56 ммоль) трет-бутилового эфира 1-{3-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты в 4 мл MeOH обрабатывали 182 мг (5 экв.) цинковой пыли и ледяной уксусной кислотой (1,57 мл, 50 экв.) при 25°C. Реакционную смесь перемешивали при 25°C в течение 1 часа. Реакционную смесь затем фильтровали через слой целита и концентрировали, получая густое масло. Остаток помещали в CH2Cl2 (50 мл) и насыщенный раствор NaHCO3 (20 мл). Органический слой отделяли, промывали H2О (2×10 мл), сушили над Na2SO4 и концентрировали, получая трет-бутиловый эфир 1-{3-[4-(2-амино-6-хлорфенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): точная масса, вычисленная для C31H38ClF3N6O2, 618,27; m/z найдено, 619,3 [M+H]+.
H. трет-Бутиловый эфир 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7--тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
Раствор трет-бутилового эфира 1-{3-[4-(2-амино-6-хлорфенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты (257 мг, 0,42 ммоль) в 4 мл CH2Cl2 обрабатывали 32 л (0,42 ммоль, 1,0 экв.) метансульфонилхлорида и 116 л (0,83 ммоль, 2 экв.) триэтиламина и реакционную смесь перемешивали при 25°C в течение 1 часа. Добавляли EtOAc (40 мл) и насыщенный раствор NaHCO3 (20 мл). Органический слой отделяли и промывали H2O (20 мл), насыщенным раствором соли (20 мл), сушили над Na2SO4 и концентрировали, получая неочищенный трет-бутиловый эфир 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты. ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): точная масса, вычисленная для С32Н40ClF3N6O4S, 696,25; m/z найдено, 697,2 [M+H]+.
I. Амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-трет-бутоксикарбонилсульфоновой кислоты
Раствор 97 мг (0,14 ммоль) трет-бутилового эфира 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты в 3 мл CH2Cl2 обрабатывали 1,5 мл трифторуксусной кислоты. Реакционную смесь перемешивали при 25°C в течение 1 часа, после чего удаляли все летучие компоненты. К этому неочищенному веществу в 0,5 мл CH2Cl2 добавляли по каплям предварительно смешанный раствор хлорсульфонилизоцианата (18 мкл, 0,209 ммоль) и 2-метил-2-пропанола (20 мкл, 0,209 ммоль) в CH2Cl2 (0,150 мл). Реакционную смесь оставляли перемешиваться при 25°C в течение ночи. Препаративная ТСХ (диоксид кремния, 2-10% MeOH/CH2Cl2) давала указанное в заголовке соединение (84 мг, 78%). ТСХ (диоксид кремния, 10% MeOH/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): точная масса, вычисленная для C32H41ClF3N7O6S2, 775,22; m/z найдено, 776,2 [M+H]+
J. Амид 1-{3-[4-(2-Хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-сульфоновой кислоты
Амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-трет-бутоксикарбонилсульфоновой кислоты (84 мг, 0,11 ммоль) растворяли в трифторуксусной кислоте (0,75 мл) и CH2Cl2 (0,75 мл). Реакционную смесь оставляли перемешиваться при 25°C в течение 2 часов. Удаление летучих компонентов в токе азота давало амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-сульфоновой кислоты с количественным выходом в виде соли трифторуксусной кислоты. Масс-спектр (электрораспыление): точная масса, вычисленная для C27H33ClF3N4S2, 675,17; m/z найдено, 676,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,73 и 7,63 (АВ система, J=8,2 Гц, 4H), 7,37 (д, J=7,8 Гц, 1H), 7,13 (т, J=7,8 Гц, 1H), 7,04 (д, J=7,8 Гц, 1H), 4,32 (с, 2H), 4,20 (т, J=6,3 Гц, 2H), 3,87-3,80 (м, 2H), 3,80-3,75 (м, 4H), 3,70-3,25 (м, 7H), 3,00-2,75 (м, 4H), 2,25-2,15 (м, 2H).
ПРИМЕР 19

N-[3-Хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]метансульфонамид
A. 5-Метансульфонил-1-оксиранилметил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
5-Метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин (10,0 г, 29,0 ммоль) и эпихлоргидрин (24 мл, 307 ммоль) оставляли перемешиваться в ДМФ (150 мл), содержащем Cs2CO3 (10,4 г, 31,9 ммоль). После перемешивания при комнатной температуре в течение 4 дней смесь упаривали, помещали в EtOAc и промывали водой. Органическую часть сушили (MgSO4) и упаривали, получая светло-желтое твердое вещество. Колоночная хроматография (диоксид кремния, 5% ацетон/CH2Cl2) давала 4,1 г (35%) белого твердого вещества. ТСХ (диоксид кремния, 5% ацетон/CH2Cl2): Rf=0,28. Масс-спектр (электрораспыление): точная масса, вычисленная для C17H18F3N3O3S, 401,10; m/z найдено, 402,1 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,84 (д, J=8,3 Гц, 2H), 7,79 (д, J=8,3 Гц, 2H), 4,70-4,62 (м, 3H), 4,25 (д, J=5,4 Гц, 1H), 3,90-3,70 (м, 2H), 3,47 (м, 1H), 3,10-2,9 (м, 6H), 2,65-2,60 (м, 1H).
B. трет-Бутиловый эфир 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 0,96 г (5,0 ммоль) 1,2-дихлор-3-нитробензола и 0,93 г (5,0 ммоль, 1 экв.) 1-трет-бутилоксикарбонилпиперазина в ацетонитриле (5 мл) добавляли 1,38 г (10 ммоль, 2 экв.) K2CO3. Смесь кипятили с обратным холодильником в течение 48 часов. Растворитель удаляли при пониженном давлении. Неочищенный продукт распределяли между EtOAc (100 мл) и 20 мл H2O. Органический слой промывали H2O (2×20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-20% EtOAc/гексаны) давала 1,2 г (70%) трет-бутилового эфира 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты. ТСХ (диоксид кремния, 20% EtOAc/гексаны): Rf=0,45. 1H ЯМР (400 МГц, CDCl3): 7,56 (дд, J=8,2, 1,4 Гц, 1H), 7,50 (дд, J=8,2, 1,4 Гц, 1H), 7,13 (т, J=8,2 Гц, 1H), 3,56-3,38 (м, 4H), 3,10-3,00 (м, 4H), 1,48 (с, 9H).
C. трет-Бутиловый эфир 4-(2-амино-6-хлорфенил)пиперазин-1-карбоновой кислоты
Раствор 342 мг (1 ммоль) трет-бутилового эфира 4-(2-хлор-6-нитрофенил)пиперазин-1-карбоновой кислоты в 5,0 мл MeOH обрабатывали 630 мг (10 ммоль, 10 экв.) формиата аммония и каталитическим количеством 10% Pd-C (34 мг). Реакционную смесь перемешивали при 65°C в течение 30 минут. Реакционную смесь затем фильтровали через слой целита и концентрировали, получая желтое твердое вещество. ТСХ (диоксид кремния, 5% ацетон/CH2Cl2): Rf=0,40. Масс-спектр (электрораспыление): точная масса, вычисленная для C15H22ClN3O2, 311,14; m/z найдено, 312,1 [M+H]+.
D. трет-Бутиловый эфир 4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-карбоновой кислоты
трет-Бутиловый эфир 4-(2-амино-6-хлорфенил)пиперазин-1-карбоновой кислоты (163 мг, 0,53 ммоль) в CH2Cl2 обрабатывали 62 л (0,80 ммоль, 1,5 экв.) метансульфонилхлорида и 148 л (1,06 ммоль, 2 экв.) триэтиламина и реакционную смесь перемешивали при 25°C в течение 1 часа. Добавляли EtOAc (40 мл) и насыщенный раствор NaHCO3 (20 мл). Органический слой отделяли и промывали H2O (20 мл), насыщенным раствором соли (20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 0-5% ацетон/CH2Cl2) давала 145 мг (70%) трет-бутилового эфира 4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-карбоновой кислоты. ТСХ (диоксид кремния, 5% ацетон/CH2Cl2): Rf=0,35. Масс-спектр (электрораспыление): точная масса, вычисленная для C16H24ClN3O4S, 389,12; m/z найдено, 388,1 (отрицательный). 1H ЯМР (400 МГц, CDCl3): 7,41 (дд, J=8,2, 1,6 Гц, 1H), 7,11 (т, J=8,2 Гц, 1H), 6,99 (дд, J=8,2, 1,6 Гц, 1H), 4,25-3,91 (м, 2H), 3,66-3,52 (м, 2H), 3,01 (с, 3H), 3,01-2,84 (м, 2H), 2,70-2,56 (м, 2H), 2,55-2,43 (м, 2H), 1,44 (с, 9H).
E. N-[3-Хлор-2-(4-(2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]метансульфонамид
трет-Бутиловый эфир 4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-карбоновой кислоты (145 мг, 0,37 ммоль) растворяли в 3 мл CH2Cl2 и обрабатывали 1,5 мл трифторуксусной кислоты. Реакционную смесь перемешивали при 25°C в течение 1 часа, после чего удаляли все летучие компоненты. Твердое вещество обрабатывали CH2Cl2 (20 мл) и водным KOH (4н., 10 мл). Органический слой отделяли, сушили над Na2SO4 и концентрировали. Неочищенное масло (90 мг) растворяли в абсолютном EtOH (1,0 мл) и обрабатывали 96 мг (0,24 ммоль) 5-метансульфонил-1-оксиранилметил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридина. Реакционную смесь кипятили с обратным холодильником при 85°C в течение 3 часов и затем растворитель удаляли. Колоночная хроматография (диоксид кремния, 0-5% MeOH/CH2Cl2) давала 138 мг (20% по 4 стадиям) N-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]метансульфонамид. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,45. Масс-спектр (электрораспыление): точная масса, вычисленная для C28H34ClF3N6O5S2, 690,17; m/z найдено, 691,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 8,28 (с, 1H), 7,65 и 7,59 (АВ система, J=8,4 Гц, 4H), 7,36 (д, J=8,1 Гц, 1H), 7,07 (т, J=8,2 Гц, 1H), 6,95 (д, J=8,2 Гц, 1H), 4,54-4,44 (м, 2H), 4,21-3,94 (м, 3H), 3,77-3,52 (м, 4H), 3,41 (м, 2H), 2,96 (с, 3H), 2,81 (с, 3H), 3,05-2,73 (м, 4H), 2,66-2,20 (м, 4H).
ПРИМЕР 20

1-[4-(2,6-Динитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол
A. трет-Бутиловый эфир 4-(2,6-динитрофенил)пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 1,01 г (5,0 ммоль) 1-хлор-2,6-динитробензола и 0,93 г (5,0 ммоль) 1-трет-бутилоксикарбонилпиперазина в ацетонитриле (5 мл) добавляли 1,38 г (10 ммоль) K2CO3, Смесь кипятили с обратным холодильником в течение 48 часов. Растворитель удаляли при пониженном давлении. Неочищенный продукт распределяли между EtOAc (100 мл) и 20 мл H2O. Органический слой промывали H2O (2×20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-20% EtOAc/гексаны) давала 1,31 г трет-бутилового эфира (85%) 4-(2,6-динитрофенил)пиперазин-1-карбоновой кислоты. ТСХ (диоксид кремния, 20% EtOAc/гексаны): Rf=0,35. 1H ЯМР (400 МГц, CDCl3): 7,75 (д, J=8,2 Гц, 2H), 7,25 (т, J=8,2 Гц, 1H), 3,30 (м, 4H), 2,95 (м, 2H), 1,44 (с, 9H).
B. 1-[4-(2,6-Динитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол
трет-Бутиловый эфир 4-(2,6-динитрофенил)пиперазин-1-карбоновой кислоты (220 мг, 0,63 ммоль) растворяли в 5,0 мл CH2Cl2 и обрабатывали 3,0 мл трифторуксусной кислоты. Реакционную смесь перемешивали при 25°C в течение 1 часа, после чего удаляли все летучие компоненты. Твердое вещество обрабатывали CH2Cl2 (20 мл) и водным KOH (4 N, 10 мл). Органический слой отделяли, сушили над Na2SO4 и концентрировали. Неочищенное масло (67 мг) растворяли в абсолютном EtOH (1,2 мл) и обрабатывали 141 мг (0,35 ммоль, 1,3 экв.) 5-метансульфонил-1-оксиранилметил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридина. Реакционную смесь кипятили с обратным холодильником при 85°C в течение 3 часов и затем растворитель удаляли. Очистка колоночной хроматографией (диоксид кремния, 10-20% ацетон/CH2Cl2) давала 150 мг (85%) 1-[4-(2,6-динитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ола. ТСХ (диоксид кремния, 10% ацетон/CH2Cl2): Rf=0,3. Масс-спектр (электрораспыление): точная масса, вычисленная для C27H30F3N7O7S, 653,19; m/z найдено, 654,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,71 (д, J=8,2 Гц, 2H), 7,64 и 7,58 (АВ система, J=8,4 Гц, 4H), 7,20 (т, J=8,2 Гц, 1H), 4,54 (с, 2H), 4,29-4,12 (м, 2H), 3,66 (т, J=5,3 Гц, 2H), 3,70-2,95 (м, 9H), 2,91 (с, 3H), 2,67-2,32 (м, 4H).
ПРИМЕР 21
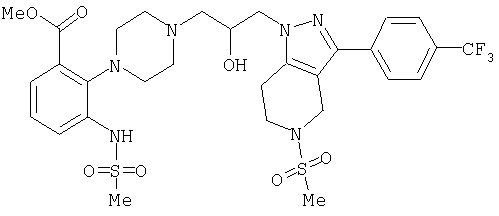
Метиловый эфир 2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)-3-метансульфониламинобензойной кислоты.
A. трет-Бутиловый эфир 4-(2-метоксикарбонил-6-нитрофенил)пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 736 мг (2,83 ммоль) этил 2-бром-3-нитробензоата и 579 мг (3,1 ммоль, 1,1 экв.) 1-трет-бутилоксикарбонилпиперазина в н-бутаноле (6 мл) добавляли 330 мг (3,1 ммоль, 1,1 экв.) Na2CO3. Смесь кипятили с обратным холодильником в течение 4 часов. Растворитель удаляли при пониженном давлении. Неочищенный продукт распределяли между EtOAc (100 мл) и 20 мл H2O. Органический слой промывали H2O (2×20 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-20% EtOAc/гексаны) давала 744 мг (72%) трет-бутилового эфира 4-(2-метоксикарбонил-6-нитрофенил)пиперазин-1-карбоновой кислоты. ТСХ (диоксид кремния, 20% EtOAc/гексаны): Rf=0,5. 1H ЯМР (400 МГц, CDCl3): 7,67 (дд, J=8,2, 1,4 Гц, 1H), 7,62 (дд, J=8,2, 1,4 Гц, 1H), 7,16 (т, J=8,2 Гц, 1H), 3,86 (с, 3H), 3,44-3,36 (м, 4H), 3,03-2,95 (м, 4H), 1,48 (с, 9H).
B. Метиловый эфир 2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)-3-метансульфониламинобензойной кислоты
Раствор 1,0 г (2,73 ммоль) трет-бутилового эфира 4-(2-метоксикарбонил-6-нитрофенил)пиперазин-1-карбоновой кислоты в 18 мл MeOH обрабатывали 893 мг (13,7 ммоль, 5 экв.) цинковой пыли и ледяной уксусной кислотой (8 мл). Реакционную смесь перемешивали при 25°C в течение 1 часа. Реакционную смесь затем фильтровали через слой целита и концентрировали, получая густое масло. Остаток помещали в EtOAc (200 мл) и насыщенный раствор NaHCO3 (100 мл). Органический слой отделяли, промывали H2O (2×50 мл), сушили над Na2SO4 и концентрировали. Колоночная хроматография (диоксид кремния, 10-30% EtOAc/гексаны) давала желаемый амин (844 мг, 92%). Амин (42 мг, 0,13 ммоль) в CH2Cl2 (0,5 мл) обрабатывали 9,7 мкл (0,13 ммоль, 1,0 экв.) метансульфонилхлорида и 34,9 мкл (0,25 ммоль, 2 экв.) триэтиламина и реакционную смесь перемешивали при 25°C в течение 1 часа. Добавляли EtOAc (20 мл) и насыщенный раствор NaHCO3 (10 мл). Органический слой отделяли и промывали H2O (10 мл), насыщенным раствором соли (20 мл), сушили над Na2SO4 и концентрировали. Неочищенное масло растворяли в 2 мл CH2Cl2 и обрабатывали 0,5 мл трифторуксусной кислоты. Реакционную смесь перемешивали при 25°C в течение 1 часа перед удалением всех летучих компонентов. Неочищенное масло растворяли в абсолютном EtOH (1,0 мл) и обрабатывали 40 мг (0,1 ммоль) 5-метансульфонил-1-оксиранилметил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридина и 200 мкл триэтиламина. Реакционную смесь кипятили с обратным холодильником при 85°C в течение 4 часов и затем растворитель удаляли. Препаративная ТСХ (диоксид кремния, 7% MeOH/CH2Cl2) давала 35 мг (49% по 3 стадиям) указанного в заголовке соединения. ТСХ (диоксид кремния, 5% MeOH/CH2Cl2): Rf=0,30. Масс-спектр (электрораспыление): точная масса, вычисленная для C30H37F3N6O7S2, 714,21; m/z найдено, 715,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 8,11 (с, 1H), 7,74-7,59 (м, 5H), 7,30 (д, J=8,1 Гц, 1H), 7,21 (т, J=8,2 Гц, 1H), 4,62-4,49 (м, 2H), 4,25-3,99 (м, 3H), 3,90 (с, 3H), 3,80-3,57 (м, 3H), 3,53-3,27 (м, 2H), 3,14-2,78 (м, 4H), 3,05 (с, 3H), 2,86 (с, 3H), 2,76-2,65 (м, 2H), 2,61-2,20 (м, 4H).
ПРИМЕР 22

1-{3-[4-(1,1-Диоксо-1H-1,6-бензо[d]изотиазол-3-ил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин.
A. 3-Пиперазин-1-ил-бензо[d]изотиазол 1,1-диоксид
POCl3 (10,2 мл, 109,2 ммоль) добавляли к сахарину (5,0 г, 27,3 ммоль) и нагревали при 120°C в течение 20 часов. Избыток реагента удаляли с использованием роторного испарителя и к остатку добавляли воду (50 мл) для образования осадка. Твердое вещество отфильтровали, промывали водой (2×20 мл) и сушили. Часть вышеуказанного неочищенного вещества (2,0 г, 9,95 ммоль) и пиперазина (4,28 г, 49,75 ммоль) помещали в диоксан (10 мл) и нагревали при 100°C в течение 24 часов. Реакционную смесь оставляли охлаждаться до комнатной температуры и выливали в ледяную воду (50 г) и нейтрализовали добавлением 10%-ного водного NaOH. Смесь экстрагировали CH2Cl2 (3×25 мл) и объединенные органические экстракты промывали насыщенным раствором соли, сушили (Na2SO4) и концентрировали. СДЖХ (диоксид кремния, 5-20% MeOH/CH2Cl2) давала производное пиперазинила (0,07 г, 4,2%). Масс-спектр (электрораспыление): точная масса, вычисленная для C11H13N3O2S, 251,07; m/z найдено, 252,1 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,72 (дд, J=0,8, 7,4 Гц, 1H), 7,64 (д, J=7,8 Гц, 1H), 7,49 (дт, J=0,8, 7,4 Гц, 1H), 7,43 (дт, J=1,2, 7,8 Гц, 1H), 3,80 (с, 4H), 2,85 (ушир. т, J=5,0 Гц, 4H), 2,07 (ушир. с, 1H). 13C ЯМР (100 МГц, CDCl3): 160,8, 145,3, 133,3, 133,0, 128,5, 125,9, 123,2, 49,8, 46,3.
B. 1-{3-[4-(1,1-Диоксо-1H-1,6-бензо[d]изотиазол-3-ил-пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
К перемешиваемому раствору 3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропиональдегида (0,040 г, 0,13 ммоль) и 1,1-диоксида 3-пиперазин-1-ил-бензо[d]изотиазола (0,050 г, 0,21 ммоль) в CH2Cl2 (0,5 мл) добавляли ледяную AcOH (12 мкл, 0,21 ммоль) и перемешивали в течение 15 минут при комнатной температуре. Добавляли NaBH(OAc)3 (0,058 г, 0,27 ммоль) и перемешивали в атмосфере азота в течение ночи. Затем добавляли насыщенный раствор NaHCO3 (0,5 мл) и перемешивали в течение 15 минут. Слои отделяли и водный слой экстрагировали CH2Cl2 (0,5 мл). СДЖХ (диоксид кремния, 2-15% MeOH/CH2Cl2) давала целевой продукт в виде белого твердого вещества (0,048 г, 76%). ТСХ (диоксид кремния, 12% MeOH/CH2Cl2): Rf=0,50. Масс-спектр (электрораспыление): точная масса, вычисленная для C28H31F3N6O4S2, 636,18; m/z найдено, 637,2 [M+H]+. 1H ЯМР (400 МГц, CDCl3): 7,94 (дд, J=0,8, 7,6 Гц, 1H), 7,86 (д, J=7,8 Гц, 1H), 7,75 (д, J=8,3 Гц, 2H), 7,73-7,63 (м, 2H), 7,68 (д, J=8,3 Гц, 2H), 4,57 (с, 2H), 4,17 (т, J=6,9 Гц, 2H), 4,04 (ушир. с, 4H), 3,69 (т, J=5,7 Гц, 2H), 2,94 (с, 3H), 2,92 (т, J=6,2 Гц, 2H), 2,62 (т, J=5,0 Гц, 4H), 2,44 (т, J=6,6 Гц, 2H), 2,13 (кв, J=6,6 Гц, 2H).
ПРИМЕР 23

1-[1-{3-[4-(6-хлорбензотиазол-2-ил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
A. 6-Хлор-2-пиперазин-1-ил-бензотиазол
К перемешиваемому раствору 1,07 г (5,24 ммоль) 2,6-дихлорбензотиазола в сухом ДМФ (25 мл) добавляли 2,4 г карбоната калия (15,7 ммоль) и 0,5 г пиперазина (5,8 ммоль). Смесь перемешивали при комнатной температуре в течение 4 часов. Когда реакция завершалась, реакционную смесь распределяли между EtOAc (150 мл) и водой (50 мл) и разделяли. Водный слой экстрагировали EtOAC (2×100 мл). Объединенные органические слои затем промывали водой (2×25 мл), насыщенным раствором соли, сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая 1,33 г (100%) целевого продукта в виде белого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C11H12ClN3S, 253,04; m/z найдено, 254,0 [M+H]+.
B. 1-[1-{3-[4-(6-Хлорбензотиазол-2-ил)пиперазин-1-ил]-2-гидроксипропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
К перемешиваемому раствору 144 мг (0,39 ммоль) 1-[1-оксиранилметил-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона в 4 мл EtOH добавляли 100 мг (0,39 ммоль) 6-хлор-2-пиперазин-1-ил-бензотиазола. Раствор нагревали при 60°C в течение ночи. Растворитель затем удаляли с использованием роторного испарения и неочищенный продукт очищали колоночной хроматографией (диоксид кремния, 0-10% MeOH/EtOAc), получая 220 мг (90%) белого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C29H30ClF3N6O2S: 618,18; m/z найдено, 619,2 [M+H]+. ВЭЖХ (условия обращенной фазы 40-90%): tR=8,27 мин. 1H ЯМР (CDCl3, 400 МГц, смесь амидных ротамеров): 7,70 (д, J=8,34 Гц, 1H), 7,62 (м, 2H), 7,57 (д, J=8,59 Гц, 1H), 7,48 (д, J=2,53 Гц, 1H), 7,36 (д, J=8,59 Гц, 1H), 7,16 (дд, J=8,59, 2,53 Гц, 1H), 4,80 и 4,68 (A и B AB квартета, J=15,92 Гц, 1H), 4,58 (с, 1H), 4,18-4,08 (м, 2H), 4,01-3,89 (м, 2H), 3,85-3,60 (м, 2H), 3,59-3,47 (м, 4H), 2,94-2,75 (м, 2H), 2,72-2,62 (м, 2H), 2,55-2,47 (м, 2H), 2,46-2,39 (м, 2H), 2,13 (с, 1,5H), 2,08 (с, 1,5H).
ПРИМЕР 24

1-[1-[3-(4-Бензо[d]изоксазол-3-ил-пиперазин-1-ил)-2-гидроксипропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
A. трет-Бутиловый эфир 4-бензо[d]изоксазол-3-ил-пиперазин-1-карбоновой кислоты
К перемешиваемому раствору 100 мг (0,65 ммоль) 3-хлор-1,2-бензизоксазола в пиридине (1 мл) добавляли 145 мг трет-бутилового эфира пиперазин-1-ил-карбоновой кислоты (0,78 ммоль) и 0,18 мл DBU (0,78 ммоль). Смесь перемешивали при 100°C в течение ночи, затем распределяли между EtOAC (50 мл) и водой (20 мл) и разделяли. Водный слой экстрагировали EtOAC (2×30 мл). Объединенные органические слои затем промывали водой (25 мл), насыщенным раствором соли, сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая неочищенный продукт. Очистка колоночной хроматографией (диоксид кремния, 60-100%CH2Cl2/гексаны) давала 82 мг (42%) целевого продукта в виде светло-желтого твердого вещества. Масс-спектр (электрораспыление): точная масса, вычисленная для C16H21N3O3, 303,16; m/z найдено, 326,1 [M+Na]+. 1H ЯМР (CDCl3, 400 МГц): 7,68 (дт, J=8,02, 0,98 Гц, 1H), 7,52-7,44 (м, 2H), 7,24 (ддд, J=8,42, 6,46, 1,57 Гц, 1H), 3,66-3,61 (м, 4H), 3,56-3,49 (м, 4H), 1,49 (с, 9H).
B. 1-[1-[3-(4-Бензо[d]изоксазол-3-ил-пиперазин-1-ил)-2-гидроксипропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанон
Раствор 82 мг (0,27 ммоль) трет-бутилового эфира 4-бензо[d]изоксазол-3-ил-пиперазин-1-карбоновой кислоты в 2 мл CH2Cl2 обрабатывали трифторуксусной кислотой (0,5 мл) при комнатной температуре в течение ночи. Растворитель затем удаляли и неочищенный продукт растворяли в EtOH и перемешивали над 100 мг бикарбоната натрия в течение 1 часа, твердое вещество затем отфильтровывали и фильтрат концентрировали. Неочищенный пиперазин затем растворяли в 4 мл EtOH и обрабатывали 100 мг (0,27 ммоль) 1-[1-оксиранилметил-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил]этанона. Раствор нагревали при 60°C в течение ночи. Растворитель затем удаляли с использованием роторного испарителя и неочищенный продукт очищали колоночной хроматографией (диоксид кремния, 0-10% MeOH/EtOAc), получая 105 мг (68%) белого твердого вещества. Масс-спектр (электрораспыление), точная масса, вычисленная для C29H31F3N6O3, 568,24; m/z найдено, 569,2 [M+H]+. 1H ЯМР (CDCl3, 400 МГц, смесь амидных ротамеров): 7,77 (д, J=8,41 Гц, 1H), 7,69 (м, 2H), 7,67-7,62 (м, 2H), 7,50-7,44 (м, 1H), 7,45-7,42 (м, 1H), 7,23-7,18 (м, 1H), 4,93 (ушир. м, 1H), 4,87 и 4,75 (A и B AB квартета, J=15,65 Гц, 1H), 4,65 (ушир. с, 1H), 4,27-4,15 (м, 2,3H), 4,09-3,95 (м, 1,7H), 3,91-3,82 (м, 0,7H), 3,81-3,66 (м, 1,3H), 3,62-3,49 (м, 4H), 3,01-2,85 (м, 1,5H), 2,85-2,74 (м, 2,5H), 2,71-2,60 (м, 2H), 2,58-2,45 (м, 2H), 2,20 (с, 1,5H), 2,15 (с, 1,5Н).
ПРИМЕР 25

1-[4-(2-Амино-6-хлорфенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол
ПРИМЕР 26
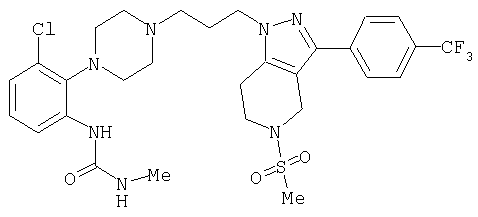
1-[3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]-3-метилмочевина
ПРИМЕР 27
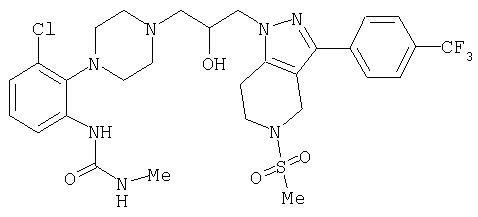
1-[3-Хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]-3-метилмочевина
ПРИМЕР 28

Метиловый эфир 3-амино-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензойной кислоты
ПРИМЕР 29

3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фениламин.
ПРИМЕР 30

1-[2-(4-{3-[3-(4-Бромфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)-3-хлорфенил]-3-метилмочевина.
ПРИМЕР 31

Амид 1-{3-[4-(2-хлор-6-метансульфониламинофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
ПРИМЕР 32

Метиловый эфир [3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]карбаминовой кислоты
ПРИМЕР 33
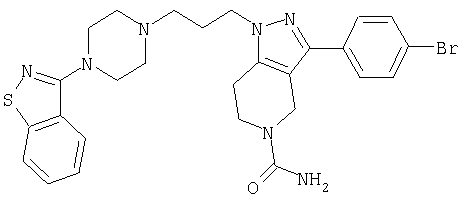
Амид 1-[3-(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)пропил]-3-(4-бромфенил)-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
ПРИМЕР 34
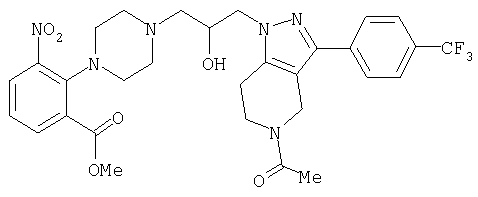
Метиловый эфир 2-(4-{3-[6-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)-3-нитробензойной кислоты
ПРИМЕР 35

1-[4-(2-Хлор-6-нитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропан-2-ол
ПРИМЕР 36
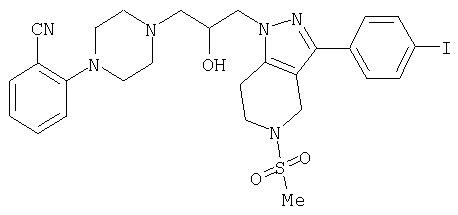
2-(4-{2-Гидрокси-3-[3-(4-иодфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрил.
ПРИМЕР 37
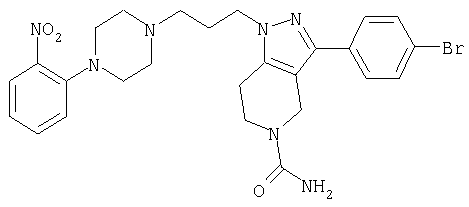
Амид 3-(4-бромфенил)-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
ПРИМЕР 38

2-(4-{3-[5-Ацетил-3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил
ПРИМЕР 39
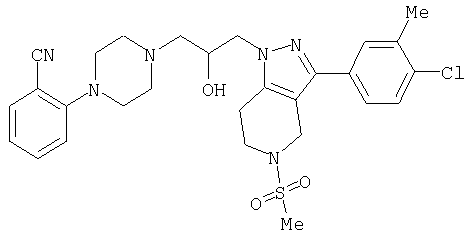
2-(4-{3-[3-(4-Хлор-3-метилфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрил
ПРИМЕР 40

1-(3-(4-Хлор-3-метилфенил)-1-{3-[4-(2,4-диметилфенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-ил)этанон
ПРИМЕР 41
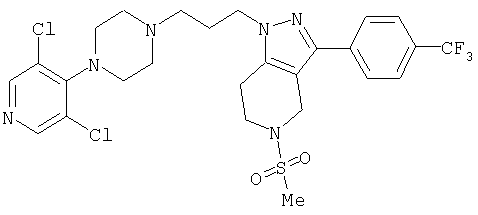
1-{3-[4-(3,5-Дихлорпиридин-4-ил)пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин
ПРИМЕР 42
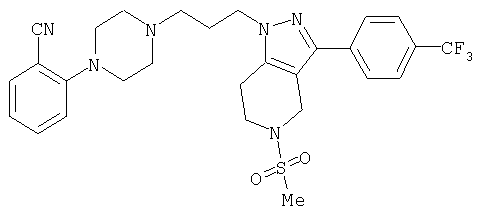
2-(4-{3-[5-Метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)бензонитрил
ПРИМЕР 43
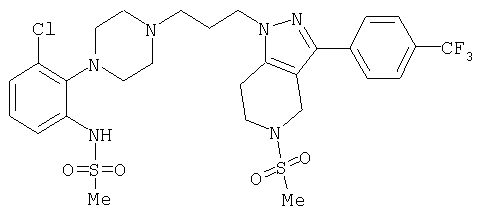
N-[3-Хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло[4,3-c]пиридин-1-ил]пропил}пиперазин-1-ил)фенил]метансульфонамид
ПРИМЕР 44
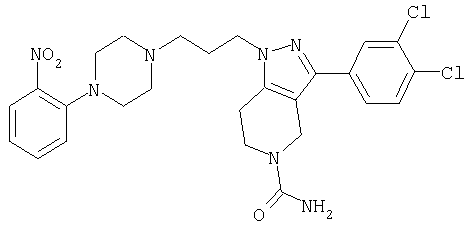
Амид 3-(3,4-дихлорфенил)-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
ПРИМЕР 45

Амид 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил}-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло[4,3-c]пиридин-5-карбоновой кислоты
ПРИМЕР 46
Анализ ингибирования катепсина S
Рекомбинантный катепсин S человека (CatS) экспрессировали в бакуловирусную систему и очищали в одну стадию с использованием колонки с тиопропилсефарозой. 10 л давало ˜700 мг CatS, и N-терминальное секвенирование (определение первичной структуры белка) подтверждало идентичность. Анализ проводили в 100 мМ растворе ацетата натрия рН 5,0, содержащем 1 мМ DTT и 100 мМ NaCl. Субстрат для анализа представлял собой
(Aedens)EKARVLAEAA(Dabcyl)K-амид
Km для субстрата составляет примерно 5 мкМ, но наличие субстратного ингибирования затрудняет кинетический анализ. При 20 мкМ субстрата скорость анализа является линейной в диапазоне 1-8 нг CatS в 100 мкл реакционной смеси. При использовании 2 нг/лунку CatS продуцирование продукта является линейным и дает ˜7-кратно усиленный сигнал через 20 минут при только 20%-ной потере субстрата. Первичные анализы проводят остановкой реакции через 20 минут 0,1% SDS, а затем измеряют флуоресценцию. Для других анализов измерения проводят каждую минуту в течение 20 минут. Скорость рассчитывают по наклону возрастания и исходя из этого рассчитывают процент ингибирования (смотри ниже таблицы 1 и 2)
ПРИМЕР 47
Ex vivo ингибирование аллергической ответной реакции ингибиторами катепсина S.
Следующий анализ показывает, что ингибиторы катепсина S блокируют ответную реакцию Т-клеток человека на неочищенные аллергеновые экстракты.
Материалы и методы
Реагенты: Глицеринированные неочищенные аллергеновые экстракты домашних пылевых клещей (Dermataphagoides pteronyssinus, Dermataphagoides farinae) и амброзии [Ambrosia trifida (гиганская), Ambrosia artemisiifolia (короткая)] получали из Hollister-Stier Laboratories (Minneapolis, MN). Конканавалин А (ConA) получали из Calbiochem (La Jolla, CA).
Доноры. Все аллергические доноры предварительно были обследованы на их специфические виды аллергии с использованием тестов RAST. Гаплоидные типы HLA класса II этих доноров определяли с использованием ПЦР.
Клеточная культура. Моноядерные клетки периферической крови человека (PBMC) очищали из образцов крови аллергических доноров с использованием градиента Ficoll-Hypaque с последующей промывкой забуференным фосфатом физиологическим раствором. РВМС культивировали в трехкратной или дупликатной последовательности из расчета 0,5-1,0×106 клеток/лунку вместе с титрованными дозами аллергеновых экстрактов в присутствии или в отсутствие известного ингибитора катепсина S, LHVS (морфолинмочевина-лейцин-гомо-фенилаланин-винилсульфонфенил) (Palmer et al. (1995), J.Med.Chem. 38:3193 и Riese et al. (1996), Immunity 4:357). Первоначально готовили серийно разведенные исходные растворы LHVS в 100% ДМСО, а затем разводили в соотношении 1:15 40% гидроксипропинилциклодекстрином (HPCD). Три микролитра LHVS в HPCD добавляли в РВМС культуры (200 мкл/лунку) Через 6 дней культивирования добавляли 1 мкКю/лунку 3Н-тимидина (TdR). Через 18 часов клетки собирали с помощью Filtermate Harvester (Packard) и подсчитывали введение 3Н-TdR на Topcount (Packard).
Ингибирование пролиферативных ответных реакций Т-клеток на домашних пылевых клещей
Примерно 10% большинства населения имеют аллергию на домашних пылевых клещей (HDM) видов Dermatophagoides, при этом Dermataphagoides pteronyssinus (Der p) и D. Farinae (Der f) являются двумя основными разновидностями, присутствующими в различных пропорциях в большинстве стран. Основными клиническими проявлениями являются астма и хронический ринит (насморк).
Действие ингибирования катепсина S на активацию HDM алллерген-специфических CD4 T-клеток было протестировано в ex vivo анализе пролиферации Т-клеток человека. Культивирование РВМС с неочищенными экстрактами либо Der p, либо Der f приводило к сильной пролиферации (фиг.1А). Такая пролиферация состояла в первую очередь из аллерген-специфических CD4 T клеток. Когда активность катепсина S блокировали специфическим ингибитором катепсина S LHVS (см. Riese et al. (1996), Immunity 4:357), пролиферация значительно ингибировалась (фиг.1В). Ингибирование LHVS было специфическим в отношении ответных реакций, индуцированных HDM экстрактами, поскольку пролиферативные ответные реакции Т-клетки, индуцированные ConA, пан-Т клеточным митогеном, не затрагивались. Кроме того, такое ингибирование наблюдалось для всех четырех исследованных HDM-аллергических доноров вне зависимости от различных гаплоидных типов HLA класса II (DR4; DR7, 15; DR11, 15 и Dr4,11).
Такая система очень похожа на ситуацию in vivo. Аллергический субъект будет подвергаться действию неочищенной смеси аллергенов, что будет приводить к пролиферации Т-клеток и аллергической ответной реакции. Наблюдение ингибирования активации CD4 Т-клеток под действием ингибитора катепсина S показывает, что такие ингибиторы могут быть эффективными при лечении обобщенной популяции пациентов, склонных к аллергии на домашних пылевых клещей.
Ингибирование пролиферативных ответных реакций Т-клеток на амброзию
Примерно 10% населения США склонно к аллергии на пыльцу амброзии, что приводит к тому, что она является одним из наиболее важных аллергенов с точки зрения клинических заболеваний. Аллергены пыльцы представляют собой основную причину усиления насморка (ринита) и астмы у этой части населения.
Эффект ингибирования катепсина S на активацию аллерген-специфических к амброзии CD4 T-клеток было исследовано в ex vivo анализе пролиферации Т-клеток человека. Культивирование РВМС с неочищенными экстрактами как короткой, так и гигантской амброзии приводило к сильной пролиферации (фиг.2А). Такая пролиферация состояла в первую очередь из аллерген-специфических CD4 T-клеток. Когда активность катепсина S блокировали специфическим ингибитором катепсина S LHVS (см. Riese et al. (1996), Immunity 4:357), пролиферация значительно ингибировалась (фиг.2В). Ингибирование LHVS было специфическим в отношении ответных реакций, индуцированных амброзией, поскольку пролиферативные ответные реакции Т-клетки, индуцированные ConA, пан-Т клеточным митогеном, не затрагивались. Кроме того, такое ингибирование наблюдалось для двух исследованных имеющих аллергию к амброзии доноров вне зависимости от различных гаплоидных типов HLA класса II (DR7, 15 и Dr4,11).
Аналогичный эксперимент проводили с использованием двух дополнительных ингибиторов CatS, соединений приведенных выше примера 11 и примера 36, при этом результаты показаны на фиг.3А и фиг.3В соответственно.
Данная система очень похожа на ситуацию in vivo. Аллергический субъект будет подвергаться действию неочищенной смеси аллергенов, что будет приводить к пролиферации Т-клеток и аллергической ответной реакции. Наблюдение ингибирования активации CD4 Т-клеток под действием ингибитора катепсина S показывает, что такие ингибиторы могут быть эффективными при лечении обобщенной популяции пациентов, склонных к аллергии на амброзию.
Пример 48
Наблюдение ингибирования катепсина S в крови человека
Действие in vivo введения ингибиторов катепсина S в серии клинических испытаний можно наблюдать, измеряя накопление промежуточного продукта разложения инвариантной цепи (Ii), например, p10Ii фрагмента, в крови субъектов, получающих дозу вещества. После введения ингибитора катепсина в течение определенного периода времени, например, от 0,01 до 50 мг/кг/день для создания концентрации в крови в диапазоне от 1 нМ до 10 мкМ в течение 16-30 часов, кровь отбирают и очищают лейкоциты (WBC), например, с помощью лизиса эритроцитов или с помощью градиентного центрифугирования Ficoll-Hypaque. Затем получают цельные клеточные лизаты лейкоцитов и анализируют их с использованием Вестерн-блоттинг анализа или ELISA анализа. Для Вестерн-блоттинг анализа клеточные лизаты первоначально разделяют на SDS-PAGE гелях. После переноса на нитроцеллюлозную мембрану Ii и промежуточные продукты его разложения, включая р10Ii, могут быть обнаружены с использованием мышиного mAb против Ii, например, Pin1.1, или кроличьих поликлональных антител, специфических в отношении С-концевого фрагмента р10Ii или против полного фрагмента р10Ii. Для ELISA анализа можно использовать пару антител против Ii, включая Pin1.1 и поликлональное антитело кролика или мышиное моноклональное антитело, специфическое в отношении р10Ii. Тот же анализ также можно использовать для наблюдения действия ингибиторов катепсина S in vivo в исследованиях на животных, например на обезьянах, собаках, свиньях, кроликах, морских свинках и грызунах.
В настоящем примере РВМС из крови человека инкубировали с ингибитором катепсина S, LHVS (морфолинмочевина-лейцин-гомо-фенилаланин-винилсульфонфенил, также называемый N-[(1S)-3-метил-1-[[[(1S,2Е)-1-(2-фенилэтил)-3-(фенилсульфонил)-2-пропенил]амино]карбонил]бутил]-4-морфолинкарбоксамид. Это соединение описано в патенте США 5976858 и в публикации Palmer et al. (1995), J.Med.Chem. 38:3193 и Riese et al. (1996), Immunity 4:357. После инкубирования в течение 24 часов образцы исследовали с использованием стандартных протоколов SDS-PAGE, переносили на нитроцеллюлозные мембраны и зондировали антителом, которое распознает инвариантные цепи, включая р10Ii фрагмент. В присутствии LHVS наблюдался р10Ii фрагмент, представляющий собой блок, образующийся при разложении Ii вследствие ингибирования катепсина S.
ПРИМЕР 49
Наблюдение in vivo ингибирования аллергической ответной реакции ингибиторами катепсина S
Для демонстрации эффективности ингибиторов катепсина S при подавлении аллергических ответных реакций in vivo подверженным аллергии добровольцам вводили дозу ингибиторов катепсина при уровнях, при которых ингибируется разложение инвариантной цепи. Аллергены вводят подкожно и размеры кожных реакций определяют через 15 минут, 6 часов и 24 часа. Кожную биопсию проводят через 24 часа. Немедленная благополучие-и-сигнал ответная реакция не опосредуется Т-клеточным ответом, и не ожидалось, что на нее будут воздействовать ингибиторы катепсина S, тогда как индурация (уплотнение) в поздней фазе (заметная через 6 часов, более явная через 24 часа) характеризуется активацией и инфильтрацией CD4 Т-клеток (а также эозинофилов) и должна ингибироваться введением ингибиторов катепсина S. Кожную биопсию используют для определения клеточного состава в индурации и предполагают, что обработанные ингибитором катепсина S субъекты имеют меньшее число присутствующих активированных CD4 T клеток по сравнению с обработанными плацебо субъектами.
Ссылки на данные методики приведены в Eberlein-Konig et al. (1999) Clin.Exp.Allergy 29: 1641-1647 и Gaga et al. (1991) J.Immunol. 147:816-822.
В качестве контроля в эксперименте будут использоваться преднизон и циклоспорин А. Преднизон будет ингибировать как немедленную ответную реакцию, так и реакцию в поздней фазе, тогда как циклоспорин А будет ингибировать только ответную реакцию в поздней фазе.
F. Другие варианты осуществления изобретения
Отличительные признаки и преимущества изобретения очевидны для обычного специалиста в данной области. Основываясь на данном описании, включая «Краткое изложение сущности изобретения», подробное описание, предпосылки создания изобретения, примеры и формулу изобретения, обычный специалист в данной области будет способен произвести модификации и адаптации к различным условиям и применениям. Такие другие варианты осуществления изобретения также входят в объем данного изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ | 2001 |
|
RU2286343C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ И СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ КАТЕПСИНА S | 2001 |
|
RU2317988C2 |
| СПОСОБ ЛЕЧЕНИЯ АЛЛЕРГИЙ С ИСПОЛЬЗОВАНИЕМ ЗАМЕЩЕННЫХ ПИРАЗОЛОВ | 2001 |
|
RU2290179C2 |
| СПОСОБ ЛЕЧЕНИЯ АЛЛЕРГИИ С ИСПОЛЬЗОВАНИЕМ ЗАМЕЩЕННЫХ ПИРАЗОЛОВ | 2001 |
|
RU2259202C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ КАТЕПСИНА S | 2001 |
|
RU2278863C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ РАЦЕМИЧЕСКОГО АМИНОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА ИЛИ РАЦЕМИЧЕСКОГО АМИНОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОИЗОХИНОЛИНА, СПОСОБЫ ИХ РАЗДЕЛЕНИЯ И РАЦЕМИЗАЦИИ, СПОСОБ ПОЛУЧЕНИЯ КЕТОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА ИЛИ КЕТОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОИЗОХИНОЛИНА, СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРА КОНДЕНСИРОВАННОГО БИЦИКЛИЧЕСКОГО КОЛЬЦА, ЗАМЕЩЕННОГО ПЕРВИЧНЫМ АМИНОМ, ПРОИЗВОДНЫЕ 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА | 2002 |
|
RU2308451C2 |
| АЗЕТИДИНИЛДИАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ МОНОАЦИЛГЛИЦЕРИН-ЛИПАЗЫ | 2010 |
|
RU2569298C2 |
| ПРОИЗВОДНЫЕ И СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИЙ ГЕПАТИТА В | 2015 |
|
RU2742305C2 |
| НОВЫЕ СОЕДИНЕНИЯ, КОТОРЫЕ ЯВЛЯЮТСЯ ИНГИБИТОРАМИ ERK | 2013 |
|
RU2660429C2 |
| АЗЕТИДИНИЛДИАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ МОНОАЦИЛГЛИЦЕРИН-ЛИПАЗЫ | 2010 |
|
RU2549547C2 |

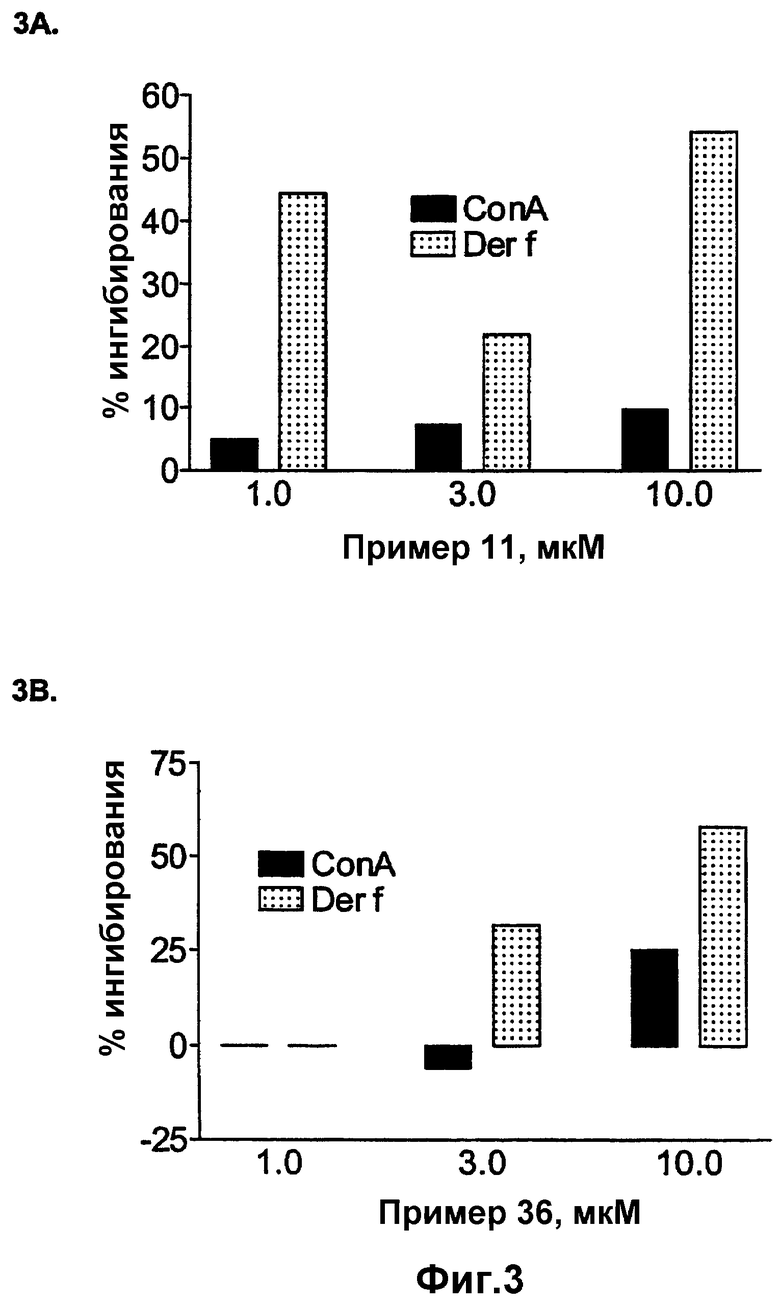
Изобретение относится к области медицины и касается способа лечения аллергии путем введения субъекту терапевтически эффективного количества фармацевтической композиции, включающей соединение формулы I. Изобретение обеспечивает повышенную эффективность лечения. 6 з.п. ф-лы, 3 ил.
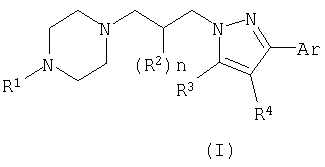
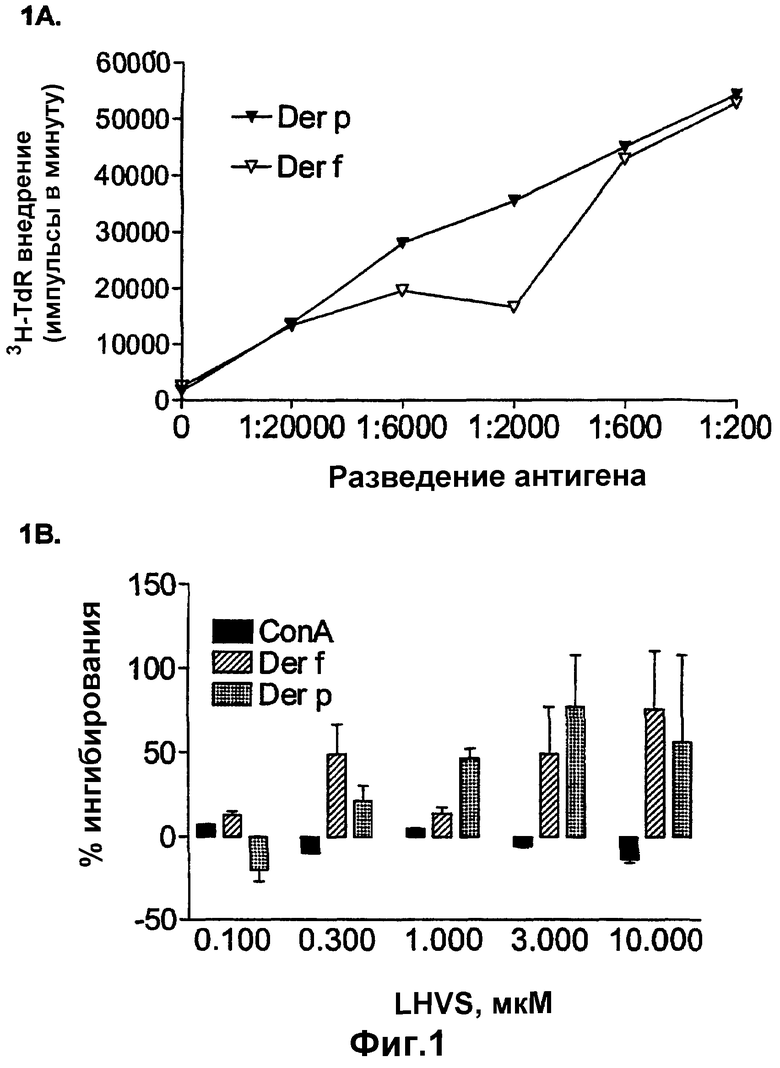
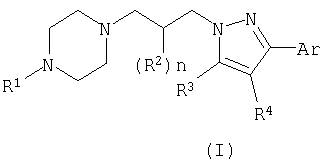
где R1 выбран из группы, включающей бензоизотиазолил, 1,1-диоксобензоизотиазолил, бензотиазолил, необязательно замещенный атомом хлора, бензоизоксазолил, а также шестичленное ароматическое карбоциклическое или азотсодержащее кольцо, которое может быть замещено по меньшей мере одной из групп, включающих Cl, F, СН3, ОН, CN, NO2, NH2, -NH-C(O)-NH2, -SO2, -NH-С(O)-NH-СН3, -С(O)O-СН3, -NH-SO2-CH3,-NH-C(O)O-CH3;
R2 выбран из группы, включающей ОН, -ОСН3, пиперазинилэтиламино, -O-C(O)-NH2, F;
n=0 или 1;
m=1 или 2;
R3 и R4 независимо означают водород или R3 и R4 вместе с пиразольным кольцом образуют азотсодержащее ненасыщенное или насыщенное шестичленное гетероциклическое кольцо, которое может быть замещено по атому азота группой -C(O)R5, -SO2-СН3 или -SO2-NH2, где
R5 означает СН3, -O-С(СН3)3, NH2, -СО(O)-СН3;
Ar означает шестичленное ароматическое кольцо, которое может быть замещено одним или несколькими заместителями, выбранными из Н, С1, NH2, СН3, I, CF3,
или его фармацевтически приемлемую соль.
1-[4-(2-амино-6-хлорфенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]пропан-2-ола;
1-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]пропил} пиперазин-1-ил)фенил]-3-метилмочевины;
1-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]пропил} пиперазин-1-ил)фенил]-3-метилмочевины;
метилового эфира 3-амино-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]пропил} пиперазин-1-ил) бензойной кислоты;
3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]пропил} пиперазин-1-ил)фениламина;
1-[2-(4-{3-[3-(4-бромфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]-2-гидроксипропил} пиперазин-1-ил)-3-хлорфенил]-3-метилмочевины;
и амида 1-{3-[4-(2-хлор-6-метансульфониламинофенил) пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-карбоновой кислоты.
метилового эфира [3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]-пиридин-1-ил]пропил} пиперазин-1-ил)фенил]карбаминовой кислоты;
амида 1-[3-(4-бензо[d]изотиазол-3-ил-пиперазин-1-ил)пропил]-3-(4-бромфенил)-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-карбоновой кислоты;
метилового эфира 2-(4-{3-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]-пиридин-1-ил]-2-гидроксипропил]пиперазин-1-ил)-3-нитробензойной кислоты;
1-[4-(2-хлор-6-нитрофенил)пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил] пропан-2-ола;
2-(4-{2-гидрокси-3-[3-(4-иодфенил)-5-метансульфонил-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил] пропил} пиперазин-1- ил) бензонитрила;
амида 3-(4-бромфенил)-1-{3-[4-(2-нитрофенил) пиперазин-1-ил] пропил}-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-карбоновой кислоты;
2-(4-{3-[5-ацетил-3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]-2- гидроксипропил]пиперазин-1-ил) бензонитрила;
2-(4-{3-[3-(4-хлор-3-метилфенил)-5-метансульфонил-4, 5,6,7 -тетрагидропиразоло [4,3-с]пиридин-1-ил]-2-гидроксипропил} пиперазин-1-ил) бензонитрила;
1-(3-(4-хлор-3-метилфенил)-1-{3-[4(2,4-диметилфенил)пиперазин-1 -ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил) этанона;
1-{3-[4-(3,5-дихлорпиридин-4-ил)пиперазин-1-ил]пропил]-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H-пиразоло [4,3-с]пиридина;
2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]пропил} пиперазин-1-ил)бензонитрила;
N-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил] пропил} пиперазин-1-ил)фенил]метансульфонамида;
амида 3-(3,4-дихлорфенил)-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]-пропил}-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-карбоновой кислоты;
и амида 3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил)пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-карбоновой кислоты.
1-(3-(4-хлорфенил)-1-{3-[4-(2-фторфенил)пиперазин-1-ил]пропил}-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил)этанона;
1-(3-(4-хлорфенил)-1-[2-гидрокси-3-(4-о-толилпиперазин-1-ил) пропил]-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-ил)этанона;
1-(3-(4-хлорфенил)-1-[2-метокси-3-(4-о-толилпиперазин-1-ил) пропил]-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил)этанона;
1-[1-{2-гидрокси-3-[4-(2-гидроксифенил)пиперазин-1-ил]пропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-ил]этанона;
1-[1-[2-гидрокси-3-(4-о-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил]этанона;
2-(4-{3-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]-2-гидроксипропил}пиперазин-1-ил)бензонитрила;
1-[3-(3,4- дихлорфенил) пиразол-1-ил]-3-(4-о-толилпиперазин-1-ил)пропан-2-ола;
1-[1-[2-(2-пиперазин-1-ил-этиламино)-3-(4-о-толилпиперазин-1-ил)пропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-ил] этанона;
трет-бутилового эфира 1-{3-[4-(2-цианофенил) пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-карбоновой кислоты;
амида 1-{3-[4-(2-цианофенил) пиперазин-1-ил]-2-гидроксипропил}-3-(4-иодфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-карбоновой кислоты;
1-[5-карбамоил-3-(4-иодфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-илметил]-2-[4-(2-цианофенил) пиперазин-1-ил] этилового эфира карбаминовой кислоты;
1-{3-(3-амино-4-хлорфенил)-1-[2-гидрокси-3-(4-о-толилпиперазин-1-ил) пропил]-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил}этанона;
(R)-1-(3-(4-бромфенил)-1-{3-[4-(5-хлор-2-метилфенил)пиперазин-1-ил]-2-гидроксипропил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-ил)этанона;
2-(4-{3-[5-ацетил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]-2-фторпропил] пиперазин-1-ил) бензонитрила;
метилового эфира (3-(4-хлор-3-метилфенил)-1-{3-[4-(2-цианофенил) пиперазин-1-ил]-2-гидроксипропил}-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил) оксоуксусной кислоты;
5-метансульфонил-1-{3-[4-(2-нитрофенил)пиперазин-1-ил]пропил}-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1H пиразоло [4,3-с] пиридина;
1-[3-хлор-2-(4-{3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил] пропил} пиперазин-1-ил)фенил] мочевины;
амида 1-{3-[4-(2-хлор-6-метансульфониламинофенил) пиперазин-1-ил]-пропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-сульфоновой кислоты;
N-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил] пропил} пиперазин-1-ил) фенил] метансульфонамида;
1-[4-(2,6-динитрофенил) пиперазин-1-ил]-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил]пропан-2-ола;
метилового эфира 2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с] пиридин-1-ил] пропил} пиперазин-1-ил)-3-метансульфониламинобензойной кислоты;
1-{3-[4-(1,1-диоксо-1Н-1,6-бензо[d] изотиазол-3-ил) пиперазин-1-ил]пропил}-5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидро-1Н-пиразоло [4,3-с] пиридина;
1-[1-{3-[4-(6-хлорбензотиазол-2-ил) пиперазин-1-ил]-2-гидроксипропил}-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил]этанона; и
1-[1-[3-(4-бензо [d]изоксазол-3-ил-пиперазин-1-ил)-2-гидроксипропил]-3-(4-трифторметилфенил)-1,4,6,7-тетрагидропиразоло [4,3-с] пиридин-5-ил]этанона.
N-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]-пиридин-1-ил]пропил}пиперазин-1-ил) фенил] метансульфонамида;
амида 1-[3-(4-бензо [d]изотиазол-3-ил-пиперазин-1-ил) пропил]-3-(4-бромфенил)-1,4,6,7-тетрагидропиразоло [4,3-с]пиридин-5-карбоновой кислоты; и
1-[3-хлор-2-(4-{2-гидрокси-3-[5-метансульфонил-3-(4-трифторметилфенил)-4,5,6,7-тетрагидропиразоло [4,3-с]пиридин-1-ил]пропил} пиперазин-1-ил) фенил]-3-метилмочевины.
| WO 9856785, A1, 17.12.1998 | |||
| ПИРАЗОЛОПИРИМИДИНОНОВЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1991 |
|
RU2114114C1 |
| US 4500525, А, 19.02.1985. | |||
Авторы
Даты
2006-06-20—Публикация
2001-09-05—Подача