Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения производных глютамата с использованием ферментативных реакций. Кроме того, настоящее изобретение относится к способу получения монатина, используемого в качестве подсластителя, из триптофана как одной из аминокислот, используемой в качестве исходного материала.
Предпосылки создания изобретения
4-(индол-3-илметил)-4-гидрокси-глютаминовая кислота (3-(1-амино-1,3-дикарбокси-3-гидрокси-бутан-4-ил)-индол) (обозначаемая далее как "монатин"), описываемая структурной формулой (6), представляет собой одну из аминокислот, содержащихся в корнях кустарникового растения Sclerochitom ilicifolius в Южной Африке, и характеризуется степенью сладости, в несколько сот раз превышающей сладость сахарозы. В этой связи, монатин представляет собой особое соединение, перспективное в качестве низкокалорийного подсластителя (см. JP-A-64-25757).
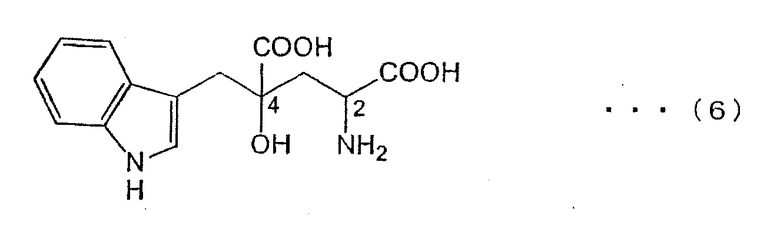
4-(индол-3-илметил)-4-гидрокси-глютаминовая кислота
Монатин имеет асимметрический атом углерода в положениях 2 и 4. Природный монатин имеет пространственную конфигурацию (2S,4S). Кроме его стереоизомеров неприродного типа, подтверждается также наличие трех типов таких стереоизомеров синтетического происхождения. Не только монатин природного типа, но также все другие стереоизомеры обладают, каждый, повышенным уровнем сладости. Исходя из этого, ожидается, что любой из них или смесь множества таких стереоизомеров могут использоваться в качестве подсластителя или компонента для получения подслащивающих средств (подсластителей).
Относительно способа производства монатина, на достигнутом уровне техники известно пять примеров его осуществления. Детали их описаны в следующих документах и статьях:
(1) Описание документа из Американской Фармакопеи (USP) No. 5994559
(2) Tetrahedron Letters, 2001, Vol.42, No.39, pp.6793-6796
(3) Organic Letters, 2000, Vol.2, No.19, pp.2967-2970
(4) Synthetic Communication, 1994, Vol.24, No.22, pp.3197-3211
(5) Synthetic Communication, 1993, Vol.23, No.18, pp.2511-2526
Однако указанные способы требуют осуществления многостадийного процесса. В промышленном масштабе еще не разработан ни один способ синтетического получения монатина. Таким образом, желательна разработка простого способа промышленного получения производных монатина с высоким выходом, включая сам монатин и его аналоги.
Таким образом, объектом настоящего изобретения является эффективный способ получения производных глютамата (включая их солевые формы), таких как монатин, в качестве перспективного компонента для получения подсластителя и т.п. и их аналогов.
Раскрытие изобретения
В указанных выше условиях авторы изобретения провели свои исследования. В результате авторы изобретения смогли добиться получения производных глютамата (включая их солевые формы) общей формулы (2)

(R1 и R2 в общей формуле (2) имеют те же значения, что R1 и R2 в общей формуле (1))
в присутствии фермента, катализирующего реакцию получения производных глютамата общей формулы (2) из замещенной α-кетокислоты общей формулы (1)
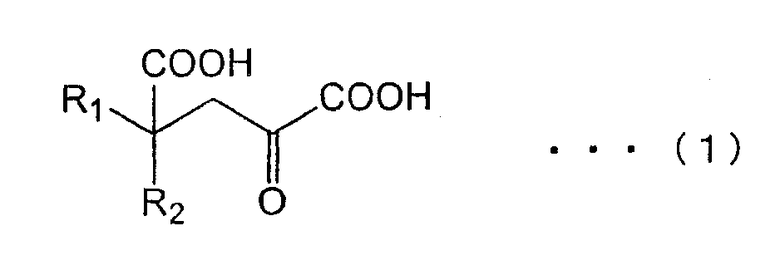
(в общей формуле (1) R1 и R2 обозначают независимо заместитель, выбранный из группы, состоящей из атома водорода, алкильных групп, включающих от 1 до 8 атомов углерода (С1-С8), С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, включающих до 20 атомов углерода, аралкильных групп, включающих до 20 атомов углерода, гетероциклических углеводородных групп, содержащих кольцо, и гидроксильных групп; если один из R1 и R2 обозначает атом водорода, другой не обозначает атом водорода, метильную группу или этильную группу; если один из R1 и R2 обозначает гидроксильную группу, другой не обозначает атом водорода или метильную группу; если R1 содержит ароматическое кольцо или гетероциклическое кольцо, указанное ароматическое кольцо или гетероциклическое кольцо может быть дополнительно замещено атомом галогена, гидроксильной группой, алкильными группами, включающими до 3 атомов углерода, алкоксильными группами, включающими до 3 атомов углерода, и аминогруппой), включая стадию развития реакции. Указанные разработки и составили суть настоящего изобретения.
Способ получения производных глютамата по настоящему изобретению позволяет эффективно получать монатин формулы (6) из 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (обозначаемой далее в описании как ИГОГ), описываемой приведенной ниже формулой (7), в ходе ферментативной реакции.


4-(индол-3-илметил)-4-гидрокси-глютаминовая кислота
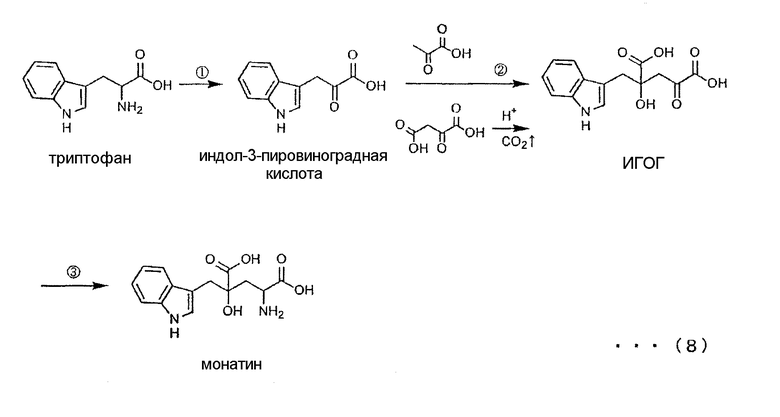
Дополнительно авторы настоящего изобретения разработали новый способ получения монатина, предусматривающий следующие реакции 1-3 с использованием в качестве исходного материала одной из аминокислот, триптофана, в способе получения глютаматных производных по настоящему изобретению. Способ получения производных глютамата по настоящему изобретению соответствует реакции 3 в способе получения монатина, включая приведенные ниже реакции 1-3. На реакционной схеме 8 показан путь получения монатина, включая указанные реакции 1-3.
Реакция 1: получение индол-3-пировиноградной кислоты из триптофана в присутствии фермента.
Реакция 2: получение предшественника кетокислоты (ИГОГ) путем альдольной конденсации индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты).
Реакция 3: синтетическое получение монатина путем аминирования ИГОГ в положении 2 в присутствии фермента.
Иными словами, настоящее изобретение может быть описано следующим образом.
[1] Способ получения производного глютамата (включая его солевые формы) общей формулы (2)

(R1 и R2 в общей формуле (2) имеют те же значения, что и R1 и R2 в общей формуле (1))
в присутствии фермента, катализирующего реакцию образования производного глютамата общей формулы (2) из замещенной
α-кетокислоты общей формулы (1)

(в общей формуле (1) R1 и R2 обозначают независимо заместитель, выбранный из группы, состоящей из атома водорода, алкильных групп, включающих до 8 атомов углерода (С1-С8), С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, включающих до 20 атомов углерода, аралкильных групп, включающих до 20 атомов углерода, углеводородной группы, содержащей гетероциклическое ядро, и гидроксильной группы; если один из R1 и R2 обозначает атом водорода, другой не обозначает атом водорода, метильную группу или этильную группу; если один из R1 и R2 обозначает гидроксильную группу, другой не обозначает атом водорода или метильную группу, если R1 содержит ароматическое кольцо или гетероциклическое кольцо, указанное ароматическое кольцо или гетероциклическое кольцо может быть дополнительно замещено атомом галогена, гидроксильной группой, алкильными группами, включающими до 3 атомов углерода, алкоксильными группами, включающими до 3 атомов углерода, и аминогруппой), включая стадию развития реакции.
[2] Способ получения производного глютамата, описанный в пункте [1], в котором R1 обозначает фенилметильную группу или 3-индолилметильную группу и R2 обозначает гидроксильную группу.
[3] Способ получения производного глютамата, описанный в пунктах [1] и [2], в котором указанный фермент представляет собой дегидрогеназу или трансаминазу.
[4] Способ получения производного глютамата, описанный в пункте [3], в котором указанный фермент представляет собой трансаминазу и реакционная система содержит один или множество типов аминокислот в качестве доноров аминогруппы.
[5] Способ получения производного глютамата, описанный в пункте [4], в котором указанные аминокислоты выбирают из группы, состоящей из глютаминовой икслоты, аспарагиновой кислоты, аланина, триптофана, фенилаланина, изолейцина, лейцина, тирозина, валина, аргинина, аспарагина, глютамина, метионина, орнитина, серина, цистеина, гистидина и лизина.
[6] Способ получения производного глютамата, описанный в пунктах [3]-[5], в котором указанный фермент представляет собой трансаминазу L-аминокислоты.
[7] Способ получения производного глютамата, описанный в пунктах [3]-[5], в котором указанный фермент представляет собой трансаминазу D-аминокислоты.
[8] Способ получения производного глютамата, описанный в пункте [7], в котором указанная реакционная система содержит фермент с активностью, катализирующей реакцию превращения L-аинокислоты в D-аминокислоту.
[9] Способ получения производного глютамата, описанный в пункте [6], в котором указанная трансаминаза L-аминокислоты представляет собой фермент, полученный из микоорганизма рода Aeromonas, Agrobacterium, Alcaligenes, Beijerinckia, Escherichia, Proteus и Morganella.
[10] Способ получения производного глютамата, описанный в пункте [9], в котором указанный микроорганизм выбирают из группы, состоящей из Aeromonas hydrophila, Agrobacterium tumefaciens, Alcaligenes faecalis, Beijerinckia indica, Escherichia coli, Proteus rettgeri и Morganella morganii.
[11] Способ получения производного глютамата, описанный в пунктах [7] или [8], в котором указанная трансаминаза D-аминокислоты представляет собой фермент, полученный из микроорганизма рода Bacillus или Paenibacillus.
[12] Способ получения производного глютамата, описанный в пункте [11], в котором указанный микроорганизм выбирают из группы, состоящей из Bacillus sphaericus, Bacillus pulvifaciens, Bacillus macerans, Bacillus lentus, Paenibacillus larvae subsp. pulvifaciens и Paenibacillus macerans.
[13] Способ получения производного глютамата, описанный в пункте [1], в котором указанный фермент представляет собой фермент, образованный микроорганизмом, содержащим введенный в него ген трансаминазы D-аминокислоты.
[14] Способ получения производного глютамата, описанный в пункте [13], в котором указанный микроорганизм представляет собой Escherichia coli.
[15] Способ получения производного глютамата, описанный в пунктах [13] или [14], в котором указанный ген трансаминазы D-аминокислоты получен из Bacillus sphaericus или Bacillus macerans.
[16] Способ получения производного глютамата, включающий по меньшей мере следующие стадии [I] и [II]:
[I] Стадия образования замещенной α-кетокислоты общей формулы (4)
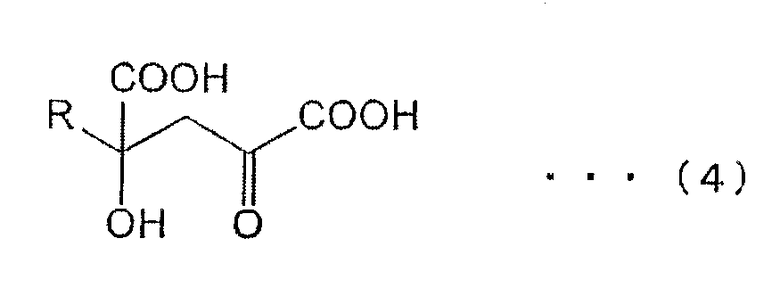
(R в общей формуле (4) имеет то же значение, что и R в общей формуле (3)) в присутствии фермента, катализирующего реакцию образования замещенной α-кетокислоты общей формулы (4) из замещенной α-кетокислоты, описываемой общей формулой (3)

(в общей формуле (3) R обозначает заместитель, выбранный из группы, состоящей из С2-С8 алкильных групп, С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, включающих до 20 атомов углерода, аралкильных групп, включающих до 20 атомов углерода, углеводородной группы, содержащей гетероциклическое ядро, и гидроксильной группы; если R содержит ароматическое кольцо или гетероциклическое кольцо, указанное ароматическое кольцо или гетероциклическое кольцо может быть дополнительно замещено атомом галогена, гидроксильной группой, алкильными группами, включающими до 3 атомов углерода, алкоксильными группами, включающими до 3 атомов углерода, и аминогруппой), и щавелевоуксусной кислоты или пировиноградной кислоты, включая стадию развития реакции.
[II] Стадия образования производного глютамата (включая его солевые формы), описываемого общей формулой (5), в присутствии фермента, катализирующего реакцию образования производного глютамата, описываемого общей формулой (5)
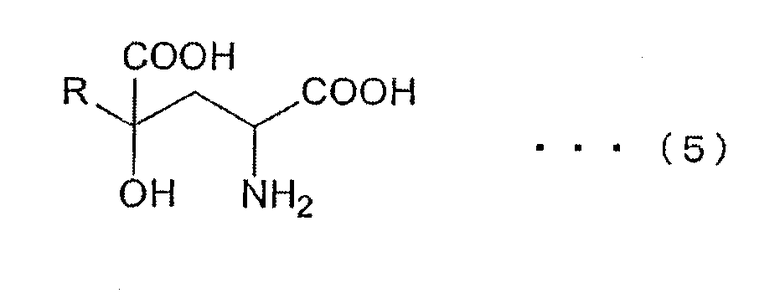
(R в общей формуле (5) имеет то же значение, что и R в общей формуле (3)), из замещенной α-кетокислоты общей формулы (4), включая стадию развития реакции.
[17] Способ получения производного глютамата, описанный в пункте [16], в котором R обозначает фенилметильную группу или 3-идолилметильную группу.
[18] Способ получения производного глютамата, описанный в пункте [16] или [17], в котором фермент, катализирующий реакцию на стадии [I], получают из микроорганизма, выбранного из группы, состоящей из Pseudomonas, Erwinia, Flavobacterium и Xanthomonas.
[19] Способ получения производного глютамата, описанный в пункте [18], в котором указанный микроорганизм представляет собой Pseudomonas taetrolens, Pseudomonas coronafaciens, Pseudomonas desmolytica, Erwinia sp., Flavobacterium rhenanum или Xanthomonas citri.
[20] Способ получения производного глютамата, описанный в пункте [19], в котором указанный микроорганизм представляет собой Pseudomonas taetrolens ATCC4683 или Pseudomonas coronafaciens AJ2791.
[21] Способ получения производного глютамата, описанный в пункте [16] или [17], в котором фермент, катализирующий реакцию на стадии [I], представляет собой один из следующих белков:
(а) белок, который включает аминокислотную последовательность SEQ ID NO.2, приведенную в перечне последовательностей;
(b) белок, который включает аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении, и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO.2, приведенной в перечне последовательностей, и обладает альдолазной активностью;
(с) белок, который включает аминокислотную последовательность SEQ ID NO.3;
(d) белок, который включает аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO.3, приведенной в перечне последовательностей, и обладает альдолазной активностью.
[22] Способ получения производного глютамата, описанный в пункте [16] или [17], в котором фермент, катализирующий реакцию на стадии [I], представляет собой фермент, полученный из рекомбинанта, в котором ген, кодирующий любой из приведенных ниже белков, амплифицирован и экспрессируется:
(а) белок, который включает аминокислотную последовательность SEQ ID NO.2, приведенную в перечне последовательностей;
(b) белок, который включает аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO.2, приведенной в перечне последовательностей, и обладает альдолазной активностью;
(с) белок, который включает аминокислотную последовательность SEQ ID NO.3;
(d) белок, который включает аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO.3, приведенной в перечне последовательностей, и обладает альдолазной активностью.
[23] Способ получения монатина, включающий по меньшей мере следующие стадии [А] - [С]:
[А] Стадия получения индол-3-пировиноградной кислоты в присутствии фермента, катализирующего реакцию превращения триптофана в индол-3-пировиноградную кислоту, путем создания условий для реакции триптофана;
[В] Стадия получения 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты из индол-3-пировиноградной кислоты и щавелевоуксусной кислоты или пировиноградной кислоты;
[С] Стадия получения монатина в присутствии фермента, катализирующего реакцию получения монатина из 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты, путем создания условий для реакции 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты.
[24] Способ получения монатина, описанный в пункте [23], в котором стадия [А] включает создание условий для реакции триптофана в присутствии фермента, катализирующего превращение триптофана в индол-3-пировиноградную кислоту, с образованием при этом индол-3-пировиноградной кислоты, и обработку полученного реакционного раствора с использованием любого из указанных видов обработки: путем дезаэрирования, дезоксигенирования и доведения значения рН до 2, максимум, для сбора индол-3-пировиноградной кислоты.
[25] Способ получения монатина, описанный в пункте [24], в котором указанная обработка дезаэрированием или обработка дезоксигенированием представляет собой способ полного или частичного замещения газа, содержащегося в реакционном растворе, инертным газом.
[26] Способ получения монатина, описанный в пункте [25], в котором указанный инертный газ представляет собой любой из указанных ниже: азот, аргон и гелий.
[27] Способ получения монатина, описанный в пунктах [24] - [26], в котором указанное доведение рН осуществляют при добавлении кислоты к реакционному раствору, и далее указанный способ включает стадию кристаллизации индол-3-пировиноградной кислоты, получаемый в результате такого доведения рН, и сбор полученной индол-3-пировиноградной кислоты.
[28] Способ получения монатина, описанный в пункте [27], в котором указанная кислота представляет собой любую кислоту из указанных ниже: серная кислота, хлористоводородная кислота, азотная кислота и фосфорная кислота.
[29] Способ получения монатина, описанный в пунктах [23]-[28], в котором указанный фермент, катализирующий реакцию на стадии [А], получают из микроорганизма, обладающего оксидазной и каталазной активностью.
[30] Способ получения монатина, описанный в пунктах [23]-[29], в котором указанный фермент, катализирующий реакцию на стадии [А], получают из любого представителя рода Achromobacter, Proteus и Morganella.
[31] Способ получения монатина, описанный в пункте [30], в котором указанный фермент получают из любого из указанных ниже: Achromobacter sp. AJ2425, Proteus rettgeri IFO13501 и Morganella morganii IFO3168.
[32] Способ получения монатина, описанный в пункте [23], в котором стадия [А] включает взаимодействие культуры микроорганизма с триптофаном, причем указанный микроорганизм обладает способностью превращать триптофан в индол-3-пировиноградную кислоту и выбирается из представителей рода Achromobacter, Proteus, Morganella, Pseudomonas и Neurospora, а также включает продуцирование индол-3-пировиноградной кислоты и далее сбор индол-3-пировиноградной кислоты.
[33] Способ получения монатина, описанный в пунктах [23] - [32], в котором указанную стадию В проводят в присутствии фермента, катализирующего реакцию.
[34] Способ получения монатина, описанный в пунктах [23] - [32], в котором указанную стадию В проводят посредством химического синтеза.
Наилучший способ осуществления изобретения
Способ получения производных глютамата, разработанный авторами, направлен на получение производных глютамата общей формулы (2) из замещенной α-кетокислоты общей формулы (1) и относится к способу получения производных глютамата, включающему стадию, на которой создаются условия, позволяющие ферменту катализировать реакцию трансаминирования или микроорганизму продуцировать фермент, способный далее вступать в соответствующую реакцию.


Дополнительно, разработанный авторами изобретения способ получения монатина из триптофана, взятого в качестве исходного материала, включает указанные ниже реакции 1-3. В способе получения монатина, включающем указанные ниже реакции 1-3, используется процесс образования производных глютамата, относящийся к реакции 3, в рамках описания способа настоящего изобретения.
Реакция 1: синтез индол-3-пировиноградной кислоты из триптофана в присутствии фермента.
Реакция 2: синтез кетокислоты, как предшественника (ИГОГ), путем альдольной конденсации индол-3-пировиноградной кислотой и пировиноградной кислотой (или щавелевоуксусной кислотой).
Реакция 3: синтез монатина путем аминирования ИГОГ в положении 2 в присутствии фермента.

Среди реакций 1-3 реакции 1 и 3 представляют собой ферментативные реакции. Однако, реакция 2 может быть успешно проведена с использованием любого способа химического синтеза и ферментативного синтеза, без каких-либо конкретных ограничений.
Способ получения монатина по настоящему изобретению не ограничивается способом получения монатина с использованием триптофана в качестве исходного материала, но может быть успешно осуществлен с включением реакции 3 в качестве обязательной стадии в число указанных реакций 1-3. Иными словами, настоящее изобретение также включает способ получения монатина из коммерчески доступной индол-3-пировиноградной кислоты в качестве исходного материала в ходе реакций 2 и 3 и способ получения монатина из предшественника - кетокислоты (ИГОГ), используемой в качестве исходного материала, посредством реакции 3. Таким образом, способ получения монатина по настоящему изобретению включает все способы от (а) до (с).
(а) Реакции 1 + 2 + 3
(b) Реакции 2 + 3
(с) Одна только реакция 3
Дополнительно, реакция 2 в способе получения монатина может использоваться не только для синтеза предшественника монатина, кетокислоты (ИГОГ), но также для получения замещенной α-кетокислоты, используемой в качестве субстрата в способе получения производных глютамата по настоящему изобретению. Как видно из приведенной ниже схемы (10), способ получения производных глютамата общей формулы (5) через реакцию 3 с использованием замещенной α-кетокислоты общей формулы (4), получаемой в ходе реакции 2 (Реакция 2 + Реакция 3), также включается в способ получения производных глютамата по настоящему изобретению.
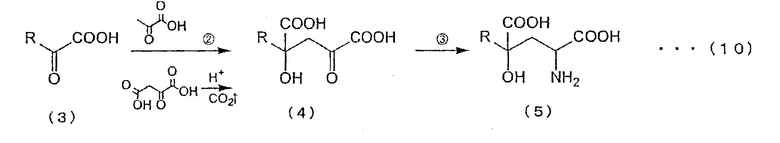
Ниже приводится подробное описание изобретения со ссылкой на прилагаемые чертежи, в следующей последовательности: [А] Реакция 1, [В] Реакция 2 и [С] Реакция 3.
[А] Реакция 1
Реакция 1, показанная на приведенной ниже схеме (11), представляет собой реакцию, относящуюся к образованию индол-3-пировиноградной кислоты. Реакция 1 по настоящему изобретению включает в качестве одной из характерных особенностей стадию, способствующую реакции триптофана в присутствии фермента, катализирующего реакцию превращения триптофана в индол-3-пировиноградную кислоту, приводящей к образованию индол-3-пировиноградной кислоты, с последующими обработкой полученного реакционного раствора путем использования любого из указанных способов обработки: дезаэрирования, дезоксигенирования и доведения рН до 2, как максимального значения, и сбором полученной индол-3-пировиноградной кислоты.
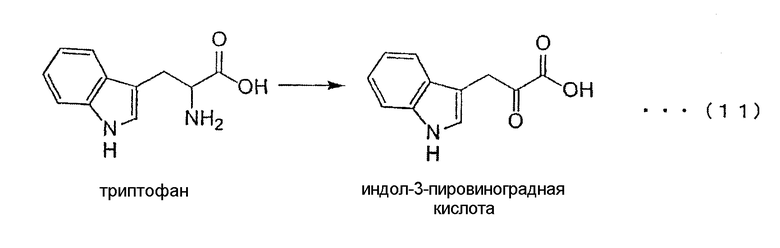
На достигнутом уровне техники известен химический способ получения индол-3-пировиноградной кислоты, предложенный Giovanna De Luca, et al., который включает стадию, на которой триптофан, как исходный материал, подвергают реакции с пиридиновым альдегидом в присутствии основания для дегидратации акцепторов протона с получением индол-3-пировиноградной кислоты с выходом от 50 до 62% (см. публикацию по патенту (TOKUHYO) No.Sho 62-501912, брошюра с Международной публикацией WO 87/00169). Согласно описанному способу, основание и пиридиновый альдегид как обязательные материалы являются очень дорогими, тогда как выход реакции очень низкий. В этой связи, возникают проблемы, определяемые очень высокой стоимостью продукции. Кроме того, известен способ получения индол-3-пировиноградной кислоты с выходом 64%, предложенный Politi Vincenzo et al., который включает стадию проведения реакции конденсации с использованием индола и оксима сложного эфира этил-3-бромпирувата, в качестве исходных материалов, с последующим кислотным гидролизом (ЕР 421 946). Согласно указанному способу, для его осуществления требуется стадия очистки на силикагеле, которая является дорогой. Кроме того, сырье является дорогостоящим. Таким образом, указанный способ характеризуется наличием недостатков, определяемых его высокой стоимостью при использовании в масштабах промышленного производства.
Что касается ферментативного способа, известен также способ, в котором используется трансаминаза (см. приведенную ниже схему (12)).
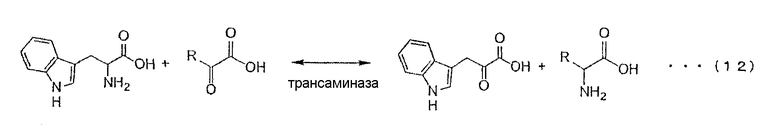
Имеются изданные отчеты, описывающие способ получения индол-3-пировиноградной кислоты, включающий стадию, на которой созданы условия, способствующие взаимодействию L-триптофана с трансаминазой L-триптофана (L-trp) из Candida maltose, с последующим образованием индол-3-пировиноградной кислоты из 40 мМ L-Trp и 80 мМ 2-кетоглутаровой кислоты и стадию очистки на ионообменной смоле с получением в итоге индол-3-пировиноградной кислоты с выходом 72 % (см. патент Восточной Германии (East Germany Patent DD 297190 (Bobe Ruediger, et al)); а также способ получения индол-3-пировиноградной кислоты, включающий стадию, на которой созданы условия, способствующие взаимодействию трансаминазы аспартата с L-Trp и 2-кетоглутаровой кислотой с образованием индол-3-пировиноградной кислоты, стадию экстракции полученного реакционного раствора петролейным эфиром и стадию очистки индол-3-пировиноградной кислоты путем разделения на хроматографической колонке и сбора очищенной индол-3-пировиноградной кислоты (см. JP-A-59-95894 (Mario Matterazzi, et al.)). Указанные способы, в которых используется трансаминаза, дают очень низкий выход и требуют наличия кетокислоты, такой как 2-кетоглутаровая кислота, функционирующей в качестве акцептора аминогруппы, материал, отличный от L-Trp, в качестве исходного материала, и дополнительно включают вторичную продукцию аминокислоты, соответствующей акцептору аминогруппы, в молярном соотношении, эквивалентном молярному количеству образованной индол-3-пировиноградной кислоты. Кроме того, в реакционной системе требуется присутствие кетокислоты в количестве, избыточном относительно L-Trp, для повышения выхода, так что после завершения реакции все еще сохраняются остаточные количества кетокислоты. На основании указанных причин, для сбора целевой индол-3-пировиноградной кислоты из реакционного раствора требуется стадия очистки с использованием ионообменной хроматографии или аналогичного способа, которые включают сложные процедуры очистки и сопряжены с высокой стоимостью.
В том, что касается способа получения индол-3-пировиноградной кислоты из L-Trp, следует отметить также известный способ с использованием оксидазы L-аминокислоты. Поскольку индол-3-пировиноградная кислота разлагается до индолуксусной кислоты (см. схему реакции (14)), образуя при окислении триптофана оксидазой L-аминокислоты пероксид водорода в качестве вторичного продукта (см. приведенную ниже реакцию (13)), в настоящем изобретении предлагается способ, включающий добавление каталазы к реакционной системе с целью разложения пероксида водорода (см. приведенную ниже реакцию (15)) (см. спецификацию из текста Американской Фармакопеи USP 5002963; Tetrahedron Letters, 1987, Vol. 28, No. 12, pp. 1277-1280).

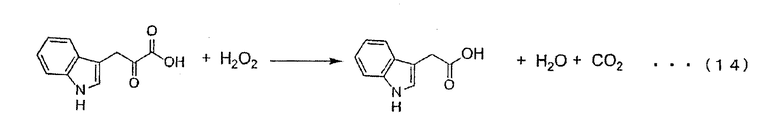

Конкретно, данный способ включает стадию использования колонки с иммобилизованным ферментом, полученной путем иммобилизации оксидазы L-аминокислоты из змеиного яда и каталазы из печени быка на носителе, с целью прохождения раствора, содержащего L-Trp, через колонку для вступления в реакцию, стадию абсорбции образованной индол-3-пировиноградной кислоты на ионообменной колонке, стадию элюции метанолом и стадию сушки продукта с последующим сбором продукта. Однако, согласно настоящему способу, 0,5 г исходного L-Trp дает только 0,2 г индол-3-пировиноградной кислоты с таким низким выходом, как 40%; процедура иммобилизации и процедура очистки на ионообменной смоле являются трудоемкими; и при этом требуется стадия отбора и направления на повторную обработку остаточного L-Trp. Таким образом, недостатком указанного процесса является его высокая стоимость.
В том, что касается оксидазы L-аминокислоты, полученной из микроорганизмов, John A. Duerre, et al. нашли альтернативный вариант обнаружения активности по окислению L-Trp путем измерения активности, включающий стадию неполной очистки оксидазы L-аминокислоты из Proteus rettgeri и стадию выявления потребления кислорода (см. Journal of Bacteriology, 1975, Vol. 121, No. 2, pp. 656-663). Дополнительно, Furuyama et al. подтвердили, что оксидаза L-фенилаланина, полученная из Pseudomonas sp. P-501, взаимодействует с L-Trp, по способу измерения активности, включающему стадию выявления потребления кислорода (см. Noda Institute for Scientific Research, Kiyofumi Maruyama, Journal of Biochemistry, 1990, 108, pp. 327-333).
В каждом из указанных отчетов оксидазную активность выявляли путем изменения потребления L-триптофана, потребления кислорода и количества образованного пероксида водорода в ходе ферментативной реакции, но никогда не определяли непосредственно индол-3-пировиноградную кислоту. Такой подход мог быть связан с тем фактом, что индол-3-пировиноградная кислота разлагается до индолуксусной кислоты с образованием пероксида водорода в результате реакции, протекающей с оксидазой аминокислоты. Тем не менее, не описан пример получения индол-3-пировиноградной кислоты с использованием микробных клеток или обработанного продукта из микробных клеток. В этой связи, неизвестно, как триптофан разлагается микроорганизмами или какие продукты разложения он производит.
Кроме того, способ, включающий использование трансаминазы, и способ, включающий использование оксидазы L-аминокислоты из змеиного яда, в методике сбора продуцированной индол-3-пировиноградной кислоты, приведенной выше в контексте описания достигнутого уровня техники, характеризуется низким выходом реакции и требует стадий осуществления хроматографического разделения для регенерации индол-3-пировиноградной кислоты, в связи с наличием кетокислоты в качестве побочного продукта и остаточного количества L-триптофана. Таким образом, практикуемые в настоящее время способы требуют дорогостоящих процедур и приводят к высокой стоимости получаемого продукта.
В таких условиях авторы изобретения провели исследования с целью разработки способа получения индол-3-пировиноградной кислоты в простом варианте осуществления и с низкой стоимостью. Авторы обнаружили, что взаимодействие микроорганизма, обладающего активностью оксидазы аминокислоты и каталазы, с триптофаном может приводить к образованию индол-3-пировиноградной кислоты, которую можно собрать, то есть указанное взаимодействие с триптофаном может продуцировать индол-3-пировиноградную кислоту, предпочтительно при подавлении процесса разложения целевого продукта путем замещения инертным газом или путем коррекции рН реакционного раствора, который далее может быть собран. При проведении последующих исследований, кроме результатов, относящихся к разложению индол-3-пировиноградной кислоты до индолуксусной кислоты пероксидом водорода, авторы выявили проблему, связанную с тем, что индол-3-пировиноградная кислота подвергается воздействию кислорода и подобными соединениями в растворе с образованием продуктов разложения, так что происходит постепенное окрашивание раствора, содержащего индол-3-пировиноградную кислоту, а вместе с тем и способ решения такой проблемы.
Согласно настоящему изобретению, индол-3-пировиноградную кислоту подвергают реакции преобразования в индол-3-пировиноградную кислоту в присутствии фермента, катализирующего указанную реакцию, с получением в результате такой реакции индол-3-пировиноградной кислоты, затем образовавшийся раствор обрабатывают путем деаэрации, деоксигенации или доведения рН до pH 2, максимум, с тем чтобы можно было собрать индол-3-пировиноградную кислоту.
Разложение или окрашивание индол-3-пировиноградной кислоты может развиваться при ее нахождении в растворенном состоянии в растворе. Однако, при добавлении кислоты индол-3-пировиноградная кислота кристаллизуется на ранней фазе стадии сбора образовавшейся индол-3-пировиноградной кислоты. При этом, сравнение с другими стадиями очистки и обработки показывает, что способ добавления кислоты успешно приводит к подавлению разложения и окрашивания.
Индолуксусная кислота как продукт разложения индол-3-пировиноградной кислоты не всегда легко удаляется путем прямой кристаллизации в кислых условиях. При использовании способа замещения инертным газом можно эффективно подавить вторичное образованием индолуксусной кислоты. Сочетание процесса кристаллизации с обработкой в виде замещения инертным газом в кислых условиях может быть более эффективным в том, что касается сбора индол-3-пировиноградной кислоты высокой чистоты.
Дополнительно, предлагается другой способ осуществления реакции 1 по настоящему изобретению, который включает в качестве характерной особенности стадию взаимодействия культуры микроорганизма с триптофаном, где указанный микроорганизм обладает способностью преобразовывать триптофан в индол-3-пировиноградную кислоту, для целей получения и сбора индол-3-пировиноградной кислоты.
Как указывалось, отсутствует какое-либо сообщение относительно взаимодействия культуры микроорганизма с триптофаном, где указанный микроорганизм обладает способностью преобразовывать триптофан в индол-3-пировиноградную кислоту, для целей получения и сбора индол-3-пировиноградной кислоты. Таким образом, настоящий способ представляет собой новый и полезный способ получения и сбора индол-3-пировиноградной кислоты в рамках осуществления ферментативного процесса.
Способ осуществления реакции 1 по настоящему изобретению ниже описывается последовательно, начиная с раздела (А-1), озаглавленного как "Фермент, используемый в реакции 1", и далее в разделе (А-2), озаглавленном как "Реакционные условия для проведения реакции 1", в указанном порядке.
(А-1)Фермент, используемый в реакции 1
Фермент, подходящий для использования в реакции 1, включает любой фермент, обладающий способностью преобразовывать триптофан в индол-3-пировиноградную кислоту, без каких-либо ограничений. В качестве фермента, подходящего для использования в реакции 1, предпочтительны ферменты, обладающие активностью оксидазы аминокислоты, и ферменты, обладающие каталазной активностью.
Термин "активность оксидазы аминокислоты" в контексте описания реакции 1 обозначает активность, катализирующую реакцию, показанную далее на схеме (13). В основном, оксидаза L-аминокислоты продуцирует кетокислоту из соответствующей L-аминокислоты, тогда как оксидаза D-аминокислоты продуцирует кетокислоту из соответствующей D-аминокислоты. Конкретно, в соответствии с настоящим изобретением, микроорганизм, обладающий отдельно активностью оксидазы L-аминокислоты, может использоваться с L-триптофаном, взятым в виде неочищенного сырья, тогда как микроорганизм, обладающий активностью оксидазы D-аминокислоты, может работать с D-триптофаном, только при использовании его в очищенном виде. Кроме того, применим также способ получения с использованием DL-триптофана. В случае проведения реакции оксидаз D- и L-аминокислоты с DL-триптофаном можно достичь количественного выхода целевой индол-3-пировиноградной кислоты. И наоборот, в случае проведения реакции оксидазы D- или L-аминокислоты с DL-триптофаном целевая индол-3-пировиноградная кислота может быть получена с выходом 50%.
Дополнительно, термин "каталазная активность" обозначает активность, катализирующую реакцию, приведенную на реакционной схеме (15), ниже.


Фермент, обладающий активностью оксидазы аминокислоты, для использования в реакции 1 можно выбрать при использовании различных методов оценки, таких как метод определения потребления кислорода за счет окислительной активности аминокислоты (см., например, Journal of Bacteriology, 1975, Vol. 121, No. 2, pp. 656-663) и метод измерения уровня пероксида водорода, образованного в ходе рассматриваемой реакции (см., например, M. Gabler, et al., Enzyme and Microbial Technology, 2000, 27, pp. 605-611), а также метод прямого измерения количества индол-3-пировиноградной кислоты, образованной из триптофана, которые будут описаны ниже, согласно настоящему изобретению.
Фермент с каталазной активностью для проведения реакции 1 может быть выбран с использованием любого из известных методов, таких как метод измерения снижения уровня пероксида водорода как результат каталазной реакции, основанный на изменении поглощения при длине волны 230-250 нм, метод измерения остаточного количества пероксида водорода в реакционном растворе с использованием MnSO4 и метод манометрического измерения количества образованного в реакции кислорода. В качестве одного из примеров, приводится спектроскопический метод измерения остаточного количества пероксида водорода, который включает стадию окисления доноров электронов, таких как о-дианизидин, посредством пероксидазной реакции, как описано в работе M. Gabler, et al., Enzyme and Microbial Technology, 2000, 27, pp. 605-611. С использованием перечисленных методов может быть выбран фермент с каталазной активностью.
Кроме того, фермент, подходящий для использования в реакции 1, может быть выбран путем выявления активности, направленной на продукцию индол-3-пировиноградной кислоты из триптофана, в соответствии с методикой, описанной ниже, в примере 1.
Микроорганизм, образующий фермент, подходящий для использования в реакции 1, может быть выбран, например, из представителей рода Achromobacter, Proteus, Morganella, Pseudomonas и Neurospora. Такой микроорганизм представляет собой предпочтительно микроорганизм, содержащий аминокислотную последовательность, обладающую оксидазной и каталазной активностью. Конкретно, указанный микроорганизм выбирают, например, из представителей рода Achromobacter, Proteus и Morganella. В особенности, в качестве таких микроорганизмов предпочтительны Achromobacter sp. AJ2425, Proteus rettgeri IFO13501 и Morganella morganii IFO3168.
Приведенный в настоящем описании Achromobacter sp. AJ2425 был депонирован в следующих условиях.
Achromobacter sp.штамм AJ2425
(а) Номер доступа в Депозитарии No. FERM BP-8244 (перенесен из FERM P-18786 в Международный Депозитарий патентованных организмов (International Patent Organism Depositary) 22 ноября 2002 г.)
(b) Дата депонирования: 20 марта 2002 г.
(с) Депонирующая Организация: Международный Депозитарий патентованных организмов, Институт современной промышленной науки и технологии (International Patent Organism Depositary, The Institute of Advanced Industrial Science and Technology) (No. 6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония (код: 305-8566))
Дополнительно указанный микроорганизм, депонированный в Институте ферментации, Осака (Institute of Fermentation, Osaka (IFO), имеется и может быть получен из Института ферментации (2-17-85, Tomimoto-cho, Yodogawa-ku, Osaka, Japan (Осака, Япония) (код: 532-8686)).
Указанные микроорганизмы могут представлять собой микробные штаммы, впервые выделенные из природных источников, таких как почва или растения, или они могут относиться к микробным штаммам, искусственно выращенным при обработке химическими мутагенами, или могут быть получены методами рекомбинантной ДНК.
Культивирование микроорганизма, образующего фермент, подходящий для использования в реакции 1, может быть осуществлено на основе широко применяемых в данной области культуральных сред, содержащих источники углерода, источники азота, неорганические соли, соли следовых количеств металлов, витамины и т.п. В качестве источников углерода, например, может быть использован любой источник углерода, который данный микроорганизм может утилизировать. Примеры таких источников углерода включают, в частности, сахара, такие как глюкоза, сахароза и декстрин, спирты, такие как сорбит, этанол и глицерин, органические кислоты, такие как фумаровая кислота, лимонная кислота, уксусная кислота и пропионовая кислота, и их соли, углеводороды, такие как парафин, или описанные выше их смеси.
В качестве источников азота, например, могут быть использованы сульфат аммония, хлорид аммония, мочевина, дрожжевой экстракт, мясной экстракт, жидкий кукурузный экстракт и продукты гидролиза казеина. В качестве конкретного примера композиции культуральной среды может быть приведена культуральная среда следующего состава: 1,0 % глюкозы, 0,3 % сульфата аммония, 1,0 % экстракта дрожжевого порошка, 1,0 % пептона, 0,1% KH2PO4, 0,3% K2HPO4, 0,05% MgSO4 · 7H2O, 0,001% FeSO4 · 7H2O и 0,001% MgSO4 · 4 H2O (pH 7,0).
Дополнительно, микробные клетки, обладающие высокой способностью преобразовывать триптофан в индол-3-пировиноградную кислоту, могут быть получены при добавлении к культуральной среде L-аминокислоты или D-аминокислоты в качестве индуктора фермента.
Для усиления проникновения субстрата внутрь микробных клеток могут также использоваться детергенты, такие как Тритон Х и Твин, а также органические растворители, такие как толуол и ксилол.
Что касается температуры реакции, то в основном реакцию проводят в температурном диапазоне, в котором используемый микроорганизм может расти, например, в температурном диапазоне примерно от 20 до 45°С, предпочтительно от 25 до 37°С. Что касается значения рН культуральной среды, то рН доводят до значения примерно от 3 до 10 и более предпочтительно, примерно от 4 до 8. Что касается условий аэрации, то указанные условия должны устанавливаться такими, чтобы они были пригодны для роста используемого микроорганизма. Предпочтительно, указанные условия представляют собой аэробные условия. Что касается продолжительности культивирования, то указанную реакцию проводят в течение периода времени примерно от 12 до 120 часов и предпочтительно примерно от 16 до 96 часов.
(А-2) Реакционные условия, подходящие для проведения реакции 1
Характерной особенностью реакции 1 является то, что она включает стадию образования индол-3-пировиноградной кислоты из триптофана в присутствии соответствующего фермента и стадию обработки полученного реакционного раствора любым из приведенных видов обработки: путем деаэрации, деоксигенации и доведения рН максимум до рН 2, с целью сбора индол-3-пировиноградной кислоты.
В контексте реакции 1 термин "в присутствии фермента" обозначает создание условий, допускающих существование фермента в данной реакционной системе в таком виде, когда указанный фермент способен осуществлять преобразование триптофана в индол-3-пировиноградную кислоту. Иными словами, фермент может присутствовать в реакционной системе в любом состоянии, при условии, что он способен осуществлять преобразование триптофана в индол-3-пировиноградную кислоту. Так, например, может быть добавлен только сам фермент в реакционную систему или в реакционную систему могут быть добавлены: микроорганизм, обладающий соответствующей ферментативной активностью (микроорганизм, образующий фермент, клетки, трансформированные рекомбинантной ДНК), культура микроорганизма (жидкая культура, твердая культура и т.п.), культуральная среда (полученная при предварительном удалении микробных клеток из культуры) или обработанный продукт из такой культуры. В случае использования культуры микроорганизма реакция 1 может развиваться одновременно с культивированием микроорганизма. В ином случае, реакция 1 может осуществляться с использованием культуры, подходящей для получения фермента. В контексте настоящего описания термин "обработка" обозначает обработку, направленную на регенерацию ферментов в микробных клетках. Указанная обработка включает, например, обработку ультразвуком, стеклянными шариками, под френч-прессом и лиофилизацию, а также обработку с использованием лизирующих ферментов, органических растворителей, детергентов и т.п. Дополнительно, после проведения указанных видов обработки обработанные продукты подвергаются воздействию традиционных процедур (жидкостная хроматография, фракционирование сульфатом аммония и т.п.) с целью получения фракции неочищенного фермента или очищенного фермента, которые могут быть далее с успехом использованы, если указанные фракция или сам фермент обладают требуемой способностью.
Для целей использования культуры или обработанного продукта из нее такие культура или обработанный продукт, перед непосредственным использованием, могут быть также введены в каррагенан или полиакриламид или могут быть иммобилизованы на пленке из полиэфирсульфона или регенерированной целлюлозы.
Микробные клетки или обработанный продукт из микробной клетки могут использоваться в количестве (эффективное количество), достаточном для проявления целевого эффекта в случае данной реакции. Что касается эффективного количества, то специалист со средним уровнем знаний в данной области может легко определить такое количество в рамках простого предварительного эксперимента. В случае промытых влажных микробных клеток указанное количество составляет, например, от 1 до 40 г на 100 мл реакционного раствора.
Что касается субстрата триптофана, то может быть использована любая его форма: L-форма, D-форма и DL-форма. В связи с доступностью и приемлемой стоимостью принято использование L-формы. Триптофан добавляют в разном режиме: в объединенном виде, одной порцией, в перемежающемся режиме или постоянно, с достижением концентраций в соответствующем диапазоне, без подавления целевой реакции. Что касается способа добавления, то триптофан может добавляться непосредственно к микробным клеткам в процессе культивирования. В ином случае, после окончания культивирования отделяют микробные клетки и смешивают с ними триптофан. Триптофан может быть смешан с обработанным продуктом для дальнейшего использования. В случае добавления указанное добавление осуществляют на стадии водного раствора или суспензии. С целью повышения растворимости или усиления диспергирования органические растворители или детергенты, которые не оказывают влияния на данную реакцию, могут быть смешаны с триптофаном для последующего добавления.
Реакцию по настоящему изобретению проводят в диапазоне pH, составляющем предпочтительно примерно от pH 3 до рН 10, более предпочтительно, примерно от pH 5 до рН 9, и в температурном диапазоне, составляющем предпочтительно от 10 до 60°С, более предпочтительно от 20 до 40°С, в течение времени реакции, составляющем предпочтительно примерно от 0,5 до 120 часов, более предпочтительно, примерно от 0,5 до 24 часов, при перемешивании или при выдерживании реакционной смеси без какого-либо воздействия. Указанный субстрат может использоваться в рассматриваемой реакции в любой концентрации, без определенных ограничений, но предпочтительно может использоваться в концентрации примерно от 0,1% до 10%.
Что касается количественного определения триптофана, оставшегося в жидкой культуре или в реакционном растворе, то образовавшаяся индол-3-пировиноградная кислота или ее интермедиат могут быть легко количественно измерены с использованием известного способа анализа методом высокоэффективной жидкостной хроматографии.
Жидкая культура, в которой накоплена образованная таким образом индол-3-пировиноградная кислота (реакционный раствор), подвергается обработке путем деаэрации или деоксигенации для подавления разложения индол-3-пировиноградной кислоты. Что касается способа деаэрации и деоксигенации, то в качестве его примера может быть приведен способ замещения газа (полностью или частично), содержащегося в реакционном растворе, инертными газами, например, азотом и аргоном.
В контексте настоящего описания термин обработка "деаэрацией" обозначает процедуру удаления компонентов, обладающих реакционноспособностью с индол-3-пировиноградной кислотой, таких как кислород и пероксид водорода, имеющихся в растворе, путем замещения реакционного раствора инертнымии газами или путем помещения реакционного раствора в условия пониженного давления с использованием аспиратора или вакуумного насоса. Дополнительно, термин обработка "деоксигенацией" обозначает процедуру удаления растворенного кислорода, имеющегося в реакционном растворе, или снижения его концентрации. Конкретно, способ удаления имеющегося в растворе кислорода включает, например, способ удаления кислорода инертным газом или способ добавления к раствору деоксигенирующего агента.
При замещении реакционного раствора инертным газом кислород, остающийся в реакционном растворе, может быть удален для завершения реакции, а также для предупреждения разложения образовавшейся индол-3-пировиноградной кислоты и остаточного триптофана. В контексте настоящего описания, термин "инертный газ" обозначает газ, никогда не взаимодействующий, непосредственно или опосредованно, с индол-3-пировиноградной кислотой, но обладающий способностью эффективно снижать содержание компонентов, реакционноспособных в отношении индол-3-пировиноградной кислоты и триптофана, таких как кислород или следовые количества оставшегося пероксида водорода. Примеры инертного газа, используемого по настоящему изобретению, включают азот, аргон и гелий. Замещение инертным газом может быть проведено сразу после завершения реакции. В случае проведения реакции с использованием промытых микробных клеток указанное замещение может быть проведено после отделения микробных клеток.
Способ введения инертного газа включает, например, процесс замещения газообразной фазы инертным газом для снижения концентрации кислорода в газообразной фазе и процесс введения инертного газа в раствор для удаления растворенного кислорода. Способ введения конкретно не ограничивается. Что касается концентрации кислорода в газообразной фазе, принимается значение, равное 5% или менее, предпочтительно 3% или менее, более предпочтительно 1% или менее. Желательно, чтобы концентрация кислорода в растворе составляла 1 м.д. или менее, предпочтительно 0,1 м.д. или менее и более предпочтительно 0,01 м.д. или менее.
Далее, реакция может быть остановлена и разложение индол-3-пировиноградной кислоты может быть подавлено путем добавления соответствующих веществ, таких как сульфит натрия, в отношении которых известно, что они снижают концентрацию растворенного кислорода в реакционном растворе.
В качестве дезоксигенирующего средства по настоящему изобретению может использоваться сульфитный ион. В качестве источника сульфитного иона могут применяться соли, такие как сульфит натрия, сульфит калия, сульфит аммония и сернистая кислота, или гидросульфит. Они используются в концентрации сульфитного иона, или гидросульфита предпочтительно от 20 м.д. или более до 1% или менее, более предпочтительно, от 100 м.д. или более до 0,5% или менее.
Обработка путем замещения инертным газом и способ добавления дезоксигенирующих средств к раствору могут быть осуществлены в сочетании или может быть выполнена лишь одна из указанных процедур.
Образованную в ходе реакции индол-3-пировиноградную кислоту перед использованием отбирают из жидкой среды реакционного раствора с помощью распространенных методов. Для ее отбора из жидкой культуры или из реакционного раствора могут использоваться такие широко известные в данной области техники процедуры, как, например, фильтрование, центрифугирование, концентрирование в вакууме, ионообменная или адсорбционная хроматография или кристаллизация, и при необходимости, в соответствующем сочетании.
В одном предпочтительном варианте осуществления настоящего изобретения рН реакционного раствора снижают, достигая при этом кристаллизации или осаждения индол-3-пировиноградной кислоты, которая может быть далее отделена и отобрана из смеси после завершения реакции. Что касается корректировки уровня pH в реакционном растворе, то указанный уровень pH предпочтительно корректируется до значение рН 2 или менее, более предпочтительно до рН 1 или менее. Согласно настоящему изобретению, индол-3-пировиноградная кислота может быть получена с высоким выходом, тогда как концентрации побочных продуктов - кетокислоты и остатка триптофана в реакционном растворе снижены. В этой связи, путем прямой кристаллизации индол-3-пировиноградной кислоты в кислых условиях может быть упрощена стадия очистки. В более предпочтительном варианте осуществления настоящего изобретения индол-3-пировиноградная кислота может быть непосредственно подвергнута кристаллизации путем соответствующего добавления к реакционному раствору кислоты, такой как серная кислота и хлористоводородная кислота. В соответствии с данным способом, индол-3-пировиноградная кислота может быть получена с высоким выходом, тогда как концентрации побочных продуктов - кетокислоты и остатка триптофана в реакционном растворе будут снижены. Таким образом, процедура очистки может быть упрощена путем проведения непосредственной кристаллизации индол-3-пировиноградной кислоты в кислых условиях.
Для корректировки с целью создания кислых условий тип кислоты конкретно не ограничивается, главное, чтобы указанный метод позволял достичь кислотности раствора. Примеры кислот, которые могут быть использованы, включают хлористоводородную кислоту, серную кислоту, азотную кислоту и фосфорную кислоту. Специалист со средним уровнем знаний в данной области сможет выбрать соответствующим образом температуру кристаллизации, количество нужной для использования кислоты, длительность процесса кристаллизации и способ добавления кислоты, так чтобы все параметры были в диапазоне значений, не оказывающих вредного воздействия на практику осуществления настоящего изобретения.
Что касается температуры кристаллизации, то более предпочтительной является температура примерно от -20°С до 100°С, более предпочтительно, может быть выбрана температура примерно от 0°С до 60°С. Что касается количества кислоты, которая может быть использована, то может быть выбрано количество, нужное для коректировки реакционного раствора предпочтительно до значения pH 2 или менее, более предпочтительно до значения pH 1 или менее. Кислота может быть добавлена в таком количестве, чтобы концентрация иона водорода в растворе после добавления кислоты составляла предпочтительно примерно от 0,01 до 10 моль/л, более предпочтительно примерно от 0,1 до 1 моль/л.
Что касается длительности процесса кристаллизации, то ее предпочтительно проводить в течение периода времени примерно от 1 до 100 часов, более предпочтительно, может быть выбран период времени примерно от 1 до 24 часов.
[B] Реакция 2
Реакция 2 по настоящему изобретению представляет собой реакцию синтеза предшественника монатина в виде кетокислоты (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Однако реакция 2 может использоваться не только для синтеза ИГОГ, но также для синтеза замещенной α-кетокислоты с целью использования ее в качестве субстрата в реакции 3, описанной ниже.
Конкретно, реакция 2 может также широко применяться для получения замещенной α-кетокислоты, описываемой общей формулой (4)

из замещенной α-кетокислоты, описываемой общей формулой (3)

и щавелевоуксусной кислоты или пировиноградной кислоты.
Замещенная α-кетокислота общей формулы (4), полученная в ходе реакции 2, может быть использована в описанной ниже реакции 3 в качестве субстрата.
В общих формулах (3) и (4) R обозначает заместитель, выбранный из группы, состоящей из C2-С8 алкильных групп, С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, включающих до 20 атомов углерода, аралкильных групп, включающих до 20 атомов углерода, углеводородной группы, содержащей гетероциклическое кольцо, и гидроксильной групы. В том случае, когда R включает ароматическое кольцо или гетероциклическое кольцо, указанное ароматическое кольцо или гетероциклическое кольцо могут быть далее замещены атомами галогена (атомом йода, атомом брома, атомом хлора, атомом фтора и т.п.), гидроксильной группой, алкильными группами, включающими до 3 атомов углерода, алкоксильными группами, включающими до 3 атомов углерода и аминогруппой.
R обозначает предпочтительно фенилметильную группу или 3-идолилметильную группу, особенно предпочтительно 3-идолилметильную группу. Конкретно, замещенная α-кетокислота общей формулы (3) представляет собой предпочтительно фенилпировиноградную кислоту или индол-3-пировиноградную кислоту, особенно предпочтительно индол-3-пировиноградную кислоту. Что касается индол-3-пировиноградной кислоты, то предпочтительна индол-3-пировиноградная кислота, полученная по способу, описанному в разделе [А] "Реакция 1". Однако, очевидно, что способ получения индол-3-пировиноградной кислоты не ограничивается указанным процессом.
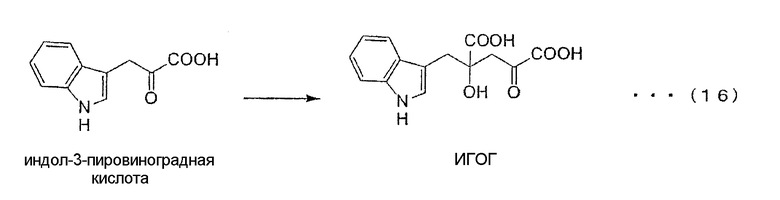
В том случае, когда индол-3-пировиноградная кислота используется в качестве замещенной α-кетокислоты общей формулы (3), ИГОГ как важное промежуточное соединение для получения монатина, может быть получена по указанной ниже процедуре (реакционная схема (16)).
В том случае, когда фенилпировиноградную кислоту используют в качестве замещенной α-кетокислоты общей формулы (3), ФГОГ (4-фенилметил-4-гидрокси-2-оксоглутаровая кислота) в качестве промежуточной кетокислоты в способе получения аналога монатина 4-фенилметил-4-гидроксиглютаминовой кислоты (ФГГ) может быть получена по приведенной ниже процедуре (реакционная схема (17)).
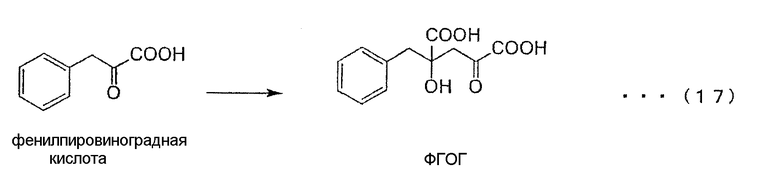
Способ проведения реакции 2 конкретно не ограничивается. При этом могут быть использованы любые системы химических реакций и ферментативных реакций. Способ проведения реакции 2 разделяется на системы химических реакций и ферментативные системы, которые ниже описываются в следующем порядке:
[B-1] система химической реакции;
[B-2] система ферментативной реакции;
[I] ферменты, используемые в реакции 2;
(1) ДНК, кодирующая альдолазу;
(2) свойства альдолазы;
(3) способ получения альдолазы;
[II] реакционные условия для проведения реакции 2;
(B-1) Система химической реакции
Реакция 2 с использованием системы химической реакции может быть успешно проведена с использованием описанного ниже способа, проиллюстрированного в приведенном примере 2, который, однако, не ограничивает рассматриваемый способ получения.
Так, например, замещенная α-кетокислота, описываемая приведенной ниже общей формулой (4), может быть получена с использованием замещенной α-кетокислоты общей формулы (3) и щавелевоуксусной кислоты для проведения перекрестной альдольной реакции и реакции декарбоксилирования. Соединение, получаемое в альдольной реакции, предварительно было получено в реакционной системе и представляет собой важный интермедиат. Следующая стадия декарбоксилирования может быть осуществлена без выделения указанного соединения.
Условия проведения альдольной реакции можно подобрать без каких-либо затруднений. Реакция может легко проходить только с использованием замещенной пировиноградной кислоты и щавелевоуксусной кислоты, которые могут вступать во взаимодействие друг с другом в соответствующем растворителе в присутствии неорганического основания или органического основания.
Тип растворителя, используемого в реакции, конкретно не ограничивается, при условии, что растворитель не активен в отношении компонентов реакции.
Специалист со средним уровнем знаний в данной области может без труда подобрать соответствующие температурные реакции, количество необходимого для использования основания, длительность реакции и способ добавления исходных материалов, которые будут укладываться в интервал значений, не оказывающих пагубного воздействия на осуществление настоящего изобретения.
Растворитель предпочтительно включает, например, полярные растворители, такие как вода, метанол, ацетонитрил и диметилформамид.
Основание, в случае его использования, предпочтительно включает, например, гидроксиды или карбонаты неорганических оснований, например, щелочных металлов или щелочноземельных металлов, включая гидроксид лития, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия и карбонат кальция, а также органические основания, например, триэтиламин.
Что касается температуры реакции, то предпочтительна температура примерно от -20°С до 100°С, более предпочтительна температура примерно от 0°С до 60°С.
Что касается реакции декарбоксилирования конденсата, получаемого в альдольной реакции, то указанная реакция может быть проведена путем спонтанного декарбоксилирования, однако декарбоксилирование может быть эффективно осуществлено при добавления кислоты или иона металла или их обоих к реакционному раствору. Подходящая для использования в данном случае кислота включает, например, хлористоводородную кислоту, серную кислоту, фосфорную кислоту, уксусную кислоту, п-толуолсульфоновую кислоту и твердые кислоты, такие как ионообменные смолы, а варианты иона металла включают, например, ионы переходного металла, такие как ион никеля, ион меди и ион железа. Что касается температуры реакции, то предпочтительно может быть выбрана температура примерно от -10°С до 100°С и более предпочтительно, температура примерно от 0°С до 60°С.
[В-2] Система ферментативной реакции
(1) Фермент, используемый в реакции 2
В качестве фермента, используемого в реакции 2, может использоваться, без каких-либо ограничений, любой фермент, катализирующий реакцию синтеза замещенной α-кетокислоты общей формулы (4) путем альдольной конденсации, осуществляемой между замещенной α-кетокислотой общей формулы (3) и щавелевоуксусной кислотой или пировиноградной кислотой. Иными словами, может успешно использоваться любой фермент, полученный из микроорганизмов или полученный методами генетической рекомбинации, при условии, что указанный фермент катализирует данную реакцию.
Исследования, проведенные авторами изобретения, подтвердили, что микробные штаммы, продуцирующие альдолазу с активностью по разложению 4-фенилметил-4-гидрокси-2-оксоглутаровой кислоты (ФГОГ), существуют в роде Pseudomonas, Erwinia, Flavobacterium и Xanthomonas.
Альдолаза, продуцируемая указанными микроорганизмами, катализирует реакцию разложения молекулы ФГОГ с образованием одной молекулы фенилпировиноградной кислоты и одной молекулы пировиноградной кислоты. Авторы изобретения полагают, что альдолаза может катализировать реакцию синтеза 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Исходя из этого предположения, авторы выделили и очистили альдолазу из культуры микробных клеток ряда микробных штаммов, с тем чтобы идентифицировать наличие новой альдолазы. Кроме того, авторы выявили, что благодаря наличию фермента, ИГОГ синтезируется путем альдольной конденсации, осуществляемой между индол-3-пировиноградной кислотой и пировиноградной кислотой (или щавелевоуксусной кислотой).
Что касается микробных ферментов, катализирующих реакцию альдольной конденсации двух молекул α-кетокислоты (и замещенной α-кетокислоты) в качестве субстрата, то на достигнутом уровне техники имеется сообщение о двух таких примерах, которые описывают альдолазу 4-гидрокси-4-метил-2-оксоглутарата из бактерии рода Pseudomonas и альдолазу 4-гидрокси-2-оксоглутарата из E. coli, B. subtilis и т.п. В указанном отчете показано, что указанная альдолаза 4-гидрокси-4-метил-2-оксоглутарата катализирует реакцию образования 4-гидрокси-4-метил-2-оксоглутарата (4-ГМГ) из двух молекул пировиноградной кислоты и реакцию образования одной молекулы щавелевоуксусной кислоты и одной молекулы пировиноградной кислоты из 4-оксалоцитрамалата (см. Kiyofumi Maruyama, Joirnal of Biochemisrty, 1990, 108, pp. 327-333). Кроме того, известно, что указанная альдолаза 4-гидрокси-2-оксоглутарата катализирует реакцию образования 4-гидрокси-2-оксоглутарата (4ГГ) из одной молекулы глиоксиловой кислоты и одной молекулы пировиноградной кислоты.
Однако, абсолютно отсутствует сообщение или какие-либо данные о наличии в любом из указанным микробных штаммов активности по разложению 4-фенилметил-4-гидрокси-2-оксоглутаровой кислоты (далее называемой как ФГОГ) или активности по синтезу кетокислотного предшественника монатина (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Совершенно неизвестно, может ли альдолаза, образованная указанными микробными штаммами, использоваться для целей указанного выше синтеза.
До открытия авторами настоящего изобретения, иными словами, в любом из имевшихся ранее отчетов, не было приведено примеров получения синтетическими способами кетокислоты-предшественника (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты) с использованием микробной ферментативной системы.
Дополнительно, авторы изобретения выделили и очистили альдолазу из Pseudomonas taetrolens ATCC4683 и определили аминокислотную последовательность полученной альдолазы. Кроме того, авторы осуществили успешный синтез молекулы ДНК размером примерно 30 нп на основе данных об аминокислотной последовательности альдолазы, провели выделение и регенерацию части ДНК, кодирующей альдолазу, с помощью ПЦР, а также выделение ДНК полной длины, кодирующей альдолазу Pseudomonas taetrolens, из библиотеки хромосомных генов Pseudomonas taetrolens с использованием полученного фрагмента ДНК в качестве зонда.
В приведенном перечне последовательность SEQ ID No. 1 представляет собой ДНК, кодирующую альдолазу по настоящему изобретению, идентифицированную по описанному выше методу. Дополнительно, последовательности SEQ ID No. 2 и 3 показывают аминокислотные последовательности альдолазы, кодируемой нуклеотидной последовательностью SEQ ID No. 1, приведенной в перечне последовательностей. SEQ ID No. 2 в перечне последовательностей представляет собой аминокислотную последовательность альдолазы, которая кодируется нуклеотидной последовательностью на участке от 456-ого до 1118-ого положения в нуклеотидной последовательности SEQ ID No. 1, приведенной в перечне последовательностей. Дополнительно, SEQ ID No. 3 в перечне последовательностей показывает аминокислотную последовательность альдолазы, кодируемой нуклеотидной последовательностью на участке от 444-ого до 1118-го положения в нуклеотидной последовательности SEQ ID No. 1. Любая альдолаза, описанная в виде SEQ ID No. 2 и 3, обладает альдолазной активностью и катализирует реакцию синтеза 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ) из одной молекулы индол-3-пировиноградной кислоты и одной молекулы пировиноградной кислоты (или щавелевоуксусной кислоты).
(1) ДНК, кодирующая альдолазу
Как указывалось выше, ген альдолазы с нуклеотидной последовательностью SEQ ID No. 1, приведенной в перечне последовательностей, был выделен из хромосомной ДНК Pseudomonas taetrolens, штамм ATCC4683. Нуклеотидная последовательность SEQ ID No. 1, приведенная в перечне последовательностей, обладает 29% гомологией с известной альдолазой 4-гидрокси-4-метил-2-оксоглутарата (наименование гена: proA), выделенной из бактерии Pseudomonas ochraceae (см. Maruyma K., et al., Biosci. Biotechnol. Biochem., 2001, 65 (12), pp. 2701-2709) по аминокислотной последовательности. Исходя из этого, вычисляется гомология с использованием программного обеспечения для генного анализа "genetyx ver. 6" и с использованием других исходно установленных параметров.
Ниже описывается способ получения ДНК, кодирующей альдолазу, из бактерии, продуцирующей альдолазу.
Вначале определяют аминокислотную последовательность очищенной альдолазы. Аминокислотная последовательность может быть определена по методу Эдмана (Edman, P., Acta Chem. Scand., 1950, 4, p. 227). С использованием секвенатора Applied Biosystems Inc., может быть проведено альтернативное определение аминокислотной последовательности. Альдолаза, полученная из Pseudomonas taetrolens штамм ATCC4683, по настоящему изобретению разлагается протеазой в ограниченных размерах. Полученные пептидные фрагменты отделяют и регенерируют с помощью ВЭЖХ с обращением фазы. Определяют внутренние аминокислотные последовательности двух указанных фрагментов, которые были идентифицированы как последовательности SEQ ID No. 4 и 5.
На основе идентифицированных последовательностей, может быть далее вычислена нуклеотидная последовательность ДНК, кодирующей указанную последовательность. Для вычисления нуклеотидной последовательностью ДНК используют универсальные кодоны.
На основе вычисленной нуклеотидной последовательности получают синтетическим способом молекулы ДНК размером 30 нуклеотидных пар. Способ получения ДНК путем синтеза описан в литературе (Tetrahedron Letters, 1981, 22, p. 1859). Дополнительно, молекула ДНК может быть синтезирована с использованием синтезатора Applied Biosystems Inc. Молекула ДНК может быть использована в качестве зонда для выделения ДНК полной длины, кодирующей альдолазу из библиотеки хромосомных генов микроорганизма, продуцирующего альдолазу. В ином случае, молекула ДНК может использоваться в качестве праймера для амплификации ДНК, кодирующей альдолазу по настоящему изобретению, методом ПЦР. Поскольку ДНК, амплифицированная по методу ПЦР, никогда не содержит ДНК полной длины, кодирующей альдолазу, используют ДНК, амплифицированную методом ПЦР, для выделения ДНК полной длины, кодирующей альдолазу, из библиотеки хромосомных генов микроорганизма, продуцирующего альдолазу.
Процедура проведения ПЦР описана в литературе (White, T. J., et al., Trends Genet. 5, 1989, p. 185). Указанный способ получения хромосомной ДНК и способ выделения желательной молекулы ДНК из генной библиотеки с использованием молекулы ДНК в качестве зонда, описаны в соответствующем руководстве (Molecular Cloning, 2nd edition, Cold Spring Harbor press, 1989).
Способ определения нуклеотидной последовательности выделенной ДНК, которая кодирует альдолазу, описан в соответствующем руководстве (A Practical Guide to Molecular Cloning, John Wiley & Sons, Inc., 1985). Нуклеотидная последовательность может быть также определена с использованием секвенатора ДНК производства компании Applied Biosystems Inc. SEQ ID No. 1 в перечне последовательностей показывает ДНК, кодирующую альдолазу, полученную из Pseudomonas taetrolens, штамм ATCC4683.
ДНК, приведенная в виде SEQ ID No. 1, не является единственной ДНК, кодирующей альдолазу, которая катализирует реакцию синтеза ИГОГ из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Иными словами, вполне очевидно, что каждый вид и каждый штамм из рода Pseudomonas, продуцирующий альдолазу, которая катализирует реакцию синтеза ИГОГ из индол-3 пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты), будет иметь отличительные особенности в своей нуклеотидной последовательности.
Вполне очевидно, что даже ДНК, полученная в результате искусственной мутации ДНК, кодирующей альдолазу, и выделенная из хромосомной ДНК бактерии, продуцирующей альдолазу, может также использоваться в реакции 2, в том случае, если указанная искусственная ДНК кодирует альдолазу. Сайт-специфичная мутация, описанная в соответствующем руководстве (Method. in Enzymol; 1987, p. 154), часто используются в качестве способа внесения такой искусственной мутации.
Дополнительно, ДНК, гибридизирующаяся с ДНК, имеющей нуклеотидную последовательность, комплементарную к нуклеотидной последовательности SEQ ID No. 1, показанной в перечне последовательностей, в жестких условиях и кодирующая белок с альдолазной активностью, может быть также использована в реакции 2. В настоящем описании термин "жесткие условия" обозначает условия образования так называемого специфического гибрида, но не образования неспецифических гибридов. Хотя трудно четко проиллюстрировать такие условия в числовых параметрах, можно привести один следующий пример: в указанных условиях ДНК с высокой гомологией, составляющей примерно 50% или более, предпочтительно 80% или более, более предпочтительно 90% или более и особенно предпочтительно 95% или более, могут гибридизироваться друг с другом, но ДНК с меньшей гомологией не могут гибридизироваться друг с другом (термин гомология предпочтительно используется для выражения величины, вычисленной для сравниваемых последовательностей, когда число одинаковых оснований является наибольшим). В ином случае, указанные условия являются условиями, позволяющими осуществлять гибридизацию при концентрации соли, соответствующей основным условиям промывки в методе по Саузерен-гибридизации, а именно: 0,1 х SSC, 0,1% х ДСН при 37°С, предпочтительно 0,1 х SSC, 0,1% х ДСН при 60°С, более предпочтительно 0,1 х SSC, 0,1% х ДСН при 65°С. Далее термин "активность альдолазы" обозначает активность в отношении ИГОГ, синтетически полученной из индол-3 пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). В случае нуклеотидной последовательности, гибридизирующейся с нуклеотидной последовательностью, комплементарной нуклеотидной последовательности SEQ ID No. 1, показанной в перечне последовательностей, в жестких условиях, активность составляет 10% или более, предпочтительно 30% или более, более предпочтительно 50% или более, еще более предпочтительно 70% или более, от альдолазной активности белка с аминокислотной последовательностью SEQ ID No. 2 или 3, показанной в перечне последовательностей, при 33°С и при pH 9.
Далее, ДНК, кодирующая по существу тот же белок, что и альдолаза, кодируемая ДНК, описанная как SEQ ID No. 1, может также использоваться для реакции 2. Другими словами, приведенная ниже ДНК также включаются в область настоящего изобретения как соответствующая ДНК.
(a) ДНК, кодирующая белок с аминокислотной последовательностью SEQ ID No. 2, показанной в перечне последовательностей.
(b) ДНК, кодирующая белок с аминокислотной последовательностью, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 2, показанной в перечне последовательностей, и обладающей альдолазной активностью.
(с) ДНК, кодирующая белок с аминокислотной последовательностью SEQ ID No. 3, показанной в перечне последовательностей.
(d) ДНК, кодирующая белок с аминокислотной последовательностью, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 3, приведенной в перечне последовательностей, и обладающей альдолазной активностью.
В настоящем описании термин "один или несколько" обозначает диапазон аминокислотных остатков, которые могут использоваться без внесения серьезного ухудшения в пространственную структуру полученного белка или в альдолазную активность, и конкретно включает от одного до 50, предпочтительно от одного до 30, более предпочтительно от одного до 10. Как указывалось выше, термин "активность альдолазы" дополнительно обозначает активность в отношении синтеза ИГОГ из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). В случае аминокислотной последовательности, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 2, приведенной в перечне последовательностей, полученная альдолазная активность в условиях температуры 33°С и pH 9 составляет 10% или более, предпочтительно 30% или более, более предпочтительно 50% или более и еще более предпочтительно 70% или более от альдолазной активности белка с аминокислотной последовательностью SEQ ID No. 2 или 3, показанной в перечне последовательностей, при 33°С и при pH 9.
(2) Свойства альдолазы
Далее описываются свойства альдолазы, выделенной и очищенной из Pseudomonas taetrolens, штамм ATCC4683.
Альдолаза, полученная из Pseudomonas taetrolens, штамм ATCC4683, имеет аминокислотную последовательность SEQ ID No. 2 или 3, как было четко показано при выделении и анализе описанного выше гена. Однако, очевидно, что белок с аминокислотной последовательностью, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 2 или 3, приведенной в перечне последовательностей, и обладающей альдолазной активностью, также может использоваться в реакции 2.
Иными словами, приведенные ниже белки (а) - (d) могут также использоваться в качестве фермента, катализирующего реакцию 2.
(a) Белок с аминокислотной последовательностью SEQ ID No. 2, приведенной в перечне последовательностей.
(b) Белок с аминокислотной последовательностью, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 2, приведенной в перечне последовательностей, и обладающий альдолазной активностью.
(с) Белок с аминокислотной последовательностью SEQ ID No. 3, приведенной в перечне последовательностей.
(d) Белок с аминокислотной последовательностью, полученной после замены, делеции, вставки, добавления или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID No. 3, приведенной в перечне последовательностей, и обладающий альдолазной активностью.
В настоящем описании термины "несколько" и "альдолазная активность" имеют те же значения, что и в описании, приведенном в разделе "ДНК, кодирующая альдолазу" (1).
Такая альдолаза может катализировать реакцию синтеза 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ) путем альдольной конденсации из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты).
Альдолазную активность альдолазы можно определить путем измерения количества ИГОГ, образованного из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты), методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Конкретно, альдолазная активность может быть определена при добавлении альдолазы к реакционному раствору, содержащему 100 мМ буфера, 50 мМ из индол-3-пировиноградной кислоты, 250 мМ пировиноградной кислоты, 1 мМ MgCl2, и 1 объемн.% толуола, для проведения реакции при встряхивании при 33°С в течение 4 часов, с последующим измерением количества образованного ИГОГ с помощью ВЭЖХ.
ИГОГ может быть определена количественно методом ВЭЖХ с использованием колонки Inertsil ODS-2 (5 мкм, 4,6 x 250 мм), производство компании GL Science, Inc. Один из примеров условий анализа приведен ниже.
Мобильная фаза: 40 объемн.% ацетонитрила/5 мМ раствор дигидрофосфата в тетрабутиламмонии
Скорость течения: 1 мл/мин
Температура колонки: 40°С
Обнаружение: УФ, длина волны 210 нм
Ниже описаны ферментативные и химические свойства альдолазы, полученной из Pseudomonas taetrolens, определяемые с использованием указанного выше метода анализа.
Альдолаза, полученная из Pseudomonas taetrolens, может катализировать реакцию синтетического получения ИГОГ путем альдольной конденсации индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Относительно микробных ферментов, катализирующих альдольную конденсацию из двух молекул α-кетокислоты (или замещенной α-кетокислоты) в качестве субстрата, имеется сообщение о двух таких ферментах, которые представляют собой альдолазу 4-гидрокси-4-метил-2-оксоглутаровой кислоты из бактерий рода Pseudomonas и альдолазу 4-гидрокси-2-оксоглутарата, имеющуюся в E. coli и B. subtilis. Однако, абсолютно нет каких-либо данных относительно их взаимодействия с ФГОГ и ИГОГ. В этой связи, абсолютно неизвестно, может или нет ФГОГ (и ИГОГ) быть получен синтетическим способом с использованием фермента. Кроме того, не было найдено активности по разложению ФГОГ, в связи с чем синтез ФГОГ (и ИГОГ) с использованием фермента становится невозможным. Иными словами, альдолаза, полученная из Pseudomonas taetrolens, обладает характерным свойством катализировать реакцию синтеза ИГОГ путем альдольной конденсации индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты), что отличает ее от альдолазы, описанной ранее.
Оптимум pH для альдолазы, полученной из Pseudomonas taetrolens, составляет примерно 9 при 33°С.
Молекулярная масса альдолазы, полученной из Pseudomonas taetrolens, при измерении методом гель-фильтрации составляет примерно 146 кДа, а при измерении электрофорезом в ДСН-ПААГ - примерно 25 кДа. В этой связи, следует полагать, что альдолаза по настоящему изобретению, возможно, образует гомогексамер, состоящий из единиц с молекулярной массой примерно 25 кДа.
(3) Способ получения альдолазы
Ниже описывается способ получения альдолазы. Способ получения альдолазы с целью использования в реакции 2 по настоящему изобретению включает два процесса, а именно: (i) процесс образования и накопления альдолазы путем культивирования в микробиологически приемлемых условиях бактерии, продуцирующей альдолазу, и (ii) способ образования и накопления альдолазы путем образования методами рекомбинантной ДНК трансформанта, образующего альдолазу, с последующим культивированием трансформанта.
(i) Способ образования и накопления альдолазы при микробном культивировании
Для способа образования и накопления альдолазы путем культивирования бактерии, образующей альдолазу, микроорганизм, используемый в качестве источника альдолазы, включает, например, микроорганизмы, принадлежащие к роду Pseudomonas, Erwinia, Flavobacterium и Xanthomonas.
Среди представителей рода Pseudomonas, Erwinia, Flavobacterium и Xanthomonas может использоваться, в соответствии с настоящим изобретением, любой микроорганизм, образующий альдолазу, которая катализирует реакцию синтеза предшественника кетокислоты (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты). Предпочтительно указанный микроорганизм включает Pseudomonas taetrolens ATCC4683, Pseudomonas coronafaciens AJ2791, Pseudomonas desmolytica AJ1582, Erwinia sp. AJ2917, Xanthomonas citri AJ2797 и Flavobacterium rhenanum AJ2468. Среди них особенно предпочтительны Pseudomonas taetrolens ATCC4683 и Pseudomonas coronafaciens AJ2791. Организации, осуществляющие депонирование указанных микроорганизмов, приведены ниже.
(1) Pseudomonas coronafaciens, штамм AJ2791
(a) No. доступа FERM BP-8246 (перенесен из FERM P-18881 в Международный Депозитарий 22 ноября 2002 года)
(b) Дата депонирования: 10 июня 2002 года
(c) Депозитарий: Международный Депозитарий патентованных организмов (International Patent Organism Depositary), Институт современной промышленной науки и технологии (Institute of Advanced Industrial Science and Technology, No.6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония)
(2) Pseudomonas desmolytica AJ1582
(a) Номер доступа: No. FERM BP-8247 (перенесен из FERM P-18882 в Международный Депозитарий 22 ноября 2002 года)
(b) Дата депонирования: 10 июня 2002 года
(c) Депозитарий: Международный Депозитарий патентованных организмов (International Patent Organism Depositary), Институт современной промышленной науки и технологии (Institute of Advanced Industrial Science and Technology No.6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония)
(3) Erwinia sp. AJ2917
(a) No. доступа FERM BP-8245 (перенесен из FERM P-18880 в Международный Депозитарий 22 ноября 2002 года)
(b) Дата депонирования: 10 июня 2002 года
(c) Депозитарий: Международный Депозитарий патентованных организмов (International Patent Organism Depositary), Институт современной промышленной науки и технологии (Institute of Advanced Industrial Science and Technology No.6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония)
(4) Flavobacterium rhenanum AJ2468
(a) No. доступа FERM BP-1862
(b) Дата депонирования: 30 сентября 1985 года
(с) Депозитарий: Международный Депозитарий патентованных организмов (International Patent Organism Depositary), Институт современной промышленной науки и технологии (Institute of Advanced Industrial Science and Technology No.6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония)
(5) Xanthomonas citri AJ2797
(a) No. доступа FERM BP-8250 (перенесен из FERM P-4347 в Международный Депозитарий 27 ноября 2002 года)
(b) Дата депонирования: 30 сентября 1985 года
(с) Депозитарий: Международный Депозитарий патентованных организмов (International Patent Organism Depositary), Институт современной промышленной науки и технологии (Institute of Advanced Industrial Science and Technology No.6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония)
Способ культивирования микроорганизма, используемого в качестве источника получения альдолазы, может включать любую жидкую культуру и твердую культуру. Удобный для использования в промышленных масштабах способ включает погруженную аэрируемую культуру. В качестве источника питательных компонентов в питательных культуральных средах обычно используются те компоненты, которые обычно применяют для культивирования микробов, такие как источники углерода, источники азота, неорганические соли и других следовых количеств питательных компонентов. Могут также использоваться микробные штаммы, утилизирующие любые источники питательных компонентов.
Для создания условий аэрирования приемлемы любые условия. Температура культивирования может находиться в диапазоне, приемлемом для роста микробов, продуцирующих альдолазу. Иными словами, не существует строгих условий культивирования. В основном температура составляет от 10 до 50°С, предпочтительно от 30 до 40°С. Длительность процесса культивирования варьируется в зависимости от других условий культивирования. Так, например, время культивирования может достигать периода, включающего максимальную продукцию альдолазы, что составляет примерно от 5 часов до 7 дней, предпочтительно от 10 часов до 3 дней.
После культивирования микробные клетки собирают центрифугированием (например, со скоростью 10000 x g в течение 10 минут). В связи с тем, что альдолаза содержится в наибольших количествах в микробных клетках, такие микробные клетки разрушают или лизируют для солюбилизации альдолазы. С целью разрушения микробной клетки используют обработку, такую как ультразвуковое разрушение, разрушение под френч-прессом и разрушение стеклянными шариками. В случае лизиса может использоваться дополнительная обработка лизоцимом яичного белка или пептидазой, или соответствующее сочетание таких видов обработки.
Для очистки альдолазы, полученной из бактерии, продуцирующей альдолазу, используют в качестве исходного материала для очистки раствора с солюбилизированным ферментом. В том случае, когда остается неразрушенный или нелизированный остаток, солюбилизированный раствор подвергают повторным процедурам центрифугирования для удаления осажденного остатка, который подвергают вновь очистке.
В целом, для очистки альдолазы может использоваться любой традиционный способ очистки ферментов, включающий, например, высаливание сульфатом аммония, гель-фильтрационную хроматографию, ионообменную хроматографию, гидрофобную хроматографию и хроматографию на гидроксиапатите. При этом могут быть получены фракции, содержащие альдолазу с более высокой активностью.
(ii) Способ получения с использованием методик рекомбинантной ДНК
Ниже описывается способ получения альдолазы с использованием методик рекомбинантной ДНК. Известно множество способов получения полезных белков, таких как ферменты и физиологически активные вещества, с использованием методик рекомбинантной ДНК. С использованием методик рекомбинантной ДНК могут быть получены в крупных масштабах полезные белки, которые встречаются в природе лишь в следовых количествах.
Любая ДНК, подлежащая конъюгированию с векторной ДНК, может быть приемлема, если указанная ДНК может экспрессировать альдолазу.
В качестве примера гена альдолазы, конъюгированного с векторной ДНК, может быть использована приведенная в настоящем описании (1) ДНК в разделе "ДНК, кодирующая альдолазу".
В случае получения массы белка с использованием методик рекомбинантной ДНК предпочтительно, чтобы указанный белок был связан вместе с трансформантом с образованием белкового тела включения. Ниже приводится перечень преимуществ описываемого способа экспрессии и получения. Целевой белок может быть защищен от расщепления протеазой в микробных клетках, и указанный целевой белок может быть выделен и очищен простым способом путем центрифугирования с последующим разрушением микробных клеток.
Белковое тело включения, получаемое при таком способе, солюбилизируют с использованием средства, денатурирующего белок, и далее обрабатывают с помощью процедуры, направленной на восстановление активности с последующим удалением в основном денатурирующего средства, и затем превращают его в физиологически активный белок, обладающий правильной складчатой структурой. В частности, имеется много такого рода примеров, в частности, регенерация активности человеческого интерлейкина-2 (JP-A-61-257931).
Таким образом, для получения активного типа белка из такого белкового тела включения требуется серия процедур, таких как солюбилизация и регенерация активности, и они более сложны, чем процедуры, направленные на непосредственное получение активного типа белка. В случае получения массы белка, оказывающего влияние на рост микробной клетки, указанное воздействие может быть подавлено путем накопления белка в виде неактивного белкового тела включения в микробной клетке.
Способ получения массы целевого белка в виде тела включения охватывает однократную экспрессию целевого белка под контролем сильного промотора и способ экспрессии целевого белка в виде белка слияния с белком, в отношении которого известно, что он экспрессируется в крупных масштабах.
После экспрессии белка в виде белка слияния, с тем чтобы удалить белок слияния и достичь эффективного получения целевого белка, распознаваемые последовательности рестрикционных протеаз в соответствующих сайтах должны быть определенным образом ориентированы.
В случае получения массы белка с использованием методики рекомбинантной ДНК в качестве хозяйских клеток для трансформации могут быть использованы микробные клетки, клетки актиномицетов, дрожжевые клетки, грибные клетки, растительные клетки и клетки животных. Микробные клетки, для которых разработаны системы хозяин-вектор, включают, например, микроорганизм из рода Escherichia, микроорганизм из рода Pseudomonas, микроорганизм из рода Corynebacterium и микроорганизм из рода Bacillus. Предпочтительно использовать Escherichia coli, поскольку имеются многочисленные опытные данные относительно методик использования Escherichia coli для получения белка в крупных масштабах. Ниже будет описан способ получения альдолазы с использованием Escherichia coli.
В качестве промотора для экспрессии ДНК, кодирующей альдолазу, в основном могут использовать промоторы Escherichia coli для получения экзогенного белка, которые включают, например, сильные промоторы, такие как промотор Т7, trp промотор, lac промотор, tac промотор и PL промотор.
Для получения альдолазы в теле включения белка слияния ген, кодирующий другой белок, предпочтительно гидрофильный пептид, конъюгируют вверх по направлению транскрипции гена или вниз по направлению транскрипции гена альдолазы с получением гена белка слияния. Ген, кодирующий такой другой белок, может представлять собой любой ген, способный повышать накопление белка слияния и усиливать растворимость белка слияния после стадий денатурации и регенерации. Например, могут найти потенциальное применение ген 10 из Т7, ген β-галактозидазы, ген дегидрофолиат-восстанавливающего фермента, ген γ-интерферона, ген интерлейкина-2 и ген прохимозина.
Для конъюгации указанных генов с геном, кодирующим альдолазу, указанные гены должны иметь одну рамку считывания их кодонов. Указанные гены конъюгируют в соответствующих сайтах рестрикции или конъюгируют с использованием синтетической ДНК с подходящей последовательностью.
Далее, для повышения получаемого количества предпочтительно конъюгируют терминатор в виде последовательности терминации транскрипции вниз по направлению транскрипции гена белка слияния. Терминатор включает, например, терминатор Т7, терминатор фага fd, терминатор T4, терминатор для гена устойчивости к тетрациклину и терминатор из Escherichia coli для гена trpA.
Вектор для введения гена, кодирующего альдолазу, или гена, кодирующего белок слияния альдолазы с другим белком, предпочтительно относится к так называемому мультикопийному типу и включает, например, плазмиду с ориджином репликации, полученным из Col E1, такой как плазмида на основе pUC, плазмида на основе pBR322 или их производные. В настоящем описании термин "производное" обозначает такие плазмиды, которые были денатурированы путем замещения, делеции, вставки, добавления или инверсии нуклеотидов. В настоящем описании термин "денатурация" означает мутагенную обработку с использованием мутагенов и УФ излучения или спонтанную мутацию.
Для целей скрининга трансформантов вектор предпочтительно включает маркеры, такие как ген устойчивости к ампициллину. В качестве такой плазмиды могут использоваться коммерчески доступные векторы экспрессии с сильными промоторами (серия pUC (производство TAKARA BIO INC.), серия pPROK (производство Clontech Laboratories, Inc.), серия pKK233-2 (производство Clontech Laboratories, Inc.).
Фрагмент ДНК, в котором промотор, ген, кодирующий альдолазу, или ген, кодирующий белок слияния альдолазы с другим белком, и терминатор последовательно конъюгированы друг с другом в указанном порядке, подвергают конъюгированию с векторной ДНК с образованием рекомбинантной ДНК.
С использованием рекомбинантной ДНК проводят трансформацию Escherichia coli. Полученную Escherichia coli культивируют для экспрессии и генерирования альдолазы или белка слияния альдолазы с другим белком. В качестве хозяйской клетки, подлежащей трансформации, могут быть использованы штаммы, которые в основном используют для экспрессии экзогенного гена. В частности, предпочтительно используют Escherichia coli штаммы JM109 (DЕ3) и JM109. Способ указанной трансформации и способ скрининга полученного трансформанта описан в соответствующих руководствах (Molecular Cloning, 2-nd edition, Cold Spring Harbor press, 1989 и т.п.).
В случае экспрессии в виде белка слияния, альдолаза может быть успешно разрезана с использованием рестрикционных протеаз, таких как фактор Ха коагуляции крови и калликреин, который распознает последовательности, никогда не присутствующие в альдолазе, в качестве распознаваемых последовательностей.
В качестве культуральной среды для продуцирования могут использоваться культуральные среды для обычных случаев культивирования Escherichia coli, такие как культуральная среда с казаминовыми кислотами М9 и культуральная среда LB. Дополнительно, могут быть выбраны соответствующим образом условия культивирования и условия индукции продуцирования, в зависимости от типа маркера, промотора и хозяйской бактерии для данного используемого вектора.
Для регенерации альдолазы или белка слияния с другим белком используют указанные ниже способы. В том случае, когда альдолаза или белок слияния солюбилизированы в микробных клетках, регенерируют микробные клетки, которые затем разрушают или лизируют с целью последующего использования в виде раствора неочищенного фермента. Далее, при необходимости, альдолаза и ее белок слияния перед использованием могут быть очищены с использованием обычных методов, таких как осаждение, фильтрование и колоночная хроматография. В данном случае могут также использоваться способы очистки с применением антител против альдолазы или белка слияния.
Тело белка включения при его формировании солюбилизируют с использованием денатурирующего средства. Белковое тело включения может быть солюбилизировано вместе с белком микробной клетки. В контексте последующего процесса очистки тело включения предпочтительно отбирают и затем солюбилизируют. Тело включения может быть восстановлено из микробных клеток известными в данной области техники способами. Так, например, микробные клетки разрушают с целью восстановления тела включения путем центрифугирования и т.п. Денатурирующее средство для солюбилизации белкового тела включения включает, например, гидрохлорид гуанидина (например, 6М, pH 5-8) и мочевину (например, 8М).
При удалении указанных денатурирующих средств путем диализа и т.п. полученный белок может быть восстановлен в виде белка с нужной активностью. В качестве диализирующего раствора, используемого в ходе диализа, может быть использован Tris-HCl буфер и фосфатный буфер. Концентрация указанного буфера составляет, например, от 20 мМ до 0,5 М при pH 5-8.
Концентрацию белка на стадии регенерации предпочтительно снижают до примерно 500 мкг/мл или менее. Для того чтобы подавить процесс самосшивки регенерированной альдолазы, температуру в ходе диализа поддерживают на уровне предпочтительно 5°С или ниже. Способ удаления денатурирующего средства включает процесс разбавления и процесс ультрафильтрования, кроме процесса диализа. Использованием любого из указанных способов можно достичь регенерации нужной активности.
В том случае, когда ген альдолазы получают из микроорганизма рода Pseudomonas, альдолаза дополнительно, в виде предпочтительного варианта осуществления изобретения, может быть экспрессирована и генерирована в хозяйском организме рода Pseudomonas. Так например, Shi-En Lu, et. al. описали способ трансформации и экспрессии в Pseudomonas syringae, взятой в качестве хозяйской клетки (FEMS Microbiology Letters, 2002, 210, pp. 115-121). Кроме того, дополнительно Olsen, R.H. et al. опубликовали сообщение о методе трансформации и экспрессии в клетках Pseudomonas aerugenosa (Journal of Bacteriology, 1982, 150, pp. 60-69). Далее, Grapner et al. опубликовали сообщение о методе трансформации и экспрессии в клетках Pseudomonas stutzeri (Biomol. Eng., 2000, 17, pp. 11-16). Однако, экспрессия альдолазы не ограничивается указанными микроорганизмами из рода Pseudomonas, используемыми в качестве хозяйских клеток.
Что касается вектора для введения гена альдолазы в микроорганизм из рода Pseudomonas, то можно указать на использование плазмиды с ориджином репликации, функционирующим внутри клеток микроорганизмов рода Pseudomonas. Так например, Eza Kalyaeva et al. сообщает о плазмиде pKLH4.05 с репликоном TFK, функционирующим а клетках Pseudomonas aeruginosa. Дополнительно, могут использоваться так называемые векторы для широкого перечня хозяйских организмов, которые используются для трансформации Грам-отрицательного микроорганизма. Среди указанных векторов известны, например, RK404, (Ditta, G. et al., Plasmid, 1985, 13, pp. 149-153) и RSF1010 (Frey, J., et al., Gene, 1982, 24, pp. 289-296), функционирующие в микроорганизме рода Pseudomonas.
В том случае, когда в качестве ДНК, кодирующей альдолазу, используют ДНК с SEQ ID No. 1, показанной в перечне последовательностей, получают альдолазу с аминокислотной последовательностью SEQ ID No. 2 или 3.
(II) Реакционные условия для проведения реакции 2
Ниже описаны реакционные условия для проведения реакции 2 в случае использования ферментативной системы.
В качестве фермента, катализирующего реакцию 2, может использоваться без конкретного ограничения любой фермент, катализирующий реакцию синтеза замещенной α-кетокислоты, описываемой общей формулой (4), путем альдольной конденсации замещенной α-кетокислоты, описываемой общей формулой (3), и щавелевоуксусной кислоты или пировиноградной кислоты. Иными словами, любой фермент, полученный из микроорганизмов или созданный методами генной инженерии, может быть удовлетворительно использован в данной реакции, при условии, что данный фермент катализирует реакцию.
В качестве такого фермента предпочтительна альдолаза, описанная в Разделе (I) "Фермент, используемый в реакции 2". В данном случае может использоваться альдолаза, получаемая при культивировании микробных клеток, продуцирующих альдолазу, которая катализирует реакцию 2 в клетках представителей рода Pseudomonas, Erwinia, Flavobacterium и Xanthomonas. Альтернативно, может использоваться альдолаза, получаемая при создании трансформанта, продуцирующего альдолазу, которая катализирует реакцию, с использованием методики рекомбинантной ДНК с последующим культивированием трансформанта.
Термин "в присутствии фермента" в контексте реакции 2 означает, что в данной реакционной системе разрешается присутствие фермента и при этом фермент находится в таком состоянии, которое позволяет осуществлять катализ реакции синтетического получения замещенной α-кетокислоты, описываемой общей формулой (4), из замещенной α-кетокислоты, описываемой общей формулой (3), и щавелевоуксусной кислоты или пировиноградной кислоты. Так, например, фермент может быть один раз добавлен к реакционной системе или микроорганизм, содержащий активность данного фермента (микроорганизм, продуцирующий альдолазу, клетки, трансформированные рекомбинантной ДНК), культура микроорганизма (жидкая культура, твердая культура и т.п.), культуральная среда (среда, из которой удалены микробные клетки) и обработанные продукты из культуры могут быть добавлены к реакционной системе. В случае использования культуры микроорганизма развивается реакция 2 при одновременном культивировании микроорганизма. В ином случае, реакция 2 удовлетворительно проходит при использовании культуры, получаемой путем предварительного культивирования с целью получения фермента. Дополнительно, термин "обработка" означает обработку с целью выделения фермента из микробных клеток и включает, например, способы обработки с использованием ультразвука, стеклянных шариков, френч-пресса и лиофильной сушки, а также способы обработки лизирующими ферментами, органическими растворителями, детергентами и т.п. Дополнительно, может с успехом использоваться любой полученный в ходе фракционирования неочищенный фермент или очищенный фермент, получаемый путем дальнейшей обработки продукта, получаемого после обработки рутинными способами (с использованием жидкостной хроматографии, фракционирования сульфатом аммония и т.п.) при условии, что указанные неочищенный или очищенный фермент обладают требуемой способностью.
В случае получения замещенной α-кетокислоты общей формулой (4) с использованием бактерии, продуцирующей альдолазу, или клетки, трансформированной рекомбинантной ДНК, субстраты могут быть добавлены к жидкой культуре в процессе культивирования. В ином случае, могут использоваться микробные клетки после отделения их от жидкой культуры и промытые микробные клетки. Дополнительно, может использоваться продукт в виде обработанных микробных клеток, полученный после разрушения или лизирования микробных клеток, или используют альдолазу, регенерированную из такого продукта в виде обработанных микробных клеток, как раствор неочищенного фермента, из которого фермент затем выделяют, чистят и используют.
В случае использования культуры или обработанного продукта указанные культура или обработанный продукт могут быть включены в состав каррагенана и полиакриламида или они могут быть иммобилизованы на пленке из полиэфирсульфона и регенерированной целлюлозы для дальнейшего использования.
Для развития реакции 2 в присутствии фермента реакционный раствор, содержащий по меньшей мере одну замещенную α-кетокислоту, описываемую общей формулой (3), щавелевоуксусную кислоту или пировиноградную кислоту и фермент, катализирующий реакцию 2, доводят до соответствующей температуры от 20°С до 50°С, при которой раствор оставляют выстаиваться или перемешивают, поддерживая значение pH от 6 до 12 в течение периода времени от 30 минут до 5 дней.
Скорость реакции может быть повышена при добавлении к реакционному раствору двухвалентных катионов, таких как Mg2+, Mn2+, Ni2+ и Co2+. С точки зрения стоимости, иногда предпочтительно использовать Mg2+.
Для добавления указанных двухвалентных катионов к реакционному раствору может с успехом использоваться любая соль, при условии, что указанная соль не будет ингибировать реакцию. Предпочтительно, используют MgCl2, MgSO4, MnSO4 и т.п. Специалист в данной области может легко определить необходимую для добавления концентрацию указанных двухвалентных катионов с помощью простых предварительных экспериментов. Двухвалентные катионы могут быть добавлены в диапазоне от 0,01 мМ до 10 мМ, предпочтительно от 0,1 мМ до 5 мМ и более предпочтительно от 0,5 мМ до 2 мМ.
Ниже описан один пример, иллюстрирующий условия реакции, предпочтительные для проведения реакции 2. К реакционному раствору, состоящему из 100 мМ буфера, 50 мМ индол-3-пировиноградной кислоты, 250 мМ пировиноградной кислоты, 1 мМ MgCl2, и 1 объемн.% толуола добавляют в качестве источника фермента промытые клетки Escherichia coli, экспрессирующие альдолазу, до концентрации 10% (вес/объем) для проведения реакции при встряхивании при температуре 33°С в течение 4 часов с получением 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ).
Полученная замещенная α-кетокислота, описываемая общей формулой (4), может быть выделена и очищена известными способами. Один из таких способов включает, например, способ приведения замещенной α-кетокислоты в контакт с ионообменной смолой для абсорбции основных аминокислот и элюции с последующей кристаллизацией полученной замещенной α-кетокислоты; а также способ элюции замещенной α-кетокислоты, обесцвечивания и фильтрования замещенной α-кетокислоты на активированном древесном угле с последующей кристаллизацией замещенной α-кетокислоты.
С помощью реакции 2 кетокислота (ИГОГ), как предшественник, используемая в качестве интермедиата при синтезе монатина, может быть получена из индол-3-пировиноградной кислоты и пировиноградной кислоты (или щавелевоуксусной кислоты).
[C] Реакция 3
Реакция 3 по настоящему изобретению представляет собой реакцию, направленную на образование монатина, и которая предпочтительно используется для синтеза монатина из предшественника кетокислоты (ИГОГ). Однако, реакция 3 может использоваться не только для синтеза монатина, но также может широко использоваться для проведения реакции образования производных глютамата общей формулы (2) из замещенной α-кетокислоты общей формулы (1).


В приведенных формулах R1 и R2 независимо обозначают заместитель, выбранный из группы, состоящей из атома водорода, С1-С8 алкильных групп, С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, включающих до 20 атомов углерода, аралкильных групп, включающих до 20 атомов углерода, углеводородной группы, содержащей гетероциклическое кольцо, и гидроксильной группы. В том случае, когда один из R1 и R2 обозначает атом водорода, другой из них не может представлять атом водорода, метильную группу или этильную группу. В том случае, когда один из R1 и R2 обозначает гидроксильную группу, другой из них не может быть атомом водорода или метильной группой.
Ароматическое кольцо или гетероциклическое кольцо, имеющееся в заместителе R1 в указанной формуле, может содержать по меньшей мере один атом галогена, гидроксильную группу, алкильные группы, включающие до 3 атомов углерода, алкоксильную группу, включающую до 3 атомов углерода, и аминогруппу.
Среди них R1 предпочтительно выбирают из группы, состоящей из С2-С4 алкильных групп, С2-С4 карбоксиалкильных групп, фенилметильной группы и 3-индолилметильной группы (бензольное кольцо или индольное кольцо может дополнительно содержать по меньшей мере один атом галогена (атома йода, атома брома, атома хлора, атома фтора и т.п.)), гидроксильной группы, алкильных групп, включающих до 3 атомов углерода, алкоксильных групп, включающих до 3 атомов углерода, и аминогруппы, и R2 обозначает гидроксильную группу. Более предпочтительно, R1 обозначает фенилметильную группу или 3-индолилметильную группу и R2 обозначает гидроксильную группу.
В том случае, когда R1 обозначает 3-индолилметильную группу и R2 обозначает гидроксильную группу, то есть когда в качестве замещенной α-кетокислоты формулы (1) используют ИГОГ (4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровая кислота), монатин может быть получен в качестве производного глютамата общей формулы (2).
В том случае, когда R1 обозначает фенилметильную группу и R2 обозначает гидроксильную группу, то есть когда в качестве замещенной α-кетокислоты общей формулы (1) используют ФГОГ (4-фенилметил-4-гидрокси-2-оксоглутаровая кислота), может быть получен аналог монатина, 4-фенилметил-4-гидрокси-глютаминовая кислота (ФГГ), в качестве производного глютамата общей формулы (2).
Что касается замещенной α-кетокислоты общей формулы (1), используемой в качестве субстрата, то предпочтительно используют замещенную α-кетокислоту общей формулы (4), получаемую по способу, приведенному в разделе [B] при описании реакции 2. Более предпочтительно, используют ИГОГ, полученную по способу, приведенному в разделе [B] при описании реакции 2, с использованием индол-3-пировиноградной кислоты, полученной по способу, приведенному в разделе [А] при описании реакции 1. Однако, очевидно, что способ получения замещенной α-кетокислоты, описываемой общей формулой (1), не ограничивается описанными выше способами.
В реакции 3 функционирует механизм реакции, катализируемой ферментом, в результате которой образуется аминокислота, соответствующая замещенной α-кетокислоте, взятой в качестве субстрата. Реакция 3 относится к примеру способа получения производных глютамата за счет реакции взаимодействия белка, катализирующего трансаминирование, или микроорганизма, продуцирующего такой белок. В настоящем описании термин "трансаминирование" относится к реакции преобразования предшественника кетонного соединения в соответствующее аминосоединение путем переноса аминогруппы от субстрата-донора к кетонной группе соединения-акцептора.
Способ проведения реакции 3 по настоящему изобретению будет подробно описан в указанном ниже порядке.
(С-1) Фермент, используемый в реакции 3
(С-2) Реакционные условия для проведения реакции 3
(С-1) Фермент, катализирующий реакцию образования аминокислоты
В реакции 3 фермент, катализирующий реакцию образования аминокислоты, соответствующей замещенной α-кетокислоте, используемой в качестве субстрата, включает, например, трансаминазу в качестве фермента, катализирующего трансаминирование, и дополнительно включают дегидрогеназу в качестве фермента, катализирующего восстановительное аминирование кетокислоты. Трансаминаза, используемая в реакции 3, может быть успешно представлена ферментом, катализирующим реакцию образования производного глютамата из соответствующей замещенной α-кетокислоты и донора аминогруппы, взятых в качестве исходного материала. За счет действия такого фермента замещенная α-кетокислота, описываемая общей формулой (1), может быть преобразована в соответствующее производное глютамата (описываемое общей формулой (2)).
Затем в качестве донора аминогруппы используют соединение, содержащее аминогруппу. Так, например, указанное соединение включает аминосоединения, такие как L-аминокислоты и D-аминокислоты природного и неприродного происхождения. Конкретно, аминокислоты включают, например, глютаминовую кислоту, аспарагиновую кислоту, аланин, триптофан, фенилаланин, изолейцин, лейцин, тирозин, валин, аргинин, аспарагин, глютамин, метионин, орнитин, серин, цистеин, гистидин и лизин. Донор аминогруппы, добавляемый к реакционной смеси, может быть представлен соединением одного типа или может представлять собой смесь разных типов таких доноров.
В основном, трансаминаза L-аминокислоты образует целевую L-аминокислоту путем переноса аминогруппы от L-аминокислотного донора к кетокислоте-предшественнику, тогда как трансаминаза D-аминокислоты образует целевую D-аминокислоту путем переноса аминогруппы от D-аминокислотного донора к кетокислоте-предшественнику. Путем выбора соответствующего фермента может быть также отобран оптический изомер получаемого производного глютамата. Так, например, реакция с трансаминазой D-аминокислоты в присутствии D-аминокислот, таких как D-аланин, D-глютаминовая кислота и D-аспарагиновая кислота, может селективно приводить к образованию производных D-глютамата из предшественника-кетокислоты.
Как указывалось выше, монатин, представляющий собой объект настоящего изобретения как одно из производных глютамата, включает три оптических изомера дополнительно к природному типу (2S, 4S). Было подтверждено, что любой из указанных изомеров обладает степенью сладости, превышающей от нескольких сот до нескольких тысяч раз сладость сахарозы. В одном предпочтительном варианте осуществления настоящего изобретения реакция трансаминазы D-аминокислоты с кетокислотой-предшественником, используемая для получения монатина, может генерировать 2R форму монатина стереоселективно, тогда как реакция трансаминазы L-аминокислоты с указанным предшественником может стереоселективно генерировать 2S форму монатина. В одном из более предпочтительных вариантов осуществления изобретения использование трансаминазы D-аминокислоты приводит селективно к образованию 2R формы как изомера, обладающего более высокой степенью сладости.
В случае использования D-аминокислоты в качестве донора аминогруппы по настоящему изобретению к реакционному раствору добавляют соответствующую L-аминокислоту для создания условий конкурентного взаимодействия аминокислоты с ферментом, катализирующим реакцию рацемизации аминокислоты, для которой донор поставляется в виде D-аминокислотного донора. Что касается рацемизирующего фермента, то предпочтительные примеры такого фермента включают аланинрацемазу, рацемазу глютаминовой кислоты, рацемазу аспарагиновой кислоты и рацемазу фенилаланина. В таком случае к реакционному раствору могут быть добавлены L-аланин, L-глютаминовая кислота, L-фенилаланин, L-аспарагиновая кислота или рацемическая смесь указанных L-аминокислот, при том условии, что продуцироваться будут производные D-глютамата.
Фермент, катализирующий трансаминирование, может быть также получен путем культивирования микроорганизма, продуцирующего такой фермент. Указанные микроорганизмы включают, например, микроорганизмы из рода Aeromonas, Agrobacterium, Alcaligenes, Bacillus, Beijerinckia, Escherichia, Proteus, Morganella и Paenibacillus.
Конкретно, указанные микроорганизмы включают, например, указанные ниже микроорганизмы. Иными словами, микроорганизм, продуцирующий трансаминазу L-аминокислоты, обладающую активностью по образованию производных глютамата общей формулы (2) из замещенной α-кетокислоты общей формулы (1), включает следующие примеры таких микроорганизмов.
hydrophila IF03820
tumefaciens IFO3058
faecalis ATCC8750
indica ATCC9037
coli ATCC12814
rettgeri IFO13501
morganii IFO3848
Дополнительно, микроорганизмы, продуцирующие трансаминазу D-аминокислоты, включают следующие примеры:
Bacillus sphaericus ATCC10208
Bacillus pulvifaciens AJI1327
Paenibacillus larvae subsp. pulvifaciens ATCC13537
Bacillus macerans AJ1617
Paenibacillus macerans ATCC8244
Bacillus lentus AJ12699
Bacillus lentus АТСС10840
Приведенный в настоящем описании Bacillus macerans AJ1617 был депонирован в следующих условиях.
Bacillus macerans штамм AJ1617
(а) No. доступа FERM BP-8243 (перенесен из FERM P-18653 в Международный Депозитарий патентованных организмов (International Patent Organism Depositary) 2 ноября 2002 года.
(b) Дата депонирования: 13 декабря 2001 года.
(с) Депонирующая организация: Международный Депозитарий патентованных организмов, Институт современной промышленной науки и методики (Institute of Advanced Indusrtial Science and Technology) (No. 6, Chuo, 1-1-1, Higashi, Tsukuba, Ibaraki, Япония).
Используемые микроорганизмы могут с успехом представлять микробные штаммы, впервые выделенные из натуральных источников, таких как почва или растения, или они могут представлять микробные штаммы, искусственно полученные при обработке химическими мутагенами и методами рекомбинантной ДНК.
В одном из предпочтительных вариантов осуществления настоящего изобретения целевой ген, кодирующий фермент, который катализирует целевое трансаминирование замещенной α-кетокислоты до производных глютамата, может быть также интегрирован в микробные клетки. Известно множество примеров получения полезных белков, таких как фермент и физиологически активные вещества, с использованием методов рекомбинантной ДНК. Использование методов рекомбинантной ДНК позволяет осуществлять масштабное получение полезных белков из источников природного происхождения, включающих их в следовых количествах. Интегрируемый ген включает гены трансаминазы L-аминокислоты и гены трансаминазы D-аминокислоты. Одним из примеров возможного способа является введение генов трансаминазы D-аминокислоты из Bacillus sphaericus или Bacillus macerans в данные микроорганизмы.
Публикация по европейскому патенту 0 736 604 и в работе Taylor et al., Journal of Bacteriol., 1998, Vol. 180, No. 16, p. 4319 сообщается о гене трансаминазы D-аминокислоты, полученном из Bacillus sphaericus.
В качестве гена трансаминазы D-аминокислоты, полученного из Bacillus macerans, дополнительно может использоваться ДНК с геном трансаминазы D-аминокислоты, полученным из Bacillus macerans, которая описана в виде последовательности SEQ ID No. 17 в перечне последовательностей. В случае использования ДНК, описанной в виде SEQ ID No. 17 в перечне последовательностей, с геном трансаминазы D-аминокислоты, полученным из Bacillus macerans, может быть получена трансаминаза D-аминокислоты с последовательностью SEQ ID No. 18, приведенной в перечне последовательностей. В настоящем описании авторы изобретения прежде всего приводят данные по гену, кодирующему трансаминазу D-аминокислоты из Bacillus macerans, и ее аминокислотной последовательности.
Происхождение гена трансаминазы D-аминокислоты не ограничивается указанным примером. Может быть с успехом применен любой ген, кодирующий трансаминазу D-аминокислоты, продуцирующую целевое производное D-глютамата.
В случае масштабного получения белка с использованием методов рекомбинантной ДНК в качестве подлежащих трансформации хозяйских клеток могут использоваться микробные клетки, клетки актиномицетов, дрожжевые клетки, клетки грибов, растительные клетки, клетки животных и т.п. Среди них микроорганизмы, в отношении которых имеется опыт работы методами рекомбинантной ДНК, включают, например, Bacillus, Pseudomonas, Brevibacrerium, Corynebacterium, Streptomyces и Escherichia coli. В связи с наработкой экспериментального материала по масштабному получению белка с использованием Escherichia, в основном используют бактерии из рода Escherichia. Предпочтительно используют Escherichia coli.
При использовании векторов, таких как плазмида или фаг, несущих целевой ген трансаминазы, указанный ген может быть успешно введен в указанные микроорганизмы. В ином случае, целевой ген может быть успешно интегрирован в хромосому клетки путем гомологичной рекомбинации. Предпочтительны так называемые мультикопийные плазмидные векторы, которые включают, например, плазмиды с ориджином репликации, полученным из Co1 E1, в качестве вектора для Escherichia coli, и которые представляют собой, например, плазмиды на основе pUC, плазмиды на основе pBR322 или их производные. В случае указанных векторов промоторы, обычно используемые при получении белка в Escherichia coli, могут использоваться в качестве промотора для экспрессии целевого гена трансаминазы, и они включают сильные промоторы, например, промотор Т7, trp промотор, lac промотор, tac промотор и PL промотор. С целью повышения производительности, терминатор в виде последовательности терминации транскрипции предпочтительно конъюгируют вниз по ходу транскрипции гена белка. Такой терминатор включает, например, терминатор из Т7, терминатор фага fd, терминатор T4, терминаторы гена устойчивости к тетрациклину и терминаторы trp A гена из Escherichia coli. Дополнительно, для скрининга получаемых трансформантов предпочтительный вектор несет маркер, такой как ген устойчивости к ампициллину. В качестве таких плазмид могут использоваться коммерчески доступные векторы экспрессии с сильным промоторами, такие как векторы серии pUC (производство TAKARA BIO INC.), серии pPROK (производство Clontech Laboratories, Inc.) и серии pKK233-2 (производство Clontech Laboratories, Inc.).
В способе получения микроорганизма, продуцирующего фермент, используемый в реакции 3, могут использоваться общеприменимые в данной области культуральные среды, а именно: культуральные среды, содержащие источники углерода, источники азота, неорганические соли, соли следовых количеств металла и витамины. В зависимости от типа микроорганизма или условий культивирования, к такой культуральной среде добавляют примерно от 0,1 до 1,0 г/дл аминосоединений, таких как аминокислоты, для усиления трансаминирующей активности.
В случае культивирования генетически рекомбинантных клеток, в зависимости от выбранного маркера в применяемом векторе, могут быть добавлены соответствующие химические вещества, такие как ампициллин, канамицин, неомицин и хлорамфеникол. В зависимости от промотора, содержащегося в векторе, уровень экспрессии рекомбинантного гена может быть повышен путем добавления соответствующего количества индуцирующего агента. В случае конъюгирования целевого гена вниз по ходу транскрипции от lac промотора для создания вектора, в одном примере реализации изобретения можно добавить изопропил-1-тио-β-D-галактопиранозид (ИПТГ) в количестве, соответствующем конечной концентрации от 0,1 мМ до 5 мМ. В ином случае, может быть добавлена в соответствующем количестве галактоза до конечной концентрации от 0,1 до 5 г/дл, предпочтительно от 0,5 г до 2 г/дл.
В качестве веществ, представляющих собой компоненты культуральной среды, может, например, использоваться любой источник углерода, который может утилизироваться микроорганизмами, без каких-либо конкретных ограничений. Так, например, может использоваться глюкоза, сахароза, фруктоза, глицерин и уксусная кислота или их смеси. В качестве источника азота могут использоваться сульфат аммония, хлорид аммония, мочевина, дрожжевой экстракт, мясной экстракт, жидкий кукурузный экстракт и продукты гидролизации казеина или их смеси. Что касается состава культуральной среды, то может быть приведен следующий пример культуральной среды, содержащей 0,5 г/дл фумаровой кислоты, 1 г/дл дрожжевого экстракта, 1 г/дл пептона, 0,3 г/дл сульфата аммония, 0,3 г/дл K2HPO4, 0,2 г/дл KH2PO4, 1 мг/дл FeSO4 · 7H2O и 1 мг/дл MnSO4 · 4H2O, при pH 7,0.
Температура культуры поддерживается в основном в диапазоне, пригодном для роста микроорганизмов, а именно: в диапазоне от 10 до 45°С. Предпочтительно температура поддерживается в диапазоне от 20 до 40°С, более предпочтительно, в диапазоне от 25 до 37°С. pH культуральной среды доводят до значения от 2 до 12, более предпочтительно от 3 до 10 и еще более предпочтительно от 4 до 8. Условия аэрации устанавливаются в соответствии с условиями, пригодными для роста используемых микроорганизмов. Предпочтительно это аэробные условия. Длительность культивирования составляет от 12 до 120 часов, предпочтительно от 24 до 96 часов.
(С-2) Реакционные условия для проведения реакции 3
В ходе реакции 3 из замещенной α-кетокислоты общей формулы (1) образуются характерные производные глютамата общей формулы (2).
Термин "в присутствии фермента" в контексте описания реакции 3 означает, что фермент должен находиться в реакционной системе в состоянии, позволяющем продуцировать производные глютамата общей формулы (2) из замещенной α-кетокислоты, описываемой общей формулой (1). Иными словами, фермент может находиться в реакционной смеси в любом состоянии, при условии, что указанный фермент способен превращать замещенную α-кетокислоту, описываемую общей формулой (1), в производное глютамата общей формулы (2). Так, например, фермент может быть один раз добавлен в реакционную систему. В ином случае, к реакционной системе могут быть также добавлены: микроорганизм, содержащий ферментативную активность (микроорганизм, продуцирующий фермент, клетки, трансформированные рекомбинантной ДНК), культура микроорганизма (жидкая культура, твердая культура и т.п.), культуральная среда (культуры, из которых предварительно были удалены микробные клетки) и обработанные продукты из культуры. В случае использования культур микроорганизмов, реакция 3 может быть проведена при одновременном культивировании микроорганизмов, или реакция 3 может проводиться с использованием культур, предварительно подготовленных для целей получения данного фермента. В настоящем описании термин "обработка" обозначает обработку с целью регенерации фермента в микробных клетках, включая, например, способ обработки ультразвуком, стеклянными шариками, под френч-прессом и лиофильную сушку, а также способы обработки с использованием лизирующих ферментов, органических растворителей, детергентов и т.п. Обработанные продукты после указанных видов обработки могут быть также подвергнуты дополнительным, рутинным способам обработки (жидкостная хроматография, обработка сульфатом аммония и т.п.) для регенерирования неочищенных ферментов, полученных при фракционировании, или очищенных ферментов. Когда указанные ферменты обладают требуемой способностью, они могут быть использованы.
Кроме того, используемые культура или обработанный продукт могут быть включены в гель каррагенана или полиакриламид или они могут быть иммобилизованы на пленках с полиэфирсульфоном, регенерированной целлюлозой и т.п.
В реакции 3 замещенная α-кетокислота, используемая в качестве субстрата, включает, например замещенную α-кетокислоту, описываемую общей формулой (1).
Реакционная система может с успехом включать коферменты, детергенты, органические растворители и т.п. для целей ускорения реакции. Так, с целью повышения проницаемости в микробные клетки замещенных α-кетокислот, взятых в качестве субстрата, могут также использоваться детергенты, такие как Тритон Х и Твин, а также органические растворители, такие как толуол и ксилол. Кроме того, к культуральной среде могут быть добавлены коферменты, такие как пиридоксаль-5-фосфат.
В случае разделения культуры с целью продуцирования фермента и осуществления реакции 3 с последующим проведением указанных стадий, последняя стадия реакции 3 необязательно проводится в аэробных условиях. Реакция 3 по анаэробному типу может быть проведена в реакционной системе, из которой растворенный в реакционном растворе кислород был удален путем замещения газообразным азотом, аргоном и путем добавления сульфита натрия. Что касается температуры реакции, в основном указанную реакцию проводят в условиях температурного диапазона, в котором используемый фермент обладает активностью, предпочтительно, в диапазоне от 10 до 50°С, более предпочтительно в диапазоне от 20 до 40°С и еще более предпочтительно в диапазоне от 25 до 37°С. Значение pH реакционного раствора доводят в основном до уровня от 2 до 12, предпочтительно от 6 до 11 и еще более предпочтительно от 7 до 9. Время реакции составляет в основном от 1 до 120 часов, предпочтительно от 1 до 72 часов и более предпочтительно от 1 до 24 часов.
В случае определения количества производного глютамата или замещенной α-кетокислоты в жидкой культуре или реакционном растворе, указанные производное глютамата или замещенная α-кетокислота могут быть проанализированы известными способами. В рамках простой процедуры, может использоваться метод тонкослойной хроматографии на силикагеле 60F254 производства Merck Ltd. Для повышения точности анализа может быть проведена высокоэффективная жидкостная хроматография (ВЭЖХ) с использованием колонок для оптического разрешения, таких как Inertsil ODS-80A, производства компании GL Science, Inc. и CROWNPAK CR (+) производства компании Daicel Chemical Industries, Ltd. В рамках такого способа, производные глютамата, накапливаемые в жидкой культуре или в реакционном растворе, перед использованием могут быть собраны из указанной жидкой культуры или указанного раствора обычными способами. Для отбора из жидкой культуры или реакционного раствора может использоваться соответствующее сочетание хорошо известных процедур, таких как, например, фильтрование, центрифугирование, концентрирование в вакууме, ионообменная хроматография, абсорбционная хроматография и кристаллизация.
Целевое производное глютамата может быть получено в свободном виде. При необходимости, производное глютамата может быть также восстановлено из его соли. Солевая форма включает его соли с основаниями. Так, например, могут использоваться неорганические основания, такие как гидроксид натрия, гидроксид калия и гидроксид кальция, а также органические основания, такие как аммиак и различные амины.
ПРИМЕРЫ
Ниже настоящее изобретение подробно описывается с помощью приведенных примеров, однако настоящее изобретение не ограничивается только указанными примерами.
Пример 1
Пример 1 относится к реакции 1 настоящего изобретения. В примере 1 L-триптофан, индол-3-пировиноградную кислоту и индолуксусную кислоту количественно определяют методом высокоэффективной жидкостной хроматографии (колонка: Inertsil ODS-2 (4,6 X 250 мм); температура колонки: 40°С; элюат: 0,1 М KH2PO4-H3PO4 (pH 2,80)/CH3CH = 1/9 - 5/5; скорость течения 1,0 мл/мин; обнаружение проводят при УФ с длиной волны 210 нм.
(1-1) Получение индол-3-пировоногридной кислоты из L-Trp посредством реакции микробных клеток с носителем оксидазной активности в отношении аминокислоты
50 мл культуральной среды, pH 7,0, содержащей 1 г/дл дрожжевого экстракта, 1 г/дл полипептона, 0,3 г/дл (NH4)2SO4, 0,3 г/дл K2HPO4, 0,1 г/дл KH2PO4, 0,05 г/дл MgSO4 · 7H2O, 1 мг/дл FeSO4 · 7H2O и 1 мг/дл MnSO4 · 4H2O помещают в колбу Сакагучи на 500 мл для стерилизации при 110°С в течение 10 минут.
Одну петлю Achromobacter sp. AJ2425, Proteus rettgeri IFO13501 или Morganella morganii IFO3168, предварительно культивированные на культуральной среде с бульонным агаром при 30°С в течение 24 часов, инокулируют в культуральную среду и культивируют при встряхивании при 30°С в течение 24 часов. После культивирования микробные клетки собирают из культуры с помощью центрифугирования, промывают 50 мл 20 мМ Трис-HCl буфера, pH 7,6 и полученные промытые микробные клетки вновь подвергают центрифугированию.
Указанные сырые микробные клетки добавляют к реакционному раствору, содержащему 1 г/дл L-триптофана и 20 мМ Tris-HCl буфера, pH 8,0, до достижения веса сырых микробных клеток 1% (вес/объем). 1 мл реакционного раствора переносят в опытную пробирку на 5 мл и встряхивают в течение одного часа при 30°С для прохождения реакции. После завершения реакции измеряют количество продуцированной индол-3-пировиноградной кислоты, количество остаточного L-триптофана (L-Trp) и количество побочного продукта в виде индолуксусной кислоты (ИУК) (см. таблицу 1).
Количество индолпировиноградной кислоты, образованной из L-триптофана
Впоследствии индол-3-пировиноградная кислота в количестве от 0,97 до 0,99 г/дл накапливается в любом из экспериментальных лотов, в которых присутствуют промытые микробные клетки. Так, индол-3-пировиноградная кислота образуется практически количественно из 1 г/дл L-триптофана.
(1-2) Регенерация индол-3-пировиноградной кислоты путем заместительной обработки газообразным азотом реакционного раствора, содержащего промытые клетки Morganella morganii IFO3168, с последующей кристаллизацией в хлористоводородной кислоте
(а) Получение реакционного раствора с промытыми микробными клетками Morganella morganii IFO3168
По методу, описанному в (1-1), получают промытые микробные клетки Morganella morganii IFO3168. Подготавливают шесть колб Сакагучи, содержащих 50 мл реакционного раствора, включающего 1 г/дл L-триптофана и 20 мМ Трис-HCl буфера, pH 8,0. Подготовленные сырые микробные клетки добавляют к отдельным колбам до достижения веса сырых микробных клеток 1% (вес/объем) для проведения реакции при встряхивании при 30°С в течение одного часа. После завершения реакции микробные клетки удаляют центрифугированием с получением реакционного раствора объемом примерно 290 мл.
(b) Регенерация индол-3-пировиноградной кислоты путем замещения реакционного раствора газообразным азотом и последующей кристаллизации в кислоте
74 мл реакционного раствора, полученного в пункте (а), переносят в круглодонную колбу для проведения заместительной обработки газообразным азотом. Добавляют хлористоводородную кислоту, так чтобы значение pH реакционного раствора составляло 2 или менее. 15 мл 6N хлористоводородной кислоты добавляют к 74 мл реакционного раствора (до достижения конечной примерно 1 N концентрации хлористоводородной кислоты) и смесь перемешивают при 20°С. В ходе данной процедуры осаждаются кристаллы. Через 24 часа смесь фильтруют. Полученные кристаллы промывают 15 мл воды. Полученные таким образом сырые кристаллы сушат при пониженном давлении при 40° С с получением индол-3-пировиноградной кислоты в количестве 684 мг (выход 79,5% от исходного триптофана). Полученная индол-3-пировиноградная кислота представляет собой желтовато-белые кристаллы с содержанием 97,2 вес.%, по данным высокоэффективной жидкостной хроматографии (ВЭЖХ).
(с) Восстановление индол-3-пировиноградной кислоты путем кристаллизации реакционного раствора в кислоте
66 мл реакционного раствора, полученного в пункте (а), переносят в круглодонную колбу. Добавляют 6N хлористоводородную кислоту в количестве 13 мл, так чтобы довести pH реакционного раствора до 2 или менее, и перемешивают при 20°С. В ходе данной процедуры происходит осаждение кристаллов. Через 24 часа смесь фильтруют. Образовавшиеся кристаллы промывают 13 мл воды. Полученные таким образом сырые кристаллы сушат при пониженном давлении при 40° С с получением индол-3-пировиноградной кислоты в количестве 538 мг (выход 58,2% от исходного триптофана). Полученная индол-3-пировиноградная кислота представляет собой темно-коричневые кристаллы с содержанием 80,5 вес.%, по данным высокоэффективной жидкостной хроматографии (ВЭЖХ).
(d) Сравнительный анализ полученной индол-3-пировиноградной кислоты
Полученную в пункте (b) индол-3-пировиноградную кислоту (ИПК) сравнивают с кислотой, полученной по способу пункта (с), с точки зрения качества кристаллов (см. таблицу 2).
Как видно из приведенных результатов, лот (b), при получении которого использовался метод замещения газообразным азотом, характеризуется более высоким содержанием ИПК и сниженным содержанием побочного продукта в виде индолуксусной кислоты (ИУК), представляющего собой примесь в кристалле. Кроме того, окрашивание полученного кристалла подавляется в лоте, полученном с использованием заместительной обработки газообразным азотом. Кристаллы в индивидуальных лотах разбавляют до концентрации 10 мг/дл и измеряют коэффициент пропускания при 450 нм и 400 нм. Делается вывод о том, что коэффициент пропускания в лоте, полученном с использованием замещения газообразным азотом, снижен, то есть подавляется окрашивание, возникающее за счет разложения.
Качество кристаллов ИПК
(b)
(с)
Как видно из приведенных результатов, индол-3-пировиноградная кислота может быть эффективно получена простым способом из триптофана.
Пример 2
Описываемую в примере 2 реакцию 2 проводят с использованием системы химического синтеза.
(2-1) Синтез 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ)
Добавляют 7,50 г индол-3-пировиноградной кислоты (35,8 ммоль; содержание 97,0 вес.%) и 14,18 г щавелевоуксусной кислоты (107,4 ммоль) и растворяют в 64,45 мл воды, в которой предварительно было растворено 18,91 г гидроксида калия (286,5 ммоль; содержание 85 вес.%). Раствор смеси перемешивают при 35°С в течение 24 часов.
Далее, добавляют 40,0 мл 3N хлористоводородной кислоты для нейтрализации (pH 7,0) с получением 153,5 г нейтрализованного реакционного раствора. Полученный нейтрализованный реакционный раствор содержит 5,55 г ИГОГ, так что выход составляет 53,3 % (по индол-3-пировиноградной кислоте).
К нейтрализованному реакционному раствору добавляют 168 мл воды и пропускают через колонку со смолой (диаметр 4,8 см), заполненную 840 мл синтетического сорбента (DIAION-SР207, производство компании Mitsubishi Chemical Corporation). Далее, через колонку пропускают чистую воду со скоростью течения 23,5 мл/минуту и собирают 1,73 - 2,55 (L/L-R) с получением водного раствора, содержащего 3,04 г ИГОГ с высокой чистотой и выходом 54,7% (в сравнении с количеством, осевшим на смолу).
(Измерение спектра ЯМР)
1Н-ЯМР (100 МГц, D2O): 3,03 (д, 1Н, J=14,6 Гц), 3,11 (д, 1Н, J=14,6 Гц), 3,21 (д, 1Н, J=18,1 Гц), 3,40 (д, 1Н, J=18,1 Гц), 7,06-7,15 (м, 3Н), 7,39 (д, 1Н, J=7,8 Гц), 7,66 (д, 1Н, J=7,8 Гц).
13C-ЯМР (100 МГц, D2O): 35,43, 47,91, 77,28, 109,49, 112,05, 119,44, 119,67, 121,91, 125,42, 128,41, 136,21, 169,78, 181,43, 203,58
(2-2) Синтез 4-фенилметил-4-гидрокси-2-оксоглутаровой кислоты (ФГОГ)
5,0 г (30,5 ммоль) фенилпировиноградной кислоты и 12,1 г (91,4 ммоль) щавелевоуксусной кислоты добавляют в 25 мл воды, в которой предварительно было растворено 13,8 гидроксида калия (чистота 85 %) для проведения реакции при температуре окружающей среды в течение 72 часов. С использованием концентрированной хлористоводордной кислоты доводят pH реакционного раствора до 2,2 для последующей экстракции этилацетатом. Органический слой промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом магния и концентрируют с получением остатка. Остаток рекристаллизуют в этилацетате и толуоле с получением ФГОГ в количестве 2,8 г (11,3 ммоль) в виде кристаллов.
(Измерение спектров ЯМР)
1Н-ЯМР (D2O) δ: 2,48 (д, J=14,4 Гц, 0,18Н), 2,60 (д, J=14,4 Гц, 0,18Н), 2,85-3,30 (м, 3,64Н), 7,17-7,36 (м, 5Н).
(Измерение молекулярной массы)
Теоретическое значение по данным ESI-MS: C12H12O6 = 252,23
Полученное в эксперименте значение: 251,22 (МН-)
Пример 3
В примере 3 реакцию 2 проводят с использованием ферментативной системы. В описанном примере 3 используемые в качестве субстратов ИГОГ и ФГОГ получены путем синтеза по способу, описанному в примере 2.
(3-1) Скрининг микроорганизмов на активность альдолазы в отношении ФГОГ (далее определяемую как ФГОГ активность)
Скрининг микробных штаммов, обладающих альдолазной активностью, проводят с использованием в качестве субстрата 4-фенилметил-4-гидрокси-2-оксоглутаровой кислоты (ФГОГ).
Тест-микроорганизмы (бактерии и дрожжи) инокулируют в культуральную среду на чашки с бульонным агаром (Eiken Chemical Co., Ltd) и культивируют при 30°С в течение 24 часов. Полученную культуру инокулируют в чашки, содержащие 0,5 г/дл глицерина, 0,5 г/дл фумаровой кислоты, 0,3 г/дл дрожжевого экстракта, 0,2 г/дл пептона, 0,3 г/дл сульфата аммония, 0,3 г/дл K2HPO4, 0,1 г/дл KH2PO4, 0,05 г/дл MgSO4 · 7H2O, 0,25 г/дл фталата натрия и 2 г/дл агарового порошка (pH 6,5), и культивируют при 30°С в течение 24 часов. Далее полученные микробные клетки инокулируют в реакционный раствор, содержащий 100 мМ Tris-HCl, pH 8,0, 50 мМ ФГОГ, 1 мМ MgCl2, 5 мМ раствора фосфата калия (KPi) и 1 объемн.% толуола, в количестве примерно 1% (вес/объем), по сырой массе микробных клеток, для проведения реакции при 30°С в течение 24 часов. Концентрацию свободной пировиноградной кислоты в реакционном растворе измеряют ферментативным методом с использованием лактатдегидрогеназы (ЛДГ). Добавляют 10 мкл образца к 200 мкл реакционного раствора, содержащего 100 мМ Tris-HCl, pH 8,0, 1,5 мМ НАДН, 5 мМ MgCl2 и 25 Ед/мл ЛДГ для инкубирования при 30°С в течение 10 минут. Измеряют поглощение при длине волны 340 нМ после прохождения реакции с целью определения по уровню восстановленного НАДН количества пировиноградной кислоты, имеющегося в образце.
Дополнительно, оценивают количество образованной фенил-пировиноградной кислоты методом ВЭЖХ с использованием колонки Inertsil ODS-2 (5 мкм, 4,6 x 250 мм), производство компании GL Science, Inc. Для анализа используют следующие условия:
Мобильная фаза: 20 объемн.% ацетонитрила/0,05 объемн.% водного раствора трифторуксусной кислоты
Скорость течения: 1 мл/мин
Температура колонки 40°С
Обнаружение: УФ 210 нм
В указанных условиях ФГОГ элюируется со временем удерживания примерно 9,8 минут, тогда как фенилпировиноградная кислота элюируется со временем удерживания примерно 12 минут. Указанные соединения, каждое по отдельности, подвергают функционированию и анализируют.
Количество пировиноградной кислоты или фенилпировиноградной кислоты, полученных из ФГОГ, в испытуемом лоте с наличием добавленных микробных клеток за минусом ее количества в контрольном лоте (без добавления лота с микробным клетками) дает количество, продуцированное альдолазой. Соответственно, альдолазная активность в отношении субстрата ФГОГ была обнаружена в микробных штаммах, показанных в таблице 3.
Результаты скрининга микробных штаммов на наличие активности ФГОГ альдолазы
Отбирают Pseudomonas taetrolens ATCC4683 и оценивают реакцию синтеза ФГОГ из фенилпировиноградной кислоты и щавелевоуксусной кислоты или пировиноградной кислоты. Микробные клетки P. taetrolens ATCC4683 (AJ2212) инокулируют в реакционный раствор, содержащий 100 мМ Трис-HCl, pH 8,0, 50 мМ фенилпировиноградной кислоты, 1 мМ MgCl2, 5 мМ (KPi), 100 мМ щавелевоуксусной кислоты или пировиноградной кислоты и 1 мас.% толуола до конечной концентрации примерно 1% (вес/объем) для проведения реакции при 30°С в течение 24 часов. После завершения реакции оценивают методом ВЭЖХ количество образованного ФГОГ. Количество ФГОГ, образованного из фенилпировиноградной кислоты и щавелевоуксусной кислоты или пировиноградной кислоты, показано в таблице 4.
Количество ФГОГ, образованного из фенилпировиноградной кислоты и щавелевоуксусной кислоты или пировиноградной кислоты
Из данных таблицы 4 видно, что количество образованного ФГОГ в лоте с микробными клетками повышается и что альдолазная активность может продуцировать ФГОГ из любого сочетания: из фенилпировиноградной кислоты + щавелевоуксусная кислота и фенилпировиноградной кислоты + пировиноградная кислота.
(3-2) Очистка альдолазы, полученной из Pseudomonas taetrolens ATCC4683, используемой для получения ИГОГ
Альдолазу, используемую для получения ИГОГ (иногда называемую далее как ИГОГ альдолаза), очищают приведенным ниже способом из растворимой фракции P. taetrolens ATCC4683. Для анализа альдолазной активности измеряют активность альдолазного разложения (ретроальдольную активность) с использованием ФГОГ в качестве субстрата в следующих условиях.
Условия реакции: 50 мМ Трис-HCl, pH 8,0, 2 мМ ФГОГ, 0,2 мМ НАДН, 0,2 мМ KPi, 1 мМ MgCl2, 16 Ед/мл лактатдегидрогеназы и 3 мкл фермента/600 мкл реакционного раствора для измерения поглощения при 30°С и длине волны 340 нм.
1. Получение растворимой фракции
Одну петлю микробных клеток P. taetrolens ATCC4683, предварительно культивированных в культуральной среде на чашках с бульонным агаром при 30°С в течение 24 часов, инокулируют в колбу на 500 мл, содержащую 50 мл культуральной среды, продуцирующей фермент (0,5 г/дл глицерина, 0,5 г/дл фумаровой кислоты, 0,5 г/дл сульфата аммония, 0,3 г/дл K2PO4, 0,1 г/дл KH2PO4, 0,05 г/дл MgSO4 · 7H2O, 0,3 г/дл дрожжевого экстракта, 0,2 г/дл пептона, 0,25 г/дл фталата натрия и 0,005% пеногасителя А (производство Сигма) после доведения значения pH до 6,5 с использованием KOH) на качалке при 30°С в течение 24 часов. 0,5 мл жидкой культуры инокулируют в 40 колбах объемом 500 мл, каждая из которых содержит 50 мл культуральной среды, продуцирующей фермент, для культивирования на качалке при 30°С в течение 24 часов. Микробные клетки собирают из полученной жидкой культуры центрифугированием, суспендируют и далее промывают буфером А (20 мМ Трис-HCl, pH 7,6), с последующим центрифугированием вновь для сбора микробных клеток. Полученные промытые микробные клетки суспендируют в 200 мл буфера А для ультразвукового разрушения при 4°С в течение 30 минут. Полученный после ультразвуковой обработки раствор центрифугируют (х 8000 об/мин, два раза по 10 минут) с удалением оставшихся микробных клеток и затем проводят дополнительное ультрацентрифугирование (х 50000 об/мин, 30 минут) с получением супернатанта, который представляет собой растворимую фракцию.
2. Анионообменная хроматография: Q-сефароза FF
80 мл растворимой фракции обрабатывают на анионообменной колонке с Q-сефарозой FF 26/10 (производство Фармация (Pharmacia) объем слоя = 20 мл) для адсорбции на носитель. Белки, не адсорбируемые носителем (неадсорбированные белки), вымываются буфером А. Затем адсорбированный белок элюируют при поддерживании градиента концентрации KCl в линейном диапазоне от 0 М до 0,7 М (всего берут 140 мл). При обнаружении активности альдолазы для ФГОГ (иногда называемой далее как ФГОГ альдолаза) в каждой из элюированных фракций определяют пик ФГОГ альдолазной активности во фракции, соответствующей примерно 0,5 М. Ту же самую процедуру повторяют еще два раза.
3. Гидрофобная хроматография: Фенилсефароза HP HR 16/10
Раствор с выявленной альдолазной активностью собирают и диализуют против буфера В (50 мМ Трис-HCl, pH 7,6, 1М сульфат аммония, pH 7,6) при 4°С в течение ночи и затем фильтруют через фильтр с размером пор 0,45 мкм. Полученный фильтрат подвергают гидрофобной хроматографии на колонке с фенилсефарозой HP HR 16/10 (производство Фармация (Pharmacia), уравновешенной буфером В. В ходе указанной процедуры альдолаза адсорбируется на носителе.
Неадсорбированные белки, которые не адсорбируются на носителе, вымывают буфером В. Затем альдолазу элюируют при линейном изменении концентрации сульфата аммония от 1 М до 0 М. При измерении альдолазной активности в каждой из элюированных фракций определяют наличие пика альдолазной активности во фракции, соответствующей примерно 0,2 М концентрации сульфата аммония.
4. Гель-фильтрационная хроматография: Сефадекс 200 HP 16/60
Отдельные фракции, содержащие альдолазу, объединяют вместе и диализуют с использованием буфера А, после чего фильтруют через фильтр с размером пор 0,45 мкм. Полученный фильтрат концентрируют ультрафильтрацией на мембране centriprep 10. Полученный фильтрат подвергают гель-фильтрации на колонке с Сефадексом 200 HP 16/60 (производство Фармация (Pharmacia), уравновешенной буфером С (20 мМ Трис-HCl, pH 7,6, 0,1 М KCl) для проведения элюции со скоростью течения 1 мл/мин. В ходе указанных процедур альдолаза элюируется во фракциях, соответствующих объему от 66 до 71 мл. На основании положения пика элюированной активности было установлено, что молекулярная масса альдолазы составляет примерно 146 кДа.
5. Анионообменная хроматография: Моно Q НR5/5
Полученные фракции фильтруют через фильтр с размером пор 0,45 мкм. Полученный фильтрат подвергают хроматографии на анионообменной колонке Моно-Q НR5/5 (производство Фармация (Pharmacia), уравновешенной буфером А. В ходе указанных процедур альдолаза адсорбируется на носителе. Неадсорбированные белки вымывают буфером А. Затем белок элюируют при линейном изменении концентрации KCl от 0 мМ до 700 мМ (используют всего 24 мл). При измерении альдолазной активности в каждой из элюированных фракций определяют положение пика альдолазной активности, соответствующее примерно 0,4 М концентрации KCl.
6. Хроматография на гидроксиапатите: CHT-II
Полученные фракции диализуют против буфера D (10 мМ калий-фосфатного буфера, pH 7,0) при 4°С в течение ночи и фильтруют через фильтр с размером пор 0,45 мкм. Полученный фильтрат подвергают хроматографии на колонке с гидроксиапатитом CHT-II, в количестве 5 мл (производство Bio-Rad Laboratories Inc.), уравновешенной буфером D. В ходе указанных процедур альдолаза может отделиться от адсорбированных белков, поскольку не адсорбируется на носителе.
Фракцию, очищенную с помощью указанных выше хроматографических процедур, обрабатывают на ДСН-ПААГ. Обнаруживается практически единственная полоса в положении, соответствующем примерно 25 кДа. Поскольку ранее, при проведении гель-фильтрации, было установлено, что молекулярная масса составляет примерно 146 кДа, было высказано предположение, что альдолаза, возможно, образует гексамер. В таблице 5 проиллюстрирована схема очистки.
Схема очистки ИГОГ альдолазы из Pseudomonas taetrolens штамм ATCC4683
апатит
CHT-II
(3-3) Определение внутренней аминокислотной последовательности ИГОГ альдолазы
Примерно порцию в 2 мкг очищенной альдолазы анализируют в ДСН-ПААГ. Затем образец в ДСН-ПААГ геле обрабатывают трипсином (pH 8,5, 35°C, 20 часов) и разделяют методом ВЭЖХ с обращением фазы для отделения фрагментированных пептидов. Аминокислотные последовательности двух отдельных фракций определяют указанным ниже способом, при этом было показано, что они состоят из 20 остатков и 12 остатков, показанных в виде SEQ ID No. 4 и 5, соответственно (см. табл.6).
Идентифицированная внутренняя аминокислотная последовательность
(3-4) Клонирование гена ИГОГ альдолазы, полученного из P. taetrolens, штамм ATCC4683
1. Получение хромосомной ДНК
P. taetrolens, штамм ATCC4683 культивируют в 50 мл бульонной культуральной среды при 30°С в течение ночи (пре-культура). 5 мл жидкой культуры используют для посева бактерий с последующим культивированием в 50 мл бульонной культуральной среды. После культивирования до достижения поздней логарифмической стадии роста, 50 мл жидкой культуры подвергают центрифугированию (12000 х g, 4°C, 15 минут) и отбирают микробные клетки. Из указанных микробных клеток традиционным способом получают хромосомную ДНК.
2. Определение внутренней последовательности методом ПЦР
На основании идентифицированной внутренней аминокислотной последовательности ИГОГ альдолазы был получен смешанный праймер (SEQ ID No. 6 и 7) (см. табл. 7).
Смешанный праймер, разработанный и синтезированный на основе внутренней аминокислотной последовательности
С использованием изготовленного смешанного праймера проводят ПЦР амплификацию с использованием в качестве матрицы хромосомной ДНК из P. taetrolens, штамм ATCC4683. ПЦР проводят с использованием набора для проведения ПЦР Thermal PERSONEL (производство компании TAKARA BIO INC.) в течение 30 циклов в следующих условиях:
94°С в течение 30 секунд;
55°С в течение 30 секунд;
72°С в течение 1 минуты.
Продукты ПЦР подвергают электрофорезу в геле агарозы с тем, чтобы подтвердить наличие амплифицированного фрагмента размером примерно 500 нп. ДНК фрагмент клонируют в pUC18 для определения его нуклеотидной последовательности. Аминокислотная последовательность, предположенная на основе полученного фрагмента ДНК, была идентична внутренней аминокислотной последовательности ИГОГ альдолазы, так что регенерация целевого альдолазного гена была таким образом подтверждена.
3. Клонирование гена полной длины путем гибридизации колоний
Была предпринята попытка восстановить ген полной длины с использованием фрагмента ДНК, амплифицированного методом ПЦР, путем саузерн-анализа и гибридизации колоний. Зонд ДНК готовят с использованием набора DIG High Prime (производство компании Roche Diagnostics) в соответствии с руководством пользователя, и затем зонд метят в течение ночи в процессе инкубации при 37°С. Саузерн-анализ проводят на полностью расщепленной хромосомной ДНК в количестве 1 мкг с различными ферментами рестрикции при проведении далее электрофореза в 0,8% агарозном геле, блоттинга на нейлоновую мембрану и других процедур, в соответствии с руководством. Гибридизацию проводят с использованием набора DIG Easy Hyb (производство компании Roche Diagnostics) в рамках предварительной гибридизации при 50°С в течение одного часа. Затем добавляют зонд для гибридизации в течение ночи. Определяют полученные полосы с использованием набора DIG Nucleotide Detection Kit. Затем выявляют фрагмент PstI размером примерно 4 кнп, сильно гибридизирующийся с ПЦР фрагментом в качестве зонда. Далее указанный фрагмент PstI восстанавливают путем гибридизации колоний. 20 мкг хромосомной ДНК обрабатывают PstI и подвергают электрофорезу в агарозном геле для восстановления фрагмента размером 4 кнп. Фрагмент конъюгируют в pUC118 с получением библиотеки генов E. coli JM109. Колонии переносят на фильтр с нейлоновой мембраной (Hybond-N производство компании Амершам (Amersham)), проводят впоследствии щелочную денатурацию, нейтрализацию и иммобилизацию. Гибридизацию проводят с использованием набора DIG Easy Hyb. Фильтр погружают в буфер на один час для проведения предварительной гибридизации при 42°С. Затем добавляют подготовленный меченный зонд для проведения гибридизации при 42°С в течение 16 часов. После промывания в SSC, с помощью набора DIG Nucleotide Detection Kit (производство компании Roche Diagnostics) идентифицируют колонию, подвергшуюся гибридизации с зондом. В итоге получат клон, сильно гибридизующийся с зондом.
Определяют нуклеотидную последовательность плазмидной ДНК, выделенной из полученного клона. Показано, что указанная ДНК имеет нуклеотидную последовательность, показанную как SEQ ID No. 1. Обнаружен ориджин репликации размером 678 нп, содержащий нуклеотидную последовательность (с 507-ого по 566-ое положение и с 1046-ого по 1082-ое положение на SEQ ID No. 1), которая соответствует идентифицированной внутренней аминокислотной последовательности, и таким образом была получена целевая альдолаза полной длины.
4. Экспрессия ИГОГ альдолазы в E. Coli (No. 1)
С использованием праймеров (SEQ ID No. 8 и 9), показанных в Таблице 8, амплифицированный фрагмент из хромосомной ДНК P. taetrolens, штамм ATCC4683 обрабатывают BamHI/HindIII и вставляют в сайт BamHI/HindIII в pUC18 для конструирования плазмиды pUCALD. Сконструированную плазмиду экспрессии вводят в E. coli JM109. Полученный трансформант культивируют при встряхивании на культуральной среде LB, содержащей 50 мкг/мл ампициллина при 37°С в течение дня и ночи (пре-культура). Затем жидкую пре-культуру высевают в количестве 1% в 50 мл культуральной среды LB для культивирования при 37°С. Примерно через 2 часа после начала культивирования добавляют ИПТГ до конечной концентрации 1 мМ и продолжают культивирование дополнительно в течение 3 часов. После завершения культивирования собирают микробные клетки, промывают их и суспендируют в 1 мл 20 мМ Трис-HCl, pH 7,6. Затем микробные клетки разрушают на приборе Multi-Bead Shocker (производство компании Yasui Kikai Corporation). Раствор, полученный после разрушения клеток, центрифугируют со скоростью 15000 об/мин в течение 10 минут, и полученный супернатант используют как раствор неочищенного фермента.
Праймеры
С использованием раствора неочищенного фермента определяют альдолазную активность с использованием ФГОГ в качестве субстрата. Тогда как в Е. coli, несущей pUC18 (контроль), не обнаруживается активность ФГОГ альдолазы, в штамме, содержащем pUCADL, обнаруживается активность ФГОГ альдолазы, равная 0,81 Ед/мг белка. Приведенный факт указывает на то, что данный ген кодирует целевую альдолазу.
(3-5) Синтез 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты с использованием штамма, экспрессирующего альдолазу
Используют промытые микробные клетки Е. coli, экспрессирующие альдолазу, полученные по методу пункта (3-4), в качестве источника фермента для проведения синтеза 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты (ИГОГ) из индол-3-пировиноградной кислоты и пировиноградной кислоты. Количество ИГОГ определяют методом ВЭЖХ с использованием колонки Inertsil ODS-2 (5 мкм, 4,6 х 250 мм) (производство GL Science, Inc.). Анализ проводят в следующих условиях:
Мобильная фаза: 40 объемн.% ацетонитрила/5 мМ раствора дегидрофосфата в тетрабутиламмонии
Скорость течения: 1 мл/мин
Температура колонки: 40°С
Обнаружение: УФ при длине волны 210 нм
Промытые микробные клетки E. coli, экспрессирующие альдолазу, добавляют к реакционному раствору, содержащему 100 мМ буфера (Трис-HCl, pH 8,0 или pH 9,0, и глицин-NaOH, pH 10,0), 50мМ индол-3-пировиноградной кислоты, 250 мМ пировиноградной кислоты, 1 мМ MgCl2 и 1 объемн.% толуола, до 10% (вес/объем) для проведения реакции при встряхивании при 33°С в течение 4 часов. Реакционный раствор, содержащий фермент, разбавляют соответствующим образом для измерения полученного ИГОГ (см. табл. 9).
Количество ИГОГ, синтезированной с использованием альдолазы
Как видно из приведенных данных, количество синтезированной ИГОГ повышается в лоте, в который добавлены клетки E. coli, экспрессирующие альдолазу. Таким образом, ИГОГ была получена по пути синтеза, связанного с альдолазой.
(3-6) Масштабная экспрессия ИГОГ альдолазы в E. coli (No. 2)
1. Конструирование плазмиды pTrp4, содержащей trp промотор и rrnB терминатор
С использованием олигонуклеотидов, показанных в таблице 10, в качестве праймеров (сочетание SEQ ID NoNo. 10 и 11) амплифицируют методом ПЦР промоторный регион в trp опероне на хромосомной ДНК Е. coli W3110 в качестве участка целевого гена. Полученный фрагмент ДНК лигируют с вектором pGEM-Teasy (производство Promega Ltd.). В лигирующем растворе E. coli JM109 трансформируют для отбора штамма, в который вставлена целевая плазмида с промотором trp в направлении, обратном направлению lac промотора, среди полученных штаммов с устойчивостью к ампициллину. Затем указанную плазмиду обрабатывают Eco0109I/EcoRI с получением фрагмента ДНК, содержащего trp промотор, который затем лигируют с продуктом pUC19, расщепленным под действием Eco0109I/EcoRI (производство TAKARA BIO INC.). В лигирующем растворе проводят затем трансформацию E. coli JM109 с последующим отбором штамма, содержащего целевую плазмиду, среди полученных штаммов с устойчивостью к ампициллину. Указанную плазмиду обозначают как pTrp1. Затем pKK223-3 (производство Amersham Pharmacia) обрабатывают HindIII/HincII с получением фрагмента ДНК, содержащего терминатор rrnB, который затем лигируют с продуктом расщепления pTrp1 под действием HindIII/PvuII. В указанном лигирующем растворе E. coli JM109 трансформируют с получением штамма, содержащего целевую плазмиду, среди полученных штаммов с устойчивостью к ампициллину. Указанную плазмиду обозначают как pTrp2. Далее олигонуклеотиды, показанные в таблице 10, в качестве праймеров (сочетание SEQ ID NoNo. 10 и 12) и pTrp2 в качестве матрицы используют для проведения ПЦР с целью амплификации участка trp промотора. Полученный фрагмент ДНК обрабатывают Eco0109I/NdeI и лигируют с продуктом расщепления pTrp2 под действием Eco0109I/NdeI. В лигирующем растворе E. coli JM109 трансформируют и отбирают штамм, несущий целевую плазмиду, среди полученных штаммов с устойчивостью к ампициллину. Указанную плазмиду обозначают как pTrp4.
Eco01091
Nde I
Nde I
2. Конструирование плазмид ptrpALD1 и ptrpALD2, экспрессирующих ген альдолазы, и экспрессия в E. coli
С использованием праймеров, показанных в таблице 11 (SEQ ID No.No 9 и 13), амплифицированный фрагмент из хромосомной ДНК P. taetrolens, штамм ATCC4683 обрабатывают NdeI/HindIII и вставляют в сайт NdeI/HindIII в pTrp4 с получением сконструированной плазмиды ptrpALD1. Указанная плазмида экспрессирует ген альдолазы, имеющей аминокислотную последовательность SEQ ID No. 3, начиная с 444-ого кодона ATG в качестве кодона инициации трансляции в нуклеотидной последовательности SEQ ID No. 1. Дополнительно с использованием праймеров (SEQ ID No.No 9 и 14) амплифицированный фрагмент из хромосомной ДНК P. taetrolens, штамм ATCC4683 обрабатывают NdeI/HindIII и вставляют в сайт NdeI/HindIII в pTrp4 с получением сконструированной плазмиды ptrpALD2. Указанная плазмида экспрессирует ген альдолазы, имеющей аминокислотную последовательность SEQ ID No.2, начиная с 456-ого кодона ATG в качестве кодона инициации трансляции в нуклеотидной последовательности SEQ ID No. 1. Индивидуально сконструированные плазмиды экспрессии вставляют в E. coli JM109.
Полученный трансформант культивируют при встряхивании в культуральной среде LB, содержащей 50 мкг/мл ампициллина, при 37°С в течение дня и ночи (пре-культура). 50 мл жидкой пре-культуры высевают в количестве 1% в 50 мл культуральной среды LB для культивирования при 37°С. Примерно через 2 часа после начала культивирования добавляют ИПТГ до конечной концентрации 1 мМ и продолжают культивирование дополнительно в течение 3 часов. После завершения культивирования собирают и промывают микробные клетки, суспендируют их в 1 мл 20 мМ Трис-HCl, pH 7,6 и разрушают в аппарате Multi-bead Shocker (производство компании Yasui Kikai Corporation). Раствор, полученный после разрушения клеток, центрифугируют со скоростью 15000 об/мин в течение 10 минут, и полученный супернатант используют в качестве раствора неочищенного фермента.
Праймеры
В растворе неочищенного фермента определяют активность альдолазы с использованием ФГОГ в качестве субстрата. В то время, как в E. coli, несущей pТrp4 (контроль), не обнаруживается активности ФГОГ альдолазы, в штамме, содержащем ptrpALD1, обнаруживается активность ФГОГ альдолазы, равная 16,1 Ед/мгелка, а в штамме, содержащем ptrpALD2, обнаруживается активность ФГОГ альдолазы, равная 36,0 Ед/мг белка. Этот факт указывает на то, что альдолаза с последовательностями SEQ ID No. 2 и 3 обладает альдолазной активностью.
Пример 4
Пример 4 относится к реакции 3 по настоящему изобретению. В данном примере 4 монатин и 4-фенилметил-4-гидрокси-глютаминовую кислоту (ФГГ) анализируют методом высокоэффективной жидкостной хроматографии с использованием колонки Inertsil ODS-80A (5 мкм, 6 х 150 мм) (производство GL Science, Inc.). Анализ проводят с соблюдением указанных ниже условий.
Мобильная фаза: 12 объемн.% ацетонитрила/ 0,05 объемн.% водного раствора трифторуксусной кислоты
Скорость течения: 1,5 мл/мин
Температура колонки: 30°С и
Обнаружение: УФ, при длине волны 210 нм
В указанных аналитических условиях подвергаются фракционированию и анализу (2S, 4S)-монатин и (2R, 4R)-монатин, имеющие время удерживания 12,1 минут, а также (2S, 4R)-монатин и (2R, 4S)-монатин, имеющие время удерживания 9,7 минут, (2S, 4S)-ФГГ и (2R, 4R)-ФГГ, имеющие время удерживания 7,2 минут, и (2S, 4R)-ФГГ и (2R, 4S)-ФГГ, имеющие время удерживания 6,0 минут.
При необходимости дополнительно проводят анализ методом ВЭЖХ с использованием колонки для оптического разрешения CROWNPAK CR (+) (4,6 х 150 мм) (производство компании Daicel Chemical Industries, Ltd.). Анализ проводят с соблюдением указанных ниже условий.
(В случае монатина)
Мобильная фаза: водный раствор перхлорной кислоты, рН 1,5/10 объемн.% метанола
Скорость течения:0,5 мл/мин.
Температура колонки 30°С и
Обнаружение: УФ, при длине волны 210 нм
В указанных аналитических условиях фракционируют и анализируют оптические изомеры монатина (2R, 4S), (2R, 4R), (2S, 4R) и (2S, 4S) со значениями времени удерживания 42, 57, 64 и 125 минут, соответственно, в указанном порядке.
(В случае ФГГ)
Мобильная фаза: водный раствор перхлорной кислоты, pH 1,5
Скорость течения: 1 мл/мин
Температура колонки 30°С и
Обнаружение: УФ, при длине волны 210 нм
В указанных аналитических условиях фракционируют и анализируют оптические изомеры ФГГ (2R, 4S), (2R, 4R), (2S, 4R) и (2S, 4S) со значениями времени удерживания 20 минут, 28 минут, 31 минута и 46 минут, соответственно, в указанном порядке.
(4-1) Получение (2S, 4S)-монатина с использованием трансаминазы L-аминокислоты
Микроорганизмы, показанные ниже в таблице 12, инокулируют в бульонную культуральную среду в чашках Петри (Eiken Chemical Со., Ltd.) с последующим культивированием при 30°С в течение 24 часов. Микробные клетки инокулируют в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 7,6, 30 мМ ИГОГ, 100 М однонатриевой соли L-глютамата, 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола до 5 мас.% по весу влажных микробных клеток с последующим инкубированием при 30°С в течение 16 часов. После завершения реакции анализируют полученный монатин. Результаты анализа показаны в таблице 12. Видно, что (2S, 4S)-монатин может быт получен из ИГОГ.
(4-2) Получение (2S, 4S)-ФГГ с использованием трансаминазы L-аминокислоты
Микроорганизмы, показанные ниже в таблице 13, инокулируют в бульонную культуральную среду в чашках Петри (Eiken Chemical Со., Ltd.) с последующим культивированием при 30°С в течение 24 часов. Микробные клетки инокулируют в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 7,6, 30 мМ ФГОГ, 100 мМ однонатриевой соли L-глютамата или L-аспартата, 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола до уровня 5 мас.% по весу влажных микробных клеток с последующим инкубированием при 30°С в течение 16 часов. После завершения реакции оценивают уровень образованного ФГГ. Результаты анализа приведены в таблице 13. Показано, что (2S, 4S)-ФГГ может быт получен из ФГОГ.
(4-3) Получение (2S, 4S)-ФГГ с использованием трансаминазы L-аминокислоты
Микроорганизмы, показанные ниже в таблице 14, инокулируют в бульонную культуральную среду в чашках Петри (Eiken Chemical Со., Ltd.) с последующим культивированием при 30°С в течение 24 часов. Культуральную среду, содержащую 0,5 г/дл фумаровой кислоты, 1 г/дл дрожжевого экстракта, 1 г/дл пептона, 0,3 г/дл сульфата аммония, 0,3 г/дл K2HPO4, 0,1 г/дл KH2PO4, 1 мг/дл FeSO4 · 7H2O и 0,1 г/дл MnSO4 · 4H2O, pH 7,0, разделяют на порции по 50 мл, вносят в колбы Сакагучи на 500 мл и стерилизуют при 110°С в течение 10 минут. В полученную жидкую культуральную среду инокулируют одну петлю культуры для культивирования при встряхивании при 30°С в течение 16 часов. Центрифугируют 1 мл жидкой культуры с получением микробных клеток, которые затем промывают и собирают в 20 мМ Трис-HCl, pH 7,6, после чего суспендируют в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 7,6, 50 мМ ФГОГ, 100 мМ однонатриевой соли L-глютамата, 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола. Полученную суспензию переносят в опытные пробирки на 10 мл с последующим проведением реакции при встряхивании при 30°С в течение 18 часов. Образованный ФГГ анализируют после завершения реакции. Результаты анализа показаны в таблице 14. Показано, что (2S, 4S)-ФГГ может быть получен из ФГОГ.
(4-4) Получение 2R-ФГГ с использованием трансаминазы D-аминокислоты
Микроорганизмы, показанные ниже в таблице 15, инокулируют в бульонную культуральную среду в чашках Петри (Eiken Chemical Со., Ltd.) с последующим культивированием при 30°С в течение 24 часов. Инокуляцию проводят в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 7,6, 50 мМ ФГОГ, 100 мМ D-глютаминовой кислоты, 100 мМ D-аланина, 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола до достижения 5 мас.% по весу влажных микробных клеток с последующим инкубированием при 30°С в течение 16 часов. После завершения реакции оценивают уровень образованного ФГГ. Результаты анализа приведены в таблице 15. Показано, что (2R, 4S)-ФГГ и (2R, 4R)-ФГГ могут быть получены из ФГОГ.
(4-5) Получение E. coli, экспрессирующей DAT, полученный из Bacillus sphaericus (обозначаемый далее как BSDAT ), и образование 2R-ФГГ в реакции с промытыми микробными клетками
1. Конструирование плазмиды экспрессии
Для экспрессии в E. coli гена трасаминазы D-аминокислоты (обозначаемого далее сокращенно как "bsdat"), полученного из Bacillus sphaericus, конструируют плазмиду pUCBSDAT, таким образом, чтобы ген bsdat был конъюгирован вниз по ходу транскрипции от lac промотора pUC18. С использованием хромосомной ДНК из Bacillus sphaericus, штамм ATTC10208 в качестве матрицы и олигонуклеотидов, показанных ниже в таблице 16, в качестве праймеров проводят вначале амплификацию данного гена методом ПЦР. Таким способом может быть амплифицирован фрагмент ДНК, соответствующий участку от 8-ого до 1278-ого положения в нуклеотидной последовательности bsdat, описанной как SEQ ID No. 2 в тексте публикации по Европейскому патенту
0 736 604. Указанный фрагмент обрабатывают BamHI и PstI, конъюгируют с продуктом расщепления pUC18 под действием BamHI/PstI и вводят в E. coli JM109. Из полученных устойчивых к ампициллину штаммов отбирают штамм с целевой плазмидой для конструирования плазмиды экспрессии pUCBSDAT.
2. Получение E. coli, экспрессирующей BSDAT
Трансформированную E. coli, содержащую pUCBSDAT, высевают для культивирования в культуральную среду LB (1 г/дл бактотриптона, 0,5 г/дл дрожжевого экстракта и 1 г/дл NaCl), содержащую 0,1 мг/мл ампициллина при 37°С в течение 16 часов. 1 мл жидкой культуры вносят в качестве посевного материла в колбу Сакагучи объемом 500 мл, содержащую 50 мл культуральной среды LB, и далее культивируют при 37°С. Через 2,5 часа после начала культивирования добавляют изопропил-1-тио-β-D-галактопиранозид (ИПТГ) до конечной концентрации 1мМ и продолжают культивирование дополнительно в течение 4 часов. Из полученной жидкой культуры собирают микробные клетки и промывают их с получением клеток E. coli, экспрессирующих BSDAT.
3. Реакция с добавлением промытых микробных клеток при использовании, в качестве последних, E. coli, экспрессирующей BSDAT
Микробные клетки, полученные по описанному выше способу пункта 2, суспендируют в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 7,6, 50 мМ ФГОГ, 100 мМ доноров аминокислоты (D-Glu, D-Ala, L-Glu, L-Ala), 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола до достижения 5 мас.% по весу влажных микробных клеток и полученную суспензию переносят в опытные пробирки на 10 мл для проведения реакции при встряхивании при 30°С в течение 18 часов. Образованный ФГГ анализируют после завершения реакции. Результаты анализа показаны в таблице 17. Показано, что (2R, 4R), (2R, 4S) и (2S, 4S)-ФГГ могут быть получены из ФГОГ.
ФГГ (мМ), полученный в реакции с промытыми микробными клетками с использованием в качестве последних E. coli, экспрессирующей BSDAT
(4-6) Получение E. coli, экспрессирующей DAT из Bacillus macerans AJ1617 (обозначаемый далее как BMDAT ), и образование 2R-монатина в реакции с промытыми микробными клетками
1. Получение хромосомной ДНК
Bacillus macerans, штамм AJ1617 культивируют в течение ночи в бульонной культуральной среде в колбах на 50 мл при 30°С (пре-культура). 5 мл жидкой культуры высевают в качестве посевного бактериального материла для культивирования в 50 мл бульонной культуральной среды. После достижения при культивировании микробного штамма поздней логарифмической фазы роста 50 мл жидкой культуры подвергают центрифугированию (12000 х g, 4°C, 15 минут) и отбирают микробные клетки. Из указанных микробных клеток обычным способом получают хромосомную ДНК.
2. Выделение гена трансаминазы D-аминокислоты из Bacillus macerans (обозначаемого далее как bmdat) из библиотеки генов
Вначале добавляют одну единицу рестрикционного фермента EcoRI к 30 мкг хромосомной ДНК из Bacillus macerans, штамм AJ1617 с проведением 3-часовой реакции при 37°С для достижения частичного расщепления. Затем регенерируют фрагменты размером 3-6 кнп из ДНК с помощью электрофореза в агарозном геле. Указанные фрагменты лигируют с 1 мкг продукта расщепления плазмиды pUC118 под действием EcoRI (после обработки BAP; производство TaKaRa Brewery, Co., Ltd.) для трансформации E. coli JM109 с получением генной библиотеки, которую далее добавляют в культуральную среду LB (1% триптофана, 0,5% дрожжевого экстракта, 1% хлорида натрия, 2% агара, pH 7,0), содержащую ампициллин, с получением колоний. Образованные колонии культивируют в течение ночи в жидкой культуральной среде LB, содержащей ампициллин и изобутил-1-тио-β-D-галактопиранозид (ИПТГ) в количестве 1 мМ при 37°С с последующим центрифугированием для сбора образованных микробных клеток. Полученные микробные клетки инокулируют в реакционный раствор, содержащий 100 М Трис-HCl, pH 8,0, 50 мМ пирувата натрия, 100 мМ D-глютаминовой кислоты, 1 мМ пиридоксаль-5'-фосфата и 1 объемн.% толуола для проведения реакции при 30°С в течение 30 минут. После завершения реакции реакционный раствор центрифугируют. 5 мкл полученного отделенного супернатанта вносят в ячейки 96-ячеечного планшета, содержащие по 200 мкл реакционного раствора для анализа пировиноградной кислоты (100 мМ Трис-HCl, pH 7,6, 1,5 мМ НАДН, 5 мМ MgCl2, 16 Ед/мл лактатдегидрогеназы (производство Oriental Yeast Co., Ltd.), и проводят реакцию при 30°С в течение 10 минут. Затем определяют поглощение при длине волны 340 нм на счетчике для анализа планшетов (SPECTRA MAX190, производство Molecular Device). Тот же самый тест проводят при добавлении пирувата натрия до конечной концентрации от 0,2 мМ до 1 мМ. С использованием указанного соединения в качестве стандарта оценивают количество восстановленной пировиноградной кислоты для обнаружения трансаминазной активности D-аминокислоты.
Путем скрининга клонов на DAT активность отбирают клоны, обладающие DAT активностью. Из указанных трансформантов выделяют плазмиды, содержащие bmdat, и обозначают как pUCBMDAT. Плазмиду pUCBMDAT обрабатывают EcoRI и подвергают электрофорезу в агарозном геле, подтверждая, что вставленный фрагмент имеет длину примерно 3,3 кнп.
3. Нуклеотидная последовательность вставленного фрагмента
Нуклеотидную последовательность вставленного фрагмента плазмиды pUCBMDAT определяют дидезокси методом. Идентифицируют открытую рамку для считывания (ОРС) размером примерно 850 нп, соответствующую участку от 630-ого до 1481-ого положения в последовательности SEQ ID No.17, приведенной в перечне последовательностей.
Оценивается гомология данной ОРС с известными последовательностями. ОРС обладает 91% уровнем гомологии с геном трансаминазы D-аминокислоты из Bacillus sphaericus ATTC10208 по аминокислотной последовательности, 66% уровнем гомологии с геном трансаминазы D-аминокислоты из Bacillus sp. YM-1 по аминокислотной последовательности и 42% уровнем гомологии с геном трансаминазы D-аминокислоты из Bacillus licheniformis ATCC10716 по аминокислотной последовательности. Полученные результаты четко показывают, что ОРС кодирует гены трансаминазы D-аминокислоты. Исходя из полученных данных, была вычислена гомология с помощью программного обеспечения для генного анализа "genetyx ver.6" (GENETYX), для которой использовались также другие исходно установленные параметры.
4. Получение E. coli, экспрессирующей BMDAT
Трансформант E. coli, содержащий pUCBMDAT, высевают с последующим культивированием в культуральной среде LB (1 г/дл бактотриптона, 0,5 г/дл дрожжевого экстракта и 1 г/дл NaCl), содержащей 0,1 мг/мл ампициллина, при 37°С в течение 16 часов. Добавляют 1 мл жидкой культуры в качестве посевного материала в колбу Сакагучи объемом 500 мл, содержащую 50 мл культуральной среды LB, и далее культивируют при 37°С. Через 2,5 часа после начала культивирования добавляют изопропил-1-тио-β-D-галактопиранозид (ИПТГ) до конечной концентрации 1мМ и продолжают культивирование дополнительно в течение 4 часов. Из полученной жидкой культуры отбирают микробные клетки и промывают их с получением клеток E. coli, экспрессирующих BMDAT.
5. Реакция с промытыми микробными клетками с использованием в качестве последних E. coli, экспрессирующей BMDAT
Микробные клетки, полученные по описанному выше в пункте 4 способу, суспендируют в 1 мл реакционного раствора, содержащего 100 мМ Трис-HCl, pH 8,0, 50 мМ ИГОГ, 200 мМ D-аланина, 1 мМ пиридоксаль-5'-фосфата и 0,5 объемн.% толуола, до достижения 5 мас.% по весу сырых микробных клеток и полученную суспензию переносят в опытные пробирки на 10 мл для проведения реакции при встряхивании при 30°С в течение 20 часов. После завершения реакции оценивают наличие образованного 2R-монатина. Делается вывод, что может продуцироваться 22 мМ 2R-монатин.
Промышленная применимость
В соответствии с настоящим изобретением, описываемый в нем способ получения производных глютамата может использоваться для эффективного получения определенных производных глютамата, включая монатин, перспективный как подсластитель, и т.п., с использованием ферментативной реакции. Таким образом, настоящий процесс является чрезвычайно полезным для промышленного применения.
Кроме того, способ получения монатина по настоящему изобретению включает способ получения производных глютамата по настоящему изобретению, в соответствии с которым может быть получен монатин очень эффективно с использованием в качестве исходного материала триптофана, как одной из аминокислот, путем ферментативной реакции. Способ очень полезен в промышленном приложении, особенно в области пищевой промышленности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИНДОЛ-3-ПИРОВИНОГРАДНОЙ КИСЛОТЫ И ЕЕ ПРОИЗВОДНЫХ | 2006 |
|
RU2325442C2 |
| НОВАЯ АЛЬДОЛАЗА И СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ α-КЕТОКИСЛОТ | 2003 |
|
RU2307871C2 |
| НОВАЯ АЛЬДОЛАЗА И СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ IHOG И МОНАТИНА | 2005 |
|
RU2313579C2 |
| ПИТЬЕВАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ МОНАТИН, И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ | 2004 |
|
RU2380989C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНАТИНА | 2011 |
|
RU2505606C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4-ДИГИДРОКСИБУТИРАТА | 2013 |
|
RU2645260C2 |
| ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ ЧЕТЫРЕХУГЛЕРОДНЫХ СПИРТОВ | 2006 |
|
RU2394913C2 |
| Новые трансаминазы и способ дезаминирования аминосоединения с их применением | 2016 |
|
RU2718778C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИПЕПТИДА (ВАРИАНТЫ) | 2005 |
|
RU2316596C2 |
| ГЕН ПЕПТИДООБРАЗУЮЩЕГО ФЕРМЕНТА, ПЕПТИДООБРАЗУЮЩИЙ ФЕРМЕНТ И СПОСОБ ПОЛУЧЕНИЯ ДИПЕПТИДА | 2002 |
|
RU2280077C2 |
Изобретение относится к биотехнологии. Способ получения производного глютамата, например монатина, включает ферментативное получение замещенной α-кетокислоты, из которой затем в присутствии фермента, такого как трансаминаза получают желаемый продукт. Заявленное изобретение позволяет упростить и удешевить способ получения производных глютамата, включая его соли. 3 н. и 31 з.п. ф-лы, 17 табл.
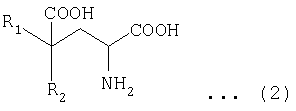
(в общей формуле (2) имеют те же значения, что R1 и R2 в общей формуле (1))
в присутствии фермента, катализирующего реакцию получения производного глютамата общей формулы (2) из замещенной α-кетокислоты общей формулы (1)

(в общей формуле (1) R1 представляет собой заместитель, выбранный из группы, состоящей из арильной группы, содержащей до 20 атомов углерода, аралкильной группы, содержащей до 20 атомов углерода, и углеводородной группы, содержащей гетероциклическое кольцо, а R2 представляет собой гидроксильную группу), включая стадию развития реакции.
[I] Стадия образования замещенной а-кетокислоты общей формулы (4)

(R в общей формуле (4) имеет то же значение, что и R в общей формуле (3)) в присутствии фермента, катализирующего реакцию образования замещенной α-кетокислоты общей формулы (4) из замещенной α-кетокислоты, описываемой общей формулой (3)

(в общей формуле (3) R обозначает заместитель, выбранный из группы, состоящей из С2-С8 алкильных групп, С1-С8 алкоксильных групп, С2-С9 карбоксиалкильных групп, арильных групп, содержащих по 20 атомов углерода, аралкильных групп, содержащих до 20 атомов углерода, углеводородной группы, содержащей гетероциклическое кольцо, и гидроксильной группы; если R содержит ароматическое кольцо или гетероциклическое кольцо, указанное ароматическое кольцо или гетероциклическое кольцо может быть дополнительно замещено атомом галогена, гидроксильной группой, алкильными группами, содержащими до 3 атомов углерода, алкоксильными группами, содержащими до 3 атомов углерода, и аминогруппой), и щавелевоуксусной кислоты или пировиноградной кислоты, включая стадию развития реакции; и
[II] стадия образования производного глютамата (включая его солевые формы), описываемого общей формулой (5), в присутствии фермента, катализирующего реакцию образования производного глютамата, описываемого общей формулой (5)

(R в общей формуле (5) имеет то же значение, что и R в общей формуле (3)), из замещенной α-кетокислоты общей формулы (4), включая стадию развития реакции.
(a) белок, который содержит аминокислотную последовательность SEQ ID NO. 2, приведенную в перечне последовательностей;
(b) белок, который содержит аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO. 2, приведенной в перечне последовательностей, и обладает альдолазной активностью;
(c) белок, который содержит аминокислотную последовательность SEQ ID NO. 3;
(d) белок, который содержит аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO. 3, приведенной в перечне последовательностей, и обладает альдолазной активностью.
(a) белок, который содержит аминокислотную последовательность SEQ ID NO. 2, приведенную в перечне последовательностей;
(b) белок, который содержит аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO. 2, приведенной в перечне последовательностей, и обладает альдолазной активностью;
(c) белок, который содержит аминокислотную последовательность SEQ ID NO.3;
(d) белок, который содержит аминокислотную последовательность, полученную при замещении, делеции, вставке, добавлении и/или инверсии одного или нескольких аминокислотных остатков в аминокислотной последовательности SEQ ID NO. 3, приведенной в перечне последовательностей, и обладает альдолазной активностью.
[A] стадия получения индол-3-пировиноградной кислоты в присутствии фермента, катализирующего реакцию превращения триптофана в индол-3-пировиноградную кислоту, путем создания условий для реакции триптофана;
[B] стадия получения 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты из индол-3-пировиноградной кислоты и щавелевоуксусной кислоты или пировиноградной кислоты;
[C] стадия получения монатина в присутствии фермента, катализирующего реакцию получения монатина из 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты, путем создания условий для реакции 4-(индол-3-илметил)-4-гидрокси-2-оксоглутаровой кислоты.
| VIRGIL HELAINE et al., Tetrahedron letters, vol 40, no 36, 1999, p.6577-6580 | |||
| DAVI DE JESUS OLIVEIRA et al., Tetrahedron letters, vol 42, 2001, p.6793-6796 | |||
| А.МАЙСТЕР Биохимия аминокислот, М., Издательство иностранной литературы, 1961, с.228-239. |
Авторы
Даты
2006-07-20—Публикация
2002-12-09—Подача