Текст описания приведен в факсимильном виде.




























































































































































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| НОВАЯ АЛЬДОЛАЗА И СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ IHOG И МОНАТИНА | 2005 |
|
RU2313579C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ГЛЮТАМАТА (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ МОНАТИНА | 2002 |
|
RU2280078C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНДОЛ-3-ПИРОВИНОГРАДНОЙ КИСЛОТЫ И ЕЕ ПРОИЗВОДНЫХ | 2006 |
|
RU2325442C2 |
| ПИТЬЕВАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ МОНАТИН, И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ | 2004 |
|
RU2380989C2 |
| НОВАЯ АЛЬДОЛАЗА, ДНК, КОДИРУЮЩАЯ АЛЬДОЛАЗУ, КЛЕТКИ, ТРАНСФОРМИРОВАННЫЕ ДНК, СПОСОБ ПОЛУЧЕНИЯ АЛЬДОЛАЗЫ И СПОСОБ ПОЛУЧЕНИЯ 4-ГИДРОКСИ-L-ИЗОЛЕЙЦИНА (ВАРИАНТЫ) | 2006 |
|
RU2338784C2 |
| Новый вариант аминотрансферазы аминокислот с разветвленной цепью и способ получения лейцина с его использованием | 2020 |
|
RU2802274C1 |
| БАКТЕРИЯ - ПРОДУЦЕНТ ПРОДУКТА РЕАКЦИИ, КАТАЛИЗИРУЕМОЙ БЕЛКОМ, ОБЛАДАЮЩИМ АКТИВНОСТЬЮ 2-ОКСОГЛУТАРАТ-ЗАВИСИМОГО ФЕРМЕНТА, И СПОСОБ ПРОДУКЦИИ УКАЗАННОГО ПРОДУКТА | 2008 |
|
RU2444568C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛИРОВАННОГО L-ЛЕЙЦИНА И БАКТЕРИЯ, ТРАНСФОРМИРОВАННАЯ ДНК, КОДИРУЮЩЕЙ ДИОКСИГЕНАЗУ | 2011 |
|
RU2468085C1 |
| МАЛАЯ СУБЪЕДИНИЦА ИЗОЗИМА III И ИЗОЗИМ III СИНТЕТАЗЫ АЦЕТОГИДРОКСИКИСЛОТ ИЗ ESCHERICHIA COLI, ФРАГМЕНТ ДНК (ВАРИАНТЫ), ШТАММ БАКТЕРИИ ESCHERICHIA COLI - ПРОДУЦЕНТ L-ВАЛИНА (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ L-ВАЛИНА | 2000 |
|
RU2209246C2 |
| СПОСОБ ПРОДУКЦИИ 2-АМИНО-3-МЕТИЛ-4-КЕТОПЕНТАНОАТА | 2007 |
|
RU2392323C2 |
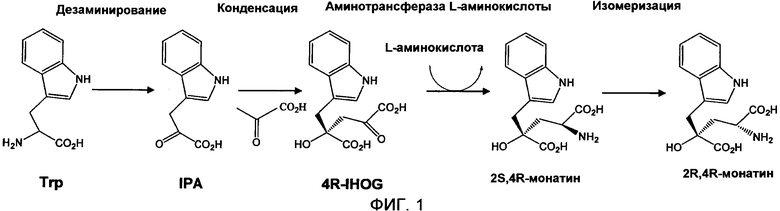




Настоящее изобретение относится к области биохимии, и представляет собой способ получения 2S,4R-монатина или его соли, предусматривающий контактирование 4R-IHOG с аминотрансферазой L-аминокислоты в присутствии L-аминокислоты, и способ получения 2R,4R-монатина или его соли, предусматривающий изомеризацию 2S,4R-монатина. Также настоящее изобретение раскрывает аминотрансферазы L-аминокислоты для осуществления способов получения монатина и способ получения таких L-аминотрансфераз, предусматривающий культивирование бактериальной клетки, в которую введен вектор экспрессии, содержащий полинуклеотид, кодирующий представленную аминотрансферазу. Настоящее изобретение позволяет получить 2S,4R-монатин и 2R,4R-монатин с улучшенным выходом благодаря использованию раскрытых аминотрансфераз L-аминокислоты. 9 н. и 18 з.п. ф-лы, 6 ил., 23 табл., 48 пр.
1. Способ получения 2S,4R-монатина или его соли, предусматривающий контактирование 4R-IHOG с аминотрансферазой L-аминокислоты в присутствии L-аминокислоты, с образованием 2S,4R-монатина, где в котором аминотрансфераза L-аминокислоты состоит из аминокислотной последовательности, которая на 90% или более идентична аминокислотной последовательности, представленной последовательностью SEQ ID NO:2, SEQ ID NO:48, SEQ ID NO:53, SEQ ID NO:61, SEQ ID NO:65, SEQ ID NO:67, SEQ ID NO:69, SEQ ID NO:73, SEQ ID NO:75, SEQ ID NO:77, SEQ ID NO:83, SEQ ID NO:85, SEQ ID NO:87, SEQ ID NO:89, SEQ ID NO:91, SEQ ID NO:93, SEQ ID NO:95, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:101, SEQ ID NO:103, SEQ ID NO:105, SEQ ID NO:107, SEQ ID NO:109 или SEQ ID NO:111.
2. Способ получения по п.1, дополнительно предусматривающий контактирование кето-кислоты с декарбоксилазой для деградации кето-кислоты, при этом кето-кислота образуется из L-аминокислоты под действием аминотрансферазы L-аминокислоты.
3. Способ получения по п.1, в котором L-аминокислота является L-аспартатом.
4. Способ получения по п.3, дополнительно предусматривающий контактирование оксалоацетата с оксалоацетатдекарбоксилазой для необратимого образования пирувата, при этом оксалоацетат образуется из L-аспартата под действием аминотрансферазы L-аминокислоты.
5. Способ получения по п.1, в котором аминотрансфераза L-аминокислоты получена из микроорганизма, относящегося к роду Arthrobacter, роду Bacillus, роду Candida, роду Corynebacterium, роду Lodderomyces, роду Micrococcus, роду Microbacterium, роду Nocardia, роду Pseudomonas, роду Rhizobium, роду Stenotrophomonas, роду Dietzia, роду Ochrobactrum, роду Brevundimonas, роду Burkholderia, роду Carnimonas, роду Yarrowia, роду Clostridium, роду Deinococcus, роду Eubacterium, роду Lactobacillus, роду Methanothermobacter, роду Phormidium, роду Pyrococcus, роду Rhodococcus, роду Saccharomyces, роду Saccharophagus, роду Sinorhizobium, роду Thermoanaerobacter, роду Thermotoga или роду Thermus.
6. Способ получения по п.5, в котором аминотрансфераза L-аминокислоты получена из микроорганизма, относящегося к виду Arthrobacter sp., Bacillus altitudinis, Bacillus cellulosilyticus, Bacillus pumilus, Bacillus sp., Candida norvegensis, Candida inconspicua, Corynebacterium ammoniagenes, Corynebacterium glutamicum, Lodderomyces elongisporus, Micrococcus luteus, Microbacterium sp., Nocardia globerula, Pseudomonas chlororaphis, Pseudomonas citronocllolis, Pseudomonas fragi, Pseudomonas putida, Pseudomonas synxantha, Pseudomonas taetrolens, Pseudomonas sp., Rhizobium radiobacter, Rhizobium sp., Stenotrophomonas sp., Dietzia marts, Ochrobactrum pseudogrignonense, Brevundimonas diminuta, Burkholderia sp., Carnimonas sp., Yarrowia lypolytica, Clostridium cellulolyticum, Deinococcus geothermalis, Eubacterium rectale, Lactobacillus acidophilus, Methanothermobacter thermautotrophicus, Phormidium lapideum, Pyrococcus horikoshii, Rhodococcus erythropolis, Saccharomyces cerevisiae, Saccharophagus degradans, Sinorhizobium meliloti, Thermoanaerobacter tengcongensis, Thermotoga maritima или Thermus thermophilus.
7. Способ получения по п.1, в котором аминотрансфераза L-аминокислоты содержит одну или несколько мутаций аминокислотных остатков, выбранных из группы, состоящей из аминокислотных остатков в положении 39, в положении 109, в положении 128, в положении 150, в положении 258, в положении 287, в положении 288, в положении 289, в положении 303, в положении 358 и в положении 431 в аминокислотной последовательности, представленной последовательностью SEQ ID NO:2.
8. Способ получения по п.7, в котором одна или несколько мутаций аминокислотных остатков выбраны из группы, состоящей из
i) замены лизина в положении 39 аргинином;
ii) замены серина в положении 258 глицином;
iii) замены глутамина в положении 287 глутаминовой кислотой;
iv) замены треонина в положении 288 глицином;
v) замены изолейцина в положении 289 аланином;
vi) замены аспарагиновой кислоты в положении 109 глицином;
vii) замены гистидина в положении 150 тирозином;
viii) замены фенилаланина в положении 303 лейцином;
ix) замены аспарагиновой кислоты в положении 358 тирозином;
х) замены серина в положении 431 треонином; и
xi) замены глутаминовой кислоты в положении 128 глицином.
9. Способ получения по п.1, в котором 4R-IHOG приводят в контакт с аминотрансферазой L-аминокислоты, используя трансформант, который экспрессирует указанную аминотрансферазу L-аминокислоты.
10. Способ получения по п.1, дополнительно предусматривающий конденсацию индол-3-пирувата и пирувата, с образованием 4R-IHOG.
11. Способ получения по п.10, в котором индол-3-пируват и пируват конденсируют путем контактирования индол-3-пирувата и пирувата с альдолазой.
12. Способ получения по п.10, в котором по меньшей мере часть пирувата, используемого при образовании 4R-IHOG, получена из пирувата, образованного из оксалоацетата под действием оксалоацетатдекарбоксилазы.
13. Способ получения по п.10, дополнительно предусматривающий дезаминирование триптофана с образованием индол-3-пирувата.
14. Способ получения по п.13, в котором триптофан дезаминируют контактированием триптофана с ферментом, осуществляющим дезаминирование.
15. Способ получения по п.10 или 13, в котором получение 2S,4R-монатина или его соли осуществляют в одном реакторе.
16. Способ получения 2R,4R-монатина или его соли, предусматривающий следующее (I) и (II):
(I) осуществление способа по п.1 с образованием 2S,4R-монатина; и
(II) изомеризацию 2S,4R-монатина с образованием 2R,4R-монатина.
17. Способ получения по п.16, в котором изомеризацию 2S,4R-монатина осуществляют в присутствии ароматического альдегида.
18. Способ получения по п.16, в котором солью является натриевая соль или калиевая соль.
19. Аминотрансфераза L-аминокислоты, которая является белком, выбранным из группы, состоящей из следующих (А) и (В):
(A) белка, состоящего из аминокислотной последовательности, которая на 90% или более идентична аминокислотной последовательности, представленной последовательностью SEQ ID NO:2, и обладающего активностью аминотрансферазы L-аминокислоты;
где белок (А) содержит в качестве основной мутации одну или несколько мутаций аминокислотных остатков, выбранных из группы, состоящей из:
i) замены лизина в положении 39 аргинином;
ii) замены серина в положении 258 глицином;
iii) замены глутамина в положении 287 глутаминовой кислотой;
iv) замены треонина в положении 288 глицином;
v) замены изолейцина в положении 289 аланином;
(B) белка, состоящего из аминокислотной последовательности, содержащей мутацию от одного до тридцати аминокислотных остатков, которые выбраны из группы, состоящей из делеции, замены, добавления и вставки аминокислотных остатков в аминокислотной последовательности, представленной последовательностью SEQ ID NO:2, и обладающего активностью аминотрансферазы L-аминокислоты,
где белок (В) содержит в качестве основной мутации одну или несколько мутаций аминокислотных остатков, выбранных из группы, состоящей из:
i) замены лизина в положении 39 аргинином;
ii) замены серина в положении 258 глицином;
iii) замены глутамина в положении 287 глутаминовой кислотой;
iv) замены треонина в положении 288 глицином;
v) замены изолейцина в положении 289 аланином.
20. Полинуклеотид, который кодирует аминотрансферазу L-аминокислоты по п.19.
21. Вектор экспрессии, содержащий полинуклеотид по п.20.
22. Бактериальная клетка, в которую введен вектор экспрессии по п.21.
23. Способ получения L-аминотрансферазы, предусматривающий культивирование бактериальной клетки по п.22 в среде, с получением аминотрансферазы L-аминокислоты.
24. Способ получения 2S,4R-монатина или его соли, предусматривающий контактирование 4R-IHOG с аминотрансферазой L-аминокислоты по п.19 в присутствии L-аминокислоты, с образованием 2S,4R-монатина.
25. Способ получения 2R,4R-монатина или его соли, предусматривающий следующее (I') и (II'):
(I') осуществление способа по п.24 с образованием 2S,4R-монатина; и
(II') изомеризацию 2S,4R-монатина, с образованием 2R,4R-монатина.
26. Способ получения по п.25, в котором изомеризация 2S,4R-монатина происходит в присутствии ароматического альдегида.
27. Способ получения по п.25, в котором солью является натриевая соль или калиевая соль.
| WO 2005001105 А1, 06.01.2005 | |||
| US 6582935 B2, 24.06.2003 | |||
| WO 03059865 А1, 24.07.2003 | |||
| СПОСОБ ПОЛУЧЕНИЯ МОНАТИНА | 2005 |
|
RU2351587C2 |
Авторы
Даты
2014-01-27—Публикация
2011-10-12—Подача