Настоящее изобретение относится к способу получения 14b-гидрокси-1,14-карбонатбаккатина III. Продукт, полученный способом данного изобретения, можно использовать для получения новых таксановых производных, обладающих противоопухолевой активностью.
Таксаны являются одним из наиболее важных классов противоопухолевых агентов, созданных в последние годы. Паклитаксель представляет собой дитерпеновый комплекс, полученный из коры Taxus brevifolia, и считается одним из основных лекарственных средств в терапии рака. В настоящее время проводится интенсивный поиск новых таксановых производных, обладающих превосходящей фармакологической активностью и улучшенным фармакокинетическим профилем. Особый подход относится к производным баккатина III, модифицированным различным образом относительно исходной структуры. Примеры указанных соединений представлены производными 14b-гидроксибаккатина III, описанными в патенте США 5705508, WO 97/43291, WO 96/36622. В настоящее время производные 14b-гидроксидеацетилбаккатина III-1,14-карбоната получают исходя из предшественника 14b-гидроксидеацетилбаккатина III, который представляет собой природное соединение, добываемое в небольших количествах в результате экстракции листьев Taxus wallichiana, как описано в ЕР 559019. Существует огромная потребность в новых способах простого эффективного получения больших количеств 14b-гидрокси-1,14-карбонатбаккатина III и, следовательно, его производных.
В настоящее время было найдено, что 14b-гидроксибаккатин III-1,14-карбонат можно получить способом исходя из 13-кетобаккатина III, при этом последнее соединение можно легко получить из 10-деацетилбаккатина III, который, в свою очередь, легко выделить в больших количествах из листьев Taxus baccata, в отличие от 14b-гидроксибаккатина III.
Таким образом, изобретение относится к способу получения 14b-гидроксибаккатин III-1,14-карбоната, который включает следующие стадии:
а. обработку 7-Вос-13-кетобаккатина III формулы
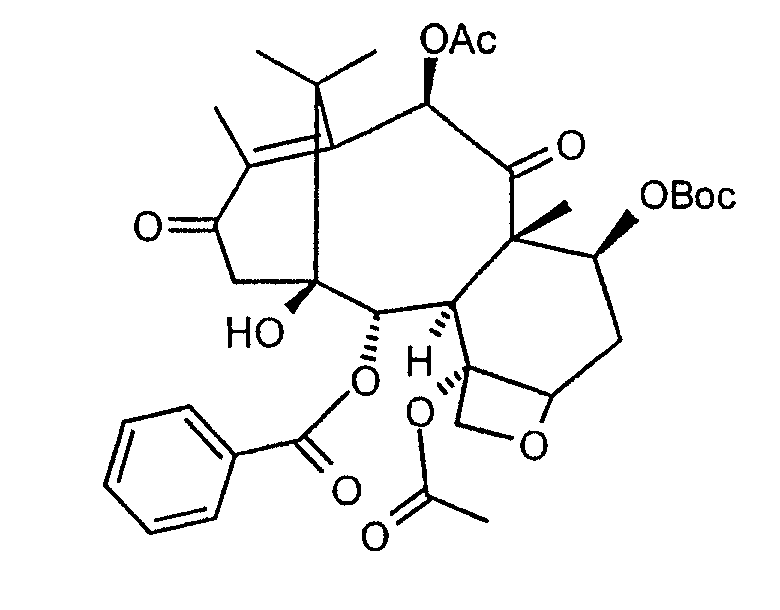
подходящими основаниями и окислителями с получением 7-Вос-13-кето-14-гидроксибаккатина III:
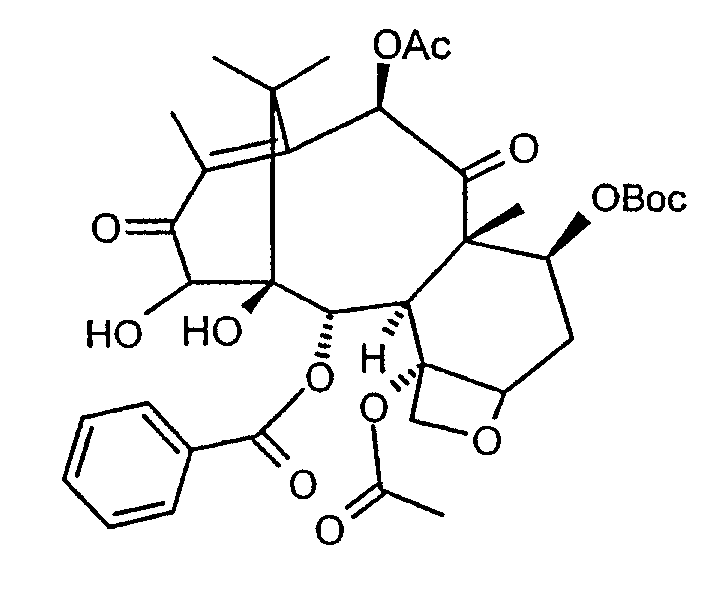
b. карбонизацию 1 и 14 гидроксильных групп с получением 14b-гидрокси-7-Вос-13-кетобаккатин III-1,14-карбоната:

с. восстановление кетона в 13-положении и снятие защитной группы в 7 или наоборот.
Исходный 13-кетобаккатин III обычно защищают в 7 положении подходящей защитной группой, предпочтительно трет-бутоксикарбонильной (Вос). Стадию а) осуществляют путем обработки подходящим основанием, в частности третбутилатом калия (t-BuOK) или бис(триметилсилил)амидом калия (KHMDS). Данные реакции можно проводить в интервале температуры от -40 до -78°С. Подходящми растворителями для этой реакции явлются простые эфиры, такие как тетрагидрофуран или диэтиловый эфир, в частности, в виде смеси с гексаметилфосфорамидом (HMPA) или 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)пиримидиноном (DMPU). После этого енолят обрабатывают окислителем, таким как производные оксазиридина (в частности, N-бензолсульфонилфенилоксазиридином, N-бензолсульфонил-м-нитрофенилоксазиридином и камфорсульфонилоксазиридином), получая 7-защищенное производное 13-кето-14-гидроксибаккатина III.
Затем осуществляют стадию b) путем обработки карбонилирующим агентом (например, карбонилдиимидазолом или фосгеном) в условиях, обычно описанных в литературе, получая производное 1,14-карбоната. Обычно данную реакцию можно осуществить в инертных растворителях, предпочтительно простых эфирах, или хлорсодержащих растворителях в присутствии основания (предпочтительно пиридина, или триэтиламина) в интервале температур от -40°С до комнатной температуры. Реакцию можно проводить как с чистым исходным веществом, так и с сырым продуктом предшествующей стадии.
Восстановление карбонила в 13-положении на стадии с) легко проводится при действии боргидрида тетрабутиламмония в этаноле при температуре, обычно находящейся в интервале от -20 до -50°С, и завершается в течение 2-6 часов. Реакцию можно также проводить в метаноле, изопропаноле или в смеси метанола и тетрагидрофурана. Восстанавливающий агент можно использовать в стехиометрическом количестве, хотя предпочтительно используют избыток гидрида. Кроме того, восстановление можно проводить при помощи других гидридов, предпочтительно боргидрида лития, боргидрида натрия, триацетоксиборгидрида натрия, в условиях, известных в данной области техники.
Защиту из 7-положения снимают в условиях, зависящих от используемой защитной группы. Например, если защитная группа в 7-положении представляет собой трет-бутоксикарбонил, можно успешно использовать гидролиз муравьиной кислотой.
Исходный 13-кетобаккатин III можно легко получить по одной из двух следующих методик.
10-Деацетилбаккатин III селективно окисляют по 13-положению озоном, получая 13-кето-10-деацетилбаккатин III. Окисление можно проводить в спиртовых или хлорсодержащих растворителях, в частности в метаноле или хлористом метилене, при температуре, изменяющейся в интервале от -78°С до комнатной температуры. После этого 13-кето-10-деацетилбаккатин III региоселективно ацетилируют, получая 13-кетобаккатин III.
Альтернативно 13-кетобаккатин III можно получить окислением баккатина III, либо природного, либо полученного региоселективным ацетилированием 10-деацетилбаккатина III. Окисление можно проводить либо озоном или также диоксидом марганца в апротонных растворителях, таких как хлористый метилен, при температуре, изменяющейся в интервале от 0 до 60°С, более предпочтительно при комнатной температуре.
Процессы данного изобретения суммированы на следующей схеме:

Следующие примеры дополнительно иллюстрируют изобретение.
Использованы следующие аббревиатуры:
AcOEt = этилацетат, TES = триэтилсилил, TESCl = триэтилсилихлорид, DCM = хлористый метилен (дихлорметан), ТГФ = тетрагидрофуран, HMPA = гексаметилфосфорамид, DMPU = 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)пиримидинон.
ПРИМЕР 1
10-Деацетил-13-кетобаккатин III
10-Деацетилбаккатин III (3 г, 5 ммоль) растворяли в смеси DCM-MeOH 1:1 (250 мл) и охлаждали до -78°С. Через раствор барботировали ток озона (1,4 г/мл) до исчезновения исходного вещества (2 ч). Ток озона заменяли на азот. После этого раствор обрабатывали диметилсульфидом (1 мл) и пиридином (1 мл), растворитель выпаривали, а сырой остаток растворяли в EtOAc (100 мл) и промывали 0,1 н. HCl и льдом. После выпаривания растворителя продукт получали с выходом 90%.
ПРИМЕР 2
13-Кетобаккатин III
Баккатин III (150 г, 0,25 моль) растворяли в ацетоне (1,43 л). При интенсивном перемешивании в виде трех порций прибавляли коммерчески доступный диоксид марганца (450 г). После исчезновения исходного вещества (4 ч) суспензию фильтровали и выпаривали растворитель. Сырой остаток суспендировали в EtOAc (100 мл) и кипятили 1 ч, затем добавляли ц-гексан (100 мл). Указанное в заголовке соединение получали в виде белого твердого вещества из маточных растворов после выпаривания растворителя (140 г, 95%).
ПРИМЕР 3
7-Boc-13-кетобаккатин III
Раствор 13-кетобаккатина III (1,1 г, 1,9 ммоль) в хлористом метилене (0,5 мл) растворяли в четыреххлористом углероде (14 мл) при комнатной температуре. После этого при интенсивном перемешивании прибавляли 1-метилимидазол (35 мл, 0,282 ммоль) и Boc2O (1,026 г, 4,7 ммоль). Раствор оставляли при перемешивании при 20°С на 18 часов. После этого растворитель заменяли на ацетон (5 мл), раствор выливали в воду (5 мл) и оставляли при перемешивании на ночь. Выпавший осадок собирали на воронке Бюхнера, промывали н-пентаном и сушили, получая 1,1 г указанного в заголовке продукта (1,78 ммоль, 94%).
ПРИМЕР 4
14-Гидрокси-7-Boc-13-кетобаккатин III
Раствор 7-Boc-13-кетобаккатина III (0,65 г, 0,95 ммоль) в смеси ТГФ-DMPU 8:2 (10 мл) прибавляли к раствору t-BuOK (0,425 г, 3,79 ммоль) в безводном ТГФ (10 мл) при перемешивании при -60°С. Через 15 минут прибавляли раствор камфорсульфонилоксазиридина (2,63 ммоль) в смеси ТГФ-DMPU 8:2 (10 мл). После исчезновения исходного вещества (45 мин) реакционную смесь гасили ледяной уксусной кислотой (0,4 мл) и разбавляли смесь 10%-ным водным NH4Cl (25 мл). Органический слой промывали водой, сушили над сульфатом натрия и упаривали при пониженном давлении. Продукт использовали на следующей стадии без очистки.
ПРИМЕР 5
1,14-Карбонат 14b-гидрокси-7-Boc-13-кетобаккатина III
14-Гидрокси-7-Boc-13-кетобаккатин III (2,0 г) и карбонилдиимидазол (0,65 г, 4,0 ммоль) растворяли в толуоле (11 мл) и нагревали при 75°С при перемешивании в течение 90 мин. Раствор охлаждали до комнатной температуры и обрабатывали 0,2 н. HCl (5 мл). Органический слой разбавляли EtOAc (15 мл), промывали водой, сушили и выпаривали растворитель. Указанное в заголовке соединение получали флэш-хроматографией (силикагель, ц-гексан/DCM/Et2O, 14:3,5:2,5) в виде белого твердого вещества (0,87 г, 1,20 ммоль, 82% после двух стадий).
ПРИМЕР 6
1,14-Карбонат 14b-гидрокси-7-Boc-баккатина III
Раствор 1,14-карбоната 14b-гидрокси-7-Boc-13-кетобаккатина III в ТГФ (3 мл) прибавляли к раствору боргидрида тетрабутиламмония (1,29 г) в сухом метаноле (11 мл) при -50°С в инертной атмосфере. Через 4 часа реакционную смесь гасили раствором лимонной кислоты (1,5 г) в воде (5 мл). Смесь экстрагировали этилацетатом. Органическую фазу сушили над сульфатом магния и упаривали при пониженном давлении. Сырой остаток очищали колоночной хроматографией, получая 1,14-карбонат 14b-гидрокси-7-Boc-баккатина III (68%) и 1,14-карбонат 13-эпи-14b-гидрокси-7-Boc-баккатина III (28%) с выходом конверсии 70%.
ПРИМЕР 7
1,14-Карбонат 14b-гидроксибаккатина III
К раствору 1,14-карбоната 14b-гидрокси-7-Boc-баккатина III (0,50 г, 0,68 моль) в хлористом метилене (3 мл) прибавляли раствор 97%-ной муравьиной кислоты (5 мл) при -8°С. Реакционную смесь выдерживали при перемешивании в течение 5 дней, затем нейтрализовали 2 н. раствором аммиака. Органическую фазу экстрагировали этилацетатом, сушили и выпаривали при пониженном давлении. В результате хроматографии на силикагеле (гексан-этилацетат = 1,0:1,3) получали продукт в виде белого твердого вещества с выходом 65%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 14БЕТА-ГИДРОКСИБАККАТИН III-1,14-КАРБОНАТА | 2002 |
|
RU2291866C2 |
| ПРОИЗВОДНЫЕ ТАКСАНА, ФУНКЦИОНАЛИЗИРОВАННЫЕ ПО 14-ПОЛОЖЕНИЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2320652C2 |
| ПРОИЗВОДНЫЕ ТАКСАНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2245882C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТАКСАНА | 2001 |
|
RU2275365C2 |
| ПРОИЗВОДНЫЕ ТАКСАНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2168513C2 |
| С-2'-МЕТИЛИРОВАННЫЕ ПРОИЗВОДНЫЕ ПАКЛИТАКСЕЛА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВЫХ АГЕНТОВ | 2002 |
|
RU2287528C2 |
| ПОЛУСИНТЕТИЧЕСКИЕ ТАКСАНЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2001 |
|
RU2259363C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ТАКСАНА | 2007 |
|
RU2434014C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БАККАТИНА III | 2001 |
|
RU2264394C2 |
| ПРОИЗВОДНЫЕ 10-ДЕАЦЕТИЛБАККАТИНА III И 10-ДЕАЦЕТИЛ-14β-ГИДРОКСИБАККАТИНА III, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2152936C1 |
Изобретение относится к новому способу получения 14β-гидроксибаккатина III-1,14-карбоната, который включает: а. обработку 7-Вос-13-кетобаккатина III формулы
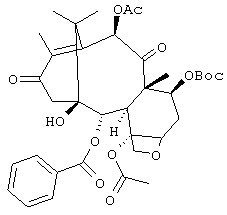
подходящими основаниями и окислителями с получением 7-Вос-13-кето-14-гидроксибаккатина III:

b. карбонизацию 1 и 14 гидроксигрупп с получением 14b-гидрокси-7-Вос-13-кетобаккатин III-1,14-карбоната:
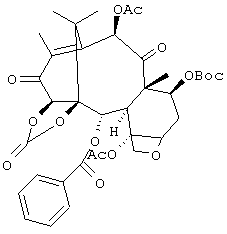
с. восстановление кетона в 13-положении и снятие защитной группы в 7. Изобретение также относится к новым промежуточным соединениям этого способа. Технический результат - упрощение процесса за счет использования в качестве исходного 13-кетобаккатина III. 4 н. и 7 з.п. ф-лы.
а. обработку 7-Вос-13-кетобаккатина III формулы
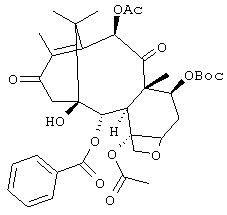
подходящими основаниями и окислителями с получением 7-Вос-13-кето-14-гидроксибаккатина III:

b. карбонизацию 1 и 14 гидроксигрупп с получением 14b-гидрокси-7-Вос-13-кетобаккатин III-1,14-карбоната:

с. восстановление кетона в 13-положении и снятие защитной группы в 7.

в качестве нового промежуточного соединения.
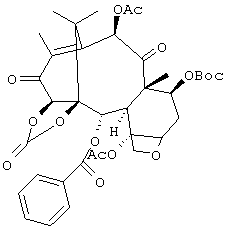
в качестве нового промежуточного соединения.
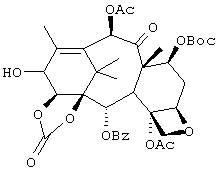
в качестве нового промежуточного соединения.
| WO 9636622 A1, 21.11.1996 | |||
| US 5705508 A, 06.01.1998 | |||
| СПОСОБ ПОЛУЧЕНИЯ 7-ТРИАЛКИЛСИЛИЛ-БАККАТИНА III | 1995 |
|
RU2127729C1 |
| RU 96120192 A, 20.11.1999. | |||
Авторы
Даты
2006-10-10—Публикация
2002-07-18—Подача