Изобретение относится к области органической химии, а конкретно способу получения 3,6-диазагомоадамантана, который имеет следующую структуру:
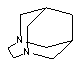
Соединения класса 3,6-диазагомоадамантана обладают противовирусным действием, сравнимым с противовирусным действием аминоадамантана, проявляют стрихниноподобную активность, а также обладают бактерицидными, фунгицидными и альгицидными свойствами.
Известен способ получения 1-алкил- и 1-арил-3,6-диазагомоадамантана восстановлением соответствующих гидразонов при температуре 220-240°С в присутствии щелочи по реакции Кижнера-Вольфа [Кузнецов А.И., Владимирова И.А., Серова Т.М., Московкин А.С. Гетероадамантаны и их производные. 17. Восстановление 3,6-диазагомоадамантанонов по Кижнеру-Вольфу. // ХГС. - 1992. - №5 - С.653-657.]. Однако в условиях данной реакции гидразон 3,6-диазагомоадамантана без заместителей в узловых положениях превращается в азин. Наличие объемных заместителей в молекуле диазагомоадамантана уменьшает биологическую активность вещества.
Технической задачей предлагаемого изобретения является разработка доступного метода синтеза 3,6-диазагомоадамантана без заместителей в узловых положениях.
Технический результат предлагаемого достижения заключается в том, что 1-фенилтио-3,6-диазагомоадамантан-9-он, который получают по известной методике [Кузнецов А.И., Владимирова И.А., Басаргин Е.Б. и др. Гетероадамантаны и их
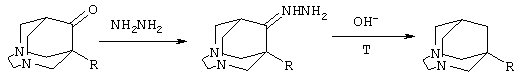
R=Me, Et, Pr, Ph
производные. II. Синтез 3,6-диазагомоадамантан-9-она и его производных с заместителями в узловых положениях. // ХГС. - 1990. - №5. - С.675-680.] при нагревании фенилтиоацетона с тетраметилендиэтилентетрамином при кипении в изопропиловом спирте в присутствии уксусной кислоты в качестве катализатора, превращают в гидразон 1-фенилтио-3,6-диазагомоадамантан-9-она при кипении в 65-66%-ом гидразингидрате, который затем подвергают восстановлению в 1-фенилтио-3,6-диазагомоадамантан по реакции Кижнера-Вольфа сплавлением со щелочью, и полученный 1-фенилтио-3,6-диазагомоадамантан десульфурируют никелем Ренея при кипении в изопропиловом спирте. Выход 3,6-диазагомоадамантана составил 76%. Синтез осуществляется по следующей схеме:
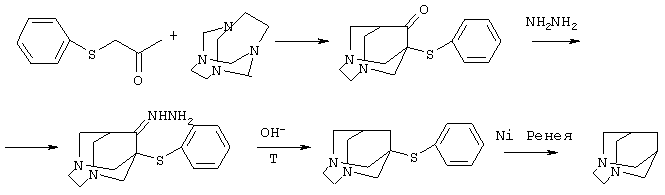
Пример 1
1-фенилтио-3,6-диазагомоадамантан-9-он
Раствор 3.66 г (21.78 ммоль) тетраметилендиэтилентетрамин и 3.27 мл (54.45 ммоль) уксусной кислоты в 30 мл изопропилового спирта нагревали до 60°С. Затем прибавляли 3.61 г (21.78 ммоль) фенилтиоацетона и перемешивали при комнатной температуре в течение 1 ч. Растворитель упаривали в вакууме. Реакционную массу обрабатывали горячим гептаном (3×100 мл), экстрагент упаривали в вакууме. После перекристаллизации из гептана получали 2 г 1-фенилтио-3,6-диазагомоадамантан-9-она. Выход 35%. Тпл 133-134°С. ИК спектр, ν, см-1: 1695 (СО), 1600 (аром). 1Н-ЯМР Спектр, δ, м.д.: 3.02 м (4Н, NCH2CH2N); 3.55-3.25 м (8Н, NCH2C, 2J=14.0 Гц); 0.80 уш.с (1Н, СН); 7.45 д, 7.12 д (С6Н5). Масс-спектр, m/z (Iотн., %): 274[M+]
Гидразон 1-фенилтио-3,6-диазагомоадамантан-9-она
Нагревали при кипении 3 ч раствор 2.37 г (8.64 ммоль) 1-тиофенил-3,6-диазагомоадамантан-9-она в 40 мл 66%-ного водного раствора гидразингидрата. Охлаждали до 0°С, выпавший осадок отфильтровывали. После перекристаллизации из изопропилового спирта получали 2 г гидразона 1-тиофенил-3,6-диазагомоадамантан-9-она. Выход 80%. Тпл 189-190°С. ИК спектр, ν, см -1: 3300, 1560 (NH), 1680 (C=N), 1600 (аром). 1Н-ЯМР Спектр, δ, м.д.: 2.98 м (4Н, NCH2CH2N); 3.52-2.75 м (8Н, NCH2C, 2J=14.0 Гц); 5.20 уш.с (NH2); 1.90 уш.с.(1Н, СН) 7.55 д, 7.35 д (С6Н5). Масс-спектр, m/z (Iотн., %): 288[M+]
1-фенилтио-3,6-диазагомоадамантан 13
Сплавляли 2 ч при 220-240°С тщательно перемешанную смесь 1.90 г (6.59 ммоль) гидразона 1-фенилтио-3,6-диазагомоадамантан-9-она и 1.75 г порошкообразного гидроксида калия. Остывший сплав экстрагировали диэтиловым эфиром (2×25 мл), растворитель отгоняли в вакууме. После перекристаллизации из гептана получали 1.30 г 1-фенилтио-3,6-диазагомоадамантана. Выход 76%. Тпл 87-89°С. ИК спектр, ν, см-1: 1600 (аром). 1Н-ЯМР Спектр, δ, м.д.: 3.00 м (4Н, NCH2CH2N); 3.35-2.60 м (8Н, NCH2C, 2J=14.0 Гц); 1.85 уш. с (1Н, СН); 1.25 с (2 Н, СН2). Масс-спектр, m/z (Iотн., %): 260[M+]
3,6-Диазагомоадамантан
К раствору 0.40 г (2.33 ммоль) 1-фенилтио-3,6-диазагомоадамантана в 20 мл изопропилового спирта добавляли 2 г свежеприготовленного никеля Ренея и смесь кипятили 20 ч, дополнительно прибавляя каждые 7 ч по 2 г никеля Ренея. Катализатор отфильтровывали, промывали изопропиловым спиртом, фильтрат упаривали в вакууме. После перекристаллизации из гептана получали 0.18 г 3,6-диазагомоадамантана. Выход 76% (в расчете на 1-фенилтио-3,6-диазагомоадамантан). Тпл 250-251°С.
1Н-ЯМР Спектр, δ. м.д.: 3.12 м (4Н, NCH2CH2N); 3.42 д, 2.80 д (8Н, CCH2N 2J=14.0 Гц); 1.85 уш.с (1Н, СН), 1.30 с (2Н, СН2). 13С-ЯМР спектр, δ, м.д.: 29.79 (С-1,8), 34.07 (С-8), 57.27 (С-5, 4), 62.37 (С-2, 7, 10, 11). Масс-спектр, m/z (Iотн., %): 152 [M+](97), 108 (97), 95 (66), 85 (30), 72 (17), 60 (45), 55 (57), 57 (100), 42 (65). Элементный анализ: вычислено, % С 71.05, Н 10.52, N 18.52, найдено, % С 71.09, Н 10.50, N 18.50.
Индивидуальность соединений подтверждена совокупностью масс-спектрометрии, ИК-, 1Н-ЯМР-13С-ЯМР-спектроскопии, а также элементным анализом.
Таким образом, данный способ позволяет получить 3,6-диазагомоадамантан без заместителей в узловых положениях, который может найти применение в качестве противовирусного препарата.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 9-ФЕНИЛ-3,6-ДИАЗАТРИЦИКЛО[4.3.1.1]УНДЕКАНА | 2007 |
|
RU2333911C1 |
| ДУШИСТЫЕ 3,6-ДИАЗАГОМОАДАМАНТАН-9-ОНЫ | 2014 |
|
RU2559051C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,8-ДИМЕТИЛ-3,6-ДИАЗАДИГОМОАДАМАНТАН-9,10-ДИОНА | 2005 |
|
RU2282630C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,9-ДИФЕНИЛ-3,7-ДИАЗАТРИЦИКЛО[5.3.1.1]ДОДЕКАН-10-ОНА | 2015 |
|
RU2593144C1 |
| N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНЫ И СПОСОБ ПОЛУЧЕНИЯ N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ ПО ОТНОШЕНИЮ К ГРИБАМ Bipolaris sorokiniana и Rhizoctonia solani | 2019 |
|
RU2727138C1 |
| СПОСОБ ПОЛУЧЕНИЯ 8-НИТРО-1,3,6-ТРИАЗАГОМОАДАМАНТАНА | 2006 |
|
RU2316558C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-ДИ(АЛКАДИИНИЛ)АМИНОВ | 2015 |
|
RU2626008C2 |
| Способ получения замещенных (4R*,5S*,6R*)-2-тиогексагидропиримидин-5-карбогидразидов | 2021 |
|
RU2776954C1 |
| Способ получения замещенных 8-гидрокси-1,2,3,4,4a,10b-гексагидро-2H-хромено[4,3-d]пиримидин-2,5(1H)-дионов | 2022 |
|
RU2785713C1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДРАЗОНОВ 4-R-1,2,5-ОКСАДИАЗОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2014 |
|
RU2557659C1 |
Изобретение относится к новому способу получения нового соединения - 3,6-диазагомоадамантана формулы:
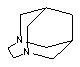
Соединения класса 3,6-диазагомоадамантана обладают противовирусным действием, сравнимым с противовирусным действием аминоадамантана, проявляют стрихниноподобную активность, а также обладают бактерицидными, фунгицидными и альгицидными свойствами и могут найти применение в качестве противовирусного препарата. Способ получения 3,6-диазагомоадамантана заключается во взаимодействии 1-фенилтио-3,6-диазагомоадамантан-9-она с 65-66% гидразингидратом при кипении с образованием гидразона 1-фенилтио-3,6-диазагомоадамантан-9-она. Полученный продукт подвергается восстановлению по реакции Кижнера-Вольфа сплавлением со щелочью, а затем 1-фенилтио-3,6-диазагомоадамантан десульфурируется никелем Ренея при кипении в изопропиловом спирте.
Способ получения 3,6-диазагомоадамантана, заключающийся во взаимодействии 1-фенилтио-3,6-диазагомоадамантан-9-она с 65-66% гидразингидратом при кипении с образованием гидразона 1-фенилтио-3,6-диазагомоадамантан-9-она, который подвергают восстановлению по реакции Кижнера-Вольфа сплавлением со щелочью, а полученный 1-фенилтио-3,6-диазагомоадамантан десульфурируют никелем Ренея при кипении в изопропиловом спирте.
| Кузнецов А.И | |||
| и др | |||
| Гетероадамантаны и их производные | |||
| Химия гетероциклических соединений | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Кузнецов А.И | |||
| и др | |||
| Гетероадамантаны и их производные | |||
| Химия гетероциклических соединений | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| ДИАЗАГОМОАДАМАНТАНЫ В КАЧЕСТВЕ АНТИВУАЛИРУЮЩИХ ВЕЩЕСТВ В ПРОЦЕССЕ ПРОЯВЛЕНИЯ ЧЕРНО-БЕЛЫХ ФОТОГРАФИЧЕСКИХ МАТЕРИАЛОВ | 1988 |
|
SU1536768A1 |
| Sasaki Tadashi et al | |||
| Heterocage compounds | |||
| Journal of Organic Chemistry | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
Авторы
Даты
2006-10-10—Публикация
2005-06-22—Подача