Настоящее изобретение относится к гидроксиамидам (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановых кислот или к их фармацевтически приемлемым солям. Установлено, что эти соединения обладают антипролиферативной активностью, такой как противоопухолевая активность, и, следовательно, могут применяться при лечении человека или животных. Кроме того, изобретение относится к способам получения указанных гидроксиамидов (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановых кислот, к фармацевтическим композициям, содержащим эти соединения, и к их применению для изготовления лекарственных средств, предназначенных для стимуляции антипролиферативного действия у теплокровного животного, такого как человек.
Уровень техники
Регуляция транскрипции является основным событием в клеточной дифференциации, пролиферации или апоптозе. Транскрипционная активация ряда генов определяет дальнейшую судьбу клетки и поэтому сама транскрипция строго регулируется множеством факторов. Один из ее регуляторных механизмов включает способ изменения третичной структуры ДНК, что оказывает влияние на транскрипцию за счет изменения доступности тех сегментов ДНК, которые являются мишенями для факторов транскрипции. Степень интеграции нуклеосом регулируется степенью ацетилирования гистонов кора. При пониженном уровне ацетилирования нуклесомы упакованы достаточно плотно и, следовательно, процесс транскрипции невозможен. С другой стороны, при ацетилировании гистонов кора нуклеосомы релаксируют, что позволяет развиваться процессу транскрипции. Степень ацетилирования гистонов зависит от баланса активности гистонацетилтрансферазы (ГАТ) и гистондеацетилазы (ГДАЦ). В последнее время установлено, что ингибиторы ГДАЦ останавливают рост и вызывают апоптоз некоторых типов опухолевых клеток, включая клетки толстой кишки, Т-клеточной лимфомы и эритролейкемических клеток. Если предположить, что решающим фактором (остановки) опухолевой прогрессии является апоптоз, то ингибиторы ГДАЦ являются перспективными реагентами для терапии опухолей в качестве эффективных индукторов апоптоза.
Из уровня техники известно несколько структурных классов ингибиторов ГДАЦ (см. обзор Marks P.M. и др., J. Natl. Cancer. Inst. 15, 1210-1216 (2000). Соединения гидроксамовой кислоты, обладающие ингибирующей активностью в отношении ГДАЦ, описаны в WO 98/55449 и US 5369108.
В последнее время установлено, что гидроксиамиды (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановых кислот обладают антипролиферативными свойствами благодаря наличию у них ингибирующей активности в отношении ГДАЦ. Ингибирующая активность в отношении ГДАЦ некоторых гидроксамидов (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановых кислот, описанных в настоящей заявке, превосходит активность САГК (субероиланилидгидроксамой кислоты, которая обладает ингибирующей активностью в отношении ГДАЦ, см. US 5369108).
Описание изобретения
Настоящее изобретение относится к новым соединениям общей формулы (I) и их применению в качестве противоопухолевых агентов
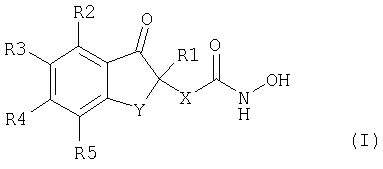
где
R1 выбирают из ряда: водород, С1-С4алкил, СООН, СОО(С1-С4)алкил,
R2, R3, R4, R5 независимо выбирают из ряда: водород, галоген, С1-С4алкил, гидрокси, С1-С4алкокси,
Y означает -СН2-СН2-,
Х означает алкиленовую цепь, содержащую от 4 до 10 атомов углерода, которая является насыщенной или ненасыщенной, может содержать одну двойную связь и которая может быть разветвленной или неразветвленной цепью.
Кроме того, в объем настоящего изобретения включены энантиомеры соединений формулы (I), их диастереизомеры, рацематы и их смеси, а также соли соединений формулы (I) с фармацевтически приемлемыми кислотами или основаниями.
Кроме того, предполагается, что некоторые производные формулы (I) могут существовать в сольватированных и несольватированных формах, таких, например, как гидратированные формы. Предполагается, что изобретение включает все такие сольватированные формы, которые обладают противоопухолевой активностью.
Предпочтительными соединениями формулы (I) являются такие соединения, в которых R2 и R5 означают водород. Преимущественно предпочтительными соединениями формулы (I) являются такие соединения, в которых три из четырех радикалов R2, R3, R4 и R5 означают водород.
Приемлемыми заместителями галоген являются, например, фтор, хлор, бром и иод; приемлемыми заместителями С1-С4алкил являются, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил; приемлемыми заместителями С1-С4алкокси являются, например, метокси, этокси, пропокси, изопропокси или бутокси.
Описывается также широкий круг соединений, в котором R2, R3, R4 и R5 независимо выбирает из ряда водород, галоген, С1-С4алкил-, трифторметил-, гидрокси-, С1-С4алкокси-, арилокси-, арилалкилокси-, нитро-, амино-, C1-С4алкиламино-, ди[С1-С4алкил]амино-, пиперидино, морфолино, пирролидино, С1-С4алканоиламино- или арил, или гетероарил, или R2 и R3 вместе или R3 и R4 вместе или R4 и R5 вместе, соответственно, образуют цикл C1-С3алкилендиокси, или R2 и R3 вместе или R3 и R4 вместе или R4 и R5 вместе, соответственно, образуют С3-С5алкиленовую цепь. Y означает -СН2-СН2-. Х означает алкиленовую цепь, содержащую от 4 до 10 атомов углерода, которая является насыщенной или ненасыщенной, может содержать одну или две двойные связи или одну или две тройные связи, или одну двойную и одну тройную связь, может быть разветвленной или неразветвленной или прерванной циклом С3-С7циклоалкил. При этом приемлемыми заместителями С1-С4алкиламино являются, например, метиламино, этиламино или изопропиламино; приемлемыми заместителями ди[С1-С4алкил]амино являются, например, диметиламино, N-этил-N-метиламино, диэтиламино, N-метил-N-пропиламино или дипропиламино; приемлемыми заместителями С1-С4алканоиламино являются, например, формиламидо, ацетамидо, пропионамидо или бутирамидо; приемлемыми заместителями C1-С3алкилендиокси являются, например, метилендиокси, этилендиокси или пропилендиокси.
Арильная группа означает карбоциклическую конденсированную кольцевую систему, например фенил, нафтил, предпочтительно фенил, который является незамещенным или замещенным 1, 2 или 3 заместителями, независимо выбранными из ряда галоген, С1-С4алкил-, трифторметил-, гидрокси-, C1-С4алкокси-, арилалкилокси, арилокси-, C1-С3алкилендиокси-, нитро-, амино-, С1-С4алкиламино-, ди[С1-С4алкил]амино- и С1-С4алканоиламино-, имеющими значения, указанные выше.
Гетероарильная группа означает 5- или 6-членную циклическую систему с сопряженными двойными связями, содержащую один или два гетероатома, незвисимо выбранных из ряда азот, кислород и сера, например, пиридинил, тиофенил, фурил или пирролил, или аннелярную бициклическую кольцевую систему с сопряженными двойными связями, такую как индолил-, хинолил- или изохинолил-, которая может быть незамещенной или замещенной 1, 2 или 3 заместителями, независимо выбранными из ряда галоген, С1-С4алкил-, трифторметил-, гидрокси-, С1-С4алкокси-, арилалкилокси-, арилокси-, С1-С3алкилендиокси-, нитро-, амино-, С1-С4алкиламино-, ди[С1-С4алкил]амино и С1-С4алканоиламино-, имеющими значения, указанные выше.
Предпочтительными значениями радикала арилалкилокси является бензилокси.
Предпочтительным С3-С7циклоалкильным кольцом является циклопропил или циклобутил, причем цикл присоединен к цепи 1,1'-связью.
Предпочтительными значениями цепи Х являются -(СН2)n- и -СН=СН-(CH2)n-2-, где n означает целое число от 3 до 7, наиболее предпочтительно от 4 до 6. Другими предпочтительными значениями являются -(СН2)n-1-СН(СН3)-, -(СН2)n-1-С(СН3)2- или -(СН2)n-1-С(-СН2-СН2-)-, где n означает целое число от 3 до 7, наиболее предпочтительно от 4 до 6.
В качестве другого объекта изобретения предлагается фармацевтическая композиция, которая включает фармацевтически эффективное количество одного или более соединений формулы I или его фармацевтически приемлемой соли в смеси с фармацевтически приемлемым разбавителем, эксципиентом или носителем. Композицию можно приготовить в форме для перорального введения, например в форме таблетки или капсулы, для парентеральной инъекции (включая внутривенное, подкожное, внутримышечное, внутрисосудистое введение или вливание) в форме стерильного раствора, суспензии или эмульсии, для местного введения в форме мази или крема, или для ректального введения в виде суппозитория. В общем случае указанные композиции можно приготовить в смеси с обычными эксципиентами.
Указанные композиции можно вводить пероральным способом, например, в форме таблеток, таблеток в оболочке, твердых или мягких желатиновых капсул, растворов, эмульсий или суспензий. Кроме того, они могут вводиться ректальным способом, например, в форме суппозиториев или парентерально, например, в форме инъекционных растворов.
Фармацевтические композиции по настоящему изобретению, включающие соединения формулы I, их диастереомеры, рацематы и смеси или их соли, изготовляют известным способом, например, с использованием обычных процессов смешивания, капсулирования, растворения, гранулирования, эмульгирования, включения, покрытия таблеток оболочкой или лиофилизации. Эти фармацевтические препараты можно смешать с терапевтически инертными неорганическими или органическими носителями. При получении таблеток, таблеток в оболочке, драже или твердых желатиновых капсул в качестве таких носителей используются лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли. Пригодными носителями для мягких желатиновых капсул являются растительные масла, воски, жиры, полутвердые или жидкие полиолы. В зависимости от природы активного соединения в случае мягких желатиновых капсул обычно не требуется никаких носителей. Пригодными носителями для приготовления растворов и сиропов являются вода, полиолы, сахароза, инвертированный сахар и глюкоза. Пригодными носителями для инъекции являются вода, спирты, полиолы, глицерин, растительные масла, фосфолипиды и ПАВ. Пригодными носителями для суппозиториев являются природные или отвержденные масла, воски, жиры и полужидкие полиолы. Фармацевтические препараты могут также включать консерванты, солюбилизирующие агенты, стабилизирующие агенты, смачивающие агенты, эмульгирующие агенты, подсластители, красители, ароматизаторы, соли для регуляции осмотического давления, буферные вещества, обволакивающие агенты или антиоксиданты. Кроме того, они могут содержать другие терапевтически ценные соединения, включая дополнительные активные ингредиенты, иные, чем соединения формулы I.
Гидроксиамиды (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановых кислот обычно вводят теплокровному животному в виде стандартной дозы, которая содержит от 5 до 5000 мг на квадратным метр площади тела животного, т.е. приблизительно 0,1-100 мг/кг, что обычно составляет терапевтически эффективную дозу. Стандартная доза в форме таблетки или капсулы обычно содержит, например, 1-250 мг активного ингредиента. Предпочтительная суточная доза составляет от 1 до 100 мг/кг. Однако суточная доза может изменяться в зависимости от пациента, способа введения и тяжести заболевания. Оптимальную дозу определяет практикующий врач, который лечит конкретного пациента.
Производное гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты формулы I может быть использовано для лечения человека или животного. В настоящее время установлено, что соединения по настоящему изобретению обладают антипролиферативными свойствами благодаря наличию ингибирующей активности в отношении гистондеацетилазы. Следовательно, соединения по настоящему изобретению можно использовать в способе подавления пролиферации злокачественных клеток. Потому предполагается, что соединения по настоящему изобретению можно использовать при лечении опухолевых заболеваний благодаря наличию антипролиферативного действия, прежде всего при лечении рака молочных желез, легких, толстой кишки, прямой кишки, желудка, предстательной железы, мочевого пузыря, поджелудочной железы и яичника. Кроме того, предполагается, что соединение по настоящему изобретению может обладать активностью в отношении ряда лейкозов, злокачественных образований лимфоидных тканей и солидных опухолей, таких как карциномы и саркомы тканей, таких как печень, почки, предстательная железа и поджелудочная железа. Соответственно возможно применение производного гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты формулы I или его фармацевтически приемлемой соли, имеющего значения, указанные выше, при изготовлении лекарственного средства для применения с целью стимуляции антипролиферативного действия в организме теплокровного животного, такого как человек.
В изобретении предлагается способ стимуляции антипролиферативного действия в организме теплокровного животного, такого как человек, нуждающегося в таком лечении, причем указанный способ включает введение указанному животному эффективного количества производного гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты, имеющего значения, указанные выше.
Вышеуказанное антипролиферативное лечение можно проводить с использованием одного препарата на основе производного гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты по настоящему изобретению или в сочетании с одним или более другими противоопухолевыми веществами, например, выбранными из группы, включающей ингибиторы митоза, например винбластин; алкилирующие агенты, например цис-платин, карбоплатин и циклофосфамид; ингибиторы сборки микротрубочек, например паклитаксел или другие таксаны; антиметаболиты, например 5-фторурацил, капецитабин, арабинозид цитозина и гидроксимочевина, или, например, интеркалирущие антибиотики, например адриамицин и блеомицин; иммуномодуляторы, например трастузумаб; ингибитор синтеза ДНК, например гемцитабин; ферменты, например аспарагиназа; ингибиторы топоизомеразы, например этопозид; модуляторы биологического ответа, например интерферон; антигормоны, например антиэстрогены, такие как тамоксифен, или, например, антиандрогены, такие как (4'-циано-3-(4-фторфенилсульфонил)-2-гидрокси-2-метил-3'-трифторметил)пропионанилид, или другие терапевтические агенты или препараты, описанные, например, в сборнике Cancer: Principles and Practice of Oncology, Vincent T. De Vita, Jr., Samuel Hellmann, Steven A. Rosenberg, 5th ed., Lippincott-Raven Publishers (1997). Такую сочетанную терапию можно проводить при одновременном, последовательном или раздельном введении индивидуальных компонентов. Следовательно, согласно изобретению предлагается фармацевтический препарат, включающий производное гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты формулы I, имеющее значения, указанные выше, и дополнительное вышеуказанное противоопухолевое вещество, для сочетанной терапии опухолевых заболеваний.
Примерами физиологически приемлемых солей соединений формулы I являются соли физиологически приемлемых оснований. Обычно это соли щелочных, щелочно-земельных металлов, соли аммония или алкиламмония, например соли натрия, калия, кальция и тетраметиламмония.
Разделение рацемических соединений на энантиомеры осуществляют методом хроматографии на аналитическом, полупрепаративном или препаративном уровне при использовании оптически активных неподвижных фаз и соответствующих элюентов. Пригодные оптически активные неподвижные фазы включают, без ограничения перечисленным, силикагель (например, ChiraSper™, фирма Merck; Chiralpak™ OT/OP, фирма Baker), сложные эфиры или карбаматы целлюлозы (например, Chiracel™ OB/OY, фирма Baker) или др. (например, Crownpak™, Daicel™ или Chiracel™ OJ-R, фирма Baker). Кроме того, можно использовать другие методы разделения энантиомеров, такие как образование диастереомерных соединений, включающих соединения формулы I и другие оптически активные соединения, например камфорсульфоновую кислоту или бруцин, и последующее разделение этих диастереомерных соедиений с высвобождением оптически активного агента. Энантиомерно обогащенные или чистые соединения формулы I можно также получить из оптически чистых исходных материалов.
Получение соединений по изобретению
Соединения формулы (I) можно получить известными способами, описанными в литературе (например, в общеизвестных руководствах, таких как Houben-Weyl, Methoden der Organischen Chemie, Georg Thieme Verlag, Stuttgart; Organic Reactions, John Wiley&Sons, Inc., New York) и в источниках, цитированных в примерах, а именно в условиях реакции, известных и пригодных для указанных реакций. Кроме того, можно использовать известные варианты, которые подробно не указаны в описании заявки. Соединения формулы (I) можно получить любым известным способом, который применяется для получения близких в химическом отношении соединений. Кроме того, из соединения формулы (I) известными способами можно получить другое соединение формулы (I).
Такие способы, которые используются для получения производного гидроксиамида (1-оксо-1,2,3,4-тетрагидронафталин-2-ил)алкановой кислоты формулы I или его фармацевтически приемлемой соли, также являются объектом изобретения и иллюстрируются следующими типичными примерами, в которых, если не указано иное, X, Y, R1, R2, R3, R4, R5 и n имеют любое из значений, указанных выше. Необходимые исходные материалы можно получить обычными методами органической химии. Получение таких исходных материалов описано в приведенных, без ограничения перечисленным, примерах. В другом варианте необходимые исходные материалы можно получить аналогично тем методикам, которые иллюстрируются примерами и которые известны специалисту в области органического синтеза.
(А) Предпочтительным методом получения соединений формулы I является удаление защитных групп в соединениях формулы II
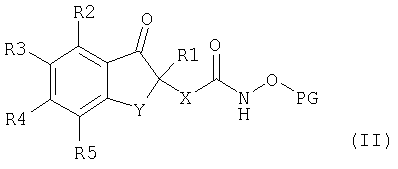
где PG означает соответствующую защитную группу, a R1, R2, R3, R4, R5, Х и Y имеют значения, указанные выше.
Соединения формулы (II) являются новыми и включены в объем настоящего изобретения.
Пригодными защитными группами PG являются, например, бензил-, пара-метоксибензил-, трет-бутилоксикарбонил-, тритил- или силильные группы, такие как триметилсилил- или диметил-трет-бутилсилил-. Условия реакции при удалении защитной группы зависят от типа защитной группы. Если защитная группа означает бензил- или пара-метоксибензил-, реакцию проводят гидрогенолизом в инертном растворителе, таком как спирт, например метанол или этанол, в присутствии катализатора на основе благородного металла, такого как палладий или платина, на соответствующем носителе, таком как уголь, сульфат бария или карбонат бария, при комнатной температуре и атмосферном давлении. Если защитная группа означает трет-бутилоксикарбонил- или тритил-, реакцию проводят в присутствии кислот при температуре от -20°С до 60°С, предпочтительно от 0°С до комнатной температуры. Кислота может представлять собой раствор хлористоводородной кислоты в инертном растворителе, таком как диэтиловый эфир или диоксан, или трифторуксусной кислоты в дихлорметане. Если защитная группа означает силилгруппу, такую как триметилсилил- или диметил-трет-бутилсилил-, реакцию предпочтительно проводят в присутствии соединения фтора, такого как фторид натрия или фторид тетрабутиламмония, в инертном растворителе, таком как дихлорметан.
Соединения формулы (II), в которых R1 означает СООН, можно получить из соединений формулы (II), в которых R1 означает СОО(С1-С4)алкил, гидролизом сложноэфирной группы. Реакцию проводят в условиях, которые зависят от типа С1-С4алкильной группы. Если С1-С4алкил- означает метил- или этил-, реакцию проводят в присутствии основания, например гидроксида лития, гидроксида натрия или гидроксида калия, в инертном растворителе, например в метаноле, этаноле или тетрагидрофуране. Если С1-С4алкил- означает трет-бутил-, реакцию проводят в присутствии кислоты, например в растворе хлористоводородной кислоты, в инертном растворителе, таком как диэтиловый эфир или диоксан, или трифторуксусной кислоты в дихлорметане.
Соединения формулы (II), в которых R1 означает водород, можно получить из соединений формулы (II), в которых R1 означает СООН, термическим декарбоксилированием. Реакцию проводят при нагревании в инертном растворителе в течение от 1 ч до 48 ч, предпочтительно от 5 ч до 9 ч, при температуре от 60°С до 200°С, предпочтительно от 80°С до 120°С.
Соединения формулы (II), в которых R1 означает С1-С4алкил или СОО(С1-С4)алкил, можно получить при взаимодействии соединения формулы (III)
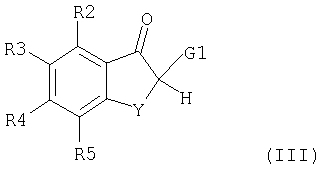
где R2, R3, R4, R5 и Y имеют значения, указанные выше, a G1 означает С1-С4алкил или СОО(С1-С4)алкил, с соединением формулы (IV)
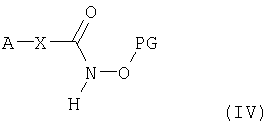
где А означает уходящую группу, PG имеет значения, указанные выше, и Х имеет значения, указанные выше, в отсутствии или в присутствии соответствующего основания.
Пригодной уходящей группой А является, например, галоген или сульфонилоксигруппа, например хлор, бром, метансульфонилокси или пара-толуолсульфонилокси. Пригодным основанием является, например, органический амин, например пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, морфолин, N-метилморфолин или диазабицикло[5.4.0]ундец-7-ен, или, например, карбонат или гидроксид щелочного или щелочно-земельного металла, например карбонат натрия, карбонат калия, карбонат кальция, гидроксид натрия или гидроксид калия.
Обычно реакцию проводят в соответствующем инертном растворителе или разбавителе, например в спирте или сложном эфире, таком как метанол, этанол, изопропанол или этилацетат, в галогенированном растворителе, таком как хлористый метилен, хлороформ или четыреххлористый углерод, в простом эфире, таком как тетрагидрофуран или 1,4-диоксан, в ароматическом растворителе, таком как толуол, или в полярном апротонном растворителе, таком как N,N-диметилформамид, N,N-диметилацетамид, N-этилпирролидин-2-он или диметилсульфоксид. Обычно реакцию проводят при температуре от 10°С до 250°С, предпочтительно от 50°С до 150°С.
Соединения формулы (II), в которых R1 означает водород, С1-С4алкил или СОО(С1-С4)алкил, можно также получить при взаимодействии соединения формулы (V)
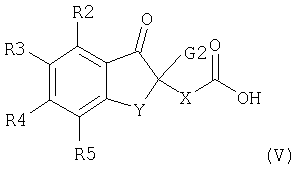
где R2, R3, R4, R5, Х и Y имеют значения, указанные выше, a G2 означает водород, С1-С4алкил или СОО(С1-С4)алкил, с соединением формулы (VI)
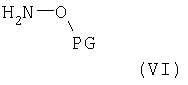
где PG означает защитную группу, имеющую значения, указанные выше.
Обычно эту реакцию проводят в две стадии в одной колбе. На первой стадии активируют карбоксилат формулы V. Эту реакцию проводят в инертном растворителе или разбавителе, например в дихлорметане, диоксане или тетрагидрофуране, в присутствии активирующего агента. Пригодным реакционноспособным производным кислоты является, например, ацилгалогенид, например ацилхлорид, полученный при взаимодействии кислоты с хлорангидридом неорганической кислоты, например с тионилхлоридом; смешанный ангидрид, например ангидрид, полученный при взаимодействии кислоты с хлорформиатом, таким как изобутилхлорформиат; активированный сложный эфир, например, полученный при взаимодействии кислоты с фенолом, таким как пентафторфенол; активированный сложный эфир, полученный при взаимодействии кислоты с N-гидроксибензотриазолом; ацилазид, например азид, полученный при взаимодействии с азидом, таким как дифенилфосфорилазид; ацилцианид, например цианид, полученный по реакции кислоты с цианидом, таким как диэтилфосфорилцианид; или продукт реакции кислоты с карбодиимидом, таким как дициклогексилкарбодиимид, или продукт реакции кислоты с бис-(2-оксо-3-оксазолидинил)фосфорилхлоридом. Реакцию проводят при температуре от -30°С до 60°С, обычно при 0°С или ниже. На второй стадии при температуре активации к раствору добавляют гидроксиламин и температуру медленно повышают до комнатной температуры. Указанные методы известны специалисту в данной области. По существу в данном случае можно использовать все методы синтеза амидов, которые используются в химии пептидов и которые приведены в монографии Methoden der organischen Chemie (Houben-Weyl), т.XV/1 и XV/2.
Соединения формулы (V) получают гидролизом соединений формулы (VII)
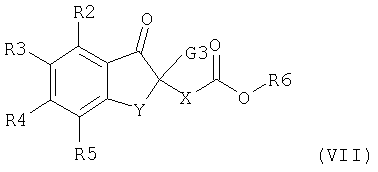
где X, Y, R2, R3, R4 и R5 имеют значения, указанные выше, G3 означает водород или С1-С4алкил, a R6 означает группу алкил, например метил, этил, трет-бутил или бензил. Условия реакции гидролиза зависят от природы группы R6. Если R6 означает метил или этил, реакцию проводят в присутствии основания, например гидроксида лития, гидроксида натрия или гидроксида калия, в инертном растворителе или разбавителе, например в метаноле или этаноле. Если R6 означает трет-бутил, реакцию проводят в присутствии кислоты, например раствора хлористоводородной кислоты, в инертном растворителе, таком как диэтиловый эфир или диоксан, или трифторуксусной кислоты в дихлометане. Если R6 означает бензил, реакцию проводят гидрогенолизом в присутствии катализатора на основе благородного металла, такого как палладий или платина, на соответствующем носителе, таком как уголь.
Соединения формулы (VII) получают из соединений формулы (VIII)
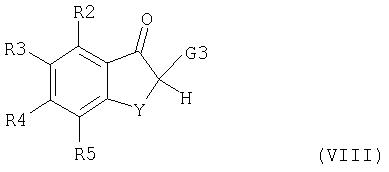
где R2, R3, R4, R5, Y и G3 имеют значения, указанные выше, при взаимодействии соединений формулы (IX)
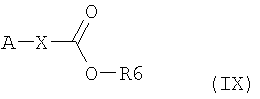
где А, X и R6 имеют значения, указанные выше, в отсутствии или в присутствии соответствующего основания. Пригодным основанием является, например, органический амин, такой, например, как пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, морфолин, N-метилморфолин или диазабицикло[5.4.0]ундец-7-ен, или, например, карбонат или гидроксид щелочного или щелочно-земельного металла, например карбонат натрия, карбонат калия, карбонат кальция, гидроксид натрия или гидроксид калия, или гидрид, например гидрид натрия.
Обычно реакцию проводят в соответствующем инертном растворителе или разбавителе, например в спирте или сложном эфире, таком как метанол, этанол, изопропанол или этилацетат, в галогенированном растворителе, таком как хлористый метилен, хлороформ или четыреххлористый углерод, в простим эфире, таком как тетрагидрофуран или 1,4-диоксан, в ароматическом растворителе, таком как толуол, или в полярном апротонном растворителе, таком как N,N-диметилформамид, N,N-диметилацетамид, N-этилпирролидин-2-он или диметилсульфоксид. Обычно реакцию проводят при температуре, например, от 10°С до 250°С, предпочтительно от 50°С до 150°С.
Кроме того, получение соединений формулы (VII) из соединений формулы (VIII) описано Ugi I. и др., Liebigs Ann. Chem., 641, 63-70 (1961).
(Б) Другим предпочтительным способом получения соединений формулы I является реакция соединения формулы (V) с гидроксиламином. Обычно эту реакцию проводят в две стадии в одной колбе. На первой стадии активируют карбоксилат формулы (V). Эту реакцию проводят в инертном растворителе или разбавителе, например в дихлорметане, диоксане или тетрагидрофуране, в присутствии активирующего агента. Пригодным реакционноспособным производным кислоты является, например, ацилгалогенид, например ацилхлорид, полученный при взаимодействии кислоты с хлорангидридом неорганической кислоты, например с тионилхлоридом; смешанный ангидрид, например ангидрид, полученный при взаимодействии кислоты с хлорформиатом, таким как изобутилхлорформиат; активированный сложный эфир, например, полученный при взаимодействии кислоты с фенолом, таким как пентафторфенол; активированный сложный эфир, полученный при взаимодействии кислоты с N-гидроксибензотриазолом; ацилазид, например азид, полученный при взаимодействии с азидом, таким как дифенилфосфорилазид; ацилцианид, например цианид, полученный при взаимодействии кислоты с цианидом, таким как диэтилфосфорилцианид; или продукт реакции кислоты с карбодиимидом, таким как дициклогексилкарбодиимид, или продукт реакции кислоты с бис-(2-оксо-3-оксазолидинил)фосфорилхлоридом. Реакцию проводят при температуре от -30°С до 60°С, обычно при 0°С или ниже. На второй стадии к раствору добавляют гидроксиламин при температуре активации и температуру медленно повышают до комнатной температуры. Эти методы известны специалисту в данной области. По существу в данном случае можно использовать все методы синтеза амидов, которые используются в химии пептидов и которые приведены в монографии Methoden der organischen Chemie (Houben-Weyl), т.XV/1 и XV/2.
(В) Третий предпочтительный способ получения соединений формулы (I) включает реакцию соединений формулы (X)
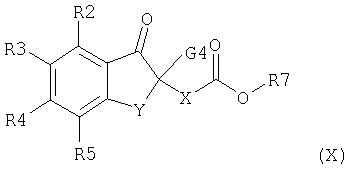
где X, Y, R2, R3, R4 и R5 имеют значения, указанные выше, G4 означает водород или С1-С4алкил, или СОО-трет-бутокси, a R7 означает С1-С4алкил, предпочтительно метил или этил, с гидроксиламином в присутствии соответствующего основания. Реакцию проводят в инертном растворителе или разбавителе, таком как метанол или этанол, при температуре от 0°С до 100°С, обычно при комнатной или приблизительно при комнатной температуре, и при pH от 10 до 12. Пригодным основанием является, например, алкоголят, например метилат натрия. Соединения формулы (X) получают аналогично тому, как описано при получении соединений формулы (VII).
Изобретение иллюстрируется следующими, без ограничения перечисленным, примерами, причем, если не указано иное, в указанных примерах:
(I) упаривание проводят в вакууме на роторном испарителе, а последующую обработку проводят после отделения твердого материала, такого как осушители, фильтрованием;
(II) реакции проводят при комнатной температуре, т.е. от 18°С до 25°С, и в атмосфере инертного газа, такого как азот;
(III) хроматографию на колонке (экспресс-хроматографию) и жидкостную хроматографию высокого разрешения (ЖХВР) проводят на силикагеле (Kieselgel Merck) или на силикагеле для обращенно-фазовой хроматографии (Lichroprep™ RP-18, фирма Е.Merck, Дармштадт, Германия);
(IV) выходы приводятся только для иллюстрации и необязательно означают максимально возможный выход;
(V) температуры плавления определяют на приборе для определения температуры плавления Buchi 510;
(VI) структуру конечных продуктов формулы I подтверждают методами ядерного (обычно протонного) магнитного резонанса (ЯМР) и масс-спектрометрии;
(VII) промежуточные соединения обычно характеризуют лишь некоторыми параметрами, а очистку проводят тонкослойной хроматографией (ТСХ);
(VIII) в примерах используют следующие сокращения:
ДМФ N,N-диметилформамид,
ДМСО диметилсульфоксид,
ТГФ тетрагидрофуран,
МеОН метанол,
HCl хлористоводородная кислота,
NaH гидрид натрия,
СН2Cl2 дихлорметан,
H2SO4 серная кислота,
КТ комнатная температура.
Пример 1
Гидроксиамид 5-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (1 г)

К раствору 5,0 г (22,9 ммоля) этилового эфира 1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (1a) (Pradeep К. и Saravanan К., Tetrahedron, 54, 2161-2168 (1998)) и 5,79 г (27,7 ммоля) этилового эфира 5-бромпентановой кислоты в 10 мл этанола при кипячении с обратным холодильником добавляли свежеприготовленный раствор 0,53 г натрия в 15 мл этанола и смесь кипятили с обратным холодильником в течение 10 ч. Затем добавляли немного воды для растворения осадка, растворитель выпаривали, остаток растворяли в растворе 3,85 г КОН в 7 мл МеОН и 5 мл Н2О, и смесь кипятили с обратным холодильником в течение еще 10 ч. После охлаждения смесь выливали в 25 мл 4 н. HCl при охлаждении льдом и экстрагировали СН2Cl2. После выпаривания растворителя получали неочищенную 5-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановую кислоту (1б). Продукт растворяли в 100 мл МеОН, добавляли несколько капель H2SO4 и раствор кипятили с обратным холодильником в течение ночи. Затем добавляли раствор бикарбоната натрия, растворитель выпаривали, остаток очищали хроматографией на колонке, при этом получали 1,9 г метилового эфира 5-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (1в). К раствору 1,6 г (23 ммоля) гидрохлорида гидроксиламина в 40 мл МеОН добавляли 15 мл раствора 0,8 г (35 ммолей) натрия в 30 мл МеОН, а затем добавляли раствор 3,0 г (11,5 ммолей) метилового эфира 5-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (1в) в 20 мл МеОН и оставшиеся 15 мл раствора метилата натрия. Смесь перемешивали при КТ в течение 6 ч, растворитель выпаривали, остаток подкисляли 2 н. HCl и экстрагировали СН2Cl2. Растворитель выпаривали, остаток очищали хроматографией на колонке, указанное в заголовке соединение получали в виде масла (2,2 г). МС (APCI): 260,1 (М-1).
Пример 2
Гидроксиамид 5-(6-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (2 г)
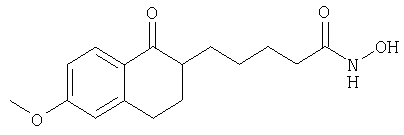
5-(6-Метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановую кислоту (2б) получали из этилового эфира 6-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (2а) (Basu В. и др., Synth. Commun., 11, 10, 803-810 (1981)) аналогично тому, как описано в примере 1 при получении соединения 1б. Соединение 2б (6,6 г, 24,3 ммоля) растворяли в 140 мл CH2Cl2. К полученному раствору последовательно добавляли 3,3 мл триэтиламина, 6,9 г бис-(2-оксо-3-оксазолидинил)фосфорилхлорида, 3,0 г О-бензилгидроксиламина, вторую порцию (10,2 мл) триэтиламина и смесь перемешивали в течение ночи. Затем раствор промывали 2 н. HCl, насыщенным раствором NaCl и упаривали. Остаток обрабатывали диэтиловым эфиром, при этом получали 8,5 г бензилоксиамида 5-(6-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (2в) в виде кристаллов белого цвета. Соединение 2в (0,5 г) гидрогенизировали в метаноле в присутствии катализатора Pd/ВаСО3/Pb, растворитель выпаривали, продукт обрабатывали диэтиловым эфиром, при этом получали 0,3 г указанного в заголовке соединения, tпл. 118-120°С.
Энантиомеры соединения 2 г разделяли полупрепаративной ЖХВР на колонке с сорбентом Chiracel OJ-R (элюент: вода/метанол). Степень очистки определяли аналитической ЖХВР (колонка 4,6 мм ×15 см, Chiracel OJ-R, размер частиц 5 мкм, элюент: вода/метанол, 35:65 об./об., скорость элюции 0,6 мл/мин, объем образца 5 мкл). Время удерживания и содержание каждого энантиомера составляли 17,53 мин (91%) и 21,9 мин (84%) соответственно.
Пример 3
Гидроксиамид 6-(6-хлор-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (3в)
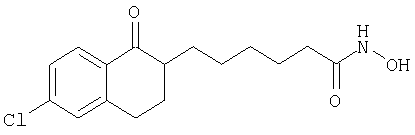
6-(6-Хлор-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановую кислоту (3б) получали из этилового эфира 6-хлор-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (3а) (WO 98/54350) аналогично тому, как описано в примере 1 при получении соединения 1б, при замене этилового эфира 5-бром-пентановой кислоты на этиловый эфир 6-бромгексановой кислоты. К 1,6 г соединения 3б в 20 мл СН2Cl2 добавляли 3,7 мл триэтиламина и 1,5 г (9 г) бис(2-оксо-3-оксазолидинил)фосфорилхлорида. После перемешивания в течение 30 мин добавляли 1,7 г О-тритилгидроксиламина и перемешивали в течение ночи. Раствор экстрагировали 2 н. HCl и упаривали, продукт получали в виде масла (2,9 г). Полученное масло растворяли в 20 мл СН2Cl2 и 10 мл трифторуксусной кислоты и смесь перемешивали в течение 4 ч. Затем смесь промывали водой и выпаривали растворитель, неочищенный продукт очищали хроматографией на колонке, указанное в заголовке соединение получали в виде масла (60 мг). МС (APCI): 308,1 (М-1).
Пример 4
Гидроксиамид 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (4в)
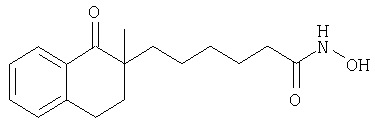
К суспензии 0,7 г NaH в 40 мл сухого ТГФ добавляли 4,0 г 2-метил-1-тетралона в 20 мл ТГФ и перемешивали в течение 30 мин. Затем добавляли 5,5 г этилового эфира 6-бромгексановой кислоты в 10 мл ТГФ и смесь кипятили с обратным холодильником в течение 6 ч. Растворитель выпаривали, остаток растворяли в растворе 4,16 г гидроксида калия в 50 мл МеОН и 20 мл Н2О и кипятили с обратным холодильником в течение ночи. МеОН выпаривали, водную фазу экстрагировали этилацетатом, подкисляли добавлением 2 н. HCl и снова экстрагировали этилацетатом. Полученный экстракт упаривали, при этом получали 4,2 г неочищенной 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (4а). Указанное в заголовке соединение 4в получали в виде масла из соединения 4а аналогично тому, как описано в примере 3 при получении соединения 3в из соединения 3б. МС (APCI): 288,1 (М-1).
Энантиомеры соединения 4в разделяли полупрепаративной ЖХВР на колонке с сорбентом Chiracel OJ-R (элюент: вода/метанол). Степень очистки определяли аналитической ЖХВР (колонка 4,6 мм ×15 см, Chiracel OJ-R, размер частиц 5 мкм, элюент: вода/метанол, 40:60 об./об., скорость элюции 0,6 мл/мин, объем образца 10 мкл). Время удерживания и содержание каждого энантиомера составляли 16,75 мин (100%) и 20,25 мин (87%) соответственно.
Пример 5
Гидроксиамид 6-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (5в)
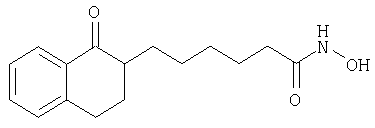
Гидроксиамид 6-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (5в) получали из этилового эфира 1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (1а) аналогично тому, как описано в примере 3 при получении соединения Зв из соединения За. Выход на последней стадии составлял 10%. МС (APCI): 274,1 (М-1).
Пример 6
Гидроксиамид 5-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (6б)
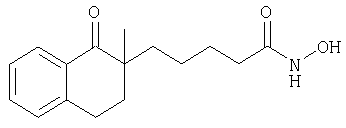
К суспензии 0,86 г NaH в 40 мл сухого ТГФ добавляли 5,0 г 2-метил-1-тетралона в 20 мл ТГФ и перемешивали в течение 30 мин. Затем добавляли 7,5 г этилового эфира 5-бромпентановой кислоты в 20 мл ТГФ и смесь кипятили с обратным холодильником в течение 6 ч. Смесь охлаждали, выливали в воду и экстрагировали этилацетатом. Экстракт упаривали, при этом получали неочищенный этиловый эфир 5-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты (6а), который очищали хроматографией на колонке, при этом получали 3,6 г очищенного соединения 6а. Соединение 6б получали в виде масла из соединения 6а аналогично тому, как описано в примере 1 при получении соединения 1г из соединения 1в. МС (APCI): 274,1 (М-1).
Энантиомеры соединения 6б разделяли полупрепаративной ЖХВР на колонке с сорбентом Chiracel OJ-R (элюент: вода/метанол). Степень очистки определяли аналитической ЖХВР (колонка 4,6 мм ×15 см, Chiracel OJ-R, размер частиц 5 мкм, элюент: вода/метанол, 40:60 об./об., скорость элюции 0,6 мл/мин, объем образца 10 мкл). Время удерживания и содержание каждого энантиомера составляли 11,48 мин (100%) и 13,86 мин (95%) соответственно.
Пример 7
Гидроксиамид 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гекс-5-еновой кислоты (7в)
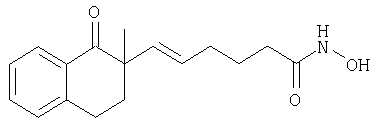
К 1,55 мл диизопропиламина в 40 мл ТГФ при -75°С добавляли раствор 4,36 мл н-бутиллития (2,5 М раствор) в гексане. Через 10 мин к смеси добавляли 1,63 г 2-метил-1-тетралона в 5 мл ТГФ и перемешивали в течение 50 мин. Затем по каплям добавляли 1,60 г метилового эфира 6-оксогексановой кислоты в 5 мл ТГФ и перемешивали в течение 15 мин, после чего охлаждающую баню удаляли и смесь нагревали до КТ. К смеси добавляли конц. раствор хлорида аммония и экстрагировали этилацетатом. Растворитель выпаривали, остаток очищали хроматографией на колонке, при этом получали 0,8 г метилового эфира 6-гидрокси-6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (7а). Соединение 7а (2,5 г) растворяли в 50 мл дихлорметана и добавляли 2,27 мл триэтиламина. После охлаждения до 0°С по каплям добавляли 2,86 г ангидрида метансульфокислоты в 20 мл дихлорметана, охлаждающую баню удаляли и перемешивали в течение ночи. Раствор промывали 2 н. HCl и водой, слои разделяли, органический слой сушили и упаривали. Неочищенный продукт и 1,6 г 1,8-диазабицикло[5.4.0]ундец-7-ена (ДБУ) растворяли в 60 мл толуола и кипятили с обратным холодильником в течение 24 ч. Затем смесь выливали в 2 н. HCl и экстрагировали дихлорметаном. Экстракт упаривали, остаток очищали хроматографией на колонке, при этом получали 0,6 г метилового эфира 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гекс-5-еновой кислоты (7б). Соединение 7в получали из соединения 7б в виде масла аналогично тому, как описано в примере 1 при получении соединения 1г из соединения 1в. МС (APCI): 286,1 (М-1).
Пример 8
Гидроксиамид 5-(5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (8е)
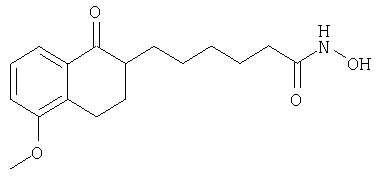
Этиловый эфир 5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (2,34 г, 8а) (Genet J.P. и др., Tetrahedron Lett., 35, 4559-4562 (1994)) обрабатывали этиловым эфиром 6-бромгексановой кислоты аналогично тому, как описано в примере 3 при модификации соединения 3а. При этом получали смесь 6-(5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (8б) и этилового эфира 2-(5-карбоксипентил)-5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (8в) в соотношении приблизительно 1:1. Полученную смесь кислот разделяли обработкой O-бензилгидроксиламином аналогично тому, как описано в примере 2 при получении соединения 2в из соединения 2б. Неочищенный продукт очищали хроматографией на колонке, при этом получали неразделимую смесь этилового эфира 2-(5-бензилоксикарбамоилпентил)-5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (8 г) и бензилоксиамида 6-(5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты (8д). Полученную смесь гидрогенизировали в метаноле в присутствии катализатора Pd/C/BaSO4.
Полученный неочищенный продукт очищали методами ЖХ/МС. Указанное в заголовке соединение получали после обработки объединенных фракций, содержащих продукт с ММ 305. МС (APCI): 306,1 (М+1).
Пример 9
Этиловый эфир 2-(5-гидроксикарбамоилпентил)-5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (9а)
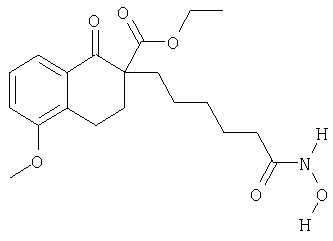
Указанное в заголовке соединение получали после разделения и последующей обработки объединенных фракций, содержащих продукт с ММ 377, методом ЖХ/МС, описанным в примере 8. МС (APCI): 378,3 (М+1).
Пример 10
Этиловый эфир 2-(7-гидроксикарбамоилгептил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (10г)
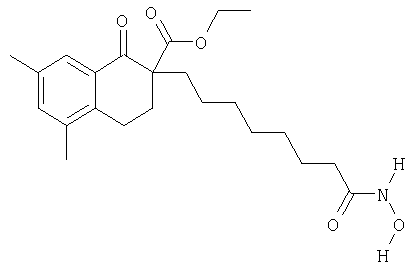
Этиловый эфир 5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (10а) получали из 5,7-диметил-1-тетралона обычным способом. К раствору 3,5 г соединения 10а и 4,5 г метилового эфира 8-бромоктановой кислоты в 30 мл этанола при кипячении с обратным холодильником добавляли свежеприготовленный раствор 0,35 г натрия в 15 мл этанола и кипятили с обратным холодильником в течение 15 ч, затем выпаривали этанол и добавляли дихлорметан и воду. После разделения слоев и очистки хроматографией на колонке получали 4,0 г продукта в виде масла желтого цвета. Продукт растворяли в растворе 690 мг КОН в 10 мл воды и 10 мл МеОН и кипятили с обратным холодильником в течение еще 13 ч. Затем раствор охлаждали, подкисляли 2 н. HCl и экстрагировали CH2Cl2. После выпаривания растворителя получали остаток, содержащий неочищенный этиловый эфир 2-(7-карбоксигептил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (10б). После очистки хроматографией на колонке получали 1,2 г соединения 10б. Соединения 10б (603 мг) растворяли в 10 мл диэтилового эфира, добавляли 0,3 мл N-метилморфолина, 0,33 мл изобутилхлорформиата, а затем 270 мг O-бензилгидроксиламина. После обычной обработки получали 600 мг (71%) этилового эфира 2-(7-бензилоксикарбамоилгептил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты (10в). Указанное в заголовке соединение получали из соединения 10в аналогично тому, как описано в примере 2 при получении соединения 2г из соединения 2в. МС (APCI): 402,52 (М-1).
Пример 11
Следующие соединения получали аналогично тому, как описано в примерах 1-10, и при использовании известных методов, описанных в литературе (например, в руководствах по оргсинтезу, таких как Houben-Weyl, Methoden der Organischen Chemie, Georg Thieme Verlag, Stuttgart; Organic Reactions, John Wiley&Sons, Inc., New York):
а) гидроксиамид 5-(6,7-диметокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
б) гидроксиамид 6-(6-диметиламино-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
в) гидроксиамид 6-(6,7-диметокси-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
г) гидроксиамид 5-(6,7-диметокси-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
д) гидроксиамид 6-(6-диэтиламино-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
е) гидроксиамид 6-(2-метил-1-оксо-6-пирролидин-1-ил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
ж) гидроксиамид 6-(2-метил-1-оксо-6-пиперидин-1-ил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
з) гидроксиамид 6-(2-метил-1-оксо-6-фенил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
и) гидроксиамид 6-(6-бром-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
к) гидроксиамид 5-(7-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
л) гидроксиамид 5-(5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
м) гидроксиамид 5-(5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
н) гидроксиамид 6-(2-метил-1-оксо-6-пиридин-2-ил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
о) гидроксиамид 6-(2-метил-1-оксо-6-пиридин-3-ил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
п) гидроксиамид 6-(2-метил-1-оксо-6-пиридин-4-ил-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
р) гидроксиамид 5-(7-диметиламино-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
с) гидроксиамид 5-(7-амино-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
т) гидроксиамид 6-(2,6-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
у) гидроксиамид 5-(2-этил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
ф) гидроксиамид 6-(2,5,8-триметил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
х) гидроксиамид 5-(6,7-диметокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
ц) метиловый эфир 2-(4-гидроксикарбамоилбутил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты,
ч) метиловый эфир 2-(5-гидроксикарбамоилпентил)-6-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты,
ш) 2-(4-гидроксикарбамоилбутил)-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновая кислота,
щ) гидроксиамид 5-(7-диметиламино-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)-2,2-диметилпентановой кислоты,
э) гидроксиамид 2-метил-5-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
ю) гидроксиамид 1-[3-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пропил]циклопропанкарбоновой кислоты,
я) гидроксиамид 5-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пент-4-еновой кислоты,
аа) гидроксиамид 6-(7-хлор-2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
бб) этиловый эфир 2-(5-гидроксикарбамоилпентил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты.
Пример 12
Определение ингибирующих свойств соединений по изобретению
Для определения ингибирующих свойств соединений по изобретению был разработан метод тестирования с использованием в качестве субстрата фермента аминокумарин-производного ω-ацетиллизина. Более подробно этот метод анализа описан Hoffman К. и др., Nucleic Acid Research, 27, 2057-2058 (1999). В описанной методике ингибирующее действие новых соединений определяли при концентрации 10 нМ. Степень ингибирования, определенная для отдельных соединений, приведена в таблице.
При анализе указанным методом субероиланилидгидроксамовая кислота (указанная на стр.2) при аналогичной концентрации (10 нМ) характеризуется степенью ингибирования 42%.
Пример 13
Соединение 2г описано в примере 2
Методика
1. Компоненты 1, 2 и 3 пермешивают в соответствующем смесителе в течение 15 мин.
2. Смесь, полученную на стадии 1, гранулируют в смеси с 20% раствором повидона К30 (компонент 4).
3. Гранулят, полученный на стадии 2, высушивают при 50°С.
4. Гранулят, полученный на стадии 3, измельчают на соответствующем оборудовании.
5. К измельченному грануляту, полученному на стадии 4, добавляют компонент 5 и перемешивают в течение 3 мин.
6. Гранулят, полученный на стадии 5, прессуют на соответствующем прессе.
Пример 14
Методика
1. Компоненты 1, 2 и 3 перемешивают в соответствующем смесителе в течение 15 мин.
2. Добавляют компоненты 4 и 5 и перемешивают в течение 3 мин.
3. Заполняют соответствующую капсулу.
Литература
Basu В. и др., Synth. Commun. 11, 10, 803-810 (1981).
DeVita M.E., Jr., Hellmann S., Rosenberg S.A., Cancer: Principles and Practice of Oncology, 5th ed., Lippincott-Raven Publishers (1997).
Genet J.P. и др., Tetrahedron Lett., 35, 4559-4562 (1994).
Hoffman К. и др., Nucleic Acids Research, 27, 2057-2058 (1999).
Houben-Weyl, Methoden der organischen Chemie, т.XV/1 и XV/2.
Houben-Weyl, Methoden der Organischen Chemie, Georg Thieme Verlag, Stuttgart.
Marks P.M. и др., J. Natl. Cancer. Inst. 15, 1210-1216 (2000).
Organic Reactions, John Wiley&Sons, Inc., New York.
Pradeep К. и Saravanan K., Tetrahedron, 54, 2161-2168 (1998).
Ugi I. и др., Liebigs Ann. Chem., 641, 63-70 (1961).
US 5369108.
WO 98/54350.
WO 98/55449.
Изобретение относится к соединениям формулы (I)
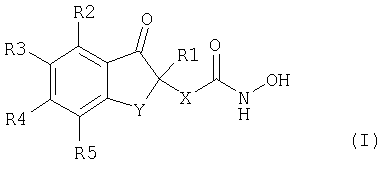
где R1 выбирают из ряда водород, С1-С4алкил, СООН, СОО(С1-С4)алкил; R2, R3, R4, R5 независимо выбирают из ряда водород, галоген, С1-С4алкил-, гидрокси-, С1-С4алкокси-; Y означает -СН2-СН2-; Х означает алкиленовую цепь, содержащую от 4 до 10 атомов углерода, которая является насыщенной или ненасыщенной, может содержать одну двойную связь, может быть разветвленной или неразветвленной, его энантиомеры, а также его соли с фармацевтически приемлемыми кислотами и основаниями. Изобретение также относится к фармацевтической композиции, обладающей ингибирующей активностью в отношении гистондеацетилазы, содержащей активный ингредиент в виде соединения формулы I, в смеси с фармацевтически приемлемым носителем, эксципиентами или разбавителями. Технический результат - производные тетралона, обладающие противоопухолевой активностью. 2 н. и 4 з.п. ф-лы, 1 табл.
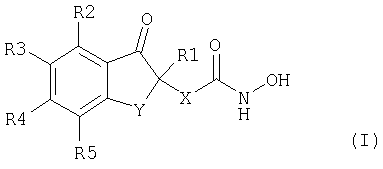
где R1 выбирают из ряда водород, С1-С4алкил, СООН, СОО(С1-С4)алкил;
R2, R3, R4, R5 независимо выбирают из ряда водород, галоген, С1-С4алкил-, гидрокси-, С1-С4алкокси-;
Y означает -СН2-СН2-;
Х означает алкиленовую цепь, содержащую от 4 до 10 атомов углерода, которая является насыщенной или ненасыщенной, может содержать одну двойную связь, может быть разветвленной или неразветвленной,
его энантиомеры, а также его соли с фармацевтически приемлемыми кислотами и основаниями.
гидроксиамид 5-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
гидроксиамид 5-(6-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
гидроксиамид 6-(6-хлор-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
гидроксиамид 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
гидроксиамид 6-(1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
гидроксиамид 5-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)пентановой кислоты,
гидроксиамид 6-(2-метил-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гекс-5-еновой кислоты,
гидроксиамид 5-(5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-ил)гексановой кислоты,
этиловый эфир 2-(5-гидроксикарбамоилпентил)-5-метокси-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты,
этиловый эфир 2-(7-гидроксикарбамоилгептил)-5,7-диметил-1-оксо-1,2,3,4-тетрагидронафталин-2-карбоновой кислоты,
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| US 5369108 A, 29.11.1994 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ АРИЛАЦЕТГИДРОКСАМОВЫХ КИСЛОТ | 0 |
|
SU309511A1 |
Авторы
Даты
2006-11-27—Публикация
2001-12-06—Подача