Изобретение относится к способу получения неизвестных ранее замещенных арилацетгидроксамовых кислот общей формулы
/,0
R- -y-CHgC
NHOH XI)
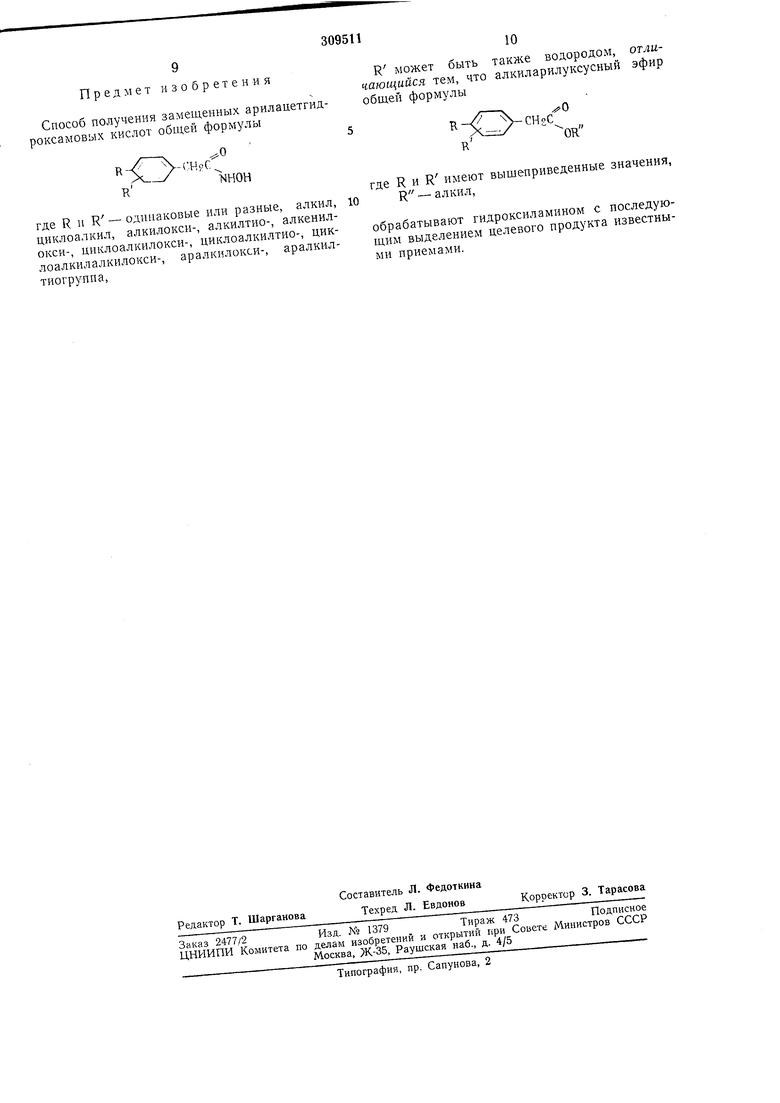
где R и R - одинаковЕяе или разные, алкнл, циклоалкил, алкилоксн-, алкилтио-, алкенилОКСИ-, циклоалкилокси-, циклоалкилтио-, цнклоалкилалкилокси-, аралкилокси-, аралкилтиогруппа, кроме того R может быть водородом, которые могут найти применение в качестве физиологически активных веществ.
Способ получения соединений формулы I состоит в том, что алкиларилуксусный эфир общей формулы
0
СИ 2 с OR
Г.
где R н R имеют вышеуказанные значения,
R - алкил, обрабатывают гидроксиламином н выделяют целевой продукт известными приемами.
Исходный алкиларилуксусный эфир получают при конденсации р-алкил-, / -циклоалкил-, /9-алкилокси-, f-алкилтио-, р-цнклоалкнлокси-, р-циклоалкнлтио-, арилалкилтио- или арилалкилокснбензилгалогенида с цианидом щелочного металла и обработке полученного арилацетонитрила кислотой н спиртом, либо нрн обработке ацетофенона, замещенного в параположении к кетонной группе алкнльным, циклоалкнльным, алкплокси-, алкилтио-, циклоалкилокси-, циклоалкнлтно-, арилалкилоксннли арилалкилтиорадикалом, серой и вторичным основанием, например морфолином, с получением комплекса, который гидролизуют в
соответствующую арнлуксусную кислоту и последнюю этерифицируют.
Для синтеза соединений формулы I хлористый /)-алкилбензнл, получаемый хлорметилированием /5-алкилбензола, конденсируют с цианндом щелочного металла, полученный р-гпкилфенилацетоннтрил этерифицируют спиртом, например метиловым, этиловым или пропиловым, в присутствии серной кислоты, получая р-алкилфенилуксусный эфир, который в сыром
виде обрабатывают гидроксиламином с получением соответствующей фенилацетгидроксамовой кислоты.
CHgCl 4- NaCN--R-CHgCOOR RП p и M e j I. уУ-трег-Бутилфеиилацетгидроксамовая кислота.
-СНгС - NaCN-(СНз)зС -« CHaCN+NeCl
(СНз)зС-(СН5)зС-(Г$ -СН2СООСН5 к раствору 15,5 г цианистого натрия в 15 мл воды добавляют в течение 30 мин раствор 45 г хлористого р-т оег-бутилбензила (т. кип. 88-89° С/3 мм. рт. ст. ) в 45 мл этилового спирта. Полученную смесь нагревают 4 час с обратным холодильником и охлаждают. Отфильтрованный осадок нромывают небольшим количеством снирта. Из фильтрата отгоняют снирт, растворяют остаток в эфире и нромывают раствор водой, после чего высушивают над сернокислым магнием. После выпаривания эфира перегоняют остаток в вакууме и отбирают -грет-бутилфенилацетонитрил, т. кин. 149-152° С/16 мм рт. ст. Смешивают 20 г (25 мл) метилового спирта и 20 г (10,9 мл) концентрированной серной кислоты при перемешивании и охлаждении, приливают 17,3 г р-грег-бутилфенилацетонитрила и нагревают 10 час с обратным холодильником. Охлажденную смесь выливают в воду со льдом. Отделяют органический слой, высушивают его над сернокислым магнием и отгоняют метиловый снирт. Метиловый эфир p-rpei-CH2CN- -NaCl
H2S04
0
- СНгС
-ШОН
СЙзОН HgSO
Таблица 1 (CHjjsC -СНгС бутилфенилуксусной кислоты не выделяют, а используют в сыром виде. Растворы 5 г металлического натрия в 150 мл абсолютного метанола и 7 г солянокислого гидроксиламина в 100 мл абсолютного метанола смешивают, отделяют хлористый натрий. К фильтрату добавляют сырой метиловый эфир р-грег-бутилфенилуксусной кислоты и нагревают с обратным холодильником 1 час. После охлаждения подкисляют 20%-ной соляной кислотой и отделяют осадок р-грег-бутилфанилацетгидроксамовой кислоты. После однократной перекристаллизации из ацетона получают белый продукт, т. пл. 115-118° С. Этот продукт при растворении в метаноле дает винно-красное окрашивание с хлорным железом (общая реакция на гидроксамовые кислоты). Найдено, %: С 69,2; Н 8,4; N 6,68. Вычислено, %: С 69,2; Н 8,21; N 6,76. Пример 2. Аналогично примеру 1 получают ряд соединений формулы I (см. табл. 1), дающих винно-красное окрашивание с хлорным железом.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных изофлавона | 1971 |
|
SU508205A3 |
| Способ получения производных пиридина или их солей | 1974 |
|
SU633475A3 |
| СПОСОБ ПОЛУЧЕНИЯ N-ОКСИАМИДОВ ПАРААЛКИЛОКСИ- АРИЛУКСУСНЫХ КИСЛОТ | 1970 |
|
SU274732A1 |
| Способ получения ацетгидроксамовых кислот или их солей | 1977 |
|
SU689617A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОКСИМОВ | 1972 |
|
SU340160A1 |
| Способ получения ксантонов или их солей | 1975 |
|
SU593665A3 |
| Способ получения производных -фенилжирной кислоты | 1969 |
|
SU528864A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦИКЛОГЕПТЕНА | 1973 |
|
SU383288A1 |
| Способ получения производных 2-нитроаминопиримидона-4 | 1980 |
|
SU906376A3 |
| Способ получения гетероциклических соединений | 1971 |
|
SU462335A3 |

При получении кислот общей формулы I, исходя из замещенного ацетофенона, последний синтезируют при конденсации р-оксиацетофенона, его гомолога или аналога с алкилгалогенидом, например алкилбромидом.
со - CHj4- RBr- RO fb
но
Реакция получения р-алкилоксифенилацетгидроксамовой кислоты из р-алкилоксиацетофенона идет по схеме
(2)
Уснгсоон но
9 Ч
сн:соосгщ Исходный замещенный ацетофенон можно получить также при конденсации фенола с алкилталогенидом, например с алкилбромидом, и последующей обработке полученного алкилоксибензола уксусным ангидридом в5
- ОН RBr
(CH3CO)s;0,
ZnClg Ц77Ц (
N/
Дальнейшие реакции проводятся, как указано в предыдущей реакционной схеме, начиная с реакции 2.
Пример 1. Смешивают 136 г р-оксианетофенона, 140 г бутилбромида, 152 г углекислого калия, 17 г йодистого калия и 275 мл этанола и нагревают 48 час с обратным холодильником. После охлаждения, разбавления водой и экстрагирования эфиром эфирную фазу промывают сначала 10%-ным раствором едкого натра, затем водой, высушивают, вьшаривают эфир и перегоняют продукт в вакууме. Получают 168 г р-бутилоксиапетофенона, выход 87%, т. кип. 160-162°С/П мм рт. ст.
Смешивают 192 г р-бутилоксиацетофенона, 42 г серы и 130 г морфолина. нагревают 14 час с обратным холодильником, полученный раствор выливают в воду и перемешивают до кристаллизации 5-содержап1его комплексного соединения, которое отфильтровывают, промывают водой и высушивают. Выход 270 г (88% от теории). Раствор 200 г едкого натра -в 1500 мл этанола добавляют к раствору 293 г указанного S-содержашего комплекса. Смесь нагревают с обратным холодильником в течение ночи. Отгоняют спирт и разбавляют водой. Полученный раствор подкисляют соляной кислотой и экстрагируют эфиром. Эфирную фазу -промывают водой, экстрагируют 10%-ным раствором углекислого натрия и подкисляют шелочной раствор 10%-ной соляной кислотой. Отфильтровывают выпавший осадок и высушивают его. Получают 100 г (выход 70%) чистой р-н-бутилоксифенилуксусной кислоты.
208 г р-н-бутилоксифенилуксусной кислоты, 368 г этилового спирта и 18 мл сериой кислоты нагревают 5 час с обратным холодильником. Разбавляют смесь водой и экстрагируют ее эфиром. Эфирную фазу последовательно
NaOH (З)
снгсоон
RO
СгНзОН
H2SOi,
KHgOH (5)
VcHzf
СНлОН
МНОБ
-О
t-0
com.
промывают водой, раствором углекислого натрия и вновь водой, высушивают и выпаривают. Полученный этиловый эфир р-н-бутилоксифенилуксусной кислоты перегоняют, в вакууме. Выход 61%. Т. кип. 186° С/8 мм рт. ст.
К раствору 7 г солянокислого гидроксиламина в 100 мл метанола добавляют раствор
5 г металлического натрия в 150 мл метаиола
и отфильтровывают выпавшую соль. Добавляют 22 г этилового эфира р-н-бутилоксифенилуксусной кислоты и нагревают 1 час с обратным холодильником. Смесь охлаждают и подкисляют 20%-ной соляной кислотой. Получают 14,7 г р-н-бутилокснфеиилаиетгилпоксамовой
кислоты, выход 71%, т. пл. 153-155°С.
Пример 2. Получение /о-циклопентилоксифенилацетгидроксамовой кислоты.
Смешивают 200 г пиклопентилбромида, 181, г р-оксиацетофенонл, 23 г йодистого калия
и 203 г углекислого калия в 370 мл этанола, нагревают 48 час с обратным холодильником, проводя опыт, как в примере 1. Получают 195 г р-циклопентилоксиацетофенона, выход 68%.
195 г р-циклопентилоксиацетофенона, 45 г серы и 117 г морфолипа нагревают в течение ночи с обратным холодильником, гидролизуют раствором 188 г едкого натра в 1900 мл спирта. При обычной обработке получают 180 г
р-циклопентилоксифенилуксусной .кислоты, выход 85%. 180 г р-циклопентилоксифенилуксусной кислоты этерифицируют 296 г абсолютного этанола и 15 мл серной кислоты. Получают 152 г этилового эфира р-циклопентиЛоксифенилуксусной кислоты, выход 76%, т. кип. 180°С/7 мм рт. ст. 134 г указанного эфира обрабатывают раствором 27 г металлического натрия в 810 мл метанола, предварительно смешанного с раствором 33 г соляноприсутствии кислотного катализатора Льюиса (например, хлористого металла, полифосфорпои кислоты или трехфтористого бора) по схеме Всю смесь нагревают 1 час с обратным холодильником. После подкисления 20%-ной соляной кислотой получают 87 г р-циклопентилоксифенилацетгидроксамовой кислоты, выход 71%, т. пл. 122-124° С. Пример 3. Получение р-фенилэтилоксифенилацетгидроксамЪвой кислоты. Смешивают 130 г 1-бром-2-фенилэтана, 95 з р-оксиацетофенона, 12 г йодистого калия и 106 г углекислого калия в 200 мл этанола. После нагревания в течение 48 час с обратным холодильником и обычной обработки получают 110 г р-фенилэтилоксиацетофенона, выход 65%. 84 г /7-фенилэтилоксиацетофенона, 17 г серы и 46 г морфолина нагревают в течение ночи с обратным холодильником, гидролизуют раствором 66 г едкого натра в 400 мл этанола и после обычной переработки получают 70 г р-фенилэтилоксифенилуксусной кислоты, выход 72%. 120 г этой кислоты этерифицируют 184 г абсолютного этанола , и 9,2 мл серной кислоты. Получают 101 г этилового эфира рфенилэтилоксифенилуксусной кислоты, выход 68%, т. кип. 204° С/2 мм рт. ст. 43 г полученного эфира обрабатывают раствором 5 г металлического натрия в 150 м.л метанола, предварительно смешанным с раствором 7 г солянокислого гидроксиламина в 100 мл метанола. Смесь кипятят 1 час с обратным холодильником. После подкисления 20%-ной соляной кислотой получают 26 г р-фенилэтилоксифенилацетгидроксамовой кислоты, выход 62%, т. пл. 154-156° С. Аналогично получают кислоты, приведенные в табл. 2. Таблица 2 Кроме того, были получены р-н-бутилокси/и-изопропил- и р-н-бутилокси-т-метил-о-метилфенилацетгидроксамовые кислоты, т. пл. 127-128°С и 178-180°С соответственно. Все полученные кислоты дают винно-красное окрашивание с хлорным железом. Пример 4. р-н-Бутилокси-т-метилфенилацетгидроксамовая кислота и -е у- снгс -/ шон Смешивают 216 г о-крезола, 500 мл этанола, 140 г едкого кали в 100 мл воды и 300 г бутилбромида. После нагревания в течение 2 час с обратным холодильником отгоняют из реакционной смеси спирт. Остаток обрабатывают водой, экстрагируют эфиром или четыреххлористым углеродом, промывают углекислым натрием и водой и высушивают раствор. Прод кт перегоняют, получают 278 г о-метилбутилоксибензола, т. кип. 222°С. Выход 85%. 278 г о-метилбутилоксибензола обрабатывают 260 г уксусного ангидрида и 19 г хлористого цинка, кипятят 1 час с обратным холодильником при перемешивании, оазбавляют водой и экстрагируют эфиром. ЭсЬирный раствор промывают водой, углекислой щелочью и вновь волой и высушивают над сернокислым магнием. Продукт выкипает при 150° С и остаточном давлении 2 мм.. Получают 254 г о-нбутилокси-/п-метилацетофенона, выход 73%. 254 г р-н-бутилокси-те-метилацетофенона, 58 г серы и 156 г морфолина смешивают и кипятят в течение ночи с обратным холодильником. Затем добавляют 240 г едкого натра и 1200 мл этанола и вновь кипятят в течение ночи с обратным холодильником. КИСЛОТУ выделяют обычным методом. Получают 218 г р-«-бУтилокси-т-метилуксусной кислоты, выход 78%. Смешивают 185 г этанола, 9,2 мл концентрированной серной кислоты и 112 г р-н-бутилокси-т-метилфенилуксусной кислоты, нагревают 2 час с обратным холодильником и перегоняют в вакууме. Получают 83 г этилового эфира р-н-бутилокси-/п-метил6енилуксусной кислоты, т. кип. 162-163° С/3 мм рт. ст. Выход 66%. 23,1 г солянокислого гидроксиламина в 330 мл метанола смешивают пастворолг 15,5г металлического натрия в 495 мл метанола. К фильтрату прикапывают при перемешивании 83 г этилового эфира р-н-бутилокси-тметилфенилуксусной кислоты и перемешивают еще 1 час. Смесь выливают на летт и ттодкисляют 20%-ной соляной кислотой. ПРИ обработке петролейным эфиром выделяют 52 г р-н-бутипокси-т-метилфенилацетгидроксамовой кислоты, выход 65%, т. пл. ПО-111°С. Пример 5. Получение р-изобутилокси-тметилфенилацетгидроксамовой кислоты. Синтез проводят, как в примере 4, но применяют изобутилбромид вместо я-бутилбромида. Получают 48 г р-изобутилокси-т-метилфениляцетгидроксамовой кислоты из 70 г этилового эфира р-изобутилоксн-т-метилфенилуксусной кислоты. Выход , т. пл, 117,5- 118,5° С. 9 П р е д м е т и 3 о б р е т е н и я Способ получения замещенных арилацетгидроксамовых кислот формулы -№.) NHOH где R н R - одинаковые или разные, алкил, ю циклоалкил, алкилокси-, алкилтио-, алкенилОКСИ-, диклоалкилокси-, циклоалкилтио-, циклоалкилалкилокси-, аралкилокси-, аралкилтиогруппа, 3095 11 10 R может быть также водородом, отличающийся тем, что алкиларилуксусный эфир общей формулы нЧ VcHpc- ° R где R и R имеют выщеприведенные значения, R - алкил, обрабатывают гидроксиламином с последующим выделением целевого продукта известными приемами.
Авторы
Даты
1971-01-01—Публикация