Изобретение относится к области медицины, а именно к способам лабораторной диагностики.
В понятие "лекарственная непереносимость" входят специфические и неспецифические реакции больного на лекарства. Специфические - это истинно аллергические и псевдоаллергические реакции, а неспецифические реакции это фармакологические осложнения лекарственной терапии. К ним относятся: интоксикация лекарственными препаратами, абсолютная и относительная передозировка, кумуляция, вторичное действие, полипрагмазия и т.д. (Северова Е.Я. Неспецифические реакции больных на лекарства. - М., 1069, С.8-190; Пыцкий В.И., Артамонова Н.В., Артомосова А.В. - Аллергические заболевания. - М., 1991. С.149-175. Частная аллергология, под редакцией Г.Б.Федосеева, 2001, Т.2, С.255-265).
В отечественной и зарубежной литературе имеется достаточно много сведений о попытках диагностики истинной лекарственной непереносимости (ЛН) с помощью отдельных методов. В таблице 1 приведены наиболее информативные методы диагностики ЛН.
Определенную диагностическую ценность представляют тесты дегрануляции тучных клеток, дегрануляции базофилов по Шелли, РТМЛ и иммунотермистометрия. Однако в большинстве работ корреляция результатов с клинической картиной оказалась не выше 50% (Пыцкий В.И., Адрианова Н.В., Артомасова А.В. Аллергические заболевания. - М., 1999. C.119). То же относится и к тесту бласттрансформации лейкоцитов.
PACT - радиоаллергосорбентный тест (Wide L., Bennich I., Johansson S. // Lancet. - 1967 - N 7526. - P.1105; Patriaca G., Schiavino D., Nucera E., Milani A. Positive allergological tests may tern negative in further exposure to the specific allergens: a long term? Prospective, follow up study in patients allergic to penicillin // J. Investig.Allergol.Clin.Immunol. 1996, Vol 6. N 3, Р.162-165) разработан преимущественно для определения антител к антибиотикам пенициллинового ряда.
Для диагностики истинных аллергических реакций, связанных с иммунологической стадией, существуют современные иммуноферментные методы определения специфических IgE и IgG антител к некоторым лекарственным препаратам в сыворотке крови. Обнаружение специфических антител к лекарствам затруднено, либо из-за постоянно меняющегося их титра, либо из-за их полного отсутствия, поскольку многие препараты не являются аллергенами или имеют много метаболитов, каждый из которых может действовать самостоятельно. Следует также обратить внимание на то, что многие побочные реакции на лекарства являются либо псевдоаллергическими, либо токсическими или фармакологическими, при которых специфические антитела не образуются. Кроме того, лекарственные препараты не являются аллергенами. Даже, если из них образуются гаптены, то они могут и не обладать свойствами, необходимыми для антительного ответа организма. И, наконец, присутствие антител чаще не приводит к клиническим проявлениям аллергической реакции и не свидетельствует о ней. Поэтому подобные методы не следует рассматривать как диагностические.
Таким образом, перечисленные лабораторные методы включают в большинстве случаев иммунологические тесты, рассчитанные на определенные типы аллергических реакций, которые, на самом деле, встречаются крайне редко. Информативность результатов, по данным многих авторов, оцениваются по совпадению с анамнезом или с клинической картиной. Однако, чаще всего больные обращаются к специалистам в том случае, когда клинические проявления уже прошли и им нужно узнать причинно-значимый препарат, а также определить переносимые лекарства, необходимые для проведения дальнейшей терапии.
В литературе отсутствуют данные о профилактическом значении используемых методов диагностики ЛН.
В терапевтической практике в настоящее время применяется комплексная терапия, состоящая из ряда препаратов, обладающих различными точками приложения, поэтому необходимо определить эффект комбинированного действия препаратов.
Стало быть, способ диагностики лекарственной непереносимости должен быть универсальным, интегральным, позволяющим определять переносимые препараты до лечения и эффекты их комбинированного действия, учитывающие межлекарственные взаимодействия. Арсенал исследуемых лекарственных препаратов должен быть достаточно широким (не менее 1000).
Прототипом заявляемого способа выбран метод кислотных эритрограмм (Терсков И.Ф., Гительзон И.И. Метод химических (кислотных) эритрограмм. Биофизика. - 1957 - Т.2, С.259-266), который применяется для диагностики лучевой болезни и ее тяжести, гепатитов, различных отравлений по резистентности эритроцитов к химическому гемолитику.
Заявленный способ осуществляется следующим образом:
1. Берется гепаринизированная кровь в разведении 1:1000 в физиологическом растворе в количестве 2 мл.
2. В разведенную кровь добавляется лекарственный препарат в концентрации 1·10-6 М/л в количестве 0,2 мл и ставится в термостат при t 24°С на 10 мин.
3. После термостатирования добавляется 2 мл рабочего гемолитического раствора (0.004N HCl) и кювета устанавливается в ФЭК. Фотометрирование проводится при длине волны 670 нМ. Отсчет времени начинается каждые 30 секунд с момента введения гемолитика до получения двух совпадающих показателей, до завершения гемолиза.
4. Показания фотометрии вводятся в компьютер и обрабатываются по разработанной нами программе, позволяющей получить "столбиковую диаграмму" с доверительным интервалом, позволяющим оценить достоверность гемолитической стойкости эритроцитов под влиянием лекарственных препаратов по сравнению с воздействием физиологического раствора (контроль).
Прототип имеет ряд существенных недостатков:
1. Не предусматривает введение лекарственного препарата в реакционную среду (in vitro).
2. Обладает низкой информативностью и точностью диагностики.
3. Пробы обладают низкой информативностью.
4. Не предусматривает оценку комплексного действия нескольких препаратов.
Все недостатки в предлагаемом способе устраняются тем, что в исследуемую кровь вводятся лекарственные препараты в низких молярных концентрациях (10-6 М/л), что позволяет точно измерить их переносимость, используя процесс гемолиза как индикатор степени стойкости мембраны эритроцита под воздействием исследуемого вещества.
Разработанная нами компьютерная обработка результатов фотометрии повышает информативность и точность диагностики.
Высокая воспроизводимость результатов обеспечивается за счет правильной постановки контроля, компьютеризации. В качестве контрольной пробы используется кровь того же больного, в которую вместо препарата добавляется физраствор, а в протипе - донорская кровь.
Выбор концентрации препаратов, исследуемых в реакциях in vitro, нам представляется чрезвычайно важным, так как от этого зависит характер взаимодействия с эритроцитами крови. В доступной нам литературе (Бадина А.К. Диагностика лекарственной непереносимости. Клиническая медицина №7, 1990, С.78-80) указывается об использовании медикаментов в стандартных концентрациях, составляющих не менее 10-2-10-3 М/л. Медикаменты в таких концентрациях могут вызвать лишь разрушение мембраны эритроцитов и клеток с последующим гемолизом даже без добавления гемолитика.
Нами впервые было изучено в предварительных экспериментах с кровью практически здоровых доноров (без каких-либо признаков ЛН по данным анамнеза) воздействие антибиотиков и витаминов в концентрациях 10-2-10-22 М/л. Результаты показали, что лекарственные препараты в концентрациях 10-6-10-8 М/л оказались нейтральными для эритроцитов здорового человека.
В дальнейших исследованиях были использованы препараты в концентрациях 10-6 М/л (в качестве рабочей), что, возможно, более соответствовало реальным терапевтическим концентрациям препаратов в крови больного.
Нами впервые был изучен механизм взаимодействия лекарственных препаратов с мембраной эритроцитов в молярных концентрациях. Он заключается в том, что в плазматической мембране эритроцитов, помещенных в гипотоническую среду (гемолитическая среда в заявленном способе), в присутствии малых концентраций лекарственных препаратов - 10-6 М/л наступает нарушение транспорта ионов (увеличение тока ионов в клетку) и соответственно увеличение проницаемости мембраны и ускорение гемолиза эритроцитов. У больного с непереносимостью того или иного препарата гемолиз происходит быстрее, чем у здоровых доноров. При этом не наступает никаких изменений мембраны эритроцитов и тем более ее разрушений.
Способ осуществляется следующим образом. Регистрация изменений кинетики гемолиза производится на установке, основой которой является фотоэлектрический колориметр концентрационный с микропроцессором - КФК-2 МП. Используются кюветы толщиной 20 мм. В рабочую кювету вводится 2 мл равномерно перемешанной крови в разведении 1:1000, туда же добавляется лекарственный препарат в концентрации 10-6 М/л в количестве 0,2 мл, тщательно перемешивается. Кювета ставится на 10 мин в термостат при температуре 24°С. Через 10 мин добавляется 2 мл рабочего гемолизирующего раствора (0,004N HCl). Кювета устанавливается в ФЭК, против кюветы с дистиллированной водой. Фотометрирование производится при длине волны 670 нм. Отсчет времени начинается (при включении микропроцессора и одновременно секундомера), каждые 30 сек с момента введения гемолитика до получения двух совпадающих показателей, то есть до завершения гемолиза. Экстинкция к концу гемолиза не достигает 0 (нуля), что объясняется поглощением света, вышедшим из эритроцитов гемоглобином, который под воздействием соляной кислоты превращается в соляно-кислый гематин.
Оценка полученных результатов проводится следующим образом. В результате отсчетов получается ряд убывающих экстинкций, каждая из которых соответствует степени гемолиза к моменту отсчета. Показания фотометрии вводятся в компьютер и обрабатываются по разработанной нами программе, в результате чего получается "столбиковая диаграмма" вместе с доверительным интервалом (±5%, так как определенный в эксперименте коэффициент вариации метода не превышает 5%), позволяющим оценить достоверность гемолитической стойкости эритроцитов под влиянием лекарственных препаратов по сравнению с воздействием физиологического раствора (контроль). Снижение стойкости эритроцитов на 10% можно считать достоверным, свидетельствующим о непереносимости того или иного препарата.
Пример, полученной путем обработки на компьютере, приведен на фиг.1.
СПСЭ - суммарный показатель стойкости эритроцитов - площадь под кривой распределения. На фиг.1 видно, что препараты: бициллин, вибромицин, канамицин, линкомицин, левомицетин не переносимы, так как их белые столбики и доверительные интервалы ниже нижней доверительной границы столбиков - площадей с физраствором (косая штриховка). Остальные препараты - переносимы. Для данной больной был рекомендован и выбран гентамицин. Лечение этим антибиотиком прошло без осложнений.
В клинической практике приходится часто сталкиваться с применением комплекса препаратов. Определить оптимально переносимые сочетания препаратов помогает предлагаемый способ диагностики ЛН.
Приводим клинические примеры:
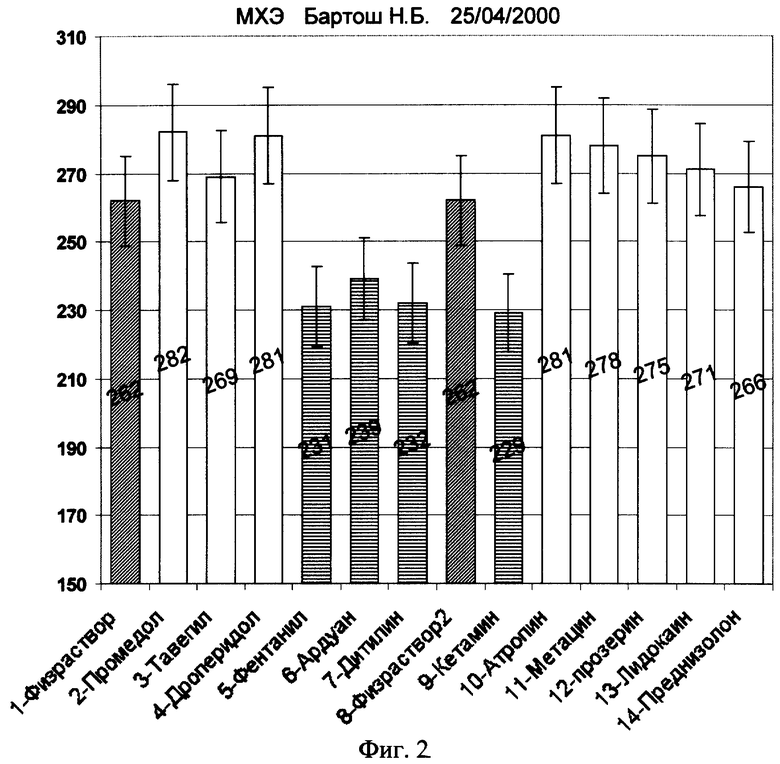
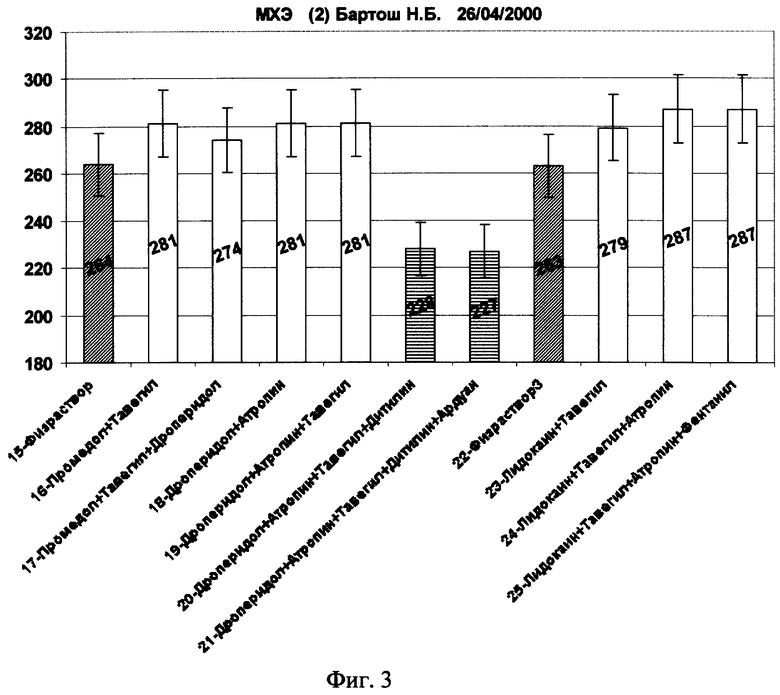
Больной Бартош Н.Б., 43 года, в связи с маточным кровотечением, в 1996 году сделали диагностическое выскабливание с применением наркотических анальгетиков (фентанил), холинолитиков (атропин) и других, после чего у нее был анафилактический шок - это происходило в Тюменской области. В г.С-Петербурге в СПбГМУ им. акад. И.П.Павлова был поставлен диагноз: миома матки и назначена операция. Перед аллергологами была поставлена задача - определить и выбрать переносимые сочетания наркотических анальгетиков для проведения внутривенного и ингаляционного наркоза или перидуральной анестезии. С помощью предлагаемого способа была определена переносимость 21 препарата и их сочетаний. Результаты представлены на фиг.2 и фиг.3.
Как видно из представленных на фиг.2 и фиг.3 диаграмм, многие отдельно взятые препараты - переносимы (белые столбики, выше физраствора - косая штриховка столбиков), тогда как сочетания этих препаратов большей частью не переносимы. Наиболее удачные сочетания видны на фиг.3 (МХЭ - (2) Бартош Н.Б. 26/04/2000) - последние три белых столбика. Эти три столбика и есть перидуральный наркоз, который был применен и больная перенесла его без осложнений. Операция прошла успешно.
Таким образом, заявленный способ позволяет наиболее точно определить причинно-значимый препарат, произвести профилактический выбор препаратов, предназначенных для проведения терапии, определить переносимые сочетания препаратов при комплексном их применении.
Всего было обследовано более 800 пациентов с ЛН, у каждого пациента определялась переносимость не менее 10 препаратов (8000 обследованных препаратов). В реакциях использованы препараты из 40 классов химических соединений: антибиотики - 52%, местные анестетики - 25%, витамины - 14%, сульфаниламиды - 12%, пиразолоновые производные - 9%, средства для внутривенного наркоза - 7%, антигистаминные препараты - 5%, инсулины - 6%, глюкокортикоиды - 5%, сердечно-сосудистые средства - 4%, психотропные средства - 3%, и др.
Результаты исследования показали, что точность способа составляет 97%. Это означает, что в 97% случаев профилактически отобранные препараты не вызывали осложнений при проведении последующей терапии. В 80% случаев ретроспективно был определен этиологически значимый препарат или сочетания различных препаратов.
Применение неразрешенных препаратов приводило к развитию нежелательных реакций (таких случаев было зарегистрировано 9).
Таким образом, предлагаемый способ диагностики лекарственной непереносимости in vitro является универсальным, интегральным, позволяющим определить непереносимые препараты до лечения и эффекты их комбинированного, сочетанного действия. Он является малозатратным, экономически выгоден. Доступен, надежен и может выполняться в условиях любых медицинских учреждений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ СЕНСИБИЛИЗАЦИИ К ЛЕКАРСТВЕННЫМ АЛЛЕРГЕНАМ | 1995 |
|
RU2143696C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНДИВИДУАЛЬНОЙ ДОЗЫ АЛЛЕРГЕНА ДЛЯ ПРОВЕДЕНИЯ АЛЛЕРГОПРОБЫ IN VITRO | 2011 |
|
RU2480750C1 |
| СПОСОБ ДИАГНОСТИКИ in vitro ПОВЫШЕННОЙ ЧУВСТВИТЕЛЬНОСТИ К ПСЕВДОАЛЛЕРГЕНАМ И ПОДБОРА ПРОТИВОАЛЛЕРГИЧЕСКИХ ПРЕПАРАТОВ | 2014 |
|
RU2575567C2 |
| Способ выявления у пациента аллергии на пыльцу берёзы | 2023 |
|
RU2826340C1 |
| Способ диагностики неиммунологической лекарственной непереносимости | 1989 |
|
SU1675771A1 |
| СПОСОБ ДИАГНОСТИКИ ПАТОЛОГИИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА БОЛЬНОГО | 1994 |
|
RU2098819C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СПЕЦИФИЧЕСКОЙ ГИПЕРЧУВСТВИТЕЛЬНОСТИ И ЕЕ ХАРАКТЕРА in vitro | 2005 |
|
RU2295726C2 |
| Способ определения формы бронхиальной астмы | 1990 |
|
SU1829009A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТЕПЕНИ РИСКА РАЗВИТИЯ ГЕМОЛИТИЧЕСКИХ ОСЛОЖНЕНИЙ ПОСЛЕ ОПЕРАЦИИ КОРОНАРНОГО ШУНТИРОВАНИЯ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2013 |
|
RU2542434C1 |
| СПОСОБ АЛЛЕРГОДИАГНОСТИКИ ПО ПОКАЗАТЕЛЯМ ХЕМИЛЮМИНЕСЦЕНТНОГО СВЕЧЕНИЯ НЕЙТРОФИЛОВ | 2004 |
|
RU2289138C2 |

Изобретение относится к области медицины, а именно к лабораторной диагностике. Способ диагностики лекарственной непереносимости отдельных препаратов или смесей осуществляют путем оценки степени стойкости эритроцитов при воздействии препаратов in vitro в низких молярных концентрациях (10-6 М/л), воздействующих на плазматическую мембрану эритроцитов, помещенных в гипотоническую среду. Изобретение направлено на создание универсального, интегрального и надежного способа, позволяющего определить переносимые препараты и их сочетания для проведения последующей терапии, а также определить причинно-значимый препарат, вызвавший ту или иную побочную реакцию. 3 ил., 1 табл.
Способ диагностики лекарственной непереносимости отдельных лекарственных препаратов или смесей лекарственных препаратов, характеризующийся тем, что включает следующие этапы: отбирают образец крови у пациента и разводят указанный образец физиологическим раствором в соотношении 1:1000; добавляют лекарственный препарат или смесь лекарственных препаратов, подлежащих исследованию, в концентрации 10-6 М/л к разведенному образцу крови; термостатируют смесь образца крови и лекарственного препарата или смесь лекарственных препаратов в течение 10 мин при 24°С; вводят гемолизирующий раствор с концентрацией HCl 0,004 N к термостатированной смеси образца крови и лекарственного препарата или смеси лекарственных препаратов; оценивают стойкость эритроцитов посредством фотометрирования указанной смеси образца крови и лекарственного препарата или смеси лекарственных препаратов при длине волны 670 нм с момента введения гемолизирующего раствора до завершения гемолиза, причем снижение стойкости эритроцитов на 10% свидетельствует о непереносимости указанным пациентом указанного лекарственного препарата или смеси лекарственных препаратов, при этом в качестве контроля используется образец крови указанного пациента, разведенный физиологическим раствором.
| СПОСОБ ДИАГНОСТИКИ ЛЕКАРСТВЕННОЙ НЕПЕРЕНОСИМОСТИ У БОЛЬНЫХ С РАЗЛИЧНОЙ ФОРМОЙ АЛЛЕРГИИ | 1992 |
|
RU2070322C1 |
| RU 2155963 C1, 10.02.2005 | |||
| US 4812402 А, 14.03.1989 | |||
| УСТРОЙСТВО ДЛЯ БЕССТУПЕНЧАТОГО РЕГУЛИРОВАНИЯ СКОРОСТЕЙ РАБОЧИХ ОРГАНОВ ГИДРАВЛИЧЕСКИХ ПРЕССОВ | 1949 |
|
SU85362A1 |
| ЦЕНТРОБЕЖНО-ВИХРЕВАЯ МЕЛЬНИЦА | 0 |
|
SU349412A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОВЕРХНОСТИ РАЗДЕЛА ФАЗ | 0 |
|
SU213409A1 |
| ТЕРСКОВ И.Ф | |||
| и др | |||
| Метод химических (кислотных) эритрограмм, Биофизика, 1957, т.2, с.259-266 | |||
| БАДИНА А.К | |||
| Диагностика лекарственной непереносимости, Клиническая медицина, 1990, №7, с.78-80. | |||
Авторы
Даты
2007-01-27—Публикация
2003-04-16—Подача