Изобретение относится к медицине, а именно к фармации и биотехнологии, и может быть использовано для получения лекарственных средств с противовоспалительным, иммуномодулирующим и ранозаживляющим свойствами на основе культур клеток.
Известен способ получения аллотрансплантата для восстановления кожных покровов путем выращивания и последующего использования культуры аллогенных диплоидных эмбриональных фибробластов (RU 2023424). В данном методе используется культура аллогенных диплоидных фибробластов, получаемая из дермы в постнатальном периоде или из эмбрионов и плодов человека. Доказана высокая эффективность клинического применения указанного способа для лечения ожоговых ран в качестве самостоятельной терапии и для подготовки ран к аутодермопластике (А.А.Алексеев, А.Ю.Яшин. Комбинированная аутодермопластика с трансплантацией культивированных фибробластов при обширных глубоких ожогах: клинические результаты и перспективы // Междунар. симп. «Новые методы лечения ожогов с использованием культивированных клеток кожи» (30-31 мая 1996 г., г.Тула). - Тула, 1996. - С.1-3; Алексеев, А.А. Современные методы лечения ожогов и ожоговой болезни / А.А.Алексеев // Комбустиология (электронный журнал). - 2000. - №1; 60. Туманов В.П. Морфологический анализ клеточного состава ожоговой раны при трансплантации культивированных аллофибробластов // II Междунар. симп. «Новые методы лечения ожогов с использованием культивированных клеток кожи» (май 1998 г., г.Саратов). Саратов: Сарат. ун-т, 1998. - С.40-42).
Наиболее близким является решение по использованию в качестве действующего вещества лекарственного средства «Культура клеток диплоидных человека для заместительной терапии» (ФСП 42-0393252302, Регистрационное удостоверение Р №001402/01-2002 от 23.05.2002 г.), которое получают путем механической и ферментативной дезагрегации фрагментов эмбриона человека.
Однако использование трансплантации АДФ в целом и вышеуказанного лекарственного средства, в частности, требует для своего применения определенных условий со стороны участка повреждения, а именно санации раны от бактериальной флоры, купирования активного воспалительного процесса (Теоретические и практические аспекты использования культивированных фибробластов при восстановлении кожных покровов / Д.С.Саркисов, В.Д.Федоров, Е.В.Глущенко и др. // Вести. Рос. АН. - 1994. - №6. - С.6-11). Кроме того, получение достаточного для закрытия обширного участка повреждения количества фибробластов связано со значительными финансовыми затратами, требует дополнительного использования подложек для выращивания клеток, соответствующих определенным требованиям, предъявляемым к биологическим покрытиям, и при этом нетоксичных для клеток и выдерживающих ферментативное воздействие среды в процессе культивирования. Еще одним фактором, ограничивающим возможность использования АДФ и «Культуры клеток диплоидных человека для заместительной терапии», является невозможность их длительного хранения и жесткие ограничения по условиям транспортировки.
В связи с этим задачей изобретения является получение нового биологически активного вещества, содержащего комплекс гуморальных факторов АДФ, для создания на его основе лекарственных средств, а также разработка способа его получения. Вещество должно обладать противовоспалительными, иммуномодулирующими и ранозаживляющими свойствами, иметь меньше ограничений в применении, в условиях хранения и транспортировки и быть дешевле в получении по сравнению с клеточной культурой.
Поставленная задача достигается использованием в качестве указанного вещества супернатанта культуры АДФ, представляющего собой кондиционированную ими среду культивирования. Для получения культуры АДФ используется способ бесферментативной дезагрегации фрагментов донорских тканей.
Изобретение поясняется следующими таблицами и фигурами:
- на табл.1 - показатели функциональной активности нейтрофилов in vitro;
- на табл.2 - показатели продукции цитокинов мононуклеарами периферической крови здоровых доноров медиана, 1-й и 3-й квартили;
- на фиг.1 - влияние супернатантов АДФ на адгезию нейтрофилов к пластику;
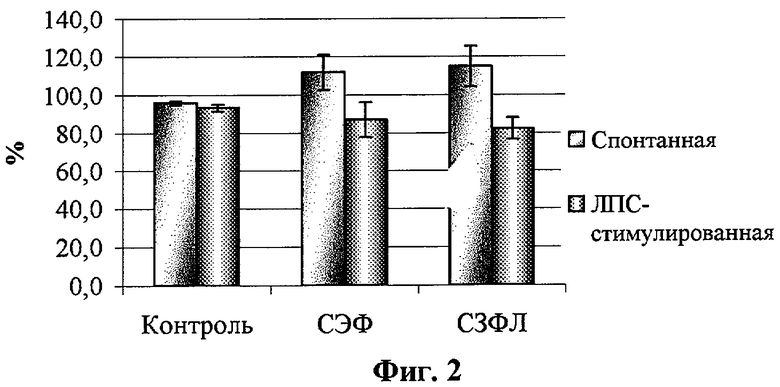
- на фиг.2 - влияние супернатантов АДФ на активность миелопероксидазы нейтрофилов in vitro;
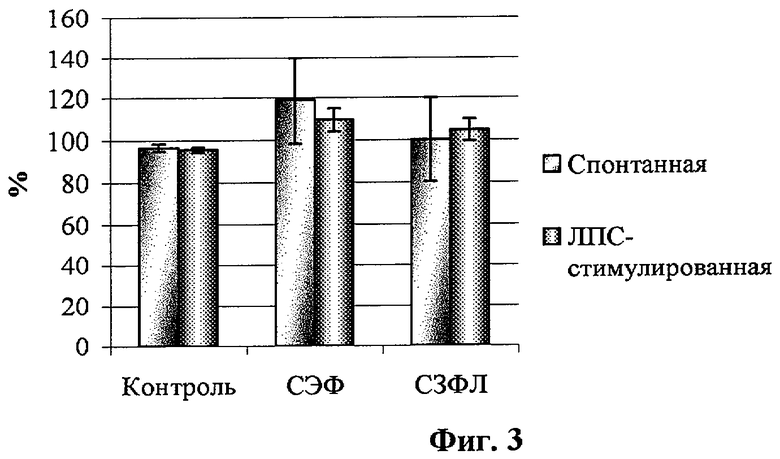
- на фиг.3 - влияние супернатантов АДФ на активность кислой фосфатазы нейтрофилов in vitro;
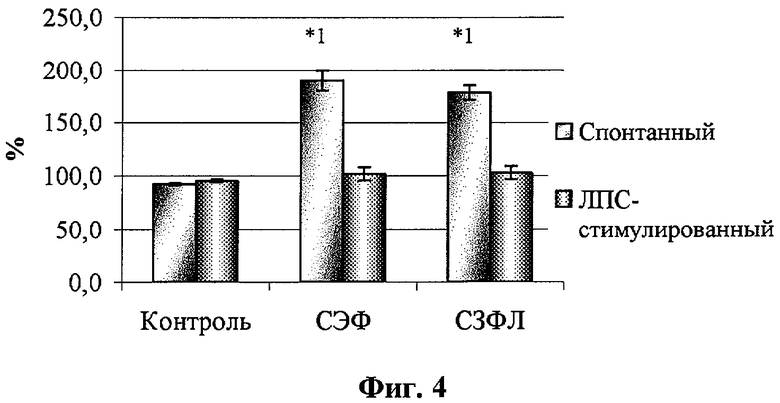
- на фиг.4 - влияние супернатантов АДФ на показатели НСТ-теста нейтрофилов in vitro;
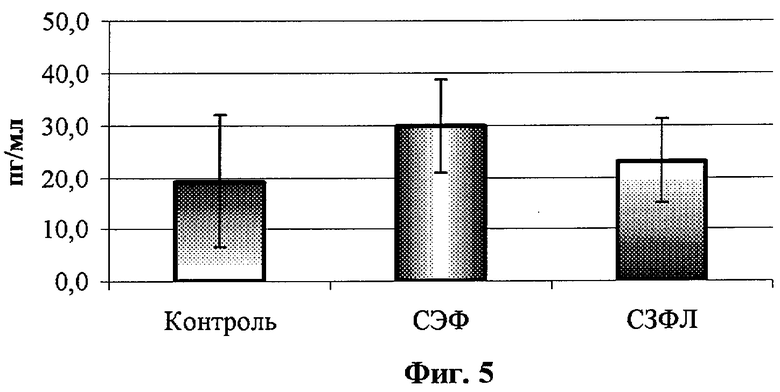
- на фиг.5 - влияние супернатантов АДФ на спонтанную продукцию ФНО-α мононуклеарами периферической крови здоровых доноров;
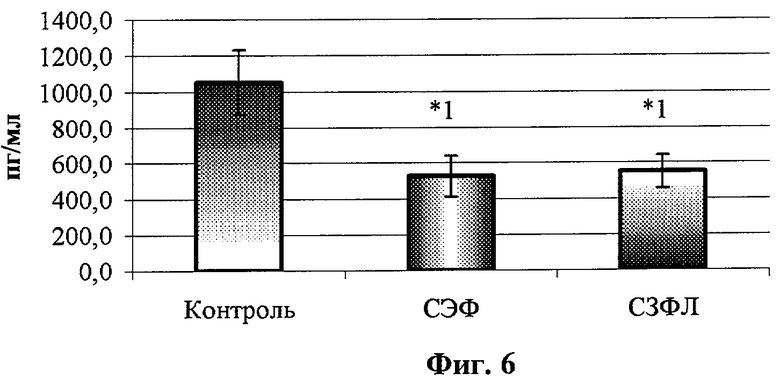
- на фиг.6 - влияние супернатантов АДФ на ЛПС-стимулированную продукцию ФНО-α мононуклеарами периферической крови здоровых доноров;
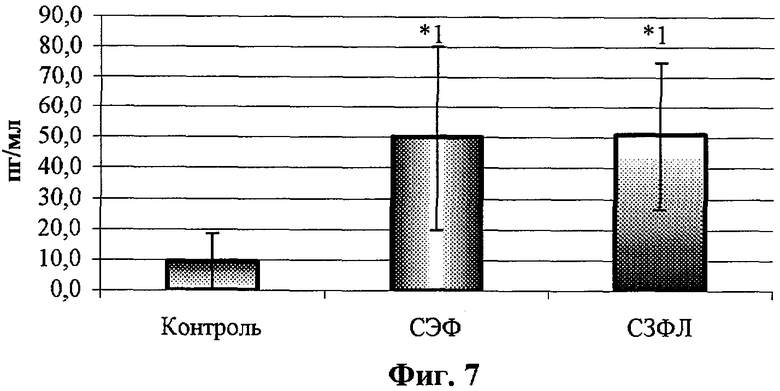
- на фиг.7 - влияние супернатантов АДФ на спонтанную продукцию ИЛ-1β мононуклеарами периферической крови здоровых доноров;
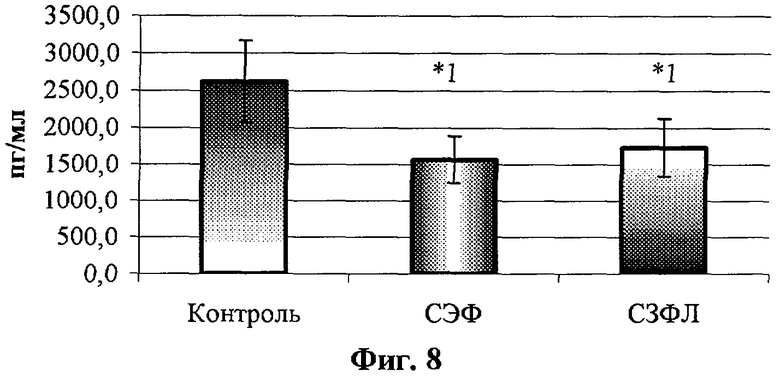
- на фиг.8 - влияние супернатантов АДФ на ЛПС-стимулированную продукцию ИЛ-1β мононуклеарами периферической крови здоровых доноров;
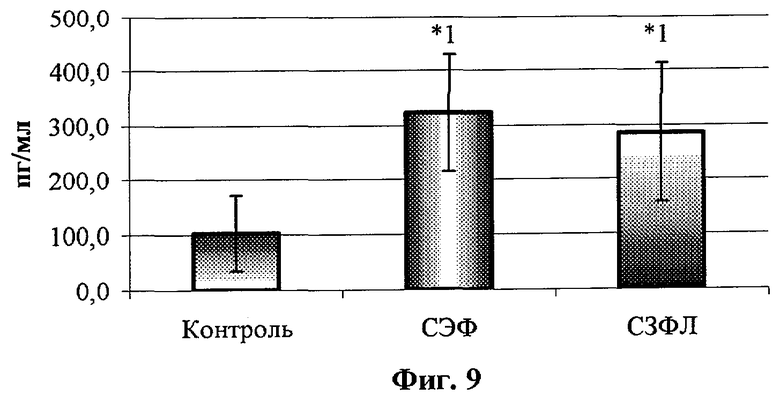
- на фиг.9 - влияние супернатантов АДФ на спонтанную продукцию раИЛ-1 мононуклеарами периферической крови здоровых доноров;
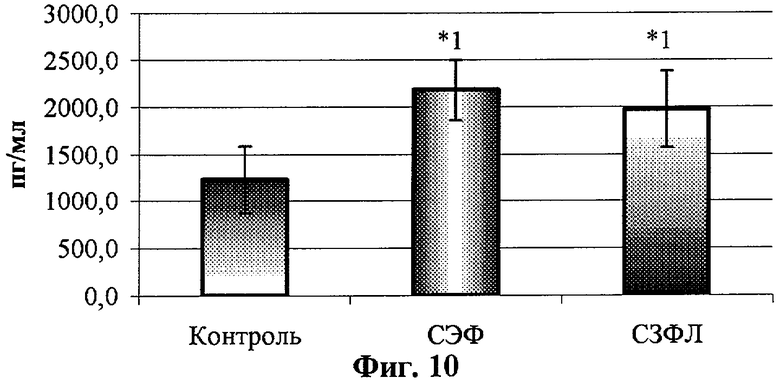
- на фиг.10 - влияние супернатантов АДФ на ЛПС-стимулированную продукцию раИЛ-1 мононуклеарами периферической крови здоровых доноров.
На всех фигурах и во всех таблицах: *1 - р<0,05 по сравнению с контролем. Для статобработки использовали дисперсионный анализ и критерий Ньюмена-Кейлса.
Способ осуществляется следующим образом.
Перевиваемые линии АДФ получали оригинальным бесферментативным методом, отличающимся от общепринятого отказом от использования протеолитических ферментов (трипсин, коллагеназа, террилитин и др.). Кусочки тканей (абортный материал, кусочки дермы, костный мозг, легких) подвергали механической дезагрегации до фрагментов размером 0,1-0,2 мм3, добавляли питательную среду 199, дополненную 10% сыворотки крови крупного рогатого скота, - для эмбриональных и фетальных тканей, или питательную среду RPMI 1640, дополненную 20% сыворотки эмбрионов коров, - для постнатального материала. Фрагменты тканей ресуспендировали в указанной среде, вносили в культуральные пластиковые флаконы и культивировали во влажной атмосфере с 5% СО2. В течение 1-3 суток происходила миграция фибробластов из тканевых фрагментов и прикрепление к дну культуральных флаконов. После этого фрагменты тканей со средой из флаконов удаляли, а к прикрепленным клетками добавляли свежую среду, соответствующую степени зрелости их источника. После формирования на дне культуральных флаконов монослоя АДФ отработанную питательную среду удаляли, к клеткам добавляли бессывороточную среду 199 и вновь культивировали в течение 24 ч в стандартных условиях. Через сутки кондиционированную АДФ среду сливали и проверяли в последующих экспериментах на биологическую активность, а клеточный монослой пересевали на новые флаконы со сменой среды и контролем бактериологической чистоты и кариотипа клеток.
Предлагаемый способ бесферментативного получения культур клеток позволяет обеспечить минимальное повреждение клеток и снизить экономические затраты на начальном этапе.
Биологическая активность вещества иллюстрирована в нижеприведенных экспериментах.
Пример 1. Влияние супернатантов АДФ на функциональную активность Нф периферической крови здоровых доноров in vitro.
В качестве супернатантов использовали кондиционированную в течение 24 ч эмбриональными (СЭФ) или зрелыми легочными (СЗФЛ) фибробластами среду 199. МНК и нейтрофилы (Нф) получали из венозной крови здоровых добровольцев общепринятым методом выделения на двойном градиенте плотности фиколл-гипак 1,077 и 1,114. После отмывки Нф ресуспендировали в бессывороточной среде 199 и вносили в лунки 96-луночного планшета в конечной концентрации 2×105/лунку. К МНК добавляли суточный СЭФ и СЗФЛ в конечной концентрации 25%, в контрольные лунки добавляли аналогичный объем бессывороточной среды 199. Клетки инкубировали в течение 2 ч в термостате при +37°С, по окончании инкубации трижды отмывали от неприкрепившихся клеток подогретым до +37°С фосфатно-солевым буфером. Дальнейшие эксперименты проводили по методикам, описанным Р.М.Хаитовым и соавт. (Экологическая иммунология / Р.М.Хаитов, Б.В.Пинегин, Х.И.Истамов. - М.: ВНИРО, 1995. - 219 с.).
Показатели активности нейтрофилов представлены в табл. 1 и на фиг.1-4.
Пример 2. Влияние супернатантов АДФ на продукцию ФНО-α и ИЛ-1β мононуклеарными клетками (МНК) периферической крови здоровых доноров in vitro.
После отмывки МНК ресуспендировали в полной питательной среде RPMI-1640 с добавлением 5% эмбриональной телячьей сыворотки и вносили в лунки 24-луночного планшета в конечной концентрации 1×106/лунку. К МНК добавляли суточный СЭФ и СЗФЛ в конечной концентрации 25%, в контрольные лунки добавляли аналогичный объем бессывороточной среды 199. В часть лунок вносили ЛПС в концентрации 10 мкг/лунку. Клетки инкубировали в течение суток в СО2-инкубаторе и по окончании инкубации оценивали концентрацию ФНОα и ИЛ-1β в твердофазном ИФА с использованием тест-систем фирмы «Протеиновый контур» (Санкт-Петербург, Россия). Полученные результаты представлены в табл.1 и на фиг.1-4. Как видно из фиг.5 и 6 и табл.2, СЭФ и СЗФЛ статистически значимо стимулируют спонтанную продукцию ФНО-α, однако данный эффект не имеет клинического значения, поскольку концентрации ФНО-α сопоставимы с нормальным содержанием данного цитокина в сыворотке крови здорового человека. Аналогичный, статистически значимый эффект СЭФ и СЗФЛ оказывают и на спонтанную продукцию ИЛ-1β (табл.2 и фиг.7 и 8). При стимуляции МНК с помощью ЛПС отмечено значительное статистически значимое ингибирующее влияние обоих супернатантов на продукции провоспалительных цитокинов ФНО-α и ИЛ-1β.
Пример 3. Влияние супернатантов АДФ на продукцию рецепторного антагониста ИЛ-1 (раИЛ-1) МНК периферической крови здоровых доноров in vitro.
Общая схема опытов идентична описанной для исследования продукции ФНО-α и ИЛ-1β, за исключением тест-систем для определения концентрации раИЛ-1 («Цитокин», Санкт-Петербург, Россия). Полученные результаты представлены в табл. 2 и на фиг.9 и 10. Видно, что супернатанты АДФ статистически значимо усиливали как спонтанную, так и ЛПС-стимулированную продукцию МНК доноров этого важного противовоспалительного цитокина.
Таким образом, супернатанты АДФ in vitro оказывали противовоспалительное влияние, выражавшееся в подавлении продукции провоспалительных цитокинов аллогенными мононуклеарными клетками в условиях стимуляции липополисахаридом, подавление адгезионной способности аллогенных нейтрофилов. При этом отмечается стимуляция продукции раИЛ-1 мононуклеарами, особенно в условиях индукции липополисахаридом, и повышение активности факторов бактерицидности нейтрофилов.
Пример 4. Влияние супернатантов АДФ на сроки эпителизации экспериментальной ожоговой раны (ЭОР) у крыс.
Под эфирным наркозом 10 крысам линии Вистар раскаленным до 200°С электродом площадью 1 см2 путем контактного воздействия в течение 2 с наносили 3 экспериментальных ожоговых раны (ЭОР) на область спины. На каждую из ран накладывали стерильную салфетку, пропитанную раствором 0,05% фурацилина (контроль), СЭФ или СЗФЛ, которые фиксировали лейкопластырем. На шею крысы фиксировали пластиковый воротник и каждую крысу помещали в отдельную клетку для исключения самостоятельного и взаимного повреждения наклеек. Под эфирным наркозом ежедневно в течение 21 дня производили перевязку со сменой салфеток с супернатантами АДФ и раствором антисептика. При формировании струпа на ране во время перевязки его тангенциально иссекали. За указанный период отмечена полная эпителизация ЭОР, леченных СЭФ, - у 8 крыс, леченных СЗФЛ - у 7 крыс, леченных раствором фурацилина - у 2 крыс.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МЕСТНОГО ЛЕЧЕНИЯ ЭРОЗИВНО-ЯЗВЕННЫХ ПОРАЖЕНИЙ КОЖИ И СЛИЗИСТЫХ | 2003 |
|
RU2250108C2 |
| СРЕДСТВО С РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ НА ОСНОВЕ СУПЕРНАТАНТА ЧЕЛОВЕЧЕСКИХ ФИБРОБЛАСТОВ | 2007 |
|
RU2369398C2 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 1998 |
|
RU2157269C2 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРИТОНИТА | 2000 |
|
RU2169570C1 |
| СРЕДСТВО НА ОСНОВЕ АРАБИНОГАЛАКТОУРОНАНОВ, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2024 |
|
RU2836422C1 |
| ПРОТИВОЭНТЕРОВИРУСНОЕ И ИММУНОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 2014 |
|
RU2554761C1 |
| СПОСОБ ОЦЕНКИ ИММУНОГЕННОСТИ ПРОТИВОБРУЦЕЛЛЕЗНЫХ ВАКЦИННЫХ ШТАММОВ | 2009 |
|
RU2419096C2 |
| СОВМЕСТНАЯ ДИФФЕРЕНЦИРОВКА МОНОЦИТОВ ОТ АЛЛОГЕННЫХ ДОНОРОВ | 2013 |
|
RU2668816C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩИМ И ГЕМОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2009 |
|
RU2414223C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТИМУЛИРОВАННЫХ ДЕНДРИТНЫХ КЛЕТОК ДЛЯ ИНДУКЦИИ ИММУННОГО ОТВЕТА ПРОТИВ ТУБЕРКУЛЕЗА ЧЕЛОВЕКА | 2009 |
|
RU2401664C1 |
Изобретение относится к медицине, в частности к фармации и биотехнологии, и может быть использовано для получения лекарственных средств с противовоспалительным, иммуномодулирующим и ранозаживляющим свойствами и касается нового биологически активного вещества, содержащего комплекс гуморальных факторов аллогенных диплоидных фибробластов (АДФ), и полученное механической дезагрегацией донорской ткани, добавлением питательной среды, культивированием во влажной атмосфере с 5% CO2 и отделением супернатанта. Изобретение обеспечивает уменьшение ограничения в применении и удешевление в получении. 2 табл., 10 ил.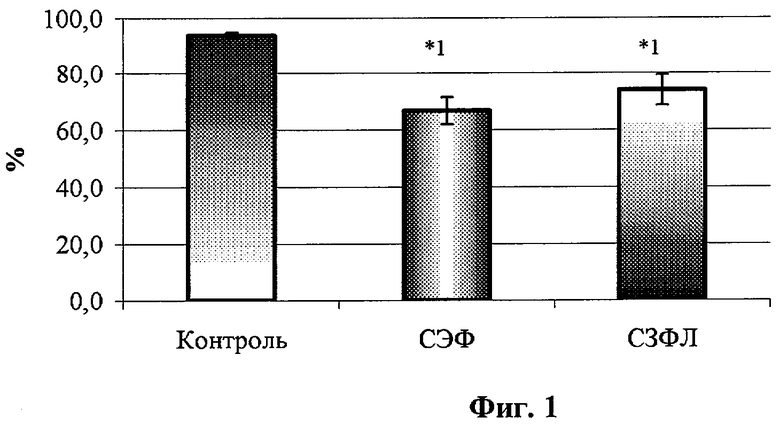
Вещество, обладающее противовоспалительной, иммуномодулирующей и ранозаживляющей активностью, характеризующееся тем, что содержит супернатант культуры аллогенных диплоидных фибробластов (АДФ), включающий комплекс гуморальных факторов, продуцируемых АДФ, и полученное механической дезагрегацией донорской ткани, добавлением питательной среды, культивированием во влажной атмосфере с 5% CO2 и отделением супернатанта.
| Приспособление для посадки выдувательных головок в конвейерных стеклодельных машин | 1931 |
|
SU29001A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КЛЕТОЧНОГО ТРАНСПЛАНТАТА ИЗ ФЕТАЛЬНЫХ ТКАНЕЙ | 2000 |
|
RU2160112C1 |
| JP 2004339107, 02.12.2004 | |||
| ПРИРОДНЫЕ ПРОТИВООПУХОЛЕВЫЕ ИЛИ ПРОТИВОВИРУСНЫЕ ВЕЩЕСТВА И ИХ ПРИМЕНЕНИЕ | 1998 |
|
RU2205010C2 |
| СПОСОБ ЛЕЧЕНИЯ РАНЫ | 1993 |
|
RU2023424C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНО-ДЕСТРУКТИВНЫХ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2002 |
|
RU2231986C1 |
Авторы
Даты
2007-06-10—Публикация
2005-01-31—Подача