Настоящее изобретение относится к псевдополиморфным формам (±)-1-(4-карбазолилокси)-3-[2-(2-метоксифенокси)этиламино]-2-пропанола (карведилола), а также к его оптически активным формам или фармацевтически приемлемым солям. Настоящее изобретение относится также к способам получения таких псевдополиморфных форм карведилола и к содержащим их фармацевтическим композициям.
Карведилол представляет собой β-блокатор неизбирательного типа действия, обладающий сосудорасширяющим свойством, которое обусловлено его антагонизмом в отношении α1-адренорецепторов. Кроме того, карведилол обладает также антиоксидантными свойствами. Карведилол является объектом заявки ЕР 0004920 и его можно получать согласно описанному в этой заявке способу.
Карведилол имеет хиральный центр и поэтому может существовать как в виде индивидуальных стереоизомеров, так и в рацемической форме. Как рацемат, так и стереоизомеры можно получать известными в данной области методами (ЕР-В-0127099).
В WO 99/05105 описана термодинамически стабильная модификация карведилола, которая имеет температуру плавления (tпл) 123-126°С (в настоящем описании обозначена как форма I карведилола), в отличие от формы карведилола, описанной в ЕР 0004920, которая имеет tпл 114-115°С (в настоящем описании обозначена как форма II карведилола).
При значениях рН, находящихся в фармацевтически приемлемом диапазоне 1-8, растворимость карведилола в водных средах составляет от приблизительно 1 до 100 мг на 100 мл (в зависимости от значения рН). Установлено, что это приводит к трудностям прежде всего при приготовлении высококонцентрированных композиций для парентерального введения, таких, например, как инъецируемые растворы, или других композиций, предназначенных для приготовления малообъемных лекарственных форм для глазного или перорального введения.
В случае перорального введения композиций карведилола с быстрым высвобождением, например поступающих в продажу композиций, доли поглощаемого карведилола составляют до 80%, причем значительная часть поглощенного карведилола очень быстро метаболизируется.
При исследовании поглощения карведилола в желудочно-кишечном тракте было установлено, что поглощение карведилола уменьшается по мере прохождения через желудочно-кишечный тракт и, например, в подвздошной кишке и ободочной кишке оно составляет только часть того поглощения, которое имеет место в желудке. Установлено, что это приводит к трудностям прежде всего при разработке форм типа "ретард", из которых высвобождение должно происходить в течение нескольких часов. Слабое поглощение, по-видимому, целиком или частично обусловлено уменьшением растворимости карведилола при увеличении значения рН. В очень кислых условиях (при значениях рН приблизительно 1-2) растворимость также может быть очень слабой.
Для увеличения поглощаемой доли, прежде всего в низших отделах кишечника, были проведены исследования с целью выявления адъювантов и соответственно разработки композиций, пригодных для повышения растворимости и/или скорости растворения карведилола.
В соответствии с этим одной из задач, положенных в основу изобретения, было повысить поглощение карведилола, прежде всего в случае перорального введения и прежде всего в низших отделах кишечника, с помощью агентов, которые можно применять в фармацевтике.
При создании изобретения неожиданно было установлено, что псевдополиморфные формы (±)-1-(4-карбазолилокси)-3-[2-(2-метоксифенокси)этиламино]-2-пропанола (карведилола), предлагаемые в настоящем изобретении, прежде всего гидраты карведилола, особенно полугидрат карведилола (в настоящем описании обозначен как форма IV карведилола), можно включать в высоких концентрациях в композицию, которая содержит дополнительно определенные выбранные адъюванты. Такие композиции, содержащие форму IV карведилола, характеризуются более высоким поглощением действующего вещества и, следовательно, улучшенной биологической доступностью по сравнению с формами I или II карведилола.
Таким образом, карведилол можно выделять в различных модификациях в зависимости от метода получения. Три полиморфные формы являются монотропными и различаются своими инфракрасными спектрами и спектрами дифракции рентгеновских лучей на порошке, и своими температурами плавления.
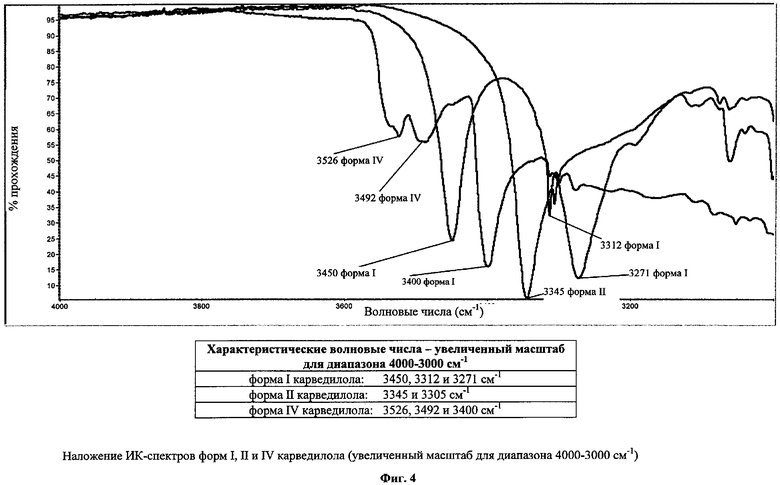
Один из предпочтительных вариантов осуществления настоящего изобретения относится к новой кристаллической модификации (форма IV) карведилола, практически не содержащей других физических форм, которая по данными измерений с помощью дифференциальной сканирующей калориметрии (ДСК) имеет температуру плавления приблизительно 94-96°С. ИК-спектр формы IV имеет большие отличия в концевом диапазоне колебаний (при волновых числах 3526, 3492 и 3400 см-1) от спектров форм I и II. На картине дифракции рентгеновских лучей на порошке формы IV карведилола имеются характеристические пики при 2θ=7, 0, 8, 3, 11, 5, 15, 7 и 17, 2.
В контексте настоящего описания понятие "псевдополиморфные формы" относится к гидратам и сольватам, предпочтительно к гидратам. Псевдополиморфные формы карведилола, такие как гидраты и сольваты, содержат различные количества воды или растворителей в кристаллической решетке.
Понятие "гидраты" включает соединения, содержащие различные количества воды в кристаллической решетке, такие как полугидраты, моногидраты, дигидраты, причем особенно предпочтительными являются полугидраты.
Понятие "фармацевтически приемлемые соли" карведилола включает соли щелочных металлов, такие как соли Na или К, соли щелочно-земельных металлов, такие как соли Са и Mg, а также соли органических или неорганических кислот, таких, например, как соляная кислота, бромистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота или толуолсульфоновая кислота, которые нетоксичны для живых организмов.
Для разделения рацематов можно использовать, например, винную кислоту, яблочную кислоту, камфорную кислоту или камфорсульфоновую кислоту.
Если в настоящем описании упоминается форма I, II и IV карведилола, практически не содержащая других физических форм, то это означает, что в композиции доля формы I, II и IV карведилола соответственно составляет по меньшей мере 75 мас.%, предпочтительно 90 мас.%, более предпочтительно 95 мас.%.
Псевдополиморфные формы карведилола, т.е. гидраты и сольваты, как правило, можно получать путем кристаллизации из растворителей, в которых растворим карведилол, например в спиртах, таких как метанол, этанол и изопропанол, ацетоне, ацетонитриле, хлороформе, диметилформамиде, диметилсульфоксиде, метиленхлориде или их смесях или смесях с водой.
Кроме того, кристаллическую форму IV карведилола можно получать путем выделения формы IV из отвержденного распылением карведилола, получение которого описано ниже, и последующей перекристаллизации в метаноле/воде. Так, форму IV карведилола сначала выделяют из отвержденного распылением продукта, полученного согласно методу, описанному в примере 4 WO 01/74357. Затем, используя форму II карведилола в качестве исходного продукта и внося затравку в виде формы IV карведилола, получают путем кристаллизации форму IV.
Следующим объектом настоящего изобретения являются фармацевтические композиции, включающие псевдополиморфную форму карведилола, прежде всего форму IV карведилола, практически не содержащую других физических форм карведилола, фармацевтически приемлемый носитель и/или адъювант и при необходимости другие действующие вещества. Такие композиции можно применять для лечения или профилактики заболеваний.
Соединения, предлагаемые в настоящем изобретении, можно вводить любым пригодным путем, предпочтительно в форме фармацевтической композиции, адаптированной к такому пути введения, и в дозе, эффективной для требуемого лечения. Соединения и композиции можно вводить, например, перорально, внутрисосудисто, внутрибрюшинно, подкожно, внутримышечно или местно. Предпочтительным является пероральный путь введения. Фармацевтическая композиция может находиться, например, в форме таблетки, капсулы, крема, мази, геля, лосьона, суспензии или жидкости. Фармацевтическую композицию предпочтительно приготавливают в виде стандартной дозы, содержащей конкретное количество действующего вещества. Примерами таких стандартных доз являются таблетки или капсулы.
Специалист в данной области легко может оценить терапевтически эффективные дозы соединений, предлагаемых в настоящем изобретении, которые требуются для предупреждения или прекращения развития медицинского состояния. Схему приема лекарственного средства при лечении болезненного состояния с помощью соединений и/или композиций, предлагаемых в настоящем изобретении, выбирают с учетом различных факторов, включая тип, возраст, вес, пол и медицинские состояния пациента, а также серьезность заболевания, и поэтому она может варьироваться в широких пределах. Соответствующая суточная доза для млекопитающего может варьироваться в широких пределах в зависимости от состояния пациента и других факторов. Однако можно применять дозу от приблизительно 0,01 до 100 мг/кг веса тела, в частности от приблизительно 0,05 до 3 мг/кг веса тела, соответственно от 0,01 до 10 мг/см2 кожи. Действующее вещество можно вводить также путем инъекции.
Для терапевтических целей соединения, предлагаемые в изобретении, как правило, объединяют с одним или несколькими адъювантами, пригодными для показанного пути введения. Для перорального введения соединение можно смешивать с лактозой, сахарозой, порошкообразным крахмалом, эфирами целлюлозы и алкановых кислот, алкиловым эфиром целлюлозы, тальком, стеариновой кислотой, стеаратом магния, оксидом магния, натриевыми и кальциевыми солями фосфорной и серной кислот, желатином, аравийской камедью, альгинатом натрия, поливинилпирролидоном и/или поливиниловым спиртом, и полученный продукт подвергать таблетированию или капсулированию для удобства введения. В альтернативном варианте соединение можно растворять в воде, полиэтиленгликоле, пропиленгликоле, этаноле, кукурузном масле, хлопковом масле, арахисовом масле, кунжутном масле, бензиловом спирте, хлориде натрия и/или различных буферах. Пригодными добавками при приготовлении мазей, кремов или гелей могут служить, например, парафин, вазелин, природные воски, крахмал, целлюлоза или полиэтиленгликоль (ПЭГ). В области фармацевтики широко известны другие адъюванты и пути введения.
Предпочтительные фармацевтические композиции, содержащие псевдополиморфную форму карведилола, прежде всего форму IV карведилола, можно получать с использованием определенных адъювантов, которые не обладают поверхностно-активными свойствами, таких, как полиэтиленгликоли (ПЭГ) или заменители сахара, а также неионогенных поверхностно-активных веществ, таких как полиоксиэтиленстеараты, например Myrj® 52, или сополимеры полиоксиэтилена и полиоксипропилена, например Pluronic® F 68.
Содержание гидрофильных полиоксиэтиленовых групп в указанных выше сополимерах полиоксиэтилена и полиоксипропилена предпочтительно составляет 70-90%. В наиболее предпочтительном варианте осуществления изобретения соотношение гидрофильных полиоксиэтиленовых групп и гидрофобных полиоксипропиленовых групп составляет приблизительно 80:20, а средняя молекулярная масса предпочтительно составляет приблизительно 8750.
Величина гидрофильно-липофильного баланса (ГЛБ) указанных выше полиоксиэтиленстеаратов предпочтительно составляет 10-20, предпочтительно 14-20, более предпочтительно 16-18.
Было установлено, что среди заменителей сахара наиболее предпочтительным является изомальт (гидрированная изомальтулоза), например Palatinit®. Palatinit® представляет собой гидрированную изомальтулозу, которая состоит из приблизительно равных частей дигидрата 1-O-α-D-глюкопиранозил-D-сорбита и дигидрата 1-О-α-D-глюкопиранозил-D-маннита.
Кроме того, при создании настоящего изобретения было установлено, что особенно предпочтительными являются полиэтиленгликоли с молекулярной массой 200-20000, предпочтительно 1000-20000, более предпочтительно 4000-10000, наиболее предпочтительно 6000-8000.
В предпочтительном варианте осуществления настоящего изобретения форму I, II или IV карведилола растворяют в неионогенном поверхностно-активном веществе, предпочтительно Pluronic® F 68, или в адъюванте, который не обладает поверхностно-активными свойствами, предпочтительно в полиэтиленгликоле 6000.
Так, форму I, II или IV карведилола можно растворять в полиэтиленгликоле 6000, который плавится при приблизительно 70°С. Таким путем можно получать высококонцентрированные композиции карведилола (до 500 мг/мл). Кроме того, для контроля скорости высвобождения действующего вещества можно вносить в смесь другие добавки, например производные целлюлозы, такие как гидроксипропилметилцеллюлозы или гидроксипропилцеллюлозы. Кроме того, композиции, предлагаемые в изобретении, могут содержать в качестве агента, препятствующего слипанию, высокодисперсный диоксид кремния.
В предпочтительном варианте осуществления изобретения содержание формы IV карведилола в композициях, предлагаемых в изобретении, составляет от 5 до 60 мас.%, предпочтительно от 5 до 50 мас.%, более предпочтительно от 10 до 40 мас.%, где величины в мас.% даны в пересчете на общую массу композиции (действующее вещество и адъювант).
В предпочтительном варианте осуществления изобретения адъюванты, предлагаемые в изобретении, имеют температуру плавления ниже 120°С, предпочтительно температуру плавления 30-80°С.
Указанные выше адъюванты можно применять индивидуально или в виде комбинации двух или большего количества адъювантов. Особенно предпочтительной является комбинация, включающая адъювант, не обладающий поверхностно-активными свойствами, предпочтительно полиэтиленгликоль, и неионогенное поверхностно-активное вещество, предпочтительно сополимер полиоксиэтилена и полиоксипропилена, например Pluronic® F 68, поскольку добавление поверхностно-активных веществ может ускорять высвобождение действующего вещества из композиции.
Было установлено, что наиболее предпочтительными являются композиции на основе формы IV карведилола, которые содержат в качестве адъювантов полиэтиленгликоль, предпочтительно полиэтиленгликоль 6000, а также 0,1-50%, предпочтительно 0,1-10%, сополимеров полиоксиэтилена и полиоксипропилена, например Pluronic® F 68.
В конкретном варианте осуществления настоящего изобретения соотношение вышеуказанного адъюванта, не обладающего поверхностно-активными свойствами, например полиэтиленгликоля 6000, и поверхностно-активного адъюванта, например Pluronic® F 68, составляет от 1000:1 до 1:1, предпочтительно от 100:1 до 10:1.
Композиции, содержащие форму IV карведилола, предлагаемые в изобретении, и полученные на их основе лекарственные средства могут содержать другие добавки, такие, например, как связующие вещества, пластификаторы, разбавители, носители, вещества, улучшающие скольжение, антистатики, антиоксиданты, адсорбенты, агенты, способствующие разделению, разрыхлители, лак для драже, антивспениватели, пленкообразующие вещества, эмульгаторы и наполнители.
Вышеуказанные добавки могут представлять собой органические или неорганические субстанции, например воду, сахар, соли, кислоты, основания, спирты, органические полимеры и т.п. Предпочтительными добавками являются лактоза, сахароза, таблеттоза, натрийкарбоксиметилкрахмал, стеарат магния, различные типы целлюлоз и замещенных целлюлоз, такие, например, как метилгидроксипропилцеллюлоза, полимерные соединения на основе целлюлозы, высокодисперсный диоксид кремния, кукурузный крахмал, тальк, различные полимерные соединения на основе поливинилпирролидона, а также поливиниловые спирты и их производные. Необходимым условием является то, чтобы все применяемые в процессе производства добавки были нетоксичными и предпочтительно не изменяли биологическую доступность действующего вещества.
В предпочтительном варианте осуществления изобретения композиции, предлагаемые в изобретении, содержат форму IV карведилола в практически чистом виде, полиэтиленгликоль, сополимер полиоксиэтилена и полиоксипропилена, а также высокодисперсный диоксид кремния. В наиболее предпочтительном варианте осуществления изобретения композиции, предлагаемые в изобретении, содержат 10-20 мас.% формы IV карведилола, 65-85 мас.% полиэтиленгликоля, 1-10 мас.% сополимера полиоксиэтилена и полиоксипропилена и 0,1-10 мас.% высокодисперсного диоксида кремния, где проценты приведены в пересчете на суммарную массу четырех указанных субстанций вне зависимости от того, присутствуют ли в композиции другие адъюванты.
Композиции, содержащие форму IV карведилола в адъювантах, можно получать путем растворения формы I, II или IV карведилола в расплавленных адъювантах и последующего быстрого отверждения расплава адъювантов, содержащих растворенное действующее вещество, например, путем отверждения распылением. В альтернативном варианте композиции, содержащие форму IV карведилола в адъювантах, можно получать путем растворения полимерного носителя (ПЭГ) в соответствующем органическом растворителе или смеси растворителей (например, этаноле, метаноле, изопропаноле, ацетонитриле, ацетоне или их смеси и/или воде), и последующего добавления формы I, II или IV карведилола. После этого растворитель удаляют сушкой распылением. Хранение в течение приблизительно 1-2 месяцев при комнатной температуре приводит к получению композиции, содержащей в качестве действующего вещества практически чистую форму IV карведилола. В зависимости от условий, используемых на стадии сушки распылением, образование формы IV может происходить в течение периода времени от одной недели до нескольких месяцев.
Настоящее изобретение относится также к способу получения композиций, содержащих форму IV карведилола, который предусматривает смешение карведилола с расплавленными гидрофильными адъювантами, такими, например, как полиэтиленгликоль, и/или поверхностно-активными веществами, такими, например, как Pluronic®F 68. В альтернативном варианте действующее вещество и адъюванты можно смешивать и затем расплавлять. В предпочтительном варианте осуществления изобретения полученную таким путем композицию затем отверждают распылением.
В случае сушки распылением продукт, подлежащий сушке, распыляют в виде раствора или суспензии в верхней части широкого цилиндрического контейнера с помощью распылительного устройства, получая туман, состоящий из капелек. Образовавшийся состоящий из капель туман смешивают с горячим воздухом (предпочтительно имеющим температуру >100°С) или инертным газом, который подают в сушилку вокруг области, где осуществляют распыление. Возникающие пары растворителя поглощаются высушивающим воздухом и удаляются, а образующийся при этом порошок удаляют из контейнера с помощью сепаратора.
В случае отверждения распылением продукт, предназначенный для отверждения, распыляют в виде расплава в верхней части широкого цилиндрического контейнера с помощью снабженного нагревательным устройством распылительного приспособления, получая состоящий из капель туман. Образовавшийся состоящий из капель туман смешивают с охлажденным воздухом (предпочтительно имеющим температуру <25°С), который подают в сушилку вокруг области, где осуществляют распыление. Тепло, которое выделяется при отверждении, поглощается воздухом и удаляется, а образующийся при этом отвердевший порошок удаляют из контейнера с помощью сепаратора. В качестве распылительных приспособлений можно применять снабженные нагревательным устройством форсунки, работающие под давлением (например, центробежную форсунку, работающую под давлением), пневматические форсунки (двойные/тройные форсунки) или центробежные распылители.
Полученные композиции, содержащие форму IV карведилола, можно успешно применять различным образом в области фармацевтики. Так, например, такие композиции можно подвергать дальнейшей обработке, получая формы введения с быстрым высвобождением, такие, например, как таблетки, филмтаблетки, капсулы, гранулы, пеллеты и т.д., обладающие повышенной способностью к поглощению. Это позволяет в определенных обстоятельствах уменьшать величины доз в композиции по сравнению с дозами, необходимыми в случае применения обычных пероральных лекарственных средств с быстрым высвобождением, которые получают с использованием кристаллической формы II карведилола.
Полученные композиции, содержащие форму IV карведилола, наиболее предпочтительно можно применять также для приготовления лекарственных средств, имеющих модифицированные характеристики высвобождения. В контексте настоящего описания понятие "модифицированная характеристика высвобождения" означает, например, что 95% действующего вещества высвобождается по истечении периода времени, превышающего 2 ч, предпочтительно через 2-24 ч, или что высвобождение зависит от значения рН, в результате чего происходит задержка начала высвобождения. Для этой цели композиции, содержащие карведилол, можно подвергать обработке индивидуально или в сочетании с любыми обычными фармацевтическими лекарственными средствами с модифицированным высвобождением, предназначенными для перорального введения.
Примерами лекарственных средств с модифицированными характеристиками высвобождения являются филмтаблетки, которые являются устойчивыми к действию желудочных соков, или формы типа "ретард", такие, например, как гидроколлоидные матриксы или лекарственные средства аналогичного типа, из которых действующее вещество высвобождается в результате эрозии или диффузии. Композиции, предлагаемые в изобретении, можно подвергать обработке путем введения дополнительных адъювантов или пленочных покрытий или путем их включения в обычные фармацевтические системы с соответствующим профилем высвобождения, получая композиции с модифицированным высвобождением действующего вещества. Так, композиции, предлагаемые в изобретении, можно включать, например, в гидроколлоидные матриксные системы, прежде всего в системы на основе производных целлюлозы, таких как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, метилцеллюлоза, или производные полиакрилата, такие, например, как Eudragit RL. Вышеуказанные матриксы могут содержать дополнительно или в виде альтернативного варианта вещество, образующее гидроколлоидный матрикс, степень набухания которого зависит от значения рН, такое, например, как альгинат натрия или натрийкарбоксиметилцеллюлоза. Путем добавления такого адъюванта можно достигать целенаправленного высвобождения, приспособленного к конкретным условиям. Таким образом, применение композиций, предлагаемых в изобретении, позволяет существенно увеличить уровень поглощения по сравнению с уровнем поглощения кристаллической формы IV карведилола, используемого в качестве действующего вещества.
Так, отвержденные распылением композиции, предлагаемые в изобретении, которые содержат карведилол, предпочтительно композиции, содержащие Pluronic® F 68, полиэтиленгликоль 6000, высокодисперсный диоксид кремния и карведилол (предпочтительно полученные согласно методу, описанному в примере 4), можно спрессовывать в таблетки, например, путем непосредственного прессования, грануляции и уплотнения вместе с веществами, образующими гидрофильный матрикс, которые позволяют осуществлять контролируемое высвобождение, такими, например, как гидроксипропилметилцеллюлозы 2208, имеющие среднее значение вязкости приблизительно 100 мПа·с (Methocel® K100 LV-Premium), и гидроксипропилметилцеллюлозы 2208, имеющие среднее значение вязкости приблизительно 4000 мПа·с (Methocel® K4M-Premium), и с веществами, улучшающими скольжение, или агентами, препятствующими слипанию, такими, например, как стеарат магния и микрокристаллические целлюлозы (Avicel® РН102). Кроме того, на таблетки можно наносить покрытие с помощью обычных лаков, таких, например, как Opadryl® II White Y-30-18037 и Opadryl® II Clear YS-1-7006.
Фармацевтические композиции, предлагаемые в изобретении, можно использовать для получения обычных фармацевтических форм введения, предпочтительно форм для перорального введения, предназначенных для лечения и/или профилактики сердечных заболеваний и нарушений кровообращения, таких, например, как гипертензия, сердечная недостаточность и стенокардия.
Дозы, в которых вводят фармацевтические композиции, предлагаемые в изобретении, зависят от возраста и индивидуального состояния пациентов и пути введения. В целом для перорального введения можно применять однократные дозы карведилола, составляющие приблизительно 0,1-50 мг в день. Для этого используют композиции, содержащие в качестве действующего вещества приблизительно 1-50 мг карведилола.
Таким образом, объектом настоящего изобретения является также способ лечения заболеваний, таких как гипертензия, сердечная недостаточность или стенокардия, который предусматривает введение лекарственных средств, содержащих указанные выше фармацевтические композиции.
Характеристики формы IV карведилола
Дифференциальная сканирующая калориметрия (ДСК)
Анализ методом ДСК (дифференциальная сканирующая калориметрия) проводили с использованием системы типа Mettler ТА 8000, снабженной DSC 821е, автоматизированным устройством для образцов и внутренним охладителем. В качестве продувочного газа (скорость потока 150 мл/мин) и осушенного газа (скорость потока 150 мл/мин) использовали осушенный азот. Скорости сканирования составляли 5°С/мин и 1°С/мин (циклы нагрева и охлаждения), а масса образца составляла от 1 до 12 мг. Применяли герметически запечатываемые алюминиевые баллоны объемом 40 мкл, герметически закрытые перфорированной крышкой. Перед измерениями крышку автоматически прокалывали, получая точечные отверстия размером приблизительно 1,5 мм. Все измерения проводили с использованием проколотых крышек. Калибровку температуры теплоты плавления проводили с использованием индия с чистотой 99,999% (фирма Mettler-Toledo AG (Швейцария); СН-Грейфензее); tпл 156,6°С; теплота плавления 28,45 Дж/г.
Измеренная температура плавления формы IV карведилола составляла приблизительно 94-96°С. Теплота плавления формы IV карведилола составляла ΔHf 144-154 Дж/г, что для полугидрата (молекулярная масса: 406,5+9) соответствует 60-64 кДж/моль.
ТГА (термический гравиметрический анализ) проводили с использованием системы типа Mettler ТА 8000, снабженной TGA 851е и автоматизированным устройством для образцов и внутренним охладителем. В качестве продувочного газа (скорость потока 50 мл/мин) и осушенного газа (скорость потока 20 мл/мин) использовали осушенный азот. Скорости сканирования составляли 5°С/мин и 1°С/мин (циклы нагрева и охлаждения), а масса образца составляла от 10 до 50 мг. Применяли герметически запечатываемые алюминиевые баллоны объемом 100 мкл, герметически закрытые перфорированной крышкой. Перед измерениями крышку автоматически прокалывали, получая точечные отверстия размером приблизительно 1,5 мм. Герметически закрытые баллоны предотвращали любой обмен между растворителями и атмосферной влагой в течение периода ожидания при нахождении в автоматизированном устройстве для образцов.
Установлено, что потеря массы (скачок массы) в интервале температур от 50 до 140°С составляла приблизительно 2,2 мас.%, что соответствует 1/2 моля воды для молекулярной массы полугидрата.
ФТ-ИК (ИК-спектрометрия с фурье-преобразованием) и дифрактометрия в рентгеновских лучах.
ИК-спектр образца получали на основе измерения коэффициента прохождения с помощью ФТ-ИК-спектрометра с использованием пленки суспензии Nujol, содержащей приблизительно 15 мг образца и приблизительно 15 мг Nujol, которая находилась между двумя пластинами хлорида натрия. Использовали спектрометр типа Nicolet 20SXB или эквивалентный спектрометр (разрешение 2 см-1, 32 или 64 совместных сканирований, МСТ-детектор).
Дифракцию рентгеновских лучей на порошке изучали, измеряя коэффициент прохождения с помощью рентгеновского дифрактометра Stoe типа STADIP, снабженного источником излучения CuКα1 Ge-монохроматором, в процессе эксперимента осуществляли вращение образца, используя датчик положения (ДП), при этом углы изменяли в диапазоне от 2° до 32° (2θ) с шагом 0,5° (2θ), время измерения составляло 40 с на шаг.
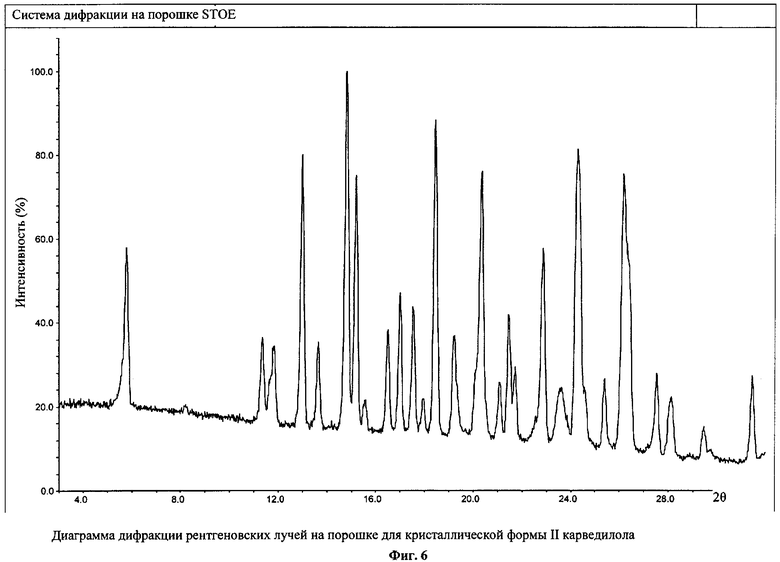
Картина дифракции рентгеновских лучей на порошке формы IV имеет характеристические пики при 2θ=7,0°, 8,3° (подразделяется на два пика: при 8,235° и 8,383°), 11,5°, 15,7° и 17,2° (фиг.5). Характеристические пики формы II находились при 2θ=5,9°, 14,9°, 17,6°, 18,5° и 24,4° (фиг.6), а формы I при 10,5°, 11,7°, 14,3°, 18,5°, 19,3°, 21,2°, 22,1° (фиг.7).
Данные о кристаллическом строении C24H26N2О4·C24H26N2О4·H2О (две молекулы карведилола и одна молекула воды), моноклинная группа P21/n, а=13,517(3) Å, b=16,539(3) Å, с=19,184(4) Å, β=94,27(3)°, V=4276,9(15) Å3, Z=8, регистрировали с помощью плоского приемника изображений типа STOE с использованием источника излучения Mokα (графитный монохроматор), при этом применяли бесцветный кристалл, имеющий размеры 0,3×0,3×0,05 мм, и регистрировали в общей сложности данные 5298 уникальных измерений. Структуру идентифицировали прямыми методами и уточняли с помощью коэффициента Rfactor, равного 0,0764. Асимметричная элементарная кристаллическая ячейка состоит из двух молекул карведилола и одной молекулы воды. Картина дифракции рентгеновских лучей на порошке, рассчитанная теоретическим путем на основе этой структуры, хорошо совпадала с картиной дифракции рентгеновских лучей на порошке, полученной в эксперименте для образца кристаллической формы IV.
ИК-спектр формы IV карведилола сильно отличается от спектров форм I и II карведилола в хвостовой области диапазона колебаний: форма IV: 3400 см-1; форма: I 3450 см-1; форма: II 3345 см-1 (см. фиг.1-4), что обусловлено наличием различных водородных мостиков.
Предпочтительные варианты осуществления изобретения проиллюстрированы ниже на примерах, которые не ограничивают объем изобретения.
Пример 1
Получение отвержденного распылением карведилола
Отвержденный распылением карведилол, применяемый для выделение формы IV, получали согласно следующему методу: сначала расплавляли Macrogol 6000 (полиэтиленгликоль) при 70-85°С. Путем последующего растворения Pluronic F 68 (полипропиленгликоль) и формы II карведилола при 70-85°С получали расплав, имеющий следующий состав (объем партии: приблизительно 10 кг): 16,84% карведилола; 5,05% Pluronic F68 и 78,11% Macrogol 6000.
Этот расплав отверждали с помощью холодного азота (0-5°С) с использованием снабженной нагревателем двухкомпонентной форсунки. Отвержденный распылением продукт собирали с помощью циклонного сепаратора. Перед дальнейшим использованием партию хранили при 4-8°С в течение 8 месяцев.
Пример 2
Способ получения формы IV карведилола
9 г отвержденного распылением карведилола и 100 мл дистиллированной воды перемешивали в течение ночи при комнатной температуре (КТ) с помощью магнитной мешалки. Полученную суспензию фильтровали через фильтр с размерами отверстий 0,45 мкм и промывали дважды 20 мл дистиллированной воды. Осадок на фильтре ресуспендировали в 100 мл дистиллированной воды и еще раз перемешивали в течение ночи. Полученную таким путем суспензию снова фильтровали через фильтр с размерами отверстий 0,45 мкм, промывали дважды 20 мл дистиллированной воды и сушили в вакууме (10-15 мбар) при КТ в течение по меньшей мере 12 ч, получая приблизительно 1,6 г формы IV. Характеристики полученной формы IV измеряли, как описано выше.
Для получения чистой формы IV 130 мг выделенного, как описано выше, продукта суспендировали в 3,25 мл смеси метанол/вода (90:10 (об./об.)) и нагревали до 50-60°С до тех пор, пока не растворится весь продукт. Раствор охлаждали до КТ в течение 1 ч и хранили в течение ночи при КТ. Полученный таким путем кристаллический продукт выделяли и сушили в потоке осушенного азота, получая 70-100 мг чистой кристаллической формы IV. Характеристики полученной формы IV измеряли, как описано выше.
Для получения более крупных кристаллов формы IV для рентгеноструктурного анализа элементарной кристаллической ячейки 100 мг выделенного, как описано выше, продукта суспендировали в 4 мл смеси метанол/вода (90:10 (об./об.)) и нагревали до 50-60°С до тех пор, пока не растворится весь продукт. Раствор очень медленно охлаждали в течение 50 ч от 55°С до -10°С. Полученный таким путем кристаллический продукт выделяли и сушили в потоке осушенного азота, получая 50-80 мг чистой кристаллической формы IV. Полученные таким путем кристаллы можно применять для рентгеноструктурного анализа элементарной кристаллической ячейки.
Пример 3
Способ получения формы IV карведилола
118 мг формы II карведилола суспендировали в 3 мл смеси метанол/вода (90:10 (об./об.)) и нагревали до 50-60°С до тех пор, пока не образовывался прозрачный раствор. Раствор охлаждали до 40-50°С и вносили затравку в виде небольшого количества кристаллической формы IV (полученной, как описано в примере 2). Раствор с затравкой охлаждали до КТ и хранили в течение ночи при 5-8°С. Полученные таким путем кристаллы выделяли и сушили в потоке осушенного азота, получая 50-80 мг чистой кристаллической формы IV. Характеристики полученной формы IV измеряли, как описано выше.
Пример 4
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 5
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Форму I карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 6
Композиция, содержащая форму IV карведилола
Сополимер полиоксиэтилена и полиоксипропилена расплавляли при 70°С. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 7
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
При необходимости технические характеристики обрабатываемых продуктов, такие, например, как текучесть растворов, можно улучшать путем добавления дополнительных адъювантов (см. пример 9).
Пример 8
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму I карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
При необходимости технические характеристики обрабатываемых продуктов, такие, например, как текучесть растворов, можно улучшать путем добавления дополнительных адъювантов (см. пример 9).
Пример 9
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. Затем композицию, содержащую карведилол, обрабатывали высокодисперсным диоксидом кремния и перемешивали до гомогенного состояния. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 10
Композиция, содержащая форму IV карведилола
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 11
Композиция, содержащая форму IV карведилола
Изомальт расплавляли при температуре, превышающей его температуру плавления. Затем форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 12
Композиция, содержащая форму IV карведилола - таблетки с быстрым высвобождением
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном как указано выше расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. Затем смесь обрабатывали высокодисперсным диоксидом кремния и перемешивали до гомогенного состояния. Полученную смесь обрабатывали таблеттозой и перемешивали. К полученной, как описано выше, смеси добавляли внешнюю фазу (замасливатель, агент, повышающий текучесть, агент, способствующий разделению, и наполнитель), состоящую из натрийкарбоксиметилкрахмала, высокодисперсного диоксида кремния и стеарата магния, и смешивали до гомогенного состояния. Затем образовавшуюся смесь прессовали, получая фармацевтические формы, или заполняли ею капсулы с помощью обычных методов с учетом требуемого содержания действующего вещества. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 13
Композиция, содержащая форму IV карведилола - таблетки типа "ретард"
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. Затем смесь обрабатывали высокодисперсным диоксидом кремния и перемешивали до гомогенного состояния. Полученную смесь обрабатывали таблеттозой и перемешивали. К полученной, как описано выше, смеси добавляли внешнюю фазу (замасливатель, агент, повышающий текучесть, агент, способствующий разделению и наполнитель), состоящую из гидроксипропилметилцеллюлозы 2208, высокодисперсного диоксида кремния и стеарата магния, и перемешивали до гомогенного состояния. Затем образовавшуюся смесь прессовали, получая фармацевтические формы, или заполняли ею капсулы с помощью обычных методов с учетом требуемого содержания действующего вещества. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
Пример 14
Композиция, содержащая форму IV карведилола - таблетки типа "ретард"
Полиэтиленгликоль 6000 расплавляли при 70°С. Затем сополимер полиоксиэтилена и полиоксипропилена, расплавленный аналогичным образом, перемешивали в полученном, как указано выше, расплаве и расплав гомогенизировали. Форму II карведилола перемешивали в образовавшемся расплаве и растворяли до гомогенного состояния. После этого расплав отверждали распылением. В альтернативном варианте расплав можно отверждать другими методами при условии, что отверждение происходит быстро. Затем смесь обрабатывали высокодисперсным диоксидом кремния и перемешивали до гомогенного состояния. Полученную смесь обрабатывали таблеттозой и перемешивали. К полученной, как описано выше, смеси добавляли внешнюю фазу (замасливатель, агент, повышающий текучесть, агент, способствующий разделению и наполнитель), состоящую из альгината натрия, высокодисперсного диоксида кремния и стеарата магния, и перемешивали до гомогенного состояния. Затем образовавшуюся смесь прессовали, получая фармацевтические формы, или заполняли ею капсулы с помощью обычных методов с учетом требуемого содержания действующего вещества. После хранения в течение приблизительно 2 месяцев при комнатной температуре получали композицию, содержащую в качестве действующего вещества карведилол в виде практически чистой формы IV.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИДРОФИЛЬНЫЕ МОЛЕКУЛЯРНЫЕ ДИСПЕРСНЫЕ РАСТВОРЫ КАРВЕДИЛОЛА | 2001 |
|
RU2248204C2 |
| ТЕРМОДИНАМИЧЕСКИ СТАБИЛЬНАЯ МОДИФИКАЦИЯ (±)1-(4-КАРБАЗОЛИЛОКСИ)-3-[2-(2-МЕТОКСИФЕНОКСИ)ЭТИЛАМИНО]-2-ПРОПАНОЛА , СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2202542C2 |
| СТАБИЛЬНАЯ, СОСТОЯЩАЯ ИЗ ЧАСТИЦ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СОЛИФЕНАЦИН ИЛИ ЕГО СОЛЬ | 2005 |
|
RU2397767C2 |
| ФАРМАЦЕВТИЧЕСКАЯ ДОЗИРОВАННАЯ ФОРМА, СОДЕРЖАЩАЯ ПОЛИМЕРНУЮ КОМПОЗИЦИЮ-НОСИТЕЛЬ | 2009 |
|
RU2519679C9 |
| КОМПОЗИЦИЯ СОЛИФЕНАЦИНА ИЛИ ЕГО СОЛИ ДЛЯ ИСПОЛЬЗОВАНИЯ В ТВЕРДОМ ПРЕПАРАТЕ | 2005 |
|
RU2359670C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ГЕПАТИТА С | 2013 |
|
RU2665365C2 |
| СИСТЕМА ДОСТАВКИ АКТИВНОГО ИНГРЕДИЕНТА | 2011 |
|
RU2527540C1 |
| ПЛЕНКООБРАЗУЮЩАЯ КОМПОЗИЦИЯ СО СПОСОБНОСТЬЮ К РАСТЕКАНИЮ | 2007 |
|
RU2517960C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКИХ МУЛЬТИЧАСТИЦ | 2004 |
|
RU2331410C2 |
| ПОКРЫТАЯ РАСПЛАВОМ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С БЫСТРЫМ ВЫСВОБОЖДЕНИЕМ | 2009 |
|
RU2554768C2 |




Изобретение относится к фармацевтически приемлемой композиции для лечения или профилактики заболеваний сердца, которая содержит полугидрат кристаллической формы IV (±)-1-(4-карбазолилокси)-3-[2-(2-метоксифенокси)этиламино]-2-пропанола (карведилола), имеющий температуру плавления 94-96°С, или его фармацевтически приемлемые соли и фармацевтически приемлемый носитель и/или адъювант, который не обладает поверхностно-активными свойствами, имеет температуру плавления ниже 120°С и выбран из полиэтиленгликоля и/или изомальта, и/или неоногенное поверхностно-активное вещество, такое как сополимер полиоксиэтилена и полиоксипропилена. Композицию получают расплавлением кристаллической формы (±)-1-(4-карбазолилокси)-3-[2-(2-метоксифенокси)этиламино]-2-пропанола (карведилола) с tпл 123-126°С или с tпл 114-115°С или его фармацевтически приемлемых солей в адъюванте и/или неоногенном поверхностно-активном веществе, которые указаны выше, с последующим быстрым отверждением и последующим добавлением фармацевтически приемлемого носителя. 3 н. и 12 з.п. ф-лы, 7 ил.
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Устройство для магнитно-абразивной обработки | 1978 |
|
SU918055A1 |
| Устройство для компенсации постоянной составляющей при сварке на переменном токе | 1980 |
|
SU893440A1 |
| СПОСОБ ЛЕЧЕНИЯ СОСТОЯНИЯ, В КОТОРОМ ПОКАЗАН 5НТ-ПОДОБНЫЙ АГОНИСТ, ПРОИЗВОДНОЕ ТЕТРАГИДРОКАРБАЗОЛА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ АГОНИСТА 5НТ-ПОДОБНЫХ РЕЦЕПТОРОВ | 1992 |
|
RU2137474C1 |
Авторы
Даты
2007-10-20—Публикация
2002-09-18—Подача