Изобретение относится к медицине, а более конкретно - к офтальмологии и предназначено для хирургического лечения рефрактерной глаукомы.
Известна модель дренажа для антиглаукомных операций, выполненная в виде трубки цилиндрической формы с пористыми стенками, описанная в патенте США №5968058. Этот вид дренажа применяется при вторичной глаукоме и имплантируется одним концом в переднюю камеру глаза, а другим, наружным концом, под конъюнктиву.
Тем не менее данная модель не лишена определенных недостатков. В частности, предложенная конструкция дренажа не исключает его дислокации в переднюю камеру глаза в разные сроки после имплантации, что может привести к травматизации радужки или эндотелия роговицы и вызвать рецидивирующие гифемы, иридоциклиты и эпителиально-эндотелиальную дистрофию роговой оболочки. Кроме того, недостаточная эластичность, жесткость цилиндрического дренажа может привести к излишнему расширению прокола склеророговичной ткани в месте введения дренажа в переднюю камеру при движениях глазного яблока и, в свою очередь, привести к развитию синдрома мелкой передней камеры, а затем и к полному ее опорожнению, что чревато отслойкой сосудистой оболочки, длительной гипотонией и макулярному отеку. Дренаж предложенной формы и с предложенным способом фиксации может также смещаться под конъюнктиву, что приводит к утрате его дренирующей роли. Кроме того, просвет дренажа может забиваться кровью или гемозным фибрином, что препятствует выполнению дренажом своей функции и уменьшает гипотензивный эффект антиглаукомной операции. Кроме того, имплантация данной модели дренажа способствует фильтрации внутриглазной жидкости в основном под конъюнктиву, что недостаточно для лечения трудноизлечимых форм глауком. Также имплантация цилиндрического дренажа требует дополнительной шовной фиксации, для чего необходимы дополнительное время и определенная квалификация хирурга. Кроме того, материал, из которого выполнена данная модель, не препятствует образованию соединительно-тканной капсулы вокруг, и, таким образом, происходит быстрая облитерация сформированных дренажных путей и утрата дренажом своих функций.
Целью изобретения является создание новой модели эксплантодренажа из нового полимерного материала для хирургического лечения глаукомы, особенно ее тяжелых, рефрактерных форм, где требуется минимальная реакция на имплант со стороны окружающих тканей, минимальная травматизация окружающих тканей в сочетании с простой в исполнении имплантацией эксплантодренажа без дополнительной шовной фиксации с целью получения стойкого гипотензивного эффекта в результате стимулирования всех возможных путей оттока внутриглазной жидкости (ВГЖ).
Техническим результатом изобретения является перфорированный эксплантодренаж из нового полимерного материала - дигеля, позволяющий благодаря своим составу, форме и структуре длительно сохранять сформированную во время антиглаукомной операции интрасклеральную полость, добиться высокого уровня биосовместимости, позволяющего многолетнее ареактивное присутствие импланта в глазу в условиях минимальных интра- и послеоперационных осложнений.
Технический результат достигается тем, что для изготовления дренажа синтезирован новый полимерный материал - дигель. Материал дренажа представляет собой прозрачный полимер, полученный в результате фотополимеризации химической композиции, состоящей из следующих веществ, взятых в определенных соотношениях: монометакриловый эфир этиленгликоля (10-40 мас.%), метакриловая кислота (2,0-8,0 мас.%), 2,2-диметокси-2-фенилацетофенон (0,1-0,7 мас.%), 2,4-дитретбутилортохинон (0,001-0,006 мас.%), олигоуретанметакрилат - остальное. После фотоотверждения композиции получаем дренаж в виде прямоугольника с закругленными углами с радиусом закругления не менее 1 мм и расположенными по его площади отверстиями таким образом, что расстояние от краев прямоугольника до периферийных рядов отверстий составляет от 0,5 до 1 мм, способный к сворачиванию после набухания в воде и восстановлению заданной формы, с повышенной прочностью и эластичностью, повышенной устойчивостью в биологически активных средах, повышенной устойчивостью к окислительным процессам и процессам адсорбции белков на поверхности, предотвращающий образование грубой соединительно-тканной капсулы.
Совокупность минимальных значений ингредиентов определяет пороговое значение с точки зрения минимума, ниже которого либо не достигается требуемой прочности изделия, либо процесс полимеризации осуществляется неполностью, что приводит к возникновению острых реакций в тканях глаза, а также снижению устойчивости в биологически активных средах (камерной влаге глаза), устойчивости к окислительным процессам и процессам адсорбции белков на поверхности.
Максимальные значения ингредиентов определяются тем, что при больших значениях проявляется либо излишняя жесткость, либо ухудшение таких характеристик как искажение формы, появление мутности и т.д., что приводит к травматизации прилежащих тканей глаза.
Пример 1. Олигоуретанметакрилат (ОУА) получают каталитическим взаимодействием
лапрола 2102, ТУ 2226-411-05761784-95 строения
НО-(СН(СН3)-СН2)n-ОН, где n=36;
2,4-толуилендиизоцианата (ТДИ) ТУ 113-38-95-90, строения
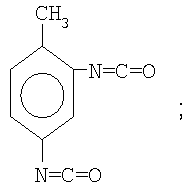
монометакрилового эфира этиленгликоля (МЭГ) ТУ 6-01-1240-80 строения
НО-(СН2)2-O-С(СН3)=СН2.
В качестве катализатора добавляют дибутилдилаурат олова, строения
(СН3(СН2)3)2Sn(СН3(СН2)10СОО)2.
В качестве ингибитора используют 2,4-дитретбутилортохинон, строения
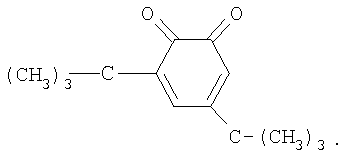
Расходная норма на 1 кг готового продукта, исходя из 100% содержания основного вещества для всех исходных реагентов, составляет:
лапрол 2102-766,77 г;
ТДИ - 133,53 г;
МЭГ - 99,67 г;
дибутилдилаурат олова - 0,027 г;
2,4-дитретбутилортохинон - 0,003 г.
Практическая расходная норма рассчитывается по результатам анализа определения ОН-групп и NCO-групп в исходных лапроле и ТДИ, и промежуточном продукте - макродиизоцианате. Все сырье, применяемое для получения олигоуретанметакрилата ОУА, должно соответствовать научно-технической документации, содержание влаги в лапроле не должно превышать 0,1%. Дополнительно лапрол 2102 сушат в роторно-пленочном испарителе при 100°С в течение 3 часов. После этого определяют содержание ОН-групп по ГОСТ 25261-82. ТДИ перед синтезом перегоняют в приборе для вакуумной разгонки и определяют содержание NCO групп по ТУ 113-03-413-89.
Сначала синтезируют макродиизоцианат строения
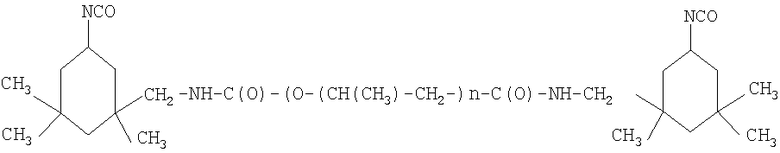
Синтез ведут при соотношение NCO групп в реакционной смеси к количеству ОН групп, равном 2:1, следующим образом: в реактор, представляющий собой цилиндрический аппарат объемом 5-6 л, изготовленный из стали марки 12Х18Н10Т, с крышкой, на которой расположены штуцеры для холодильника, загрузочного устройства реагентов и ввода инертного газа (аргон), снабженный мешалкой, с редуктором, обеспечивающим скорость вращения мешалки 60-90 об/мин, и проводящей рубашкой для подогрева реакционной смеси загружают последовательно при температуре 30-40°С осушенный лапрол 2102; свежеперегнанный ТДИ; катализатор дибутилдилаурат олова при включенной мешалке и потоке сухого инертного газа. Синтез макродиизоцианата ведут при температуре 50-55°С до содержания NCO-групп в макродиизоцианате, равного 0,5 от загруженного количества NCO-групп, примерно в течение 2 часов, после чего отбирают пробу и определяют содержание NCO-групп. Содержание NCO-групп определяют по ТУ 113-03-413-89. При содержании NCO-групп более 0,5 пробу отбирают повторно через 1 час после первого отбора. Далее в расчетное количество МЭГ (NCO:OH=1:1) вносят ингибитор полимеризации 2,4-дитретбутилортохинон. МЭГ приливают в реактор при работающей мешалке и выдерживают реакционную смесь при температуре 50-55°С до содержания остаточных NCO-групп не выше 0,05%. После слива ОУА в тару тара укупоривается и выдерживается в течение 5 дней в закрытом складском помещении.
Пример 1. В реакционную колбу, снабженную мешалкой, последовательно вводят компоненты в следующем соотношении, г:
Полученную смесь перемешивают при комнатной температуре в течение 40 минут до полного растворения 2,2-диметокси-2-фенилацетофенона и 2,4-дитретбутилортохинона.
Дренаж изготавливают в стеклянных формах, состоящих из двух половинок, на одной из которых выполнен рисунок, например, из оксида железа с геометрическими размерами, точно соответствующими дренажу (см. чертеж). На стеклянную половинку с рисунком прикрепляют ограничивающую рамку толщиной 150 мкм, например, из лавсана, равномерно распределяют композицию по внутреннему объему ограничивающей рамки и накрывают верхней стеклянной половинкой формы. Переносят собранную стеклянную форму в установку экспонирования, состоящую из источника света (ртутно-кварцевая лампа марки ДРТ-120) и коллиматора, и проводят облучение в течение времени, необходимого для полного воспроизведения формы дренажа, указанной на чертеже. При интенсивности света, падающего на поверхность литьевой формы, 440 Вт/м2 оптимальное время экспонирования составляет 2 мин. После облучения форму разбирают, отделяя одну половинку формы от другой и удаляя ограничительную прокладку. Далее все операции выполняют с половинкой формы, на которой сформирован дренаж. Половинку формы с дренажом помещают в установку проявления, состоящую из кюветы для проявителя объемом 200 мл, насоса, обеспечивающего циркуляцию проявителя, и форсунки, расположенной в крышке кюветы. Форму с дренажом помещают в кювету, наливают проявитель - изопропиловый спирт, закрывают крышкой и включают насос. Время проявления дренажа - 2 минут. Во время проявления происходит удаление незаполимеризованной части фотоотверждаемого материала, который во время экспонирования находился под непрозрачными для УФ-света участками рисунка, выполненного на нижней половинке формы (см. чертеж). После проявления дренаж высушивают в потоке теплого обеспыленного воздуха в течение 1 мин. Далее дренаж на половинке формы переносят в установку экспонирования, состоящую из источника (ртутно-кварцевой лампы марки ДРТ-120) и вакуумного насоса, обеспечивающего вакуум 10-1 мм рт.ст., и проводят стадию отжига, состоящую в дополнительном облучении дренажа. При интенсивности света, падающего на поверхность, 330 Вт/м2 время облучения составляет 10 мин. После дополнительного облучения дренаж отделяют от формы. Получается дренаж, способный к сворачиванию после набухания в воде и восстановлению заданной формы, с повышенной прочностью и эластичностью, повышенной устойчивостью в биологически активных средах, повышенной устойчивостью к окислительным процессам и процессам адсорбции белков на поверхности, характеристики которого приведены в таблице.
Пример 2
Композицию готовят, как в примере 1, при следующем соотношении компонентов, г:
Изготавливают дренаж, как в примере 1. Характеристики приведены в таблице.
Пример 3
Композицию готовят, как в примере 1, при следующем соотношении компонентов, г:
Изготавливают дренаж, как в примере 1. Характеристики приведены в таблице.
Пример 4
Композицию готовят, как в примере 1, при следующем соотношении компонентов, г:
Изготавливают дренаж, как в примере 1. Характеристики приведены в таблице.
Пример 5
Композицию готовят, как в примере 1, при следующем соотношении компонентов, г:
Изготавливают дренаж, как в примере 1. Характеристики приведены в таблице.
Конструкция эксплантодренажа из дигеля позволяет надежно фиксировать его без дополнительной шовной фиксации и, таким образом, предотвратить грозные осложнения, связанные с возможной дислокацией имплантов, в частности - выпадение его в переднюю камеру или под конъюнктиву. Отсутствие в необходимости шовной фиксации позволяет избежать такого грозного осложнения, как перфорация цилиарного тела и гемофтальм.
Перфорированная, сетчатая структура нашей модели эксплантодренажа не затрудняет свободной циркуляции поступающей жидкости во всех направлениях - под конъюнктиву, в интрасклеральные коллекторы и в сосудистую сеть хориоидеи и, таким образом, стимулирует все возможные пути оттока внутриглазной жидкости у больных с рефрактерной глаукомой.
Перфорированный дренаж из дигеля имплантируется интрасклерально. Предварительно после разреза конъюнктивы и отсепаровки поверхностного склерального лоскута расслаивателем для антиглаукомных операций формируют дополнительную интрасклеральную полость (карман) до размеров 6,0×8,0 мм по всем сторонам на уровне поверхностного разреза склеры. Перфорированный дренаж имплантируют в сформированную внутрисклеральную полость при помощи 2 микрохирургических пинцетов для завязывания швов. При необходимости дренаж расправляют в кармане при помощи микрохирургического шпателя. Дополнительной шовной фиксации дренажа не требуется. Адаптацию операционной раны проводят традиционным способом.
Предлагаемое изобретение поясняется чертежом, где схематически представлен вид спереди на предлагаемую модель дренажа для антиглаукомных операций (1) с многочисленными отверстиями (2), распределенными равномерно по всей поверхности дренажа.
Предлагаемое изобретение поясняется следующими клиническими примерами.
Пример 1. Больная К.,56 лет. Диагноз при поступлении - вторичная декомпенсированная факотопическая глаукома обоих глаз, неполная осложненная катаракта, подвывих хрусталика. Острота зрения обоих глаз - 0,1, не корригирует. Внутриглазное давление (ВГД) правого глаза - 41 мм рт.ст., ВГД левого глаза - 39 мм рт.ст. В анамнезе - подъем ВГД в течение 1-1,5 лет. Закапывает гипотензивные препараты (арутимол 0,5% 2-3 раза в день). На фоне медикаментозной терапии ВГД обоих глаз некомпенсировано.
На правом глазу произведена операция непроникающая глубокая склерэктомия с интрасклеральной имплантацией перфорированного дренажа из дигеля согласно изобретению. Через неделю аналогичная операция произведена на левом глазу. Операции и послеоперационный период протекали без осложнений. При выписке - острота обоих глаз осталась без изменений, ВГД обоих глаз -18 мм рт.ст.
При осмотре через 6 месяцев после операции ВГД остается компенсированным и составляет 19-20 мм рт.ст. На фоне нормализованного ВГД произведены операции по замене подвывихнутого мутного хрусталика на искусственный. При осмотре через 1 год - острота обоих глаз - 0,5-0,6. ВГД обоих глаз - 20 мм рт.ст. Данные ультразвуковой биомикроскопии подтверждают наличие обширной интрасклеральной полости с четко визуализирующимся дренажом. Также присутствуют признаки вновь сформированных путей оттока ВГЖ, в частности увеосклерального.
Пример 2. Больной С., 69 лет. Предоперационный диагноз правого глаза - О/У III соперированная глаукома. Левый глаз энуклеирован по поводу терминальной болящей глаукомы. В анамнезе - глаукома в течение 10 лет. Антиглаукомная операция на правом глазу 2 года назад. На момент поступления закапывает гипотензивные препараты, которые не оказывают удовлетворительного эффекта. При поступлении: острота зрения правого глаза - 1,0 при суженном до трубчатого поле зрения. ВГД - 36 мм рт.ст.
Произведена операция глубокая склерэктомия с интрасклеральной имплантацией перфорированного дренажа из дигеля согласно изобретению. Операция и послеоперационный период протекали без осложнений. При выписке острота зрения - без изменений, ВГД - 16 мм рт.ст.
При осмотре через 3, 6, 12, 24 месяца после операции острота зрения и ВГД стабильны, поле зрения расширилось на 5 град. от точки фиксации. Данные ультразвуковой биомикроскопии подтверждают сохранность вновь сформированных путей оттока ВГЖ.
состоянии, соответствие заданной форме
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ РЕФРАКТОРНОЙ ГЛАУКОМЫ | 2006 |
|
RU2313314C1 |
| ДРЕНАЖ ДЛЯ ОТТОКА ВНУТРИГЛАЗНОЙ ЖИДКОСТИ | 2015 |
|
RU2614102C2 |
| Способ непроникающей глубокой склерэктомии с дренированием лентикулярной тканью при первичной открытоугольной глаукоме | 2023 |
|
RU2809524C1 |
| ДРЕНАЖ ДЛЯ ИНТРАСКЛЕРАЛЬНОГО ОТТОКА ВНУТРИГЛАЗНОЙ ЖИДКОСТИ | 2015 |
|
RU2614103C2 |
| ЭКСПЛАНТОДРЕНАЖ ДЛЯ АНТИГЛАУКОМАТОЗНЫХ ВМЕШАТЕЛЬСТВ | 2010 |
|
RU2434614C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФРАКТЕРНОЙ ГЛАУКОМЫ | 2010 |
|
RU2427355C1 |
| МОНОЛИТНЫЙ ТВЕРДЫЙ ИСКУССТВЕННЫЙ ХРУСТАЛИК ГЛАЗА | 2003 |
|
RU2253482C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛАУКОМЫ | 2017 |
|
RU2644550C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФРАКТЕРНОЙ ГЛАУКОМЫ | 2008 |
|
RU2367395C1 |
| Имплант антиглаукомный для поддержания интрасклеральной полости | 2024 |
|
RU2824429C1 |
Изобретение относится к эксплантодренажу для хирургического лечения рефрактерной глаукомы. Эксплантодренаж позволяет благодаря своим составу и форме длительно сохранять сформированную во время антиглаукомной операции интрасклеральную полость, добиться высокого уровня биосовместимости, позволяющего многолетнее ареактивное присутствие импланта в глазу в условиях минимальных интра- и послеоперационных осложнений. Для изготовления дренажа синтезирован новый полимерный материал - дигель, представляющий собой прозрачный полимер, полученный в результате фотополимеризации смеси мономеров и олигомеров. Конструкция предложенного эксплантодренажа из дигеля позволяет надежно фиксировать его без дополнительной шовной фиксации. Перфорированная структура дренажа позволяет поступающей ВГЖ циркулировать во всех направлениях и стимулирует все возможные пути оттока внутриглазной жидкости у больных с рефрактерной глаукомой. 1 з.п. ф-лы, 1 ил., 1 табл.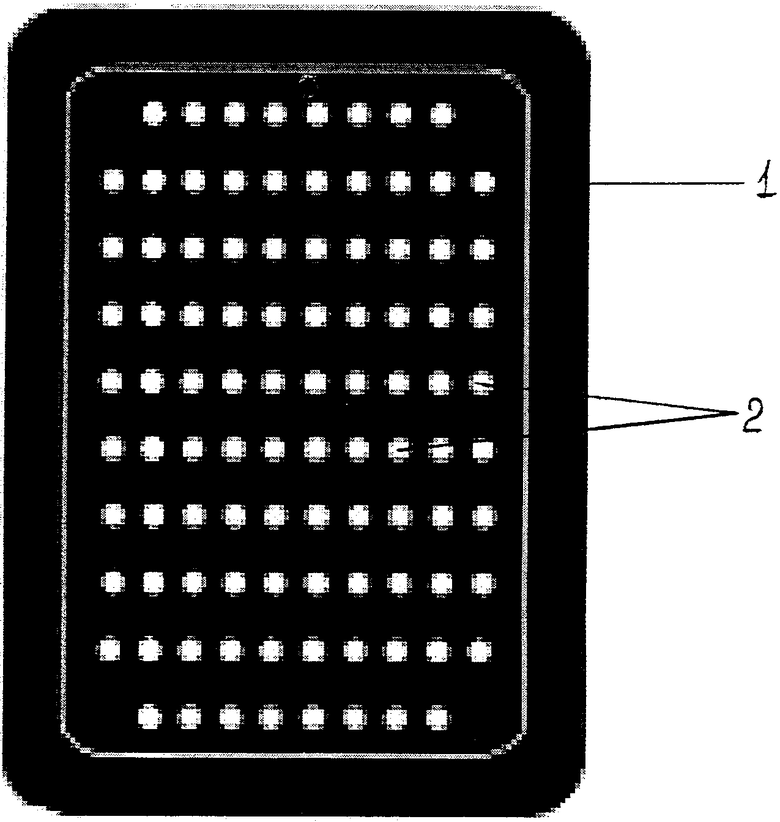
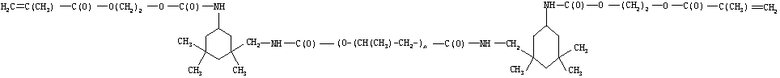
n=36
2,2-диметокси-2-фенилацетофенон строения
Ph-С(O)-С(СН3)2-Ph
2,4-дитретбутилортохинона строения
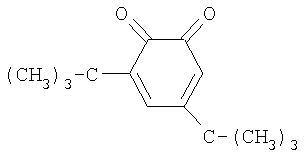
монометакриловый эфир этиленгликоля строения
НО-СН2-СН2-O-С(O)-С(СН3)=СН2,
метакриловая кислота строения
НО-С(O)-С(СН3)=СН2
при этом вышеуказанные компоненты взяты в следующем соотношении, мас.%:
в виде прямоугольника с закругленными углами с радиусом закругления не менее 1 мм и расположенными по его площади отверстиями таким образом, что расстояние от краев прямоугольника до периферийных рядов отверстий составляет от 0,5 до 1 мм.
| Паштаев Н.П | |||
| Новый вид дренажа из дигеля | |||
| Бюллетень ВСНЦ СО РАМН, 2004, №2, с.159-161 | |||
| RU 2002110377 A, 10.12.2003 | |||
| ЭЛАСТИЧНЫЙ ИСКУССТВЕННЫЙ ХРУСТАЛИК ГЛАЗА | 2000 |
|
RU2198661C2 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| US 2005125003, 09.06.2005 | |||
| US 5882327 А, 16.03.1999 | |||
| Имплантат для дренирования при лечении глаукомы | 1991 |
|
SU1805938A3 |
Авторы
Даты
2007-11-10—Публикация
2006-05-25—Подача