Предлагаемое изобретение относится к способам получения новых магнийорганических соединений (МОС), конкретно к способу получения 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионов общей формулы (1):

Предлагаемые соединения могут найти применение в тонком и металлоорганическом синтезе, а также в качестве сокатализаторов в процессах олиго- и полимеризации олефинов и сопряженных диенов.
Известен способ [1, D.P.Lewis, P.M.Muller, R.J.Whitby, R.V.H.Jones. A zirconium catalysed synthesis of 1,4-dimagnesium reagents // Tetrahedron Lett., 1991, 32, p.6797] получения циклических кислородсодержащих магнийорганических соединений (2) взаимодействием 1-[(4-пентенилокси)метил]бензола с диэтилмагнием (MgEt2) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2) по схеме:

Известный способ не позволяет получать 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионы (1).
Известен способ [2, J.-G.Duboudin, B.Jousseaume. Reactifs de Grignard vinyliques γ-fonctionnels: III. Addition a quelques derives carbonyles // J.Organomet. Chem., 1979, 168, p.227] получения непредельных циклических кислородсодержащих магнийорганических соединений (3) взаимодействием дизамещенного ацетилена с реагентами Гриньяра (RMgBr) в присутствии катализатора иодида меди (CuI) при комнатной температуре по схеме:

Известным способом не могут быть получены 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-3-ен-3,5-дионы (1).
Таким образом, в литературе отсутствуют сведения по селективному получению 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионов (1).
Предлагается новый способ получения 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-3-ен-3,5-дионов (1).
Сущность способа заключается во взаимодействии диалкилзамещенных ацетиленов общей формулы  , где R=Et, н-Pr, н-Bu, с бутилмагнийбромидом (BuMgBr) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2), взятыми в мольном соотношении
, где R=Et, н-Pr, н-Bu, с бутилмагнийбромидом (BuMgBr) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2), взятыми в мольном соотношении  :BuMgBr:Cp2ZrCl2, равном 20:(20-24):(0.4-0.6), предпочтительно 20:22:0.5, в атмосфере аргона при комнатной температуре ˜20°С и атмосферном давлении в диэтиловом эфире (Et2O) в качестве растворителя в течение 3 часов с последующим вакуумированием эфира, добавлением при температуре -5°С малеинового ангидрида в эквимольном по отношению к BuMgBr количестве с перемешиванием реакционной массы 6-8 часов, предпочтительно 7 часов, в толуоле при комнатной температуре (˜20°С). Реакция протекает с образованием 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионов (1) с выходом 48-57% по схеме:
:BuMgBr:Cp2ZrCl2, равном 20:(20-24):(0.4-0.6), предпочтительно 20:22:0.5, в атмосфере аргона при комнатной температуре ˜20°С и атмосферном давлении в диэтиловом эфире (Et2O) в качестве растворителя в течение 3 часов с последующим вакуумированием эфира, добавлением при температуре -5°С малеинового ангидрида в эквимольном по отношению к BuMgBr количестве с перемешиванием реакционной массы 6-8 часов, предпочтительно 7 часов, в толуоле при комнатной температуре (˜20°С). Реакция протекает с образованием 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионов (1) с выходом 48-57% по схеме:

1,7,8,9-Тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионы (1) образуются только лишь с участием BuMgBr, дизамещенных ацетиленов, циркониевого катализатора Cp2ZrCl2 и малеинового ангидрида. В присутствии других соединений магния (например, PhMgBr, Ph2Mg, AllMgBr, MeOMgBr), других ацетиленов (например, терминальных), других катализаторов (например, Zr(acac)4, Cp2TiCl2, Pd(acac)2, Ni(асас)2, NiCl2, Fe(acac)2), других ангидридов карбоновых кислот (например, уксусный или фталевый ангидриды) целевые продукты (1) не образуются.
Реакции проводили при комнатной температуре (˜20°С). При более высокой температуре (например, 40°С) не наблюдается существенного увеличения выхода целевых продуктов (1), а при меньшей температуре (например, 0°С) снижается скорость реакции.
Изменение соотношения исходных реагентов (BuMgBr, малеиновый ангидрид) и катализатора (Cp2ZrCl2) в сторону увеличения по отношению к исходному дизамещенному ацетилену (R-≡-R) не приводит к существенному повышению выхода целевых продуктов (1). Изменение соотношения исходных реагентов и катализатора в сторону их уменьшения по отношению к исходному дизамещенному ацетилену снижает выход целевых продуктов (1).
Существенные отличия предлагаемого способа.
В предлагаемом способе для получения непредельных циклических кислородсодержащих МОС используются в качестве исходных соединений диалкилзамещенные ацетилены (R-≡-R), малеиновый ангидрид и катализатор Cp2ZrCl2. В известном способе непредельные циклические кислородсодержащие МОС получают из пропаргиловых спиртов с участием катализатора CuI.
Предлагаемый способ обладает следующими преимуществами:
Способ позволяет получать с высокой селективностью 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дионы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 5 мл Et2O, 20 ммолей гекс-1-ина. Смесь охлаждают до 0°С, добавляют 0.5 ммолей катализатора Cp2ZrCl2, 22 ммолей BuMgBr (в Et2O) и перемешивают 3 часа при температуре ˜20°С, затем вакуумируют эфир, добавляют 6 мл толуола и 12 ммолей малеинового ангидрида при температуре -5°С, после чего реакционную массу перемешивают 7 часов при температуре ˜20°С. Получают 1,7,8,9-тетраэтил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-8-ен-3,5-дион (1) с выходом 55%. Выход целевого продукта определен по продукту гидролиза (4).
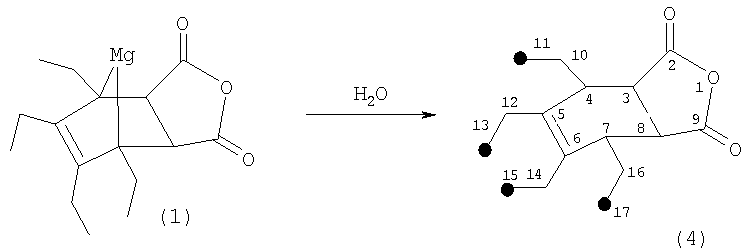
Спектральные характеристики 4,5,6,7-тетраэтил-3а,4,7,7а-тетрагидро-1,3-изобензофуран-2,9-диона (4): Спектр ЯМР 13С CDCl3, δ, м. д.: 172.44 (С2, С9), 42.68 (С3, С8), 41.68 (С4, С7), 138.42 (С5, С6), 20.70 (С10, С16), 12.53 (С11, С17), 20.01 (С12, С14), 14.90 (С13, С15). Другие примеры, подтверждающие способ, приведены в табл.1.
Реакции проводили при температуре ˜20°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,7,8,9-ТЕТРААЛКИЛ-4-МЕТИЛ-4-АЗА-10-МАГНЕЗАТРИЦИКЛО[5.2.1.0]ДЕЦ-8-ЕН-3,5-ДИОНОВ | 2006 |
|
RU2313529C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,7,8,9-ТЕТРААЛКИЛ-10-ЭТИЛ-4-ОКСА-10-АЛЮМИНАТРИЦИКЛО[5.2.1.0]ДЕЦ-8-ЕН-3,5-ДИОНОВ | 2004 |
|
RU2275374C2 |
| СПОСОБ ПОЛУЧЕНИЯ 10-ХЛОРО-1,7,8,9-ТЕТРААЛКИЛ-4-МЕТИЛ-4-АЗА-10-АЛЮМИНАТРИЦИКЛО [5.2.1.0]ДЕЦ-8-ЕН-3,5-ДИОНОВ | 2005 |
|
RU2295529C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,8,9,10-ТЕТРААЛКИЛ-11-МАГНЕЗАТРИЦИКЛО[6.2.1.0]УНДЕЦ-9-ЕН-3,6-ДИОНОВ | 2006 |
|
RU2313528C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,12,13,14-ТЕТРААЛКИЛ-15-МАГНЕЗАТЕТРАЦИКЛО-[10.2.1.0.0]ПЕНТАДЕКА-4(9),5,7,13-ТЕТРАЕН-3,10-ДИОНОВ | 2006 |
|
RU2313530C1 |
| СПОСОБ ПОЛУЧЕНИЯ 11-ХЛОРО-1,8,9,10-ТЕТРААЛКИЛ-11-АЛЮМИНАТРИЦИКЛО [6.2.1.0]УНДЕЦ-9-ЕН-3,6-ДИОНОВ | 2005 |
|
RU2295530C1 |
| СПОСОБ ПОЛУЧЕНИЯ 15-ХЛОРО-1,12,13,14-ТЕТРААЛКИЛ-15-АЛЮМИНАТЕТРАЦИКЛО[10.2.1.0.0]ПЕНТАДЕКА-4(9),5,7,13-ТЕТРАЕН-3,10-ДИОНОВ | 2005 |
|
RU2295531C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ(АРИЛ)МАГНЕЗАЦИКЛОПЕНТ-2-ЕНОВ | 2009 |
|
RU2409583C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(АЛКОКСИ)-2,3,4,5- ТЕТРААЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПЕНТАДИЕНОВ И 1-(АЛКОКСИ)-2,3- ДИАЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПРОПЕНОВ | 1997 |
|
RU2130024C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИН)-2,3,4,5-ТЕТРААЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПЕНТАДИЕНОВ И 1-(ДИАЛКИЛАМИН)-2,3-ДИАЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПРОПЕНОВ | 1997 |
|
RU2131432C1 |
Предлагаемое изобретение относится к способам получения новых магнийорганических соединений, которые могут найти применение в тонком органическом и металлоорганическом синтезе, а также в качестве сокатализаторов в процессах олиго- и полимеризации олефинов и сопряженных диенов. Сущность способа заключается во взаимодействии дизамещенных ацетиленов с бутилмагнийбромидом в присутствии катализатора в атмосфере аргона при атмосферном давлении и температуре ˜20°С в эфирном растворителе в течение 3 часов с последующим вакуумированием эфира, добавлением при температуре -5°С малеинового ангидрида и перемешиванием реакционной массы в течение 6-8 часов при температуре ˜20°С в толуоле. Выход целевого продукта составляет 48-57%. Технический результат - предложенный способ позволяет получать с высокой селективностью соединения формулы 1, где R=Et, н-Pr, н-Bu, синтез которых в литературе не описан. 1 табл.

Способ получения 1,7,8,9-тетраалкил-4-окса-10-магнезатрицикло[5.2.1.02,6]дец-В-ен-3,5-дионов (1) общей формулы:
 , где R=Et, н-Pr, н-Bu
, где R=Et, н-Pr, н-Bu
заключающийся в том, что дизамещенные ацетилены общей формулы R-≡-R, где R - Et, н-Pr, н-Bu, взаимодействуют с бутилмагнийбромидом BuMgBr в присутствии катализатора цирконацендихлорида Cp2ZrCl2 в мольном соотношении R-≡-R:BuMgBr:Cp2ZrCl2, равном 20:20-24:0,4-0,6, в атмосфере аргона при атмосферном давлении и комнатной температуре ˜20°С в диэтиловом эфире в качестве растворителя в течение 3 ч с последующим вакуумированием эфира и добавлением при температуре -5°С малеинового ангидрида, взятого в эквимольном по отношению к BuMgBr количестве, с перемешиванием реакционной массы в течение 6-8 ч при комнатной температуре ˜20°С в толуоле.
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-5-АЛКИЛИДЕНМАГНЕЗАЦИКЛОПЕНТ-2-ЕНОВ | 2005 |
|
RU2291870C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 2-АЛКИЛИДЕНМАГНИЙЦИКЛОПЕНТАНОВ И 2-АЛКИЛ-3-МЕТИЛИДЕНМАГНИЙЦИКЛОПЕНТАНОВ | 2003 |
|
RU2245885C1 |
| LEWIS D.P | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Tetrahedron Letters | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| DUBOUDIN J.G | |||
| et al | |||
| Reactifs de Grignard vinyliques γ-fonctionnels: III | |||
| Addition a quelques derives carbonyls | |||
| Journal of Organometallic chemistry | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
2007-12-27—Публикация
2006-05-06—Подача