Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики эпидемического гриппа среди взрослых и детей живой интраназальной гриппозной вакциной из штамма А/17/Калифорния/04/6 (H3N2). Этот вакцинный штамм был получен с помощью созданного для этой цели донора аттенуации А/Ленинград/134/17/К7/57 (H2N2).
Известный вакцинный штамм вируса гриппа А/17/Панама/99/242 (H3N2) - прототип [Патент РФ №2248395 от 11.07.2003. - Опубл. БИ 2005. - №8] - утратил антигенную актуальность и вследствие этого не сможет вызвать защитную реакцию во время эпидемии гриппа, вызванной штаммом вируса гриппа, аналогичным вирусу А/Калифорния/7/04 (H3N2).
Задачей, на решение которой направлено заявляемое изобретение, является получение вакцинного штамма для взрослых и детей актуальной антигенной разновидности на основе современного эпидемического вируса А/Калифорния/7/04 (H3N2).
Такой штамм создан - это вакцинный штамм А/17/Калифорния/04/6 (H3N2). Он получен методом генетической реассортации эпидемического вируса А/Калифорния/7/04 (H3N2) с холодоадаптированным температурочувствительным донором аттенуации с последующей селекцией при пониженной до 25°С температуре инкубации в присутствии антисыворотки к донору аттенуации.
Для получения вакцинного штамма в качестве донора аттенуации был использован новый, созданный методом клонирования штамм А/Ленинград/134/17/К7/57 (H2N2).
Известен донор аттенуации А/Ленинград/134/17/57 (H2N2) для получения безвредных живых интраназальных вакцин для взрослых [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука. - 1994. - 151 с.]. Указанный штамм А/Ленинград/134/17/57 (H2N2) является прототипом созданного нами штамма А/Ленинград/134/17/К7/57 (H2N2).
Прототип А/Ленинград/134/17/57 (H2N2) представляет собой гетерогенную популяцию клонов, отличающихся по набору мутаций в генах, кодирующих внутренние белки вируса [Youil R., Kiseleva I., Kwan W-S., Szymkowiak C., Toner T.J., Su Q., Klimov A., Rudenko L, Shaw A.R. Phenotypic and genetic analyses of the heterogeneous population present in the cold-adapted master donor strain: A/Leningrad/134/17/57 (H2N2) // Virus Research, 2004. - Vol.102. - P.165-176]. Причиной создания нового донора было следующее.
Одним из этапов подготовки вакцинного штамма является клонирование смеси реассортантов в куриных эмбрионах методом предельных разведений, и вакцинный реассортант наследует гены, кодирующие внутренние белки вируса, от какого-то одного клона, содержащегося в гетерогенной популяции донора аттенуации А/Ленинград/134/17/57 (H2N2).
Некоторые клоны из этой популяции близки по набору мутаций к гиператтенуированному донору аттенуации А/Ленинград/134/47/57 (H2N2), ранее используемому при подготовке живой гриппозной вакцины для детей [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука. - 1994. - 151 с.]. Так как "детские" вакцинные штаммы, подготовленные на этом доноре, являлись низкоиммуногенными для взрослых людей, то существует вероятность того, что вакцинный штамм, унаследовавший внутренние гены от клона из популяции донора А/Ленинград/134/17/57 (H2N2), который близок по набору мутаций донору А/Ленинград/134/47/57 (H2N2), также окажется низкоиммуногенным. Таким образом, используя в качестве донора аттенуации гетерогенный А/Ленинград/134/17/57 (H2N2), невозможно заранее предугадать, какой из клонов передаст в геном вакцинного штамма гены, кодирующие внутренние белки вируса. Поэтому для получения вакцинного штамма А/17/Калифорния/04/6 (H3N2) необходимо было иметь в качестве донора аттенуации чистый клон из популяции донора А/Ленинград/134/17/57 (H2N2).
Клон А/Ленинград/134/17/К7/57 (H2N2) был получен с помощью клонирования донора аттенуации А/Ленинград/134/17/57 (H2N2) в развивающихся куриных эмбрионах и содержит 7 мутаций во внутренних генах: РВ2 (Val-478-Leu), РВ1 (Lys-265-Asn и Val-591-Ile), PA (Leu-28-Pro и Val-341-Leu), M1 (Ile-15-Val) и NS2 (Met-100-Ile). У клона А/Ленинград/134/17/К7/57 (H2N2) отсутствует мутация в гене М2 (Ala-86-Thr), свойственная части популяции донора А/Ленинград/134/17/57 (H2N2).
Клон А/Ленинград/134/17/К7/57 (H2N2) был изолирован из популяции донора А/Ленинград/134/17/57 (H2N2), который является аттенуированным для людей, так как обладает свойствами температурочувствительности и холодоадаптированности. Полученный нами клонированный донор аттенуации А/Ленинград/134/17/К7/57 (H2N2) также обладает признаками температурочувствительности и холодоадаптированности. Поэтому клонированный донор также должен быть аттенуированным для человека.
Пример выполнения
Клон А/Ленинград/134/17/К7/57 (H2N2) был получен в результате двукратного клонирования донора аттенуации А/Ленинград/134/17/57 (H2N2) предельными разведениями от 10-7 до 10-10 в развивающихся куриных эмбрионах. Каждым разведением вируса было заражено по 20 куриных эмбрионов. Аллантоисную жидкость единственного положительного в реакции гемагглютинации эмбриона, зараженного разведением вируса 10-9, использовали для второго раунда клонирования. После второго раунда клонирования был выбран клон К7, также полученный из разведения 10-9.
Клонированный донор аттенуации А/Ленинград/134/17/К7/57 (H2N2) характеризовался признаками температурочувствительности и холодоадаптированности, характерными для неклонированного донора А/Ленинград/134/17/57 (H2N2). Он обладал пониженным уровнем репродукции в куриных эмбрионах при 40°С (RCT40, разница в активностях репродукции клона при 33 и 40°С составляла 7,7 Ig ЭИД50/0,2 мл) и активно размножался при температуре 25°С (RCT25, разница в репродукциях при 32 и 25°С составляла 2,9 Ig ЭИД50/0,2 мл). Таким образом по этим двум признакам клонированный вирус не отличался от неклонированного донора аттенуации А/Ленинград/134/17/57 (H2N2) (таблица 1).
Аттенуацию клонированного донора оценивали по интенсивности его репродукции в респираторном тракте (носовых ходах и легких) хорьков в сравнении с неклонированным донором А/Ленинград/134/17/57 (H2N2) и вирусом «дикого» типа А/Ленинград/134/57 (H2N2). Репродукция в носовых ходах хорьков всех исследованных вирусов колебалась в пределах 3,2-5,6 Ig ЭИД50/мл/г. «Дикий» вирус активно репродуцировался в легких. Отмечен сниженный уровень репродукции в легких хорьков неклонированного донора аттенуации А/Ленинград/134/17/57 (H2N2) по сравнению с «диким» вирусом (1,7-1,8 Ig ЭИД50/мл/г против 3,9-4,1 Ig ЭИД50/мл/г соответственно). Клонированный донор А/Ленинград/134/17/К757 (H2N2) из легких хорьков не выделялся вообще, что свидетельствовало о его высокой аттенуации для хорьков (таблица 1).
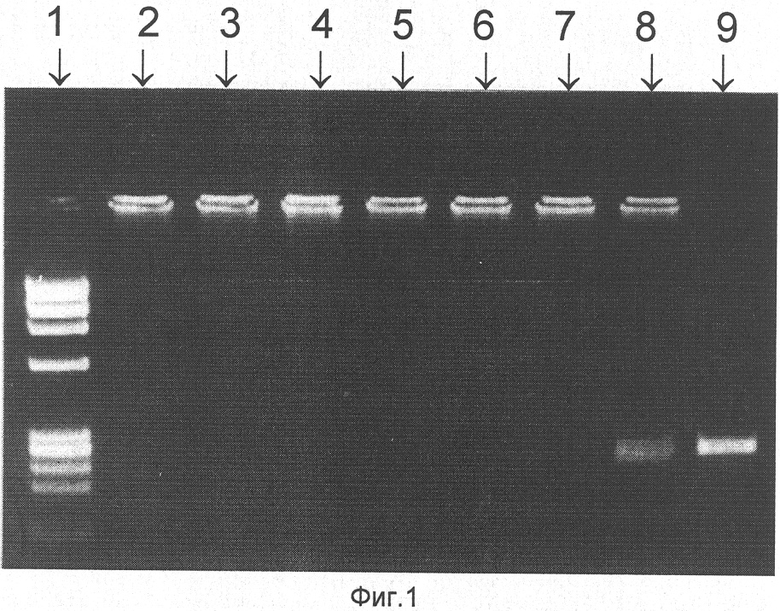
На фиг.1 представлен ПЦР-рестрикционный анализ ДНК-фрагментов М2 гена А/Ленинград/134/17/57 (H2N2), А/Ленинград/134/17/К7/57 (H2N2) и его «дикого» предшественника - вируса А/Ленинград/134/57 (H2N2). 1-я дорожка - ДНК маркер молекулярного веса IX; 2-я, 4-я и 6-я дорожки - А/Ленинград/134/57 (H2N2); 3-я, 5-я и 7-я дорожки - клон А/Ленинград/134/17/К7/57 (H2N2); 8-я дорожка - неклонированный донор аттенуации А/Ленинград/134/17/57 (H2N2), 9-я дорожка-донор аттенуации А/Ленинград/134/47/57 (H2N2). Видно, что обработанная рестриктазой Fok I ДНК-копия М2 гена вируса А/Ленинград/134/17/57 (H2N2) имеет дополнительную полосу, характерную для «дикого» вируса А/Ленинград/134/57 (H2N2) (8-я дорожка), что подтверждает данные литературы о гетерогенности неклонированного донора в этой позиции М2 гена.
В таблице 2 представлены результаты анализа всех значащих мутаций в геноме нового клонированного донора аттенуации А/Ленинград/134/17/К7/57 (H2N2) в сравнении с неклонированными донорами А/Ленинград/134/17/57 (H2N2) и А/Ленинград/134/47/57 (H2N2) и их «диким» предшественником - вирусом А/Ленинград/134/57 (H2N2).
Таким образом, установлено, что заявляемый донор аттенуации имеет семь значащих мутаций во внутренних генах: РВ2 (Val-478-Leu), РВ1 (Lys-265-Asn и Val-591-Ile), PA (Leu-28-Pro и Val-341-Leu), M1 (Ile-15-Val) и NS2 (Met-100-Ile).
Вакцинный штамм А/17/Калифорния/04/6 (H3N2) получен методом генетической реассортации эпидемического вируса А/Калифорния/7/04 (H3N2) с клонированным холодоадаптированным температурочувствительным донором аттенуации А/Ленинград/134/17/К7/57 (H2N2) с последующей селекцией при пониженной до 25°С температуре инкубации в присутствии антисыворотки к донору аттенуации.
Вакцинный штамм А/17/Калифорния/04/6 (H3N2) является температурочувствительным (разность в показателях инфекционной активности при температуре инкубации 33 и 40°С составляет 7,5 Ig ЭИД50/0,2 мл) и холодоадаптированным (разность в показателях инфекционной активности при температуре инкубации 33 и 25°С равна 3,5 Ig ЭИД50/0,2 мл).
Ответственный за антигенную специфичность поверхностный белок вакцинного штамма - гемагглютинин (НА) - в РТГА идентичен вирусу А/Калифорния/7/04 (H3N2), антисывороткой к которому полностью нейтрализуется.
Методом рестрикционного анализа ДНК копий генов установлено, что вакцинный штамм А/17/Калифорния/04/6 (H3N2) унаследовал семь генов, кодирующих внутренние белки (РВ1, РВ2, PA, NP, NA, M, NS) и поверхностный белок нейраминидазу (NA), - от донора аттенуации А/Ленинград/134/17/К7/57 (H2N2). Рестрикционный метод основан на ДНК амплификации участков РНК длиной около 150-300 нуклеотидов, включающих уникальные нуклеотидные последовательности, характерные только для донора аттенуации, но не для современных эпидемических вирусов гриппа [Киселева И.В., Климов А.И. Анализ мутаций в геноме холодоадаптированных штаммов вируса гриппа А с использованием расширенной модификации ПЦР-рестрикционного метода // Вопросы вирусологии. - 2002. - №6. - С.24-26]. Обработка амплифицированных фрагментов ДНК специфическими рестриктазами с последующим электрофорезом обработанных рестриктазами фрагментов ДНК в 1,7%-ном агарозном геле, содержащем 0,5 мкг/мл этидиума бромида, позволяет четко дифференцировать принадлежность генов исследуемых реассортантных штаммов к эпидемическому вирусу или донору аттенуации.
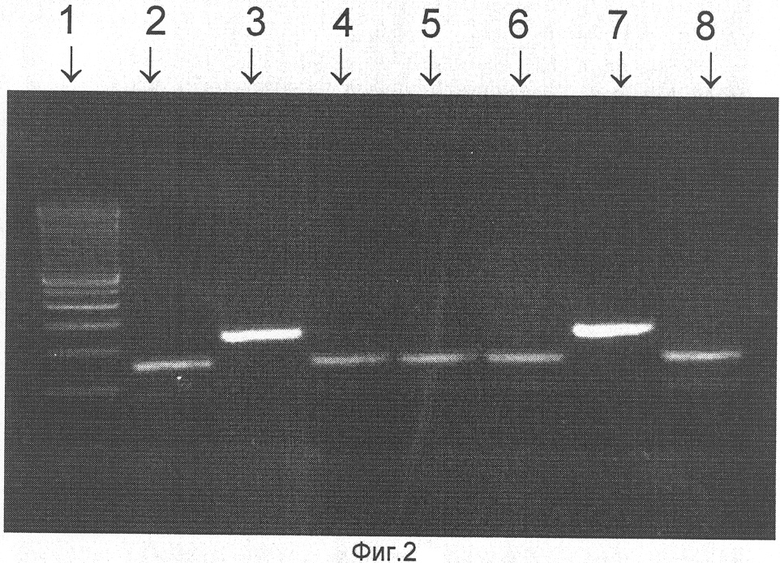
На фиг.2 в качестве примера представлена рестрикция ДНК-копии фрагмента гена РВ2 эндонуклеазой Mse I. 1-я дорожка - ДНК маркер молекулярного веса; 2-я, 5-я и 8-я дорожки - донор аттенуации; 3-я и 7-я дорожки - эпидемический вирус А/Калифорния/7/04 (H3N2); 4-я и 6-я дорожки - кандидат в вакцинные штаммы А/17/Калифорния/04/6 (H3N2). В РВ2 гене донора аттенуации в позиции нуклеотида 1459 имеется замена G→T по сравнению с современными эпидемическими штаммами, приведшая к аминокислотной замене валина эпидемических вирусов на лейцин у донора аттенуации. Донор аттенуации имеет на этом участке сайт рестрикции для экзогенной рестриктазы Mse I. У эпидемических вирусов этот рестрикционный сайт отсутствует. Таким образом, обработка всех исследуемых фрагментов ДНК данным ферментом приводит к разрезанию амплифицированного участка гена РВ2 длиной 240 нуклеотидов на два более мелких фрагмента (85 и 155 нуклеотидов), если он происходит от донора аттенуации. В случае РВ2 гена от эпидемического вируса расщепления не происходит.
Результаты рестрикционного анализа всех генов вакцинного штамма А/17/Калифорния/04/6 (H3N2) представлены в таблице 3.
Таким образом, представленный вакцинный штамм А/17/Калифорния/04/6 (H3N2) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью эпидемического вируса А/Калифорния/7/04 (H3N2), структурой генома, оптимальной для реассортантных вакцинных штаммов, температурочувствительностью и холодоадаптированностью, что коррелирует с аттенуацией для человека, характерной для донора аттенуации.
Морфология штамма - полиморфная, типичная для вируса гриппа.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность при репродукции в развивающихся куриных эмбрионах при 33-34°С в течение 48 часов - 8,0 Ig ЭИД50/0,2 мл.
Гемагглютинирующая активность - 1:1024.
Штамм проявляет генетическую стабильность биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
Пример получения вакцинного штамма А/17/Калифорния/04/6 (H3N2) представлен в прилагаемом паспорте.
ПАСПОРТ ШТАММА
1. Название штамма - А/17/Калифорния/04/6 (H3N2).
2. Серия - серия 1.
3. Метод получения - реассортация; характеристика родительских вирусов:
а) эпидемический вирус - А/Калифорния/7/04 (H3N2);
б) донор аттенуации - А/Ленинград/134/17/К7/57 (H2N2);
4. Количество пассажей - 5 в процессе реассортации.
5. Характеристика штамма:
а) оптимальные условия репродукции - 33°С, 48 часов;
б) гемагглютинирующая активность - 1:1024;
в) инфекционная активность - 8,0 Ig ЭИД50/0,2 мл;
г) чувствительность к ингибиторам - ингибиторочувствительный в РТГА с нормальной лошадиной сывороткой;
д) разность в показателях инфекционной активности при 33 и 40°С - 7,5 Ig ЭИД50/0,2 мл;
е) разность в показателях инфекционной активности при 33 и 25°С - 3,5 Ig ЭИД50/0,2 мл;
ж) структура генома реассортанта:
- гены от эпидемического вируса - НА;
- гены от донора аттенуации - РВ2, РВ1, PA, NP, M, NS, NA.
6) Характеристика штамма после лиофилизации:
а) дата лиофилизации - 11.04.2005;
б) объем материала в ампуле - 1,0 мл;
в) количество доз в ампуле - 4;
г) инфекционная активность - 7,5 Ig ЭИД50/0,2 мл;
д) гемагглютинирующая активность - 1:256.
7. Рекомендуемое разведение при вакцинации - 1:2.
8. Антигенная специфичность:
а) гемагглютинина - идентичен вирусу А/Калифорния/7/04 (H3N2) по данным РТГА с иммунной крысиной антисывороткой;
б) нейраминидазы - идентична вирусу А/Ленинград/134/17/К7/57 (H2N2) по данным ПЦР-рестрикционного анализа ДНК-копий генов.
9. Безвредность для мышей при подкожном и внутрибрюшинном введении - безвреден.
10. Бактериологический контроль:
дата проведения - 04.04.2005 г.;
результат - стерилен.
11. Контроль на отсутствие посторонних вирусов - посторонние вирусы отсутствуют.
ШТАММ А/17/КАЛИФОРНИЯ/04/6 (H3N2) АРЕАКТОГЕНЕН И ИММУНОГЕНЕН ДЛЯ ВЗРОСЛЫХ ЛИЦ
Пример 1. При вакцинации 51 взрослого человека интраназально реассортантным вакцинным штаммом А/17/Калифорния/04/6 (H3N2) с инфекционной активностью 7,5 Ig ЭИД50/0,2 мл в разведении 1:2 в объеме 0,5 мл сильных температурных реакций с повышением температуры свыше 38,5°С не наблюдалось. Слабые температурные реакции (до 37,5°С) наблюдались в 1,96% случаев. Средние температурные реакции с кратковременным повышением температуры в диапозоне 37,6-38,5°С наблюдались также в 1,96% случаев. Катаральные явления отмечены в 7,84% случаев. Результаты обследования приведены в таблице 4.
В получившей плацебо группе из 48 лиц температурные реакции не наблюдались. Катаральные явления отмечены в 2,08% случаев.
Показатель реактогенности (разница в проценте средних реакций у привитых вакциной и получивших плацебо) составил 1,96%.
При изучении в реакции РТГА сывороток крови 26 серонегативных вакцинированных лиц был обнаружен 4-кратный и более прирост сывороточных антител к эпидемическому штамму А/Калифорния/7/04 (H3N2) в 50% случаев. Средние геометрические титры антител во вторых сыворотках у лиц с 4-кратными и более приростами антител составили 1:34,09. Результаты серологического исследования приведены в таблице 5.
Таким образом, испытания на волонтерах подтвердили, что вакцинный штамм А/17/Калифорния/04/6 (H3N2) по показателям реактогенности и иммуногенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 от 26.03.2003 г. на живую сухую гриппозную аллантоисную вакцину для интраназального применения.
ШТАММ А/17/КАЛИФОРНИЯ/04/6 (H3N2) АРЕАКТОГЕНЕН ДЛЯ ДЕТЕЙ 3-14 ЛЕТ
До 2004 г. реассортантные вакцинные штаммы живой гриппозной вакцины для детей и для взрослых готовили на двух разных донорах аттенуации. Вакцинные штаммы живой гриппозной вакцины для взрослых готовили на доноре аттенуации А/Ленинград/134/17/57 (H2N2) [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука. - 1994. - 151 с.], а вакцинные штаммы живой гриппозной вакцины для детей - на более аттенуированном доноре А/Ленинград/134/47/57 (H2N2) [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука. - 1994. - 151 с.]. В 2003 г. Комитет медицинских иммунобиологических препаратов счел целесообразным рекомендовать «Вакцину гриппозную аллантоисную интраназальную живую сухую для взрослых» для иммунизации детей в возрасте 3-6 лет с внесением соответствующих изменений в «Инструкцию по применению» препарата [Инструкция по применению вакцины гриппозной аллантоисной интраназальной живой сухой. - Утверждена Главным санитарным врачом РФ Г.Г.Онищенко 16.06.2004 г.].
В этой связи нами была изучена реактогенность вакцинного штамма А/17/Калифорния/04/6 (H3N2) на детях.
Пример 2. Группу из 67 детей в возрасте 3-14 лет вакцинировали интраназально в объеме 0,5 мл реассортантным вакцинным штаммом А/17/Калифорния/04/6 (H3N2) с инфекционной активностью 7,5 Ig ЭИД50/мл в разведении 1:2. Группа детей того же возраста из 30 человек получила плацебо. Результаты исследований приведены в таблице 6.
В группе вакцинированных детей сильные температурные реакции с повышением температуры свыше 38,5°С не наблюдались. Средние реакции с кратковременным повышением температуры до 37,6-38,5°С наблюдались в 1,5% случаев. Слабые температурные реакции в диапазоне до 37,5°С также были отмечены в 1,5% случаев. Признаки интоксикации (головная боль) наблюдались у 3,0% привитых. Катаральные явления отмечены в 4,5% случаев.
В группе детей, получивших плацебо, отмечены слабые температурные реакции (до 37,5°С) в 3,3% случаев. Признаки интоксикации (головная боль) наблюдались в 3,3% случаев. Катаральные явления отмечены у 6,7%.
Показатель реактогенности (разница в проценте средних реакций у привитых вакциной и получивших плацебо) составил 1,5%.
Испытания на волонтерах подтвердили, что вакцинный штамм А/17/Калифорния/04/6 (H3N2) по показателям реактогенности и иммуногенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 от 26.03.2003 г. на живую сухую гриппозную аллантоисную вакцину для интраназального применения.
На основе вышесказанного предлагаемый по изобретению вакцинный штамм вируса гриппа может быть использован для профилактики гриппа как у взрослых, так и у детей с трехлетнего возраста, что подтверждают результаты изучения его реактогенности для разных возрастных групп.
Фенотипическая характеристика неклонированного донора аттенуации А/Ленинград/134/17/57 (H2N2) (Лен/17) и клонированного донора А/Ленинград/134/17/К7/57 (H2N2) (К7) в сравнении с вирусом «дикого» типа А/Ленинград/134/57 (H2N2) (Лен/wt)
Кодирующие мутации во внутренних генах неклонированных доноров аттенуации А/Ленинград/134/17/57 (Н2N2) (Лен/17) и А/Ленинград/134/47/57 (H2N2) (Лен/47) и клонированного нового донора А/Ленинград/134/17/К7/57 (H2N2) (К7) в сравнении с вирусом «дикого» типа А/Ленинград/134/57 (H2N2) (Лен/wt)
Перечень праймеров и рестриктаз, использованных для изучения состава генома реассортантного вакцинного штамма А/17/Калифорния/04/6 (H3N2), полученного на основе эпидемического вируса А/Калифорния/7/04 (H3N2) и клонированного донора аттенуации А/Ленинград/134/17/К7/57 (H2N2)


Реактогенность вакцинного штамма А/17/Калифорния/04/6 (H3N2) для детей 3-14 лет
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/КАЛИФОРНИЯ/2009/38 (H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2009 |
|
RU2413765C1 |
| ШТАММ ВИРУСА ГРИППА А/17/ВИКТОРИЯ/2011/89 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2012 |
|
RU2532844C2 |
| ШТАММ ВИРУСА ГРИППА А/17/ИНДИАНА/11/72 (H3N2v) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2013 |
|
RU2545706C1 |
| ШТАММ ВИРУСА ГРИППА А/17/Техас/2012/30 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2013 |
|
RU2563352C2 |
| Вакцинный штамм вируса гриппа А/17/ГОНКОНГ/2014/8296 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2606019C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Тасмания/2020/151 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825672C1 |
| Реассортантный штамм вируса гриппа А/17/Ньюкасл/2018/22 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783887C1 |
| ШТАММ ВИРУСА ГРИППА А/17/Ануи/2013/61 (H7N9) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ИНТРАНАЗАЛЬНОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2013 |
|
RU2563351C2 |
| Реассортантный штамм вируса гриппа А/17/Южная Австралия/2019/122 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783877C1 |
| Реассортантный штамм вируса гриппа А/17/Гонконг/2019/2573 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783894C1 |
Изобретение относится к области вирусологии и медицины. Вакцинный штамм А/17/Калифорния/04/6 (H3N2) - реассортант, полученный путем скрещивания эпидемического вируса А/Калифорния/7/04 (H3N2) с клонированным холодоадаптированным температурочувствительным вирусом А/Ленинград/134/17/К7/57 (H2N2). Штамм А/Ленинград/134/17/К7/57 (H2N2), полученный для этого, является донором аттенуации, безвредным для людей, свойства которого дают возможность гарантированно получать реассортантные вакцинные штаммы из вновь появляющихся эпидемических вирусов. Штамм А/17/Калифорния/04/6 (H3N2) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 33°С. Штамм характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал ген, кодирующий основной поверхностный антиген вируса (гемагглютинин), от эпидемического вируса и остальные семь генов, кодирующих негликозилированные белки и поверхностный белок нейраминидазу, от донора аттенуации. Штамм А/17/Калифорния/04/6 (H3N2) ареактогенен для взрослых и для детей при интраназальном введении. Изобретение может быть использовано в медицине. 2 н.п. ф-лы, 2 ил., 6 табл.
| Youil R | |||
| et al | |||
| Халат для профессиональных целей | 1918 |
|
SU134A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| ШТАММ ВИРУСА ГРИППА А/17/ПАНАМА/99/242(Н3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 2003 |
|
RU2248395C1 |
Авторы
Даты
2008-01-20—Публикация
2006-01-10—Подача