Область техники, к которой относится изобретение
Данное изобретение относится к хромсодержащим композициям и их получению и применению для каталитической переработки углеводородов и/или галогенированных углеводородов.
Предпосылки создания изобретения
Хорошо известно, что α-Cr2O3 и α-Fe2O3 имеют в общем структуру α-Al2O3 (корунда) с ионами М+3, занимающими октаэдральные узлы в гексагональной плотно упакованной оксидной решетке. Напротив, NiO и СоО имеют искаженные кубические решетки, тогда как Со3О4 имеет структуру нормальной шпинели. Указанные основные структуры описаны в общеизвестных научных трудах; см., например, Structural Inorganic Chemistry by A.F. Wells, 5-th ed. Clarendon Press, Oxford, UK (1986), pp. 538, 543-545, 550. γ-Оксид хрома (CrO2,44) описан в Wilhelmi, Acta Chemica Scandinavica, vol. 22, pp. 2565-2573 (1968).
Были получены многочисленные смешанные оксиды металлов, у которых катионные узлы решетки заняты различными ионами металлов. Например, известны твердые растворы типа (CrmFe1-m)2O3, где 0<m<1. Указанные материалы были получены по стандартной керамической или золь-гель технологии, как описано в работах Music et al., J. Materials Science, vol.31, pp. 4067-4076 (1996) и Bhattacharya et al., J. Materials Science, vol. 32, pp. 577-560 (1997).
Смешанные Cr-Ni-оксиды являются известными (см., например, Chamberland and Cloud, J. of Applied Physics, vol. 40, pp. 434-435 (1969), где рассматривается NiCrO3, который имеет структуру, подобную корунду; Muller et al., Z. Kristallogr., Kristallgeom., Kristallphys., Kristallchem., vol. 130, pp. 112-120 (1969); Prince, J. of Applied Physics, vol. 32, pp. 68S-69S (1961); и Nowotny et al., Bulletin of Polish Academy of Sciences, Chemistry, vol. 33, pp. 111-119 (1985)). Смешанные Cr-Co-оксиды, имеющие шпинельную структуру, являются известными (см., например, Bracconi et al., Ann. Chim. Fr., vol. 4, pp. 331-338 (1979) и Hanck and Laitinen, J. Inorg. Nucl. Chem., vol. 33, pp. 63-73 (1971)).
CrCoO3 упоминается в качестве соединительного материала в узле топливного элемента (см. Chem. Abs. 118:9397). Различные смешанные оксиды металлов, содержащие кобальт и хром, также рассматриваются в работах Castiglioni et al., J. Solid State Chemistry, vol. 152, 526-532 (2000); Nowotny et al., J. Am. Ceram. Soc., vol. 65, pp. 192-196 (1982); и Zhang et al., Journal of Power Sources, vol. 83, pp. 121-127 (1999).
Некоторые оксиды металлов используются в качестве катализаторов и/или предшественников катализаторов в получении фторированных углеводородов. Оксид хрома (III), в частности, используется, т.к. было установлено, что он может быть фторирован HF при повышенной температуре с получением смеси частиц фторида хрома и оксифторида хрома, которые являются активными катализаторами превращения C-Cl-связей в C-F-связи в присутствии HF. Данное превращение C-Cl-связей в C-F-связи под действием HF, обычно известное как галогенный обмен, является ключевой стадией во многих способах получения фторированных углеводородов.
Композиции оксида хрома, используемые в качестве предшественников катализаторов, могут быть получены различными способами или могут принимать различные формы. Оксид хрома, подходящий для реакций фторирования в парообразной фазе, может быть получен восстановлением триоксида Cr(VI), дегидратацией гидроксида хрома или осаждением солей Cr(III) основаниями (см. патент США № 3258500). Другой используемой формой оксида хрома является гидроксид гексагонального оксида хрома с низким содержанием иона щелочного металла, как рассмотрено в патенте США № 3978145. Соединения, такие как MF4 (M=Ti, Th, Ce), MF3 (M=Al, Fe, Y) и MF2 (M=Ca, Mg, Sr, Ba, Zn), были добавлены к гидроксиду гексагонального оксида хрома для увеличения срока службы катализатора, как рассмотрено в патенте США № 3992325. Формой оксида хрома, который является предшественником особенно активного катализатора фторирования, является форма, полученная пиролизом дихромата аммония, как рассмотрено в патенте США № 5036036.
Было рассмотрено введение других соединений (например, других солей металлов) в хромсодержащие катализаторы фторирования на носителе и без носителя. Австралийский патент № AU-A-8034/94 рассматривает блочные катализаторы или катализаторы на носителе на основе оксида хрома (или оксидов хрома) и, по меньшей мере, одного другого каталитически активного металла (например, Mg, V, Mn, Fe, Co, Ni или Zn), в которых большая часть оксида (оксидов) находится в кристаллическом состоянии (и когда катализатором является блочный катализатор, его удельная поверхность после активации HF составляет не менее 8 м2/г). Рассмотренные кристаллические фазы включают Cr2O3, CrO2, NiCrO3, NiCrO4, NiCr2O4, MgCrO4, ZnCr2O4 и смеси указанных оксидов. Австралийский патент AU-А-29972/92 рассматривает массовый катализатор на основе оксидов хрома и никеля, в которых атомное соотношение Ni:Cr находится между 0,05 и 5. Опубликованная заявка на патент США № US 2001/0011061 А1 рассматривает хромдиоксидсодержащие катализаторы фторирования (необязательно содержащие Mg, Zn, Co и Ni), в которых диоксид хрома является, по меньшей мере, частично кристаллическим. Фторированные катализаторы, содержащие кобальт и хром в комбинации (например, пропитанные на носителе), рассмотрены среди других в патенте США № 5185482. Патент США № 5559069 рассматривает гомогенно диспергированные многофазные каталитические композиции, характеризующиеся дисперсными фазами некоторых фторидов двухвалентных металлов (некоторых фторидов Mn, Co, Zn, Mg и/или Cd) и некоторых фторидов трехвалентных металлов (фторидов Al, Ga, V и/или Cr).
Остается потребность в катализаторах галогенного обмена, которые могут использоваться для таких способов, как селективное фторирование и хлорфторирование насыщенных и ненасыщенных углеводородов, хлоруглеводородов, хлорфторуглеводородов и хлорфторуглеродов, фторирование ненасыщенных фторированных углеводородов, изомеризация и диспропорционирование фторированных органических соединений, дегидрофторирование фторуглеводородов и хлордефторирование фторированных углеводородов.
Краткое описание изобретения
Данное изобретение предусматривает кристаллический альфа-оксид хрома, где от примерно 0,05% ат. до примерно 2% ат. атомов хрома в решетке альфа-оксида хрома замещено атомами никеля, и, необязательно, дополнительные атомы хрома в решетке альфа-оксида хрома замещены атомами трехвалентного кобальта, при условии, что общее количество атомов никеля и атомов трехвалентного кобальта в решетке альфа-оксида хрома составляет не более 6% ат.
Данное изобретение также предусматривает хромсодержащую каталитическую композицию, содержащую в качестве хромсодержащего компонента, указанный кристаллический замещенный альфа-оксид хрома.
Данное изобретение также предусматривает способ получения композиции, содержащей указанный кристаллический замещенный альфа-оксид хрома. Способ включает (а) соосаждение твердого вещества добавлением гидроксида аммония (водного аммиака) к водному раствору растворимой соли двухвалентного никеля, растворимой соли трехвалентного хрома и, необязательно, растворимой соли двухвалентного или трехвалентного кобальта, который содержит не менее трех молей нитрата (т.е., NO3 -) на моль хрома (т.е., Cr3+) в растворе, имеет концентрацию никеля от примерно 0,05% мол. до примерно 2% мол. от общего содержания никеля, хрома и кобальта (если присутствует) в растворе и имеет общую концентрацию никеля и кобальта (если присутствует) не более 6% мол. от общего содержания никеля, хрома и кобальта (если присутствует) в растворе; и затем вводят в раствор не менее трех молей аммония (т.е., NH4 +) на моль хрома (т.е., Cr3+); (b) собирание соосажденного твердого вещества, образованного на стадии (а); (с) сушку собранного твердого вещества; и (d) прокаливание высушенного твердого вещества.
Данное изобретение также предусматривает хромсодержащую каталитическую композицию, содержащую хромсодержащий компонент, полученный обработкой указанного кристаллического замещенного альфа-оксида хрома фторирующим агентом (например, фторидом водорода).
Данное изобретение также предусматривает способ изменения распределения фтора (т.е., содержания и/или размещения) в углеводороде или галогенированном углеводороде в присутствии катализатора. Способ характеризуется применением в качестве катализатора композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из указанных кристаллических замещенных альфа-оксидов хрома и указанных обработанных замещенных альфа-оксидов хрома.
Краткое описание чертежей
На фиг.1 представлен спектр, полученный спектроскопией с рассеянием энергии, образца смешанного никель- и кобальтзамещенного альфа-оксида хрома, номинально содержащего 3% ат. кобальта и 2% ат никеля.
На фиг.2 представлен спектр, полученный спектроскопией с рассеянием энергии, образца альфа-оксида хрома без никелевого или кобальтового замещения.
На фиг.3 представлен спектр, полученный спектроскопией с рассеянием энергии, образца никель-хромовой шпинели.
На фиг.4 представлен спектр, полученный спектроскопией с рассеянием энергии, образца кобальт-хромовой шпинели.
На фиг.5 представлен спектр, полученный спектроскопией с рассеянием энергии, образца никельзамещенного альфа-оксид хрома, номинально содержащего 2% ат. никеля.
На фиг.6 представлен график функции радиального распределения (т.е., вероятности нахождения атома на некотором расстоянии r от центрального атома), связанной с локальной атомной структурой вокруг (А) центрального атома никеля в NiO, (B) никеля в образце NiCr2О4, (C) центрального атома хрома в альфа-Cr2O3 и (D) никеля в образце смешанного никель- и кобальтзамещенного альфа-оксида хрома, номинально содержащего 3% ат. кобальта и 2% ат. никеля.
На фиг.7 представлен график функции радиального распределения, связанной с локальной атомной структурой вокруг (А) центрального атома кобальта в СоО, (B) центрального атома кобальта в Со3О4, (C) центрального атома хрома в альфа-Cr2O3 и (D) атома кобальта в образце смешанного никель- и кобальтзамещенного альфа-оксида хрома, номинально содержащего 3% ат. кобальта и 2% ат. никеля.
На фиг.8 представлен график функции радиального распределения, связанной с локальной атомной структурой вокруг (А) центрального атома никеля в NiO, (B) никеля в образце NiCr2О4, (C) центрального атома хрома в альфа-Cr2O3 и (D) атома никеля в образце никельзамещенного альфа-оксида хрома, номинально содержащего 2% ат. никеля.
Подробное описание изобретения
Новые композиции данного изобретения содержат замещенный альфа-оксид хрома, содержащий никель или как никель, так и кобальт, который сохраняет структуру корунда. Данное изобретение включает каталитическую композицию, содержащую указанный кристаллический замещенный α-Cr2O3. Содержание никеля в замещенном альфа-оксиде хрома составляет от примерно 0,05% ат. до примерно 2% ат. общего содержания никеля, хрома и кобальта (если присутствует) в альфа-оксиде хрома. Общее содержание никеля и кобальта в альфа-оксиде хрома составляет не более 6% ат. общего содержания никеля, хрома и кобальта. Кристаллические замещенные альфа-оксиды хрома имеют общую формулу
α-NixCoyCr2-x-yО3, где х=0,001-0,04, и y составляет от 0 до 0,12-х.
Композиции настоящего изобретения могут быть получены способом, описанным выше, с использованием соосаждения. В обычной технологии соосаждения получают водный раствор солей никеля (II) и хрома (III) и, необязательно, солей кобальта (II) или кобальта (III). Относительные концентрации солей никеля (II), кобальта и хрома (III) в водном растворе определяются размером мольного процентного содержания никеля и кобальта относительно хрома, желательного в получаемом катализаторе. Концентрация хрома (III) в водном растворе находится обычно в интервале от 0,3 до 3 моль/л, причем предпочтительная концентрация составляет 0,75-1,5 моль/л. Солями хрома (III), подходящими для получения водного раствора, являются нитрат, сульфат, ацетат, формиат, оксалат, фосфат, бромид и хлорид и различные гидратированные формы указанных солей. Другие соли хрома (III), которые используются для получения водных растворов, включают гексакоординационные комплексы формулы
[CrL6-zAz]+3-z, где каждый L представляет собой нейтральный (т.е., незаряженный) лиганд, выбранный из группы, состоящей из H2O, NH3, первичных, вторичных или третичных органических С1-С4-аминов, С1-С4-алкилнитрилов, или пиридина, где каждый А представляет собой анионный лиганд, выбранный из группы, состоящей из фторида, хлорида, бромида, иодида, гидроксида, нитрита и нитрата, и где z имеет значение от 0 до 3 включительно. Включенными являются нейтральные бидентатные лиганды, такие как этилендиамин, которые являются эквивалентными двум L, в которых они могут занимать два координационных узла. Также включенными являются анионные бидентатные лиганды, такие как С1-С4-карбоксилат, которые могут занимать два координационных узла. Также включенными являются дианионные лиганды, такие как сульфат, которые являются эквивалентными двум А-лигандам и могут занимать более одного координационного узла.
Соли, содержащие щелочные металлы, такие как сульфат хрома-калия, не являются предпочтительными, потому что присутствие щелочных металлов может мешать каталитической активности катализатора (см. патент США 4843181). Хром(VI)содержащие предшественники, такие как CrO3, хотя не являются предпочтительными, могут использоваться, но требуют восстановления до Cr(III) соединением, таким как этанол, перед осаждением.
Нитрат хрома (III) или его гидратированные формы, такие как [Cr(NO3)3(H2О)9], являются наиболее предпочтительной солью хрома (III) для получения указанного водного раствора.
Солями никеля (II), подходящими для получения водного раствора, являются нитрат, ацетат, ацетилацетонат, сульфат, формиат, оксалат, бромид, хлорид и фторид и различные гидратированные формы указанных солей. Гидрат нитрата никеля (II) (например, [Ni(NO3)2(H2О)6]) является наиболее предпочтительной солью никеля (II).
Солями кобальта (II), подходящими для получения водного раствора, являются нитрат, сульфат, формиат, оксалат, бромид и хлорид и различные гидратированные формы указанных солей. Соли, содержащие щелочные металлы, такие как бисульфат кобальта - калия, не являются предпочтительными, потому что присутствие щелочных металлов может мешать каталитической активности. Гидрат нитрата кобальта (II) (например, [Co(NO3)2(H2O)6]) является наиболее предпочтительной солью кобальта (II).
Соли кобальта (III), которые используются для получения водных растворов, включают гексакоординационные комплексы формулы [CoL6-zAz]+3-z, где каждый L представляет собой нейтральный (т.е., незаряженный) лиганд, выбранный из группы, состоящей из H2O, NH3, первичных, вторичных или третичных органических С1-С4-аминов, С1-С4-алкилнитрила, или пиридина, где каждый А представляет собой анионный лиганд, выбранный из группы, состоящей из фторида, хлорида, бромида, иодида, гидроксида, нитрита и нитрата, и где z имеет значение от 0 до 3 включительно. Включенными являются нейтральные бидентатные лиганды, такие как этилендиамин, которые являются эквивалентными двум L, в которых они могут занимать два координационных узла. Также включенными являются анионные бидентатные лиганды, такие как С1-С4-карбоксилат, которые могут занимать два координационных узла. Также включенными являются дианионные лиганды, такие как сульфат, которые являются эквивалентными двум А-лигандам и могут занимать более одного координационного узла. Предпочтительными кобальт (III) исходными материалами являются гексамминные соли (например, [Co(NH3)6]+3, где противоионом является хлорид или нитрат. Гексамминкобальт (III) хлорид (например, [Co(NH3)6]Cl3) является наиболее предпочтительной солью кобальта (III).
Водный раствор солей никеля (II) и хрома (III) и, необязательно, солей кобальта (II) и кобальта (III) может быть затем выпарен либо в вакууме, либо при повышенной температуре с получением твердого вещества, которое затем прокаливают.
Предпочтительно, однако, водный раствор солей никеля (II) и хрома (III) и, необязательно, солей кобальта затем обрабатывают основанием, таким как гидроксид аммония (водный аммиак), с осаждением никеля и хрома и, необязательно, кобальта в виде гидроксидов. Основания, содержащие щелочные металлы, такие как гидроксид натрия или калия, или карбонаты, могут использоваться, но не являются предпочтительными. Введение гидроксида аммония в водный раствор солей никеля (II) и хрома (III) и, необязательно, соли (солей) кобальта обычно выполняют постепенно в период времени 1-12 ч. рН раствора регулируют в процессе введения основания. Конечный рН обычно находится в интервале 6,0-11,0, предпочтительно, от примерно 7,5 до примерно 9,0, и наиболее предпочтительно, от примерно 8,0 до 8,7. Осаждение смеси гидроксид никеля/гидроксид кобальта/гидроксид хрома обычно проводят при температуре примерно 15-60°С, предпочтительно, от примерно 20°С до примерно 40°С. После введения гидроксида аммония смесь обычно перемешивают в течение до 24 ч.
Известны способы получения, где избыток нитрата аммония (т.е., более трех молей нитрата аммония на моль хрома) присутствует в водном растворе. Например, помимо нитрата аммония, уже присутствующего в результате взаимодействия гидроксида аммония с нитратом хлора, от примерно 0,1 моль до примерно 0,7 моль дополнительного нитрата аммония на моль хрома может быть введено в раствор до, в процессе или после соосаждения композиций. Неожиданно авторами было найдено, что введение избытка нитрата аммония в осажденную смесь гидроксидов никеля и хрома и необязательно кобальта до стадии дегидратации снижает размер частиц α-NixCoyCr2-x-yO3-фазы, что, в свою очередь, увеличивает площадь поверхности данной фазы и активность катализатора.
После введения нитрата аммония в смесь ее перемешивают в течение примерно 0,5-10 ч, предпочтительно, в течение примерно одного-пяти часов, при температуре от примерно 20°С до примерно 60°С. Смесь затем сушат и прокаливают, как указано ниже.
Другие агенты, которые служат указанной цели, включают водный пероксид водорода (1-30% растворы), озон, надкислоты, такие как надуксусная кислота, и персульфат аммония. Такие агенты, как галогены, могут использоваться, но не являются предпочтительными. Агенты, содержащие щелочные металлы, такие как персульфат калия или перборат натрия, могут также использоваться, но не являются предпочтительными.
После того, как заканчивается осаждение смеси гидроксидов никеля, хрома и, необязательно, кобальта, и введены, если желательно, нитрат аммония или другие агенты, смесь сушат выпариванием.
Необязательно, осажденная смесь гидроксидов металлов может быть собрана и, если желательно, промыта деионизованной водой перед сушкой. Это может влиять на активность катализатора.
После того, как смесь гидроксидов металлов высушивают, нитратные соли тогда разлагаются при нагревании твердого вещества от примерно 250°С до примерно 350°С. Полученное твердое вещество затем прокаливают при температуре от примерно 375°С до примерно 1000°С, предпочтительно, от примерно 400°С до примерно 600°С. Температура прокаливания может влиять на активность катализаторов и, в свою очередь, на распределение продукта, когда катализаторы используются для изменения фторораспределения в углеводородах и галогенированных углеводородах (см. примеры 9, 10, 11 и 12).
Прокаливание, предпочтительно, проводят в присутствии кислорода, наиболее предпочтительно, в присутствии воздуха.
Композиции оксидов металлов данного изобретения могут быть определены хорошо известными аналитическими методами, включая рентгеновскую абсорбционную спектроскопию ((XAS) (РАС)), диффракцию рентгеновских лучей ((XRD) (ДРЛ)), трансмиссионную электронную микроскопию ((ТЕМ)(ТЭМ)), энергорассеивающую спектроскопию ((EDS)(ЭРС)). ЭРС является аналитическим методом, используемым в сочетании со сканирующей или аналитической ТЭМ.
После прокаливания полученные никельзамещенные кристаллиты визуально не отличаются от α-Cr2O3 методом ТЭМ. Кроме того, результаты рентгеновских и электронно-диффракционных исследований полностью соответствуют структуре α-Cr2O3 с некоторой сжатой или расширенной решеткой пропорционально количеству Ni и, если присутствует, Co(III), которое замещает Cr(III) в структуре. Поэтому делается вывод, что составы имеют общую формулу α-NixСоyCr2-х-yО3, где х=0,001-0,04, и y составляет от 0 до 0,12-х.
Присутствие различных никель/хром- и никель/кобальт/ хромсодержащих композиций данного изобретения четко подтверждается элементарным анализом с использованием ЭРС. На фиг.1 представлен ЭРС-спектр образца смешанного никель- и кобальтзамещенного α-Cr2O3, номинально содержащего 2% ат. никеля и 3% ат. Со. Для сравнения на фиг.2 представлен ЭРС-спектр α-Cr2O3 без никелевого или кобальтового замещения. На фиг.3 и 4 представлен ЭРС-спектр коммерчески доступных хромита никеля NiCr2O4 и хромита кобальта CoCr2O4, соответственно. На фиг.5 представлен ЭРС-спектр образца никельзамещенного α-Cr2O3, номинально содержащего 2% ат. никеля. На каждой из указанных пяти фигур интенсивность рентгеновского излучения I, представляющая тысячи импульсов, изображена в зависимости от уровня энергии Е, представляющей тысячи электрон-Вольт (кэВ). Пики на каждом спектре соответствуют присутствию некоторых элементов.
Присутствие никеля и кобальта ясно показано на ЭРС-спектре на фиг.1, а присутствие никеля (но не кобальта) ясно показано на фиг. 5, тогда как пики никеля и кобальта отсутствуют на фигуре 2. Относительные высоты 2:1 для Kα пиков Cr (атомная масса 52) и Ni (атомные массы 58 и 60), соответственно, на фиг.3 и относительные высоты 2:1 для Kα пиков Cr и Со (атомная масса 59) на фиг.4 указывают, что ЭРС-данные основаны на количественной базе.
РАС и ДРЛ данные были получены для композиции, которая составляет номинально 100% Cr (без введения кобальта), для композиции, которая составляет номинально 95% Cr, 3% Co и 2% Ni, для композиции, которая составляет номинально 98% Cr и 2% Ni, и для композиции, которая составляет номинально 95% Cr и 5% Ni. РАС и ДРЛ анализ четко показывает, что кобальт и никель замещают хром в α-Cr2O3.
ДРЛ-результаты для композиции, которая номинально составляет 2% ат. никеля, 3% ат. кобальта и 95% ат. хрома, показаны в таблице 1. Диффракционные пики, имеющие d-расстояния 3,1176, 1,9144, 1,3559, 1,2440 и 1,1076, обусловлены внутренним эталоном кремния, введенным в образец для калибрования диффрактометра. Все другие диффракционные пики могут быть отнесены к α-Cr2O3-структуре со слегка сниженным объемом элементарной ячейки.
ДРЛ-результаты для композиции, которая номинально составляет 2% ат. никеля и 98% ат. хрома, показаны в таблице 2. Диффракционные пики, имеющие d-расстояния 3,1336, 1,92, 1,6375, 1,3579, 1,246 и 1,1085, обусловлены внутренним эталоном кремния, введенным в образец для калибрования диффрактометра. Все другие диффракционные пики могут быть отнесены к α-Cr2O3-структуре с слегка увеличенным объемом элементарной ячейки.
ДРЛ-результаты для композиции Ni- и Со-замещенного α-Cr2O3, которая номинально содержит 95% ат. Cr, 2% ат. Ni и 3% ат. Со
ДРЛ-результаты для композиции Ni-замещенного α-Cr2O3, которая номинально содержит 98% ат. Cr и 2% ат. Ni
На фиг.6, 7 и 8 представлена функция радиального распределения ((RDF)(ФРР)) для нескольких материалов. Функция радиального распределения представляет вероятность нахождения атома на некотором расстоянии r от центрального атома. Эти вероятности отягощены факторами, которые зависят от типа атома. Таким образом, ФРР является отображением локальной атомной структуры вокруг центрального атома. ФРР получается Фурье-преобразованием данных расширенного поглощения рентгеновских лучей тонкой структурой (EXAFS) и может быть представлена графической зависимостью безразмерной характеристики Фурье-преобразования F от расстояния разделения пары в ангстремах. В упрощенной форме можно видеть пик на ФРР-графике как показатель расстояния, на котором имеется координационная сфера вокруг центрального атома. Ожидается небольшое различие между фактическим расстоянием разделения и "r", показанным на графике, когда коррекция не принимается в расчет для фазового сдвига от обратного рассеяния возбужденных электронов.
На фиг.6 представлена графическая зависимость F от расстояния разделения пары r (показанного в ангстремах, неоткорректированного для фазового сдвига) для каждого из четырех материалов. На фиг.6 показаны кривая А, представляющая локальную структуру вокруг никеля в NiO, кривая В, представляющая локальную структуру вокруг никеля в NiCr2О4, кривая С, представляющая локальную структуру вокруг хрома в α-Cr2O3, и кривая D, представляющая локальную структуру вокруг никеля в образце смешанного никель- и кобальтзамещенного альфа-оксида хрома, номинально содержащего 3% ат. кобальта и 2% никеля. Шпинельная фаза не обнаружена электронной микроскопией в данном образце, так что считается, что все атомы Ni и Со связаны с α-Cr2O3-фазой либо как отдельное металлоксидное покрытие, либо как заместитель Cr в α-Cr2O3-решетке.
На фиг.7 представлена графическая зависимость F от расстояния разделения пары r (показанного в ангстремах, неоткорректированного для фазового сдвига) для каждого из четырех материалов. На фиг.7 показаны кривая А, представляющая локальную структуру вокруг кобальта в СоО, кривая В, представляющая локальную структуру вокруг кобальта в Со3О4, кривая С, представляющая локальную структуру вокруг хрома в α-Cr2O3, и кривая D, представляющая локальную структуру вокруг кобальта в таком же образце смешанного никель- и кобальтзамещенного альфа-оксида хрома, как показано на фиг.6 (номинально содержащего 3% ат. кобальта и 2% ат. никеля).
На фиг.8 представлена графическая зависимость F от расстояния разделения пары r (показанного в ангстремах, неоткорректированного для фазового сдвига) для каждого из четырех материалов. На фиг.8 показаны кривая А, представляющая локальную структуру вокруг никеля в NiO, кривая В, представляющая локальную структуру вокруг никеля в NiCr2О4, кривая С, представляющая локальную структуру вокруг хрома в α-Cr2O3, и кривая D, представляющая локальную структуру вокруг никеля в образце никельзамещенного альфа-оксида хрома, номинально содержащего 2% ат. никеля. Шпинельная фаза не обнаружена электронной микроскопией в данном образце, так что считается, что все атомы Ni связаны с α-Cr2O3-фазой либо как отдельное металлоксидное покрытие, либо как заместитель Cr в α-Cr2O3-решетке.
Кривая на фиг.6, представляющая локальную структуру вокруг никеля в смешанном никель- и кобальтзамещенном альфа-оксиде хрома, и кривая на фиг.7, представляющая локальную структуру вокруг кобальта в той же композиции, показывают, что локальная атомная структура вокруг Ni и Со в данном образце не имеет сходства со структурой ожидаемых общих никель- и кобальтоксидных фаз, но очень подобна структуре Cr в α-Cr2O3-фазе. Подобное заключение может быть сделано при сравнении кривых на фиг.8; а именно, что локальная атомная структура вокруг Ni в образце Cr/Ni 98/2 не имеет сходства со структурой ожидаемой общей никельоксидной фазы, но очень похожа на структуру Cr в α-Cr2O3-фазе.
В таблице 3 приведены параметры элементарной ячейки и объем элементарной ячейки для незамещенного альфа-оксида хрома, а также для трех композиций замещенного альфа-оксида хрома. Изменение объема элементарной ячейки может быть понято в плане различий ионных радиусов замещенных металлов. Согласно данным, приведенным в работе Shannon and Prewitt, Acta Crystallografica, Volume B25, pages 925-945 (1969), ионные радиусы высокоспинового Cr+3, низкоспинового Со+3, низкоспиновых Ni+3 и Ni+2 составляют 62 пм, 53 пм, 56 пм, 60 пм и 69 пм, соответственно. Как указано в одновременно рассматриваемой заявке на патент США CL-2099, замещение Cr+3 на Со+3 в α-Cr2O3-решетке дает в результате незначительное сокращение элементарной ячейки. В случае настоящего изобретения, где никель или как никель, так и кобальт замещают хром в α-Cr2O3-решетке, элементарная ячейка может расширяться или сокращаться в зависимости от состояния окисления и спинового состояния никеля и от того, присутствует ли кобальт или нет.
Характеристики металлзамещенного альфа-оксида хрома (III)
0,00002 нм и 0,000013 нм3, соответственно.
Результаты для композиций кобальтзамещенного альфа-оксида хрома, рассмотренные в одновременно рассматриваемой заявке на патент США № 60/405220 [CL2099 US PRV], зарегистрированной 22 августа 2002 г. показывают, что предел растворимости для кобальта в α-Cr2O3-фазе составляет около 6% ат. РАС- и ДРЛ-данные для композиций никельзамещенного альфа-оксида хрома, содержащих номинально 2% никеля и 5% никеля, показывают, что предел растворимости для никеля в α-Cr2O3 составляет около 2% ат. (см. примеры получения 7 и 8).
Другие фазы, такие как хром-никель- и хром-кобальт-шпинельные фазы, могут присутствовать в хромоксидных композициях настоящего изобретения, в частности, при высоком содержании кобальта или никеля. Присутствие указанных фаз определено методами ЭРС, ТЭМ и РАС.
Удельная площадь поверхности хромоксидных композиций настоящего изобретения обычно находится в интервале примерно 1-100 м2/г. Фаза α-NixСоyCr2-х-yO3, присутствующая в композициях, полученных способом данного изобретения, обычно состоит из кристаллитов, имеющих размеры частиц в интервале от примерно 20 до примерно 400 нм, обычно от примерно 40 до примерно 250 нм. В данное изобретение включены микрокристаллические материалы с размерами частиц меньше 20 нм.
Прокаленные хромоксидные композиции настоящего изобретения могут быть формованы в различные формы, такие как таблетки, гранулы и экструдаты, для использования в реакторах с насадками. Они могут также использоваться в порошкообразной форме.
Композиции данного изобретения могут дополнительно содержать одну или более добавок в форме соединений металлов, которые изменяют селективность или активность кристаллических никельзамещенных или кристаллических смешанных никель- и кобальтзамещенных альфа-оксидов хрома или фторированных замещенных альфа-оксидов хрома. Подходящие добавки могут быть выбраны из группы, состоящей из фторидов, оксидов или оксифторидных соединений Mg, Ca, Sc, Y, La, Ti, Zr, Hf, V, Nb, Ta, Mo, W, Mn, Re, Ru, Co, Rh, Ir, Ni, Pd, Pt, Cu, Ag, Au, Ce и Zn.
Общее содержание добавки (добавок) в композициях настоящего изобретения может быть от примерно 0,05% ат. до примерно 15% ат. по отношению к общему содержанию металлов в композициях. Добавки могут быть введены в композиции настоящего изобретения стандартными способами, такими как пропитка.
Обычно прокаленные композиции предварительно обрабатываются фторирующим агентом перед использованием в качестве катализаторов для изменения содержания фтора галогенированных углеводородных соединений. Обычно указанным фторирующим агентом является HF, хотя могут использоваться другие материалы, такие как тетрафторид серы, карбонилфторид и фторированные углеводородные соединения, такие как трихлорфторметан, дихлордифторметан, хлордифторметан, трифторметан или 1,1,2-трихлортрифторэтан. Указанная предварительная обработка может быть выполнена, например, при помещении катализатора в подходящий контейнер, которым может быть реактор, используемый для осуществления способа данного изобретения, и затем пропускании HF через высушенный, прокаленный катализатор с тем, чтобы частично насытить катализатор HF. Это удобно выполняется пропусканием HF через катализатор в течение периода времени, например, около 0,1-10 ч при температуре, например, около 200-450°С. Тем не менее, указанная предварительная обработка не является важной.
Как отмечено выше, катализаторы, предусмотренные согласно настоящему изобретению, могут использоваться для изменения фторораспределения в углеводородах и/или галогенированных углеводородах. Фторораспределение в углеводороде или галогенированном углеводороде может быть изменено увеличением содержания фтора в углеводороде или галогенированном углеводороде. Фторораспределение галогенированного углеводорода также может быть изменено снижением содержания фтора в галогенированном углеводороде и/или перегруппировкой расположения атомов фтора на углеродных атомах галогенированного углеводорода. Известны способы, где изменяется фторораспределение в галогенированных углеводородах, содержащих от 1 до 12 углеродных атомов, в частности способы, где изменяется фторораспределение в галогенированных углеводородах, содержащих от 1 до 6 углеродных атомов. Также известны способы, где содержание фтора углеводородов, содержащих от 1 до 12 углеродных атомов, увеличивается, в частности способы, где содержание фтора в углеводородах, содержащих 1-6 углеродных атомов, увеличивается. Способы изменения фторораспределения в галогенированных углеводородах включают фторирование, хлорфторирование, изомеризацию, диспропорционирование, дегидрофторирование и хлордефторирование. Способы увеличения содержания фтора в углеводородах включают фторирование и хлорфторирование. Способы данного изобретения характеризуются применением в качестве катализатора композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома, кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Типичными насыщенными галогенированными углеводородами, подходящими для способов фторирования, хлорфторирования, изомеризации, диспропорционирования, дегидрофторирования и хлордефторирования, являются галогенированные углеводороды, имеющие формулу CnHaBrbClcFd, в которой n представляет собой целое число от 1 до 6, а представляет собой целое число от 0 до 12, b представляет собой целое число от 0 до 4, с представляет собой целое число от 0 до 13, d представляет собой целое число от 0 до 13, сумма b, c и d равна не менее 1 и сумма a, b, c и d равна 2n+2, при условии, что n равно не менее 2 для способов изомеризации, диспропорционирования и дегидрофторирования, а равно не менее 1 для способа дегидрофторирования, b равно 0 для способа хлордефторирования, (b+c) равно не менее 1 для способа фторирования и равно 0 для способа дегидрофторирования, (a+b+c) равно не менее 1 для способов фторирования, хлордефторирования, изомеризации, диспропорционирования и дегидрофторирования, и d равно не менее 1 для способов изомеризации, диспропорционирования, дегидрофторирования и хлордефторирования. Типичными ненасыщенными галогенированными углеводородами, подходящими для способов фторирования, хлорфторирования, изомеризации, диспропорционирования и хлордефторирования, являются галогенированные углеводороды, которые имеют формулу CpHeBrfClgFh, в которой p представляет собой целое число от 2 до 6, e представляет собой целое число от 0 до 10, f представляет собой целое число от 0 до 2, g представляет собой целое число от 0 до 12, h представляет собой целое число от 0 до 11, сумма f, g и h равна не менее 1 и сумма е, f, g и h равна 2р, при условии, что f равно 0 для способа хлордефторирования, (e+f+g) равно не менее 1 для способов изомеризации и диспропорционирования и h равно не менее 1 для способов изомеризации, диспропорционирования и хлордефторирования. Типичными насыщенными углеводородами, подходящими для хлорфторирования, являются углеводороды, которые имеют формулу CqHr, где q представляет собой целое число от 1 до 6, и r равно 2q+2. Типичными ненасыщенными углеводородами, подходящими для фторирования и хлорфторирования, являются углеводороды, которые имеют формулу CiHj, где i представляет собой целое число от 2 до 6, и j равно 2i.
Фторирование
В данное изобретение включен способ увеличения содержания фтора в галогенированном углеводороде или ненасыщенном углеводородном соединении при взаимодействии указанного соединения (соединений) с фторидом водорода в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома или кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Каталитическая композиция может необязательно содержать дополнительные компоненты, такие как добавки для изменения активности и селективности катализатора.
Галогенированные углеводородные соединения, подходящие в качестве исходных материалов для способа фторирования данного изобретения, могут быть насыщенными или ненасыщенными. Насыщенные галогенированные углеводородные соединения, подходящие для способа фторирования данного изобретения, включают насыщенные галогенированные углеводородные соединения общей формулы CnHaBrbClcFd, в которой n представляет собой целое число от 1 до 6, а представляет собой целое число от 0 до 12, b представляет собой целое число от 0 до 4, с представляет собой целое число от 0 до 13, d представляет собой целое число от 0 до 13 и сумма a, b, c и d равна 2n+2, при условии, что (b+c) равно не менее 1. Ненасыщенные галогенированные углеводородные соединения, подходящие для способа данного изобретения, представлены общей формулы CpHeBrfClgFh, в которой p представляет собой целое число от 2 до 6, e представляет собой целое число от 0 до 10, f представляет собой целое число от 0 до 2, g представляет собой целое число от 0 до 12, h представляет собой целое число от 0 до 11, сумма f, g и h равна не менее 1 и сумма е, f, g и h равна 2р. Ненасыщенными углеводородами, подходящими для фторирования, являются ненасыщенные углеводороды, которые имеют формулу CiHj, где i представляет собой целое число от 2 до 6, и j равно 2i. Содержание фтора насыщенных соединений формулы CnHaBrbClcFd, ненасыщенных соединений формулы CpHeBrfClgFh и/или ненасыщенных соединений формулы CiHj может быть увеличено при взаимодействии указанных соединений с HF в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома, описанного выше, кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Такой способ называется здесь реакцией фторирования в парообразной фазе.
Реакции фторирования в парообразной фазе обычно проводят при температурах от примерно 150°С до 500°С. Для насыщенных соединений фторирование предпочтительно проводят при температуре от примерно 175°С до 400°С, и более предпочтительно, от примерно 200°С до примерно 350°С. Для ненасыщенных соединений фторирование обычно проводят при температуре от примерно 150°С до 350°С, и более предпочтительно, от примерно 175°С до примерно 300°С.
Реакции фторирования в парообразной фазе обычно проводят при атмосферном давлении и давлении выше атмосферного. В целях удобства в способах разделения с нисходящим потоком (например, дистилляции) могут использоваться давления до примерно 30 атм.
Реакции фторирования в парообразной фазе обычно проводят в трубчатом реакторе. Реактор и его соответствующие линии питания, выпускные линии и связанные установки должны быть сконструированы из материалов, стойких к фториду водорода и хлориду водорода. Типичные материалы конструкции, хорошо известные в технике фторирования, включают нержавеющие стали, в частности, аустенитичного типа, хорошо известные высоконикелевые сплавы, такие как никель-медные сплавы Monel®, никельсодержащие сплавы Hastelloy® и хром-никелевые сплавы Inconel®, и сталь с медным покрытием.
Время взаимодействия в реакторе обычно составляет от примерно 1 до примерно 120 с и, предпочтительно, от примерно 5 до примерно 60 с.
Количеством HF, взаимодействовавшего с ненасыщенными углеводородами или галогенированными углеводородными соединениями, должно быть, по меньшей мере, стехиометрическое количество. Стехиометрическое количество основано на числе Br и/или Cl заместителей, замещаемых на F, в дополнение к одному молю HF для насыщения двойной связи углерод-углерод, если присутствует. Обычно мольное соотношение HF и указанных соединений формул CnHaBrbClcFd, CpHeBrfClgFh и CiHj может быть в интервале от примерно 0,5:1 до примерно 100:1, предпочтительно, от примерно 2:1 до примерно 50:1, и более предпочтительно, от примерно 3:1 до примерно 20:1. В общем случае для данной каталитической композиции, чем выше температура и больше время взаимодействия, тем больше превращение во фторированные продукты. Вышеуказанные параметры могут быть сбалансированы друг с другом, так что образование более высокозамещенных продуктов максимизируется.
Примеры насыщенных соединений формулы CnHaBrbClcFd, которые могут взаимодействовать с HF в присутствии катализатора данного изобретения, включают CH2Cl2, CH2Br2, CHCl3, CCl4, C2Cl6, C2BrCl5, C2Cl5F, C2Cl4F2, C2Cl3F3, C2Cl2F4, C2ClF5, C2HCl5, C2HCl4F, C2HCl3F2,
C2HCl2F3, C2HClF4, C2HBrF4, C2H2Cl4, C2H2Cl3F, C2H2Cl2F2, C2H2ClF3, C2H3Cl3, C2H3Cl2F, C2H3ClF2, C2H4Cl2, C2H4ClF, C3Cl6F2, C3Cl5F3, C3Cl4F4, C3Cl3F5, C3HCl7, C3HCl6F, C3HCl5F2,
C3HCl4F3, C3HCl3F4, C3HCl2F5, C3H2Cl6, C3H2BrCl5, C3H2Cl5F, C3H2Cl4F2, C3H2Cl3F3, C3H2Cl2F4, C3H2ClF5, C3H3Cl5, C3H3Cl4F, C3H3Cl3F2, C3H3Cl2F3, C3H3ClF4, C3H4Cl4, C4Cl4Cl4, C4Cl4Cl6, C4H5Cl5, C4H5Cl4F, и C5H4Cl8.
Отдельные примеры реакций фторирования насыщенных галогенированных углеводородных соединений, которые могут быть проведены в условиях, описанных выше, с использованием катализаторов данного изобретения, включают превращение CH2Cl2 в CH2F2, превращение CHCl3 в смесь CHCl2F, CHClF2 и CHF3, превращение CH3CHCl2 в смесь CH3CHClF и CH3CHF2, превращение CH2ClCH2Cl в смесь CH3CHClF и CH3CHF2, превращение CH3CCl3 в смесь CH3CCl2F, CH3CClF2 и CH3CF3, превращение CH2ClCF3 в CH2FCF3, превращение CHCl2CF3 в смесь CHClFCF3 и CHF2CF3, превращение CHClFCF3 в CHF2CF3, превращение CHBrFCF3 в CHF2CF3, превращение CCl3CF2CCl3 в смесь CCl2FCF2CClF2 и CClF2CF2CClF2, превращение CCl3CH2CCl3 в CF3CH2CF3, превращение CCl3CH2CHCl2 в смесь CF3CH2CHF2, CF3CH=CHCl и CF3CH=CHF, превращение CF3CCl2CClF2 в смесь CF3CCl2CF3 и CF3ClFCF3, превращение CF3CCl2CF3 в CF3ClFCF3 и превращение смеси, содержащей CF3CF2CHCl2 и CClF2CF2CHClF, в смесь CF3CF2CHClF и CF3CF2CHF2.
Примеры ненасыщенных соединений формул CpHeBrfClgFh и CiHj, которые могут взаимодействовать с HF в присутствии катализаторов данного изобретения, включают C2Cl4, C2BrCl3, C2Cl3F, C2Cl2F2, C2ClF3, C2F4, C2HCl3, C2HBrCl2, C2HCl2F, C2HClF2, C2HF3, C2H2Cl2, C2H2ClF, C2H2F2, C2H3Cl, C2H3F, C2H4, C3H6, C3H5Cl, C3H4Cl2, C3H3Cl3, C3H2Cl4, C3HCl5, C3Cl6, C3Cl5F, C3Cl4F2, C3Cl3F3, C3Cl2F4, C3ClF5, C3HF5, C3H2F4, C3F6, C4Cl8, C4Cl2F6, C4ClF7, C4H2F6 и C4HClF6.
Отдельные примеры реакций фторирования ненасыщенных галогенированных углеводородных соединений, которые могут быть проведены с использованием катализаторов данного изобретения, включают превращение CHCl=CCl2 в смесь CH2ClCF3 и CH2FCF3, превращение CCl2=CCl2 в смесь CHCl2CF3, CHClFCF3 и CHF2CF3, превращение CCl2=CH2 в смесь CH3CCl2F, CH3CClF2 и CH3CF3, превращение CH2=CHCl в смесь CH3CHClF и CH3CHF2, превращение CF2=CH2 в CH3CF3, превращение CCl2=CClCF3 в смесь CF3CHClCClF2, CF3CHClCF3 и/или CF3CCl=CF2, превращение CF3CF=CF2 в CF3CHFCF3, превращение CF3CH=CF2 в CF3CH2CF3 и превращение CF3CH=CHF в CF3CH2CHF2.
Смеси насыщенных галогенированных углеводородных соединений или смеси ненасыщенных углеводородов и/или галогенированных углеводородных соединений могут также использоваться в реакциях фторирования в парообразной фазе, а также смеси, содержащие как насыщенные углеводороды, так и галогенированные углеводородные соединения. Отдельные примеры смесей насыщенных галогенированных углеводородных соединений и смесей ненасыщенных углеводородов и ненасыщенных галогенированных углеводородных соединений, которые могут подвергаться фторированию в парообразной фазе с использованием катализаторов данного изобретения включают смесь CH2Cl2 и CCl2=CCl2, смесь CCl2FCClF2 и CCl3CF3, смесь CCl2=CCl2 и CCl2=CClCCl3, смесь СН2=СНСН3 и CH2=CClCH3, смесь CH2Cl2 и CH3CCl3, смесь CHF2CClF2 и CHClFCF3, смесь CHCl2CCl2CH2Cl и CCl3CHClCH2Cl, смесь CHCl2CH2CCl3 и CCl3CHClCH2Cl, смесь CHCl2CHClCCl3, CCl3CH2CCl3 и CCl3CCl2CH2Cl, смесь CHCl2CH2CCl3 и CCl3CH2CCl3, смесь CF3CH2CCl2F и CF3CH=CCl2 и смесь CF3CH=CHCl и CF3CH=CCl2.
Хлорфторирование
В данное изобретение включен способ увеличения содержания фтора в углеводородном соединении или галогенированном углеводородном соединении при взаимодействии указанного соединения с фторидом водорода (HF) и хлором (Cl2) в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома, описанного выше, кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Каталитическая композиция может необязательно содержать дополнительные компоненты, такие как другой каталитически эффективный металл.
Галогенированные углеводородные соединения, подходящие в качестве исходных материалов для способа хлорфторирования данного изобретения, могут быть насыщенными или ненасыщенными. Насыщенные галогенированные углеводородные соединения, подходящие для способов хлорфторирования данного изобретения, включают насыщенные галогенированные углеводородные соединения общей формулы CnHaBrbClcFd, в которой n представляет собой целое число от 1 до 6, а представляет собой целое число от 0 до 12, b представляет собой целое число от 0 до 4, с представляет собой целое число от 0 до 13, d представляет собой целое число от 0 до 13, сумма b, c и d равна не менее 1, и сумма a, b, c и d равна 2n+2, при условии, что (а+b+c) равно не менее 1. Предпочтительные способы хлорфторирования включают указанные насыщенные исходные материалы, где а равно не менее 1. Насыщенными углеводородными соединениями, подходящими для хлорфторирования, являются насыщенные углеводородные соединения, которые имеют формулу CqHr, где q представляет собой целое число от 1 до 6, и r равно 2q+2.
Ненасыщенные галогенированные углеводородные соединения, подходящие для способов хлорфторирования данного изобретения, включают ненасыщенные галогенированные углеводородные соединения общей формулы CpHeBrfClgFh, в которой p представляет собой целое число от 2 до 6, e представляет собой целое число от 0 до 10, f представляет собой целое число от 0 до 2, g представляет собой целое число от 0 до 12, h представляет собой целое число от 0 до 11, сумма f, g и h равна не менее 1 и сумма е, f, g и h равна 2р. Ненасыщенными углеводородными соединениями, подходящими для хлорфторирования, являются ненасыщенные углеводороды, которые имеют формулу CiHj, где i представляет собой целое число от 2 до 6, и j равно 2i. Содержание фтора насыщенных соединений формул CnHaBrbClcFd и CqHr и/или ненасыщенных соединений формул CpHeBrfClgFh и CiHj может быть увеличено при взаимодействии указанных соединений с HF и Cl2 в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома, описанного выше, кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Такой способ называется здесь реакцией хлорфторирования в парообразной фазе.
Условия реакций хлорфторирования в парообразной фазе являются подобными условиям, описанным выше для реакций фторирования в парообразной фазе в плане температурных интервалов, времени взаимодействия, давлений и мольных соотношений HF и галогенированных углеводородных соединений. Количество хлора (Cl2), подаваемого в реактор, основано на том, являются ли ненасыщенными галогенированные углеводородные соединения, подаваемые в реактор, и на числе водородов в CnHaBrbClcFd, CqHr, CpHeBrfClgFh и CiHj, которые должны быть замещены хлором и фтором. Один моль Cl2 требуется для насыщения двойной связи углерод-углерод, и моль Cl2 требуется для каждого водорода, замещаемого хлором или фтором. Небольшой избыток хлора по сравнению со стехиометрическим количеством может быть необходим по практическим причинам, но большие избытки хлора будут давать полное хлорфторирование продуктов. Соотношение Cl2 и галогенированного углеводородного соединения составляет обычно от примерно 1:1 до примерно 10:1.
Отдельные примеры реакций хлорфторирования в парообразной фазе насыщенных галогенированных углеводородных соединений общей формулы CnHaBrbClcFd и насыщенных углеводородных соединений общей формулы CqHr, которые могут быть проведены с использованием катализаторов данного изобретения, включают превращение С2Н6 в смесь, содержащую CH2ClCF3, превращение CH2ClCF3 в смесь CHClFCF3 и CHF2CF3, превращение CCl3CH2CH2Cl в смесь CF3CCl2CClF2, CF3CCl2CF3, CF3CClFCClF2 и CF3CClFCF3, превращение CCl3CH2CHCl2 в смесь CF3CCl2CClF2, CF3CCl2CF3, CF3CClFCClF2 и CF3CClFCF3, превращение CCl3CHClCH2Cl в смесь CF3CCl2CClF2, CF3CCl2CF3, CF3CClFCClF2 и CF3CClFCF3, превращение CHCl2CCl2CCl2CH2Cl в смесь CF3CCl2CClF2, CF3CCl2CF3, CF3CClFCClF2 и CF3CClFCF3, превращение CCl3CH2CH2Cl в смесь CF3CCl2CHF2, CF3CClFCHF2, CF3CClFCClF2 и CF3CCl2CF3 и превращение CCl3CH2CHCl2 в смесь CF3CCl2CHF2, CF3CClFCHF2, CF3CClFCClF2 и CF3CCl2CF3.
Отдельные примеры реакций хлорфторирования в парообразной фазе ненасыщенных галогенированных углеводородных соединений общей формулы CpHeBrfClgFh и ненасыщенных углеводородных соединений общей формулы CiHj, которые могут быть проведены с использованием катализаторов данного изобретения, включают превращение С2Н4 в смесь CCl3CClF2, CCl2FCCl2F, CClF2CCl2F, CCl3CF3, CF3CCl2F и CClF2CClF2, превращение C2Cl4 в смесь CCl3CClF2, CCl2FCCl2F, CClF2CCl2F, CCl3CF3, CF3CCl2F и CClF2CClF2 и превращение С3Н6 или CF3CCl=CCl2 в смесь CF3CCl2CClF2, CF3CCl2CF3, CF3CClFCClF2 и CF3CClFCF3.
Известен каталитический способ получения смеси 1,2,2-трихлор-1,1,3,3,3-пентафторпропана (т.е. CClF2CCl2CF3, или CFC-215aa), 2,2-дихлор-1,1,1,3,3,3-гексафторпропан(т.е. CF3CCl2CF3, или CFC-216aa), 1,2-дихлор-1,1,1,3,3,3-гексафторпропана (т.е. CClF2CClFCF3, или CFC-216ba) и 2-хлор-1,1,1,2,3,3,3-гептафтор-пропана (т.е. CF3CClFCF3, или CFC-217ba) хлорфторированием гексагалогенпропена формулы C3Cl6-xFx, в которой х равен 0-4. Предпочтительные гексагалогенпропены формулы C3Cl6-xFx включают 1,2,2-трихлор-3,3,3-трифтор-1-пропен (т.е. CCl2=CClCF3, или CFC-1213xa) и гексахлорпропен (т.е. CCl2=CClCCl3). Смесь CFC-215aa, CFC-216aa, CFC-216ba и CFC-217ba получают взаимодействием вышеуказанных ненасыщенных соединений с Cl2 и HF в парообразной фазе в присутствии катализаторов данного изобретения при температурах от примерно 150°С до примерно 450°С, предпочтительно, примерно 250-400°С.
Количеством HF, подаваемого в реактор, должно быть, по меньшей мере, стехиометрическое количество на основе числа Cl заместителей в C3Cl6-xFx исходном материале (материалах) и желаемой композиции конечного продукта. В случае хлор-фторирования CFC-1213ха до смеси хлорфторпропанов, имеющих среднее число фторзаместителей шесть, стехиометрическое соотношение HF:CFC-1213ха составляет 3:1. Предпочтительные соотношения HF и C3Cl6-xFx исходного материала (материалов) находятся обычно в интервале от примерно стехиометрического соотношения до примерно 30:1, более предпочтительно, от примерно 8:1 до 25:1.
Количество хлора, подаваемого в реактор, должно быть, по меньшей мере, стехиометрическим количеством. Предпочтительные мольные соотношения Cl2 и CFC-1213xa составляют от примерно 1:1 до примерно 5:1.
Предпочтительные времена взаимодействия составляют от примерно 5 с до примерно 60 с.
Дополнительная информация по хлорфторированию CFC-1213xa предусматривается в заявке на патент США 60/405222 [CL2108 US PRV], зарегистрированной 22 августа 2002 г и поэтому приведенной здесь в качестве ссылки в ее полноте.
Смеси насыщенных углеводородных соединений и насыщенных галогенированных углеводородных соединений и смеси ненасыщенных углеводородных соединений и ненасыщенных галогенированных углеводородных соединений, а также смеси, содержащие как насыщенные, так и ненасыщенные соединения, могут хлорфторироваться с использованием катализаторов настоящего изобретения. Отдельные примеры смесей насыщенных и ненасыщенных углеводородов и галогенированных углеводородов, которые могут быть использованы, включают смесь CCl2=CCl2 и CCl2=CClCCl3, смесь CHCl2CCl2CH2Cl и CCl3CHClCH2Cl, смесь CHCl2CH2CCl3 и CCl3CHClCH2Cl, смесь CHCl2CHClCCl3, CCl3CH2CCl3 и CCl3CCl2CH2Cl, смесь CHF2CH2CF3 и CHCl=CHCF3 и смесь СН2=СН2 и СН2=СНСН3.
Изомеризация и диспропорционирование
В изобретение входит способ изменения фторораспределения в галогенированном углеводородном соединении изомеризацией указанного галогенированного углеводородного соединения в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллического никельзамещенного альфа-оксида хрома, описанного выше, кристаллического смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом.
Также включенным в данное изобретение является способ изменения фторораспределения в галогенированном углеводородном соединении диспропорционированием указанного галогенированного углеводородного соединения в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного никельзамещенного (и необязательно кобальтзамещенного) альфа-оксида хрома, который обработан фторирующим агентом.
Галогенированные углеводородные соединения, подходящие в качестве исходных материалов для способов изомеризации и диспропорционирования данного изобретения, могут быть насыщенными или ненасыщенными. Насыщенные галогенированные углеводородные соединения, подходящие для способов изомеризации и диспропорционирования данного изобретения, включают насыщенные галогенированные углеводородные соединения общей формулы CnHaBrbClcFd, в которой n представляет собой целое число от 2 до 6, а представляет собой целое число от 0 до 12, b представляет собой целое число от 0 до 4, с представляет собой целое число от 0 до 13, d представляет собой целое число от 1 до 13 и сумма a, b, c и d равна 2n+2, при условии, что (а+b+c) равно не менее 1. Ненасыщенные галогенированные углеводородные соединения, подходящие для способов изомеризации и диспропорционирования данного изобретения, включают ненасыщенные галогенированные углеводородные соединения общей формулы CpHeBrfClgFh, в которой p представляет собой целое число от 2 до 6, e представляет собой целое число от 0 до 10, f представляет собой целое число от 0 до 2, g представляет собой целое число от 0 до 12, h представляет собой целое число от 1 до 11 и сумма е, f, g и h равна 2р, при условии, что сумма e, f и g равна не менее 1.
В одном варианте настоящего изобретения фторораспределение галогенированного углеводородного соединения изменяется перегруппировкой заместителей H, Br и/или Cl в молекуле (обычно термодинамически предпочтительной перегруппировкой) при сохранении того же числа заместителей H, Br, Cl и F, соответственно. Данный способ называется здесь изомеризацией.
В другом варианте настоящего изобретения фторораспределение галогенированного углеводородного соединения изменяется при замещении, по меньшей мере, одного F-заместителя одной молекулы галогенированного углеводородного исходного материала, по меньшей мере, одним заместителем H, Br и/или Cl другой молекулы галогенированного углеводородного исходного материала с образованием в результате одного или более галогенированных углеводородных соединений, имеющих сниженное содержание фтора по сравнению с галогенированным углеводородным исходным материалом, и одного или более галогенированных углеводородных соединений, имеющих повышенное содержание фтора по сравнению с галогенированным углеводородным исходным материалом. Данный способ называется здесь диспропорционированием.
В другом варианте настоящего изобретения указанное взаимодействие галогенированных углеводородных соединений может привести к образованию одной или более пар галогенированных углеводородных соединений. В данном случае один представитель пары имеет большее число заместителей H, Br, Cl или F, а другой представитель пары имеет меньшее число заместителей H, Br, Cl или F. Данный способ называется здесь диспропорционированием.
В другом варианте настоящего изобретения реакции как изомеризации, так и диспропорционирования могут протекать одновременно.
При проведении изомеризации, диспропорционирования или как изомеризации, так и диспропорционирования фторораспределение насыщенных соединений формулы CnHaBrbClcFd и/или ненасыщенных соединений формулы CpHeBrfClgFh может быть изменено в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, обработанного фторирующим агентом.
Реакции изомеризации и диспропорционирования обычно проводят при температурах от примерно 150°С до 500°С, предпочтительно, от примерно 200°С до примерно 400°С. Время взаимодействия в реакторе составляет обычно от примерно 1 до примерно 120 с и, предпочтительно, от примерно 5 до примерно 60 с. Реакции изомеризации и диспропорционирования могут осуществляться в присутствии инертного газа, такого как гелий, аргон или азот, хотя это не является предпочтительным. Реакции изомеризации и диспропорционирования могут осуществляться в присутствии небольших количеств HF и HCl, но это не является предпочтительным.
Отдельные примеры реакций изомеризации в парообразной фазе, которые могут осуществляться с использованием катализаторов данного изобретения, включают превращение CClF2CCl2F в CCl3CF3, превращение CClF2CClF2 в CF3CCl2F, превращение CHF2CClF2 в CF3CHClF, превращение CHF2CHF2 в CF3CH2F, превращение CF3CClFCClF2 в CF3CCl2CF3 и превращение CF3CHFCHF2 в CF3CH2CF3.
Отдельные примеры реакций диспропорционирования в парообразной фазе, которые могут осуществляться с использованием катализаторов данного изобретения, включают превращение CClF2CClF2 в смесь CClF2CCl2F, CCl3CF3 и CF3CClF2 и превращение CHClFCF3 в смесь CHCl2CF3 и CHF2CF3.
Известен способ превращения смеси 2-хлор-1,1,2,2-тетрафторэтана (т.е., CHF2CClF2, или HCFC-124a) и 2-хлор-1,1,1,2-тетрафторэтана (т.е., CF3CHClF, или HCFC-124) в смесь, содержащую 2,2-дихлор-1,1,1-трифторэтан (т.е., CHCl2CF3, или HCFC-123) и 1,1,1,2,2-пентафторэтан (т.е., CF3CHF2, или HFC-125) помимо непревращенных исходных материалов. Смесь, содержащая HFC-125 и HCFC-123, может быть получена в парообразной фазе при взаимодействии смеси HCFC-124a и HCFC-124 c катализаторами данного изобретения необязательно в присутствии разбавителя, выбранного из группы, состоящей из HF, HCl, азота, гелия, аргона и диоксида углерода. Диспропорционирование, предпочтительно, проводят при температуре примерно 150-400°С, более предпочтительно, примерно 250-350°С. Если используется, разбавитель-газ может присутствовать в мольном соотношении разбавитель:галогенэтан от примерно 1:1 до примерно 5:1. Предпочтительные времена взаимодействия составляют от примерно 10 с до примерно 60 с.
Дегидрофторирование
В данное изобретение включен способ снижения содержания фтора в галогенированном углеводородном соединении дегидрофторированием указанного галогенированного углеводородного соединения в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом.
Галогенированные углеводородные соединения, подходящие в качестве исходных материалов для способа дегидрофторирования данного изобретения, являются обычно насыщенными. Насыщенные галогенированные углеводородные соединения, подходящие для способов дегидрофторирования данного изобретения, включают насыщенные галогенированные углеводородные соединения общей формулы CnHaFd, в которой n представляет собой целое число от 2 до 6, а представляет собой целое число от 1 до 12, d представляет собой целое число от 1 до 13 и сумма а и d равна 2n+2. Содержание фтора в насыщенных соединениях формулы CnHaFd может быть снижено в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Указанное снижение содержания фтора обычно связано с удалением фторида водорода (HF) из молекулы и называется здесь дегидрофторированием.
Реакции дегидрофторирования обычно проводят при температурах от примерно 200°С до 500°С, предпочтительно, от примерно 300°С до примерно 450°С. Время взаимодействия в реакторе составляет обычно от примерно 1 до примерно 360 с и, предпочтительно, от примерно 5 до примерно 120 с. Проведение реакций дегидрофторирования в присутствии инертного газа, такого как гелий, аргон или азот, способствует диссоциации фторированного углеводородного соединения, но данная практика может также привести к трудностям в разделении и не является предпочтительной.
Продукт реакции дегидрофторирования состоит из HF и ненасыщенного фторированного углеводородного соединения, образованного в результате потери HF исходным материалом. Отдельные примеры реакций дегидрофторирования в парообразной фазе, которые могут осуществляться с использованием катализаторов данного изобретения, включают превращение CH3CHF2 в CH2=CHF, превращение CH3CF3 в CH2=CF2, превращение CF3CH2F в CF2=CHF, превращение CHF2CH2CF3 в CHF=CHCF3 и превращение CF3CH2CF3 в CF3CH=CF2.
Известен каталитический способ получения фторэтена (т.е. CH2=CHF, или винилфторида) дегидрофторированием 1,1-дифторэтана (т.е., CHF2CH3, или HFC-152a). Смесь, содержащая винилфторид и непревращенный HFC-152a, может быть получена в парообразной фазе при взаимодействии HFC-152a c катализаторами данного изобретения необязательно в присутствии разбавителя, выбранного из группы, состоящей из HF, азота, гелия, аргона и диоксида углерода. Дегидрофторирование, предпочтительно, проводят при температурах от примерно 150°С до примерно 400°С, более предпочтительно, от примерно 250°С до примерно 350°С. Если используется, разбавитель-газ может присутствовать в мольном соотношении разбавитель:галогенэтан от примерно 1:1 до примерно 5:1. Предпочтительное время взаимодействия составляет от примерно 10 с до примерно 60 с.
Хлордефторирование
В данное изобретение включен способ снижения содержания фтора в галогенированном углеводородном соединении при взаимодействии указанного галогенированного углеводородного соединения с хлоридом водорода (HCl) в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом.
Галогенированные углеводородные соединения, подходящие в качестве исходных материалов для способа хлордефторирования данного изобретения, могут быть насыщенными или ненасыщенными. Насыщенные галогенированные углеводородные соединения, подходящие для способов хлордефторирования данного изобретения, включают насыщенные галогенированные углеводородные соединения общей формулы CnHaClcFd, в которой n представляет собой целое число от 1 до 6, а представляет собой целое число от 0 до 12, c представляет собой целое число от 0 до 13, d представляет собой целое число от 1 до 13, и сумма а, с и d равна 2n+2. Ненасыщенные галогенированные углеводородные соединения, подходящие для способов хлордефторирования данного изобретения, включают ненасыщенные галогенированные углеводородные соединения общей формулы CpHeClgFh, в которой р представляет собой целое число от 2 до 6, е представляет собой целое число от 0 до 10, g представляет собой целое число от 0 до 12, h представляет собой целое число от 1 до 11 и сумма e, g и h равна 2р. Содержание фтора в насыщенных соединениях формулы CnHaClcFd и/или ненасыщенных соединениях формулы CpHeClgFh может быть снижено при взаимодействии указанных соединений с HCl в парообразной фазе в присутствии каталитической композиции, содержащей, по меньшей мере, один хромсодержащий компонент, выбранный из группы, состоящей из кристаллических никельзамещенного альфа-оксида хрома, описанного выше, смешанного никель- и кобальтзамещенного альфа-оксида хрома, описанного выше, и указанного замещенного альфа-оксида хрома, который обработан фторирующим агентом. Такой способ называется здесь реакцией хлордефторирования в парообразной фазе. Хлордефторирование рассмотрено в патенте США № 5345017 и патенте США № 5763698, и поэтому описания указанных двух патентов приводятся здесь в качестве ссылки.
Реакции хлордефторирования обычно проводят при температурах от примерно 250°С до 450°С, предпочтительно, от примерно 300°С до примерно 400°С. Время взаимодействия в реакторе составляет обычно от примерно 1 до примерно 120 с и, предпочтительно, от примерно 5 до примерно 60 с. Реакции наиболее удобно проводить при атмосферном давлении или давлении выше атмосферного.
Хлордефторирование, включающее насыщенные галогенированные углеводороды, является особенно известным. Мольное соотношение HCl и насыщенного галогенированного углеводородного соединения обычно составляет от примерно 1:1 до примерно 100:1, предпочтительно, от примерно 3:1 до примерно 50:1, и наиболее предпочтительно, от примерно 4:1 до примерно 30:1. В общем случае для данной каталитической композиции, чем выше температура, чем больше время взаимодействия и больше мольное соотношение HCl и насыщенного галогенированного углеводородного соединения, тем больше превращение в соединения, имеющие более низкое содержание фтора. Вышеуказанные параметры могут быть сбалансированы друг с другом, так что образование хлорзамещенных продуктов максимизируется.
Продукт реакций хлордефторирования обычно содержит непрореагировавший HCl, HF, непревращенный исходный материал и насыщенные галогенированные углеводородные соединения, имеющие более низкое содержание фтора, чем у исходного материала, в силу замещения одного или более фторзаместителей хлором. Отдельные примеры реакций хлордефторирования в парообразной фазе, которые могут осуществляться с использованием катализаторов данного изобретения, включают превращение CHF3 в смесь CHCl3, CHCl2F и CHClF2, превращение CClF2CClF2 в смесь CCl3CCl3, CCl3CCl2F, CCl3CClF2, CCl2FCCl2F, CClF2CCl2F и CCl3CF3, превращение CF3CClF2 в смесь CCl3CCl3, CCl3CClF2, CCl2FCCl2F, CCl3CF3, CClF2CClF2 и CF3CCl2F, превращение CF3CCl2CF3 в смесь CF3CCl2CClF2, CF3CCl2CCl2F, CF3CCl2CCl3 и CClF2CCl2CCl3 и превращение CF3CH2CF3 в смесь CCl2=CHCF3 и CCl2=CClCF3.
Известен каталитический способ получения смеси, содержащей 1,1-дихлор-3,3,3-трифтор-1-пропен (т.е., CCl2=CHCF3, или HCFC-1223za) и 1,1,2-трихлор-3,3,3-трифтор-1-пропен (т.е., CCl2=CClCF3, или CFC-1213xa), хлордефторированием 1,1,1,3,3,3-гексафторпропана (т.е., CF3CH2CF3, или HFC-236fa) при взаимодействии HFC-236fa c HCl в парообразной фазе в присутствии катализаторов данного изобретения. Реакцию, предпочтительно, проводят при температурах от примерно 275°С до 450°С, более предпочтительно, от примерно 300°С до примерно 400°С при мольном соотношении HCl:HFC-236fa, предпочтительно, от примерно 3:1 до примерно 20:1. Предпочтительное время взаимодействия составляет от примерно 1 c до примерно 40 с. Кислород в виде воздуха или совместного питания с инертным разбавителем, таким как азот, гелий или аргон, может вводиться вместе с реагентами или как отдельная каталитическая обработка, если желательно.
Реакционные продукты, полученные способами данного изобретения, могут быть выделены традиционной технологией, такой как комбинации, включающие (но не ограничиваясь этим) использование скрубберов, декантацию или дистилляцию. Некоторые из продуктов различных вариантов данного изобретения могут образовывать одну или более азеотропных смесей друг с другом или с HF.
Способы данного изобретения могут быть легко осуществлены с использованием хорошо известной химической технологии.
Применимость
Некоторые реакционные продукты, полученные с использованием катализаторов, рассмотренных здесь, имеют желаемые свойства для прямого промышленного использования. Например, CH2F2 (HFC-32), CHF2CF3 (HFC-125), CHF2CF3 (HFC-125), CH2FCHF2 (HFC-134), CF3CH2CF3 (HFC-236fa) и CF3CH2CHF2 (HFC-245fa) нашли применение в качестве хладагентов, CH2FCF3 (HFC-134a) и CF3CHFCF3 (HFC-227ea) нашли применение в качестве пропеллентов, CH2FCHF2 (HFC-134) и CF3CH2CHF2 (HFC-245fa) нашли применение в качестве вспенивающих агентов и CHF2CF3 (HFC-125), CF3CH2CF3 (HFC-236fa) и CF3CHFCF3 (HFC-227ea) нашли применение в качестве пламягасителей.
Другие реакционные продукты, полученные с использованием данного изобретения, используются в качестве промежуточных химических веществ для получения полезных продуктов. Например, CCl3CF3 (CFC-113a) может использоваться для получения CFC-114a, который затем может быть превращен в CH2FCF3 (HFC-134a) гидродехлорированием. Аналогично, CF3CCl2CF3 (CFC-216aa) может использоваться для получения CF3CH2CF3 (HFC-236fa) гидродехлорированием, и CF3CCl=CF2 (CFC-1215zc) может использоваться для получения CF3CH2CHF2 (HFC-245fa) гидрированием.
Предполагается, что без дополнительного усовершенствования специалист в данной области техники с использованием данного описания сможет использовать настоящее изобретение в его самой полной степени. Поэтому следующие отдельные варианты истолковываются только как иллюстративные и не ограничивают оставшуюся часть описания совсем никаким образом.
Примеры
Характеристика катализатора
Энергорассеивающая спектроскопия ((EDS)(ЭРС)) и трансмиссионная электронная микроскопия ((ТЕМ)(ТЭМ))
В данных исследованиях кристаллиты анализируют с использованием трансмиссионного электронного микроскопа высокого разрешения Philips CM-20, работающего при ускоряющем напряжении 200 кВ и спаренного с безоконной ЭРС-системой Oxford c Si (Li) элементарным детектором. В ЭРС-анализах используют электронопрозрачные тонкие сечения образцов для минимизации эффектов толщины образца, таких как флуоресценция. Также благодаря подобию их атомных масс было принято, что рентгеновское поглощение поперечных сечений для Cr, Co и Ni является одинаковым (см. работу Zaluzek, Introduction to Analytical Electron Microscopy (pp. 121-167), ed. by J.J.Hren, J.I.Goldstein and D.C.Joy (Plenum Press, New York, 1979)). Присутствие меди в ЭРС-спектрах на фигурах 1, 2, 3, 4 и 5 обусловлено ТЭМ-сеткой и фоном в микроскопе.
Рентгеновская абсорбционная спектроскопия ((XAS)(РАС)) и
диффракция рентгеновских лучей ((XRD)(ДРЛ))
ДРЛ-данные получают и анализируют в соответствии с методиками, описанными в Warren, X-Ray Diffraction (Addison-Wesley, Reading, MA, 1969). ДРЛ-данные получают при излучении источника 5MBD, DND-CAT Advanced Photon Source, Argonne National Laboratory. РАС-данные получают и анализируют с использованием методик, описанных в Koningsberger and Prins, X-ray Absorption: Principles, Applications, Techniques of EXAFS, SEXAFS and XANES (John Wiley & Sons, New Jork, 1988). Спектры получают для К-краев Cr, Co и Ni. Cr-края получают в трансмиссионной геометрии, тогда как Со- и Ni-края получают в флуоресцентном варианте благодаря их низким концентрациям.
Использование источника излучения Advanced Photon Source для получения ДРЛ- и РАС-данных подтверждено by the U.S. Department of Energy, Office of Basic Energy Sciences, under Contract # W-31-109-Eng-38.
Получение катализатора
Пример получения 1
Получение катализатора 95% хрома/3% кобальта/2% никеля (6,2 экв. избытка NH4NO3; 400°С)
Получают раствор 380,14 г Cr(NO3)3[9(H2O)] (0,95 моль), 8,73 г Co(NO3)3[6(H2O)] (0,030 моль) и 5,82 г Ni(NO3)3[6(H2O)] (0,020 моль) в 1000 мл деионизованной воды. Повышают рН раствора от 3,1 до 8,5 обработкой 7,4 М водным гидроксидом аммония. Взвесь перемешивают при комнатной температуре в течение 21 ч при рН 8,5. Смесь затем обрабатывают раствором 472,24 г NH4NO3 (5,90 моль), растворенного в 500 мл воды. Взвесь перемешивают в течение 1 ч при комнатной температуре и затем сушат при 110-120°С в воздушной среде в течение примерно 96 ч. Высушенные твердые вещества измельчают в порошок и затем помещают в закрытый тигель и прокаливают при 400°С в течение 24 ч в воздушной среде.
Анализ методами ТЭМ и ЭРС показывает, что большая часть кристаллов являются размером <50 нм с однородным введением как кобальта, так и никеля в α-Cr2O3-решетку. Шпинельподобные фазы не обнаруживаются. Анализ образца методами ДРД и РАС подтверждает, что кристаллиты имеют α-Cr2O3-структуру, и что среднее состояние окисления кобальта составляет 2,89. Количество кобальта, введенного в α-Cr2O3-решетку, составляет примерно 2,5-2,7% ат. ДРЛ подтверждает, что появившийся никель также полностью введен в α-Cr2O3-решетку.
Пример получения 2
Получение катализатора 98% хрома/1% кобальта/1% никеля (500°С)
[Cr(NH3)6]Cl3] (16,7755 г, 64,6 ммоль) и [Co(NH3)6[Cl3] (0,1757 г, 0,657 ммоль) и Ni(NO3)2[6(H2O)] (0,1891 г, 0,650 ммоль) растворяют в деионизованной воде. Затем водный гидроксид аммония добавляют к раствору до полного осаждения. Полученный осадок отфильтровывают и сушат в воздушной среде при 110°С в течение 12 ч. Полученный продукт тщательно измельчают в агатовой ступке и затем нагревают при 550°С в воздушной среде в течение 12 ч.
Анализ образца методами ТЭМ и ЭРС показывает наличие небольшого количества шпинельной фазы, содержащей кобальт, никель и хром; данная фаза является богаче кобальтом, чем никелем. Фаза α-Cr2O3 присутствует в виде 100-400 нм кристаллов; данная фаза содержит как никель, так и кобальт с незначительным избытком никеля. РАС показывает, что кобальт полностью введен в α-Cr2O3-решетку. Структура вблизи Ni-края является подобной композиции из примера получения 1 и соответствует некоторому введению никеля в α-Cr2O3-решетку.
Пример получения 3
Получение катализатора 98% хрома/2% никеля (550°С)
[Cr(NH3)6]Cl3] (16,7727 г, 64,38 ммоль) и Ni(NO3)2[6(H2O)] (0,3783 г, 1,30 ммоль) растворяют в деионизованной воде. Затем водный гидроксид аммония добавляют к раствору до полного осаждения. Полученный осадок отфильтровывают и сушат в воздушной среде при 110°С в течение 12 ч. Полученный продукт тщательно измельчают в агатовой ступке и затем нагревают при 550°С в воздушной среде в течение 12 ч.
Анализ образца методами ТЭМ и ЭРС показывает наличие никельзамещенной α-Cr2O3-фазы, главным образом, в виде 200 нм кристаллов; некоторые из кристаллов являются размером в пределах 300-400 нм. Отсутствует подтверждение наличия никель/хром-шпинельной фазы. Часть никеля является введенной в α-Cr2O3-решетку, потому что структура вблизи Ni-края является подобной катализатору из примера получения 1.
Пример получения 4
Получение катализатора 98% хрома/2% никеля (550°С)
[Cr(NO3)3][9H2O] (50,5 г, 0,126 моль) и Ni(NO3)2[6(H2O)] (0,816 г, 0,00280 моль) взвешивают в фарфоровом тигле и расплавляют вместе с перемешиванием на открытом воздухе. Смесь нагревают до разложения. Часть полученного твердого вещества затем прокаливают в печи при 550°С в течение 12 ч.
Аналогично указанному выше получают и прокаливают при 550°С никель/хромоксидные композиции, имеющие массовый состав 0,5% ат. никеля/99,5% ат. хрома и 1% ат. никеля/99% ат. хрома.
Анализы методами ТЭМ и ЭРС композиций 98/2 Cr/Ni и 99,5/0,5 Cr/Ni показывает, что указанные образцы содержат никельзамещенные кристаллы α-Cr2O3 размером в интервале 200-400 нм. Также присутствует шпинельная фаза с соотношение Ni/Cr примерно 3/1, имеющая размер кристаллитов в интервале от примерно 10 до 30 нм, особенно, в образце Cr/Ni 98/2.
Анализ методом РАС указанных трех образцов подтверждает введение никеля в α-Cr2O3-решетку. Среднее состояние окисления составляет +3,20, причем также присутствует фаза, содержащая небольшое количество Cr+6.
Пример получения 5
Получение катализатора 98% хрома/2% никеля (900°С)
Раствор 392,15 г [Cr(NO3)3][9H2O] (0,98 моль), растворенных в 1 л деионизованной воды, обрабатывают 20 мл 1 М водного раствора Ni(NO3)2[6(H2O)] (0,020 моль). Полученный раствор обрабатывают по каплям 225 мл 7,4 М водного гидроксида аммония; рН увеличивается от 1,98 до 8,53 в процессе добавления. Взвесь перемешивают при комнатной температуре в течение 24 ч и затем выпаривают досуха в воздушной среде при 110°С и выдерживают при этой температуре до утра. Высушенный катализатор измельчают в порошок и затем прокаливают в воздушной среде при 900°С в течение 20 ч.
Анализы методами ТЭМ и ЭРС показывают, что данная композиция состоит из кристаллов α-Cr2O3 размером в интервале от примерно 300 до 400 нм с приблизительно однородным введением никеля.
Пример получения 6
Получение катализатора 95% хрома/5% никеля (900°С)
Раствор 380,14 г [Cr(NO3)3][9H2O] (0,95 моль), растворенных в 1 л деионизованной воды, обрабатывают 50 мл 1 М водного раствора Ni(NO3)2[6(H2O)] (0,050 моль). Полученный раствор обрабатывают водным гидроксидом аммония, сушат и прокаливают, как в примере получения 5.
Пример получения 7
Получение катализатора 98% хрома/2% никеля (400°С)
Раствор 588,3 г [Cr(NO3)3][9H2O] (1,47 моль) и 8,72 г (0,030 моль) Ni(NO3)2[6(H2O)], растворенных в 1,5 л деионизованной воды, обрабатывают 7,4 М водного гидроксида аммония до тех пор, пока рН не достигнет 8,5. Введение гидроксида аммония занимает 1,5 ч. Взвесь перемешивают при комнатной температуре в течение 24 ч; гидроксид аммония добавляют время от времени для поддержания рН при примерно 8,5. Смесь затем выпаривают досуха в воздушной среде при 110°С в течение 40 ч. Высушенный катализатор измельчают в порошок и затем прокаливают в воздушной среде при 400°С в течение 24 ч.
Анализы методами ТЭМ и ЭРС показывают, что данный образец состоит из кристаллов α-Cr2O3 размером в интервале от примерно 20 до 100 нм с приблизительно однородным введением никеля. Отсутствует подтверждение образования второй шпинельной фазы в данном образце.
Анализ образца методами ДРЛ и РАС подтверждает, что кристаллиты имеют α-Cr2O3-структуру. Окружение вокруг Ni-атома является сходным с окружением вокруг атомов хрома. Количество никеля, введенного в α-Cr2O3-решетку, составляет примерно 1,6% ат. Шпинельная фаза не наблюдается.
Пример получения 8
Получение катализатора 95% хрома/5% никеля (400°С)
Повторяют методику примера получения 7 с использованием раствора 760,3 г [Cr(NO3)3][9H2O] (1,90 моль) и 29,08 г (0,10 моль) Ni(NO3)2[6(H2O)], растворенных в 2 л деионизованной воды. После введения гидроксида аммония и выпаривания при 110°С твердое вещество прокаливают в воздушной среде при 400°С в течение 24 ч.
Анализы методами ТЭМ и ЭРС показывают, что данный образец состоит из кристаллов α-Cr2O3 с намного большим интервалом размеров (от 10 до 200 нм), чем композиция из примера получения 7, с приблизительно однородным введением никеля в альфа-хромоксидную решетку. Отсутствует подтверждение образования второй шпинельной фазы.
Анализ образца методами ДРЛ и РАС подтверждает, что кристаллиты имеют α-Cr2O3-структуру. Окружение вокруг Ni-атома является сходным с окружением вокруг атомов хрома. Количество никеля, введенного в α-Cr2O3-решетку, составляет примерно 2,0% ат. Наблюдается небольшое количество второй никельсодержащей фазы.
Общая методика анализа продукта
Следующая общая методика поясняет метод, используемый для анализа продуктов реакций фторуглеводородов. Часть общего потока, выходящего из реактора, отбирается в виде образцов под управлением ЭВМ для анализа органического продукта с использованием газового хроматографа, оборудованного селективным детектором массы (ГХ-МС). Газовую хроматографию выполняют с трубкой длиной 20 фут (6,1 м) и диаметром 1/8 дюйм (0,32 см), содержащей перфторированный полиэфир Krytox на инертной углеродной подложке. Поток гелия составляет 30 мл/мин (5,0×10-7 м3/с). Условиями газовой хроматографии являются 60°С в течение начального периода удерживания три минуты с последующим температурным программированием до 200°С со скоростью 6°С/мин.
Массу потока, выходящего из реактора, содержащего органические продукты, а также неорганические кислоты, такие как HCl и HF, обрабатывают водным каустиком перед сбросом.
Все реакции в парообразной фазе проводят при номинальном давлении одна атмосфера.
Пример 9
Никельзамещенный оксид хрома (Cr/Ni 98/2, прокаленный при 400°С, 29,6 г, 20 мл, -12 - +20 меш (1,68-0,84 мм)), полученный как описано в примере получения 7, помещают в реакторную трубу диаметром 5/8 дюйм (1,58 см) из никелевого сплава Inconel™, нагреваемую на псевдоожиженной песочной бане. Катализатор нагревают от 88°С до 175°С в токе азота (50 см3/мин, 8,3×10-7 м3/с) в течение примерно 40 мин. HF и азот совместно подают в реактор при скорости потока каждого 50 см3/мин (8,3×10-7 м3/с). Через 1,8 ч поток азота снижают до 20 см3/мин (3,3×10-7 м3/с), а поток HF увеличивают до 80 см3/мин (1,3×10-6 м3/с). Температуру реактора постепенно увеличивают до 247°С в течение периода времени 1,6 ч и затем продувают азотом 20 см3/мин (3,3×10-7 м3/с) до утра. Обработку HF продолжают со скоростью потока 80 см3/мин (1,3×10-6 м3/с) и азот совместно подают при 20 см3/мин (3,3×10-7 м3/с). Указанные газовые потоки поддерживают в течение 1,8 ч, когда температура возрастает от 249°С до 402°С. Температуру реактора поддерживают при 402°С в течение 0,5 ч. Поток азота затем прекращают и фторирование CFC-1213xa начинают при 300°С с мольным соотношением 20:1 HF:CFC-1213xa с временем взаимодействия 15 с. В указанных условиях потоком, выходящим из реактора, является 94,4 ГХ% поверхности HCFC-226da и 4,1 ГХ% CFC-216aa при 100% превращения CFC-1213xa. Хлор затем совместно подают в реактор; мольное соотношение HF:CFC-1213xa:Cl2 составляет 20:1:4. Состав потока, выходящего из реактора при 350°С, приводится ниже:
Другие продукты включают PCE, CFC-114, CFC-115, FC-218, CFC-1215.
Пример 10
Никельзамещенный оксид хрома (Cr/Ni 95/5, прокаленный при 400°С, 29,2 г, 20 мл, -12 - +20 меш (1,68-0,84 мм)), полученный как описано в примере получения 8, помещают в реакторную трубу диаметром 5/8 дюйм (1,58 см) из никелевого сплава Inconel™, нагреваемую на псевдоожиженной песочной бане. Катализатор нагревают от 68°С до 176°С в токе азота (50 см3/мин, 8,3×10-7 м3/с) в течение примерно 1 ч. HF и азот совместно подают в реактор при скорости потока каждого 50 см3/мин (8,3×10-7 м3/с). Через 1,3 ч поток азота снижают до 20 см3/мин (3,3×10-7 м3/с), а поток HF увеличивают до 80 см3/мин (1,3×10-6 м3/с). Температуру реактора постепенно увеличивают от 176°С до 402°С в течение периода времени 3,3 ч и затем выдерживают при 400°С в течение 0,5 ч. Поток HF затем прекращают и реактор продувают азотом, что позволяет его охладить до 300°С. Фторирование CFC-1213xa начинают при 300°С с мольным соотношением 20:1 HF:CFC-1213xa с временем взаимодействия 15 с. В указанных условиях потоком, выходящим из реактора, является 93,4 ГХ% поверхности HCFC-226da и 4,9 ГХ% CFC-216aa при 100% превращения CFC-1213xa. Хлор затем совместно подают в реактор; мольное соотношение HF:CFC-1213xa:Cl2 составляет 20:1:4 (время взаимодействия 15 с). Состав потока, выходящего из реактора при 350°С, приводится ниже:
Другие продукты включают CFC-13, CFC-114, CFC-114a, CFC-115, CFC-1215, CFC-216cb, CFC-214ab, PCE.
Пример 11
Никельзамещенный оксид хрома (Cr/Ni 98/2, прокаленный при 900°С, 40,27 г, 25 мл, -12 - +20 меш (1,68-0,84 мм)), полученный как описано в примере получения 5, помещают реакторную трубу диаметром 5/8 дюйм (1,58 см) из никелевого сплава Inconel™, нагреваемую на псевдоожиженной песочной бане. Катализатор нагревают от 57°С до 175°С в токе азота (50 см3/мин, 8,3×10-7 м3/с) в течение примерно 1 ч. HF и азот совместно подают в реактор при скорости потока каждого 50 см3/мин (8,3×10-7 м3/с). Через 11 мин поток азота снижают до 20 см3/мин (3,3×10-7 м3/с), а поток HF увеличивают до 80 см3/мин (1,3×10-6 м3/с). Температуру реактора постепенно увеличивают до 400°С в течение периода времени 2,7 ч и поддерживают при 400°С в течение еще 1 ч. В конце указанного периода поток HF прекращают и реактор охлаждают до 280°С и продувают азотом до утра. Хлорфторирование CFC-1213xa начинают при 280°С с HF, CFC-1213xa и хлором в мольном соотношении 20:1:4 с временем взаимодействия 30 с. Состав потока, выходящего из реактора при 340°С, приводится ниже:
Другие продукты включают CFC-1215, CFC-217ca.
Пример 12
Никельзамещенный оксид хрома (Cr/Ni 95/5, прокаленный при 900°С, 40,27 г, 25 мл, -12 - +20 меш (1,68-0,84 мм)), полученный как описано в примере получения 6, помещают реакторную трубу диаметром 5/8 дюйм (1,58 см) из никелевого сплава Inconel™, нагреваемую на псевдоожиженной песочной бане. Катализатор нагревают при 100°С в токе азота (50 см3/мин, 8,3×10-7 м3/с) в течение 40 мин. HF и азот совместно подают в реактор при скорости потока каждого 50 см3/мин (8,3×10-7 м3/с). Через 30 мин поток азота снижают до 20 см3/мин (3,3×10-7 м3/с), а поток HF увеличивают до 80 см3/мин (1,3×10-6 м3/с). Температуру реактора затем постепенно увеличивают до 400°С в течение периода времени 5 ч. В конце указанного периода поток HF прекращают и реактор охлаждают до 280°С и продувают азотом до утра. Хлорфторирование CFC-1213xa начинают при 280°С с HF, CFC-1213xa и хлором, совместно подаваемыми в реактор в мольном соотношении 20:1:4 с временем взаимодействия 30 с. Состав потока, выходящего из реактора при 340°С, приводится ниже:
Другие продукты включают CFC-1215, CFC-1214.
Пример 13
Смешанный никель- и кобальтзамещенный оксид хрома (Cr/Со/Ni 95/3/2, 26,37 г, 19 мл, -12 - +20 меш (1,68-0,84 мм)), полученный как описано в примере получения 1, помещают реакторную трубу диаметром 5/8 дюйм (1,58 см) из никелевого сплава Inconel™, нагреваемую на псевдоожиженной песочной бане. Катализатор нагревают от 81°С до 175°С в токе азота (50 см3/мин, 8,3×10-7 м3/с) в течение примерно 1 ч. HF и азот совместно подают в реактор при скорости потока каждого 50 см3/мин (8,3×10-7 м3/с). Через 0,3 ч поток азота снижают до 20 см3/мин (3,3×10-7 м3/с), а поток HF увеличивают до 80 см3/мин (1,3×10-6 м3/с). Температуру реактора постепенно увеличивают до 400°С в течение периода времени 3,6 ч. Поток HF прекращают и реактор охлаждают до 298°С в токе азота 20 см3/мин (3,3×10-7 м3/с). Хлорфторирование CFC-1213xa начинают при 300°С с HF, CFC-1213xa и хлором, совместно подаваемыми в реактор в мольном соотношении 20:1:4, соответственно, с временем взаимодействия 15 с. Анализ методом ГХ-МС потока, выходящего из реактора при 320°С (мольное соотношение питания 20:1:4) и при 375°С (мольное соотношение питания 30:1:2), приводится ниже:
Другие продукты включают CFC-1215, CFC-114, CFC-114a, HCFC-225da, CFC-113.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ КОБАЛЬТЗАМЕЩЕННОГО ОКСИДА ХРОМА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ КАТАЛИЗАТОРОВ И ПРЕДШЕСТВЕННИКОВ КАТАЛИЗАТОРОВ | 2003 |
|
RU2318594C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ 2-ХЛОР-1,1,1,2,3,3,3-ГЕПТАФТОРПРОПАНА, ГЕКСАФТОРПРОПЕНА И 1,1,1,2,3,3,3-ГЕПТАФТОРПРОПАНА | 2003 |
|
RU2326859C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,1,1,2,2-ПЕНТАФТОРЭТАНА | 2003 |
|
RU2328482C2 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ФТОРИРОВАНИЯ ГАЛОГЕНИРОВАННЫХ УГЛЕВОДОРОДОВ | 2009 |
|
RU2402378C1 |
| СПОСОБ АКТИВАЦИИ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ФТОРСОДЕРЖАЩИХ УГЛЕВОДОРОДОВ | 2015 |
|
RU2594485C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ФТОРИРОВАНИЯ ГАЛОГЕНИРОВАННЫХ УГЛЕВОДОРОДОВ | 2010 |
|
RU2431524C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И АКТИВАЦИИ И СПОСОБ ФТОРИРОВАНИЯ ГАЛОГЕНИРОВАННЫХ УГЛЕВОДОРОДОВ | 2007 |
|
RU2322291C1 |
| КАТАЛИЗАТОР ДЛЯ ФТОРИРОВАНИЯ ГАЛОГЕНИРОВАННЫХ АЛИФАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1990 |
|
RU2007212C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,3,3-ТЕТРАФТОРОПРОПЕНА ГАЗОФАЗНЫМ ФТОРИРОВАНИЕМ ПЕНТАХЛОРОПРОПАНА | 2011 |
|
RU2548902C2 |
| КАТАЛИТИЧЕСКОЕ ГАЗОФАЗНОЕ ФТОРИРОВАНИЕ | 2011 |
|
RU2571415C2 |
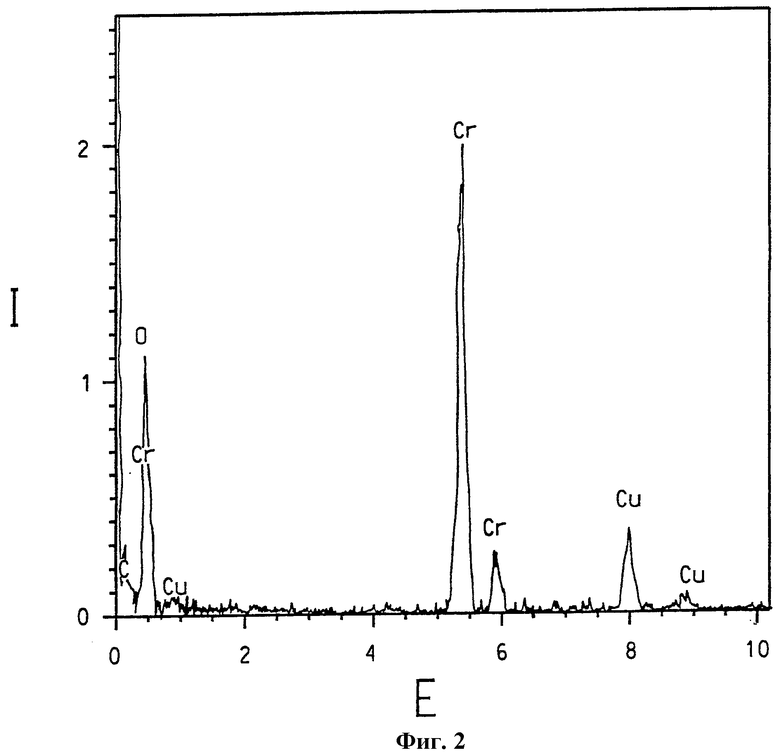
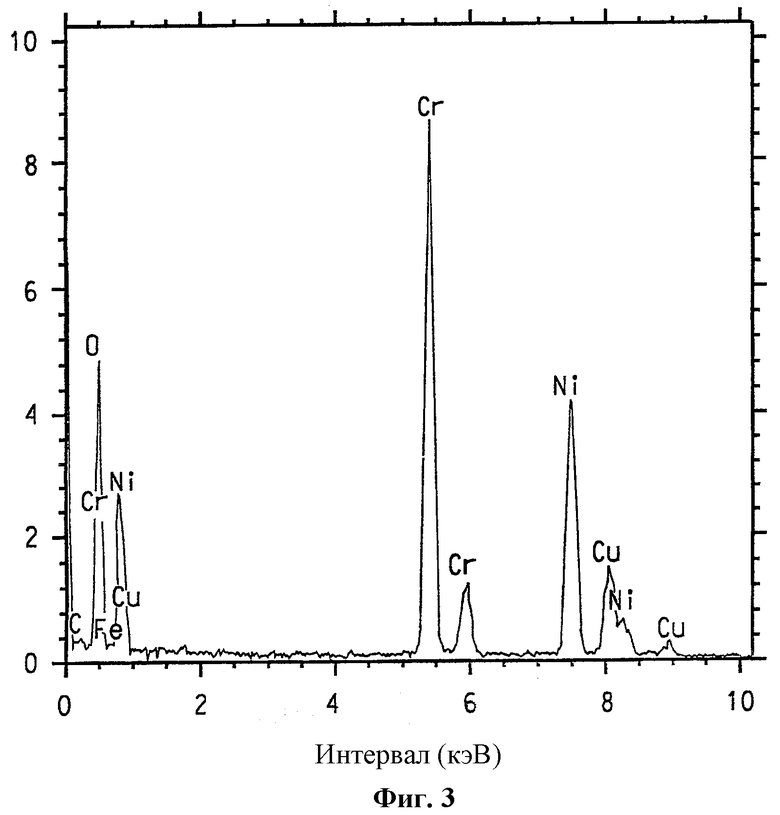
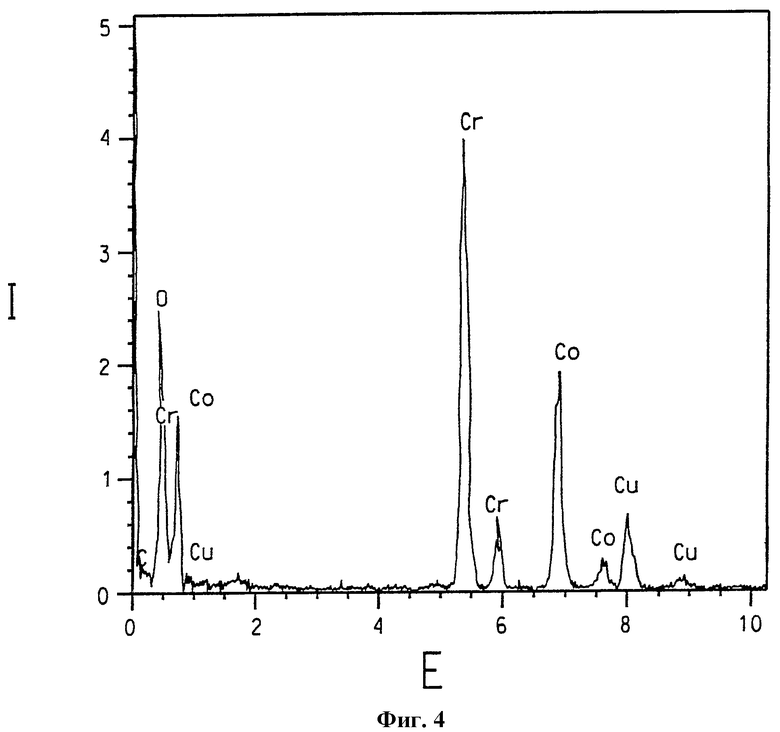
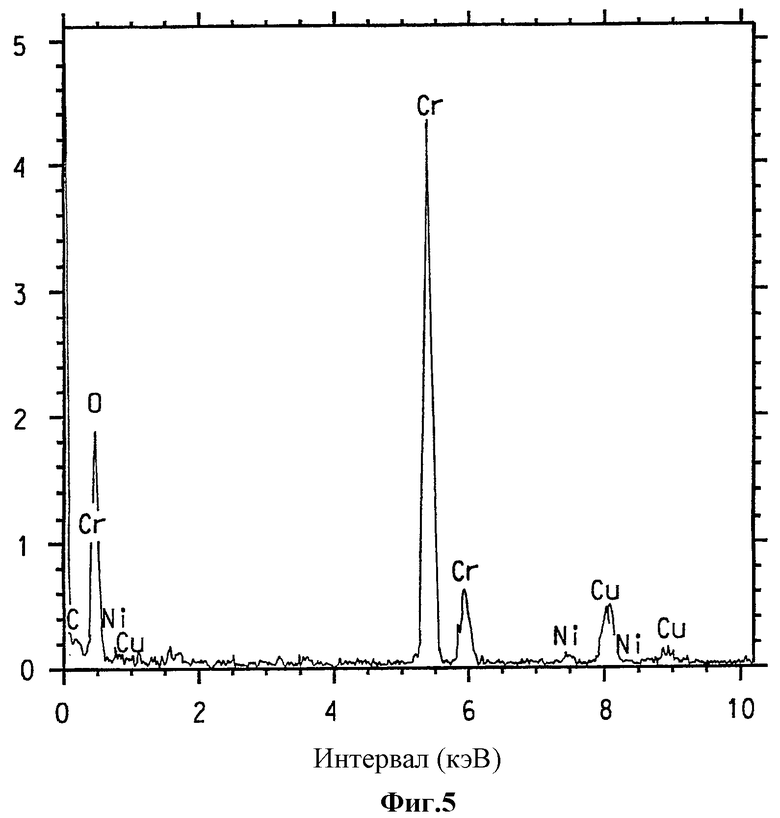
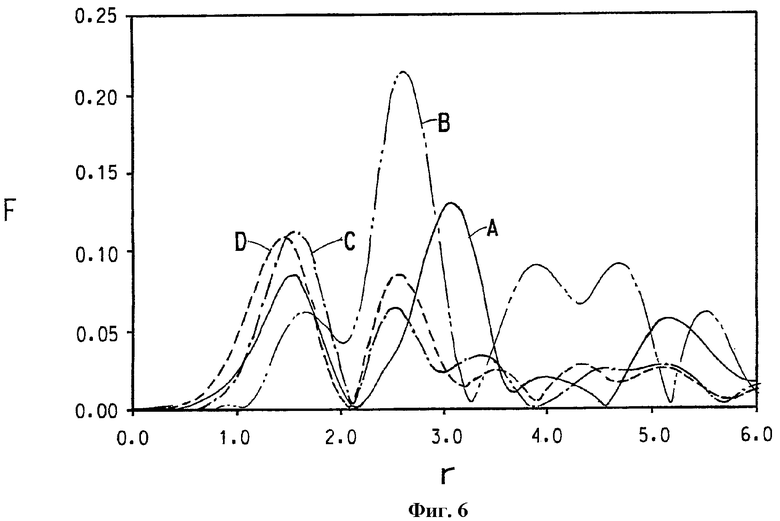
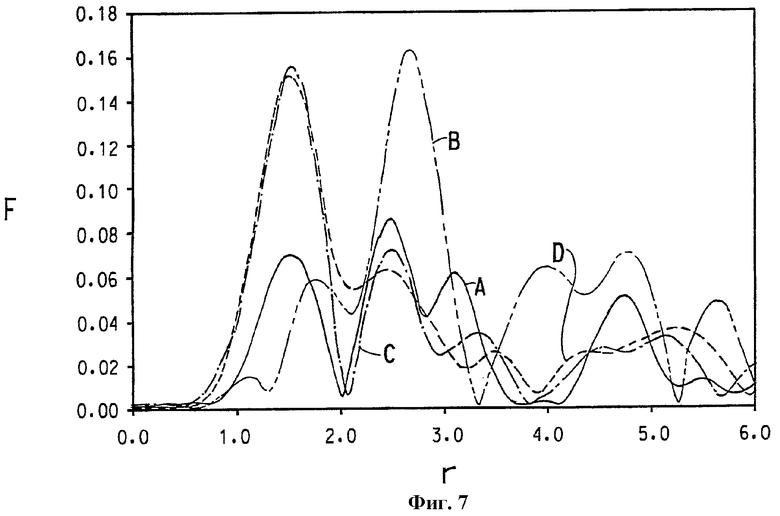
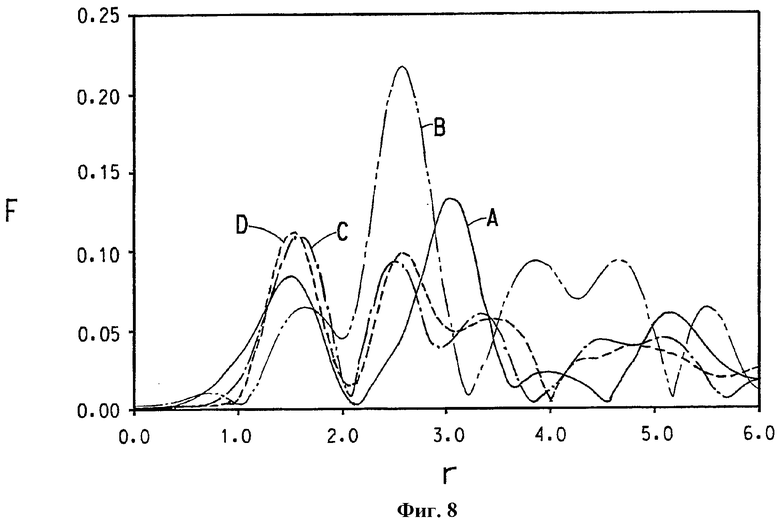
Данное изобретение относится к кристаллическому альфа-оксиду хрома, хромсодержащим каталитическим композициям, способу их получения и к способу изменения фторораспределения в углеводороде и/или галогенированном углеводороде в присутствии указанных каталитических композиций. В заявленном кристаллическом альфа-оксиде хрома от примерно 0,05% ат. до примерно 2% ат. атомов хрома в решетке альфа-оксида хрома замещено атомами никеля и, необязательно, дополнительные атомы хрома в решетке альфа-оксида хрома замещены атомами трехвалентного кобальта при условии, что общее количество атомов никеля и атомов трехвалентного кобальта в решетке альфа-оксида хрома составляет не более 6% ат. При этом указанный оксид хрома получают методом соосаждения твердого вещества введением гидроксида аммония, причем указанный метод включает стадию дополнительного введения избытка нитрата аммония в осажденную смесь до стадии дегидратации и стадию прокаливания при температуре от 375 до 1000°С в присутствии кислорода. Также заявлены хромсодержащие каталитические композиции, содержащие в качестве хромсодержащего компонента кристаллический никельзамещенный альфа-оксид хрома, необязательно обработанный фторирующим агентом. Способ получения композиции включает (а) соосаждение твердого вещества введением гидроксида аммония в водный раствор растворимой соли двухвалентного никеля, растворимой соли трехвалентного хрома и, необязательно, растворимой соли двухвалентного или трехвалентного кобальта, который содержит не менее трех молей нитрата на моль хрома в растворе, имеет концентрацию никеля от примерно 0,05% мол. до примерно 2% мол. от общего содержания никеля, хрома и кобальта (если присутствует) в растворе и имеет общую концентрацию никеля и кобальта (если присутствует) не более 6% мол. от общего содержания никеля, хрома и кобальта (если присутствует) в растворе; и последующим введением в раствор не менее трех молей аммония на моль хрома в растворе; (b) сбор соосажденного твердого вещества, образованного на стадии (а); (с) сушку собранного твердого вещества; и (d) прокаливание высушенного твердого вещества при температуре от 375 до 1000°С в присутствии кислорода. Технический результат - высокая активность каталитической композиции в указанных процессах, 5 н. и 10 з.п. ф-лы, 8 ил., 3 табл.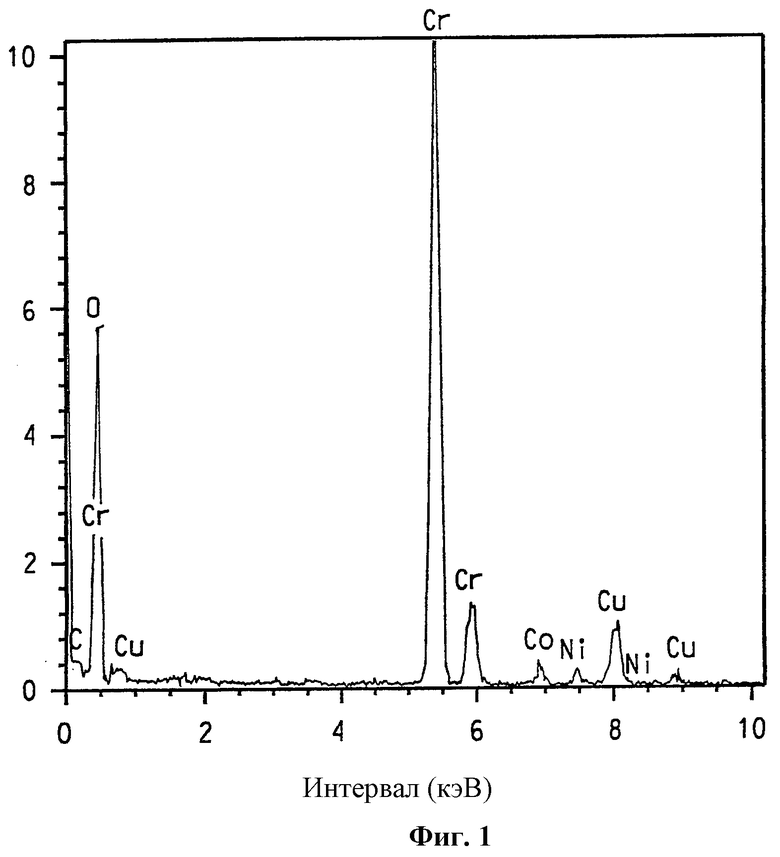
(a) соосаждение твердого вещества введением гидроксида аммония в водный раствор растворимой соли двухвалентного никеля, растворимой соли трехвалентного хрома и, необязательно, растворимой соли двухвалентного или трехвалентного кобальта, который содержит не менее трех молей нитрата на моль хрома в растворе, имеет концентрацию никеля от примерно 0,05 мол.% до примерно 2 мол.% от общего содержания никеля, хрома и кобальта (если присутствует) в растворе, и имеет общую концентрацию никеля и кобальта (если присутствует) не более 6 мол.% от общего содержания никеля, хрома и кобальта (если присутствует) в растворе; и последующим введением в раствор не менее трех молей аммония на моль хрома в растворе;
(b) сбор соосажденного твердого вещества, образованного на стадии (а);
(c) сушку собранного твердого вещества;
(d) прокаливание высушенного твердого вещества при температуре от 375 до 1000°С в присутствии кислорода.
| Устройство для опрессовки сердечников электрических машин при склеивании | 1977 |
|
SU641598A1 |
| Устройство для умножения | 1974 |
|
SU546883A1 |
| US 3804778 А, 16.04.1974 | |||
| US 2001011061 A, 02.08.2001 | |||
| КАТАЛИЗАТОР ДЛЯ ФТОРИРОВАНИЯ НИЗШИХ АЛИФАТИЧЕСКИХ ГАЛОИДУГЛЕВОДОРОДОВ И СПОСОБ ФТОРИРОВАНИЯ НИЗШИХ АЛИФАТИЧЕСКИХ ГАЛОИДУГЛЕВОДОРОДОВ | 1992 |
|
RU2040333C1 |
| RU 2000109577 A, 20.03.2002 | |||
| US 2002006374 A1, 17.01.2002 | |||
| ЕР 0847801 A1, 17.06.1998 | |||
| US 5185482 A, 09.02.1993. | |||
Авторы
Даты
2008-03-10—Публикация
2003-08-21—Подача