Область изобретения
Данное изобретение касается кристаллической формы малеата 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины и ее фармацевтических композиций, промежуточных соединений и способов получения и выделения таких кристаллических форм и композиций, и способов применения таких кристаллических форм и композиций в лечении аномального роста клеток у млекопитающих, в частности людей.
Предпосылки создания изобретения
Мономалеатная соль 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины имеет структуру формулы (I):
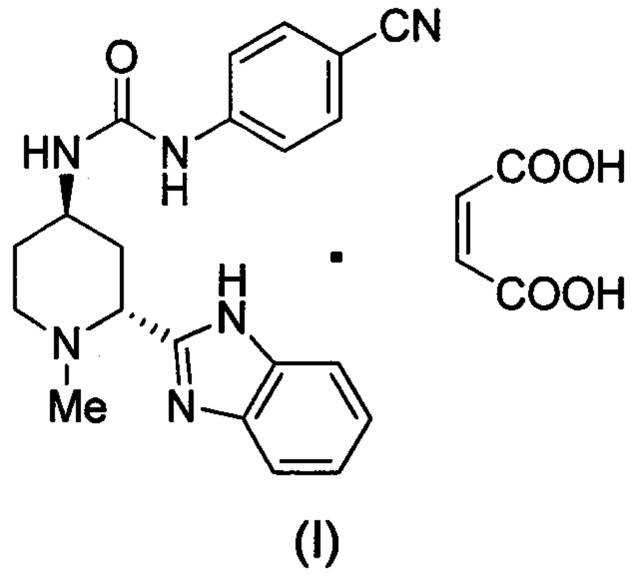
Соединению 1 -((2R,4R)-2-(1H-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевина (PF-04449913) было присвоено международное непатентованное название (INN) гласдегиб, как описано в WHO Drug Information, Vol. 29, No. 1, page 89 (2015), ссылаясь на альтернативное химическое название N-[(2R,4R)-2-(1Н-бензоимидазол-2-ил)-1-метилпиперидин-4-ил]-N'-(4-цианофенил)мочевина. Малеатная соль формулы (I) может быть названа в данном документе как 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины малеат или гласдегиба малеат.
Получение гласдегиба в виде гидрохлоридной соли описывается в международной патентной заявке №PCT/IB2008/001575, опубликованной как WO 2009/004427, и в патентах США №№8,148,401 и 8,431,597, содержание каждого из которых включено в данный документ в виде ссылки в их полном объеме.
Гласдегиб представляет собой ингибитор рецептора белка somoзатемеd (Smo), компонент пути передачи сигналов hedgehog (Hh), который является потенциальной терапевтической мишенью при ряде раковых заболеваний человека, в частности гематологических злокачественных новообразований, включая острый миелоидный лейкоз (AML), острый лимфобластный лейкоз (ALL), острый лимфобластный лейкоз (смML), миелофиброз (MF) и миелодиспластические синдромы (MDS). Открытие гласдегиба и его получение в виде соли моногидрата дигидрохлорида было описано Munchhof et al. (Med. Chem., Lett, 2012, 3:106-111). Способ асимметрического синтеза гласдегиба было описан Peng et al. (Org. Lett., 2014,16:860-863).
Представленное изобретение предусматривает кристаллический гласдегиба малеат, который имеет улучшенные свойства, такие как улучшенная химическая и термическая стабильность при хранении, и пониженная гигроскопичность, при этом сохраняя химическую и энантиомерную стабильность.
Изобретение также предусматривает комплекс (1:1) кристаллический гласдегиб - имидазол и кристаллическую соль гласдегиба (S)-манделат, которые используются для получения гласдегиба малеата и других солей с высоким выходом и с высокой химической чистотой.
Краткое описание изобретения
Каждый из вариантов осуществления, описанных ниже, может быть объединен с каким-либо другим вариантом осуществления, описанным в данном документе, не противоречащим варианту осуществления, с которым он объединяется.
В одном аспекте, изобретение предусматривает кристаллическую форму гласдегиба малеата. В конфетном аспекте, изобретение предусматривает кристаллический гласдегиба малеат (форма 1), как далее описано в данном документе.
В конкретных вариантах осуществления каждого из аспектов изобретения, кристаллический гласдегиба малеат (форма 1) характеризуется одним или несколькими из следующих способов: (1) порошковая рентгеновская дифрактография (PXRD) (2θ); (2) спектроскопия комбинационного рассеяния (см-1); или (3) 13С твердотельная ЯМР-спектроскопия (м.д.).
В другом аспекте, изобретение предусматривает кристаллический гласдегиба малеат (форма 1), которая характеризуется наличием:
(1) порошковой рентгеновской дифрактограммы (PXRD) (2θ), содержащей: (а) один, два, три, четыре, пять или больше, чем пять пиков, выбранных из группы, состоящей из пиков в таблице 1 при °2θ±0,2 °2θ; (b) один, два или три пика выбранных из группы, состоящей из характерных пиков в таблице 1 при °2θ±0,2°2θ; или (с) пики при значениях 2θ, по существу, такие же, как показано на фигуре 1; или
(2) спектр комбинационного рассеяния, содержащий: (а) один, два, три, четыре, пять, или больше, чем пять значений волнового числа (см-1), выбранных из группы, состоящей из значений в таблице 2 в см-1 ± 2 см-1; (b) один, два, три, четыре, пять, или больше, чем пять значений волнового числа (см-1), выбранных из группы, состоящей из характерных значений в таблице 2 в см-1 ± 2 см-1; или (с) значения волнового числа (см-1), по существу, такие же, как показано на фигуре 2; или
(3) 13С твердотельный ЯМР спектр (м.д.), содержащий: (а) один, два, три, четыре, пять, или больше, чем пять значений резонанса (м.д.), выбранных из группы, состоящей из значений в таблице 3 в м.д. ± 0,2 м.д.; (b) один, два или три значения резонанса (м.д.), выбранных из группы, состоящей из характерных значений в таблице 3 в м.д. ± 0,2 м.д.; или (с) значения резонанса (м.д.), по существу, такие же, как показано на фигуре 3;
или комбинация каких-либо двух или трех из вышеперечисленных вариантов осуществления (1)(а)-(с), (2)(а)-(с) или (3)(а)-(с), при условии, что они не противоречат друг другу.
В другом аспекте, изобретение, кроме того, предусматривает фармацевтическую композицию, содержащую кристаллический гласдегиба малеат (форма 1), в соответствии с каким-либо из аспектов или вариантов осуществления, описанных в данном документе, и фармацевтически приемлемый эксципиент.
В другом аспекте, изобретение предусматривает способ лечения аномального роста клеток у млекопитающего, включая человека, включающий введение млекопитающему терапевтически эффективного количества кристаллического гласдегиба малеата (форма 1).
В другом аспекте, изобретение предусматривает способ лечения аномального роста клеток у млекопитающего, включая человека, включающий введение млекопитающему терапевтически эффективного количества фармацевтической композиции, согласно представленному изобретению, содержащей кристаллический гласдегиба малеат (форма 1), в соответствии с каким-либо из аспектов или вариантов осуществления, описанных в данном документе.
Краткое описание чертежей
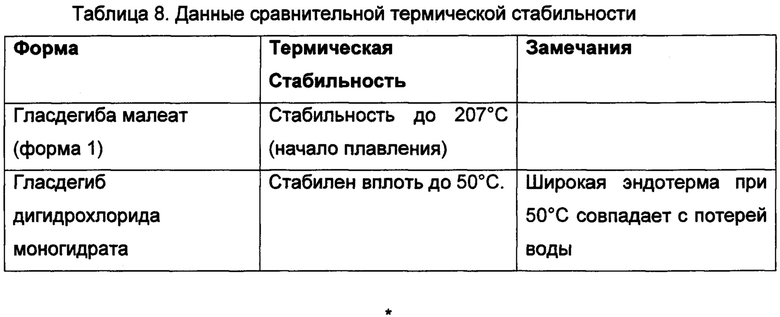
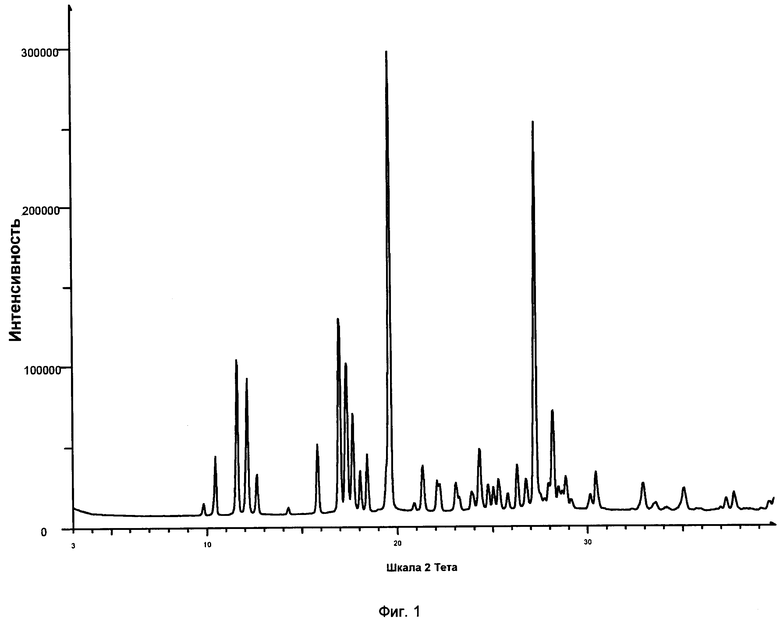
Фигура 1. PXRD дифрактограмма кристаллического гласдегиба малеата (форма 1).
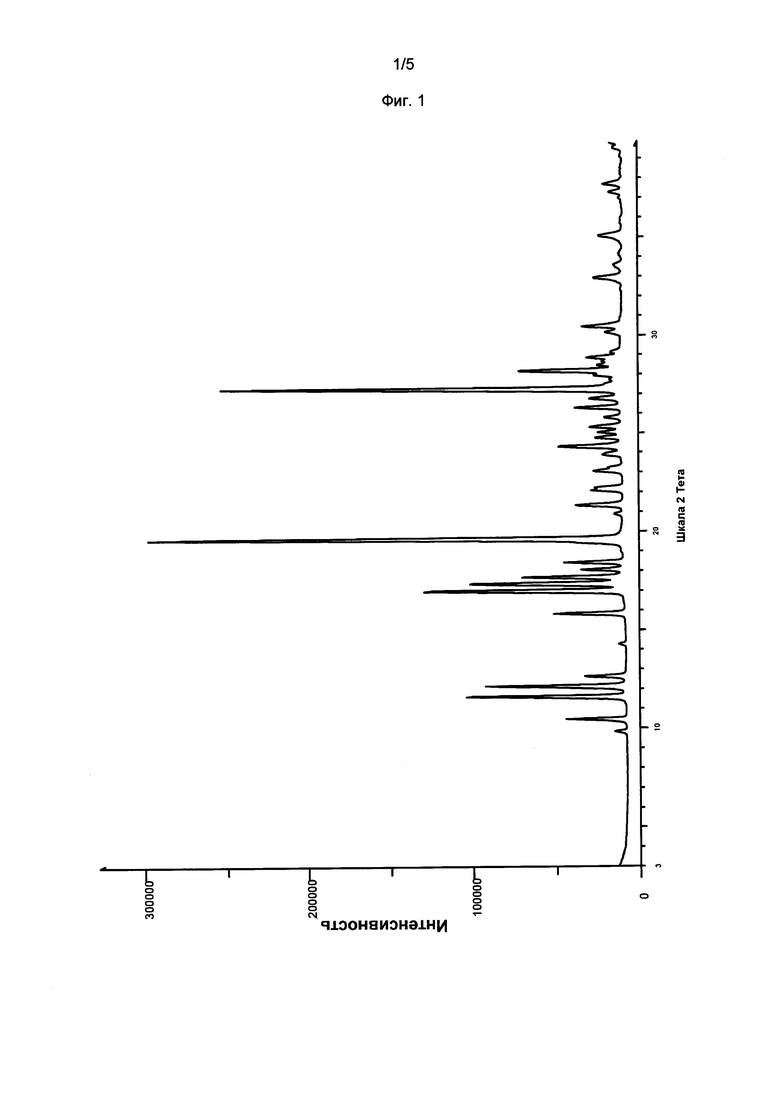
Фигура 2. ФТ-спектр комбинационного рассеяния кристаллического гласдегиба малеата (форма 1).
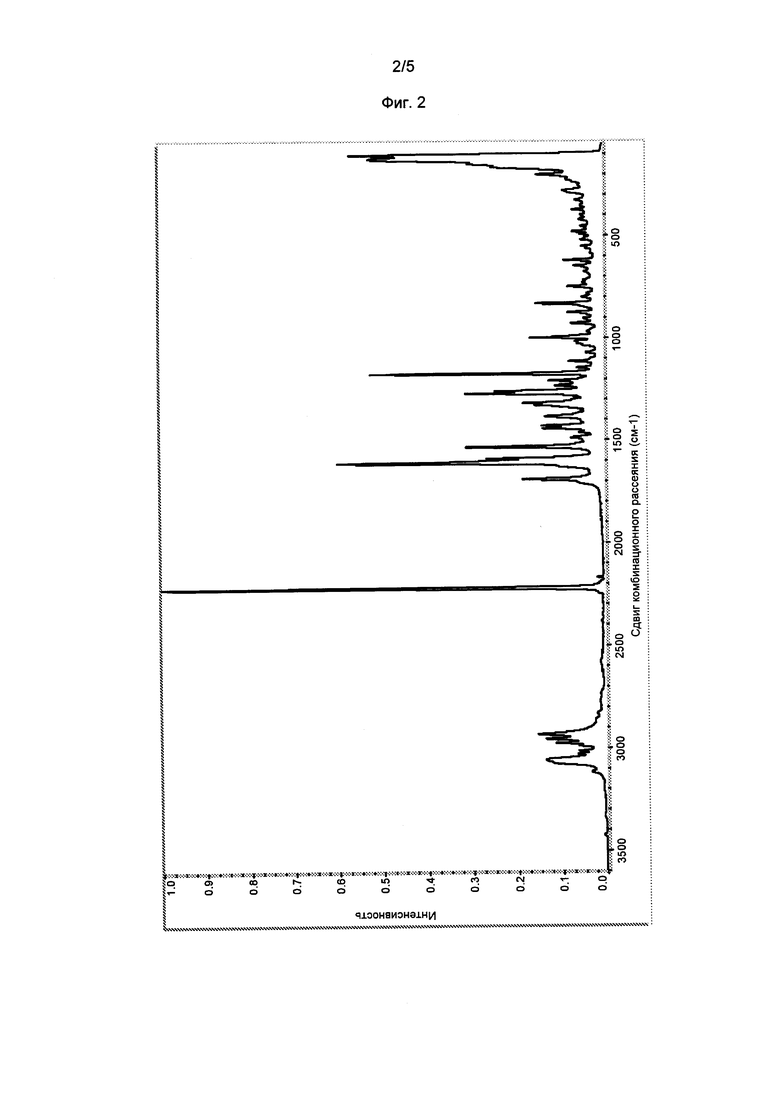
Фигура 3. 13С твердотельный ЯМР спектр кристаллического гласдегиба малеата (форма 1).
Фигура 4. PXRD дифрактограмма кристаллического комплекса гласдегиб - имидазол (1:1).
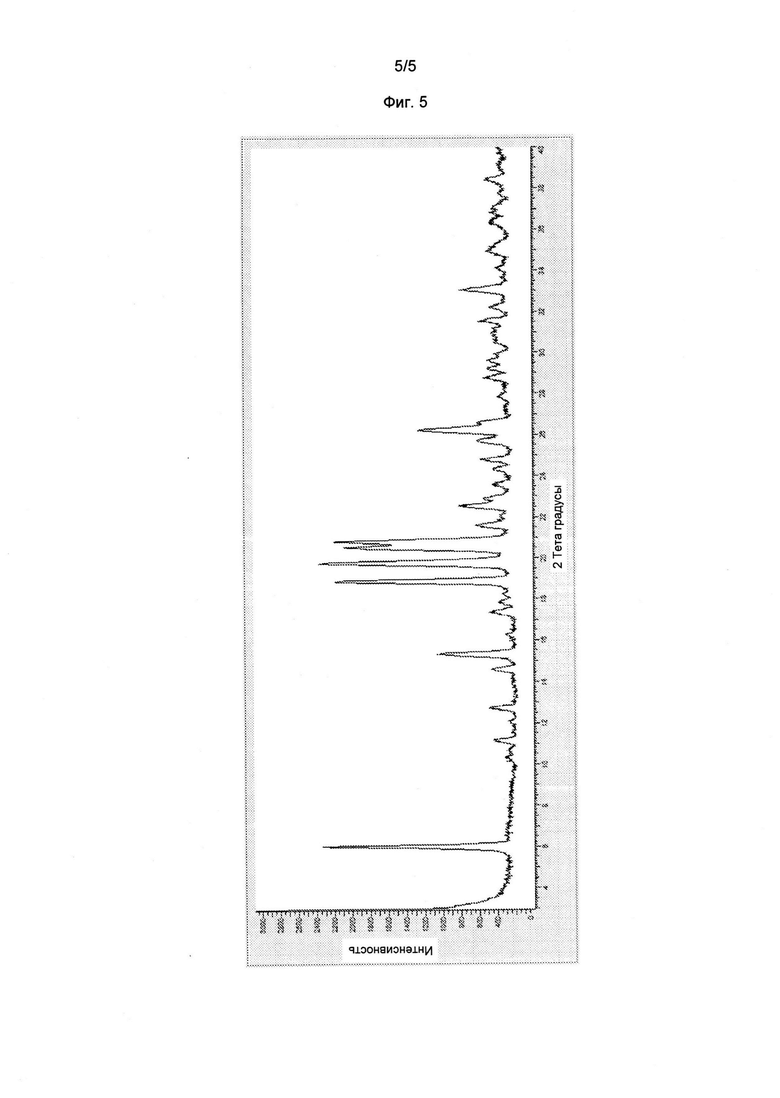
Фигура 5. PXRD дифрактограмма кристаллического гласдегиба (S)-манделата.
Подробное описание изобретения
Представленное изобретение может быть понято более легко с помощью ссылки на следующее подробное описание вариантов осуществления изобретения и примеры, включенные в данный документ. Следует понимать, что терминология, используемая в данном документе, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения. Кроме того, следует понимать, что, если конкретно не определено в данном документе, терминология, используемая в данном документе, должна иметь свое традиционное значение, которое известно в соответствующем уровне техники.
Как используется в данном документе, форма единственного числа включает ссылки на множественное число, если не указано иное. Например, «заместитель» включает один или несколько заместителей.
Как используется в данном документе, если не указано иначе, термин "аномальный рост клеток" касается клеточного роста, который не зависит от нормальных регуляторных механизмов (например, потеря контактного торможения).
Как используется в данном документе, если не указано иначе, термин "лечить" или "лечение" означает изменение на обратное развития, облегчение, подавление развития или предотвращение расстройства, или состояния, к которому такой термин применяется, или одного или нескольких симптомов такого расстройства или состояния. Термин «лечение», как используется в данном документе, если не указано иное, касается действия лечения, поскольку «лечение» определено непосредственно выше.
Термин "приблизительно", как используется в данном документе, означает, что имеющееся значение попадает в пределы приемлемого стандарта погрешности среднего значения, когда рассматривается квалифицированным специалистом в данной области, например, ±20%, предпочтительно ±10% или более предпочтительно ±5% от среднего значения.
Как используется в данном документе, термин "по существу такой же самый" означает, что во внимание принимается вариабельность, характерная для конкретного способа. Например, что касается положений пика рентгеновской дифракции лучей, термин "по существу такой же самый" означает, что во внимание принимается характерная вариабельность положения и интенсивности пика. Специалисту в данной области техники будет понятно, что положения пиков (2θ) будут демонстрировать некоторую вариабельность, обычно вплоть до ±0,2°. Кроме того, квалифицированный специалист в данной области будет понятно, что относительная интенсивность пиков будет показывать вариабельность между аппаратами, а также вариабельность из-за степени кристалличности, предпочтительной ориентации, поверхности подготовленного образца и других факторов, известных квалифицированным специалистам в данной области, и их следует рассматривать только как качественные критерии. Аналогично, значения волнового числа спектра комбинационного рассеяния (см-1) показывают вариабельность, обычно вплоть до ±2 см-1, в то время как спектры 13С и 19F твердотельного ЯМР (м.д.) проявляют вариабельность, как правило, вплоть до ±0,2 м.д.
Термин "кристаллический", как используется в данном документе, означает наличие регулярно повторяющегося расположения молекул или внешних поверхности плоскостей. Кристаллические формы могут отличаться в зависимости от термодинамической стабильности, физических параметров, рентгеновской структуры и способа получения.
Изобретение, описанное в данном документе, подходящим образом может быть осуществлено на практике в отсутствие какого(их)-либо элемента(ов), которые конкретно не раскрыты в данном документе. Таким образом, например, в каждом случае в данном документе какой-либо из терминов "содержащей", "состоящий в основном из", и "состоящий из" может быть заменен каким-либо из двух других терминов.
В некоторых вариантах осуществления каждого из аспектов изобретения, кристаллический гласдегиба малеат (форма 1) характеризуется своей порошковая рентгеновской дифрактограмма (PXRD). В других вариантах осуществления каждого из аспектов изобретения, кристаллический гласдегиба малеат (форма 1) характеризуется своим спектром комбинационного рассеяния. В других вариантах осуществления каждого из аспектов изобретения, кристаллический гласдегиба малеат (форма 1) характеризуется свим спектром 13С твердотельного ЯМР.
В следующих вариантах осуществления, кристаллическая форма характеризуется комбинацией двух или больше из данных способов.
Кристаллический гласдегиба малеат (Форма 1)
В одном аспекте, изобретение предусматривает кристаллический гласдегиба малеат (форма 1).
В некоторых вариантах осуществления, гласдегиба малеат (форма 1) имеет PXRD дифрактограму, содержащую пик при значении 2θ: 11,6 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограму, содержащую пик при значении 2θ: 12,1 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограму, содержащую пик при значении 2θ: 19,6 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограму, содержащую пик при значении 2θ: 17,0 °2θ±0,2° 2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пик при значении 2θ: 17,7 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пики при значениях 2θ: 11,6 и 12,1 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пики при значениях 2θ: 11,6 и 19,6 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пики при значениях 2θ: 12,1 и 19,6 °2θ±0,2 °2θ. В другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пики при значениях 2θ: 11,6, 12,1 и 19,6 °2θ±0,2 °2θ. В еще другом варианте осуществления, форма 1 имеет PXRD дифрактограмму, содержащую пики при значениях 2θ:11,6, 12,1, 17.0, 17,7 и 19,6 °2θ±0,2 °2θ.
В конкретных вариантах осуществления, гласдегиба малеат (форма 1) имеет PXRD дифрактограму, содержащую: (а) один, два, три, четыре, пять или больше, чем пять пиков, выбранных из группы, состоящей из пиков в таблице 1 при °2θ±0,2 °2θ; (b) один, два, три, четыре, пять или шесть характерных пиков, выбранных из группы, состоящей из пиков в таблице 1; или (с) пики при значениях 20, по существу, таких же, как показано на фигуре 1.
В некоторых вариантах осуществления, гласдегиба малеат (форма 1) имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 2219 см-1 ± 2 см-1. В других вариантах осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 см-1 ± 2 см-1. В другом варианте осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1534 см-1 ± 2 см-1. В другом варианте осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1175 см-1 ± 2 см-1. В других вариантах осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1. В других вариантах осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1534 и 2219 см-1 ± 2 см'-1. В следующих вариантах осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1534, 1612 и 2219 см-1 ± 2 см-1. В следующих вариантах осуществления, форма 1 имеет спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1175, 1534, 1612 и 2219 см-1 ± 2 см-1.
В конкретных вариантах осуществления, гласдегиба малеат (форма 1) имеет спектр комбинационного рассеяния, включающий: (а) один, два, три, четыре, пять или больше, чем пять значений волнового числа (см-1), выбранных из группы, состоящей из значений в таблице 2 в см-1 ± 2 см-1; (b) один, два, три, четыре, пять или больше, чем пять значений волнового числа (см-1), выбранных из группы, состоящей из характерных значений в таблице 2 в см-1 ±2 см-1; или (с) значения волнового числа (см-1), по существу, такие же, как показано на фигуре 2.
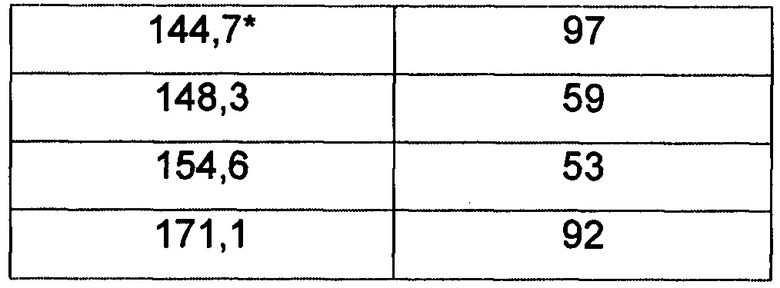
В некоторых вариантах осуществления, гласдегиба малеат (форма 1) имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 134,8 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 144,7 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 148,3 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8 и 134,8 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8 и 144,7 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8 и 148,3 м.д. ±0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 134,8 и 144,7 м.д. ± 0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 134,8 и 148,3 м.д.±0,2 м.д. В другом варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 144,7 и 148,3 м.д. ± 0,2 м.д. В следующем варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8, 134,8 и 144,7 м.д. ± 0,2 м.д. В следующем варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8, 134,8 и 148,3 м.д. ± 0,2 м.д. В следующем варианте осуществления, форма 1 имеет спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8, 134,8, 144,7 и 148,3 м.д. ± 0,2 м.д.
В конкретных вариантах осуществления, гласдегиба малеат (форма 1) имеет спектр 13С твердотельного ЯМР (м.д.), содержащий: (а) один, два, три, четыре, пять или больше, чем пять значений резонанса (м.д.), выбранных из группы, состоящей из значений в таблице 3 в м.д. ± 0,2 м.д.; (b) один, два или три значений резонанса (м.д.), выбранных из группы, состоящей из характерных значений в таблице 3 в м.д. ± 0,2 м.д.; или (с) значения резонанса (м.д.) по существу, такие же, как показано на фигуре 3.
В следующих вариантах осуществления, гласдегиба малеат (форма 1) характеризуется комбинацией каких-либо двух или трех из вариантов осуществления, описанных выше применительно к форме 1, которые являются не противоречащими друг другу. Иллюстративные варианты осуществления, которые могут быть использованы для однозначной характеристики кристаллической формы 1, представлены ниже.
В одном варианте осуществления, форма 1 имеет: (а) порошковую рентгеновскую дифрактограму, содержащую пик при значении 2θ: 11,6 и 12,1 °2θ±0,2 °2θ; и (b) спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1.
В одном варианте осуществления, форма 1 имеет: (а) порошковую рентгеновскую дифрактограмму, включающую пик при значении 2θ: 11,6 и 12,1 °2θ±0,2 °2θ; (b) спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1; и (с) спектр 13С твердотельного ЯМР, включающий значение резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
В еще одном варианте осуществления, форма 1 имеет: (а) спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1; и (b) спектр 13С твердотельного ЯМР, включающий значение резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
В одном варианте осуществления, форма 1 имеет: (а) порошковую рентгеновскую дифрактограмму, включающую пик при значении 2θ: 11,6 и 12,1 °2θ±0,2 °2θ; и (b) спектр 13С твердотельного ЯМР, включающий значение резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
В следующем варианте осуществления, форма 1 имеет: (а) порошковую рентгеновскую дифрактограмму, включающую пик при значении 2θ: 19,6 °2θ±0,2 °2θ; (b) спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 2219 см-1 ± 2 см-1; и (с) спектр 13С твердотельного ЯМР, включающий значение резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
В другом аспекте, изобретение предусматривает гласдегиб в виде 1:1 комплекса с имидазолом. Имидазольный комплекс выделяется с высоким химическим выходом и чистотой, и может использоваться для очистки примесей, образующихся во время химического синтеза, до образования гласдегиба малеат.В следующем аспекте, изобретение предусматривает способ получения гласдегиба малеат, включающий обработку комплекса гласдегиб-имидазол (1:1) малеиновой кислотой, тем самым обеспечивая соль. В другом аспекте, изобретение предусматривает гласдегиба малеат (форма 1), полученный из комплекса гласдегиб - имидазол в соответствии с описанным способом.
В другом аспекте, изобретение предусматривает соль гласдегиба (S)-манделат. Манделатная соль выделяется с высоким химическим выходом и чистотой, и может также использоваться для очистки примесей, образующихся во время химического синтеза. Манделатная соль может быть получена in situ во время окончательного выделение и очистки соединений или за счет раздельного взаимодействия свободного основания гласдегиба с миндальной кислотой и выделения образовавшейся таким образом соли. После этого соль может быть преобразована в форму свободного основания и затем подвергнута взаимодействию с достаточным количеством малеиновой кислоты для получения соли гласдегиба малеата обычным способом.
В другом аспекте, изобретение предусматривает фармацевтическую композицию, содержащую кристаллический гласдегиба малеат (форма 1) в соответствии с каким-либо из аспектов или вариантов осуществления, описанных в данном документе, и фармацевтически приемлемый эксципиент.
Фармацевтические композиции согласно представленному изобретению могут, например, быть в форме, приемлемой для перорального введения в виде таблетки, капсулы, пилюли, порошка, композиций с замедленным высвобождением, раствора или суспензии для парентеральной инъекции в виде стерильного раствора, суспензии или эмульсии, для местного применения в виде мази или крема или для ректального введения в виде суппозитория. Фармацевтическая композиция может быть в стандартных лекарственных формах, подходящих для однократного введения точных доз. Фармацевтическая композиция будет включать обычный фармацевтический носитель или эксципиент и активный фармацевтический ингредиент. Кроме того, она может включать другие медицинские или фармацевтические агенты, носители, адъюванты и т.д.
Иллюстративные формы для парентерального введения включает растворы или суспензии, содержащие активные соединения в стерильных водных растворах, например, водные растворы пропиленгликоля или декстрозы. При желании такие лекарственные формы могут быть соответствующим образом забуферированы.
Подходящие фармацевтические носители включают инертные разбавители или наполнители, воду и различные органические растворители. Фармацевтические композиции могут, при желании, содержать дополнительные ингредиенты, такие как ароматизаторы, связующие вещества, эксципиенты и тому подобное. Таким образом, для перорального введения могут быть использованы таблетки, содержащие различные эксципиенты, такие как лимонная кислота, вместе с различными разрыхлителями, такими как крахмал, альгиновая кислота и некоторые сложные силикаты, а также связывающие агенты, такие как сахароза, желатин и аравийская камедь. Кроме того, смазывающие агенты, такие как стеарат магния, лаурилсульфат натрия и тальк, часто используются в процессе таблетирования. Твердые композиции аналогичного типа также могут быть использованы в мягких и твердых заполненных желатиновых капсулах. Предпочтительные материалы включают лактозу или молочный сахар и высокомолекулярные полиэтиленгликоли. Когда желательными являются водные суспензии или эликсиры для перорального введения, активное соединение в них может быть комбинировано с различными подслащивающими или ароматизирующими агентами, окрашивающими веществами или красителями и, по необходимости, эмульгирующими агентами или суспендирующими агентами вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин или их комбинации.
Способы получения различных фармацевтических композиций с определенным количеством активного соединения известны или будут очевидны для квалифицированных специалистов в данной области. В качестве примеров, смотрите Remington's Pharmaceutical Sciences. Mack Publishing Company, Easter, Pa., 15th Edition (1975).
Примеры
Приведенные ниже примеры и получения дополнительно иллюстрируют и поясняют конкретные аспекты и варианты осуществления изобретения. Следует понимать, что объем представленного изобретения не ограничивается областью применения следующих примеров.
Общий способ 1. Порошковая рентгеновская дифрактография (PXRD)
Анализ порошковой рентгеновской дифрактографии проводили с использованием дифрактометра Bruker AXS D8 ADVANCE, снабженного источником излучения Cu (среднее значение K-α). Система снабжена 2,5 аксиальными щелями Soller на первичной стороне. Вторичная сторона использует 2,5 аксиальных щелей Soller и механизированные щели. Дифрагированное излучение обнаруживалось детектором Lynx Eye ХЕ. Напряжение и сила тока рентгеновской трубки были установлены на 40 кВ и 40 мА, соответственно. Данные собирались в тета-тета гониометре на длине волны Cu от 3,0 до 40,0 градусов 2-тета с размером шага 0,037 градуса и шагом времени 1920 секунд. Образцы готовили, помещая их в держатель с низким фоном и вращали во время сбора. Данные собирались с использованием программного обеспечения Bruker DIFFRAC Plus (версия 9.0.0.2), и анализ выполнялся с использованием программного обеспечения EVA diffract plus.
Файл данных PXRD не был обработан до поиска пиков. Используя алгоритм поиска пиков в программном обеспечении EVA, пики, выбранные с пороговым значением 1 и значением ширины 0,3, использовались для предварительных пиковых присвоений. Вывод автоматических заданий визуально проверяется для того, чтобы обеспечить правильность и, при необходимости, внести изменения вручную. Обычно выбирались пики с относительной интенсивностью ≥2%. Пики, которые не были разрешены или соответствовали шуму, не выбирались. Типичная вариабельность, связанная с положением пика из PXRD составляет +/-0,2° 2-тета.
Общий способ 2. ФТ-спектроскопии комбинационного рассеяния
Спектры комбинационного рассеяния были собраны с использованием оборудования Nicolet NXR FT-Raman, присоединенного к FT-IR монтажным столикам. Спектрометр оснащен лазером 1064 нм Nd:YVO4 и германиевым детектором, охлаждаемым жидким азотом. Перед сбором данных проводилась верификации инстументального выполнения и калибровки с использованием полистирола. Образцы анализировали в стеклянных ЯМР-пробирках, которые вращались во время спектрального сбора. Оптимальные спектры API были собраны с использованием лазера мощности 0,5 Вт и 128 дополнительных сканирований. Диапазон сбора составлял 3700-50 см-1. Данные спектры регистрировали с использованием разрешения 4 см-1 и аподизации Happ-Genzel.
Шкала интенсивности была нормализована до 1 перед тем как пики собирались. Пики были идентифицированы вручную с использованием программного обеспечения Thermo Nicolet Omnic 7.3. Положение пика выбиралось на пике максимума, и пики определялись только как таковые, если на каждой стороне был наклон; плечи на пиках не были включены. Для оптимального API абсолютный порог 0,015 с чувствительностью 77 был использован во время сбора пиков. Положение пика округлялось до ближайшего целого числа, используя стандартную практику (0,5 округляется в большую сторону, 0,4 округляется в меньшую сторону). Пики с нормированной пиковой интенсивностью между (1-0,75), (0,74-0,30), (0,29-0) были обозначены как сильные, средние и слабые, соответственно. Ожидается, что, поскольку ФТ-комбинационного рассеяния и дисперсного комбинационного рассеяния спектроскопии являются подобными методами, положения пиков, указанные в данном документе для ФТ-спектров комбинационного рассеяния будут соответствовать тем, которые будут наблюдаться с использованием измерений дисперсного комбинационного рассеяния, при условии соответствующей калибровки прибора. Используя описанный выше метод комбинационного рассеяния, вариабельность, связанная со спектральным измерением, составляет +/- 2 см-1.
Обший способ 3. Твердотельный ЯМР
Твердотельный ЯМР (ттЯМР) анализ проводили при температуре и давлении окружающей среды в зонде Bruker-BioSpin CPMAS, расположенном в ЯМР спектрометре Bruker-BioSpin Avance III 500 МГц (1H частота). Упакованный ротор был ориентирован под магическим углом и вращался на 14,0 кГц. Углеродный ттЯМР спектр собирали, используя эксперимент по кросс-поляризации и вращению под магическим углом развязанного протона (CPMAS). При спектральном захвате применялось фазово-модулированное поле развязки протонов 80-100 кГц. Время контакта кросс-поляризации было установлено равным 2 мс, и время рециркуляции - до 11 секунд. Количество сканирований было скорректировано для получения адекватного соотношения сигнал к шуму. Углеродный спектр соотносили, используя внешний стандарт кристаллического адамантана, устанавливая его резонанс в верхнем поле до 29,5 м.д. (как определено по чистому ТМС).
Автоматический подбор пиков выполнялся с использованием программного обеспечения Bruker-BioSpin TopSpin версии 3.2. Как правило, для предварительного выбора пиков использовалось пороговое значение относительной интенсивности 5%. Вывод автоматизированной подборки пиков визуально проверяется, чтобы убедиться в истинности, и регулируется, при необходимости, были сделаны вручную. Хотя в данном документе указываются конкретные значения пика в 13С твердотельном ЯМР, существует диапазон для данных значений пиков из-за различий в инструментах, образцах и подготовке образцов. Это является обычной практикой в области твердотельного ЯМР из-за вариации, присущей пиковым значениям. Типичная вариабельность для значения Х-оси химического сдвига 13С составляет порядка плюс-минус 0,2 м.д. для кристаллического твердого вещества. Высоты пиков твердотельного ЯМР, описанные в данном документе представляют собой относительные интенсивности. Интенсивности твердотельного ЯМР могут варьировать в зависимости от фактической установки экспериментальных параметров CPMAS и тепловой истории образца.
Пример 1
Получение комплекса 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины и имидазола (1:1)
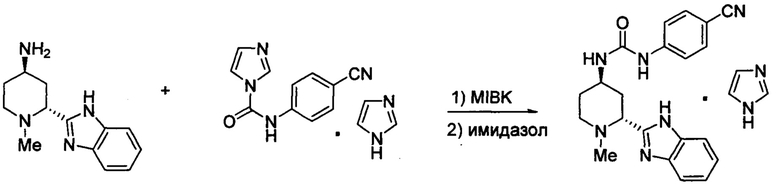
В реактор объемом 250 мл, снабженный верхнеприводной мешалкой добавляли (2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-амин (3,24 г, 14,1 ммоль) (полученный в соответствии с Peng et al., Org. Lett. 2014, 16:860-863) в виде раствора в воде (63 мл), содержащего 20% диметилсульфоксид. К раствору добавляли 4-метил-2-пентанон (метил изобутил кетон, MIBK) (91 мл), с последующим добавлением комплекса N-(4-цианофенил)-1Н-имидазол-1-карбоксамида и H-имидазола (1:1) (5,18 г, 17,6 ммоль) (полученный в соответствии с Peng et al.). Реакционную смесь нагревали при 45°С в течение 1 часа. Добавляли диатомовую землю (0,5 г, фильтрующую добавку), и фильтровали двухфазную смесь. Водный слой удаляли, и органический слой промывали водой (33 мл). Имидазол (0,96 г, 14,1 ммоль) добавляли вместе с дополнительным 4-метил-2-пентаноном (18 мл). Раствор перегоняли до конечного объема of 50 мл. Полученную в результате суспензию фильтровали и промывали 4-метил-2-пентаноном (13 мл). Полученное в результате твердое вещество сушили в вакуумной печи при 60°С в течение 12 часов, получая комплекс 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины и имидазола (1:1) (4,55 г, 10,3 ммоль, 73% выход). 1Н ЯМР (400 МГц, ДМСО-d6): δ 12,38 (ш с, 1Н); 12,07 (ш с, 1Н); 8,94 (с, 1Н); 7,67 (д, J=8,4 Гц, 2 Н); 7,65 (м, 1Н); 7,58 (д, J=8,4 Гц, 2Н); 7,55 (д, J=7,5 Гц, 1Н); 7,43 (ш д, J=7,5 Гц, 1 Н); 7,14 (м, 2Н); 7,02 (с, 2Н); 6,75 (д, J=7,1 Гц, 1 Н); 4,08 (м, 1Н); 3,63 (дд, J=10,4, 3,2 Гц, 1Н); 2,90 (дт, HJ=11,9, 4,2 Гц, 1Н); 2,51 (р, J=1,8 Гц, 2 Н); 2,40 (тд„ J=11,7, 3,0 Гц, 1Н); 2,06 (с, ЗН); 2,03 (м, 1Н); 1,92 (м, 1Н); 1,86 (м, 1Н); 1,72 (м, 1Н); 13С ЯМР (101 МГц, ДМСО) δ 156,17, 154,34, 145,2, 135,6, 133,7, 122,3, 121,5, 119,9, 118,9, 117,8, 111,7, 102,9, 59,1,50,4, 44,2,42,9, 36,5, 30,3.
Характеристика комплекса гласдегиба и имидазола
Данные PXRD
Фигура 4 показывает данные PXRD для кристаллического комплекса гласдегиба и имидазола (1:1), собранные в соответствии с общим способом 1.
Пример 2
Получение малеата 1-((2R,4R)-2-(1H-бензо[d]иимидазол-2-ил)-1 -метилпиперидин-4-ил)-3-(4-цианофенил)мочевины (форма 1)
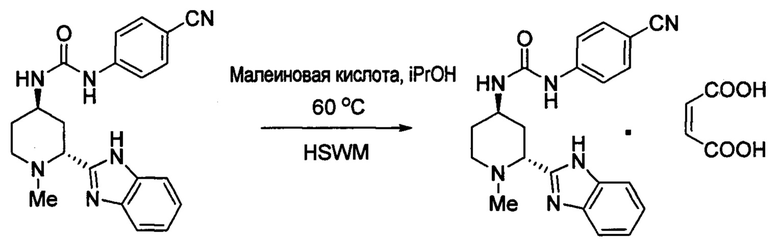
В реактор объемом 1 л, снабженный верхнеприводной мешалкой и мельницей влажного помола с высоким усилием сдвига (HSWM), добавляли 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевину в виде свободного основания (38,2 д; 102 ммоль) (полученную, как описано Munchhof et al., Med. Сhem., Lett, 2012, 3:106-111) и изопропанол (988 мл; 26 мл/г). Суспензию затем нагревали до 60°С для того, чтобы получить прозрачный раствор. Раствор малеиновой кислоты в изопропаноле отдельно получали за счет растворения малеиновой кислоты (14,28 г; 123 ммоль; 1,2 экв.) в изопропаноле (115 мл; 3 мл/г). При этом HSWM работал (3200-8500 об./мин.), добавляли 20% раствор малеиновой кислоты, и реакция поддерживалась до тех пор, пока раствор не стал туманным. HSWM замедлялся (3500 об./мин.), и остальная часть раствора малеиновой кислоты добавлялась в течение 1 часа. После выдерживания суспензии в течение 1 часа при 60°С, партию охлаждали до 10°С в течение 2 часов и гранулировали в течение ночи. Твердое вещество выделяли фильтрованием, промывали и сушили при 60°С.Названное соединение (40,1 г; 801 ммоль) выделяли в виде белого до не совсем белого порошка с выходом 80%. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,00 (с, 1Н), 7,70 (д, J=8,8 Гц, 2Н), 7,62 (дд, J=6,0, 3,3 Гц, 2Н), 7,57 (д, J=8,8 Гц, 2Н), 7,25 (дд, J=6,1, 3,2 Гц, 2Н), 6,73 (д, J=7,5 Гц, 1Н), 6,08 (с, 2Н), 4,40 (с, 1Н), 3,91 (д, J=11,5 Гц, 1Н), 3,44 (д, J=12,2 Гц, 1Н), 3,19 (с, 1Н), 2,53 (с, 3Н), 2,35 (д, J=13,2 Гц, 1Н), 2,08 (д, J=13,3 Гц, 1Н), 1,91 (кв, J=12,4 Гц, 1Н), 1,79 (кв, J=12,4 Гц, 1Н); 13С ЯМР (101 МГц, ДМСО) δ 168,0, 154,7, 105,0, 145,3, 138,4, 135,6, 133,7, 123,0, 119,9, 118,0, 115,9, 103,1, 57,9, 50,5, 41,9, 41,7, 34,6, 28,0.
Пример 3
Получение малеата 1-((2R,4R)-2-(1H-бензо[d]имидазол-2-ил)-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины (форма 1)
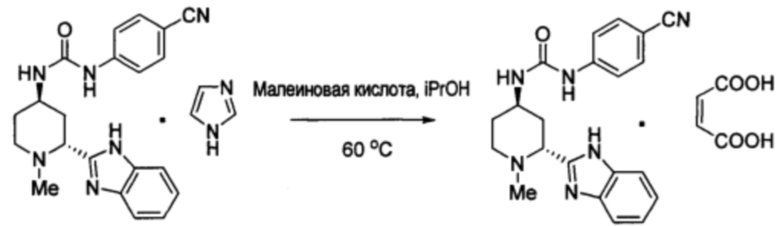
В 250 мл кубический реактор Flexy, снабженный верхнеприводной мешалкой, добавляли комплекс 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины и имидазола (1:1) (7 г, 15,8 ммоль) и изопропанол (140 мл; 20 мл/г имидазольного комплекса). Суспензию нагревали до 60°С и выдерживали до тех пор, пока не был получен прозрачный раствор. Раствор малеиновой кислоты (34,8 ммоль, 2,2 экв.) в водн. изопропаноле (1% масс/масс.) получали отдельно. Добавляли тридцати процентный раствор малеиновой кислоты, и смесь перемешивали в течение 5 мин. Гласдегиба малеат (77,6 мг, 1%) добавляли в качестве затравки, с последующим добавлением оставшейся части раствора малеиновой кислоты в течение 30 мин. После выдерживания при 60°С в течение 30 мин., суспензию охлаждали до 20°С в течение 60 минут и гранулировали в течение дополнительных 60 мин. После диспергирования с помощью ультразвука в течение 3 мин., суспензию фильтровали, промывали изопропанолом (16 мл), с последующим промыванием водой (2×31 мл). Твердое вещество сушили в печи при 60°С в течение 12 часов, получая гласдегиба малеат (форма 1) (15,1 ммоль, 7,40 г) в виде коричневого порошка с выходом 95,4% с чистотой >98%. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,00 (с, 1Н), 7,70 (д, J=8,8 Гц, 2Н), 7,62 (дд, J=6,0, 3,3 Гц, 2Н), 7,57 (д, J=8,8 Гц, 2Н), 7,25 (дд, J=6,1, 3,2 Гц, 2Н), 6,73 (д, J=7,5 Гц, 1Н), 6,08 (с, 2Н), 4,40 (с, 1Н), 3,91 (д, J=11,5 Гц, 1Н), 3,44 (д, J=12,2 Гц, 1Н), 3,19 (с, 1Н), 2,53 (с, 3Н), 2,35 (д, J=13,2 Гц, 1Н), 2,08 (д, J=13,3 Гц, 1Н), 1,91 (кв, J=12,4 Гц, 1Н), 1,79 (кв, J=12,4 Гц, 1Н); 13С ЯМР (101 МГц, ДМСО) δ 168,0, 154,7, 105,0, 145,3, 138,4, 135,6, 133,7, 123,0, 119,9, 118,0, 115,9, 103,1, 57,9, 50,5, 41,9, 41,7, 34,6, 28,0.
Характеристика гласдегиба малеата (форма 1)
Данные PXRD
Фигура 1 показывает данные PXRD для кристаллического гласдегиба малеата (форма 1), собранные в соответствии с общим способом 1. Список пиков PXRD при углах дифракции 2-тета° (°2θ)±0,2 °2θ и их относительные интенсивности представлены в таблице 1. Характерные положения пиков PXRD обозначаются звездочкой.
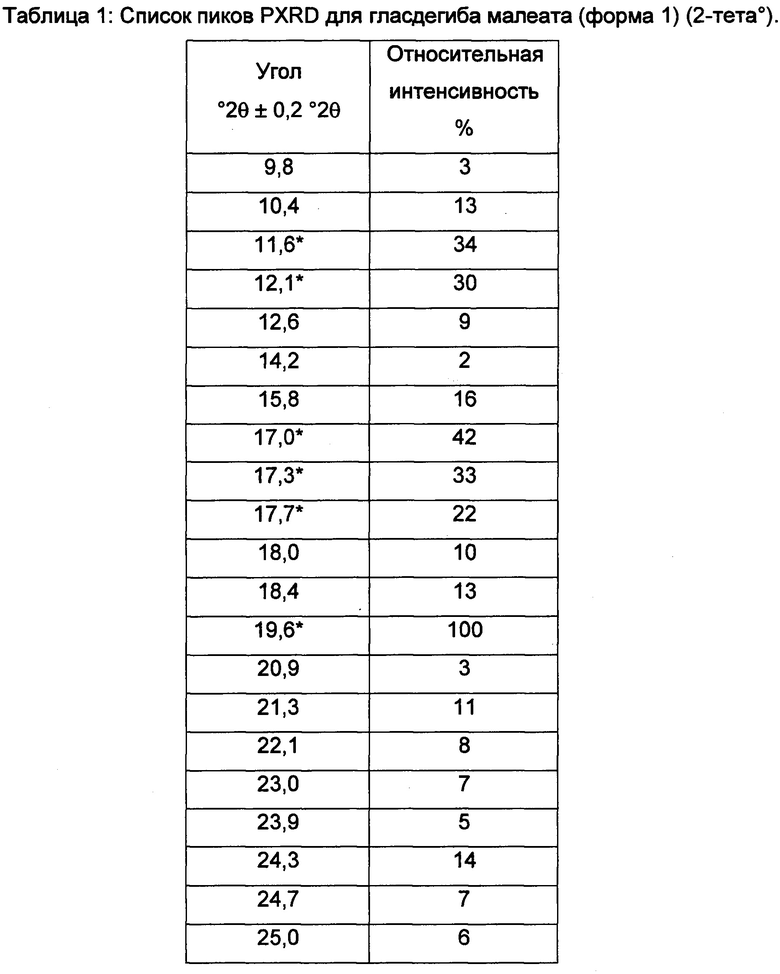
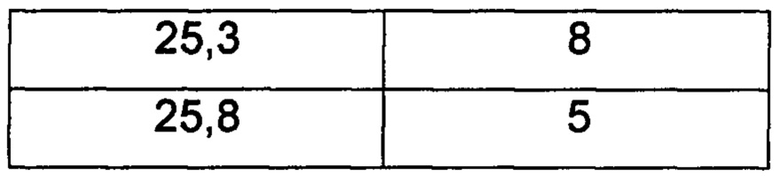
Данные ФТ-комбинационного рассеяния
Фигура 2 показывает FT-Спектр комбинационного рассеяния для кристаллического гласдегиба малеата (форма 1), собранные в соответствии с общим способом 2. Список пиков ФТ-комбинационного рассеяния (см-1) и качественные интенсивности представлены в таблице 2 в см-1 ± 2 см-1. Характерные пики ФТ-комбинационного рассеяния (см-1) обозначены звездочкой. Нормализованные интенсивности пиков указаны следующим образом: сл. = слабый; ср. = средний; с = сильный.


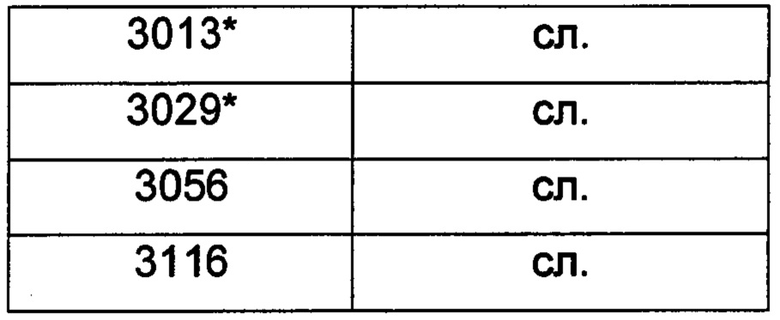
Данные ттЯМР
Фигура 3 показывает углеродный CPMAS спектр кристаллического гласдегиба малеата (форма 1), который был собран в соответствии с общим способом 3. Химические сдвиги выражаются в миллионных долях (м.д.) и ссылаются на внешний образец твердофазного адамантана при 29,5 м.д. Список химических сдвигов ттЯМР 13С (м.д.) представлены в таблице 3 в м.д. ± 0,2 м.д. Характеристические химические сдвиги ттЯМР 13С (м.д.) обозначены звездочкой.
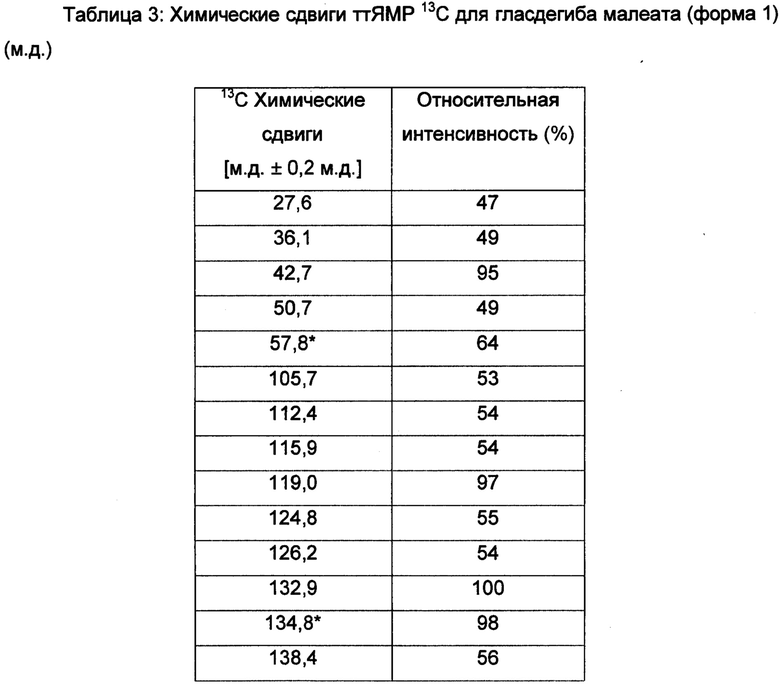
Пример 4
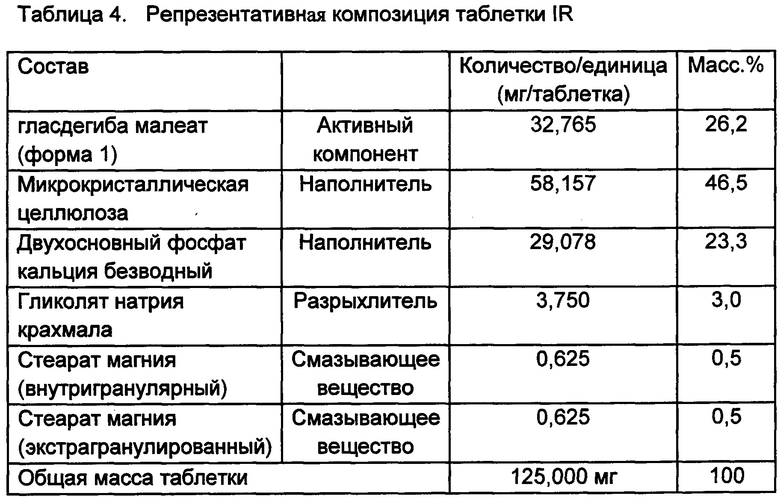
Репрезентативный состав лекарственного препарата гласдегиба малеата (форма 1)
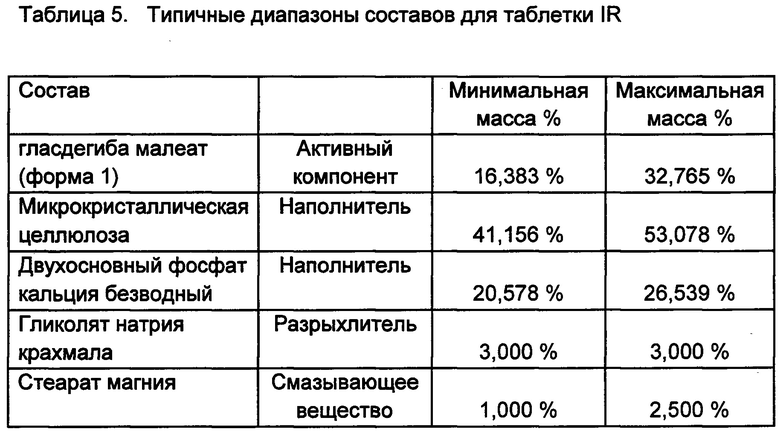
Репрезентативный препарат немедленного высвобождения (IR) кристаллического гласдегиба малеата (форма 1) представлен в таблице 4. Типичные диапазоны для эксципиентов в таких препаратах представлены в таблице 5.
Данные PXRD
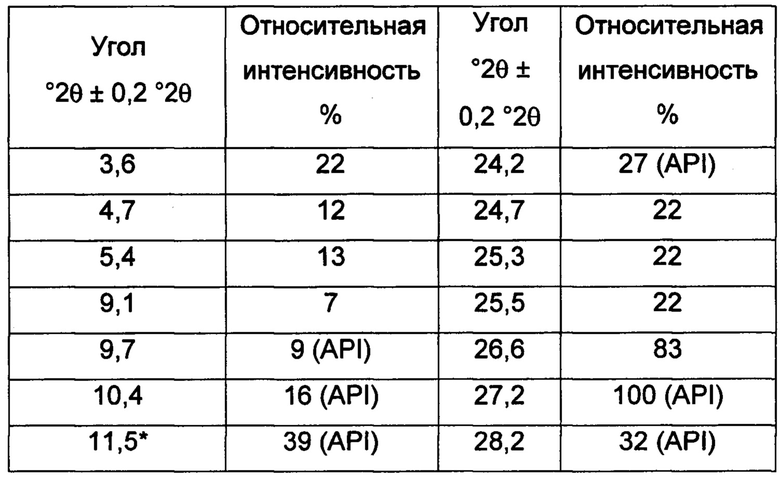
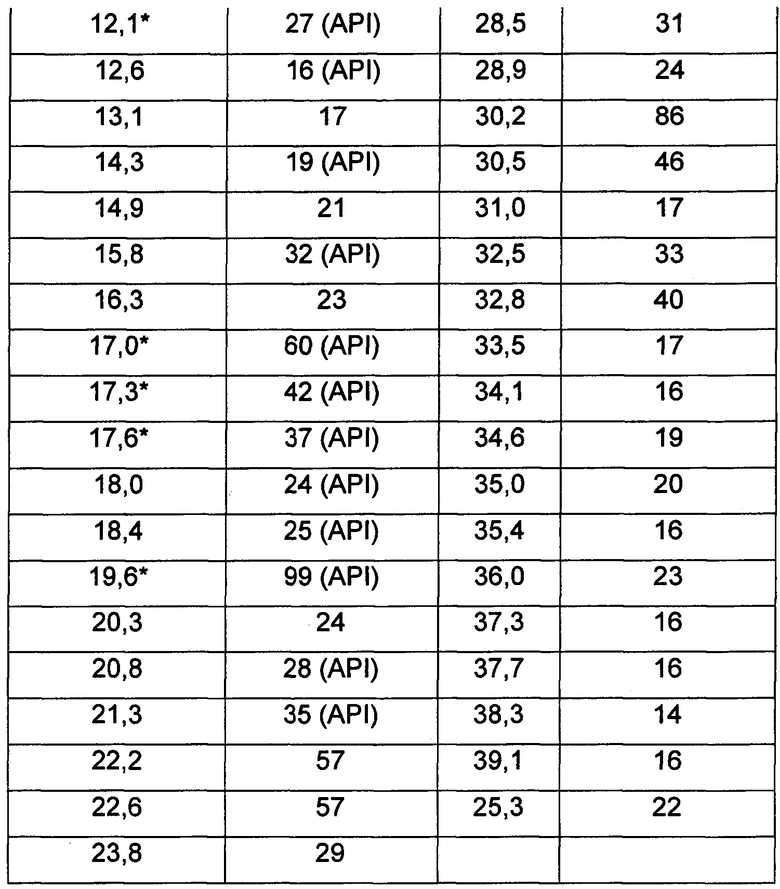
Таблица 6 представляет список пиков PXRD при углах дифракции 2-тета° (°2θ)±0,2 °2θ и их относительные интенсивности для лекарственного продукта, содержащего кристаллический гласдегиба малеат (форма 1), собранные в соответствии с общим способом 1. Характерные PXRD положения пиков обозначены звездочкой.
Таблица 6: Список пиков PXRD для лекарственного продукта гласдегиба малеата (форма 1) (2-тета°). Отмеченные звездочкой положения пиков представляют собой характерные пики.
Пример 5
Получение соли (S)-манделата 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины
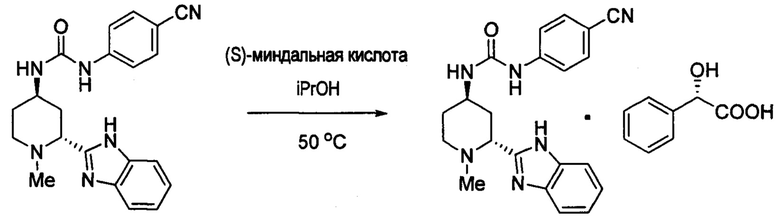
1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевину в виде свободного основания (318 мг, 0,85 ммоль) растворяли в 10 мл изопропанола в сцинтилляционном флаконе, снабженном стержнем мешалки. Раствор нагревали до 50°С для того, чтобы обеспечить полное растворение. К раствору медленно добавляли S-(+)-миндальную кислоту (~1,1 экв.) в виде раствора 30 мг/мл в изопропиловом спирте. После добавления небольшого количества кристаллов соли (S)-манделата в качестве затравки, раствор становился мутным. Суспензию выдерживали при 50°С в течение ~1 часа перед тем, как вернуть ее к комнатной температуре и гранулировали в течение 12 часов. Полученное в результате твердое вещество выделяли фильтрованием с использованием фильтра Ватмана №2 и сушили в течение 12 часов при 50°С в вакуумной печи. Приблизительно 400 мг гласдегиба (S)-манделата было получено. Кристаллы затравки получали путем осаждения из смеси гласдегиба в виде свободного основания, полученного из исходного раствора в ацетонитриле (~30 мг/мл), и S-(+)-миндальной кислоты в виде раствора ТГФ, который перемешивали при комнатной температуре в течение ночи после нагревания при 60°С в течение ~1 часа. Спектры 1Н ЯМР spectra согласуются с (S)-манделатной солью.
Характеристика соли гласдегиба (S)-манделата
Масштабную партию (S)-манделатной соли анализировали с использованием PXRD и дифференциальной сканирующей калориметрии (ДСК). PXRD получали на рентгеновском порошковом дифрактометре Bruker D8 с системой GADDS С2. Образцы сканировали от ~6 до 38 градусов 2-тета в течение 60 секунд и осциллировали на 0,5 мм по центру. ДСК получали ТА ДСК Q1000. Образец нагревали при 10°С/мин от 25°С до 300°С.
Данные PXRD
Фигура 5 показывает данные PXRD для кристаллического гласдегиба (S)-манделата, собранные в соответствии с общим способом 1.
ДСК
Термограмма ДСК показала резкую эндотерму при 216°С.
Пример 6
Сравнительные данные по стабильности
Сравнительные данные по химической и физической стабильности были получены для ядер таблеток, содержащих моногидрат дигидрохлорида гласдегиба (диНСl⋅Н2O) и гласдегиба малеата (форма 1), которые хранили при 50°С/75% относительной влажности (отн. вл.) в течение 6 недель. Ядра таблеток были получены в процессе выполнения сухой грануляции в композиции состава, содержащей, содержащей микрокристаллическую целлюлозу, дикальция фосфат, гликолят натрия крахмала и стеарат магния при активном уровне загрузки лекарственного средства 5%. Ядра таблеток хранили в открытой посуде (без упаковки), расположенной в каиере с 50°С/75% отн. вл., и анализировали через 6 недель хранения. Аналитические испытания включали ВЭЖХ/анализ на чистоту и твердотельный ЯМР (для твердой формы).
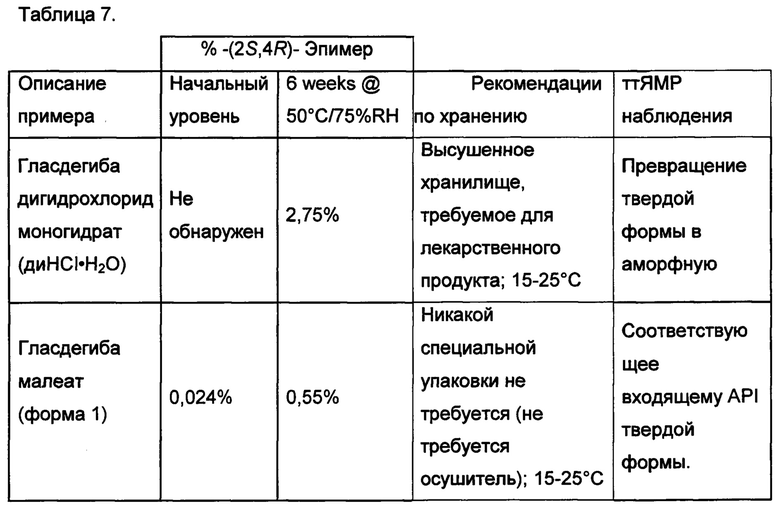
Контролируемый первичный продукт разложения представляет собой эпимерный 1-((2S,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевину, которая имеет структуру:
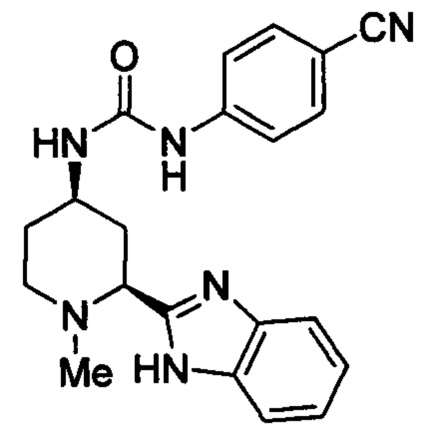
Статистически разработанное 21-дневное исследование на стабильность было проведено для таблеток гласдегиба малеата и таблеток гласдегиб дигидрохлорида, содержащих 5% нагрузки активного лекарственного средства. Дизайн исследования основан на работе с литературой, которая демонстрирует моделирование разложения, наблюдаемых твердых пероральных лекарственных форм. Смотрите Waterman et al., Pharmaceutical Research, 24(4): 780-790 (2007). Таблетки хранились в открытых стеклянных бутылках и подвергались воздействию различных температур, влажности и продолжительности.
Рекомендуемая упаковка для таблеток гласдегиба дигидрохлорида моногидрата представляет собой бутылочку HDPE/IS с осушителем. Отмеченые условия хранения данного продукта составляют 15-25°С. Основываясь на исследовании ускоренной стабильности, сфокусированном на образовании (2S,4R)-эпимера с целевым ограничением спецификации NMT 0,5%, срок годности предписанный для гласдегиба дигидрохлорида моногидрата (бутылка 60сс HDPE, 30 счетных таблеток) при 25°С/60% отн. вл. составляет приблизительно 5 лет с осушителем, и меньше, чем 2 года, при хранении без осушителя.
Рекомендуемая упаковка для таблеток гласдегиба малеата представляет собой бутылочку HDPE/IS, и никакой осушитель не требуется. Отмеченые условия хранения данного продукта составляют 15-25°С. Основываясь на исследовании ускоренной стабильности, сфокусированном на образовании (2S,4R)-эпимера с целевым ограничением спецификации NMT 0,5%, срок годности предписанный для гласдегиба малеата (бутылка 60сс HDPE, 30 счетных таблеток) при 25°С/60% отн. вл. составляет больше, чем 6 лет при хранении без осушителя.
Пример 7.
Данные сравнительной термостабильности
Данные сравнительной термостабильности были получены для гласдегиба дигидрохлорида моногидрата (диНСl⋅H2O) и гласдегиба малеата (форма 1). Измерения дифференциальной сканирующей калориметрии (ДСК) проводились с использованием оборудования Discovery DSC (ТА инструмент), снабженного охлаждающим аксессуаром для охлаждения. Все эксперименты проводились в стандартных/Tzero алюминиевых тиглях. Константу ячейки определяли с использованием индия, и калибровку температуры проводили с использованием индия и олова в качестве стандартов. Все измерения проводились при непрерывной продувке сухим азотом (50 мл/мин). Приблизительно 2-5 мг твердого образца взвешивали в стандартном/Tzero алюминиевом тагле, закупоривали не герметично и нагревали от 25°С до 250°С со скоростью нагрева 10°С/мин. Экспериментальные данные были проанализированы с использованием коммерчески доступного программного обеспечения (программное обеспечение ТА Universal Analysis 2000/Trios, ТА Instruments).
Основываясь на данных о термической стабильности, твердая форма диНСl моногидрата может быть неустойчивой при определенных условиях выделения и хранения из-за низкой температуры дегидратации. Малеатная форма оказывается стабильной в широком температурном диапазоне. Высокий уровень стабильности формы для малеатной соли может обеспечить улучшенный контроль в технологическом процессе, обработке, изготовлении и хранении для для данной формы.
Модификации могут быть сделаны для указанного выше без отхода от основных аспектов изобретения. Хотя изобретение подробно описано со ссылкой на один или несколько конкретных вариантов осуществления, квалифицированным специалистам в данной области будет понятно, что могут быть внесены изменения в варианты осуществления, конкретно раскрытые в данной заявке, и все же данные модификации и улучшения находятся в пределах объема и духа изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКИЕ ТВЕРДЫЕ ФОРМЫ 6-КАРБОКСИ-2-(3,5-ДИХЛОРФЕНИЛ)БЕНЗОКСАЗОЛА | 2015 |
|
RU2692252C2 |
| СОЛИ И ПОЛИМОРФЫ 8-ФТОР-2-{4-[(МЕТИЛАМИНО)МЕТИЛ]ФЕНИЛ}-1,3,4,5-ТЕТРАГИДРО-6Н-АЗЕПИНО[5,4,3-cd]ИНДОЛ-6-ОНА | 2011 |
|
RU2570198C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА 6-[(4R)-4-МЕТИЛ-1,1-ДИОКСИДО-1,2,6-ТИАДИАЗИНАН-2-ИЛ]ИЗОХИНОЛИН-1-КАРБОНИТРИЛА | 2015 |
|
RU2698194C2 |
| СОЛЬ ПЕНТАЦИКЛИЧЕСКОГО СОЕДИНЕНИЯ И ЕГО КРИСТАЛЛ | 2020 |
|
RU2820938C2 |
| КРИСТАЛЛИЧЕСКИЕ МОДИФИКАЦИИ 3-(1Н-ИНДОЛ-3-ИЛ)-4-[2-(4-МЕТИЛПИПЕРАЗИН-1-ИЛ)ХИНАЗОЛИН-4-ИЛ]ПИРРОЛ-2,5-ДИОНА | 2007 |
|
RU2481341C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 6-(1Н-ИМИДАЗОЛ-1-ИЛ)-2-ФЕНИЛХИНАЗОЛИНА И ЕГО СОЛЕЙ | 2010 |
|
RU2557547C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 6-[2-(МЕТИЛКАРБАМОИЛ)ФЕНИЛСУЛЬФАНИЛ]-3-Е-[2-(ПИРИДИН-2-ИЛ)ЭТЕНИЛ]ИНДАЗОЛА, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ АНОМАЛЬНОГО РОСТА КЛЕТОК У МЛЕКОПИТАЮШИХ | 2008 |
|
RU2518898C2 |
| СОЛИ 1-(4-(2-((1-(3,4-ДИФТОРФЕНИЛ)-1Н-ПИРАЗОЛ-3-ИЛ)МЕТОКСИ)ЭТИЛ)ПИПЕРАЗИН-1-ИЛ)ЭТАНОНА | 2016 |
|
RU2727974C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 3-(2,6-ДИХЛОР-3,5-ДИМЕТОКСИФЕНИЛ)-1-{ 6-[4-(4-ЭТИЛПИПЕРАЗИН-1-ИЛ)-ФЕНИЛАМИНО]-ПИРИМИДИН-4-ИЛ} -1-МЕТИЛМОЧЕВИНЫ И ЕЕ ДОЛЕЙ | 2010 |
|
RU2572848C2 |
| СТАБИЛЬНЫЕ СОСТАВЫ ИМАТИНИБА | 2008 |
|
RU2470641C2 |

Изобретение относится к области органической химии, а именно к кристаллической форме малеата1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины, которая имеет порошковую рентгеновскую дифрактограмму, включающую пики при значениях 2θ: 11,6, 12,1 и 19,6 °2θ ± 0,2 °2θ. Также описывается фармацевтическая композиция на основе кристаллической формы указанного малеата мочевины. Технический результат: получение малеата мочевины, который имеет улучшенную химическую и термическую стабильность при хранении, пониженную гигроскопичность при сохранении химической и энантиомерной стабильности. 2 н. и 10 з.п. ф-лы, 7 пр., 8 табл., 5 ил.
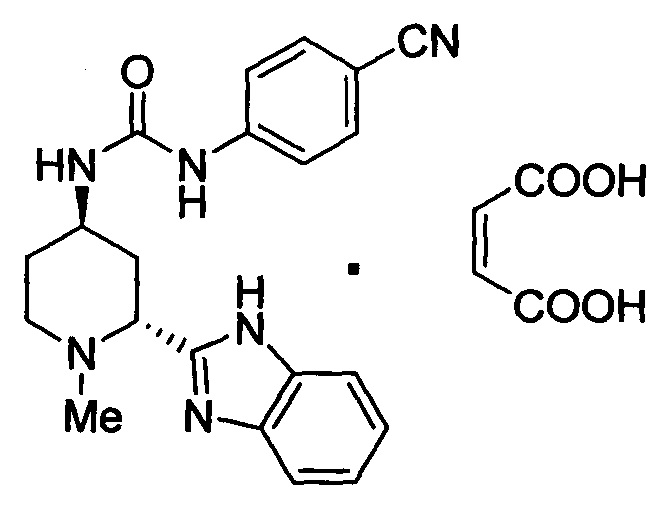
1. Кристаллическая форма малеата 1-((2R,4R)-2-(1Н-бензо[d]имидазол-2-ил)-1-метилпиперидин-4-ил)-3-(4-цианофенил)мочевины, соответствующего структурной формуле:
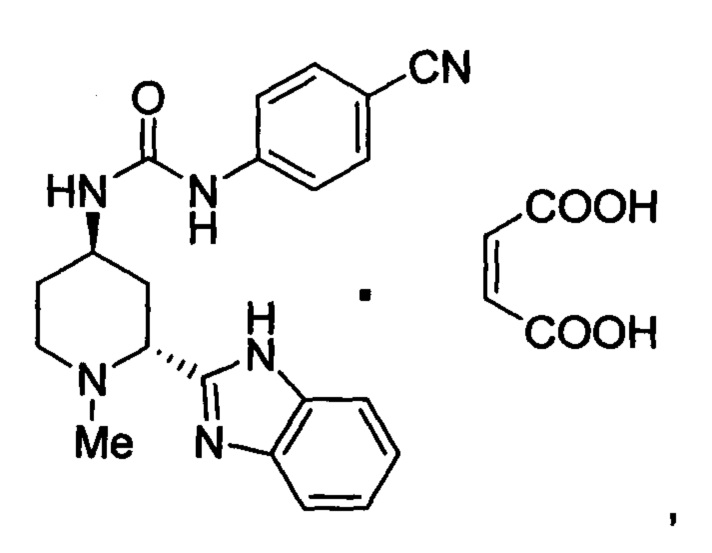
имеющая порошковую рентгеновскую дифрактограмму, включающую пики при значениях 2θ: 11,6, 12,1 и 19,6 °2θ ± 0,2 °2θ.
2. Кристаллическая форма по п. 1, имеющая порошковую рентгеновскую дифрактограмму, включающую пики при значениях 2θ: 11,6, 12,1, 17,0, 17,7 и 19,6 °2θ ± 0,2 °2θ.
3. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 2219 см-1 ± 2 см-1.
4. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 см-1 ± 2 см-1.
5. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1.
6. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1534, 1612 и 2219 см-1 ± 2 см-1.
7. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1175, 1534, 1612 и 2219 см-1 ± 2 см-1.
8. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
9. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8, 134,8 и 148,3 м.д. ± 0,2 м.д.
10. Кристаллическая форма по какому-либо одному из пп. 1 или 2, имеющая спектр 13С твердотельного ЯМР, включающий значения резонанса (м.д.): 57,8, 134,8, 144,7 и 148,3 м.д. ± 0,2 м.д.
11. Кристаллическая форма по п. 1, имеющая: (а) спектр комбинационного рассеяния, включающий значения волнового числа (см-1): 1612 и 2219 см-1 ± 2 см-1; и (b) спектр 13С твердотельного ЯМР, включающий значение резонанса (м.д.): 148,3 м.д. ± 0,2 м.д.
12. Фармацевтическая композиция для лечения ненормального клеточного роста у млекопитающего, содержащая кристаллическую форму по какому-либо одному из пп. 1-11, и фармацевтически приемлемый носитель или эксципиент.
| US 2009005416 A1, 01.01.2009 | |||
| Sherry L.Morissette et al.: "High-throughput crystallization: polymorphs, salts, co-crystals and solvates of pharmaceutical solids", ADVANCED DRUG DELIVERY REVIEWS, 2004, v.56, pp.275-300 (section1; 3.1) (DOI:10.1016/J.ADDR.2003.10.020) | |||
| STEPHEN M.BERGE et al., Pharmaceuticals Salts, JOURNAL of PHARMACEUTICAL |
Авторы
Даты
2020-03-24—Публикация
2016-04-13—Подача