Настоящее изобретение относится к улучшенному способу введения молекул в цитозоль клеток с использованием фотосенсибилизирующего средства и облучения клеток светом с длиной волны, эффективной для активации фотосенсибилизирующего средства.
Большинство молекул не способны легко проникать через клеточные мембраны. Способы введения молекул в цитозоль живых клеток представляют собой полезный инструмент для изучения биологических процессов и манипуляции ими. В число наиболее часто используемых в настоящее время способов входят микроинъекции, слияние, опосредованное гемолизированными эритроцитами, и липосомное слияние, осмотический лизис пиносом, введение соскобом, электропорация и опосредованная фосфатом кальция и вирусом трансфекция. Указанные методики используются для исследования клеток в культуре, хотя во многих случаях они могут оказаться непрактичными, поскольку занимают много времени, неэффективны или могут индуцировать гибель значительной части клеток. В этой связи, подобные методики не оптимальны для использования в биологических или медицинских исследованиях или в терапии, где требуется, чтобы клетки оставались жизнеспособными и/или функциональными.
Хорошо известно, что порфирины и многие другие фотосенсибилизирующие соединения могут индуцировать цитотоксические эффекты в клетках и тканях. Указанные эффекты основаны на том факте, что при воздействии света фотосенсибилизирующее соединение может становиться токсичным или может высвобождать токсичные вещества, такие как синглетный кислород или другие окислительные радикалы, которые повреждают компоненты клеток или биомолекулы, включая мембраны клеток и клеточные структуры, причем такие клеточные или мембранные повреждения могут постепенно приводить к гибели клеток. Указанные эффекты использовались при лечении различных аномалий или расстройств, включая, в особенности, неопластические заболевания. Такой метод получил название фотодинамической терапии (ФДТ(PDT)) и включает введение фотосенсибилизирующих (фотохимиотерапевтических) агентов в пораженный участок тела с последующим воздействием активирующего света, с тем, чтобы активировать фотосенсибилизирующие средства и перевести их в цитотоксическую форму, при этом пораженные клетки гибнут или снижается их пролиферативный потенциал. Известны фотосенсибилизирующие средства, которые локализуются предпочтительно или селективно в желательном целевом участке, например в опухоли или другом поражении.
Известен перечень фотосенсибилизирующих средств, включающий, прежде всего, псоралены, порфирины, хлорины и фталоцианины. Подобные лекарственные средства становятся токсичными под воздействием света.
Фотосенсибилизирующие средства могут проявлять свое действие посредством множества механизмов, непосредственно или опосредованно. Так, например, некоторые фотосенсибилизаторы становятся токсичными непосредственно при активации светом, тогда как другие действуют посредством генерирования токсичных продуктов, например, окисляющих агентов, таких как синглетный кислород, или других получаемых из кислорода свободных радикалов, которые являются чрезвычайно разрушительными в отношении клеточных материалов и биомолекул, таких как липиды, белки и нуклеиновые кислоты.
Порфириновые фотосенсибилизаторы действуют опосредованно за счет генерирования токсичных форм кислорода и рассматриваются как особенно благоприятные кандидаты для проведения ФДТ. Порфирины представляют собой естественные предшественники в синтезе гема. В частности, гем образуется в том случае, когда железо (Fe3+) включается в фотопорфирин IX (PpIX) за счет действия фермента феррохелатазы. PpIX представляет собой чрезвычайно мощный фотосенсибилизатор, тогда как гем не оказывает фотосенсибилизирующего действия. В технике известно множество порфириновых или связанных с порфирином фотосенсибилизаторов, и все они описаны в литературе.
Цитотоксическое действие большинства сенсибилизаторов, используемых для проведения ФДТ, осуществляется в основном через образование синглетного кислорода под действием света на фотосенсибилизаторы. Указанный реакционноспособный промежуточный продукт имеет очень короткое время жизни в клетках (<0,04 мксек). Таким образом, первичный цитотоксический эффект ФДТ осуществляется во время воздействия света, и он очень близок к участкам образования 1О2. 1О2 вступает в реакцию с сопутствующим окислением с белками (гистидин, триптофан, метионин, цистеин, тирозин), ДНК (гуанин), ненасыщенными жирными кислотами и холестерином. Одним из достоинств ФДТ является то, что ткани, не подвергающиеся воздействию света, остаются незатронутыми, то есть достигается селективный эффект ФДТ. Имеется обширный документальный материал, связанный с использованием ФДТ для разрушения нежелательных клеточных популяций, например неопластических клеток. В патентной литературе описано большое число фотодинамических соединений, которые действуют сами по себе или в виде конъюгатов с нацеливающими агентами, например с иммуноглобулинами, имеющими сродство к рецепторным детерминантам неопластических клеток, что делает такой комплекс более специфичным к указанным клеткам. Некоторые фотохимические соединения, такие как производные гематопорфиринов, имеют также свойственную им способность локализоваться в клетках злокачественных опухолей. Такие способы и соединения описаны в патенте Норвегии №173319 и в заявках на патент Норвегии №№900731, 176645, 176947, 180742, 176786, 301981, 300499 и 891491.
В документе WO 93/14142 описана система доставки лекарств, которая включает противораковое средство и фотоактивируемое вещество (то есть фотосенсибилизатор), которые присоединяются к сополимерным носителям. При введении указанный комплекс поступает внутрь клетки посредством пиноцитоза или фагоцитоза и локализуется внутри эндосом и лизосом. В лизосомах связь между антинеопластическим средством и полимером гидролизуется, что создает условие для пассивной диффузии указанного средства через мембрану лизосомы в цитозоль. Использование указанного способа таким образом, ограничено низкомолекулярными соединениями, которые способны диффундировать через мембрану лизосом. После некоторого промежутка времени, необходимого для диффузии, применяют источник света с соответствующей длиной волны и энергией для активации фотоактивируемого соединения. Комбинированный эффект воздействия противоракового агента и фотоактивируемого соединения разрушает соответствующую клетку. ФДТ методы, подобные описанным выше, направлены, таким образом, на разрушение клеточных структур, ведущее к гибели клетки.
С другой стороны, в документах WO96/07432 и WO00/54802 рассматриваются способы, которые используют фотодинамический эффект в качестве механизма введения не проникающих через мембрану молекул внутрь цитозоля клетки таким способом, который не приводит в обязательном порядке к обширной деструкции клеток или к гибели клеток. В рамках такого способа, молекулу, которую необходимо ввести внутрь, и фотосенсибилизирующее соединение вводят в клетки одновременно или последовательно, при этом фотосенсибилизирующее соединение и указанная молекула подвергаются эндоцитозу, либо, в ином варианте, помещаются в эндосомы, лизосомы или другие внутриклеточные компартменты, ограниченные мембраной.
Молекула, которую нужно поместить во внутриклеточные компартменты, и фотосенсибилизирующее соединение вводят в клетку вместе или последовательно, и оба они поглощаются клеткой в одни и те же внутриклеточные компартменты (то есть перемещаются совместно). Молекула, предназначенная для интернализации, затем высвобождается посредством воздействия на клетку светом с подходящей длиной волны с целью активации фотосенсибилизирующего соединения, которое, в свою очередь, ведет к разрушению мембран соответствующих компартментов и последующему высвобождению молекулы, которая располагается в том же компартменте, что и фотосенсибилизирующее средство, в цитозоль. Такой способ получил название "фотохимическая интернализация" или ФХИ (PCI). Таким образом, на конечной стадии воздействия света на клетки в рамках указанного способа происходит высвобождение рассматриваемой молекулы из того же внутриклеточного компартмента, где находится фотосенсибилизирующее средство, и она появляется в цитозоле.
Считалось, что для того, чтобы данный способ был эффективным, необходимо, чтобы и фотосенсибилизирующее средство, и молекула, которая должна быть высвобождена в цитозоль, находились в одних и тех же компартментах при проведении облучения.
Сейчас неожиданно было обнаружено, что молекулы могут быть введены в цитозоль клеток способами, аналогичными ФХИ, но в которых экспозиция клеток на свету необязательно является окончательной стадией, при этом указанные способы не зависят от того, находятся ли молекула и фотосенсибилизирующее средство в одних и тех же внутриклеточных компартментах во время воздействия света. В таких способах фотосенсибилизирующее соединение может вступать в контакт с клетками и активироваться посредством облучения до того, как рассматриваемая молекула, подлежащая интернализации и таким образом попадающая в цитозоль, будет приведена в контакт с указанными клетками. Таким образом, несмотря на то что подвергаемая интернализации молекула и фотосенсибилизирующее средство необязательно локализованы в одних и тех же внутриклеточных компартментах во время воздействия света, молекула, тем не менее, входит в клетку и доставляется в цитозоль. Указанные результаты представляются чрезвычайно неожиданными, а такие способы дают значительные преимущества по сравнению со способами, в которых световое облучение представляет собой окончательную стадию.
Таким образом, в своем наиболее общем виде настоящее изобретение относится к способу введения молекулы внутрь цитозоля клетки, при этом указанный способ включает контакт данной клетки с фотосенсибилизирующим средством, контакт данной клетки с вводимой молекулой и облучение данной клетки светом с длиной волны, эффективной для активации фотосенсибилизирующего средства, причем указанное облучение проводится перед поглощением указанной молекулы во внутриклеточный компартмент, содержащий указанное фотосенсибилизирующее средство, предпочтительно перед поглощением клеткой указанной молекулы в любой внутриклеточный компартмент.
Так, в одном альтернативном варианте, указанное облучение может быть проведено после поглощения молекулы во внутриклеточный компартмент, что позволяет, чтобы подлежащая интернализации указанная молекула и фотосенсибилизирующее средство находились во время облучающего воздействия света не в одних и тех же внутриклеточных компартментах. Однако в предпочтительном варианте реализации настоящего изобретения облучение проводят перед поглощением клеткой молекулы, подлежащей интернализации.
Термин "интернализация" в контексте настоящего изобретения относится к доставке молекул в цитозоль. Так, в данном случае "интернализация" включает стадию высвобождения молекул из внутриклеточных/связанных с мембраной компартментов в цитозоль клеток.
В контексте настоящего описания термин "поглощение клеткой" или "перемещение" относится к одной из стадий интернализации, на которой молекулы, внешние для клеточной мембраны, захватываются внутрь клетки, так что они оказываются внутри внешней клеточной мембраны, например, посредством эндоцитоза или других соответствующих механизмов поглощения, например, внутрь или ассоциированно с ограниченными мембраной внутриклеточными компартментами, такими, например, как эндоплазматический ретикулум, тельца Гольджи, лизосомы, эндосомы и т.п.
В частности, в предпочтительном аспекте настоящего изобретения рассматривается способ введения молекулы в цитозоль клетки, причем указанный способ включает контакт данной клетки с фотосенсибилизирующим средством, облучение указанной клетки светом с длиной волны, эффективной для активации фотосенсибилизирующего средства, и, по существу, в то же самое время или несколько позже облучения, контакт данной клетки с молекулой, подлежащей введению.
Предпочтительно, клетки приводят в контакт с молекулами, подлежащими введению или интернализации (обозначаемые здесь и далее как "переносимые молекулы"), в момент времени после того, как было проведено облучение или, иными словами, фотохимическая обработка клеток посредством контакта их с фотосенсибилизирующим средством и последующим облучением, производится перед тем, как указанные молекулы добавляют к клеткам. В данном варианте молекулы, подлежащие введению в цитозоль, могут быть приведены в контакт с клетками, которые были подвергнуты фотохимической обработке, в любой момент времени после такой обработки, при условии, что переносимые молекулы еще могут быть захвачены клетками. Временной интервал, в течение которого указанные молекулы могут быть приведены в контакт с клетками и все еще могут быть поглощены ими, зависит от множества факторов, таких, например, как тип клеток, конкретная природа данной молекулы, конкретная природа используемого фотосенсибилизирующего средства и длительность световой обработки. Указанный временной интервал может быть, при необходимости, определен для определенного набора состояний. Однако предпочтительно, чтобы молекулы, подлежащие переносу в цитозоль, добавлялись к клеткам относительно скоро после фотохимической обработки, например, в течение 24 часов после такой фотохимической обработки, и более предпочтительно в течение первых 10 часов после фотохимической обработки, например, в течение первых 5 часов или, более предпочтительно, в течение первого часа. Так, например, in vitro или ex vivo переносимая молекула может быть введена в течение определенного периода времени, например в течение времени от 30 минут до 24 часов, предпочтительно в течение времени от 1 до 2 часов, при этом введение начинается сразу же или вскоре после облучения, например, если конец облучения рассматривать как исходную точку, то переносимая молекула должна быть внесена в момент времени от 0 минут до 24 часов, например, в момент времени от 0 до 4 часов. Было показано, что даже в том случае, если переносимая молекула контактирует с клеткой через достаточно длительное время после облучения, интернализация в клетку все еще возможна. Так, например, переносимая молекула может быть внесена более чем через час после облучения, например, более чем 2, 4, 8, 10 или даже 12 часов после облучения.
Таким образом, в предпочтительном варианте реализации указанная клетка вступает в контакт с указанной переносимой молекулой в период времени от 0 до 4 часов после облучения, длящегося от 1 до 2 или 3 часов или дольше, например, в период времени по меньшей мере от 0,5 до 3 часов. Время, в которое вводится переносимая молекула, варьируется в зависимости от используемых для введения in vitro или in vivo способов. Для способов введения in vitro переносимые молекулы могут быть, в основном, приведены в контакт со всеми целевыми клетками одновременно, например, если клетки растут в культуре in vitro, и, таким образом, относительно легко привести искомые молекулы в контакт с клетками в соответствующей временной точке. In vivo, однако, стадия контакта целевых клеток с переносимыми молекулами очевидно более усложнена и будет зависеть от способа введения и от локализации целевых клеток. Так, например, в том случае, когда переносимая молекула может быть введена непосредственно в целевые клетки, например, посредством местной инъекции, переносимая молекула вступит в контакт с целевыми клетками (или по меньшей мере с частью их) относительно быстро, например, в течение порядка минут или часов после введения. С другой стороны, если переносимые молекулы вводят посредством внутривенной инъекции в отдаленную мишень, то указанным молекулам может потребоваться гораздо больше времени для того, чтобы вступить в контакт с целевыми клетками. Так, например, им может потребоваться от 24 до 96 часов после введения для достижения целевых клеток. Такое "время путешествия" должно быть принято во внимание при решении вопроса о соответствующем времени введения переносимых молекул относительно времени введения фотосенсибилизирующего средства и времени облучения.
В альтернативном варианте осуществления настоящего изобретения переносимая молекула может быть приведена в контакт с клетками по существу в то же самое время, что и время облучения, а не после облучения. Выражение "по существу в то же самое время" в настоящем описании означает точно в то же самое время, то есть одновременно, но также включает добавление молекул к клеткам незадолго перед облучением, например, за один или два часа перед облучением, при условии, что клеточное поглощение переносимой молекулы не происходило во время облучения, хотя и может все еще иметь место после облучения, или при условии, что если клеточное поглощение переносимой молекулы происходило, то при этом переносимая молекула и фотосенсибилизирующий агент не локализованы в одних и тех же внутриклеточных компартментах во время экспозиции на свету.
Как отмечалось выше, для определения точного времени добавления переносимой молекулы и фотосенсибилизирующего средства, а также времени облучения, необходимого для достижения указанных выше эффектов, следует учесть различные факторы, включая клетки, подлежащие обработке, используемые средства и молекулы и окружение клеток, особенно в отношении того, в какой системе - in vivo или in vitro - происходит процесс. С учетом указанных соображений, соответствующие временные параметры легко могут быть определены.
В качестве основного принципа для определения соответствующих условий можно указать, что стадия облучения должна проходить либо перед поглощением клеткой переносимой молекулы (при условии, что само фотосенсибилизирующее средство уже было перенесено во внутриклеточные компартменты), либо после поглощения клеткой переносимой молекулы при условии, что переносимая молекула и фотосенсибилизирующее средство не локализованы в одних и тех же внутриклеточных компартментах в момент воздействия света. В отношении последнего варианта очевидно, что переносимая молекула вступает в контакт с клетками в момент времени, предшествующий началу воздействия облучения. Такие условия составляют один из предпочтительных вариантов осуществления настоящего изобретения.
Описанные ранее способы фотохимической интернализации, при которых переносимая молекула и фотосенсибилизирующее средство добавлялись к клеткам перед облучением, зависели от природы рассматриваемых молекул в плане возможности локализации в одних и тех же внутриклеточных компартментах перед воздействием света, так что лизис указанных внутриклеточных компартментов в результате активации светом фотосенсибилизирующего средства приводил к высвобождению в цитозоль и рассматриваемой молекулы, и указанного фотосенсибилизирующего средства.
Указанный процесс схематически изображен на фиг.7. Что касается настоящего изобретения, то очевидно, что фотосенсибилизирующее средство и переносимая молекула, предназначенная для введения в цитозоль, не находятся в одних и тех же внутриклеточных компартментах в момент воздействия света, поскольку переносимую молекулу добавляют к клеткам только незадолго до или уже после экспозиции на свету.
Механизм действия указанных способов до сих пор не известен, и в действительности уже сам факт, что данный способ работает, является удивительным. Не ограничивая себя рамками какой-либо теории, можно указать, что причиной таких удивительных открытий может быть слияние фотохимически поврежденных везикул со вновь сформированными внутриклеточными везикулами, что затем приводит к высвобождению заново захваченных посредством эндоцитоза молекул в цитозоль. Указанный процесс изображен схематически на диаграмме, представленной на фиг.7.
Альтернативно, фотохимическое повреждение лизосомных ферментов или везикул, содержащих лизосомные ферменты, таких как указанные эндосомы, может снижать скорость внутриклеточной деградации молекул, подлежащих интернализации. Такой процесс может быть связан либо со сниженным транспортом к везикулам, содержащим лизосомные ферменты, либо с транспортом к внутриклеточным везикулам, характеризующимся меньшей гидролитической активностью. В этом случае, указанные молекулы будут иметь больше времени для того, чтобы избегнуть эндоцитозного включения в компартменты, чем в том случае, когда активен процесс лизосомной деградации. Еще одним альтернативным объяснением может быть тот факт, что фотохимическая обработка клеток приводит к небольшому повреждению плазматических мембран клеток, что ведет к повышению проникновения макромолекул через клеточную мембрану. Однако проведенные эксперименты (см. пример 7) свидетельствуют о том, что это, скорее всего, не может служить искомой причиной.
Настоящее изобретение относится, таким образом, к способам транспортировки или трансфекции любых молекул в цитозоль живых клеток как in vitro (то есть в культуре клеток), так и in vivo, после чего указанные молекулы становятся доступными в цитозоле.
Такие способы могут использоваться не только для переноса молекул (или их частей или фрагментов) во внутреннюю область клетки, но также, в некоторых случаях, могут доставлять или экспрессировать их на поверхность клетки. Таким образом, после перемещения и высвобождения молекулы в клеточный цитозоль согласно способу настоящего изобретения, в том случае, если указанные(ая) клетки(а) представляют(ет) собой специализированные клетки, такие как, например, антиген-презентирующая клетка, молекула или ее фрагмент могут переноситься на поверхность клетки, где они могут быть представлены на внешней стороне клетки, то есть на клеточной поверхности. Такие способы могут иметь особую практическую ценность в области вакцинации, когда компоненты вакцин, то есть антигены или иммуногены, могут быть введены в клетку для представления на поверхности такой клетки, с тем чтобы индуцировать, облегчить или повысить иммунный ответ. Дополнительные детали, связанные с использованием способа, делающего возможным экспрессирование молекул на клеточную поверхность, описаны в документе WO00/54802.
Переносимые молекулы, которые могут быть введены в цитозоль клеток с использованием способов настоящего изобретения, включают молекулы, которые не способны легко проникать через клеточные мембраны. Кроме того, настоящее изобретение может способствовать увеличению доставки в цитозоль и активности молекул, которые способны лишь частично проникать через мембрану клетки или мембраны внутриклеточных везикул. Переносимые молекулы могут представлять собой органические соединения, белки или фрагменты белков, такие, например, как пептиды, антитела, или антигены, или их фрагменты. Другой класс переносимых молекул, пригодных для использования согласно настоящему изобретению, включает цитотоксические средства, такие как белковые токсины или цитотоксические органические соединения, например блеомицин. Еще один класс подходящих переносимых молекул включает нуклеиновые кислоты.
Нуклеиновые кислоты могут использоваться в виде генов, кодирующих, например, терапевтические белки, антисмысловые молекулы РНК, рибозимы, аптамеры или триплексы РНК, образующие олигонуклеотиды. Альтернативно, нуклеиновые кислоты могут использоваться в виде некодирующих молекул, таких как, например, синтетическая ДНК или антисмысловые молекулы РНК, рибозимы, аптамеры, триплексы, образующие олигонуклеотиды, пептидные нуклеиновые кислоты (ПНК), фактор транскрипции "ложной" ДНК или химерные олигонуклеотиды, используемые для репарации специфических мутаций у пациента. Там, где это приемлемо, молекулы нуклеиновой кислоты могут иметь вид полных генов или фрагментов нуклеиновой кислоты, необязательно включенных в векторную молекулу или структуру, например, в плазмидный вектор или в вирусную частицу или бактериофаг. Последняя форма имеет особую применимость в том случае, когда переносимая молекула предназначена для использования в генной терапии.
Фотосенсибилизирующее средство, которое может использоваться согласно настоящему изобретению, представляет собой любой такой агент, который локализуется во внутриклеточных компартментах, в особенности в эндосомах или лизосомах. Набор таких фотосенсибилизирующих средств известен в технике и описан в литературе, включая документ WO96/07432. В этом аспекте могут быть отмечены ди- и тетрасульфонированный фталоцианин алюминия (например, AlPcS2a), сульфонированные тетрафенилфосфины (TPPSn) (ТФФС), нильский голубой, производные хлорина е6, уропорфирин I, филлоэритрин, гематопорфирин и метиленовый синий, которые, как было показано, локализуются в эндосомах и лизосомах клеток в культурах клеток. Это в большинстве случаев обусловлено эндоцитозным характером поглощения фотосенсибилизаторов. Таким образом, фотосенсибилизирующее средство предпочтительно представляет собой вещество, которое поглощается во внутренние компартменты лизосом или эндосом. Однако могут быть использованы также и другие фотосенсибилизирующие средства, которые локализуются в других внутриклеточных компартментах, например в эндоплазматическом ретикулуме или аппарате Гольджи. Понятно также, что такие механизмы могут работать и в тех случаях, когда результаты фотохимической обработки воздействуют на другие клеточные компоненты (то есть на компоненты, отличные от компартментов, изолированных мембранами). Так, например, одна из возможностей может заключаться в том, что фотохимическая обработка разрушает молекулы, важные для внутриклеточного транспорта или слияния везикул. Такие молекулы могут необязательно быть локализованы в компартментах, ограниченных мембраной, но фотохимическое повреждение таких молекул может, тем не менее, вести к фотохимической интернализации переносимых молекул, например, посредством механизма, при котором фотохимические воздействия на такие молекулы ведут к уменьшению транспорта молекулы, подлежащей интернализации (то есть переносимой молекулы), к деградируемым везикулам, таким как лизосомы, так что данная молекула, подлежащая интернализации, может выйти в цитозоль до ее деградации. Примеры таких молекул, которые необязательно локализованы в компартментах с ограничивающей мембраной, включают несколько молекул микротрубчатой транспортной системы, таких как динеин и компоненты динактина, и, например, rab5, rab7, фактор чувствительности к N-этилмалеимиду (NSF), растворимый белок связывания фактора NSF (SNAP) и им подобные.
Классы подходящих фотосенсибилизирующих средств, которые могут быть отмечены применительно к данному случаю, включают порфирины, фталоцианины, пурпурины, хлорины, бензопорфирины, нафталоцианины, катионные красители, тетрациклины и лизомотропные слабые основания или их производные (Berg et al., J. Photochemistry and Photobiology, 1997, 65, 403-409). Другие подходящие фотосенсибилизирующие средства включают тексафирины, феофорбиды, порфицены, бактериохлорины, кетохлорины, производные гематопорфирина и их производные, эндогенные фотосенсибилизаторы, индуцируемые 5-аминолевулиновой кислотой и их производные, димеры или другие конъюгаты фотосенсибилизаторов.
Предпочтительно, фотосенсибилизатор находится в свободной форме, то есть он не конъюгирован с какой-либо другой макромолекулой. Однако альтернативно фотосенсибилизатор может быть ассоциирован, присоединен или конъюгирован с носителем или другой молекулой, приведенной в настоящем описании, например, присоединен к нацеливающему антителу или связан с носителем, таким как полилизин.
Предпочтительные фотосенсибилизирующие средства включают TPPS4, TPPS2a, AlPcS2a и другие амфифильные фотосенсибилизаторы. В предпочтительном аспекте настоящее изобретение предлагает способы, в которых пригодные для использования фотосенсибилизирующие средства относятся к соединениям, представленным 5-аминолевулиновой кислотой или сложными эфирами 5-аминолевулиновой кислоты или их фармацевтически приемлемыми солями.
В таких сложных эфирах 5-аминогруппа может быть замещенной или незамещенной, в последнем случае они представляют собой сложные эфиры АЛК (ALA).
Более конкретно, сложные эфиры АЛК, используемые согласно настоящему изобретению, представляют собой сложные эфиры 5-аминолевулиновых кислот с необязательно замещенными алканолами, то есть алкильные сложные эфиры или замещенные алкильные сложные эфиры.
Соответственно, сложные эфиры АЛК, которые могут использоваться согласно настоящему изобретению, представляют собой соединения формулы I,
R2 2N-CH2COCH2-CH2CO-OR1 (I)
(где R1 может представлять собой алкил, необязательно замещенный гидрокси-, алкокси-, ацилокси-, алкоксикарбонилокси-, амино-, арил-, оксо- или фтор-группами с необязательным включением атомов кислорода, азота, серы или фосфора; и R2, каждый из которых может быть одинаковым или различным, представляет собой атом водорода или группу R1) или их соли.
Замещенные алкильные группы R1 могут быть моно- или полизамещенными. Так, замещенные R1 группы включают, например, незамещенный алкил, алкоксиалкил, гидроксиалкоксиалкил, полигидроксиалкил, гидроксиполиалкиленоксиалкил и т.п. Термин "ацил" в контексте настоящего описания включает и карбоксилатные, и карбонатные группы; так, ацилокси-замещенные алкильные группы включают, например, алкилкарбонилоксиалкил. В таких группах любой алкиленовый фрагмент предпочтительно содержит атомы углерода в количестве, определенном для алкильных групп ниже. Предпочтительные арильные группы включают фенил и моноциклические 5-7-членные гетероароматические соединения, особенно фенил, причем сами такие группы могут быть необязательно замещены.
Репрезентативные замещенные группы R1 включают алкоксиметильную, алкоксиэтильную и алкоксипропильную группы или ацилоксиметильную, ацилоксиэтильную и ацилоксипропильную группы, например, пивалоилоксиметил.
Сложные эфиры АЛК, предпочтительные для использования в качестве фотосенсибилизирующих средств согласно настоящему изобретению, включают те из них, в которых R1 обозначает незамещенную алкильную группу и/или каждый R2 обозначает атом водорода.
В контексте настоящего описания термин "алкил" включает любую длинноцепочечную или короткоцепочечную, линейную или разветвленную алифатическую насыщенную или ненасыщенную углеводородную группу. Ненасыщенные алкильные группы могут быть моно- или полиненасыщенными и включают и алкенильные, и алкинильные группы. Такие группы могут содержать вплоть до 40 атомов углерода. Однако предпочтительными являются алкильные группы, содержащие вплоть до 10, например 8, более предпочтительно вплоть до 6, и особенно предпочтительно вплоть до 4 атомов углерода.
Следует особо отметить сложный АЛК-метиловый эфир, сложный АЛК-этиловый эфир, сложный АЛК-пропиловый эфир, сложный АЛК-гексиловый эфир, сложный АЛК-гептиловый эфир и сложный АЛК-октиловый эфир и их соли, которые представляют собой предпочтительные фотосенсибилизирующие средства для использования согласно настоящему изобретению.
Необходимо, чтобы фотосенсибилизирующее средство контактировало с клеткой до облучения. Однако, в отличие от переносимой молекулы, указанное средство должно вводиться до облучения, так чтобы к моменту облучения указанное средство уже было включено во внутриклеточный компартмент. В этой связи, данный агент вводится за 1-72 часа до облучения, например за 4-48 часов, например, за 4-24 часа до облучения. И снова, как обсуждалось выше в отношении стадии приведения переносимой молекулы в контакт с клетками, время введения фотосенсибилизирующего средства для достижения контакта с целевой клеткой относительно времени облучения зависит от того времени, которое потребуется фотосенсибилизирующему средству для достижения целевых клеток и поглощения ими. Указанное время может варьировать в зависимости от используемых способов, т.е. от того, проводится оно in vivo или in vitro, и от того, проводится ли введение непосредственно в целевую ткань или в отдаленный участок. Во всех случаях важно, чтобы фотосенсибилизирующее средство поглощалось целевыми клетками перед процессом облучения. Указанное средство может быть приведено в контакт с целевыми клетками непосредственно до облучения, например, за 1 или 4-72 часа, предпочтительно за 4-24 часа, например, за 12-20 часов, или оно может быть удалено для прекращения контакта непосредственно перед облучением, например, более чем за 5 минут, например за 10 минут - 8 часов, например, за 1-4 часа с использованием свободной от агента среды.
Необязательно, один или другой или оба компонента - фотосенсибилизирующее средство и переносимая молекула, подлежащая введению в клетки, могут быть присоединены, или ассоциированы, или конъюгированы с одной или более молекулами носителя, нацеливающими молекулами или векторами, которые могут действовать в направлении облегчения или увеличения поглощения фотосенсибилизирующего средства или переносимой молекулы, или могут способствовать достижению мишени или доставке указанных структур в конкретный тип клеток, ткани или внутриклеточного компартмента. Примеры систем носителей включают полилизин или другие поликатионы, сульфат декстрана, различные катионные липиды, липосомы, восстановленные ЛНП-частицы, пространственно стабилизированные липосомы или аденовирусные частицы. Такие системы переносчиков в основном улучшают фармакокинетические свойства и увеличивают поглощение клетками переносимой молекулы и/или фотосенсибилизирующего средства и могут также направлять переносимую молекулу и/или фотосенсибилизирующее средство во внутриклеточные компартменты, для которых достижение фотохимической интернализации было бы особенно благоприятным, хотя сами данные системы в основном не обладают способностью направлять переносимую молекулу и/или фотосенсибилизирующее средство в специфические клетки (например, раковые клетки) или ткани. Однако для достижения такого специфического или селективного нацеливания молекулы указанного носителя, переносимая молекула и/или фотосенсибилизатор могут быть ассоциированы или конъюгированы со специфическими нацеливающими молекулами, которые облегчают специфическое поглощение клетками переносимой молекулы в желательные типы клеток или тканей. Такие нацеливающие молекулы могут также направлять переносимую молекулу во внутриклеточные компартменты, для которых особенно благоприятно достижение фотохимической интернализации.
Могут быть использованы различные нацеливающие молекулы, такие, например, как описанные в литературе (Curiel, D.T. (1999), Ann. New York Acad. Sci., 886, 158-171; Bilbao, G., et al. (1998), in Gene Therapy of Cancer (Walden et al., eds., Plenum Press, New York); Peng K.W. and Russell S.J. (1999), Curr. Opin. Biotechnol. 10, 454-457; Wickham T.J. (2000), Gene Ther. 7, 110-114).
Молекула носителя и/или нацеливающая молекула могут быть ассоциированы, связаны или конъюгированы с переносимой молекулой, фотосенсибилизирующим средством или с ними обоими и при этом может использоваться один и тот же или разные носители или нацеливающие молекулы. Если в качестве носителя используют, например, аденовирусные частицы, то переносимая молекула может быть включена в состав аденовирусных частиц. Так, например, если рассматриваемая переносимая молекула представляет собой молекулу ДНК, кодирующую белок, или молекулу РНК, то такая ДНК включается в вирусный вектор и после фотохимической интернализации указанная молекула ДНК будет присутствовать в правильном внутриклеточном сайте, так что будет происходить экспрессия кодируемой молекулы.
Экспрессия таких молекул может контролироваться с помощью вектора, разработанного с помощью хорошо известных в технике и задокументированных способов. Так например, могут использоваться регуляторные элементы, такие как, например, тканеспецифичные или регуляторные промоторы, для достижения регулируемой экспрессии специфичной для определенной ткани или заболевания. Например, может использоваться тканеспецифичный промотор тирозиназы, специфичной к меланоме. Хорошо известны регулируемые промоторы, такие как промоторы, регулируемые тетрациклином. В литературе имеется достаточное число примеров специфических или регулируемых промоторов, которые могут быть использованы согласно настоящему изобретению (Hart, I.R., 1996, Semin. Oncol. 23, 154-158; Hallahan, D.E. et al., 1995, Nature Med. 1, 786-791; Luna, M.C. et al., 2000, Cancer Res. 60, 1637-1644; Miller N. and Whelan, J., 1997, Hum. Gene Ther.; Wickham, T.J., 2000 Gene Ther. 7, 110-114; Nettelbeck D.M. and Muller, J.V., 2000 Trends Genet. 16, 174-181; Clackson, Т., 2000, Gene Ther. 1 120-125; Freundlieb, S. et al., 1999, J. Gene Med. 1, 4-12; Spear M.A., 1998, Anticancer Res. 18, 3223-31; Harvey, D.M. and Caskey C.T., 1998, Curr. Opin. Chem. Biol. 2, 512-518; Clary B.M. and Lyerly, H.K., 1998, Surg. Oncol. Clln. North Am. 1 565-574; Luna, M.C. et al., Cancer Res. 60, 1637-1644 и содержащиеся в них ссылки).
Как отмечалось выше, одновременно может использоваться более чем один носитель и/или нацеливающая молекула или вектор. Так, например, векторы могут заключаться в носитель, например вирусные векторы, такие как аденовирус, могут доставляться например, в составе липосомы или поликатионной структуры.
Носители и векторы, предпочтительные для использования согласно настоящему изобретению, особенно для использования в сочетании с переносимой молекулой, включают аденовирусы поликатионы, такие как полилизин (например, поли-L-лизин или поли-D-лизин), полиэтиленимин или дендримеры (например, катионные дендримеры, такие как SuperFect®); катионные липиды, такие как ДОТАП или Lipofectin; пептиды и целевые векторы, такие как, например, трансферрин-полилизин или целевые аденовирусные векторы. В особенно предпочтительном варианте настоящего изобретения носителем является аденовирус.
Такие нацеливающие молекулы или носители, как описанные выше, могут также использоваться для направления переносимой молекулы в определенный внутриклеточный компартмент, особенно подходящий в случае использования ФХИ, например, в лизосомы или эндосомы.
Внутриклеточным компартментом, ограниченным мембраной, может быть любая такая полость, которая присутствует в клетке. Предпочтительно такой компартмент представляет собой везикулу, в особенности эндосому или лизосому. Однако внутриклеточный компартмент может также включать аппарат Гольджи или эндоплазматический ретикулум.
Стадия светового облучения, проводимая для активации фотосенсибилизирующего средства, может проводиться с использованием методик и процедур, известных в технике. Так например, длина волны и интенсивность освещения могут быть выбраны в соответствии с природой используемого фотосенсибилизирующего средства. Подходящие источники света известны в технике. Время, в течение которого клетки подвергаются воздействию света, в применяемых методах согласно настоящему изобретению может варьировать. Эффективность интернализации переносимой молекулы в цитозоль клетки, по всей видимости, повышается с увеличением времени воздействия света. Предпочтительная продолжительность стадии облучения зависит от природы фотосенсибилизатора, количества фотосенсибилизатора, накопленного в целевых клетках или тканях, и наличием общих участков между спектром поглощения фотосенсибилизатора и спектром эмиссии светового источника. В целом, продолжительность стадии облучения составляет порядка от минут до нескольких часов, например, предпочтительно вплоть до 60 минут, например, от 0,5 или 1 до 30 минут, например, от 0,5 до 3 минут, или от 1 до 5 минут, или от 1 до 10 минут, например, от 3 до 7 минут, и предпочтительно примерно 3 минуты, например, от 2,5 до 3,5 минут. Специалистом в данной области может быть выбрана соответствующая доза облучения, и она вновь будет зависеть от природы фотосенсибилизатора и от количества фотосенсибилизатора, накопленного в целевых клетках или тканях. Например, доза облучения, обычно используемая для фотодинамической обработки раковых клеток с фотосенсибилизатором Photofrin и протопорфириновым предшественником 5-аминолевулиновой кислотой, находится в диапазоне 50-150 Дж/см2 в диапазоне воздействия менее чем 200 мВт/см2 для того, чтобы избежать перегрева. Дозы облучения обычно бывают ниже в случае использования фотосенсибилизаторов с высокими коэффициентами экстинкции в красной области видимого спектра. Однако для обработки нераковых тканей, в случае аккумуляции меньшего количества фотосенсибилизатора, общее необходимое количество облучения может быть существенно выше, чем при обработке раковых тканей.
Определение подходящих доз целевых молекул для использования в способах настоящего изобретения представляет собой рутинную процедуру для специалиста в данной области. В том случае, когда переносимая молекула представляет собой белок или пептид, для применения in vitro переносимые молекулы используются в основном в дозах менее чем 5 мг/мл (например, 0,1-5 мг/мл), а для применения in vivo переносимые молекулы используются обычно в дозах менее чем 5 мг/кг (например, 0,1-5 мг/кг). В том случае, когда переносимая молекула представляет собой нуклеиновую кислоту, для применения in vitro примерная доза переносимых молекул будет составлять примерно 0,1-50 мкг нуклеиновой кислоты на 104 клеток, а для применения in vivo при лечении людей - примерно 10-6-1 г нуклеиновой кислоты в расчете на инъекцию. В случае, когда переносимая молекула ассоциирована с аденовирусным носителем, для применения in vitro примерная доза будет варьировать между 1-1х105 физических вирусных частиц, например, 1х103-1х105 частиц на клетку, а для применения in vivo молекула, вводимая в ассоциации с аденовирусным носителем, может присутствовать в концентрации 1х10-9-50 вес.%, такой как 3х10-6-50 вес.%, например, 0,003-30 вес.%, например, 0,2-10 вес.%, вирусных частиц в композиции, готовой для применения in vivo, где весовые проценты относятся к весу вирусного носителя в сочетании с молекулой, подлежащей введению, относительно общего веса готовой композиции. Если используются инъекции по 1 мл, то это будет соответствовать дозе примерно 105-1015 физических вирусных частиц.
Способы настоящего изобретения неизбежно будут приводить к гибели некоторых клеток в результате фотохимической обработки, то есть через воздействие фотосенсибилизирующего средства. Однако такая гибель клеток не вызывает проблем и, в действительности, может быть благоприятной для многих приложений (например, при лечении рака), и способы настоящего изобретения могут быть модифицированы таким образом, чтобы фракция или доля выживающих клеток могла регулироваться путем выбора дозы облучения в соответствии с концентрацией фотосенсибилизирующего средства. И такие методики также известны в технике. Независимо от уровня гибели клеток, индуцированного собственно фотохимической обработкой, важно, чтобы доза освещения регулировалась так, чтобы некоторые из индивидуальных клеток, в которых проявляется ФХИ эффект, не были уничтожены собственно фотохимической обработкой (хотя они могут быть впоследствии уничтожены посредством ФХИ эффекта).
В некоторых приложениях разумно сохранять большое число жизнеспособных клеток после ФХИ обработки. Так, например, при вакцинации и в некоторых способах генной терапии важно наличие жизнеспособных клеток, которые обеспечивают представление антигена или экспрессию белка. В таких приложениях приемлемо, чтобы популяция или множество клеток, по существу все клетки или значительное их количество (например, по меньшей мере 50%, более предпочтительно по меньшей мере 60, 70, 80 или 90% клеток) не погибали. Разумеется, такая ситуация не всегда желательна, особенно когда ФХИ используется для введения цитотоксических переносимых молекул и последующая гибель клеток не является недостатком. Цитотоксические эффекты могут быть также достигнуты при использовании, например, генной терапии, при которой терапевтический ген интернализуется в опухолевые клетки по способу настоящего изобретения, так чтобы указанные клетки могли продуцировать иммунологически активные вещества, которые будут индуцировать иммунологическую локальную гибель остающихся раковых клеток или индуцировать системный иммунный ответ на опухолевые клетки. В таких случаях, сразу после ФХИ обработки требуется наличие части жизнеспособных клеток.
Достоинства настоящих способов и последовательности стадий обработки, в особенности вариантов, в которых переносимую молекулу добавляют к клеткам после стадии облучения светом, по сравнению с описанными ранее способами, включают:
а) фотохимическое повреждение переносимой молекулы снижается;
b) упрощается ФХИ обработка внутренних повреждений в сочетании с хирургическим вмешательством, поскольку фотохимическая обработка может производиться после хирургического вскрытия повреждения с последующей, например, внутриопухолевой инъекцией или другим способом местного введения переносимой молекулы;
с) способы более независимы от точного времени обработки, то есть время добавления молекулы, которая должна быть введена в клетки, относительно времени облучения. Последнее означает, что имеется больший временной диапазон для обработки. Это важно, поскольку поглощение терапевтической молекулы может широко варьировать в различных клинических ситуациях и, более того, поглощение трудно оценить для индивидуальных поражений в конкретной клинической ситуации, что делает более широкий временной диапазон чрезвычайно выгодным;
d) происходит быстрое перемещение переносимой молекулы в цитозоль, за счет чего по существу снижается вероятность лизосомной деградации переносимой молекулы.
Указанные преимущества сочетаются с преимуществами, связанными с ФХИ методами интернализации молекул per se, то есть 1) нет ограничений по размеру молекулы, подлежащей интернализации и доставке в цитозоль, поскольку молекула может быть подвергнута эндоцитозу целевой клеткой; 2) способы не зависят от клеточной пролиферации; 3) способы являются сайт-специфичными за счет того, что только участки, открытые для действия облучения, подвергаются воздействию; 4) данный способ не является онкогенным.
Стадии "контакта" клеток с фотосенсибилизирующим средством и с переносимой молекулой могут быть проведены любым удобным или желательным способом. Так, например, если стадия контакта проводится in vitro, клетки могут удобным образом поддерживаться в водной среде, такой как, например, подходящая среда для клеточной культуры, и в соответствующей временной точке фотосенсибилизирующее средство или переносимая молекула могут быть легко добавлены к среде в определенных условиях, например, в соответствующей концентрации и в течение определенного периода времени.
Фотосенсибилизирующее средство приводят в контакт с клетками в определенной концентрации и в течение соответствующего периода времени, которые могут быть легко определены специалистом с использованием рутинных методик и которые будут зависеть от конкретного используемого фотосенсибилизирующего средства и от типа клеток. Концентрация фотосенсибилизирующего средства должна быть такой, чтобы при поглощении его в клетку, например, внутрь клетки или при ассоциировании с одной или более ее внутриклеточными компартментами, и при активации облучением одна или более клеточных структур подвергались разрушению, например, одна или более внутриклеточных полостей лизировались или разрушались. Так, например, фотосенсибилизирующие средства, используемые в описанных примерах, могут применяться в концентрации, например, 10-50 мкг/мл. В режиме использования in vitro диапазон может быть значительно шире и составлять, например, 0,05-500 мкг/мл. В режиме использования in vivo с целью лечения людей фотосенсибилизирующее средство может использоваться в диапазоне концентраций 0,05-20 мг/кг веса тела - в случае системного введения или 0,1-20% в растворителе - для местного нанесения. В случае более мелких животных, диапазон концентраций может оказаться другим и его можно соответствующим образом скорректировать.
Время инкубации клеток с фотосенсибилизирующим средством (то есть "контактное" время) может варьировать от нескольких минут до нескольких часов и составлять, например, даже до 48 часов или более. Время инкубации должно быть таким, чтобы фотосенсибилизирующее средство поглощалось бы соответствующими клетками.
После инкубации клеток с фотосенсибилизирующим средством может необязательно следовать период инкубации в среде, свободной от фотосенсибилизатора, перед тем как клетки будут облучены светом или будет добавлена переносимая молекула.
Переносимая молекула может представлять собой любую молекулу из числа обсуждавшихся выше, которую приводят в контакт с клетками в соответствующей концентрации и в течение определенного периода времени. Неожиданно было обнаружено, что контакт может быть инициирован даже через несколько часов после облучения. Соответствующая концентрация может быть определена в зависимости от эффективности поглощения рассматриваемой молекулы клетками и от конечной концентрации, которую желательно иметь внутри клеток. Таким образом, "время трансфекции" или "время поглощения клетками", то есть время нахождения молекул в контакте с клетками, может составлять от нескольких минут до нескольких часов, например, может использоваться время трансфекции от 10 минут до 24 часов, например, от 30 минут до 10 часов или, например, от 30 минут до 2 часов или 6 часов. Увеличенное время трансфекции обычно приводит к увеличению поглощения рассматриваемой в данной ситуации молекулы. Однако более короткие периоды инкубации, например в течение от 30 минут до 1 часа, по всей видимости, могут привести к повышению специфичности поглощения молекулы. Следовательно, при выборе продолжительности трансфекции в любом из применяемых способов должен быть соблюден определенный соответствующий баланс между достижением достаточной степени поглощения молекулы и сохранением удовлетворительной специфичности поглощения.
Для применения in vivo соответствующий способ и длительность инкубации, при которой переносимая молекула и фотосенсибилизирующее средство приводятся в контакт с целевыми клетками, будет зависеть от режима введения, от типа переносимой молекулы и от природы фотосенсибилизирующих средств. Так, например, если переносимая молекула инъецируется в опухоль, которая подлежит лечению, клетки около точки инъекции придут в контакт с ней и, в этой связи, будут иметь возможность поглотить переносимую молекулу быстрее чем клетки, расположенные на большем расстоянии от точки инъекции, которые, вероятно, могут вступить в контакт с переносимой молекулой в более поздний момент времени и при сниженной ее концентрации. Кроме того, переносимая молекула, которая вводится посредством внутривенной инъекции, должна иметь время для достижения целевых клеток, и это может занять более длительный период времени после введения, например, несколько дней, с тем чтобы в целевой клетке или ткани накопилось достаточное или оптимальное количество указанной переносимой молекулы. Разумеется, те же рассуждения применимы и для решения вопроса о времени введения, необходимом для поглощения фотосенсибилизирующего средства внутрь клеток. Таким образом, длительность введения, необходимая для индивидуальных клеток in vivo, как видно, варьирует в зависимости от указанных и других параметров.
Тем не менее, несмотря на то, что ситуация in vivo более сложна, чем in vitro, основная идея настоящего изобретения является неизменной, то есть время, в течение которого рассматриваемые молекулы вступают в контакт с целевыми клетками, должно быть таким, чтобы перед облучением соответствующее количество фотосенсибилизирующего средства было поглощено целевыми клетками и: либо (i) перед или во время облучения указанная переносимая молекула либо уже была поглощена, либо поглощалась бы, после достаточного периода контакта с целевыми клетками, внутрь различных внутриклеточных компартментов, либо (ii) после облучения указанная переносимая молекула приводилась бы в контакт с указанными клетками на период времени, достаточный для достижения ее поглощения внутрь клеток. С учетом того, что рассматриваемая переносимая молекула может быть поглощена в другие внутриклеточные компартменты относительно фотосенсибилизирующего средства, поглощение указанной переносимой молекулы может быть осуществлено перед или после облучения.
Термин "клетка" в контексте настоящего изобретения включает все эукариотические клетки (включая клетки насекомых и клетки грибов). Репрезентативные "клетки" включают, таким образом, все типы клеток млекопитающих и немлекопитающих животных, клетки растений, клетки насекомых, клетки грибов и простейших.
Способы настоящего изобретения могут использоваться in vitro или in vivo, либо при обработке in situ (например, при использовании целевых фрагментов), либо при обработке ex vivo с последующим введением обработанных клеток в организм.
Способы настоящего изобретения могут использоваться, например, при лечении рака. Некоторые фотосенсибилизаторы накапливаются предпочтительно в неопластических тканях, и селективность для опухоли относительно окружающей ткани соответствует обычно фактору 2-3, но указанный фактор может в некоторых случаях, например, в случае тканей мозга, быть выше, то есть достигать до 30. Альтернативно, определенное фотосенсибилизирующее средство может направляться в конкретную опухоль путем использования описанных выше способов. Кроме того, молекулы, которые могут представлять клинический интерес в плане лечения рака, но характеризуются низким поглощением в цитозоль или отсутствием такового, что ограничивает их применение, могут вводиться в цитозоль и направляться в специфические клетки посредством способа настоящего изобретения. Как показано ниже, гелонин представляет собой пример такой молекулы. Могут быть использованы другие молекулы, либо самостоятельно, либо присоединенные к другим молекулам, которые нацеливают подлежащую интернализации молекулу на конкретную клетку (например, антитела, трансферрин, фотосенсибилизаторы, apoB на восстановленных ЛНП-частицах). Преимущество такого комбинированного лечения заключается в: (1) усиленном цитотоксическом эффекте в более глубоких слоях опухолевых тканей, поскольку для разрушения лизосом и эндосом достаточно низких и субтоксических доз облучения; (2) увеличенной специфичности лечения, поскольку ФХИ воздействует только на зону опухоли.
Способы настоящего изобретения могут также применяться для лечения различных иных заболеваний, что определяется выбором молекулы, вводимой в клетку, таких как ревматоидный артрит, атеросклероз и другие сердечно-сосудистые заболевания, вирусные и другие инфекции, псориаз, солнечный кератоз, процесс заживления ран, процесс заживления переломов, бородавки и наследственные генетические нарушения, такие как фиброзно-кистозная дегенерация, синдром Горлина и атаксия - телеангиэктазия.
Способы настоящего изобретения могут также использоваться в генной терапии, то есть при терапевтическом переносе генов в клетки пациента. Генная терапия представляет собой многообещающий инструмент для лечения многих заболеваний, таких как рак, сердечно-сосудистые заболевания, вирусные инфекции, моногенные заболевания, такие как фиброзно-кистозная дегенерация и многие другие состояния, в том числе описанные выше. Одной из важнейших проблем в генной терапии сегодняшнего дня является достижение in vivo высокой эффективности и специфичности генного переноса. В применяемых в настоящее время в рамках генной терапии способах для переноса генов используется много различных носителей или векторов. В качестве примеров можно указать на поликатионные соединения, катионные липиды и вирусные системы, но до сегодняшнего момента генная терапия in vivo имеет лишь незначительный успех. Среди множества известных недостатков существующих способов можно назвать низкую стабильность векторов в сыворотке, ограниченную специфичность доставки гена, низкую эффективность доставки гена и т.п. Способы ФХИ согласно настоящему изобретению предлагают средство существенного улучшения как эффективности, так и специфичности многих методов доставки гена из числа используемых в генной терапии за счет улучшения стадии высвобождения из эндосом, которая может представлять собой фактор, ограничивающий эффективность как многих векторов доставки синтетических генов, так и некоторых вирусных систем. Производимая в рамках способа ФХИ световая обработка также дает возможность точно определить, в каком месте организма должен осуществляться усиленный перенос гена, поскольку увеличение эффективности генного переноса происходит только лишь в облучаемых зонах. Трансфекция может производиться in vitro, in vivo или ex vivo (путем введения пациенту подходящих клеток или тканей). Предпочтительно подходящие носители и векторы для целей трансфекции включают аденовирусы, поликатионы, такие как полилизин (например, поли-D-лизин или поли-L-лизин), SuperFect®, полиэтиленимин или дендримеры, катионные липиды, такие как ДОТАП или Lipofectin, или катионные липиды, полученные с помощью "хелперного липида", такие как ДОФЭ, пептиды и целевые векторы, такие как, например, трансферрин-полилизин или целевые аденовирусные векторы. В предпочтительном варианте реализации изобретения носитель, используемый для доставки терапевтического гена, представляет собой аденовирус.
Другой предпочтительный аспект настоящего изобретения связан с использованием невирусных систем носителей, таких как, например, катионные полимеры, включающие пептиды и катионные липиды. Типичные полимеры включают, например, полиамин, полиаминокислоты, включая основные полиаминокислоты, синтетические и натуральные катионные полимеры сахаров, метакрилатные полимеры, дендримеры, полиалкиленимины и другие полимеры, известные в технике как применимые для доставки лекарственных средств, в особенности полимеры, используемые для доставки генов. Типичные соединения, полезные в рамках настоящего изобретения, включают полилизин, полиаргинин, поли-L-глютаминовую кислоту, поливинилпиридин, хитозан, полиэтиленимин, поли(2-диметиламино)этилметакрилат, гистоны, протамин, поли(L-орнитин), авиден, спермин, спермидин и любые их производные. В предпочтительном аспекте настоящего изобретения описанные полимеры могут объединяться с другими полимерами или объединяться с другими системами доставки генов. Невирусные системы доставки генов, полезные в рамках настоящего изобретения, включают, например, описанные в литературе системы (R.I.Mahato et al., in Advances in Genetics (Eds. J.C.Hall et al.) (1999), 41, 95-156). Катионные полимеры описаны также в других работах (M.C.Garnett in Critical Reviews in Therapeutic Drug Carrier Systems (1999), 16, 147-207; K.A.Howard et al. In Biochimica et Biophysica Acta (2000), 1475, 245-255; H.K.Nguyen et al. in Gene Therapy (2000), 7, 126-138; A.Bragonzi et al. in J. Controlled Release (2000), 65, 187-202; S.C.DeSmedt et al. in Pharmaceutical Reseach (2000), 17, 113-126; and R.I.Mahoto in J. Drug Targeting (1999), 7, 249-268).
Другой аспект настоящего изобретения включает использование липосом или других конструкций на основе липидов в качестве невирусных систем носителей. Липосомы могут представлять собой рН-чувствительные липосомы или нечувствительные к рН липосомы. Липосомы, чувствительные к рН, состоят по меньшей мере из одного рН-чувствительного компонента в липосомной мембране. Типичные соединения включают жирные кислоты, такие как олеиновая кислота, пальмитоилгомоцистеин, холестерин, гемисукцинатную соль морфолина и диэлоилсукцинилглицерин. В дополнение к рН-чувствительным компонентам, липосомы могут содержать диолеоилфосфатидилэтаноламин (ДОФЭ) и/или другие сходные фосфолипиды.
Липосомы или другая система доставки на основе липидов содержит предпочтительно по меньшей мере один катионный липид.
Система доставки на основе липидов может быть представлена в виде различных типов водных композиций. В литературе используются различные термины для обозначения таких композиций: многослойные липосомы, однослойные липосомы, рН-чувствительные липосомы, наноэмульсии, наночастицы, протеолипосомы, виросомы, химерасомы, кохелаты, липофектин® (Lipofectin®) и липоплекс (lipoplex). Ссылки на использование катионных липидов для транспортировки генов включают приведенные ниже работы (P.L.Felgner et al. in Proc. Natl. Acad. Sci. USA (1987), 84, 7413-7417; D.D.Lasic et al. in Adv. Drug Del Rev (1996), 20, 221-266; L.G.Barron et al. in Gene Therapy (1999), 6, 1179-1183; S.Kawakami et al. in Pharmaceutical Research (2000), 17, 306-313; N.S.Templeton et al. in Molecular Biotechnology (1999), 11, 175-180; Y.Zou et al. in Cancer Gene Therapy (2000), 7, 683-696; D.D.Stuart et al. in Biochemistry et Biophysica Acta (2000), 1463, 219-229; R.I.Mahato et al. in Drug Deliv (1997), 4, 151; and R.J.Lee et al. in Crit Rev Drug Carrier Systems (1997), 14, 173).
Липиды, полезные в рамках настоящего изобретения, включают, например, те из них, которые описаны в патентах США US 6120751, US 6056938, US 6093816, US 6039936, US 6034137, US 6034135, US 6020526, US 5980935, US 5958935, US 5935936, US 5877220, US 5830430, US 5777153, US 5705693, US 5459127, US 5334761, US 5264618 и содержащихся в них ссылках.
Типичные примеры катионных липидов включают хлорид N[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония (ДОТМА), бромид 1,2-димиристилоксипропил-3-диметилгидроксиэтиламмония (ДМРИЭ), 1,2-бис-(олеоилокси)-3-(триметиламино)пропан (ДОТАП), 3β-(N',N'-диметиламиноэтан)карбамоилхолестерин (Дк-Хол), трифторацетат 2,3-диолеилокси-N-[2-сперминкарбоксиламидо]этил-N,N-диметил-1-пропанаминия (ДОСПА, 3β-(N4-спермидинкарбамоил)холестерин и диоктадециламидоглилспермин (ДОГС).
Как указывалось выше, в одном из предпочтительных вариантов осуществления настоящего изобретения в качестве носителя выступают катионные липиды. Ранее сообщалось, что фотохимическая обработка оказывает ингибирующее воздействие на трансфекцию, опосредованную катионными липидами, в том случае, когда облучение светом проводят после введения переносимой молекулы (Prasmickaite et al. (2000), J. Gene Med., 6, в печати). Однако в настоящее время очень неожиданно было показано, что когда облучение светом проводят перед введением переносимой молекулы, ФХИ может оказывать стимулирующий эффект на трансфекцию с помощью катионных липидов (см. пример 9).
Таким образом, еще один аспект настоящего изобретения относится к композициям, включающим переносимую молекулу и фотосенсибилизирующее средство, с целью использования в терапии. Переносимая молекула и/или фотосенсибилизирующее средство в таких композициях могут быть необязательно ассоциированы с молекулами носителя, такими как было указано выше. Предпочтительно композиции используют для лечения рака или в генной терапии. Для генной терапии предпочтительной молекулой носителя является аденовирус. Другие предпочтительные носители представляют собой катионные липиды.
В этой связи, в еще одном аспекте настоящее изобретение относится к использованию переносимой молекулы и/или фотосенсибилизирующего средства, указанных выше, для получения лекарственного средства с целью использования в терапии, причем указанное фотосенсибилизирующее средство и отдельно переносимую молекулу приводят в контакт с клетками или тканями пациента и указанные клетки облучают светом с длиной волны, эффективной для активации указанного фотосенсибилизирующего средства, причем облучение проводят перед поглощением клетками указанной переносимой молекулы во внутриклеточные компартменты, содержащие указанное фотосенсибилизирующее средство, предпочтительно перед поглощением клеткой указанной переносимой молекулы в какой-либо внутриклеточный компартмент. Способы обработки, включающие такие методы, образуют альтернативные аспекты настоящего изобретения.
Таким образом, настоящее изобретение относится к способу лечения или предупреждения заболевания, расстройства или инфекции у пациента, включающему введение переносимой молекулы в одну или более клеток in vitro, in vivo или ex vivo в соответствии с приведенным в описании способом, и там, где это необходимо (то есть, когда трансфекцию проводят in vitro или ex vivo), введение указанных клеток данному пациенту.
В контексте настоящего описания термин "лечение"/"обработка" относится к снижению, облегчению или устранению одного или более симптомов заболевания, расстройства или инфекции, подлежащих лечению, по сравнению с симптомами, имевшимися до такого лечения. Термин "профилактика" относится к задержке или предупреждению начала развития симптомов заболевания, расстройства или инфекции.
Как указывалось ранее, такие способы также могут применяться при вакцинации. Соответственно, другим аспектом настоящего изобретения является способ экспрессии или презентации антигенной молекулы (переносимой молекулы) или ее части на поверхности клетки, предпочтительно клетки, презентирующей антиген, причем указанный способ включает определенные в настоящем описании стадии.
В контексте настоящего описания термин "экспрессия" или "презентация" относится к присутствию молекулы или ее части на поверхности указанной клетки, так что по меньшей мере часть данной молекулы становится открытой и доступной для окружения данной клетки. Может быть достигнута такая экспрессия на "поверхности", при которой указанная молекула, подлежащая экспрессии, находится в контакте с клеточной мембраной и/или компонентами клетки, которые могут присутствовать или обеспечивают присутствие в данной мембране.
Указанный способ может быть осуществлен in vitro или in vivo. Предпочтительно, однако, подобная антигенная презентация может оказать благоприятное воздействие с точки зрения стимуляции иммунного ответа, предпочтительно иммунного ответа, который создает защиту против последующей атаки структуры, включающей или содержащей такую антигенную молекулу или ее часть, и, следовательно, настоящее изобретение рассматривает конкретную процедуру как способ вакцинации. Предпочтительно, в этой связи, настоящее изобретение относится к способу вакцинации, включающему приведенный в настоящем описании способ.
В таком аспекте изобретения переносимую молекулу определяют как "антигенную молекулу". Указанная антигенная молекула может представлять собой любую молекулу, если такая молекула или ее часть способна к стимулированию иммунного ответа, в случае ее попадания соответствующим образом в иммунную системы. В этой связи выгодно, чтобы антигенная молекула представляла собой антиген вакцины или компонент вакцины, такой как структура, содержащая полипептид.
Многие такие антигены или компоненты антигенных вакцин известны в технике и включают все возможные варианты бактериальных и вирусных антигенов, причем или истинных антигенов, или антигенных компонентов любых патогенных видов, включая простейших или высшие организмы. Традиционно, антигенные компоненты вакцин включали целые организмы (либо живые, либо убитые или ослабленные), то есть это были вакцины с целыми клетками, кроме того, субъединичные вакцины, то есть вакцины, построенные на определенных антигенных компонентах организма, например на белках или пептидах, или даже на углеводах широко исследовались, и результаты этих исследований освещены в литературе. Любой такой компонент субъединичной вакцины может использоваться в качестве антигенной молекулы согласно настоящему изобретению. Однако настоящее изобретение рассматривает, в особенности, применение в области пептидных вакцин. Таким образом, предпочтительной антигенной молекулой согласно настоящему изобретению является пептид (который, по определению настоящего изобретения, включает пептиды, как короткие, так и длинные, то есть пептиды, олигопептиды или полипептиды, а также белковые молекулы или их фрагменты, то есть пептиды, содержащие 5-500 аминокислотных остатков, например от 10 до 250, такие как 15-75 или 8-25 аминокислот). Части антигенных молекул, которые презентируются или экспрессируются, предпочтительно включают те части, которые генерируются внутри клетки механизмом антигенного процессинга. Эти части, однако, могут генерироваться при помощи других средств, что достигается созданием определенных антигенных конструкций (например, рН-чувствительных участков) или посредством других механизмов клеточного процессинга. Соответственно, такие части характеризуются размером, достаточным для генерирования иммунного ответа, например, в случае пептидов, они имеют длину более 5, например больше, чем 10 или 20 аминокислот.
В литературе описано огромное количество пептидов, которые могут быть кандидатами на использование в составе вакцин, например, при лечении вирусных заболеваний и инфекций, таких как СПИД/ВИЧ инфекции или грипп, парвовирус собак, вирус лейкоза крупного рогатого скота, гепатит и пр. (см., например, Phanuphak et al., Asian Pac. J. Allergy. Immunol. 1997, 15(1), 41-8; Naruse, Hokkaido Igaku Zasshi 1994, 69(4), 811-20; Casal et al., J. Virol. 1995, 69(11), 7274-7; Belyakov et al., Proc. Natl. Acad. Sci. USA, 1998, 95(4), 1709-14; Naruse et al., Proc. Natl. Acad. Sci. USA, 1994, 91(20), 9588-92; Kabeya et al., Vaccine 1996, 14(12), 1118-22; Itoh et al., Proc. Natl. Acad. Sci. USA 1986, 83(23)9174-8). Аналогично могут использоваться бактериальные пептиды, если такие пептидные антигены могут быть получены из других организмов или видов.
В дополнение к антигенам, полученным из патогенных организмов, были также предложены пептиды для использования в качестве вакцин против рака или других заболеваний, таких как множественный склероз. Так, например, пептиды мутантного онкогена являются очень многообещающими в качестве антигенов противораковых вакцин, действующих в направлении стимуляции цитотоксических Т-лимфоцитов (Schirrmacher, Journal of Cancer Research and Clinical Oncology 1995, 121, 443-451; Curtis Cancer Chemotherapy and Biological Response Modifiers, 1997, 17, 316-327). Была также исследована синтетическая пептидная вакцина, применяемая для лечения метастазов меланомы (Rosenberg et al., Nat. Med. 1998, 4(3), 321-7). В литературе также описана пептидная вакцина на основе рецептора Т-клеток для лечения множественного склероза (Wilson et al., J. Neuroimmunol. 1997, 76(1-2), 15-28). Любой компонент такой пептидной вакцины может использоваться в качестве антигенной молекулы согласно настоящему изобретению, если такие пептиды описаны или предложены в качестве пептидных вакцин в литературе. Следовательно, такой пептид может быть синтетическим или может быть выделен или иным образом получен из организма.
Клетка, которая является объектом данных способов, вариантов использования и т.п. согласно настоящему изобретению, может представлять собой любую клетку, которая способна к экспрессии или презентации на своей поверхности молекулы, которая вводится или переносится в ее цитозоль.
Поскольку основное использование согласно настоящему аспекту изобретения связано с презентацией антигена или вакцинацией, указанная клетка представляет собой, соответственно, эффекторную клетку иммунитета, то есть клетку, участвующую в иммунном ответе. Однако другие клетки также могут презентировать антиген для иммунной системы, и такие клетки также охватываются областью данного аспекта настоящего изобретения. Клетки согласно данному аспекту представляют собой, таким образом, подходящие для презентации антигена клетки. Такие презентирующие антиген клетки могут участвовать в любом аспекте или в "ответвлении" иммунного ответа, включая и гуморальный, и клеточный иммунитет, например, в стимуляции образования антител или в стимуляции цитотоксичных или киллерных клеток, которые могут распознавать и разрушать (или иным способом элиминировать) клетки, экспрессирующие на своей поверхности "чужеродные" антигены. Термин "стимулирующие иммунный ответ" включает таким образом все типы иммунного ответа и механизмы их стимуляции.
Для стимуляции цитотоксичных клеток или клеток, образующих антитела, требуется, чтобы антигены, подлежащие презентации клетками, определенным образом стимулировались презентирующими антиген клетками, например, презентация MHC класса 1 (например, активация CD8+ цитотоксичных Т-клеток нуждается в презентации антигена MHC-1).
Антиген-презентирующие клетки известны в технике и описаны в литературе и включают, например, лимфоциты (клетки типа Т и В), дендритные клетки, макрофаги и т.п. Другие клетки включают, например, раковые клетки, например клетки меланомы.
Для антигенного представления антиген-презентирующей клетки в цитотоксическую Т-клетку (CTL) указанная антигенная молекула должна войти в цитозоль антиген-презентирующей клетки (Germain, Cell, 1994, 76, 287-299). Настоящее изобретение предлагает эффективные способы доставки антигенной молекулы в цитозоль. Антигенная молекула после высвобождения в цитозоле с помощью фотохимического процесса интернализации может быть процессирована посредством механизма антигенного процессинга клетки и соответствующим образом презентирована на клеточной поверхности, например, посредством MHC класса I. Такой процессинг может включать деградацию антигена, например, деградацию белкового или полипептидного антигена до пептидов, причем указанные пептиды затем образуют комплексы с молекулами MHC для целей презентации. Таким образом, антигенные молекулы, экспрессируемые или презентируемые на поверхности клетки согласно настоящему изобретению, могут представлять собой часть или фрагмент антигенной молекулы, которая поглощается клеткой.
Антигены могут быть поглощены антиген-презентирующими клетками посредством эндоцитоза и далее подвергнуты деградации во внутриклеточных везикулах до пептидов. Указанные пептиды могут связываться с молекулами MHC класса II в эндосомах и далее могут быть перемещены на клеточную поверхность, где комплекс пептид-MHC класса II может быть распознан CD4-T+ хелперными клетками, и индуцировать иммунный ответ. Альтернативно, белки в цитозоле могут быть разложены на составляющие части, например, с помощью протеосом с последующим транспортом в эндоплазматический ретикулум с помощью TAP (переносчик, ассоциированный с презентацией антигена), при этом пептиды могут связываться с молекулами MHC класса I и далее переноситься на клеточную поверхность, как показано на фиг.1 (Yewdell and Bennink, 1992, Adv. Immunol. 52: 1-123). Если происхождение пептида связано с чужеродным антигеном, то комплекс пептид-MHC класса I будет распознаваться CD8+ цитотоксичными Т-клетками (CTL). CTL будут связываться комплексом пептид-MHC (HLA) класса I и будут, таким образом, активироваться, запускать пролиферацию и образовывать клон CTL. Целевая клетка и другие целевые клетки, включающие тот же комплекс пептид-MHC класса I на клеточной поверхности, могут быть элиминированы клоном CTL. Иммунитет против чужеродного антигена может быть установлен, если в цитозоль вводится достаточное количество антигена (Yewdell and Bennink, 1992, supra; Rock, 1996, Immunology Today, 17: 131-137). Указанный механизм представляет собой основу для развития, в том числе, и противораковых вакцин. Одной из самых больших практических проблем является необходимость введения достаточных количеств антигенов (или частей антигена) в цитозоль. Указанная проблема может быть решена в соответствии с настоящим изобретением посредством ФХИ.
Композиции согласно настоящему изобретению могут также включать клетку, содержащую транспортируемую молекулу, которая была интернализована в цитозоль указанной клетки по способу настоящего изобретения, с целью использования в терапии, в особенности при лечении рака, в генной терапии и при вакцинации.
Таким образом, еще один аспект настоящего изобретения относится к клетке или популяции клеток, содержащих транспортную молекулу, которая подверглась интернализации в цитозоль указанной клетки, причем указанную клетку получают по способу настоящего изобретения.
Еще один аспект настоящего изобретения относится к использованию такой клетки или популяции клеток для получения композиции или лекарственного средства с целью их использования в терапии, предпочтительно при лечении рака, в генной терапии и при вакцинации.
Настоящее изобретение относится также к способу лечения пациента, включающему введение указанному пациенту клеток или композиций согласно настоящему изобретению, например к способу, включающему стадии введения молекулы в клетку, как указано в настоящем описании, и затем введения полученной таким образом клетки указанному пациенту. Предпочтительно данные способы используются для лечения рака, при генной терапии или при вакцинации.
Для применения in vivo может использоваться любой режим введения, который является обычным или стандартным для данной области техники, например, могут использоваться инъекция, инфузия, местное введение как во внутренние, так и во внешние поверхности тела и т.п. В случае in vivo настоящее изобретение может быть осуществлено применительно к любой ткани, содержащей клетки, в которых локализуется фотосенсибилизирующее средство и переносимая молекула, включая локализацию в жидкостях организма, а также в твердых тканях. Все ткани могут быть обработаны при условии, если фотосенсибилизатор поглощается целевыми клетками и свет может быть соответственным образом к ним доставлен.
Таким образом, композиции согласно настоящему изобретению могут быть получены любым удобным способом с использованием методик и процедур, известных в фармацевтической области, например, с использованием одного или более фармацевтически приемлемых носителей или наполнителей. Термин "фармацевтически приемлемый" в контексте настоящего описания относится к ингредиентам, который совместимы с другими ингредиентами композиции, а также являются физиологически приемлемыми для реципиента. Природа композиции и материалы носителей или эксципиента, дозировки и т.п. могут быть выбраны традиционным способом в зависимости от потребности, от желаемого способа введения, цели введения и т.п. Дозировки могут быть соответствующим образом определены рутинными методами и могут зависеть от природы молекулы, цели обработки, возраста пациента, способа введения и т.п. В том, что касается фотосенсибилизирующего средства, во внимание также должны приниматься активность/способность к разрушению мембран при облучении.
Ниже настоящее изобретение будет описано более детально с помощью не ограничивающих примеров, в которых имеется ссылка на прилагаемые чертежи, в которых:
На фиг.1 показана индуцированная светом трансфекция THX клеток комплексом pEGFP-N1-полилизин, где клетки контактируют с pEGFP-N1-полилизиновым комплексом до или после обработки клеток светом, как показано на чертеже.
На фиг.2 показана индуцированная светом трансфекция HCT-116 клеток pEGFP-N1-полилизиновым комплексом, в ходе которой клетки вступают в контакт с pEGFP-N1-полилизиновым комплексом до или после экспозиции клеток на свету, как показано на чертеже.
На фиг.3 показана индуцированная светом обработка THX клеток гелонином и достигаемое при этом снижение синтеза белка, при которой клетки контактируют с молекулой гелонина до или после обработки клеток светом, как показано на чертеже.
На фиг.4 показано влияние на эффективность индуцированной светом трансфекции THX клеток при контактировании клеток с pEGFP-N1-полилизиновым комплексом сразу после воздействия светом и в более поздние моменты времени после воздействия света.
На фиг.5 показано влияние на эффективность индуцированной светом трансфекции THX клеток в том случае, когда клетки контактируют с pEGFP-N1-полилизиновым комплексом в разные моменты времени до и после световой экспозиции.
На фиг.6 показано влияние на индуцированную светом трансфекцию THX клеток в том случае, когда клетки контактируют с pEGFP-N1-полилизиновым комплексом в течение разных периодов времени после воздействия света.
На фиг.7 показано схематическое изображение потенциальной модели, посредством которой может работать настоящее изобретение.
A.I. фотосенсибилизатор S подвергается эндоцитозу (I) и заключается во внутриклеточные везикулы (II). Указанные везикулы разрушаются при воздействии света (III).
B. После фотохимической обработки, описанной в пункте А, клетки обрабатывают молекулой M, которая подверглась эндоцитозу и была заключена во внутриклеточные везикулы. Указанные везикулы сливаются с фотохимически поврежденными везикулами и молекула M высвобождается в цитозоль.
На фиг.8 показано влияние на трансфекцию pEGFP-N1-полилизинового комплекса при обработке клеток при 0°С.
На фиг.9 показана индуцированная светом трансфекция pEGFP-N1-полилизинового комплекса в том случае, когда в качестве сенсибилизирующего средства используют 3-THPP, который в основном не локализуется во внутриклеточных везикулах.
На фиг.10 показан эффект сочетания фотосенсибилизатора и световой предобработки на трансфекцию клеток катионными липидами.
На фиг.11 показан эффект фотохимической обработки на аденовирусную трансдукцию THX клеток.
На фиг.12 показан эффект фотохимической обработки на внутриклеточную локализацию FITC-дикстрана. THX клетки инкубируют с 20 мкг/мл ALPcS2a в течение 18 часов с последующей 4-часовой инкубацией в среде без ALPcS2a. Далее клетки либо подвергают воздействию света в течение 4 минут (B, D), либо выдерживают в темноте (A, C) перед 3-х часовой инкубацией с 5 мг/мл FITC-декстраном. Приведены микрофотографии, полученные с помощью флуоресцентного (A, B) и фазово-контрастного микроскопа (C, D).
На фиг.13 показан эффект фотохимической обработки на токсичность гелонина в THX и HCT 116 клетках. В случае стратегии "свет раньше" клетки вначале инкубируют с 20 мкг/мл ALPcS2a в течение 18 часов, затем еще в течение 4 часов в среде без ALPcS2a с последующим воздействием света, как показано на чертеже. После освещения добавляют 1 мкг/мл гелонина и клетки инкубируют в течение 18 часов. В случае стратегии "свет после" клетки инкубируют совместно с 20 мкг/мл ALPcS2a и 1 мкг/мл гелонина в течение 18 часов с последующим воздействием света, как показано на чертеже. Контрольные клетки обрабатывают только 1 мкг/мл гелонина в течение 18 часов и подвергают воздействию света или обрабатывают только 20 мкг/мл ALPcS2a в течение 18 часов с заменой на 4 часа на среду без ALPcS2a и подвергают световой обработке. Включение [3H]-лейцина в белки измеряют на следующий день после световой обработки и выражают в виде относительной доли белкового синтеза. Приведенные данные по точкам отражают среднее значение ± стандартную ошибку (СО) трехкратных повторов.
На фиг.14 показан эффект фотохимической обработки на экспрессию β-галактозидазы в THX клеток, инфицированных AdHCMV-lacZ. В случае стратегии "свет раньше" предварительно обработанные ALPcS2a клетки инкубируют еще 4 часа в среде без ALPcS2a перед световой экспозицией в течение 3 минут. После освещения клетки инфицируют AdHCMV-lacZ (при МИ 1) в течение 30 минут при 37°С. Затем добавляют 2 мл среды и клетки инкубируют в течение двух дней перед проведением анализа на экспрессию β-галактозидазы. В случае стратегии «свет позже» обработанные ALPcS2a клетки инкубируют в течение 3 часов в среде без ALPcS2a с последующей инфекцией AdHCMV-lacZ. После добавления 2 мл культуральной среды клетки инкубируют в течение еще 30 минут с последующим освещением в течение 3 минут и через два дня проводят анализ на экспрессию β-галактозидазы.
На фиг.15 показан эффект времени инкубации на эффективность светоиндуцированной трансфекции pEGFP/полилизином в ТНХ и НСТ 116 клетки. Предварительно обработанные ALPcS2a клетки промывают и инкубируют в среде без ALPcS2a в течение 4 часов перед световой экспозицией в течение 3 минут (ТНХ клетки) или 7 минут (НСТ клетки).После освещения добавляют pEGFP-N1/полилизиновый комплекс (плазмида, 5 мкг/мл) и клетки инкубируют в течение разных периодов времени, как показано на чертеже. После удаления комплекса добавляют свежую среду без указанного комплекса и клетки инкубируют в течение двух дней перед проведением анализа на экспрессию EGFP.
На фиг.16 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию ТНХ клеток, опосредованную поли-L-лизином при использовании TPPS2a в качестве фотосенсибилизатора в сравнении c результатами обработки по стратегии «свет после» при разной продолжительности облучения. PLL-L: Облучение после добавления pEGFP-N1/PLL комплекса. L-PLL: Облучение перед добавлением pEGFP-N1/PLL комплекса. Незатемненные прямоугольники - без световой обработки, затемненные прямоугольники - облучение в течение 70 секунд, черные прямоугольники - облучение в течение 100 секунд.
На фиг.17 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию ТНХ клеток, опосредованную поли-L-лизином при использовании TPPS4 в качестве фотосенсибилизатора в сравнении c результатами обработки по стратегии «свет после» при разной продолжительности облучения. PLL-L: Облучение после добавления pEGFP-N1/PLL комплекса. L-PLL: Облучение перед добавлением pEGFP-N1/PLL комплекса. Незатемненные прямоугольники - без световой обработки, горизонтально затемненные прямоугольники - облучение в течение 50 секунд, вертикально затемненные прямоугольники - облучение в течение 70 секунд, черные прямоугольники - облучение в течение 100 секунд. На фиг.18 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию HCT 116, опосредованную поли-L-лизином, при использовании TPPS2a в качестве фотосенсибилизатора в сравнении с результатами обработки по стратегии «свет после» при разной продолжительности облучения. PLL-L: Облучение после добавления pEGFP-N1/PLL комплекса. L-PLL: Облучение перед добавлением pEGFP-N1/PLL комплекса. Незатемненные прямоугольники - без световой обработки, затемненные прямоугольники - облучение в течение 70 секунд, черные прямоугольники - облучение в течение 100 секунд.
На фиг.19 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию HCT 116 клеток, опосредованную поли-L-лизином, при использовании TPPS4 в качестве фотосенсибилизатора в сравнении с результатами обработки по стратегии «свет после» при разной продолжительности облучения. PLL-L: Облучение после добавления pEGFP-N1/PLL комплекса. L-PLL: Облучение перед добавлением pEGFP-N1/PLL комплекса. Незатемненные прямоугольники - без световой обработки, горизонтально затемненные прямоугольники - облучение в течение 1,5 минут, вертикально затемненные прямоугольники - облучение в течение 2 минут, черные прямоугольники - облучение в течение 3 минут.
На фиг.20 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию, опосредованную ДОТАП, при использовании TPPS4 в качестве фотосенсибилизатора в сравнении в сравнении с результатами обработки по стратегии «свет после» при разной продолжительности облучения. ДОТАП-L: Облучение после добавления pEGFP-N1/ДОТАП комплекса. L-ДОТАП: Облучение перед добавлением pEGFP-N1/ДОТАП комплекса. Незатемненные прямоугольники - без световой обработки, затемненные прямоугольники - облучение в течение 70 секунд, черные прямоугольники - облучение в течение 100 секунд.
На фиг.21 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию, опосредованную SuperFect®, при использовании TPPS2a в качестве фотосенсибилизатора, при разной продолжительности освещения и трансфекции и при варьировании количества ДНК, применяемой для трансфекции. ▪ - трансфекция в течение 1 часа с использованием 0,75 мкг ДНК; ▴ - трансфекция в течение 4 часов с использованием 0,75 мкг ДНК; ○ - трансфекция в течение 1 часа с использованием 1,5 мкг ДНК.
На фиг.22 показан эффект световой обработки по первой стратегии ФХИ на генную трансдукцию, опосредованную аденовирусом, HCT 116 клеток с использованием ALPcS2a в качестве фотосенсибилизатора, при которой вирус добавляют в разные временные точки. Процент трансдуцированных клеток в случае добавления вируса в разные временные точки анализируют методом проточной цитометрии, как описано в приведенном примере. Временные точки добавления вирусных комплексов показаны на чертеже. Временные точки слева от оси Y иллюстрируют ситуацию добавления вируса до облучения, временные точки справа иллюстрируют ситуацию добавления вируса после облучения. ▪ - 1 минута облучения; □ - без облучения.
На фиг.23 показан эффект световой обработки по первой стратегии ФХИ на трансфекцию HCT 116 клеток, опосредованную поли-D-лизином, с использованием ALPcS2a в качестве сенсибилизатора при варьировании времени облучения.
На фиг.24 показан эффект световой обработки по первой стратегии ФХИ на количество клеток, убитых цитостатическим агентом блеомицина, с использованием TPPS2a в качестве фотосенсибилизатора при использовании варьирующих количеств блеомицина, разного времени облучения и разного времени трансфекции.  TPPS-; 1 час = 5 мкМ блеомицина без TPPS2a, 1 час инкубации; ◆ - 5 TPPS+, 1 час = 5 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; Δ 25 TPPS-, 1 час = 25 мкМ блеомицина, без TPPS2a, 1 час инкубации; ▴ - 25 TPPS+; 1 час = 25 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; □ - 100 TPPS-, 1 час = 100 мкМ блеомицина без TPPS2a, 1 час инкубации; ▪ - 100 TPPS+, 1 час = 100 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; ○ - 100 TPPS-, 4 часа = 100 мкМ блеомицина без TPPS2a, 4 часа инкубации; ● - 100 TPPS+; 4 часа = 100 мкМ блеомицина с использованием TPPS2a, 4 часа инкубации.
TPPS-; 1 час = 5 мкМ блеомицина без TPPS2a, 1 час инкубации; ◆ - 5 TPPS+, 1 час = 5 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; Δ 25 TPPS-, 1 час = 25 мкМ блеомицина, без TPPS2a, 1 час инкубации; ▴ - 25 TPPS+; 1 час = 25 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; □ - 100 TPPS-, 1 час = 100 мкМ блеомицина без TPPS2a, 1 час инкубации; ▪ - 100 TPPS+, 1 час = 100 мкМ блеомицина с использованием TPPS2a, 1 час инкубации; ○ - 100 TPPS-, 4 часа = 100 мкМ блеомицина без TPPS2a, 4 часа инкубации; ● - 100 TPPS+; 4 часа = 100 мкМ блеомицина с использованием TPPS2a, 4 часа инкубации.
На фиг.25 показан эффект ФХИ с использованием гелонина для обработки опухолей у мышей на модели in vivo. Используют следующие группы: (Δ) только гелонин; (▪) обработка плацебо для проведения инъекции фосфатно-буферного раствора (ФБР), объединенной с освещением; ( ) только фотохимическая обработка (то есть ALPcS2a + свет), но без гелонина; (●) полная обработка гелонином в сочетании с ФХИ обработкой (то есть ALPcS2a + гелонин + свет).
) только фотохимическая обработка (то есть ALPcS2a + свет), но без гелонина; (●) полная обработка гелонином в сочетании с ФХИ обработкой (то есть ALPcS2a + гелонин + свет).
Примеры
Материалы и методы
Клеточные линии
Из опухолевой ткани, полученной от пациента, подвергавшегося лечению по поводу метастазов злокачественной меланомы в Норвежском радиологическом госпитале, устанавливают клеточную линию меланомы человека THX (Aamdal et al., 1986., Int. J. Cancer, 37, 579) и растят ее в среде RMPI 1640 (Gibco-BRL) с добавкой 10% ФСТ (Gibco-BRL) и 2 мМ глютамина (Gibco-BRL). Клеточную линию карциномы толстого кишечника человека HCT 116 получают из Американской коллекции культур (American Type Culture Collection, ATCC no. CCL-247) и растят в среде RPMI 1640 с добавкой 10% фетальной сыворотки теленка, 100 Ед/мл пенициллина, 100 мг/мл стрептомицина и 2 мМ глютамина (все препараты от Gibco-BRL, Paisley, UK).
Облучение
Для обработки клеток используют два равных источника света, состоящие оба из панели с 4 флуоресцентными трубками. Клетки обрабатывают TPPS4, TPPS2a и 3-THPP (Porphyrin Products, Logan, UT) и подвергают воздействию синего света (модель 3026; Appl. Photophysics, London, UK) с интенсивностью воздействия на клетки 1,5 мВт/см2, а клетки, обработанные ALPcS2a (Porphyrin Products, Logan, UT) подвергают воздействию красного света (Philips TL 20W/09), пропущенного через фильтр Cinemoid 35 с интенсивностью воздействия света на клетки 1,35 мВт/см2.
Флуоресцентная микроскопия
Клетки анализируют под флуоресцентным микроскопом, как описано Бергом с соавт. (Berg. et al., Biochem. Biophys. Acta, 1370: 317-324, 1998). Для анализа флуоресцентно меченных молекул микроскоп снабжают фильтром на волну возбуждения 450-490 нМ, устройством для расщепления дихроического луча на 510 нМ и фильтром эммиссии с полосой пропускания в диапазоне 510-540 нМ.
Получение комплекса плазмида-pLys и обработка клеток
Комплексы плазмида-pLys (коэффициент нагрузки 1,7, как описано Бергом с соавт. (Berg. et al. (1999) Cancer Res. 59: 1180-83) получают при осторожном смешивании 5 мкг плазмиды (pEGFP-N1; Clontech Laboratories, Inc., Palo Alto, CA) в 75 мкл HBS с 5,3 мкг pLys (M.в. 20700; Сигма, St. Louis, MO) в 75 мкг HBS. Раствор инкубируют в течение 30 минут при комнатной температуре, разбавляют культуральной средой и добавляют к клеткам.
THX клетки инкубируют с 20 мкг/мл ALPcS2a в течение 18 часов при температуре 37°С, промывают и инкубируют в среде, не содержащей сенсибилизатора, в течение 3 часов до инкубации с комплексами плазмида-pLys в течение 1 часа с последующим воздействием на них света. Альтернативно, после инкубации с ALPcS2a клетки промывают и инкубируют в среде без сенсибилизатора в течение 4 часов перед экспозицией на свету с последующей 1-часовой инкубацией с комплексами плазмида-pLys. Клетки инкубируют при 37°С в течение 2 дней, затем проводят анализ на экспрессию GFP методом проточной цитометрии.
Клетки HCT-116 инкубируют в 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в течение 4 часов в отсутствии ALPcS2a перед экспозицией на свету. Далее клетки обрабатывают pEGFP-N1-полилизиновым комплексом в течение 4 часов непосредственно перед или сразу после световой экспозиции. После 2-дневной инкубации при 37°С исследуют экспрессию GFP методом проточной цитометрии.
Анализ методом проточной цитометрии
Клетки обрабатывают трипсином, центрифугируют, ресуспендируют в 400 мкл культуральной среды и фильтруют через нейлоновый фильтр 50 меш. Затем клетки анализируют с помощью проточного цитометра FACS-Calibur (Becton Dickinson). Для каждого образца проводят 10000 наблюдений. Флуоресцеиновую флюоресценцию (например, зеленого флуоресцентного белка (GFP)) измеряют при использовании фильтра на 510-530 нм после возбуждения аргоновым лазером (200 мВт), настроенного на 488 нм. ALPcS2a измеряют с использованием длинноволнового фильтра на 670 нм после возбуждения диодным лазером (50 мВт), настроенного на 635 нм. Клеточные дублеты и мертвые клетки отбрасывают от единичных жизнеспособных клеток путем селектирования. Полученные данные анализируют с помощью программного обеспечения CELLQuest Software (Becton Dickinson).
Пример 1
Индуцированная светом трансфекция как функция дозы света
THX клетки обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в среде, не содержащей сенсибилизатора, в течение 3 часов с последующей 1-часовой инкубацией с 5 мкг pEGFP-N1/полилизинового комплекса с последующей экспозицией на свету в течение 1, 2, 3 или 4 минут. Альтернативно, после инкубации с ALPcS2a клетки промывают и инкубируют в течение 4 часов в среде без сенсибилизатора перед световой обработкой в течение 1, 2, 3 или 4 минут с последующей 1-часовой инкубацией с pEGFP-N1/полилизиновым комплексом, как показано на фиг.1. Экспрессию GFP анализируют методом проточной цитометрии через 48 часов после световой экспозиции. Коэффициент нагрузки комплексом pEGFP-N1/полилизин составляет 1,7.
Полученные результаты приведены на фиг.1, из которых можно видеть, что когда комплекс плазмида-pLys (то есть pEGFP-N1/pLys) добавляют к клеткам после, а не перед экспозицией на свету, трансфекция GFP в равной степени эффективна. Можно также видеть, что при обоих видах обработки процент трансфицированных клеток зависит от продолжительности экспозиции клеток на свету, причем указанный процент достигает максимального уровня примерно к 2 минутам и затем начинает снижаться.
Пример 2
Экспрессия GFP в HCT- 116 клетках
HCT-116 клетки инкубируют с 20 мкг/мл ALPcS2a в течение 18 часов с последующей инкубацией в течение 4 часов в отсутствии ALPcS2a перед последующей экспозицией на свету. Клетки обрабатывают pEGFP-N1/полилизиновым комплексом в течение 4 часов непосредственно перед или сразу после световой экспозиции, как показано на фиг.2. Экспрессию GFP измеряют методом проточной цитометрии через 2 дня после экспозиции на свету.
Из результатов, показанных на фиг.2, можно видеть, что, как и в случае трансфекции THX клеток в примере 1, трансфекция GFP в равной мере эффективна, когда комплекс плазмида-pLys (т.е. pEGFP-N1-pLys) добавляют к клеткам после, а не перед световой экспозицией. И вновь процент трансфицированных клеток варьирует в зависимости от продолжительности воздействия света на клетки.
Пример 3
Синергический эффект добавления гелонина перед и после фотохимической обработки
Гелонин представляет собой растительный токсин, который, присутствуя цитозоле клеток, эффективно ингибирует синтез белка. THX клетки инкубируют с 20 мкг/мл ALPcS2a в течение 18 часов и затем в течение 4 часов в среде без сенсибилизатора перед экспозицией на свету. Клетки обрабатывают ALPcS2a и 1 мкг/мл гелонина, либо гелонин (1 мкг/мл) добавляют к среде сразу после световой экспозиции в течение 18 часов, после чего его удаляют из среды, как показано на фиг.3. Синтез белка измеряют через 24 часа после световой экспозиции.
Результаты приведены в Таблице 3, из которых можно видеть, что несмотря на то, что фотохимическая обработка сама по себе в отсутствие гелонина ведет к некоторому снижению синтеза белка, присутствие гелонина либо перед, либо после фотохимической обработки индуцирует значительно большее ингибирование синтеза белка. Такого рода данные результаты указывают на то, что гелонин интернализуется в клетке независимо от того, когда происходит контакт гелонина с клетками: перед или после фотохимической обработки.
Пример 4
Эффект временного параметра на индуцированную светом трансфекцию
THX клетки обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в среде без сенсибилизатора в течение 4 часов перед последующей 3-минутной световой обработкой. Клетки инкубируют в ростовой среде в течение времени, указанного на фиг.4, перед обработкой pEGFP-N1/полилизиновым комплексом (коэффициент нагрузки 1,7) в течение 1 часа. Экспрессию GFP измеряют методом проточной цитометрии через 48 часов после экспозиции светом.
Результаты приведены на фиг.4, из которых можно видеть, что для достижения наилучших результатов молекула, подлежащая интернализации, должна быть подвержена воздействию клеток относительно скоро после фотохимической обработки, поскольку трансфекция pEGFP-N1 снижается с периодом полужизни примерно 5 часов после световой экспозиции.
Пример 5
Эффективность трансфекции как функция пульсовой трансфекции в сочетании с режимами освещения
THX клетки обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в среде без сенсибилизатора. Проводят пульсовую обработку клеток (0,5 или 1 час, ширина прямоугольника ни фиг.5 отражает начало и конец обработки pEGFP-N1/полилизиновым комплексом либо перед (негативное значение абсциссы), либо после (позитивное значение абсциссы) 3-минутной световой экспозиции. Экспрессию GFP анализируют методом проточной цитометрии через 48 часов после экспозиции светом. Данные, полученные из нескольких экспериментов, нормализуют, принимая эффективность трансфекциии в случае проведения ее непосредственно перед или сразу после воздействия света за 100%. Результаты наблюдений показаны на фиг.5, из которых можно видеть, что для наилучшей эффективности трансфекции к клеткам должны быть внесены молекулы, подлежащие интернализации, либо непосредственно перед, либо сразу после воздействия света.
Пример 6
Индуцированная светом трансфекция - зависимость от времени инкубации с pEGFP-N1/полилизиновым комплексом
THX клетки обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в среде без сенсибилизатора в течение 4 часов перед обработкой светом с последующим инкубированием с pEGFP-N1/полилизиновым комплексом (коэффициент нагрузки 1,7) в течение 6 часов, как показано на фиг.6А. Экспрессию GFP анализируют методом проточной цитометрии через 48 часов после экспозиции на свету. Количество GFP-экспрессирующих клеток после обработки показано на фиг.6B и специфичность различных видов обработки проиллюстрирована на фиг.6С.
Результаты исследования, показанные на фиг.6, показывают, что несмотря на то, что количество трансфицированных клеток повышается с увеличением времени инкубации с pEGFP-N1/полилизиновым комплексом (фиг.6B), максимальная специфичность трансфекции имеет место при самых коротких периодах инкубации (фиг.6С).
Пример 7
Обработка pEGFP-N1/полилизиновым комплексом при 0°С
Данный эксперимент был проведен для выяснения, ведет ли фотохимическая обработка к незначительным изменениям клеточных мембран, иными словами, могут ли плазмиды, приведенные в контакт с клетками после световой обработки, проникать через плазматическую мембрану.
THX клетки обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, промывают и инкубируют в среде без сенсибилизатора в течение 4 часов перед обработкой светом, после которой сразу следует инкубация в течение 45 минут при 0°С с pEGFP-N1/полилизиновым комплексом (коэффициент нагрузки 1,7). Клетки представляют собой либо А) обработанные трипсином и высеянные перед переносом в условия с температурой 37°С, либо B) перенесенные в температурные условия 37°С без обработки трипсином. Клетки подвергают воздействию светом, как показано на фиг.8. Экспрессию GFP анализируют методом проточной цитометрии через 48 часов после экспозиции на свету.
После инкубации клеток в течение 45 минут при 0°С с pEGFP-N1/полилизиновым комплексом указанный комплекс прилипает к поверхности клеток, но не подвергается эндоцитозу. Далее THX клетки либо инкубируют в среде без плазмиды при 37°С (фиг.8B), либо обрабатывают трипсином (фиг.8А) с целью удаления плазмиды с поверхности и высевают на новые чашки при 37°С. Результаты эксперимента показывают, что комплекс плазмида/полилизиновый комплекс не проникает через плазматическую мембрану после фотохимической обработки.
Пример 8
Сочетание 3-THPP и света с обработкой pEGFP-N1/полилизиновым комплексом
THX клетки обрабатывают 0,25 мкг/мл 3-THPP в течение 18 часов, промывают и инкубируют в среде без сенсибилизатора в течение 4 часов перед обработкой светом, за которой сразу следует инкубация в течение 1 часа с pEGFP-N1/полилизиновым комплексом (коэффициент нагрузки 1,7). Клетки подвергают воздействию светом, как показано на фиг.9, и анализируют на наличие экспрессии GFP методом проточной цитометрии через 48 часов после экспозиции на свету.
3-THPP представляет собой фотосенсибилизатор, основное месторасположение которого не связано с эндосомами или лизосомами. Из результатов исследования, показанных на фиг.9, видно, что обработка клеток 3-THPP перед облучением индуцирует лишь небольшие изменения в экспрессии GFP в сравнении с ситуацией предыдущих примеров, где использовалось сенсибилизирующее средство ALPcS2a. Полученные результаты показывают, что фотосенсибилизирующее средство, место локализации которого связано эндосомами или лизосомами, может быть вполне удачным для целей настоящего изобретения.
Пример 9
Сочетание фотосенсибилизитора и световой предобработки позволяет проводить трансфекцию клеток c использованием катионных липидов
HCT 116 клетки высевают с плотностью 75000 клеток/ячейка в 12-ячеечный планшет за один день до эксперимента. Клетки инкубируют с фотосенсибилизатором ALPcS2a (20 мкг/мл) в течение 18 часов с последующей 7-часовой заменой на инкубацию в среде без фотосенсибилизатора и подвергают экспозиции красным светом в течение 7 минут. Затем клетки инкубируют с ДОТАП-комплексом (ДОТАП приобретают от компании Boehringer) и плазмидой pEGFP-N1 (ДОТАП/плазмида, 5:1, 1 уг/мл pEGFP-N1) в течение 3 часов, промывают ростовой средой и инкубируют при 37°С в течение 21 часа перед измерением экспрессии EGFP методом проточной цитометрии, как описано в разделе "Материалы и методы". Контрольные клетки не подвергают световой экспозиции, а в остальном обработка была идентичной.
Результаты показаны на фиг.10, из которых можно видеть, что ФХИ обработка повышает эффективность трансфекции ДОТАП/плазмидным комплексом примерно в 4 раза.
Пример 10
Влияние ФХИ на аденовирусную трансдукцию THX клеток
Материал
Флуоресцеин ди-β-D-галактопиранозид (ФДГ) получают от компании Molecular Probes (F-1179). 20 мМ стандартный раствор готовят при растворении порошка в смеси ДМСО/этанол (1:1). Смесь постепенно добавляют к соответствующему объему охлажденной льдом воды с получением раствора H2O/ДМСО/этанол (8:1:1).
Получают рекомбинантный вирус AdCA17lacZ и размножают его в клеточной линии человека 293, Ad E1-трансформированную клеточную линию эмбриона почки поддерживают в среде MEM F-11 с добавкой 10% ФСТ, 100 Ед/мл пенициллина (Gibco-BRL), 0,1 мг/мл стрептомицина (Gibco-BRL) и 2 мМ глутамина.
Конструирование рекомбинантного вируса
Рекомбинантный аденовирус AdCA17lacZ, кодирующий ген lacZ в E.coli в условиях контроля промотора человеческого CMV получают путем гомологичной рекомбинации с использованием системы pJM17 в 293 клетках (Addison et al., 1997, J. Gen. Virol., 78, 1653-1661). Рекомбинантные векторы очищают бляшкообразованием, выращивают до высокого титра в клетках 293 и очищают центрифугированием с хлоридом цезия, как было описано ранее (Hitt et al., 1995, Methods in Mol. Genetics, 7, 15-30).
Сенсибилизация клеток
THX клетки (4х105 клеток) высевают на чашки размером 6 см и оставляют расти в течение ночи. При наличии примерно 60% слияния клеток ростовую среду заменяют на 2 мл среды роста с добавкой 20 мкг/мл ALPcS2a, и чашки возвращают в инкубатор на 16-18 часов. Среду, содержащую сенсибилизатор, отсасывают и клетки инкубируют в простой ростовой среде по меньшей мере за 4 часа до световой обработки и инфекции вирусом.
Инфицирование клеток
Для отслаивания клеток от трех чашек используют трипсин-ЭДТА и подсчитывают с помощью камеры Бюрхера среднее количество клеток на чашку. Готовят разбавление аденовируса в ФБР с использованием 0,68 мМ CaCl2 и 0,5 мМ MgCl2 в соответствии с количеством клеток, необходимым для инфицирования. Обычно клетки инфицируют при МИ (множественность инфекции) 1 и 10.
Перед добавлением вирус клетки подвергают воздействию красным светом (Philips TL 20W/09, пропущенный через фильтр Cinemoid 35, с интенсивностью при воздействии на клетки 1,35 мВт/см2) в течение 3 минут. Далее среду отбирают и добавляют в каждую чашку 200 мкл суспензии вируса (или ФБР с содержанием 0,68 мМ CaCl2 и 0,5 мМ MgCl2, в случае контролей не обработанных вирусом). После инкубации в течение 30 минут при 37°С добавляют 5 мл обычной среды роста и клеткам дают подрасти в течение 48 часов.
Определение активности β-галактозидазы
Клетки отслаивают обработкой трипсином-ЭДТА и ресуспендируют в 5 мл среды роста. После центрифугирования в течение 5 минут при 1000 оборотах/мин среду отбирают, клеточный осадок суспендируют в 50 мкл среды роста и пробирки помещают в водяную баню при 37°С на 5 минут. Затем добавляют 50 мкл 2 мМ раствора ФДГ, подогретого до температуры 37°С, и пробирки вновь помещают в водяную баню на 1 минуту. В конце добавляют 900 мкл среды роста и пробирки инкубируют на льду в течение 30-60 минут до проведения анализа образцов методом проточной цитометрии, как было описано выше.
THX клетки обрабатывают ALPcS2a (обозначен на фиг.11 как PS) и аденовирусом (обозначен на фиг.11 как "вирус") и проводят экспозицию на свету в течение 3 или 4 минут, как описано в разделе "Материалы и методы", и определяют активность β-галактозидазы (β-gal) методом проточной цитометрии. Общую активность β-gal определяют при интегрировании значений β-gal активности в положительных по указанной активности клетках. Количество β-gal положительных клеток и средняя величина активности β-gal повышается при ФХИ обработке.
Полученные результаты показывают, что минимальная инфекция THX клеток происходит в том случае, когда клетки инкубируют только с вирусом или с вирусом и фотосенсибилизирующим средством, тогда как фотохимическая обработка, то есть добавление световой обработки к фотосенсибилизирующему средству, значительно усиливает трансдукцию клеток (что видно по увеличению активности β-gal).
Пример 11
Влияние фотохимической обработки на внутриклеточную локализацию поглощенной энодоцитозным путем маркерной молекулы
THX клетки высевают на чашки Falcon 3001 (2,5х104 клеток на чашку) и на следующий день обрабатывают 20 мкг/мл ALPcS2a в течение 18 часов, отмывают от ALPcS2a и инкубируют в среде без ALPcS2a в течение 4 часов. Затем клетки подвергают воздействию света в течение 4 минут перед последующей 3-часовой инкубацией с 5 мг/мл маркера на эндоцитоз FITC-декстраном.
Неосвещенные клетки обрабатывают аналогичным образом, за исключением процедуры освещения. Внутриклеточную локализацию FITC-декстрана в нефиксированных клетках определяют под флуоресцентным микроскопом Zeiss Axioplan (Oberkochen, Германия) с объективом с увеличением 63 и фильтром с полосой пропускания возбуждения в диапазоне 450-490 нм и фильтром с полосой пропускания эмиссии в диапазоне 510-540 нм. Флуоресцентные микрофотографии получают с помощью видеокамеры, соединенной с охлаждаемым устройством загрузки (CCD) (Photometrics Inc., Tucson, AZ).
Результаты показывают (фиг.12), что ФХИ в случае обработки светом перед введением флуоресцентного маркера на эндоцитоз FITC-декстрана меняет локализацию указанного маркера от эндоцитозных везикул (пятна, заметные на панели А в случае неосвещенных клеток) на цитозоль (диффузная флуоресценция, отмечаемая на панели B в освещенных клетках). Таким образом, в том случае, когда обработку светом проводят перед введением макромолекулы, подлежащих интернализации, указанная макромолекула быстро перемещается в цитозоль, тем самым значительно снижая возможность лизосомной деградации макромолекулы.
Пример 12
Влияние фотохимической обработки на токсичность гелонина в THX и HCT-116 клетках
Гелонин представляет собой растительный токсин, который, присутствуя в цитозоле клетки, эффективно ингибирует синтез белка, но который сам по себе не может поступить в цитозоль, и в этой связи является практически нетоксичным для интактных клеток. Для обработки гелонином в 24-ячеечный планшет высевают по 25х103 клеток на ячейку (Nunc, Дания). На следующий день добавляют 20 мкг/мл ALPcS2a и клетки инкубируют в течение 18 часов при 37°С. Все процедуры после добавления ALPcS2a проводят на затемненном свете. В случае стратегии "свет раньше" клетки отмывают от ALPcS2a и инкубируют в среде без ALPcS2a в течение 4 часов. Затем клетки подвергают световой экспозиции (как показано на чертежах) перед обработкой 1 мкг/мл гелонина в течение 18 часов. В случае стратегии "свет после" клетки подвергают совместной инкубации с 20 мкг/мл ALPcS2a и 1 мкг/мл гелонина в течение 18 часов и промывают перед экспозицией светом, как указано на чертеже.
Неосвещенные клетки обрабатывают аналогичным образом, за исключением освещения. Обработанные клетки промывают один раз культуральной средой и после добавления свежей культуральной среды инкубируют при 37°С перед проведением анализа. Ингибирование синтеза белка оценивают по включению [3H]-лейцина в белок через 24 часа после световой экспозиции. Освещение обеспечивают при помощи панели с четырьмя световыми трубками (Philips, TL 20W) и длинноволновым фильтром, отсекающим диапазон 550-600 нм. Интенсивность света при достижении клеток составляет 13,5 Вт/м2.
Результаты данного примера показывают, что и в THX (фиг.13А), и в HCT 116 (фиг.13 B) клетках стратегия "свет раньше" работает лучше, чем стратегия "свет позже". Так, для THX-клеток при наивысшей дозе света ингибирование синтеза белка примерно в 3 раза сильнее в случае стратегии "свет раньше", чем в случае стратегии "свет позже". Можно также видеть, что в обеих клеточных линиях гелонин сам по себе не оказывает токсического воздействия без ФХИ обработки, указывая на активность и специфичность индукции эффекта токсина, достигаемой в процессе фотохимической обработки.
Пример 13
Фотохимическая стимуляция опосредованной аденовирусом трансдукции гена
5х104 THX клеток на ячейку высевают в 6-ячеечные планшеты. На следующий день добавляют 20 мкг/мл ALPcS2a и клетки инкубируют в течение 18 часов при 37°С. Все процедуры после добавления ALPcS2a проводят при затемненном свете. В случае стратегии "свет раньше" клетки отмывают от ALPcS2a и инкубируют в среде без ALPcS2a в течение 4 часов. Затем клетки подвергают воздействию света в течение 3 минут перед обработкой аденовирусным вектором AdHCMV-lacZ (также называемым в примере 10 как AdCA17lacZ) с множественностью инфекции 1 в течение 30 минут. Данный вектор содержит репортерный ген β-галактозидазы, экспрессия которого может быть определена методу проточной цитометрии (см. ниже).
В случае стратегии "свет позже" обработанные ALPcS2a и промытые клетки вначале обрабатывают аденовирусом в той же концентрации и в то же время, как указано выше, промывают и после добавления свежей культуральной среды выставляют на свет. Неосвещенные клетки промывают аналогичным образом, за исключением процедуры освещения.
Обработанные клетки промывают один раз культуральной средой и после добавления свежей среды инкубируют при 37°С перед проведением анализа. Экспрессию β-галактозидазы анализируют методом проточной цитометрии через два дня после световой экспозиции. В примере 10 описаны подробные методики конструирования вируса (который называют как AdHCMV-lacZ или как AdCA17lacZ), обработки клеток, освещения и анализа β-галактозидазы.
Результаты (фиг.14) показывают, что описанная фотохимическая обработка с использованием процедуры "свет раньше" (показанная в виде прямоугольников справа на фиг.14) повышает процент β-галактозидаза-экспрессирующих клеток примерно в 6 раз; в указанных экспериментальных условиях от 2,5% до 15%. Можно также видеть, что эффект использования процедуры "свет раньше" практически равен таковому, полученному по способу "свет позже" (показан в виде прямоугольников слева на фиг.14).
Пример 14
Влияние времени инкубации на эффективность индуцированной светом трансфекции
5х104 THX клеток или 7,5х104 HCT 116 на ячейку высевают в 6-ячеечные и 12-ячеечные планшеты, соответственно. На следующий день добавляют 20 мкг/мл ALPcS2a и клетки инкубируют в течение 18 часов при 37°С. Все процедуры после добавления ALPcS2a проводят в затемненном свете. Клетки отмывают от ALPcS2a и инкубируют в среде без ALPcS2a в течение 4 часов. Затем клетки подвергают воздействию света (3 минуты в случае THX клеток и 7 минут в случае HCT 116 клеток) перед обработкой pEGFP-N1/полилизиновым (5 мкг/мл pEGFP-N1) комплексом в периоды времени, указанные на фиг.15. Аналогично обрабатывают неосвещенные клетки, за исключением процедуры освещения. Обработанные клетки промывают один раз культуральной средой и после добавления свежей среды проводят инкубацию при 37°С в течение 2 дней перед проведением анализа на экспрессию EGFP методом проточной цитометрии (см. раздел "Материалы и методы"). Освещение обеспечивают при помощи панелей с четырьмя световыми трубками (Philips, TL 20W/09) и длинноволновым фильтром, который отсекает диапазон 550-600 нм. Интенсивность света при достижении клеток составляет 13,5 Вт/м2. pEGFP-N1/Полилизиновый комплекс (коэффициент нагрузки 1,7) получают при осторожном смешивании плазмиды и растворов полилизина, приготовленных отдельно: 5 мкг плазмиды pEGFP-N1 разбавляют 75 мкл воды и 5,3 мкг полилизина разбавляют 75 мкл воды. Далее растворы смешивают и инкубируют в течение 30 минут при комнатной температуре, разбавляют культуральной средой до 1 мл и добавляют к клеткам.
Результаты (фиг.15) показывают, что и в THX, и в HCT-116 клетках трансфекция ДНК/полилизиновыми комплексами может быть сильно индуцирована посредством фотохимической обработки по стратегии "свет раньше". Можно также видеть, что стимуляция трансфекции становится эффективной уже после непродолжительных периодов инкубации с ДНК, по меньшей мере до 30 минут инкубации. Индуцированная светом трансфекция повышается с увеличением времени инкубации, однако, как видно, начинает снижаться примерно к 2 часам инкубации с ДНК.
Пример 15
Влияние световой обработки по первой стратегии ФХИ на трансфекцию THX клеток, опосредованную поли-L-лизином, с использованием TPPS2a в качестве фотосенсибилизатора
Тетрафенилфосфиндисульфонат (TPPS2a), лот № 04197, получают от компании Porphyrin Products (UT, США). TPPS2a растворяют в ДМСО.
Плазмиды pEGFP-N1 приобретают от компании Clontech Laboratories Inc. (CA, США; Cat. no. 6085-1). Используемую в эксперименте партию продукта (lot# EGFP-N1-1002) получают от компании ELIM Biophatmaceuticals, Inc. (CA, США) и используют в концентрации 5 мг/мл в стерильной воде для целей доставки. Готовят раствор для хранения (0,5 мг/мл) в стерильном ТЕ-буфере, pH 7,4 (1 мМ Tris-HCl, 1 мМ ЭДТА) и хранят при температуре -20°С.
THX клетки меланомы человека культивируют в среде RPMI 1640 с добавкой 10% ФСТ (фетальная сыворотка теленка), пенициллина/стрептомицина и L-глютамина. При затемненном свете среду удаляют и добавляют среду, содержащую 2 мкг/мл TPPS2a.. Клетки (защищенные от света) инкубируют при 37°С в течение 18 часов. Затем клетки промывают три раза средой, в образцы PLL-L ("свет после") добавляют 1 мл среды, содержащей pEGFP-N1/поли-L-лизиновый комплекс. Комплекс содержит 5 мкг pEGFP-N1 и характеризуется коэффициентом соотношения поли-L-лизина (PLL) к ДНК, равным 1,7. После дальнейшей 4-часовой инкубации при 37°С в темноте среду удаляют и клетки промывают один раз средой. Добавляют 1 мл среды и клетки подвергают экспозиции голубым светом, как указано на фиг.16, и как описано в разделе "Материалы и методы". В случае L-PLL образцов ("свет раньше") первые 4 часа инкубации проводят в среде без pEGFP-N1/PLL комплекса, указанный комплекс добавляют сразу же после освещения и удаляют через 4 часа после инкубации. Клетки инкубируют в течение 2 дней (все еще в защищенном от света состоянии) перед проведением анализа на экспрессию EGFP методом проточной цитометрии. Для проведения данного анализа клетки обрабатывают трипсином (трипсин-ЭДТА, Sigma, MO, США) ресуспендируют в 400 мкл RPMI и фильтруют через нейлоновый фильтр с ячейками 50 мкм с последующим проведением анализа на проточном цитометре FACSCalibur (Becton, Dickinson, CA, США). Уровень EGFP промеряют с использованием фильтра на 510-5410 нм после возбуждения с длиной волны 488 нм. Используют иодид пропидия (1 мкг/мл) для отделения мертвых клеток от жизнеспособных и проводят пульсовую обработку для отделения клеточных дуплетов от одиночных клеток. Для каждого образца проводят 10000 определений и полученные данные обрабатывают с использованием программного обеспечения CELLQuest Software (Becton, Dickinson, CA, США).
Результаты
Как видно на фиг.16, в случае поли-L-лизин-опосредованной трансфекции THX клеток по стратегии "свет раньше" процедура добавления переносимой молекулы срабатывает так же хорошо, как и в случае подхода "свет после", когда используют фотосенсибилизатор TPPS2a.
Пример 16
Влияние световой обработки по первой стратегии ФХИ на трансфекцию THX клеток, опосредованную поли-L-лизином, с использованием TPPS2а в качестве фотосенсибилизатора
THX клетки растят и обрабатывают как описано в примере 15, за исключением того, что используют фотосенсибилизатор TPPS4 (75 мкг/мл) вместо TPPS2а.
Результаты
Из фиг.17 следует, что поли-L-лизин-опосредованная трансфекция THX клеток по методу "свет раньше" работает несколько лучше, чем подход "свет после" при использовании фотосенсибилизатора TPPS4, хотя оба метода приводят к достижению трансфекции.
Пример 17
Влияние световой обработки по первой стратегии ФХИ на трансфекцию, опосредованную поли-L-лизином, HCT 116 клеток с использованием TPPS2а в качестве фотосенсибилизатора
HCT 116 клетки растят и обрабатывают, как было описано в примере 15. Результаты
Из фиг.18 видно, что опосредованная поли-L-лизином трансфекция HCT 116 клеток по методу "свет раньше" работает так же хорошо, как и стратегия "свет после" при использовании фотосенсибилизатора TPPS2а в качестве фотосенсибилизатора.
Пример 18
Влияние световой обработки по первой стратегии ФХИ на трансфекцию HCT 116 клеток, опосредованную поли-L-лизином, с использованием TPPS4 в качестве фотосенсибилизатора
THX клетки растят и обрабатывают, как было описано в примере 15, за исключением того, что используют фотосенсибилизатор TPPS4 (75 мкг/мл) вместо TPPS2а.
Результаты
На фиг.19 показано, что опосредованная поли-L-лизином трансфекция THX клеток по методу "свет раньше" работает так же хорошо, как и стратегия "свет после" при использовании в качестве фотосенсибилизатора TPPS4.
Пример 19
Влияние световой обработки по первой стратегии ФХИ на трансфекцию, опосредованную ДОТАП, с использованием TPPS4 в качестве фотосенсибилизатора
HCT 116 клетки культивируют в среде RPMI 1640 с добавлением 10% ФСТ (фетальная сыворотка теленка), пенициллина/стрептомицина и L-глютамина. В затемненном свете среду удаляют и добавляют среду, содержащую 75 мкг/мл TPPS4. Клетки (защищенные от света) инкубируют при 37°С в течение 18 часов. Затем клетки промывают три раза средой, и в случае образцов ДОТАП-L ("свет после") добавляют 1 мл среды, содержащей комплекс 1 мкг pEGFP-N1 и 5 мкг ДОТАП. Далее после 4-часовой инкубации при 37°С в темноте среду удаляют и клетки промывают один раз средой. Добавляют 1 мл среды и клетки подвергают воздействию синего света, как указано на фиг.20 и как описано в разделе "Материалы и методы". В случае образцов L-ДОТАП ("свет раньше") первые 4 часа инкубации проводят в среде без комплекса pEGFP-N1/ДОТАП, а указанный комплекс добавляют сразу же после освещения и удаляют после 4-часовой инкубации. Клетки инкубируют в течение 1 дня (все еще в защищенном от света состоянии) перед проведением анализа на экспрессию EGFP методом проточной цитометрии, как описано в примере 15.
Результаты
Из фиг.20 можно видеть, что трансфекция HCT 116, опосредованная катионным липидом ДОТАП, по методу "свет раньше" работает значительно лучше, чем стратегия "свет после" в случае использования TPPS4, в качестве фотосенсибилизатора. Стратегия "свет раньше" будет, по всей видимости, особенно выгодна для трансфекции, опосредованной катионными липидами.
Пример 20
Влияние световой обработки по первой стратегии ФХИ на трансфекцию, опосредованную SuperFect®, с использованием TPPS2а в качестве фотосенсибилизатора
SuperFect® приобретают от компании QIAGEN AG.
Приготовление комплексов плазмида/SuperFect®
Комплексы плазмида/SuperFect® готовят следующим образом: (i) pEGFP-N1 разбавляют средой RPMI 1640 (без сыворотки, белков и антибиотиков); (ii) добавляют SuperFect® к раствору плазмиды (2 мкл на мкг ДНК) и содержимое перемешивают в вихревом смесителе в течение 10 секунд; (iii) раствор инкубируют в течение 10-20 минут при комнатной температуре для содействия образованию комплекса; (iv) 400 мкл среды роста для клеток (с сывороткой и антибиотиками) добавляют к пробиркам, содержащим трансфицирующие комплексы, содержимое перемешивают два раза с помощью пипетки и весь объем сразу же переносят в клетки.
Обработка клеток
HCT 116 клетки (75000 клеток/ячейку, 1 мл/ячейку) высевают на 12-ячеечные планшеты (Coster Corning, NY, USA) и оставляют их для прикрепления на шесть часов. Добавляют 1 мл среды с содержанием 0,7 мкг/мл TPPS2а и клетки инкубируют в течение 18 часов (5 об.% CO2, 37°C). Клетки промывают три раза средой и инкубируют в течение 4 часов (37°С, 5 об.%) в бессывороточной среде. Клетки освещают с помощью панели из четырех флуоресцирующих трубок (Osram 18W/67) с максимумом около 420 нм. Добавляют комплексы плазмида/SuperFect® сразу же после экспозиции светом и клетки инкубируют с указанными комплексами в течение 1 или 4 часов. Затем клетки промывают 4 раза в RPMI среде и после добавления 1 мл среды инкубируют еще в течение 2 дней. Далее проводят анализ на экспрессию EGFP методом поточной цитометрии, как описано в примере 15.
Результаты
Как можно видеть из фиг.21, ФХИ значительно улучшает трансфекцию SuperFect® во всех исследованных условиях. Так, например, в случае использования 0,75 мкг ДНК и времени трансфекции 1 час может отмечаться 9-кратное усиление, тогда как в случае 0,75 мкг ДНК и времени трансфекции 4 часа наблюдается 10-кратное усиление.
Пример 21
Влияние световой обработки по первой стратегии ФХИ на опосредованную аденовирусом трансдукцию гена в клетки HCT 116 с использованием TPPS2a в качестве фотосенсибилизатора
Клетки HCT 16 культивируют в среде RPMI с добавлением 10% ФСТ (фетальная сыворотка теленка), пенициллина/стрептомицина и L-глутамина. При затемненном свете среду удаляют и к каждой ячейке добавляют среду, содержащую 1 мкг/мл TPPS2a. Клетки (защищенные от света) инкубируют при 37°С в течение 18 часов, далее клетки промывают три раза средой. После этого клетки инфицируют аденовирусом Ad-HCMV-LacZ в разные временные точки до или после освещения (что каждый раз составляет период в 4 часа после удаления фотосенсибилизатора). Клетки инкубируют далее в течение 2 дней (все еще в защищенном от света состоянии) перед проведением анализа на активность β-галактозидазы методом проточной цитометрии, как описано в примере 10 (раздел "Материалы и методы").
Результаты
Фиг.22 иллюстрирует влияние времени световой обработки с точки зрения доставки вируса на эффект ФХИ при проведении трансдукции гена, опосредованной аденовирусом. Можно видеть, что в случае стратегии "свет раньше" (правая сторона на оси Y) освещение при проведении ФХИ эффективно по меньшей мере в течение 13 часов, так что вирус может быть введен вплоть до момента 13 часов после освещения, и при этом все еще будет сохраняться позитивный эффект ФХИ на трансдукцию. С клинической точки зрения это очень важно, поскольку дает клиницистам большую гибкость в разработке методики лечения и координировании ее с другими видами лечения, которые могут требоваться пациенту, например, с хирургическими процедурами.
Пример 22
Влияние световой обработки по первой стратегии ФХИ на опосредованную поли-D-лизином трансфекцию HCT 116 клеток с использованием AlPcS2a в качестве фотосенсибилизатора
Клетки HCT 16 выращивают, обрабатывают и анализируют, как описано в примере 15, за исключением того, что используют поли-D-лизин вместо поли-L-лизина при изготовлении комплекса с pEGFP-N1.
Результаты
Фиг.23 показывает, что ФХИ по методу "свет раньше" работает также хорошо, когда используют поликатион поли-D-лизин в качестве агента для трансфекции.
Пример 23
Влияние световой обработки по первой стратегии ФХИ на уничтожение клеток цитостатическим средством блеомицин с использованием TPPS2a в качестве фотосенсибилизатора
Дисульфонат тетрафенилпорфина (TPPS2a), лот #04197, получают от компании Porphyrin Products (UT, США). TPPS2а растворяют в DMSO.
В данном исследовании используют линию фибробластов легкого китайского хомячка V-79. MTT (3-[4,5-диметилтиазол-2-ил]-2,5-дифенилтетразолия бромид) получают от компании Сигма (Sigma, MO, США; cat. No. M 2128), растворяют в ФБР до концентрации 5 мг/мл, стерилизуют фильтрованием и хранят при 4°С.
Блеомицин (ASTA Medica) 15000 МЕ/KY получают из аптеки при Норвежском радиологическом госпитале.1 МЕ соответствует 1 мг блеомицина. Порошок блеомицина растворяют в стерильном 0,9% растворе NaCl до конечной концентрации 2 мМ.
Культивирование клеток
Клетки V-79 культивируют в среде RPMI 1640 (Gibco) с добавкой 10% фетальной сыворотки теленка, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 2 мМ глютамина (все препараты Gibco BRL, Paisley, Шотландия) при 37°С и 5% CO2 во влажной среде.
Обработка клеток
Клетки (75000 клеток/ячейку, 1 мл/ячейку) высевают в 12-ячеечные планшеты (Costar Corning, NY, США) и оставляют для прикрепления на 6 часов. К некоторым ячейкам добавляют 1 мл среды с содержанием 0,7 мкг/мл TPPS2а (см. Таблицу 1) и клетки инкубируют в течение 18 часов (5 объемн.% CO2, 37°C). Клетки промывают три раза средой. Затем клетки инкубируют в среде, содержащей сыворотку, в течение 4 часов. Далее среду удаляют, добавляют новую среду и клетки освещают с использованием панели, содержащей устройство из 4 флуоресцентных трубок (Osram, 18W/67) с максимумом около 420 нм.
Сразу же добавляют различные дозы блеомицина. После 1-часовой или 4-часовой инкубации с блеомицином клетки промывают один раз средой RPMI, добавляют 1 мл среды и после 3-дневной инкубации измеряют уровень выживания клеток по методу МТТ. Указанный метод основан на восстановлении водорастворимой тетразолиевой соли (МТТ) до фиолетового нерастворимого формазанового продукта под действием митохондриальных дегидрогеназ, присутствующих в живых метаболически активных клетках. Один мл среды, содержащей 0,25 мкг МТТ, добавляют к клеткам, проводят 4-часовую инкубацию (37°C, 5 об.% CO2). Полученные формазановые кристаллы растворяют при добавлении по 200 мкл изопропанола (Sigma, MO, США) на ячейку. Раствор переносят на 96-ячеечный планшет, который промеряют на счетчике для микропланшетов Multiscan EX (Labsystems, Финляндия) с использованием фильтра с полосой пропускания при 570 нм. Уровень выживших клеток подсчитывают как процент от контрольных клеток, не получавших световой обработки.
Результаты
Фиг.24 показывает, что ФХИ по методу "свет раньше" может также увеличивать биологический эффект низкомолекулярного, клинически утвержденного химиотерапевтического средства (блеомицина). Так, можно видеть, что в случае 100 мкМ дозы блеомицина наблюдается значительное светоиндуцированное увеличение цитотоксичности блеомицина (▪ и ● фиг.24). Отсутствие эффекта при наименьшей дозе блеомицина (▾ на фиг.24) показывает, что такая повышенная цитотоксичность не является результатом фотохимической обработки per se, поскольку данная серия образцов подвергалась той же процедуре химической обработки, что и серия с 100 мкМ блеомицина без видимого светоиндуцированного эффекта на выживаемость клеток.
Пример 24
Использование ФХИ с гелонином для обработки опухолей на модели in vivo у мышей
Животные
Самок мышей Balb/c (nu/nu) nude растят в виварии Института исследования рака. Мышей выдерживают в специфических условиях без патогена. Воду и пищу дают ad libitum. Все процедуры на мышах проводят по методике, одобренной Комитетом по защите животных при Норвежском радиологическом госпитале под контролем Национального этического комитета по защите животных. Мыши имеют средний вес 20-25 г (возраст 5-8 недель) в начале эксперимента и авторы использовали по меньшей мере 5 мышей для каждой экспериментальной группы. В данном исследовании используют аденокарциному человека WiDr, которую размножают путем серийной трансплантации в мышах Balb/c (nu/nu). Опухоли разминают до гомогенности скальпелем и в правое бедро каждой мыши инъецируют подкожно 20 мкл раствора. Размер опухоли определяют два или три раза в неделю при измерении двух перпендикулярных диаметров. Объем опухоли подсчитывают по следующей формуле:
V=(W2xL)/2
где W обозначает ширину и L обозначает диаметр в длину измеряемой опухоли.
Обработка
Мышей распределяют случайным образом на различные группы, как указано в Таблице 1 и фиг.25. Раствор для хранения ALPcS2a разбавляют до концентрации 1,25 мг/мл в ФБР и инъецируют внутрибрюшинно до конечной концентрации 10 мг/кг, как только опухоли достигнут объема 100 мм3. Через 48 часов после инъекции ALPcS2a опухоли подвергают воздействию красного света в течение 16 минут (см. ниже). Сразу же после световой экспозиции внутрь опухоли инъецируют гелонин (общее количество 50 мкг в растворе с концентрацией 2 мг/мл, то есть 25 мкл). Мышей выдерживают в темноте в течение одной недели после инъекции ALPcS2a.
Световая обработка
Опухоли освещают галогеновой лампой в 150 Ватт (Xenophot HLX64640), снабженной фильтром на 580-700 нм и эмиссией 150 мВт/см2. Животных накрывают алюминиевой фольгой, за исключением области над опухолью, и делают отверстие в фольге диаметром на 2 мм больше, чем диаметр опухоли. Опухоли подвергают воздействию света в 145 Дж/см2. Объемы опухолей измеряют два или три раза в неделю, как описано выше. Мышей забивают, как только опухоли достигнут диаметра примерно 20 мм. Через 30 дней после освещения определяют долю мышей без опухолей и соответствующим образом ранжируют полученные результаты (Таблица 1) и записывают средний объем опухоли в каждой группе (фиг.25).
Результаты
Из Таблицы 1 можно видеть, что ФХИ с гелонином по способу "свет раньше" (группа 8) приводит к излечивания 80% мышей (4 из 5) от опухолей. И наоборот, один гелонин не оказывает эффекта ни в сочетании (группа 4), ни без дополнительной световой обработки (группа 3) (без ALPcS2a). Гелонин в сочетании с ALPcS2a без световой обработки (группа 6) не демонстрирует какого-либо эффекта. Низкий уровень излечивания отмечался у необработанных животных (группа 1), что, вероятно, связано со спонтанным исчезновением опухоли. Низкий уровень излечивания может также наблюдаться у животных, получающих ALPcS2a и световую обработку (группа 7), в связи с эффектом фотодинамической терапии (ФДТ), который не зависит от наличия гелонина. Однако данный эффект ФДТ (18% излечивания) значительно ниже, чем эффект, обнаруженный при ФХИ обработке с гелонином (80%, группа 8). Поскольку гелонин сам по себе не оказывает эффекта, то высокий уровень излечивания в ФХИ группе не может быть объяснен аддитивным эффектом ФДТ и гелонина, но должен быть связан с синергическим эффектом, при котором ФХИ обработка реализует токсический потенциал гелонина.
Фиг.25 показывает эффект ФХИ обработки на средний объем опухоли в некоторых группах, подвергавшихся лечению. Можно также видеть, что в группе животных, получавших только гелонин (▴), опухоли вырастали так же быстро, как и у животных, получавших плацебо в виде инъекции фосфатно-буферного раствора (ФБР) в сочетании с процедурой освещения (▪). У животных, получавших только фотохимическое лечение, но без гелонина ( ) рост опухоли замедлялся, однако примерно через 15 дней после освещения рост опухоли возобновлялся. И наоборот, у животных, получавших полный курс лечения гелонином в сочетании с ФХИ обработкой (●), не отмечалось увеличения среднего объема опухоли даже через 33 дня после освещения.
) рост опухоли замедлялся, однако примерно через 15 дней после освещения рост опухоли возобновлялся. И наоборот, у животных, получавших полный курс лечения гелонином в сочетании с ФХИ обработкой (●), не отмечалось увеличения среднего объема опухоли даже через 33 дня после освещения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ | 2002 |
|
RU2323940C2 |
| ФОТОСЕНСИБИЛИЗИРУЮЩИЕ КОМПОЗИЦИИ | 2010 |
|
RU2574019C2 |
| КОНЪЮГАТ ФОТОСЕНСИБИЛИЗАТОРА И ХИТОЗАНА И ЕГО ПРИМЕНЕНИЕ | 2013 |
|
RU2675830C2 |
| СПОСОБ ВВЕДЕНИЯ МОЛЕКУЛЫ ПНК, КОНЪЮГИРОВАННОЙ С ПОЛОЖИТЕЛЬНО ЗАРЯЖЕННЫМ ПЕПТИДОМ, В ЦИТОЗОЛЬ И/ИЛИ ЯДРО ФОТОХИМИЧЕСКОЙ ИНТЕРНАЛИЗАЦИЕЙ(PCI) | 2005 |
|
RU2435859C2 |
| ФОТОХИМИЧЕСКАЯ ИНТЕРНАЛИЗАЦИЯ ДЛЯ ОПОСРЕДОВАННОЙ ВИРУСОМ ДОСТАВКИ МОЛЕКУЛЫ В ЦИТОЗОЛЬ | 2001 |
|
RU2317827C2 |
| СПОСОБ ВВЕДЕНИЯ siRNA В КЛЕТКИ ФОТОХИМИЧЕСКОЙ ИНТЕРНАЛИЗАЦИЕЙ | 2007 |
|
RU2510826C2 |
| ФОТОХИМИОТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1998 |
|
RU2194532C2 |
| ПРЕПАРАТИВНЫЕ ФОРМЫ, СОДЕРЖАЩИЕ НЕПОЛЯРНЫЕ ФОТОСЕНСИБИЛИЗАТОРЫ, ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2004 |
|
RU2343904C2 |
| Фотосенсибилизатор на основе карбоцианинового красителя для фотодинамической терапии опухолей | 2016 |
|
RU2638131C1 |
| КОМПОЗИЦИЯ ДЛЯ ФОТОДИНАМИЧЕСКОГО ПОВРЕЖДЕНИЯ КЛЕТОК-МИШЕНЕЙ И СПОСОБ ФОТОДИНАМИЧЕСКОГО ПОВРЕЖДЕНИЯ КЛЕТОК-МИШЕНЕЙ | 1996 |
|
RU2066552C1 |
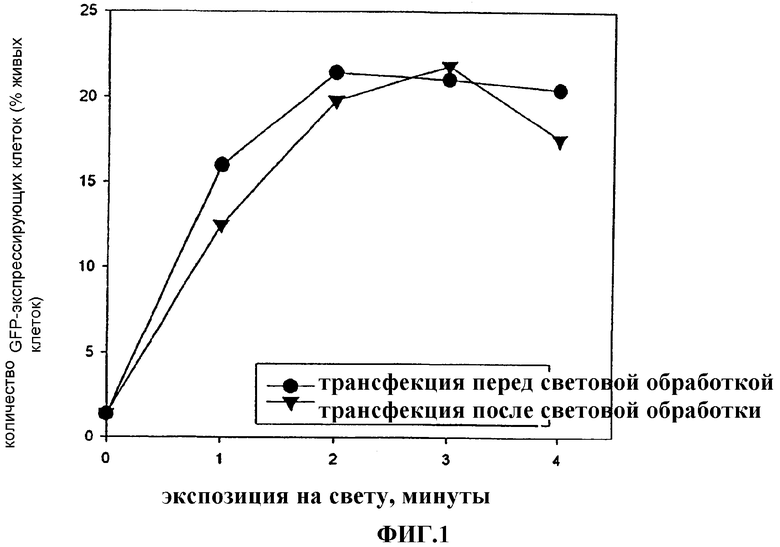
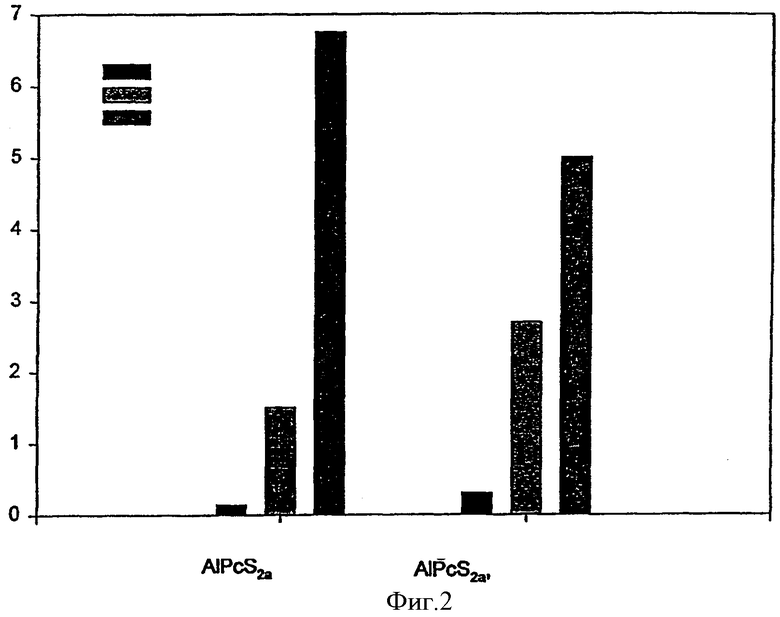
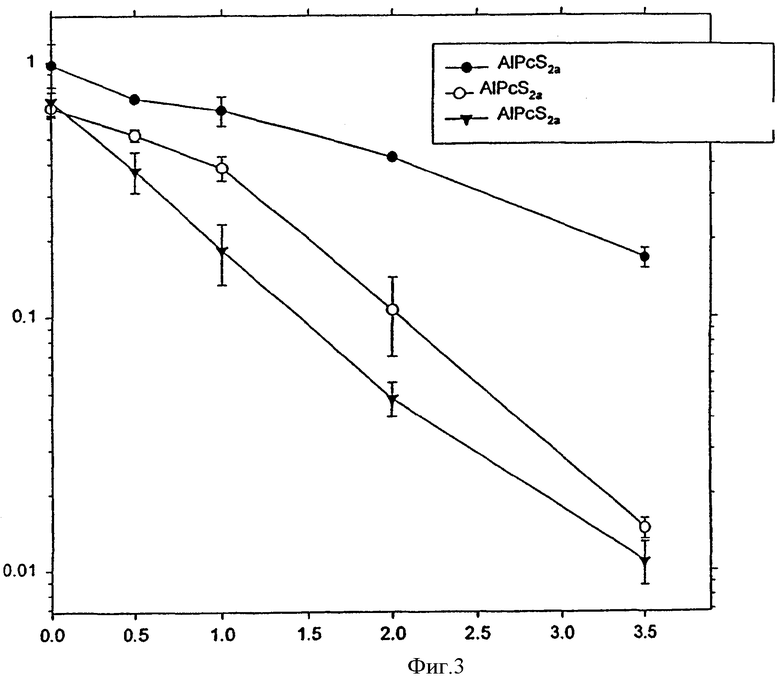
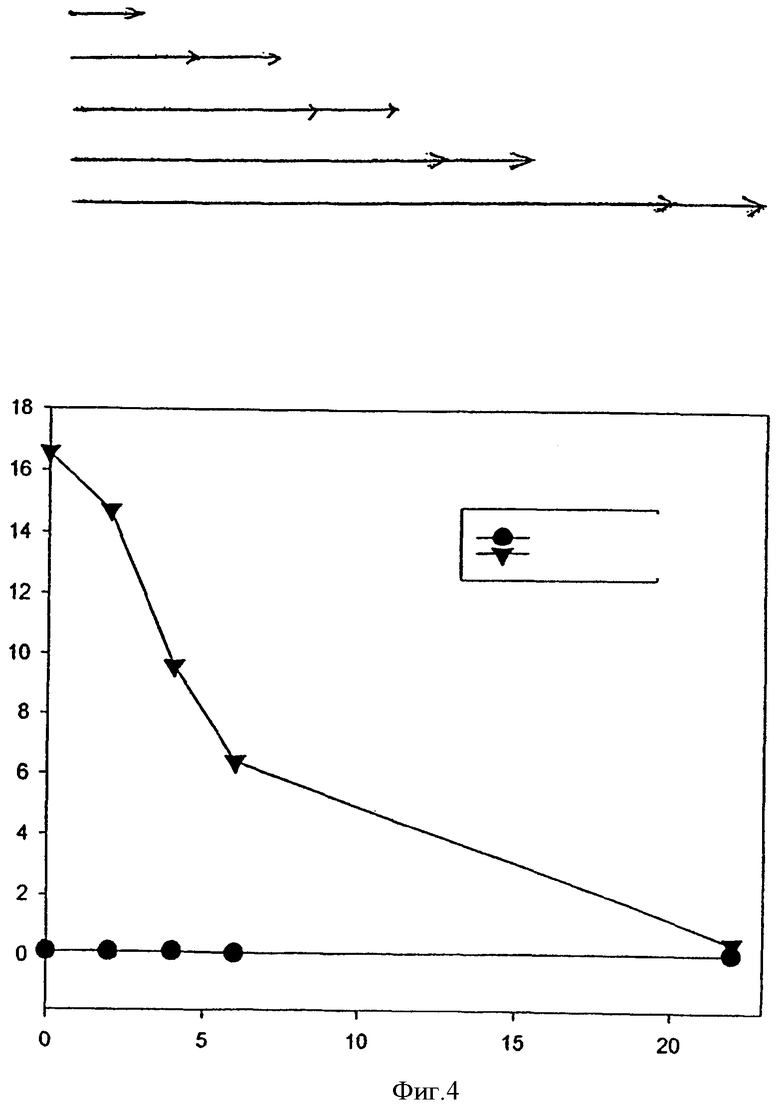
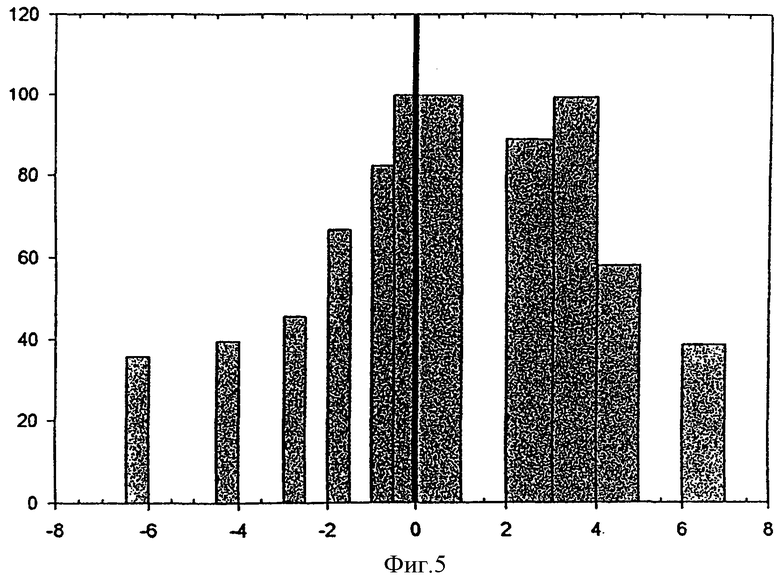
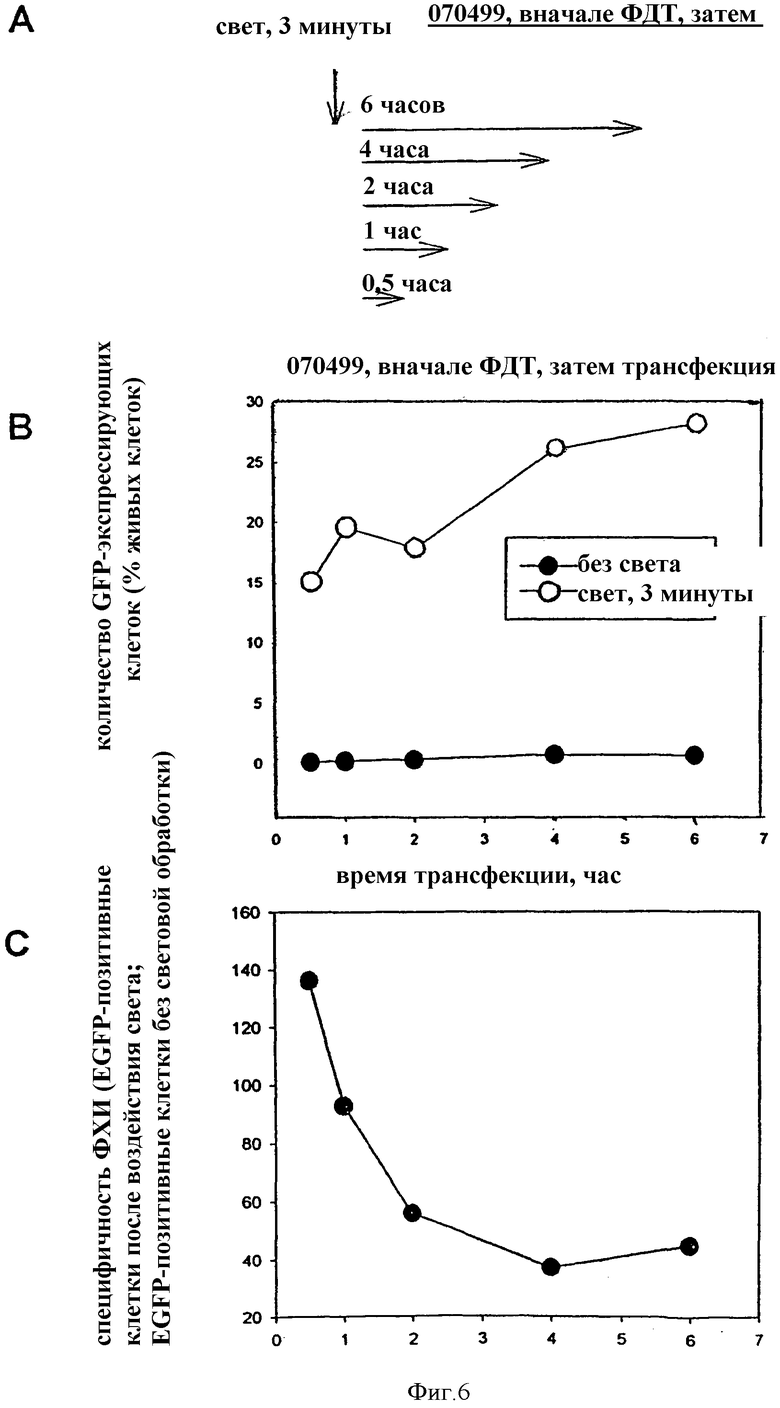
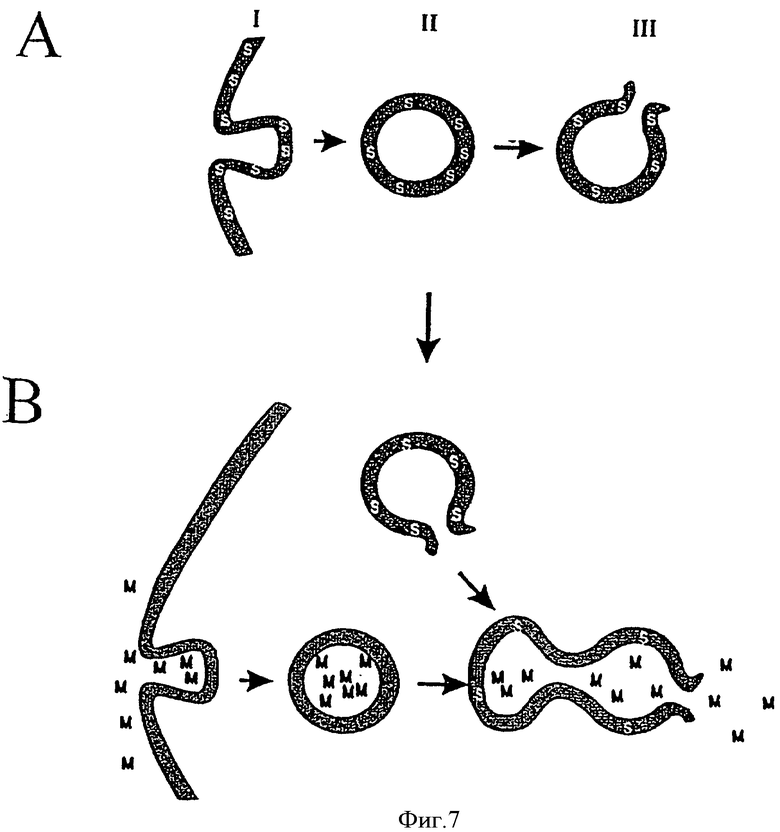
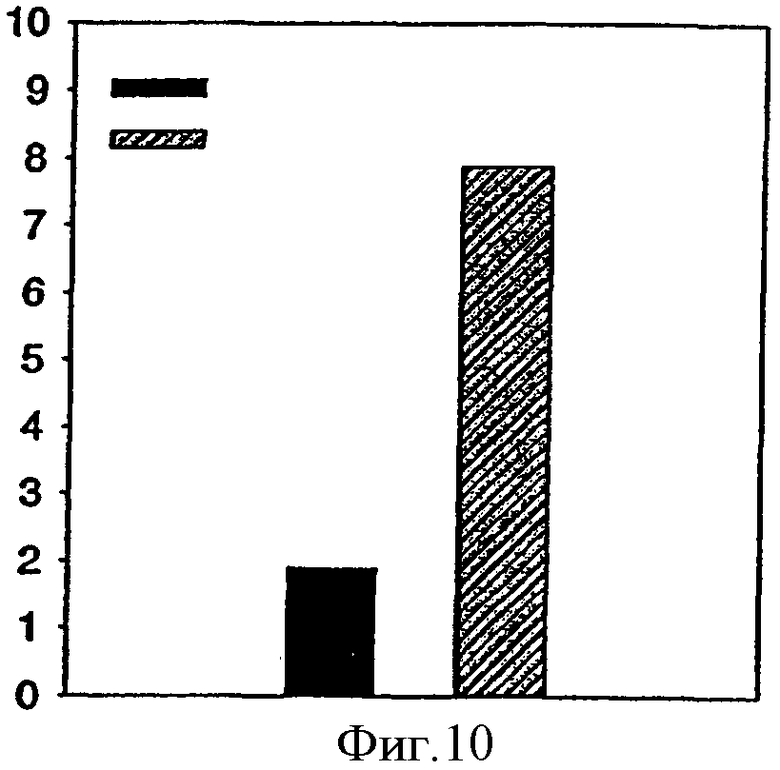
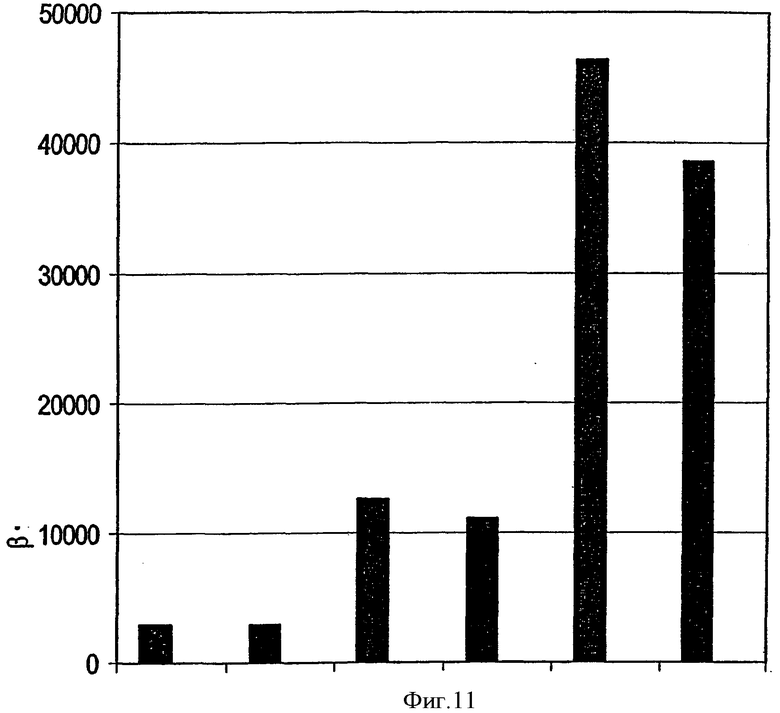
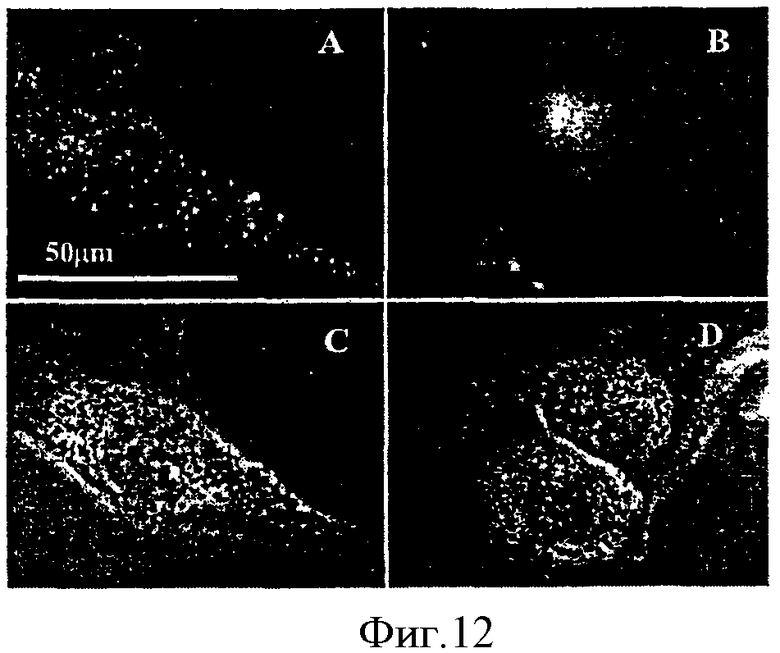
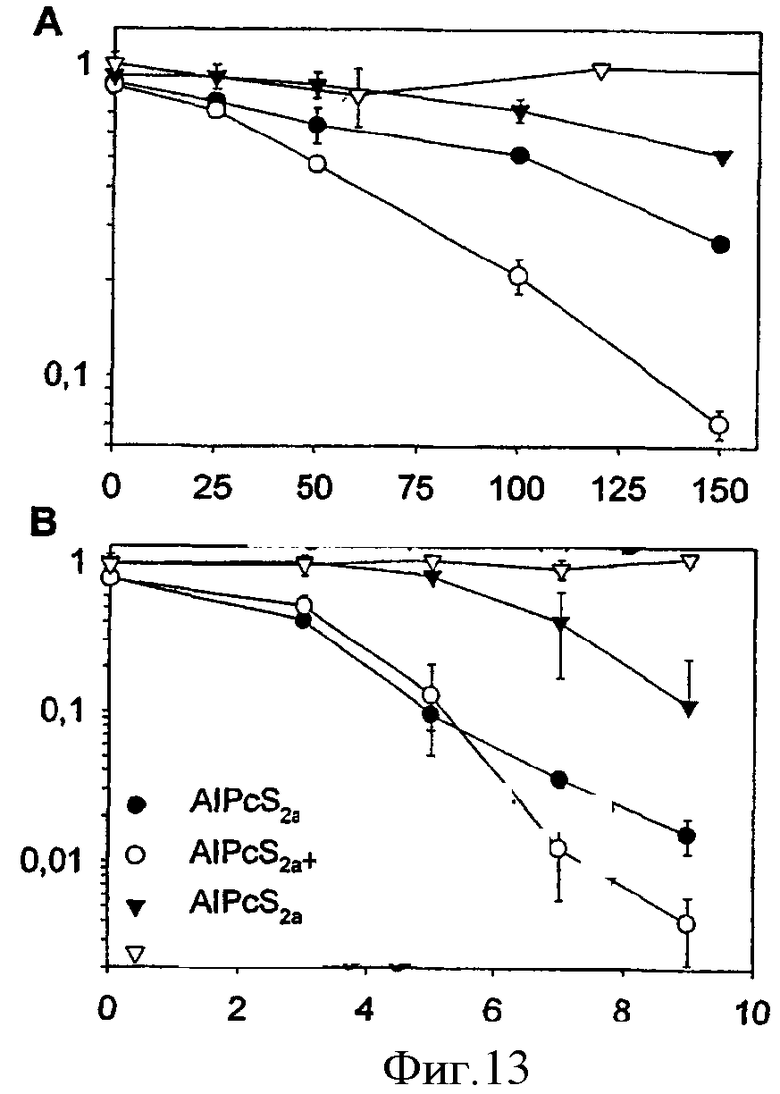
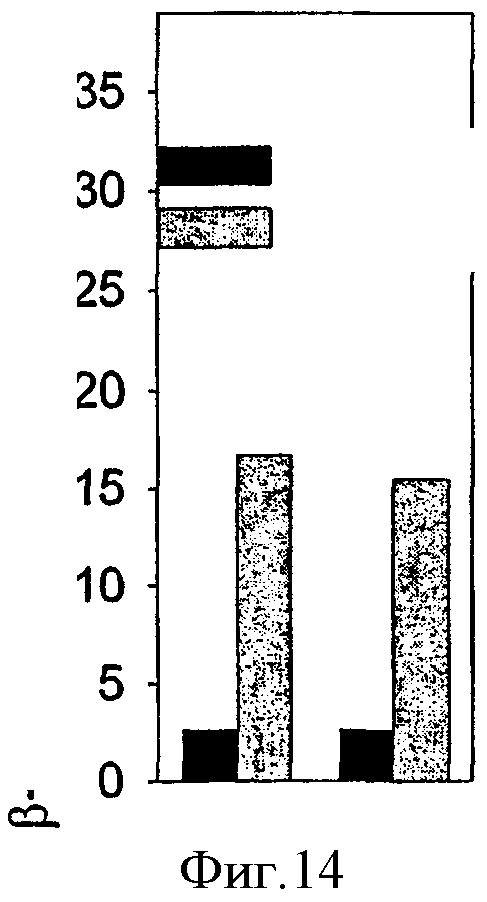
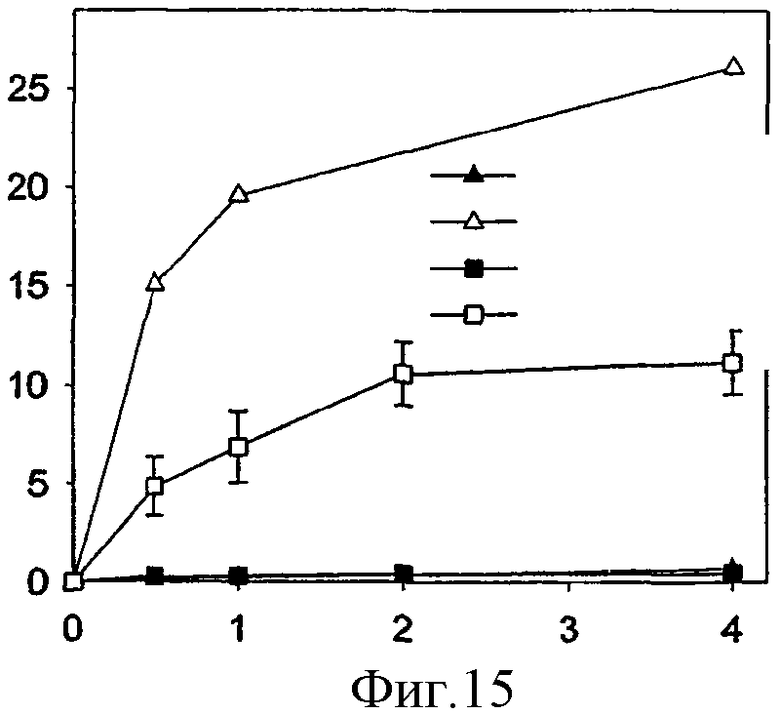
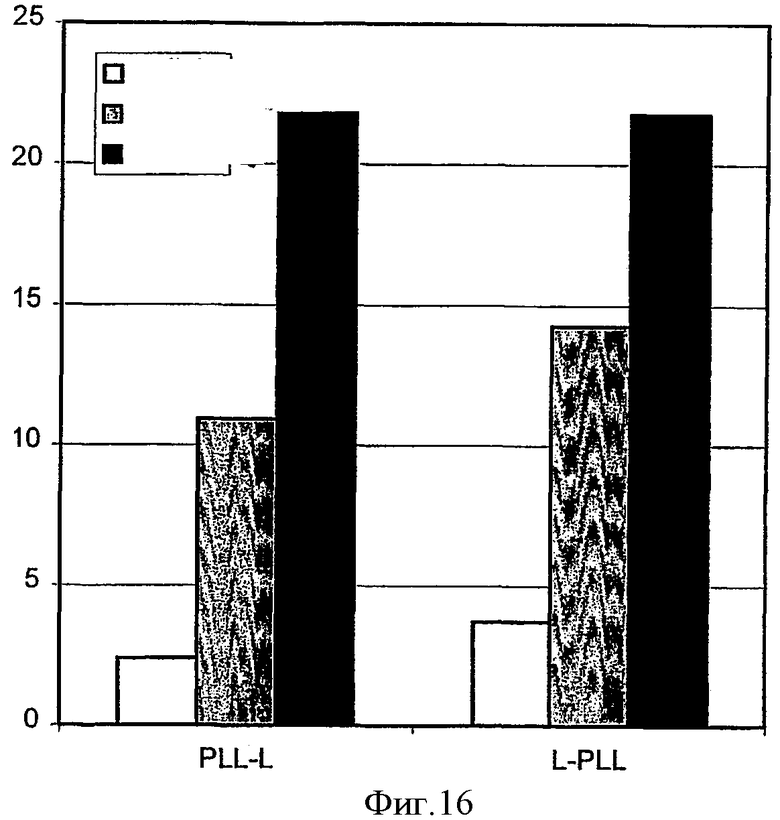
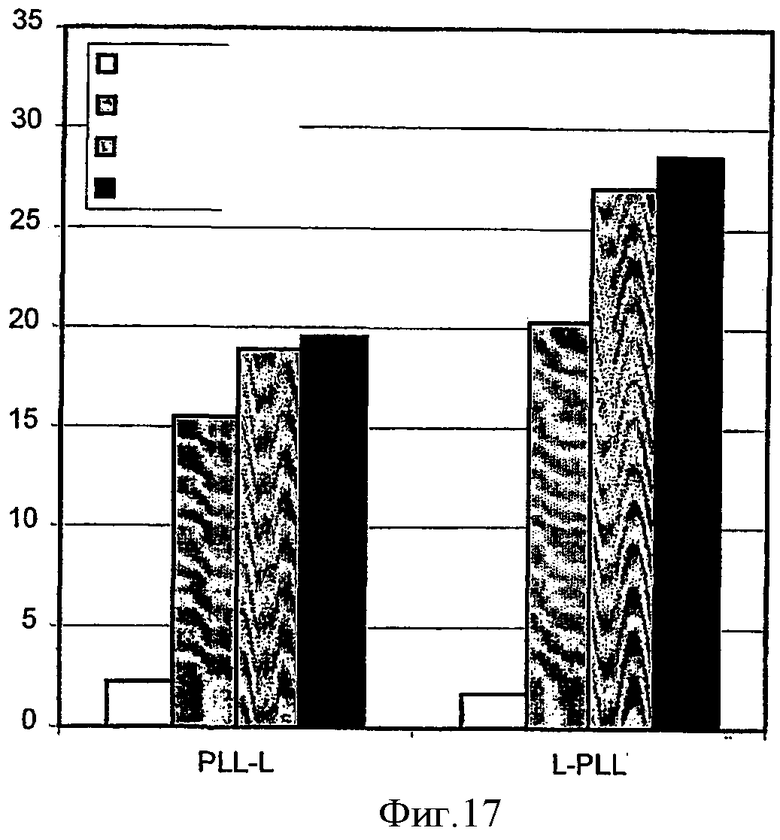
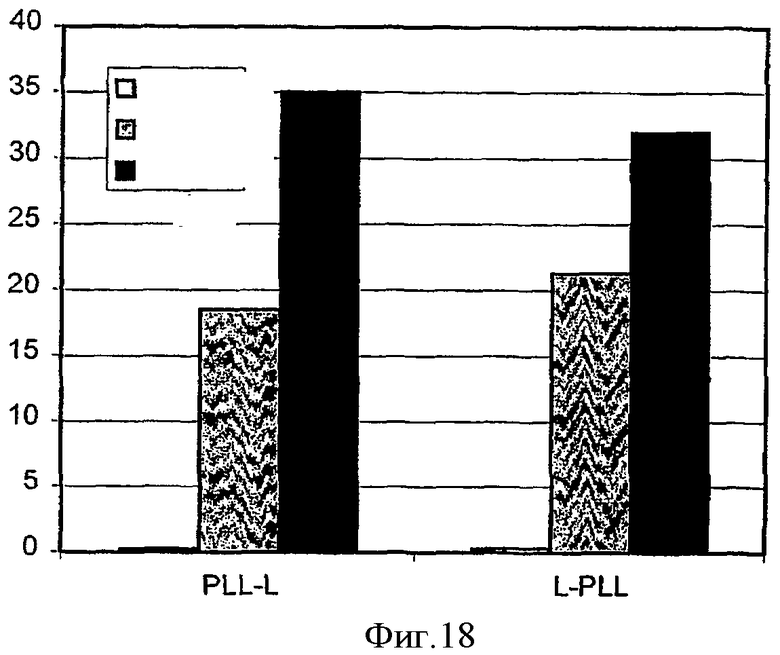

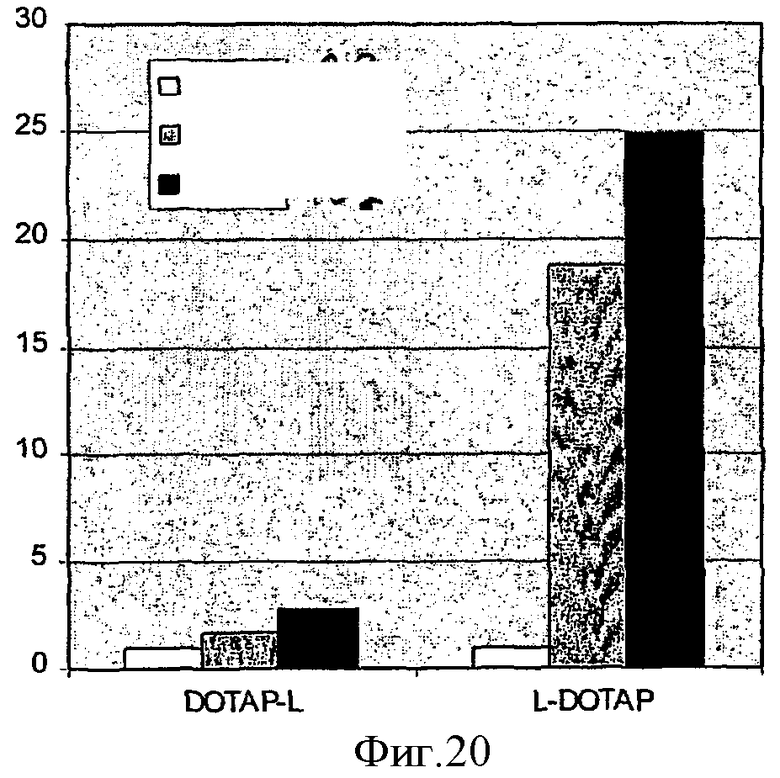
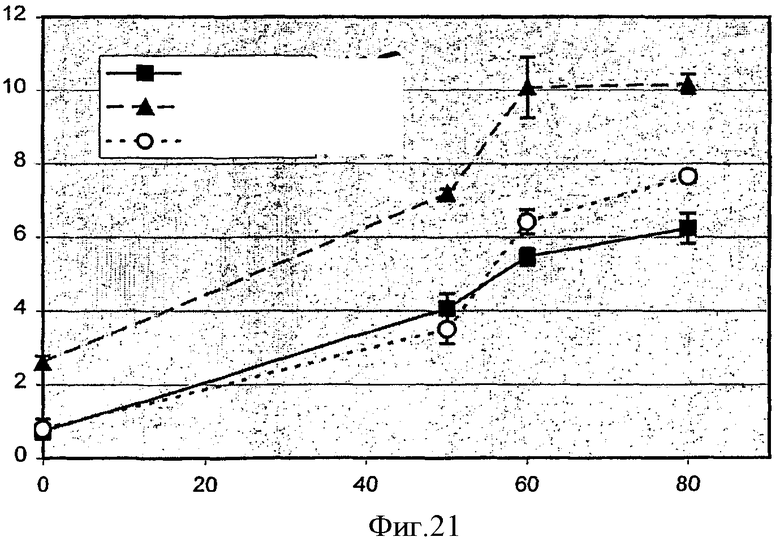
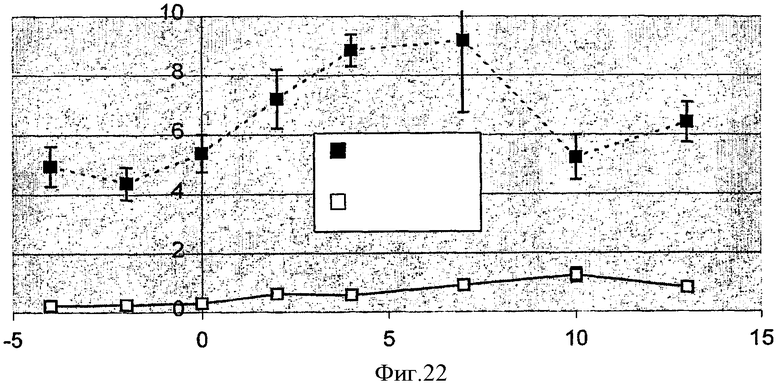
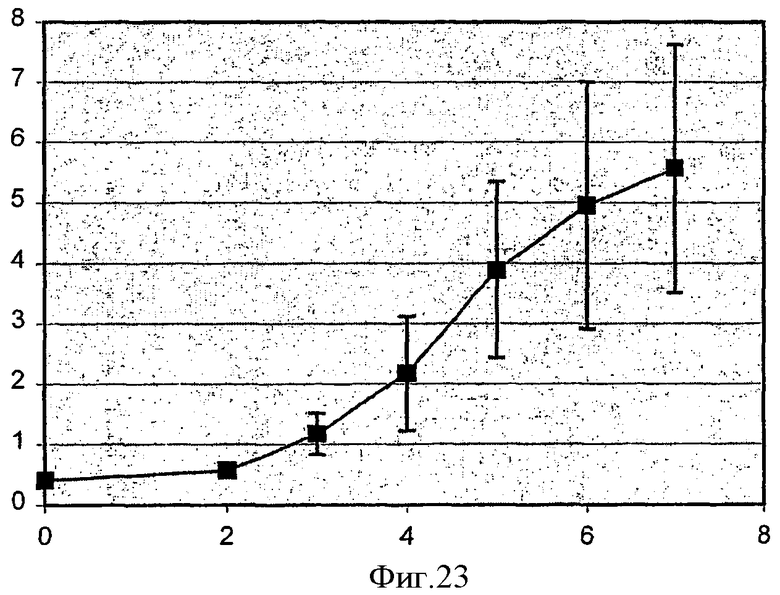
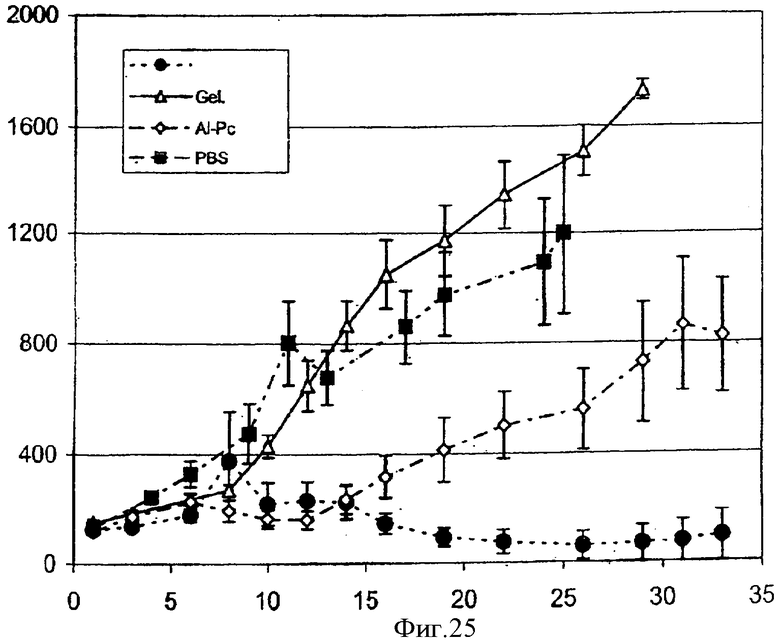
Изобретение относится к области молекулярной биологии и может быть использовано в медицине. В одном варианте способа введения молекулы в цитозоль клетки переносимую молекулу приводят в контакт с клеткой после инкубирования ее с фотосенсибилизирующим средством и облучения. В другом варианте этого способа переносимую молекулу приводят в контакт с клеткой после инкубирования ее с фотосенсибилизирующим средством и либо во время, либо после облучения. На основе данного способа разработаны способы лечения или профилактики заболевания, расстройства или инфекции у пациента, способы генной терапии, способы лечения рака и способ стимуляции иммунного ответа у пациента. С помощью данного способа также получены клетка-переносчик терапевтической переносимой молекулы и клетка, презентирующая антигенную молекулу. Применение изобретения позволяет снизить уровень фотохимических повреждений переносимой молекулы и широко варьировать время введения переносимой молекулы относительно времени облучения клетки, содержащей фотосенсибилизирующее средство. 11 н. и 42 з.п. ф-лы, 25 ил., 1 табл.
a) контактирование указанной клетки с фотосенсибилизирующим средством в течение времени, достаточного для того, чтобы указанное фотосенсибилизирующее средство поглощалось указанной клеткой при концентрации такой, чтобы при поглощении фотосенсибилизирующего средства в клетку и при активации облучением один или более внутриклеточных компартментов лизировались или разрушались;
b) облучение указанной клетки светом с длиной волны, эффективной для активации фотосенсибилизирующего средства, и
c) контактирование указанной клетки с молекулой, подлежащей введению, (переносимой молекулы) непосредственно после окончания указанной стадии облучения или вплоть до 24 часов после завершения указанной стадии облучения в течение времени и при температуре, достаточных для того, чтобы указанная переносимая молекула поглотилась указанной клеткой,
причем указанное облучение проводят перед поглощением клеткой указанной молекулы в любой внутриклеточный компартмент, где указанная переносимая молекула не способна легко проникать через клеточные мембраны и где одно или оба из указанных фотосенсибилизирующего средства и переносимой молекулы присоединены, ассоциированы или конъюгированы с одной или более молекулами носителя, нацеливающими молекулами или векторами.
а) контактирование указанной клетки с фотосенсибилизирующим средством в течение времени, достаточного для того, чтобы указанное фотосенсибилизирующее средство поглотилось указанной клеткой при концентрации такой, чтобы при поглощении один или более внутриклеточных компартаментов лизировались или разрушались при активации облучением;
b) облучение указанной клетки светом с длиной волны, эффективной для активации фотосенсибилизирующего средства, и;
c) контактирование указанной клетки с молекулой, подлежащей введению, (переносимой молекулы) в то же самое время или вплоть до 24 ч после облучения в течение времени и при температуре, достаточных для того, чтобы указанная переносимая молекула поглотилась указанной клеткой,
где указанная переносимая молекула не способна легко проникать через клеточные мембраны, и где одно или оба из указанных фотосенсибилизирующего средства и переносимой молекулы присоединены, ассоциированы или конъюгированы с одной или более молекулами носителя, нацеливающими молекулами или векторами.
Приоритет по пунктам:
| PRASMICKAITE L., HOGSET A., TJELLE Т.Е., OLSEN V.M., BERG K | |||
| Role of endosomes in gene transfection mediated by photochemical internalisation (PCI), J Gene Med | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Приспособление для обратного охлаждения охлаждающей воды конденсаторов паровых машин и особенно локомотивных машин | 1927 |
|
SU9403A1 |
| US 5658892, 19.08.1997. | |||
Авторы
Даты
2008-09-10—Публикация
2001-11-29—Подача