| название |
год |
авторы |
номер документа |
| БЕЛОК IFNAB-BPII, ОБЛАДАЮЩИЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬ ИНТЕРФЕРОН-α/β, ЕГО ПРЕДШЕСТВЕННИК И СЛИТЫЕ БЕЛКИ, СПОСОБ ПОЛУЧЕНИЯ IFNAB-BPII, МОЛЕКУЛЫ ДНК, ЭКСПРЕССИРУЮЩИЙ ВЕКТОР, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ |
1995 |
- Кохен Батия
- Новик Даниела
- Рубинштейн Менахем
|
RU2232811C2 |
| АНТИТЕЛО ПРОТИВ ИНТЕРФЕРОН-АЛЬФА/БЕТА-СВЯЗЫВАЮЩЕГО БЕЛКА II (IFNAB-BPII) |
1995 |
- Кохен Батия
- Новик Даниела
- Рубинштейн Менахем
|
RU2362781C2 |
| АНТИТЕЛО ПРОТИВ ИНТЕРФЕРОН-α/β-СВЯЗЫВАЮЩЕГО БЕЛКА I (IFNAB-BPI) |
1995 |
- Кохен Батия
- Новик Даниела
- Рубинштейн Менахем
|
RU2363705C2 |
| Вариабельные домены лёгкой и тяжёлой цепи мышиного моноклонального антитела против интерферона альфа (IFN-α) человека, антигенсвязывающий фрагмент (Fab) против IFN-α человека, содержащий указанные домены |
2018 |
- Солопова Ольга Николаевна
- Боков Максим Николаевич
- Варламов Николай Евгеньевич
- Позднякова Любовь Петровна
- Свешников Петр Георгиевич
- Шемчукова Ольга Борисовна
- Зацепин Сергей Сергеевич
- Клячко Елена Витальевна
- Ягудин Тимур Анварович
|
RU2694672C1 |
| АНТИТЕЛА РЕЦЕПТОРА 1 ИНТЕРФЕРОНА АЛЬФА И ИХ ПРИМЕНЕНИЕ |
2005 |
- Кардарелли Жозефин М.
- Витте Элисон
- Сринивасан Мохан
|
RU2600884C2 |
| НОВЫЕ ЦИТОКИНЫ ПТИЦ И КОДИРУЮЩИЕ ИХ ГЕНЕТИЧЕСКИЕ ПОСЛЕДОВАТЕЛЬНОСТИ |
2008 |
- Ловенталь, Джон, Уильям
- Бин, Эндрю, Жерард Д.
- Карпала, Адам, Джозеф
|
RU2562108C2 |
| АНТИТЕЛА РЕЦЕПТОРА 1 ИНТЕРФЕРОНА АЛЬФА И ИХ ПРИМЕНЕНИЕ |
2005 |
- Кардарелли Жозефин М.
- Витте Элисон
- Сринивасан Мохан
|
RU2412202C2 |
| Нуклеотидная последовательность, кодирующая слитый белок, состоящий из растворимого экстраклеточного фрагмента человеческого IL-6R и константной части тяжелой цепи человеческого IgG4 |
2023 |
- Аксенова Анна Юрьевна
- Волков Кирилл Владимирович
- Заварзин Алексей Алексеевич
- Малашичева Анна Борисовна
- Сайфитдинова Алсу Фаритовна
- Семенихин Вячеслав Алексеевич
|
RU2818329C1 |
| БЕЛОК, ПРОЯВЛЯЮЩИЙ ИНТЕРФЕРОНОПОДОБНЫЕ ПРОТИВОВИРУСНУЮ И АНТИПРОЛИФЕРАТИВНУЮ БИОЛОГИЧЕСКИЕ АКТИВНОСТИ (ВАРИАНТЫ), БЕЛКОВАЯ КОНСТРУКЦИЯ, КОДИРУЮЩИЙ ПОЛИНУКЛЕОТИД (ВАРИАНТЫ), ВЕКТОР ЭКСПРЕССИИ, КЛЕТКА-ХОЗЯИН, КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ БЕЛКА В КАЧЕСТВЕ ПРОТИВОВИРУСНОГО, АНТИПРОЛИФЕРАТИВНОГО, ПРОТИВОРАКОВОГО ИЛИ ИММУНОМОДУЛИРУЮЩЕГО АГЕНТА И СПОСОБ ЛЕЧЕНИЯ СОСТОЯНИЯ, ЧУВСТВИТЕЛЬНОГО К ИНТЕРФЕРОНОТЕРАПИИ, РАКА ИЛИ ВИРУСНОГО ЗАБОЛЕВАНИЯ |
2007 |
- Ван Хайтао
- Мао Чуншен
- Ли Цзичжи
- Ван Лин
- Ду Юн
- Лю Лунбинь
- Сюй Цзин
- Чжан Жуй
|
RU2469091C2 |
| АНТИТЕЛА ПРОТИВ ИНТЕРФЕРОНА-АЛЬФА |
2002 |
- Чунтхарапай Анан
- Ким Дзин К.
- Преста Леонард Г.
- Стюарт Тимоти
|
RU2314317C2 |
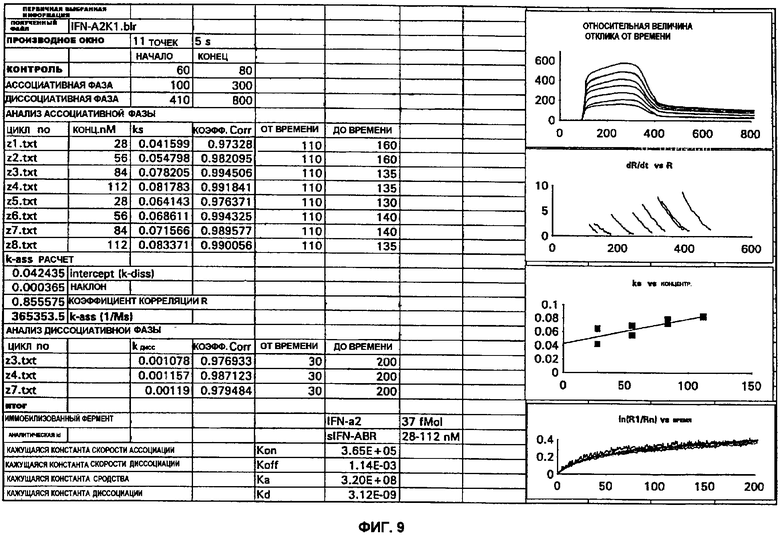
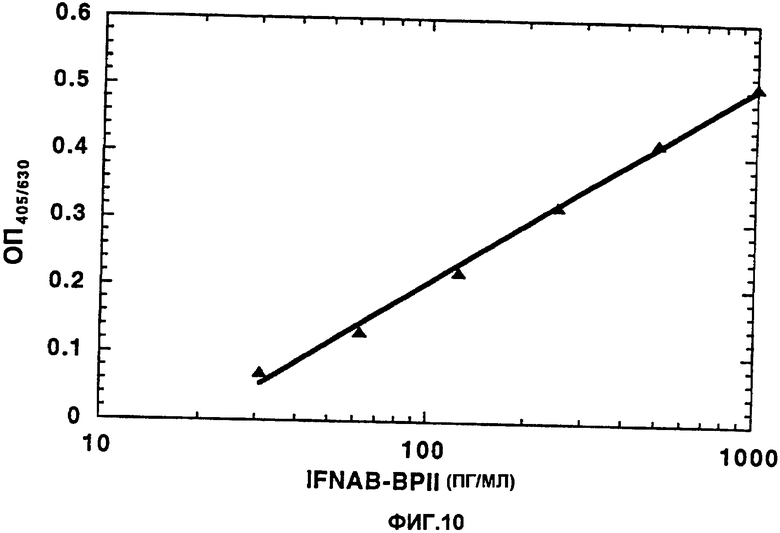
Изобретение относится к области биотехнологии, в частности к генной инженерии. Получены новые интерферон связывающие белки, которые модулируют активность различных подтипов интерферона-α, а также активность интерферона-β. Описано клонирование фрагмента ДНК, кодирующего интерферон α/β связывающий белок IFNAB-BPI, и экспрессия полученного фрагмента ДНК в клетках-хозяевах как с образованием соответствующего полипептида, так и в форме слитых белков. Предложено практическое использование полученных белков в составе фармкомпозиций для ингибирования активности IFN-α или IFN-β. Использование изобретения может найти применение в медицине для подавления нежелательного воздействия IFN-α или IFN-β. 12 н. и 1 з.п. ф-лы, 10 ил., 6 табл.
1. Белок IFNAB-BPI, обладающий способностью связывать интерферон-α/β, характеризующийся аминокислотной последовательностью
ISYDSPDYTDESCTFKISLRNFRSILSWELKNHSIVPTHYTLLYTIMSKPED LKVVKNCANTTRSFCDLTDEWRSTHEAYVTVLEGFSGNTTLFSCSHNF WLAIDMSFEPPEFEIVGFTNHINVMVKFPSIVEEELQFDLSLVIEEQSEGIV KKHKPEIKGNMSGNFTYIIDKLIPNTNYCVSVYLEHSDEQAVIKSPLKCT LLPPGQESESAESAKIGGIITVFLIALVLTSTIVTLKWIGYICLRNSLPKVLR QGLTKGWNAVAIHRCSHNALQSETPELKQSSCLSFPSSWDYKRASLCPS D, или его функционально активный мутеин, полученный путем консервативных замен в указанной последовательности, или его функционально активный фрагмент.
2. Предшественник IFNAB-BPI, характеризующийся аминокислотной последовательностьюMLLSQNAFIVRSLNLVLMVYISLVFGISYDSPDYTDESCTFKISLRNFRSIL
SWELKNHSIVPTHYTLLYTIMSKPEDLKVVKNCANTTRSFCDLTDEWRS
THEAYVTVLEGFSGNTTLFSCSHNFWLAIDMSFEPPEFEIVGFTNHINVM
VKFPSIVEEELQFDLSLVIEEQSEGIVKKHKPEIKGNMSGNFTYIIDKLIPN
TNYCVSVYLEHSDEQAVIKSPLKCTLLPPGQESESAESAKIGGIITVFLIAL
VLTSTIVTLKWIGYICLRNSLPKVLRQGLTKGWNAVAIHRCSHNALQSE
TPELKQSSCLSFPSSWDYKRASLCPSD, или его функционально активный мутеин, полученный путем консервативных замен в указанной последовательности, или его функционально активный фрагмент.
3. Слитый белок, обладающий способностью связывать интерферон-α/β и состоящий из (а) аминокислотной последовательности белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1 и (b) аминокислотной последовательности иммуноглобулина или его фрагмента.4. Слитый белок, обладающий способностью связывать интерферон-α/β и состоящий из (а) аминокислотной последовательности белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1 и (b) аминокислотной последовательности внеклеточной части рецептора α-интерферона (IFNAR) или ее фрагмента.5. Слитый белок, обладающий способностью связывать интерферон-α/β и состоящий из (а) аминокислотной последовательности белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1 и (b) аминокислотной последовательности иммуноглобулина, его фрагмента или комбинации любого из них с внеклеточной частью рецептора α-интерферона (IFNAR).6. Изолированная молекула ДНК, имеющая нуклеотидную последовательность, которая кодирует белок IFNAB-BPI по п.1 или 2.7. Молекула ДНК по п.6, которая транскрибируется в молекулу мРНК размером приблизительно 1,5 т.п.н.8. Гибридная молекула ДНК, кодирующая слитый белок по п.3 и состоящая из (а) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1, и (b) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность иммуноглобулина или его фрагмента.9. Гибридная молекула ДНК, кодирующая слитый белок по п.4 и состоящая из (а) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1, и (b) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность внеклеточной части рецептора α-интерферона (IFNAR) или ее фрагмента.10. Гибридная молекула ДНК, кодирующая слитый белок по п.5 и состоящая из (а) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность белка IFNAB-BPI или его функционально активного мутеина или фрагмента по п.1, и (b) нуклеотидной последовательности, в соответствии с генетическим кодом определяющей аминокислотную последовательность иммуноглобулина, его фрагмента или комбинации любого из них с внеклеточной частью рецептора α-интерферона (IFNAR).11. Реплицируемый экспрессирующий вектор, содержащий молекулу ДНК по любому из пп.6-10 и регуляторные элементы, оперативно связанные с указанной молекулой ДНК и обеспечивающие ее экспрессию в трансформированной клетке млекопитающего.12. Фармацевтическая композиция для ингибирования активности IFN-α или IFN-β, содержащая белок IFNAB-BPI по любому из пп.1 и 3-5 в сочетании с фармацевтически приемлемым носителем.13. Способ продукции белка IFNAB-BPI, предусматривающий культивирование культуры клеток млекопитающего, трансформированных экспрессирующим вектором по п.11, и выделение указанного белка.Приоритет по пунктам:
07.02.1994 по пп.1-13.