Область изобретения
Эта заявка относится к рекомбинантным белкам, обладающим биологическими активностями подобно человеческим интерферонам.
Предшествующий уровень техники
В этой заявке принята номенклатура интерферонов (IFN), опубликованная в Nature (1).
Человеческие интерфероны (HuIFN), которые были открыты Isaacs и Lindenmann в 1957 году (2), представляют собой хорошо известное семейство цитокинов, секретируемых большим разнообразием эукариотических клеток под воздействием различных стимулов, таких как вирусная инфекция или воздействие митогенов. IFN может вызывать многие изменения в клеточном поведении, включая влияние на рост и дифференцировку клеток и модулирование иммунной системы (3-7). HuIFN были классифицированы на шесть подгрупп, а именно IFN-α, IFN-β, IFN-γ, IFN-ω, IFN-ε и IFN-κ. HuIFN-α (лейкоцитарный интерферон) продуцируется в человеческих лейкоцитах и, вместе с минорными количествами HuIFN-β (интерферон фибробластов), в лимфобластоидных клетках. Кроме того, по своим химическим и биологическим характеристикам HuIFN были классифицированы на две общие категории, а именно на тип I и тип II. Тип I состоит из подгрупп IFN-α и INF-β, а также не так давно открытых подгрупп IFN-ω, IFN-ε и IFN-κ. Тип II имеет только один член: IFN-γ (иммунный интерферон).
Разные подгруппы интерферонов имеют разные структурные и биологические характеристики. HuIFN-β представляет собой N-гликопротеин (8, 9), который был очищен до гомогенного состояния и охарактеризован. Он гетерогенен по размеру, главным образом из-за своей углеводной группировки. Однако имеется только один ген IFN-β человека, кодирующий белок из 166 аминокислот. IFN-β имеет низкую гомологию с IFN-α, проявляя приблизительно 30-40% идентичности.
В противоположность единственности гена IFN-β, HuIFN-α представляет собой подгруппу, состоящую из мультигенного семейства по существу из 14 генов. Минорные варианты, образованные отличиями в одной или двух аминокислотах, являются причиной множественных аллелей (10). Исключив псевдоген 1FNAP22, имеем 13 генов, кодирующих 13 белков. Каждый белок содержит 165-166 аминокислот. Белок, кодируемый геном IFNA13, идентичен белку IFNA1. Таким образом, имеются 12 индивидуальных белков интерферона-альфа: IFNA1, IFNA2, IFNA4, IFNA5, IFNA6, IFNA7, IFNA8, IFNA10, IFNA14, IFNA16, IFNA17 и IFNA21. Гомология аминокислотной последовательности среди подтипов IFN-α обычно составляет 80-85% (11).
Зрелый IFN-ω демонстрирует 60% гомологии нуклеотидной последовательности с семейством разновидностей IFN-α, но он длиннее на 6 аминокислот на своем С-конце. IFN-ω имеет более отдаленное родство с интерфероном-β (имеет приблизительно 30% гомологии последовательности). Человеческий IFN-ω не классифицируется в группе IFN-α, поскольку по своим антигенным свойствам отличается от IFN-α и различается по своему взаимодействию с рецептором IFN-α, тип I (12). IFN-ω секретируется инфицированными вирусами лейкоцитами в виде главного компонента человеческих лейкоцитарных интерферонов.
Зрелый белок человеческого IFN-ε содержит 185 аминокислот, имея приблизительно 33% и 37% гомологии последовательности с IFN-α2 и IFN-β, соответственно (13, 14). Функция и биофизические свойства IFN-ε по существу детально не охарактеризованы; однако он действует подобно интерферонам, тип I. Кроме того, IFN-ε может играть роль в выполнении репродуктивной функции (15).
IFN-κ, состоящий из 180 аминокислот человеческий цитокин, представляет собой недавно идентифицированный IFN, тип I. Кодирующая последовательность IFN-κ приблизительно на 30% идентична другим интерферонам, тип I, обнаруженным у людей. Характерной особенностью IFN-κ является заметная конститутивная экспрессия его транскрипта в неиндуцированных клетках, в частности кератиноцитах. IFN-κ может играть роль в регуляции системных или местных иммунных функций посредством его воздействия на клетки врожденной иммунной системы (16). Однако IFN-κ демонстрирует низкую противовирусную активность (17).
По-видимому, человеческий интерферон, тип I, связывается с двумя рецепторными субъединицами, IFNAR-1 и -2, которые широко распространены на клеточной поверхности различных типов клеток. Вовлечение лиганда приводит к индукции фосфорилирования тирозинкиназ TYK2 и JAK-1 (янус-киназа 1), которые связаны с IFNAR-1 и -2, соответственно. После фосфорилирования белки STAT (signal transducer and activator of transcription) высвобождаются из комплекса с рецептором и образуют гомодимеры, а также гетеродимеры (18, 19). После высвобождения димеры STATA ассоциируют с интерфероночувствительным фактором 9 (IRF-9), связывающимся с ДНК-белком, образуя комплекс, называемый IFN-стимулируемый генный фактор-3 (ISGF-3), который мигрирует в ядро. Далее комплекс ISGF-3 связывается с элементом ДНК, расположенным "вверх по течению" у всех IFN-индуцибельных генов. Это так называемый "классический" путь сигнальной трансдукции.
Непрерывно открывают новые способы действия и биохимические пути, регулируемые IFN, тип I. Например, расположенные "вниз по течению" от Р13К (фосфоинозитид-3ОН-киназа) в пути сигнальной трансдукции ядерный фактор каппа-В (NF-κВ) и PKC-d ассоциируют с антиапоптотическими эффектами, наблюдаемыми в нейтрофилах, инкубированных с IFN-β (20).
Более 300 генов, называемые интерферон-индуцируемые гены, чувствительны к воздействию IFN. Наиболее изученными белками IFN являются белки с противовирусными свойствами. Например, фермент семейства 2,5-олигосинтетаз (OAS-1 и -2) катализирует синтез коротких олигоаденилатов, которые связываются с и активируют РНКазу L (RNAseL), фермент, расщепляющий вирусные и клеточные РНК, таким образом ингибируя синтез белка. Дц(двухцепочечная)-РНК-активированная протеинкиназа (PKR) фосфорилирует фактор инициации трансляции elF2a, что также приводит к ингибированию синтеза вирусных и клеточных белков. Совсем недавно также было обнаружено, что PKR необходима для активации фактора транскрипции NF-κВ, центрального действующего субъекта в индукции воспалительных цитокинов, иммунном модулировании и апоптозе. Белки Мх (миксовирус-устойчивость) ингибируют репликацию РНК вирусов посредством либо предотвращения транспорта вирусных частиц в клетке, либо транскрипции вирусной РНК. РНК-специфическая аденозин-деаминаза (ADAR) превращает аденозин в инозин, вызывая таким образом гипермутацию вирусных РНК-геномов (21).
HuIFN обладают широким спектром биологических активностей, включая противовирусную, противоопухолевую и иммунорегуляторную функции. Клинические возможности человеческих интерферонов широко исследованы и суммированы ниже.
Что касается противоопухолевых применений, то HuIFN могут опосредовать противоопухолевые эффекты либо косвенно путем регулирования иммуномодуляторных и антиангиогенезных ответов, либо путем непосредственного воздействия на пролиферацию или клеточную дифференцировку опухолевых клеток (22). Интерферонотерапия использована в лечении различных лейкозов (23), например лейкозного ретикулоэндотелиоза (24), острого и хронического миелоидного лейкоза (25-27), остеосаркомы (28), базалиомы (29), глиомы (30), почечно-клеточного рака (31), множественной миеломы (32), меланомы (33), саркомы Капоши (23) и болезни Ходжкина (34). Комбинированная терапия с использованием IFN-α с цитарабином (ara-С), 5-FU (5-фторурацилом), гидроксимочевиной и IL-2 (интерлейкином-2) хорошо изучена и в большинстве случаев демонстрирует значительно более хорошие результаты по сравнению с терапией только одним HuIFN-α (3). Сообщали также о синергическом лечении прогрессирующего рака комбинацией HuIFN и темозоломида (35).
Что касается противовирусных применений, то HuIFN использованы клинически для противовирусной терапии, например в лечении СПИДа (36), вирусного гепатита, включая хронический гепатит В, гепатит С (37, 38), инфекции папиллома-вирусом (39), инфекции вирусом герпеса (40), вирусного энцефалита (41) и в профилактике ринита и респираторных инфекций (40).
Кроме того, HuIFN использованы клинически для антибактериальной терапии (42), например аэрозолизированный HuIFN-γ (43) и HuIFN-α использованы на пациентах с диагнозом туберкулез легких с множественной лекарственной устойчивостью (44). HuIFN-γ использован в лечении туберкулеза мозга с множественной лекарственной устойчивостью (45).
Кроме того, HuIFN использованы клинически для иммуномодулирующей терапии, например для предупреждения отторжения "трансплантат против хозяина" или уменьшения прогрессирования аутоиммунных заболеваний, таких как множественный склероз (46, 47) и синдром Шегрена (48). IFN-β одобрен FDA в Соединенных Штатах для лечения множественного склероза. Недавно появилось сообщение о том, что у пациентов с множественным склерозом снижено продуцирование интерферонов типа I и интерлейкина-2 (49). К тому же, иммуномодулирующая терапия с использованием HuIFN-α по-видимому будет представлять собой эффективную терапию у пациентов с хроническим миелоидным лейкозом (CML), переносящих рецидив после трансплантации костного мозга (50).
Что касается применения их с составе вакцин, то HuIFN использованы клинически в качестве адъюванта в лечении меланомы (51) и также могут быть использованы в качестве адъюванта или соадъюванта для повышения или моделирования иммунного ответа в случаях профилактической или терапевтической вакцинации для многих других заболеваний (52).
HuIFN-α2a был первым ингибитором ангиогенеза, который использован в клинических испытаниях, и оказался эффективным у детей для лечения представляющей угрозу для жизни гемангиомы (53, 54). Другим клиническим показанием является гигантоклеточная опухоль кости. Kaban и др. докладывали о поразительной регрессии большой, быстро растущей, рецидивирующей гигантоклеточной опухоли нижней челюсти (55).
Несмотря на то, что HuIFN имеют многие важные клинические применения, они демонстрируют значительные побочные эффекты и другие ограничения. Большинство цитокинов, включая HuIFN, имеют относительно короткие периоды полувыведения из кровотока, так как они индуцируются in vivo для осуществления локального и кратковременного действия. Поскольку обычно HuIFN вводят в виде системных терапевтических средств, то их необходимо вводить часто и в относительно больших дозах. Частые парентеральные введения неудобны и болезненны. Кроме того, токсичные побочные эффекты, ассоциированные с введение HuIFN, часто оказываются такими тяжелыми, что некоторые люди не могут переносить такого лечения. По всей вероятности эти побочные эффекты ассоциируются с системным введением высоких дозировок. Кроме того, в клинических исследованиях обнаружено, что некоторые пациенты продуцируют антитела к rHuIFN ("r" от рекомбинантный), что нейтрализует его биологическую активность (56).
Несомненно, что разработка новых интерфероновых белков с повышенной эффективностью является срочной необходимостью для многочисленных применений, например противораковых терапий, а также противовирусной, иммунотерапии, антипаразитической, антибактериальной терапии, или для любого медицинского состояния или ситуации, где требуются повышенная интерфероновая активность и/или сниженные побочные эффекты. В целом, с высокой вероятностью можно сказать, что HuIFN будут играть главную роль в следующем поколении новых противоопухолевых и противовирусных терапий (10).
В данной области техники хорошо известно, что большинство эффективных способов для улучшения фармацевтических свойств цитокиновых лекарственных средств состоит в изменении самого цитокинового белка. За это время установлены различные стратегии и методики изменения интерфероновых пептидов. Как правило, в настоящее время используют три стратегии для создания мутантов HuIFN-α.
Первая стратегия заключается в получении гибридов IFN. Некоторые исследователи воспользовались преимуществом наличия в IFN-кодирующих последовательностях существующих в природе сайтов расщепления рестрикционными эндонуклеазами (РЭ), чтобы соединять вместе гомологические кодирующие фрагменты (57, 58). Обзор по получению ряда гибридных IFN приведен Horisberger и Di Marco (11); в этой статье дается общее представление способа конструирования таких молекул. Описаны конкретные примеры способов конструирования гибридных интерферонов. Некоторые исследователи воспользовались преимуществом ПЦР-амплификации для конструирования мутантных IFN-α, чтобы таким образом создать конкретно желаемые нуклеиновокислотные фрагменты и затем улучшить возможности соединенных вместе новых кусков разных IFN (59). В патенте США №6685933 (60) также описаны методики ПЦР-амплификации для создания гибридов человеческих IFN. Гибриды интерферонов могут быть созданы внутри интерфероновой подгруппы, как, например, описано в патенте США №5137720 (61) и патенте США №6685933 (60), или между по меньшей мере двумя разными интерфероновыми классификационными группами, как, например, описано в патенте США №6174996 (62) и патенте США №6685933 (60). В дополнение к этому, исходные гены гибрида могут происходить из одного вида (главным образом от человека), например гибриды между HuIFN-α и HuIFN-ω, или от более чем одного вида животных, например гибриды между человеческим и мышиным интерферонами-α (63).
Вторая стратегия конструирования интерфероновых мутантов заключается в использовании сайтнаправленного точечного мутагенеза путем введения изменений одного или более нуклеотидов в молекулы ДНК IFN (64). В последнее время в качестве руководящего принципа белкового мутагенеза используются направленная мутация и вычислительные методы (65).
Третья стратегия конструирования HuIFN, тип I, заключается в перетасовке (шаффлинге; от англ. shuffling) фрагментов гена IFN, полученных в результате переваривания их РЭ, ПЦР-амплификации, химического синтеза или переваривания ДНКазой, с последующим применением ПЦР для случайного соединения фрагментов вместе и затем их амплификации. Полученные в результате ПЦР-продукты фактически представляют собой пул перегруппированных фрагментов гена интерферона-альфа, которые могут быть использованы для конструирования библиотеки ДНК, из которой могут быть выделены клоны ДНК с желаемыми фенотипами (66). Например, Chang и др. описали способ конструирования и скрининга шаффлинг-библиотеки для HuIFN с целью идентификации производных HuIFN с повышенной противовирусной и антипролиферативной активностями в клетках мыши (67).
Человеческий интерферон-альфа-con-1 (консенсусный интерферон) представляет собой рекомбинантный в природе не существующий HuIFN-α из 166 аминокислот. Он был создан путем оценки самых высококонсервативных аминокислот в каждой соответствующей области на основании известных клонированных последовательностей HuIFN-α. Он имеет 89% гомологии последовательности на аминокислотном уровне по отношению к HuIFN-α2b и удельную противовирусную активность, составляющую приблизительно 109 IU (международных единиц)/мг. Человеческий интерферон-альфа-con-1 апробирован для лечения хронической инфекции HCV (вирус гепатита С) у пациентов 18 лет или старше с компенсированным заболеванием печени (68).
Несмотря на то, что некоторые рекомбинантные интерфероновые белки известны в предшествующем уровне техники, существует необходимость в получении новых интерфероноподобных белков и белковых композиций, имеющих повышенные биологические активности.
Сущность изобретения
Согласно изобретению описан выделенный полинуклеотид, кодирующий белок, имеющий биологические активности подобно человеческим интерферонам. В одном воплощении полинуклеотид содержит нуклеотидную последовательность, по меньшей мере на 93% идентичную SEQ ID No: 1. В других воплощениях нуклеотидная последовательность по меньшей мере на 95% идентична или по меньшей мере на 98% идентична SEQ ID No: 1.
В одном воплощении изобретение включает белок, выбранный из группы, состоящей из белков, каждый из которых имеет аминокислотную последовательность, по меньшей мере на 85% идентичную SEQ ID No: 2. Предпочтительно, белок является несуществующим в природе белком и имеет повышеную противовирусную и антипролиферативную активность по сравнению с человеческим интерфероном-альфа-2b (HuIFN-α2b). Например, белок может иметь противовирусную активность по меньшей мере в 2 раза больше, чем HuIFN-α2b, и антипролиферативную активность по меньшей мере в 10 раз больше, чем HuIFN-α2b. В конкретных воплощениях аминокислотная последовательность данного белка по меньшей мере на 90% идентична или по меньшей мере на 95% идентична SEQ ID No: 2
Данное изобретение охватывает рекомбинантные векторы, содержащие последовательность данного полинуклеотида, и клетки хозяина, содержащие эти векторы. Изобретение также охватывает полипептидные фрагменты, проявляющие биологические активности подобно человеческим интерферонам. Кроме того, изобретение включает белковые конструкции и другие композиции, проявляющие интерфероноподобные биологические активности, такие как конъюгаты, содержащие белок и другой компонент, например неорганический полимер. Кроме того, изобретение включает способы и применения белка и композиций для терапевтических целей, например в качестве противовирусных или противораковых агентов. Кроме того, изобретение может быть применено для лечения других состояний, чувствительных к интерферонотерапии.
Краткое описание графических материалов
На Фиг.1 изображена полная последовательность ДНК, кодирующая новый белок по изобретению, упоминаемый в данном описании как Novaferon™ (SEQ ID No: 1) (А). На Фиг.1 также показана предсказанная аминокислотная последовательность Новаферона (SEQ ID No: 2) (В) и выравнивание этой аминокислотной последовательности Новаферона относительно последовательности ДНК Новаферона (С). Первая аминокислота, цистеин, в зрелом белке Новафероне обозначена как остаток 1.
На Фиг.2 показано выравнивание нуклеотидной последовательности гена Новаферона относительно гена HuIFN-α14 (номер в Genebank: NM_002172) (А) и выравнивание аминокислотной последовательности белка Новаферона относительно белка HuIFN-α14 (транслированного, номер в Genebank: NM_002172) (В). Первая аминокислота, цистеин, в зрелом белке Новафероне обозначена как остаток 1. Новаферон имеет приблизительно 93% идентичности последовательности (462/498) с HuIFN-α14 на нуклеотидном уровне и приблизительно 87% идентичности последовательности (144/166) на аминокислотном уровне. Отличающиеся нуклеотиды показаны как пустое место в середине линии.
На ФИГ.3 показано выравнивание нуклеотидной последовательности гена Новаферона относительно гена HuIFN-α2b (номер в Genebank: NM_000605) (А) и выравнивание аминокислотной последовательности белка Новаферона относительно белка HuIFN-α2b (транслированного с гена HuIFN-α2b с номером в Genebank: NM_000605) (В). Первая аминокислота, цистеин, в зрелом белке Новафероне обозначена как остаток 1. Новаферон имеет приблизительно 89% идентичности последовательности (445/498) с HuIFN-α2b на нуклеотидном уровне и приблизительно 81% идентичности последовательности (135/166) на аминокислотном уровне. Отличающиеся нуклеотиды показаны как пустое место в середине линии.
Фиг.4 представляет собой график, показывающий антипролиферативное ингибирование in vitro клеток Дауди под действием Новаферона по сравнению с HuIFN-α2b.
Фиг.5 представляет собой график, показывающий противоопухолевые эффекты in vivo Новаферона и HuIFN-α2b на бестимусных мышах с ксенотрансплантатами РС-3 рака предстательной железы человека.
Фиг.6 представляет собой график, показывающий противоопухолевые эффекты in vivo Новаферона и HuIFN-α2b на бестимусных мышах с ксенотрансплантатами Hep G2 рака печени человека.
Фиг.7 представляет собой график, показывающий противоопухолевые эффекты in vivo Новаферона и HuIFN-α2b на бестимусных мышах с ксенотрансплантатами А-375 меланомы человека.
Фиг.8 представляет собой график, показывающий противоопухолевые эффекты in vivo Новаферона и HuIFN-α2b на бестимусных мышах с ксенотрансплантатами LS 180 рака толстой кишки.
Фиг.9 представляет собой график, показывающий противоопухолевые эффекты in vivo Новаферона и HuIFN-α2b на бестимусных мышах с ксенотрансплантатами HL 60(3) лейкоза человека.
Подробное описание
На всем протяжении следующего далее описания приведены конкретные подробности с целью обеспечения более всестороннего понимания изобретения. Однако изобретение может быть осуществлено на практике без этих подробностей. В других случаях, чтобы избежать внесения ненужной неопределенности в изобретение, подробно не показаны или не описаны хорошо известные факторы. Соответственно, описание и фигуры следует рассматривать в иллюстративном, а не в ограничивающем смысле.
Определение терминов
Перед тем, как дать подробное описание настоящего изобретения, следует понимать, что это изобретение не ограничено конкретными белковыми молекулами, методологией, протоколами, клеточными линиями, векторами и реагентами, описанными во всем своем возможном разнообразии. Также следует понимать, что используемая в данном описании терминология предназначена только для описания конкретных воплощений и не предназначена для ограничения объема настоящего изобретения, который будет ограничен только прилагаемой формулой изобретения.
С целью более полного понимания изобретения, изложенного в данном описании, применены следующие далее термины, и их определение показано ниже. Следует понимать, что используемая в данном описании терминология предназначена только для описания конкретных воплощений и не предназначена для ограничения объема настоящего изобретения, который будет ограничен только прилагаемой формулой изобретения.
Если не определено иное, все технические и научные термины, используемые в данном описании, имеют те же значения, которые обыкновенно понимаются специалистом обычной квалификации в данной области техники, к которой это изобретение соответствует. Все публикации, упомянутые в данном описании, включены в данное описание посредством ссылки с целью описания и раскрытия клеточных линий, векторов и методологий, обзоры по которым приведены в этих публикациях и которые могли быть использованы в связи с данным изобретением. Ничто в данном описании не должно быть истолковано как допущение того, что данное изобретение дает право датировать более ранним числом такие открытия на основании предшествующего изобретения.
Термин "интерферон" относится к семейству секретируемых белков, продуцируемых рядом эукариотических клеток под воздействием различных окружающих стимулов, включая вирусную инфекцию или подвергание воздействию митогена. В дополнение к обладанию противовирусными свойствами показано, что интерфероны воздействуют на большое разнообразие клеточных функций. Все интерфероновые единицы выражены в данном описании со ссылкой на международные стандарты ВО3 (Всемирная организация здравоохранения) 94/786 (rHuIFN-α-консенсус) и 95/650 (rHuIFN-α2a).
Термин "интерфероноподобный" (или «подобные интерферону») относится к функциональным и/или структурным признакам, демонстрируемым известными интерферонами или аналогами интерферонов либо сходным с таковыми известных интерферонов или аналогов интерферонов. Например, термин "интерфероноподобные биологические активности" включает в себя противовирусную и антипролиферативную активности. В данном описании приведены и другие примеры интерфероноподобных биологических активностей, и они будут очевидны специалисту в данной области техники. Термин во множественном числе "активности" включает в себя термин в единственном числе "активность"; то есть изобретение охватывает рекомбинантные белки или другие белковые конструкции или композиции, демонстрирующие по меньшей мере одну интерфероноподобную активность.
Термин "консенсусный интерферон" относится к типу синтетического интерферона, имеющего аминокислотную последовательность, представляющую собой приблизительное усреднение последовательностей всех известных подтипов человеческих альфа-интерферонов. Сообщалось, что консенсусный интерферон обладает более высокой (приблизительно в 5 раз) противовирусной, антипролиферативной активностью и активностью в отношении активации NK-клеток, чем любой природный подтип человеческого IFN-α.
Термин "выделенный", использованный в данном описании, относится к таким молекулам, как ДНК или РНК, которые извлечены из их нативного окружения. Например, молекулы рекомбинантных ДНК, содержащиеся в векторе, считаются выделенными для задач настоящего изобретения. Дополнительные примеры выделенных молекул ДНК включают молекулы рекомбинантных ДНК, содержащиеся в гетерологических клетках хозяина, или очищенные (частично или по существу) молекулы ДНК в растворе. "Выделенная" ДНК также включает молекулы ДНК, полученные из библиотеки, которая может содержать природные или искусственные представляющие интерес фрагменты ДНК, а также химически синтезированные нуклеиновые кислоты. Следовательно, выделенные нуклеиновые кислоты могут быть получены рекомбинантной технологией.
Термин "нуклеотидная последовательность" относится к последовательности нуклеотидов, содержащей молекулу олигонуклеотида, полинуклеотида или нуклеиновой кислоты и их фрагменты или части. В случае молекулы ДНК последовательность может содержать ряд дезоксирибонуклеотидов, а в случае молекулы РНК последовательность может содержать соответствующий ряд рибонуклеотидов. Олигонуклеотидная, полинуклеотидная молекула или молекула нуклеиновой кислоты может быть одно- или двухцепочечной, а нуклеотидная последовательность может представлять собой смысловую или антисмысловую цепь.
Термины "олигонуклеотидный фрагмент" или "полинуклеотидный фрагмент", "часть", или "сегмент", или "зонд", или "праймер" используются взаимозаменяемо и относятся к последовательности нуклеотидных остатков длиной по меньшей мере приблизительно 5 нуклеотидов. Предпочтительно, фрагменты могут быть использованы для гибридизации с целевой нуклеотидной последовательностью. Праймер служит в качестве сайта инициации полимеризации нуклеотидов, катализируемой либо ДНК-полимеразой, либо РНК-полимеразой, либо обратной транскриптазой. Фрагмент или сегмент может однозначно идентифицировать каждую полинуклеотидную последовательность по настоящему изобретению. Предпочтительно, фрагмент содержит последовательность, в значительной степени схожую с SEQ ID No: 1.
Термины "белок", или "пептид", или "олигопептид", или "полипептид" относятся к существующим в природе или синтетическим молекулам, содержащим последовательность аминокислот.
Термин "открытая рамка считывания" или ОРС означает ряд нуклеотидных триплетов для кодирования аминокислот без какого-либо терминирующего кодона и обычно обозначает последовательность, транслируемую в белок.
Термин "последовательность, кодирующая зрелый белок" относится к последовательности, которая кодирует белок или пептид без сигнальной или лидерной последовательности. Этот белок может быть получен путем процессинга в клетке, в результате которого удаляется любая лидерная/сигнальная последовательность. Белок может быть получен синтезом или только путем использования полинуклеотида, кодирующего последовательность, кодирующую только зрелый белок.
Термины "очищенный" или "по существу очищенный", которые использованы в данном описании, означают, что указанный белок представлен по существу в отсутствие других биологических макромолекул, например других белков, полипептидов и тому подобного. Белок очищен таким образом, что он составляет по меньшей мере 95% по массе от присутствующих указанных биологических макромолекул (но вода, буферы и другие небольшие молекулы, особенно молекулы с молекулярной массой менее 1000 дальтон, могут присутствовать).
Термин "рекомбинантный экспрессирующий носитель или вектор" относится к плазмиде, или фагу, или вирусу, или вектору для экспрессии белка из последовательности ДНК (РНК). Экспрессирующий вектор может содержать транскрипционную единицу, содержащую набор из (1) генетических элемента или элементов, играющих регуляторную роль в генной экспрессии, например промоторов или энхансеров, (2) структурной или кодирующей последовательности, которая транскрибируется в мРНК и транслируется в белок, и (3) соответствующих последовательностей инициации и терминации транскрипции. Структурные единицы, предназначенные для применения в экспрессирующих системах дрожжей или эукариот, предпочтительно содержат лидерную последовательность, позволяющую осуществлять внеклеточную секрецию транслируемого белка клеткой-хозяином. Альтернативно, когда рекомбинантный белок экспрессируется без лидерной или транспортной последовательности, он может содержать на аминоконце остаток метионина. Этот остаток впоследствии может быть или может не быть отщеплен от экспрессированного рекомбинантного белка с получением конечного продукта.
Термин "существенное сходство" относится к нуклеиновой кислоте или ее фрагменту, которая(ый) имеет высокую степень идентичности последовательности с другой нуклеиновой кислотой после оптимального выравнивания ее с другой нуклеиновой кислотой или ее комплементарной цепью. Идентичность или гомологичность последовательности может быть определена с использованием программного обеспечения для анализа последовательностей, например BLASTN. Считается, что первая нуклеиновая кислота имеет существенное сходство со второй нуклеиновой кислотой, если они показывают идентичность последовательности по меньшей мере приблизительно 85-95% или более после их оптимального выравнивания. Например, для определения идентичности или гомологичности последовательности между двумя разными нуклеиновыми кислотами используется программа BLASTN "BLAST (Basic Local Aligment Search Tool) 2 Sequences". Эта программа доступна для общественного пользования из Национального центра по биотехнологической информации (National Center for Biotechnology Information (NCBI)) (69). В качестве неограничивающего примера, такие сравнения могут быть выполнены с использованием программного обеспечения, установленного в режиме установок по умолчанию (expect=10, filter=default, open gap=5, extension gap=2 penalties, gap x dropoff=50). Аналогично считается, что первый белок или полипептид имеет существенное сходство со вторым белком или полипептидом, если они показывают идентичность последовательности по меньшей мере приблизительно 85-95% или более после их оптимального выравнивания и сравнения с применением программного обеспечения BLAST (blastp) с установками по умолчанию.
В качестве другой иллюстрации, полинуклеотид, имеющий нуклеотидную последовательность, по меньшей мере, например, на 95% "идентичную" ссылочной нуклеотидной последовательности, кодирующей белок, означает, что нуклеотидная последовательность данного полинуклеотида идентична ссылочной последовательности за исключением того, что данная полинуклеотидная последовательность может включать до пяти включительно точечных мутаций на каждые 100 нуклеотидов ссылочной нуклеотидной последовательности, кодирующей белок. Другими словами, для получения полинуклеотида, имеющего нуклеотидную последовательность, по меньшей мере на 95% идентичную ссылочной нуклеотидной последовательности, до 5% нуклеотидов включительно в ссылочной последовательности могут быть делегированы или заменены другим нуклеотидом или ряд нуклеотидов до 5% включительно от всех нуклеотидов в ссылочной последовательности может быть вставлен в ссылочную последовательность.
Термины "комплементарный" или "комплементарность", которые использованы в данном описании, относятся к природному связыванию полинуклеотидов путем спаривания оснований в рекомендуемых солевых и температурных условиях. Например, последовательность "A-G-T" связывается с комплементарной последовательностью "Т-С-А". Комплементарность между двумя одноцепочечными молекулами может быть "частичной", при этом связываются только несколько нуклеиновых кислот, или может быть полной, когда существует тотальная комплементарность между одноцепочечными молекулами. Степень комплементарности между цепями нуклеиновых кислот оказывает существенные эффекты на эффективность и строгость гибридизации между цепями нуклеиновых кислот. Это особенно важно в реакциях амплификации, которая зависит от связывания между цепями нуклеиновых кислот.
Термин "трансформация" означает введение ДНК в организм с тем, чтобы ДНК была способна к репликации, либо в виде внехромосомного элемента, либо путем хромосомной интеграции. Термин "транфекция" относится к доставке экспрессирующего вектора в подходящую клетку хозяина, независимо от того, будут или нет какие-либо кодирующие последовательности действительно экспрессироваться.
Термины "лечение", "подвергание лечению" и их грамматические эквиваленты используются в широком смысле и включают терапевтическое лечение, предупреждение, профилактику и ослабление некоторых нежелательных симптомов или состояний.
Термины "биологическая активность" и "биологические активности", которые использованы в данном описании, относятся к структурным, регуляторным, биохимическим или другим биологическим функциям в живых системах, например схожим или идентичным таковым существующих или несуществующих в природе молекул.
Термин "антипролиферация" и "антипролиферативный", который использован в данном описании, относится к замедлению и/или предотвращению роста и деления клеток, приводящему к уменьшению общего количества клеток и/или уменьшению процента клеток-мишеней в любой одной или всех фазах клеточного цикла. Кроме того, клетки могут быть конкретизированы, как находящиеся в состоянии ареста на конкретной стадии клеточного цикла: G1 (промежуток (дар) 1), S-фаза (синтез ДНК), G2 (промежуток 2) или М-фаза (митоз). Термин "антипролиферативная активность", который использован в данном описании, относится к активности белка, белковой конструкции или композиции, ингибирующей клеточную пролиферацию, особенно неопластическую клеточную пролиферацию, например раковых клеток, либо in vitro, либо in vivo.
Термин "противоопухолевый" или "противораковый", который использован в данном описании, относится к противодействию или предотвращению образования злокачественных опухолей. "Противоопухолевая активность" или "противораковая активность" при использовании в данном описании относится к активности белка, белковой конструкции или композиции, ингибирующей клеточную пролиферацию, особенно неопластическую клеточную пролиферацию, например раковых клеток, либо in vitro, либо in vivo.
Термин "IC50" или "половина максимальной ингибирующей концентрации" представляет собой концентрацию ингибитора, как например белка, которая необходима для 50% ингибирования клеточного роста in vitro.
Термины "противовирусный" и "против вируса", которые использованные в данном описании, относятся к замедлению и/или предотвращению вирусной инфекции клеток или воздействию на репликацию вируса в клетках in vitro и/или in vivo, приводящему к замедлению или остановке размножения вируса или уменьшению общего количества вирусных частиц. "Противовирусная активность", которая использована в данном описании, означает активность белка, белковой конструкции или композиции, ингибирующую вирусные инфекции или воздействующую на репликацию вируса или in vitro, и/или in vivo.
Белок Новаферон
Настоящее изобретение относится к получению и охарактеризованию нового человеческого интерфероноподобного белка, обозначенного в данном описании как "Novaferon"™. Как подробно описано ниже, белок Новаферон проявляет повышенные противовирусную и антипролиферативную биологические активности по сравнению с существующим в природе HuIFN-α2b, как измерено в стандартных in vitro тестах. В частности, белок Новаферон показывает 12,5-кратное увеличение в противовирусной активности при тестировании в системе Wish-VSV (Wish-клетки/вирус везикулярного стоматита) и приблизительно 400-кратное улучшение в антипролиферативном ингибировании роста клеток Дауди по сравнению с HuIFN-α2b в одних и тех же тестируемых системах.
В одном воплощении белок Новаферон кодируется полинуклеотидом, состоящим из 498 нуклеотидов, которые показаны на SEQ ID No: 1 и Фиг.1(А). Зрелый белок Новаферон состоит из 166 аминокислот, которые показаны на SEQ ID No: 2 и Фиг.1(В). Полинуклеотидные и аминокислотные последовательности и их варианты, охваченные изобретением, описаны с дальнейшими подробностями ниже.
Для сравнительных целей авторами изобретения была исследована гомология Новаферона с существующими в природе HuIFN. С использованием blast-поисков было обнаружено, что Новаферон имеет наивысшую гомологию с HuIFN-α14 на обоих нуклеотидном и аминокислотном уровнях. Как показано на Фиг.2, полинуклеотидная последовательность (SEQ ID No: 1), кодирующая Новаферон, имеет гомологию приблизительно на 93% (462/498) относительно HuIFN-α14, а аминокислотная последовательность имеет гомологию приблизительно на 87% (144/166) относительно HuIFN-α14. При сравнении с HuIFN-α2b, наиболее широко используемым человеческим интерфероновым продуктом, гомология составляет приблизительно 89% на нуклеотидном уровне (445/498) и приблизительно 81% (135/166) на аминокислотном уровне, как показано на Фиг.3.
Относительно синтетического IFN-альфа-con-1 (консенсусного интерферона) Новаферон имеет приблизительно 91% идентичности последовательности на нуклеотидном уровне (453/498) и приблизительно 84% идентичности последовательности на аминокислотном уровне (140/166).
Как описано подробно в экспериментальном разделе ниже, полинуклеотидная последовательность (SEQ ID No: 1) была выбрана из ДНК-шаффлинг-библиотеки человеческого интерферона, тип I. Кратко, белок Новаферон получали путем транфекции клеток хозяина рекомбинантным вектором, содержащим полную полинуклеотидную последовательность SEQ ID No: 1. Белок Новаферон, содержащийся в супернатанте линии клеток хозяина, очищали, и было показано, что он проявляет биологические активности подобно человеческим интерферонам, как например противовирусную и антипролиферативную функции.
Полинуклеотид и варианты
Новая полинуклеотидная последовательность/молекула нуклеиновой кислоты по настоящему изобретению состоит из 498 нуклеотидов, которые показаны на Фиг.1 (SEQ ID No: 1). С использованием предложенной в данном описании информации, такой как нуклеотидная последовательность, молекула нуклеиновой кислоты по настоящему изобретению, кодирующая белок Новаферон (SEQ ID No: 2), может быть получена путем рекомбинантной экспрессии, химического синтеза или путем использования других стандартных методик молекулярной биологии, таких как методики для ДНК-мутагенеза.
Данное изобретение, в дополнение к выделенной молекуле нуклеиновой кислоты (SEQ ID No: 1), также включает молекулы ДНК, имеющие последовательности, отличающиеся от последовательности ДНК, описанной в SEQ ID No: 1, но, вследствие вырожденности генетического кода, все еще кодирующие ту же самую или по существу ту же самую аминокислотную последовательность белка Новаферона (SEQ ID No: 2). Генетические коды и видоспецифические предпочтения кодонов хорошо известны в данной области техники. Таким образом, общепринятой практикой для специалиста в данной области техники будет создание вырожденных вариантов последовательностей ДНК, отличающихся от последовательности ДНК из SEQ ID No: 1, например, с целью оптимизации экспрессии кодонов для конкретного хозяина (например, чтобы изменить кодоны в человеческой мРНК до таковых, которые предпочтительны для бактериального хозяина, такого как E.coli).
Кроме того, согласно изобретению предложена выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность, показанную на ФИГ.1 (SEQ ID No: 1), или молекула нуклеиновой кислоты, имеющая последовательность, комплементарную нуклеиновокислотной последовательности в SEQ ID No: 1. Настоящее изобретение также обеспечивает информацию о нижеследующем и относится к рекомбинантным векторам, включающим в себя выделенные молекулы нуклеиновой кислоты по настоящему изобретению, и к клеткам хозяина, содержащим рекомбинантные векторы, а также к способам изготовления таких векторов и создания клеток хозяина, экспрессирующих белок Новаферон, и к применению клеток хозяина для получения Новаферона рекомбинантными методиками.
На основании нуклеиновокислотной последовательности по настоящему изобретению (SEQ ID No: 1, Фиг.1(А)) данное изобретение охватывает молекулы нуклеиновой кислоты, по существу являющиеся к тому же схожими, как например нуклеиновые кислоты, имеющие по меньшей мере приблизительно 85-95% или более идентичности последовательности по отношению к SEQ ID No: 1 после их оптимального выравнивания. Например, в одном аспекте нуклеиновые кислоты, имеющие приблизительно 93%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к нуклеотидной последовательность, показанной в SEQ ID No: 1, находятся в пределах объема изобретения независимо от того, кодируют ли они белки или полипептиды, имеющие биологические активности, схожие с Новафероном (такие активности включают, но этим не ограничиваются, повышенную противовирусную, антипролиферативную и противоопухолевую функции по сравнению с HuIFN). Такие молекулы нуклеиновой кислоты могли бы быть использованы, например, в качестве зондов для определения мРНК в клетках, уже трансфецированных вектором, содержащим нуклеотидную последовательность по настоящему изобретению, для получения Новаферона. Другими словами, эти нуклеиновокислотные последовательности, по меньшей мере приблизительно на 93%, 95%, 96%, 97%, 98% или 99% идентичные последовательности, показанной в SEQ ID No: 1, могли бы быть использованы в качестве маркеров для определения экспрессии гетерологических генов в клетке-хозяине.
Кроме того, изобретение включает полинуклеотид, содержащий любую часть из по меньшей мере приблизительно 30 следующих один за другим нуклеотидов, предпочтительно из по меньшей мере приблизительно 50 следующих один за другим нуклеотидов, из SEQ ID No: 1.
В более общем случае это изобретение включает и охватывает фрагменты любых и всех выделенных молекул нуклеиновой кислоты, которые идентичны неполной(ым) последовательности(ям) нуклеотидной последовательности, показанной на ФИГ. 1 (SEQ ID No: 1). В одном воплощении длина таких фрагментов может составлять по меньшей мере приблизительно 15 нуклеотидов, и они полезны в качестве диагностических зондов и праймеров, которые рассмотрены в данном описании. Более того, это изобретение включает и охватывает более длинные фрагменты, составляющие приблизительно 50 нуклеотидов или более по длине.
В дополнение к нуклеиновокислотной последовательности, описанной в SEQ ID No: 1, кодирующей белок Новаферон, настоящее изобретение также включает, но этим не ограничивается, нуклеиновокислотные последовательности, кодирующие аминокислотную последовательность полного белка Новаферона вместе с дополнительными аминокислотами/пептидом(ами)/полипептидом(ами), например добавленной секреторной лидерной последовательностью.
Кроме того, в данное изобретение включены последовательности нуклеиновых кислот, имеющие нуклеиновокислотную последовательность, описанную в SEQ ID No: 1, а также дополнительные некодирующие последовательности, включая, например, но этим не ограничиваясь, интроны и некодирующие 5'- и 3'-последовательности, такие как транскрибируемые, нетранслируемые последовательности, которые играют роль в транскрипции, процессинге мРНК (т.е. сплайсинге и сигналах полиаденилирования, связывании с рибосомами и стабилизации мРНК), и дополнительные кодирующие последовательности, которые кодируют дополнительные аминокислоты с функциональностями или без них.
Кроме того, настоящее изобретение относится к вариантам молекул нуклеиновой кислоты по настоящему изобретению (SEQ ID No: 1), которые кодируют части, аналоги или производные белка Новаферона. Варианты могут быть получены путем скрининга шаффлинг-библиотеки для интерферонов или с использованием методик мутагенеза или/и других известных методик, описанных в данной области техники.
Как объяснено выше, такие варианты могут включать варианты, получаемые путем вставки, делеции или замены нуклеотидов. Вставки, делеции или замены могут затрагивать один или более нуклеотидов. Эти мутации могут иметь место по 5'- или 3'-концевым положениям ссылочной нуклеотидной последовательности или где-либо еще между этими конечными положениями, разбросанными либо по отдельности среди нуклеотидов в ссылочной последовательности, либо в одной или более следующих одна за другой группах в пределах ссылочной последовательности. Изменения могут приводить к получению консервативных или неконсервативных аминокислотных замен, делеции или добавок. Особенно предпочтительными среди них являются молчащие замены, добавки и/или делеции, которые не оказывают влияния на свойства и активности белка Новаферона или его частей. Также особенно предпочтительны в этом отношении консервативные замены.
Согласно одному аспекту изобретения предложена выделенная молекула нуклеиновой кислоты, содержащая полинуклеотид, имеющий нуклеотидную последовательность, по меньшей мере на 93% идентичную и более предпочтительно по меньшей мере приблизительно на 95%, 96%, 97%, 98% или 99% идентичную полинуклеотиду, выбранному из группы, состоящей из: (а) нуклеотидной последовательности, кодирующей белок Новаферон, имеющий полную аминокислотную последовательность в SEQ ID No: 2 (т.е. положения 1-166 SEQ ID No: 2); и (б) нуклеотидной последовательности, кодирующей биологически активный фрагмент белка из (а); и (в) нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей в (а) или (б), выше.
Вследствие вырожденности генетического кода специалисту обычной квалификации в данной области техники сразу же будет очевидно, что большое количество молекул нуклеиновых кислот, имеющих последовательность, по меньшей мере приблизительно на 93%, 95%, 96%, 97%, 98% или 99% идентичную нуклеиновокислотной последовательности из нуклеиновокислотной последовательности, показанной в ФИГ. 1 (SEQ ID No: 1), будет кодировать белок, имеющий активность, схожую или идентичную белку Новаферону. В действительности, поскольку все вырожденные варианты кодируют один и тот же белок, это факт будет очевиден специалисту даже без проведения сравнительного анализа. В данной области техники также будет очевидно, что среди таких молекул нуклеиновой кислоты, которые не являются вырожденными вариантами, разумное количество также будет кодировать белок, имеющий интерфероноподобные биологические активности. Это объясняется тем, что вероятность аминокислотных замен в отношении значительного воздействия на белковую функцию (например, замена одной алифатической аминокислоты на другую алифатическую аминокислоту) либо мала, либо ее нет, как дополнительно описано ниже, и специалист полностью осведомлен об этом. Например, руководство, касающееся того, как сделать фенотипически молчащие аминокислотные замены, предложено Bowie и др. (70), где авторы показывают, что многие белки толерантны к аминокислотным заменам.
Белковые и полипептидные варианты и конструкции
Настоящее изобретение охватывает белок Новаферон с SEQ ID No: 2 и белковые или полипептидные варианты, по существу сходные с ним, как например несуществующие в природе белки, имеющие по меньшей мере приблизительно 85-95% или более идентичности аминокислотной последовательности по отношению к SEQ ID No: 2. Например, несуществующие в природе белки, имеющие по меньшей мере приблизительно 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к аминокислотной последовательности, показанной в SEQ ID No: 2, находятся в пределах объема изобретения. Кроме того, белок Новаферон по изобретению может быть структурно модифицирован путем слияния его с другими белками или белковыми фрагментами либо другими молекулами с целью усиления его функций и свойств. Примеры включают, но этим не ограничиваются, слияние его с другими белками/белковыми фрагментами с целью увеличения экспрессии или с целью дальнейшей стабилизации белка Новаферона.
В одном воплощении Новаферон-кодирующая нуклеиновокислотная последовательность и/или белки Новаферона по изобретению могут быть помечены меткой, отличающейся от остова. "Меченый" в данном описании означает, что структура нуклеиновокислотной последовательности (SEQ ID No: 1) или белка Новаферона (SEQ ID No: 2) соединена по меньшей мере с одним элементом, изотопом или другими химическими реагентами (метками) для того, чтобы сделать возможной детекцию данной структуры. В общем случае метки делятся на три класса: а) изотопные метки, которые могут представлять собой радиоактивные или тяжелые изотопы; б) иммунные метки, которые могут представлять собой антитела или антигены; и в) цветные или флуоресцентные красители. Метки могут быть введены в структуру по любому положению.
После получения белок Новаферон также может быть ковалентно модифицирован. Один тип ковалентной модификации включает обработку белка Новаферона органическим агентом для получения производных, способным взаимодействовать с выбранными боковыми цепями или N- либо C-концевыми остатками белка Новаферона. Получение производных с использованием бифункциональных агентов является полезным, например, для перекрестного связывания белка Новаферона с нерастворимой в воде матрицей или поверхностью носителя с целью применения в очистке антител против Новаферона или скрининг-анализах. Обычно используемые перекрестно связывающие агенты включают 1,1-бис(диазоацетил)-2-фенилэтан, глутаровый альдегид, N-гидроксисукцинимидные сложные эфиры (например, эфиры с 4-азидосалициловой кислотой), гомобифункциональные имидоэфиры, включая дисукцинимидиловые эфиры, такие как 3,3'-дитиобис(сукцинимидилпропионат), бифункциональные малеимиды, такие как бис-N-малеимидо-1,8-октан, и такие агенты, как метил-3-[(п-азидофенил)дитио]пропиоимидат.
Другие модификации белка Новаферона включают деамидирование остатков глутаминил и аспарагинил до соответствующих остатков глутамил и аспартил, соответственно; гидроксилирование пролина и лизина; фосфорилирование гидроксильных групп остатков серил или треонил; метилирование аминогрупп боковых цепей лизина, аргинина и гистидина (71); ацетилирование N-концевого амина и амидирование любой C-концевой карбоксильной группы.
Другой тип ковалентной модификации белка Новаферона по настоящему изобретению включает изменение нативной картины гликозилирования данного белка. Этого можно достичь, например, путем (1) делегирования и/или добавления одной или более углеводных группировок, обнаруженных в нативной последовательности белка Новаферона, или (2) добавления и/или делетирования одного или более сайтов гликозилирования, которых нет в нативной последовательности белка Новаферона.
Добавление сайтов гликозилирования в белок Новаферон может быть достигнуто путем изменения аминокислотной последовательности белка Новаферона. Это изменение может быть сделано, например, путем добавления одного или более остатков серина или треонина либо замены на один или более остатков серина или треонина в нативной последовательности белка Новаферона (для сайтов O-гликозилирования). Такое изменение аминокислотной последовательности белка Новаферона может быть достигнуто посредством изменений на уровне ДНК, в частности путем введения мутаций в последовательность ДНК, кодирующую белок Новаферон, по предварительно выбранным нуклеотидным основаниям с тем, чтобы измененные кодоны транслировались бы в желаемые аминокислоты.
Другим способом увеличения количеств углеводных группировок на белке Новафероне является химическое или ферментативное связывание гликозидов с белком. Такие способы описаны в данной области техники, например, уже в 1981 году Aplin JD и Wriston JC Jr. описали получение, свойства и применения углеводных конъюгатов белков и липидов (72).
Удаление углеводных группировок, присутствующих на белке Новафероне, может быть достигнуто химически или ферментативно или путем мутационной замены кодонов, кодирующих аминокислотные остатки, которые служат в качестве мишеней для гликозилирования. Методики химического дегликозилирования известны в данной области техники и описаны, например, Edge AS и др. (73). Ферментативного отщепления углеводных группировок от полипептидов можно достичь путем использования ряда эндо- и экзогликозидаз, как описано Thotakura и др. (74).
Такие дериватизированные конструкции могут включать группировки, улучшающие растворимость, всасывание, проникновение через гематоэнцефалический барьер, биологический период полувыведения и т.д. Благодаря таким группировкам или модификациям белка Новаферона можно альтернативно устранить или ослабить любые возможные нежелательные побочные эффекты белка и тому подобное. Группировки, способные опосредовать такие эффекты, описаны, например, в Remington: The Science and Practice of Pharmacy (75).
Другой тип ковалентной модификации Новаферона включает связывание белка Новаферона с одним из ряда небелковых полимеров, например полиэтиленгликолем, полипропиленгликолем или полиоксиалкиленами, например, способом, приведенным в патентах США №№4640835 (76), 4496689 (77), 4791192 (78) или 4179337 (79).
Кроме того, белок Новаферон по настоящему изобретению также может быть модифицирован способом с образованием химерных молекул, содержащих белок Новаферон, слитый с другой гетерологической полипептидной или аминокислотной последовательностью. В одном воплощении такая химерная молекула содержит слитую структуру белка Новаферона с полипептидом-меткой, что позволяет получить эпитоп, с которым может избирательно связываться антитело против метки. Эпитоп-метку обычно помещают на амино- или карбоксильном конце белка Новаферона. Наличие таких форм белка Новаферона с меченым эпитопом может быть задетектировано с использованием антитела против полипептида-метки. Кроме того, снабжение эпитопом-меткой дает возможность легко очищать белок Новаферон путем аффинной очистки с использованием антител против метки или аффинной матрицы другого типа, связывающейся с эпитопом-меткой. В альтернативном воплощении химерная молекула может содержать слитую структуру белка Новаферона с иммуноглобулином или конкретным участком/фрагментом иммуноглобулина. Например, для образования бивалентной формы химерной молекулы белок Новаферон может быть слит с Fc-участком молекулы IgG.
Различные полипептиды-метки и соответствующие им антитела хорошо известны в данной области техники. Примеры включают метки поли-гистидин (поли-гис) или поли-гистидин-глицин (поли-гис-гли); полипептид-метку flu-HA (гемагглютинина вируса гриппа) и антитело к ней 12СА5 (80); метку c-myc и 8F9, 3С7, 6Е10, G4, В7 и 9Е10 и антитела к ней (81); и метку гликопротеин D (gD) вируса простого герпеса и антитело к нему (82). Другие полипептиды-метки включают Flag-пептид (83); эпитопный пептид тубулина (84) и пептидную метку белка 10 Т7-гена (85).
Кроме того, белок Новаферон по настоящему изобретению может быть получен методиками химического синтеза, известными специалистам обычной квалификации в данной области техники. Например, полипептиды длиной приблизительно до 80-90 аминокислотных остатков включительно могут быть получены на имеющемся в продаже пептидном синтезаторе, модели 433А (Applied Biosystems, Inc., Foster City, CA, US). Кроме того, также имеются в продаже более длинные химически синтезированные пептиды до 120 остатков включительно, например, от Bio-syhthesis, Inc., Lewisville, TX, USA. Таким образом, как легко можно понять, полноразмерный зрелый белок Новаферон может быть получен синтетическим путем (например, в виде фрагментов, которые затем можно собрать воедино).
Следовательно, белок Новаферон по настоящему изобретению (SEQ ID No: 2) включает все белковые и полипептидные композиции и конструкции, имеющие ту же самую аминокислотную последовательность, которая описана в SEQ ID No: 2, невзирая на то, получены ли эти белки Новаферона и белковые производные с использованием методик химического синтеза и/или путем рекомбинантных методик из прокариотических или эукариотических клеток хозяина или других клеток и хозяев, включая, но этим не ограничиваясь, бактерии, дрожжи, растения, насекомые и клетки млекопитающих. В зависимости от хозяев, используемых в методе рекомбинантного получения, белки по настоящему изобретению могут быть гликозилированы или негликозилированы, пэгилированы или непэгилированы. К тому же, белки по изобретению также могут включать в себя, в некоторых случаях, изначально модифицированный остаток метионина как результат опосредованных хозяином процессов. Так, в данной области техники хорошо известно, что N-концевой метионин, кодируемый кодоном инициации трансляции, обычно удаляется с высокой эффективностью из всех белков после трансляции во всех эукариотических клетках. Несмотря на то, что N-концевой метионин большинства белков также эффективно удаляется в большинстве прокариотов, для некоторых белков этот процесс прокариотического удаления является неэффективным в зависимости от природы аминокислоты, с которой ковалентно связан N-концевой метионин.
Получение
Настоящее изобретение также относится к рекомбинантным векторам, которые состоят из выделенных молекул ДНК по настоящему изобретению, к клеткам хозяина, которые генетически конструируют/трансфецируют с использованием этих рекомбинантных векторов, и к получению белка Новаферона или его фрагментов посредством рекомбинантных методик. Вектором может быть, например, плазмида, фаг, вирусный или ретровирусный вектор. Ретровирусные векторы могут быть компетентны по репликации или дефектны по репликации. В последнем случае размножение вируса обычно будет происходить только в комплементирующих клетках хозяина. Примеры, подробно описывающие получение Новаферона, приведены ниже.
Предпочтительные векторы для экспрессии белка Новаферона по настоящему изобретению включают, но этим не ограничиваются, векторы, содержащие цис-действующие контрольные участки, эффективные для экспрессии в хозяине, оперативно связанные с полинуклеотидом для его экспрессии. Соответствующие транс-действующие факторы доставляются либо хозяином посредством комплементирующего вектора, либо самим вектором после введения в хозяина.
Описанная в настоящем изобретении нуклеиновокислотная последовательность (SEQ ID No: 1) может быть оперативно связана с соответствующим промотором. "Промотор" в данном описании означает любые нуклеиновокислотные последовательности, способные к связыванию с РНК-полимеразой и к инициации экстронной (обычно в прямом направлении (3')) транскрипции кодирующей последовательности для белка Новаферона в мРНК. Бактериальный промотор имеет участок инициации транскрипции, который обычно расположен проксимально 5'-концу кодирующей последовательности. Этот участок инициации транскрипции обычно включает сайт связывания с РНК-полимеразой и сайт инициации транскрипции. Последовательности, кодирующие ферменты метаболических путей, обеспечивают особенно полезные промоторные последовательности. Примеры включают промоторные последовательности для ферментов метаболизма сахаров, таких как галактоза, лактоза и мальтоза, и последовательности для ферментов биосинтеза, например триптофана. Также можно использовать промоторы из бактериофага, и они известны в данной области техники. В дополнение к этому также полезны синтетические промоторы и гибридные промоторы; например, промотор tac представляет собой гибрид промоторных последовательностей trp и lac. Кроме того, бактериальный промотор может включать существующие в природе промоторы небактериального происхождения, которые обладают способностью связываться с бактериальной РНК-полимеразой и инициировать транскрипцию. Предпочтительные бактериальные промоторы включают, но этим не ограничиваются, промоторы E.coli laci, trp, phoA и lacZ, Т3- и Т7-промоторы, промотор gpt, лямбда-PR, PL-промоторы и промотор trp.
Эукариотические промоторы имеют участок инициации транскрипции, который обычно расположен проксимально 5'-концу кодирующей последовательности, и ТАТА-бокс, обычно расположенный на расстоянии 25-30 пар оснований (п.о.) "вверх по течению" от сайта инициации транскрипции. Полагают, что ТАТА-бокс направляет РНК-полимеразу II на начало синтеза РНК с корректного сайта. Промотор млекопитающих также содержит промоторный элемент (энхансерный элемент) "вверх по течению", обычно расположенный в пределах 100-200 пар оснований "вверх по течению" от ТАТА-бокса. Расположенный "вверх по течению" промоторный элемент определяет скорость, с которой инициируется транскрипция, и может действовать в любой из двух ориентаций. Конкретное применение в качестве промоторов млекопитающих находят промоторы вирусных генов у млекопитающих, так как вирусные гены зачастую являются высокоэкспрессируемыми и обладают широким диапазоном хозяев. Примеры включают ранний промотор SV40 (обезьяний вирус 40), вирусный LTR-промотор опухоли молочной железы мыши. Предпочтительные промоторы клеток животных включают, но этим не ограничиваются, аденовирусный главный поздний промотор, промотор вируса простого герпеса и CMV (цитомегаловирусный) промотор. Среди известных эукариотических промоторов подходящими в этом отношении являются CMV немедленно ранний промотор, промотор фактора элонгации 1 альфа (EF1A), промотор тимидинкиназы HSV (вируса простого герпеса), ранний и поздний промоторы SV40 и промоторы ретровирусных LTR, как например таковые из вируса саркомы Рауса ("RSV"). Предпочтительные промоторные последовательности для экспрессии в дрожжах включают индуцибельный промотор GAL1/10, промоторы гена алкогольдегидрогеназы, енолазы, глюкокиназы, глюкоза-6-фосфат-изомеразы, глицеральдегид-3-фосфат-дегидрогеназы, гексокиназы, фосфофруктокиназы, 3-фосфоглицерат-мутазы, пируваткиназы и кислой фосфатазы.
Кроме того, векторы для размножения и экспрессии обычно включают один или более селектируемых маркеров. Такие маркеры могут подходить для амплификации или векторы могут содержать дополнительные маркеры для этой цели. В этом отношении экспрессирующие векторы предпочтительно содержат один или более селектируемых маркерных генов с целью обеспечения фенотипической особенности для выбора трансфецированных клеток хозяина, хотя специалистам в данной области техники будет известно, что некоторые селектируемые в системах маркеры могут быть представлены на отдельных векторах. Предпочтительные маркеры включают, например, гены устойчивости к ампициллину (Amp), тетрациклину (Tet) или гигромицину (HYG) для культивирования в E.coli и других бактериях. Селектируемые в дрожжах маркеры включают ADE2, HIS4, LEU2, TRP1 и ALG7, которые придают устойчивость к туникамицину; ген неомицин-фосфотрансферазы, который придает устойчивость к G418; и ген CUP1, позволяющий дрожжам расти в присутствии ионов меди. Селектируемые в клетках животных маркеры включают ген дигидрофолатредуктазы (DHFR), гены устойчивости к неомицину (Neo) или гигромицину (HYG).
Кроме того, векторы для размножения и экспрессии обычно содержат один или более сайтов инициации, терминации, транскрипции и, в транскрибируемом участке, сайт связывания с рибосомой для трансляции. Кодирующая часть транскриптов, экспрессируемых посредством этих конструкций, предпочтительно включает кодон инициации трансляции в начале и терминирующий кодон (UAA, UGA или UAG), соответственно расположенный на конце транслируемой последовательности ДНК. Выбор промоторов, терминаторов, селектируемых маркеров, векторов и других элементов представляет собой вопрос общепринятого конструирования, соответствующего уровню обычной квалификации в данной области техники. Многие такие элементы описаны в литературе и доступны у коммерческих поставщиков.
Следующие далее векторы имеются в продаже, и они предпочтительны для применения в бактериях: pBV220 (86) и его производные от Shanghai Sangon; pQE разновидности от Qiagen; рЕТ-векторы от Qiagen; pBS-векторы, Phagescript-векторы, Bluescript-векторы, pNH8A, pNH16a, pNH18A, pNH46A от Stratagene; и ptrc99a, pKK223-3, pKK233-3, pDR540, pRIT5 от Pharmacia. Среди предпочтительных эукариотических векторов находятся pCI-векторы от Promega, pcDNA-векторы от Invitrogen, pSV2CAT, pOG44, pXT1 и pSG от Stratagene; и pSVK3, pBPV, pMSG и pSVL от Pharmacia. Эти векторы перечислены исключительно в качестве примеров, чтобы продемонстрировать, что многие имеющиеся в продаже и хорошо известные векторы доступны специалистам в данной области техники для применения в получении белка Новаферона, описанного в настоящем изобретении, генетическими/рекомбинантными способами.
В некоторых предпочтительных воплощениях в этом смысле векторы обеспечивают средства для специфической экспрессии. Такая специфическая экспрессия может быть индуцибельной экспрессией или экспрессией только в некоторых типах клеток либо может быть как индуцибельной, так и клеточно-специфической. Особенно предпочтительными среди индуцибельных векторов являются векторы, которые могут быть индуцированы для экспрессии под действием факторов окружающей среды, которыми легко манипулировать, таких как температура и питательные добавки. Ряд векторов, подходящих для этого применения, в том числе конститутивный и индуцибельный экспрессирующие векторы для применения в прокариотических и эукариотических хозяевах, хорошо известны и регулярно применяются специалистами в данной области техники.
Вектор, содержащий последовательность ДНК, описанную в SEQ ID No: 1, например, а также соответствующий промотор и другие соответствующие контрольные последовательности могут быть введены с использованием ряда известных в данной области техники методик в соответствующую клетку хозяина, подходящую для экспрессии желаемого белка. Характерные примеры таких подходящих хозяев включают бактериальные клетки, такие как E.coli, Bacillus subtilis, клетки Streptomyces; дрожжевые клетки, такие как клетки Pichia pastoris; клетки насекомых, такие как клетки Drosophila S2 и Spodoptera Sf9; клетки млекопитающих, такие как СНО (яичников китайского хомячка) и COS (фибробласты африканской зеленой мартышки); и клетки растений. Хозяева для целого ряда экспрессирующих конструкций хорошо известны, и специалисты в данной области техники будут способны с использованием информации, описанной в настоящем изобретении, легко выбрать хозяина для экспрессии белка Новаферона, описанного в SEQ ID No: 2.
Клетки хозяина могут быть сконструированы генетически с целью включения Новаферон-кодирующих полинуклеотидов и экспрессии белков Новаферона по настоящему изобретению. Например, Новаферон-кодирующие полинуклеотиды могут быть введены в клетки хозяина с использованием известных в данной области техники методик транфекции. Такие методы описаны во многих стандартных лабораторных руководствах, как например рассмотренные Kingston (87). Новаферон-кодирующие полинуклеотиды могут быть введены/трансфецированы сами по себе или с другими полинуклеотидами. Такие другие полинуклеотиды могут быть введены независимо, введены совместно или введены одновременно с Новаферон-кодирующими полинуклеотидами, описанными в SEQ ID No: 1.
Например, Новаферон-кодирующие полинуклеотиды по изобретению могут быть трансфецированы в клетки хозяина вместе с отдельным полинуклеотидом, кодирующим селектируемый маркер для совместной транфекции и селекции данного маркера в клетках млекопитающих. Альтернативно, Новаферон-кодирующие полинуклеотиды могут быть включены в вектор, содержащий кодирующую селектируемый маркер последовательность ДНК, для индукции размножения в клетках хозяина.
Сконструированные клетки хозяина, трансфецированные с использованием векторов, содержащих Новаферон-кодирующий полинуклеотид, можно культивировать в традиционных питательных средах, которые могут быть модифицированы конкретно для активации промоторов, отбора трансформантов или амплификации генов-мишеней. Подбирают условия культивирования, такие как температура, рН и т.д., которые подходят для выбранных клеток хозяина с целью экспрессии белка Новаферона по настоящему изобретению.
Могут быть инкорпорированы подходящие сигналы секреции, и они могут совместно экспрессироваться с белком Новафероном для стимуляции секреции транслированного белкового полипептида в просвет эндоплазматического ретикулума, в периплазматическое пространство или во внеклеточное окружение.
Очистка
Для экспрессии целевого рекомбинантного белка обычно выбирают подходящий тип клеток хозяина в зависимости от природы целевого белка и учета других условий, таких как стоимость получения, наличие возможности легкого масштабирования, объем промышленного получения и т.д. Затем отбирают клоны трансфецированных клеток, экспрессирующих целевой белок с наиболее высоким выходом, окончательный клон с оптимальной экспрессией называют экспрессирующей целевой белок клеточной линией и используют для получения целевого белка. Клеточную линию, экспрессирующую целевой белок, растят в среде, содержащей различные питательные вещества. С целью оптимального роста клеток и/или оптимальной экспрессии целевого белка используют различные агенты или условия, чтобы индуцировать селективный промотор, инкорпорированный вместе с последовательностью кДНК целевого белка в трансфецирующий вектор. Если типом клетки-хозяина/экспрессирующей системой являются бактерии, культивируемые клетки собирают из этой среды обычно путем центрифугирования. Основную часть собранных клеток разрушают физическими или химическими способами и собранные неочищенные экстракты, содержащие синтезированный целевой белок, сохраняют для дальнейшей очистки белка. Методы, применимые для разрушения микробных клеток, включают, но этим не ограничиваются, циклическую обработку путем замораживания-оттаивания, ультразвуковое облучение, механическое разрушение или использование лизирующих клетки агентов. Такие методы хорошо известны специалистам в данной области техники.
Авторы изобретения использовали бактерии E.coli в качестве клетки-хозяина для экспрессии рекомбинантного белка Новаферона. Как описано ниже, E.coli трансфецировали с использованием вектора, который содержал Новаферон-кодирующую полинуклеотидную последовательность, и один штамм E.coli, который обладал оптимальной экспрессией белка Новаферона, был выбран для получения белка Новаферона. Будучи синтезированным, белок может сохраняться в цитоплазме в виде нерастворимых гранул или может секретироваться в цитоплазму в растворимой форме. В первом случае гранулы извлекают после лизиса телец включения и подвергают денатурации с использованием, например, гуанидинизотиоцианата или мочевины. Рефолдинга денатурированного полипептида/белка Новаферона далее достигают, разбавляя денатурирующий агент избытком разбавляющего раствора или диализуя против раствора мочевины и комбинации восстановленного и окисленного глутатиона с последующим диализом против забуференного физиологического раствора. Во втором случае белок может быть непосредственно извлечен без денатурирующего агента из периплазматического пространства в растворимой и функциональной форме после разрушения собранных клеток. Растворимый белок Новаферон, избежавший применения методики денатурации и рефолдинга, является не поврежденным и не содержащим деформированных или неправильно свернутых белковых молекул.
Авторы изобретения обнаружили, что значительная часть синтезированного белка Новаферона, полученного в клеточной линии E.coli, секретировалась в цитоплазму. Эту часть затем очищали, как описано ниже.
Анализы активности и медицинские применения
Как указано выше, белок Новаферон показывает гомологию последовательности со многими членами интерферонового семейства, в частности с интерфероновым белком, транслированным с мРНК HuIFN-α14 (ФИГ.2). Показано, что HuIFN-α имеет широкий диапазон биологических активностей, включая противовирусную, антипролиферативную и иммуномодулирующую активности (10).
При такой гомологии с HuIFN-α можно ожидать, что Новаферон будет демонстрировать схожие с HuIFN-α биологические функции, включая, но этим не ограничиваясь, ингибирование опухолевой пролиферации, противовирусные активности, активацию NK-клеток и модулирование иммунной системы. Особую важность имеет не только сохранение HuIFN-α-подобных функциональных свойств, но также повышенная эффективность этих биологических функций белка Новаферона по сравнению с HuIFN-α. Таким образом, для проверки и определения эффективности его функциональных свойств биологические активности белка Новаферона были проверены с использованием классических и общепринятых in vitro анализов, разработанных для детекции противовирусных и антипролиферативных свойств. Как описано в экспериментальном разделе ниже, эффективность in vivo антипролиферативных свойств белка Новаферона далее наблюдали на животных моделях различных типов рака человека и сравнивали с HuIFN-a, а также с химическим противораковым агентом в некоторых экспериментах.
В данной области техники хорошо известно большое количество подходящих анализов для определения активности HuIFN. Авторы изобретения использовали клеточные аналитические системы in vitro для определения противовирусной и антипролиферативной активностей. Те же анализы in vitro были использованы для всех методик и экспериментов, относящихся к настоящему изобретению, которые включали, но не ограничивались этим, скрининг шаффлинг-библиотеки генов человеческого интерферона, тип I, селекцию Новаферона из экспрессированных белков шаффлинг-библиотеки генов человеческого интерферона, тип I, и определение биологических активностей чистого рекомбинантного белка Новаферона.
Имеется много анализов, с помощью которых измеряют противовирусные активности тестируемых образцов/агентов посредством наблюдения за степенью устойчивости клеток к вирусам (88). Были использованы три принципиальных биологических анализа для измерения противовирусных активностей HuIFN и их гибридов. Они классифицируются согласно способам определения различных аспектов вируса на культивируемые клетки.
В анализе определения ингибирования вирусиндуцированных цитопатических эффектов измеряют степень уменьшения вирусиндуцированных литических цитопатических эффектов на культивируемые клетки с предварительной обработкой IFN. Этот анализ может быть выполнен в 96-луночных планшетах (89), и он широко используется для рекомбинантного HuIFN-α, поскольку обеспечивает простой метод скрининга большого количества образцов.
Ингибирование образования вирусных бляшек представляет собой другой метод количественного определения противовирусных активностей HuIFN в тканевых культурах. Результаты анализа уменьшения количества бляшек не зависят от множественности заражения. Более того, 50%-ное уменьшение в бляшкообразовании измеряется с высокой точностью. Использование повсеместно распространенного вируса везикулярного стоматита (VSV) для индуцирования бляшкообразования, например, дает возможность определять профиль перекрестно-видовой активности конкретного рекомбинантного IFN путем скрининга ряда клеточных линий различных видов животных (90).
Третий анализ основан на определении уменьшения выхода вируса. Обычно продуцирование вируса измеряют в течение единичного цикла клеточного роста по количеству высвободившегося вируса. Этот анализ особенно полезен для тестирования противовирусных активностей IFN против вирусов, которые не вызывают цитопатических эффектов или которые не образуют бляшки в культурах клеток-мишеней. В этом тесте, однако, множественность заражения влияет на кажущуюся степень защиты, вызываемую фиксированной концентрацией IFN (91).
Противовирусные активности Новаферона измеряли с использованием стандартного анализа ингибирования цитопатического эффекта, применяя WISH-клетки и вирус везикулярного стоматита (VSV). Противовирусные активности определяли и калибровали путем использования стандартных ссылочных образцов международных стандартов ВО3: 95/650 (rHuIFN-α2a) и 94/786 (rHuIFN-α консенсусный). Одну единицу противовирусной активности определяют как количество белка, необходимое для достижения 50% ингибирования цитопатических эффектов VSV на культивируемые клетки. Как дополнительно описано ниже, активность белка Новаферона составляла 2,5×109 IU/мг, что приблизительно в 12,5 раз больше, чем активность HuIFN-α2b. Эти тесты демонстрируют, что противовирусные свойства Новаферона значительно улучшены по сравнению с HuIFN-α2b. Эта повышенная эффективность в отношении вируса, проявляемая белком Новафероном, обеспечивает основу для предполагаемых улучшенных противовирусных эффектов in vivo в отношении людей. Основываясь на природе HuIFN, разумно ожидать наличия у Новаферона очень широкого противовирусного профиля. Другими словами, Новаферон должен быть более эффективным по отношению к широкому диапазону вирусов, чем природные HuIFN. Повышенная противовирусная эффективность Новаферона может выразиться в виде улучшенных противовирусных эффектов или улучшенных терапевтических эффектов в клинических условиях для пациентов с различными вирусными заболеваниями.
Как объяснено выше, IFN также ингибируют клеточную пролиферацию и оказывают мощные противоопухолевые эффекты, используя ряд механизмов. В данной области техники утверждены и хорошо описаны несколько антипролиферативных тестов in vitro с использованием систем клеточных культур. Клеточная пролиферация в этих анализах может быть измерена путем подсчета количества клеток; биологического анализа с использованием кристаллического фиолетового (92, 93); химической чувствительности к красителю нейтральному красному (neutral red dye) (94-96); включения радиоактивных меченых нуклеотидов (97); включения 5-бром-2'-дезоксиуридина (BrdU) в ДНК пролиферирующих клеток (98); использования солей тетразолия (99, 100).
Линия человеческих лимфобластоидных клеток Дауди очень чувствительна к антипролиферативному эффекту HuIFN-α, и ее рост в суспензионных культурах облегчает определение количества ее клеток (101). Эта клеточная линия используется для измерения антипролиферативной активности HuIFN-α и гибридов в течение многих лет (102). Другие клеточные линии также используются для тестирования антипролиферативной активности тестируемого агента.
Антипролиферативные активности белка Новаферона наблюдали in vivo, отслеживая ингибирование роста опухолевой массы под действием введения Новаферона в животные модели с различными ксенотрансплантатами человеческих опухолей. Противоопухолевые эффекты in vivo Новаферона сравнивали с HuIFN-α2b и, в некоторых моделях ксенотрансплантатов, также с химическим противоопухолевым агентом.
Как подробно описано ниже, авторы изобретения обнаружили, что антипролиферативная активность in vitro Новаферона, измеренная путем использования стандартного метода с клетками Дауди, была в 400 раз более сильной, чем у природного HuIFN-α2b, который демонстрирует вероятно наиболее сильные антипролиферативные активности среди всех природных HuIFN. Повышенная антипролиферативная эффективность Новаферона имела широкий и универсальный характер, поскольку он демонстрировал более эффективное и повышенное ингибирование, чем природный HuIFN-α2b, для всех человеческих раковых клеточных линий, протестированных in vitro авторами изобретения. Это указывает на то, что эффективное ингибирование человеческого рака Новафероном не является селективным. Несмотря на то, что степень его повышенной антипролиферативной активности в отношении всех тестируемых типов человеческих раковых клеточных линий варьировала, Новаферон обладает потенциалом противоракового агента широкого действия в клинических условиях. Это представляет собой значительное преимущество перед химическими противораковыми агентами, моноклональными антителами и другими противораковыми агентами, направленными на конкретные мишени.
В экспериментах на животных моделях с ксенотрансплантатами, описанных ниже, дополнительно установлено, что:
(1) антипролиферативные эффекты in vivo Новаферона были значительно усилены или более эффективны по сравнению с природным HuIFN-α2b;
(2) антипролиферативные эффекты in vivo Новаферона в более низких дозах были лучше, чем у тестируемого химического агента 5-фторурацила (5-FU) в одной и той же ксенотрансплантатной модели;
(3) применение Новаферона дало возможность достичь более 90% ингибирования ракового роста в ксенотрансплантатных моделях, однако он не индуцировал уменьшения массы, изменений в активности и другие негативные побочные эффекты у лечемых животных, что резко контрастировало со значительным уменьшением массы и снижением активности у 5-FU-лечемых животных.
Эти результаты показывают, что антипролиферативные свойства in vitro и in vivo Новаферона значительно усилены по сравнению с природным HuIFN-α2b. Повышенная антипролиферативная эффективность Новаферона выражается в эффективном ингибировании (более 90%) роста опухоли человека в мышиной животной модели, и, по-видимому, это ингибирование действует в очень широких пределах для всех типов тестируемого человеческого рака и лучше, чем у классического химического противоракового агента 5FU. Эти результаты также показывают, что эффективное ингибирование роста раковых клеток Новафероном очень специфично по отношению к раковой клетке, но не по отношению к нормальным клеткам, что подтверждается наблюдением нормального приема корма и активного поведения и отсутствием какого-либо уменьшения массы у Новаферон-лечемых животных. Поэтому Новаферон имеет потенциал к воздействию на все или большинство типов рака человека.
В предпочтительном воплощении полноразмерная молекула(ы) или неполная молекула(ы) белка Новаферона (SEQ ID No: 2), полученная рекомбинантными методиками с использованием полинуклеотидной последовательности SEQ ID No. 1 или химически синтезированная, могла бы быть применена для лечения и/или предупреждения любых и/или всех опухолей и типов рака человеческого происхождения или нечеловеческого происхождения, у людей и/или не являющихся людьми видов. Эти опухоли, например, включают, но этим не ограничиваются, остеогенную саркому; множественную миелому; болезнь Ходжкина; узелковую слабо дифференцируемую лимфому; острый лимфоцитарный лейкоз; острый миелоидный лейкоз; рак молочной железы; меланому; папиллому; рак носоглоточной области, рак толстой кишки, рак печени и меланому.
В другом воплощении полноразмерная молекула(ы) или неполная молекула(ы) белка Новаферона (SEQ ID No: 2), полученная рекомбинантными методиками с использованием полинуклеотидной последовательности SEQ ID No: 1 или химически синтезированная, могла бы быть применена для лечения и/или предупреждения любых и/или всех вирусных заболеваний у людей и/или не являющихся людьми видов. Примеры чувствительных вирусных инфекций включают, но этим не ограничиваются, вирусный энцефаломиокардит, грипп и другие вирусные инфекции дыхательных путей, бешенство и другие вирусные зоонозы, и арбовирусные инфекции, а также герпетический кератит, острый геморрагический конъюнктивит, ветряная оспа плюс опоясывающий лишай (varicella zoster) и гепатит В и С, SARS (атипичная пневмония) и птичий грипп, синдром человеческого иммуннодефицита (СПИД, ВИЧ).
В другом воплощении полноразмерная молекула(ы) или неполная молекула(ы) белка Новаферона (SEQ ID No: 2), полученная рекомбинантными методиками с использованием полинуклеотидной последовательности SEQ ID No: 1 или химически синтезированная, могла бы быть применена для лечения и/или предупреждения любых и/или всех расстройств иммунной системы у людей. Примеры иммунных расстройств включают, но этим не ограничиваются, ревматоидный артрит, множественный склероз и диабет при синдроме Шегрена. Кроме того, белок Новаферон также может быть применен для предотвращения отторжения "трансплантат против хозяина".
В другом воплощении полноразмерная молекула(ы) или неполная молекула(ы) белка Новаферона (SEQ ID No: 2), полученная рекомбинантными методиками с использованием полинуклеотидной последовательности SEQ ID No: 1 или химически синтезированная, могла бы быть применена для лечения и/или предупреждения, в качестве иммуноадъюванта, любых и/или всех ангиогенезных заболеваний. Примеры ангиогенезных заболеваний включают, но этим не ограничиваются, гемангиомы, опухолеиндуцированную неоваскуляризацию, возрастную дегенерацию желтого пятна и диабетическую ретинопатию.
Белок Новаферон, один или вместе в любыми другими белками/веществами-носителями или другими конструкциями, может быть введен людям и/или не являющимся людьми видам в любых фармацевтически приемлемых препаратах/композициях любыми способами введения/путями доставки, которые включают, но этим не ограничиваются, пероральный прием, ингаляцию, интраназальное распыление, внутрибрюшинную, внутривенную, внутримышечную инъекцию, инъекцию внутрь поражения или подкожную инъекцию.
Фармацевтические препараты/композиции, содержащие белок Новаферон в качестве активного ингредиента, могли бы быть изготовлены путем включения соответствующего твердого или жидкого носителя, в формах жидкости, твердого вещества, полутвердого вещества и/или любых других клинически приемлемых формах, таких как таблетки, пилюли, порошки, жидкие растворы или суспензии, липосомы, суппозитории, растворы для инъекции и инфузии. Новаферонсодержащие препараты/композиции могли бы быть изготовлены путем использования традиционных носителей, веществ, способов, описанных в данной области техники или обычно принятых практикой фармацевтической промышленности. Новаферонсодержащие препараты/композиции также могли бы быть изготовлены путем использования нетрадиционных способов, веществ, которые не описаны в данной области техники и также не используются фармацевтической промышленностью.
Например, парентеральные композиции обычно представляют собой вводимые инъекцией жидкости, состоящие из фармацевтически и физиологически приемлемых веществ, таких как вода, физиологический раствор, другие сбалансированные солевые растворы, водный раствор декстрозы, глицерина и т.д. К тому же, вводимые инъекцией жидкости также могли бы содержать, в дополнение к белку Новаферону, другие белки в качестве носителей, такие как человеческий сывороточный альбумин или препараты плазмы. Фармацевтические препараты/композиции также могут содержать минорные количества нетоксичных вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, консерванты и поддерживающие рН буферные агенты (например, ацетат натрия или сорбитанмонолаурат). Способы изготовления композиций хорошо известны в данной области техники и описаны, например, в Remington: The Science and Practice of Pharmacy. Phamaceutical Sciences (75).
Конкретные препараты/композиции на основе белка Новаферона будут определены в соответствии с планируемыми клиническими применениями и/или способами введения, и они могли бы быть изготовлены специалистом в данной области техники с использованием известных методик. Например, в дополнение к вводимым инъекцией жидкостям могут быть применены местные и пероральные композиции. Препараты для местного применения могут включать, но этим не ограничиваться, глазные капли, мази и спреи. Пероральные композиции включают, но этим не ограничиваются, формы жидкостей (например, сиропы, растворы или суспензии) или твердых веществ (например, порошки, пилюли, таблетки или капсулы). Для твердых препаратов/композиций традиционные нетоксичные твердые носители включают, но этим не ограничиваются, фармацевтические сорта маннита, лактозы, крахмала или стеарата магния. Реальные методики и/или способы изготовления этих препаратов/композиций известны или будут очевидны специалистам в данной области техники (75).
Фармацевтически приемлемые препараты/композиции белка Новаферона могут быть введены людям и/или не являющимся людьми видам рядом путей, которые включают, но этим не ограничиваются, пероральную, подкожную, внутривенную, интраназальную, трансдермальную, внутрибрюшинную, внутримышечную, внутрилегочную, вагинальную, ректальную или внутриглазную доставку, и в лечении ран путем прямого местного наложения.
Концентрации/количества белка Новаферона в препаратах/композициях могут варьировать от более 0 до 1,0 молярных и/или от более 0 до 100% (масс./масс.) в зависимости от клинической практики. Точные дозы, интервалы введения и продолжительность лечения каждым и/или всеми препаратами/композициями Новаферона будут определяться клиническими испытаниями, болезненными состояниями, статусом пациента и поставщиками медико-санитарной помощи. В предпочтительном воплощении вследствие деградации белка, системной, в сравнении с локализованной, доставки и скорости синтеза новых протеаз, а также возраста, массы тела, общего состояния здоровья, пола, питания, времени введения, взаимодействия лекарственных средств, тяжести состояния и т.д. могут быть необходимы корректировки на введение Новаферона, включая, но этим не ограничиваясь, индивидуальные и/или общие дозы, интервалы введения, продолжительность лечения и необходимые курсы лечения, и они будут уточнены с использованием общепринятого экспериментирования специалистами в данной области техники.
В предпочтительном воплощении период полувыведения белка Новаферона из кровотока после введения его в организм людей и/или не являющихся людьми видов может меняться. Изменения включают, но этим не ограничиваются, удлинение или укорочение периода полувыведения Новаферона in vivo. Удлинение периода полувыведения белка Новаферона in vivo может быть достигнуто различными путями, которые включают, но этим не ограничиваются:
(1) образование комплекса между молекулой Новаферона и моноклональным антителом. Такое антитело будет предпочтительно связано с белком Новафероном по сайтам, связь по которым принципиально не ухудшает его терапевтические функции (103);
(2) образование комплекса слияния Новаферона с другими белками/полипептидами. Молекула Новаферона может быть рекомбинантно слитой с другими белками/полипептидами, такими как фрагмент константного участка иммуноглобулина (Fc) (104);
(3) конъюгацию белка Новаферона. Например, белок Новаферон может быть конъюгирован с неантигенными полимерами, такими как полиэтиленгликоль или родственные полиалкиленгликольные группировки (105-108).
В другом предпочтительном воплощении с антителом, предпочтительно антителом против белка Новаферона, могло бы быть конъюгировано терапевтическое соединение. Терапевтическим соединением может быть цитотоксичный агент. В этом способе цитотоксичные агенты могут быть нацелены, путем связывания конъюгированного антитела с молекулами Новаферона, на ткань или клетки опухоли, таким образом разрушая и уменьшая количество пораженных клеток для достижения уменьшения симптомов рака. Цитотоксичные агенты включают, но этим не ограничиваются, цитотоксичные лекарственные средства, токсины или активные фрагменты таких токсинов и радиоактивные химические соединения. Подходящие ткосины и их соответствующие фрагменты включают цепь А дифтерийного токсина, цепь А экзотоксина, цепь А рицина, цепь А абрина, курцин, кротин, феномицин, эномицин и тому подобное.
В предпочтительном воплощении полноразмерная последовательность, неполные последовательности и/или регуляторная последовательность кодирующей белок Новаферон полинуклеотидной последовательности (SEQ ID No: 1) могут быть использованы для генотерапевтического введения любым специалистом в данной области техники. Применение антисмысловых последовательностей на основании кодирующей белок Новаферон полинуклеотидной последовательности (SEQ ID No: 1) также может быть использовано либо в виде генотерапевтических (т.е. для включения в геном), либо в виде антисмысловых композиций, как будет очевидно специалистам в данной области техники.
Что касается генотерапевтических применений, то гены вводят в клетки для достижения in vivo синтеза белков-мишеней, кодируемых этими генами. Традиционной генотерапией добиваются устойчивых терапевтических эффектов в результате разового лечения или повторного введения терапевтически эффективной ДНК или мРНК. С другой стороны, антисмысловые РНК и ДНК также могут быть использованы в качестве терапевтических агентов для блокирования экспрессии некоторых генов in vivo. Уже показано, что короткие антисмысловые олигонуклеотиды могут доставляться в клетки, где они действуют в качестве ингибиторов (109).
В предпочтительном воплощении кодирующая белок Новаферон полинукпеотидная последовательность (SEQ ID No: 1), полноразмерная или неполной длины, может быть использована в качестве ДНК-вакцин. Вообще вакцины на основе голых ДНК известны в данной области техники (110). Способы применений Новаферон-кодирующего гена (SEQ ID No: 1), полноразмерного или неполной длины, в качестве ДНК-вакцин хорошо известны специалисту обычной квалификации в данной области техники и включают, но этим не ограничиваются, помещение гена Новаферона или части гена Новаферона под контроль промотора для экспрессии полноразмерного белка Новаферона или белка Новаферона неполной длины у людей и/или не являющихся людьми видов.
Примеры
Следующие далее примеры служат для более полного представления способа применения описанного выше изобретения, а также для изложения наилучших способов, предполагаемых для осуществления различных аспектов данного изобретения. Понятно, что эти примеры никоим образом не ограничивают истинный объем этого изобретения, а скорее представлены для иллюстративных целей. Все ссылки, приведенные в данном описании, специально включены во всей своей полноте посредством ссылки.
Пример 1. ПЦР-амплификация генов человеческого IFN-α из лейкоцитарной кДНК человека
Общую мРНК экстрагировали из лейкоцитов периферической крови человека. Получение кДНК осуществляли с использованием набора Advantage™ RT-for-PCR (Clontech, Mountain View, CA, US) и синтетических праймеров кДНК (олиго-dT18) в соответствии с рекомендациями производителя.
Амплификацию кДНК человеческого IFN-α осуществляли с использованием ПЦР-технологии на термоамплификаторе MJ РТС, применяя следующие условия: 2,5 мкл 10х pfx буфера для амплификации (Invitrogen, Carlsbad, CA, US); 0,75 мкл 10 мМ dNTP (декоксинуклеотидтрифосфаты); 0,5 мкл 25 мМ MgSO4; 0,25 мкл Platinum pfx ДНК-полимеразы (2,5 ед/мкл; Invitrogen, Carlsbad, CA, US); 0,75 мкл кДНК; 0,75 мкл 5'-праймера (10 мкМ; IFNaO5: 5'-TGGTGCTCAGCT(A/G)CAAGTC-3'), (SEQ ID No: 3); 0,75 мкл смеси 3'-праймеров (1,7 мкМ каждый:
IFNaO3-1: 5'-AATCATTTCCATGTTG(A/G)ACCAG-3' (SEQ ID No: 4);
IFNaO3-2: 5'-AATCATTTCCCGGTTGTACCAG-3' (SEQ ID No: 5);
IFNaO3-3: 5'-AATCATTTCCATGTTGAAACAG-3' (SEQ ID No: 6);
IFNaO3-4: 5'-AATCATTTCAAGATGAGCCCAG-3' (SEQ ID No: 7);
IFNaO3-5: 5'-AATGATnTCATGTTGAACCAG-3' (SEQ ID No: 8);
IFNaO3-6: 5'-AATCATTT(C/G)(C/G)ATGTTGAACCAG-3' (SEQ ID No: 9);
IFNaO3-7: 5'-GATCATTTCCATGTTGAATGAG-3' (SEQ ID No: 10);
IFNaO3-8: 5'-GAGTCGTTTCTGTGTTGGATCAG-3' (SEQ ID No: 11).
Амплифицированые ПЦР-продукты подвергали электрофорезу в 1,0%-ном агарозном геле, вырезали, очищали от геля и клонировали в вектор pCRII-TOPO или pCR-4-TOPO (Invitrogen, Carlsbad, CA, US) в соответствии с рекомендациями производителя. Секвенирование в автоматическом режиме осуществляли на автоматическом секвенаторе ABI (РЕ Applied Biosystems, CA, US) с использованием смеси Prism Ready Reaction Dye Termination.
Поскольку в указанных выше клонах не было обнаружено никаких желаемых вставок для кодирующих последовательностей IFNa6, IFNa7 и IFNa16, ПЦР проводили еще раз в описанных выше условиях за исключением типа специфических праймеров. Для специфической амплификации IFNa6 использовали 5'- и 3'-праймеры IFNaO5: 5'-TGGTGCTCAGCT(A/G)CAAGTC-3' (SEQ ID No: 3) и IFNaO3-8: 5'-GAGTCGTTTCTGTGTTGGATCAG-3' (SEQ ID No: 11), соответственно. Для специфической амплификации IFNa7 использовали 5'- и 3'-праймеры IFNa7UO: 5'-ATGCCCCTGTCCTTTTCTTTAC-3' (SEQ ID No: 12) и эквимолярную смесь IFNaO3-5 и IFNaO3-6, соответственно. Для специфической амплификации IFNa16 использовали 5'- и 3'-праймеры IFNa7UO и IFNaO3-7: 5'-GATCATTTCCATGTTGAATGAG-3' (SEQ ID No: 10), соответственно. Амплифицированные фрагменты клонировали в вектор pCRII-TOPO или pCR-4-TOPO и секвенировали, как описано выше.
Все клонированные гены человеческого IFN-альфа, тип I, индивидуально выравнивали с соответствующими последовательностями ДНК из Genebank. Для этих генов, на которые сделаны ссылки в данном описании, использовали инвентарные номера для нуклеотидов в GeneBank: NMJ524013 (IFN-α1), NM_000605 (IFN-α2b), NM_010504 (IFN-α4), NM_010505 (IFN-α5), NM_008335 (IFNα6), NM_008334 (IFN-α7), NMJ508336 (IFN-α8), NM_002171 (IFN-α10), NM_002172 (IFN-α14), NM_002173 (IFN-α16), NM_021268 (IFN-α17), NM_002175 (IFN-α21).
Пример 2. Конструирование шаффлинг-библиотек плазмид, несущих HuIFN, тип I
Для конструирования плазмид, несущих кодирующую последовательность одного из человеческих IFN-α, тип I, синтезировали 15 пар олигонуклеотидов, с сайтами рестрикции для BamHI и EcoRI (Genentech, South San Francisco, CA, US), на основании кодирующей области индивидуальной кДНК для зрелых человеческих белков IFN, тип I. Для этих генов, на которые сделаны ссылки в данном описании, использовали инвентарные номера для нуклеотидов из GeneBank: NM_024013 (IFN-α1), NM_000605 (IFN-α2), NM_010504 (IFN-α4), NM_010505 (IFN-α5), NM_008335 (IFN-α6), NM_008334 (IFN-α7), NM_008336 (IFN-α8), NM_002171 (IFN-α10), NM_002172 (IFN-α14), NM_002173 (IFN-α16), NM_021268 (IFN-α17), NM_002175 (IFN-α21). Праймеры и плазмиды, сконструированные в Примере 1 в качестве матриц, использовали в стандартной ПЦР (111). Полученные в результате продукты расщепляли рестрикционными эндонуклеазами (РЭ) BamHI и EcoRI и клонировали в E.coli экспрессирующий вектор pBVB, который представляет собой производное экспрессирующей плазмиды pBV220 (86), содержащее сайт BamHI и сайт EcoRI в своей области множественного клонирования. Все эти окончательные конструкции проверяли анализом с секвенированием ДНК (РЕ Applied Biosystems, US).
Фрагменты ДНК, содержащие ОРС человеческого IFN, амплифицировали с использованием ПЦР, применяя пары олигонуклеотидов, BVF4: 5'-AGGGCAGCATTCAAAGCAG-3' (SEQ ID No: 13) и BVR3: 5'-TCAGACCGCTTCTGCGTTCTG-3' (SEQ ID No: 14), и применяя сконструированные ранее плазмиды, несущие HuIFN, тип I. Полученные продукты смешивали в равных количествах и подвергали перевариванию ДНКазой I и ПЦР-сборке (PCR assembly) в соответствии с методикой, описанной Stemmer (112).
Скомпонованные ПЦР-продукты далее амплифицировали с парой внутренних праймеров: BVF: 5'-GAAGGCTTTGGGGTGTGTG-3' (SEQ ID No: 15) и BVR: 5'-AATCTTCTCTCATCCGC-3' (SEQ ID No: 16), с последующим перевариванием BamHI и EcoRI и клонированием обратно в E.coli экспрессирующий вектор pBVB, расщепленный с использованием РЭ BamHI и EcoRI. Все эти окончательные конструкции проверяли анализом с секвенированием ДНК. Плазмидами, несущими перетасованные гены HuIFN-a, трансформировали компетентные клетки E.coli DH5α.
Во всех приведенных выше методиках с применением ПЦР, либо ПЦР-амплификации, либо ПЦР-сборки, использовали обычную ДНК-полимеразу (New England Biolab, MA, US), вместо ДНК-полимеразы высокой точности (high fidelity).
Пример 3. Скрининг шаффлинг-библиотек
Свежетрансформированные клетки E.coli DH5α выращивали в течение ночи на чашках с LB (бульон Луриа) при 37°C. Единичные колонии отбирали индивидуально и ими инокулировали 100 мкл среды LB, содержащей 50 мкг/мл ампициллина, в 96-луночных планшетах. Колонии встряхивали при 250 об/мин при 30°C. По окончании культивирования в течение ночи по 10 мкл бактериальных культур в двух повторах инокулировали 100 мкл среды LB, содержащей 50 мкг/мл ампициллина, в 96-луночных планшетах. Исходные чашки (так называемые сток-чашки (stock plates)) временно хранили при 4°C. Клетки на планшетах в двух повторах выращивали при 30°C до достижения OD600, равной 0,4, и затем индуцировали на 42°C. После 4-часовой тепловой индукции бактериальные культуры непосредственно переносили в морозильник на -80°C для того, чтобы начать цикл замораживания-оттаивания. Через 2 цикла замораживания-оттаивания бактериальную суспензию/лизат разбавляли до желаемой концентрации и этим воздействовали на культуру клеток Дауди для теста на антипролиферацию (101) или культуру Wish-клеток для противовирусного теста (113).
В каждом раунде стадий скрининга первоначально скринировали 20000 колоний, а для последующего подтверждающего тестирования отбирали приблизительно по 100 колоний с наивысшей антипролиферативной или противовирусной активностью. Отобранные бактериальные культуры на сток-чашках пересевали штрихом на LB-чашки, содержащие 50 мкг/мл ампициллина. Единичные колонии выращивали в течение ночи при 37°C, отбирали и ими инокулировали 1 мл среды LB, содержащей 50 мкг/мл ампициллина, в пробирках для тестирования. Бактерии в пробирках выращивали в течение ночи при 30°C со встряхиванием при 250 об/мин. Затем выросшими бактериями, по 40 мкл, инокулировали другой набор пробирок, содержащих по 1 мл LB с ампициллином (50 мкг/мл). Затем образцы подвергали стадиям индукции экспрессии, сбора клеточной культуры, цикла обработки замораживанием-оттаиванием и тестированию на антипролиферативную или противовирусную активность, как описано выше в отношении стадий первичного скрининга.
В каждом раунде стадий скрининга после подтверждающего тестирования отбирали приблизительно 20 колоний с наивысшей антипролиферативной или противовирусной активностью для получения плазмид и их вставки секвенировали в автоматическом режиме. Вставки, имеющие уникальную последовательность ДНК, далее амплифицировали, используя пару ПЦР-праймеров, BVBF: 5'-ACCATGAAGGTGACGCTC-3' (SEQ ID No: 17) и BVR: 5'-AATCTTCTCTCATCCGC-3' (SEQ ID No: 16), которые представляют собой фланкирующие последовательности "вверх по течению" и "вниз по течению" сайтов множественного клонирования вектора pBVB, соответственно. Амплифицированые ПЦР-продукты использовали для следующего раунда конструирования шаффлинг-библиотек.
Основываясь на увеличении либо антипролиферативной, либо противовирусной активности, проводили пять циклов стадий скрининга.
Пример 4. Экспрессия рекомбинантного белка Новаферона в E.coli и его очистка
Белок Новаферон (SEQ ID No: 2) экспрессировали в E.coli. Рамку считывания SEQ ID No: 1 с искусственным добавлением инициирующего кодона ATG клонировали в термоиндуцибельном векторе pBVB под контролем промотора λPRPL (114). Экспрессирующей плазмидой Новаферона, pBVBNF, трансформировали клетки DH5α. Единичные колонии индивидуально отбирали, ими инокулировали 2 мл среды LB, содержащей 50 мкг/мл ампициллина, и инкубировали при 30°C в течение 8 часов. Затем по 2 мл культивируемых бактерий дополнительно инкубировали с 50 мл среды, содержащей 50 мкг/мл ампициллина, в течение ночи при 30°C с перемешиванием. На следующее утро культивированные в течение ночи бактерии высевали в отношении 1:10~1:20 в большой объем среды LB, содержащей 50 мкг/мл ампициллина, и инкубировали при 30°C с перемешиванием. Когда культуры достигали середины логарифмической фазы роста (А550=0,5-0,6), температуру инкубации быстро поднимали до 42°C и выдерживали в течение 4 часов с целью индукции экспрессии Новаферона. По окончании 4-часовой тепловой индукции бактериальные клетки подвергали центрифугированию и промывали 3 раза PBS (забуференный фосфатом физиологический раствор) (137 мМ NaCl; 2,7 мМ KCl; 10 мМ Na2HPO4; 2 мМ KH2PO4), затем хранили при -80°C до начала очистки.
Большинство молекул белка Новаферона были растворимы в представленной в данном описании продуцирующей системе E.coli, несмотря на то, что они сверхэкспрессируются в цитоплазму. Поэтому клетки разрушали, переваривая лизоцимом в буфере I для лизиса клеток (50 мМ трис-Cl (рН 8,0); 1 мМ EDTA (этилендиаминтетрауксусная кислота) (рН 8,0); 100 мМ NaCl) (115). Лизат далее обрабатывали ультразвуком для разрушения оставшихся интактных клеток и соединения (splice) молекул ДНК. Затем лизат подвергали центрифугированию.
Растворимые молекулы белка Новаферона в супернатантах последовательно очищали гидрофобной, ионообменной хроматографией и гель-фильтрацией. Сначала супернатанты наносили на колонку и пропускали через колонку с Phenyl-Sepharose 6 Fast Flow (GE Healthcare, US). Во-вторых, фракции, содержащие белок Новаферон, наносили на колонку POROS 50 D (Applied Biosystems, US). В-третьих, фракции, содержащие молекулы Новаферона, подвергали очистке на колонке POROS 50 HS (Applied Biosystems, US) и окончательно собранные молекулы Новаферона дополнительно очищали на HiLoad 26/100 Superdex 75pg (Amersham, US).
Чистоту очищенного белка Новаферона проверяли, анализируя путем электрофореза в 15%-ном полиакриламидном геле (ПААГ) в присутствии додецилсульфата натрия (ДСН). Очищенный рекомбинантный белок Новаферон демонстрировал единичную зону с молекулярной массой (ММ) 19-20 кДа. Масс-спектрометрический анализ показал, что чистота очищенного Новаферона составляла более 98%, а молекулярная масса равнялась 19313 дальтон, что было идентично предсказанной из аминокислотной последовательности молекулярной массе в 19315 дальтон.
Пример 5. Экспрессия рекомбинантного HuIFN-α2b в E.coli и его очистка
Экспрессирующая HuIFN-α2b плазмида, pBV2b, содержит кДНК кодирующей области зрелого белка HuIFN-α2b (инвентарный номер для нуклеотидов из GeneBank: NM_000605), которая находится под контролем термоиндуцибельного промотора λ PRPL. Экспрессию HuIFN-α2b осуществляли, следуя протоколам, описанным Joseph S и David WR (116).
Экспрессирующей плазмидой pBV2bF трансформировали клетки DH5-α. Единичные колонии отбирали индивидуально и ими инокулировали 2 мл среды LB, содержащей 50 мкг/мл ампициллина, и инкубировали при 30°C в течение 8 часов. Затем по 2 мл культивируемых бактерий дополнительно инкубировали с 50 мл среды, содержащей 50 мкг/мл ампициллина, в течение ночи при 30°C с перемешиванием. На следующее утро бактериальную культуру высевали в отношении 1:10~1:20 в большой объем среды LB, содержащей 50 мкг/мл ампициллина, и инкубировали при 30°C с перемешиванием. Когда культуры достигали середины логарифмической фазы роста (A550=0,5-0,6), температуру инкубации быстро поднимали до 42°C и выдерживали в течение 4 часов с целью индукции экспрессии HuIFN-α2b. По окончании 4-часовой тепловой индукции бактериальные клетки подвергали центрифугированию и промывали PBS (137 мМ NaCl; 2,7 мМ KCl; 10 мМ Na2HPO4; 2 мМ KH2PO4), затем хранили при -80°C до начала очистки.
Белок HuIFN-α2b экспрессировался в нерастворимой форме в представленной в данном описании продуцирующей системе E.coli и поэтому применяли методики извлечения и промывки телец включения в соответствии с протоколами, описанными в Molecular Cloning (115). Кратко, собранные бактериальные клетки ресуспендировали в буфере I для лизиса клеток (50 мМ трис-Cl (рН 8,0); 1 мМ EDTA (рН 8,0); 100 мМ NaCl) и лизировали лизоцимом и обработкой ультразвуком. Тельца включения три раза промывали охлажденным во льду буфером II для лизиса клеток (буфер I для лизиса клеток, дополненный 0,5% (об./об.) Тритона Х-100).
Извлеченные тельца включения разрушали, суспендируя в 7 н. гуанидине при комнатной температуре с перемешиванием в течение 4 часов. После центрифугирования при 4°C в течение 15 минут денатурированный белок подвергали рефолдингу в 0,15 М (рН 9,5) Borex-буфере в течение 48 часов при 4°C. На последней стадии рефолдинга рН подводили до 7,4, используя HCl.
Раствор, содержащий подвергнутый рефолдингу HuIFN-α2b, затем очищали гидрофобной и ионообменной хроматографией и гель-фильтрацией. Сначала раствор наносили на колонку и пропускали через колонку с Phenyl-Sepharose 6 Fast Flow (GE Healthcare, US). Во-вторых, фракции, содержащие HuIFN-α2b, наносили на колонку POROS 50 D (Applied Biosystems, US). В-третьих, фракции, содержащие HuIFN-α2b, подвергали очистке на колонке POROS 50 HS (Applied Biosystems, US). Окончательно собранные молекулы HuIFN-α2b дополнительно очищали на HiLoad 26/100 Superdex 75pg (Amersham, US). Очищенный белок HuIFN-α2b демонстрировал единственную зону при анализе путем 15% ПААГ-электрофореза в присутствии ДСН, и его чистота составляла более 98%, что подтверждено масс-спектрометрией.
Пример 6. Определение противовирусной активности Новаферона
Противовирусную активность определяли, используя систему WISH-VSV, как описано в классических протоколах, приведенных Armstrong JA (113). В первый день WISH-клетки (АТСС, № по каталогу CCL 25) высевали в 96-луночные планшеты при плотности 14000 клеток/лунка и инкубировали при 37°C. Через 24 часа в каждую лунку добавляли 2-кратные серийные разведения Новаферона, HuIFN-α2b, международные стандарты ВО3 для человеческого IFN или культуральную среду сравнения и инкубировали при 37°C в течение следующих 24 часов. На третий день среду удаляли и заменяли средой, содержащей 1000 PFU (бляшкообразующих единиц) вируса везикулярного стоматита (VSV, АТСС, № по каталогу VR-1421). Клетки снова инкубировали в течение 24 часов при 37°C и затем промывали 0,85%-ным NaCl для удаления мертвых клеток. Затем культуральные планшеты погружали в раствор красителя-фиксатора (0,5% кристаллического фиолетового (crystal violet), 5% формалина (об./об.), 50% этанола (об./об.) и 0,85% NaCl) на 1 час. Раствор красителя-фиксатора затем удаляли, микропланшеты обильно промывали водопроводной водой и оставляли подсыхать. Окрашенные клетки растворяли, используя 0,2 мл 2-метоксиэтанола. Планшеты прочитывали при 550 нм в Model Opsys MR (Thermo Labsystems, US) для биологического анализа кристаллического фиолетового.
Все эксперименты проводили в трех повторах и образцы Новаферона и HuIFN-α2b тестировали в одном и том же планшете. Противовирусную активность полученных в данном примере Новаферона и HuIFN-α2b оценивали в параллели и противовирусные единицы (международная единица или IU) определяли с отсылкой к международным стандартам ВО3, 94/786 (rHuIFN-α консенсусный) и 95/650 (rHuIFN-α2a), которые приобретали в Национальном институте по биологическим стандартам и контролю (NIBSC, США).
Измеренная противовирусная активность очищенного белка Новаферон в отношении VSV на WISH-клетках составляла 2,5×109 IU/мг, в то время как противовирусная активность HuIFN-α2b составляет 2,0×108 IU/мг. Эти данные указывают на то, что противовирусная активность белка Новаферона приблизительно в 12,5 раза сильнее, чем таковая у HuIFN-α2b.
Пример 7. Антипролиферативная активность Новаферона
Анализ антипролиферативной активности проводили в основном как описано Evinger и Pestka (101).
А. Клеточная культура линий опухолевых клеток человека
Линии опухолевых клеток человека приобретали в разных организациях (Таблица 1, ниже), а именно АТСС (Американская коллекция типовых культур, P.O. Box 1549, Manassas, VA 20108, USA), DSMZ (German National Resource Centre for Biological Material, Deutsche Sammlung von Mikroorganismen und Zeilkulturen GmbH, Mascheroder Weg Ib, 38124 Braunschweig, Germany), JCRB (Japanese Collection of Research Bioresources-Cell Bank, National Institute of Biomedial Innovation, 7-6-8 Saito-Asagi, Ibaraki-shi, Osaka 567-0085, Japan).
Все клетки, использованные в тесте на антипролиферативную активность, культивировали при 37°C в увлажненной атмосфере, содержащей 5% CO2. Клетки выращивали в соответствии с руководством для выращивания каждого типа клеток на основных средах для роста, таких как DMEM (модифицированная Дульбекко среда Игла), MEM (минимальная незаменимая среда), F12K и 1640 или 1640 плюс F12 (все от Gibco BRL, US), дополненных 5-20% инактивированной нагреванием фетальной телячьей сыворотки (FBS) от Gibco BRL, US. Основные среды для роста каждой индивидуальной клеточной линии приведены в Таблице 2, ниже. Все клеточные линии ежедневно индивидуально проверяли на планшетах для культивирования под инвертированным микроскопом. Клетки собирали и использовали для экспериментов в их логарифмической фазе роста с жизнеспособностью, превышающей 90%, что определено по исключению красителя трипанового голубого. Подсчеты клеток и определение жизнеспособности осуществляли в стандартном гемоцитометре.
В. Методика анализа антипролиферативной активности
Клеточные линии в логарифмической фазе роста осторожно суспендировали в нагретых (36°C) средах до плотности 2×103-6×104 клеток/мл (в зависимости от клеточной линии, см. Таблица 2). По 100 мкл клеточной суспензии высевали в каждую лунку 96-луночного планшета с последующей инкубацией в течение 6-8 часов при 37°C. Затем в лунки в трех повторах добавляли равные объемы (100 мкл) Новаферона или HuIFN-α2b, разведенных в культуральной среде. Содержимое планшетов осторожно перемешивали в течение 4-5 секунд и инкубировали при 37°C в течение 6 суток. Образцы Новаферона и HuIFN-α2b тестировали в одном и том же планшете для того, чтобы гарантировать сравнимость.
Для определения количеств клеток в содержащей клетки лунке и для расчета антипролиферативных активностей Новаферона и HuIFN-α2b, соответствующих этим количествам клеток, использовали два метода.
Для определения количества суспендированных клеток использовали метод прямого подсчета клеток. Через 6 суток культивирования суспендированные клеточные культуры разводили трипановым голубым (конечная концентрация: 0,02%) и количество клеток подсчитывали напрямую, используя гемоцитометр.
Для определения числа адгезивных клеток применяли метод биологического анализа с использованием кристаллического фиолетового (93). Через 6 суток культивирования мертвые клетки удаляли, отбирая пипеткой PBS из лунок с культурой. Далее лунки заполняли раствором красителя-фиксатора для окрашивания живых клеток в течение 1 часа. Раствор красителя-фиксатора содержал 0,5% кристаллического фиолетового, 5% формалина (об./об.), 50% этанола (об./об.) и 0,85% NaCl в дистиллированной воде. Затем микропланшеты обильно промывали водопроводной водой и оставляли подсыхать. Окрашенные клетки растворяли, используя 0,2 мл 2-метоксиэтанола. Измеряли оптическую плотность при 550 нм (ОП550) (планшетный ридер Model Opsys, Thermo Labsystems, US) и использовали в качестве относительного показателя количеств клеток.
Степень ингибирования роста рассчитывали по следующей формуле:
степень ингибирования в %=(1-(Е-В)/(С-В))Х100, где Е представляло собой количество клеток или величину ОП550 в обработанных Новафероном или HuIFN-α2b лунках на 6-е сутки; В представляло собой количество клеток или величину ОП550 в клеточной культуре на 0-е сутки; С представляло собой количество клеток или величину ОП550 в необработанных лунках на 6-е сутки.
Степень ингибирования выражали через концентрации соединений. IC50 Новаферона или HuIFN-α2b оценивали, используя ряд образцов с разными концентрациями. Данные подгоняли к сигмоидной кривой (117) с наклоном Хилла (Hill slope): Y=Min+(Max-Min)/(1+10^(IC50-X)), где Х представляет собой log концентраций лекарственного средства; Y представляет собой степень ингибирования; Min или Мах представляет собой минимальную или максимальную степень ингибирования, соответствующую плато. Можно сравнивать IC50 для различных соединений относительно конкретной мишени, при этом более низкая IC50 указывает на более сильнодействующее соединение.
Концентрации Новаферона и HuIFN-α2b и соответствующие степени ингибирования клеточного роста для линии клеток Дауди представлены на Фиг.4. На основании этих данных IC50 Новаферона и HuIFN-α2b в отношении ингибирования роста клеток Дауди были рассчитаны как 0,0174 нмоль и 6,9550 нмоль. Таким образом, IC50 Новаферона составляет приблизительно 1/400 от таковой для HuIFN-α2b, характеризуя приблизительно 400-кратное увеличение антипролиферативной эффективности Новаферона по сравнению с HuIFN-α2b.
Антипролиферативные активности Новаферона оценивали и сравнивали с таковыми для HuIFN-α2b на 23 линиях опухолевых клеток, включая 4 клеточные линии, происходящие из меланомы (А-375, IGR-1, IGR-37, IPC-298), 5 клеточных линий колоректальной аденокарциномы (НСТ-8, SW1116, LS 180, DLD-1, LS174T), 4 клеточные линии рака печени (Hep G2, Нер 3 В, HuH-7, PLC/PRF/5), 3 клеточные линии лимфомы (HL-60(S), Дауди, L-428), 2 клеточные линии рака предстательной железы (DU 145, PC-3), 2 клеточные линии цервикального рака (HeLa, C-33A), 1 клеточную линию аденокарциномы желудка (MKN 1), 1 клеточную линию рака легких (А 549) и одну клеточную линию рака пищевода (KYSE 30). Новаферон демонстрирует более сильные антипролиферативные активности по сравнению с HuIFN-α2b в отношении всех протестированных раковых клеточных линий. Степень увеличения эффективности варьировала для разных раковых клеточных линий и изменялась с кратностью от 16 до 1134 (Таблица 3, ниже).
Пример 8. Эксперименты на моделях опухоли in vivo
А. Клеточная культура и модели ксенотрансплантата опухолей человека in vivo
Клеточная линия рака толстой кишки (LS 180), клеточная линия меланомы (А-375) и клеточная линия рака печени (Hep G2) были получены из Американской коллекции типовых культур (АТСС, Rockville, MD). Клеточная линия рака предстательной железы (РС-3) была получена из German National Resource Centre for Biological Material (DSMZ, Deutsche Sammlung von Mikroorganismen und Zeilkulturen, Germany). Лимфоцитарная клеточная линия (HL 60(s)) была приобретена у Japanese Collection of Research Bioresources Cell Bank (JCRB, Japan). Все клетки культивировали в соответствии с инструкциями для них (см. Таблицу 1). Кратко, LS 180 и Hep G2 культивировали в среде MEM. A-375 культивировали в DMEM. Обе среды были дополнены 10% фетальной телячьей сыворотки (FBS), 2 мМ глутамином, 100 ед./мл пенициллина, 100 мг/мл стрептомицина, 0,1 мМ несущественными (non-essential) аминокислотами и 1,0 мМ пируватом натрия. Клетки PC-3 и HL 60(8) культивировали в RPMI 1640 (среда 1640 от Roswell Park Memorial Institute), дополненной 10% FBS, 100 ед./мл пенициллина и 100 мг/мл стрептомицина. Все клетки поддерживали в атмосфере 5% CO2 при 37°C.
Модели ксенотрансплантата опухолей человека создавали, используя методы, описанные Beverly и др. (118). Раковые клетки в логарифмической фазе роста собирали с планшетов для культивирования тканей, промывали и ресуспендировали в забуференном фосфатом физиологическом растворе (PBS, рН=7,5; 20 мМ). У бестимусных голых мышей Balb/c возрастом 6 недель генерировали подкожные опухолевые ксенотрансплантаты посредством инъекции 6×106 клеток/0,3 мл (PC-3, HepG2), 4×106 клеток/0,3 мл (LS 180), 2×107 клеток/0,3 мл (HL 60(s)) или 8×106 клеток/0,3 мл (A-375) подкожно с обеих сторон боковой области. Для каждой модели опухоли in vivo на 6-е сутки после инокуляции опухолевых клеток опухоленесущих мышей (объем опухоли составляет приблизительно 100 мм3) случайным образом делили на 7 или 8 групп с одинаковым количеством животных в каждой группе и начинали лечение.
Новаферон и HuIFN-α2b готовили с использованием PBS-раствора. Ежедневные подкожные инъекции только PBS, различных доз Новаферона или HuIFN-α2b продолжали в целом в течение 30 суток (PC-3, HepG2, A-375), 28 суток (LS 180) или 21 суток (HL 60(s)), начиная со дня формирования групп мышей. Для лечения с использованием 5-FU один раз каждые двое суток, в целом 5 раз, вводили в/в (внутривенно) 30 мг/кг 5-FU. Группы и лекарственные дозы суммированы ниже.
Группа 1 (контроль): PBS ежедневно.
Группа 2 (низкая доза Новаферона): 1,25 мкг/кг ежедневно.
Группа 3 (средняя доза Новаферона): 12,5 мкг/кг ежедневно.
Группа 4 (высокая доза Новаферона): 125 мкг/кг ежедневно.
Группа 5 (низкая доза HuIFN-α2b): 1,25 мкг/кг ежедневно.
Группа 6 (средняя доза HuIFN-α2b): 12,5 мкг/кг ежедневно.
Группа 7 (высокая доза HuIFN-α2b): 125 мкг/кг ежедневно.
Группа 8 (5-FU): 30 мг/кг, в/в введение один раз каждые 2 суток, 5 раз.
После начала лечения производили измерения опухолей с помощью кронциркуля один раз в неделю. Объемы опухолей рассчитывали, используя следующую формулу: объем=0,5×(ширина)2×(длина). Мышей умерщвляли в день окончания лечения (30-й день после начала лечения). Солидные опухоли извлекали, фотографировали и измеряли.
Степень ингибирования роста рассчитывали, используя следующую формулу: степень ингибирования=[1-Т/С]×100%, где Т представляет собой средний вес опухоли в Новаферон-, HuIFN-α2b- или 5-FU-лечемых группах; С представляет собой средний вес опухоли в контрольной группе после лечения.
В. Модель ксенотрансплантата рака предстательной железы человека
Ксенотрансплантаты РС-3 рака предстательной железы обрабатывали п/к (подкожной) инъекцией 1,25, 12,5 или 125 мкг/кг Новаферона в течение 30 суток. Новаферон демонстрировал сильное, дозозависимое ингибирование роста опухоли PC-3 (P<0,05). Как показано на Фиг.5 и в Таблице 4, ниже, рост опухоли PC-3 в Новаферон-лечемых группах был более сильно подавлен по сравнению с контрольной группой лечения PBS. Например, средний вес опухолевой массы ксенотрансплантата PC-3 в Новаферон-лечемой группе (125 мкг/кг), 0,091±0,081 г, был очень значительно снижен по сравнению с контрольными животными, 1,948±0,567 г (Р<0,001) (Таблица 4). Другими словами, в результате 30-суточного лечения 125 мкг/кг было достигнуто 95,3% ингибирования роста опухоли PC-3 (Таблица 4).
Голых бестимусных мышей Balb/с обрабатывали ежедневно п/к инъекцией Новаферона (1,25 мкг/кг, 12,5 мкг/кг или 125 мкг/кг) в течение 30 суток после подкожного введения мышам 6×106 живых клеток PC-3. Результаты выражали в виде среднего объема опухоли (мм3). На Фиг.5 показано, что все три дозы Новаферона демонстрировали дозозависимое ингибирование роста опухоли PC-3 по сравнению с контрольной группой PBS (Р<0,05). 125 мкг/кг Новаферона индуцировали очень сильное или почти полное ингибирование роста опухоли PC-3 по сравнению с таковым для HuIFN-α2b в той же дозе (95,3% против 75,6%, Р<0,01) (Таблица 4).
Интересно отметить, что более длительное лечение Новафероном или HuIFN-α2b приводило к более заметным различиям в ингибировании опухолевого роста в группах, лечемых большой дозой (125 мкг/кг). Средний объем массы опухоли PC-3 в Новаферон-лечемой группе составлял 107,9±68,7 мм3 по сравнению с 620,7±296,6 мм3 в HuIFN-α2b-лечемой группе на 28-е сутки (Р<0,001) и 122,1±100,7 мм3 по сравнению с 691,9±428,3 мм3 на 30-е сутки (Р<0,001). Это также относится к случаю, когда рассматривали средний вес опухоли после окончания наблюдения (0,091±0,081 г для группы с высокой дозировкой Новаферона по сравнению с 0,476±0,271 г для группы с высокой дозировкой HuIFN-α2b, P<0,001). Это подтверждает то, что более длительное лечение Новафероном в этой дозе может демонстрировать более хорошее или полное ингибирование роста опухоли РС-3 в этой модели ксенотрансплантата.
С. Модель ксенотрансплантата рака печени человека
Противоопухолевую активность Новаферона in vivo также оценивали на модели ксенотрансплантата Hep G2 рака печени. Новаферон демонстрировал эффективное, дозозависимое ингибирование роста опухоли Мер G2 по сравнению с контрольной группой (Р<0,001). Средние объемы опухолей в Новаферон-лечемых группах (ежедневная подкожная инъекция 1,25, 12,5 или 125 мкг/кг в течение 30 суток) составляли 783,2±270,0, 459,3±414,3 и 104,6±56,5 мм3, соответственно, по сравнению с 2125,8±743,1 мм3 в контрольной группе PBS. В результате 30-суточного лечения 125 мкг/кг Новаферона достигали наивысшего ингибирования Hep G2 (96,6%), которое было более значительным по сравнению с таковым для 125 мкг/кг HuIFN-α2b (89,2%, Р<0,01). Более длительное лечение Новафероном в этой дозе демонстрировало тенденцию к еще более лучшему или полному ингибированию. Средний вес опухоли в конце периода наблюдения составлял 0,074±0,083 г для Новаферон-лечемой группы (125 мкг/кг), что значительно ниже, чем таковой для HuIFN-α2b-лечемой группы (125 мкг/кг) (0,235±0,199 г, Р<0,001) (Таблица 5, ниже).
Голых бестимусных мышей Balb/c обрабатывали ежедневно п/к инъекцией Новаферона (1,25 мкг/кг, 12,5 мкг/кг и 125 мкг/кг) в течение 30 суток после подкожного введения мышам 6×106 живых клеток Hep G2. Результаты выражали в виде среднего объема опухоли (мм3). На Фиг.6 показано, что все три дозы Новаферона демонстрировали дозозависимое ингибирование роста опухоли Нер G2 по сравнению с контрольной группой PBS (Р<0,001). 125 мкг/кг Новаферона индуцировали очень сильное или почти полное ингибирование роста опухоли Нер G2 по сравнению с таковым для HuIFN-α2b в той же самой дозе (96,6% против 89,2%, Р<0,05) (Таблица 5).
D. Модель ксенотрансплантата меланомы человека
Противоопухолевую активность Новаферона in vivo дополнительно оценивали на модели ксенотрансплантата А-375 злокачественной меланомы человека. Клеточную линию А-375 (номер в АТСС: CRL-1619) извлекали из человеческой злокачественной солидной опухоли. Новаферон демонстрировал эффективное, дозозависимое ингибирование роста опухоли А-375 по сравнению с контрольной группой (Р<0,001). Степени ингибирования в Новаферон-лечемых группах (ежедневная п/к инъекция 1,25, 12,5 или 125 мкг/кг в течение 28 суток) составляли 40,1%, 75,0% и 82,8%, соответственно, по сравнению с контрольной группой PBS (Р<0,001) (Таблица 6, ниже).
В результате 30-суточного лечения 125 мкг/кг Новаферона достигали наивысшего ингибирования А-375 (82,8%), которое было более значительным по сравнению с таковым для 125 мкг/кг HuIFN-α2b (69,9%; Р<0,001).
Интересно, что Новаферон демонстрировал более эффективное ингибирование роста клеток меланомы А-375 по сравнению с химиотерапевтическим агентом 5-FU (Таблица 6). На 30-е сутки, например, средний вес опухолей в группах, лечемых 12,5 мкг/кг или 125 мкг/кг Новаферона, составлял 0,763±0,187 (Р<0,01) и 0,527±0,149 (Р<0,001) г, в то время как средний вес опухолей в группе, лечемой 5-FU, 30 мг/кг, составлял 1,004±0,105 г (Таблица 6). Это указывает на то, что Новаферон может быть более эффективным для лечения меланомы А-375 человека, чем 5-FU.
Голых бестимусных мышей Balb/c обрабатывали ежедневно п/к инъекцией Новаферона (1,25 мкг/кг, 12,5 мкг/кг и 125 мкг/кг) в течение 28 суток после подкожного введения мышам 8×106 клеток А-375. Результаты выражали в виде среднего объема опухоли (мм3). На Фиг.7 показано, что все три дозы Новаферона демонстрировали дозозависимое ингибирование роста опухоли А-375 по сравнению с контрольной группой PBS (Р<0,001). 125 мкг/кг Новаферона индуцировали более сильное ингибирование роста опухоли А-375 по сравнению с таковым для HuIFN-α2b в той же дозе (82,8% против 69,9%, Р<0,001) (Фиг.7). Как 12,5 мкг/кг, так и 125 мкг/кг Новаферона демонстрировали более хорошее подавление (75,0% и 82,8% соответственно) опухолевого роста, чем 5-FU (67,2%, Р<0,01 и Р<0,001)(Фиг.7).
Е. Модель ксенотрансплантата рака толстой кишки человека
Противоопухолевую активность Новаферона in vivo дополнительно оценивали на модели ксенотрансплантата LS 180 рака толстой кишки. Клеточную линию LS 180 (номер в АТСС: CL-187) извлекали из аденокарциномы толстой кишки человека. Новаферон демонстрировал эффективное, дозозависимое ингибирование роста опухоли LS 180 по сравнению с контрольной группой (Р<0,001). Степени ингибирования в Новаферон-лечемых группах (ежедневная п/к инъекция 1,25, 12,5 или 125 мкг/кг в течение 28 суток) составляли 75,0%, 80,5% и 92,5%, соответственно, по сравнению с контрольной группой PBS (Р<0,001) (Таблица 7, ниже). В результате 28-суточного лечения 125 мкг/кг Новаферона достигали наивысшего ингибирования роста опухоли LS 180 (92,5%), которое было более значительным по сравнению с таковым для 125 мкг/кг HuIFN-α2b (82,3%, Р<0,001).
После 28-суточного лечения Новафероном (12,5 мкг/кг) рост ксенотрансплантатов рака LS 180 ингибировался аналогично 5-FU (30 мг/кг) в терминах среднего веса опухолей (0,815±0,221 г по сравнению 0,758±0,227 г). 125 мкг/кг Новаферона ингибировали рост опухоли LS 180 значительно лучше, чем 30 мг/кг 5-FU (92,5% по сравнению с 81,8%, Р<0,001) (Таблица 7 и Фиг.8). Эти наблюдения были чрезвычайно интересными, принимая во внимание общепринятое клиническое применение 5-FU в стандартной химиотерапии пациентов с раком толстой кишки. Наилучшее подавление Новафероном роста опухоли LS 180 в животной модели показывает, что Новаферон обладает потенциалом быть очень эффективным агентом против рака толстой кишки в клинических условиях.
Голых бестимусных мышей Balb/c обрабатывали ежедневной инъекцией Новаферона (1,25 мкг/кг, 12,5 мкг/кг и 125 мкг/кг) в течение 28 суток после подкожного введения мышам 4×106 клеток LS 180. Результаты выражали в виде среднего объема опухоли (мм3). На Фиг.8 показано, что все три дозы Новаферона демонстрировали дозозависимое ингибирование роста опухоли LS180 по сравнению с контрольной группой PBS (Р<0,001). 125 мкг/кг Новаферона индуцировали более сильное ингибирование роста опухоли LS 180, чем таковое для HuIFN-α2b в той же дозе (92,5% против 82,3%, Р<0,001) (Таблица 7). С использованием как 1,25 мкг/кг, так и 12,5 мкг/кг Новаферона достигали аналогичного подавления (75,0% и 80,5%, соответственно) роста опухоли по сравнению с 5-FU (81,8%) (Таблица 7, Фиг.8). Однако 125 мкг/кг Новаферона демонстрировали значительно более сильное ингибирование роста опухоли LS 180, чем таковое под действием 5-FU (92,5% против 81,8%, Р<0,001).
F. Модель ксенотрансплантата лейкоза человека
Противоопухолевую активность Новаферона in vivo также оценивали в модели ксенотрансплантата лимфоцитарного лейкоза HL 60(s). Новаферон демонстрировал эффективное, дозозависимое ингибирование роста опухоли HL 60(s) по сравнению с контрольной группой (Р<0,001). Степени ингибирования в Новаферон-лечемых группах (ежедневная п/к инъекция 1,25, 12,5 или 125 мкг/кг в течение 28 суток) составляли 43,8%, 55,2% и 80,4%, соответственно, по сравнению с контрольной группой PBS (Р<0,001, Таблица 8, ниже). После 21-суточного лечения Новафероном (125 мкг/кг) достигали наивысшего ингибирования роста опухоли HL 60(s) (80,4%), которое было значительно лучше, чем таковое под действием 125 мкг/кг HuIFN-α2b (69,8%, Р<0,05).
Мышей Balb/c обрабатывали ежедневно п/к инъекцией Новаферона (1,25 мкг/кг, 12,5 мкг/кг и 125 мкг/кг) в течение 21 суток после подкожного введения мышам 2×107 живых клеток HL 60(s). Результаты выражали в виде среднего объема опухоли (мм3). На Фиг.9 показано, что все три дозы Новаферона демонстрировали дозозависимое ингибирование роста опухоли HL 60(s) по сравнению с контрольной группой PBS (Р<0,001). 125 мкг/кг Новаферона индуцировали более сильное ингибирование роста опухоли HL 60(s), чем таковое под действием HuIFN-α2b в той же дозе (80,4% против 69,8%, Р<0,05), и схожее ингибирование, сравнимое с таковым для 5-FU (Фиг.9, Таблица 8).
G. Общее состояние мышей в процессе лечения Новафероном
За мышами с различными ксенотрансплантатами человеческого рака тщательно наблюдали во время периода лечения Новафероном, HuIFN-α2b или 5-FU. В отличие от 5-FU-лечемых групп мыши во всех Новаферон- или HuIFN-α2b-лечемых группах обычно принимали корм и вели себя нормально и не демонстрировали уменьшения массы. 5-FU-лечемые мыши демонстрировали типичные изменения в приеме корма и поведении и уменьшение массы. Эти наблюдения показывают, что несмотря на то, что Новаферон демонстрирует схожую или лучшую противораковую эффективность, чем 5-FU, в животных моделях ксенотрансплантата, он может быть более специфичным в отношении ингибирования раковой клетки и оказывать меньшее влияние на нормальные клетки и/или физиологические функции. Это может приводить к лучшей толерантности и более сильным терапевтическим эффектам при применениях на людях.
Как будет очевидно специалистам в данной области техники в свете приведенного выше описания, при применении на практике данного изобретения возможны многие изменения и модификации без отклонения от его сущности или объема. Следовательно, объем изобретения следует истолковывать в соответствии с содержанием, определенным прилагаемой формулой изобретения.
ССЫЛКИ
1. Interferon nomenclature. Nature. 1980; 286 (5769): 110.
2. Isaacs A and Lindenmann J. Production of virial interfering substance. US Pat No: 369922. October 17, 1972.
3. Jonasch E and Haluska FG. Interferon in oncological practice: review of interferon biology, clinical applications, and toxicities. Oncologist. 2001; 6(1); 34-55.
4. Lengyel P. Biochemistry of interferons and their actions. Annu Rev Biochem. 1982; 51:251-282.
5. Grosser I and Tovey MG. Antitumor effects of interferon. Biochim Biophys Acta. 1978; 516(2): 231-247.
6. Samuel CE. Antiviral actions of interferons. Clin Microbiol Rev. 2001; 14(4): 778-809.
7. Theofilopoulos AN, et al. Type I interferons (alpha/beta) in immunity and autoimmunity. Annu Rev Immunol. 2005; 23: 307-336.
8. Uze G, et al. Alpha and beta interferons and their receptor and their friends and relations. J Interferon Cytokine Res. 1995; 15(1): 3-26.
9. Knight E Jr. Interferon: purification and initial characterization from human diploid cells. Proc Natl Acad Sci USA. 1976; 73(2); 520-523.
10. Pestka S, et al. Interferons, interferon-like cytokines, and their receptors. Immunol Rev. 2004; 202: 8-32.
11. Horisberger MA and Di Marco S. Interferon-alpha hybrids. Pharmacol Ther. 1995; 66(3): 507-534.
12. Horton HM, et al. Antitumor effects of interferon-omega: in vivo therapy of human tumor xenografts in nude mice. Cancer Res. 1999; 59(16): 4064-4068.
13. Hardy MP, et al. Characterization of the type I interferon locus and identification of novel genes. Genomics. 2004; 84(2): 331-345.
14. Chen J. et al. Human interferon-ε: a type I interferon. US Pat No: 6569420. May 27, 2003.
15. Pestka S, et al. lnterleukin-10 and releated cytokines and receptors. Annu Rev Immunol 2004, 22: 929-979.
16. Nardelli В, et al. Regulatory effect of IFN-kappa, a novel type I IFN, on cytokine production by cells of the innate immune system. J. Immunol. 2002; 169(9): 4822-4830.
17. LaFleur DW, et al. Interferon-kappa, a novel type I interferon expressed in human keratinocytes. J Biol Chem. 2001; 276(43): 39765-39771.
18. Subramaniam PS, Johnson HM. The IFNAR1 subunit of the type I IFN receptor complex contains a functional nuclear localization sequence. FEBS Lett. 2004; 578(3): 207-210.
19. Goodbourn S, et al. Interferons: cell signalling, immune modulation, antiviral response and virus countermeasures. J Gen Virol. 2000; 81 (Pt 10): 2341-2364.
20. Wang K. et al. Inhibition of neutrophil apoptosis by type 1 IFN depends on cross-talk between phosphoinositol 3-kinase, protein kinase C-delta, and NF-kappa В signaling pathways. J Immunol. 2003; 171(2): 1035-1041.
21. Katze MG. Interferon, PKR, virology, and genomics: what is past and what is next in the new millennium? J Interferon Cytokine Res. 2002; 22(3): 283-286.
22. Chawla-Sarkar M. et al. Apoptosis and interferons: role of interferon-stimulated genes as mediators of apoptosis. Apoptosis. 2003; 8(3): 237-249.
23. Kirkwood J. Cancer immunotherapy: the interferon-alpha experience. Semin Oncol. 2002; 29(3 SuppI 7): 18-26.
24. Hofmann V, et al. Hairy cell leukemia: an interferon deficient disease? Cancer Treat Rev. 1985; SuppI B: 33-37.
25. Stone RM, et al. Recombinant human gamma interferon administered by continuous intravenous infusion in acute myelogenous leukemia and myelodysplastic syndromes. Am J Clin Oncol. 1993; 16(2): 159-163.
26. Talpaz M, et al. Human leukocyte interferon to control thrombocytosis in chronic myelogenous leukemia. Ann Intern Med. 1983; 99(6): 789-792.
27. Talpaz M, et al. Changes in granulocyte-monocyte colony-forming cells among leukocyte-interferon-treated chronic myelogenous leukemia patients. Exp Hematol. 1986; 14(7): 668-671.
28. Strander H, et al. Long-term adjuvant interferon treatment of human osteosarcoma. A pilot study. Acta Oncol. 1995; 34(6): 877-880.
29. Dogan В, et al. Intralesional alfa-2a interferon therapy for basal cell carcinoma. Cancer Lett. 1995; 91(2): 215-219.
30. Fetell MR, et al. Intratumor administration of beta-interferon in recurrent malignant gliomas. A phase I clinical and laboratory study. Cancer. 1990; 65(1): 78-83.
31. Muss HB. The use of interferon in renal cell carcinoma. Eur J Cancer. 1991; 27 (SuppI 4): S84-87.
32. Peest D, et al. Cytokine therapy in multiple myeloma. Br. J Haematol. 1996; 94(3): 425-432.
33. Ikic D, et al. Local interferon therapy for melanoma patients. Int. J Dermatol. 1995; 34(12): 872-874.
34. Rybak ME, et al. Interferon therapy of relapsed and refractory Hodgkin's disease: Cancer and Leukemia Group В Study 8652. J Biol. Response Mod. 1990; 9(1): 1-4.
35. Kaufmann R, et al. Temozolomide in combination with interferon-alpha versus temozolomide alone in patients with advanced metastatic melanoma: a randomized, phase III, multicenter study from the Dermatologic Cooperative Oncology Group. J Clin Oncol. 2005; 23(35): 9001-9007.
36. Lane HC. The role of alpha-interferon in patients with human immunodeficiency virus infection. Semin Oncol. 1991; 18(SuppI 7): 46-52.
37. Woo MH and Brunakis TG. Interferon alfa in the treatment of chronic viral hepatitis В and C. Ann. Pharmacother. 1997; 31(3): 330-337.
38. Gibas AL. Use of interferon in the treatment of chronic viral hepatitis. Gastroenterologist. 1993; 1(2): 129-142.
39. Levine LA, et al. Treatment of subclinical intraurethral human papilloma virus infection with interferon alfa-2b. Urology. 1996; 47(4): 553-557.
40. Но М. Interferon for the treatment of infections. Annu Rev Med. 1987; 38: 51-59.
41. Wintergerst U and Belohradsky BH. Acyclovir monotherapy versus acyclovir plus beta-interferon in focal viral encephalitis in children. Infection. 1992; 20(4): 207-212.
42. Bogdan С.et al. The role of type I interferons in non-viral infections. Immunol Rev. 2004; 202: 33-48.
43. Condos R, et al. Treatment of multidrug-resistant pulmonary tuberculosis with interferon-gamma via aerosol. Lancet. 1997; 349(9064): 1513-1515.
44. Giosue S, et al. Aerosolized interferon-alpha treatment in patients with multidrug-resistant pulmonary tuberculosis. Eur Cytokine Netw. 2000; 11(1): 99-104.
45. Raad I, et al. Use of adjunctive treatment with interferon-gamma in an immunocompromised patient who had refractory multidrug-resistant tuberculosis of the brain. Clin Infect Dis. 1996; 22: 572-574.
46. Fernandez O. et al. Treatment of relapsing-remitting multiple sclerosis with natural interferon beta: a multicenter, randomized clinical trial. Mult. Scler. 1995; SuppI 1: S67-69.
47. Freedman MS, et al. Randomized study of once-weekly interferon beta-la therapy in relapsing multiple sclerosis: three-year data from the OWIMS study. Mult Scler. 2005; 11(1): 41-45.
48. Shiozawa S, et al. Single-blinded controlled trial of low-dose oral IFN-alpha for the treatment of xerostomia in patients with Sjogren's syndrome. J Interferon Cytokine Res. 1998; 18(4): 255-262.
49. Wandinger KP, et al. Diminished production of type-I interferons and interleukin-2 in patients with multiple sclerosis. J Neurol Sci. 1997; 149(1): 87-93.
50. Steegmann JL, et al. Interferon alpha for chronic myeloid leukemia relapsing after allogeneic bone marrow transplantation. Bone Marrow Transplant. 1999; 23(5): 483-488.
51. Kirkwood JM, et al. High dose Interferon alfa 2b significantly prolongs relapse free survival compared with GM2-KLH/QS-21 vaccine in patients with resected stage IIB-III melanoma: Results of Intergroup Trial E1694/S9512/C509081. J Clin Oncol 2001; 19:2370-2380.
52. Bonnem EM. alpha Interferon: the potential drug of adjuvant therapy: past achievements and future challenges. Eur J Cancer. 1991; 27 SuppI 4: S2-6.
53. Folkman J. Successful treatment of an angiogenic disease. N EngI J Med. 1989:320: 1211-1212.
54. Clifford JL, et al. Retinoids and interferons as antiangiogenic cancer drugs. In: Teicher BA, ed. Antiangiogenic Agents in Cancer Therapy. Totowa, NJ: Humana Press Inc; 1999; 355-370.
55. Kaban LB, et al. Antiangiogenic therapy of a recurrent giant cell tumor of the mandible with interferon alfa-2a. Pediatrics. 1999; 103: 1145-1149.
56. Sleijfer S, et al. Side effects of interferon-alpha therapy. Pharm World Sci. 2005; 27(6): 423-431.
57. Bell L et al. Structure and properties of modified Interferons. US Pat No: 4914033. April 3, 1990.
58. Meyer F. et al. Hybrid Interferons. US Pat No: 5071761. December 10, 1991.
59. Streuli M, et al. Target cell specificity of two species derived from them. Proc Natl Acad Sci USA. 1981; 78(5): 2848-2852.
60. Zoon K. et al. Interferon alpha hybrids. US Pat No: 6685933. February 3, 2004.
61. Gangemi JD. Antiviral combination, and method of treatment. US Pat No: 5137720. August 11, 1992.
62. Johnson HM. et al. Hybrid interferon tau/type I interferon polypeptides. US Pat No:6174996.January 16, 2001.
63. Raj, NB, et al. Synthesis, antiviral activity, and conformational characterization of mouse-human a-interferon hybrids. J Biol Chem. 1988; 263(18): 8943-8952.
64. Mark DF, et al. Site-specific mutagenesis of the human fibroblast interferon gene. Proc Natl Acad Sci USA 1984; 81(18): 5662-5666.
65. Bentzien J. et al. Recombinant interferon-beta mutants. US Pat No: 6514729. February 4, 2003.
66. Stemmer WPC. Methods for in vitro recombination. US Pat No: 5605793. February 25, 1997.
67. Chang CC, et al. Evolution of a cytokine using DNA family shuffling. Nat Biotechnol. 1999; 17(8): 793-797.
68. Blatt LM, et al. The biologic activity and molecular characterization of a novel synthetic interferon-alpha species, consensus interferon. J interferon cytokine Res. 1996; 16:489-499.
69. Tatusova ТА and Madden TL. BLAST 2 Sequences, a new tool for comparing protein and nucleotide sequences. FEMS Microbiol Lett. 1999; 174(2): 247-250.
70. Bowie JU, et al. Deciphering the Message in Protein Sequences: Tolerance to Amino acid Substitutions. Science 1990; 247(4948): 1306-1310.
71. Creighton ТЕ. Posttranslational covalent modification of polypeptide chains. In Proteins: Structure and Molecular Properties. Ed by Creighton ТЕ. W.H. Freeman & Co. 1993; pp.78-99. San Francisco, US.
72. Aplin JD and Wriston JC Jr. Preparation, properties, and applications of carbohydrate conjugates of proteins and lipids. CRC Crit Rev Biochem. 1981; 10(4): 259-306.
73. Edge AS, et al. Deglycosylation of glycoproteins by trifluoromethanesulfonic acid. Anal Biochem. 1981; 118(1): 131-137.
74. Thotakura NP and Bohl OP. Enzymatic deglycosylation of glycoproteins. Meth Enzymol.1987; 138: 350-359.
75. Peck GE, et al. Pharmaceutical manufacturing. In Remington: The Science and Practice of Pharmacy. 21st ed. Edited by University of the Sciences in Philadelphia (USIP), Lippincott Williams and Wilkins. 2006, page: 691-1094. PA, US.
76. Shimizu K. et al. Plasminogen activator derivatives US Pat No: 4640835. February 3, 1987.
77. Mitra G. Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer. US Pat No: 4496689. January 29, 1985.
78. Nakagawa Y. et al. Chemically modified protein with polyethyleneglycol. US Pat No: 4791192. December 13, 1988.
79. Davis F. et al. Non-immunogenic polypeptides. US Pat No: 4179337. December 18, 1979.
80. Field J, et al. Purification of a RAS-responsive adenylyl cyclase complex from Saccharomyces cerevisiae by use of an epitope addition method. Mol Cell Biol. 1988; 8(5): 215921-2165.
81. Evan Gl, et al. Isolation of monoclonal antibodies specific for human c-myc proto-oncogene product. Mol Cell Biol. 1985; 5(12); 3610-3616.
82. Paborsky LR, et al. Mammalian cell transient expression of tissue factor for the production of antigen. Protein Eng. 1990; 3(6): 547-553.
83. Einhauer A and Jungbauer A. The FLAG peptide, a versatile fusion tag for the purification of recombinant proteins. J Biochem Biophys Methods. 2001; 49(1-3): 455-465.
84. Skinner H, et al. Use of the Glu-Glu-Phe C-terminal epitope for rapid purification of the catalytic domain of normal and mutant ras GTPase-activating proteins. J Biol Chem. 1991; 266(22): 14163-14166.
85. Lutz-Freyermuth С, et al. Quantitative determination that one of two potential RNA-binding domains of the A protein component of the U1 small nuclear ribonucleoprotein complex binds with high affinity to stem-loop II of U1 RNA. Proc Natl Acad Sci USA. 1990; 87(16): 6393-6397.
86. Zhang ZQ. et al. Construction and application of a high level expression vector containing PRPL promoter. Chinese J of Virol. 1990: 2: 18-23.
87. Kingston RE, et al. Introduction of DNA into mammalian cells. In Current Protocols In Molecular Biology edited by Ausubel FM, et al. 2003; page: 9.0.1-9.15.20, John Wiley & Sons, Inc. US.
88. McNeill ТА. Interferon assay. J Immunol Methods. 1981; 46(2): 121-127.
89. Rubinstein S, et al. Convenient assay for interferon. 1. Viral. 1981; 37: 755-758.
90. Horisberger MA and de Staritzky K. A recombinant human interferon-α B/D hybrid with a broad hostrange. J Gen Virol. 1987; 68: 945-948.
91. Stitz L and Schellekens H. Influence of input multiplicity of infection on the antiviral activity of interferon. J Gen Virol. 1980; 46: 205-210.
92. Yeo EY, et al. Effect of short-term ethanol on the proliferative response of Swiss 3T3 cells to mitogenic growth factors. Exp Mot Med. 2000; 32: 161-169.
93. Vignesh RC, et al. Effect of ethanol on human osteosarcoma cell proliferation, differentiation and mineralization. Toxicology. 2006; 220(1): 63-70.
94. Cavanaugh PF Jr, et al. A semi-automated neutral red based chemosensitivity assay for drug screening. Investigational New Drugs. 1990; 8(4): 347-354.
95. Raines EW and Ross R. Purification of human platelet-derived growth factor. Methods Enzymol. 1985; 109: 749-773.
96. Wahl AF, et al. Gene expression of human DNA polymerase alpha during cell proliferation and the cell cycle. Mol Cell Biol. 1988; 8(11): 5016-5025.
97. Cook JA and Mitchel JB. Viability measurements in mammalian cell systems. Anal Biochem. 1989; 179(1): 1-7.
98. Porstmann T, et al. Quantitation of 5-bromo-2-deoxyuridine incorporation into DNA: an enzyme immunoassay for the assessment of the lymphoid cell proliferative response. J Immunol Methods. 1985; 82(1): 169-179.
99. Mosmann T. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods. 1983; 65(1-2): 55-63.
100. Scudiero DA, et al. Evaluation of a soluble tetrazolium/formazan assay for cell growth and drug sensitivity in culture using human and other tumor cell lines. Cancer Res. 1988; 48(17); 4827-4833.
101. Evinger M and Pestka S. Assay of growth inhibition in lymphoblastoid cell cultures. Methods Enzymol. 1981; 79(Pt B): 362-368.
102. Meister A, et al. Biological activities and receptor binding of two human recombinant interferons and their hybrids. J Gen Virol. 1986; 67(Pt 8): 1633-43.
103. Frincke J. et al. Interferon antibody compositions having an extended serum half-life. US Pat No: 5055289. October 8, 1991.
104. Chang T and Yu L. Hybrid with interferon-beta and an immunoglobulin Fc joined by a peptide linker. US Pat No: 5908626. June 1, 1999.
105. Nieforth KA, et al. Use of an indirect pharmacodynamic stimulation model of MX protein induction to compare in vivo activity of interferon alfa-2a and a polyethylene glycol-modified derivative in healthy subjects. Clin Pharmacol Ther. 1996; 59(6): 636-646.
106. Ekwuribe NN. Conjugation-stabilized therapeutic agent compositions, delivery and diagnostic formulations comprising same, and method of making and using the same. US Pat No: 5681811. October 28, 1997.
107. Gilbert CW and Cho M-O. Interferon polymer conjugates. US Pat No: 5711944. January 27, 1998.
108. Greenwald R and Gilbert CW. Interferon polymer conjugates and process for preparing the same. US Pat No: 5738846. April 14, 1998.
109. Letsinger RL, et al. Cholesteryl-conjugated oligonucleotides: synthesis, properties, and activity as inhibitors of replication of human immunodeficiency virus in cell culture. Proc Natl Acad Sci USA. 1989; 86(17): 6553-6556.
110. Brower V. Naked DNA vaccines come of age. Nat Biotechnol. 1998; 16(13): 1304-1305.
111. Coen DM. The polymerase chain reaction. In: Current Protocols in Molecular Biology. Edited byAusubel FM. 2001, page: 15.01-15.7.8. John Wiley & Sons, Inc. US.
112. Stemmer WP. DNA shuffling by random fragmentation and reassembly: in vitro recombination for molecular evolution. Proc Natl Acad Sci USA. 1994; 91(22): 10747-10751.
113. Armstrong JA. Cytopathic effect inhibition assay for interferon: microculture plate assay. Methods Enzymol. 1981; 78(ptA): 381-387.
114. Sambrook J and Russell DW. In: Molecular Cloning. 2001; page: 15.25-15.35, Cold Spring Harbor Laboratory Press, New York, US.
115. Sambrook J and Russell DW. In: Molecular Cloning. 2001; page: 15.51-15.52, Cold Spring Harbor Laboratory Press, New York, US
116. Sambrook J and Russell DW. In: Molecular Cloning. 2001; page: 15.25-15.29 and 15.49-15.53, Cold Spring Harbor Laboratory Press, New York, US.
117. Chou TC, et al. Reversal of anticancer multidrug resistance by the ardeemins. Proc Natl Acad Sci USA. 1998; 95(14): 8369-8374.
118. Corbell T, et al. in vivo methods for screening and preclinical testing: use of rodent solid tumors for drug discovery. In: Anticancer Drug Development Guide: preclinical screening, clinical trails, and approval. Edited by Teicher BA and Andrews PA. 2004; page: 79-124. Humana Press, New Jersey, US.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ, АНТИПРОЛИФЕРАТИВНОЙ И/ИЛИ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ, ВЫДЕЛЕННЫЙ ПОЛИНУКЛЕОТИД, КОДИРУЮЩИЙ ПОЛИПЕПТИД И ИХ ПРИМЕНЕНИЕ | 2002 |
|
RU2328528C2 |
| БЕЛОК СЛИЯНИЯ НАЦЕЛЕННОГО НА GPC3 АНТИТЕЛА И ИНТЕРФЕРОНА α И ЕГО ПРИМЕНЕНИЕ | 2022 |
|
RU2836245C2 |
| РЕКОМБИНАНТНЫЙ ХИМЕРНЫЙ БЕЛОК ANTH1, КОДИРУЮЩАЯ ЕГО НУКЛЕИНОВАЯ КИСЛОТА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2322455C2 |
| ИНТЕРФЕРОН-ПОДОБНЫЙ БЕЛОК ZCYTO21 | 2001 |
|
RU2292394C2 |
| АНТИТЕЛА ПРОТИВ ИНТЕРФЕРОНА-АЛЬФА | 2002 |
|
RU2314317C2 |
| Гуманизированное нейтрализующее антитело к интерферону-бета человека | 2019 |
|
RU2737466C1 |
| СЛИТЫЙ БЕЛОК, ОБЛАДАЮЩИЙ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ ИНТЕРФЕРОНА-АЛЬФА, ДИМЕРНЫЙ СЛИТЫЙ БЕЛОК, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИХ СОДЕРЖАЩАЯ, МОЛЕКУЛА ДНК (ВАРИАНТЫ) И СПОСОБ АДРЕСОВАНИЯ ИНТЕРФЕРОНА-АЛЬФА В ТКАНИ ПЕЧЕНИ | 2000 |
|
RU2262510C9 |
| Штамм бактерий Escherichia coli - продуцент рекомбинантного белка NS1 | 2021 |
|
RU2789735C1 |
| Моноклональное антитело, способное нейтрализовать биологическую активность интерферона бета-1а человека | 2018 |
|
RU2729391C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ ИНТЕРФЕРОНА-АЛЬФА И СПОСОБЫ ПРИМЕНЕНИЯ | 2006 |
|
RU2431638C2 |






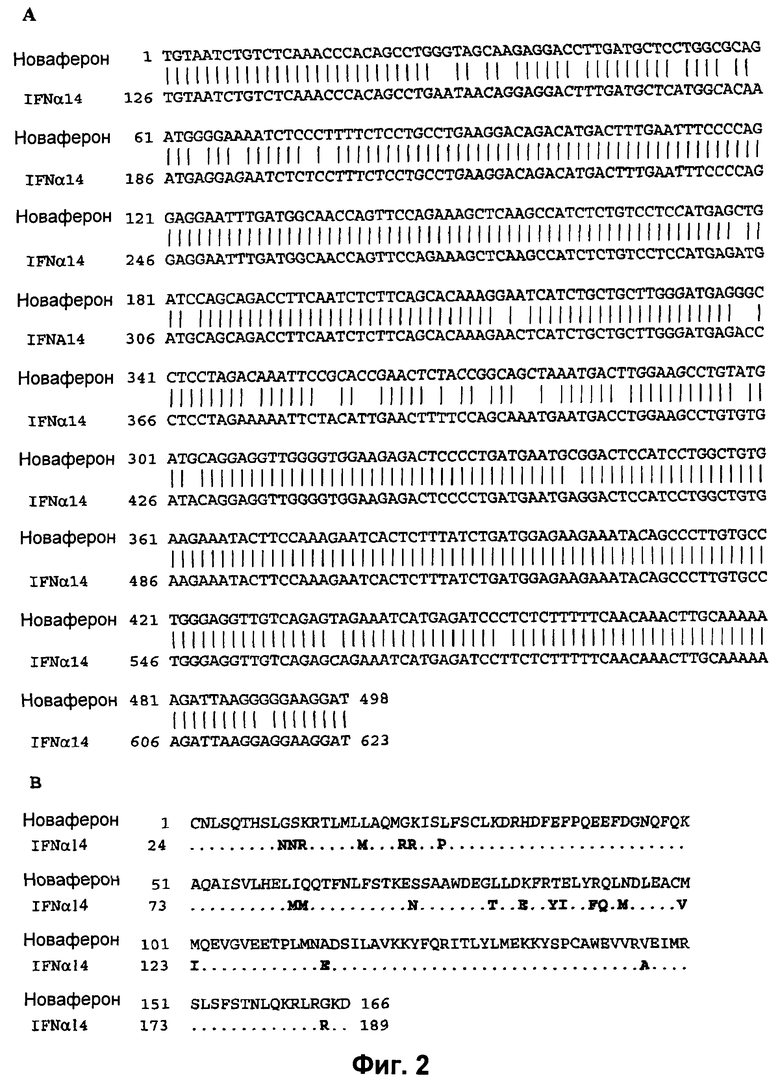
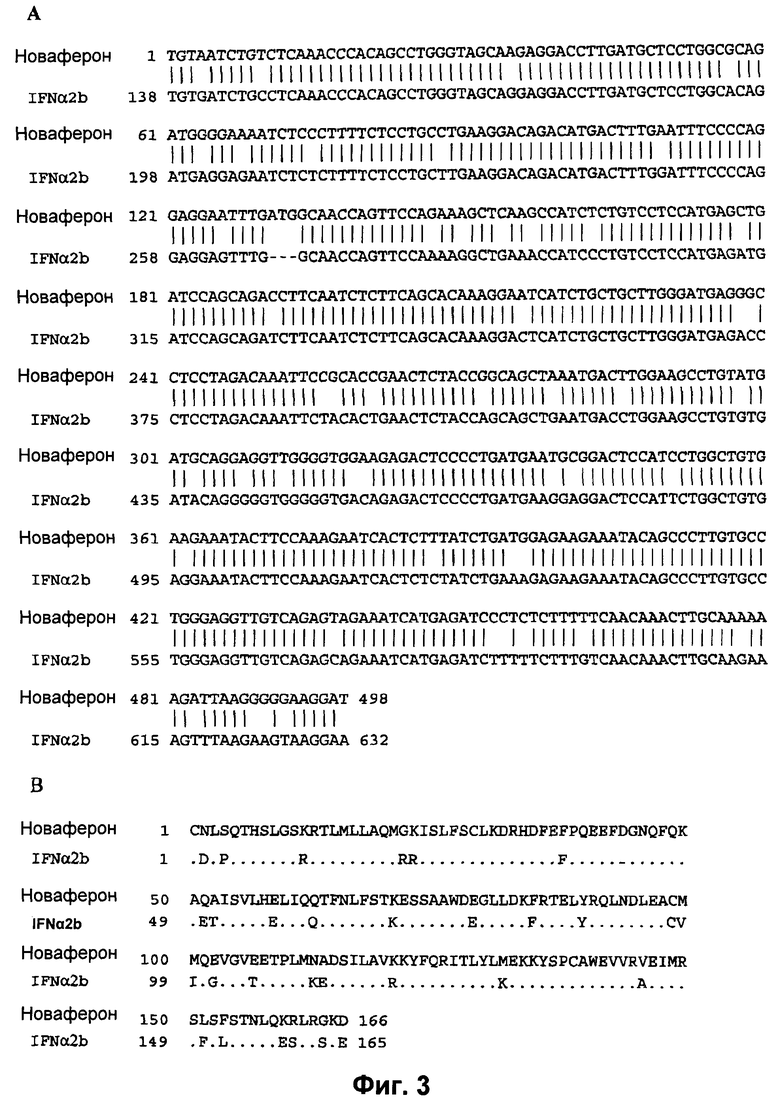
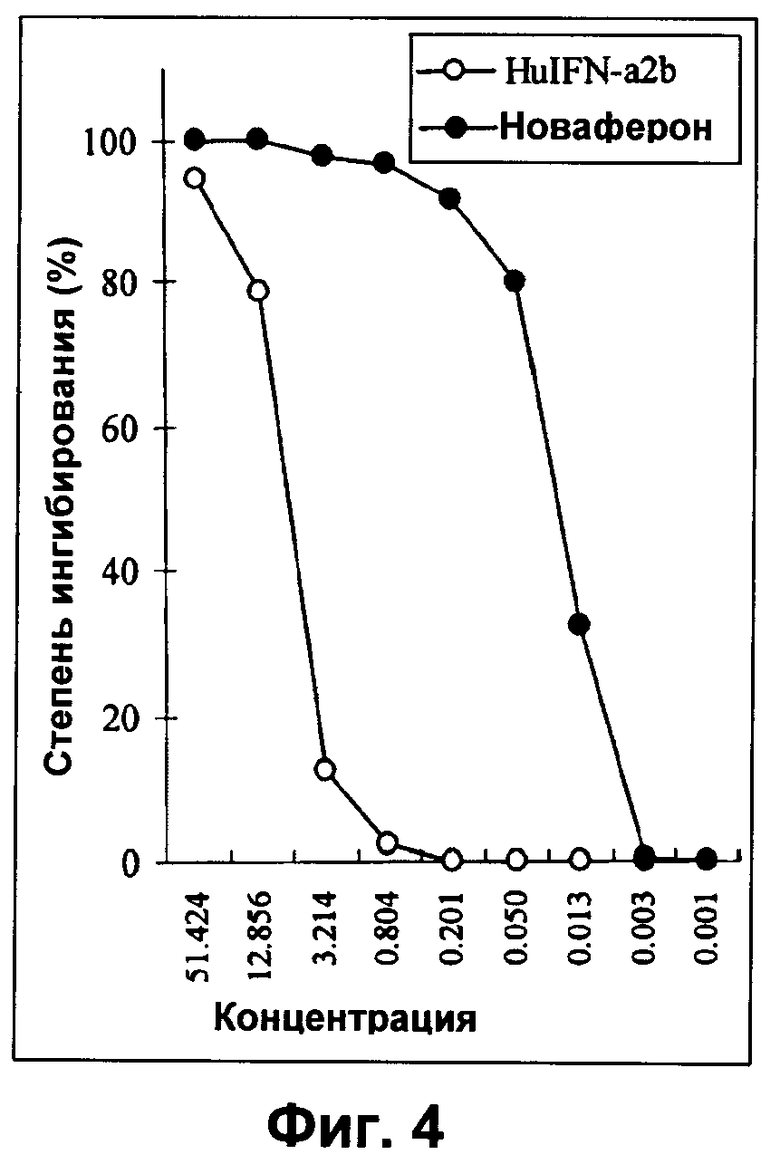
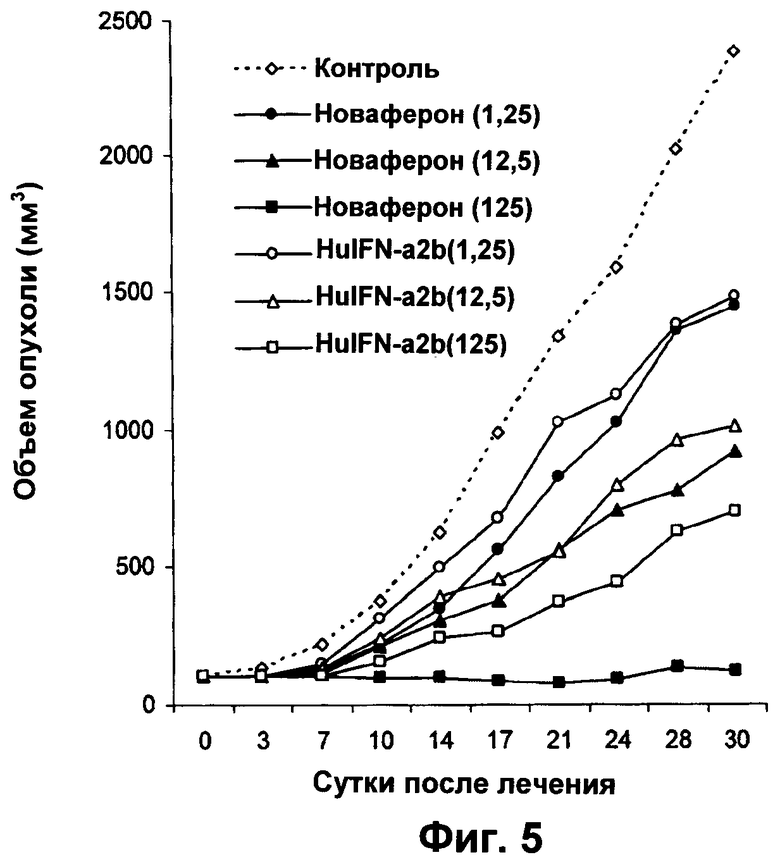
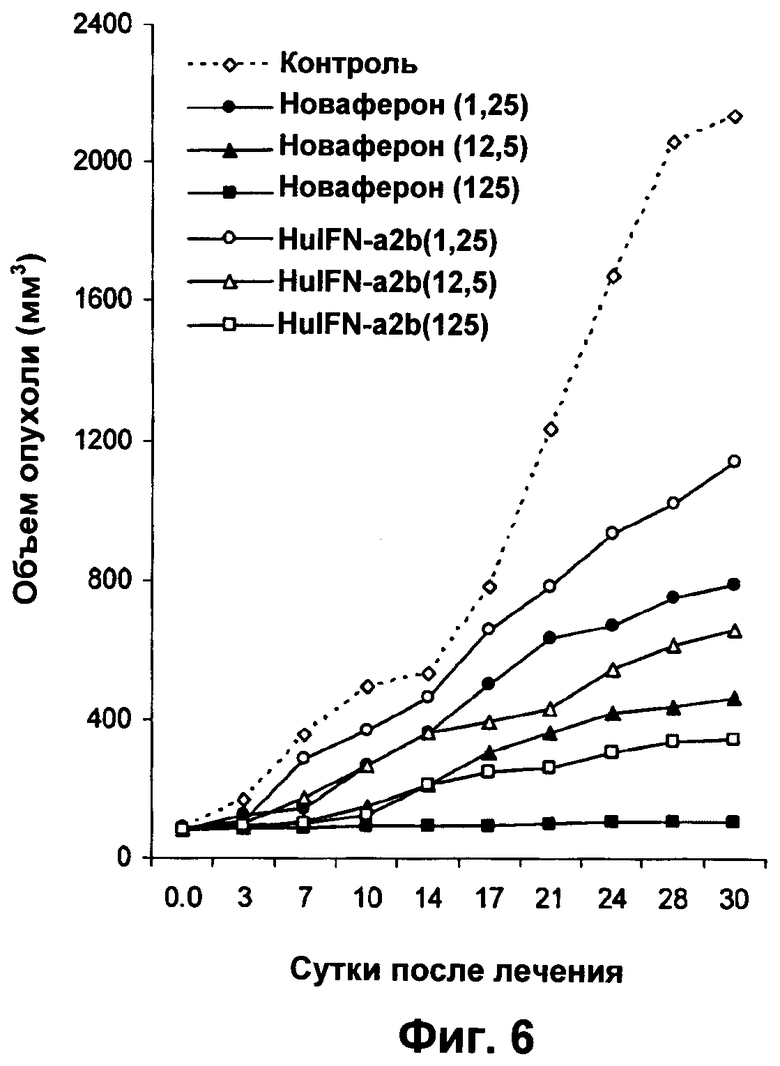
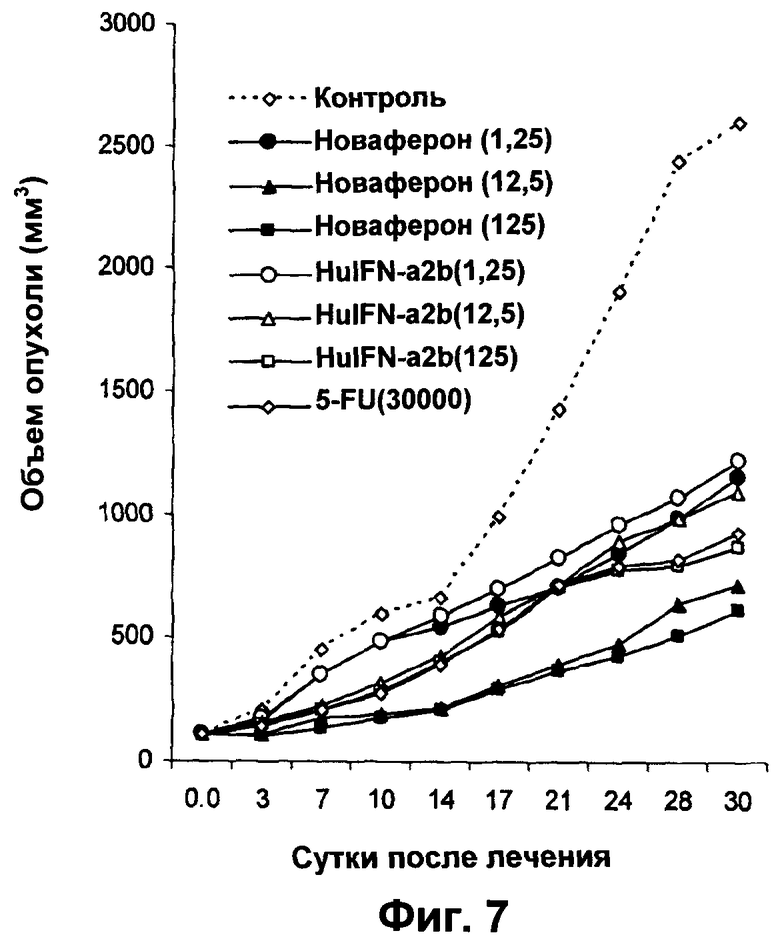
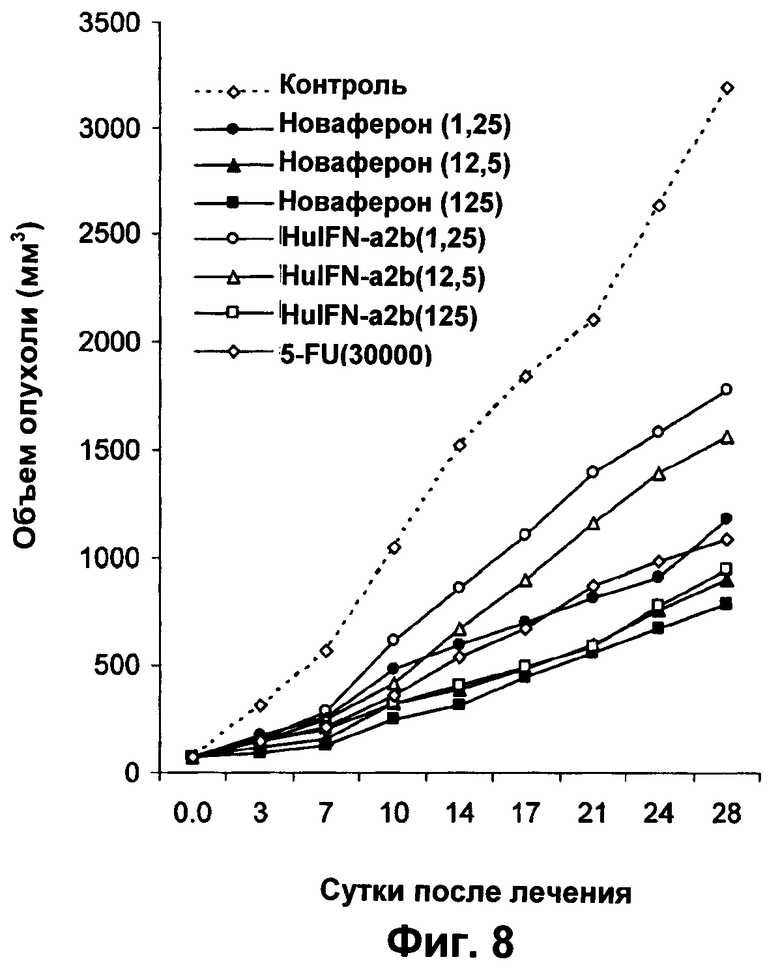
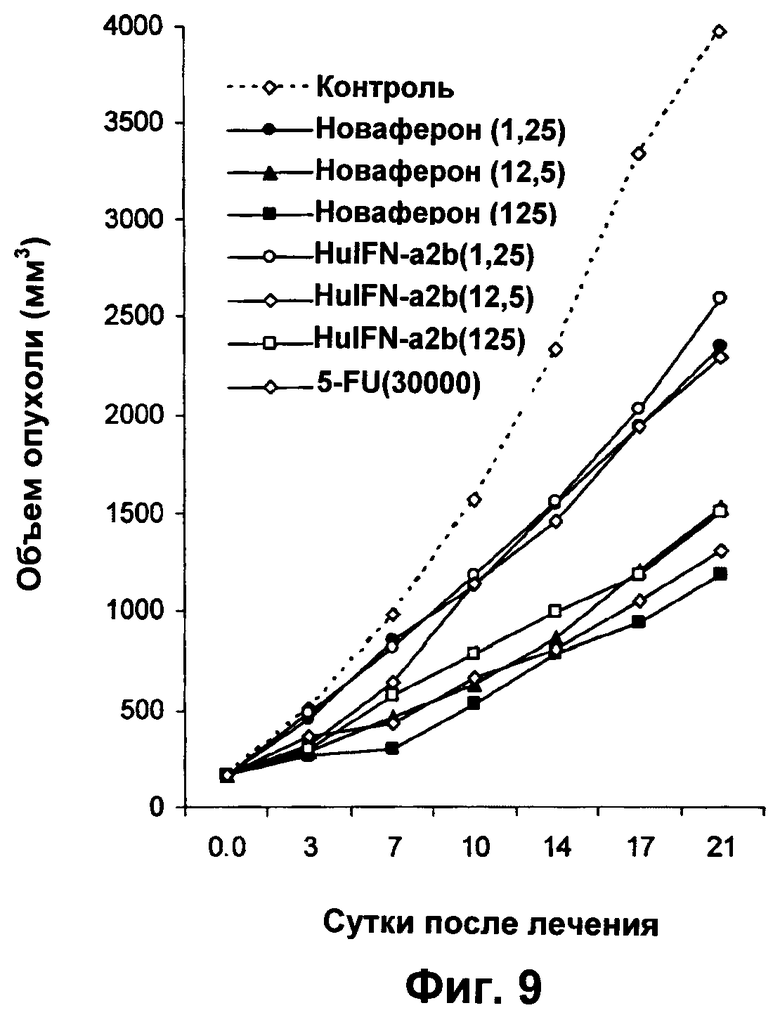
Изобретение относится к области биотехнологии, конкретно к получению интерфероноподобных белков, и может быть использовано в медицине. Получен рекомбинантный белок, созданный путем технологии перетасовки (шаффлинга; от англ. shuffling) генов, обладающий повышенными противовирусной и антипролиферативной активностями по сравнению с существующим в природе человеческим интерфероном-альфа-2b (HulFN-α2b). Полученный полипептид используют в составе композиции в качестве противовирусного, антипролиферативного, противоракового или иммуномодулирующего агента. Изобретение позволяет использовать полученный высокоактивный интерфероноподобный белок для лечения состояния, чувствительного к интерферонотерапии, рака или вирусного заболевания. 11 н. и 38 з.п. ф-лы, 9 ил., 8 табл., 7 пр.
1. Белок, проявляющий интерфероноподобные противовирусную и антипролиферативную биологические активности, где указанный белок характеризуется аминокислотной последовательностью, по меньшей мере на 89% идентичной SEQ ID No:2.
2. Белок по п.1, где указанная последовательность по меньшей мере на 90% идентична SEQ ID No:2.
3. Белок по п.1, где указанная последовательность по меньшей мере на 95% идентична SEQ ID No:2.
4. Белок по любому из пп.1-3, где указанный белок обладает повышенной противовирусной и антипролиферативной активностью по сравнению с HuIFN-α2b.
5. Белок по п.4, где указанный белок имеет противовирусную активность по меньшей мере в 2 раза больше, чем HuIFN-α2b.
6. Белок по п.5, где указанный белок имеет противовирусную активность по меньшей мере в 5 раз больше, чем HuIFN-α2b.
7. Белок по п.6, где указанный белок имеет противовирусную активность по меньшей мере в 10 раз больше, чем HuIFN-α2b.
8. Белок по п.4, где указанный белок имеет антипролиферативную активность по меньшей мере в 10 раз больше, чем HuIFN-α2b.
9. Белок по п.8, где указанный белок имеет антипролиферативную активность по меньшей мере в 50 раз больше, чем HuIFN-α2b.
10. Белок по п.9, где указанный белок имеет антипролиферативную активность по меньшей мере в 100 раз больше, чем HuIFN-α2b.
11. Белок по п.10, где указанный белок имеет антипролиферативную активность по меньшей мере в 200 раз больше, чем HuIFN-α2b.
12. Белок по п.1, где указанный белок является рекомбинантным.
13. Белок по п.1, где указанный белок имеет молекулярную массу 19315 дальтон.
14. Белок по п.1, возможно содержащий остаток метионина на N-конце.
15. Белок по п.1, проявляющий интерфероноподобные противовирусную и антипролиферативную биологические активности, где указанный белок имеет аминокислотную последовательность, по меньшей мере на 95% идентичную SEQ ID No:2, и где указанный белок обладает повышенными противовирусной и антипролиферативной активностями по сравнению с HuIFN-α2b.
16. Белок по п.1, проявляющий интерфероноподобные противовирусную и антипролиферативную биологические активности, где указанный белок характеризуется аминокислотной последовательностью, по меньшей мере на 95% идентичной SEQ ID No:2.
17. Белок по п.1, содержащий последовательность, которая отличается от SEQ ID No:2 по аминокислотам в количестве от 0 до 8, где указанный белок проявляет интерфероноподобные противовирусную и антипролиферативную биологические активности.
18. Белок, содержащий последовательность, которая отличается от SEQ ID No:2 по аминокислотам в количестве от 0 до 19, где указанный белок проявляет интерфероноподобные противовирусную и антипролиферативную биологические активности.
19. Белок по п.18, где указанный белок обладает повышенной противовирусной и антипролиферативной активностью по сравнению с HuIFN-a2b.
20. Белок по п.19, где указанный белок имеет противовирусную активность по меньшей мере в 2 раза больше, чем HuIFN-α2b.
21. Белок по п.18, где указанный белок имеет антипролиферативную активность по меньшей мере в 10 раз больше, чем HuIFN-α2b.
22. Белок по п.21, где указанный белок имеет антипролиферативную активность по меньшей мере в 100 раз больше, чем HuIFN-α2b.
23. Белок по п.18, где указанный белок является рекомбинантным.
24. Белок, имеющий аминокислотную последовательность SEQ ID No:2 или ее фрагмент, содержащие по меньшей мере 146 аминокислот, проявляющий интерфероноподобные противовирусную и антипролиферативную биологические активности.
25. Белковая конструкция, содержащая белок по любому из пп.1-24, функциональным образом соединенный с сахарной, пептидной или полимерной группировкой или меченой молекулой, где указанная конструкция проявляет указанные интерфероноподобные противовирусную и антипролиферативную биологические активности.
26. Белковая конструкция по п.25, где указанный белок гликозилирован.
27. Белковая конструкция по п.25, где указанная группировка представляет собой полипептид.
28. Белковая конструкция по п.25, где указанная группировка не является полипептидом.
29. Белковая конструкция по п.28, где указанная группировка представляет собой молекулу полимера.
30. Белковая конструкция по п.29, где указанной молекулой полимера является линейный или разветвленный полиэтиленгликоль.
31. Белковая конструкция по п.25, где указанная группировка представляет собой меченую молекулу.
32. Полинуклеотид, кодирующий белок по любому из пп.1-24.
33. Полинуклеотид, кодирующий белок, имеющий интерфероноподобные противовирусную и антипролиферативную биологические активности, где указанный полинуклеотид характеризуется нуклеотидной последовательностью, по меньшей мере на 95% идентичной SEQ ID No:1.
34. Полинуклеотид по п.33, где указанная последовательность по меньшей мере на 97% идентична SEQ ID No:1.
35. Полинуклеотид по п.34, где указанная последовательность по меньшей мере на 98% идентична SEQ ID No:1.
36. Полинуклеотид по любому из пп.33-35, где указанный белок является несуществующим в природе.
37. Полинуклеотид по п.36, где указанный белок обладает повышенными противовирусной и антипролиферативной активностями по сравнению с человеческим интерфероном-альфа-2b (HuIFN-α2b).
38. Полинуклеотид по п.37, где указанный белок имеет противовирусную активность по меньшей мере в 2 раза больше, чем HuIFN-α2b.
39. Полинуклеотид по п.37, где указанный белок имеет антипролиферативную активность по меньшей мере в 10 раз больше, чем HuIFN-α2b.
40. Полинуклеотид по п.33, кодирующий белок, имеющий интерфероноподобные противовирусную и антипролиферативную биологические активности, где указанный полинуклеотид характеризуется нуклеотидной последовательностью, по меньшей мере на 97% идентичной SEQ ID No:1.
41. Вектор экспрессии, содержащий полинуклеотид по любому из пп.33-40.
42. Клетка-хозяин для продуцирования белка, проявляющего интерфероноподобные противовирусную и антипролиферативную биологические активности, содержащая рекомбинантный вектор по п.41.
43. Композиция, пригодная в качестве противовирусного агента, антипролиферативного агента, противоракового агента или иммуномодулирующего агента, содержащая белок по любому из пп.1-24 и фармацевтически приемлемый носитель, разбавитель или эксципиент.
44. Композиция по п.43, содержащая белок по п.15.
45. Применение белка по любому из пп.1-24 в качестве противовирусного агента, антипролиферативного агента, противоракового агента или иммуномодулирующего агента.
46. Способ лечения состояния, чувствительного к интерферонотерапии, рака или вирусного заболевания, включающий введение субъекту, нуждающемуся в терапии, терапевтически эффективного количества белка по любому из пп.1-24.
47. Способ по п.46, где указанным субъектом является человек.
48. Способ по п.46, где указанный белок вводят вместе с фармацевтически приемлемым носителем, разбавителем или эксципиентом.
49. Способ по п.46, где указанный белок терапевтически эффективен в отношении широкого диапазона разных типов рака, при этом указанный рак выбран из группы, состоящей из меланомы, колоректальной аденокарциномы, почечно-клеточного рака, гепатомы, лимфомы, рака предстательной железы, аденокарциномы желудка, рака пищевода, рака легкого, цервикальной аденокарциномы и цервикального рака.
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНЫХ И ТРОФИЧЕСКИХ ПРОЦЕССОВ В ТКАНЯХ ОРГАНИЗМА | 1994 |
|
RU2095067C1 |
| WO 2005023290 А2, 17.03.2005 | |||
| КВАЗИУРАВНОВЕШЕННЫЙ ИЗМЕРИТЕЛЬ КОМПЛЕКСНЫХПАРАМЕТРОВ | 0 |
|
SU236627A1 |
| Электромагнитное приспособление для зажимания свариваемых предметов | 1925 |
|
SU7838A1 |
Авторы
Даты
2012-12-10—Публикация
2007-06-22—Подача