Настоящее изобретение относится к новым производным бензо[g]хинолина, их получению, их применению в качестве фармацевтических средств и содержащим их фармацевтическим композициям.
Настоящее изобретение относится к соединению, выбранному из группы, состоящей из соединения формулы Ia,
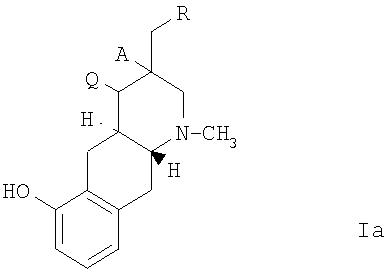
где А и Q каждый представляет собой Н или вместе образуют дополнительную связь и где асимметричный центр в положении 3 может быть рацемическим или в виде оптически активной формы, и где R представляет собой формулу Ib или Ic,
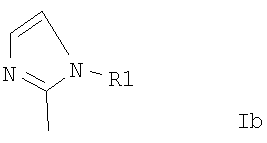
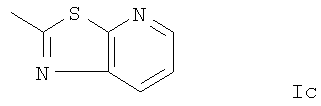
и где R1 представляет собой алкил в форме свободного основания или в форме кислотной аддитивной соли.
В предпочтительном варианте осуществления А и Q каждый представляет собой Н. В дальнейшем предпочтительном варианте осуществления А и Q вместе образуют дополнительную связь.
Заместитель CH2-R в положении 3 формулы Ia предпочтительно находится в конфигурации 3R при условии, что А и Q каждый представляет собой Н.
R1 предпочтительно выбирается из алкила, имеющего от 1 до 4 атомов углерода. Соответственно, используемый здесь алкил представляет собой особенно С1-С4-алкил, например н-бутил, втор-бутил, трет-бутил, н-пропил, изопропил или особенно метил или также этил.
В более предпочтительном варианте осуществления R1 представляет собой С1-алкил, например метил.
Более конкретно настоящее изобретение относится к соединению, выбранному из группы, состоящей из соединения формулы I и соединения формулы II,
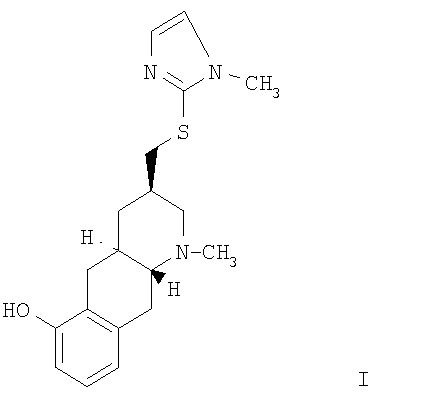
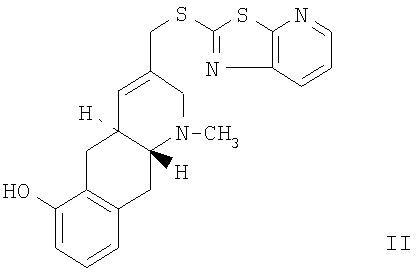
где СН2-S-имидазольный заместитель в формуле I представлен конфигурацией 3R в форме свободного основания или в форме кислотной аддитивной соли.
Еще более предпочтительным вариантом осуществления настоящего изобретения является соединение формулы I, как указано выше. Также особо предпочтительным является соединение формулы II, как указано выше.
Кислотные аддитивные соли могут быть получены из свободных оснований известным способом и наоборот. Подходящие кислотные аддитивные соли для применения в соответствии с данным изобретением включают, например, гидрохлорид.
Соединения формулы Ia, I и II и их физиологически приемлемые кислотные аддитивные соли, обозначенные в дальнейшем как соединения по изобретению, проявляют ценные фармакологические свойства в испытаниях на животных и поэтому полезны в качестве фармацевтических средств.
Предшествующий уровень техники
Соединения настоящего изобретения проявляют улучшенные фармакологические свойства по сравнению с похожими соединениями предшествующего уровня техники, например ЕР 912'553.
Подробное описание настоящего изобретения
В частности, соединения по изобретению приводят к уменьшению внутриглазного давления (IOP) у кроликов в концентрации от 10 до 100 мкМ. Самцов кроликов весом около 2,5 кг закрывали и клетках таким образом, что головы оставались в свободном положении. Растворы с тестируемым соединением применяли для правого глаза и плацебо растворы для левого глаза (2 капли в каждый, то есть приблизительно 40 мкл). Глаза сначала обезболивали раствором, содержащим новезин (0,4%) и флуоресцеин (0,05%), и определяли глазное давление с различными интервалами после введения (10, 20, 30, 60, 90, 120, 180 и 240 минут), для чего использовался тонометр согласно Голдбергу.
Неожиданно выяснилось, что соединения по изобретению проявляют сильную IOP-понижающую эффективность, превосходную толерантность и длительный срок действия и поэтому особенно полезны для лечения глаукомы и миопии. В предпочтительном варианте это относится к лечению глаукомы.
Для вышеупомянутого показания соответствующая дозировка будет, конечно, изменяться в зависимости от, например, используемого соединения, пациента, способа введения и серьезности излечиваемого заболевания. Однако обычно удовлетворительные результаты у животных обнаружены при применении ежедневной дозировки приблизительно от 0,1 приблизительно до 10 мг/кг веса животного. Для крупных млекопитающих, например людей, обозначенная ежедневная дозировка находится в диапазоне приблизительно от 5 приблизительно до 200 мг, предпочтительно приблизительно от 10 приблизительно до 100 мг соединения, удобно вводимого в раздельных дозах до 4 раз в день или в форме длительного высвобождения.
Соединения по изобретению могут вводиться в свободной форме или в форме фармацевтически приемлемой соли. Такие соли могут быть получены обычным способом и могут проявлять ту же самую активность, как и свободные соединения.
Согласно настоящему изобретению обеспечивается соединение по изобретению для применения в качестве фармацевтического средства, например, для лечения глаукомы и миопии.
Настоящее изобретение, кроме того, предусматривает фармацевтическую композицию, включающую соединение по изобретению в смеси по крайней мере с одним фармацевтически приемлемым разбавителем или носителем. Такие композиции могут быть получены обычным способом. Единичные дозированные формы содержат, например, приблизительно от 0,25 приблизительно до 50 мг соединения согласно изобретению.
Соединения согласно изобретению могут вводиться любым обычным способом, например парэнтерально, например в форме инъекционных растворов или суспензий, или энтерально, предпочтительно орально, например в форме таблеток или капсул.
Более предпочтительно, они применяются местно в глаз в концентрации от 0,002 до 0,02% офтальмологического раствора.
Офтальмологический носитель является таким, что соединение находится во взаимодействии с поверхностью глаза в течение достаточного периода времени, чтобы позволить соединению проникнуть в роговичные и внутренние области глаза.
Фармацевтически приемлемый офтальмологический носитель может представлять собой, например, мазь, растительное масло или инкапсулирующий материал.
В соответствии с вышеизложенным настоящее изобретение также обеспечивает соединение по изобретению для применения в качестве фармацевтического средства для лечения глаукомы и миопии.
Кроме того, настоящее изобретение относится к применению соединения по изобретению для изготовления лекарственного средства для лечения глаукомы и миопии.
В следующем варианте осуществления настоящее изобретение обеспечивает способ лечения глаукомы и миопии субъекта, который нуждается в таком лечении, который включает введение такому субъекту терапевтически эффективного количества соединения по изобретению.
Пример 1
[3R,4aR,10aR]-1-метил-3β-гидроксиметил-6-метокси-1,2,3,4,4аα,5,10,10αβ-октагидробензо[g]хинолин
К раствору 5,78 г (20 мМ) [3R, 4aR, 10aR]-1-метил-3β-метоксикарбонил-6-метокси-1,2,3,4,4аα,5,10,10αβ-октагидробензо[g]хинолина в 100 мл толуола добавляли по каплям раствор, содержащий 12 мл SDBA (натрий дигидро-бис-(2-метоксиэтокси) алюминат) (70% в толуоле, 42 мм) в атмосфере аргона при комнатной температуре в течение одного часа. Затем добавляли по каплям в охлажденную льдом реакционную смесь 10 мл NaOH (30%). Осажденные кристаллы отфильтровывали, промывали водой и толуолом и высушивали. Полученное соединение, указанное в заголовке, имеет tпл 148°С; [α]20 D=-120° (с=0,425 в этаноле).
Пример 2
[3R, 4aR, 10aR]-1-метил-3β-мезилоксиметил-6-метокси-1,2,3,4,4аα,5,10,10αβ-октагидробензо[g]хинолин
12 мл (153 мМ) метансульфохлорида добавляли по каплям при комнатной температуре к раствору 20 г (76,5 мМ) соединения, полученного в примере 1, в 150 мл пиридина. Температуру ниже 45°С поддерживали охлаждением льдом. После перемешивания в течение 2 часов при комнатной температуре рН раствора доводили до 7-8 насыщенным раствором КНСО3 при 0°С и экстрагировали этилацетатом. После высушивания над Na2SO4, фильтрации и концентрирования в вакууме соединение, указанное в заголовке, получали в виде бежевых кристаллов и использовали непосредственно на следующей стадии.
Пример 3
Раствор 2 г (5,9 ммоль) мезилата, полученного в примере 2, и 1 г (8,8 мМ) 1-метил-2-меркаптоимидазола в 30 мл диметилформамида смешивали с 2 мл 10 N NaOH и перемешивали при 60°С в течение 3 часов. Полученную суспензию концентрировали в вакууме и затем экстрагировали этилацетатом/изопропанолом (9:1). После высушивания над Na2SO4, фильтрации и удаления растворителя в вакууме получали метиловый эфир соединения формулы I, который затем непосредственно использовали на следующей стадии.
Пример 4 => соединение формулы I:
К раствору 1,76 г (5 ммоль) соединения, полученного в примере 1 в 10 мл метиленхлорида, медленно добавляли по каплям при температуре -50°С 25 мл трибромида бора (1 молярный в метиленхлориде). Суспензию перемешивали в течение 3 часов при комнатной температуре, нейтрализовали водным аммиаком и экстрагировали этилацетатом/изопропанолом (9:1). Экстракт высушивали над сульфатом натрия, фильтровали и удаляли растворитель в вакууме. Добавляли избыточное количество соляной кислоты в метаноле до тех пор, пока не будет достигнут уровень рН 1. Затем растворитель постепенно удаляли до кристаллизации. Гидрохлорид перекристаллизовывали из метанола/этанола (1:1), tпл 272-274°С. αD 20=-38° (с=0,375 в этаноле/воде). C19H25N3OS (2 HCl), MW=416,4.
Пример 5
К раствору 4 г (15,4 мМ) 1,2,4aS-транс-5,10,10а-гексагидро-6-метокси-1-метил-3-гидроксиметилбензо[g]хинолина (см. №201869-32-1, Chem. Abstr.) в 40 мл толуола медленно добавляли по каплям 1,3 мл (17,9 мМ) тионилхлорида при температуре 0°С. Суспензию перемешивали в течение 12 часов при комнатной температуре. Полученный хлорид кристаллизовался произвольно. После фильтрации и промывки толуолом продукт непосредственно использовали на следующей стадии.
Пример 6
К раствору 4 г (17,6 мМ) хлорида, полученного в примере 5, в 100 мл дихлорметана медленно добавляли 50,5 мл 1 молярного трибромида бора в дихлорметане при -70°С. Суспензию перемешивали в течение 3 часов при комнатной температуре, нейтрализовали NaHCO3 и экстрагировали этилацетатом/изопропанолом (9:1). После высушивания над Na2SO4, фильтрования и концентрации в вакууме соответствующее производное 6-гидроксибензо[г]хинолина непосредственно использовали на следующей стадии.
Пример 7 => (соединение формулы II)
Раствор 930 мг (3,5 мМ) производного 6-гидроксибензо[г]хинолина примера 6 и 705 мг (4,2 мМ) тиазоло[4,5-b]пирридин-2-тиола в 30 мл диметилформамида смешивали с 10N NaOH и перемешивали при комнатной температуре в течение 1 часа. Полученную суспензию концентрировали в вакууме и затем экстрагировали этилацетатом/изопропанолом (9:1). После высушивания над Na2SO4, фильтрации и удаления растворителя в вакууме полученный остаток хроматографировали на силикагеле, используя дихлорметан/этилацетат/метанол в соотношении 40:55:5. Очищенный материал затем преобразовывали в гидрохлорид добавлением HCl в этаноле и последующим упариванием. Перекристаллизация из метанола/этанола приводила к получению соединения формулы II в виде гидрохлорида с tпл 240°C (разруш.), αD20=-101° (с=0,405 в этаноле/воде). C21H21N3OS2 (HCl), MW=432,01.
Описываются соединение формулы 1а, где А и Q каждый представляет собой Н и где асимметричный центр в положении 3 может быть в виде оптически активной формы, R представляет собой формулу 1b и где R1 представляет собой алкил, содержащий от 1 до 4 атомов углерода, в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли, и фармацевтически приемлемая композиция, обладающая действием, уменьшающим внутриглазное давление, на основе этого соединения. Описываются также способ лечения глаукомы или миопии и применение соединения формулы 1а для изготовления лекарственного средства для лечения глаукомы и миопии. 4 н. и 3 з.п. ф-лы.
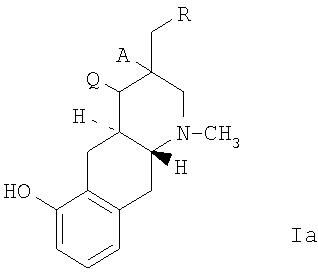
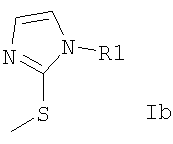
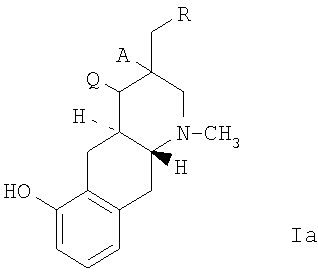
где А и Q каждый представляет собой Н, и где асимметричный центр в положении 3 может быть в виде оптически активной формы, и где R представляет собой формулу Ib
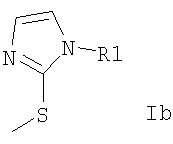
и где R1 представляет собой алкил, содержащий от 1 до 4 атомов углерода, в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли.
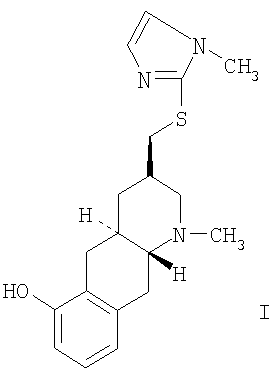
где СН2-S-имидазольный заместитель в формуле I находится в 3R конфигурации, как указано выше в формуле I в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли.
| WO 9801444 А1, 15.01.1998 | |||
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: ООО «Новая Волна», т.1, 2001, с.258. |
Авторы
Даты
2009-02-10—Публикация
2003-03-06—Подача