Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к способу и к вспомогательной или дополняющей композиции к традиционной терапии при лечении или профилактике рака предстательной железы у млекопитающих, а также к способу и композиции, пригодным для профилактики возникновения рака предстательной железы у млекопитающих. Композиция по настоящему изобретению включает витамин Е или производное витамина Е в сочетании с селеном, в связанной или в несвязанной форме, в количествах, которые обеспечивают профилактический и терапевтический эффект в отношении карциномы предстательной железы млекопитающих.
Предпосылки изобретения
Злокачественная опухоль предстательной железы является наиболее типичным видом рака у млекопитающих, особенно у людей среди мужчин Северной Америки, и она является второй основной причиной смерти от рака у мужчин в странах Запада, см. Parker SI, и соавт., "Cancer Statistics 1997", CA Cancer J Clin (1997) 47:5-27. Осложнению данного заболевания способствуют разнообразные факторы, такие как неизвестная этиология, изменчивая патология, запутанная взаимосвязь с эндокринными факторами и анапластическое развитие.
Данные эпидемиологических, клинических и лабораторных исследований подтверждают концепцию, что комплексное взаимодействие между системой антиоксидантной защиты хозяина и антиоксидантами, поступающими с пищей, может принимать участие в происхождении и развитии рака предстательной железы, а также и других видов рака. Например, дополнительное потребление антиоксиданта витамина Е связывают со снижением примерно на одну треть смертности от рака предстательной железы, см., например, Fleshner NE, "Vitamin E Inhibits the High-Fat Diet Promoted Grown of Established Human Prostate LNCaP Tumors in Nude Mice", J Urol (1999) 161:1651-1654. Все больший интерес вызывает вопрос о возможной роли микроэлементов в профилактике рака и воздействии на него. Сообщается также о наличии косвенной взаимосвязи между уровнями биологической доступности селена в среде, окружающей человека, и смертностью от рака. См. Hunter DJ, Morris JS, Stampfer MJ и соавт., "A Prospective Study of Selenium Status and Breast Cancer Risk", JAMA (1990) 264:1128-1131; см. Van den Brandt PA, Goldbohn RA, Bode P и соавт., "A Prospective Study on Toenail Selenium Levels and Risk of Gastrointestinal Cancer", J Natl Cancer Inst (1993) 85:224-229; см. Van Den Brandt PA, Goldbohn RA, Bode P и соавт., "Prospective Study On Selenium Status And The Risk Of Lung Cancer", Cancer Res (1993) 53:4860-4865; см. Helzlsouer KJ, Comstock GW, Morris JS и соавт., "Selenium, Lycopene, A-Tocopherol, B-Carotene, Retinol and Subsequent Bladder Cancer", Cancer Res (1989) 49:6144-6148; см. Willet We, Polk BF, Morris JS и соавт., "Prediagnostic Serum Selenium and Risk of Cancer", Lancet (1983) 2:130-134; см. Levander OA, "Scientific Rationale for the 1989 Recomended Dietary Allowance for Selenium", Perspect Pract (1991) 91:1572-1576. Накопленные данные дают основание полагать, что при постановке многих моделей экспериментального канцерогенеза добавление в пищу селенита натрия ведет к снижению частоты возникновения карцином, индуцированных химическими канцерогенами, см. Heinonen OP, и соавт., "Prostate Cancer and Supplementation with Alpha-Tocopherol and Beta-Carotene: Incidence and Mortality in a Controlled Trial", J Natl Cancer Inst. (1998) 90:440-446.
Эпидемиологические данные и связанное с ними предшествующее исследование позволяют предположить, что принимаемый внутрь c пищей микроэлемент и диета играют решающую роль в канцерогенезе предстательной железы. Показано также, что в канцерогенезе предстательной железы участвуют и андрогены, см. Ripple MO, и соавт., "Prooxidant-Antioxidant Shift Induced by Androgen Treatment of Human Prostate Carcinoma Cells", J Natl Cancer Inst (1997) 89:40-48. Диету и андрогены может соединять окислительный стресс. Данный процесс может быть обусловлен разновидностями химически активного кислорода хозяина, которые могут запускать канцерогенез. Предшествующим исследованием установлено, что экзогенный андроген повышает окислительный стресс в линиях злокачественных клеток предстательной железы человека, см. Fleshner, J Urol (1995) 161:1651-1654.
Биологические часы клеточного цикла регулируют развитие клеток через их рост и циклы деления. Так, например, они определяют, продолжать ли клетке пролиферацию или нет и входить ли в состояние покоя. В этой связи репликация ДНК и митоз контролируются путем активации специфичных для S-фазы и М-фазы циклинзависимых белковых киназ (CDK). Каталитические субъединицы CDK активны лишь в комплексе с их специфичными регуляторными субъединицами, именуемыми циклинами. CDK контролируют различные клеточные процессы путем фосфорилирования соответствующих субстратов в клетке, см. Solomon MJ, "Activation of the Various Cyclin/cdk2 Proteins", Curr. Opin. Cell Biol. (1993) 5:180-186. Циклины регулируют, связывают и направляют CDK к соответствующим субстратам на протяжении разных фаз клеточного цикла, диктуя таким образом, где и когда эти субстраты должны фосфорилироваться, см. Hartwell L, "Defects in a Cell Cycle Checkpoint May Be Responsible for the Genomic Instability of Cancer Cells", Cell (1992) 71:543-546. Другими важными компонентами являются ингибиторы CDK (CKI), такие как р21 и р27, которые блокируют действие специфичных циклин-CDK-комплексов. Это препятствует клеточной пролиферации, ускоряя тем самым вхождение клеток в состояние покоя, именуемого фазой G0. См. Sherr CJ и соавт. Genes Dev. (1999) 13:1501-1512.
Неконтролируемая клеточная пролиферация является признаком рака. Злокачественные клетки содержат или приобретают поврежденные гены, которые непосредственно регулируют их клеточный цикл. Подобно другим видам рака злокачественная опухоль предстательной железы связана с потерей контроля над клеточным циклом, что приводит к нерегулируемому росту клеток. Точный механизм, с помощью которого это происходит, до сих пор не известен, см. La Thangue NB, "Introduction: Cell Cycle Regulation and Cancer", Seminars in Cancer Biol. (1995) 6:61-62. Прекращение клеточного цикла опосредуется с помощью p27 и p21 CKI. Смотрите Tslhlias J и соавт., "Involved of p27Kip1 in G1 Arrest by High-Dose 5α-Dihydrotestosterone in LNCaP Human Prostate Cancer Cells", Oncogenes (2000) 19:670-679.
Основу механизма, контролирующего клеточный цикл, составляют регуляторные циклиновые субъединицы, объединенные с каталитическими серин/треониновыми CDK-субъединицами, которые специфически фосфорилируют субстраты клеточного цикла. См., напр., Morgan DO, "Cyclin-Dependent Kinases: Engines, Clocks and Microprocessors", Ann. Rev. Dev. Biol. (1997) 13:261-291. Активация CDK2 с помощью циклина Е в поздней G1/в конце G1 и с помощью циклина А на переходе фаз G1 и S, а также активация CDK2 циклином В на переходе фаз G2 и М подтверждает участие этих циклин-CDK-комплексов в специфичных контрольных точках регуляции клеточного цикла. Также известно, что р21, ингибитор циклинзависимой киназы, может вызывать задержку клеточного цикла в G1- и/или G2-фазе вследствие ингибирования киназной активности. Кроме того, р27 регулируется с помощью ряда митогенных и ростовых ингибиторных цитокинов, а также путем контактного ингибирования. См. Polyak C и соавт., "p27Kip1, a Cyclin-cdk Inhibitor, Links Transforming Growth Factor-β and Contact Inhibition to Cell Cycle Arrest", Genes Dev. (1994) 8:9-22. Хотя прекращение роста не всегда связано с повышением уровня белка р27, равным образом он является существенным медиатором прекращения G1, потому что он действует во время фазы G0 и в ранней фазе G1 клеточного цикла и подавляет комплексы циклин-D1-CDK4 и циклин E-CDK2. См. Pagano M и соавт., "Role of Ubiquitin-Proteasome Pathway in Regulating Abundance of the Cyclin-Dependent Kinase Inhibitor p27", Science (1995) 269:682-685.
Несмотря на антиканцерогенное действие витамина Е и селена, которое было обнаружено и изучено, применение сочетания этих двух веществ для профилактики и/или лечения рака предстательной железы млекопитающих не было описано. Кроме того, хотя существуют и другие агенты, пригодные для химиотерапии рака, а также другие инвазивные факультативные средства лечения рака предстательной железы, такие как иссечение раковой предстательной железы или лучевая терапия для уменьшения размера опухоли, более желательно было бы создать композицию, пригодную в качестве вспомогательных или дополняющих веществ с низкой токсичностью к традиционной терапии, и которая могла бы служить в качестве антиканцерогенного агента, в частности для рака предстательной железы. В качестве альтернативы, желательно создать композиции, которые повышают уровни р21 и/или р27, а также других CDK-ингибиторов для профилактики и лечения рака предстательной железы млекопитающих.
Краткое изложение сущности изобретения
Цель настоящего изобретения заключается в создании композиции и в разработке способа, которые можно было бы использовать для лечения или профилактики рака предстательной железы млекопитающих.
Кроме того, цель настоящего изобретения заключается в создании композиции, включающей витамин Е, или производные витамина Е, или аналоги витамина Е и селен, или соль селена, или производное селена, в свободной или в связанной форме, в которой данная композиция проявляет повышенные антиканцерогенные свойства, в частности для профилактики или лечения рака предстательной железы млекопитающих.
Другая цель настоящего изобретения заключается в разработке способа и создании вспомогательной или дополняющей композиции к традиционной терапии для лечения или профилактики возникновения рака предстательной железы у млекопитающих.
Еще одна цель настоящего изобретения заключается в разработке способа и создании композиции, которые подавляют образование белковых комплексов циклин-CDK путем повышающей регуляции р21 или р27 для профилактики и лечения рака предстательной железы у млекопитающих.
Краткое описание чертежей
Фиг.1а и 1b
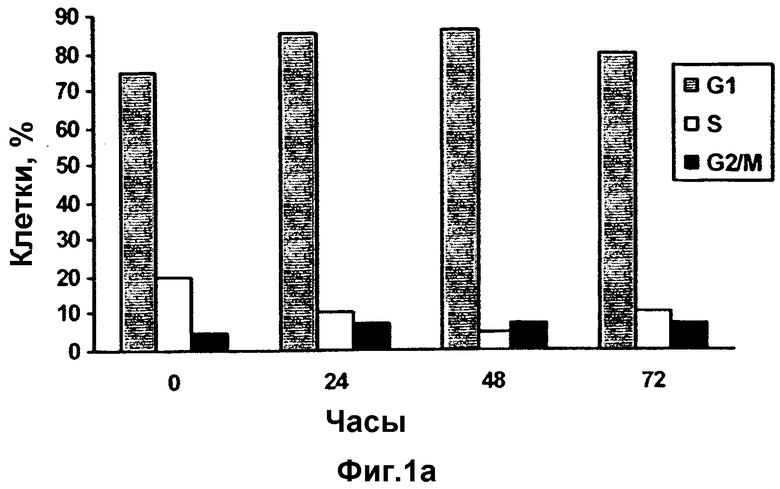
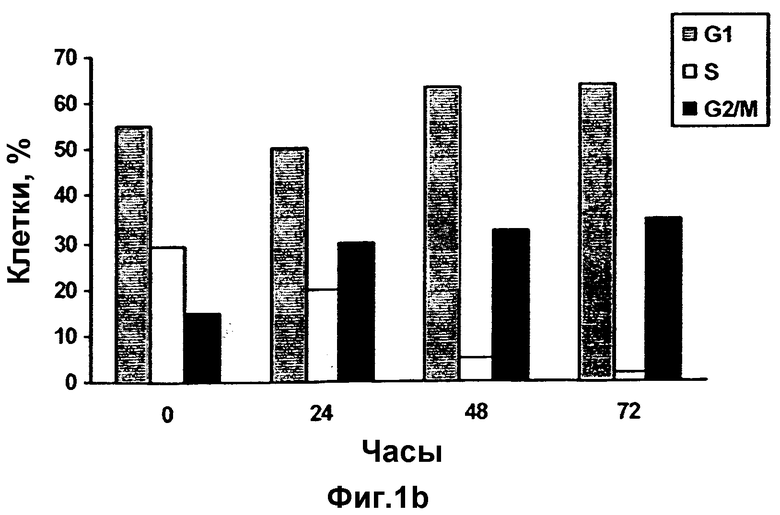
FACS-анализ клеток LNCaP (a) и PC3 (b), обработанных 20 мкг/мл витамина Е: после добавления к культуральной среде витамина Е клетки собирают с разными интервалами времени и готовят их для FACS-анализа. Наблюдают прекращение фазы G1 у клеток LNCaP и прекращение фазы G2/M у клеток РС3.
Фиг.2а и 2b
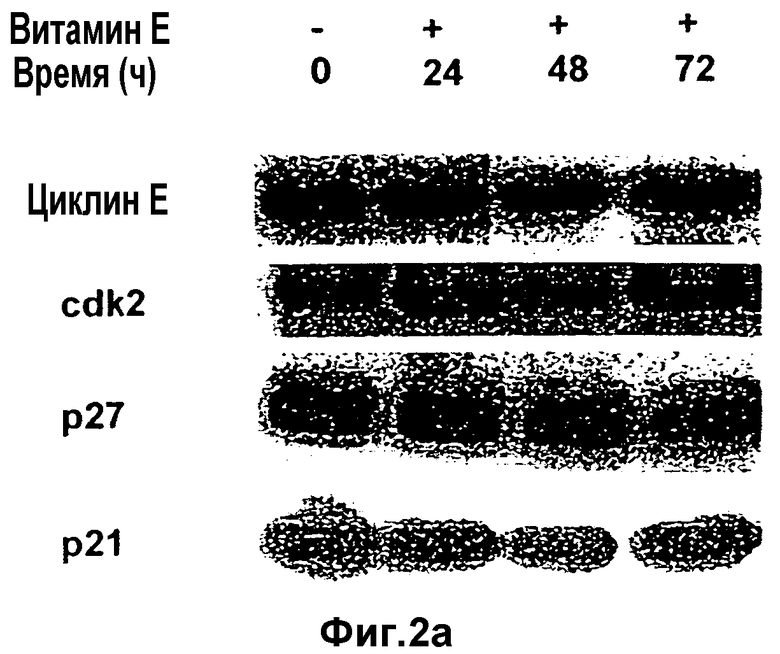
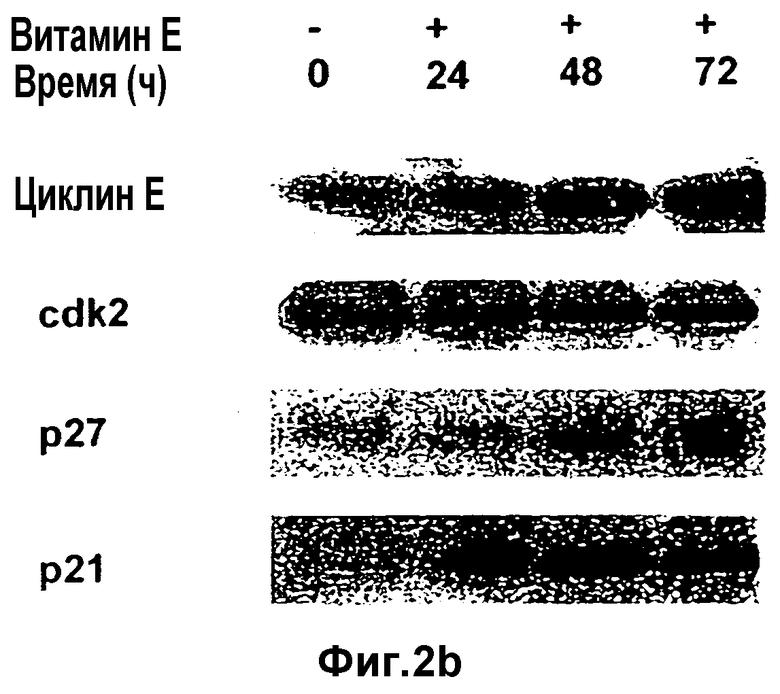
Регуляторы клеточного цикла во время прекращения с помощью витамина Е: после добавления к культуральной среде витамина Е клетки собирают с указанными временными интервалами. Получают лизаты (а) LNCaP и (b) PC3 и подвергают их фракционированию в SDS-PAGE. Белки детектируют иммуноблоттингом с помощью индикаторных антител.
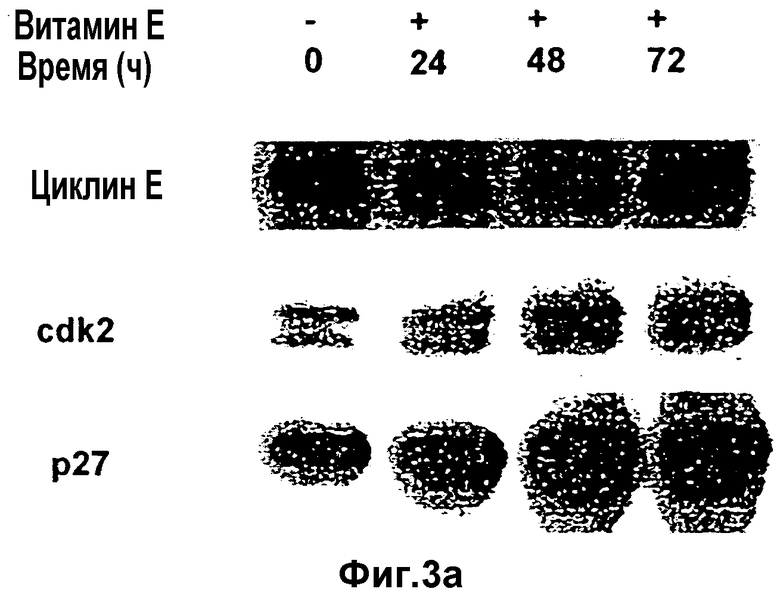
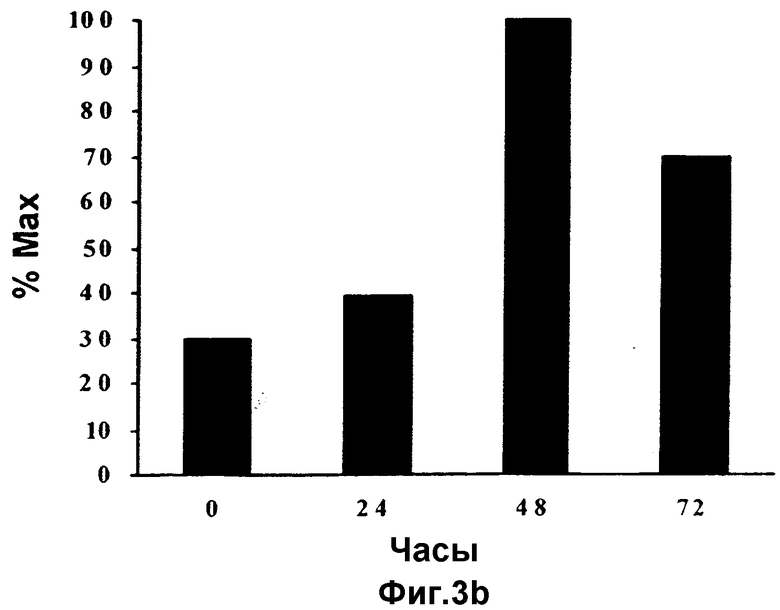
Фиг.3а и 3b(а) Циклин Е-иммунные комплексы (LNCaP): после добавления к культуральной среде витамина Е клетки извлекают с различными временными интервалами. Иммунопреципитируют циклин Е, комплексы подвергают фракционированию с помощью SDS-PAGE и иммуноблоты взаимодействуют с антителами для детекции связавшихся белков. (b)Циклин Е-ассоциированный р27 подвергают количественному анализу с помощью денситометрии вышеуказанных блотов (а). Клетки LNCaP демонстрируют трехкратное увеличение содержания циклина Е, связанного р27.
Фиг.4а и 4b
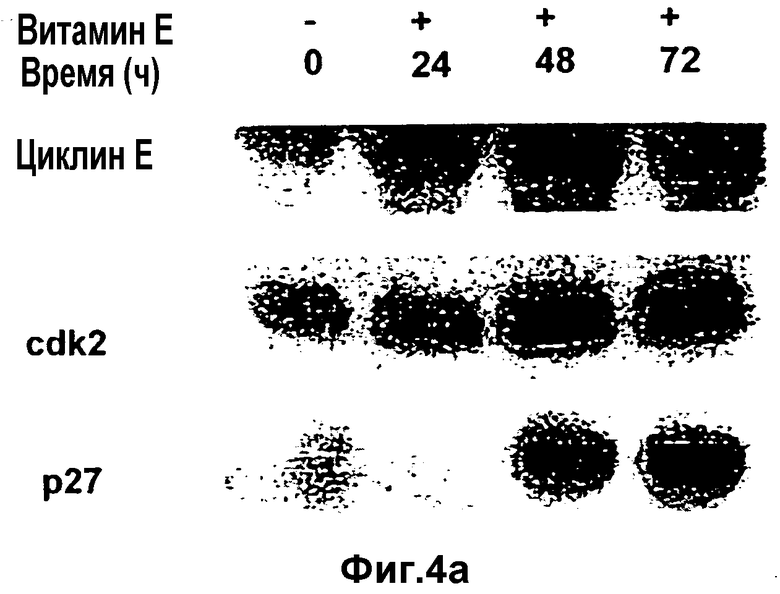
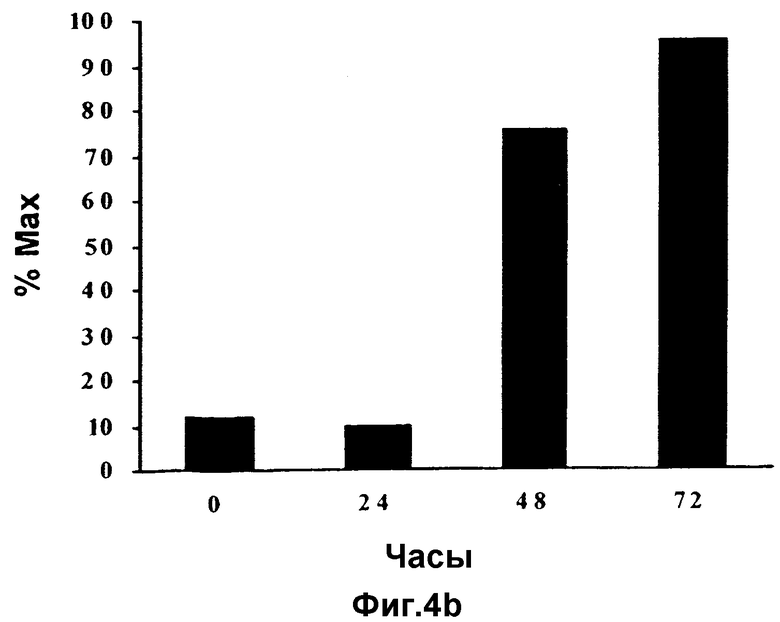
(а) Циклин Е-иммунные комплексы (РС3): после добавления к культуральной среде витамина Е клетки извлекают с временными интервалами. Иммунопреципитируют циклин Е, комплексы подвергают фракционированию с помощью SDS-PAGE и иммуноблоты взаимодействуют с антителами для детекции связавшихся белков. (b) Циклин Е-ассоциированный р27 подвергают количественному анализу с помощью денситометрии вышеуказанных блотов (а). Клетки РС3 демонстрируют шестикратное увеличение содержания циклин Е-связанного р27.
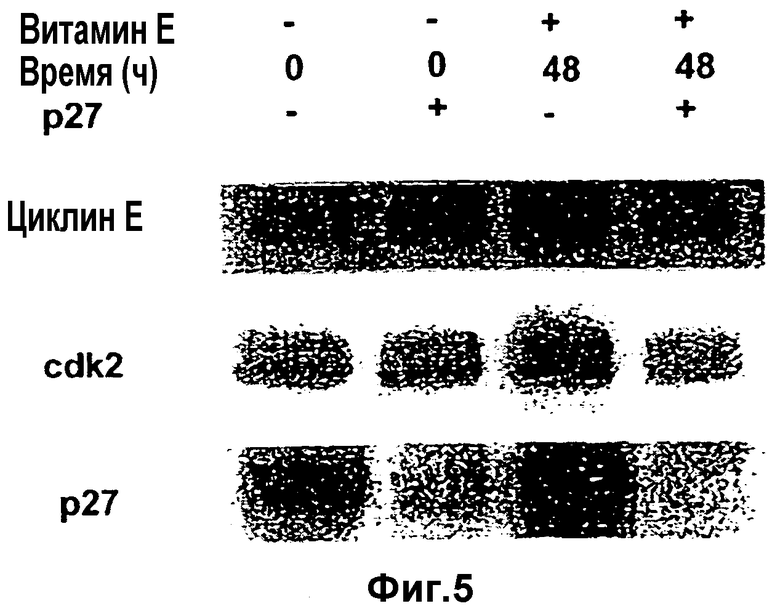
Фиг.5
Витамин Е вызывает увеличение уровня р27, который насыщает мишень циклин Е/cdk2: в клеточных лизатах LNCaP, собранных через 48 часов, в которых после добавления витамина Е наблюдается максимальное ингибирование, последовательно иммунологически истощают содержание р27. Циклин Е-ассоциированный белок анализируют до и после иммунного истощения р27 в 0-час. и 48-час. образцах.
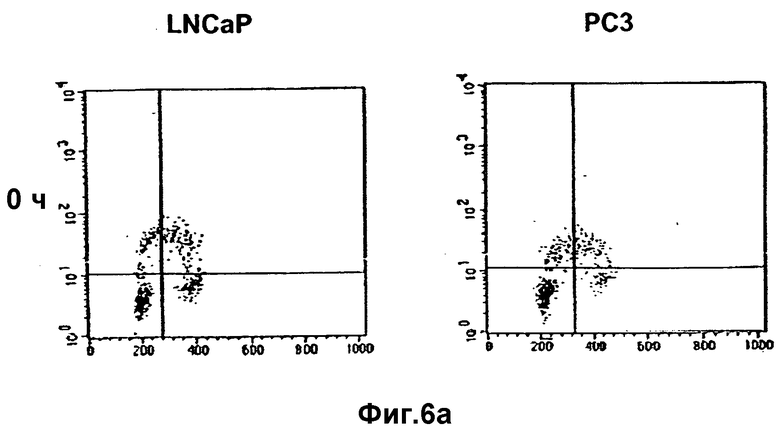
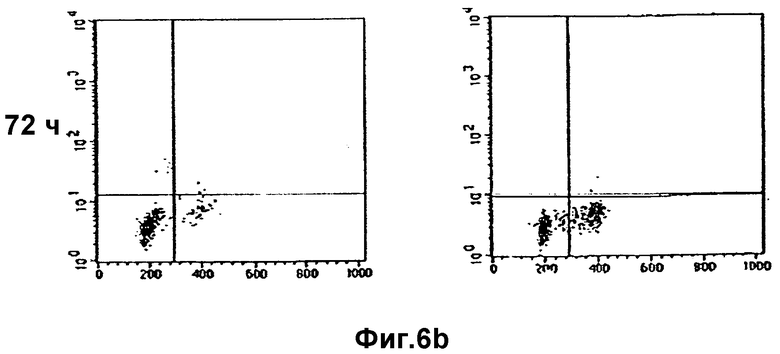
Фиг.6
(а) На дот-графике показано поглощение BrdU и PI в асинхронно растущих клетках LNCaP и PC3. (b) Сниженное поглощение BrdU свидетельствует о прекращении синтеза ДНК после 72 часов обработки с помощью 20 мкг/мл витамина Е.
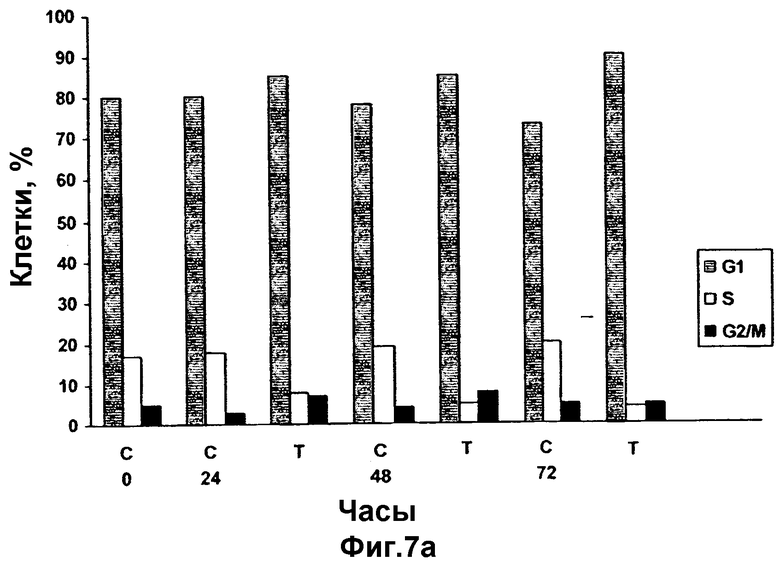
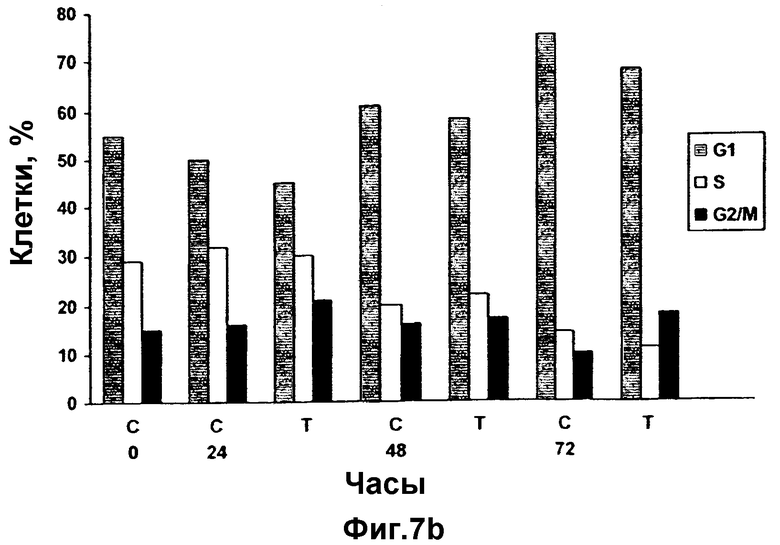
Фиг.7а и 7b
FACS-анализ клеток LNCaP (а) и PC3 (b), обработанных 30 мкг селена: после добавления к культуральной среде селена клетки собирают с разными временными интервалами и готовят их для FACS-анализа. Показано прекращение фазы G1 в клетках LNCaP.
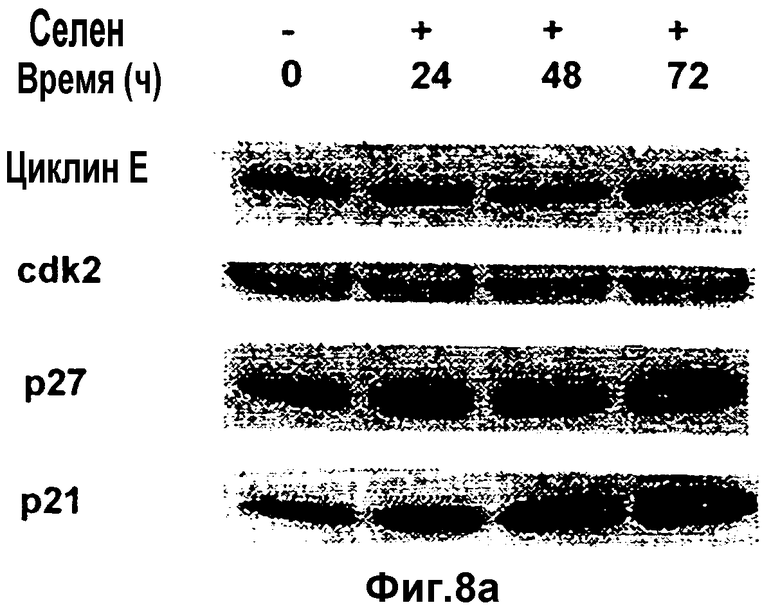
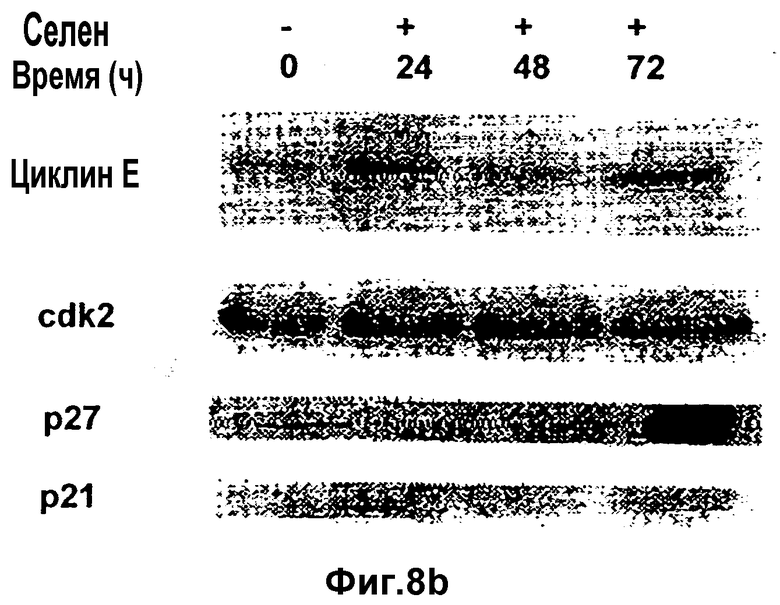
Фиг.8а и 8b
Регуляторы клеточного цикла во время прекращения с помощью селена: после добавления к культуральной среде селена клетки собирают с различными временными интервалами. Получают лизаты (а) LNCaP и (b) PC3 и подвергают их фракционированию в SDS-PAGE. Белки детектируют путем иммуноблоттинга с помощью индикаторных антител.
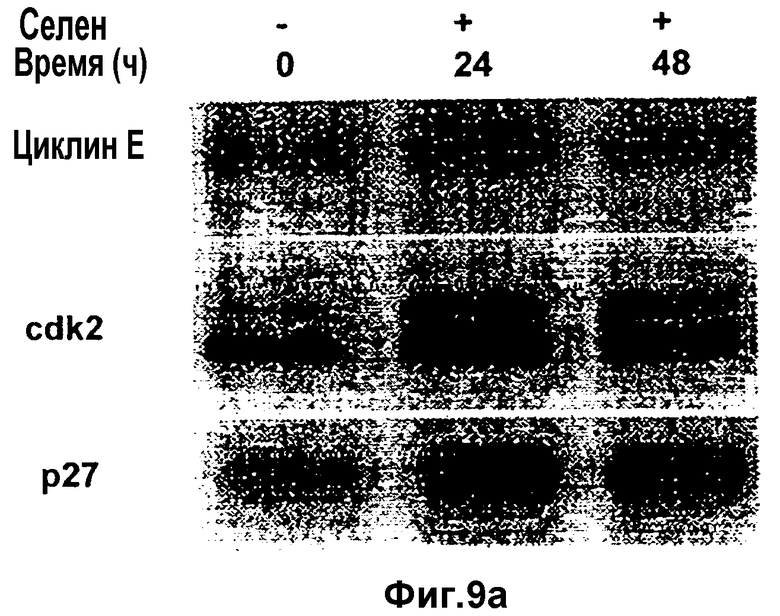
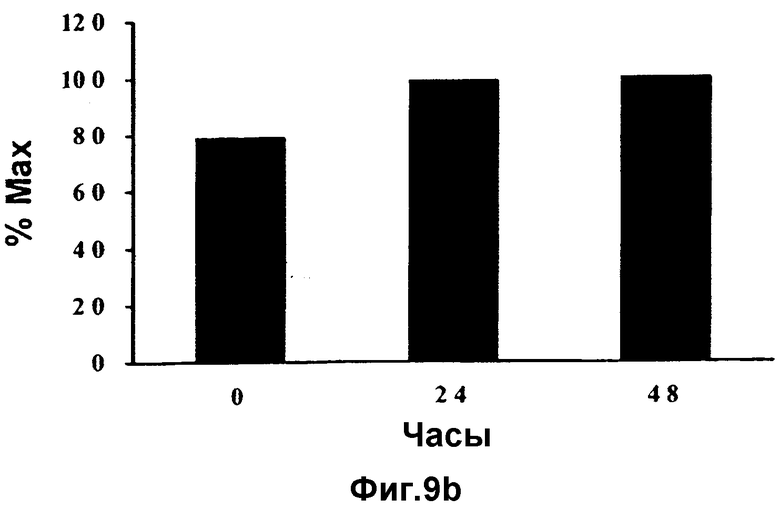
Фиг.9а и 9b
(а) Циклин Е-иммунные комплексы (LNCaP): после добавления к культуральной среде селена клетки извлекают с различными временными интервалами. Иммунопреципитируют циклин Е, комплексы подвергают фракционированию с помощью SDS-PAGE, и иммуноблоты взаимодействуют с антителами для детекции связавшихся белков.
(b) Циклин Е-ассоциированный р27 подвергают количественному анализу с помощью денситометрии в указанных выше (а) блотах. Клетки LNCaP демонстрируют увеличение содержания циклин Е-связанного р27.
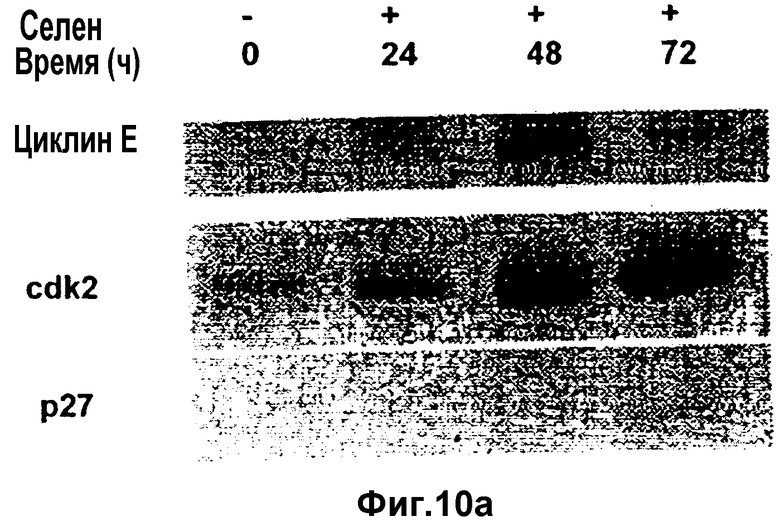
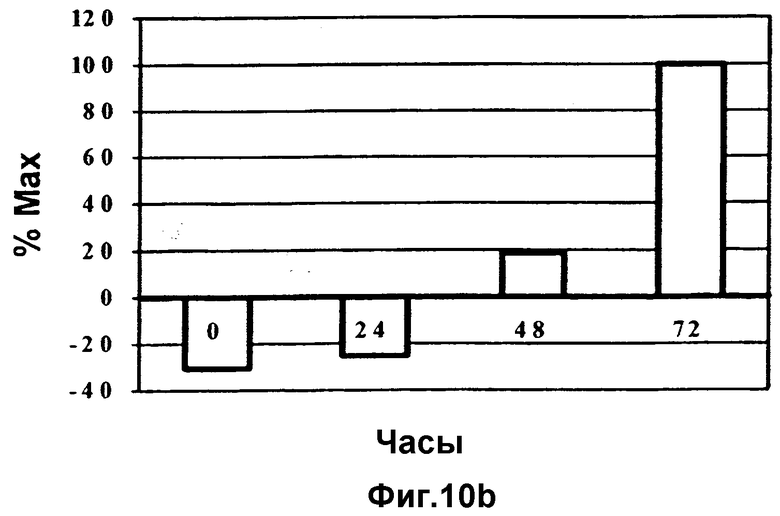
Фиг.10а и 10b
(а) Циклин Е-иммунные комплексы (РС3): Из культуральной среды после добавления селена клетки извлекают с разными интервалами времени. Иммунопреципитируют циклин Е, комплексы подвергают фракционированию с помощью SDS-PAGE, и иммуноблоты взаимодействуют с антителами для детекции ассоциированных белков.
(b) Циклин Е-ассоциированный р27 подвергают количественному анализу с помощью денситометрии в указанных выше (а) блотах. Клетки РС3 не обнаруживают присутствия циклин Е-связанного р27 на детектируемом уровне в течение 72 часов после обработки.
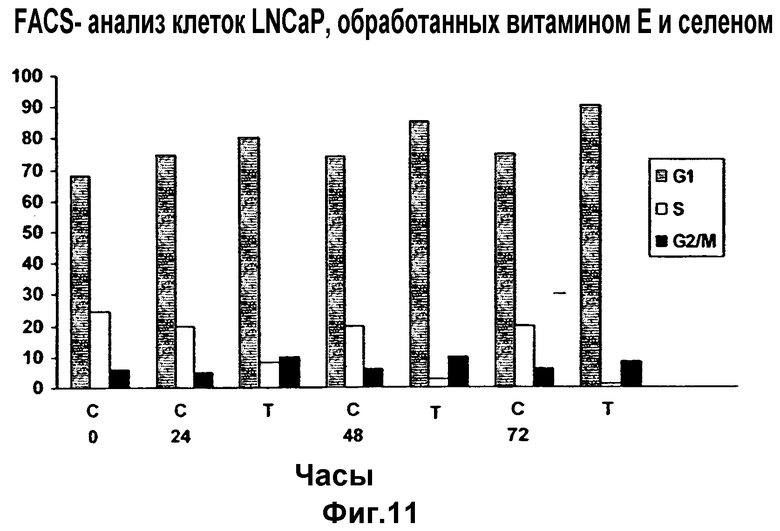
Фиг.11
FACS-анализ клеток LNCaP, обработанных с помощью 20 мкг/мл витамина Е и 30 мкг/мл селена. После добавления к культуральной среде питательных микроэлементов клетки извлекают с разными временными интервалами и готовят их для FACS-анализа. Через 72 часа отмечаются синергические эффекты с фактическим прекращением остановленного клеточного цикла.
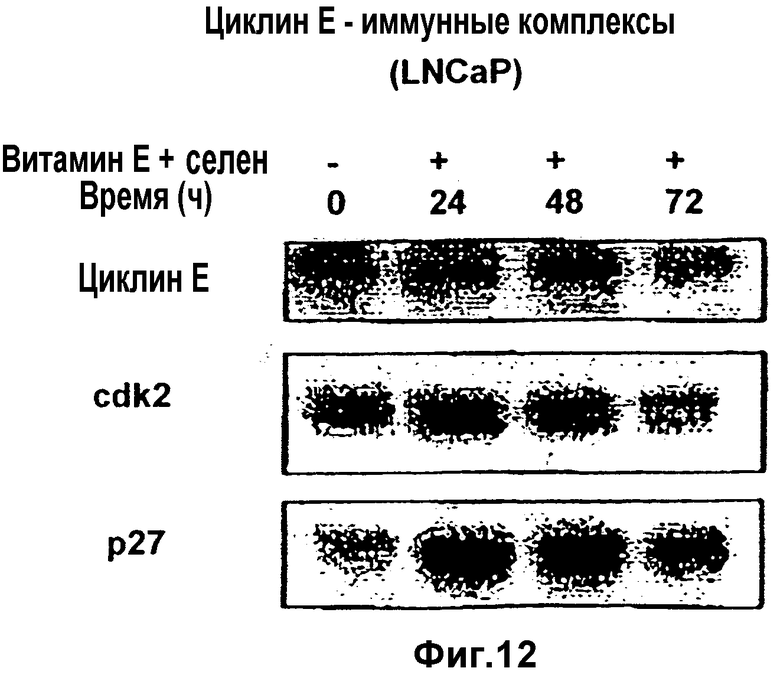
Фиг.12
Регуляторы клеточного цикла во время его прекращения в клетках LNCaP с помощью сочетания витамина Е и селена. После экспонирования из культуральной среды клетки собирают с разными временными интервалами. Получают лизаты и подвергают их фракционированию в SDS-PAGE. Белки детектируют путем иммуноблоттинга с помощью индикаторных антител. Отмечена повышающая регуляция р27.
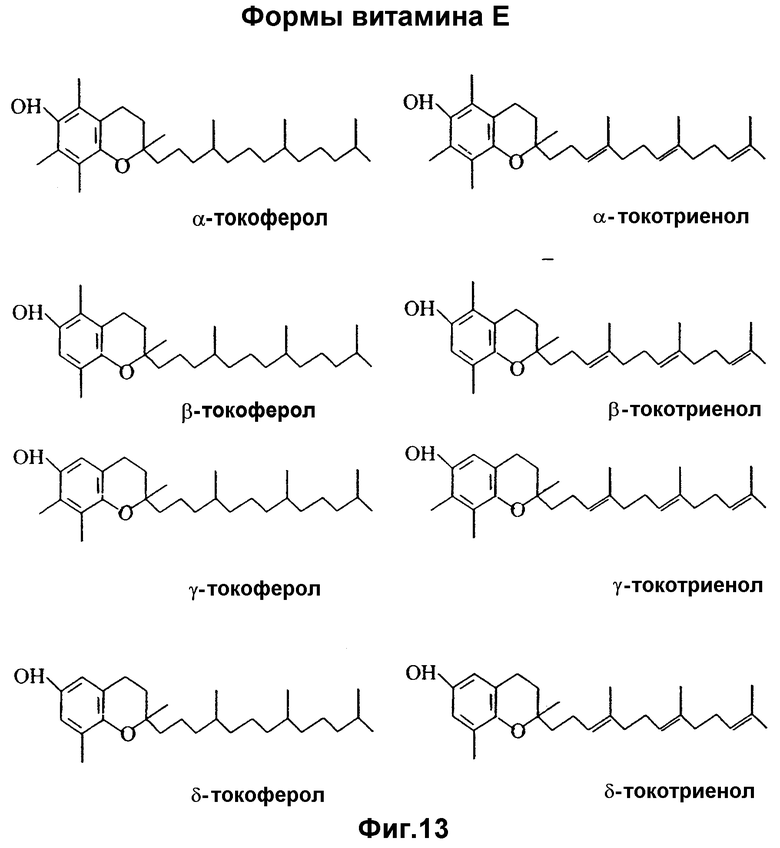
На Фиг.13 представлены химические формулы, иллюстрирующие производные витамина Е.
Подробное описание изобретения
Способ настоящего изобретения заключается в доставке композиции, включающей витамин Е, или производные, или аналоги витамина Е и селен, или соль селена, или производного селена, в связанной или в несвязанной форме, с низким уровнем токсичности, тем млекопитающим, у которых диагностируют рак предстательной железы, или тем млекопитающим, которые нуждаются в профилактике такого рака. В качестве альтернативы, способ настоящего изобретения заключается в доставке композиции, представленной смесью агентов, которые подавляют образование циклин-CDK-белковых комплексов посредством повышенной регуляции р21 и р27, для профилактики и лечения рака предстательной железы у млекопитающих.
Лабораторные исследования и механизм противоракового действия витамина Е и селена
Исследования были осуществлены для выяснения вопроса, действительно ли антиоксиданты, подобные витамину Е и биодоступному селену, могут опосредовать свое действие, индуцируя прекращение клеточного цикла в фазе G1/S в клеточных линиях рака предстательной железы у человека путем модуляции ингибиторов CDK.
Методы исследования
Две стабильные клеточные линии рака предстательной железы человека, LNCaP (андрогензависимая) и РС3 (андрогеннезависимая), получают из Американской коллекции типовых культур (Rockville, MD). Клетки LNCaP культивируют в среде RPMI 1640 (Gibco BRL, Grand Island, NY), с добавлением 10% сыворотки плода коровы (FBS) и 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина, при 37°С в увлажненной атмосфере, содержащей 5% СО2. Клетки РС3 культивируют в среде DMEM/F12 с 10% FBS и с антибиотиками. Оба набора клеточных культур выращивают в 10 см чашках для культивирования тканей до 80%-го слияния и разделяют 1:8.
Один набор клеточных культур LNCaP и РС3 обрабатывают витамином Е [сукцинат α-токоферола, перерастворенный в 95% этаноле] и вносят в культуры в концентрации 20 мкг/мл. Другой набор клеточных культур LNCaP и РС3 обрабатывают селеном [L-селенометионин, перерастворенный в 0,005N HCl] и вносят в культуры в концентрации 30 мкг/мл. В контроле содержится только носитель. Обработку начинают через 48 часов после прикрепления клеток. Экспериментальные клетки выдерживают в чашках в течение до 72 часов перед их извлечением для проточной цитометрии и белкового анализа.
Асинхронно растущие клетки, обработанные или необработанные витамином Е или селеном, в течение 2 часов метят радиоактивной меткой с помощью 10 мМ бромдезоксиуридина (BrdU). Затем клетки собирают, фиксируют 70% этанолом, обрабатывают 0,1% HCl и нагревают в течение 10 мин при 90°С с получением меченой ДНК. Клетки окрашивают анти-BrdU конъюгированным FITC (Becton-Dickinson) и обратно окрашивают радиоактивным пропидиййодидом. Анализ клеточного цикла осуществляют в Becton-Dickinson FACScan с использованием программы Lysis II.
Затем клетки лизируют в ледяном NP-40-лизирующем буфере (0,1% NP-40, 50 нм Трис с рН 7,5, 150 мМ NaCl, 1 мМ фенилметилсульфонилфторида, и по 0,02 мг/мл апротинина, лейпепсина или пепстатина). Лизаты обрабатывают ультразвуком и осветляют центрифугированием. Белки определяют количественно по Bradford и 20-100 мкг белка на дорожку подвергают SDS-полиакриламидному гелевому электрофорезу (SDS-PAGE). Осуществляют перенос и блоттинг, и белки детектируют с помощью электрохемилюминесценции (ECL). Денситометрию осуществляют с использованием системы формирования молекулярного изображения и программы квантования изображения, чтобы количественно определить относительные количества p27 белков, детектированных в Вестерн-блотах. Для детектирования белков, ассоциированных с циклином Е, с помощью иммунопреципитации-Вестерн-анализа (IP-Western), циклин Е иммунопреципитируют из 200 мкг белковых лизатов, комплексы электрофоретически разделяют, блоттируют и блоты взаимодействуют с антителами к циклину Е, CDK2, p21 и р27. Чтобы иммунологически истощить р27, его последовательно иммунопреципитируют (трижды) из 200 мкг белковых лизатов, после чего из лизатов, истощенных по р27, иммунопреципитируют циклин Е. С использованием IP-Вестерн-блоттинга сравнивают количества иммунопреципитируемого циклин Е-белка, ассоциированного CDK2 и белка р27, до и после иммунологического истощения р27.
Антитела, используемые в экспериментах по иммуноблоттингу, представляют собой мышиные моноклональные антитела к β-актину от Sigma Laboratories; мышиные моноклональные антитела Е172 к циклину Е для иммунопреципитации и моноклональные антитела Е12 для иммуноблоттинга от E Harlow (Mass General, MA); мышиные моноклональные антитела PSTAIRE к CDK2 от S. Reed (The Scripps Research Institute, CA); мышиные моноклональные антитела к р27 от Transduction Laboratories (Lexington, KY); и кроличьи поликлональные антитела к р21 из Santa Cruz Biotechnology, Cedarlane, CA, α Brdu-FITC-конъюгат.
Витамин Е вызывает прекращение фазы G1 у клеток LNCaP и фазы G2/M у клеток РС3
Результатами данного эксперимента являются прекращение клеточного цикла в трех из четырех клеточных культуральных средах. Обработка асинхронно растущих клеток LNCaP и РС3 витамином Е в течение до 72 часов вызывает прекращение фазы G1 у LNCaP и прекращение фазы G2/M у РС3 уже через 24 часа после обработки, что показано по содержанию ДНК на гистограммах в проточноцитометрических исследованиях. При обработке РС3-клеток витамином Е в промежутке между 24 и 72 часами наблюдаемое существенное увеличение клеточной популяции в фазе G2/M связано со снижением численности клеток РС3 в фазе S. Спустя 24 часа уменьшение численности клеток фазы S, выраженное в процентах, составляет 49,5% (Фиг.1а) и 37,3% (Фиг.1b) соответственно для LNCaP и РС3. Задержка клеточного цикла устойчиво сохраняется в течение 72 часов в среде с добавленным витамином Е, понижающим численность клеток в фазе S максимум на 69,6% и 95,0% соответственно для LNCaP и РС3 (Таблица 1).
Судя по морфологическому виду клеток, цитотоксичность отсутствует. В контроле, где клетки обрабатывают только носителем, прекращение роста не наблюдается.
Изменение р21 и р27 во время индуцированного витамином Е прекращения клеточного цикла
Известно, что р21, циклинзависимый ингибитор киназы, участвует в прекращении фазы G2/M. Данные проточной цитометрии (Фиг.1b) свидетельствуют, что хотя витамин Е прекращает клеточный цикл обоих линий клеток, он действует также на фазу G2/M РС3. Поэтому, чтобы выяснить, вовлечен ли р21 также в индуцированный витамином Е процесс ингибирования роста раковых клеток предстательной железы, в клетках LNCaP и в клетках РС3 после воздействия на них витамина Е анализируют содержание р21. Существенного изменения уровня р21 в клетках LNCaP не отмечено (Фиг.2а), однако уровень р21 оказывается существенно повышенным в клетках РС3 (Фиг.2b). Данное повышение уровня р21 видно уже через 24 часа обработки.
Ингибирование активности циклин Е/CDK2 наблюдается в пределах 24 часов после обработки витамином Е. Чтобы выяснить, является ли достаточным увеличение р27 для мишени циклин Е/CDK2 и индуцирует ли оно прекращение клеточного цикла, р27 иммунологически истощают тремя последовательными иммунопреципитациями в контрольном и обработанном витамином Е лизатах клеток LNCaP. Циклин Е-иммунокомплексы анализируют до и после иммунологического истощения р27. Иммунологическое истощение р27 является причиной снижения количества циклина Е и белка CDK2 (Фиг.5). Это свидетельствует о существенной доле клеток, находящихся в фазе G1 клеточного цикла.
Клеточные линии LNCaP и РС3 в ответ на действие витамина Е демонстрируют характерную колоколообразную форму кривой роста (Фиг.6а и 6b). Настоящее исследование предполагает, что в ответ на воздействие витамина Е повышенный уровень р27 и его связывание и ингибирование циклин Е/CDK2 способствует прекращению фазы G1 клеток LNCaP. Для того чтобы разобраться в механизме ингибирования циклин Е/CDK2, эти комплексы исследуют путем иммунопреципитации циклина Е с последующим Вестерн-блоттингом для детектирования ассоциированных белков (Фиг.3а и 4а). В клеточных культурах, обработанных витамином Е, количество циклин Е-ассоциированного р27 в клетках LNCaP увеличено в 3-4 раза в соответствии с данными по денситометрии (Фиг.3b), поскольку в клетках происходит прекращение G1. Аналогичное увеличение обнаруживается и для клеток РС3, а детектируемые уровни р27 видны через 48 часов после обработки (Фиг.4b). Представленные данные дают основание полагать, что такое увеличение содержания р27 свидетельствует о насыщении циклин Е/CDK2.
Селен вызывает прекращение G1 у клеток LNCaP и не оказывает влияния на клетки РС3
Обработка асинхронно растущих клеток LNCaP и РС3 с помощью 30 мкг/мл селена в течение 72 часов индуцирует прекращение клеточного цикла у LNCaP уже через 24 часа после начала обработки, что следует из гистограмм содержания ДНК, полученных в проточно цитометрических исследованиях (Фиг.7а). Выраженное в процентах снижение численности клеток в фазе S составляет 58.1% за 24 часа обработки. Прекращение клеточного цикла сохраняется в течение 72 часов в среде с добавленным селеном, понижающим численность клеток в фазе S максимумом на 80,3% (Таблица 2). Цитотоксическое действие селена на эти клетки морфологически не обнаруживается. В контроле у клеток, обработанных только носителем, прекращение роста не наблюдается. Напротив, обработанные РС3-клетки демонстрирует несущественное изменение в числе клеток в фазе S, даже через 72 часа обработки, что тем самым свидетельствует об отсутствии прекращения роста (8.4%) (Фиг.7b) (Таблица 2).
Изменение уровней р21 и р27 при индуцированном селеном прекращении клеточного цикла
Известно, что циклинзависимый ингибитор киназы р21 участвует в прекращении фазы G2/M. Поскольку в фазе G2/M происходит удвоение числа клеток, в настоящем исследовании выясняют также вопрос об участии р21 в индуцированное селеном ингибирование роста злокачественных клеток предстательной железы. Уровни р21 анализируют в клетках LNCaP и РС3 после воздействия на них селеном. Уровни р21 были существенно повышенными в клетках LNCaP (Фиг.8а). Данное повышение уровней р21 наблюдается уже через 24 часа обработки селеном. Уровни р21 в обработанных селеном клетках РС3 не изменяются (Фиг.8b).
Ингибирование активности циклин Е/CDK2 в клетках LNCaP и РС3 наблюдают в пределах 24 часов после обработки селеном. Чтобы охарактеризовать механизм ингибирования циклин Е/cdk2, данные комплексы анализируют путем иммунопреципитации циклина Е с последующим Вестерн-блоттингом для детектирования ассоциированных белков (Фиг.9 и 10). При наступлении прекращения фазы G1 в клетках LNCaP происходит 25% увеличение количества циклина Е, ассоциированного р27, что измерено с помощью денситометрии (Фиг.9b). В противоположность этому, поведение клеток РС3, обработанных селеном, весьма отличается от клеток LNCaP в том, что содержание циклина увеличивается через 72 часа.
Результаты для клеточных культур, обработанных селеном, иные, чем обработанных витамином Е. В этих культурах обнаруживается 25% увеличение количества циклина Е, ассоциированного р27, для LNCaP, что измерено с помощью денситометрии, клетки которой подвергаются прекращению фазы G1. В противоположность этому, в культуре клеток РС3 содержание циклина Е увеличилось через 72 часа. В культуре клеток РС3 не наблюдаются детектируемые уровни р27 до конца периода обработки; две отдельные дорожки CDK2 в SDS-PAGE видны лишь через 72 часа. Поэтому постулируется, что увеличение содержания р21 и р27, а также их связывание и ингибирование циклина Е/CDK2 играет роль в ингибировании клеточной пролиферации по мере того, как регенерирующая ткань предстательной железы подвергается дифференциации.
Таким образом, исследование дает основание полагать, что увеличенные уровни р27 участвуют в прекращении фазы G1 раковых клеток LNCaP предстательной железы человека в ответ на действие витамина Е и что увеличенные уровни р21 участвуют в прекращении фазы G2/M раковых клеток РС3 предстательной железы человека в ответ на воздействие витамина Е. Антипролиферативный эффект селена в двух клеточных линиях различен: в андрогеннезависимых клетках РС3 ингибирование роста не происходит в сравнении с отчетливым снижением роста в фазе S андрогензависимых клеток LNCaP, обусловленное увеличением содержания р21. Это можно приписать тому факту, что селен может опосредовать свое действие с помощью рецептора андрогена, а не в результате ускорения клеточной пролиферации. Хотя мало известно о том, связывается ли рецептор андрогена непосредственно с компонентами аппарата клеточного цикла, и каким образом такое взаимодействие может модулировать трансактивационную активность рецептора при раке предстательной железы, эстрогены и андрогены регулируют активность CDK, модулируя экспрессию циклинов или CDK-ингибиторов, способствуя тем самым прохождению через G1-S-фазу клеточного цикла.
Доказательство усиливающего действия с использованием витамина Е и селена
На Фиг.11 и 12 показано синергическое действие на клеточный цикл при использовании витамина Е и селена в комбинации. Если клетки LNCaP обрабатывают комбинацией витамина Е и селена, прекращение клеточного цикла оказывается более существенным, чем с каким-либо одним агентом. Через 48 и 72 часа фаза S угнетается соответственно на 4% и 1% при одновременном увеличении G1- и G2/M-компонентов. Это является причиной 63,1, 84,2 и 94,7%-го угнетения S-фазы соответственно через 24, 48 и 72 часа по сравнению с контролем (Таблица 3). Эти данные дают основание полагать, что противоопухолевые свойства данных агентов достаточно настолько разные, что синергическое действие реализуется в том случае, если они оба представлены в клетке.
Витамин Е представляет собой жирорастворимый витамин, обнаруживаемый в зародышах хлебных злаков и в листьях зелени (овощи), помимо присущих ему указанных здесь противоопухолевых свойств предотвращает также окисление ненасыщенных жирных кислот в таких местах, как клеточные мембраны, помогая тем самым сохранять их структуру. Он может усваиваться либо в виде α-токоферола, либо в виде эфира α-токоферола, например в виде сукцината токоферола. Селен является микроэлементом, который может усваиваться в таких формах, как селенит натрия или селенометионин.
Композицию можно принимать перорально либо в виде капсулы, пищевой добавки, либо в виде муки, богатой обоими компонентами. В качестве альтернативы, данные противоопухолевые агенты можно вводить в кровоток с помощью шприца для подкожных инъекций.
Компоненты композиции можно вводить совместно или раздельно. Введение композиции может быть парентеральным, пероральным, внутривенным, ректальным, интраплевральным, интратекальным, внутрибрюшинным, аэрозольным или чрескожным, достаточным для достижения требуемого профилактического или терапевтического эффекта. При пероральном введении данная композиция может быть представлена в виде таблеток (однократной или многократной, покрытой или непокрытой), капсул, или драже. Эти пероральные составы можно смешать с твердым наполнителем, таким как лактоза, сахароза, крахмал, микрокристаллическая целлюлоза, стеарат магния или тальк. При назначении парентерального введения можно использовать водный раствор или масляную композицию данного агента. Водные растворы можно получать в воде, физиологическом растворе, растворе Рингера, с буферами или без них. Масляные составы можно готовить, например, на природных маслах (например, на арахисовом масле или оливковом масле), или на бензилбензоате.
Введение фактического дозированного количества можно определить с помощью физических и физиологических факторов, таких как активность конкретного используемого соединения; возраста, массы тела, общего состояния здоровья, диеты, времени введения, пути введения, скорости выделения, возможного сочетания лекарственного средства, а также идиопатии и тяжести состояния пациента или субъекта. Клинически безопасные и эффективные дозы соединений настоящего изобретения определяют с помощью клинических испытаний, как того требуют распорядительные органы в данной области.
Кроме того, для использования в качестве противоопухолевых агентов доступны и другие химические соединения, безопасные для потребления человеком, которые повышают внутриклеточное содержание р21 и р27 и тем самым увеличивают ингибирование циклин-CDK-комплексов.
Витамин Е не является однородным веществом. Под этим наименованием описывают семейство близкородственных соединений, названных токоферолами и токотриенолами, см. Brigelius-Flohe R, Traber MG, "Vitamin E: Function and Metabolism", FASEB (1999) 13:1145-1155. Существует 4 токоферола и 4 токотриенола: соответственно альфа, бета, гамма и дельта (Фиг.13). Альфа-токоферол является наиболее распространенной природной формой витамина Е, представляя приблизительно 90% токоферолов в большинстве тканей млекопитающих. Он обладает наивысшей биологической активностью и устраняет дефицит витамина Е у людей, см. Traber MG, Arai H, "Molecular Mechanisms of Vitamin E Transport", Annu Rev Nutr (1999) 19:343-55.
У семейства токоферолов существует три хиральных центра, которые определяют их стереоспецифичность. Природные формы (преимущественно растительного происхождения) α-токоферола представляют собой исключительно правовращающий (RRR) изомер. Однако витамин Е в виде добавок может содержать либо RRR (d-α-токоферол), либо синтетический витамин Е. Синтетические формы витамина Е, известные также в качестве all rac α-токоферола (или dl-α-токоферола), содержат все 8 возможных стереоизомеров. См. Brigelius-Flohe R, Traber MG, "Vitamin E: Function and Metabolism", FASEB (1999) 13:1145-1155. Биологические активности этих соединений не идентичны. Как правило, при использовании синтетического dl-α-токоферола в качестве стандарта d- α-токоферол (природная форма) составляет 1,49 его биоактивности. См. Pryor WA, "Vitamin E and Heart Disease: Basic Science to Clinical Intervation Trials", Free Radic Biol Med (2000 Jan 1) 28(1):141-64.
Коммерчески доступный витамин Е получают либо в этерифицированной, либо в неэтерифицированной форме. Все этерифицированные формы природного витамина Е обладают сходной биологической активностью. Преобразование миллиграммов в международные единицы зависит от состава витамина Е. Вообще, 1 МЕ равна активности 1 мг dl-α-токоферолацетата (т.е., синтетической формы). Существует целый ряд соображений, поясняющих изменчивость биологической активности разных форм витамина Е, включая: 1) раличные биологические активности самих изомеров; см. Brigelius-Flohe R, Traber MG, "Vitamin E: Function and Metabolism", FASEB (1999) 13:1145-1155; 2) разные скорости и способы транспортировки; 3) существование для RRR-α-токоферола специфичных механизмов транспортировки, см. Traber MG, Arai H, "Molecular Mechanisms of Vitamin E Transport", Annu Rev Nutr (1999) 19:343-55 и 4) специфика взаимодействия разных изомеров с рецепторами; см. Traber MG, Arai H., "Molecular Mechanisms of Vitamin E Transport", Annu Rev Nutr (1999) 19"343-55.
Витамин Е принимают внутрь перорально с пищей либо в виде пищевых добавок. Хорошие пищевые источники витамина Е, представленные продуктами, богатыми растительными маслами, включают авокадо, орехи, яйца, ореховую пасту, соевые бобы и готовый к употреблению завтрак из цельных зерен хлебных злаков. Готовые растительные масла рассматривают в качестве наилучших пищевых источников витамина Е в рационе, см. Rao AV, Fleshner N, Agarwal S. Nutr Cancer (1999) 33(2):159-64.
Рекомендуемая ежедневная норма потребления витамина Е составляет 10 мг/день. Данное количество обычно присутствует в пищевых источниках у тех индивидуумов, которые придерживаются здорового рациона. Однако только рацион не может обеспечить необходимым количеством витамина Е для профилактики хронических заболеваний. Это особенно справедливо для рациона с низким содержанием жиров. Принятие пищи, богатой витамином Е, несет и проблемы, потому что витамин Е является жирорастворимым и, следовательно, находится в жирах. Теоретически, повышенное потребление витамина Е лучше всего осуществлять путем добавления.
При усвоении витамин Е всасывается через лимфатические сосуды кишечника вместе со среднецепочечными жирными кислотами. Затем он упаковывается в хиломикроны и транспортируется в печень. После прохождения через печень α-токоферол в основном секретируется в плазму. Ответственным за этот путь является белок, переносящий α-токоферол, (α-ТТР), специфичный белок печени. См. Azzi A, Breyer I, Feher M, Pastori M, Ricciarelli R, Spycher S, Staffieri M, Stocker A, Zimmer S, Zingg JM, "Specific Cellular Responses to Alpha-Tocopherol", J Nutr (2000 Jul) 130(7):1649-52. Формы β-, δ-, и γ-токоферола в основном секретируются в желчь, а экскретируются с калом. Уровни насыщения витамина Е в плазме соответствуют 80 мкМ; уровни, превышающие 80 мкМ, недосягаемы даже при очень больших дозах витамина Е. Для достижения уровня насыщения в крови требуется 800 МЕ в день. См. Brigelius-Flohe R, Traber MG, "Vitamin E: Function and Metabolism", FASEB (1999) 13:1145-1155.
Если не оговорено особо, все технические и научные используемые здесь термины обладают тем же значением, которое понятно рядовому специалисту в данной области техники, к которой относится настоящее изобретение. Несмотря на то, что для осуществления настоящего изобретения на практике можно использовать любые способы и материалы, аналогичные или эквивалентные описанным, к настоящему времени описаны предпочтительные способы и материалы. Все публикации и патентные документы, на которые ссылаются в настоящей заявке, включены здесь в виде ссылок в полном объеме, как если бы каждая из них, а также каждая публикация и патентный документ были, в частности, включены здесь в виде ссылки в полном объеме.
Настоящее изобретение не ограничивается объемом какого-либо раскрытого варианта осуществления настоящего изобретения, который подразумевается в качестве иллюстрации одного из аспектов настоящего изобретения, или каким-либо способом, который функционально эквивалентен объему настоящего изобретения. В действительности, разные модификации настоящего изобретения, помимо представленных и описанных здесь, должны быть очевидны специалистам в данной области из вышеприведенного описания. Подразумевается, что такие модификации находятся в рамках объема нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ бесконтактной стимуляции транскрипционной активности гена ингибитора циклинзависимой киназы 2 в опухолевых клетках предстательной железы | 2020 |
|
RU2763992C1 |
| СПОСОБ ЛЕЧЕНИЯ ПРОСТАТИЧЕСКОЙ ИНТРАЭПИТЕЛИАЛЬНОЙ НЕОПЛАЗИИ (ПИН) | 2014 |
|
RU2564438C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,4-ДИАМИНОТИАЗОЛ-5-ОНА | 2005 |
|
RU2395501C2 |
| КОМПОЗИЦИИ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ КОЖНЫХ ПРИЗНАКОВ СТАРЕНИЯ | 2005 |
|
RU2409290C2 |
| КОМБИНАЦИЯ ИНГИБИТОРОВ ЧЕКПОЙНТ-КИНАЗЫ 1 И ИНГИБИТОРОВ КИНАЗЫ WEE 1 | 2011 |
|
RU2627841C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,6-ДИАМИНОПИРИДИН-3-ОНА | 2005 |
|
RU2385866C2 |
| СИНЕРГИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2438664C2 |
| 6,9-ДИЗАМЕЩЕННЫЕ 2-[ТРАНС-(-4-АМИНОЦИКЛОГЕКСИЛ)АМИНО]ПУРИНЫ | 1999 |
|
RU2191777C2 |
| ЛЕЧЕНИЕ ОПУХОЛЕЙ КОМБИНАЦИЕЙ ОНКОЛИТИЧЕСКОГО АДЕНОВИРУСА И ИНГИБИТОРА CDK4/6 | 2019 |
|
RU2811278C2 |
| СПОСОБЫ ЛЕЧЕНИЯ КОЛОРЕКТАЛЬНОГО РАКА | 2014 |
|
RU2674147C2 |
В настоящем изобретении представлены комбинация и способ профилактики и лечения рака предстательной железы млекопитающих с использованием витамина Е, или производных витамина Е, или аналогов витамина Е и селена, или соли селена, или производного селена, в связанной или в свободной форме, отдельно или в сочетании с традиционной терапией. В настоящем изобретении представлены также композиция и способ профилактики или лечения рака предстательной железы млекопитающих с использованием витамина Е, или производных витамина Е, или аналогов витамина Е и селена, или соли селена, или производных селена, в связанной или в свободной форме, отдельно или в сочетании с традиционной терапией, посредством повышения внутриклеточного содержания р21 и/или р27. Комбинация витамина Е, или производных витамина Е, или аналогов витамина Е и селена, или соли селена, или производного селена, в связанной или в свободной форме обладает синергетическим действием и повышает уровень Т-клеток, ингибирует образование белковых комплексов циклин-CDK. 4 н. и 27 з.п. ф-лы, 3 табл., 22 ил.
| US 6197309 В1, 06.03.2001 | |||
| Rose A.T | |||
| et al | |||
| Alpha-tocopherol succinate inhibits growth of gastric cancer cells in vitro | |||
| J Surg Res | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Hammerer P | |||
| et al | |||
| Chemoprevention of prostatic carcinoma | |||
| Urologe A | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ ПИЩЕВОЙ КОМПЛЕКС "ЖЕНЬШЕНЬВИТАМ" | 1998 |
|
RU2138170C1 |
| ФАРМАЦИЯ | |||
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
2009-02-20—Публикация
2002-04-05—Подача