Изобретение относится к области прикладной биохимии, в частности к сорбционным материалам, предназначенным для сорбции и разделения белковых молекул, но может применяться и для сорбции других веществ.
Известен алмазный сорбент, используемый в хроматографических колонках высокого давления для разделения р- и о-ксилола, и способ его получения, заключающийся в прессовании наноалмазного порошка, спекании при высоких давлениях в области стабильности алмаза, дроблении компактов и классификации микропорошков [Patel B.A., Rutt K.J., Padaiko V.I., Mikhalovsky S.V. Use of industrial diamonds in HPLC // Сверхтвердые материалы, 2002, №6 (140), с.51-54].
Недостатком данного сорбента является невозможность его использования в хроматографии белков, являющихся высокомолекулярными соединениями, т.к. при диаметре частиц 3,8±0,1 мкм радиус пор составляет 25 нм.
Известен сорбент и способ его получения на основе целлюлозного носителя, обработанного перманганатом калия с образованием слоя диоксида марганца на носителе с дальнейшей обработкой раствором ферроцианида калия в присутствии уксусной кислоты [п. РФ №2172208, МПК B01J 20/02, опубл. 2001.08.20].
Недостаток этого сорбента заключается в том, что он не разделяет высокомолекулярные соединения.
Известен сорбент, предназначенный для хроматографии белков, и способ его получения при использовании готового торгового продукта сефарозы (Sepharose. RTM. CL-6B, производитель Pharmacia). Способ получения заключается в отмывании сефарозы, ее активации и ряда последовательных химических реакций, приводящих к присоединению Ni2+, в концентрации примерно 7,1 микромоль/мл геля [пат. США №72452, 1989].
Недостаток данного сорбента заключается в том, что он предназначен для сорбции белков, имеющих «якорные» гистидиновые участки, а способ его получения является многостадийным и длительным.
Известен сорбент для хроматографии, полученный путем полимеризации на поверхности ультрадисперсного алмаза с размером частиц 0,1 - 50 мк мономеров стирола, этилвинилбензола, винилацетата, метилметакрилата [RU №94005691, C08F 292/00, опубл. 10.11.1995 (прототип)].
Включение ультрадисперсного алмаза обеспечивает высокую прочность гранул сорбента, но не позволяет химически активным поверхностным группам на частицах участвовать в процессах сорбции-десорбции, т.к. они закрыты полимерной матрицей.
Техническим результатом изобретения является создание полифункционального наноалмазного сорбента, способного адсорбировать разные белки, различающиеся физико-химическими свойствами.
Технический результат достигается тем, что в сорбенте для хроматографии, содержащем наночастицы алмаза, иммобилизованные на полимерной матрице, новым является то, что сорбент содержит наночастицы алмаза, полученные детонационным синтезом, которые иммобилизованы на полисахаридной матрице в количестве 8,2-12,0 мг на 1 мл сорбента. Наночастицы алмаза иммобилизованы из устойчивого гидрозоля с дзета-потенциалом от минус 40 до минус 85 мВ при размере наночастиц алмаза и их кластеров 3-250 нм.
Технический результат достигается также и тем, что в способе получения сорбента для хроматографии, включающем иммобилизацию наночастиц алмаза на полимерной матрице, новым является то, что в качестве матрицы используют полисахаридную матрицу, которую подвергают отмывке дистиллированной водой, обрабатывают устойчивым наноалмазным гидрозолем, имеющим концентрацию наноалмазных частиц 0,5-10,0 мас.%, и промывают водой. В качестве полисахаридной матрицы используют сефарозу 2В. Процесс проводят в хроматографической колонке.
В способе получения наноалмазного сорбента полисахаридная матрица не подвергается активации или каким-либо химическим реакциям. Процесс получения наноалмазного сорбента быстр и заключается в создании контакта частиц гидрозоля наноалмаза с матрицей и удалении не связавшихся с матрицей наноалмазов. Процесс получения наноалмазного сорбента можно проводить в объеме жидкостей и в хроматографической колонке.
Сравнение заявляемых технических решений с прототипом позволило установить их соответствие критерию «новизна». При изучении других известных технических решений в данной области техники признаки, отличающие заявляемые изобретения от прототипа, не были выявлены и потому они обеспечивают заявляемым техническим решениям соответствие критерию «изобретательский уровень».
Для получения наноалмазного сорбента необходимы:
- активное адсорбирующее вещество, которое готовят добавлением дистиллированной воды к навеске сухого порошка наноалмазов детонационного синтеза, обладающих при концентрации до 10 мас.% следующими характеристиками - образуют гидрозоли с размером наночастиц и их кластеров в диапазоне 3-250 нм, имеют повышенную коллоидную устойчивость частиц и дзета-потенциал -40÷-85 мВ;
- отмытая от консервантов (дистиллированной водой не менее 3 раз) сефароза 2В (Sepharose® 2В - концентрация агарозы 2%, диаметр набухших гранул 60 - 200 мкм, область фракционирования для глобулярных белков 70 - 40000 тыс. дальтон).
Пример 1
Способ получения сорбента.
Сефароза 2В (Sepharose® 2В - производитель Pharmacia Fine Chemicals) в количестве 20 мл отбирается из транспортной упаковки и переносится в мерный стеклянный стакан объемом 250 мл. Проводится ее отмывка любым из известных способов (декантация, фильтрование, центрифугирование), позволяющих отделить сорбент от консервирующего раствора, представляющего смесь 0,01% Merthiolate® и 0,1% dimethoxane. Для этого в стакан приливается 200 мл дистиллированной воды (пример приводится для способа декантации). Все тщательно перемешивается. После выпадения в осадок частиц сефарозы надосадочная жидкость сливается и добавляется новая порция чистой дистиллированной воды. После 3-5 смен порций воды к осадку сефарозы приливается 5 мл гидрозоля, содержащего 10,0 мас.% наноалмазов. Стакан помещается на магнитную мешалку и перемешивается в течение 5-10 мин. Сефароза отмывается от остатков, неиммобилизованных наноалмазов водой аналогично консервирующему раствору. Качество удаления наночастиц проверяется спектрофотометрическим методом в диапазоне длин волн 200-400 нм. При достижении уровня, не превышающего по отношению к дистиллированной воде 0,002 оптической единицы, сорбент готов для набивки колонки.
Пример 2.
Способ получения сорбента.
Сефароза 2В (Sepharose® 2В - производитель Pharmacia Fine Chemicals) с использованием дистиллированной воды стандартным образом набивается в хроматографическую колонку низкого давления (производитель фирма «Pharmacia»). После заполнения колонки проводится отмывка носителя дистиллированной водой от консервирующего раствора, представляющего смесь 0,01% Merthiolate® и 0,1% dimethoxane. Затем проводится стандартный хроматографический процесс. В качестве образца используется 0,5 мас.% гидрозоль наноалмазов. После заполнения гидрозолем 3/4 объема на вход колонки подается дистиллированная вода. Колонка промывается дистиллированной водой для удаления наночастиц, не иммобилизованных на носителе. Критерием удаления наноалмазов является уровень сигнала хроматографической системы, регистрирующей оптическую плотность раствора, на выходе колонки. После промывки колонка готова для использования.
Пример 3.
Проведение хроматографического процесса маркерного белка цитохрома С.
Колонка диаметром 1,6 см, содержащая 12 мл упакованного наноалмазного сорбента, подключается к хроматографической системе «BIO-RAD BioLogic LP» (USA). Для определения емкости сорбента используется маркерный белок цитохром С (фирма Sigma). Препарат для определения сорбционной емкости содержит 10 мг/мл белка в водном растворе 50 мМ NaCl. Результаты представлены на фиг.1. Препарат белка в количестве, перекрывающем сорбционную емкость сорбента, прокачивается через хроматографическую колонку. Критерием является увеличение поглощения раствора, выходящего из колонки, регистрируемого системой «BIO-RAD BioLogic LP» (USA) при длине волны 280 нм (фиг.1, область а-б). После нанесения маркерного белка на сорбент колонка промывается от неадсорбированного белка буферным раствором, содержащим 20 мМ Трис-HCl (фиг.1, область б-в). Десорбцию белка осуществляют градиентом (0,0-0,5 М) фосфатного буфера рН 7,0 (фиг.1, область в-г). Процесс десорбции контролируется по изменению оптической плотности на выходе колонки (фиг.1 область г-д). Хроматографический процесс проводится при скорости протока 1 мл/мин и продолжается 100 мин.
Пример 4.
Определение содержания активного адсорбирующего вещества (наноалмазов) в наноалмазном сорбенте.
В хроматографическую колонку обычного давления вносят 1 мл полученного наноалмазного адсорбента. Колонку подключают к хроматографической системе «BIO-RAD BioLogic LP» (USA) и промывают водой. Через колонку прокачивают водный раствор маркерного белка цитохрома С с концентрацией 1 мг/мл. Белковый раствор вводят в колонку до момента полного насыщения сорбента белком и начала его выхода из колонки. После этого ввод белкового раствора в колонку прекращают, а колонку промываю дистиллированной водой до момента полного выхода не связанного с сорбентом белка. Контроль выхода белка из колонки осуществляют с помощью системы «BIO-RAD BioLogic LP» (USA) при длине волны 280 нм. Растворы, содержащие несвязавшийся маркерный белок, объединяют, измеряют объем и оценивают концентрацию цитохрома С спектрофотометрическим методом на UV/VIS спектрофотометре UVIKON 943 (Kontron Instruments, Italy) no величине оптической плотности при длине волны 410 нм (характерный спектральный максимум для данного белка). Аналогичным образом оценивают величину поглощения в исходном растворе цитохрома С, имеющем концентрацию белка 1 мг/мл. Из полученных величин рассчитывают суммарное количество белка, адсорбированного на наноалмазном сорбенте. Из известного количества адсорбированного белка и известной адсорбционной емкости наночастиц алмаза, составляющей 0,5 мг белка на 1 мг наночастиц [Бондарь B.C., Пузырь А.П. Возможность и перспективы создания новых нанотехнологий на основе частиц детонационных наноалмазов: медико-биологический и технический аспекты // Конструкции из композиционных материалов, 2005, вып.4, с.80-94], рассчитывают количество миллиграммов наноалмазов (активного адсорбирующего вещества), содержащееся в 1 мл полученного сорбента. Данные по содержанию наноалмазов (активного адсорбирующего вещества) в разных образцах наноалмазного сорбента представлены в таблице 1.
Данный прием определения характеристик сорбента основан на том, что гель Sepharose® не производится и не применяется в сухом виде. Поэтому весовые отношения не имеют смысла. Общее количество иммобилизованного наноалмаза является некорректной величиной, т.к. часть материала может по разным причинам не взаимодействовать с молекулами белка и, следовательно, важно определение количества активно адсорбирующего вещества.
Пример 5.
Выделение белка люциферазы из грубого белкового экстракта Е. coli.
Через колонку с наноалмазным сорбентом прокачивается препарат грубого белкового экстракта рекомбинантного штамма Е. coli. Промывка осуществляется буфером, содержащим 20 мМ Трис-HCl рН 7.0 и 20 мМ ДТТ. Элюция осуществляется градиентом буфера, содержащим 100 мМ Трис-HCl рН 8.8, 100 мМ ЭДТА, 20 мМ ДТТ. Регистрация хроматографического процесса системой «BIO-RAD BioLogic LP» (USA) приведена на фиг.2, где а - пик неадсорбированных белков, не содержащих люциферазу: б - десорбированная люцифераза. Отсутствие люциферазы в неадсорбированных белках и сохранение ферментных функций десорбированного белка проверено по активности люминесцентной реакции, улучшение чистоты десорбированной люциферазы подтверждено SDS-электрофорезом.
Заявляемый способ получения наноалмазного сорбента занимает мало времени, не требует специализированного оборудования, прост и экономичен и может быть реализован в любой лаборатории.
Определение сорбционной емкости наноалмазного сорбента по маркерному белку цитохром С показало его высокую сорбционную емкость, которая в зависимости от содержания активного адсорбирующего вещества - наноалмазов составляет на 1 мл сорбента 4 - 6 мг белка. Примеры 3-5 являются подтверждением полифункциональности полученного наноалмазного сорбента.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ПРИРОДНЫХ И РЕКОМБИНАНТНЫХ БЕЛКОВ И ДРУГИХ БИОЛОГИЧЕСКИХ СОЕДИНЕНИЙ | 2007 |
|
RU2366713C2 |
| СОРБЕНТ ДЛЯ ХРОМАТОГРАФИИ | 2009 |
|
RU2451544C2 |
| СМАЗОЧНАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2356938C2 |
| РАБОЧЕЕ ВЕЩЕСТВО ОГРАНИЧИТЕЛЯ ИНТЕНСИВНОСТИ МОЩНОГО ОПТИЧЕСКОГО ИЗЛУЧЕНИЯ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2009 |
|
RU2410737C1 |
| СИНТЕТИЧЕСКИЕ АЛМАЗОСОДЕРЖАЩИЕ ВЕЩЕСТВА И СПОСОБ ИХ ВЫДЕЛЕНИЯ | 2006 |
|
RU2306258C1 |
| СПОСОБ ВЫДЕЛЕНИЯ НАНОАЛМАЗОВ ДЕТОНАЦИОННОГО СИНТЕЗА С ПОВЫШЕННОЙ КОЛЛОИДНОЙ УСТОЙЧИВОСТЬЮ | 2010 |
|
RU2458858C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОАЛМАЗОВ ВЗРЫВНОГО СИНТЕЗА С ПОВЫШЕННОЙ КОЛЛОИДНОЙ УСТОЙЧИВОСТЬЮ | 2003 |
|
RU2252192C2 |
| СПОСОБ ИММОБИЛИЗАЦИИ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ НА ПОВЕРХНОСТЬ ДЕТОНАЦИОННЫХ НАНОАЛМАЗОВ | 2013 |
|
RU2561592C2 |
| СПОСОБ ОБРАБОТКИ НАНОАЛМАЗОВ | 2003 |
|
RU2258671C2 |
| Способ ковалентной иммобилизации лизоцима для последующего применения иммобилизованного лизоцима для снижения бактериальной обсемененности биологических жидкостей | 2018 |
|
RU2694883C1 |
Изобретение относится к материалам, предназначенным для сорбции и хроматографического разделения, в частности, белковых молекул. Наноалмазный сорбент содержит иммобилизованные на полисахаридной матрице наноалмазы детонационного синтеза при содержании наноалмазов в сорбенте 8,2-12,0 мг/мл. Наноалмазы иммобилизованы из гидрозоля с дзета-потенциалом -40÷-85 мВ и фракционным размером наночастиц и их кластеров 3-250 нм. Способ получения сорбента включает обработку полисахаридной матрицы, которую вначале отмывают от консервантов дистиллированной водой, а затем обрабатывают 0,5-10,0 мас.% наноалмазным гидрозолем. Техническим результатом является создание полифункционального наноалмазного сорбента, способного адсорбировать белки, различающиеся физико-химическими свойствами. 2 н. 3 з.п. ф-лы, 2 ил., 1 табл.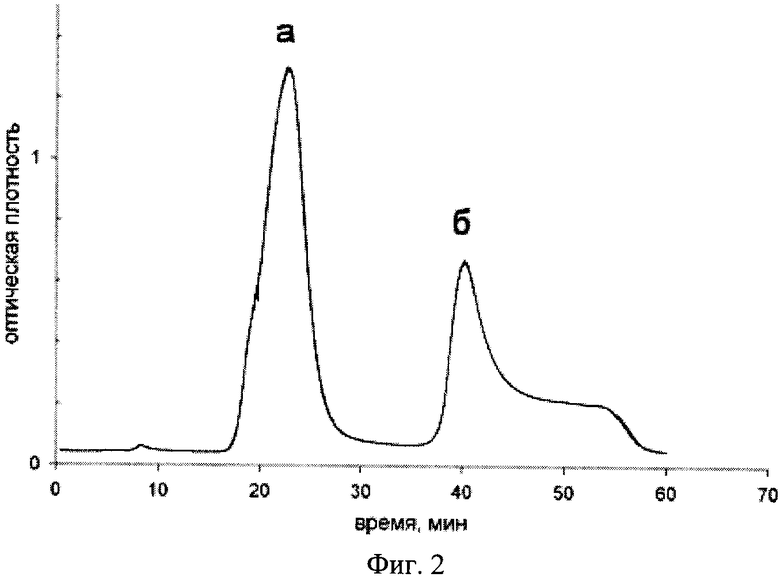
1. Сорбент для хроматографии, содержащий наночастицы алмаза, иммобилизованные на полимерной матрице, отличающийся тем, что сорбент содержит наночастицы алмаза, полученные детонационным синтезом, которые иммобилизованы на полисахаридной матрице в количестве 8,2-12,0 мг на 1 мл сорбента.
2. Сорбент по п.1, отличающийся тем, что наночастицы алмаза иммобилизованы из устойчивого гидрозоля с дзета-потенциалом от -40 до -85 мВ при размере наночастиц алмаза и их кластеров 3-250 нм.
3. Способ получения сорбента для хроматографии, включающий иммобилизацию наночастиц алмаза на полимерной матрице, отличающийся тем, что в качестве матрицы используют полисахаридную матрицу, которую подвергают отмывке дистиллированной водой, обрабатывают устойчивым наноалмазмым гидрозолем, имеющим концентрацию наноалмазных частиц 0,5-10,0 мас.%, и промывают водой.
4. Способ по п.3, отличающийся тем, что в качестве полисахаридной матрицы используют сефарозу 2В.
5. Способ по п.3, отличающийся тем, что процесс проводят в хроматографической колонке.
| RU 94005691 A1, 10.11.1995 | |||
| RU 200112254 A1, 10.06.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ НАНОАЛМАЗОВ ВЗРЫВНОГО СИНТЕЗА С ПОВЫШЕННОЙ КОЛЛОИДНОЙ УСТОЙЧИВОСТЬЮ | 2003 |
|
RU2252192C2 |
| СИНТЕТИЧЕСКИЙ УГЛЕРОДНЫЙ АЛМАЗСОДЕРЖАЩИЙ МАТЕРИАЛ | 1993 |
|
RU2046094C1 |
| RU 20049723 C2, 10.12.1995 | |||
| US 7115325 A, 03.10.2006. | |||
Авторы
Даты
2009-04-20—Публикация
2007-07-19—Подача