Текст описания приведен в факсимильном виде.







































































| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДНК ДЛЯ ВЫЗОВА ИММУННОГО ОТВЕТА ПРОТИВ ОПУХОЛЕАССОЦИИРОВАННЫХ МАКРОФАГОВ | 2007 |
|
RU2459631C2 |
| КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ ПОКСВИРУСА, ЭКСПРЕССИРУЮЩЕГО ОПУХОЛЕВЫЙ АНТИГЕН, И АНТАГОНИСТА И/ИЛИ АГОНИСТА ИНГИБИТОРА ИМУННОЙ КОНТРОЛЬНОЙ ТОЧКИ | 2014 |
|
RU2714142C2 |
| ИНГИБИРОВАНИЕ МЕТАСТАЗОВ ОПУХОЛИ АНТИТЕЛАМИ ПРОТИВ НЕЙРОПИЛИНА-2 | 2007 |
|
RU2437677C2 |
| АНТИТЕЛА, МОДИФИЦИРУЮЩИЕ РАКОВЫЕ ЗАБОЛЕВАНИЯ | 2008 |
|
RU2468036C2 |
| АНТАГОНИСТЫ АКТИВИНА-ActRIIa-Fc И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2008 |
|
RU2473362C2 |
| ВАРИАНТЫ ИЛ-21 | 2006 |
|
RU2412199C2 |
| АНТАГОНИСТЫ РЕЦЕПТОРОВ ДЛЯ ЛЕЧЕНИЯ МЕТАСТАТИЧЕСКОГО РАКА | 2009 |
|
RU2455026C2 |
| АНТИТЕЛА ПРОТИВ PDGFRα ДЛЯ ЛЕЧЕНИЯ ВТОРИЧНОЙ ОПУХОЛИ КОСТИ | 2006 |
|
RU2502523C2 |
| РАКОВЫЙ МАРКЕР И ТЕРАПЕВТИЧЕСКАЯ МИШЕНЬ | 2008 |
|
RU2529797C2 |
| ИНГИБИРОВАНИЕ AXL СИГНАЛИЗАЦИИ В АНТИМЕТАСТАТИЧЕСКОЙ ТЕРАПИИ | 2011 |
|
RU2556822C2 |
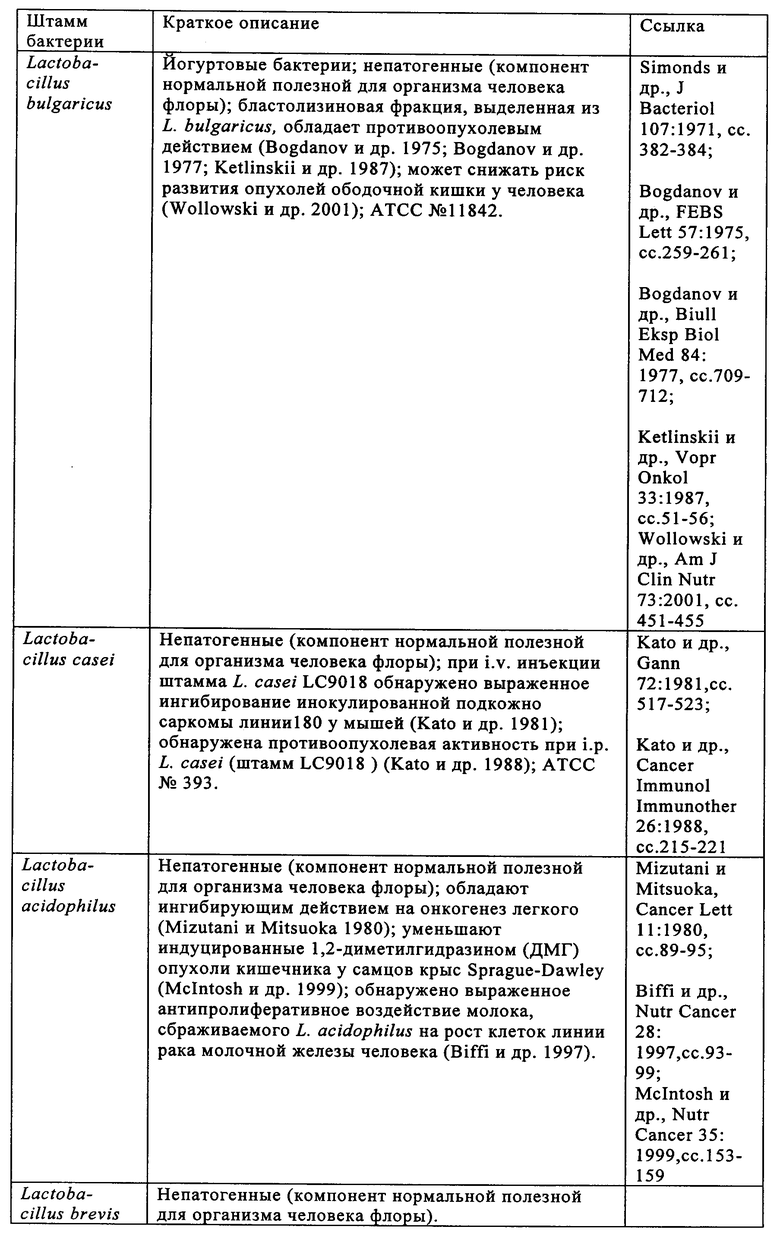
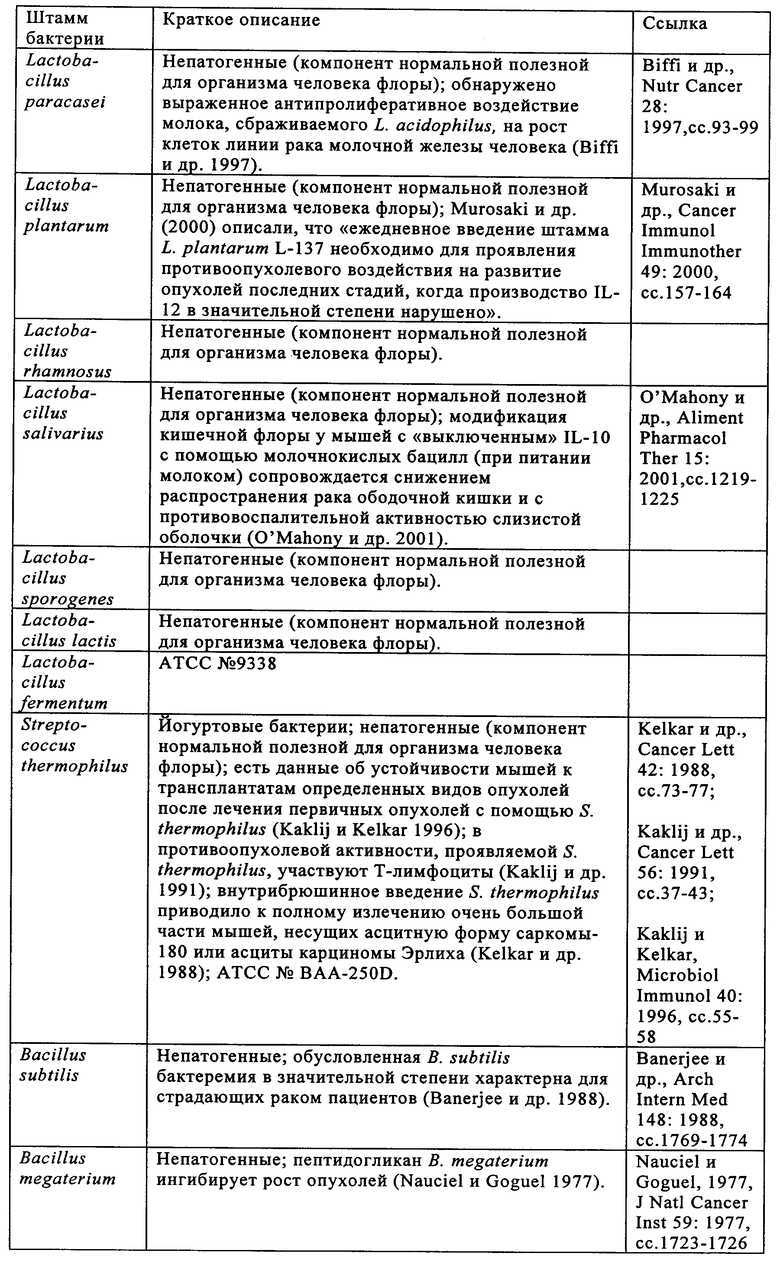
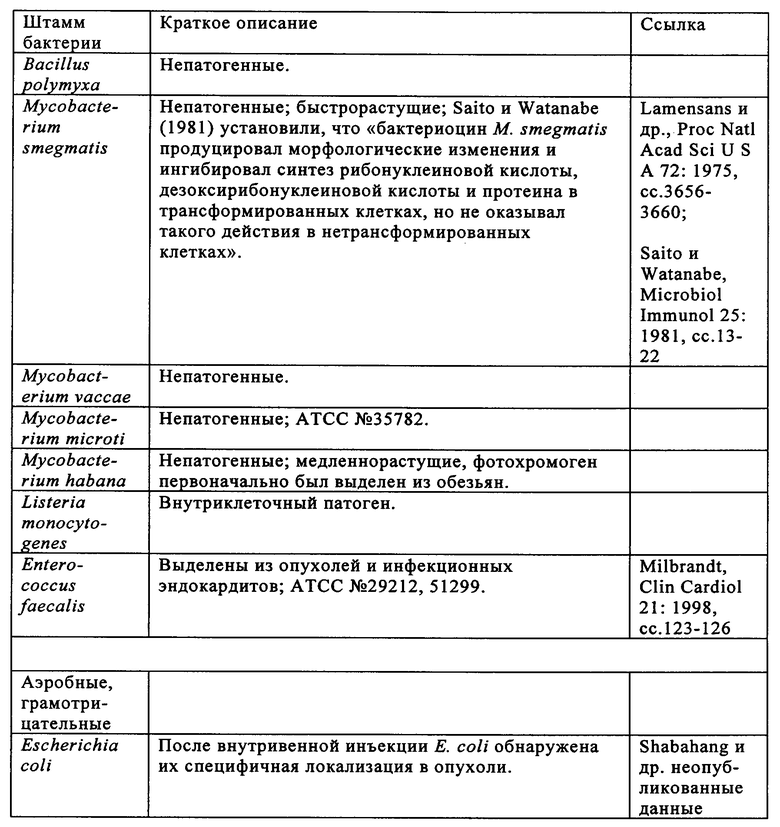
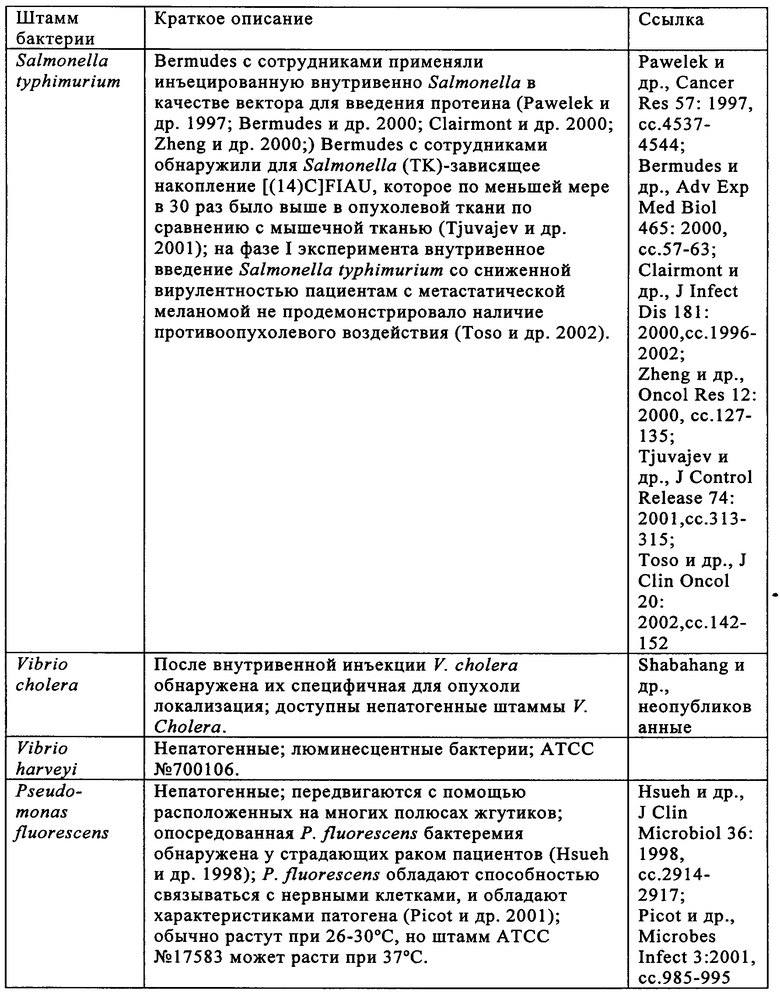
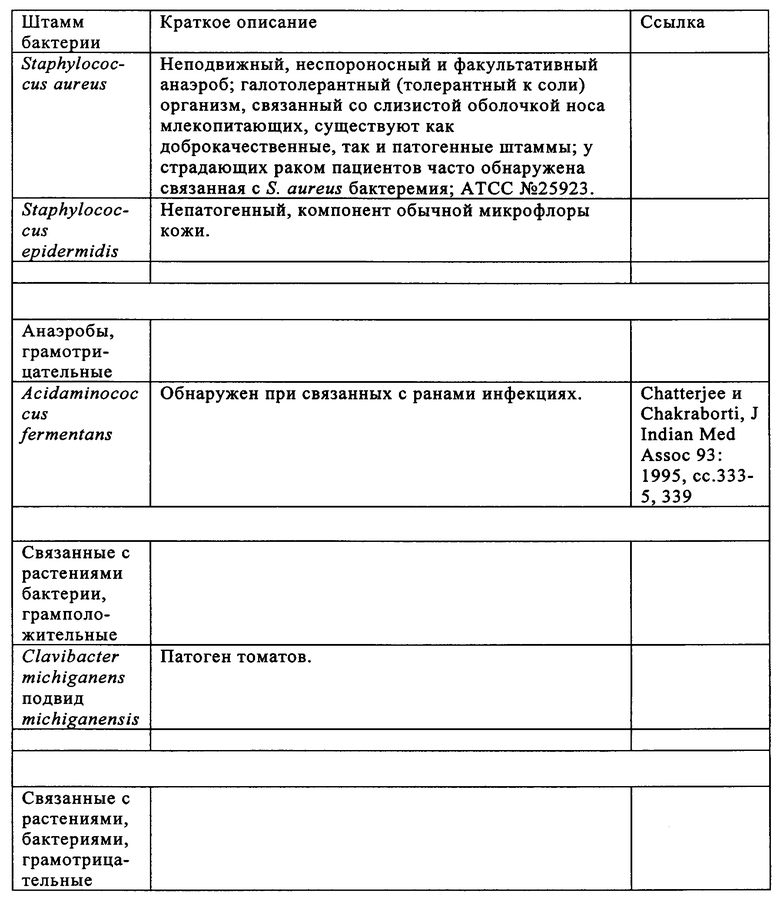
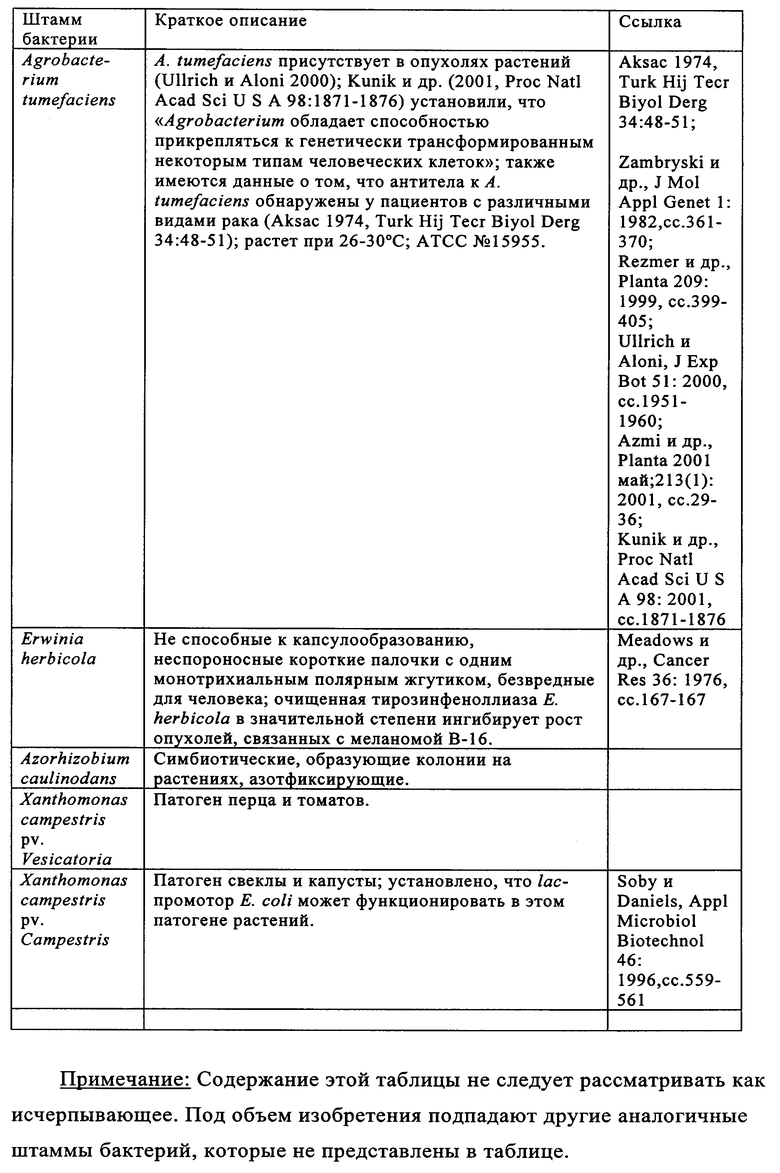
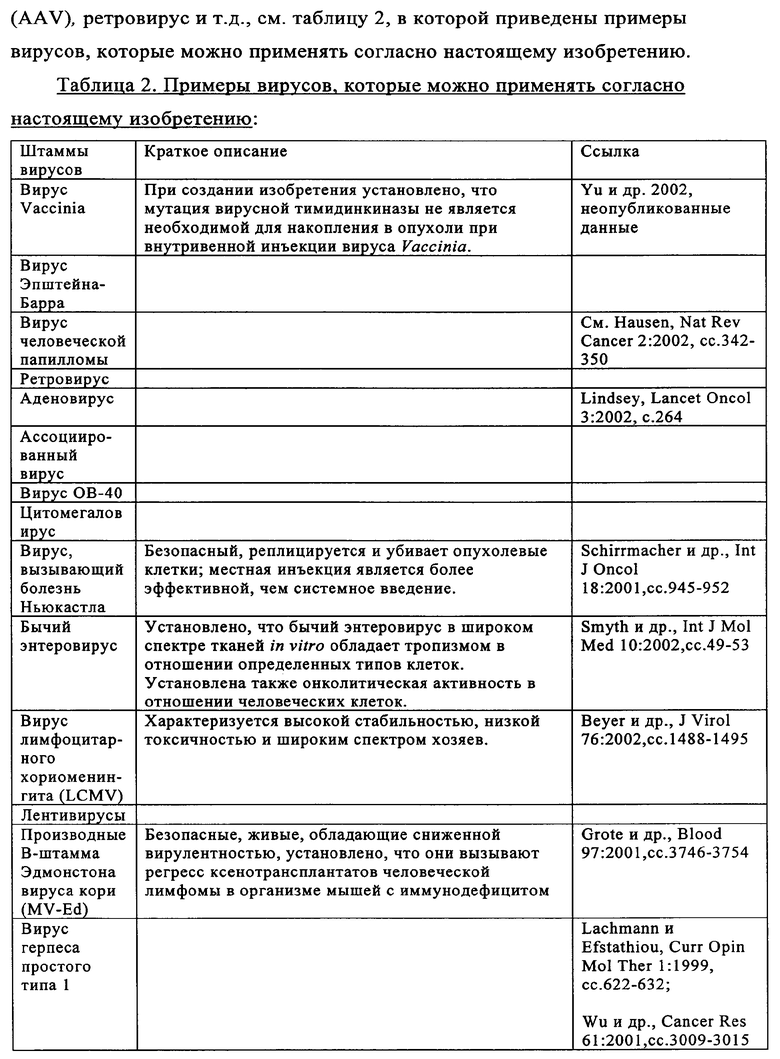
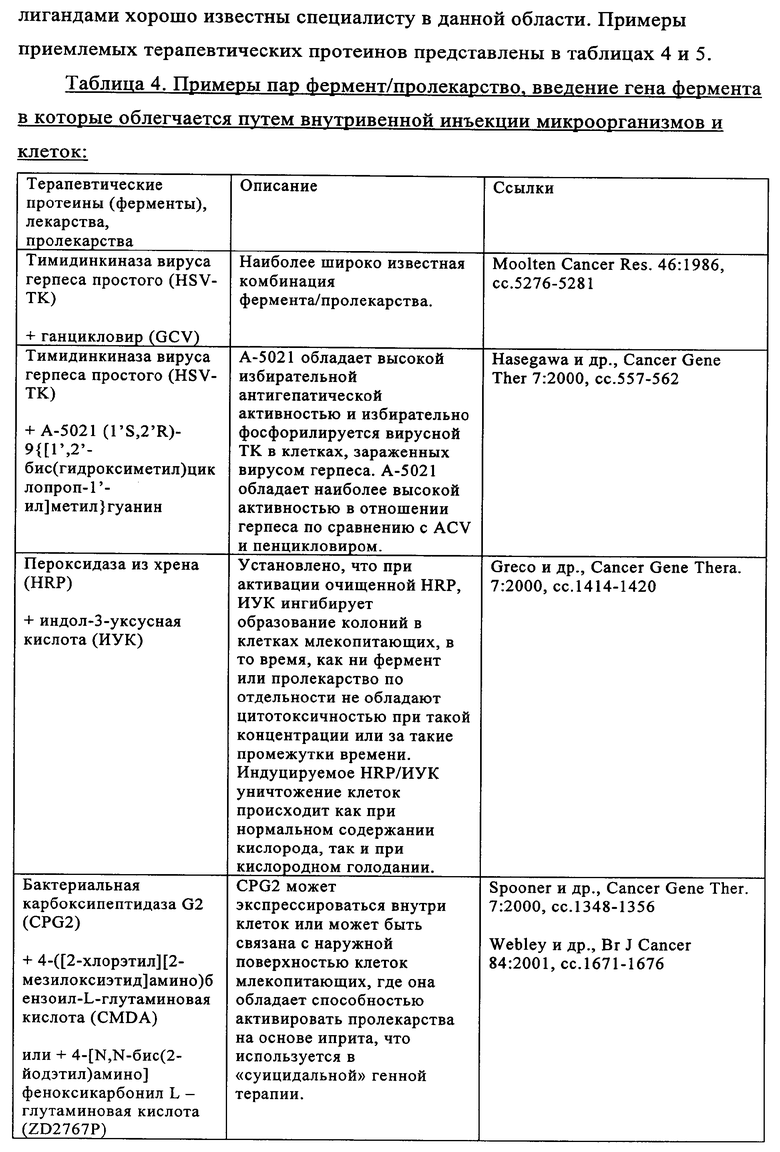
Изобретение относится к области биотехнологии. Предложено применение аттенуированной бактерии Vibrio cholerae для получения фармацевтической композиции, предназначенной для лечения опухоли и/или элиминации метастатической опухоли у пациента. При этом бактерия содержит ДНК, кодирующую белок для лечения опухоли и/или элиминации метастатической опухоли, обладает способностью накапливаться в опухоли и распознается иммунной системой пациента. Также предложено применение штамма LIVP вируса коровьей оспы для тех же целей. Изобретение позволяет проводить мониторинг и лечение опухоли у пациента. Изобретение может быть использовано в медицине. 5 н. и 45 з.п. ф-лы, 14 ил., 6 табл.
1. Применение аттенуированной бактерии Vibrio cholerae для получения фармацевтической композиции, предназначенной для лечения опухоли и/или элиминации метастатической опухоли у пациента, где бактерия:
(i) содержит ДНК, кодирующую белок для лечения опухоли и/или элиминации метастатической опухоли;
(ii) обладает способностью накапливаться в опухоли; и
(iii) распознается иммунной системой пациента.
2. Применение по п.1, где бактерия способна реплицироваться в пациенте.
3. Применение п.1, где композиция предназначена для системного введения.
4. Применение по п.1, где композиция предназначена для внутривенного введения.
5. Применение по п.1, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой цитотоксический белок, цитостатический белок, ингибитор ангиогенеза, белок, стимулирующий апоптоз, белок, ингибирующий фактор элонгации, белок, связывающийся с рибосомальной субъединицей, белок, модифицирующий нуклеотид, нуклеазу, протеазу, цитокин, фермент или рецептор.
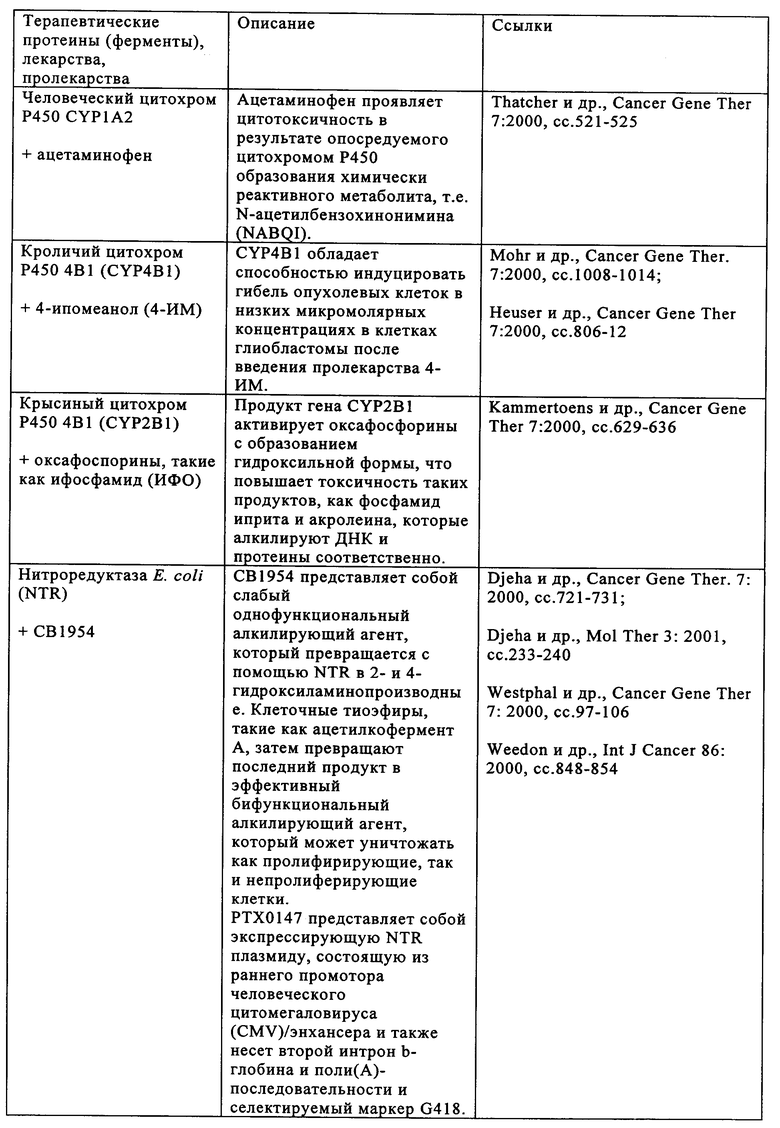
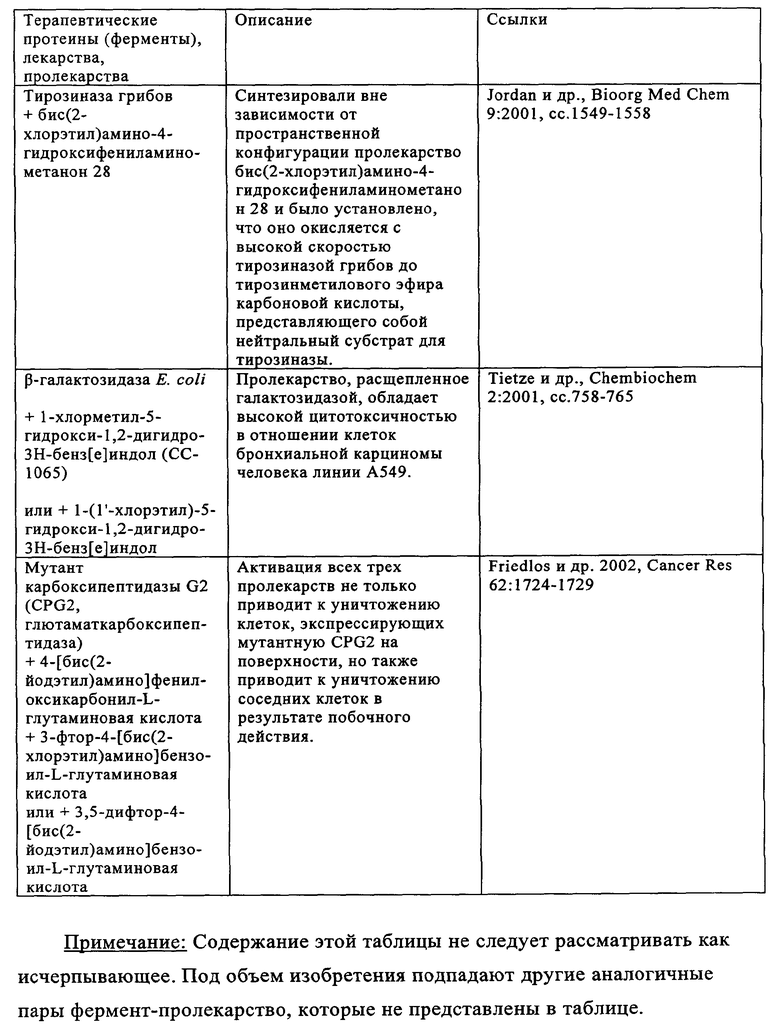
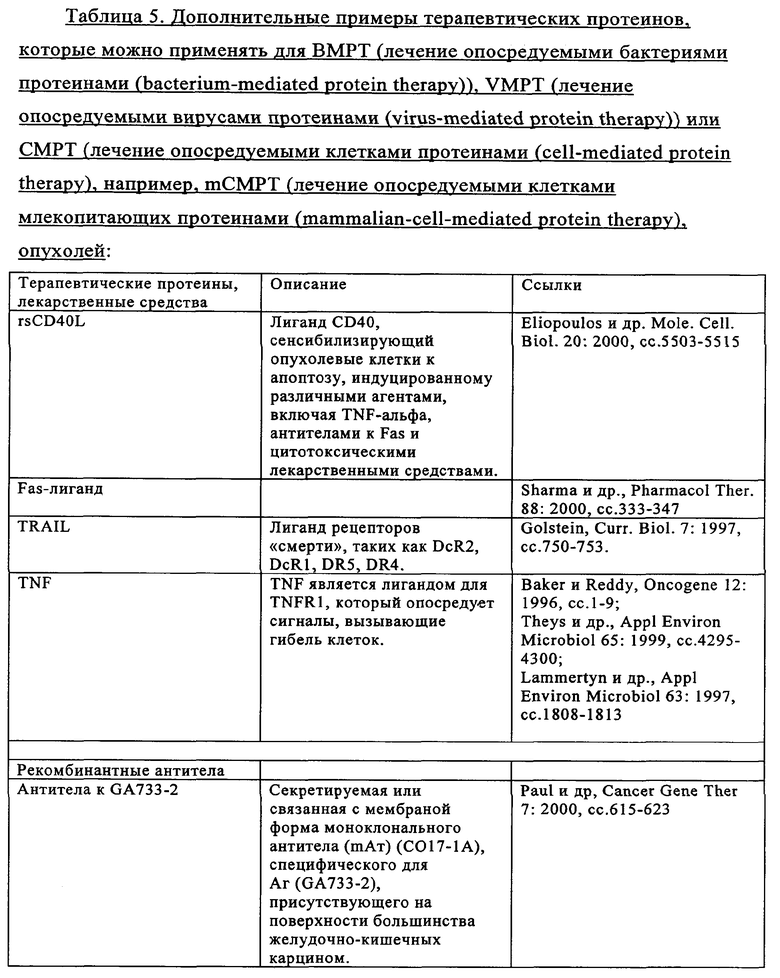
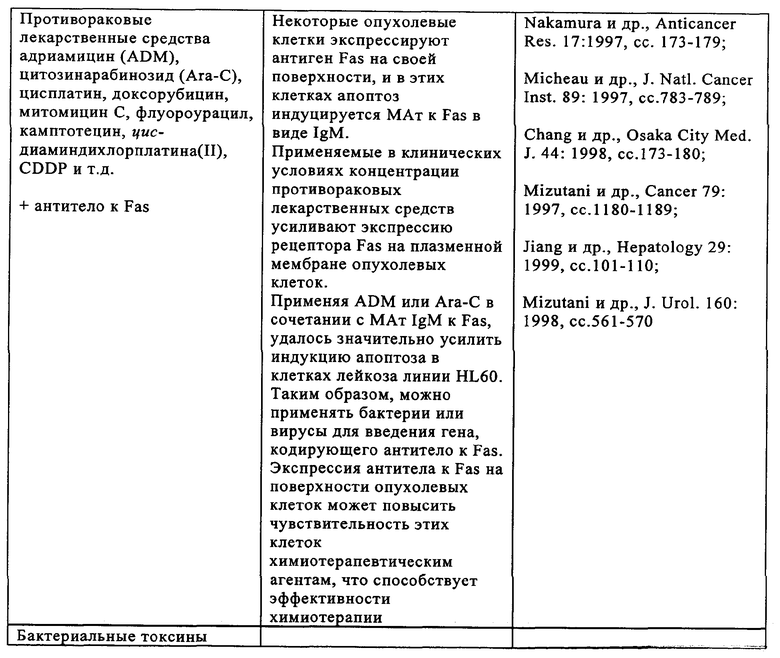
6. Применение по п.5, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой rsCD40L, Fas-лиганд, TRAIL, TNF, антитело к GA733-2, микроцин Е492, дифтерийный токсин, экзотоксины Pseudomonas, токсин Шига, эндостатин, глюкуронидазу, бета-галактозидазу, тимидинкиназу, пероксидазу хрена, карбоксипептидазу G2, цитохром Р450, нитроредуктазу, цитозиндезаминазу, карбоксилэстеразу, тирозиназу или веротоксин.
7. Применение по п.5, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой клеточный рецептор, который способен связывать терапевтический лиганд для лечения опухоли.
8. Применение по п.7, где терапевтический лиганд включает лиганд, связанный с токсином.
9. Применение по п.1, где бактерия позволяет внешне визуализировать опухоль, опухолевую ткань, рак или метастазы.
10. Применение по п.1, где опухоль представляет собой опухоль молочной железы, опухоль предстательной железы, опухоль мочевого пузыря, опухоль мозга, опухоль ободочной (толстой) кишки, опухоль легкого, опухоль яичников, опухоль поджелудочной железы, опухоль печени или кожи.
11. Применение штамма LIVP вируса коровьей оспы для получения фармацевтической композиции, предназначенной для лечения опухоли и/или элиминации метастатической опухоли у пациента, где фармацевтическая композиция разработана для внутривенного введения.
12. Применение по п.11, где вирус кодирует белок для лечения опухоли.
13. Применение по п.11, где вирус способен реплицироваться в пациенте.
14. Применение по п.11, где композиция предназначена для системного введения.
15. Применение по п.11, где композиция предназначена для внутривенного введения.
16. Применение по п.11, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой цитотоксический белок, цитостатический белок, ингибитор ангиогенеза, белок, стимулирующий апоптоз, белок, ингибирующий фактор элонгации, белок, связывающийся с рибосомальной субъединицей, белок, модифицирующий нуклеотид, нуклеазу, протеазу, цитокин, фермент или рецептор.
17. Применение по п.16, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой rsCD40L, Fas-лиганд, TRAIL TNF, антитело к GA733-2, микроцин Е492, дифтерийный токсин, экзотоксины Pseudomonas, токсин Шига, эндостатин, глюкуронидазу, бета-галактозидазу, тимидинкиназу, пероксидазу хрена, карбоксипептидазу G2, цитохром Р450, нитроредуктазу, цитозиндезаминазу, карбоксилэстеразу, тирозиназу или веротоксин.
18. Применение по п.16, где белок для лечения опухоли и/или элиминации метастатической опухоли представляет собой клеточный рецептор, который способен связывать терапевтический лиганд, подходящий для лечения опухоли.
19. Применение по п.18, где терапевтический лиганд включает лиганд, связанный с токсином.
20. Применение по п.11, где вирус позволяет внешне визуализировать опухоль, опухолевую ткань, рак или метастазы.
21. Применение по п.11, где опухоль представляет собой опухоль молочной железы, опухоль предстательной железы, опухоль мочевого пузыря, опухоль мозга, опухоль ободочной (толстой) кишки, опухоль легкого, опухоль яичников, опухоль поджелудочной железы, опухоль печени или опухоль кожи.
22. Применение бактерии для получения диагностической композиции, предназначенной для визуализации опухоли и/или для мониторинга терапевтического лечения опухоли у пациента, где эта бактерия:
(i) содержит ДНК, кодирующую обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал; и
(ii) представляет собой Vibrio cholerae.
23. Применение по п.22, где бактерия позволяет внешне визуализировать опухоль, опухолевую ткань, рак или метастазы.
24. Применение по п.22, где белок, способный индуцировать обнаруживаемый сигнал, индуцирует сигнал, который обнаруживается методом визуализации с помощью магнитного резонанса (MRI), однофотонной эмиссионной компьютерной томографии (SPECT), эмиссионной позитронной томографии (PET), сцинтиграфии, гамма камеры, β+ детектора или γ детектора.
25. Применение по п.22, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, излучает свет или индуцирует излучение света.
26. Применение по п.25, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, является флуоресцентным или люминисцентным белком.
27. Применение по п.25, где белок, способный индуцировать обнаруживаемый сигнал, представляет собой люциферазу, зеленый флуоресцентный белок или красный флуоресцентный белок.
28. Применение по п.22, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, связывает контрастирующий агент или хромотофор.
29. Применение по п.22, где белок, способный индуцировать обнаруживаемый сигнал, является металлсвязывающим белком.
30. Применение по п.22, где белок, способный индуцировать обнаруживаемый сигнал, является клеточным рецептором, который может связывать обнаруживаемый лиганд для обнаружения опухоли, опухолевой ткани, рака или метастаз у пациента.
31. Применение по п.30, где клеточный рецептор является рецептором трансферрина.
32. Применение по п.30, где обнаруживаемым лигандом является меченный металлом лиганд или лиганд, который связывает металл.
33. Применение по п.22, где опухолью является опухоль молочной железы, опухоль предстательной железы, опухоль мочевого пузыря, опухоль мозга, опухоль ободочной (толстой) кишки, опухоль легкого, опухоль яичников, опухоль поджелудочной железы, опухоль печени или опухоль кожи.
34. Применение по п.22, где бактерия содержит ДНК, кодирующую белок для лечения.
35. Применение штамма Lister вируса коровьей оспы для приготовления диагностической композиции для визуализации опухоли и/или для мониторинга терапевтического лечения опухоли, где вирус подготовлен для внутривенного введения и вирус
(i) содержит ДНК, кодирующую обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал;
(ii) обладает способностью накапливаться в опухоли и (iii) распознается иммунной системой пациента.
36. Применение п.35, где штаммом Lister является LIVP.
37. Применение по п.35 или 36, где вирус позволяет внешне визуализировать опухоль, опухолевую ткань, рак или метастазы.
38. Применение по п.35 или 36, где белок, способный индуцировать определяемый сигнал, индуцирует сигнал, который обнаруживается методом визуализации с помощью магнитного резонанса (MPI), однофотонной эмиссионной компьютерной томографии (SPECT), эмиссионной позитронной томографии (PET), сцинтиграфии, гамма камеры, β+детектора или γ детектора.
39. Применение по п.35 или 36, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, излучает свет или индуцирует излучение света.
40. Применение по п.39, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, является флуоресцентным или люминисцентным белком.
41. Применение по п.39, где белок, способный индуцировать обнаруживаемый сигнал, представляет собой люциферазу, зеленый флуоресцентный белок или красный флуоресцентный белок.
42. Применение по п.35 или 36, где обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал, связывает контрастирующий агент или хромотофор.
43. Применение по п.35 или 36, где белок, способный индуцировать обнаруживаемый сигнал, является металлсвязывающим белком.
44. Применение по п.35 или 36, где белок, способный индуцировать обнаруживаемый сигнал, является клеточным рецептором, который может связывать обнаруживаемый лиганд для обнаружения опухоли, опухолевой ткани, рака или метастаз у пациента.
45. Применение по п.44, где клеточный рецептор является рецептором трансферрина.
46. Применение по п.44, где обнаруживаемым лигандом является меченный металлом лиганд или лиганд, который связывает металл.
47. Применение по п.35 или 36, где опухолью является опухоль молочной железы, опухоль предстательной железы, опухоль мочевого пузыря, опухоль мозга, опухоль ободочной (толстой) кишки, опухоль легкого, опухоль яичников, опухоль поджелудочной железы, опухоль печени или опухоль кожи.
48. Применение по п.35 или 36, где вирус кодирует белок для лечения.
49. Применение штамма LIVP вируса коровьей оспы для получения фармацевтической композиции, предназначенной для лечения и мониторинга лечения опухоли, опухолевой ткани, рака или метастаз у пациента, где вирус содержит ДНК, кодирующую обнаруживаемый белок или белок, способный индуцировать обнаруживаемый сигнал.
50. Применение по п.49, где вирус кодирует белок для лечения.
| Устройство для определения распределения частиц полидисперсных сред | 1959 |
|
SU125399A1 |
| PUHLMANN M | |||
| et al | |||
| Vaccinia as a vector for tumor-directed gene therapy: biodistribution of a thymidine kinase-deleted mutant, Cancer Gene Ther | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Способ высушивания и дегазации изоляционных масел | 1938 |
|
SU54795A1 |
| Машина для нанизывания бараночных изделий на шпагат | 1955 |
|
SU105229A1 |
| Устройство для усиления квазиплоской волны | 1948 |
|
SU118195A1 |
Авторы
Даты
2009-06-10—Публикация
2002-07-31—Подача