Настоящее изобретение относится к пиразолопиридиновым соединениям, способам их получения, промежуточным соединениям, полезным в этих способах, и фармацевтическим композициям, содержащим такие соединения. Изобретение также относится к применению пиразолопиридиновых соединений в терапии, например в качестве ингибиторов фосфодиэстераз и/или для лечения, и/или профилактики воспалительных и/или аллергических заболеваний, таких как хроническая обструктивная болезнь легких (COPD), астма, ревматоидный артрит или аллергический ринит.
В US 3979399, US 3840546 и US 3966746 (E.R.Squibb & Sons) раскрыты 4-аминопроизводные пиразоло[3,4-b]пиридин-5-карбоксамидов, где 4-аминогруппа
NR3R4 может представлять собой ациклическую аминогруппу, где каждый из R3 и R4 может представлять собой водород, низший алкил (например, бутил), фенил и т. д.; NR3R4 альтернативно может представлять собой 3-6-членную гетероциклическую группу, такую как пирролидино, пиперидино и пиперазино. Эти соединения раскрыты как депрессанты центральной нервной системы, полезные в качестве атарактических, анальгезирующих и гипотензивных агентов.
В US 3925388, US 3856799, US 3833594 и US 3755340 (E.R.Squibb & Sons) раскрыты 4-аминопроизводные пиразоло[3,4-b]пиридин-5-карбоновых кислот и сложных эфиров. 4-Аминогруппа NR3R4 может представлять собой ациклическую аминогруппу, где каждый из R3 и R4 может представлять собой водород, низший алкил (например, бутил), фенил и т.д.; NR3R4 может альтернативно представлять собой 5-6-членную гетероциклическую группу, в которой присутствует дополнительный атом азота, такую как пирролидино, пиперидино, пиразолил, пиримидинил, пиридазинил или пиперазинил. Эти соединения упоминаются как депрессанты центральной нервной системы, полезные в качестве атарактических агентов или транквилизаторов, как обладающие противовоспалительными и анальгезирующими свойствами. Эти соединения упоминаются как повышающие внутриклеточную концентрацию аденозин-3',5'-циклического монофосфата, а также облегчающие симптомы астмы.
В Н.Hoehn et al., J.Heterocycl. Chem., 1972, 9(2), 235-253 раскрыт ряд производных 1H-пиразоло[3,4-b]пиридин-5-карбоновой кислоты с 4-гидрокси-, 4-хлор-, 4-алкокси-, 4-гидразино- и 4-амино-заместителями.
В СА 1003419, СН 553799 и Т.Denzel, Archiv der Pharmazie, 1974, 307(3), 177-186 раскрыты 4,5-двузамещенные 1H-пиразоло[3,4-b]пиридины, незамещенные по положению 1.
В выложенной заявке Японии JP-2002-20386-A (Ono Yakuhin Kogyo КК), опубликованной 23 января 2002 года, раскрыты пиразолопиридиновые соединения следующей формулы:
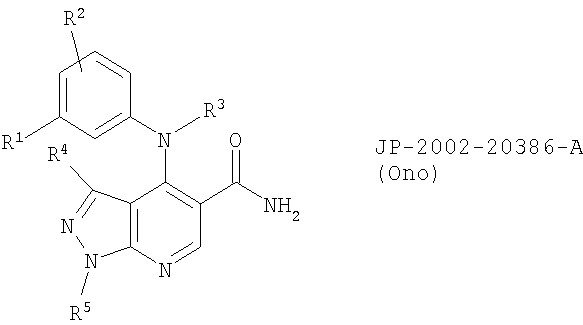
где R1 обозначает 1) группу -OR6, 2) группу -SR7, 3) С2-8алкинильную группу, 4) нитрогруппу, 5) цианогруппу, 6) С1-8алкильную группу, замещенную гидроксигруппой или С1-8алкоксигруппой, 7) фенильную группу, 8) группу -C(O)R8, 9) группу -SO2NR9R10, 10) группу -NR11SO2R12, 11) группу -NR13C(O)R14 или 12) группу CH=NR15, R6 и R7 обозначают 1) атом водорода, 2) С1-8алкильную группу, 3) С1-8алкильную группу, замещенную С1-8алкоксигруппой, 4) тригалогенометильную группу, 5) С3-7циклоалкильную группу, 6) С1-8алкильную группу, замещенную фенильной группой или 7) 3-15-членное моно-, би- или трициклическое гетерокольцо, содержащее 1-4 атома азота, 1-3 атома кислорода и/или 1-3 атома серы. R2 обозначает 1) атом водорода или 2) С1-8алкоксигруппу. R3 обозначает 1) атом водорода или 2) С1-8алкильную группу. R4 обозначает 1) атом водорода, 2) С1-8алкильную группу, 3) С3-7циклоалкильную группу, 4) С1-8алкильную группу, замещенную С3-7циклоалкильной группой, 5) фенильную группу, которая может быть замещена атомами галогена в количестве 1-3 или 6) 3-15-членное моно-, би- или трициклическое гетерокольцо, содержащее 1-4 атома азота, 1-3 атома кислорода и/или 1-3 атома серы. R5 обозначает 1) атом водорода, 2) С1-8алкильную группу, 3) С3-7циклоалкильную группу, 4) С1-8алкильную группу, замещенную С3-7циклоалкильной группой или 5) фенильную группу, которая может быть замещена 1-3 заместителями. В группе R3 предпочтительным является атом водорода. В группе R4 предпочтительными являются метил, этил, циклопропил, циклобутил или циклопентил. Установлено, что соединения из JP-2002-20386-A обладают ингибиторной активностью в отношении PDE4 (фосфодиэстеразы 4) и полезны в предупреждении и/или лечении воспалительных заболеваний и многих других заболеваний.
В ЕР 0076035 А1 (ICI Americas) раскрыты производные пиразоло[3,4-b]пиридина в качестве депрессантов центральной нервной системы, полезных в качестве транквилизаторов или атарактических агентов для ослабления тревоги и состояний напряжения.
Известно соединение картазолат (cartazolate), этил-4-(н-бутиламино)-1-этил-1Н-пиразоло[3,4-b]-пиридин-5-карбоксилат. В J.W.Daly et al., Med. Chem. Res., 1994, 4, 293-306, и D.Shi et al., Drug Development Research, 1997, 42, 41-56 раскрыт ряд 4-(амино)замещенных производных 1Н-пиразоло[3,4-b]-пиридин-5-карбоновой кислоты, включая этил-4-циклопентиламино-1-метил-1Н-пиразоло[3,4-b]-пиридин-5-карбоксилат и их аффинности и антагонистические активности в отношении A1- и А2A-аденозиновых рецепторов, и в последней работе раскрыты их аффинности к различным сайтам связывания GABAA (гамма-аминомасляная кислота)-рецепторного канала. В S.Schenone et al., Bioorg. Med. Chem. Lett., 2001, 11, 2529-2531, и F.Bondavalli et al., J. Med. Chem., 2002, vol.45 (Issue 22, 24 October 2002, предположительно опубликован в Web 09/24/2002), pp.4875-4887 раскрыт ряд этиловых эфиров 4-амино-1-(2-хлор-2-фенилэтил)-1Н-пиразоло[3,4-b]-пиридин-5-карбоновой кислоты в качестве лигандов A1-аденозинового рецептора.
В WO 02/060900 А2 раскрыт в качестве антагонистов МСР-1 (моноцитарного хемотаксического белка-1) для лечения аллергических, воспалительных или аутоиммунных расстройств или заболеваний ряд бициклических гетероциклических соединений с -C(O)-NR4-C(O)-NR5R6 заместителем, включая изоксазоло[5,4-b]пиридины и 1Н-пиразоло[3,4-b]-пиридины (названные пиразоло[5,4-b]-пиридины) с группой -C(O)-NR4-C(O)-NR5R6 в качестве заместителя по положению 5 и возможно замещенные по 1-, 3-, 4- и/или 6-положениям. Бициклические гетероциклические соединения с -C(O)NH2 заместителем вместо -C(O)-NR4-C(O)-NR5R6 заместителя заявлены как раскрытые в WO 02/060900 в качестве промежуточных соединений в синтезе соединений, замещенных группой -С(O)-NR4-С(О)-NR5R6.
Желательно найти новые соединения, которые связываются с фосфодиэстеразой типа IV (PDE4) и предпочтительно ингибируют ее.
В настоящем изобретении предложено соединение формулы (I) или его соль (в частности, его фармацевтически приемлемая соль)
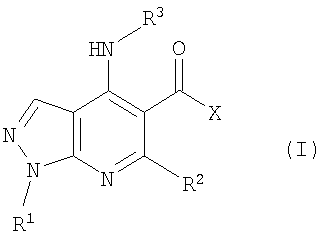
где:
R1 представляет собой С1-4алкил, C1-3фторалкил, -CH2CH2OH или -СН2СН2CO2С1-2алкил;
R2 представляет собой атом водорода (Н), метил или С1фторалкил;
R3 представляет собой возможно замещенный С3-8циклоалкил, или возможно замещенный мононенасыщенный С5-7циклоалкенил, или возможно замещенную гетероциклическую группу подформулы (аа), (bb) или (cc);
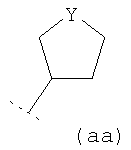 или
или 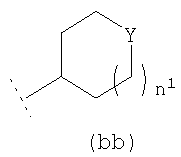 или
или 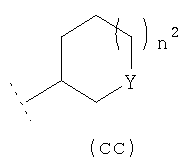
где n1 и n2 независимо равны 1 или 2, и где Y представляет собой О, S, SO2 или NR10; где R10 представляет собой атом водорода (Н), С1-4алкил (например, метил или этил),
С1-2фторалкил, СН2С(O)NH2, С(O)NH2, С(O)-С1-2алкил, С(O)-С1фторалкил или -С(O)-СН2O-С1-2алкил;
и где в R3 С3-8циклоалкильная или гетероциклическая группа подформулы (аа), (bb) или (cc) возможно замещена одним или двумя заместителями, независимо представляющими собой (например, представляющими собой) оксо (=O); ОН; С1-2алкокси; С1-2фторалкокси (например, трифторметокси); NHR21, где R21 представляет собой атом водорода (Н) или С1-5алкил с прямой цепью (например, Н или С1-4алкил с прямой цепью); С1-2алкил; С1-2фторалкил (например, С1фторалкил, такой как -CH2F или -CHF2); -СН2OH; -СН2СН2OH; -CH2NHR22, где R22 представляет собой Н или С1-2алкил; -C(O)OR23, где R23 представляет собой Н или С1-2алкил; -C(O)NHR24, где R24 представляет собой Н или С1-2алкил; -C(O)R25, где R25 представляет собой С1-2алкил; фторо, гидроксиимино (=N-ОН) или (С1-4алкокси)имино (=N-OR26, где R26 представляет собой С1-4алкил); и где любой ОН, алкокси, фторалкокси или NHR21 заместитель не замещает по атому углерода кольца
R3, соединенному (связанному) с -NH- группой формулы (I), и не замещает по любому атому углерода кольца R3, связанному с группой Y гетероциклической группы (аа), (bb) или (cc);
и где, когда R3 представляет собой возможно замещенный мононенасыщенный С5-7циклоалкенил, тогда этот циклоалкенил возможно замещен одним или двумя заместителями, представляющими собой фторо или С1-2алкил, при условии, что если присутствуют два заместителя, то они не представляют собой оба С2алкил, и атом углерода кольца R3, связанный с -NH-группой формулы (I), не задействован в циклоалкенильной двойной связи;
или R3 представляет собой бициклическую группу подформулы 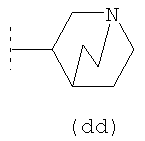 (dd): или подформулы (ее):
(dd): или подформулы (ее): 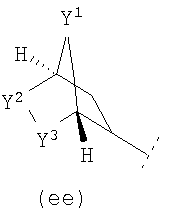 ,
,
где Y1, Y2 и Y3 независимо представляют собой СН2 или атом кислорода (О), при условии, что не более чем один из Y1, Y2 и Y3 представляют собой атом кислорода (О);
и Х представляет собой NR4R5 или OR5a, где:
R4 представляет собой атом водорода (Н); С1-6алкил; C1-3фторалкил; или С2-6алкил, замещенный одним заместителем R11; и
R5 представляет собой атом водорода (Н); С1-8алкил; С1-8фторалкил; С3-8циклоалкил, возможно замещенный С1-2алкильной группой; или -(CH2)n 4-C2-8циклоалкил, возможно замещенный в группировке -(СН2)n 4- либо в С3-8циклоалкильной группировке С1-2алкильной группой, где n4 равно 1, 2 или 3;
либо R5 представляет собой С2-6алкил, замещенный одним или двумя независимыми заместителями R11;
где каждый заместитель R11 независимо от любого другого присутствующего заместителя R11 представляет собой: гидрокси (ОН); C1-6алкокси; фенилокси; бензилокси; -NR12R13; -NR15-C(O)R16; -NR15-C(O)-O-R16; -NR15-C(O)-NH-R15 или -NR15-SO2R16; и где любой заместитель R11, который представляет собой ОН, алкокси или -NR12R13, не является заместителем по любому атому углерода любого R4 или R5 замещенного алкила, который связан с атомом азота в NR4R5;
либо R5 представляет собой -(CH2)n 11-C(O)R16; -(CH2)n 12-C(O)NR12R13; -CHR19-C(O)NR12R13; -(CH2)n-C(O)OR16; -(CH2)n 12-C(O)OH; -CHR19-C(O)OR16; -CHR19-C(O)OH; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN; где n11 равно 0, 1, 2, 3 или 4 и n12 равно 1, 2, 3 или 4;
либо R5 представляет собой -(CH2)n 13-Het; где n13 равно 0, 1, 2, 3 или 4 и Het представляет собой 4-, 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один или два кольцевых гетероатома, независимо выбранных из О, S и N; где любые присутствующие кольцевые гетероатомы не связаны с группировкой -(СН2)n 13-, когда n13 равно 1, и не связаны с атомом азота из NR4R5, когда n13 равно 0; где любые кольцевые атомы азота, которые присутствуют и которые не являются ненасыщенными (то есть которые не задействованы в двойной связи), присутствуют в виде NR17, где R17 является таким, как определено здесь; и где один или два из кольцевых атомов углерода возможно независимо замещены С1-2алкилом;
либо R5 представляет собой фенил, возможно независимо замещенный одним, двумя или тремя из: атома галогена; C1-6алкила (например, С1-4алкила или С1-2алкила); С1-2фторалкила (например, трифторметила); С1-4алкокси (например, С1-2алкокси); С1-2фторалкокси (например, трифторметокси); С3-6циклоалкокси; -C(O)R16a; -C(O)OR30; -SO2-R16а (например, С1-2алкилсульфонил или С1-2алкил-SO2-);
R16a-S(O)2-NR15a- (например, С1-2алкил-SO2-NH-); R7R8N-S(O)2-; С1-2алкил-С(O)-R15aN-S(O)2-;
С1-4алкил-S(O)-; Ph-S(O)-, R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметила;
С1-4алкоксиэтила; С1-2алкил-S(O)2-CH2-; R7R8N-S(O)2-CH2-; C1-2алкил-S(O)2-R15a-CH2-; -CH2-OH; -CH2CH2-OH; -CH2-NR7R8; -CH2-CH2-NR7R8; -CH2-C(O)OR30; -CH2-C(O)-NR7R8; -CH2-NR15a-C(O)-C1-3алкил; -(CH2)n 14-Het1, где n14 равно 0 или 1; циано (CN); Ar5a; или фенила, пиридинила или пиримидинила, где фенил, пиридинил или пиримидинил возможно независимо замещены одним или двумя заместителями фторо, хлоро, С1-2алкил, С1фторалкил, С1-2алкокси или С1фторалкокси; или где два соседних заместителя, взятых вместе, представляют собой -O-(СМе2)-O- или -O-(CH2)n 14-O-, где n14 равно 1 или 2;
где R7 и R8 независимо представляют собой атом водорода (Н); С1-4алкил (например, С1-2алкил, такой как метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; или R7 и R8 вместе представляют собой -(СН2)n 6-, либо -С(O)-(СН2)n 7-, либо -С(O)-(СН2)n 7-С(O)-, либо -(CH2)n 8-X7-(CH2)n 9-, либо -C(O)-X7-(CH2)n 10-, где: n6 равно 3, 4, 5 или 6, n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3 (предпочтительно независимо 2), и X7 представляет собой О или NR14, где R14 представляет собой Н, С1-2алкил или С(O)Ме (предпочтительно Н или С1-2алкил);
либо R5 имеет подформулу (х), (y), (y1) или (z):
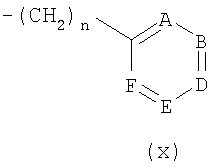
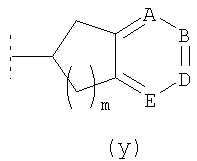
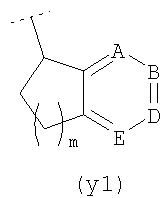
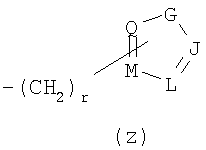
где в подформуле (х) n=0, 1 или 2; в подформуле (y) и (y1) m=1 или 2 и в подформуле (z) r=0, 1 или 2;
где в подформуле (х) и (y) и (y1) ни один из, один или два из А, В, D, Е и F независимо представляют собой атом азота или оксид азота (N+-O-), при условии, что не более чем один из А, В, D, Е и F представляет собой оксид азота; и остальные из А, В, D, Е и F независимо представляют собой СН или CR6;
при условии, что, когда n равно 0 в подформуле (х), тогда один или два из А, В, D, Е и F независимо представляют собой атом азота или оксид азота (N+-O-), и не более чем один из А, В, D, Е и F представляет собой оксид азота;
где каждый R6, независимо от любого другого присутствующего R6, представляет собой: атом галогена; С1-6алкил (например, С1-4алкил или С1-2алкил); С1-4фторалкил (например, С1-2фторалкил); С1-4алкокси (например, С1-2алкокси); С1-2фторалкокси; С3-6циклоалкилокси; -C(O)R16a; -C(O)OR30; -SO2-R16a (например, С1-2алкилсульфонил, то есть С1-2алкил-SO2-); R16a-S(O)2-NR15a (например, С1-2алкил-SO2-NH-); R7R8N-S(O)2-; С1-2алкил-С(O)-R15aN-S(O)2-; С1-4алкил-S(O)-, Ph-S(O)-, R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметил; С1-4алкоксиэтил; С1-2алкил-S(O)2-СН2-; R7R8N-S(O)2-CH2-; C1-2алкил-S(O)2-R15a-CH2-; -СН2-ОН; -СН2СН2-ОН; -CH2-NR7R8; -CH2-CH2-NR7R8; -CH2-C(O)OR30; -CH2-C(O)-NR7R8; -CH2-R15a-C(O)-C1-3алкил; -(CH2)n 14-Het1, где n14 равно 0 или 1; циано (CN); Ar5b; или фенил, пиридинил или пиримидинил, где фенил, пиридинил или пиримидинил возможно независимо замещены одним или двумя из фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; либо где два соседние R6, взятые вместе, представляют собой -O-(СМе2)-O- или -O-(CH2)n 14-О-, где n14 равно 1 или 2;
где R7 и R8 такие, как определено здесь;
где подформула (y) и (y1) возможно независимо является замещенной оксо (=O) по кольцевому атому углерода, соседнему с 6-членным ароматическим кольцом (например, подформула (y) возможно может представлять собой 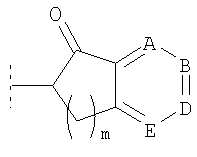 или
или 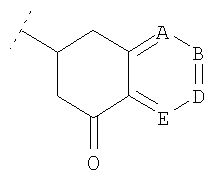 , либо подформула (y1) возможно может представлять собой
, либо подформула (y1) возможно может представлять собой 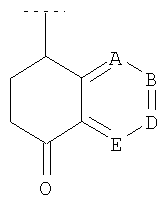 или
или 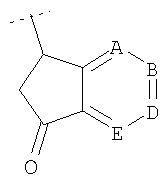 );
);
где в подформуле (z) G представляет собой О, или S, или NR9, где R9 представляет собой атом водорода (Н), С1-4алкил или С1-4фторалкил; ни один из, один, два или три из J, L, М и Q представляют собой атом азота; и остальные из J, L, М и Q представляют собой СН или CR6, где R6 независимо от любого другого присутствующего R6 является таким, как определено здесь;
либо R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, или -С(O)-(СН2)p 2-, или -(СН2)p 3-Х5-(СН2)p 4-, или -С(O)-Х5-(СН2)p 5-, где: р1 равно 3, 4, 5 или 6 (предпочтительно р=4 или 5), р2 равно 2, 3, 4 или 5 (предпочтительно р2 равно 2, 3 или 4), и р3, и р4, и р5 независимо равны 2 или 3 (независимо предпочтительно 2), и X5 представляет собой О или NR17;
и где, когда R4 и R5, взятые вместе, представляют собой -(СН2)p 1- или -С(O)-(СН2)p 2-, гетероцикл NR4R5 возможно замещен одним заместителем R18, где R18 представляет собой: С1-4алкил (например, С1-2алкил); С1-2фторалкил; С3-6циклоалкил; С1-2алкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); С1фторалкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); ОН (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); -(СН2)p 7-C(O)R16, где р7 равно 0, 1, 2 или 3 (предпочтительно р7 равно 0 или 1); -(CH2)p 7-C(O)OR16; -(CH2)p 7-OC(O)R16; -(CH2)p 7-C(O)NR12R13; -(CH2)p 7-NR15C(O)R16; -(CH2)p 7-NR15C(O)NR12R13; -(CH2)p 7-NR15C(O)OR16; -(CH2)p 7-SO2R16; -(CH2)p 7-SO2NR12R13; -(CH2)p 7-NR15SO2R16; -(CH2)p 7-ОН; -(CH2)p 7-OR16; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, либо -С(O)-(СН2)p 2-, либо -(CH2)p 3-Х5-(CH2)p 4-, либо -С(O)-Х5-(CH2)p 5-, как определено здесь, и где гетероцикл NR4R5 конденсирован с фенольным кольцом, возможно замещенным на фениле одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси, и
R5a представляет собой С1-8алкил, С1-8фторалкил, С3-8циклоалкил; -(СН2)n 4a-С3-8циклоалкил, где n4a равно 1 или 2; фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5a имеет подформулу (х), (y) или (z), как определено здесь, и где:
R12 и R13 независимо представляют собой Н; С1-5алкил (например, C1-3алкил); С3-6циклоалкил или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R12 и R13 вместе представляют собой -(СН2)n 6-, либо -C(O)-(CH2)n 7-, либо -C(O)-(CH2)n 7-C(O)-, либо -(CH2)n 8-X12-(CH2)n 9-, либо -С(O)-Х12-(CH2)n 10-, где n6 равно 3, 4, 5 или 6 (предпочтительно n6 равно 4 или 5), n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3 (независимо предпочтительно 2), и X12 представляет собой О или NR14a, где R14a представляет собой Н, С1-2алкил или С(O)Ме (предпочтительно Н или С1-2алкил);
R15 представляет собой атом водорода (Н); С1-4алкил (например, tBu (трет-бутил) или С1-2алкил, например метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
R15a, независимо от другого R15a, представляет собой атом водорода (Н) или С1-4алкил (например, Н, tBu или С1-2алкил, такой как метил; предпочтительно R15a представляет собой Н или С1-2алкил, более предпочтительно Н);
R16 и R16a независимо представляют собой:
С1-6алкил (например, С1-4алкил или С1-2алкил);
С3-6циклоалкил (например, С5-6циклоалкил), возможно замещенный одним оксо (=O), ОН или С1-2алкильным заместителем (например, возможно замещенный по 3-му или 4-му положению С5-6циклоалкильного кольца; и/или предпочтительно незамещенный С3-6циклоалкил);
С3-6циклоалкил-СН2- (например, С5-6циклоалкил-СН2-);
пиридинил (например, пиридин-2-ил), возможно замещенный на кольцевом атоме углерода одним из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
Ar5c;
фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
бензил, возможно замещенный по ароматическому атому углерода одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; или
4-, 5-, 6- или 7-членное насыщенное гетероциклическое кольцо, соединенное по кольцевому атому углерода и содержащее один или два кольцевых гетероатома, независимо выбранных из О, S и N; где любые кольцевые атомы азота, которые присутствуют, находятся в виде NR27, где R27 представляет собой Н, С1-2алкил или -С(O)Ме; и где это кольцо возможно замещено по атому углерода одним С1-2алкильным или оксо (=O) заместителем, при условии, что любой оксо (=O) заместитель является заместителем по кольцевому атому углерода, связанному с кольцевым атомом азота;
где Ar5a, Ar5b и Ar5c независимо представляет/(ют) собой 5-членное ароматическое гетероциклическое кольцо, содержащее один О, S или NR15a в этом 5-членном кольце, где 5-членное кольцо возможно может дополнительно содержать один или два атома N, и где это гетероциклическое кольцо возможно замещено по кольцевому атому углерода одним из: атома галогена, С1-2алкила, С1фторалкила, -СН2OH, -СН2-ОС1-2алкил, ОН (включая его кето-таутомер) или -CH2-NR28R29, где R28 и R29 независимо представляют собой Н или метил;
и R17 представляет собой атом водорода (Н); С1-4алкил (например, С1-2алкил); С1-2фторалкил; С3-6циклоалкил; -(CH2)p 6-C(O)R16, где р6 равно 0, 1, 2 или 3 (предпочтительно р6 равно 0); -(CH2)p 6-C(O)NR12R13; -(CH2)p 6-C(O)OR16; -(CH2)p 6-C(O)OH; -SO2R16; -C(O)-CH2-NR12R13; -С(O)-CH2-NR15a-С(O)-С1-3алкил; -С(O)-СН2-O-С1-3алкил; либо фенил или бензил, где фенил или бензил возможно замещены по ароматическому атому углерода одним или двумя из: атома галогена,
С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
R19 представляет собой С1-4алкил; -(CH2)n 20-OR20, где n20 равно 1, 2, 3 или 4, и R20 представляет собой атом водорода (Н) или С1-4алкил; -СН(Ме)-ОН; -CH2-SH;
-CH2-CH2-S-Me; бензил; или (4-гидроксифенил)метил (то есть 4-гидроксибензил); и
R30, независимо от другого R30, представляет собой атом водорода (Н), С1-4алкил или С3-6циклоалкил; и
Het1, независимо от другого Het1, представляет собой 4-, 5-, 6- или 7-членное насыщенное гетероциклическое кольцо, соединенное по кольцевому атому углерода и содержащее один или два кольцевых гетероатома, независимо выбранных из О, S и N; где любые кольцевые атомы азота, которые присутствуют, находятся в виде NR31, где R31 представляет собой Н, С1-2алкил или -С(O)Ме; и где это кольцо возможно замещено по атому углерода одним С1-2алкильным или оксо (=O) заместителем, при условии, что любой оксо (=O) заместитель является заместителем по кольцевому атому углерода, связанному с кольцевым атомом азота;
при условии, что:
когда R3 представляет собой гетероциклическую группу подформулы (bb), n1 равно 1 и Y представляет собой NR10, тогда:
либо (а) R10 не является С1-2алкилом, С1-2фторалкилом или СН2С(O)NH2;
либо (б) R10 представляет собой метил, и соединение представляет собой: 1-этил-N-(2-этилбутил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид или 1-этил-N-(4-фторфенил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид.
Предпочтительно, где Х представляет собой OR5a, это соединение является иным чем соединение, где R1 представляет собой метил, Х представляет собой OEt и R3 представляет собой циклопентил.
В одном возможном воплощении изобретения R1 представляет собой С1-4алкил или С1-2фторалкил.
Альтернативно или дополнительно в одном возможном воплощении данного изобретения R2 представляет собой атом водорода (Н).
Альтернативно или дополнительно в одном возможном воплощении изобретения R3 представляет собой С3-8циклоалкил или гетероциклическую группу, представляющую собой 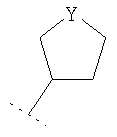 или
или 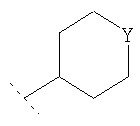 , где Y представляет собой О, S, SO2 или NR10, где R10 представляет собой водород, С1-4алкил, С1-2фторалкил, С(O)-С1-2алкил или С(O)-CF3;
, где Y представляет собой О, S, SO2 или NR10, где R10 представляет собой водород, С1-4алкил, С1-2фторалкил, С(O)-С1-2алкил или С(O)-CF3;
и где в R3 С3-8циклоалкил или гетероциклическая группа возможно замещены одним или двумя заместителями, представляющими собой ОН, С1-2алкокси, триметокси или С1-2алкил; и где любой ОН, алкокси или триметокси заместитель не является заместителем по (R3) кольцевому атому углерода, соединенному (связанному) с -NH- группой формулы (I), и не является заместителем по любому (R3) кольцевому атому углерода, связанному с Y группой гетероциклической группы.
Альтернативно или дополнительно в одном возможном воплощении изобретения R4 представляет собой водород, С1-2алкил или С1-2фторалкил.
Альтернативно или дополнительно в одном возможном воплощении изобретения R5 представляет собой водород, С1-8алкил, С1-8фторалкил или С3-8циклоалкил; либо фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5 имеет подформулу (х), (у) или (z):


 ,
,
где в подформуле (х) n=1 или 2; в подформуле (y) m=1 или 2; и в подформуле (z) r=1 или 2;
где в подформуле (х) и (y) ни один из, один или два из А, В, D, Е и F представляют собой атом азота, а остальные из А, В, D, Е и F представляют собой СН или CR6, где R6 представляет собой атом галогена, С1-4алкил, С1-4фторалкил, С1-2алкокси, С1-2фторалкокси, С1-2алкилсульфонил (С1-2алкил-SO2-), С1-2алкил-SO2-NH-, R7R8N-SO2-, R7R8N-CO-, R7R8N, ОН, С1-4алкоксиметил или С1-2алкил-SO2-CH2-, где R7 и R8 независимо представляют собой водород или С1-2алкил;
где в подформуле (z) G представляет собой О или S или NR9, где R9 представляет собой С1-4алкил или С1-4фторалкил; ни один из, один или два из J, L, М и Q представляют собой атом азота; а остальные из J, L, М и Q представляют собой СН или CR6, где R6 является таким, как определено здесь.
В качестве альтернативы к указанным выше возможным воплощениям R4 и/или R5, в одном возможном воплощении изобретения R4 и/или R5, взятые вместе, могут представлять собой -(СН2)p 1-, где р1 равно 3, 4 или 5 (предпочтительно р1=4 или 5).
В одном возможном воплощении изобретения R3 представляет собой возможно замещенный С3-8циклоалкил или возможно замещенную гетероциклическую группу подформулы (аа), (bb) или (cc):
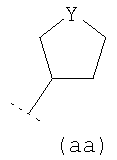 или
или 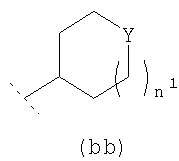 или
или 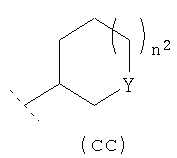 ,
,
где n1 и n2 независимо равно 1 или 2; и где Y представляет собой О, S, SO2 или NR10; где R10 представляет собой атом водорода (Н), С1-4алкил (например, метил или этил),
С1-2фторалкил, CH2C(O)NH2, C(O)NH2, С(O)-С1-2алкил или С(O)-С1фторалкил;
и где в R3 С3-8циклоалкильная или гетероциклическая группа подформулы (аа), (bb) или (cc) возможно замещена одним или двумя заместителями, представляющими собой оксо (=O), ОН, С1-2алкокси, C1-2фторалкокси (например, трифторметокси) или С1-2алкил; и где любой ОН, алкокси или фторалкокси заместитель не является заместителем по атому углерода кольца R3, соединенному (связанному) с -NH- группой формулы (I), и не является заместителем по любому атому углерода кольца R3, связанному с Y группой гетероциклической группы (аа), (bb) или (cc).
Альтернативно или дополнительно к указанному выше возможному определению
R3 в одном возможном воплощении изобретения Х представляет собой NR4R5 или OR5a, где
R4 представляет собой атом водорода (Н); С1-6алкил; С1-3фторалкил или С2-6алкил, замещенный одним заместителем R11; и
R5 представляет собой атом водорода (Н); С1-8алкил; С1-8фторалкил; С3-8циклоалкил, возможно замещенный С1-2алкильной группой; либо -(CH2)n 4-С3-8циклоалкил, возможно замещенный в группировке -(СН2)n 4-или в С3-8циклоалкильной группировке С1-2алкильной группой, где n4 равно 1, 2 или 3;
либо R5 представляет собой С2-6алкил, замещенный одним или двумя независимыми заместителями R11;
где каждый заместитель R11, независимо от любого другого присутствующего заместителя R11, представляет собой: гидрокси (ОН); С1-6алкокси; фенилокси; бензилокси; -NR12R13; -NR15-C(O)R16; -NR15-C(O)CO-O-R16; -NR15-C(O)-NH-R15 или -NR15-SO2R16; и где любой заместитель R11, который представляет собой ОН, алкокси или -NR12R13, не является заместителем по любому атому углерода любого R4 или R5 замещенного алкила, который связан с атомом азота из NR4R5;
либо R5 представляет собой -(CH2)n 11-C(O)R16; -(CH2)n 12-C(O)NR12R13; -CHR19-C(O)NR12R13; -(CH2)n 12-C(O)OR16; -CHR19-C(O)OR16; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN; где n11 равно 0, 1, 2, 3 или 4 и n12 равно 1, 2, 3 или 4;
либо R5 представляет собой -(CH2)n 13-Het, где n13 равно 0, 1, 2, 3 или 4, а Het представляет собой 4-, 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один или два кольцевых гетероатома, независимо выбранных из О, S и N; где любые присутствующие кольцевые гетероатомы не связаны с группировкой -(СН2)n 13-, когда n13 равно 1, и не связаны с атомом азота из NR4R5, когда n13 равно 0; где любые кольцевые атомы азота, которые присутствуют и которые не являются ненасыщенными (то есть которые не задействованы в двойной связи), присутствуют в виде NR17, где R17 такой, как определен здесь; и где один или два из кольцевых атомов углерода возможно независимо замещены С1-2алкилом;
либо R5 представляет собой фенил, возможно замещенный одним или двумя из: атома галогена; С1-4алкила (например, С1-2алкила); С1-2фторалкила (например, трифторметила); С1-2алкокси (например, С1-2алкокси); С1-2фторалкокси (например, трифторметокси); С1-2алкилсульфонила (С1-2алкил-SO2-); С1-2алкил-SO2-NH-; R7R8N-S(O)2-; R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметила; С1-4алкоксиэтила; С1-2алкил-S(O)2-СН2-; циано (CN); или фенила, возможно замещенного одним или двумя из фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
где R7 и R8 независимо представляют собой атом водорода (Н); С1-4алкил (например, С1-2алкил, такой как метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; либо R7 и R8 вместе представляют собой -(СН2)n 6-, либо -C(O)-(CH2)n 7-, либо -C(O)-(CH2)n 7-C(O)-, либо -(CH2)n 8-X7-(CH2)n 9-, либо -C(O)-X7-(CH2)n 10-, где: n6 равно 3, 4, 5 или 6, n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3, и X7 представляет собой О или NR14, где R14 представляет собой Н или С1-2алкил;
либо R5 имеет подформулу (х), (y) или (z):


 ,
,
где в подформуле (x) n=1 или 2; в подформуле (y) m=1 или 2; и в подформуле (z) r=0, 1 или 2;
где в подформуле (x) и (y) ни один из, один или два из А, В, D, Е и F представляют собой атом азота, а остальные из А, В, D, Е и F независимо представляют собой СН или CR6;
где R6 представляет собой атом галогена; С1-4алкил (например, С1-2алкил); С1-4фторалкил (например, С1-2фторалкил); С1-4алкокси (например, С1-2алкокси); С1-2фторалкокси; С1-2алкилсульфонил (С1-2алкил-SO2-); С1-1алкил-SO2-NH-; R7R8N-SO2-; R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметил; С1-4алкоксиэтил; С1-2алкил-S(O)2-СН2-; циано (CN); или фенил, возможно замещенный одним или двумя из фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; где R7 и R8 такие, как определено здесь;
где в подформуле (z) G представляет собой О, или S, или NR9, где R9 представляет собой атом водорода (Н), С1-4алкил или С1-4фторалкил; ни один из, один, два или три из J, L, М и Q представляют собой атом азота, а остальные из J, L, М и Q представляют собой СН или CR6, где R6 такой, как определено здесь;
или R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, либо -С(O)-(СН2)p 2-, либо -(CH2)p 3-X5-(CH2)p 4-, либо -С(O)-Х5-(CH2)p 5-, где: р1 равно 3, 4, 5 или 6 (предпочтительно р=4 или 5), р2 равно 2, 3, 4 или 5 (предпочтительно р2 равно 2, 3 или 4), и р3 и р4 и р5 независимо равны 2 или 3 (предпочтительно независимо 2), и X5 представляет собой О или NR17;
где R17 представляет собой атом водорода (Н); С1-4алкил (например, С1-2алкил);
С1-2фторалкил; С3-6циклоалкил; -(CH2)p 6-C(O)R16, где р6 равно 0, 1, 2 или 3 (предпочтительно р6 равно 0); -(CH2)p 6-C(O)NR12R13; -(CH2)p 6-C(O)OR16; -SO2R16; либо фенил или бензил, где фенил или бензил возможно замещены по ароматическому атому углерода одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
и где, когда R4 и R5, взятые вместе, представляют собой -(СН2)p 1- или -С(O)-(СН2)p 2-, гетероцикл NR4R5 возможно замещен одним заместителем R18, где R18 представляет собой: С1-4алкил (например, С1-2алкил); С1-2фторалкил; С3-6циклоалкил; С1-2алкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); С1фторалкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); ОН (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); -(CH2)p 7-C(O)R16, где р7 равно 0, 1, 2 или 3 (предпочтительно р7 равно 0 или 1); -(CH2)p 7-C(O)OR16; -(CH2)p 7-OC(O)R16; -(CH2)p 7-C(O)ONR12R13; -(CH2)p 7-NR15C(O)R16; -(CH2)p 7-NR15C(O)NR12R13; -(CH2)p 7-NR15C(O)OR16; -(CH2)p 7-SO2R16; -(CH2)p 7-SO2NR12R13; -(CH2)p 7-NR15SO2R16; -(CH2)p 7-OH; -(CH2)p 7-OR16; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R4 и R5, взятые вместе, представляют собой -(CH2)p 1-, либо -С(O)-(СН2)p 2-, либо -(CH2)p 3-Х5-(СН2)р4-, либо -C(O)-X5-(CH2)p 5-, как определено здесь, и где гетероцикл NR4R5 конденсирован с фенильным кольцом, возможно замещенным на фениле одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; и
R5a представляет собой С1-8алкил, С1-8фторалкил, С3-8циклоалкил; фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5a имеет подформулу (х), (y) или (z), как определено здесь,
и где:
R12 и R13 независимо представляют собой Н; С1-5алкил (например, C1-3алкил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R12 и R13 вместе представляют собой -(СН2)n 6-, либо -C(O)-(CH2)n 7-, либо -C(O)-(CH2)n 7-C(O)-, либо -(CH2)n 8-X12-(CH2)n 9-, либо -C(O)-X12-(CH2)n 10-, где: n6 равно 3, 4, 5 или 6 (предпочтительно n6 равно 4 или 5), n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3 (предпочтительно независимо 2), и X12 представляет собой О или NR14a, где R14a представляет собой Н или С1-2алкил;
R15 представляет собой атом водорода (Н); С1-4алкил (например, tBu или С1-2алкил, например метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
R16 представляет собой С1-4алкил (например, С1-2алкил); С3-6циклоалкил; пиридинил (например, пиридин-2-ил); или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; и
R19 представляет собой С1-4алкил; -(CH2)n 20-OR20, где n20 равно 1, 2, 3 или 4, и R20 представляет собой атом водорода (Н) или С1-4алкил; -СН(Ме)-ОН; -CH2-SH;
-CH2-CH2-S-Me; бензил или (4-гидроксифенил)метил (то есть 4-гидроксибензил).
В соединениях, например в соединениях формулы (I) (или формулы (IA), или формулы (IB), см. ниже), "алкильная" группа или группировка может быть прямой или разветвленной. Алкильные группы, например С1-8алкил, либо C1-6алкил, либо С1-4алкил, либо С1-3алкил, либо С1-2алкил, которые могут быть использованы, включают С1-6алкил, либо С1-4алкил, либо С1-3алкил, либо С1-2алкил, такие как метил, этил, н-пропил, н-бутил, н-пентил или н-гексил или их любые разветвленные изомеры, такие как изопропил, трет-бутил, втор-бутил, изобутил, 3-метилбутан-2-ил, 2-этилбутан-1-ил или подобные.
Соответствующее значение подразумевается для "алкокси", "алкилена" и подобных терминов, производных от алкила. Например, "алкокси", такой как С1-6алкокси, либо С1-4алкокси, либо С1-2алкокси, включают метокси, этокси, пропилокси и оксипроизводные от алкилов, перечисленных выше. "Алкилсульфонил", такой как С1-4алкилсульфонил, включает метилсульфонил (метансульфонил), этилсульфонил и другие производные алкилов, перечисленных выше. "Алкилсульфонилокси", такой как С1-4алкилсульфонилокси, включает метансульфонилокси (метилсульфонилокси), этансульфонил и другие.
"Циклоалкил", например С3-8циклоалкил, включает циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и подобные. Предпочтительно
С3-8циклоалкильная группа представляет собой С3-6циклоалкил или С5-6циклоалкил, то есть содержит 3-6-членное или 5-6-членное карбоциклическое кольцо.
"Фторалкил" включает алкильные группы с одним, двумя, тремя, четырьмя, пятью или более заместителями фторо, например С1-4фторалкил, либо С1-3фторалкил, либо
С1-2фторалкил, такой как монофторметил, дифторметил, трифторметил, пентафторэтил, 2,2,2-трифторэтил(CF3СН2-), 2,2-дифторэтил(CHF2CH2-), 2-фторэтил(CH2FCH2-) и т.д. "Фторалкокси" включает С1-4фторалкокси или С1-2фторалкокси, такой как трифторметокси, пентафторэтокси, монофторметокси, дифторметокси и т.д. "Фторалкилсульфонил", такой как С1-4фторалкилсульфонил, включает трифторметансульфонил, пентафторэтилсульфонил и т.д.
Атом галогена ("галогено"), присутствующий в соединениях, например в соединениях формулы (I), может представлять собой атом фтора, хлора, брома или йода ("фторо", "хлоро", "бромо" или "йодо").
Когда в описании указано, что атом или группировка А "связаны" или "соединены" с атомом или группировкой В, это означает, что атом/группировка А непосредственно связана с атомом/группировкой В, обычно посредством одной или более ковалентных связей, и исключает А, непрямо присоединенную к В посредством одного или более промежуточных атомов/группировок (например, исключает А-С-В), если из контекста не ясно, что подразумевается другое значение.
Предпочтительно R1 представляет собой С1-4алкил (например, метил, этил, н-пропил, изопропил или н-бутил), C1-3фторалкил или -СН2СН2OH; R1 более предпочтительно представляет собой C1-3алкил (например, метил, этил или н-пропил), С1-2фторалкил или -СН2СН2OH; еще более предпочтительно C1-3алкил, С1-2фторалкил или -CH2CH2OH, такие как метил, этил, н-пропил или -СН2СН2OH. Еще более предпочтительно R1 представляет собой С2-3алкил (например, этил или н-пропил), С2фторалкил (например, С1фторалкил-CH2-, такой как CF3-СН2-) или -СН2СН2OH; в частности этил, н-пропил или -СН2СН2OH. R1 наиболее предпочтительно представляет собой этил.
Предпочтительно R2 представляет собой атом водорода (Н) или метил, более предпочтительно атом водорода (Н).
Предпочтительно в R3 есть один заместитель или нет заместителей.
В одном возможном воплощении R3 представляет собой возможно замещенный
С3-8циклоалкил или возможно замещенную гетероциклическую группу подформулы (аа), (bb) или (cc). В данном воплощении, возможно, в R3 С3-8циклоалкильная или гетероциклическая группа подформулы (аа), (bb) или (сс) возможно замещена одним или двумя заместителями, независимо представляющими собой (например, представляющими собой) оксо (=O), ОН, С1-2алкокси, С1-2фторалкокси (например, трифторметокси) или С1-2алкил; и где любой ОН, алкокси или фторалкокси заместитель не является заместителем по атому углерода кольца R3, соединенному (связанному) с -NH- группой формулы (I) и не является заместителем по любому кольцевому атому углерода R3, связанному с Y группой гетероциклической группы (аа), (bb) или (cc).
В одном возможном воплощении, где R3 представляет собой возможно замещенный С3-8циклоалкил, он не является возможно замещенным С5циклоалкилом, то есть не является возможно замещенным циклопентилом. В данном случае более предпочтительно R3 представляет собой возможно замещенный
С6-8циклоалкил.
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, более предпочтительно он представляет собой возможно замещенный С6циклоалкил (то есть циклогексил); например С6циклоалкил, возможно замещенный одним или двумя заместителями, независимо представляющими собой (например, представляющими собой) оксо (=O), ОН, C1-2алкокси, С1-2фторалкокси (например, трифторметокси) или С1-2алкил; и где любой ОН, алкокси или фторалкокси заместитель не является заместителем по атому углерода кольца R3, соединенному (связанному) с -NH- группой формулы (I).
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, один или два возможные заместителя предпочтительно включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) оксо (=O); ОН; С1алкокси; С1фторалкокси (например, трифторметокси); NHR21, где R21 представляет собой атом водорода (Н) или С1-2алкил с прямой цепью; С1-2алкил, такой как метил; С1фторалкил, такой как -CH2F или -CHF2; -СН2OH; -CH2NHR22, где R22 представляет собой Н; -C(O)OR23, где R23 представляет собой Н или метил; -C(O)NHR24, где R24 представляет собой Н или метил; -C(O)R25, где R25 представляет собой метил; фторо; гидроксиимино (=N-OH) или (С1-2алкокси)имино (=N-OR26, где R26 представляет собой С1-2алкил); и где любой ОН, алкокси, фторалкокси или NHR21 заместитель не является заместителем по кольцевому атому углерода R3, соединенному (связанному) с -NH-группой формулы (I) и не является заместителем по любому кольцевому атому углерода R3, связанному с группой Y гетероциклической группы (аа), (bb) или (cc).
Более предпочтительно, когда R3 представляет собой возможно замещенный С3-8циклоалкил, один или два возможные заместителя включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) оксо (=O); ОН; NHR21, где R21 представляет собой атом водорода (Н); С1-2алкил, такой как метил; С1фторалкил, такой как -CH2F или -CHF2; -C(O)OR23, где R23 представляет собой Н или метил; -C(O)NHR24, где R24 представляет собой Н или метил; фторо; гидроксиимино (=N-OH) или (С1-2алкокси)имино (=N-OR26, где R26 представляет собой С1-2алкил).
Еще более предпочтительно, когда R3 представляет собой возможно замещенный
С3-8циклоалкил, один или два возможных заместителя включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) оксо (=O); ОН; NHR21, где R21 представляет собой атом водорода (Н); метил; -CH2F; -CHF2; -C(O)OR23, где R23 представляет собой Н; фторо; гидроксиимино (=N-ОН) или (С1-2алкокси)имино (=N-OR26, где R26 представляет собой С1-2алкил). Еще более предпочтительно, когда R3 представляет собой возможно замещенный С3-8циклоалкил, один или два возможных заместителя включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) оксо (=O); ОН; метил; фторо; гидроксиимино (=N-ОН) или (С1-2алкокси)имино (=N-OR26, где R26 представляет собой С1-2алкил).
Наиболее предпочтительно, когда R3 представляет собой возможно замещенный
С3-8циклоалкил, один или два возможные заместителя включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) ОН; оксо (=O) или оксимо (=N-ОН). Например, один или два возможных заместителя могут включать в себя (например, представляет собой или представляют собой) ОН и/или оксо (=O).
Возможно в R3 С3-8циклоалкил может быть незамещенным.
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, например возможно замещенный С5-8циклоалкил, такой как возможно замещенный С6циклоалкил (возможно замещенный циклогексил), один или два возможные заместителя, если они присутствуют, предпочтительно включают в себя заместитель (например, представляет собой заместитель или представляют собой заместители) по
3-, 4- или 5-положению(ям) циклоалкильного кольца R3. (В связи с этим положение 1 циклоалкильного кольца R3 считается точкой присоединения с -NH- в формуле (I)).
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, любой ОН, алкокси, фторалкокси, -CH2OH, -CH2CH2OH, -CH2NHR22, -C(O)OR23, -C(O)NHR24, -C(O)R25 или фторо заместитель (в частности, любой ОН заместитель) более предпочтительно находится в 3-м, 4-м или 5-м положении, например в 3-м или 5-м положении, циклоалкильного (например, С6-8циклоалкильного) кольца R3. Например, любой ОН, алкокси, фторалкокси, -СН2OH, -CH2CH2OH, -CH2NHR22, -C(O)OR23, -C(O)NHR24, -C(O)R25 или фторо заместитель (в частности, любой ОН заместитель) может находиться в 3-м положении С6циклоалкильного (циклопентильного) кольца R3 или в 3-м, 4-м или 5-м положении, например в 3-м или 5-м положении С6циклоалкильного (циклогексильного) кольца R3. (В связи с этим, а также ниже, положение 1 циклоалкильного кольца R3 считается точкой присоединения к -NH- в формуле (I)).
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, любой заместитель NHR21 предпочтительно находится в 2-, 3-, 4- или 5-м положении, например в 2- или 3-м положении или более предпочтительно в 3-м положении, циклоалкильного (например, С6-8циклоалкильного, например циклогексильного) кольца R3.
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, любой алкильный или фторалкильный заместитель предпочтительно находится в 1-, 2-, 3-, 4- или 5-м положении, более предпочтительно в 1-, 2-, 3- или 5-м положении, еще более предпочтительно в 1- или 3-м положении циклоалкильного (например, С6-8циклоалкильного, например циклогексильного) кольца R3.
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, любой оксо (=O), гидроксиимино (=N-ОН) или (С1-4алкокси)имино (=N-OR26) заместитель предпочтительно находится в 3- или 4-м положении, предпочтительно в 4-м положении циклоалкильного (например, С6-8циклоалкильного, например циклогексильного) кольца R3.
Когда R3 представляет собой возможно замещенный С3-8циклоалкил, R3 предпочтительно представляет собой циклогексил (то есть незамещенный), или циклогексил, замещенный одним оксо (=O), ОН, NHR21, С1-2алкильным, С1-2фторалкильным, -СН2OH, -C(O)OR23, -C(O)NHR24, -C(O)R25, фторо, гидроксиимино (=N-OH), (С1-2алкокси)имино (=N-OR26) заместителем, или циклогексил, замещенный двумя заместителями фторо. Более предпочтительно R3 представляет собой циклогексил (то есть незамещенный), или циклогексил, замещенный одним оксо (=O), ОН, NHR21, С1-2алкильным, С1-2фторалкильным, -C(O)OR23, фторо, гидроксиимино (=N-OH) или (С1-2алкокси)имино (=N-OR26) заместителем, или циклогексил, замещенный двумя заместителями фторо. Еще более предпочтительно R3 представляет собой циклогексил (то есть незамещенный), или циклогексил, замещенный одним оксо (=O), гидроксиимино (=N-ОН), С1-2алкильным или ОН заместителем. Возможный заместитель может находиться в 3-м или 4-м положении, например в 3-м положении циклогексильного кольца R3; более предпочтительно любой ОН заместитель предпочтительно находится в 3-м положении циклогексильного кольца R3, и/или любой оксо (=O), гидроксиимино (=N-ОН) или (С1-2алкокси)имино (=N-OR26) заместитель предпочтительно находится в 4-м положении циклогексильного кольца R3.
Когда R3 представляет собой возможно замещенный С6циклоалкил, R3 может представлять собой, например, 4-гидрокси-циклогексил (то есть 4-гидроксициклогексан-1-ил), но более предпочтительно R3 представляет собой циклогексил (то есть незамещенный), 3-гидрокси-циклогексил (то есть 3-гидроксициклогексан-1-ил), 4-оксо-циклогексил (то есть 4-оксоциклогексан-1-ил), 4-(гидроксиимино)циклогексил (то есть 4-(гидроксиимино)циклогексан-1-ил), 4-(С1-2алкоксиимино)циклогексил, 1-метилциклогексил или 3-метилциклогексил. Когда R3 представляет собой возможно замещенный С6циклоалкил, R3 наиболее предпочтительно представляет собой циклогексил (то есть незамещенный), 4-оксо-циклогексил (то есть 4-оксоциклогексан-1-ил) или 4-(гидроксиимино)циклогексил (то есть 4-(гидроксиимино)циклогексан-1-ил).
Когда R3 представляет собой возможно замещенный С5циклоалкил (возможно замещенный циклопентил), R3 может, например, представлять собой циклопентил (то есть незамещенный) или 3-гидрокси-циклопентил.
Когда R3 представляет собой возможно замещенный мононенасыщенный С5-7циклоалкенил, предпочтительно он представляет собой возможно замещенный мононенасыщенный С5-6циклоалкенил, более предпочтительно возможно замещенный мононенасыщенный С6циклоалкенил (то есть возможно замещенный мононенасыщенный циклогексенил = возможно замещенный циклогексенил). Еще более предпочтительно R3 циклогексенил представляет собой возможно замещенный циклогекс-3-ен-1-ил.
Когда R3 представляет собой возможно замещенный мононенасыщенный С5-7циклоалкенил, предпочтительно R3 циклоалкенил возможно замещен одним или двумя заместителями, представляющими собой фторо или метил, при условии, что, если присутсвуют два заместителя, тогда они оба не являются метилом.
Предпочтительно R3 циклоалкенил возможно замещен одним заместителем, представляющим собой фторо или С1-2алкил (например, метил); более предпочтительно R3 циклоалкенил замещен одним заместителем фторо или незамещен. Для R3 циклоалкенила возможный(е) заместитель(и) может(гут) находиться в 1-, 2-, 3-, 4- или 5-м положении(ях) циклоалкенильного кольца.
Когда R3 представляет собой гетероциклическую группу подформулы (аа), (bb) или (сс), тогда Y предпочтительно представляет собой О, S, SO2, NH или N-С(O)метил, более предпочтительно О, NH или N-С(O)метил, еще более предпочтительно О или N-С(O)метил, наиболее предпочтительно О. (Когда Y представляет собой NH или N-С(O)метил, тогда R10 представляет собой Н или С(О)метил.)
Предпочтительно R10 представляет собой атом водорода (Н), метил, этил, C(O)NH2, С(O)метил или С(O)-CF3. Возможно, R10 может представлять собой атом водорода (Н), метил, этил, С(O)метил или С(O)-CF3, более предпочтительно Н, С(O)метил или С(O)-CF3, еще более предпочтительно Н или С(O)метил.
Когда R3 представляет собой гетероциклическую группу подформулы (аа), (bb) или (cc), тогда предпочтительно, чтобы R3 представлял собой гетероциклическую группу подформулы (аа) или (bb), более предпочтительно подформулы (bb).
В подформуле (bb) n1 предпочтительно равно 1. В подформуле (cc) n2 предпочтительно равно 1. Таким образом, шестичленные кольца являются предпочтительными в гетероциклической группе R3.
Приемлемо, чтобы в R3 гетероциклическая группа подформулы (аа), (bb) или (cc) являлась незамещенной. (В связи с этим, когда Y представляет собой NR10, R10 не классифицируется как заместитель.)
В гетероциклической группе R3 подформулы (аа), (bb) или (cc) один или два возможные заместителя предпочтительно включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) ОН; оксо (=O); С1-2алкил (например, метил) или С1-2фторалкил (например, С1фторалкил, такой как -CH2F или -CHF2). Более предпочтительно, в гетероциклической группе R3 подформулы (аа), (bb) или (cc) один или два возможные заместителя включают в себя (например, он представляет собой или они независимо представляют собой (например, представляет собой или представляют собой)) ОН и/или оксо (=O); наиболее предпочтительно, один или два возможные заместителя включают в себя (например, представляет собой или представляют собой) оксо (=O). В гетероциклической группе R3 подформулы (аа), (bb) или (cc) любые оксо (=O) заместители предпочтительно находятся на атоме углерода, связанном (соседним) с Х, и/или могут находиться в 2-, 3-, 4- или 5-м положении(ях) гетероциклической группы R3. (В связи с этим положение 1 гетероциклической группы R3 считается точкой присоединения к -NH- в формуле (I)). Предпочтительно только замещение С1-2алкилом, С1-2фторалкилом, фторо или окси (=O), или отсутствие замещения разрешено в каждом из 2-го и 6-го положений гетероциклического кольца R3.
Когда R3 представляет собой гетероциклическую группу подформулы (аа) и Y представляет собой NR10, тогда предпочтительно R10 не является С(O)-Ме. Более предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (аа) и Y представляет собой NR10, тогда R10 предпочтительно не является C(O)R, то есть или, например, R10 предпочтительно не является C(O)NH2, С(O)-С1-2алкилом или С(O)-С1фторалкилом. В одном воплощении Y представляет собой О, S, SO2 или NH, когда R3 представляет собой гетероциклическую группу подформулы (аа).
Возможно согласно одному воплощению данного изобретения NHR3 не представляет собой 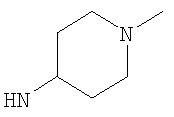 . Более предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (bb) и Y представляет собой NR10 и возможно когда n1 равно 1, тогда предпочтительно R10 не является метилом. Более предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (bb), и Y представляет собой NR10 и возможно когда n1 равно 1, тогда предпочтительно R10 не является алкилом или замещенным алкилом, то есть или, например, R10 предпочтительно не является С1-4алкилом (например, метилом или этилом), С1-2фторалкилом или CH2C(O)NH2. В одном воплощении, когда R3 представляет собой гетероциклическую группу подформулы (bb), Y предпочтительно представляет собой О, S, SO2 или NR10, где R10 представляет собой Н, C(O)NH2, С(O)-С1-2алкил или С(O)-С1фторалкил, или более предпочтительно Y представляет собой Н или С(O)Ме. Более предпочтительно для подформулы (bb) Y представляет собой О или NR10.
. Более предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (bb) и Y представляет собой NR10 и возможно когда n1 равно 1, тогда предпочтительно R10 не является метилом. Более предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (bb), и Y представляет собой NR10 и возможно когда n1 равно 1, тогда предпочтительно R10 не является алкилом или замещенным алкилом, то есть или, например, R10 предпочтительно не является С1-4алкилом (например, метилом или этилом), С1-2фторалкилом или CH2C(O)NH2. В одном воплощении, когда R3 представляет собой гетероциклическую группу подформулы (bb), Y предпочтительно представляет собой О, S, SO2 или NR10, где R10 представляет собой Н, C(O)NH2, С(O)-С1-2алкил или С(O)-С1фторалкил, или более предпочтительно Y представляет собой Н или С(O)Ме. Более предпочтительно для подформулы (bb) Y представляет собой О или NR10.
Когда R3 представляет собой бициклическую группу подформулы (dd) или (ее), предпочтительно он имеет подформулу (ее). В подформуле (ее) предпочтительно Y1,
Y2 и Y3 все представляют собой СН2.
Предпочтительно NHR3 имеет подформулу (а), (а1), (b), (с), (с1), (с2), (с3), (с4), (с5), (с6), (с7), (d), (e), (f), (g), (g1), (g2), (g3), (g4), (h), (i), (j), (k), (k1), (L), (m), (m1), (m2), (m3), (m4), (m5), (n), (o), (o1), (o2), (o3), (o4), (o5), (p), (p1), (p2), (p3), (p4), (p5), (p6), (p7), (p8) или (q):
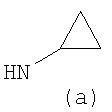
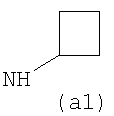
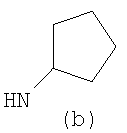
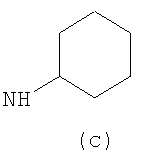
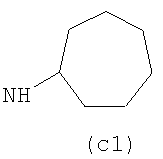
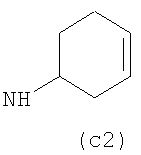
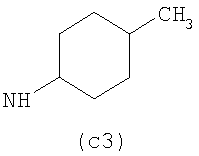
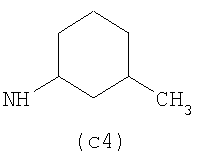
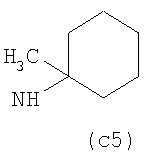
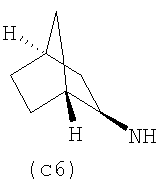
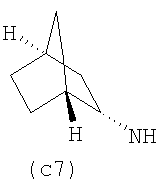
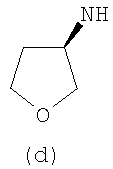
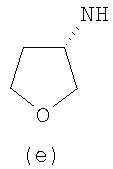
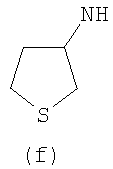
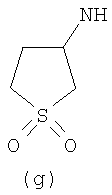
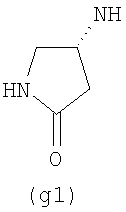
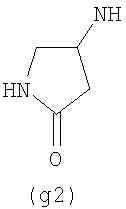
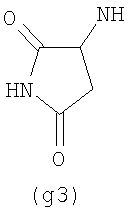
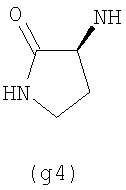
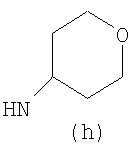
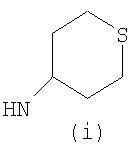
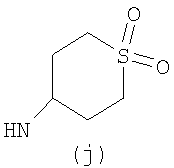
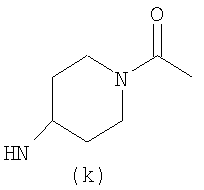
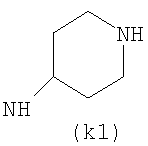
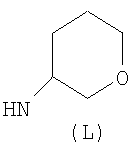
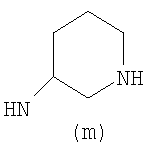
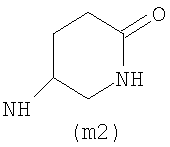
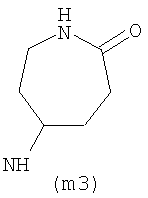
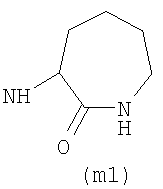
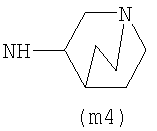
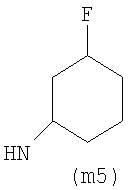
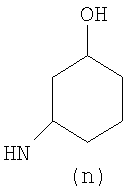
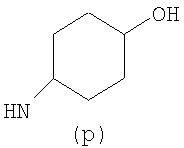
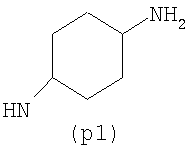
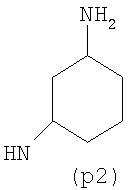
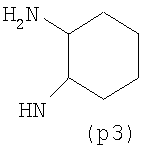
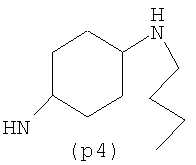
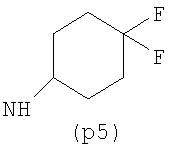
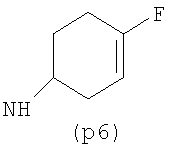
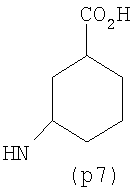
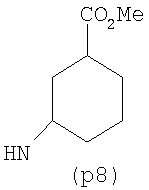
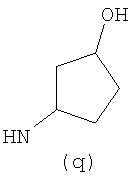
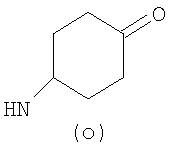
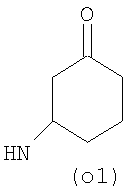
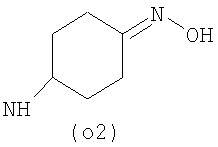
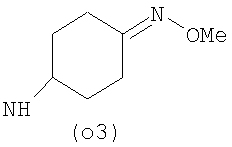
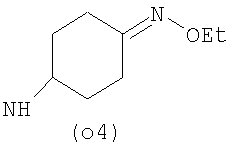
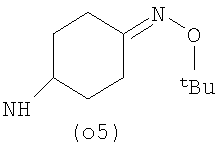
В приведенных выше подформулах (a)-(q) и т.д. точка присоединения -NH- из NHR3 группы к 4-му положению пиразолопиридина формулы (I) подчеркнута.
Предпочтительно NHR3 имеет подформулу (с), (с1), (с2), (с3), (с4), (с5), (с6), (с7), (d), (e), (f), (g1), (g4), (h), (i), (j), (k), (k1), (L), (m), (m1), (m2), (m3), (m5), (n), (o), (o1), (o2), (o3), (o4), (o5), (p), (p2), (p3), (p5), (p6), (p7) или (q). Более предпочтительно NHR3 имеет подформулу (с), (с1), (с4), (с5), (h), (i), (j), (k), (m1), (m2), (n), (о), (o2), (o3), (p2), (p5), (p6) или (q). Еще более предпочтительно NHR3 имеет подформулу (с), (h), (k), (n), (о) или (o2), например (с), (h), (о) или (o2). Наиболее предпочтительно NHR3 представляет собой тетрагидро-2Н-пиран-4-ил; то есть NHR3 наиболее предпочтительно имеет подформулу (h), как показано выше.
Согласно одному воплощению NHR3 имеет подформулу (а), (b), (с), (d), (e), (f), (g), (g1), (g2), (g3), (h), (i), (j), (k), (L), (m), (m1), (n), (о), (o1), (p) или (q). В данном воплощении предпочтительно NHR3 имеет подформулу (с), (d), (e), (f), (g1), (h), (i), (j), (k), (m), (m1), (n), (о), (o1), (p) или (q); и более предпочтительно в данном воплощении NHR3 имеет подформулу (с), (h), (i), (j), (k), (m1), (n), (о) или (q). Еще более предпочтительно в данном воплощении NHR3 имеет подформулу (с), (h), (k), (n) или (о). Наиболее предпочтительно R3 представляет собой тетрагидро-2Н-пиран-4-ил; то есть NHR3 наиболее предпочтительно имеет подформулу (h), как показано выше.
Согласно другому воплощению NHR3 имеет подформулу (а), (b), (с), (d), (e), (f), (g), (h), (i), (j) или (k). В данном воплощении предпочтительно NHR3 имеет подформулу (с), (d), (e), (f), (h), (i), (j) или (k); и более предпочтительно в данном воплощении NHR3 имеет подформулу (с), (h), (i), (j) или (k). Наиболее предпочтительно R3 представляет собой тетрагидро-2Н-пиран-4-ил; то есть NHR3 наиболее предпочтительно имеет подформулу (h), как показано выше.
Когда NHR3 имеет подформулу (n), тогда предпочтительно он представляет собой цис-(3-гидроксициклогекс-1-ил)амино-группу, например в любой энантиомерной форме или смесь форм, но предпочтительно рацемическую.
Предпочтительно Х представляет собой NR4R5.
Когда R4 представляет собой C1-6алкил, тогда предпочтительно он представляет собой С1-4алкил или С1-2алкил. Когда R4 представляет собой С1-3фторалкил, тогда предпочтительно он представляет собой С1-2фторалкил.
Наиболее предпочтительно R4 представляет собой атом водорода (Н).
Когда R4 представляет собой С2-6алкил, замещенный одним заместителем R11, тогда предпочтительно R4 представляет собой С2-4алкил (например, С2-3алкил), замещенный одним заместителем R11. Более предпочтительно R4 представляет собой -(СН2)n 3R11, где n3 равно 2, 3 или 4. Еще более предпочтительно n3 равно 2, и/или R4 представляет собой -(CH2)n 3-OH.
Когда R5 представляет собой С2-6алкил, замещенный одним или двумя независимыми заместителями R11, предпочтительно чтобы R5 представлял собой С2-4алкил (например, С2-3алкил), замещенный одним или двумя независимыми заместителями R11. Когда R5 представляет собой С2-6алкил (например, С2-4алкил или С2-3алкил), замещенный одним или двумя независимыми заместителями R11, предпочтительно, чтобы R5 представлял собой С2-6алкил (например, С2-4алкил или С2-3алкил), замещенный одним заместителем R11. Более предпочтительно, чтобы R5 представлял собой -(CH2)n 5R11, где n5 равно 2, 3 или 4. Предпочтительно n5 равно 2 или 3, более предпочтительно 2.
Предпочтительно каждый заместитель R11, независимо от любого другого присутствующего заместителя R11, представляет собой: гидрокси (ОН); C1-6алкокси (например, С1-4алкокси, такой как трет-бутокси, этокси или метокси); фенилокси; бензилокси; -NR12R13; -NR15-C(O)R16; -NR15-C(O)-NH-R15; или -NR15-SO2R16 (более предпочтительно C1-6алкокси, -NR15-C(O)-NH-R15 или -NR15-SO2R16; наиболее предпочтительно -NR15-SO2R16). Во всех случаях любой заместитель R11, который представляет собой ОН, алкокси или -NR12R13, не является заместителем по любому атому углерода любого замещенного алкила R4 или R5, который связан с атомом азота из NR4R5.
Когда R5 представляет собой С1-8алкил, тогда предпочтительно он представляет собой С1-5алкил или C1-3алкил. Когда R5 представляет собой С1-8фторалкил, тогда предпочтительно он представляет собой C1-3фторалкил или С1-2фторалкил. Когда R5 представляет собой С3-8циклоалкил, возможно замещенный С1-2алкильной группой, тогда предпочтительно С3-8циклоалкил не является замещенным по любому кольцевому атому углерода, связанному с атомом азота из NR4R5. Когда R5 представляет собой возможно замещенный С3-8циклоалкил, тогда более предпочтительно он представляет собой С3-8циклоалкил (то есть незамещенный).
Когда R5 представляет собой возможно замещенный -(СН2)n 4-С3-8циклоалкил, где
n4 равно 1, 2 или 3, тогда n4 предпочтительно равно 1 или 2 или наиболее предпочтительно 1, и/или предпочтительно R5 представляет собой возможно замещенный -(СН2)n 4-С5-6циклоалкил или возможно замещенный -(СН2)n 4-С6циклоалкил. Когда R5 представляет собой возможно замещенный -(СН2)n 4-С3-8циклоалкил, предпочтительно он является незамещенным. Наиболее предпочтительно R5 представляет собой (циклогексил)метил-, то есть -СН2-циклогексил.
Когда R19 представляет собой С1-4алкил, тогда предпочтительно он представляет собой изобутил, втор-бутил или C1-3алкил, такой как метил или изопропил. Когда R19 представляет собой -(CH2)n 20-OR20, тогда предпочтительно n20 равно 1 и/или предпочтительно R20 представляет собой атом водорода (Н).
Когда R5 представляет собой -(CH2)n 11-С(O)R16; -(CH2)n 12-C(O)NR12R13; -CHR19-C(O)NR12R13; -(CH2)n 12-C(O)OR16; -CHR19-C(O)OR16; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN; тогда в одном воплощении данного изобретения R5 может представлять собой: -(CH2)n 11-C(O)R16; -(CH2)n 12-C(O)NR12R13; -(CH2)n 12-C(O)OR16; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN.
Когда R5 представляет собой -(CH2)n 11-С(O)R16; -(CH2)n 12-CONR12R13; -(CH2)n 12-C(O)OR16; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN; тогда R5 может, например, представлять собой: -(CH2)n 11-C(O)COR16; -(CH2)n 12-C(O)NR12R13 или -(CH2)n 12-CN; предпочтительно -(CH2)n 11-C(O)R16.
Предпочтительно n11 равно 1, 2, 3 или 4; более предпочтительно n11 равно 1 или 2. Предпочтительно n12 равно 1 или 2.
Когда R5 представляет собой -(CH2)n 13-Het, предпочтительно, чтобы n13 было равно 0, 1 или 2, более предпочтительно 0 или 1.
Предпочтительно Het представляет собой 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо и/или 4-, 5-, 6- или 7-членное насыщенное гетероциклическое кольцо. Предпочтительно это гетероциклическое кольцо Het содержит один кольцевой гетероатом, выбранный из О, S и N. Предпочтительно кольцевые атомы углерода в Het являются незамещенными. Het наиболее предпочтительно представляет собой один из: 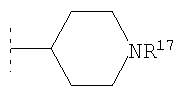 ,
, 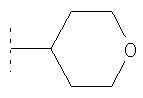 ,
, 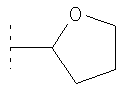 ,
, 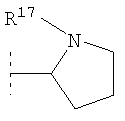 ,
,
 или
или 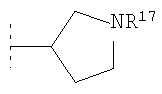 .
.
Когда R5 представляет собой возможно замещенный фенил, тогда предпочтительно он представляет собой фенил, возможно замещенный одним или двумя заместителями, определенными здесь.
Когда R5 представляет собой возможно замещенный фенил, тогда предпочтительно R5 представляет собой фенил, возможно независимо замещенный одним, двумя или тремя (предпочтительно одним или двумя; или одним) из: атома галогена (предпочтительно фторо и/или хлоро); С1-2алкила; С1-2фторалкила (например, трифторметила); С1-2алкокси (например, метокси); трифторметокси; С1-2алкилсульфонила (С1-2алкил-SO2-); С1-2алкил-SO2-NH-; R7R8N-SO2-; R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-2алкоксиметила; С1-2алкил-SO2-СН2-; циано (CN); или фенила, возможно замещенного одним из фторо, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси. Более предпочтительно R5 представляет собой фенил, возможно замещенный одним или двумя (предпочтительно одним) из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси, трифторметокси, R7R8N-SO2-, R7R8N-CO- или С1-2алкил-SO2-СН2-. Когда R5 представляет собой возможно замещенный фенил, тогда предпочтительно один или все из одного или двух возможных заместителей замещены по мета- (3 и/или 5) и/или пара- (4-) положению(ям) фенильного кольца по отношению к атому углерода фенильного кольца, связанному с атомом азота из NR4R5.
Предпочтительно R7 и/или R8 независимо представляют собой атом водорода (Н);
С1-2алкил, такой как метил; С3-6циклоалкил; или фенил, возможно замещенный одним из: фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; либо R7 и R8 вместе представляют собой -(СН2)n 6- или -(CH2)n 8-Х7-(CH2)n 9-, где X7 представляет собой NR14 или предпочтительно О.
Когда R7 представляет собой циклоалкил или возможно замещенный фенил, тогда предпочтительно R8 не является ни циклоалкилом, ни возможно замещенным фенилом.
Наиболее предпочтительно R7 и/или R8 независимо представляют собой атом водорода (Н) или С1-2алкил. Предпочтительно, чтобы R7 представлял собой атом водорода (Н).
Предпочтительно n6 равно 4 или 5. Предпочтительно n7 равно 2, 3 или 4. Предпочтительно n8, n9 и/или n10 независимо равно/равны 2.
В общем случае предпочтительно, чтобы R5 имел подформулу (х), либо (y), либо (y1), либо (z).
Когда R5 имеет подформулу (х), либо (y), либо (y1), либо (z), тогда предпочтительно R5 имеет подформулу (х), либо (y), либо (y1), или имеет подформулу (х), либо (y), либо (z). Более предпочтительно R5 имеет подформулу (х) или (y), наиболее предпочтительно (х). В одном воплощении R5 имеет подформулу (z).
Предпочтительно n равно 1 или 2. Более предпочтительно n=1. Предпочтительно m=1. Предпочтительно r=1 или 2, более предпочтительно 1.
В подформуле (х), (y) и/или (y1) предпочтительно, чтобы ни один из, один или два из А, В, D, Е и F представляли собой атом азота; ни один из, один или два из А, В, D, Е и F представляли собой CR6 и остальные из А, В, D, Е и F представляли собой CH. Более предпочтительно ни один из, один или два из А, В, D, Е и F представляют собой атом азота; ни один из, один или два из А, В, D, Е и F представляют собой CR6 и остальные из А, В, D, Е и F представляют собой СН.
В подформуле (х), (y) и/или (y1) предпочтительно ни один из или один из А, В, D, Е и F представляет собой атом азота и/или предпочтительно ни один из, один или два из А, В, D, Е и F представляют собой CR6.
Предпочтительно подформула (х) представляет собой: бензил; фенетил (Ph-C2H4-); бензил, замещенный на фенильном кольце одним или двумя заместителями R6; фенетил (Ph-С2Н4), замещенный на фенильном кольце одним или двумя заместителями R6; или один из следующих:
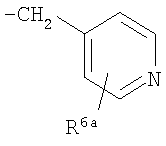
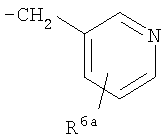
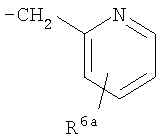
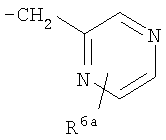
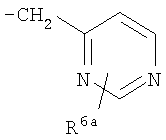
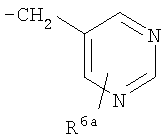 ,
,
где R6a представляет собой либо R6, как определено здесь, либо (предпочтительно) водород.
Наиболее предпочтительно подформула (х) представляет собой бензил или пиридинилметил [например, пиридин-4-илметил (то есть  ), пиридин-3-илметил, или предпочтительно пиридин-2-илметил (то есть
), пиридин-3-илметил, или предпочтительно пиридин-2-илметил (то есть  )].
)].
Предпочтительно подформула (y) представляет собой 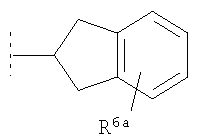 , либо
, либо 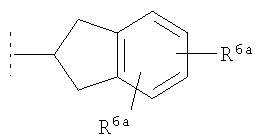 , либо
, либо 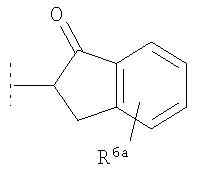 , где R6a представляет собой либо R6, как определено здесь, либо предпочтительно водород. Предпочтительно подформула (y) не замещена оксо (=O) по атому углерода между 6-членным ароматическим кольцом и атомом углерода, связанным с атомом азота из NR4R5.
, где R6a представляет собой либо R6, как определено здесь, либо предпочтительно водород. Предпочтительно подформула (y) не замещена оксо (=O) по атому углерода между 6-членным ароматическим кольцом и атомом углерода, связанным с атомом азота из NR4R5.
Предпочтительно подформула (y1) представляет собой 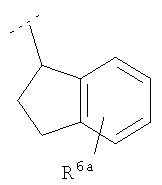 , либо
, либо 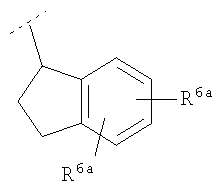 , либо
, либо 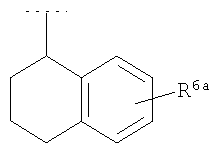 , где R6a представляет собой или независимо представляют собой либо R6, как определено здесь, либо предпочтительно водород.
, где R6a представляет собой или независимо представляют собой либо R6, как определено здесь, либо предпочтительно водород.
Предпочтительно в подформуле (z) ни один из, один или два из J, L, М и Q представляют собой атом азота.
В подформуле (х), (у) и/или (z) предпочтительно каждый R6, независимо от любого другого присутствующего R6, представляет собой: атом фтора, хлора, брома или йода, метил, этил, н-пропил, изопропил, С4алкил, трифторметил, -CH2OH, метокси, этокси, С1фторалкокси (например, трифторметокси или дифторметокси), ОН, С1-3алкилS(O)2- (такой как метилсульфонил, который представляет собой MeS(O)2-), С1-3алкил-SO2-NH-, такой как метил-SO2-NH-, Me2N-S(O)2-, H2N-S(O)2-, -CONH2, -CONHMe, -CO2Н, циано(CN), NMe2, трет-бутоксиметил или С1-3алкилS(O)2-СН2-, такой как метил-SO2-СН2-. Более предпочтительно каждый R6, независимо от любого другого присутствующего R6, представляет собой атом фтора, хлора, брома или йода, метил, этил, н-пропил, изопропил, изобутил, трифторметил,
-CH2OH, метокси, этокси, С1фторалкокси (например, трифторметокси или дифторметокси), С1-3алкилS(O)2-, такой как метилсульфонил, С1-3алкил-SO2-NH-, такой как метил-SO2-NH-, Me2N-S(O)2-, H2N-S(O)2-, -CONH2 или С1-3алкилS(O)2-СН2-, такой как метил-SO2-СН2-. Еще более предпочтительно каждый R6, независимо от любого другого присутствующего R6, представляет собой атом фтора, хлора или брома, метил, этил, н-пропил, изопропил, трифторметил, -СН2OH, метокси, дифторметокси, метилсульфонил, метил-SO2-NH- или метил-SO2-СН2-.
Указанные выше заместители R6 также независимо являются предпочтительными возможными и независимыми заместителями фенила в случае, когда R5 представляет собой возможно замещенный фенил.
В подформуле (х) и/или (y) предпочтительно один, два или три заместителя R6 присутствуют в В, D и/или Е; так что, например, в подформуле (х) один, два или три заместителя R6 находятся в мета- (3- и/или 5-) и/или пара- (4-) положениях по отношению к боковой цепи -(CH2)n-.
Предпочтительно R5 имеет подформулу (х), n равно 1 и ни один из А, В, D, Е и F не является атомом азота или оксидом азота (N+-O-); и все из А, В, D, Е и F независимо представляют собой СН или CR6; то есть R5 имеет подформулу (х) и представляет собой возможно замещенный бензил. В данном воплощении предпочтительно заместитель R6 находится в положении 4 по отношению к боковой цепи -(СН2)n- (то есть D представляет собой CR6; то есть заместитель R6 находится в D); и/или предпочтительно заместитель R6 находится в 3-м и/или 5-м положении по отношению к боковой цепи -(СН2)n- (то есть В и/или Е представляет собой CR6; то есть один или два заместителя R6 находятся в В и/или Е). Для монозамещения, то есть когда один из А, В, D, Е и F представляет собой CR6, тогда один заместитель R6 предпочтительно находится в 4-м положении по отношению к боковой цепи -(СН2)n- (то есть D представляет собой CR6). Когда имеется дизамещение, то есть когда два из А, В, D, Е и F независимо представляют собой CR6, тогда предпочтительным является 3,4-дизамещение (B+D или D+E независимо представляют собой CR6), 2,4-дизамещение (A+D или D+F независимо представляют собой CR6) или 2,3-дизамещение (А+В или E+F независимо представляют собой CR6).
В подформуле (х) и/или (y) любой возможный заместитель R6 возможно может находиться только в В, D и/или Е, так что в подформуле (х) любой возможный заместитель R6 находится только в мета- (3- и/или 5-) и/или пара- (4-) положениях по отношению к боковой цепи -(СН2)n-. Альтернативно, в подформуле (х) любой возможный заместитель R6 может находиться в орто- (2- и/или 6-) положении по отношению к боковой цепи -(СН2)n-, либо один, либо в комбинации с одним или более другими возможными заместителями R6.
В общем, что касается R5, предпочтительно, чтобы R5 представлял собой атом водорода (Н); С1-6алкил (например, С1,2или3алкил или С3-6алкил); С1-4фторалкил, С3-6циклоалкил (например, С5-6циклоалкил), (С5-6циклоалкил)метил-, фенил, возможно замещенный одним или двумя из: атома фтора или хлора, метила, трифторметила, метокси или трифторметокси; либо R5 имел подформулу (х), (y) или (z), например, как описано выше.
Еще более предпочтительно R5 представляет собой атом водорода (Н), метил, этил, н-пропил, изопропил, 2-этилбутан-1-ил, циклопентил, циклогексил, (циклогексил)метил-, возможно замещенный фенил, например фторфенил, например 4-фторфенил, возможно замещенный бензил или возможно замещенный пиридинилметил; либо R5 имеет подформулу (z).
Возможно, R5 может представлять собой бензил, пиридинилметил (например, пиридин-4-илметил, пиридин-3-илметил или предпочтительно пиридин-2-илметил) или 4-фторфенил.
В одном предпочтительном воплощении R5 имеет подформулу (х) и представляет собой: бензил, (моноалкил-фенил)метил, [моно(фторалкил)-фенил]метил, (моногалогено-фенил)метил, (моноалкокси-фенил)метил, [моно(фторалкокси)-фенил]метил, [моно(N,N-диметиламино)-фенил]метил, [моно(метил-SO2-NH-)-фенил]метил, [моно(метил-SO2-)-фенил]метил, (диалкил-фенил)метил, (моноалкил-моногалогено-фенил)метил, [моно(фторалкил)-моногалогено-фенил]метил, (дигалогено-фенил)метил, (дигалогено-моноалкил-фенил)метил, [дигалогено-моно(гидроксиметил)-фенил]метил или (диалкокси-фенил)метил, такой как (3,4-диметокси-фенил)метил. Заместители могут быть предпочтительно определены далее, как определено здесь в предпочтительных воплощениях.
В одном предпочтительном воплощении R5 имеет подформулу (х) и представляет собой: (моноалкил-фенил)метил, [моно(фторалкил)-фенил]метил, (моногалогено-фенил)метил, (моноалкокси-фенил)метил, [моно(фторалкокси)-фенил]метил, [моно(N,N-диметиламино)-фенил]метил, (диалкил-фенил)метил, (моноалкил-моногалогено-фенил)метил, (дигалогено-фенил)метил или (дигалогено-моноалкил-фенил)метил, или [дигалогено-моно(гидроксиметил)-фенил]метил. Более предпочтительно в данном воплощении R5 представляет собой:
-(моноС1-3алкил-фенил)метил, такой как (4-С1-3алкил-фенил)метил;
-(моноС1фторалкил-фенил)метил, такой как (4-С1фторалкил-фенил)метил;
-(моноС1-2алкокси-фенил)метил, такой как (4-С1-2алкокси-фенил)метил;
-[моно(С1фторалкокси)-фенил]метил, такой как (4-С1фторалкокси-фенил)метил;
-(диС1-2алкил-фенил)метил или (диметил-фенил)метил, такой как (3,4-диметил-фенил)метил, (2,4-диметил-фенил)метил, (3,5-диметил-фенил)метил, (2,3-диметил-фенил)метил или (2,5-диметил-фенил)метил; более предпочтительно (3,4-диметил-фенил)метил или (2,4-диметил-фенил)метил;
-(моноС1-2алкил-моногалогено-фенил)метил или (моноС1-2алкил-монохлор-фенил)метил, такой как (4-метил-3-хлор-фенил)метил, (3-метил-4-хлор-фенил)метил, (2-метил-4-хлор-фенил)метил;
-(дигалогено-фенил)метил, такой как (2-хлор-4-фторфенил)метил, либо (2,4-дифтор-фенил)метил, либо (4-бром-2-фторфенил)метил, либо предпочтительно (4-хлор-2-фторфенил)метил; например (дихлор-фенил)метил, такой как (3,4-дихлор-фенил)метил, либо (2,4-дихлор-фенил)метил, либо (2,6-дихлор-фенил)метил, либо предпочтительно (2,3-дихлор-фенил)метил;
-(дигалогено-моноС1-2алкил-фенил)метил, например (2,4-дихлор-6-метил-фенил)метил, или
-[дигалогено-моно(гидроксиметил)-фенил]метил, такой как [2,3-дихлор-6-(гидроксиметил)-фенил]метил.
В предпочтительном альтернативном воплощении R5 имеет подформулу (z), и один или предпочтительно ни один из J, L, М или Q представляет собой CR6, и/или R9 представляет собой атом водорода (Н) или метил. Предпочтительно r равно 1. Предпочтительно для (z) R6 независимо представляет собой ОН (включая любой его кето-таутомер), или более предпочтительно С1-2алкил (например, метил) или С1фторалкил.
Предпочтительно NR4R5 не является NH2. R5 предпочтительно не является атомом водорода (Н).
Когда R4 и R5, взятые вместе, представляют собой возможно замещенный -(СН2)p 1-, либо возможно замещенный -С(O)-(СН2)p 2-, либо -(CH2)p 3-Х5-(СН2)p 4-, либо -С(O)-Х5-(CH2)p 5-, либо частично ненасыщенное производное любого из вышеуказанных, предпочтительно R4 и R5, взятые вместе, представляют собой возможно замещенный -(СН2)p 1-, либо возможно замещенный -С(O)-(СН2)p 2-, либо -(CH2)p 3-X5-(CH2)p 4-, либо -C(O)-X5-(CH2)p 5- (то есть не являются частично ненасыщенным производным любого из них).
Когда R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, возможно замещенный R18, либо -С(O)-(СН2)p 2-, возможно замещенный R18, либо -(CH2)p 3-Х5-(CH2)p 4-, NR4R5 может представлять собой, например, 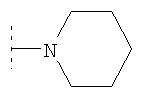 ,
,
возможно замещенный R18, либо 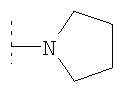 , возможно замещенный R18, либо
, возможно замещенный R18, либо 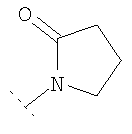 ,
,
возможно замещенный R18, либо 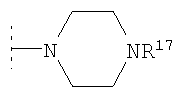 (то есть R4 и R5, взятые вместе, представляют собой -(CH2)2-N(R17)-(CH2)2-), либо
(то есть R4 и R5, взятые вместе, представляют собой -(CH2)2-N(R17)-(CH2)2-), либо 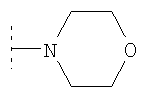 (то есть R4 и R5, взятые вместе, представляют собой -(СН2)2-O-(СН2)2-).
(то есть R4 и R5, взятые вместе, представляют собой -(СН2)2-O-(СН2)2-).
Предпочтительно R17 представляет собой атом водорода (Н); С1-4алкил (например, С1-2алкил); С3-6циклоалкил; -(CH2)p 6-C(O)R16, либо возможно замещенный фенил или бензил. Более предпочтительно R17 представляет собой Н; С1-2алкил; -(CH2)p 6-C(O)R16 или возможно замещенный фенил.
Когда R4 и R5, взятые вместе, представляют собой -(СН2)p 1- или -С(O)-(СН2)p 2-, гетероцикл NR4R5 предпочтительно не замещен R18.
Когда R4 и R5, взятые вместе, представляют собой -(CH2)p 1- или -С(O)-(СН2)p 2-, и, если гетероцикл NR4R5 замещен R18, тогда, возможно, R18 не является заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5.
Когда R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, либо -С(O)-(СН2)p 2-, либо -(СН2)p 3-Х5-(CH2)p 4-, либо -С(O)-Х5-(СН2)p 5-, либо частично ненасыщенное производное любого из них, и когда гетероцикл NR4R5 является конденсированным с фенильным кольцом, возможно замещенном на фениле одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; тогда в одном воплощении изобретения NR4R5 представляет собой 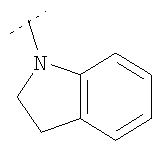 или
или 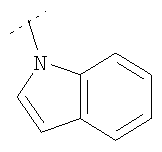 , где фенил возможно замещен одним или двумя из: атома галогена,
, где фенил возможно замещен одним или двумя из: атома галогена,
С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси.
В одном воплощении изобретения NR7R8 и/или NR12R13 могут, например, независимо представлять собой 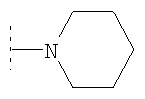 , либо
, либо 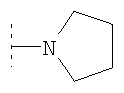 , либо
, либо 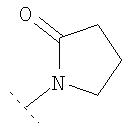 , либо
, либо 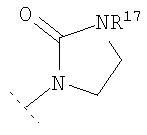 , либо
, либо 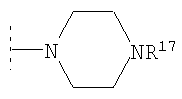
(то есть R12 и R13 вместе или R7 и R8 вместе представляют собой -(CH2)2-N(R14)-(CH2)2-), либо 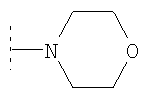
(то есть R12 и
R13 вместе или R7 и R8 вместе представляют собой -(СН2)2-O-(СН2)2-) либо NMe2.
Предпочтительно R15 представляет собой атом водорода (Н) или С1-4алкил (например, tBu или С1-2алкил, например метил); более предпочтительно R15 представляет собой атом водорода (Н).
Предпочтительными, однако, являются R4 и R5, не взятые вместе, то есть не взятые вместе с образованием кольцевых систем NR4R5, описанных здесь.
(Аналогичные предпочтения, как для R5, применимы для R51a, за исключением того, что R5a не может являться атомом водорода. Более предпочтительно R5a представляет собой этил).
В особенно предпочтительном воплощении NR4R5 представляет собой группу
NR4R5, как определено в любом из Примеров 21-98, 100-182, 187-188, 191-200, 201-203, 210-353, 355-651, 653-658, 660-664 и 665-686.
Особенно предпочтительно, чтобы соединение формулы (I) или его соль представляли собой:
Этил-4-(циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-(циклогексиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-[(1-ацетилпиперидин-4-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-(циклопентиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат (не это соединение само по себе, и для применения или способа лечения предпочтительно не это соединение),
Этил-1-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-этил-4-[(3R)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-этил-4-(тетрагидро-2Н-тиопиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-этил-4-(тетрагидротиен-3-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-(циклопропиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-[(1,1-диоксидотетрагидротиен-3-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-[(1,1-диоксидотетрагидро-2Н-тиопиран-4-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
N-Бензил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Циклопентил-4-(циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-N-циклопентил-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Циклопентил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-N-циклопентил-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Циклопентил-1-этил-5-(пирролидин-1-илкарбонил)-1Н-пиразоло[3,4-b]пиридин-4-амин,
N-Циклогексил-1-этил-5-(пирролидин-1-илкарбонил)-1H-пиразоло[3,4-b]пиридин-4-амин,
1-Этил-5-(пирролидин-1-илкарбонил)-N-тетрагидро-2Н-пиран-4-ил-1Н-пиразоло[3,4-b]пиридин-4-амин,
4-(Циклопентиламино)-1-этил-N-(пиридин-4-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-N-(пиридин-4-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(пиридин-4-илметил)-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклогексиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-N-бензил-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-1-этил-N-(2-этилбутил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-N-(2-этилбутил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(2-этилбутил)-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(2-этилбутил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-1-этил-N-(2-этилбутил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-1-этил-N-н-пропил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-N-н-пропил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-н-пропил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-1-этил-N-н-пропил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-1-этил-N-(пиридин-4-илметил)-1 Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклопентиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклогексиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-N-(2-этилбутил)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-N-(2-этилбутил)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2-Этилбутил)-1-метил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-N-(4-фторфенил)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-N-(4-фторфенил)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(4-Фторфенил)-1-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопентиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетилпиперидин-4-ил)амино]-N-бензил-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N,N-диметил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-изопропил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(3R)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-(тетрагидротиен-3-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклопропиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-[(1,1-диоксидотетрагидротиен-3-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-[(1,1-диоксидотетрагидро-2Н-тиопиран-4-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-(тетрагидро-2Н-тиопиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-[(3R)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-(тетрагидро-2Н-тиопиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-фторфенил)-4-(тетрагидротиен-3-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклопропиламино)-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1,1-Диоксидотетрагидротиен-3-ил)амино]-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид или
4-[(1,1-Диоксидотетрагидро-2Н-тиопиран-4-ил)амино]-1-этил-N-(4-фторфенил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
или его соль, например его фармацевтически приемлемую соль.
Структуры этих конкретных соединений приведены в Примерах 1-98 в описании ниже.
Альтернативно особенно предпочтительно, чтобы соединение формулы (I) или его соль представляло собой:
1-Этил-N-[4-(метилсульфонил)бензил]-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[3-(метилсульфонил)бензил]-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-5-{[5-метокси-6-(трифторметил)-2,3-дигидро-1Н-индол-1-ил]карбонил}-N-тетрагидро-2Н-пиран-4-ил-1H-пиразоло[3,4-b]пиридин-4-амин,
N-[5-(Хлорпиридин-2-ил)метил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(4-Хлорбензил)-1-этил-N-изопропил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(3-Хлорбензил)-1-этил-N-(2-гидроксиэтил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(5-метил-3-фенилизоксазол-4-ил)метил]-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2-трет-Бутоксиэтил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2H-пиран-4-иламино)-N-(1,3-тиазол-2-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(пиримидин-4-илметил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(2-метил-1,3-тиазол-4-ил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[3-(трет-Бутоксиметил)бензил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{2-[метил(метилсульфонил)амино]этил}-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(пиразин-2-илметил)-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-5-{[4-(пиридин-2-илкарбонил)пиперазин-1-ил]карбонил}-N-тетрагидро-2Н-пиран-4-ил-1H-пиразоло[3,4-b]пиридин-4-амин,
N-(2-Хлор-6-фторбензил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(6-оксо-1,6-дигидропиридин-3-ил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[3-(Аминокарбонил)бензил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{4-[(метиламино)карбонил]фенил}-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[2-(1-метил-1Н-имидазол-4-ил)этил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-{2-[(Аминокарбонил)амино]этил}-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(1H-тетразол-5-илметил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-N-[2-(1H-1,2,4-триазол-1-ил)этил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2H-пиран-4-иламино)-N-[4-(трифторметил)фенил]-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
трет-Бутил-4-({[1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)пиперидин-1-карбоксилат,
1-Этил-N-{3-[(метилсульфонил)амино]пропил}-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[2-(Диметиламино)бензил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(1-этилпирролидин-2-ил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(тетрагидрофуран-2-илметил)-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-тетрагидро-2Н-пиран-4-ил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-
пиразоло[3,4-b]пиридин-5-карбоксамид,
N-{4-[(Диметиламино)сульфонил]бензил}-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{3-[(метилсульфонил)амино]бензил}-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-метоксифенил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[3-(2-оксопирролидин-1-ил)пропил]-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[2-(1-метилпирролидин-2-ил)этил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(пиридин-3-илметил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(1-метилпиперидин-4-ил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(1-этилпропил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(2-пиперидин-1-илэтил)-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(3-морфолин-4-илпропил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(3-Этоксипропил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(Циклогексилметил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[3-(Диметиламино)пропил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-неопентил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(4-метоксибензил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{2-[(фенилсульфонил)амино]этил}-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[2-(Ацетиламино)этил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{2-[(метилсульфонил)амино]этил}-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{2-1(2-метоксифенил)(метил)амино]этил}-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(2-оксо-2-фенилэтил)-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2,5-Дифторбензил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-N-[4-(трифторметил)бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N,1-Диэтил-N-пропил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Циклопропил-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2-Амино-2-оксоэтил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-(3-метоксифенил)-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(3,4-Дифторбензил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
Этил-3-({[1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)пропаноат,
N-(1-Бензилпиперидин-4-ил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бутил-4-{[1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-ил]карбонил}пиперазин-1-карбоксамид,
1-Этил-4-(тетрагидро-2H-пиран-4-иламино)-N-(1,3,4-тиадиазол-2-ил)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2,3-Дигидро-1H-инден-2-ил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[2-(2-оксоимидазолидин-1-ил)этил]-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(3,4-Диметоксибензил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(3-Хлорбензил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-5-[(4-метилпиперазин-1-ил)карбонил]-N-(тетрагидро-2H-пиран-4-ил-1H-пиразоло[3,4-b]пиридин-4-амин,
1-Этил-N-(2-гидроксиэтил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-5-{[4-(4-метоксифенил)пиперазин-1-ил]карбонил}-N-(тетрагидро-2Н-пиран-4-ил-1H-пиразоло[3,4-b]пиридин-4-амин,
1-Этил-N-{4-[(метилсульфонил)метил]фенил}-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[3-(Диметиламино)-3-оксопропил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(1-метил-1Н-имидазол-5-ил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{4-[(метиламино)сульфонил]фенил}-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(2-Цианоэтил)-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-метил-N-[(1-метил-1Н-имидазол-2-ил)метил]-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-N-(2-тиен-2-илэтил)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[2-(4-Хлорфенил)этил]-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[2-(2-метоксифенил)этил]-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
Этил-4-(циклогексиламино)-1-(3-этокси-3-оксопропил)-1H-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-н-пропил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-1-(2-гидроксиэтил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
N-[4-(Метилсульфонил)бензил]-1-н-пропил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-(4-Фторфенил)-1-н-пропил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
Этил-1-этил-6-метил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксилат,
Этил-4-(циклогексиламино)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат,
4-(Циклогексиламино)-1-этил-6-метил-N-[4-(метилсульфонил)бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-4-(циклогексиламино)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-N-(4-фторфенил)-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-1-этил-6-метил-N-[4-(трифторметил)бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-(Циклогексиламино)-N-(2,3-дигидро-1H-инден-2-ил)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-6-метил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(2-оксоазепан-3-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(3-гидроксициклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(4-гидроксициклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-Бензил-1-этил-4-[(3-гидроксициклопентил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид или
N-Бензил-1-этил-4-[(4-оксоциклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
или его соль, например его фармацевтически приемлемую соль.
Структуры этих конкретных соединений приведены в Примерах 100-201 в описании ниже.
Альтернативно соединение формулы (I) или его соль может представлять собой:
1-Этил-N-(2-гидрокси-1-метилэтил)-4-(тетрагидро-2Н-пиран-4-иламино)-1 H-пиразоло[3,4-b]пиридин-5-карбоксамид или
Метил-(2S)-2-({[1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)-3-гидроксипропаноат
или его соль, например его фармацевтически приемлемую соль (см., например, Примеры 202-203).
Альтернативно особенно предпочтительно, чтобы соединение формулы (I) или его соль представляли собой один из Примеров 204-664 или один из Примеров 665-686, как соединение или его соль, например его фармацевтически приемлемую соль. Структуры этих конкретных соединений приведены в Примерах 204-664 и в Примерах 665-686 в описании ниже, и их названия приведены в разделе Примеры.
В одном воплощении еще более предпочтительно, чтобы соединение формулы (1) или его соль представляло собой соединение Примера 260, 261, 263,266,431, 493,494,518,528,584,626, 643, 653, 679, 680,681, 682, 683,684, 685 или 686 (более предпочтительно Примера 260, 518, 653, 679, 680, 681 или 684), как определено структурами и/или названиями, описанными здесь, либо его соль, например его фармацевтически приемлемую соль. Структуры и названия этих Примеров описаны в разделе Примеры. Эти Примеры считаются пригодными для ингаляционного введения.
В другом воплощении еще более предпочтительно, чтобы соединение формулы (I) или его соль представляло собой соединение Примера 21, 22, 83, 100, 109, 167, 172, 178 или 600, как определено структурами и/или названиями, описанными здесь, либо его соль, например его фармацевтически приемлемую соль. Структуры и названия этих Примеров описаны в разделе Примеры. Эти Примеры считаются пригодными для перорального введения.
Во втором аспекте изобретения предложено соединение формулы (IA) или его соль (в частности, его фармацевтически приемлемая соль):
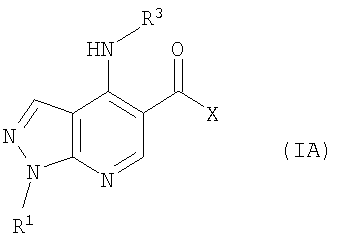
где:
Х представляет собой NR4R5 или OR5a, где:
R4 представляет собой водород, С1-2алкил или С1-2фторалкил, и
R5 представляет собой водород, С1-8алкил, С1-8фторалкил или С3-8циклоалкил, фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5 имеет подформулу (х), (y) или (z):


 ,
,
где в подформуле (х) и (z) n=1 или 2, и в подформуле (y) m=1 или 2;
где в подформуле (х) и (y) ни один из, один или два из А, В, D, Е и F представляют собой атом азота; и остальные из А, В, D, Е и F представляют собой СН или CR6, где
R6 представляет собой атом галогена, С1-4алкил, С1-4фторалкил, С1-2алкокси, С1-2фторалкокси, С1-2алкилсульфонил (С1-2алкил-SO2-), С1-2алкил-SO2-NH-, R7R8N-SO2-, R7R8N-CO-, R7R8N, ОН, С1-4алкоксиметил или С1-2алкил-SO2-СН2-, где R7 и R8 независимо представляют собой водород или С1-2алкил;
где в подформуле (z) G представляет собой О, либо S, либо NR9, где R9 представляет собой С1-4алкил или С1-4фторалкил; ни один из, один или два из J, L, М и Q представляют собой атом азота; и остальные из J, L, М и Q представляют собой СН или CR6, где R6 является таким, как определено здесь;
либо R4 и R5, взятые вместе, представляют собой -(СН2)p-, где р=3, 4 или 5 (предпочтительно р=4);
R5a представляет собой С1-8алкил, C1-8фторалкил, С3-8циклоалкил, фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5a имеет подформулу (х), (y) или (z), как определено здесь;
R3 является С3-8циклоалкилом или гетероциклической группой, представляющей собой 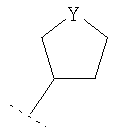 или
или 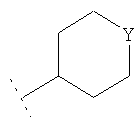 , где Y представляет собой О, S,
, где Y представляет собой О, S,
SO2 или NR10, где R10 представляет собой водород, С1-4алкил, С1-2фторалкил, С(O)-С1-2алкил или С(O)-CF3;
и где в R3 С3-8циклоалкил или гетероциклическая группа возможно замещены одним или двумя заместителями, представляющими собой ОН, С1-2алкокси, триметокси или С1-2алкильную группу; и где любой ОН, алкокси или триметокси заместитель не является заместителем по кольцевому атому углерода, присоединенному к -NH- группе формулы (IA) и не является заместителем по какому-либо кольцевому атому углерода, связанному с Y группой гетероциклической группы, и
R1=С1-4алкил или С1-2фторалкил.
В формуле (IA) предпочтительно, когда R3 является гетероциклической группой, представляющей собой  , и Y представляет собой NR10, тогда:
, и Y представляет собой NR10, тогда:
либо (а) R10 представляет собой водород, С(O)-С1-2алкил или С(O)-CF3;
либо (б) R10 представляет собой метил, и соединение представляет собой 1-этил-N-(2-этилбутил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид или 1-этил-N-(4-фторфенил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид.
В формуле (IA) предпочтительно, когда Х представляет собой OR5a, соединение является иным чем соединение, где R1 представляет собой метил, Х представляет собой OEt, и R3 представляет собой циклопентил.
В формуле (IA) в подформуле (х) и/или (у) предпочтительно, чтобы ни один из, один или два из А, В, D, Е и F представляли собой атом азота; ни один из, один, два или три из А, В, D, Е и F представляли собой CR6; и остальные из А, В, D, Е и F представляли собой СН. Более предпочтительно, чтобы ни один из, один или два из А, В, D, Е и F представляли собой атом азота; ни один из, либо один, либо два из А, В, D, Е и F представляли собой CR6; и остальные из А, В, D, Е и F представляли собой СН. В формуле (IA), в подформуле (х) и/или (y), предпочтительно ни один из или один из А, В, D, Е и F представляют собой атом азота.
В формуле (IA), предпочтительно, подформула (х) представляет собой: бензил, фенетил (Ph-С2H4-); бензил или фенетил, замещенные на фенильном кольце одним заместителем R6 или одним из следующих:






где R6a представляет собой либо R6, как определено здесь, либо (предпочтительно) водород.
В формуле (1А) подформула (у) предпочтительно представляет собой: 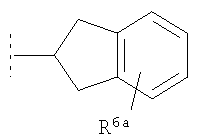 , где R6a представляет собой либо R6, как определено здесь, либо предпочтительно водород.
, где R6a представляет собой либо R6, как определено здесь, либо предпочтительно водород.
Примеры 1-99 являются примерами соединений или солей согласно второму аспекту изобретения (Формула (IA)).
В третьем аспекте настоящего изобретения предложено соединение формулы (IB) или его соль (в частности, его фармацевтически приемлемая соль):
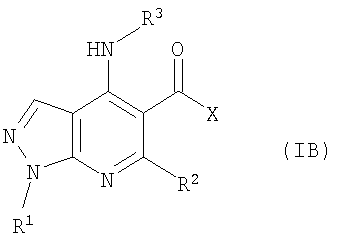
где:
R1 представляет собой С1-4алкил, C1-3фторалкил, -CH2CH2OH или -СН2СН2CO2С1-2алкил;
R2 представляет собой атом водорода (Н), метил или С1фторалкил;
R3 представляет собой возможно замещенный С3-8циклоалкил или возможно замещенную гетероциклическую группу подформулы (аа), (bb) или (bb):
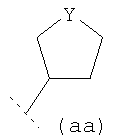 или
или 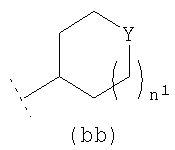 или
или 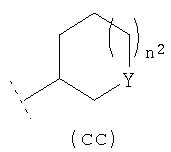
где n1 и n2 независимо равны 1 или 2 и где Y представляет собой О, S, SO2 или NR10, где R10 представляет собой атом водорода (Н), С1-4алкил (например, метил или этил),
С1-2фторалкил, CH2C(O)NH2, C(O)NH2, C(O)-C1-2алкил или С(O)-С1фторалкил;
и где в R3 С3-8циклоалкильная или гетероциклическая группа подформулы (aa), (bb) или (сс) возможно замещены одним или двумя заместителями, представляющими собой оксо (=O), ОН, С1-2алкокси, С1-2фторалкокси (например, трифторметокси) или
С1-2алкил; и где любой ОН, алкокси или фторалкокси заместитель не является заместителем по кольцевому атому углерода R3, соединенному (связанному) с -NH- группой формулы (IB) и не является заместителем по какому-либо кольцевому атому углерода R3, связанному с Y группой гетероциклической группы (aa), (bb) или (cc);
и Х представляет собой NR4R5 или OR5a, где:
R4 представляет собой атом водорода (Н); C1-6алкил; С1-3фторалкил; или С2-6алкил, замещенный одним заместителем R11; и
R5 представляет собой атом водорода (Н); C1-8алкил; С1-8фторалкил; С3-8циклоалкил, возможно замещенный группой С1-2алкил; или -(CH2)p 4-С3-8циклоалкил, возможно замещенный в группировке -(СН2)n 4- или в С3-8циклоалкильной группировке С1-2алкильной группой, где n4 равно 1, 2 или 3;
либо R5 представляет собой С2-6алкил, замещенный одним или двумя независимыми заместителями R11;
где каждый заместитель R11, независимо от любого другого присутствующего заместителя R11, представляет собой: гидрокси (ОН); C1-6алкокси; фенилокси; бензилокси; -NR12R13; -NR15-C(O)R16; -NR15-C(O)-O-R16; -NR15-C(O)-NH-R15 или -NR15-SO2R16; и где любой заместитель R11, который представляет собой ОН, алкокси или -NR12R13, не является заместителем по любому атому углерода любого алкила, замещенного R4 или R5, который связан с атомом азота из NR4R5;
либо R5 представляет собой -(СН2)n 11-С(O)R16; -(CH2)n 11-C(O)NR12R13; -CHR19-C(O)NR12R13; -(CH2)n 12-C(O)OR16; -CHR19-C(O)OR16; -(CH2)n 12-SO2-NR12R13; -(CH2)n 12-SO2R16 или -(CH2)n 12-CN; где n11 равно 0, 1, 2, 3 или 4 и n12 равно 1, 2, 3 или 4;
либо R5 представляет собой -(CH2)n 13-Het, где n13 равно 0, 1, 2, 3 или 4 и Het представляет собой 4-, 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один или два кольцевых гетероатома, независимо выбранных из О, S и N; где любые присутствующие кольцевые гетероатомы не связаны с группировкой -(СН2)n 13-, когда n13 равно 1, и не связаны с атомом азота из NR4R5, когда n13 равно 0; где любые кольцевые атомы азота, которые присутствуют и которые не являются ненасыщенными (то есть которые не задействованы в двойной связи), присутствуют в виде NR17, где R17 является таким, как определено здесь; и где один или два кольцевые атома углерода возможно независимо замещены С1-2алкилом;
либо R5 представляет собой фенил, возможно замещенный одним или двумя из: атома галогена; С1-4алкила (например, С1-2алкила); С1-2фторалкила (например, трифторметила); С1-4алкокси (например, С1-2алкокси); С1-2фторалкокси (например, трифторметокси); С1-2алкилсульфонила (С1-2алкил-SO2-); С1-2алкил-SO2-NH-; R7R8N-S(O)2-; R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметила; С1-4алкоксиэтила; С1-2алкил-S(O)2-СН2-; циано(CN); или фенила, возможно замещенного одним или двумя из фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
где R7 и R8 независимо представляют собой атом водорода (Н); С1-4алкил (например, С1-2алкил, такой как метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; или R7 и R8 вместе представляют собой -(СН2)n 6-, либо -С(O)-(СН2)n 7-, либо -С(O)-(СН2)n 7-C(О)-, либо -(CH2)n 8-X7-(CH2)n 9-, либо -С(O)-Х7-(CH2)n 10-, где: n6 равно 3, 4, 5 или 6, n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3, и X7 представляет собой О или NR14, где R14 представляет собой Н или С1-2алкил;
либо R5 имеет подформулу (х), (y) или (z):


 ,
,
где в подформуле (х) n=1 или 2; в подформуле (y) m=1 или 2; и в подформуле (z) r=0, 1 или 2;
где в подформуле (х) и (у) ни один из, один или два из А, В, D, Е и F представляют собой атом азота, и остальные из А, В, D, Е и F независимо представляют собой СН или CR6;
где R6 представляет собой атом галогена; С1-4алкил (например, С1-2алкил); С1-4фторалкил (например, С1-2фторалкил); С1-4алкокси (например, С1-2алкокси); С1-2фторалкокси; С1-2алкилсульфонил (С1-2алкил-SO2-); С1-2алкил-SO2-NH-; R7R8N-S(O)2-; R7R8N-CO-; -NR15-C(O)R16; R7R8N; ОН; С1-4алкоксиметил; С1-4алкоксиэтил; С1-2алкил-S(O)2-CH2-; циано (CN); или фенил, возможно замещенный одним или двумя из фторо, хлоро, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; где R7 и R8 являются такими, как определено здесь;
где в подформуле (z) G представляет собой О, или S, или NR9, где R9 представляет собой атом водорода (Н), С1-4алкил или С1-4фторалкил; ни один из, один, два или три из J, L, М и Q представляют собой атом азота, и остальные из J, L, М и Q представляют собой независимо СН или CR6, где R6 является таким, как определено здесь;
или R4 и R5, взятые вместе, представляют собой -(СН2)p 1-, либо -С(O)-(СН2)p 2-, либо -(CH2)p 3-X5-(CH2)p 4-, либо -C(O)-X5-(CH2)p 5-, где: р1=3, 4, 5 или 6 (предпочтительно р=4 или 5), р2 равно 2, 3, 4 или 5 (предпочтительно р2 равно 2, 3 или 4), и р3 и р4 и р5 независимо равны 2 или 3 (предпочтительно независимо 2), и X5 представляет собой О или NR17;
где R17 представляет собой атом водорода (Н); С1-4алкил (например, С1-2алкил);
С1-2фторалкил; С3-6циклоалкил; -(CH2)p 6-C(O)R16, где р6 равно 0, 1, 2 или 3 (предпочтительно р6 равно 0); -(CH2)p 6-C(O)NR12R13; -(CH2)p 6-С(O)OR16; -SO2R16; либо фенил или бензил, где фенил или бензил возможно замещены по ароматическому атому углерода одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
и где, когда R4 и R5, взятые вместе, представляют собой -(CH2)p 1- или -С(O)-(СН2)p 2-, гетероцикл NR4R5 возможно замещен одним заместителем R18, где R18 представляет собой: С1-4алкил (например, С1-2алкил); С1-2фторалкил; С3-6циклоалкил; С1-2алкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); С1фторалкокси (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); ОН (не являющийся заместителем по кольцевому атому углерода, связанному с атомом азота кольца NR4R5); -(CH2)p 7-C(O)R16, где р7 равно 0, 1, 2 или 3 (предпочтительно р7 равно 0 или 1); -(CH2)p 7-C(O)OR16; -(CH2)p 7-OC(O)R16; -(CH2)p 7-C(O)NR12R13; -(CH2)p 7-NR15C(O)R16; -(CH2)p 7-NR15C(O)NR12R13; -(CH2)p 7-NR15C(O)OR16; -(CH2)p 7-SO2R16; -(CH2)p 7-SO2NR12R13; -(CH2)p 7-NR15SO2R16; -(CH2)p 7-OH;
-(CH2)p 7-OR16; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R4 и R5, взятые вместе, представляют собой -(CH2)p 1-, либо -С(O)-(CH2)p 2-, либо -(CH2)p 3-X5-(CH2)p 4-, либо -C(O)-X5-(CH2)p 5-, как определено здесь, и где гетероцикл NR4R5 конденсирован с фенильным кольцом, возможно замещенным на фениле одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; и
R5a представляет собой C1-8алкил, С1-8фторалкил, С3-8циклоалкил; фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, трифторметила, С1-2алкокси или трифторметокси; либо R5a имеет подформулу (х), (y) или (z), как определено здесь,
и где:
R12 и R13 независимо представляют собой Н; С1-5алкил (например, С1-3алкил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
или R12 и R13 вместе представляют собой -(СН2)n 6-, либо -С(O)-(СН2)n 7-, либо -C(O)-(CH2)n 7-C(O)-, либо -(CH2)n 8-X12-(CH2)n 9-, либо -C(O)-X12-(CH2)n 10-, где: n6 равно 3, 4, 5 или 6 (предпочтительно n6 равно 4 или 5), n7 равно 2, 3, 4 или 5 (предпочтительно n7 равно 2, 3 или 4), n8 и n9 и n10 независимо равны 2 или 3 (предпочтительно независимо 2), и X12 представляет собой О или NR14, где R14 представляет собой Н или С1-2алкил;
R15 представляет собой атом водорода (Н); С1-4алкил (например, tBu или С1-2алкил, например метил); С3-6циклоалкил; или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси;
R16 представляет собой С1-4алкил (например, С1-2алкил); С3-6циклоалкил; пиридинил (например, пиридин-2-ил); или фенил, возможно замещенный одним или двумя из: атома галогена, С1-2алкила, С1фторалкила, С1-2алкокси или С1фторалкокси; и
R19 представляет собой атом водорода (Н); С1-4алкил (например, изобутил, втор-бутил или С1-3алкил, такой как метил или изопропил); -(CH2)n 20-OR20, где n20 равно 1, 2, 3 или 4 (предпочтительно 1) и R20 представляет собой атом водорода (Н) или С1-4алкил (предпочтительно R20 представляет собой Н); -СН(Ме)-ОН; -CH2-SH; -CH2-CH2-S-Me; бензил или (4-гидроксифенил)метил (то есть 4-гидроксибензил).
В формуле (IB) предпочтительно, когда R3 представляет собой гетероциклическую группу подформулы (bb), n1 равно 1, и Y представляет собой NR10, тогда:
либо (а) R10 не представляет собой С1-4алкил, С1-2фторалкил или CH2C(O)NH2;
либо (б) R10 представляет собой метил, и соединение представляет собой 1-этил-N-(2-этилбутил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид или 1-этил-N-(4-фторфенил)-4-[(1-метилпиперидин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид.
В формуле (IB) предпочтительно, когда Х представляет собой OR5a, соединение является иным, чем соединение, где R1 представляет собой метил, Х представляет собой OEt и R3 представляет собой циклопентил.
В формуле (IB), где R3 представляет собой возможно замещенный С3-8циклоалкил, один или два возможные заместителя предпочтительно включают в себя (например, представляет собой или представляют собой) ОН и/или оксо (=O). В формуле (IB), в гетероциклической группе R3 подформулы (аа), (bb) или (cc) один или два возможные заместителя предпочтительно включают в себя (например, представляет собой или представляют собой) ОН и/или оксо.
Примеры 1-203 являются примерами соединений или солей согласно третьему аспекту изобретения (Формула (IB)).
Предпочтительные или возможные признаки соединения или соли формулы (IA) и соединения или соли формулы (IB) являются аналогичными или подобными предпочтительным или возможным признакам соединения или соли формулы (I) со всеми необходимыми произведенными изменениями (например, формулы, R групп и/или заместителей). В общем случае, всякий раз, когда здесь упоминается формула (I), тогда в альтернативных воплощениях утверждение с упоминанием формулы (I) касается формулы (IA) или формулы (IB) со всеми необходимыми произведенными изменениями.
Соли, сольваты, изомеры, таутомерные формы, молекулярные массы и т.д.
В связи с их возможным применением в медицине соли соединений формулы (I) предпочтительно являются фармацевтически приемлемыми. Подходящие фармацевтически приемлемые соли могут включать в себя соли присоединения кислот или оснований. Фармацевтически приемлемая соль присоединения кислоты может быть образована путем взаимодействия соединения формулы (I) с подходящей неорганической или органической кислотой (такой как бромистоводородная, соляная, серная, азотная, фосфорная, янтарная, малеиновая, уксусная, фумаровая, лимонная, винная, бензойная, пара-толуолсульфоновая, метансульфоновая или нафталинсульфоновая кислота), возможно в подходящем растворителе, таком как органический растворитель, с получением соли, которую обычно выделяют, например, посредством кристаллизации или фильтрации. Фармацевтически приемлемая соль присоединения кислоты соединения формулы (I) может представлять собой, например, гидробромид, гидрохлорид, сульфат, нитрат, фосфат, сукцинат, малеат, ацетат, фумарат, цитрат, тартрат, бензоат, пара-толуолсульфонат, метансульфонат или нафталинсульфонатную соль. Фармацевтически приемлемая соль присоединения основания может быть образована путем взаимодействия соединения формулы (I) с подходящим неорганическим или органическим основанием, возможно в подходящем растворителе, таком как органический растворитель, с получением соли присоединения основания, которую обычно выделяют, например, посредством кристаллизации или фильтрации. Другие пригодные фармацевтически приемлемые соли включают в себя фармацевтически приемлемые соли металлов, например фармацевтически приемлемые соли щелочных металлов или щелочноземельных металлов, таких как соли натрия, калия, кальция или магния; в частности, фармацевтически приемлемые соли металлов с одной или более группировками карбоновых кислот, которые могут присутствовать в соединении формулы (I).
Другие не фармацевтически приемлемые соли, например оксалаты, можно использовать, например, в выделении соединений по изобретению, и они включены в объем данного изобретения.
В объем изобретения включены все возможные стехиометрические и не стехиометрические формы солей соединений формулы (I).
Также в объем изобретения включены все сольваты, гидраты и комплексы соединений и солей по изобретению.
Некоторые группы, заместители, соединения или соли, включенные в настоящее изобретение, могут присутствовать в виде изомеров. В объем настоящего изобретения включены все такие изомеры, включая рацематы, энантиомеры, и их смеси.
Некоторые из групп, например гетероароматические кольцевые системы, входящие в соединения формулы (I), или их соли, могут существовать в одной или более таутомерных формах. В объем настоящего изобретения включены все такие таутомерные формы, включая смеси.
Соединение формулы (I), особенно когда оно предназначено для перорального медицинского применения, возможно может иметь молекулярную массу 1000 или менее, например 800 или менее, в частности 650 или менее или 600 или менее. Молекулярная масса здесь относится к массе несольватированного соединения в форме "свободного основания", то есть исключена любая молекулярная масса, привнесенная любыми солями присоединения, молекулами растворителя (например, воды) и т.д.
Пути синтеза
Следующие способы можно использовать для получения соединений по изобретению:
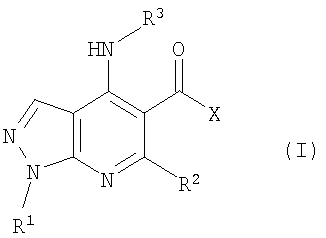
Большинство приведенных ниже способов синтеза приведены в качестве примера для соединений формулы (I), где R2 представляет собой атом водорода (Н). Однако некоторые или все эти способы также можно использовать с соответствующим изменением, например, исходных веществ и реагентов для получения соединений формулы (I), где R2 является иным, чем Н.
Способ А
Соединения формулы (I), где Х=OR5a, могут быть получены согласно способу, например, как описано Yu et al. в J. Med. Chem., 2001, 44, 1025-1027, при взаимодействии соединения формулы (II) с амином формулы R3NH2. Эту реакцию предпочтительно проводят в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, и/или в органическом растворителе, таком как этанол, диоксан или ацетонитрил. Эта реакция может требовать нагревания, например, до приблизительно 60-100°С, например до приблизительно 80-90°С.
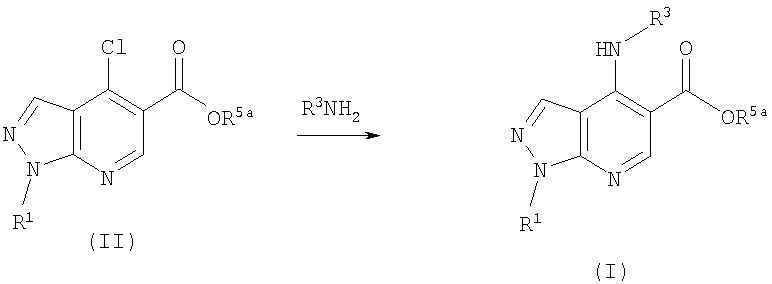
Соединения формулы (II) также описаны в приведенной выше ссылке и могут быть получены путем взаимодействия соединения формулы (III), например, с малонатом диэтилэтоксиметилена (где R5a=Et) при нагревании, с последующим взаимодействием с оксихлоридом фосфора, снова при нагревании:
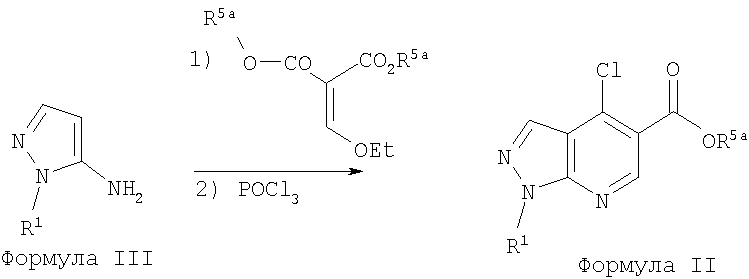
Когда нужного аминопиразола формулы (III) нет в продаже, его можно получить, используя способы, описанные Dorgan et al. в J. Chem. Soc., Perkin Trans. 1 (4), 938-42; 1980, путем взаимодействия цианоэтилгидразина с подходящим альдегидом формулы
R40CHO в растворителе, таком как этанол, при нагревании, с последующим восстановлением, например натрием, в растворителе, таком как трет-бутанол. R40 должен быть выбран таким образом, чтобы он содержал на один атом углерода меньше, чем R1, например, при R40 = метил будет R1 = этил.
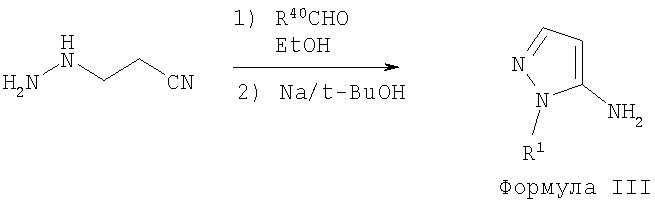
В альтернативном воплощении способа А 4-хлор-заместитель в соединении формулы (II) может быть заменен на атом галогена, такой как атом брома или предпочтительно атом хлора, в соединении формулы (IIA), как определено ниже. В данном воплощении способа А соединение формулы (IIA) взаимодействует с амином формулы R3NH2.
Способ Б
Соединения формулы (I), где Х=NR4R5, могут быть получены путем взаимодействия соединения формулы (IV) с амином формулы R3NH2. Это взаимодействие предпочтительно осуществляют в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, и/или в органическом растворителе, таком как этанол, THF (тетрагидрофуран), диоксан или ацетонитрил. Эта реакция может требовать нагревания, например, до приблизительно 60-100°С, или до приблизительно 80-90°С, например в течение 8-48 или 12-24 часов:
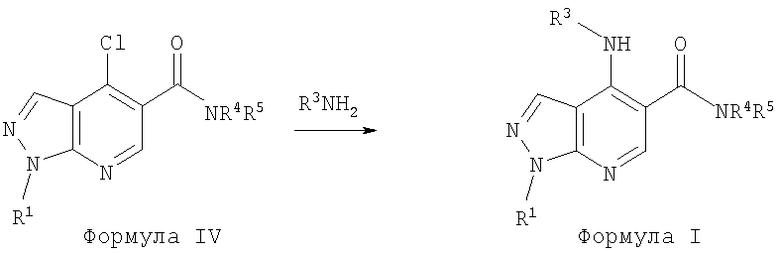
Соединения формулы (IV) могут быть получены двухстадийным способом, как описано Bare et al. в J. Med. Chem., 1989, 32, 2561-2573. Данный способ включает, во-первых, взаимодействие соединения формулы (V) с тионилхлоридом (или другим агентом, подходящим для образования хлорангидрида из карбоновой кислоты) либо в органическом растворителе, таком как хлороформ или THF, либо в виде неразбавленного раствора. Эта реакция может требовать нагревания, и образованное таким способом промежуточное соединение можно выделять или не выделять. Вторая стадия включает взаимодействие с амином формулы R4R5NH в органическом растворителе, таком как THF или хлороформ, и также может включать использование основания, такого как триэтиламин или диизопропилэтиламин:
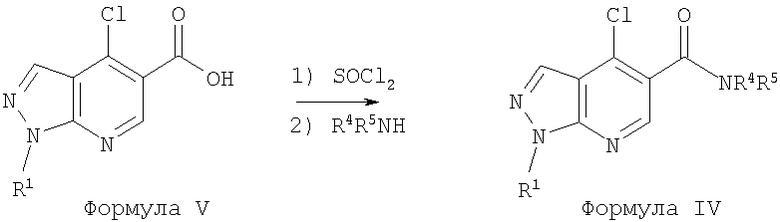
Соединения формулы (V) могут быть получены путем гидролиза эфира формулы (II) согласно способу, описанному Yu et al. в J. Med. Chem., 2001, 44, 1025-1027. Эта методика предпочтительно включает взаимодействие с основанием, таким как гидроксид натрия или гидроксид калия, в растворителе, например в водном растворителе, таком как водный этанол или водный диоксан:
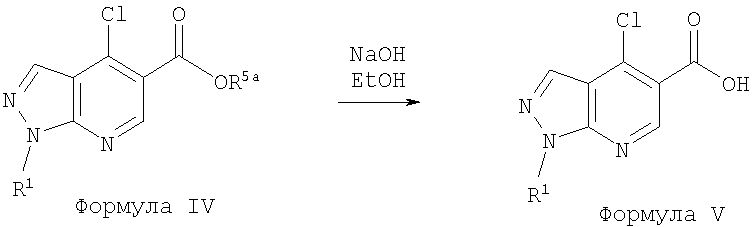
В альтернативном воплощении способа Б 4-хлор-заместитель в соединении формулы (IV) может быть заменен на атом галогена, такой как атом брома или предпочтительно атом хлора, в соединении формулы (IVA), как определено ниже. В данном воплощении способа Б соединение формулы (IVA) взаимодействует с амином формулы R3NH2.
Способ В
Соединения формулы (I) также могут быть получены согласно способу, например, описанному Bare et al. в J. Med. Chem., 1989, 32, 2561-2573, который включает взаимодействие соединения формулы (VI), где -O-R35 представляет собой уходящую группу, замещаемую амином, с амином формулы R3NH2. Уходящая группа -O-R35 может представлять собой -О-С1-4алкил (в частности, -O-Et) или -O-S(O)2-R37, где R37 представляет собой C1-8алкил (например, С1-4алкил или С1-2алкил, такой как метил), С1-6фторалкил (например, С1-4фторалкил или С1-2фторалкил, такой как CF3 или С4F9), или фенил, где фенил возможно замещен одним или двумя из независимых С1-2алкила, галогена или С1-2алкокси (такой как фенил или 4-метил-фенил). Эту реакцию можно проводить с растворителем или без растворителя, и она может требовать нагревания:
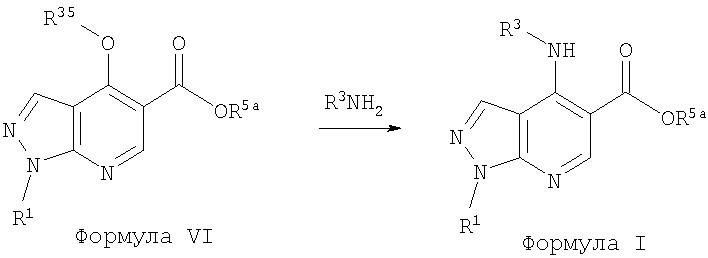
Соединения формулы (VI) (также описанные в приведенной выше ссылке) могут быть получены путем взаимодействия соединения формулы (VII) с подходящим алкилирующим агентом формулы R1-X, где Х представляет собой уходящую группу, такую как галоген. Эту реакцию предпочтительно проводят в присутствии основания, такого как карбонат калия, в безводном растворителе, таком как DMF (диметилформамид):
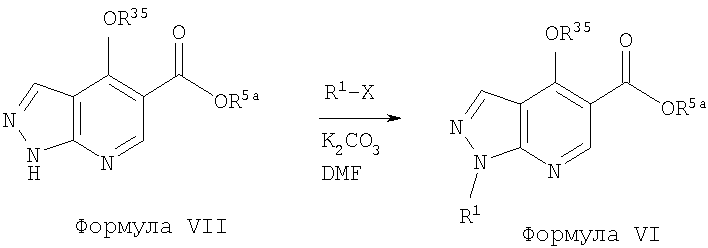
Получение соединений формулы VII, например, где OR35 представляет собой OEt, путем окислительного расщепления соединений формулы VIII описано Bare et al. в J. Med. Chem., 1989, 32, 2561-2573 (дополнительная ссылка на Zuleski et al. в J. Drug. Metab. Dispos., 1985, 13, 139).
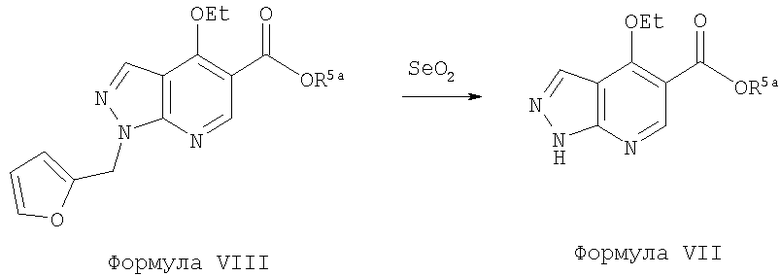
В другом воплощении способа В соединение формулы (VI) может быть заменено соединением формулы (VIA), где Х представляет собой NR4R5 или OR5a, как определено здесь:
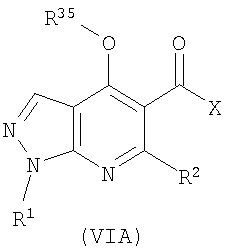
В данном воплощении способа В соединение формулы (VIA) взаимодействует с амином формулы R3NH2.
Способ Г
Для образования соединения формулы (I), где Х=NR4R5, соединение формулы (I), но где Х=ОН (карбоновая кислоту, соединение формулы (IX), как определено ниже) можно превратить в активированное соединение формулы (I), но где Х = уходящая группа X1, замещаемая амином (соединение формулы (X), как определено ниже, где X1 представляет собой уходящую группу, замещаемую амином); и затем активированное соединение можно подвергнуть взаимодействию с амином формулы R4R5NH:
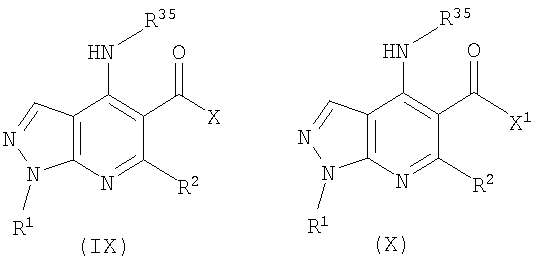
Например, активированное соединение (соединение формулы (X)) может представлять собой хлорангидрид, то есть активированное соединение формулы (I), но где уходящая группа X1=Cl. Это соединение может быть образовано из карбоновой кислоты (X=ОН, соединение формулы (IX)), например путем взаимодействия с тионилхлоридом, либо в органическом растворителе, таком как хлороформ, либо без растворителя. Смотри, например, Примеры 81-85. Альтернативно, активированное соединение (соединение формулы (X)) может представлять собой активированный сложный эфир, где уходящая группа X1 представляет собой
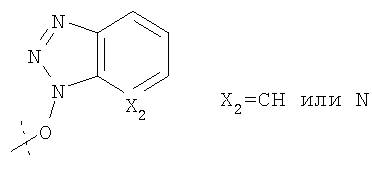
Это последнее активированное соединение формулы (X) может быть образовано из карбоновой кислоты (X=ОН, соединение формулы (IX))
либо:
(а) путем взаимодействия карбоновой кислоты с карбодиимидом, таким как EDC, который представляет собой 1-этил-3-(3'-диметиламинопропил)карбодиимид, а также 1-(3-диметиламинопропил)-3-этилкарбодиимид или его соль, например гидрохлорид, предпочтительно с последующим взаимодействием полученного в результате продукта с 1-гидроксибензотриазолом (НОВТ); причем реакцию (а) обычно проводят в присутствии растворителя (предпочтительно безводного), такого как диметилформамид (DMF) или ацетонитрил, и/или предпочтительно в безводных условиях и/или обычно при комнатной температуре (например, от приблизительно 20 до приблизительно 25°С);
либо
(б) путем взаимодействия с 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония тетрафторборатом (TBTU) или O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфатом (HATU) в присутствии основания, такого как диизопропилэтиламин (iPr2Net=DIPEA), и обычно в присутствии растворителя, такого как диметилформамид (DMF) или ацетонитрил, и/или предпочтительно в безводных условиях и/или обычно при комнатной температуре (например, от приблизительно 20 до приблизительно 25°С).
Карбоновую кислоту, где Х=ОН (соединение формулы (IX) ниже), обычно получают путем гидролиза соответствующего сложного эфира формулы (I), где Х представляет собой OR5a. Сам этот эфир может быть получен любым из способов А, В, Д или Е, как описано здесь.
Способ Г1
Этот способ является аналогичным способу Г, но включает взаимодействие активированного соединения формулы (X), где X1 = уходящая группа, замещаемая амином (например, уходящая группа, как определено здесь), с амином формулы R4R5NH.
Способ Д
Соединения формулы (I) могут быть получены путем взаимодействия соединения формулы (XI) с алкилирующим агентом формулы R1-X3, где X3 представляет собой уходящую группу, замещаемую атомом азота, находящемся в 1-м положении пиразолопиридина в соединении формулы (XI):
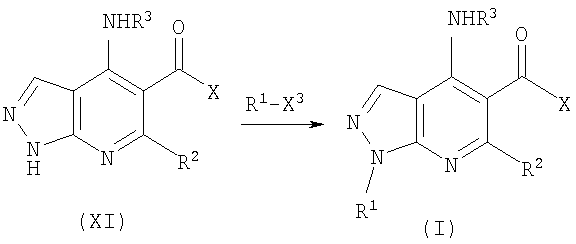
Можно использовать подходящий алкилирующий агент формулы R1-X3. Например, X3 может представлять собой атом галогена, такой как атом хлора, или более предпочтительно атом брома или йода, либо X3 может представлять собой -O-S(O)2-R36, где R36 представляет собой С1-8алкил (например, С1-4алкил или С1-2алкил, такой как метил), С1-6фторалкил (например, С1-4фторалкил или С1-2фторалкил, такой как CF3 или C4F9), или фенил, где фенил возможно замещен одним или двумя заместителями из, независимо, С1-2алкила, галогена или С1-2алкокси (такой как фенил или 4-метил-фенил). Эту реакцию предпочтительно проводят в присутствии основания; это основание может, например, содержать или представлять собой карбонат калия, карбонат натрия, гидрид натрия, гидрид калия или основную смолу, или полимер, такой как связанный с полимером 2-трет-бутиламино-2-диэтиламино-1,3-диметил-пергидро-1,3,2-диазафосфорин. Эту реакцию предпочтительно проводят в присутствии растворителя, например органического растворителя, такого как DMF; этот растворитель предпочтительно является безводным. Примеры способа алкилирования Д включают Примеры 183, 185, 186 и 354.
Предпочтительные способы получения соединений формулы (XI) смотри, например, (ссылка) в Примерах 19-20 и Промежуточных соединениях 48 и 54А.
Способ Е: Превращение одного соединения формулы (I) или его соли в другое соединение формулы (I) или его соль
Одно соединение формулы (I) или его соль можно превратить в другое соединение формулы (I) или его соль. Это превращение предпочтительно включает в себя или представляет собой один или более чем один из приведенных ниже способов Е1-Е10.
Е1. Способ окисления. Например, способ окисления может включать в себя или представлять собой окисление спирта до кетона (например, с использованием реагента Джонса, например, см. Пример 205) или окисление спирта или кетона до карбоновой кислоты. Способ окисления может, например, включать в себя или представлять собой превращение азотсодержащего соединения формулы (I) или его соли в соответствующий N-оксид (например, с использованием мета-хлорпероксибензойной кислоты), например превращение пиридинсодержащего соединения в соответствующий N-оксид пиридина (например, Примеры 210-212).
Е2. Способ восстановления, например восстановление кетона или карбоновой кислоты до спирта.
Е3. Ацилирование, например ацилирование амина (например, Примеры 329-349, Пример 353) или гидроксигруппы.
Е4. Алкилирование, например алкилирование амина или гидроксигруппы.
Е5. Гидролиз, например гидролиз эфира до соответствующей карбоновой кислоты или ее соли (например, Примеры 351, 488, 489, 650, 651).
Е6. Удаление защиты, например удаление защиты (например, дезацилирование или удаление трет-бутоксикарбонила (ВСЮ)) аминогруппы (например, Примеры 320, (321) и (352)).
Е7. Образование сложного эфира или амида, например из соответствующей карбоновой кислоты.
Е8. Превращение кетона в соответствующий оксим (например, Примеры 652, 653, 654 и 680-686).
Е9. Сульфонилирование, например образование сульфонамида путем взаимодействия амина с сульфонилгалогенидом, например сульфонилхлоридом (например, Примеры 322-328).
и/или
Е10. Превращение одного соединения формулы (I) в другое соединение формулы (I) в результате перегруппировки Бекмана, предпочтительно с использованием цианурхлорида (2,4,6-трихлор-1,3,5-триазина) вместе с формамидом, таким как DMF, при комнатной температуре (см. L.D.Luca, J. rg. Chem., 2002, 67, 6272-6274). Перегруппировка Бекмана может, например, включать превращение соединения формулы (I), где NHR3 имеет подформулу
(о2) (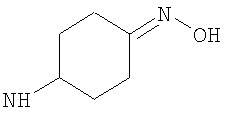 ) в соединение формулы (I), где NHR3- имеет подформулу
) в соединение формулы (I), где NHR3- имеет подформулу
(m3) (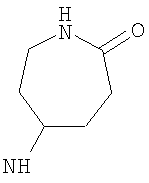 ), например, как показано в Примерах 658 и 659.
), например, как показано в Примерах 658 и 659.
В настоящем изобретении, таким образом, также предложен способ получения соединения формулы (I) или его соли:

где R1, R2 и R3 такие, как определено здесь, и Х представляет собой NR4R5 или OR5a, как определено здесь, включающий:
(а) для соединения формулы (I), где Х представляет собой OR5a, взаимодействие соединение формулы (IIA):
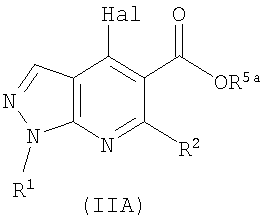
где Hal представляет собой атом галогена (такой как атом брома или предпочтительно атом хлора), с амином формулы R3NH2, либо
(б) для соединения формулы (I), где Х=NR4R5, взаимодействие соединения формулы (IVA):
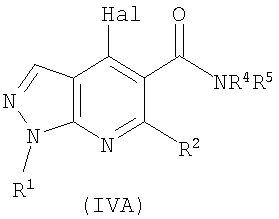
где Hal представляет собой атом галогена (такой как атом брома или предпочтительно атом хлора), с амином формулы R3NH2, либо
(в) взаимодействие соединения формулы (VIA):
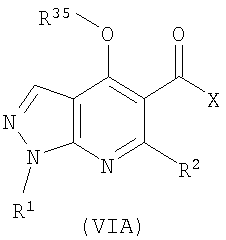
в котором -O-R35 представляет собой уходящую группу, замещаемую амином (такую как -О-С1-4алкил или -O-S(O)2R37),
с амином формулы R3NH2; либо
(г) для образования соединения формулы (I), где Х=NR4R5, превращение соединения формулы (IX) в активированное соединение формулы (X), где X1=уходящая группа, замещаемая амином:
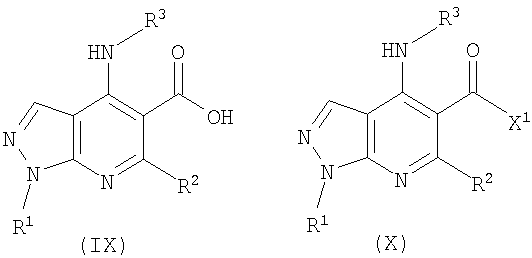
с последующим взаимодействием активированного соединения формулы (X) с амином формулы R4R5NH; либо
(г1) для образования соединения формулы (I), где Х=NR4R5, взаимодействие активированное соединение формулы (X), как определено выше, с амином формулы R4R5NH; либо
(д) взаимодействие соединения формулы (XI):
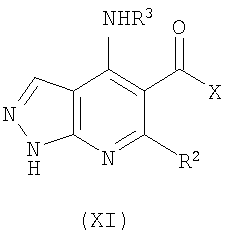
с алкилирующим агентом формулы R1-X2, где X2 представляет собой уходящую группу, замещаемую атомом азота, находящимся в 1-м положении пиразолопиридина в соединении формулы (XI); либо
(е) превращение одного соединения формулы (I) или его соли в другое соединение формулы (I) или его соль;
и, возможно, превращение соединения формулы (I) в его соль, например в его фармацевтически приемлемую соль.
В способах (г) и/или (г1) активированное соединение формулы (X), где X1 = уходящая группа, замещаемая амином, может представлять собой хлорангидрид, то есть активированное соединение формулы (X), где X1=Cl. Альтернативно, активированное соединение формулы (X) может представлять собой активированный сложный эфир, где уходящая группа X1 представляет собой
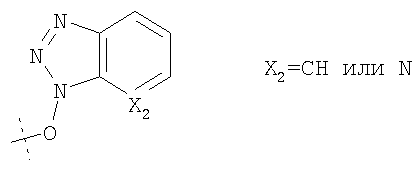
Предпочтительные признаки способов (а), (б), (в), (г), (г1) и (д) независимо друг от друга являются такими, как описаны выше для способов А, Б, В, Г, Г1 и Д, со всеми произведенными необходимыми изменениями.
В настоящем изобретении также предложен: (ж) способ получения фармацевтически приемлемой соли соединения формулы (I), включающий превращение соединения формулы (I) или его соли в его нужную фармацевтически приемлемую соль. (См., например, Примеры 490, 491, 518А, 593).
В настоящем изобретении также предложено соединение формулы (I) или его соль, полученные способом, как определено здесь.
Медицинские применения
В настоящем изобретении также предложено соединение формулы (I) или его фармацевтически приемлемая соль для применения в качестве активного терапевтического вещества у млекопитающего, такого как человек. Это соединение или соль может иметь применение в лечении и/или профилактике любого из заболеваний/состояний, описанных здесь (например, для применения в лечении и/или профилактике воспалительного и/или аллергического заболевания у млекопитающего), и/или для применения в качестве ингибитора фосфодиэстеразы, например для применения в качестве ингибитора фосфодиэстеразы 4 (PDE4).
"Терапия" может включать лечение и/или профилактику.
Также предложено применение соединения формулы (I) или его фармацевтически приемлемой соли в изготовлении лекарства (например, фармацевтической композиции) для лечения и/или профилактики любого из заболеваний/состояний, описанных здесь, у млекопитающего, такого как человек, например для лечения и/или профилактики воспалительного и/или аллергического заболевания у млекопитающего, такого как человек.
Также предложен способ лечения и/или профилактики любого из заболеваний/состояний, описанных здесь, у млекопитающего (например, человека), нуждающегося в этом, например способ лечения и/или профилактики воспалительного и/или аллергического заболевания у млекопитающего (например, человека), нуждающегося в этом, включающий введение этому млекопитающему (например, человеку) терапевтически эффективного количества соединения формулы (I), как определено здесь, или его фармацевтически приемлемой соли.
Ингибиторы фосфодиэстеразы 4 считаются полезными в лечении и/или профилактике ряда заболеваний/состояний, особенно воспалительных и/или аллергических заболеваний, у млекопитающих, таких как люди, например: астмы, хронической обструктивной болезни легких (COPD) (например, хронического бронхита и/или эмфиземы), атопического дерматита, крапивницы, аллергического ринита, аллергического конъюнктивита, весеннего конъюнктивита, эозинофильной гранулемы, псориаза, ревматоидного артрита, септического шока, неспецифического язвенного колита, болезни Крона, реперфузионного повреждения миокарда и головного мозга, хронического гломерулонефрита, эндотоксического шока, респираторного дистресс-синдрома взрослых, рассеянного склероза, когнитивного нарушения (например, при неврологическом расстройстве, таком как болезнь Альцгеймера), депрессии или боли. Неспецифический язвенный колит и болезнь Крона часто вместе упоминаются как воспалительное кишечное заболевание.
При лечении и/или профилактике воспалительное и/или аллергическое заболевание предпочтительно представляет собой хроническую обструктивную болезнь легких (COPD), астму, ревматоидный артрит или аллергический ринит у млекопитающего (например, человека). Более предпочтительно, лечение и/или профилактика представляет собой лечение и/или профилактику COPD или астмы у млекопитающего (например, человека).
Ингибиторы PDE4 считаются эффективными в лечении астмы (например, см. М.A.Giembycz, Drugs, Feb. 2000, 59(2), 193-212; Z.Huang et al., Current Opinion in Chemical Biology, 2001, 5: 432-438; H.J.Dyke et al., Expert Opinion on Investigational Drugs, January 2002, 11(1), 1-13; С.Burnout et al., Current Pharmaceutical Design, 2002, 8(14), 1255-1296; A.М.Doherty, Current Opinion Chem. Biol., 1999, 3(4), 466-473 и ссылки, указанные в этих работах).
Ингибиторы PDE4 считаются эффективными в лечении COPD (например, см. S.L.Wolda, Emerging Drugs, 2000, 5(3), 309-319; Z.Huang et al., Current Opinion in Chemical Biology, 2001, 5: 432-438; H.J.Dyke et al., Expert Opinion on Investigational Drugs, January 2002, 11(1), 1-13; С.Burnout et al., Current Pharmaceutical Design, 2002, 8(14), 1255-1296; A.M.Doherty, Current Opinion Chem. Biol., 1999, 3(4), 466-473 и ссылки, указанные в этих работах). COPD часто характеризуется наличием обструкции дыхательных путей вследствие хронического бронхита и/или эмфиземы (S.L.Wolda, Emerging Drugs, 2000, 5(3), 309-319).
Ингибиторы PDE4 считаются эффективными в лечении аллергического ринита (например, см. В.M.Schmidt et al., J.Allergy & Clinical Immunology, 108(4), 2001, 530-536).
Ингибиторы PDE4 считаются эффективными в лечении ревматоидного артрита и рассеянного склероза (например, см. H.J.Dyke et al., Expert Opinion on Investigational Drugs, January 2002, 11(1), 1-13; С.Burnouf et al., Current Pharmaceutical Design, 2002, 8(14), 1255-1296 и A.M.Doherty, Current Opinion Chem. Biol., 1999, 3(4), 466-473, а также ссылки, указанные в этих работах). Смотри, например, A.M.Doherty, Current Opinion Chem. Biol., 1999, 3(4), 466-473, и ссылки, указанные там, для применения при атопическом дерматите.
Предполагают, что ингибиторы PDE4 обладают анальгезирующими свойствами и, следовательно, эффективны в лечении боли (A.Kumar et al., Indian J. Exp. Biol., 2000, 38(1), 26-30).
Согласно изобретению можно проводить лечение и/или профилактику когнитивного нарушения, например когнитивного нарушения при неврологическом расстройстве, таком как болезнь Альцгеймера. Например, лечение и/или профилактика может включать когнитивное улучшение, например, при неврологическом расстройстве. Смотри, например, H.Т.Zhang et al. в Psychopharmacology, June 2000, 150(3), 311-316 и Neuropsychopharmacology, 2000, 23(2), 198-204; и Т.Egawa et al., Japanese J. Pharmacol., 1997, 75(3), 275-81.
Предполагается, что ингибиторы PDE4, такие как ролипрам, обладают антидепрессантными свойствами (например, J.Zhu et al., CNS Drug Reviews, 2001, 7(4), 387-398; O'Donnell, Expert Opinion on Investigational Drugs, 2000, 9(3), 621-625; и Н.Т.Zhang et al. Neuropsychopharmacology, October 2002, 27(4): 587-585).
Фармацевтические композиции и дозировка
Для применения в медицине соединения по настоящему изобретению обычно вводят в виде фармацевтической композиции.
Таким образом, в в следующем аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, и один или более чем один фармацевтически приемлемый носитель и/или эксципиент.
Фармацевтическая композиция может быть предназначена для применения в лечении и/или профилактике любого из состояний, описанных здесь.
В данном изобретении также предложен способ изготовления фармацевтической композиции, содержащей соединение формулы (I), как определено здесь, или его фармацевтически приемлемую соль, и один или более чем один фармацевтически приемлемый носитель и/или эксципиент, при котором смешивают соединение или соль с одним или более фармацевтически приемлемыми носителями и/или эксципиентами.
В данном изобретении также предложена фармацевтическая композиция, изготовленная указанным способом.
Соединения формулы (I) и/или фармацевтическую композицию можно вводить, например, путем перорального, парентерального (например, внутривенного, подкожного или внутримышечного), ингаляционного или назального введения. Соответственно, фармацевтическая композиция предпочтительно пригодна для перорального, парентерального (например, внутривенного, подкожного или внутримышечного), ингаляционного или назального введения. Более предпочтительно, фармацевтическая композиция пригодна для ингаляционного или перорального введения, например, млекопитающему, такому как человек. Ингаляционное введение включает местное введение в легкое, например, при помощи аэрозольной или сухой порошкообразной композиции. Пероральное введение человеку является наиболее предпочтительным.
Фармацевтическая композиция, пригодная для перорального введения, может быть жидкой или твердой, например, она может представлять собой сироп, суспензию или эмульсию, таблетку, капсулу или лепешку.
Жидкий препарат в общем случае будет состоять из суспензии или раствора соединения или фармацевтически приемлемой соли в фармацевтически приемлемом(ых) жидком(их) носителе(ях), например в водном растворителе, таком как вода, этанол или глицерин, или в неводном растворителе, таком как полиэтиленгликоль или масло. Препарат также может содержать суспендирующий агент, консервант, вкусоароматизирующий и/или красящий агент.
Фармацевтическая композиция, пригодная для перорального введения, представляющая собой таблетку, может содержать один или более чем один фармацевтически приемлемый носитель и/или эксципиент, пригодный для изготовления таблеточных препаратов. Примеры таких носителей включают лактозу и целлюлозу. Таблетка может также или вместо этого содержать один или более чем один фармацевтически приемлемый эксципиент, например связующие агенты, смазывающие агенты, такой как стеарат магния, и/или разрыхлители для таблеток.
Фармацевтическая композиция, пригодная для перорального введения, представляющая собой капсулу, может быть получена с использованием способов инкапсулирования. Например, гранулы, содержащие активный ингредиент, могут быть получены с использованием фармацевтически приемлемого носителя, а затем заполнены в твердую желатиновую капсулу. Альтернативно, дисперсия или суспензия может быть получена с использованием любого подходящего фармацевтически приемлемого носителя, например водной смолы или масла, и затем эту дисперсию или суспензию заполняют в мягкую желатиновую капсулу.
Предпочтительно композиция находится в стандартной лекарственной форме, такой как таблетка или капсула для перорального введения, например для перорального введения человеку.
Парентеральная композиция может содержать раствор или суспензию соединения или фармацевтически приемлемой соли в стерильном водном носителе или парентерально приемлемом масле. Альтернативно, этот раствор может быть лиофилизирован; лиофилизированная парентеральная фармацевтическая композиция может быть восстановлена подходящим растворителем непосредственно перед введением.
Композиции для назального или ингаляционного введения можно легко изготовить в виде аэрозолей, капель, гелей или сухих порошков.
Аэрозольные препараты, например для ингаляционного введения, могут содержать раствор или мелкодисперсную суспензию активного вещества в фармацевтически приемлемом водном или неводном растворителе. Аэрозольные препараты могут быть представлены в однократных или многодозовых количествах в стерильной форме в герметичном контейнере, который может принимать форму картриджа или повторно наполняться для применения с распыляющим устройством или ингалятором. Альтернативно, герметичный контейнер может представлять собой единичное дозирующее устройство, такое как назальный ингалятор с однократной дозой или аэрозольный диспенсер, оборудованный мерным клапаном (ингалятор с отмеряемой дозой), который предназначен для использования, пока содержимое контейнера полностью не израсходуется.
Когда лекарственная форма включает в себя аэрозольный диспенсер, она предпочтительно содержит подходящий пропеллент под давлением, такой как сжатый воздух, диоксид углерода или органический пропеллент, такой как хлорфторуглерод (CFC) или фторуглеводород (HFC). Подходящие CFC-пропелленты включают дихлордифторметан, трихлорфторметан и дихлортетрафторэтан. Подходящие HFC-пропелленты включают 1,1,1,2,3,3,3-гептафторпропан и 1,1,1,2-тетрафторэтан. Аэрозольные лекарственные формы могут также принимать форму накачиваемого распылителя.
Для фармацевтических композиций, пригодных и/или адаптированных для ингаляционного введения, предпочтительно, чтобы соединение или соль формулы (I) находилось в форме с уменьшенным размером частиц, и более предпочтительно эту форму с уменьшенным размером частиц получают или могут получить путем микронизации. Микронизация обычно включает воздействие на соединение/соль ударных сил и сил трения в высокоскоростном циркулярном или спиральном/вихревом потоке воздуха, часто включая циклонный компонент. Предпочтительный размер частиц (например, значение D50 (средний размер частиц)) соединения или соли с уменьшенным размером частиц (например, микронизированного) составляет от приблизительно 0,5 до приблизительно 10 микрон, например от приблизительно 1 до приблизительно 5 микрон (например, на основании измерения с использованием лазерной дифракции). Например, для соединения или соли формулы (I) предпочтительно иметь размер частиц, определенный так: D10 от приблизительно 0,3 до приблизительно 3 микрон (например, приблизительно 1 микрон), и/или D50 от приблизительно 1 до приблизительно 5 микрон (например, приблизительно 2-5 или приблизительно 2-3 микрона), и/или D90 от приблизительно 2 до приблизительно 20 микрон или от приблизительно 3 до приблизительно 10 микрон (например, приблизительно 5-8 или приблизительно 5-6 микрон), например, на основании измерения с использованием лазерной дифракции. При измерении посредством лазерной дифракции можно использовать сухой способ (суспензия соединения/соли в потоке воздуха пересекает луч лазера) или влажный способ [суспензия соединения/соли в жидкой дисперсионной среде, такой как изооктан или (например, если соединение растворимо в изооктане) 0,1%-ный Твин-80 в воде, пересекает луч лазера]. На основании лазерной дифракции размер частиц вычисляют, предпочтительно используя расчет Фраунхофера; и/или предпочтительно для измерения используют аппарат Malvern Mastersizer либо Sympatec.
Далее приведен иллюстративный неограничивающий пример процесса микронизации в небольшом масштабе.
Пример микронизации: микронизация Примера 518 или 518А
Цель: микронизировать приблизительно 600-1000 мг Примера 518 или 518А (описано здесь ниже), используя Jetpharma MC1 микронизатор.
Исходные (немикронизированные) и микронизированные вещества анализировали в отношении размера частиц посредством лазерной дифракции и в отношении кристалличности посредством PXRD (дифракции рентгеновский лучей на порошке).
Оборудование и материал
Jetpharma MC1 микронизатор содержит горизонтальный дискообразный измельчительный бокс, имеющий: трубчатый ввод для соединения (например, под углом приблизительно 30 градусов к горизонтали) для введения суспензии немикронизированного соединения формулы (I) или соли в потоке газа, отдельный ввод для газов для ввода газов, выпуск для газов для выхода газов и сосуд-коллектор для сбора микронизированного вещества. Измельчительный бокс имеет две камеры: наружную кольцевую камеру с газовым соединением с вводом газа, эта камера служит для приема сжатого газа (например, воздуха или азота), внутреннюю дискообразную измельчительную камеру внутри и соосно наружной камере для микронизации внесенного соединения/соли, причем эти две камеры разделены кольцеобразной стенкой. Кольцеобразная стенка (кольцо R) имеет множество отверстий малого диаметра, соединяющих внутреннюю и наружную камеры и расположенных по окружности на расстоянии вокруг кольцеобразной стенки. Отверстия, открытые во внутреннюю камеру, направлены под углом (направление промежуточное между радиальным и тангенциальным), и при использовании действуют как форсунки, направляющие сжатый газ с высокой скоростью из наружной камеры во внутреннюю камеру и по внутренней спирали (вихрь) вокруг внутренней камеры (циклона). Ввод соединения находится в газовом соединении с внутренней камерой через форсунку, направленную тангенциально к внутренней камере, в пределах и около кольцеобразной стенки. Верхний и нижний выход с большим диаметром выходят в центральную ось внутренней измельчительной камеры, соединенные с (а) (нижний выход) сосудом-сборником, который не имеет выхода воздуха, и (б) (верхний выход) газовым выходом, который ведет к сборнику, фильтру и газовой выпускной трубе. Внутри трубчатого ввода для соединения и продольно-подвижно в его пределах расположен ввод в виде трубки Вентури (V) для ввода газов. Ввод для соединения также имеет разветвленное соединение с направленным вверх впускным каналом для для вносимого вещества.
При использовании узкая головка трубки Вентури (V) предпочтительно расположена вниз и слегка вперед по отношению к впускному каналу для вещества, так что, когда трубка Вентури доставляет сжатый газ (например, воздух или азот), подаваемое вещество всасывается в газовый поток через ввод для соединения и разгоняет его во внутреннюю измельчительную камеру тангенциально с дозвуковой скоростью. Внутри измельчительной камеры вещество дополнительно ускоряется до сверхзвуковой скорости посредством системы отверстий/форсунок вокруг кольца (R) (кольцеобразная стенка) измельчительной камеры. Форсунки расположены слегка под углом, так что модель ускорения вещества имеет форму направленного внутрь вихря или циклона. Вещество внутри измельчительной камеры быстро циркулирует, и во время этого процесса происходят соударения частиц, что вызывает дробление частиц большего размера на более мелкие. "Центрифужное" ускорение в вихре заставляет частицы большего размера оставаться на периферии внутренней камеры, тогда как все более мелкие частицы движутся ближе к центру до тех пор, пока не выходят из измельчительной камеры, обычно через нижний выход, при низком давлении и низкой скорости. Частицы, которые выходят из измельчительной камеры, тяжелее воздуха и осаждаются вниз через нижний выход в сосуд-сборник, тогда как отработанный газ поднимается (вместе с меньшинством мелких частиц микронизированного вещества) и уходит в атмосферу при низком давлении и низкой скорости.
Процедура
Собирают микронизатор. Расстояние от выступающей части трубки Вентури до входного канала регулируют до 1,0 см соответственно (например, так, чтобы узкая головка трубки Вентури на вводе располагалась вниз и слегка вперед по отношению к входному каналу вещества) и измеряют с помощью микроштангенциркуля, чтобы убедиться, что она вставлена правильно. Давление в кольце (R) и трубке Вентури (V) регулируют в соответствии со значениями, уточненными в экспериментальной модели (смотри приведенный ниже экспериментальный раздел), путем регулирования клапанов на манометрах микронизатора. Установку проверяют на утечку, наблюдая, есть ли какие-либо колебания в показаниях манометров.
Следует отметить, что в трубке Вентури (V) поддерживают давление по меньшей мере на 2 бара (105 Па) выше, чем давление в кольце (R), чтобы предотвратить заброс вещества, например, наружу из входного канала для вещества.
Точность весов проверяют с помощью калибровочных масс. Определенное количество исходного вещества (см. раздел по ходу эксперимента) взвешивают в пластмассовой ванночке для взвешивания. Затем это вещество подают в микронизатор, используя вибрационный шпатель (например, V-образный в поперечном сечении) при определенной скорости подачи. На протяжении процесса измельчения контролируют время подачи вещества и показатели давления в оборудовании.
После завершения процесса микронизации отключают подачу азота, и по сборнику слабо постукивают, чтобы дать возможность частицам осесть в сосуд для улавливания/сбора на дне микронизатора. Сборник удаляют и отставляют в сторону. Микронизированный порошок в улавливающем сосуде (сосуде-сборнике) и циклоне (над улавливающим сосудом) собирают по отдельности в разные взвешенные + помеченные флаконы для сбора. Массу микронизированного вещества записывают. Микронизатор разбирают, и остаточное PDE4-соединение на внутренней поверхности микронизатора промывают смесью 70/30 изопропиловый спирт/вода и собирают в колбу. Затем микронизатор тщательно очищают путем промывания и протирания с подходящим растворителем и сушат перед проведением следующих действий.
Предпочтительные экспериментальные параметры
Исходное (немикронизированное) вещество (Методика 1): Пример 518 или 518А
Исходное (немикронизированное) вещество (Методика 2): Пример 518
Используемые весы: Sartorius аналитические
Глубина ввода трубки Вентури: 10,0 мм
Приведенные выше параметры можно варьировать, используя знания специалистов в данной области техники.
Результаты и/или наблюдения
% выхода=[(Вещество из сосуда + Вещество из циклона)/количество внесенного вещества]×100
В целом очень приблизительно 50-75%-ные выходы достигаются с использованием этого способа.
Процедура 1 не была завершена.
В процедуре 2 получали выход 70,8% (0,6427 г) микронизированного вещества из Примера 518, включая вещество из сосуда-сборника и вещество с внутренних стенок циклона.
Анализ размера частиц измельченного вещества из Примера 518 из процедуры 2 с использованием измерения посредством лазерной дифракции с помощью Malvern Mastersizer с удлиненным основанием, дисперсионная среда 0,1%-ный Твин-80 в воде, скорость перемешивания 1500 об/мин, 3 мин обработки ультразвуком перед конечной диспергированием и анализом, линзы 300 RF (обратного Фурье-преобразования), вычисление Фраунхофера с программным обеспечением Malvern:
- вещество из сосуда-сборника: D10=0,97 микрон, D50=3,86 микрон, D90=12,64 микрон;
- вещество с внутренних стенок циклона: D10=0,95 микрон, D50=3,42 микрон, D90=9,42 микрон.
Альтернативное воплощение: Примеры соединений/солей по изобретению, иные, чем Примеры 518 или 518А, могут быть микронизированы.
Для фармацевтических композиций, пригодных и/или адаптированных для ингаляционного введения, предпочтительно, чтобы фармацевтическая композиция представляла собой сухую порошкообразную пригодную для ингаляции композицию. Такая композиция может содержать порошковую основу, такую как лактоза или крахмал, соединение формулы (I) или его соль (предпочтительно в форме с уменьшенным размером частиц, например в микронизированной форме) и, возможно, модификатор характеристик, такой как L-лейцин, маннит, трегалоза и/или стеарат магния. Предпочтительно эта сухая порошкообразная пригодная для ингаляции композиция содержит сухую порошкообразную смесь лактозы и соединения формулы (I) или его соли. Лактоза предпочтительно представляет собой гидрат лактозы, например моногидрат лактозы, и/или предпочтительно представляет собой лактозу ингаляционного сорта и/или тонкоизмельченную лактозу. Предпочтительный размер частиц лактозы характеризуется как 90% или более (по массе или по объему) частиц лактозы имеют диаметр менее 1000 микрон (микрометров) (например, 10-1000 микрон, например 30-1000 микрон), и/или 50% или более частиц лактозы имеют диаметр менее 500 микрон (например, 10-500 микрон). Более предпочтительно размер частиц лактозы характеризуется как 90% или более частиц лактозы имеют диаметр менее 300 микрон (например, 10-300 микрон, например 50-1000 микрон), и/или 50% или более частиц лактозы имеют диаметр менее 100 микрон. Возможно, размер частиц лактозы характеризуется как 90% или более частиц лактозы имеют диаметр менее 100-200 микрон, и/или 50% или более частиц лактозы имеют диаметр менее чем 40-70 микрон. Наиболее важно, чтобы предпочтительно от приблизительно 3 до приблизительно 30% (например, приблизительно 10%) (по массе или по объему) частиц были диаметром менее 50 микрон или менее 20 микрон. Например, без ограничения, подходящей лактозой ингаляционного сорта является лактоза Е9334 (10% мелкой фракции) (Borculo Domo Ingredients, Hanzeplein 25, 8017 JD Zwolle, Netherlands).
В сухой порошкообразной подходящей для ингаляции композиции соединение формулы (I) или его соль предпочтительно присутствует в количестве от приблизительно 0,1% до приблизительно 70% (например, от приблизительно 1% до приблизительно 50%, например, от приблизительно 5% до приблизительно 40%, например, от приблизительно 20 до приблизительно 30%) мас./мас. композиции.
Далее следует иллюстративный не ограничивающий пример сухой порошкообразной ингаляционной композиции.
Пример сухого порошкообразного препарата - Сухой порошкообразный препарат лактозной смеси
Используя форму с уменьшенным размером частиц, то есть микронизированную форму соединения формулы (I) или его соли (например, такую, как получена в приведенном выше примере микронизации), сухую порошкообразную смесь готовят путем смешивания нужного количества соединения/соли (например, 10 мг, 1% мас./мас.) с лактозой ингаляционного сорта, содержащей 10% мелкой фракции (например, 990 мг, 99% мас./мас.) в Teflon™ (политетрафторэтеновом) сосуде в Mikro-дезинтегрирующей шаровой мельнице (но без шарикоподшипника) при 3/4 скорости (приблизительно 2000-2500 об/мин) в течение приблизительно 4 часов при каждой концентрации смеси. Mikro-дезинтегратор (имеется в продаже у В.Braun Biotech International, Schwarzenberger Weg 73-79, D-34212 Melsungen, Germany; www.bbraunbiotech.com) содержит основу с выступающим вверх и вибрирующим в стороны плечом, к которому прикреплен сосуд из Teflon™. Перемешивание достигается за счет вибрации плеча.
Другие смеси: 10% мас./мас. соединение/соль (50 мг) + 90% мас./мас. лактозы (450 мг, лактоза ингаляционного сорта, содержащая 10% мелкой фракции).
В результате последовательного разведения 1%-ной мас./мас. смеси можно получить, например, 0,1%-ные и 0,3%-ные мас./мас. смеси.
Возможно, в частности для сухих порошкообразных пригодных для ингаляции композиций, фармацевтическая композиция для ингаляционного введения может быть включена во множество герметичных дозировочных контейнеров (например, содержащих сухую порошкообразную композицию), установленных продольно в полосе или ленте внутри подходящего ингаляционного устройства. Этот контейнер можно вскрыть или с него снять оболочку при необходимости, и доза, например, сухой порошкообразной композиции может быть введена путем ингаляции через устройство, такое как устройство DISKUS™, продаваемое GlaxoSmithKline. Ингаляционное устройство DISKUS™ обычно является по существу таким, как описано в GB 2242134 А. В аком устройстве по меньшей мере один контейнер для фармацевтической композиции в порошкообразной форме (по меньшей мере один контейнер, предпочтительно представляющий собой множество герметичных дозировочных контейнеров, установленных продольно в полосе или ленте) находится между двумя элементами, соединенными легко отсоединяемым друг от друга способом; данное устройство содержит: средства, определяющие состояние открытия по меньшей мере для одного контейнера; средства для отсоединения элементов друг от друга в состоянии открытия для открытия контейнера; и выход, сообщающийся с открытым контейнером, через который пользователь может вдыхать фармацевтическую композицию в порошкообразной форме из открытого контейнера.
В фармацевтической композиции одна или каждая стандартная доза для перорального или парентерального введения предпочтительно содержит от 0,01 до 3000 мг, более предпочтительно от 0,5 до 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли, рассчитанные по свободному основанию. Одна или каждая стандартная доза для назального или ингаляционного введения предпочтительно содержит от 0,001 до 50 мг, более предпочтительно от 0,01 до 5 мг соединения формулы (I) или его фармацевтически приемлемой соли, рассчитанной по свободному основанию.
Фармацевтически приемлемое соединение или соль по изобретению предпочтительно вводят млекопитающему (например, человеку) в суточной пероральной или парентеральной дозе от 0,001 мг до 50 мг на кг массы тела в сутки (мг/кг/сутки), например от 0,01 до 20 мг/кг/сутки, либо от 0,03 до 10 мг/кг/сутки, либо от 0,1 до 2 мг/кг/сутки соединения формулы (I) или его фармацевтически приемлемой соли, рассчитанной по свободному основанию.
Фармацевтически приемлемое соединение или соль по изобретению предпочтительно вводят млекопитающему (например, человеку) в суточной назальной или ингаляционной дозе от 0,0001 до 5 мг/кг/сутки, либо от 0,0001 до 1 мг/кг/сутки, например от 0,001 до 1 мг/кг/сутки, либо от 0,001 до 0,3 мг/кг/сутки, либо от 0,001 до 0,1 мг/кг/сутки, либо от 0,005 до 0,3 мг/кг/сутки соединения формулы (I) или его фармацевтически приемлемой соли, рассчитанной по свободному основанию.
Фармацевтически приемлемые соединения или соли по изобретению предпочтительно вводят в суточной дозе (для взрослого пациента), например в пероральной или парентеральной дозе от 0,01 мг до 3000 мг в сутки, либо от 0,5 до 1000 мг в сутки, например от 2 до 500 мг в сутки, или в назальной или ингаляционной дозе от 0,001 до 300 мг в сутки, либо от 0,001 до 50 мг в сутки, либо от 0,01 до 30 мг в сутки, либо от 0,01 до 5 мг в сутки, либо от 0,02 до 2 мг в сутки соединения формулы (I) или его фармацевтически приемлемой соли, рассчитанной по свободному основанию.
Комбинации
Соединения, соли и/или фармацевтические композиции согласно изобретению также можно применять в комбинации с другим терапевтически активным агентом, например агонистом β2адренорецептора, антигистаминным, противоаллергическим или противовоспалительным агентом.
В изобретении, таким образом, предложена в еще одном аспекте комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль вместе с другим терапевтически активным агентом, например агонистом β2-адренорецепторов, антигистаминным, противоаллергическим, противовоспалительным агентом или противоинфекционным агентом.
Предпочтительно агонист β2-адренорецепторов представляет собой салметерол (например, в виде рацемата или отдельного энантиомера, такого как R-энантиомер), сальбутамол, формотерол, салмефамол, фенотерол или тербуталин, либо его соль (например, фармацевтически приемлемую соль), например ксинафоатную соль салметерола, сульфатную соль или свободное основание сальбутамола либо фумаратную соль формотерола. Предпочтительными являются длительно действующие агонисты β2-адренорецепторов, особенно обладающие терапевтическим эффектом в течение 12-24-часового периода, такие как салметерол или формотерол. Предпочтительно агонист β2-адренорецепторов предназначен для ингаляционного введения, например, один раз в сутки и/или для одновременного ингаляционного введения; и более предпочтительно, агонист β2-адренорецептора находится в форме с уменьшенным размером частиц, например, как определено здесь. Предпочтительно комбинация агониста β2-адренорецептора предназначена для лечения и/или профилактики COPD или астмы. Салметерол или его фармацевтически приемлемую соль, например ксинафоат салметерола, предпочтительно вводят людям в ингаляционной дозе от 25 до 50 микрограммов два раза в сутки (измеренной по свободному основанию). Комбинация с агонистом β2-адренорецепторов может быть такой, как описано в WO 00/12078.
Предпочтительные длительно действующие агонисты β2-адренорецепторов включают те, которые описаны в WO 02/066422A, WO 03/024439, WO 02/070490 и WO 02/076933.
Особенно предпочтительные длительно действующие агонисты β2-адренорецепторов включают соединения формулы (XX) (описанные в WO 02/066422):
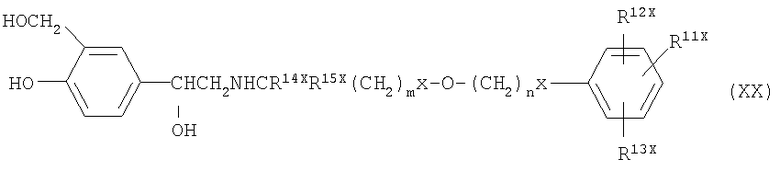
или их соли или сольваты, где в формуле (XX):
mX представляет собой целое число от 2 до 8;
nX представляет собой целое число от 3 до 11,
при условии, что mX+nX равно от 5 до 19,
R11X представляет собой -XSO2NR16XR17X, где Х представляет собой -(CH2)p X- или С2-6алкенилен;
R16X и R17X независимо выбраны из водорода, С1-6алкила, С3-7циклоалкила, C(O)NR18XR19X, фенила и фенил-(С1-4алкила)-,
либо R16X и R17X вместе с атомом азота, с которым они связаны, образуют 5-, 6- или 7-членное азотсодержащее кольцо, и каждый из R16X и R17X возможно замещены одной или двумя группами, выбранными из галогено, С1-6алкила, C1-6 галогеноалкила, С1-6алкокси, гидроксизамещенного С1-6алкокси, -CO2R18X, -SO2R18XR19X, -CONR18XR19X, -NR18XC(O)R19X или 5-, 6- или 7-членного гетероциклического кольца;
R18X и R19X независимо выбраны из водорода, С1-6алкила, С3-6циклоалкила, фенила и фенил-(С1-4алкила)-; и
pX представляет собой целое число от 0 до 6, предпочтительно от 0 до 4;
R12X и R13X независимо выбраны из водорода, С1-6алкила, С1-6алкокси, галогено, фенила и С1-6 галогеноалкила; и
R14X и R15X независимо выбраны из водорода и С1-4алкила, при условии, что общее число атомов углерода в R14X и R15X составляет не более чем 4.
Предпочтительные агонисты β2-адренорецепторов, раскрытые в WO 02/066422, включают:
3-(4-{[6-({(2R)-2-гидрокси-2-[4-гидрокси-3-(гидроксиметил)фенил]этил}амино)-гексил]окси}бутил)
бензолсульфонамид и
3-(3-{[7-({(2R)-2-гидрокси-2-[4-гидрокси-3-(гидроксиметил)-фенил]этил}амино)-гептил]окси}пропил)
бензолсульфонамид.
Предпочтительный агонист β2-адренорецепторов, раскрытый в WO 03/024439, представляет собой:
4-{(1R)-2-[6-{2-[2,6-дихлорбензил)окси]этокси}гексил)амино]-1-гидроксиэтил}-2-(гидроксиметил)фенол.
Комбинация соединения формулы (I) или соли вместе с антигистаминным агентом предпочтительно предназначена для перорального введения (например, в виде комбинированной композиции, такой как комбинированная таблетка) и может быть предназначена для лечения и/или профилактики аллергического ринита. Примеры антигистаминных агентов включают метапирилен или Н1-антагонисты, такие как цетиризин, лоратадин (например, Clarityn™), деслоратадин (например, Clarinex™) или фексофенадин (например, Allegra™).
В следующем аспекте в изобретении также предложена комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль вместе с антихолинергическим соединением, например с антагонистом мускариновых (М) рецепторов, в частности с антагонистом рецептора М1, М2, M1/M2 или М3-рецепторов, более предпочтительно с антагонистом М3-рецепторов, еще более предпочтительно с антагонистом М3-рецепторов, который является селективным антагонистом (например, является в 10 или более раз более сильным антагонистом) М3-рецепторов по сравнению с М1- и/или М2-рецепторами. Комбинации антихолинергических соединений/антагониста мускариновых (М) рецепторов с ингибиторами PDE4 смотри, например, в WO 03/011274 А2 и WO 02/069945 A2/US 2002/0193393 А1 и US 2002/052312 А1, и в некоторых или во всех из этих публикаций приведены примеры антихолинергических соединений/антагонистов мускариновых (М) рецепторов, которые можно использовать с соединениями формулы (I) или солями, и/или подходящих фармацевтических композиций. Например, антагонист мускариновых рецепторов может включать или представлять собой соль ипратропия (например, ипратропия бромид), соль окситропия (например, окситропия бромид) или более предпочтительно соль тиотропия (например, тиотропия бромид), смотри, например, тиотропий в ЕР 418716 А1.
Антихолинергическое соединение или антагонист мускариновых рецепторов, например антагонист М3-рецепторов, предпочтительно предназначен для ингаляционного введения, более предпочтительно в форме с уменьшенным размером частиц, например, как определено здесь. Более предпочтительно, как антагонист мускаринового (М) рецептора, так и соединение формулы (I) или его фармацевтически приемлемая соль предназначены для ингаляционного введения. Предпочтительно антихолинергическое соединение или антагонист мускариновых рецепторов и соединение формулы (I) или соль предназначены для одновременного введения. Комбинация с антагонистом мускариновых рецепторов предпочтительно предназначена для лечения и/или профилактики COPD.
Другие пригодные комбинации включают, например, комбинацию, содержащую соединение формулы (I) или его фармацевтически приемлемую соль вместе с другим противовоспалительным агентом, таким как противовоспалительный кортикостероид; или нестероидное противовоспалительное лекарственное средство (NSAID), такое как антагонист лейкотриена (например, монтелукаст), ингибитор iNOS (индуцибельной NO-синтазы), ингибитор триптазы, ингибитор эластазы, антагонист бета-2-интегрина, агонист а2-аденозина, CCR3-антагонист или ингибитор 5-липооксигеназы); или с противоинфекционным агентом (например, антибиотическим или противовирусным). Ингибитор iNOS предпочтительно предназначен для перорального введения. Подходящие ингибиторы iNOS (ингибиторы индуцибельной синтазы оксида азота) включают те, которые раскрыты в WO 93/13055, WO 98/30537, WO 02/50021, WO 95/34534 и WO 99/62875. Подходящие ингибиторы CCR3 включают те, которые раскрыты в WO 02/26722.
В комбинации, содержащей соединение формулы (I) или его фармацевтически приемлемую соль вместе с противовоспалительным кортикостероидом (которая предпочтительно предназначена для лечения и/или профилактики астмы, COPD или аллергического ринита), тогда противовоспалительный кортикостероид предпочтительно представляет собой флутиказон, флутиказона пропионат (например, смотри патент США 4335121), беклометазон, 17-пропионатный эфир беклометазона, 17,21-дипропионатный эфир беклометазона, дексаметазон или его сложный эфир, мометазон или его сложный эфир, циклесонид, будесонид, флунизолид или соединение, как описано в WO 02/12266 А1 (например, как заявлено в любом из пп.1-22 в этом документе), или фармацевтически приемлемая соль любого из указанного выше. Если противовоспалительный кортикостероид представляет собой соединение, как описано в WO 02/12266 А1, тогда предпочтительно он представляет собой Пример 1 этого документа {который представляет собой S-фторметиловый эфир 6α,9α-дифтор-17α-[(2-фуранилкарбонил)окси]-11β-гидрокси-16α-метил-3-оксо-андроста-1,4-диен-17β-карботиокислоты}, или Пример 41 из этого документа {который представляет собой S-фторметиловый эфир 6α,9α-дифтор-11β-гидрокси-16α-метил-17α-[(4-метил-1,3-тиазол-5-карбонил)окси]-3-оксо-андроста-1,4-диен-17β-карботиокислоты}, или его фармацевтически приемлемую соль. Противовоспалительный кортикостероид предпочтительно предназначен для интраназального или ингаляционного введения. Флутиказона пропионат является предпочтительным и предпочтительно предназначен для ингаляционного введения человеку либо (а) в дозе 250 микрограммов один раз в сутки, либо (б) в дозе от 50 до 250 микрограммов два раза в сутки.
Также предложена комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль вместе с агонистом β2-адренорецепторов и противовоспалительным кортикостероидом, например, как описано в WO 03/030939 А1. Предпочтительно эта комбинация предназначена для лечения и/или профилактики астмы, COPD и/или аллергического ринита. Агонист β2-адренорецепторов и/или противовоспалительный кортикостероид могут быть такими, как описано выше, и/или как описано в WO 03/030939 А1. Наиболее предпочтительно в этой "тройной" комбинации агонист β2-адренорецепторов представляет собой салметерол или его фармацевтически приемлемую соль (например, салметерола ксинафоат), а противовоспалительный кортикостероид представляет собой флутиказона пропионат.
Комбинации, описанные выше, могут быть удобным образом представлены для применения в форме фармацевтической композиции и, таким образом, фармацевтическая композиция, содержащая комбинацию, как определено выше, вместе с одним или более фармацевтически приемлемыми носителями и/или эксципиентами представляет собой следующий аспект изобретения.
Отдельные соединения из таких комбинаций можно вводить либо последовательно, либо одновременно в отдельной или в комбинированной фармацевтической композиции.
В одном воплощении комбинация, как определено здесь, может быть предназначена для одновременного ингаляционного введения и размещена в комбинированном ингаляционном устройстве. Такое комбинированное ингаляционное устройство составляет другой аспект изобретения. Такое комбинированное ингаляционное устройство может содержать комбинированную фармацевтическую композицию для одновременного ингаляционного введения (например, сухую порошкообразную композицию), композицию, содержащую все индивидуальные соединения этой комбинации, и композицию, включенную во множество герметичных дозировочных контейнеров, установленных продольно в полоске или ленте внутри ингаляционного устройства, причем эти контейнеры можно вскрыть или с них снять оболочку при необходимости; например, такое ингаляционное устройство может быть по существу таким, как описано в GB 2242134А (DISKUS™), и/или как описано выше. Альтернативно, комбинированное ингаляционное устройство может быть таким, чтобы индивидуальные соединения из комбинации можно было вводить одновременно, но хранить отдельно (либо полностью, либо частично хранить отдельно для тройных комбинаций), например в отдельных фармацевтических композициях, например, как описано в РСТ/ЕР03/00598, поданной 22 января 2003 (например, как описано в формуле изобретения этого документа, например, в пункте 1).
В изобретении также предложен способ получения комбинации, как определено здесь, при котором или
(а) готовят отдельную фармацевтическую композицию для введения индивидуальных соединений комбинации либо последовательно, либо одновременно, либо
(б) готовят комбинированную фармацевтическую композицию для введения индивидуальных соединений из комбинации одновременно, где эта фармацевтическая композиция содержит комбинацию вместе с одним или более фармацевтически приемлемыми носителями и/или эксципиентами.
В изобретении также предложена комбинация, как определено здесь, полученная способом, как определено здесь.
СПОСОБЫ БИОЛОГИЧЕСКОГО ТЕСТИРОВАНИЯ
Способы первичного анализа PDE3, PDE4B, PDE4D, PDE5, PDE6
Активность соединений можно измерить в способах анализа, показанных ниже. Предпочтительные соединения по изобретению являются избирательными ингибиторами PDE4, то есть они ингибируют PDE4 (например, PDE4B и/или PDE4D, предпочтительно PDE4B) сильнее, чем они ингибируют PDE3, и/или сильнее, чем они ингибируют PDE5, и/или сильнее, чем они ингибируют PDE6.
Источники фермента PDE и литературные ссылки
Человеческая рекомбинантная PDE4B, в частности ее 2В-сплайсинговый вариант (HSPDE4B2B), раскрыта в WO 94/20079, а также в М.М.McLaughlin et al., "A low Km, rolipram-sensitive, cAMP-specific phosphodiesterase from human brain: cloning and expression of cDNA, biochemical characterization of recombinant protein, and tissue distribution of mRNA", J.Biol. Chem., 1993, 268, 6470-6476. Например, в Примере 1 из WO 94/20079 человеческая рекомбинантная PDE4B описана как экспрессируемая в дефицитном по PDE штамме дрожжей Saccharomyces cerevisiae GL62, например, после индукции посредством добавления 150 мкМ CuSO4, и супернатантные фракции лизатов дрожжевых клеток, полученные при 100000g, описаны для использования в сборе фермента PDE4B.
Человеческая рекомбинантная PDE4D (HSPDE4D3A) раскрыта в P.A.Baecker et al., "Isolation of cDNA encoding a human rolipram-sensitive cyclic AMP phosphodiesterase
(PDE IVD)", Gene, 1994, 138, 253-256.
Человеческая рекомбинантная PDE5 раскрыта в К.Loughney et al., "Isolation and characterization of cDNAs encoding PDE5A, a human cGMP-binding, cGMP-specific 3',5'-cyclic nucleotide phosphodiesterase", Gene, 1998, 216, 139-147.
PDE3 очищали из бычьей аорты, как описано Н.Coste and P.Grondin, "Characterization of a novel potent and specific inhibitor of type V phosphodiesterase", Biochem. Pharmacol., 1995, 50, 1577-1585.
PDE6 очищали из бычьей сетчатки, как описано в Р.Catty and P.Deterre, "Activation and solubilization of the retinal cGMP-specific phosphodiesterase by limited proteolysis", Eur. J.Biochem., 1991,199, 263-269; A.Taretal. "Purification of bovine retinal cGMP phosphodiesterase", Methods in Enzymology, 1994, 238, 3-12 и/или D. Srivastava et al. "Effects of magnesium on cyclic GMP hydrolysis by the bovine retinal rod cGMP phosphodiesterase", Biochem. J., 1995, 308, 653-658.
Ингибирование активности PDE3, PDE4B, PDE4D, PDE5 или PDE6: радиоактивный анализ сцинтилляционной близости (SPA)
Способность соединений ингибировать каталитическую активность PDE4B или 4D (человеческих рекомбинантных), PDE3 (из бычьей аорты), PDE5 (человеческой рекомбинантной) или PDE6 (из бычьей сетчатки) определяли посредством анализа сцинтилляционной близости (SPA) в 96-луночном формате. Тестируемые соединения (предпочтительно в виде раствора в DMSO, например в объеме от 0,5 до 1 микролитра (мкл)) предварительно инкубировали при температуре окружающей среды (комнатной температуре, например 19-23°С) в Wallac Isoplates (код 1450-514) с PDE ферментом в 50 мМ Трис-HCl буфере, рН 7,5, 8,3 мМ MgCl2, 1,7 мМ EGTA (этиленбис(оксиэтиленнитрило)тетрауксусная кислота), 0,05% (мас./об.) бычьего сывороточного альбумина в течение 10-30 минут (обычно 30 минут). Концентрацию фермента регулировали таким образом, чтобы в контрольных лунках без соединения во время инкубации происходил гидролиз субстрата, определенного ниже, не более чем на 20%. Для PDE3-, PDE4B- и PDE4D-анализов добавляли [5',8'-3H]аденозин-3',5'-циклический фосфат (Amersham Pharmacia Biotech, код TRK.559 или Amersham Biosciences UK Ltd, Pollards Wood, Chalfont St Giles, Buckinghamshire HP8 4SP, UK) с получением 0,05 мКи на лунку и конечной концентрации ~10 нМ. Для PDE5- и PDE6-анализов добавляли [8-3H]гуанозин-3',5'-циклический фосфат (Amersham Pharmacia Biotech, код TRK.392) с получением 0,05 мКи на лунку и конечной концентрации ~36 нМ. Планшеты, например, содержащие приблизительно 100 мкл объем аналитической смеси, перемешивали на орбитальном шейкере в течение 5 минут и инкубировали при температуре окружающей среды в течение 1 часа. Для остановки анализа добавляли фосфодиэстеразные SPA гранулы (Amersham Pharmacia Biotech, код RPNQ 0150) (~1 мг на лунку). Планшеты герметично закрывали и встряхивали, а затем оставляли стоять при температуре окружающей среды в течение промежутка времени от 35 минут до 1 часа (предпочтительно 35 минут), чтобы дать возможность осесть гранулам. Связанный радиоактивный продукт измеряли, используя сцинтилляционный счетчик WALLAC TRILUX 1450 Microbeta. Для кривых ингибирования анализировали 10 концентраций (1,5 нМ - 30 мкМ) каждого соединения. Кривые анализировали, используя ActivityBase и XLfit (ID Business Solutions Limited, 2 Ocean Court, Surrey Research Park, Guildford, Surrey GU 7QB, United Kingdom). Результаты выражали в виде значений pIC50.
В качестве альтернативы приведенному выше радиоактивному SPA анализу ингибирование PDE4B или PDE4D можно измерять в следующем анализе поляризации флуоресценции (FP, Fluorescence Polarization).
Ингибирование активности PDE4B или PDE4D: анализ поляризации флуоресценции (FP)
Способность соединений ингибировать каталитическую активность на PDE4B(человеческих рекомбинантных) или PDE40(человеческих рекомбинантных) определяли посредством IMAP поляризации флуоресценции (набор IMAP Explorer от Molecular Devices Corporation, Sunnydale, CA, USA; код Molecular Devices: R8062) в 384-луночном формате. В IMAP FP анализе можно измерять активность PDE в формате гомогенного нерадиоактивного анализа. В FP анализе используется способность иммобилизованных трехвалентных катионов металла, нанесенных на наночастицы (крошечные гранулы), связывать фосфатную группу FI-AMP, которая образуется в результате гидролиза меченного флуоресцеином (FI) циклического аденозинмонофосфата (FI-cAMP), до нециклической формы FI-AMP. FI-cAMP не связывается. Связывание продукта FI-AMP с гранулами (покрытыми иммобилизованными трехвалентными катионами) замедляет вращение связанного FI-AMP и приводит к увеличению отношения поляризации флуоресценции параллельного света к перпендикулярному. Ингибирование PDE снижает/подавляет такое увеличение сигнала.
Тестируемые соединения (небольшой объем, например, от 0,5 до 1 мкл раствора в DMSO) предварительно инкубировали при температуре окружающей среды (комнатной температуре, например 19-23°С) в черных 384-луночных микротитровальных планшетах (поставщик NUNC, код 262260) с PDE-ферментом в 10 мМ Трис-HCl буфере, рН 7,2, 10 мМ MgCl2, с 0,1% (мас./об.) бычьего сывороточного альбумина и 0,05% NaN3 в течение 10-30 минут. Уровень фермента устанавливали экспериментальным путем, так чтобы реакция на протяжении всей инкубации была линейной. Добавляли флуоресцеин-аденозин-3',5'-циклический фосфат (от Molecular Devices Corporation, код Molecular Devices: R7091) с получением конечной концентрации приблизительно 40 нМ (конечный объем анализа обычно приблизительно 25-40 мкл). Планшеты перемешивали на орбитальном шейкере в течение 10 секунд и инкубировали при температуре окружающей среды в течение 40 мин. Добавляли IMAP связывающий реагент (как описано выше, от Molecular Devices Corporation, код Molecular Devices: R7207) (60 мкл 1:400 разведения исходного раствора из набора в связывающем буфере) для остановки анализа. Планшеты оставляли стоять при температуре окружающей среды в течение 1 часа. Отношение поляризации флуоресценции (FP) параллельного света к перпендикулярному измеряли, используя считывающее устройство для планшетов Analyst™ (от Molecular Devices Corporation). Для кривых ингибирования анализировали 10 концентраций (1,5 нМ - 30 мкМ) каждого соединения. Кривые анализировали, используя ActivityBase и XLfit (ID Business Solutions Limited, 2 Ocean Court, Surrey Research Park, Guildford, Surrey GU 7QB, United Kingdom). Результаты выражали в виде значений pIC50.
В FP-анализе все реагенты дозировали, используя Multidrop™ (имеется в продаже у Thermo Labsystems Oy, Ratastie 2, РО Box 100, Vantaa 01620, Finland).
Для данного PDE4-ингибитора значения ингибирования PDE4B (или PDE4D), измеренные с использованием SPA- и FP- анализов, могут немного отличаться. Однако обнаружено, что в регрессионном анализе 100 тестируемых соединений значения pIC50 ингибирования, измеренные с использованием SPA-и FP-анализов, в целом согласуются в пределах 0,5 логарифмических единиц для PDE4B и PDE4D (коэффициент линейной регрессии 0,966 для PDE4B и 0,971 для PDE4D; David R.Mobbs et al., "Comparison of the IMAP Fluorescence Polarization Assay with the Scintillation Proximity Assay for Phosphodiesterase Activity", стендовый доклад, представленный на 2003 Molecular Devices UK & Europe User Meeting, 2 октября 2003 года, Down Hall, Harlow, Essex, United Kingdom).
Биологические данные, полученные для некоторых Примеров (PDE4B-ингибиторная активность либо в виде одного считывания, либо в виде среднего из приблизительно 2-6 считываний), являются следующими, основанными на настоящих измерениях. В каждом из SPA- и FP-анализов абсолютная точность измерений невозможна, и данные считывания являются точными только до ±0,5 логарифмических единиц включительно в зависимости от числа проведенных и усредненных считываний:
Примеры 1-201, как правило, тестировали на ингибирование PDE4B, используя радиоактивный SPA-анализ. Из Примеров 207-665 и 677-686 все или почти все (за исключением, может быть, Примеров 451, 631-632, 635, 652) тестировали на ингибирование PDE4B; и из них некоторые тестировали с помощью радиоактивного SPA-анализа, некоторые тестировали с помощью FP-анализа. Примеры 1-201, 207-450, 452-630, 633-634, 636-651, 653-665 и 677-686, но за исключением примеров для сравнения 19-20, обладали ингибиторными активностями в отношении PDE4B в интервале pIC50 = от приблизительно 6 (± приблизительно 0,5) до приблизительно 10,0 (±приблизительно 0,5). Примеры 666-676 обладают ингибиторными активностями в отношении PDE4B в интервале pIC50 = от приблизительно 6 (± приблизительно 0,5) до приблизительно 10,0 (± приблизительно 0,5).
Примеры, где R3 = циклогексил (NHR3 = подформула (с)), тетрагидро-2Н-пиран-4-ил (NHR3 = группа (h)), 4-оксоциклогексил (NHR3 = подформула (о)) или некоторые другие типы замещенного циклогексила или некоторые гетероциклы, обычно или часто (особенно при R1 = этил) имеют более высокий уровень селективности в отношении PDE4B по сравнению с PDE5, при измерении в приведенных выше анализах ингибирования ферментов, по сравнению с селективностями сравнимых Примеров, где R3 = циклопропил (NHR3 = подформула (b)). Например, только на основании настоящих измерений и с учетом суммарных погрешностей анализа:
- Примеры 21, 40, 90, 198 и 201 (где NHR3 = подформула (h), (с), (j), (n) и (о) соответственно, R1 = этил) имеют селективности в отношении PDE4B по сравнению с PDE5 в интервале от приблизительно 3 до 20 или более раз выше, чем селективность, достигнутая для эквивалентного примера 39, где R3 = циклопропил (NHR3 = подформула (b));
- Примеры 43 и 44 (где NHR3 = подформула (с) и (h) соответственно) имеют селективности в отношении PDE4B по сравнению с PDE5 в интервале от приблизительно 4 до 8 или более раз выше, чем селективность, достигнутая для эквивалентного примера 42, где R3=циклопропил;
- Примеры 22 и 48 (где NHR3 = подформула (h) и (с) соответственно) имеют селективности в отношении PDE4B по сравнению с PDE5 в интервале от приблизительно 2,5 до 10 или более раз выше, чем селективность, достигнутая для эквивалентного примера 47, где R3 = циклопропил; и
- Примеры 2 и 3 (где NHR3 = подформула (с) и (h) соответственно) имеют селективности в отношении PDE4B по сравнению с PDE5 в интервале от приблизительно 2 до 5 или более раз выше, чем селективность, достигнутая для эквивалентного примера 1, где R3 = циклопропил;
Рвота. Некоторые известные ингибиторы PDE4 могут вызывать рвоту и/или тошноту в большей или меньшей степени (например, см. Z.Huang et al., Current Opinion in Chemical Biology, 2001, 5: 432-438, особенно страницы 433-434 и цитируемые там ссылки). Следовательно, было бы предпочтительно, но несущественно, если ингибиторное в отношении PDE4 соединение или соль по изобретению вызывало только ограниченные или управляемые рвотные побочные эффекты. Рвотные побочные эффекты можно, например, измерять посредством способности соединения или соли вызывать рвоту при введении хорькам; например, можно измерять время до возникновения, степень, частоту и/или продолжительность рвоты, позыва на рвоту и/или корчи у хорьков после перорального или парентерального введения соединения или соли. Смотри, например, в in vivo анализе 4 в описании ниже способ измерения противовоспалительного эффекта, рвотных побочных эффектов и терапевтического индекса (TI) у хорька. Также смотри, например, A.Robichaud et al., "Emesis induced by inhibitors of [PDE IV] in the ferret", Neuropharmacology, 1999, 38, 289-297, erratum Neuropharmacology, 2001, 40, 465-465. Однако, возможно, рвотные побочные эффекты и терапевтический индекс (TI) у крыс можно удобно измерять посредством мониторинга извращенного аппетита в пищевом поведении крыс после введения соединения или соли по изобретению (см. приведенный ниже in vivo анализ 2).
Другие побочные эффекты. Некоторые известные ингибиторы PDE4 могут вызывать другие побочные эффекты, такие как головная боль и другие опосредованные центральной нервной системой (ЦНС) побочные эффекты и/или расстройства желудочно-кишечного тракта (ЖКТ). Следовательно, было бы предпочтительно, но несущественно, если конкретное соединение или соль по изобретению, ингибиторное в отношении PDE4, вызывало бы только ограниченные или управляемые побочные эффекты в одной или более чем одной из таких категорий побочных эффектов.
Биологические анализы in vivo
Анализ ингибирования фермента PDE4B in vitro, описанный выше, следует рассматривать как первичный тест на биологическую активность. Однако ниже описаны дополнительные in vivo биологические тесты, которые являются возможными и которые не являются необходимой мерой эффективности или побочных эффектов.
In vivo анализ 1. Индуцированная LPS (липополисахаридами) легочная нейтрофилия у крыс: эффект перорально вводимых ингибиторов PDE4
Показано, что приток нейтрофилов в легкие является важным компонентом для семейства легочных заболеваний, таких как хроническая обструктивная болезнь легких (COPD), которая может включать в себя хронический бронхит и/или эмфизему (G.F.Filley, Chest. 2000; 117(5); 251s-260s). Целью данной модели нейтрофилии является исследование потенциально противовоспалительных in vivo эффектов перорально вводимых ингибиторов PDE4 в отношении нейтрофилии, индуцированной ингаляцией аэрозольного липополисахарида (LPS), являющейся моделью нейтрофильного(ых) воспалительного(ых) компонента(ов) COPD. Научную основу смотри в приведенном ниже разделе Литература.
Самцов крыс Lewis (Charles River, Raleigh, NC, USA) массой приблизительно 300-400 граммов предварительно обрабатывают либо (а) тестируемым соединением, суспендированным в 0,5%-ной метилцеллюлозе (имеющейся у Sigma-Aldrich, St. Louis, МО, USA), в воде, или (б) только носителем, перорально доставляемым в объеме дозы 10 мNкг. В общем случае кривые доза-ответ получают, используя следующие дозы ингибиторов PDE4: 10,0, 2,0, 0,4, 0,08 и 0,016 мг/кг. Через тридцать минут после предварительной обработки крыс подвергают воздействию аэрозольного LPS (серотип Е.coli 026:B6, полученный посредством экстракции трихлоруксусной кислотой, имеется у Sigma-Aldrich, St. Louis, МО, USA), образуемого в небулайзере, содержащем 100 мкг/мл раствора LPS. Крыс подвергают воздействию аэрозоля LPS при скорости 4 л/мин в течение 20 минут. Воздействие LPS осуществляют в закрытой камере с внутренними размерами: длина 45 см × ширина 24 см × высота 20 см. Небулайзер и камеру для воздействия содержат в проверенном вытяжном шкафу. Через 4 часа после воздействия LPS крыс подвергают эвтаназии посредством передозировки фенобарбитала в количестве 90 мг/кг, вводимого внутрибрюшинно. Бронхоальвеолярный лаваж (BAL) осуществляют через тупую иглу 14 размера в подвергаемую воздействию трахею. Проводят пять промывок по 5 мл, чтобы в сумме собрать 25 мл BAL жидкости. На BAL жидкости проводят подсчеты суммарного количества клеток и величин разницы лейкоцитов, чтобы вычислить приток нейтрофилов в легкое. Вычисляют процент нейтрофильного ингибирования для каждой дозы (по сравнению с носителем) и получают сигмовидную кривую доза-ответ с переменным наклоном, обычно используя Prism Graph-Pad. Кривую доза-ответ используют для вычисления значения ED50 (дозы, эффективной в 50% случаев) (в мг на кг массы тела) для ингибирования LPS-индуцированной нейтрофилии ингибитором PDE4.
Результаты. На основании данных измерений соединения Примеров 22, 83 и 155, вводимые перорально в вышеуказанной методике, демонстрировали значения ED50 по ингибированию нейтрофилии в интервале от приблизительно 0,5 мг/кг до приблизительно 2 мг/кг.
Альтернативный способ и результаты. В альтернативном воплощении данной методики крысам вводят однократные пероральные дозы 10 мг/кг или 1,0 мг/кг ингибитора PDE4 (или носителя) и процент ингибирования нейтрофилии для данной конкретной дозы вычисляют и протоколируют. В данном воплощении на основании настоящих измерений соединения Примеров 21, 100, 109, 167, 172 и 600, вводимые перорально в вышеуказанной методике в однократной дозе 1,0 мг/кг, демонстрировали процент ингибирования нейтрофилии в интервале от приблизительно 19% до приблизительно 69% (или в интервале от приблизительно 32% до приблизительно 69% для Примеров 21, 100, 109, 167 и 600).
Литература:
Filley G.F. Comparison of the structural and inflammatory features of COPD and asthma. Chest. 2000; 117(5) 251s-260s.
Howell RE, Jenkins LP, Fielding LE and Grimes D. Inhibition of antigen-induced pulmonary eosinophilia and neutrophilia by selective inhibitors of phosphodiesterase types 3 and 4 in brown Norway rats. Pulmonary Pharmacology. 1995:8:83-89.
Spond J, Chapman R, Fine J, Jones H, Kreutner W, Kung TT, Minnicozzi M. Comparison of PDE inhibitors, Rolipram and SB 207499 (Ariflo™) in a rat model of pulmonary neutrophilia. Pulmonary Pharmacology and Therapeutics. 2001; 14: 157-164.
Underwood DC, Osborn RR, Bochnowicz S, Webb EF, Rieman DJ, Lee JC, Romanic AM, Adams JL, Hay DWP and Griswold DE. SB 239063, a p38 МАРК inhibitor, reduces neutrophilia, inflammatory cytokines, MMP-9 and fibrosis in lung. Am J Physiol Lung Cell Mol Physiol. 2000; 279: L895-L902.
In vivo анализ 2. Модель рвоты у крыс с извращенным аппетитом
Уровень техники. Показано, что в различных in vitro и in vivo моделях избирательные ингибиторы PDE4 ингибируют воспаление посредством повышения внутриклеточных уровней сАМР многих иммунных клеток (например, лимфоцитов, моноцитов). Однако побочным эффектом некоторых ингибиторов PDE4 у многих видов является рвота. В связи с тем, что многие крысиные модели воспаления хорошо охарактеризованы, их использовали в методиках (смотри, например, вышеописанный in vivo анализ 1), чтобы показать полезные противовоспалительные эффекты ингибиторов PDE4. Однако у крыс нет рвотного ответа (у них нет рвотного рефлекса), так что непосредственно на крысах сложно исследовать взаимоотношение между полезными противовоспалительными эффектами ингибиторов PDE4 и рвотой.
Однако в 1991 Takeda et at. (см. раздел Литература ниже) показали, что ответ в виде извращенного питания у крыс аналогичен рвоте. Извращенное питание представляет собой поведенческий ответ на заболевание у крыс, при котором крысы поедают непитательные вещества, такие как земля или, в частности, глина (например, каолин), которые могут помочь адсорбировать токсины. Извращенное питание можно индуцировать испражнениями и химическими веществами (в частности, химическими веществами, которые вызывают рвоту у людей) и можно ингибировать фармакологически лекарствами, которые ингибируют рвоту у людей. В модели извращенного аппетита крыс, в in vivo анализе 2, можно определить уровень ответа извращенного аппетита крыс на ингибирование PDE4 в фармакологически релевантных дозах в параллели с in vivo противовоспалительными анализами (в отдельной группе) у крыс (например, описанный выше in vivo анализ 1). Противовоспалительный анализ и анализ извращенного аппетита у одних и тех же видов вместе могут предоставить данные по "терапевтическому индексу" (TI) у крысы соединений/солей по изобретению. Крысиный TI можно, например, вычислить как отношение а) дозы ED50 потенциального рвотного ответа в виде извращенного аппетита из анализа 2 к б) крысиной противовоспалительной дозе ED50 (например, измеренной на основании ингибирования нейтрофилии у крысы, например, в in vivo анализе 1), где более высокие отношения TI, возможно, указывают на меньшую рвоту при многих противовоспалительных дозах. Это может позволить выбрать не вызывающую рвоту или минимально вызывающую рвоту фармацевтическую дозу соединений или солей по изобретению, которая обладает противовоспалительным эффектом. Однако понятно, что достижение минимально вызывающего рвоту соединения, ингибиторного в отношении PDE4, не является необходимым.
Методика. На первые сутки эксперимента крыс по отдельности помещают в клетки без подстилки или "обогащения". Крыс держат на расстоянии от пола клетки при помощи проволочной сетки. В клетку помещают предварительно взвешенные кормушки, содержащие стандартный корм для крыс и гранулы глины. Гранулы глины, поставляемые Languna Clay Co, City of Industry, CA, USA, имеют те же размер и форму, что и гранулы корма. Крысы привыкают к глине в течение 72 часов, в течение этого времени кормушки и корм, а также отходы глины ежесуточно взвешивают на электронных весах, способных взвешивать с точностью до 0,1 грамма. По окончании этого 72-часового периода привыкания крысы, как правило, не проявляют интереса к гранулам глины.
По окончании 72 часов крыс помещают в чистые клетки и взвешивают кормушки. Крыс, которые продолжают регулярно потреблять глину, исключают из исследования. Непосредственно перед темным циклом (временем, когда животные активны и должны питаться) животных распределяют на группы обработки и им перорально дают дозу соединения/соли по изобретению (разные дозы для разных групп обработки) или один носитель в объеме дозы 2 мл/кг. При данной пероральной дозировке соединение/соль находится в форме суспензии в 0,5%-ной метилцеллюлозе (поставляемой Sigma-Aldrich, St. Louis, МО, USA) в воде. На следующие сутки взвешивают корм, глиняные кормушки и кормушки и отходы клетки и вычисляют суммарную глину и корм, потребленные в течение данной ночи каждым отдельным животным.
Ответ на дозу вычисляют, во-первых, путем перевода данных в ответ с конечным числом возможных значений, где животные имеют либо положительный, либо отрицательный ответ в виде извращенного аппетита. Крыса является "положительной по извращенному аппетиту", если она потребляет количество глины, более или равно на 0,3 грамма выше среднего, которое обычно вычисляют, используя логистическую регрессию, осуществляемую пакетом программ Statistica для обработки статистических данных. Затем можно вычислить значение ED50 ответа в виде извращенного аппетита в мг на кг массы тела.
Результаты. Используя описанную выше методику и согласно настоящим измерениям соединения Примеров 22, 83 и 155 демонстрировали ED50 ответ в виде извращенного аппетита в интервале от приблизительно 4,8 мг/кг до значения, больше или равного приблизительно 40 мг/кг. Видно, что эти ED50 дозы для ответа в виде извращенного аппетита являются более высокими, чем значения ED50 для ингибирования нейтрофилии для этих трех Примеров (см. in vivo анализ 1 выше), так что на первый взгляд кажется, что для этих трех примеров достигается терапевтический индекс (TI) у крыс >2, при измерении в анализах 1+2, и в соответствии с настоящими измерениями.
Терапевтический индекс (TI), вычисленный данным способом, часто значительно отличается от TI, вычисленного у хорька, и часто является более высоким (см. in vivo анализ 4 ниже).
Литература
Beavo JA, Contini, M., Heaslip, R.J. Multiple cyclic nucleotide phosphodiesterases. Mol Pharmacol. 1994; 46: 399-405.
Spond J, Chapman R, Fine J, Jones H, Kreutner W, Kung TT, Minnicozzi M. Comparison of PDE inhibitors, Rolipram and SB 207499 (Ariflo™) in a rat model of pulmonary neutrophilia. Pulmonary Pharmacology and Therapeutics. 2001; 14: 157-164.
Takeda N, Hasegawa S, Morita M, and Matsunaga T. Pica in rats is analogous to emesis: an animal model in emesis research. Pharmacology, Biochemistry and Behavior. 1991:45:817-821.
Takeda N, Hasegawa S, Morita M, Horii A, Uno A, Yamatodani A and Matsunaga T. Neuropharmacological mechanisms of emesis. I. Effects ofantiemetic drugs on motion- and apomorphine-induced pica in rats. Meth Find Exp Clin Pharmacol. 1995; 17(9) 589-596.
Takeda N, Hasegawa S, Morita M, Horii A, Uno A, Yamatodani A and Matsunaga T. Neuropharmacological mechanisms of emesis. I. Effects of antiemetic drugs on cisplatin-induced pica in rats. Meth Find Exp Clin Pharmacol. 1995; 17(9) 647-652.
In vivo анализ 3. Индуцированная LPS легочная нейтрофилия у крыс: эффект внутритрахеально вводимых ингибиторов PDE4
Данный анализ представляет собой животную модель воспаления в легком - специфической нейтрофилии, индуцированной липополисахаридом (LPS) - и позволяет исследовать предполагаемое ингибирование такой нейтрофилии (противовоспалительный эффект) интратрахеально (i.t.) вводимыми ингибиторами PDE4. Ингибиторы PDE4 предпочтительно находятся в форме сухого порошка или жидкой суспензии. Интратрахеальное введение является одной из моделей ингаляционного введения, дающего возможность местной доставки в легкое.
Животные. Самцов CD крыс (происхождящих от Sprague Dawley), поставляемых Charles River, Raleigh, NC, USA, содержали в группах по 5 крыс на клетку, акклиматизировали после доставки в течение по меньшей мере 7 суток, регулярно меняя подстилочный/гнездовой материал, кормили SDS диетой с R1 гранулированным кормом, даваемый по желанию, и обеспечивали пастеризованной питьевой водой ветеринарной чистоты, заменяемой ежесуточно.
Устройство для введения сухого порошка. Одноразовый 3-канальный кран между дозировочной иглой и шприцом. 3-Канальный стерильный кран (Vycon Ref 876.00) взвешивали, затем в этот кран добавляли лекарственную смесь или лактозу ингаляционного сорта (контроль-носитель), кран закрывали для предотвращения потери лекарства и повторно взвешивали для определения массы лекарства в кране. После дозирования кран снова взвешивали для определения массы лекарства, которое ушло из крана. Шприцевую иглу Sigma Z21934-7 19 размера длиной 152 мм (6 дюймов) с втулкой Люэра обрезали техническим путем до приблизительно 132 мм (5,2 дюймов), затупляли конец, чтобы предотвратить повреждение трахеи крысы, и иглу взвешивали до и после доставки лекарства, чтобы убедиться, что после дозирования лекарство не осталось в иглах.
Устройство для введения жидкой суспензии. Это устройство подобно описанному выше, но использовалась тупая дозировочная игла, прямой конец которой находился слегка под углом к оси иглы, с гибкой пластиковой съемной канюлей, вставленной в иглу.
Лекарства и вещества. Липополисахарид (LPS) (серотип: 0127:В8) (L3129 серия 61К4075) растворяют в фосфатно-солевом буфере (PBS). Ингибиторы PDE4 используют в форме с уменьшенным размером частиц (то есть в микронизированной форме), например в соответствии с Примером микронизации, приведенным выше. Для введения лекарства в виде сухого порошка можно использовать Пример сухого порошкообразного препарата, приведенный выше, содержащий лекарственное средство и лактозу ингаляционного сорта. Обычно используемая лактоза ингаляционного сорта (Серия E98L4675, Партия 845120) содержит 10% мелкой фракции (10% вещества размера частиц менее 15 мкм, измеренные при помощи анализатора размера частиц Malvern).
Жидкие суспензии лекарственного средсва можно приготовить путем добавления необходимого объема носителя к лекарственному средству; при этом используемый носитель представляет собой смесь физиологический раствор/твин (0,2%-ный твин 80). Эту жидкую суспензию перед использованием обрабатывают ультразвуком в течение 10 минут.
Подготовка и дозирование ингибитора PDE4. Крыс анестезировали, помещая животных в герметичную Perspex камеру и воздействия на них газовой смесью изофлурана (4,5%), оксида азота (3 литра, минута-1) и кислорода (1 литр, минута-1). Сразу после анестезии животных помещали на стол-подставку из нержавеющей стали, обеспечивающий интратрахеальное дозирование. Их помещали на спину под углом приблизительно 35°. Свет наклоняли к наружной части горла, чтобы сильнее осветить трахею. Открывали рот и делали видимым начало верхних дыхательных путей. Методика меняется при введении жидкой суспензии и сухого порошка ингибиторов PDE4 следующим образом.
Дозирование жидкой суспензии. Съемную канюлю вводили через тупую металлическую дозировочную иглу, которую осторожно вводили в трахею крысы. Животным давали внутритрахеально носитель или ингибитор PDE4 через дозировочную иглу с новой внутренней канюлей, используемой для каждой отличной группы лекарств. Препарат медленно (10 секунд) вводили в трахею, используя шприц, присоединенный к дозировочной игле.
Дозирование сухого порошка. Устройство с трехканальным краном и иглой вводили в трахею крысы до предварительно определенной точки, расположение которой устанавливали приблизительно на 1 см выше первичной бифуркации. Другой оператор держит иглу в указанном положении, в то время как 2×4 мл воздуха доставляются через трехканальный кран путем сжатия шприцов (в идеале совпадая с вдохом животного), чтобы вытолкнуть все количество лекарства из крана. После дозирования иглу и кран удаляют из дыхательных путей и кран закрывают, чтобы предотвратить выход какого-либо остаточного лекарства из крана.
После введения дозы влажной суспензии или сухого порошка животных снимают со стола и постоянно наблюдают до тех пор, пока они не восстановятся от действия анестезии. Животных возвращают в клетки для содержания и предоставляют свободный доступ к пище и воде; их наблюдают и отмечают любые необычные изменения в поведении.
Воздействие LPS. Приблизительно через 2 часа после интратрахеального введения дозы контроля-носителя или ингибитора PDE4 животных помещали в герметичные Perspex контейнеры и подвергали воздействию аэрозоля LPS (концентрация в небулайзере 150 мкг·мл-1) в течение 15 минут. Аэрозоли LPS получали с помощью небулайзера (DeViibiss, USA) и направляли их в Perspex камеру для воздействия. После 15-минутного периода воздействия LPS животных возвращали в клетки для содержания и предоставляли свободный доступ и к пище, и к воде.
[В альтернативном воплощении крыс можно подвергать воздействию LPS менее чем через 2 часа после интратрахеального дозирования. В другом альтернативном воплощении крыс можно подвергать воздействию LPS более чем через 2 часа (например, через приблизительно 4 или через приблизительно 6 часов) после интратрахеального дозирования носителя или ингибитора PDE4, чтобы проверить, обладает ли ингибитор PDE4 большой продолжительностью действия (что не является существенным)].
Бронхоальвеолярный лаваж. Через 4 часа после воздействия LPS животных умерщвляли посредством передозировки пентобарбитона натрия (интратрахеально). Трахею канюлировали полипропиленовой трубкой и проводили лаваж легких (промывание) 3×5 мл гепаринизированного (25 ед·мл-1) фосфатно-солевого буфера (PBS).
Подсчеты нейтрофильных клеток. Образцы из бронхоальвеолярного лаважа (BAL) центрифугировали при 1300 об/мин в течение 7 минут. Супернатант удаляли и полученный в результате клеточный осадок ресуспендировали в 1 мл PBS. Клеточный микроскопический препарат ресуспензионной жидкости готовили, помещая 100 мкл ресуспендированной BAL жидкости в держатели для центрифугирования клеток, а затем центрифугировали при 5000 об/мин в течение 5 минут. Микроскопические препараты оставляли высыхать на воздухе, а затем окрашивали красителем Лейшмана (20 минут), чтобы сделать возможным дифференциальный подсчет клеток. Общее количество клеток также подсчитывали из ресуспензии. На основании этих двух подсчетов определяли общие количества нейтрофилов в BAL. Для измерения ингибирования нейтрофилии, индуцированного ингибитором PDE4, проводили сравнение числа нейтрофилов у крыс, обработанных носителем, и крыс, обработанных ингибиторами PDE4.
Варьируя дозу ингибитора PDE4, используемого на стадии дозирования (например, 0,2 или 0,1 мг ингибитора PDE4 на кг массы тела вниз до приблизительно 0,01 мг/кг), можно получить кривую доза-ответ.
In vivo анализ 4. Оценка терапевтического индекса ингибиторов PDE4 у хорька, находящегося в сознании
1.1 Материалы
Для этих исследований используют следующие материалы.
Ингибиторы PDE4 готовят для перорального (п/о) введения, растворяя в фиксированном объеме (1 мл) ацетона и затем добавляя кремофор до 20% конечного объема. Ацетон выпаривают, направляя поток газообразного азота на раствор. После удаления ацетона раствор доводят до конечного объема дистиллированной водой.
LPS растворяют в фосфатно-солевом буфере.
1.2 Животные
Самцов хорьков (Mustela Pulorius Furo, масса 1-2 кг) транспортируют и оставляют акклиматизироваться в течение не менее 7 суток. Диета включает SDS диету С с гранулированным кормом, даваемый по желанию, с кошачьим кормом Whiskers™, даваемым 3 раза в неделю. Животных обеспечивают пастеризованной питьевой водой ветеринарной чистоты, заменяемой ежесуточно.
1.3 Протокол(ы) эксперимента(ов)
1.3.1 Дозирование ингибиторов PDE4
Ингибиторы PDE4 вводят перорально (п/о), используя объем дозы 1 мл/кг. Хорьков подвергают голоданию в течение ночи, но позволяют свободный доступ к воде. Животным перорально дают дозу носителя или ингибитора PDE4, используя 15 см дозировочную иглу, которую пропускают вниз по задней стенке горла в пищевод. После введения дозы животных возвращают в клетки для содержания, снабженные Perspex дверями, чтобы обеспечить возможность наблюдения, и предоставляют свободный доступ к воде. За животными постоянно наблюдают и регистрируют любые эпизоды рвоты (позыв к рвоте и рвоту) или изменения поведения. Животным дают доступ к пище через 60-90 минут после перорального дозирования.
1.3.2 Воздействие LPS
Через 30 минут после перорального дозирования соединения или контроля-носителя хорьков помещают в герметичные Perspex контейнеры и подвергают воздействию аэрозоля LPS (30 мкг/мл) в течение 10 минут. Аэрозоли LPS получают с помощью небулайзера (DeVilbiss, USA) и направляют их в Perspex камеру для воздействия. После 10-минутного периода воздействия животных возвращают в клетки для содержания и дают свободный доступ к воде и, на более поздней стадии, к пище. Общее наблюдение за животными продолжается в течение по меньшей мере 2,5 часов после перорального дозирования. Все эпизоды рвоты и изменения в поведении регистрируют.
1.3.3 Бронхоальвеолярный лаваж и подсчеты клеток
Через шесть часов после воздействия LPS животных умерщвляют посредством передозировки пентобарбитона натрия, вводимого внутрибрюшинно. Затем трахею канюлируют полипропиленовой трубкой и проводят лаваж легких дважды по 20 мл гепаринизированного (10 ед/мл) фосфатно-солевого буфера (PBS). Образцы из бронхоальвеолярного лаважа (BAL) центрифугируют при 1300 об/мин в течение 7 минут. Супернатант удаляют, и полученный в результате клеточный осадок ресуспендируют в 1 мл PBS. Клеточный мазок ресуспендированной жидкости готовят и окрашивают красителем Лейшмана, чтобы дать возможность дифференциального подсчета клеток. Подсчет общего количества клеток осуществляют, используя оставшийся ресуспендированный образец. На основании этого определяют суммарное число нейтрофилов в BAL образце.
1.3.4 Фармакодинамические показатели
Регистрируют следующие параметры:
а) % Ингибирования индуцированной LPS легочной нейтрофилии для определения дозы ингибитора PDE4, которая вызывает 50%-ное ингибирование (D50).
б) Эпизоды рвоты - считают число рвот и позывов на рвоту для определения дозы ингибитора PDE4, которая вызывает 20% случаев рвоты (D20).
в) Затем для каждого ингибитора PDE4 вычисляют терапевтический индекс (TI), используя данный анализ, применяя следующее уравнение:
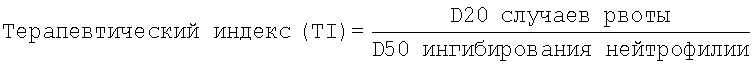
Следует отметить, что терапевтический индекс (TI), вычисленный с использованием данного in vivo анализа 4, часто значительно отличается от вычисленного с использованием анализов 1+2 перорального воспаления и пищевого извращения у крыс и часто ниже его.
Вычисление TI с использованием ингибитора PDE4 рофлумиласта в данном анализе 4 представляет собой:
D20 для рвоты = 0,5 мг/кг п/о, D50 для нейтрофилии = 0,49 мг/кг п/о, TI=1,02.
Все публикации, включая патенты и патентные заявки, цитируемые в данном описании, но не ограничиваясь ими, включены в данное описание изобретения посредством ссылки, как если бы каждая отдельная публикация была конкретно и индивидуально указана как включенная сюда посредством ссылки в полном изложении.
ПРИМЕРЫ
Различные аспекты изобретения будут далее описаны посредством ссылки на приведенные ниже примеры. Эти примеры являются исключительно иллюстративными и не должны рассматриваться как ограничивающие объем настоящего изобретения. В данном разделе в "Промежуточных соединениях" представлены синтезы промежуточных соединений, предназначенных для использования в синтезе "Примеров".
Сокращения, используемые в описании:
DMSO Диметилсульфоксид
DCM Дихлорметан
EtOAc Этилацетат
Et2O Диэтиловый эфир
DMF Диметилформамид
МеОН Метанол
ВЭЖХ Жидкостная хроматография высокого давления (высокоэффективная)
SPE Твердофазная экстракция
ЯМР Ядерный магнитный резонанс (в котором: s = синглет, d = дублет, t = триплет, q = квартет, dd = дублет дублетов, m = мультиплет, Н = число протонов)
LCMS Жидкостная хроматография/масс-спектроскопия
ТСХ Тонкослойная хроматография
ВЕМР 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфазин
EDC 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид
HATU O-(7-Азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат
HBTU O-(Бензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат
НОВТ гидроксибензотриазол = 1-гидроксибензотриазол
h часы
DIPEA диизопропилэтиламин (iPr2Net)
TRET время удерживания
THF Тетрагидрофуран
Реагент Лавессона 2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфид
Комнатная температура обычно находится в интервале от приблизительно 20 до приблизительно 25°С
Аппаратные методы, используемые здесь:
LCMS (жидкостная хроматография/масс-спектрометрия)
Масс-спектрометр Waters ZQ, действующий в режиме положительной ионизации в электроспрее, диапазон масс 100-1000 а.е.м. (единиц атомной массы).
Длина волны УФ: 215-330 нМ
Колонка: 3,3 см ×4,6 мм внутренний диаметр, 3 мкм ABZ+PLUS
Скорость потока: 3 мл/мин
Объем впрыска: 5 мкл
Растворитель А: 95%-ный ацетонитрил + 0,05%-ная муравьиная кислота
Растворитель Б: 0,1%-ная муравьиная кислота +10 мМ ацетат аммония
Градиент: 0% А/0,7 мин, 0-100% А/3,5 мин, 100% А/1,1 мин, 100-0% А/0,2 мин
Регулируемая по массе автоматическая препаративная ВЭЖХ
Используемая препаративная колонка представляла собой Supelcosil ABZplus (10 см ×2,12 см) (обычно 10 см ×2,12 см ×5 мкм).
Длина УФ-волны: 200-320 нМ
Скорость потока: 20 мл/мин
Объем впрыска: 1 мл или более предпочтительно 0,5 мл
Растворитель А: 0,1%-ная муравьиная кислота
Растворитель Б: 95% ацетонитрила + 5% муравьиной кислоты; или более типично 99,95% ацетонитрила + 0,05% муравьиной кислоты
Градиент: 100% А/1 мин, 100-80% А/9 мин, 80-1% А/3,5 мин, 1% АЛ,4 мин, 1-100% А/О, 1 мин
Промежуточные соединения и Примеры
Все реагенты, не описанные подробно в тексте, имеются в продаже у постоянных поставщиков, таких как Sigma-Aldrich. Адреса поставщиков некоторых исходных веществ, упоминаемых ниже в Промежуточных соединениях и Примерах или в приведенных выше Анализах, указаны ниже:
- ABCR GmbH & СО. RG, Р.О. Box 21 01 35 Karlsruhe, Germany
- Aceto Color Intermediates (каталожное название), Aceto Corporation, One Hollow Lane, Lake Success, NY, 11042-1215, USA
- Acros Organics, A Division of Fisher Scientific Company, 500 American Road, Morris Plains, NJ 07950, USA
- Apin Chemicals Ltd, 82 С Milton Park, Abingdon, Oxon 0Х14 4RY, United Kingdom
- Apollo Scientific Ltd, Unit 1A, Bingswood Industrial Estate, Whaley Bridge, Derbyshire SK23 7LY, United Kingdom
- Aldrich (каталожное название), Sigma-Aldrich Company Ltd, Dorset, United Kingdom, telephone: +441202733114; Fax: +441202715460; ukcustsv@eurnotes.sial.com; или
- Aldrich (каталожное название), Sigma-Aldrich Corp., P.О.Box 14508, St. Louis, МО 63178-9916, USA, telephone: 314-771-5765; Fax: 314-771-5757; custserv@sial.com или
- Aldrich (каталожное название), Sigma-Aldrich Chemie Gbmh, Munich, Germany, telephone: +498965130; Fax: +498965131169; deorders@eurnotes.sial.com.
- Alfa Aesar, A Johnson Matthey Company, 30 Bond Street, Ward Hill, MA 01835-8099, USA
- Amersham Biosciences UK Ltd, Pollards Wood, Chalfont St Giles, Buckinghamshire HP8 4SP, United Kingdom
- Array Biopharma Inc., 1885 33rd Street, Boulder, CO 80301, USA
- Asta Tech, Inc., 8301 Torresdale Ave, 19C, Philadelphia, PA 19136, USA
- Austin Chemical Company, Inc., 1565 Barclay Blvd., Buffalo Grove, IL 60089, USA
- Avocado Research, Shore Road, Port of Heysham Industrial Park, Heysham Lancashire LA3 2XY, United Kingdom
- BayerAG, Business Group Basic and Fine Chemicals, D-51368 Leverkusen, Germany
- Berk Univar plc, Berk House, P.О.Box 56, Basing View, Basingstoke, Hants RG21 2E6, United Kingdom
- Butt Park Ltd., Braysdown Works, Peasedown St. John, Bath BA2 8LL, United Kingdom
- Chemical Building Blocks (каталожное название), Ambinter, 46 quai Louis Bleriot, Paris, F-75016, France
- ChemBridge Europe, 4 dark's Hill Rise, Hampton Wood, Evesham, Worcestershire WR11 6FW, United Kingdom
- ChemService Inc., P.O.Box 3108, West Chester, PA 19381, USA
- Combi-Blocks Inc., 7949 Silverton Avenue, Suite 915, San Diego, CA 92126, USA
- Dynamit Nobel GmbH, Germany; также имеется у Saville Whittle Ltd (UK агенты Dynamit Nobel), Vickers Street, Manchester M40 8EF, United Kingdom
- E.Merck, Germany; или Е.Merck (Merck Ltd), Hunter Boulevard, Magna Park, Lutterworth, Leicestershire LE174XN, United Kingdom
- Esprit Chemical Company, Esprit Plaza, 7680 Matoaka Road, Sarasota, FL 34243, USA
- Exploratory Library (каталожное название), Ambinter, 46 quai Louis Bleriot, Paris, F-75016, France
- Fluka Chemie AG, Industriestrasse 25, P.O. Box 260, CH-9471 Buchs, Switzerland
- Fluorochem Ltd., Wesley Street, Old Glossop, Derbyshire SK13 7RY, United Kingdom
- ICN Biochemicals, Inc., 3300 Hyland Avenue, Costa Mesa, CA 92626, USA
- Interchim Intermediates (каталожное название), Interchim, 213 Avenue Kennedy, BP 1140, Montlucon, Cedex, 03103, France
- Key Organics Ltd., 3, Highfield Industrial Estate, Camelford, Cornwall PL32 9QZ, United Kingdom
- Lancaster Synthesis Ltd., Newgate, White Lund, Morecambe, Lancashire LA3 3DY, United Kingdom
- Manchester Organics Ltd., Unit 2, Ashville Industrial Estate, Sutton Weaver, Runcorn, Cheshire WA7 3PF, United Kingdom
- Matrix Scientific, P.O.Box 25067, Columbia, SC 29224-5067, USA
- Maybridge Chemical Company Ltd., Trevillett, Tintagel, Cornwall PL34 OHW, United Kingdom
- Maybridge Reactive Intermediates (catalogue name), Maybridge Chemical Company Ltd., Trevillett, Tintagel, Cornwall PL34 OHW, United Kingdom
- MicroChemistry Building Blocks (каталожное название), MicroChemistry-RadaPharma, Shosse Entusiastov 56, Moscow, 111123, Russia
- Miteni S. p. A., Via Mecenate 90, Milano, 20138, Italy
- Molecular Devices Corporation, Sunnydale, CA, USA
- N.D.Zeiinsky Institute, Organic Chemistry, Leninsky prospect 47, 117913 Moscow B-334, Russia
- Optimer Building Block (каталожное название), Array BioPharma, 3200 Walnut Street, Boulder, CO 80301, USA
- Peakdale Molecular Ltd., Peakdale Science Park, Sheffield Road, Chapelen-le-Frith, High Peak SK23 OPG, United Kingdom
- Pfaltz & Bauer, Inc., 172 East Aurora Street, Waterbury, CT 06708, USA
- Rare Chemicals (каталожное название), Rare Chemicals GmbH, Schulstrasse 6, 24214 Gettorf, Germany
- SALOR (каталожное название), (Sigma Aldrich Library of Rare Chemicals), Aldrich Chemical Company, Inc., 1001 West Saint Paul Avenue, Milwaukee, WI 53233, USA
- Sigma (каталожное название), Sigma-Aldrich Corp., P.O.Box 14508, St. Louis, МО 63178-9916, USA; см. выше в "Aldrich" другие адреса, не США, и другие подробности контактов
- SIGMA-RBI, One Strathmore Road, Natick, MA 01760-1312, USA
- Synchem OHG Heihrich-Plett-Strasse 40, Kassel, D-34132, Germany
- Syngene International Pvt Ltd., Hebbagodi, Hosur Road, Bangalore, India
- TCI America, 9211 North Harborgate Street, Portland, OR 97203, USA
- TimTec Building Blocks A, TimTec, Inc., P.O.Box 8941, Newark, DE 19714-8941, USA
- Trans World Chemicals, Inc., 14674 Southlawn Lane, Rockville, MD 20850, USA
- Ubichem PLC, Mayflower Close, Chandlers Ford Industrial Estate, Eastleigh, Hampshire S053 4AR, United Kingdom
- Ultrafine (UFC Ltd.), Synergy House, Guildhall Close, Manchester Science Park, Manchester M 15 6SY, United Kingdom


Промежуточное соединение 1: Этил-4-хлор-1-этил-1 Н-пиразоло[3,4-b]пиридин-5-карбоксилат
Получали из имеющегося в продаже 5-амино-1-этил-пиразола, как описано в G.Yu et al. J. Med. Chem., 2001, 44, 1025-1027:
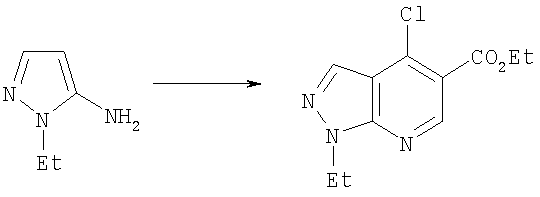
Промежуточное соединение 2: Этил-4-этокси-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
Может быть получен путем окислительного расщепления (SeO2) производного 1-фуранилметила, как описано в Т.М.Bare et al. J. Med. Chem., 1989, 32, 2561-2573 (дополнительная ссылка на Zuleski, F.R., Kirkland, К.R., Melgar, М.D.; Malbica, J. Drug. Metab. Dispos., 1985, 13, 139).
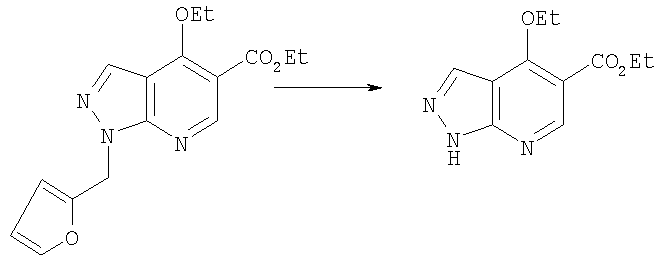
Промежуточное соединение 3: Этил-1-метил-4-этокси-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
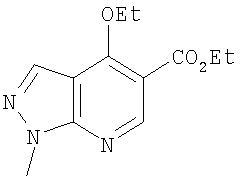
Смесь Промежуточного соединения 2 (0,47 г) и безводного карбоната калия (0,83 г) (предварительно высушенного нагреванием при 100°С) в безводном диметилформамиде (DMF) (4 мл) обрабатывали йодметаном (0,26 мл) и энергично перемешивали в течение 3 ч. Затем эту смесь фильтровали и фильтрат концентрировали в вакууме с получением остаточного масла, которое распределяли между дихлорметаном (DCM) (25 мл) и водой (25 мл). Слои разделяли и водную фазу экстрагировали дополнительным количеством DCM (2×25 мл). Объединенные органические экстракты сушили над безводным сульфатом натрия и выпаривали до оранжевого твердого вещества, которое наносили на SPE картридж (силикагель, 20 г). Этот картридж последовательно элюировали смесью EtOAc:бензин (1:4, 1:2 и 1:1), затем хлороформ:метанол (49:1, 19:1 и 9:1). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 3 (0,165 г). LCMS показала MH+=250; TRET=2,59 мин.
Промежуточное соединение 4: Этил-1-бензил-4-этокси-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
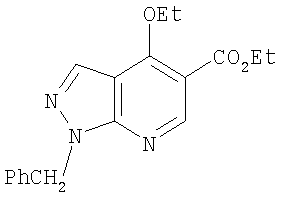
Смесь Промежуточного соединения 2 (0,47 г) и безводного карбоната калия (0,83 г) (предварительно высушенного нагреванием при 100°С) в безводном DMF (4 мл) обрабатывали бензилбромидом (0,72 г), затем энергично перемешивали и нагревали при 55°С в течение 4,5 ч. Эту смесь оставляли охлаждаться, затем фильтровали и фильтрат концентрировали в вакууме с получением остаточного масла, которое распределяли между дихлорметаном (DCM) (25 мл) и водой (25 мл). Слои разделяли и водную фазу экстрагировали дополнительным количеством DCM (2×25 мл). Объединенные органические экстракты сушили над безводным сульфатом натрия и упаривали до желтого маслянистого твердого вещества, которое растворяли в DCM и наносили на SPE картридж (силикагель, 20 г). Этот картридж элюировали градиентом EtOAc:бензин (1:4, 1:2 и 1:1), затем хлороформ:метанол (49:1, 19:1 и 9:1). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 4 (0,33 г). LCMS показала МН+=326; TRET=3,24 мин.
Промежуточное соединение 5: Этил-4-хлор-1-фенил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
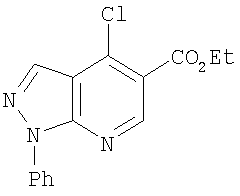
Смесь 5-амино-1-фенилпиразола (2,0 г) и диэтилэтоксиметиленмалоната (2,54 мл) нагревали в условиях Дина-Старка при 120°С в течение 16 ч. Этот раствор охлаждали, затем добавляли оксихлорид фосфора (16 мл) и смесь нагревали с обратным холодильником в течение следующих 20 ч. Избыток оксихлорида фосфора удаляли в вакууме и остаток распределяли между диэтиловым эфиром и водой, соблюдая крайнюю осторожность при добавлении воды. Эфирный слой промывали дополнительным количеством воды, затем сушили над сульфатом магния и концентрировали в вакууме с получением этил-4-хлор-1-фенил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилата (2,09 г). LCMS показала MH+=302; TRET=3,80 мин.
Промежуточное соединение 6: 1-Ацетил-4-аминопиперидин
Получали из имеющегося в продаже N1-бензил-4-аминопиперидина, как описано Yamada et al. в WO 00/42011:
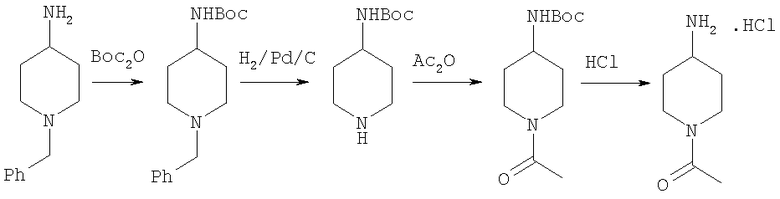
Промежуточное соединение 7:1-Метил-4-аминопиперидин
Получали из имеющегося в продаже N-метил-4-пиперидона, как описано С.М.Andersson et al. в WO 01/66521:
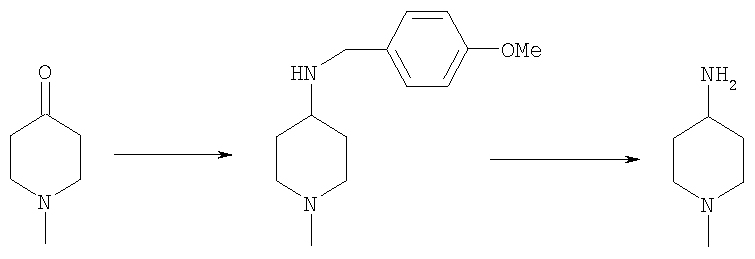
Промежуточное соединение 8: 4-Аминотетрагидропиран
Имеется в продаже у Combi-Blocks Inc., 7949 Silver-ton Avenue, Suite 915, San Diego, CA 92126, USA (CAS 38041-19-9).
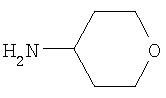
Промежуточное соединение 8А: Тетрагидро-2Н-пиран-4-амина гидрохлорид = 4-Аминотетрагидропирана гидрохлорид
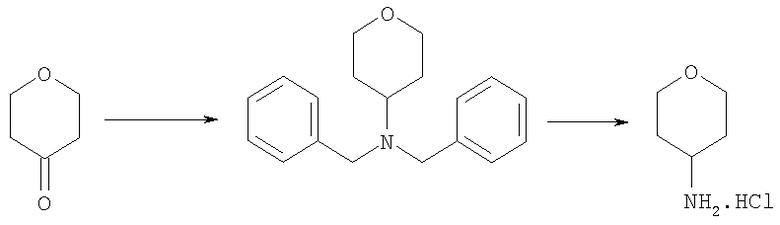
Стадия 1: N,N-дибензилтетрагидро-2H-пиран-4-амин
Дибензиламин (34,5 г) и уксусную кислоту (6,7 мл) добавляли к перемешиваемому раствору тетрагидро-4Н-пиран-4-она (16,4 г, имеется в продаже, например, у Aldrich) в дихлорметане (260 мл) при температуре от 0°С до 5°С. Через 2,5 ч при температуре от 0°С до 5°С добавляли порциями триацетоксиборгидрид натрия (38,9 г) и эту смесь оставляли нагреваться до комнатной температуры. После перемешивания при комнатной температуре в течение ночи реакционную смесь последовательно промывали 2 М гидроксидом натрия (200 мл и 50 мл), водой (2×50 мл) и рассолом (50 мл), затем сушили и выпаривали с получением желтого масла (45 г). Это масло перемешивали с метанолом (50 мл) при 4°С в течение 30 мин с получением продукта в виде белого твердого вещества (21,5 г). LCMS показала МН+=282; TRET=1,98 мин.
Стадия 2: Тетрагидро-2Н-пиран-4-амина гидрохлорид
N,N-Дибензилтетрагидро-2H-пиран-4-амин (20,5 г) растворяли в этаноле (210 мл) и гидрировали над катализатором 10%-ным палладием на угле (4 г) при давлении 100 фунт/кв. дюйм (689,5 кПа) в течение 72 ч при комнатной температуре. Реакционную смесь фильтровали, и фильтрат доводили до рН 1 с помощью 2 М хлористого водорода в диэтиловом эфире. В результате выпаривания растворителей получали твердое вещество, которое растирали с диэтиловым эфиром с получением продукта в виде белого твердого вещества (9,23 г). 1H ЯМР (400 МГц в d6-DMSO, 27°С, δ млн-1) 8.24 (br.s, 3H), 3.86 (dd, 12, 4 Гц, 2Н), 3.31 (dt, 2, 12 Гц, 2Н), 3.20 (m, 1H), 1.84 (m, 2H), 1.55 (dq, 4, 12 Гц, 2Н).
Промежуточное соединение 9: (R)-(+)-3-Аминотетрагидрофуран-4-толуолсульфонат
Имеется в продаже у Fluka Chemie AG, Germany (CAS 111769-27-8)
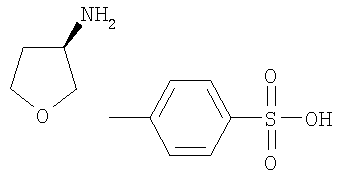
Промежуточное соединение 10: (S)-(-)-3-Аминотетрагидрофуран-4-толуолсульфонат
Имеется в продаже у Е.Merck, Germany; или Е.Merck (Merck Ltd), Hunter Boulevard, Magna Park, Lutterworth, Leicestershire LE17 4XN, United Kingdom (CAS 104530-80-5).
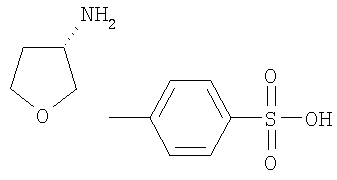
Промежуточное соединение 11: Тетрагидро-2Н-тиопиран-4-амин
Получали из имеющегося в продаже тетрагидротиопиран-4-она, как описано в Subramanian et al., J. Org. Chem., 1981, 46, 4376-4383. Последующее получение соли гидрохлорида может быть осуществлено общепринятыми способами.
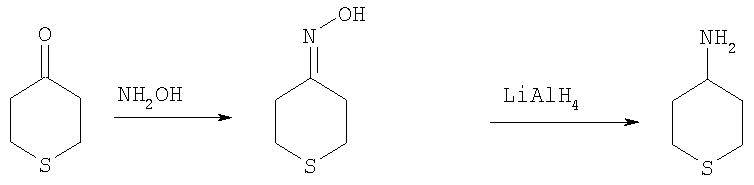
Промежуточное соединение 12: Тетрагидро-3-тиофенамин
Получали аналогично Промежуточному соединению 11 из имеющегося в продаже тетрагидротиофен-4-она. Образование оксима описано в Grigg et al., Tetrahedron, 1991, 47, 4477-4494, а восстановление оксима описано в Unterhalt et al., Arch. Pharm., 1990, 317-318.
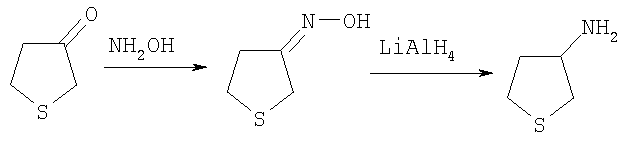
Промежуточное соединение 13: Тетрагидро-3-тиофенамин-1,1-диоксида гидрохлорид
Имеется в продаже у Sigma Aldrich Library of Rare Chemicals (SALOR) (CAS-6338-70-1). Получение соли гидрохлорида этого амина может быть осуществлено общепринятыми способами.
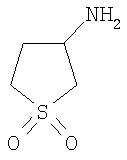
Промежуточное соединение 14: Гидрохлорид тетрагидро-2Н-тиопиран-4-амин-1,1-диоксида
Получали аналогично Промежуточному соединению 11 из имеющегося в продаже тетрагидротиофен-4-она. Окисление до 1,1-диоксо-тетрагидро-1λ6-тиопиран-4-она описано в Rule et al. J. Org. Chem., 1995, 60, 1665-1673.
Образование оксима описано в Truce et al. J. Org. Chem., 1957, 617, 620, a восстановление оксима описано в Bakenbus et al., J. Am. Chem. Soc., 1955, 77, 3866. Последующее получение соли гидрохлорида этого амина может быть осуществлено общепринятыми способами.
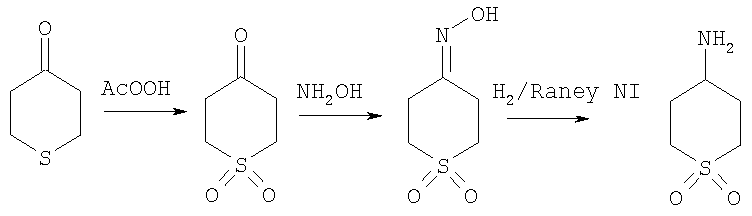
Промежуточное соединение 15: 4-Хлор-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
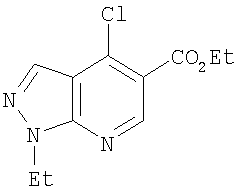
Раствор Промежуточного соединения 1 (3,5 г) в диоксане (28 мл) обрабатывали гидроксидом калия (6,3 г) в виде раствора в воде (20 мл). Смесь перемешивали в течение 2 ч, затем концентрировали в вакууме, подкисляли до рН 3 при помощи 2 М водной соляной кислоты и экстрагировали этилацетатом. Слои разделяли, органический слой сушили над сульфатом натрия, затем концентрировали в вакууме с получением Промежуточного соединения 15 в виде белого твердого вещества (2,4 г). LCMS показала МН+=226; TRET=2,62 мин.
Промежуточное соединение 17: N-Бензил-4-хлор-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
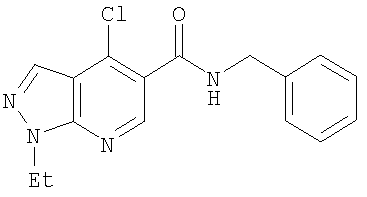
То есть промежуточное соединение 17 представляет собой:
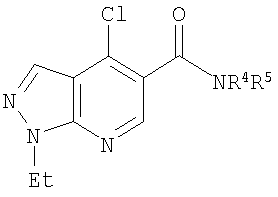 , где NR4R5 =
, где NR4R5 = 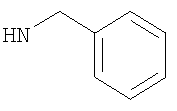
Промежуточное соединение 15 (3,5 г) сушили над пентоксидом фосфора в течение 1 ч, затем обрабатывали тионилхлоридом (47 г). Смесь перемешивали и нагревали при 75°С в течение 1,3 ч. Избыток тионилхлорида удаляли в вакууме и остаточное масло азеотропно перегоняли с дихлорметаном (DCM) с получением Промежуточного соединения 16, предполагаемого хлорангидридного производного Промежуточного соединения 15, в виде белого твердого вещества (3,3 г).
Промежуточное соединение 16 (0,473 г) растворяли в тетрагидрофуране (THF) (4 мл) и обрабатывали N,N-диизопропилэтиламином (DIPEA) (0,509 мл), затем бензиламином (0,209 г), и смесь перемешивали в атмосфере азота в течение 0,5 ч. Эту смесь концентрировали в вакууме, затем распределяли между дихлорметаном и водой. Слои разделяли и органические вещества концентрировали в вакууме с получением Промежуточного соединения 17 (0,574 г). LCMS показала MH+=315; TRET=2,90 мин.
Аналогично получали следующее:

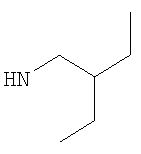
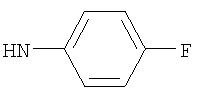
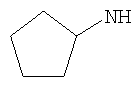
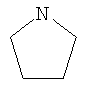
Промежуточное соединение 22: 4-Хлор-1-этил-N-(пиридин-4-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
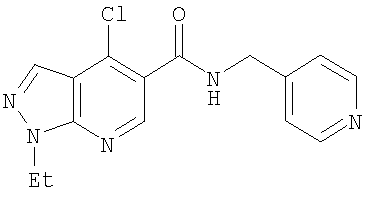
Хлорангидридное Промежуточное соединение 16 синтезировали из Промежуточного соединения 15, используя способ, показанный выше для Промежуточного соединения 17. Промежуточное соединение 16 (0,473 г) растворяли в THF (4 мл) и обрабатывали N,N-диизопропилэтиламином (DIPEA) (0,509 мл), затем 4-(аминометил)пиридином (0,211 г) и эту смесь перемешивали в атмосфере азота в течение 0,5 ч. Эту смесь концентрировали в вакууме, затем распределяли между DCM и водой. Слои разделяли и органические вещества концентрировали в вакууме, затем наносили на SPE картридж (силикагель, 10 г), который элюировали градиентом циклогексан:EtOAc (2:1, постепенно повышая до 0:1), затем МеОН:EtOAc (5:95, затем 10:90). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 22 (0,086 г). LCMS показала МН+=316; TRET=1,84 мин.
Промежуточное соединение 23: 4-Хлор-1-этил-N-н-пропил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
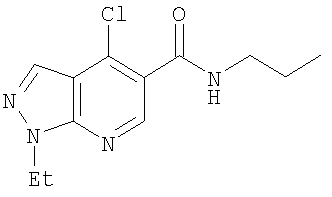
Хлорангидридное Промежуточное соединение 16 синтезировали из Промежуточного соединения 15, используя способ, показанный выше для Промежуточного соединения 17. Промежуточное соединение 16 (0,473 г) растворяли в THF (4 мл) и обрабатывали DIPEA (0,509 мл), затем н-пропиламином (0,115 г) и смесь перемешивали в атмосфере азота в течение 0,5 ч. Затем добавляли следующую порцию н-пропиламина (0,023 г) и перемешивание продолжали в течение 18 ч. Смесь концентрировали в вакууме, затем распределяли между DCM и водой. Слои разделяли и органические вещества концентрировали в вакууме с получением Промежуточного соединения 23 (0,405 г). LCMS показала МН+=267; TRET=2,54 мин.
Промежуточное соединение 24: 4-Хлор-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
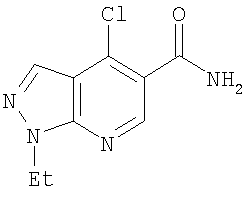
Хлорангидридное Промежуточное соединение 16 синтезировали из Промежуточного соединения 15, используя способ, показанный выше для Промежуточного соединения 17. Промежуточное соединение 16 (0,30 г) растворяли в THF (3 мл) и обрабатывали 0,5 М раствором аммиака в диоксане (4,92 мл). Эту смесь перемешивали в атмосфере азота в течение 18 ч. Добавляли следующую порцию 0,5 М аммиака в диоксане (4,92 мл), и перемешивание продолжали в течение 72 ч. Эту смесь концентрировали в вакууме, и остаток распределяли между DCM и 2 М раствором гидроксида натрия. Слои разделяли и органические вещества концентрировали в вакууме с получением Промежуточного соединения 24 (0,278 г). LCMS показала МН+=225; ТRET=2,10 мин.
Промежуточное соединение 25: Этил-4-хлор-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
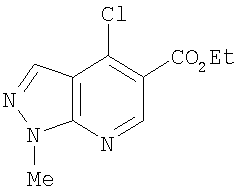
Смесь 5-амино-1-метилпиразола (4,0 г) и диэтилэтоксиметиленмалоната (9,16 мл) нагревали при 150°С в условиях Дина-Старка в течение 5 ч. К смеси осторожно добавляли оксихлорид фосфора (55 мл) и полученный в результате раствор нагревали при 130°С с обратным холодильником в течение 18 ч. Смесь концентрировали в вакууме, затем остаточное масло охлаждали в ледяной бане и осторожно обрабатывали водой (100 мл) (предупреждение: экзотермия). Полученную в результате смесь экстрагировали DCM (3×100 мл) и объединенные органические экстракты сушили над безводным сульфатом натрия и концентрировали в вакууме. Остаточное твердое вещество очищали Biotage хроматографией (силикагель, 90 г), элюируя смесью Et2O:бензин (1:3). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 25 (4,82 г). LCMS показала MH+=240; TRET=2,98 мин.
Промежуточное соединение 26: 4-Хлор-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
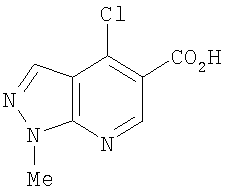
Раствор Промежуточного соединения 25 (4,0 г) в диоксане (30 мл) обрабатывали гидроксидом калия (7,54 г) в виде раствора в воде (20 мл). Эту смесь перемешивали в течение 16 ч, затем разбавляли водой (150 мл) и подкисляли до рН 3 при помощи 5 М водной соляной кислоты. Смесь перемешивали в ледяной бане в течение 15 мин, затем собирали фильтрацией, промывали ледяной водой и сушили в вакууме над пентоксидом фосфора с получением Промежуточного соединения 26 в виде белого твердого вещества (2,83 г). LCMS показала MH+=212; TRET=2,26 мин.
Промежуточное соединение 28: N-Бензил-4-хлор-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
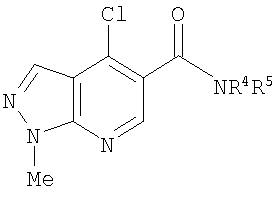 Промежуточное соединение 28 NR4R5=
Промежуточное соединение 28 NR4R5= 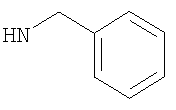
Промежуточное соединение 26 (2,5 г) (прежде высушенное над пентоксидом фосфора) обрабатывали тионилхлоридом (25 мл) и эту смесь нагревали с обратным холодильником в течение 1 ч. Избыток тионилхлорида удаляли в вакууме с получением Промежуточного соединения 27, предполагаемого хлорангидридного производного Промежуточного соединения 26, в виде белого твердого вещества (2,7 г).
Промежуточное соединение 27 (0,68 г) растворяли в THF (10 мл) и обрабатывали DIPEA (0,77 мл), затем бензиламином (0,339 г) и смесь перемешивали в атмосфере азота в течение 3 ч. Эту смесь концентрировали в вакууме, затем распределяли между DCM (20 мл) и водой (10 мл). Слои разделяли и органические вещества концентрировали в вакууме с получением Промежуточного соединения 28 (0,90 г). LCMS показала МН+=301; TRET=2,72 мин.
Аналогично получали следующее:

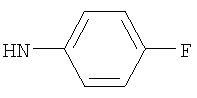
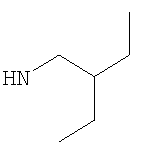
Промежуточное соединение 31: 4-Хлор-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
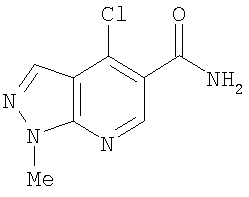
Хлорангидридное Промежуточное соединение 27 синтезировали из Промежуточного соединения 26, используя способ, показанный выше для Промежуточного соединения 28. Затем промежуточное соединение 27 (0,68 г) обрабатывали 0,5 М раствором аммиака в диоксане (17,7 мл). Затем добавляли диизопропилэтиламин (0,51 мл) и смесь перемешивали в течение 21 ч. Затем смесь распределяли между DCM (100 мл) и водой (30 мл). Нерастворимое твердое вещество отделяли фильтрацией, промывали водой (20 мл) и сушили в вакууме над пентоксидом фосфора с получением Промежуточного соединения 31 (0,544 г). LCMS показала МН+=211; TRET=1,84 мин.
Промежуточное соединение 32 (= Пример 3): Этил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
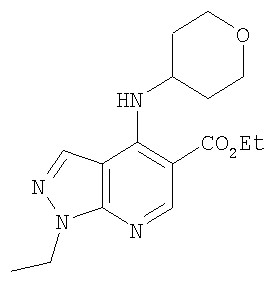
Промежуточное соединение 1 (0,20 г) и триэтиламин (0,55 мл) суспендировали в этаноле (8 мл) и добавляли 4-аминотетрагидропиран (0,088 г). Смесь перемешивали в атмосфере азота, нагревали при 80°С в течение 16 ч, затем концентрировали в вакууме. Остаток распределяли между DCM и водой. Слои разделяли и органический слой непосредственно наносили на SPE картридж (силикагель, 5 г), который элюировали последовательно: (1) DCM, (2) DCM:Et2O (2:1), (3) DCM:Et2O (1:1), (4) Et2O и (5) EtOAc. Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 32 (0,21 г). LCMS показала МН+=319; TRET=2,93 мин.
В альтернативном воплощении Промежуточное соединение 32 (= Пример 3) может быть получено, как описано ниже под заголовком "Пример 3", в частности в соответствии с "Примером 3, способ Б" ниже.
Промежуточное соединение 33: 1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
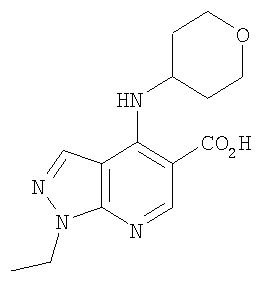
Раствор Промежуточного соединения 32 (Примера 3) (0,21 г) в смеси этанол:вода (95:5, 10 мл) обрабатывали гидроксидом натрия (0,12 г). Эту смесь нагревали при 50°С в течение 8 ч, затем концентрировали в вакууме, растворяли в воде и подкисляли до рН 4 уксусной кислотой. Полученное в результате белое твердое вещество отделяли фильтрацией и сушили в вакууме с получением Промежуточного соединения 33 в виде не совсем белого твердого вещества (0,156 г). LCMS показала MH+=291; TRET=2,11 мин.
Альтернативное получение Промежуточного соединения 33 описано ниже.
Раствор Промежуточного соединения 32 (Пример 3) (37,8 г) в смеси этанол:вода (4:1, 375 мл) обрабатывали гидроксидом натрия (18,9 г). Смесь нагревали при 50°С в течение 5 часов, затем концентрировали в вакууме, растворяли в воде и подкисляли до рН 2 водной соляной кислотой (2 М). Полученное в результате белое твердое вещество выделяли фильтрацией и сушили в вакууме с получением Промежуточного соединения 33 в виде не совсем белого твердого вещества (29,65 г). LCMS показала
MH+=291; TRET=2,17 мин.
Промежуточное соединение 34 (= Пример 8): Этил-1-этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
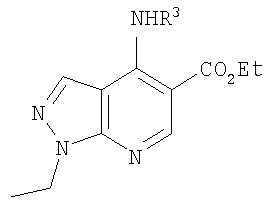 Промежуточное соединение 34 NHR3=
Промежуточное соединение 34 NHR3= 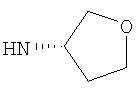
Промежуточное соединение 1 (0,05 г) и (S)-(-)-3-аминотетрагидрофуран-4-толуолсульфонат (0,052 г) суспендировали в этаноле (1 мл) и добавляли триэтиламин (0,14 мл). Эту смесь перемешивали в атмосфере азота и нагревали при 80°С в течение 24 ч. После охлаждения до комнатной температуры этанол удаляли выпариванием в потоке азота, и остаток распределяли между DCM (2 мл) и водой (1,5 мл). Слои разделяли и органический слой концентрировали до сухости. Очистку осуществляли, используя SPE картридж (силикагель, 5 г), элюируя градиентом EtOAc:циклогексан (1:16, затем 1:8, 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 34 (= Пример 8) (0,052 г). LCMS показала МН+=305; TRET=2,70 мин.
Аналогично получали следующее:
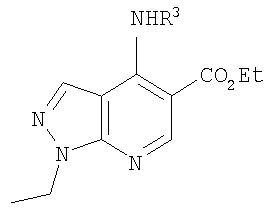
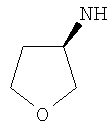
Аминотетрагидрофуран-4-
толуолсульфонат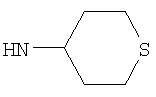
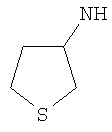
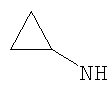
Промежуточное соединение 39 (= Пример 13): Этил-4-[(1,1'-диоксидотетрагидротиен-3-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
 Промежуточное соединение 39 NHR3=
Промежуточное соединение 39 NHR3= 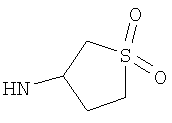
Промежуточное соединение 1 (0,05 г) и Промежуточное соединение 13 (0,027 г) суспендировали в этаноле (1 мл) и добавляли триэтиламин (0,14 мл). Смесь перемешивали в атмосфере азота и нагревали при 80°С в течение 24 ч. После охлаждения до комнатной температуры этанол удаляли выпариванием в потоке азота, и остаток распределяли между DCM (2 мл) и водой (1,5 мл). Слои разделяли и органический слой концентрировали до сухости. Очистку осуществляли, используя SPE картридж (силикагель, 5 г), элюируя градиентом EtOAc:циклогексан (1:8, затем 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Промежуточного соединения 39 (= Пример 13) (0,045 г) в виде смеси энантиомеров. LCMS показала МН+=353; RRET=2,60 мин. Аналогично получали следующее:

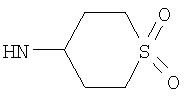
Промежуточное соединение 41 1-Этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
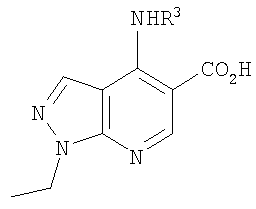 Промежуточное соединение 41 NHR3=
Промежуточное соединение 41 NHR3= 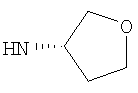
Раствор Промежуточного соединения 34 (0,037 г) в смеси этанол:вода (95:5, 3 мл) обрабатывали гидроксидом натрия (0,019 г). Смесь нагревали при 50°С в течение 16 ч, затем концентрировали в вакууме. Остаток растворяли в воде (1,5 мл) и подкисляли до рН 4 уксусной кислотой. Полученный в результате белый твердый осадок выделяли фильтрацией и сушили в вакууме. Фильтрат экстрагировали этилацетатом, и органический слой собирали и концентрировали в вакууме с получением дополнительной порции белого твердого вещества. Эти два твердых вещества объединяли с получением Промежуточного соединения 41 (0,033 г). LCMS показала МН+=277; TRET=2,05 мин.
Аналогично получали следующее:

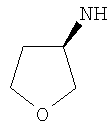
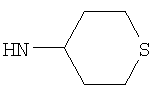
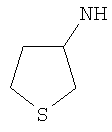
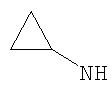
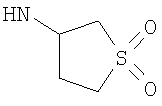
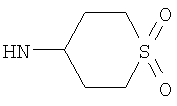
Промежуточное соединение 48: Этил-4-(циклогексиламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
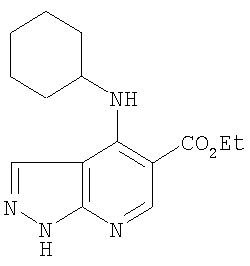
Промежуточное соединение 2 (0,69 г) суспендировали в циклогексиламине (1,01 мл) и смесь нагревали при 90°С в течение 3 ч. Остаточную смесь оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (25 мл) и водой (25 мл). Фазы разделяли и органическую фазу упаривали до сухости. Остаток растирали с Et2O (25 мл) и нерастворимое твердое вещество собирали и сушили с получением Промежуточного соединения 48 в виде бежевого твердого вещества (0,58 г). LCMS показала MH+=289; TRET=2,91 мин.
Промежуточное соединение 49: 4-(Циклогексиламино)-1N-пиразоло[3,4-b]пиридин-5-карбоновая кислота
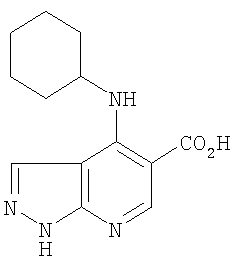
2 М раствор гидроксида натрия (0,5 мл) добавляли к перемешиваемой суспензии Промежуточного соединения 48 (0,2 г) в диоксане (4 мл) и воде (0,5 мл). После перемешивания в течение ночи при комнатной температуре реакционную смесь нагревали при 40°С в течение 8 ч. Добавляли дополнительное количество 2М раствора гидроксида натрия (1,5 мл) и реакционную смесь нагревали при 40°С в течение 48 ч. Реакционный раствор концентрировали, разбавляли водой (10 мл) и подкисляли ледяной уксусной кислотой. Полученный в результате осадок собирали фильтрацией, промывали водой и сушили с получением Промежуточного соединения 49 (0,18 г). LCMS показала МН+=261; TRET=2,09 мин.
Промежуточное соединение 50: 1-н-Пропил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоновая кислота
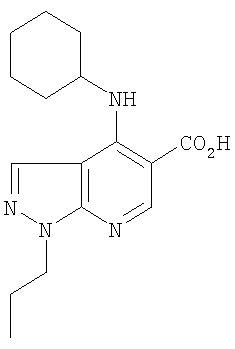
2 М раствор гидроксида натрия (0,7 мл) добавляли к перемешиваемой суспензии Примера 185 (0,23 г, описан ниже) в этаноле (5 мл) и воде (1,5 мл). После перемешивания в течение ночи при комнатной температуре добавляли дополнительное количество 2 М раствора гидроксида натрия (0,7 мл) и реакционную смесь нагревали при 43°С в течение 2,5 ч. Реакционный раствор концентрировали, разбавляли водой (5 мл) и подкисляли 2 М соляной кислотой. Полученный в результате осадок собирали фильтрацией, промывали водой и сушили с получением Промежуточного соединения 50 в виде белого твердого вещества (0,14 г). LCMS показала МН+=305; TRET=2,42 мин.
Промежуточное соединение 51: Этил-4-хлор-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
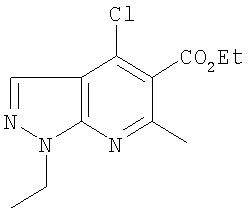
Смесь 5-амино-1-этилпиразола (1,614 г, 14,5 ммоль) и диэтил-2-(1-этоксиэтилиден)малоната (3,68 г, 16,0 ммоль, как описано в Р.Р.Т. San, J. Amer. Chem. Soc., 1931, 53, 1836) нагревали при 150°С в условиях Дина-Старка в течение 5 ч. К этой смеси осторожно добавляли оксихлорид фосфора (25 мл), и полученный в результате раствор нагревали при 130°С с обратным холодильником в течение 18 ч. Смесь концентрировали в вакууме, затем остаточное масло осторожно добавляли при охлаждении к воде (100 мл). Полученную в результате смесь экстрагировали DCM (3х100 мл) и объединенные органические экстракты сушили над безводным сульфатом натрия и концентрировали в вакууме. Остаточное масло очищали Biotage хроматографией (силикагель, 90 г), элюируя смесью этилацетат:бензин (1:19). Фракции, содержащие желаемый продукт, объединяли и концентрировали в вакууме с получением Промежуточного соединения 51 (1,15 г). LCMS показала МН+=268; TRET=3,18 мин.
Промежуточное соединение 52:
4-(Циклогексиламино)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
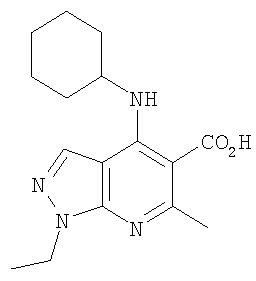
2 М раствор гидроксида натрия (0,39 мл, 0,78 ммоль) добавляли к Примеру 190 (0,128 г, 0,39 ммоль, описан ниже) в этаноле (1,5 мл) и эту смесь нагревали при 50°С в течение 16 часов. Реакционную смесь концентрировали и полученный в результате водный раствор нейтрализовали 2 М соляной кислотой с осаждением твердого вещества, которое собирали фильтрацией. Фильтрат наносили на картридж (Картриджи для HLB экстракции OASIS® продаются Waters Corporation, 34 Maple Street, Milford, MA 01757, USA. Эти картриджи включают колонку, содержащую сополимерный сорбент, имеющий такой HLB, что когда водный раствор элюируют через колонку, растворенное вещество абсорбируется или адсорбируется в сорбенте или на сорбенте, и такой, что когда элюируют органический растворитель (например, метанол), это растворенное вещество высвобождается в виде органического (например, метанольного) раствора. Это способ отделения растворенного вещества от водного растворителя.) OASIS® для экстракции за счет гидрофильно-липофильного баланса (HLB) (1 г), который элюировали водой, а затем метанолом. В результате выпаривания метанольной фракции получали твердое вещество, которое объединяли с исходным осажденным твердым веществом с получением Промежуточного соединения 52 (0,083 г) в виде белого твердого вещества, предположительно представляющего собой карбоновую кислоту.
Промежуточное соединение 53:
1-Этил-6-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоновая кислота
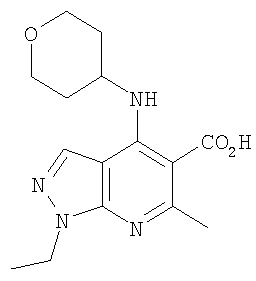
2 М раствор гидроксида натрия (0,75 мл, 1,5 ммоль) добавляли к Примеру 189 (0,248 г, 0,75 ммоль, описан ниже) в этаноле (2 мл) и смесь нагревали с обратным холодильником в течение 16 часов. Реакционную смесь концентрировали, разбавляли водой (1 мл) и подкисляли 2 М соляной кислотой (0,75 мл) с осаждением твердого вещества, которое собирали фильтрацией с получением Промежуточного соединения 53 (0,168 г). LCMS показала МН+=305; TRET=1,86 мин.
Промежуточное соединение 54: 4-Аминоциклогексанона гидрохлорид
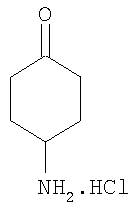
Раствор хлористого водорода в диоксане (0,5 мл, 2,0 ммоль, 4 М) добавляли к перемешиваемому раствору трет-бутил-4-оксоциклогексилкарбамата (0,043 г, 0,20 ммоль, имеется в продаже у Astatech Inc., Philadelphia, USA) в диоксане (0,5 мл) и смесь перемешивали при комнатной температуре. Через 1 ч реакционную смесь выпаривали с получением Промежуточного соединения 54 в виде кремового твердого вещества (34 мг). 1H ЯМР (400 МГц в d6-DMSO, 27°С, δ млн-1) 8.09 (br.s, 3Н), 3.51 (tt, 11, 3,5 Гц, 1Н), 2.45 (m, 2H, частично скрыт), 2.29 (m, 2H), 2.16 (m, 2H), 1.76 (m, 2H).
Промежуточное соединение 54А: N-Бензил-4-(циклогексиламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
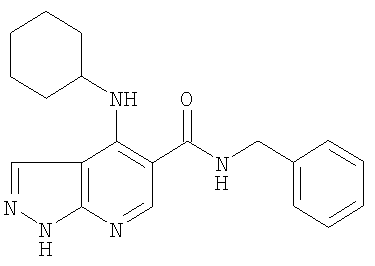
Бензиламин (0,16 мл) добавляли к перемешиваемой смеси Промежуточного соединения 49 (0,13 г), DIPEA (0,26 мл) и HATU (0,285 г) в DMF (3 мл). Полученную в результате смесь нагревали при перемешивании при 85°С в течение 16 часов. Добавляли дополнительные порции HATU (0,14 г), DIPEA (0,13 мл) и бензиламина (0,082 мл) и смесь нагревали в течение 16 часов при 88°С. Полученный в результате раствор концентрировали, разбавляли дихлорметаном (20 мл) и промывали насыщенным раствором бикарбоната натрия (20 мл), разделяли с помощью гидрофобной фритты, и органический слой концентрировали. Остаток очищали на SPE картридже (силикагель, 20 г), элюируя 60-80%-ным этилацетатом в циклогексане. Остаток дополнительно очищали на SPE картридже (картридж с сульфоновой кислотой Isolute SCX, 5 г×2), элюируя метанолом (2×20 мл) и 10%-ным аммиаком в метаноле (4×20 мл); основные фракции объединяли и концентрировали с получением Промежуточного соединения 54А в виде белого твердого вещества (0,07 г). LCMS показала MH+=350; TRET=2,99 мин.
Промежуточное соединение 55: 4-Хлор-1-этил-N-{[4-(метилокси)фенил]-метил}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
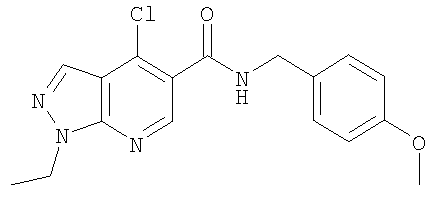
то есть промежуточное соединение 55 представляет собой: 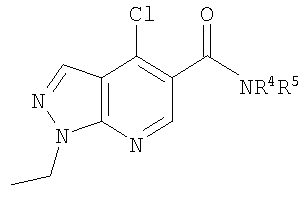 ,
,
где NR4R5= 
Промежуточное соединение 15 (1,04 г) обрабатывали тионилхлоридом (13,22 г). Эту смесь перемешивали и нагревали при 75°С в течение 2 ч. Избыток тионилхлорида удаляли в вакууме и остаточное масле азеотропно перегоняли с толуолом с получением Промежуточного соединения 16, предполагаемого хлорангидридного производного Промежуточного соединения 15, в виде кремового твердого вещества (1,12 г).
Промежуточное соединение 16 (0,997 г) растворяли в тетрагидрофуране (THF) (25 мл) и обрабатывали N,N-диизопропилэтиламином (1,07 мл), затем 1-[4-(метилокси)фенил]метанамином = 4-метоксибензиламином (0,54 мл) (может быть получен, например, от Aldrich, Acros или как описано в Tetrahedron Lett., 2002, 43(48), 8735; либо в Meindl et al., J. Med. Chem., 1984, 27(9), 1111 или в Organic Letters, 2002, 4(12), 2055), и эту смесь перемешивали в течение 3 ч. Раствор концентрировали в вакууме, затем распределяли между DCM и водой. Слои разделяли и органические вещества концентрировали в вакууме. Затем твердое вещество растирали со смесью этилацетат:циклогексан 1:1 с получением Промежуточного соединения 55 (1,27 г). LCMS показала МН+=345; TRET=2,86 мин.
Аналогично получали следующее:
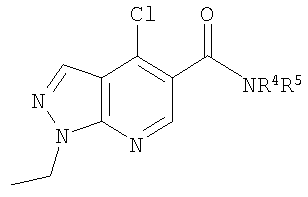
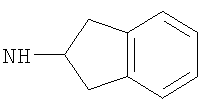
Промежуточное соединение 58: 1-Этил-4-[(4-оксоциклогексил)амино]-1H-пиразоло[3,4-b]пиридин-5-карбоновая кислота
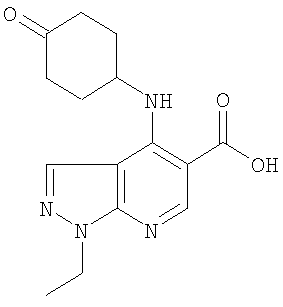
Раствор гидроксида натрия (0,053 г, 1,32 ммоль) в воде (0,41 мл) добавляли к перемешиваемому раствору Примера 205 (0,1 г, 0,303 ммоль) в этаноле (1 мл) и полученную в результате смесь нагревали при 50°С. Через 1 ч охлажденную реакционную смесь доводили до рН 3 при помощи 2 М соляной кислоты и экстрагировали EtOAc (2×6 мл). Объединенные органические экстракты сушили
(Na2SO4) и упаривали с получением Промежуточного соединения 58 (0,072 г) в виде белого твердого вещества. LCMS показала МН+=303; ТRET=2,13 мин.
Альтернативным получением Промежуточного соединения 58 является следующее.
Раствор гидроксида натрия (0,792 г, 19,8 ммоль) в воде (6 мл) добавляли к перемешиваемому раствору Примера 205 (1,487 г, 4,5 ммоль) в этаноле (15 мл) и полученную в результате смесь нагревали при 50°С. Через 1 ч охлажденную реакционную смесь доводили до рН 4 при помощи 2 М соляной кислоты и экстрагировали EtOAc (3×30 мл). Объединенные органические экстракты сушили (Na2SO4) и выпаривали с получением Промежуточного соединения 58 (1,188 г) в виде белого твердого вещества. LCMS показала МН+=303; ТRET=2,12 мин.
Промежуточное соединение 58А: Этил-1-этил-4-(тетрагидро-2Н-пиран-3-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
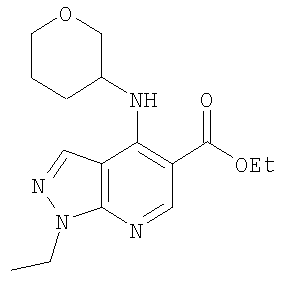
Промежуточное соединение 1 (0,76 г, 3,0 ммоль) растворяли в ацетонитриле (10 мл). Добавляли гидрохлорид тетрагидро-2Н-пиран-3-амина (0,5 г, 3,6 ммоль, Anales De Quimica, 1988, 84, 148) и N,N-диизопропилэтиламин (3,14 мл, 18,0 ммоль) и эту смесь перемешивали при 85°С в течение 24 ч. Через 24 ч добавляли дополнительную порцию гидрохлорида тетрагидро-2H-пиран-3-амина (0,14 г, 1,02 ммоль) и продолжали перемешивание при 85°С. Еще через 8 ч смесь концентрировали в вакууме. Остаток распределяли между DCM (20 мл) и водой (12 мл). Слои разделяли и водный слой экстрагировали дополнительным количеством DCM (12 мл). Объединенные органические экстракты сушили (Na2SO4) и концентрировали в вакууме с получением коричневого твердого вещества, которое очищали на SPE картридже (силикагель, 20 г), элюируя градиентом этилацетат:циклогексан (1:16, 1:8, 1:4, 1:2, 1:1, 1:0). Фракции, содержащие нужное вещество, объединяли и выпаривали с получением Промежуточного соединения 58А (0,89 г). LCMS показала MH+=319; TRET=2,92 мин.
Промежуточное соединение 59: 1-Этил-4-(тетрагидро-2Н-пиран-3-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
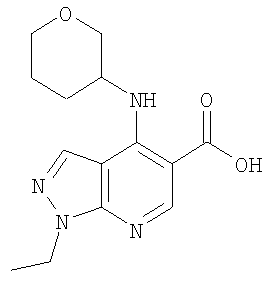
Раствор Промежуточного соединения 58А (0,89 г, 2,79 ммоль) в этаноле (16,7 мл) обрабатывали гидроксидом натрия (0,47 г, 11,7 ммоль) в виде раствора в воде (3,1 мл). Смесь перемешивали при 50°С. Через 12 ч реакционную смесь концентрировали в вакууме с получением остаточного масла, которое растворяли в воде (16 мл), затем охлаждали и подкисляли до рН 3 при помощи 2 М соляной кислоты. После перемешивания при 0°С в течение 30 мин полученный в результате осадок собирали фильтрацией, промывали охлажденной водой (2 мл) и сушили в вакууме с получением Промежуточного соединения 59 в виде белого твердого вещества (0,73 г). LCMS показала МН+=291; TRET=2,19 мин.
Промежуточное соединение 60: 4-[(1-Ацетил-4-пиперидинил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
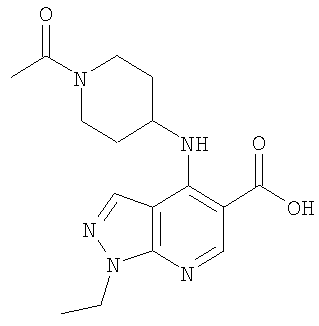
Водный раствор гидроксида натрия (8,55 мл, 2 М) добавляли к раствору Примера 207 (1,55 г) в EtOH (13 мл). Смесь нагревали при 50°С в течение 18 ч, затем нейтрализовали, используя водную соляную кислоту, и выпаривали в вакууме с получением смеси 1-этил-4-(4-пиперидиниламино)-1H-пиразоло[3,4-b]пиридин-5-карбоновой кислоты и 4-[(1-ацетил-4-пиперидинил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоновой кислоты.
Уксусную кислоту (0,36 мл) добавляли к перемешиваемой смеси HATU (2,41 г) и N,N-диизопропилэтиламина (2,21 мл) в N,N-диметилформамиде (65 мл). После перемешивания в течение 15 мин эту смесь добавляли к смеси 1-этил-4-(4-пиперидиниламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоновой кислоты и 4-[(1-ацетил-4-пиперидинил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоновой кислоты и эту реакционную смесь перемешивали в течение 15ч. Реакционную смесь упаривали в вакууме, и остаток очищали хроматографией, используя Biotage (силикагель, 90 г), элюируя DCM:МеОН (0%-5% МеОН), с получением Промежуточного соединения 60 (1,36 г) в виде белого твердого вещества. LCMS показала МН+=334; TRET=2,06 мин.
Промежуточное соединение 61: 4-(Циклогексиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
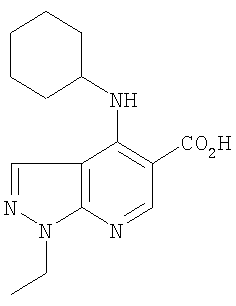
Раствор Примера 2 (5,37 г, 17 ммоль) в этаноле (30 мл) обрабатывали раствором гидроксида натрия (2,72 г, 68 ммоль) в воде (20 мл), и полученную в результате смесь перемешивали при 50°С в течение 3 ч. Реакционную смесь концентрировали в вакууме, растворяли в воде (250 мл), и охлажденный раствор подкисляли до рН 1 при помощи 5 М соляной кислоты. Полученное в результате твердое вещество собирали фильтрацией и сушили в вакууме с получением Промежуточного соединения 61 в виде белого твердого вещества (4,7 г). LCMS показала MH+=289; TRET=2,83 мин.
Промежуточное соединение 62: 1,1-Диметилэтил-(4,4-дифторциклогексил)-карбамат
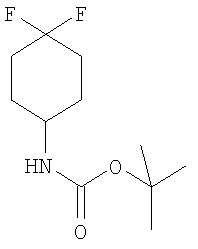
(Диэтиламино)серы трифторид (DAST) (0,06 мл, 0,47 ммоль) добавляли к перемешиваемому раствору 1,1-диметилэтил(4-оксоциклогексил)карбамата (250 мг, 1,17 ммоль, имеется в продаже у AstaTech Inc., Philadelphia, USA) в безводном дихлорметане (5 мл) и эту смесь перемешивали в атмосфере азота при 20°С. Через 22 ч реакционную смесь охлаждали до 0°С, обрабатывали насыщенным раствором гидрокарбоната натрия (4 мл), а затем оставляли нагреваться до температуры окружающей среды. Фазы разделяли пропусканием через гидрофобную фритту и водную фазу затем экстрагировали DCM (5 мл). Объединенные органические фазы концентрировали в вакууме с получением оранжевого твердого вещества (369 мг), которое дополнительно очищали хроматографией, используя SPE картридж (силикагель, 10 г), элюируя DCM, с получением Промежуточного соединения 62 (140 мг), содержащего 20% 1,1-диметилэтил-(4-фтор-3-циклогексен-1-ил)карбамата. 1H ЯМР (400 МГц в CDCl3, 27°С, δ млн-1).
Минорный компонент: δ 5.11 (dm, 16 Гц, 1Н), 4.56 (br, 1H), 3.80 (br, 1H), 2.45-1.45 (m's, 6H, избыток), 1.43 (s, 9H). Основной компонент: δ 4.43 (br, 1H), 3.58 (br, 1H), 2.45-1.45 (m's, 8H, избыток), 1.45 (s, 9H).
Промежуточное соединение 63: 4-(4,4-дифторциклогексил)амина гидрохлорид
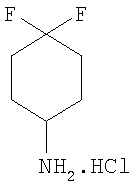
Раствор хлористого водорода в диоксане (4 М, 1,6 мл) добавляли при 20°С к перемешиваемому раствору Промежуточного соединения 62 (140 мг, 0,6 ммоль) в диоксане (1,6 мл). Через 3 ч реакционную смесь концентрировали в вакууме с получением Промежуточного соединения 63 (96,5 мг), содержащего 4-фтор-3-циклогексен-1-амин. 1H ЯМР (400 МГц в d6-DMSO, 27°C, δ млн-1). Минорный компонент: 5 8.22 (br, 3Н избыток), 5.18 (dm, 16 Гц, 1Н), 3.28-3.13 (m, 1H, избыток), 2.41-1.53 (m's, 6H, избыток). Основной компонент: δ 8.22 (br, 3Н, избыток), 3.28-3.13 (m, 1H, избыток), 2.41-1.53 (m's, 8H, избыток). Также присутствуют примеси.
Промежуточное соединение 64: 4-Хлор-1-этил-N-метил-1N-пиразоло[3,4-b]пиридин-5-карбоксамид
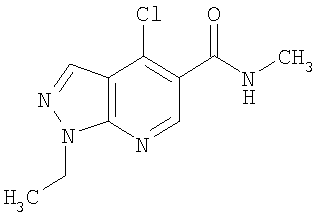
Промежуточное соединение 15 (0,06 г, 0,266 ммоль) обрабатывали тионилхлоридом (0,48 мл). Эту смесь перемешивали и нагревали при 75°С в течение 2 ч. Избыток тионилхлорида удаляли в вакууме и остаточное масло азеотропно перегоняли с дихлорметаном (DCM) с получением Промежуточного соединения 16, предполагаемого хлорангидридного производного Промежуточного соединения 15, в виде белого твердого вещества. Промежуточное соединение 16 растворяли в безводном тетрагидрофуране (THF) (2 мл) и обрабатывали N,N-диизопропилэтиламином (DIPEA) (0,069 мл), затем метиламином (2 М в тетрагидрофуране, 0,15 мл) и эту смесь перемешивали в атмосфере азота в течение 16 ч. Добавляли дополнительное количество метиламина (2 М в THF) и раствор перемешивали в течение 2 ч. Смесь концентрировали в вакууме, затем распределяли между дихлорметаном (2 мл) и водным раствором гидроксида натрия (2 М, 2 мл), затем органический слой промывали водой (2 мл). Слои разделяли и органические вещества концентрировали в вакууме с получением Промежуточного соединения 64 (0,052 г). LCMS показала МН+=239; TRET=2,17 мин.
Промежуточное соединение 65: Этил-4-[(1-{[(1,1-диметилэтил)окси]-карбонил}-4-пиперидинил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
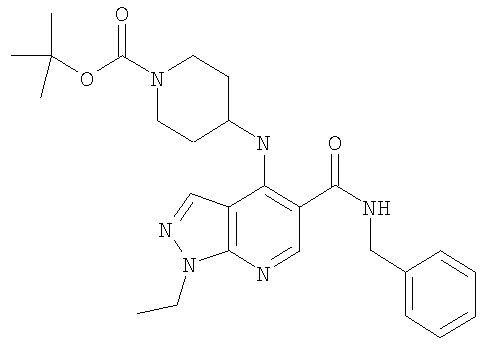
Смесь Промежуточного соединения 17 (2,0 г, 6,37 ммоль), 1,1-диметилэтил-4-амино-1-пиперидинкарбоксилата (2,04 г, 10,2 ммоль) и N,N-диизопропилэтиламина (5,54 мл, 31,9 ммоль) в MeCN (40 мл) нагревали при 85°С в течение 42 ч. Реакционную смесь выпаривали, и остатки распределяли между DCM и водой. Органическую фазу сушили (MgSO4), затем выпаривали в вакууме. Остаток хроматографировали на силикагеле (Biotage, 90 г), элюируя смесью циклогексан: EtOAc (1:1) с получением Промежуточного соединения 65 в виде белого твердого вещества (2,70 г). LCMS показала МН+=479; TRET=3,37 мин.
Промежуточное соединение 67: 3-Амино-N-циклогексил-N-метилбензамид
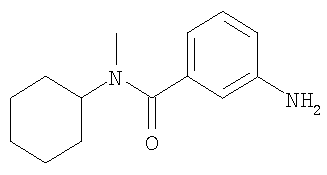
Раствор 3-нитробензоилхлорида (2,0 г, 10,78 ммоль) в DCM (20 мл) по каплям добавляли к перемешиваемой смеси N-метилциклогексиламина (1,83 мл, 14,01 ммоль), N,N-диизопропилэтиламина (3,76 мл, 21,56 ммоль) и N,N-диметиламинопиридина (0,01 г) в DCM при 20°С. Эту реакционную смесь перемешивали в течение 36 ч, затем выпаривали в вакууме. Остаток распределяли между этилацетатом и водой. Органическую фазу промывали водной HCl, затем сушили (MgSO4) и выпаривали в вакууме. Остаток очищали хроматографией на силикагеле, элюируя смесью циклогексан:EtOAc (9:1, затем 2:1) с получением N-циклогексил-N-метил-3-нитробензамида (1,40 г). MS показала МН+=263.
Смесь N-циклогексил-N-метил-3-нитробензамида (1,40 г, 5,35 ммоль) и палладия на угле (5%, 0,140 г) в этаноле (10 мл) перемешивали в атмосфере водорода в течение 1 часа. Реакционную смесь фильтровали через целит и фильтрат упаривали с получением Промежуточного соединения 67 в виде коричневого твердого вещества (0,107 г). LCMS показала МН+=233; TRET=2,56 мин.
Промежуточное соединение 68: N-Этил-4-оксо-1-пиперидинкарбоксамид
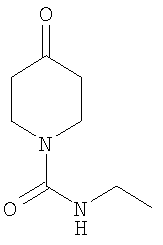
Раствор этилизоцианата (2,31 г, 32,5 ммоль) в DCM (40 мл) добавляли по каплям в течение 15 мин к энергично перемешиваемому раствору 4-пиперидона моногидрата гидрохлорида (5,0 г, 32,5 ммоль, имеется в продаже у Aldrich) и гидрокарбоната натрия (8,2 г, 97,5 ммоль) в воде (60 мл) при 0°С. Эту реакционную смесь перемешивали при комнатной температуре в течение 20 часов. К реакционной смеси добавляли хлорид натрия (7,0 г) и органическую фазу отделяли. Водную фазу экстрагировали дополнительным количеством DCM (3×75 мл). Объединенные органические экстракты сушили (Na2SO4) и выпаривали в вакууме с получением белого твердого вещества (4,0 г). В результате перекристаллизации из смеси этилацетат:циклогексан (10:1) получали Промежуточное соединение 68 в виде белого твердого вещества (2,3 г).
ТСХ (силикагель) Rf=0,24 (этилацетат). Аналитически обнаружено: С, 56,7; Н, 8,3; N, 16,35. Для C8H14N2O2 требуется С, 56,5; Н, 8,3; N, 16,5.
Промежуточное соединение 69: 4-Амино-N-этил-1-пиперидинкарбоксамид
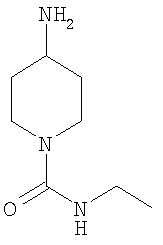
Раствор Промежуточного соединения 68 (1,5 г, 8,8 ммоль) и бензиламина (1,04 г, 9,7 ммоль) в абсолютном этаноле (60 мл) гидрировали над предварительно восстановленным катализатором 10%-ном палладии на угле (0,6 г) в этаноле (20 мл) до прекращения поглощения водорода (22 ч). Реакционную смесь фильтровали через фильтрующий агент (целит), а затем через силикагель (100 мл), элюируя раствором этанол:аммиак 0,88 (100:1), с получением черного масла. Это масло растворяли в этаноле (30 мл) и обрабатывали раствором хлористого водорода в этаноле (3 М) до тех пор, пока раствор не становылся кислым. Растворитель выпаривали и остаток растирали с этанолом с получением Промежуточного соединения 69 в виде белого твердого вещества (1,09 г).
ТСХ (силикагель) дала Rf=0,73 (этилацетатметанол, 10:1). Аналитически обнаружено: С, 45,9; Н, 8,4; N, 19,8. Для C8H18ClN3O требуется С, 46,3; Н, 8,7; N, 20,2.
Промежуточное соединение 70: 1,1-Диметилэтил({4-[(циклопропиламино)-карбонил]фенил}метил)карбамат
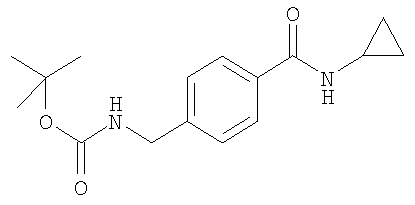
Циклопропиламин (0,136 г, 2,39 ммоль) и диизопропилэтиламин (0,68 мл, 3,9 ммоль) добавляли к перемешиваемому раствору 4-[({[(1,1-диметилэтил)окси]карбонил}амино)метил]бензойной кислоты (0,501 г, 2,0 ммоль), EDC (0,612 г, 3,2 ммоль) и НОВТ (0,35 г, 2,6 ммоль) в DMF (2 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Растворители удаляли в вакууме и остаток растворяли в этилацетате (20 мл) и промывали 0,5 М соляной кислотой (3×20 мл). Органическую фазу сушили (Na2SO4) и выпаривали в вакууме с получением неочищенного продукта, который очищали Biotage хроматографией (силикагель), элюируя смесью этилацетат:циклогексан (1,3:1), с получением Промежуточного соединения 70 в виде белого твердого вещества (0,512 г). LCMS показала MH+=291; TRET=2,75 мин.
Промежуточное соединение 71: 4-(аминометил)-N-циклопропилбензамида гидрохлорид
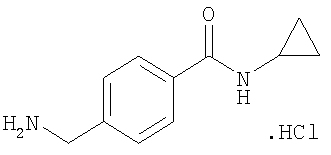
Промежуточное соединение 70 (0,506 г, 1,74 ммоль) растворяли в растворе хлористого водорода в диоксане (20 мл, 4 М) в атмосфере азота. Через 1 ч к этой смеси добавляли метанол (3 мл) и перемешивание продолжали при комнатной температуре в течение ночи. Растворители удаляли в вакууме с получением Промежуточного соединения 71 в виде белого твердого вещества (0,416 г). LCMS показала МН+=191; TRET=0,82 мин.
Промежуточное соединение 72
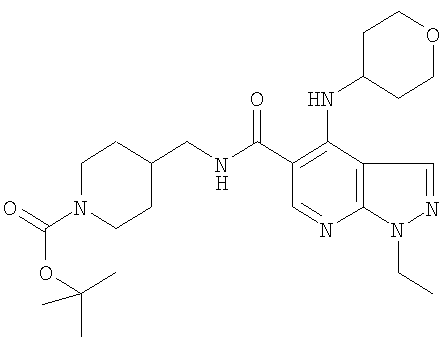
Промежуточное соединение 33 (1,36 г, 4,7 ммоль), EDC (1,26 г, 6,57 ммоль) и НОВТ (0,76 г, 5,62 ммоль) суспендировали в DMF (50 мл) и энергично перемешивали при комнатной температуре в течение 0,5 ч, после чего добавляли 1,1-диметилэтил-4-(аминометил)-1-пиперидинкарбоксилат (1,3 г, 6,07 ммоль, имеется в продаже у Maybridge Chemical Co., Ltd.). После перемешивания при комнатной температуре в течение ночи к реакционной смеси добавляли дополнительное количество 1,1-диметилэтил-4-(аминометил)-1-пиперидинкарбоксилата (1,01 г, 4,7 ммоль), после чего ее нагревали при 50°С. Через 6 ч добавляли диизопропилэтиламин (0,25 мл, 1,44 ммоль), и смесь поддерживали при 50°С в течение следующих 6 ч. Растворители удаляли в вакууме и остаток распределяли между DCM (100 мл) и водой (100 мл). Фазы разделяли путем пропускания через гидрофобную фритту и органическую фазу выпаривали в вакууме с получением неочищенного продукта. В результате дальнейшей очистки с использованием SPE картриджей (аминопропил, затем силикагель) получали Промежуточное соединение 72 в виде кремового твердого вещества (1,24 г). LCMS показала МН+=487; TRET=2,97 мин.
Промежуточное соединение 73
Промежуточное соединение 73 использовали in situ в общей методике для Примеров 360-414.
Промежуточное соединение 74: 1,1-Диметилэтил-({3-[(ацетиламино)метил]-фенил}метил)карбамат
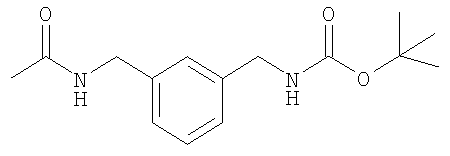
Уксусный ангидрид (0,52 мл, 5,5 ммоль) добавляли к смеси трет-бутил-N-[3-(аминометил)бензил]карбамата (1,1 г, 4,65 ммоль, имеется в продаже у AstaTech) и триэтиламина (0,7 мл, 5 ммоль) в THF (20 мл). Реакционную смесь перемешивали при 20°С в течение 16 ч, затем концентрировали в вакууме. Остаток распределяли между EtOAc и водой. Органическую фазу сушили (MgSO4) и выпаривали в вакууме. Остаток хроматографировали на силикагеле, элюируя смесью гексаны:EtOAc (1:1), затем EtOAc, с получением Промежуточного соединения 74 (1,2 г) в виде бесцветного масла. Аналитически обнаружено: С, 64,79; Н, 7,93; N, 10,10. Для C15H22N2O3 требуется С, 64,73; Н, 7,97; N, 10,06. MS (M+Na)+ 301.
Промежуточное соединение 75: N-{{3-(Аминометил)фенил]метил}-ацетамида гидрохлорид
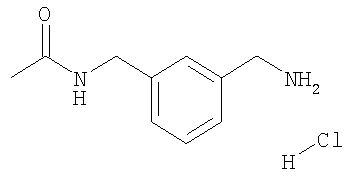
Хлористый водород в диоксане (4 мл, 4 М) добавляли к раствору Промежуточного соединения 74 (1,0 г, 3,6 ммоль) в диоксане (10 мл), и полученную в результате смесь перемешивали в течение 6 часов при 20°С. Эту реакционную смесь разбавляли Et2O (20 мл) и фильтровали с получением Промежуточного соединения 75 (0,7 г) в виде белого твердого вещества. MS MH+=179. 1Н ЯМР (300 МГц в d6-DMSO, 27°C, δ млн-1) 8.6-8.4 (br m, 3H), 7.38-7.26 (m, 3H), 7.22 (bm, 1H), 4.24 (d, J=5,7 Гц, 2H), 3.95 (dd, J=11,6, 5,7 Гц, 2Н), 1.87 (s, 3H).
Промежуточное соединение 76: 1-Этил-4-{[(1SR,3RS)-3-гидроксициклогексил]амино}-1Н-пиразоло[3,4-b]пиридин-5-карбоновая кислота
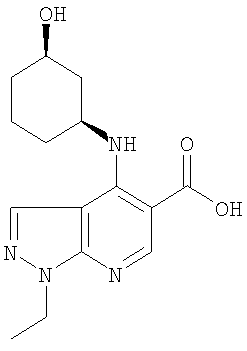
(цис-3-гидроксициклогекс-1-иламиногруппа, рацемическая)
Раствор Примера 665 (0,681 г, 2,05 ммоль) в этаноле (7 мл) обрабатывали раствором гидроксида натрия (0,362 г, 9,05 ммоль) в воде (2,9 мл). Полученную в результате смесь перемешивали при 50°С. Через 3 ч реакционную смесь концентрировали в вакууме с получением остаточного масла, которое растворяли в воде (3 мл), затем охлаждали и подкисляли до рН 3 при помощи 2 М соляной кислоты. После перемешивали при 0°С в течение 1 ч полученный в результате осадок собирали фильтрацией, промывали охлажденной водой (0,5 мл) и сушили в вакууме с получением Промежуточного соединения 76 в виде белого твердого вещества (0,491 г). LCMS показала MH+=305; ТRET=2,14 мин.
Пример 1: Этил-4-(циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
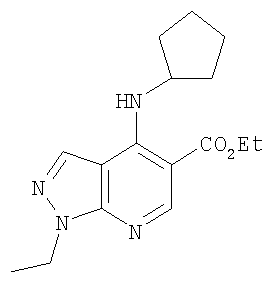
То есть Пример 1 представляет собой 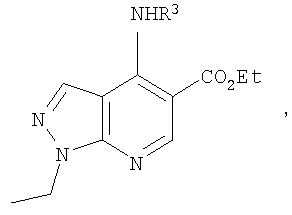 где NHR3=
где NHR3= 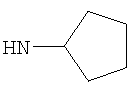
Промежуточное соединение 1 (0,051 г) и циклопентиламин (0,019 г) суспендировали в этаноле (2 мл) и добавляли триэтиламин (0,14 мл). Эту смесь перемешивали в атмосфере азота и нагревали при 80°С в течение 16 ч. После охлаждения до комнатной температуры этанол удаляли выпариванием в потоке азота, и остаток распределяли между дихлорметаном (DCM) и водой. Слои разделяли и органический слой наносили непосредственно на картридж для твердофазной экстракции (SPE) (силикагель, 5 г), который элюировали последовательно (1) DCM, (2) DCM: Et2O (2:1), (3) DCM: Et2O (1:1), (4) Et2O, (5) EtOAc, (6) МеОН. Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Примера 1 (0,074 г). LCMS показала MH+=303; TRET=3,45 мин.
Аналогично получали следующее:
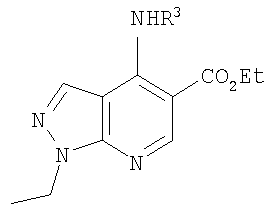
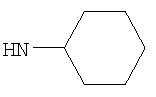
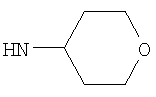
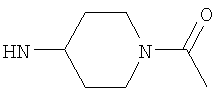
*Альтернативный синтез Примера 5, см. Пример 207 ниже.
Пример 3 (= Промежуточное соединение 32): Этил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
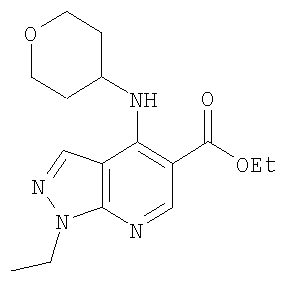
Вместо способа, показанного выше для Примеров 1-5 (называемого Способ А), соединение Примера 3 может быть получено также: либо используя небольшую вариацию Способа А, подробно описанную выше под заголовком “Промежуточное соединение 32”, либо используя приведенный ниже Способ Б.
Пример 3, Способ Б: Промежуточное соединение 1 (2,5 г) растворяли в ацетонитриле (15 мл). Добавляли гидрохлорид 4-аминотетрагидропирана (1,1 г) и N,N-диизопропилэтиламин (9,4 мл) и эту смесь перемешивали в атмосфере азота при 85°С в течение 16 ч. Осталось следовое количество исходного вещества, поэтому добавляли дополнительную порцию гидрохлорида 4-аминотетрагидропирана (0,11 г) и перемешивание продолжали при 85°С в течение еще 16 ч. Затем эту смесь концентрировали в вакууме. Остаток распределяли между DCM и водой. Слои разделяли и органический слой промывали дополнительным количеством воды (2×20 мл), затем сушили (Na2SO4) и концентрировали в вакууме. Остаток дополнительно очищали хроматографией, используя Biotage (силикагель, 90 г), элюируя смесью циклогексан:этилацетат, с получением Примера 3 (2,45 г). LCMS показала МН+=319;
ТRET=2,90 мин.
Пример 6: Этил-4-(циклопентиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
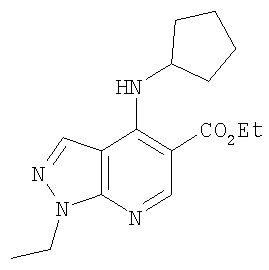
Промежуточное соединение 3 (0,045 г) помещали в Reactivial™ и обрабатывали циклопентиламином (0,07 мл). Смесь нагревали при 90°С в течение 2 ч, затем оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (2 мл) и водой (1 мл). Слои разделяли и органическую фазу выпаривали до коричневого твердого вещества, которое очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 6 в виде белого твердого вещества (0,008 г). LCMS показала MH+=289; TRET=3,22 мин.
Пример 7: Этил-1-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
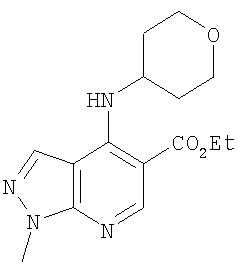
Промежуточное соединение 3 (0,035 г) помещали в Reactivial™ и обрабатывали 4-аминотетрагидропираном (0,06 мл). Смесь нагревали при 90°С в течение 2 ч, затем оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (2 мл) и водой (1 мл). Слои разделяли и органическую фазу концентрировали, затем наносили на препаративную пластину для ТСХ (силикагель, 20 см ×20 см ×1 мм), которую элюировали этилацетатом. Нужную полосу выделяли из пластины, и силикагель промывали этилацетатом (2×15 мл). В результате концентрирования этилацетатного раствора в вакууме получали Пример 7 в виде белого твердого вещества (0,008 г). LCMS показала МН+=305; TRET=2,67 мин. Пример 8: Этил-1-этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
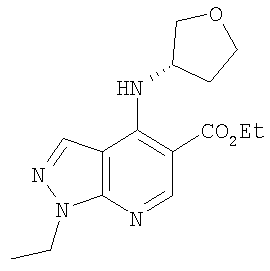
то есть: 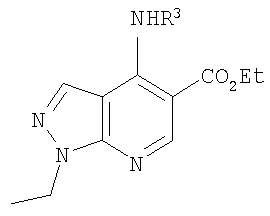 , где NHR3=
, где NHR3= 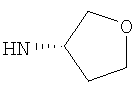
Промежуточное соединение 1 (0,05 г) и (S)-(-)-3-аминотетрагидрофурана 4-толуолсульфонат (0,052 г) суспендировали в этаноле (1 мл) и добавляли триэтиламин (0,14 мл). Эту смесь перемешивали в атмосфере азота и нагревали при 80°С в течение 24 ч. После охлаждения до комнатной температуры этанол удаляли выпариванием в потоке азота и остаток распределяли между DCM (2 мл) и водой (1,5 мл). Слои разделяли и органический слой концентрировали до сухости. Очистку проводили, используя SPE картридж (силикагель, 5 г), элюируя градиентом EtOAc: циклогексан (1:16, затем 1:8, 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Примера 8 (0,052 г). LCMS показала MH+=305; TRET=2,70 мин.
Аналогично получали следующее:

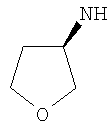
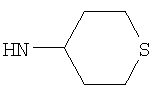
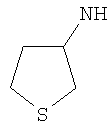
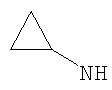
Пример 13: Этил-4-[(1,1-диоксидотетрагидротиен-3-ил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
 Пример 13 NHR3=
Пример 13 NHR3= 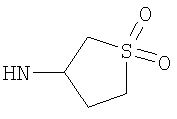
Промежуточное соединение 1 (0,05 г) и Промежуточное соединение 13 (0,027 г) суспендировали в этаноле (1 мл) и добавляли триэтиламин (0,14 мл). Смесь перемешивали в атмосфере азота и нагревали при 80°С в течение 24 ч. После охлаждения до комнатной температуры этанол удаляли выпариванием в потоке азота, и остаток распределяли между DCM (2 мл) и водой (1,5 мл). Слои разделяли и органический слой концентрировали до сухости. Очистку проводили, используя SPE картридж (силикагель, 5 г), элюируя градиентом EtOAc: циклогексан (1:8, затем 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме с получением Примера 13 (0,045 г) в виде смеси энантиомеров. LCMS показала МН+=353; RRET=2,60 мин.
Аналогично получали следующее:

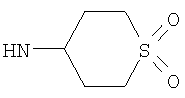
Пример 19 (справочный пример, в качестве промежуточного соединения): Этил-4-(циклопентиламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
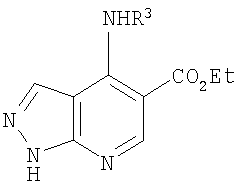 Пример 19 NHR3=
Пример 19 NHR3= 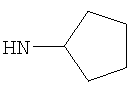
Промежуточное соединение 2 (0,035 г) помещали в Reactivial™ и обрабатывали циклопентиламином (0,05 мл). Смесь нагревали при 90°С в течение 1,5 ч, затем оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (2 мл) и водой (1 мл). Слои разделяли и органическую фазу концентрировали. Остаточное твердое вещество растирали с Et2O, и нерастворимое не совсем белое твердое вещество собирали и сушили на воздухе с получением Примера 19 (0,016 г). LCMS показала МН+=275; ТRET=2,58 мин.
Пример 20 (справочный пример, в качестве промежуточного соединения):
Этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
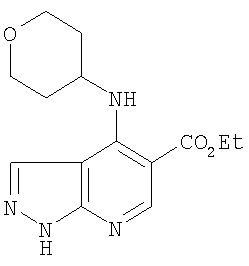
то есть:  Пример 20, NHR3=
Пример 20, NHR3= 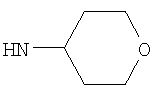
Промежуточное соединение 2 (0,035 г) помещали в Reactivial™ и обрабатывали 4-аминотетрагидропираном (0,05 мл). Смесь нагревали при 90°С в течение 1,5 ч, затем оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (2 мл) и водой (1 мл). Слои разделяли и органическую фазу концентрировали. Неочищенный продукт очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 20 в виде не совсем белого твердого вещества (0,011 г). LCMS показала МН+=291; TRET=2,08 мин.
Альтернативный способ синтеза Примера 20:
Промежуточное соединение 2 (2 г) суспендировали в 4-аминотетрагидропиране (2 г) и смесь нагревали при 90°С в течение 6 ч. Остаточную смесь оставляли охлаждаться до комнатной температуры и распределяли между хлороформом (50 мл) и водой (50 мл). Фазы разделяли и органическую фазу выпаривали до сухости. Остаток растирали с Et2O (30 мл) и нерастворимое твердое вещество собирали и сушили с получением Примера 20 в виде кремового твердого вещества (2,24 г). LCMS показала МН+=291;
ТRET=2,19 мин.
Пример 21: N-Бензил-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
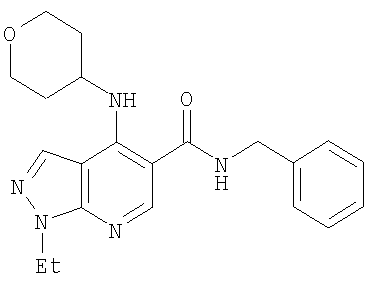
то есть Пример 21 представляет собой: 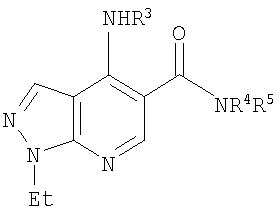 , где NR4R5=
, где NR4R5= 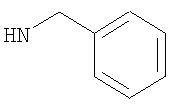 , NHR3=
, NHR3= 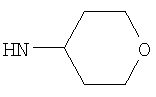
Три альтернативных способа, А, Б и В, использовали для получения Примера 21, как описано ниже.
Пример 21, Способ А:
Раствор 4-хлор-замещенного Промежуточного соединения 17 (0,031 г, 0,1 ммоль) в этаноле (1,9 мл) обрабатывали триэтиламином (0,07 мл, 0,5 ммоль), затем 0,1 М этанольным раствором 4-аминотетрагидропирана (Промежуточное соединение 8, 1,1 мл 0,1 М этанольного раствора =0,11 ммоль). Смесь нагревали с обратным холодильником (80°С) в течение 18 ч. Затем добавляли дополнительную порцию 4-аминотетрагидропирана (0,01 мл неразведенного амина, а не его раствора) и нагревание продолжали в течение еще 24 ч. Летучие вещества удаляли в вакууме и остаток растворяли в дихлорметане (DCM), затем наносили на картридж для твердофазной экстракции (SPE) (аминопропил, 1 г), который элюировали сначала DCM, затем метанолом. Фракции, содержащие нужное вещество, концентрировали в вакууме с получением Примера 21 (0,004 г). LCMS показала МН+=380; TRET=2,92 мин.
Пример 21, Способ Б:
Промежуточное соединение 17 (0,031 г, 0,1 ммоль) растворяли в ацетонитриле (1 мл).
Добавляли гидрохлорид 4-аминотетрагидропирана (Промежуточное соединение 8А, 0,015 г, 0,11 ммоль) и N,N-диизопропилэтиламин (0,08 мл, 0,5 ммоль) и эту смесь перемешивали в атмосфере азота при 85°С в течение 16 ч, затем концентрировали в вакууме. Остаток распределяли между дихлорметаном (DCM) и водой. Слои разделяли и органический слой концентрировали в вакууме с получением Примера 21 (0,027 г). LCMS показала MH+=380; TRET=2,92 мин.
Пример 21, Способ В:
Этот альтернативный путь В для примера 21 включает образование сложного эфира Примера 3 = Промежуточного соединения 32 ( ) с использованием одного из способов, описанных выше, превращение сложного эфира Примера 3/Промежуточного соединения 32 в карбоновую кислоту (Промежуточное соединение 33), используя способ, приведенный выше для Промежуточного соединения 33, и затем образование амидной связи с получением Примера 21, используя способ приведенных ниже Примеров 81-84.
) с использованием одного из способов, описанных выше, превращение сложного эфира Примера 3/Промежуточного соединения 32 в карбоновую кислоту (Промежуточное соединение 33), используя способ, приведенный выше для Промежуточного соединения 33, и затем образование амидной связи с получением Примера 21, используя способ приведенных ниже Примеров 81-84.
Следующие соединения могут быть получены аналогично, используя один или более чем один из приведенных выше способов А, Б или В, предпочтительно Способ А или Б:

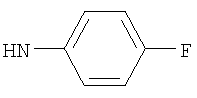
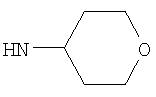
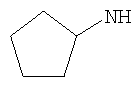
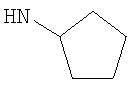

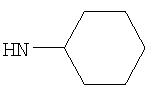



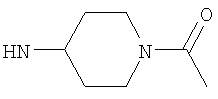
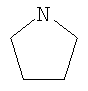





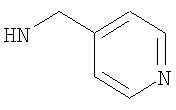








Пример 39: N-Бензил-4-(циклопентиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
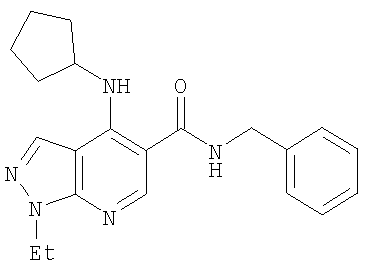
то есть Пример 39 представляет собой:  , где NR4R5=
, где NR4R5= 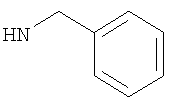 , NHR3=
, NHR3= 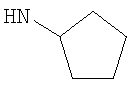
Раствор Промежуточного соединения 17 (0,031 г, 0,1 ммоль) в этаноле (1 мл) обрабатывали триэтиламином (0,07 мл, 0,5 ммоль), затем 0,1 М этанольным раствором циклопентиламина (1,1 мл 0,1 М этанольного раствора =0,11 ммоль). Смесь нагревали с обратным холодильником (80°С) в течение 18 ч. Затем добавляли дополнительную порцию циклопентиламина (0,009 мл неразведенного амина, а не его раствора), и нагревание продолжали в течение еще 24 ч. Летучие вещества удаляли в вакууме и остаток растворяли в DCM, затем наносили на SPE картридж (аминопропил, 1 г), который элюировали сначала DCM, затем метанолом. Фракцию DCM концентрировали в вакууме, затем наносили на SPE картридж (силикагель, 0,5 г), который элюировали последовательно (1) DCM, (2) Et2O, (3) EtOAc и (4) МеОН. Фракции, содержащие нужное вещество, объединяли с получением Примера 39 (0,007 г). LCMS показала MH+=364; TRET=3,38 мин.
Аналогично получали следующее:


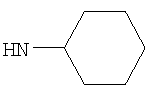

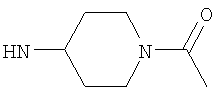
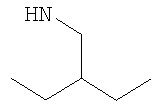
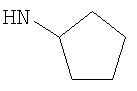



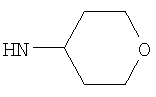

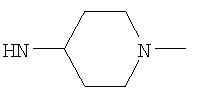


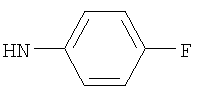















Пример 57: 4-[(1-Ацетилпиперидин-4-ил)амино]-1-этил-N-(пиридин-4-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
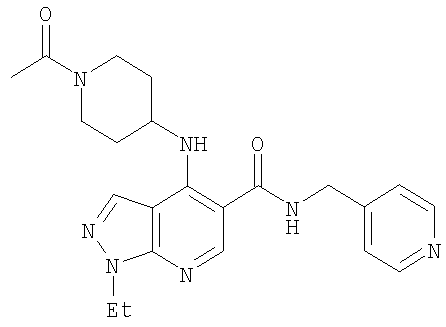
то есть Пример 57 представляет собой:  , где NR4R5=
, где NR4R5= 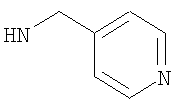 , NHR3=
, NHR3= 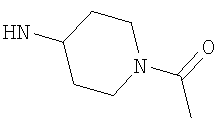
Раствор Промежуточного соединения 22 (0,03 г, приблизительно 0,1 ммоль) в этаноле (1 мл) обрабатывали триэтиламином (0,07 мл, 0,5 ммоль), затем 0,1 М этанольным раствором Промежуточного соединения 6 (1,1 мл раствора =0,11 ммоль). Смесь нагревали с обратным холодильником (80°С) в течение 18 ч. Затем добавляли дополнительную порцию Промежуточного соединения 6 (0,01 мл, неразведенный) и нагревание продолжали в течение еще 24 ч. Летучие вещества удаляли в вакууме и остаток растворяли в DCM, затем наносили на SPE картридж (аминопропил, 1 г), который элюировали сначала DCM, затем метанолом.
DCM фракцию концентрировали в вакууме, затем наносили на SPE картридж (силикагель, 0,5 г), элюируя последовательно (1) DCM, (2) EtOAc и (3) постепенно градиентом хлороформ: метанол (от 99:1 до 4:1). Фракции, содержащие нужное вещество, объединяли с получением Примера 57 (0,003 г). LCMS показала MH+=422;
TRET=2,1 мин.
Пример 61: N-Бензил-4-(циклопентиламино)-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
 Пример 61, NR4R5=
Пример 61, NR4R5= 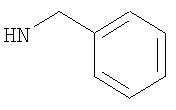 , NHR3=
, NHR3= 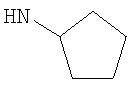
Раствор Промежуточного соединения 28 (0,03 г, 0,1 ммоль) в этаноле (1 мл) обрабатывали 0,1 М этанольным раствором циклопентиламина (1,1 мл раствора=0,11 ммоль). Затем добавляли триэтиламин (0,07 мл, 0,5 ммоль) и эту смесь нагревали с обратным холодильником (85°С) в атмосфере азота в течение 12 ч. Затем добавляли дополнительную порцию циклопентиламина (0,009 мл, неразведенный) и нагревание продолжали в течение еще 36 ч. Смеси концентрировали в вакууме и остаток обрабатывали хлороформом. Небольшое количество нерастворимого вещества собирали фильтрацией, затем фильтрат наносили на SPE картридж (аминопропил, 1 г), который элюировали сначала DCM, затем метанолом. Фракции, содержащие нужное вещество, объединяли с получением Примера 61 (0,039 г). LCMS показала МН+=350;
TRET=2,88 мин.
Аналогично получали следующее:
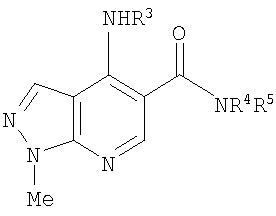

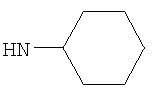

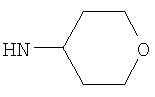
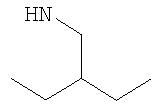
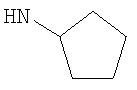




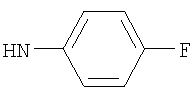







Пример 74: 4-[(1-Ацетилпиперидин-4-ил)амино]-N-бензил-1-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
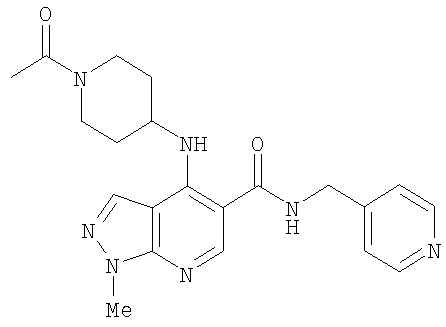
то есть Пример 74 представляет собой:  , где NR4R5=
, где NR4R5=  , NHR3=
, NHR3= 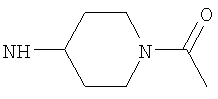
Раствор Промежуточного соединения 28 (0,03 г, 0,1 ммоль) в этаноле (1 мл) обрабатывали 0,1 М этанольным раствором Промежуточного соединения 6 (1,1 мл раствора =0,11 ммоль). Затем добавляли триэтиламин (0,07 мл, 0,5 ммоль) и эту смесь нагревали с обратным холодильником (85°С) в атмосфере азота в течение 12 ч. Затем добавляли дополнительную порцию Промежуточного соединения 6 (0,1 ммоль) и нагревание продолжали в течение еще 36 ч. Смеси концентрировали в вакууме, и остаток обрабатывали хлороформом. Небольшое количество нерастворимого вещества собирали фильтрацией, затем фильтрат наносили на SPE картридж (аминопропил, 1 г), который элюировали сначала DCM, затем метанолом. Фракции, содержащие нужное вещество, объединяли и концентрировали в вакууме. Остаток дополнительно очищали посредством SPE (силикагель, 0,5 г), элюируя (1) DCM, (2) хлороформом, (3) EtOAc и (4) постепенным градиентом хлороформ:метанол (от 99:1 до 4:1). Фракции, содержащие нужное вещество, объединяли с получением Примера 74 (0,029 г). LCMS показала МН+=407; TRET=2,57 мин.
Пример 81: 1-Этил-N-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
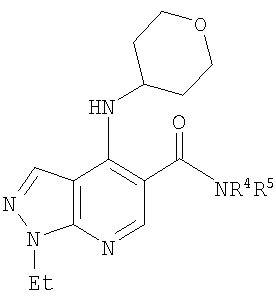 Пример 81, NR4R5=NHMe
Пример 81, NR4R5=NHMe
К перемешиваемой суспензии Промежуточного соединения 33 (0,025 г, приблизительно от 0,08 до 0,09 ммоль) в хлороформе (2 мл) добавляли тионилхлорид (0,025 мл) и смесь перемешивали при комнатной температуре в течение 1 ч. Эту смесь охлаждали до 0°С и добавляли метиламин (2 М раствор в THF, 0,69 мл=1,38 ммоль). После возвращения к комнатной температуре смесь перемешивали в течение еще 1 ч, затем гасили добавлением воды (4 мл) и слои разделяли. Органический слой концентрировали, затем наносили на SPE картридж (силикагель, 1 г), который элюировали (1) DCM, (2) Et2O (2:1), (3) EtOAc, (4) МеОН: EtOAc (1:9). Фракции, содержащие нужное вещество, объединяли с получением Примера 81 (0,019 г). LCMS показала МН+=304; TRET=2,19 мин.
Аналогично получали:

Пример 83: N,1-Диэтил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид; также называемый 1-этил-N-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид
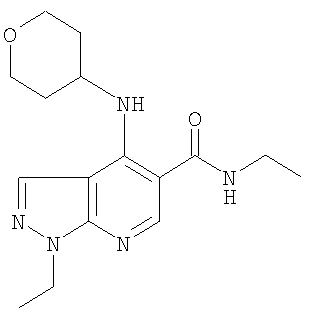
В воплощении, альтернативном способу, описанному для приведенных выше Примеров 81-84, Пример 83 может быть получен следующим способом.
Смесь Промежуточного соединения 33 (3,0 г, 10,33 ммоль), EDC (2,25 г, 11,7 ммоль) и НОВТ (1,68 г, 12,4 ммоль) перемешивали при комнатной температуре в течение 1 часа. Добавляли этиламин (6,2 мл, 12,4 ммоль, 2 М раствор в THF) и перемешивание продолжали при комнатной температуре в течение 22 часов. Растворители удаляли в вакууме и остаточное твердое вещество растворяли в хлороформе (250 мл) и промывали последовательно водой (70 мл) и 5%-ным раствором гидрокарбоната натрия (70 мл). После высушивания над безводным сульфатом натрия органический раствор упаривали в вакууме с получением бледно-оранжевого твердого вещества (4,15 г). Это твердое вещество растворяли в смеси дихлорметана (15 мл) и хлороформа (5 мл) и очищали колоночной хроматографией (Biotage, силикагель, 100 г), элюируя в начале смесью EtOAc:циклогексан (2:1) и в конце чистым EtOAc. Фракции, содержащие продукт, объединяли и выпаривали с получением Примера 83 в виде бледно-желтого твердого вещества (3,05 г). LCMS показала MH+=318; TRET=2,33 мин. 1H ЯМР (400 МГц в d6-ДМСО, 27°С, δ млн-1) 9.76 (d, 1Н), 8.35 (s, 1Н), 7.94 (s, 1H), 5.99 (br m, 1H), 4.47 (q, 2H), 4.16-4.01 (m's, 3Н), 3.62 (m, 2H), 3.48 (m, 2H), 2.13 (m, 2H), 1.77 (m, 2H), 1.49 (t, 3Н), 1.28 (t, 3H).
Пример 85: N-Бензил-1-этил-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
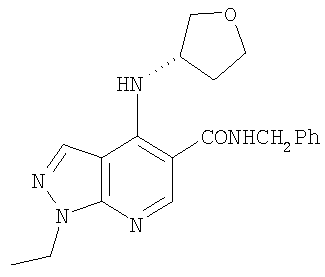
То есть Пример 85 представляет собой: 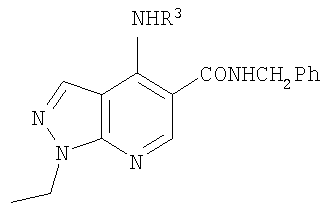 , где NHR3=
, где NHR3= 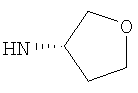
Промежуточное соединение 41 (0,017 г, 0,062 ммоль) растворяли в DMF (2 мл), затем обрабатывали HATU (0,023 г), затем диизопропилэтиламином (0,021 мл) и смесь перемешивали в течение 10 мин. Затем добавляли бензиламин (0,007 мл) и перемешивание продолжали в течение еще 64 ч. Эту смесь концентрировали в вакууме, и остаток растворяли в DCM (1,5 мл), затем обрабатывали насыщенным водным раствором бикарбоната натрия (1,5 мл). Эту смесь перемешивали в течение 30 мин, затем слои разделяли и органический слой наносили на SPE картридж (силикагель, 1 г), который последовательно элюировали градиентом этилацетат:циклогексан (1:4, затем 1:2, 1:1, 2:1 и 1:0). Фракции, содержащие нужное вещество, концентрировали в вакууме с получением Примера 85 (0,017 г). LCMS показала МН+=366; TRET=2,80 мин.
Аналогично получали следующее:

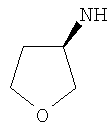
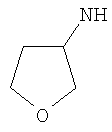
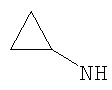
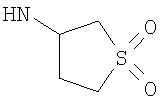
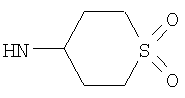
Пример 91: N-Бензил-1-этил-4-(тетрагидро-2Н-тиопиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
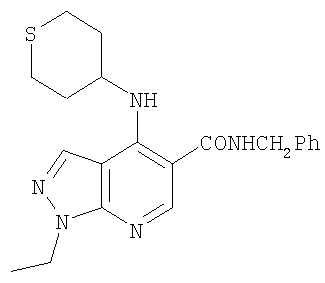
Промежуточное соединение 43 (0,019 г) растворяли в DMF (2 мл), затем обрабатывали HATU (0,024 г), затем диизопропилэтиламином (0,022 мл) и смесь перемешивали в течение 10 мин. Затем добавляли бензиламин (0,007 мл) и перемешивание продолжали в течение еще 64 ч. Смесь концентрировали в вакууме и остаток растворяли в DCM (1,5 мл), затем обрабатывали насыщенным водным раствором бикарбоната натрия (1,5 мл). Эту смесь перемешивали в течение 30 мин, затем слои разделяли и органический слой наносили на SPE картридж (силикагель, 1 г), который элюировали последовательно градиентом этилацетат:циклогексан (1:4, затем 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, концентрировали в вакууме с получением Примера 91 (0,023 г). LCMS показала МН+=396; TRET=3,26 мин.
Пример 92: 1-Этил-N-(4-фторфенил)-4-[(3S)-тетрагидрофуран-3-иламино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
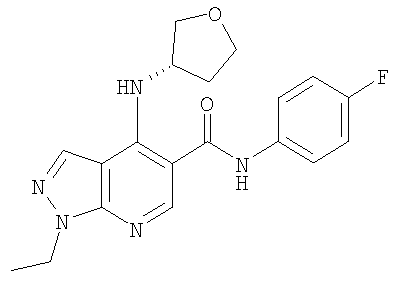
то есть Пример 92 представляет собой: 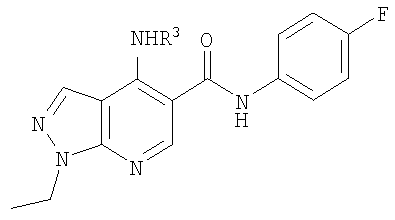 , где NHR3=
, где NHR3= 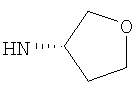
Промежуточное соединение 41 (0,017 г) растворяли в DMF (2 мл), затем обрабатывали HATU (0,023 г), затем диизопропилэтиламином (0,021 мл), и смесь перемешивали в течение 10 мин. Затем добавляли 4-фторанилин (0,006 мл), и перемешивание продолжали в течение еще 64 ч. Эту смесь концентрировали в вакууме, и остаток растворяли в DCM (1,5 мл), затем обрабатывали насыщенным водным раствором бикарбоната натрия (1,5 мл). Эту смесь перемешивали в течение 30 мин, затем слои разделяли и органический слой концентрировали в вакууме. Неочищенную смесь очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 92 (0,013 г). LCMS показала МН+=370; TRET=2,91 мин.
Аналогично получали следующее:


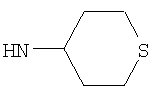




Пример 99
Во всех Примерах 22-98, когда 4-амино-5-карбоксамидный Пример приведенной ниже Формулы I синтезируют из 4-хлор-производного, тогда альтернативной конечной стадией синтеза является следующая:
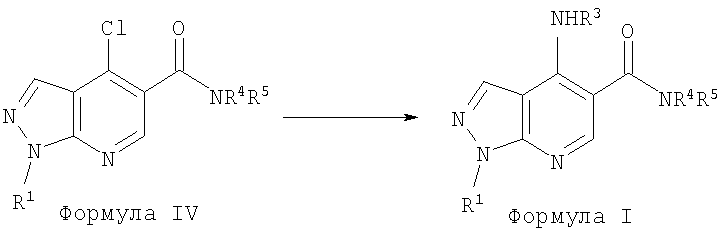
Промежуточное соединение приведенной выше Формулы IV (0,1 ммоль) растворяли в ацетонитриле (1 мл). Добавляли амин формулы R3NH2 (0,11 ммоль, 1,1 моль-эквивалента) и N,N-диизопропилэтиламин (0,5 ммоль, 5 моль-эквивалентов) и смесь перемешивали в атмосфере азота при 85°С в течение 16 ч. После концентрирования в вакууме остаток распределяли между дихлорметаном (DCM) и водой. Слои разделяли и органический слой концентрировали в вакууме с получением Примера формулы I.
Пример 100
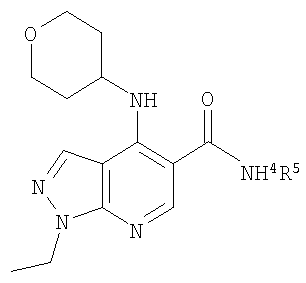
Пример 100 NR4R5= 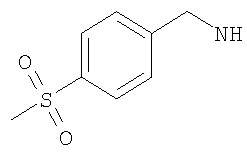
Промежуточное соединение 33 (0,048 ммоль) растворяли в DMF (0,5 мл), затем обрабатывали HATU (0,048 ммоль), затем диизопропилэтиламином (0,096 ммоль) и смесь перемешивали в течение 10 мин. Затем добавляли 4-метилсульфонилбензиламин (0,052 ммоль, продается у Acros Organics) и перемешивание продолжали в течение еще 16 часов. Эту смесь концентрировали в вакууме. Неочищенную смесь очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 100 (0,013 г). LCMS показала МН+=458; TRET=2,22 мин.
Приведенные ниже соединения (Примеры 102-182) были получены аналогично, но с заменой 4-метилсульфонилбензиламина таким же или близким числом молей другого амина R4R5NH:

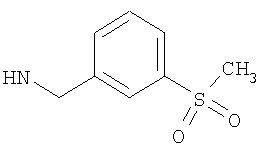
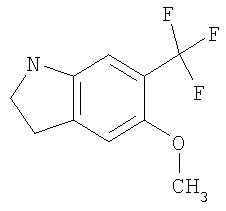
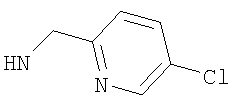
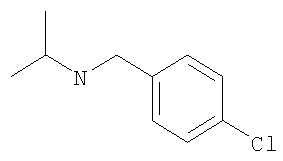
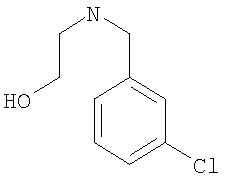
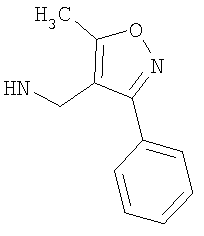
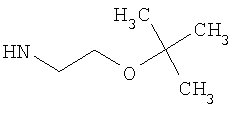
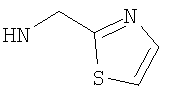
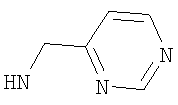
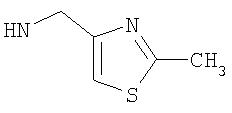
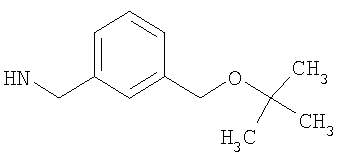
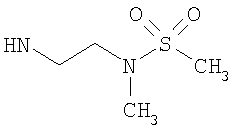
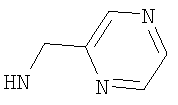
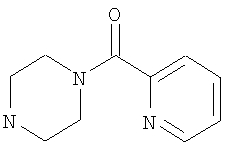
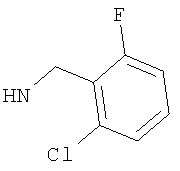
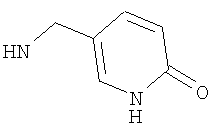
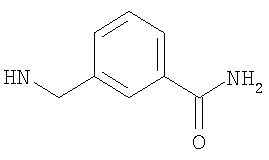
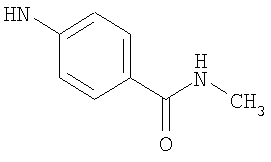
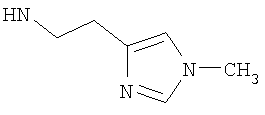
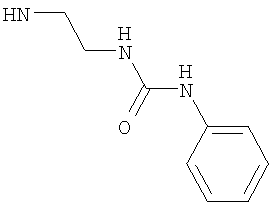
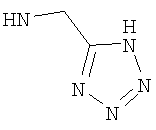
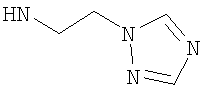
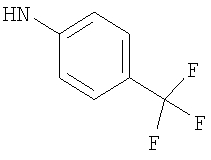
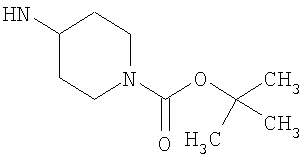
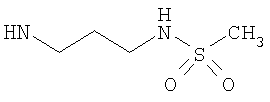
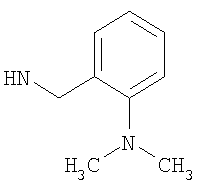
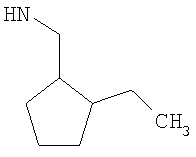
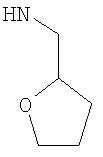
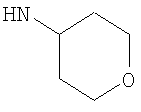
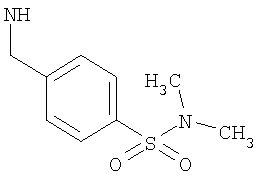
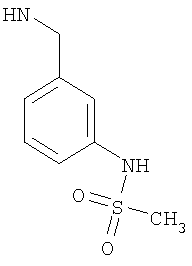
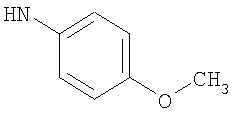
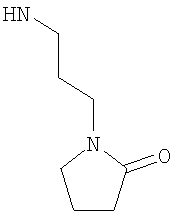
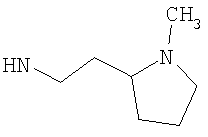
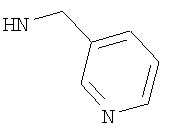
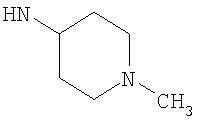
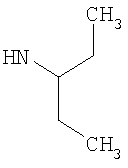
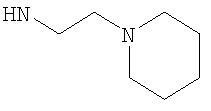
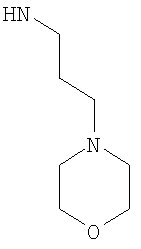

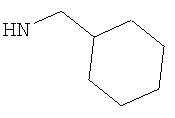
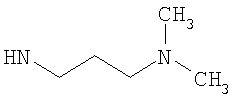
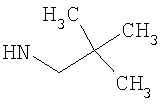
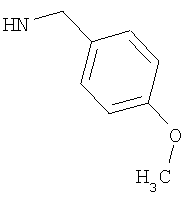
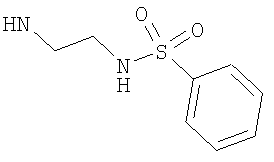
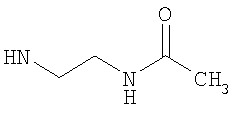
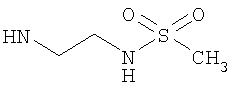
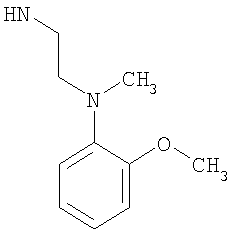
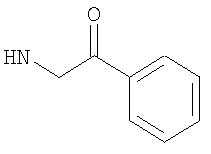
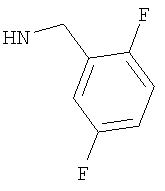
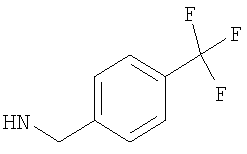
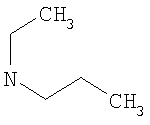
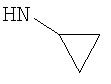
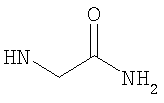
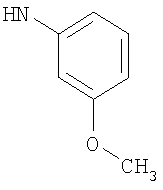
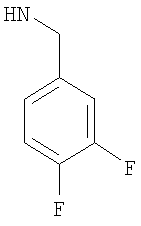
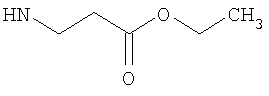
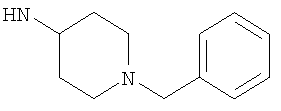
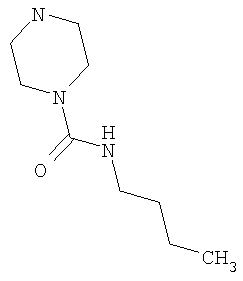
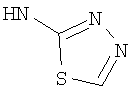
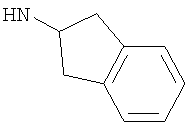
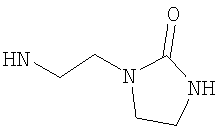
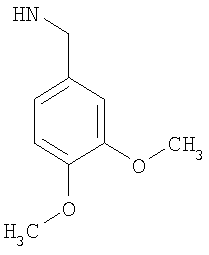
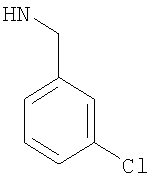
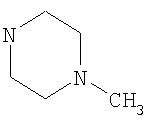

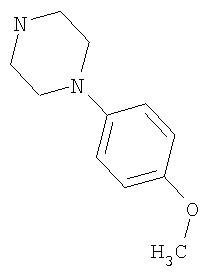
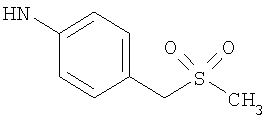
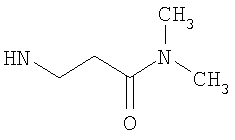
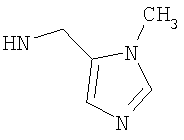
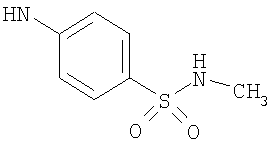
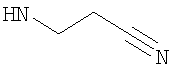
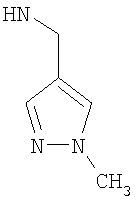
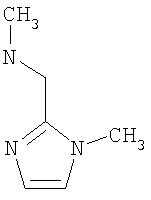
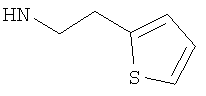
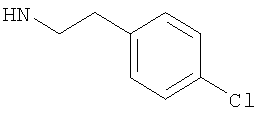
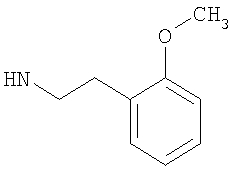
Пример 109: 1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-N-(1,3-триазол-2-илметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
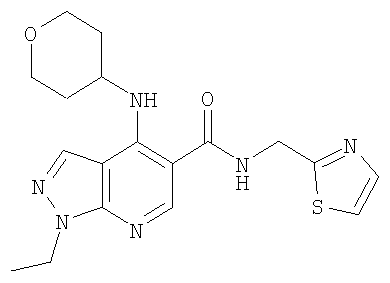
Альтернативный способ получения Примера 109 приведен ниже.
1-Гидроксибензотриазол (0,215 г, 1,59 ммоль) и гидрохлорид 1-[3-(диметиламино)пропил]-3-этил-карбодиимида (0,357 г, 1,86 ммоль) добавляли к суспензии Промежуточного соединения 33 (0,384 г, 1,32 ммоль) в DMF (10 мл). После перемешивания при комнатной температуре в течение 30 минут добавляли (1,3-тиазол-2-илметил)амин (0,182 г, 1,59 ммоль) (имеется в продаже у MicroChemistry Building Blocks (Russia) или Matrix Scientific (USA) либо может быть получен, как описано в Synthesis, 1998, 641 или Tetrahedron 1995, 51, 12731). Эту реакционную смесь перемешивали в течение 18 часов, а затем распределяли между эфиром и водой. Органическую фазу промывали рассолом, сушили (MgSO4) и выпаривали в вакууме. Остаток очищали хроматографией (Biotage, силикагель 90 г), элюируя смесью циклогексан:EtOAc, а затем EtOAc. Вещество растирали с циклогексаном и фильтровали с получением Примера 109 (0,244 г) в виде бледно-желтого твердого вещества. LCMS показала MH+=387; TRET=2,49 мин. 1Н ЯМР (400 МГц в CDCl3, δ млн-1) 9.74 (d, 1Н), 8.50 (s, 1H), 7.94 (s, 1H), 7.74 (d, 1H), 7.33 (d, 1H), 7.17 (m, 1H), 4.94 (d, 2H), 4.45 (q, 2H), 4.15-4.00 (m, 3Н), 3.63 (m, 2H), 2.15 (m, 2H), 1.85-1.73 (m, 3H), 1.48(t, 3H).
Пример 167: N-{[3,4-Бис(метилокси)фенил]метил}-1-этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
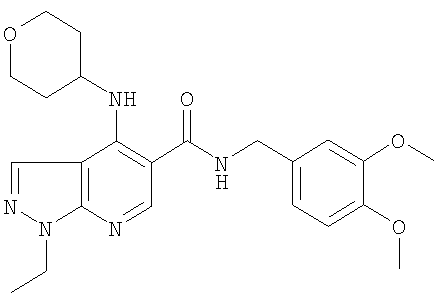
В альтернативном воплощении способа, описанного выше для Примеров 100-182, Пример 167 может быть получен в соответствии со следующим способом.
Смесь Промежуточного соединения 33 (0,498 г, 1,72 ммоль), EDC (0,46 г, 2,41 ммоль) и НОВТ (0,278 г, 1,68 ммоль) перемешивали при комнатной температуре в течение 0,25 часов. Добавляли вератриламин (3,4-диметоксибензиламин, 0,31 мл, 2,05 ммоль, можно получить у Aldrich или согласно Synlett, 1999, 4, 409) и перемешивание продолжали при комнатной температуре в течение 22 часов. Реакционную смесь распределяли между Et2O и водой. Водную фазу экстрагировали Et2O и объединенные органические фазы промывали рассолом, сушили (MgSO4) и выпаривали в вакууме. Остаток очищали хроматографией (Biotage, силикагель 40 г), элюируя EtOAc: циклогексаном (2:1). Вещество дополнительно очищали с помощью SPE (SCX-2, 10 г), элюируя метанолом, затем аммиаком в метаноле (0,5 М). Метанольные фракции аммиака объединяли и выпаривали в вакууме с получением Примера 167 в виде белой пены (0,633 г). LCMS показала МН+=440; TRET=2,65 мин. 1H ЯМР (400 МГц в CDCl3, 27°С, δ млн-1) 9.78 (d, 1H), 8.37 (s, 1H), 7.94 (s, 1H), 6.94-6.82 (m, 3Н), 6.29 (br m, 1H), 4.56 (d, 2H), 4.46 (q, 2H), 4.15-4.01. (m's, 3Н), 3.89 (s, 6H), 3.63 (m, 2H), 2.15 (m, 2H), 1.78 (m, 2H), 1.49 (t, 3Н).
Пример 178: 1-Этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
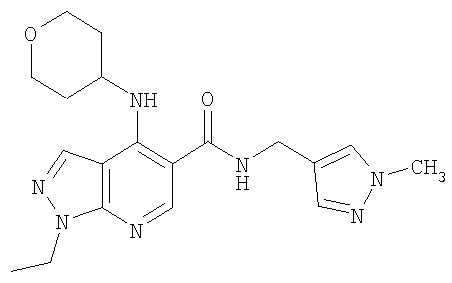
Данные 1H ЯМР для Примера 178 (полученного способом, описанным в Примерах 100-182 выше) приведены ниже:
1H ЯМР (400 МГц в CDCl3, δ млн-1) 9.90 (m, 1H), 8.37 (s, 1H), 7.94 (s, 1H), 7.49 (s, 1H), 7.40 (s, 1H), 6.39 (m, 1H), 4.50-4.42 (m, 4H), 4.15-4.00 (m, 3Н), 3.89 (s, ЗН), 3.63 (m, 2H), 2.52 (m, 2H), 2.20-2.10 (m, 2H), 1.85-1.73 (m, 3Н), 1.48 (t, 3Н).
Пример 183: Этил-4-(циклогексиламино)-1-(3-этокси-3-оксопропил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
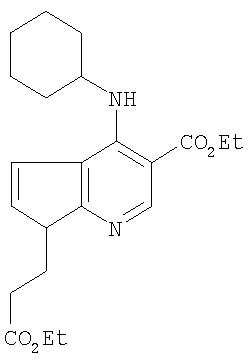
Энергично перемешиваемую смесь Промежуточного соединения 48 (40 мг), безводного карбоната калия (57 мг) и этил-3-бромпропаноата (0,027 мл) в безводном DMF (1 мл) нагревали при 65°С в течение ночи. Реакционную смесь концентрировали и остаток распределяли между дихлорметаном (5 мл) и водой (5 мл). Фазы разделяли и органическую фазу выпаривали до остаточного масла, которое очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 183 (5 мг). LCMS показала МН+=389; TREt=3,65 мин.
Пример 185: Этил-1-н-пропил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
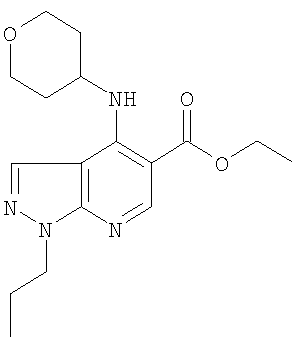
Гидрид натрия (0,067 г, 60%-ная дисперсия в масле) добавляли к перемешиваемому раствору Примера 20 (0,47 г) в DMF (19 мл) с последующим добавлением н-пропилиодида (0,17 мл). Эту смесь перемешивали при 23°С в течение 16 часов, затем концентрировали, разбавляли хлороформом (30 мл) и промывали раствором 1:1 вода: рассол (30 мл), разделяли и органический слой концентрировали. Остаток очищали на SPE картридже (силикагель, 10 г), элюируя 10 мл объемами дихлорметана, смеси 1:1 диэтиловый эфир:циклогексан и диэтилового эфира. Объединенные фракции смеси 1:1 диэтиловый эфир:циклогексан и диэтилового эфира концентрировали с получением Примера 185 в виде прозрачной смолы (0,23 г). LCMS показала МН+=333; TRET=3,14 мин.
Пример 186: Этил-1-(2-гидроксиэтил)-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
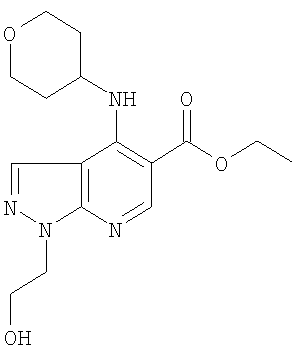
2-Бромэтанол (0,008 мл) добавляли к раствору Примера 20 (0,03 г) в безводном DMF (1,5 мл) с 2-трет-бутиламино-2-диэтиламино-1,3-диметил-пергидро-1,3,2-диазафосфорином (связанным с полимером, нагрузка 2,3 ммоль/г, 0,045 г). Эту смесь встряхивали при 23°С в течение 16 часов, затем раствор выкачивали из смолы и смолу промывали DMF. Объединенные органические вещества концентрировали и остаток очищали на SPE картридже (силикагель, 1 г), элюируя 70-100%-ным этилацетатом в циклогексане. Объединенные фракции концентрировали с получением Примера 186 в виде белого твердого вещества (0,011 г). LCMS показала МН+=335; ТRET=2,47 мин.
Пример 187: N-[4-(Метилсульфонил)бензил]-1-н-пропил-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
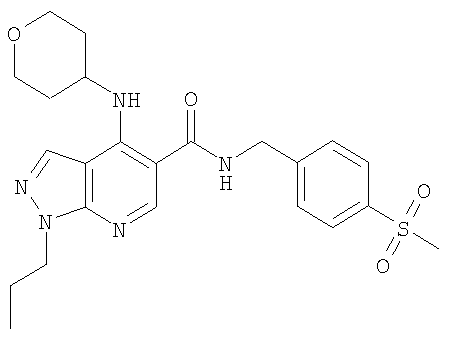
Промежуточное соединение 50 (0,03 г) перемешивали в DMF (1 мл) с DIPEA (0,035 мл) и HATU (0,038 г) в течение 20 мин. К этой смеси добавляли гидрохлорид 4-(метилсульфонил)бензиламина (0,024 г) и этот раствор перемешивали в течение 8 часов при 23°С. Раствор концентрировали и остаток растворяли в дихлорметане (6 мл), затем промывали насыщенным раствором бикарбоната натрия (6 мл) и смесью 1:1 рассол:вода (6 мл), разделяли при помощи гидрофобной фритты. Органический слой концентрировали с получением Примера 187 в виде белого твердого вещества (0,039 г). LCMS показала MH+=472; TRET=2,67 мин.
Пример 188: N-(4-Фторфенил)-1-н-пропил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
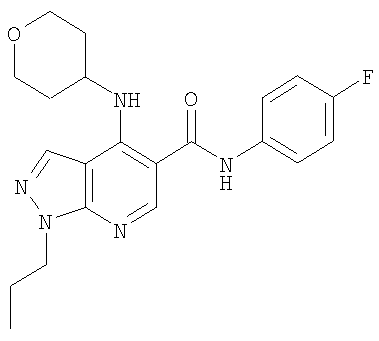
Способ синтеза является таким, как описан в Примере 187, за исключением того, что вместо гидрохлорида 4-(метилсульфонил)бензиламина к смеси добавляли 4-фторанилин (0,01 мл). Для полученного в результате продукта требовалась дополнительная очистка, которую проводили посредством регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 188 в виде прозрачной смолы (0,03 г). LCMS показала MH+=398; TRET=3,13 мин.
Пример 189: Этил-1-этил-6-метил-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
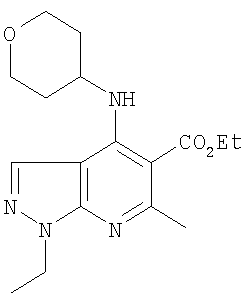
Гидрохлорид 4-аминотетрагидропирана (Промежуточное соединение 8А, 0,413 г, 3,0 ммоль) добавляли к смеси Промежуточного соединения 51 (0,268 г, 1,0 ммоль) и N,N-диизопропилэтиламина (0,87 мл, 5,0 ммоль) в ацетонитриле (3 мл). Полученную в результате смесь нагревали при 85°С в течение 24 часов. Летучие вещества удаляли в вакууме и остаток растворяли в хлороформе (1,5 мл) и наносили на SPE картридж (силикагель, 5 г). Картридж элюировали последовательно Et2O, EtOAc и EtOAc-МеОН (9/1). Фракции, содержащие нужный продукт, объединяли и концентрировали в вакууме с получением нужного продукта, загрязненного исходным веществом (Промежуточное соединение 51). В результате дополнительной очистки с использованием SPE картриджа (силикагель, 5 г), элюируя этилацетатом - циклогексаном (1/3), получали Пример 189 (0,248 г). LCMS показала МН+=333; TRET=2,75 мин.
Пример 190: Этил-4-(циклогексиламино)-1-этил-6-метил-1H-пиразоло[3,4-b]пиридин-5-карбоксилат
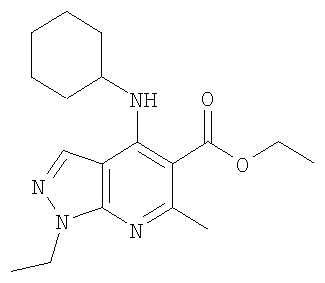
Циклогексиламин (0,149 г, 1,5 ммоль) добавляли к смеси Промежуточного соединения 51 (0,201 г, 0,75 ммоль) и N,N-диизопропилэтиламина (0,65 мл, 3,73 ммоль) в ацетонитриле (3 мл). Полученную в результате смесь нагревали при 85°С в течение 40 часов. Летучие вещества удаляли в вакууме и остаток растворяли в хлороформе (1,5 мл) и наносили на SPE картридж (силикагель, 5 г). Картридж элюировали последовательно Et2O, EtOAc и МеОН. Фракции, содержащие нужный продукт, объединяли и концентрировали в вакууме с получением Примера 190 (0,128 г). LCMS показала MH+=331; TRET=3,64 мин.
Пример 191: 4-(Циклогексиламино)-1-этил-6-метил-N-[4-(метилсульфонил)-бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
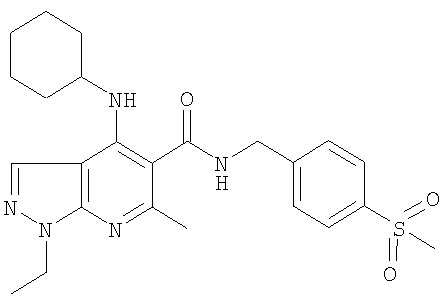
Смесь Промежуточного соединения 52 (0,014 г, 0,046 ммоль), HATU (0,018 г, 0,048 ммоль) и DIPEA (0,022 мл, 0,125 ммоль) в DMF (1 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли 1-[4-(метилсульфонил)фенил]метанамин (0,009 г, 0,046 ммоль) и смесь встряхивали еще несколько минут до получения раствора. Этот раствор хранили при комнатной температуре в течение 16 часов. Раствор концентрировали в вакууме и остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc-МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме с получением Примера 191 (0,005 г). LCMS показала MH+=470; tret=2,54 мин.
Пример 192: N-Бензил-4-(циклогексиламино)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
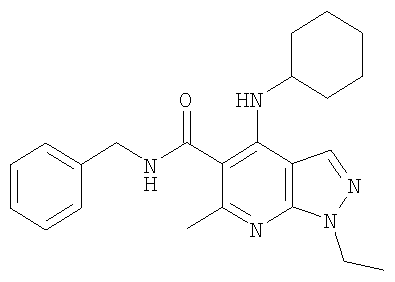
Пример 192 получали из Промежуточного соединения 52, используя способ, аналогичный Примеру 191. LCMS показала МН+=392; TRET=2,43 мин.
Пример 193: 4-(Циклогексиламино)-1-этил-N-(4-фторфенил)-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
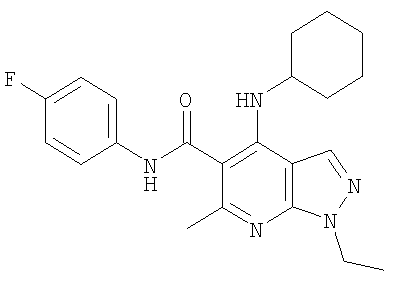
Пример 193 получали из Промежуточного соединения 52, используя способ, аналогичный Примеру 191. LCMS показала МН+=396; TRET=2,6 мин.
Пример 194: 4-(Циклогексиламино)-1-этил-6-метил-N-[4-(трифторметил)-бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
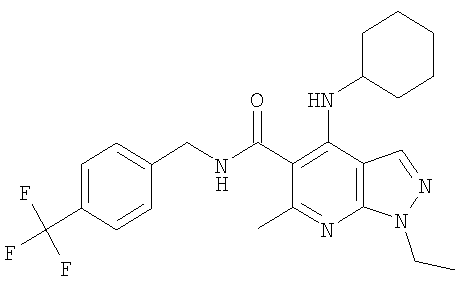
Пример 194 получали из Промежуточного соединения 52, используя способ, аналогичный Примеру 191. LCMS показала МН+=460; TRET=2,74 мин.
Пример 195: 4-(Циклогексиламино)-N-(2,3-дигидро-1Н-инден-2-ил)-1-этил-6-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
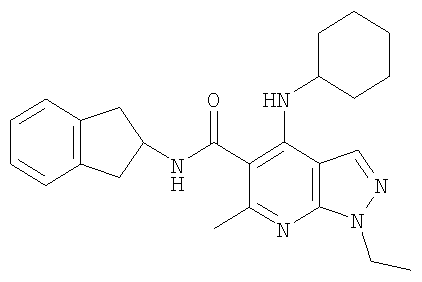
Пример 195 получали из Промежуточного соединения 52, используя способ, аналогичный Примеру 191. LCMS показала МН+=418; TRET=2,55 мин.
Пример 196: N-Бензил-1-этил-6-метил-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид
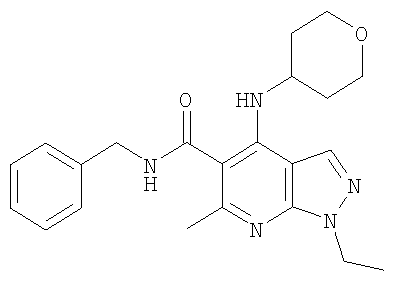
Пример 196 получали из Промежуточного соединения 53, используя способ, аналогичный Примеру 191. LCMS показала МН+=394; TRET=2,02 мин.
Пример 197: N-Бензил-1-этил-4-[(2-оксоазепан-3-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
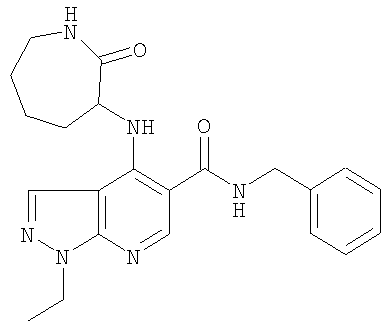
3-Аминоазепан-2-он (0,043 г, 0,335 ммоль, имеется в продаже у Sigma-Aldrich Company Ltd.) добавляли к смеси Промежуточного соединения 17 (0,021 г, 0,067 ммоль) и DIPEA (0,058 мл, 0,335 ммоль) в ацетонитриле (0,5 мл). Полученную в результате смесь нагревали при 85°С в течение 48 часов. Летучие вещества удаляли в вакууме и остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (силикагель, 0,5 г), который элюировали последовательно диэтиловым эфиром (1,5 мл), этилацетатом (1,5 мл) и смесью этилацетат - метанол (9/1, 1,5 мл). Фракции, содержащие нужное вещество, концентрировали в вакууме с получением Примера 197 (0,009 г). LCMS показала МН+=407; TRET=2,81 мин.
Приведенные ниже соединения были получены аналогично, но заменяя 3-аминоазепан-2-он таким же или аналогичным числом молей другого амина R3NH2:
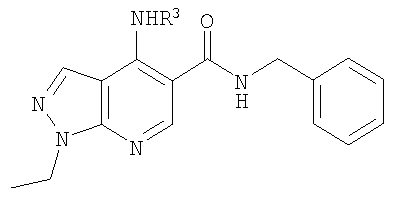
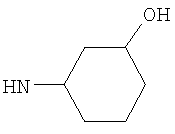
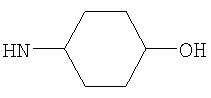
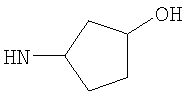
Пример 201: N-Бензил-1-этил-4-[(4-оксоциклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
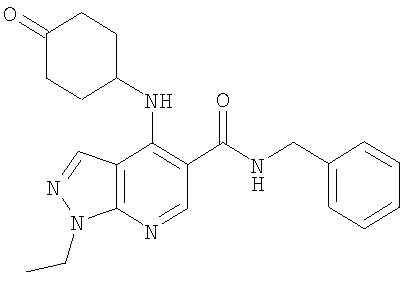
Промежуточное соединение 54 (0,048 г, 0,32 ммоль) добавляли к смеси Промежуточного соединения 17 (0,050 г, 0,16 Ммоль) и DIPEA (0,17 мл, 0,98 ммоль) в ацетонитриле (3 мл). Полученную в результате смесь нагревали с обратным холодильником. Через 12 часов к реакционной смеси добавляли дополнительные количества Промежуточного соединения 54 (0,044 г, 0,29 ммоль), DIPEA (0,17 мл, 0,98 ммоль) и ацетонитрила (1 мл) и смесь поддерживали при кипении с обратным холодильником. Через 36 часов реакционную смесь концентрировали в вакууме и остаточное масло растворяли в дихлорметане (8 мл) и промывали 5%-ным раствором бикарбоната натрия (2 мл). В результате выпаривания органического раствора получали вязкое масло, которое растворяли в дихлорметане (2 мл) и наносили на SPE картридж (силикагель, 5 г). Картридж элюировали последовательно градиентом этилацетат - циклогексан (1:16, затем 1:8, 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, концентрировали в вакууме с получением Примера 201 (0,018 г). LCMS показала МН+=392; TRET=2,95 мин.
Пример 202: 1-Этил-N-(2-гидрокси-1-метилэтил)-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
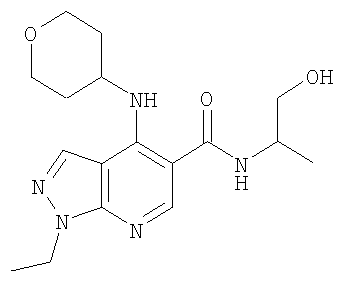
Промежуточное соединение 33 (0,1 г, 0,34 ммоль), EDC (0,066 г, 0,34 ммоль) и НОВТ (0,05 г, 0,37 ммоль) суспендировали в DMF (2 мл) и перемешивали при комнатной температуре в атмосфере азота в течение 15 мин. Добавляли 2-аминопропан-1-ол (0,026 г, 0,34 ммоль) и триэтиламин (0,036 г, 0,36 ммоль) и смесь перемешивали при комнатной температуре в атмосфере азота в течение 6 часов. Растворители удаляли в вакууме и остаток распределяли между DCM и водой. Органический слой концентрировали и наносили на SPE картридж (аминопропил, 5 г), который элюировали метанолом. В результате концентрирования в вакууме получали Пример 202 (0,095 г). LCMS показала MH+=348; TRET=2,15 мин.
Пример 203: Метил-(2S)-2-({[1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)-3-гидроксипропаноат
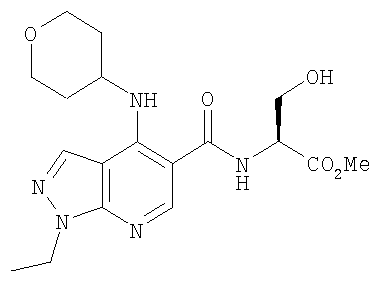
Реакционная схема:
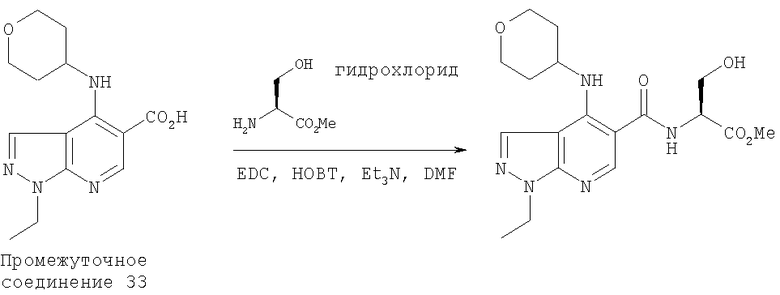
Промежуточное соединение 33 (0,1 г, 0,34 ммоль), EDC (0,066 г, 0,34 ммоль) и НОВТ (0,05 г, 0,37 ммоль) суспендировали в DMF (2 мл) и перемешивали при комнатной температуре в атмосфере азота в течение 15 мин. Добавляли гидрохлорид метилового эфира L-серина (0,054 г, 0,34 ммоль) и триэтиламин (0,036 г, 0,36 ммоль) и смесь перемешивали при комнатной температуре в атмосфере азота в течение 18 часов. Растворители удаляли в вакууме и остаток распределяли между DCM и водой. Органический слой концентрировали в вакууме и наносили на SPE картридж (аминопропил, 5 г), который элюировали метанолом. В результате концентрирования в вакууме получали неочищенный остаток, который дополнительно очищали при помощи SPE картриджа (силикагель, 5 г), элюируя этилацетатом, затем 5%-ной смесью метанол/этилацетат. Нужные фракции концентрировали в вакууме с получением Примера 203 (0,055 г). LCMS показала МН+=393; TRET=2,22 мин.
Пример 204: Этил-1-этил-4-[(4-гидроксициклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
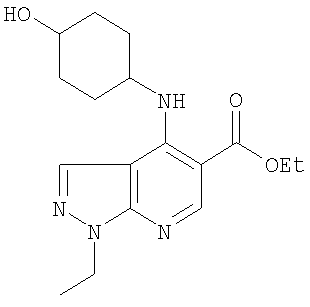
Промежуточное соединение 1 (1,5 г, 5,9 ммоль) растворяли в ацетонитриле (80 мл). Добавляли транс-4-аминоциклогексанол (0,817 г, 7,1 ммоль, имеется в продаже у TCI-America, альтернативно (например, в виде HCl соли) у Aldrich), и диизопропилэтиламин (6,18 мл, 35,5 ммоль) и эту смесь перемешивали при 85°С в течение 16 ч. Смесь концентрировали в вакууме и остаток распределяли между DCM (120 мл) и водой (30 мл). Фазы разделяли и органическую фазу сушили (Na2SO4) и выпаривали с получением бледно-желтого твердого вещества. Это твердое вещество растворяли в смеси DCM (10 мл) и хлороформа (3 мл) и наносили равными порциями на два SPE картриджа (силикагель, 20 г), которые элюировали последовательно градиентом EtOAc:циклогексан (1:16, затем 1:8, 1:4, 1:2, 1:1 и 1:0). Фракции, содержащие нужное вещество, объединяли и выпаривали в вакууме с получением Примера 204 (1,893 г) в виде белого твердого вещества. LCMS показала МН+=333;
ТRET=2,79 мин.
Пример 205: Этил-1-этил-4-[(4-оксоциклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
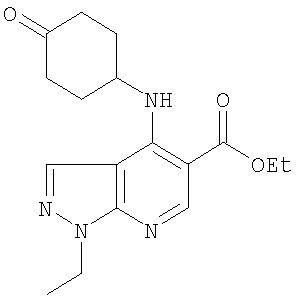
Пример 204 (1,893 г, 5,7 ммоль) суспендировали в ацетоне (12 мл) и перемешиваемую суспензию обрабатывали при 0°С реагентом Джонса (1,81 мл). Через 30 мин к реакционной смеси добавляли дополнительное количество реагента Джонса (1,81 мл) и поддерживали ее при 0°С. Еще через 2 часа к реакционной смеси добавляли последнюю порцию реагента Джонса (1,44 мл), и перемешивание при 0°С продолжали в течение 1 ч. К реакционной смеси добавляли изопропанол (3,8 мл), затем воду (15 мл). Полученную в результате смесь экстрагировали этилацетатом (2×40 мл). Объединенные органические экстракты промывали водой (8 мл), сушили (Na2SO4) и выпаривали до серого твердого вещества. Это твердое вещество растворяли в DCM (10 мл) и наносили равными порциями на два SPE картриджа (силикагель, 20 г), которые элюировали последовательно градиентом этилацетат:циклогексан (1:16, затем 1:8, 1:4, 1:2 и 1:1). Фракции, содержащие нужное вещество, объединяли и выпаривали в вакууме с получением Примера 205 (1,893 г) в виде белого твердого вещества. LCMS показала MH+=331; TRET=2,84 мин.
Пример 207 (= Пример 5): Этил-4-[(1-ацетил-4-пиперидинил)амино]-1-этил-1Н-пиразоло[3,4-6]пиридин-5-карбоксилат
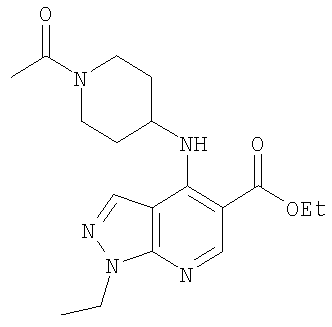
Промежуточное соединение 1 (2,58 г), Промежуточное соединение 6 (2,0 г) и N,N-диизопропилэтиламин (8,9 мл) растворяли в ацетонитриле (98 мл). Реакционную смесь нагревали при 85°С в течение 24 ч, затем добавляли дополнительную порцию Промежуточного соединения 6 (0,18 г) и нагревание продолжали в течение еще 10 ч. Реакционную смесь концентрировали в вакууме и остатки распределяли между DCM и водой. Фазы разделяли и органическую фазу выпаривали в вакууме. Остаток очищали хроматографией, используя Biotage (силикагель, 90 г), элюируя DCM: МеОН (5%), с получением Примера 207 (1,55 г) в виде белого твердого вещества. LCMS показала МН+=360; TRET=2,71 мин.
Пример 209: Этил-4-[(4-аминоциклогексил)амино]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
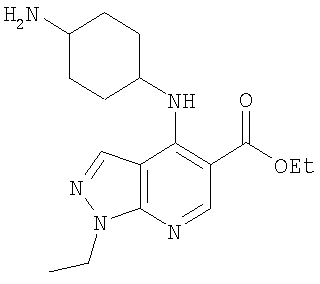
Пример 209 получали из Промежуточного соединения 1 и (4-аминоциклогексил)амина, используя способ, аналогичный использованному для получения Примера 207. LCMS показала МН+=332; TRET=2,18 мин.
Пример 210: 1-Этил-N-[(1-оксидо-3-пиридинил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
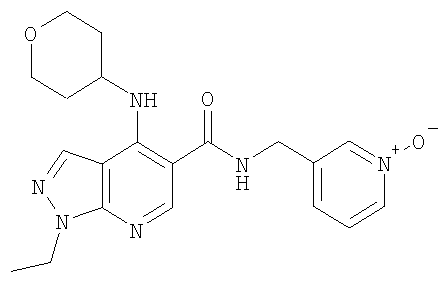
Раствор мета-хлорпероксибензойной кислоты (45 мг, 0,26 ммоль) в хлороформе (1 мл) добавляли по каплям при 0°С к перемешиваемому раствору Примера 138 (0,1 г, 0,26 ммоль) в хлороформе (1,5 мл). Через 1,5 ч при 0°С добавляли дополнительное количество мета-хлорпероксибензойной кислоты (45 мг, 0,26 ммоль) в хлороформе (1 мл) и перемешивание продолжали при 0°С в течение 1,5 ч. Оставалось следовое количество исходного вещества, поэтому добавляли дополнительное количество мета-хлорпероксибензойной кислоты (22 мг, 0,13 ммоль) в хлороформе (0,6 мл). Через 3,5 ч при 0°С к реакционной смеси добавляли 2 М раствор карбоната натрия (1 мл). Фазы разделяли пропусканием через гидрофобную фритту и водную фазу экстрагировали дополнительным количеством хлороформа (2 мл). Объединенные органические экстракты выпаривали до остаточной пены, которую очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 210 (44 мг). LCMS показала MH+=397; TRET=2,13 мин.
Пример 211: Этил-N-[(1-оксидо-2-пиридинил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
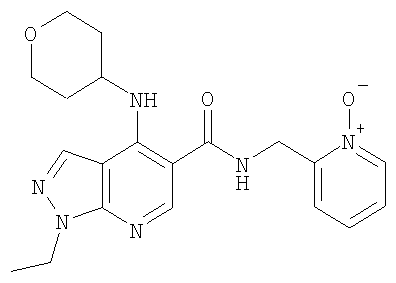
Пример 211 получали из Примера 600, используя способ, аналогичный использованному для получения Примера 210. LCMS показала МН+=397; TRET=2,20 мин.
Пример 212: 1-Этил-N-[(1-оксидо-4-пиридинил)метил]-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
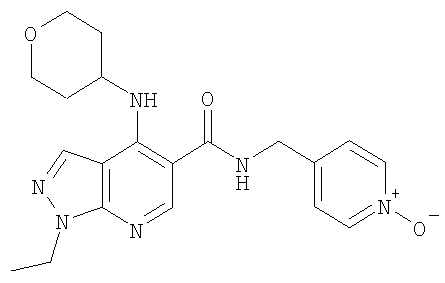
Пример 212 получали из Примера 33, используя способ, аналогичный использованному для получения Примера 210. LCMS показала MH+=397; TRET=2,13 мин.
Примеры 214-230
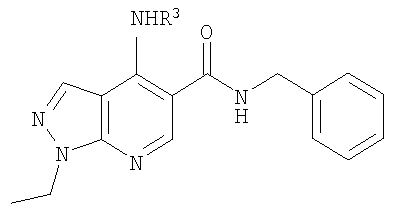
Общая методика
Промежуточное соединение 17 (0,15 ммоль) обрабатывали аликвотой амина (0,95 мл, эквивалентно 0,19 ммоль) из исходного раствора в ацетонитриле (0,2 М) и N,N-диизопропилэтиламином (0,24 ммоль). Эту смесь нагревали с обратным холодильником в течение 20 ч, затем концентрировали в вакууме. Остаток очищали при помощи SPE (силикагель) с получением нужного продукта.
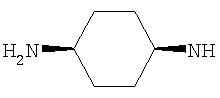
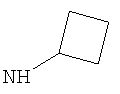
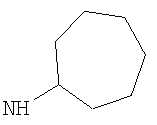
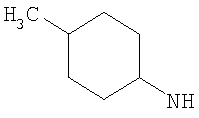
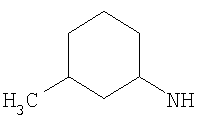
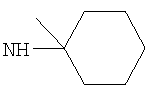
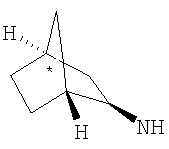

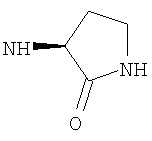
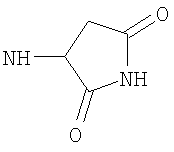
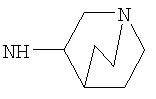
Пример 225: 1-Этил-4-[(1-метилциклогексил)амино]-N-(фенилметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
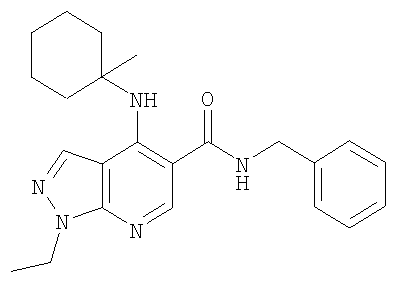
Предпочтительным способом получения Примера 225, включающим 1-метилциклогексиламин и более длительное время реакции, является следующий.
Раствор Промежуточного соединения 17 (46 мг), 1-метилциклогексиламина (26 мг) и диизопропилэтиламина (94 мг) в ацетонитриле (1 мл) перемешивали и нагревали с обратным холодильником в течение 77 ч. Добавляли дополнительные количества 1-метилциклогексиламина (102 мг), диизопропилэтиламина (93 мг) и ацетонитрила (1 мл) и реакционную смесь нагревали с обратным холодильником в течение еще 68 ч. Раствор охлаждали и концентрировали в вакууме. Остаток растирали в этилацетате и фильтровали. Фильтрат очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 225 (19 мг). LCMS показала MH+=392; TRET=3,46 мин.
Примеры 231, 247 и 257, показанные ниже и также включающие 1-метилциклогексиламин, также могут быть получены аналогичным способом.
Примеры 231-329
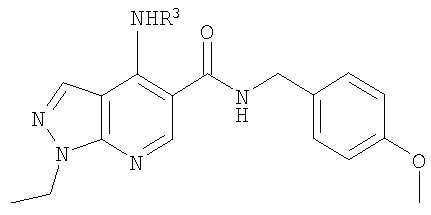
Общая методика
Промежуточное соединение 55 (0,15 ммоль) обрабатывали аликвотой амина (0,95 мл, эквивалентно 0,19 ммоль) из исходного раствора в ацетонитриле (0,2 М) и N,N-диизопропилэтиламином (0,24 ммоль). Смесь нагревали с обратным холодильником в течение 20 ч, затем концентрировали в вакууме. Остаток очищали с помощью SPE (силикагель) с получением нужного продукта.
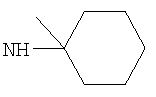
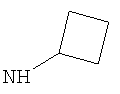
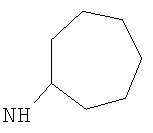

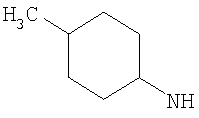
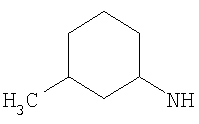

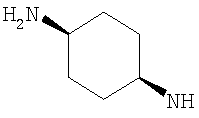
Примеры 240-249
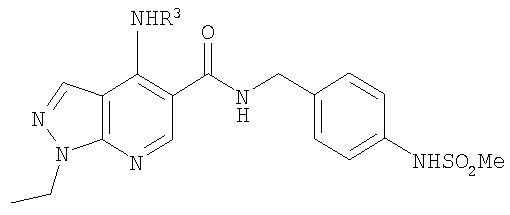
Общая методика
Промежуточное соединение 56 (0,15 ммоль) обрабатывали аликвотой амина (0,95 мл, эквивалентно 0,19 ммоль) из исходного раствора в ацетонитриле (0,2 М) и N,N-диизопропилэтиламином (0,24 ммоль). Смесь нагревали с обратным холодильником в течение 20 ч, затем концентрировали в вакууме. Остаток очищали с помощью SPE (силикагель) с получением нужного продукта.
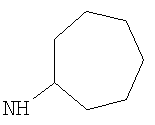
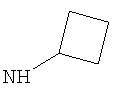

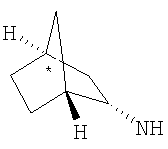
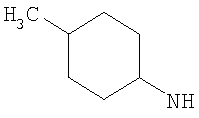
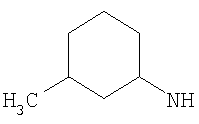
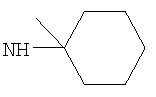
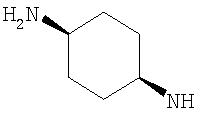
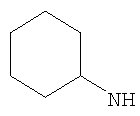
Примеры 250-258
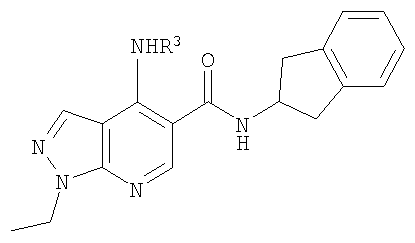
Общая методика
Промежуточное соединение 57 (0,15 ммоль) обрабатывали аликвотой амина (0,95 мл, эквивалентно 0,19 ммоль) из исходного раствора в ацетонитриле (0,2 М) и N,N-диизопропилэтиламином (0,24 ммоль). Смесь нагревали с обратным холодильником в течение 20 ч, затем концентрировали в вакууме. Остаток очищали с помощью SPE (силикагель) с получением нужного продукта.
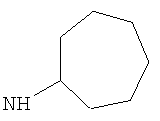
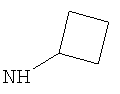
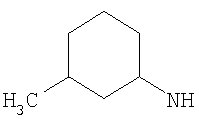
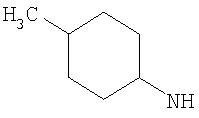

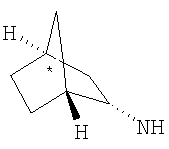
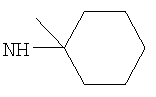
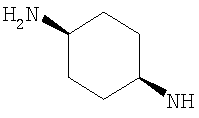
Примеры 259-275
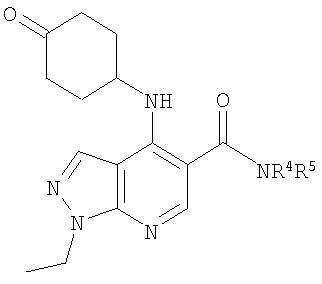
Общая методика
Смесь Промежуточного соединения 58 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,4 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина (0,1 ммоль) в DMF (0,2 мл) и эту смесь перемешивали в течение нескольких минут до получения раствора. Этот раствор хранили при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc-МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
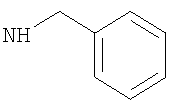
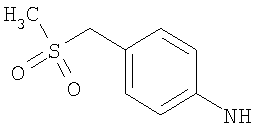
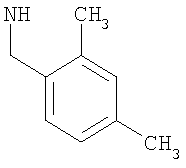
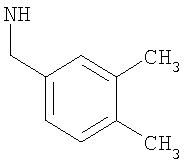
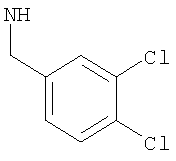
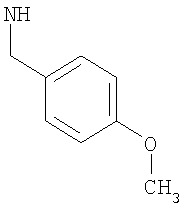
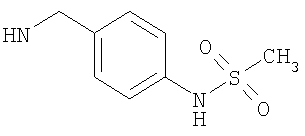
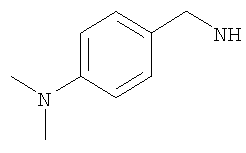
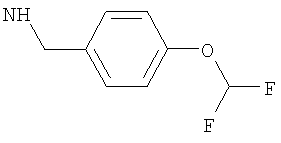
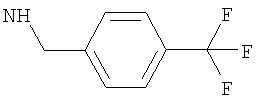
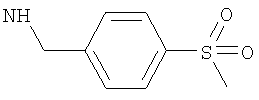
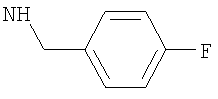
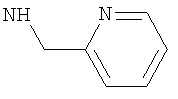
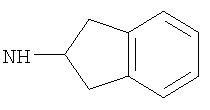
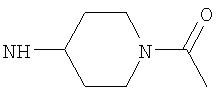
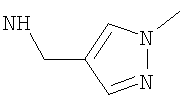
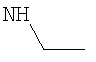
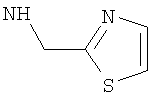
Пример 260 (Альтернативная методика)
N-[(2,4-Диметилфенил)метил]-1-этил-4-[(4-оксоциклогексил)амино]-1H-пиразоло[3,4-b]пиридин-5-карбоксамид
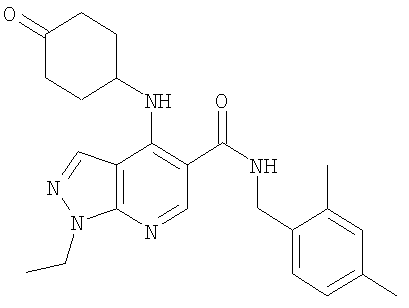
Альтернативная методика получения Примера 260.
Смесь Промежуточного соединения 58 (45 мг), HATU (63 мг) и DIPEA (39 мг) в ацетонитриле (5 мл) перемешивали в течение 10 мин. Затем добавляли раствор 2,4-диметилбензиламина (24 мг) (имеется у Salor; либо ICN Biomedicals; либо Synthesis, 1982, 12, 1036) в ацетонитриле (1 мл). Реакционную смесь перемешивали в течение 18 часов. Этот раствор концентрировали и остаток распределяли между этилацетатом (25 мл) и 0,5 М бикарбонатом натрия (20 мл). Органическую фазу отделяли, промывали водой (20 мл), сушили над Na2SO4 и концентрировали с получением смолы, которую наносили на SPE картридж (5 г). Картридж элюировали этилацетатом. Фракции, содержащие нужное соединение, объединяли и концентрировали в вакууме с получением Примера 260 (32 мг). LCMS показала МН+=420; TRET=3,16 мин. δн (CDCl3) 1.49 (3Н, t), 2.11 (2Н, m), 2.33 (3H, s), 2.35 (3H, s), 2.40 (2H, m), 2.52 (2H, m), 2.61 (2H, m), 4.36 (1H, m), 4.47 (2H, q), 4.55 (2H, d), 6.14 (1H, t), 7.01 + 7.18 (2H, AA'BB'), 7.04 (1H, s), 8.01 (1H, s), 8.36 (1H, s), 9.96 (1H, d).
Примеры 276-287
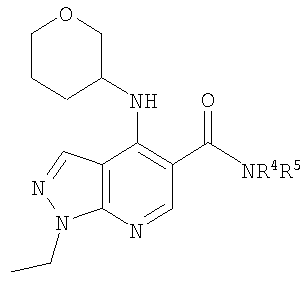
Общая методика
Смесь Промежуточного соединения 59 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,4 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина (0,1 ммоль) в DMF (0,2 мл) и эту смесь перемешивали в течение нескольких минут до получения раствора. Раствор хранили при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc:МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
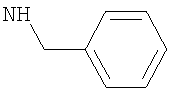
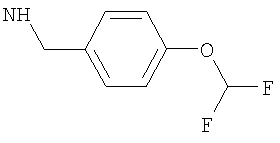
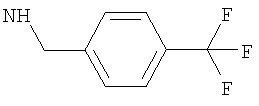
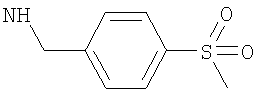
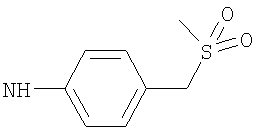
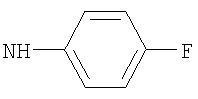
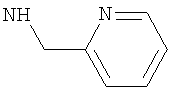

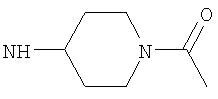
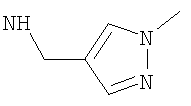
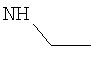
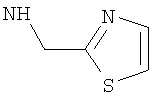
Пример 288: 4-[(4,4-Дифторциклогексил)амино]-1-этил-N-(фенилметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид и
Пример 289: 1-Этил-4-[(4-фтор-3-циклогексен-1-ил)амино]-N-(фенилметил)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
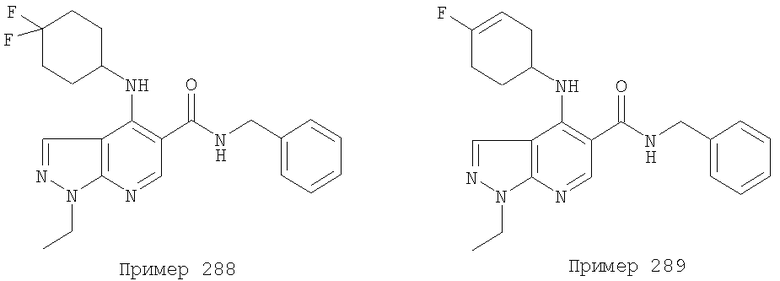
Диизопропилэтиламин (0,113 мл, 0,65 ммоль) добавляли к перемешиваемой смеси Промежуточного соединения 17 (40 мг, 0,13 ммоль) и Промежуточного соединения 63 (45 мг, 0,26 ммоль) в ацетонитриле (2 мл). Смесь перемешивали при 85°С. Через 18 часов к реакционной смеси добавляли дополнительную порцию Промежуточного соединения 63 (22,5 мг, 0,13 ммоль) и диизопропилэтиламина (0,113 мл, 0,65 ммоль) и перемешивание продолжали при 90°С в течение 24 ч. Затем эту смесь концентрировали в вакууме и остаток распределяли между DCM (20 мл) и водой (5 мл). Фазы разделяли и водную фазу экстрагировали дополнительным количеством DCM (10 мл). Объединенные органические экстракты сушили (Na2SO4) и выпаривали в вакууме с получением коричневого масла (65 мг), которое частично очищали на SPE картридже (силикагель, 10 г), элюируя смесью этилацетат:петролейный эфир (1:8, 1:4, 1:2, 1:1 и 1:0). Полученное в результате двухкомпонентное бледно-коричневое масло (34 мг) разделяли регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 288 (19 мг) в виде белой пены (LCMS показала MH+=414; TRET=3,24 мин) и Примера 289 (9 мг) в виде белого твердого вещества (LCMS показала МН+=394; TRET=3,21 мин).
Примеры 290-319
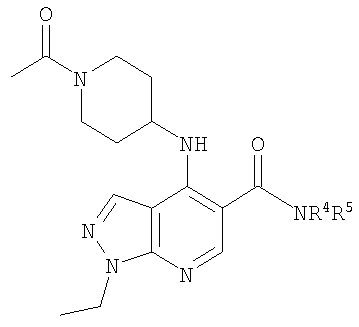
Общая методика
Смесь Промежуточного соединения 60 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,4 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина (0,1 ммоль) в DMF (0,2 мл) и смесь перемешивали в течение нескольких минут до получения раствора. Этот раствор хранили при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc:МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.

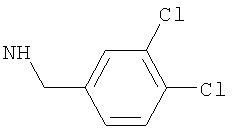
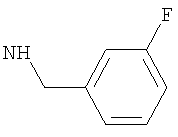
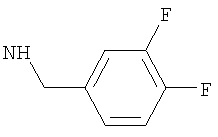
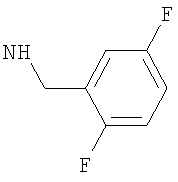
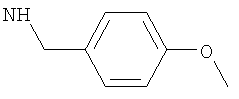
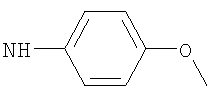
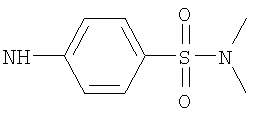
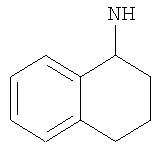
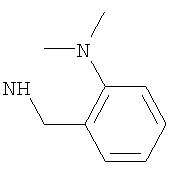
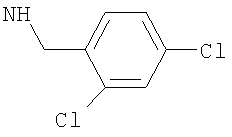
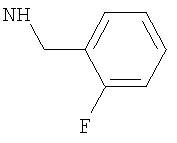
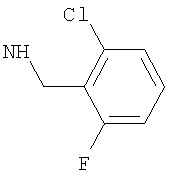
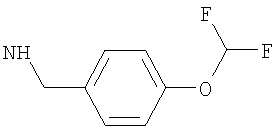
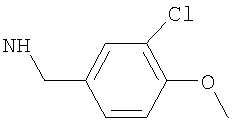
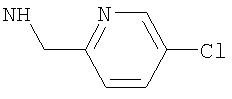
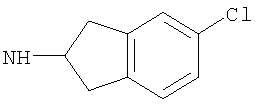
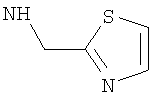
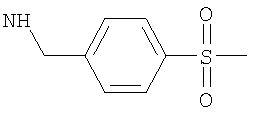
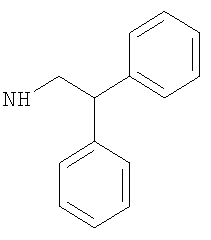
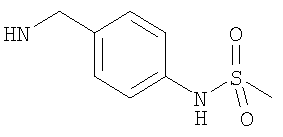
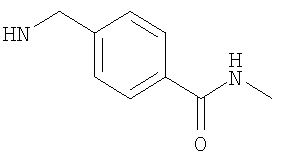
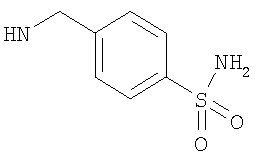
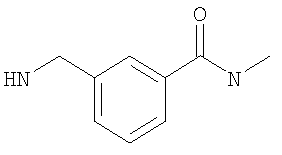
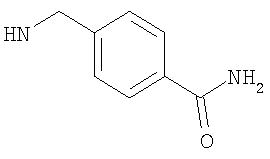
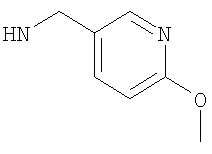
Пример 320: 1-Этил-N-4-пиперидинил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
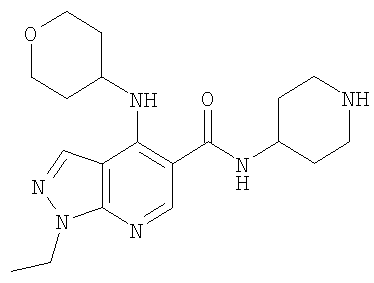
Раствор хлористого водорода в диоксане (30 мл, 4 М, 0,12 моль) добавляли к суспензии Примера 126 (1,3 г, 2,75 ммоль) в диоксане (10 мл) и смесь перемешивали при комнатной температуре в течение 6 ч. Реакционную смесь оставляли стоять в течение 14 ч, затем раствор упаривали, азеотропно перегоняли с DCM с образованием гидрохлоридной соли в виде белого твердого вещества. Это твердое вещество суспендировали в этилацетате (50 мл) и промывали раствором гидроксида натрия (2 н, 50 мл). Органический слой сушили над Na2SO4 и концентрировали в вакууме с получением Примера 320 в виде белого твердого вещества (995 мг). LCMS показала МН+=373; TRET=1,89 мин.
Пример 321: 1-Этил-N-(4-пиперидинилметил)-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
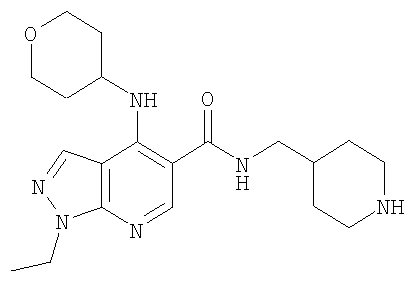
Раствор хлористого водорода в диоксане (30 мл, 4 М, 0,12 моль) добавляли к суспензии Промежуточного соединения 72 (1,2 г, 2,5 ммоль) в диоксане (10 мл) и смесь перемешивали при комнатной температуре в течение 6 ч. Реакционную смесь оставляли стоять в течение 14 ч, затем раствор выпаривали, азеотропно перегоняли с DCM с образованием белого твердого вещества (1,24 г). Часть этого твердого вещества (68 мг) суспендировали в этилацетате и промывали 2 М раствором гидроксида натрия. Органический слой сушили над Na2SO4 и концентрировали в вакууме с получением Примера 321 в виде белого твердого вещества (60 мг). LCMS показала МН+=387; TRET=1,92 мин.
Пример 322: 1-Этил-N-[1-(этилсульфонил)-4-пиперидинил]-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
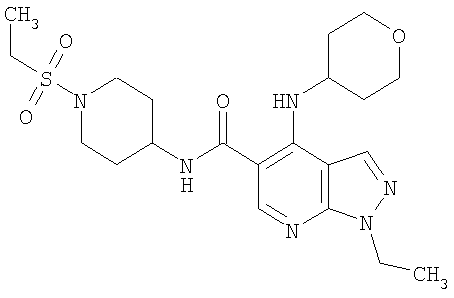
Триэтиламин (0,023 мл, 0,16 ммоль) добавляли к раствору Примера 320 (0,043 г, 0,115 моль) в DCM (1 мл). Смесь охлаждали (баня лед/вода в течение 10 мин) и добавляли этансульфонилхлорид (0,014 мл, 0,138 ммоль). Полученный в результате раствор перемешивали при комнатной температуре в течение 18 ч, затем растворитель удаляли потоком азота. Остаток растворяли в дихлорметане (1,5 мл) и перемешивали с водой (1,5 мл). Органический слой отделяли и продували азотом и наносили на SPE картридж (силикагель, 2 г), элюируя 60%-100%-ным этилацетатом в циклогексане. Нужные фракции концентрировали в вакууме с получением Примера 322 в виде белого твердого вещества (32 мг). LCMS показала МН+=465; TRET=2,52 мин.
Приведенные ниже соединения получали аналогично, используя такое же или близкое число молей реагентов и такие же или близкие объемы растворителей:
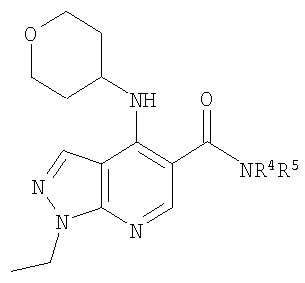
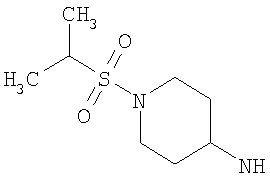
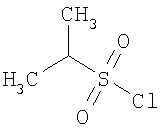
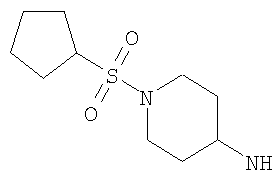
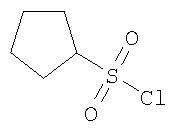
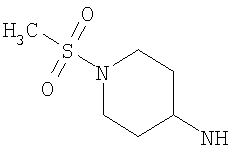
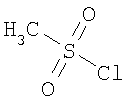
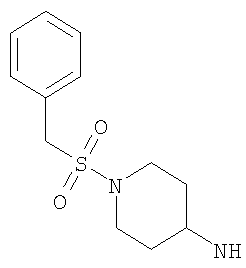
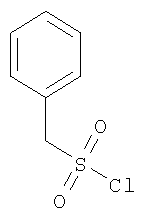
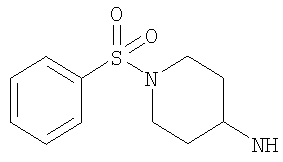
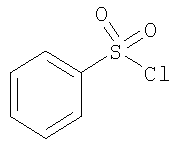
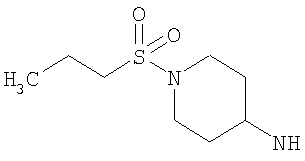
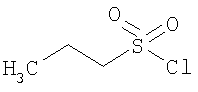
Пример 329: N-[1-(Циклопропилкарбонил)-4-пиперидинил]-1-этил-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
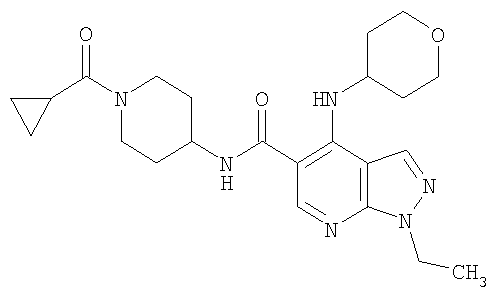
Циклопропанкарбоновую кислоту (0,011 мл, 0,138 ммоль), EDC (0,031 г, 0,161 ммоль) и НОВТ (0,019 г, 0,138 ммоль) суспендировали в DMF (2 мл) и перемешивали при комнатной температуре в течение 1 часа. Добавляли Пример 320 (0,043 г, 0,115 ммоль) и смесь перемешивали при комнатной температуре в течение 16 часов. Большую часть растворителя удаляли, используя поток азота, и остаток распределяли между DCM (3 мл) и водой (3 мл). Органический слой продували азотом и наносили на SPE картридж (аминопропил, 1 г), который элюировали метанолом. В результате концентрирования путем продувания азотом получали неочищенный остаток, который дополнительно очищали с помощью SPE картриджа (силикагель, 1 г), элюируя 50-100%-ным EtOAc в циклогексане, а затем 5%-ным метанолом в EtOAc. Нужные фракции концентрировали в вакууме с получением Примера 329 в виде белого твердого вещества (49 мг). LCMS показала МН+=441; TRET=2,23 мин.
Аналогичным образом получали приведенные ниже соединения, используя такое же или близкое число молей реагентов и объемов растворителей и используя Пример 320 в качестве исходного вещества для получения Примеров 330-343, и используя Пример 321 (близкое число молей) вместо Примера 320 в качестве исходного вещества для получения Примеров 344-349.

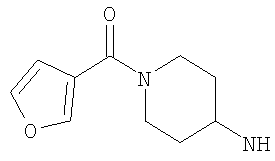
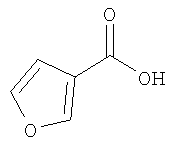
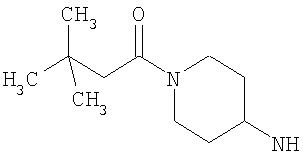
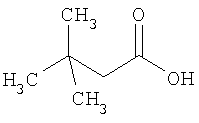
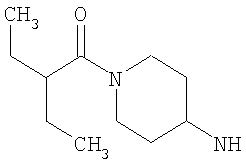
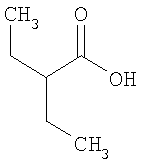
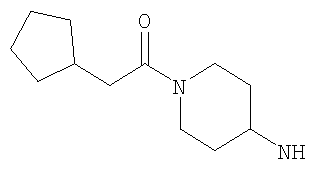
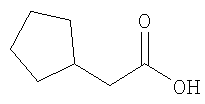
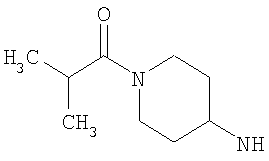
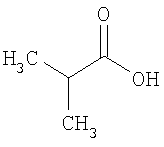
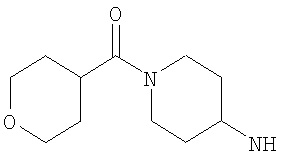
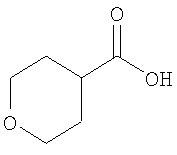
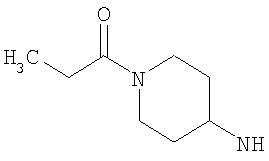
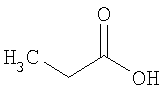
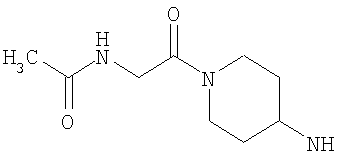
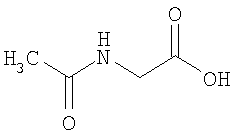
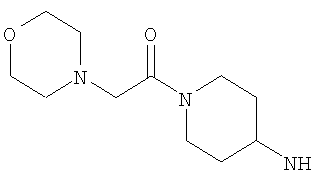
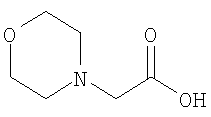
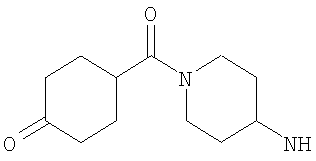
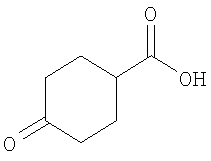
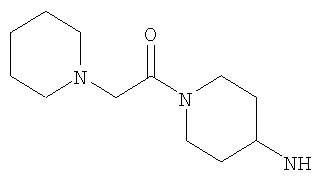
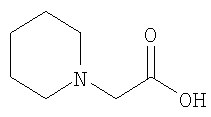
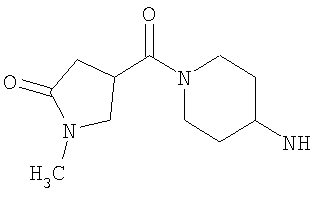
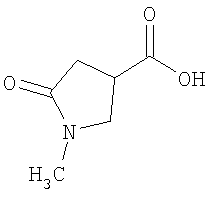
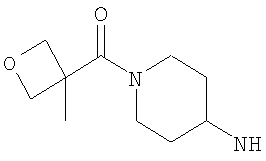
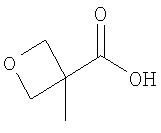
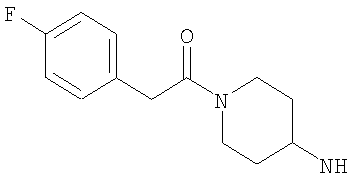
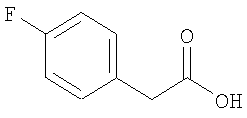
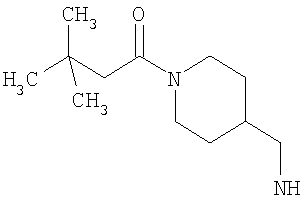
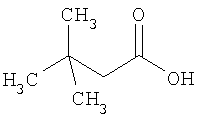
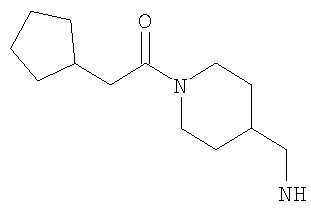
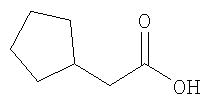
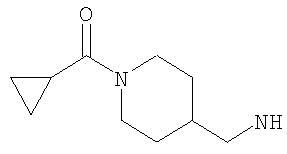
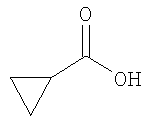
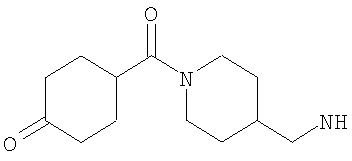
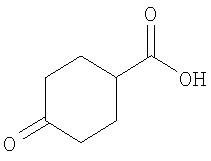
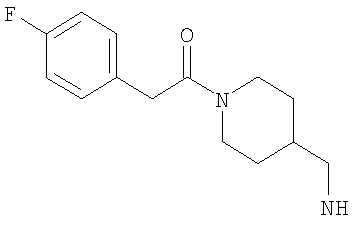
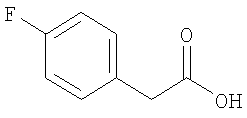
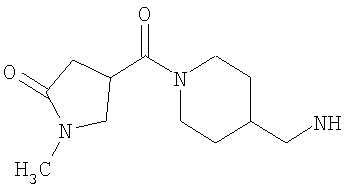
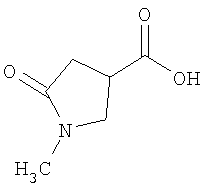
Пример 350: Метил-3-[(1-этил-5-{[(фенилметил)амино]карбонил}-1H-пиразоло[3,4-b]пиридин-4-ил)амино]циклогексанкарбоксилат
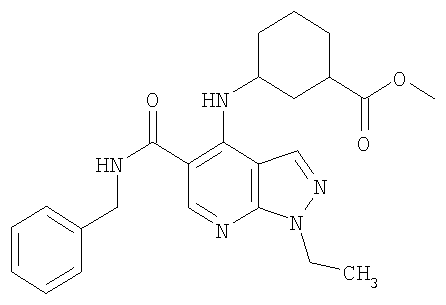
Пример 350 получали из Промежуточного соединения 17 и используя способ, аналогичный использованному для получения Примера 207. LCMS показала МН+=436; TRET=3,20.
Пример 351: 3-[(1-Этил-5-{[(фенилметил)амино]карбонил}-1Н-пиразоло[3,4-b]пиридин-4-ил)амино]циклогексанкарбоновая кислота
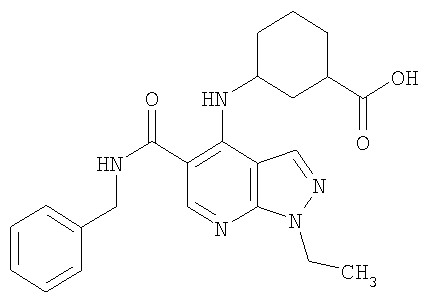
2 М Раствор гидроксида натрия (0,5 мл) добавляли к перемешиваемой суспензии Примера 350 (0,12 г, 0,275 ммоль) в метаноле (3,5 мл) и воде (0,5 мл). После перемешивания в течение ночи при комнатной температуре реакционный раствор концентрировали, разбавляли водой (3 мл) и подкисляли 2 М соляной кислотой. Полученный в результате осадок собирали фильтрацией, промывали водой и сушили с получением Примера 351 в виде белого твердого вещества (0,105 г). LCMS показала МН+=422; TRET=2,95 мин.
Пример 352: 1-Этил-N-(фенилметил)-4-(4-пиперидиниламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
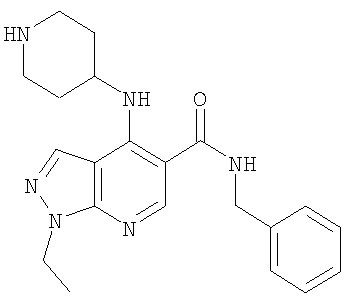
Водную соляную кислоту (20 мл, 5 М) добавляли к раствору Промежуточного соединения 65 (2,58 г, 5,405 ммоль) в тетрагидрофуране (10 мл). Реакционную смесь перемешивали при 20°С в течение 22 ч, затем выпаривали в вакууме. Остаток распределяли между DCM и водой. Водную фазу подщелачивали водным раствором гидроксида натрия (2 М) и экстрагировали диэтиловым эфиром. Органические фазы выпаривали в вакууме с получением Примера 352 в виде белого твердого вещества (2,04 г). LCMS показала MH+=379; TRET=2,10 мин.
Пример 353: Этил-1-этил-4-({1-[(метилокси)ацетил]-4-пиперидинил}амино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
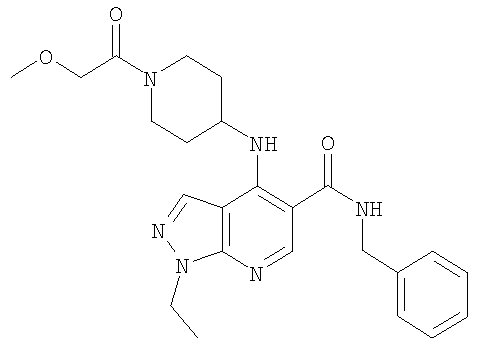
Метоксиацетилхлорид (0,016 мг, 0,144 ммоль) и триэтиламин (0,02 мл, 0,144 ммоль) добавляли к раствору Примера 352 (0,046 г, 0,122 ммоль) в DCM в Reactivial. Реакционную смесь перемешивали в течение 22 ч при 20°С, затем разбавляли DCM и промывали водным раствором гидрокарбоната натрия. Органическую фазу отделяли и наносили непосредственно на SPE картридж (силикагель, 2 г). Картридж элюировали смесью DCM:МеОН (1%, затем 3%) с получением Примера 353 в виде белого твердого вещества (0,05 г). LCMS показала МН+=451; TRET=2,66 мин.
Пример 354: Этил-1-(1-метилэтил)-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
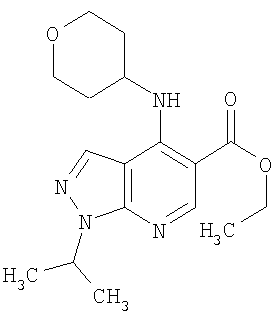
Получали аналогично Примеру 186, используя Пример 20 (0,03 г, 0,1 ммоль) с изопропилбромидом (10 мкл, 0,11 ммоль), через 16 часов дополнительно добавляли 0,11 ммоль алкилирующего агента. Конечное соединение образовывалось в виде прозрачной смолы (16 мг). LCMS показала МН+=333; TRET=3,16 мин.
Пример 355: 4-(Циклогексиламино)-1-этил-N-метил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
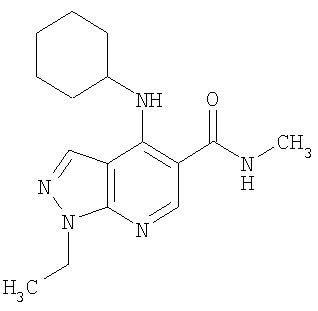
Промежуточное соединение 64 (0,02 г, 0,084 ммоль) и диизопропилэтиламин (0,044 мл, 0,252 ммоль) суспендировали в N-метилпирролидиноне (1 мл) и добавляли циклогексиламин (0,012 мл, 0,1 ммоль). Смесь нагревали при 85°С при перемешивании в Reactivial™ в течение 8 ч, затем концентрировали в вакууме. Остаток распределяли между DCM (2 мл) и водой (2 мл). Слои разделяли и органический слой концентрировали в вакууме, затем очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением Примера 355 (0,012 г). LCMS показала МН+=302; TRET=2,85 мин.
Пример 356: 1-Этил-N-(4-фторфенил)-6-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид
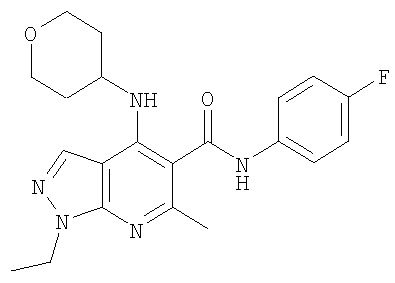
Пример 356 получали из Промежуточного соединения 53, используя способ, аналогичный Примеру 191. LCMS показала MH+=398; TRET=2,18 мин.
Пример 357: 1-Этил-6-метил-N-{[4-(метилсульфонил)фенил]метил}-4-(тетрагидро-2H-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид
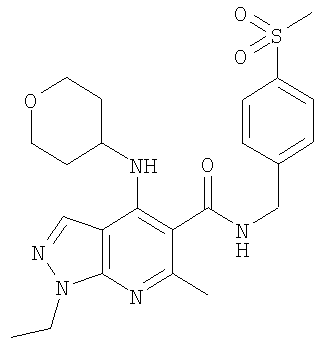
Пример 357 получали из Промежуточного соединения 53, используя способ, аналогичный Примеру 191. LCMS показала MH+=472; ТRET=2,15 мин.
Пример 358: N-(2,3-Дигидро-1Н-инден-2-ил)-1-этил-6-метил-4-(тетрагидро-2Н-пиран-4-иламино)-1N-пиразоло[3,4-b]пиридин-5-карбоксамид
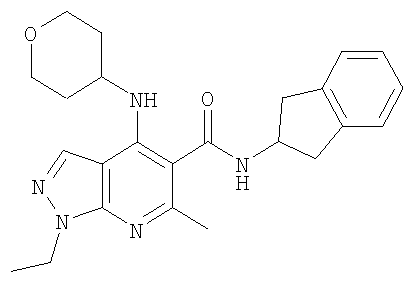
Пример 358 получали из Промежуточного соединения 53, используя способ, аналогичный Примеру 191. LCMS показала МН+=394; TRET=2,04 мин.
Примеры 360-414
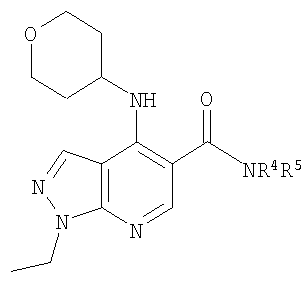
Общая методика
Промежуточное соединение 33 (1,89 г) обрабатывали тионилхлоридом (10 мл) и смесь нагревали с обратным холодильником в течение 2 ч. Избыток тионилхлорида удаляли в вакууме с получением Промежуточного соединения 73 предполагаемого хлорангидрида Промежуточного соединения 33 в виде кремового твердого вещества. Это твердое вещество суспендировали в тетрагидрофуране (32,5 мл) и аликвоту этой суспензии добавляли к смеси амина (0,11 ммоль) и диизопропилэтиламина (0,165-0,22 ммоль) в THF (0,5 мл). Реакционную смесь перемешивали в течение 24 ч и растворитель удаляли в вакууме. Остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
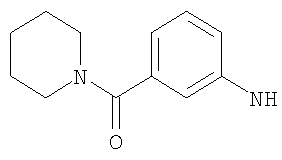
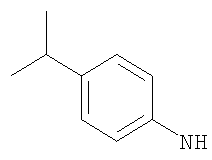
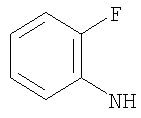
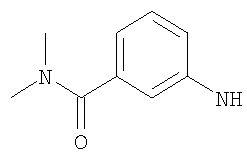
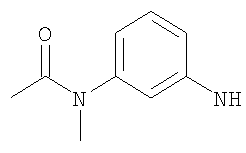
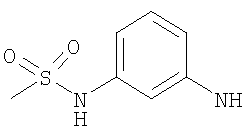
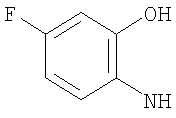
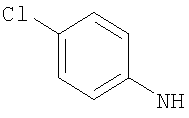
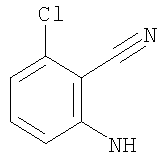
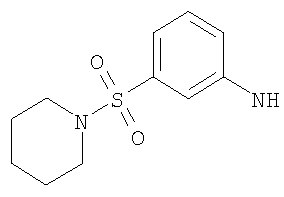
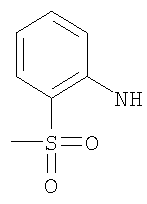
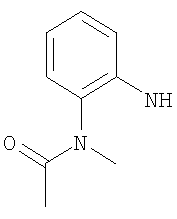
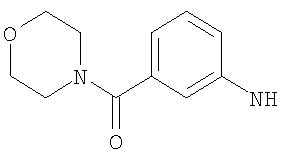
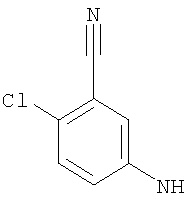
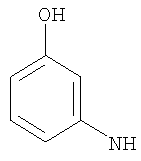
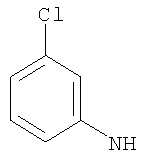
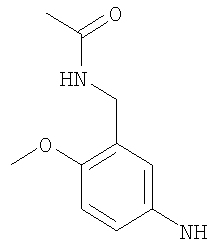
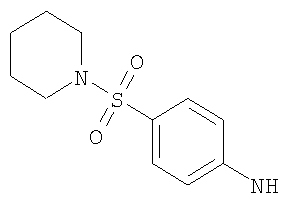
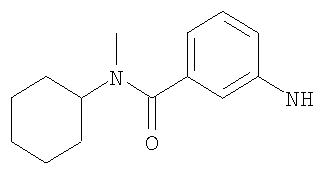
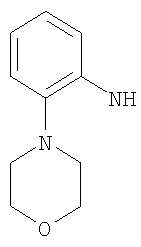
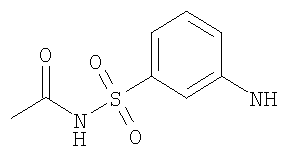
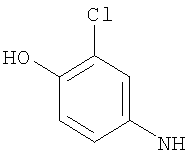
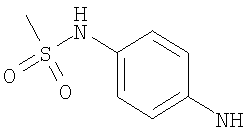
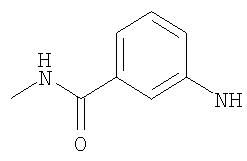
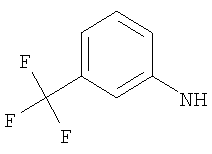
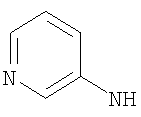
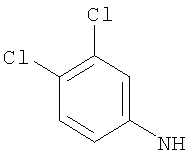
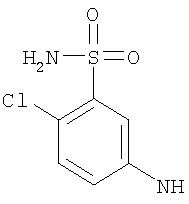
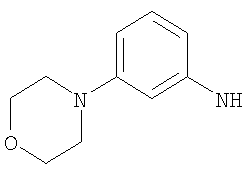
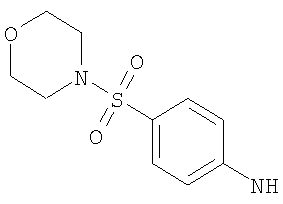
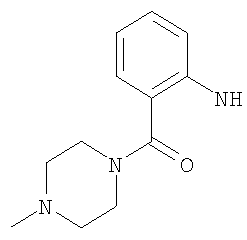
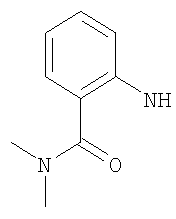
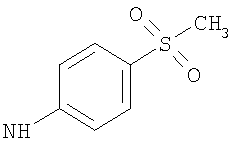
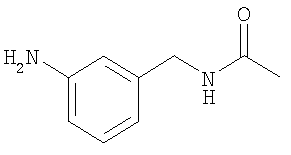
Пример 414: 1-Этил-4-(тетрагидро-2H-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
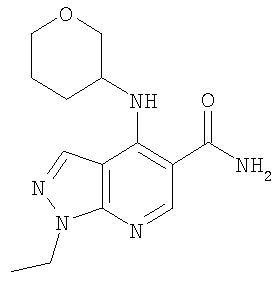
Пример 414 получали из Промежуточного соединения 59, используя общий способ, описанный для Примеров 360-413. LCMS показала МН+=398; TRET=2,90 мин.
Примеры 415-487
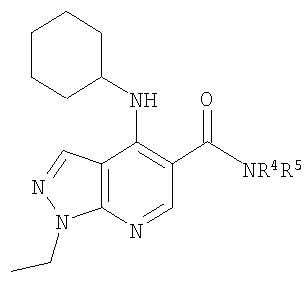
Общая методика
Смесь Промежуточного соединения 61 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,4 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина (0,1 ммоль) в DMF (0,2 мл) и смесь перемешивали еще несколько минут до получения раствора. Этот раствор хранили при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc-МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
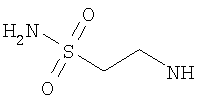
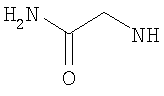
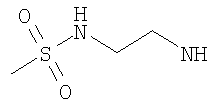
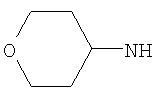
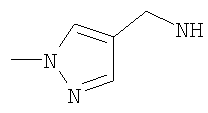
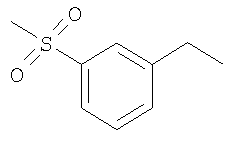
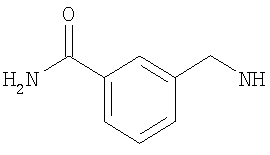
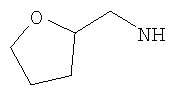
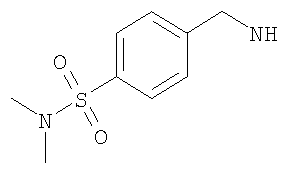
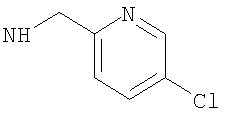
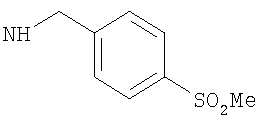
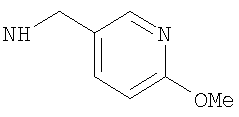
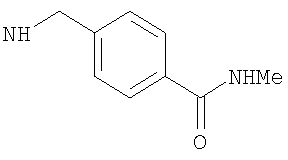
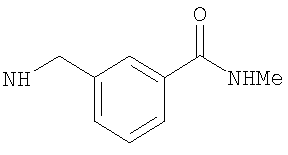
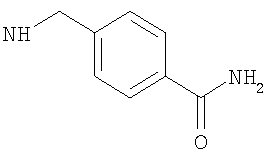
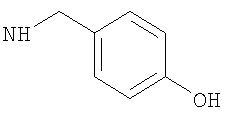
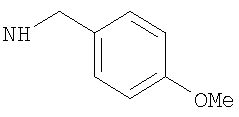
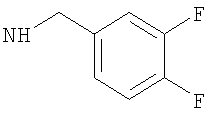
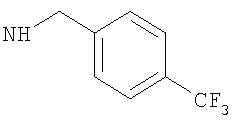
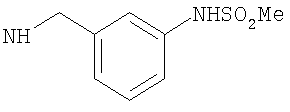
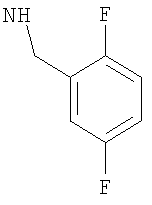
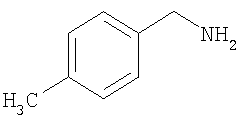
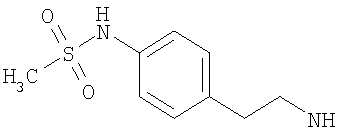
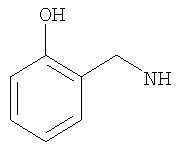
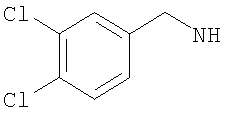
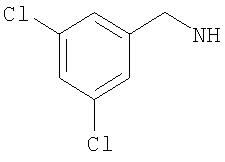
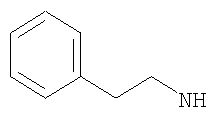
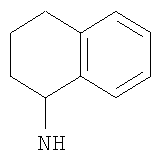
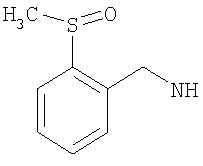
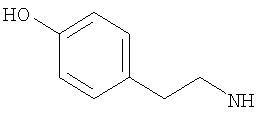
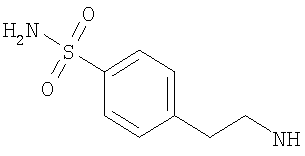
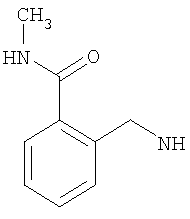
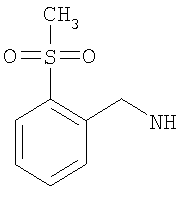
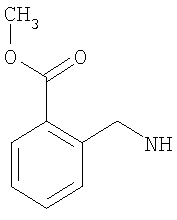
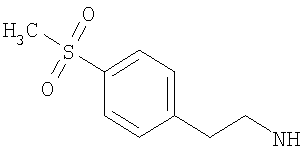
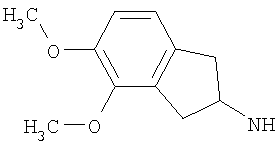
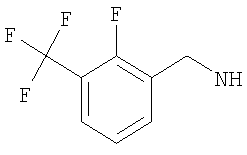
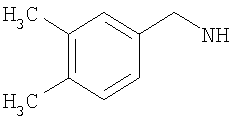
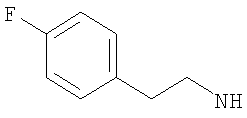
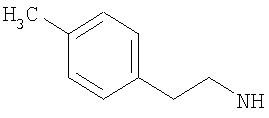
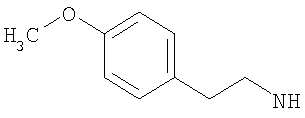
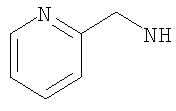
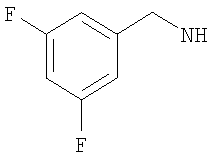
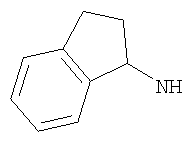
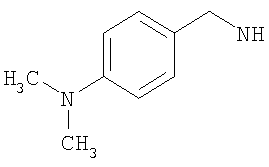
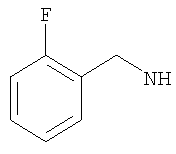
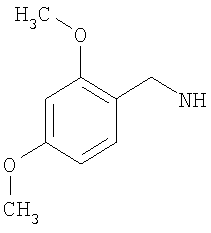
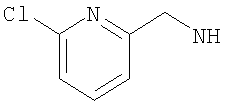
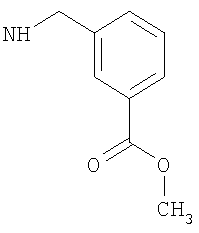
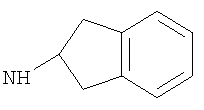
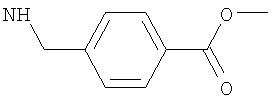
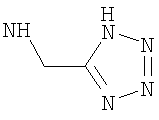
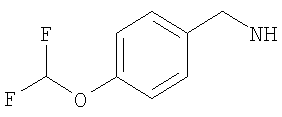
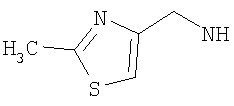
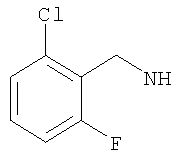
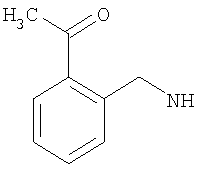
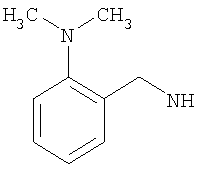
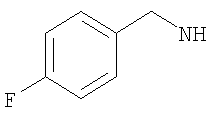
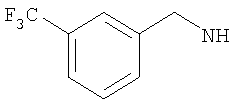
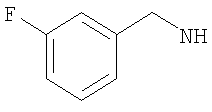
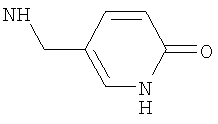
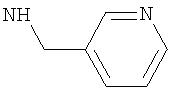
Пример 488: 4-[({[4-(Циклогексиламино)-1-этил-1H-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)метил]бензойная кислота
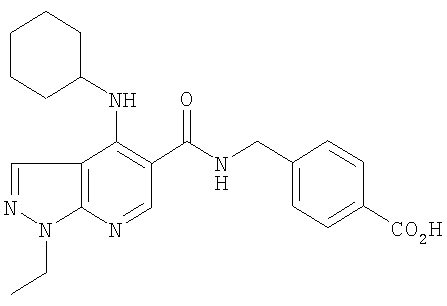
2 М Раствор гидроксида натрия (29 мкл, 0,058 ммоль) добавляли к перемешиваемому раствору Примера 470 (6 мг, 0,014 ммоль) в метаноле (28 мкл) и воде (2 мкл). Полученный в результате раствор перемешивали при 50°С в атмосфере азота. Через 16 ч эту смесь разбавляли водой (0,5 мл) и доводили до рН 4 уксусной кислотой. Выпавшее в осадок твердое вещество собирали фильтрацией и сушили в вакууме с получением Примера 488 в виде белого твердого вещества (4,5 мг). LCMS показала МН+=422; ТRET=3,26 мин.
Пример 489: 3-[({[4-(Циклогексиламино)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)метил]бензойная кислота
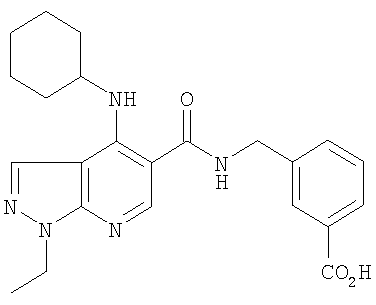
2 М Раствор гидроксида натрия (83 мкл, 0,166 ммоль) добавляли к перемешиваемому раствору Примера 468 (18 мг, 0,042 ммоль) в метаноле (88 мкл) и воде (5 мкл). Полученный в результате раствор перемешивали при 50°С в атмосфере азота. Через 16 ч к реакционной смеси добавляли дополнительное количество 2 М раствора гидроксида натрия (29 мкл, 0,058 ммоль). Через 24 ч реакционную смесь разбавляли водой (0,5 мл) и доводили до рН 4 уксусной кислотой. Смесь экстрагировали этилацетатом (2×0,5 мл) и объединенные экстракты сушили (Na2SO4) и выпаривали в вакууме с получением твердого вещества (21 мг). Это твердое вещество очищали на SPE картридже (силикагель, 1 г), элюируя смесью этилацетат:циклогексан (1:1), а затем метанолом. Фракции, содержащие нужный продукт, объединяли и концентрировали с получением Примера 489 в виде белого твердого вещества (4,6 мг). LCMS показала MH+=422; TRET=3,22 мин.
Пример 490: 4-(Циклогексиламино)-N-(2,3-дигидро-1 Н-инден-2-ил)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамида гидрохлорид
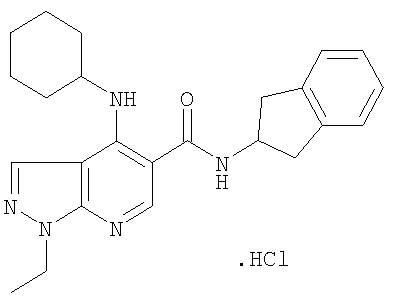
Раствор Примера 469 (71 мг, 0,17 ммоль) в безводном THF (2 мл) обрабатывали хлористым водородом в диоксане (4 М, 0,3 мл). После выстаивания при температуре окружающей среды в течение 16 часов полученное в результате твердое вещество собирали фильтрацией и сушили в вакууме с получением Примера 490 в виде палочковидных кристаллов (36 мг). LCMS показала МН+=404; TRET=3,60 мин.
Пример 491: 4-(Циклогексиламино)-N-(2,3-дигидро-1Н-инден-2-ил)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамида метансульфонат
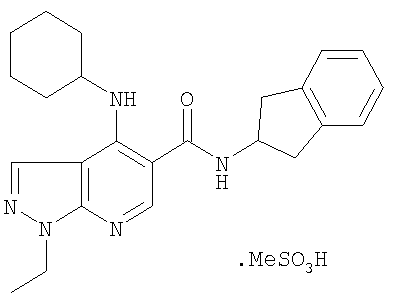
Раствор Примера 469 (71 мг, 0,17 ммоль) в безводном THF (2 мл) обрабатывали безводной метансульфоновой кислотой (11,4 мкл, 0,17 ммоль). После выстаивания при температуре окружающей среды в течение 16 часов полученное в результате твердое вещество собирали фильтрацией и сушили в вакууме с получением Примера 491 в виде палочковидных кристаллов (23 мг). LCMS показала MH+=404; tret=3,59 мин. Примеры 492-649
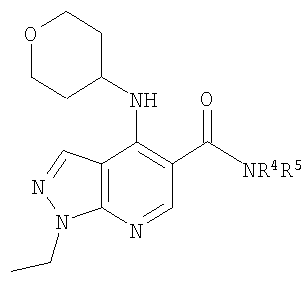
Общая методика
Смесь Промежуточного соединения 33 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,4 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина (0,1 ммоль) в DMF (0,2 мл) и эту смесь встряхивали в течение нескольких минут до получения раствора. Этот раствор держали при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток растворяли в хлороформе (0,5 мл) и наносили на SPE картридж (аминопропил, 0,5 г). Картридж элюировали последовательно хлороформом (1,5 мл), EtOAc (1,5 мл) и EtOAc:МеОН (9:1, 1,5 мл). Фракции, содержащие нужный продукт, концентрировали в вакууме и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
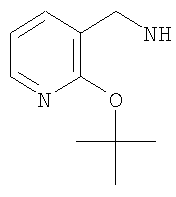
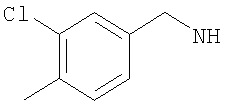
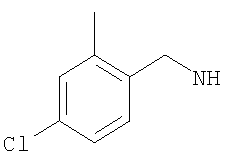
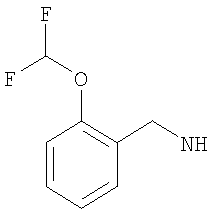
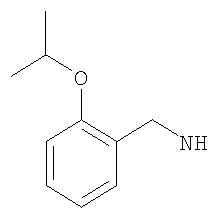
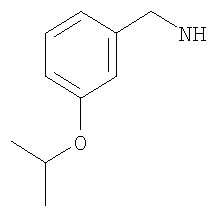
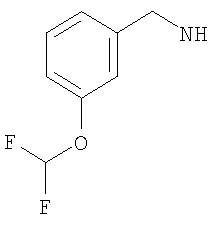
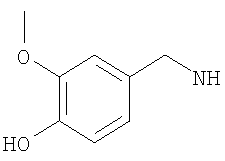
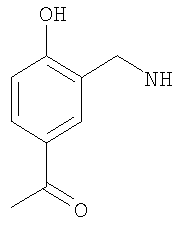
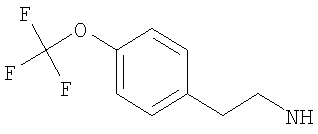
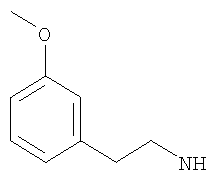
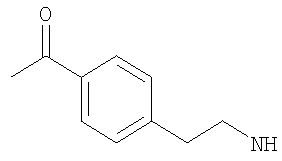
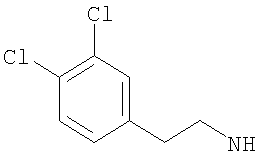
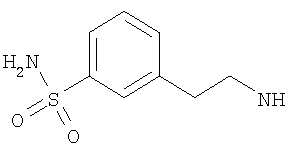
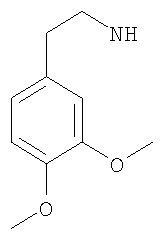
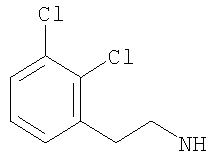
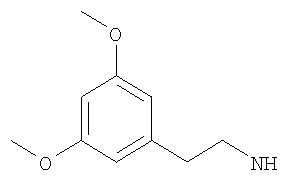
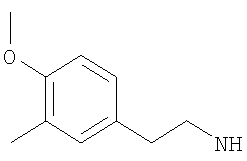
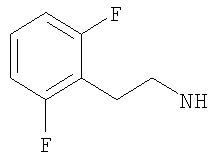
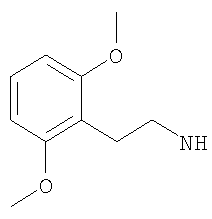
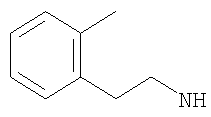
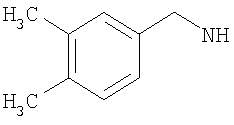
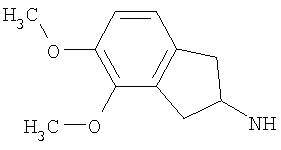
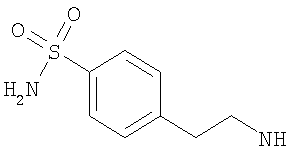
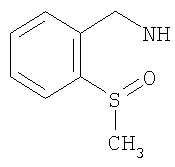
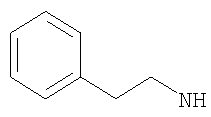
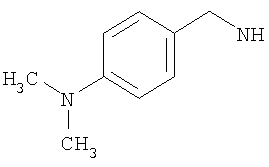
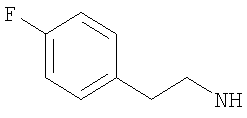
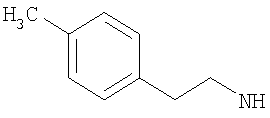
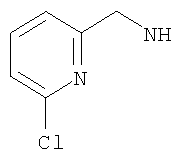
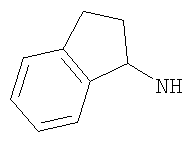
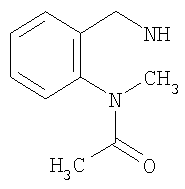
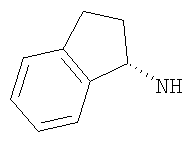
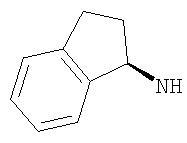
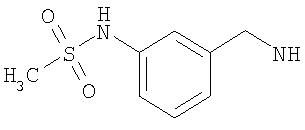
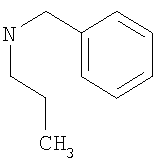
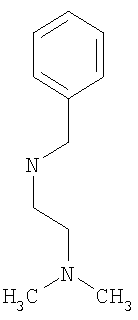
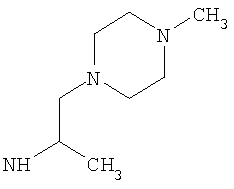
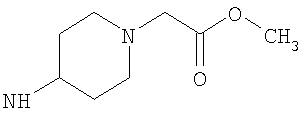
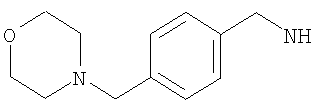
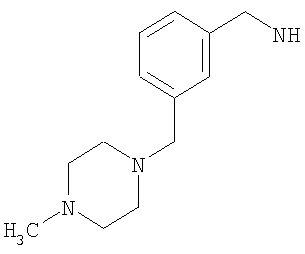
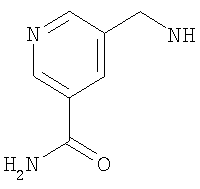
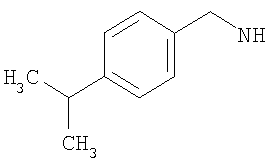
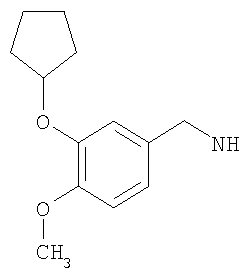
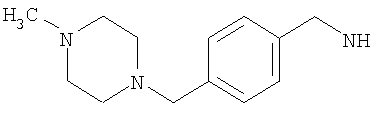
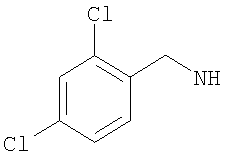
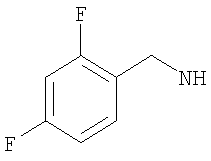
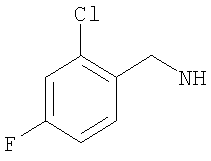
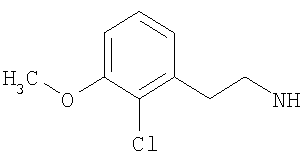
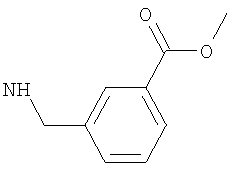
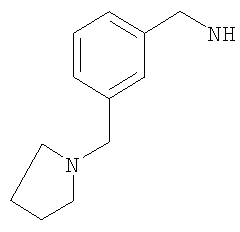
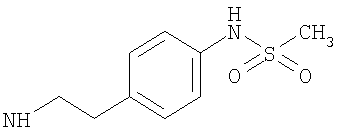
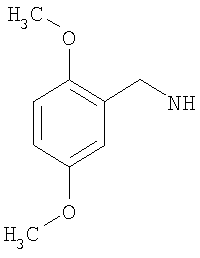
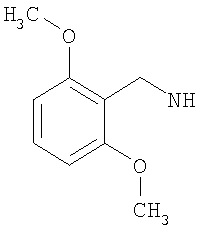
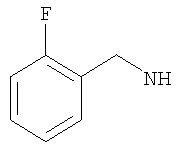
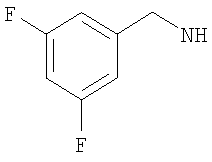
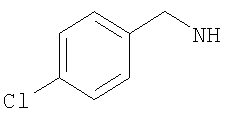
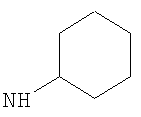
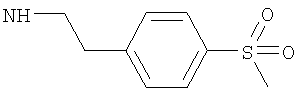
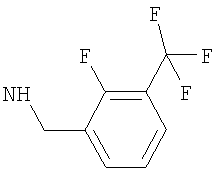
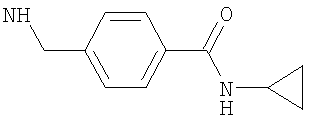
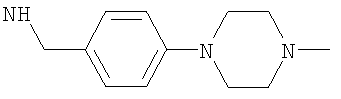
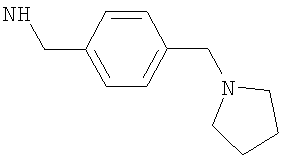
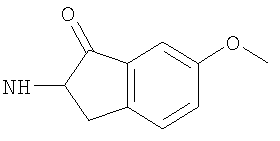
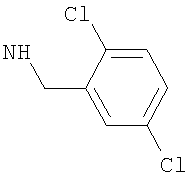
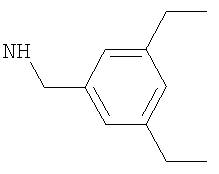
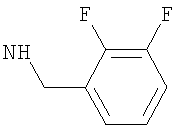
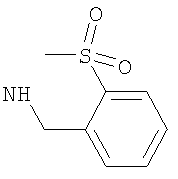
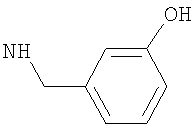
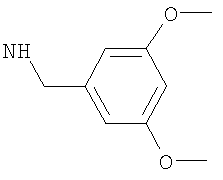
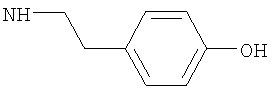
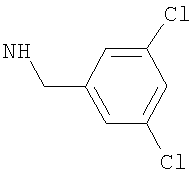
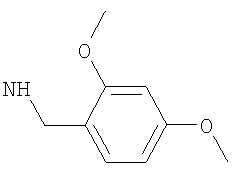
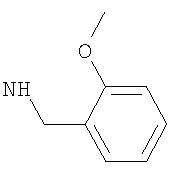
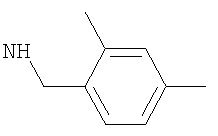
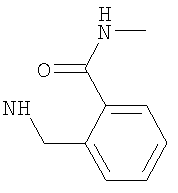
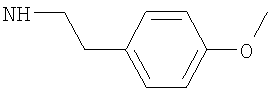
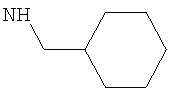
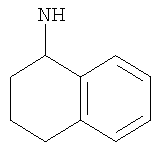
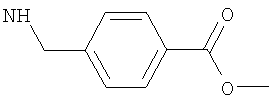
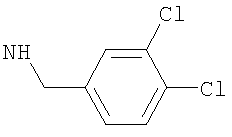
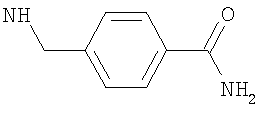
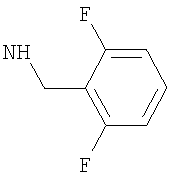
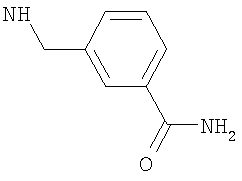
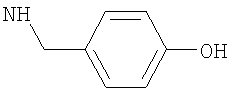
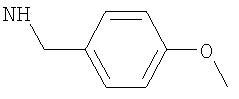
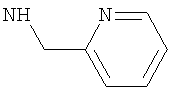
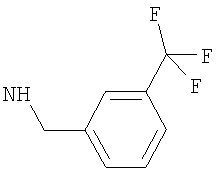
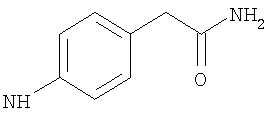
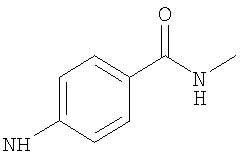
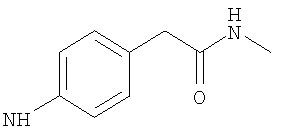
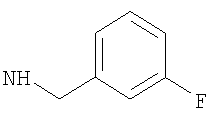
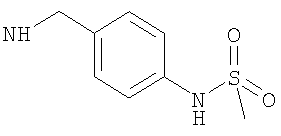
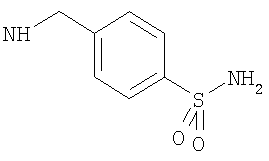
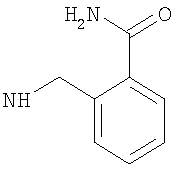
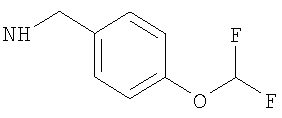
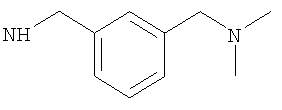
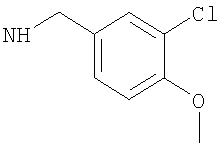
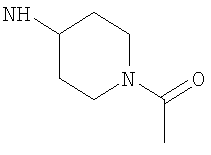
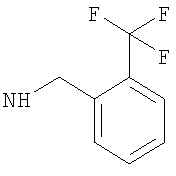
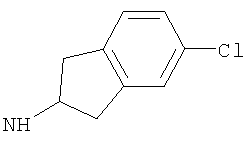
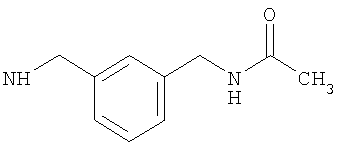
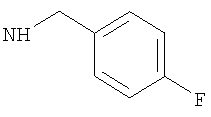
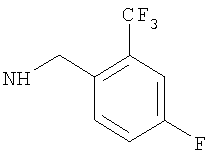
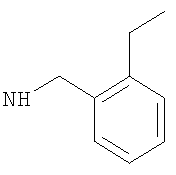
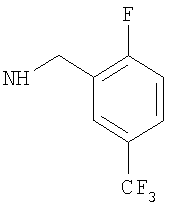
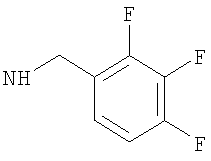
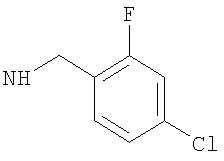
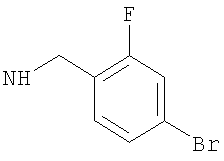
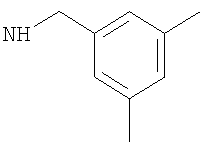
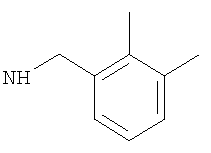
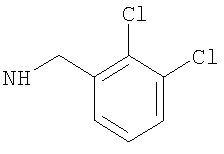
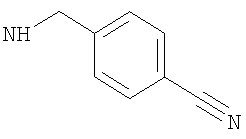
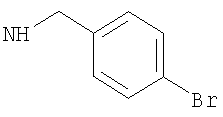
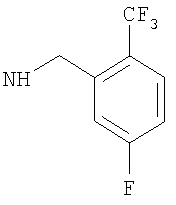
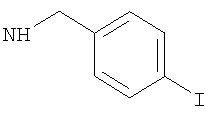
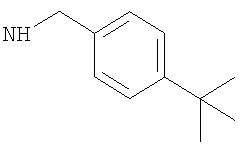
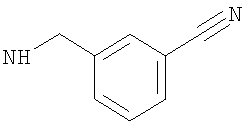
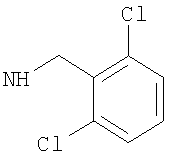
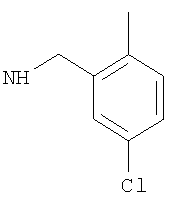
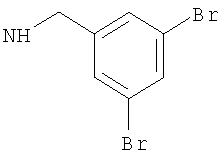
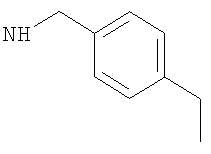
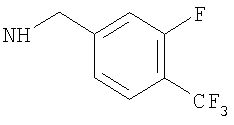
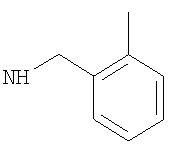
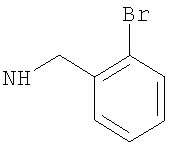
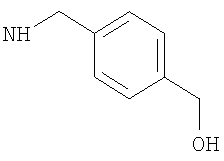
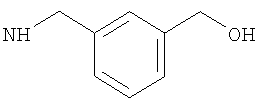
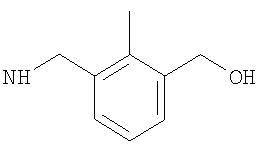
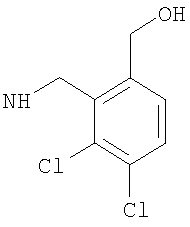
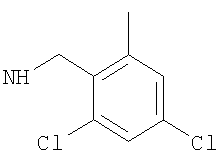
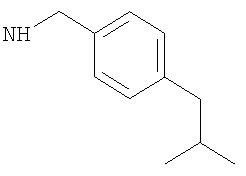
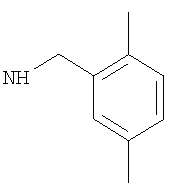
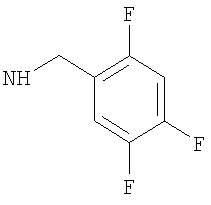
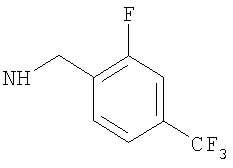
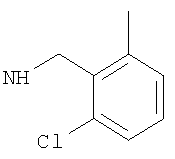
Пример 518: N-[(3,4-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид; также известен как N-(3,4-Диметилбензил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
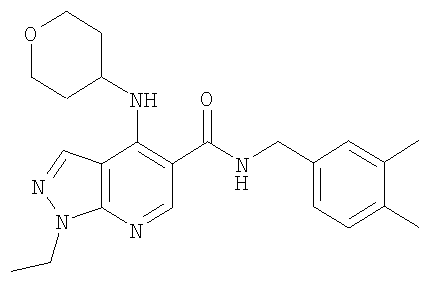
Альтернативный способ получения Примера 518 приведен ниже.
К раствору Промежуточного соединения 33 (3,5 г, 12,07 ммоль) в DMF (500 мл) добавляли HATU (4,5 г, 12,07 ммоль) и эту смесь перемешивали при комнатной температуре в течение 30 мин. Добавляли 3,4-диметилбензиламин (1,63 г, 12,07 ммоль, может быть получен от Matrix Scientific, Columbia, USA или способом, описанным в Chem. Ber., 1969, 102, 2770), а затем DIPEA (4,5 мл, 26,55 ммоль) и раствор перемешивали при комнатной температуре в течение 16 часов. Растворитель удаляли при пониженном давлении и остаток распределяли между насыщенным водным NaHCO3 (200 мл) и этилацетатом (250 мл), водную фазу повторно экстрагировали этилацетатом (2×200 мл), органические экстракты объединяли, сушили (Na2SO4) и выпаривали. Полученное в результате вязкое масло перекристаллизовали из горячего этилацетата (приблизительно 100 мл) с получением соединения, указанного в заголовке, в виде белого кристаллического твердого вещества (3,36 г, 80%). LCMS показала МН+=408; TRET=3,06 мин. δн (D6-ДМСО) 1.36 (3Н, t), 1.51 (2Н, m), 2.00 (2H, m), 2.18 (3H, s), 2.19 (3H, s), 2.50 (2H, m), 3.61 (2H, m), 3.83 (2H, m), 4.17 (1H, m), 4.36 (2H, q), 4.38 (2H, d), 7.02-7.09 (3H, m), 8.17 (1H, s), 8.62 (1H, s), 8.93 (1H, t), 9.96 (1H, d). δс (D6-ДМСО) 14.65, 18.91, 19.33, 32.81, 41.06, 41.86, 48.57, 64.94, 101.69, 102.18, 124.44, 128.22, 129.24, 133.28, 134.31, 135.78, 136.91, 149.26, 149.59, 151.36, 168.81.
Пример 518А: N-[(3,4-Диметилсренил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамида гидрохлорид; также известен как N-(3,4-диметилбензил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамида гидрохлорид
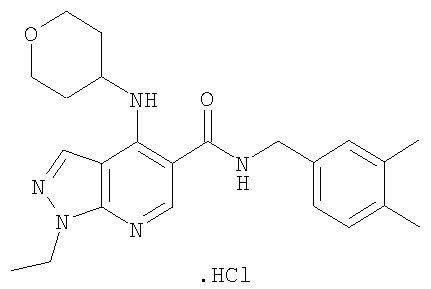
Раствор Примера 518 (1,3 г, 3,19 ммоль) в безводном тетрагидрофуране (200 мл) обрабатывали раствором хлористого водорода в диоксане (4 M, 8 мл) и эту смесь перемешивали при температуре окружающей среды в течение 16 часов. Полученный в результате белый осадок собирали фильтрацией и перекристаллизовали из горячего метанола (100 мл) с получением соединения, указанного в заголовке Примера 518А, в виде белого кристаллического твердого вещества (1,12 г, 79%).
LCMS показала MH+=408; TRET=3,21 мин. δн (D6-ДМСО) 1.39 (3H, t), 1.59 (2H, m), 2.01 (2H, m), 2.19 (3H, s), 2.20 (3H, s), 3.64 (2H, t), 3.83 (2H, m), 4.28 (1H, m), 4.40 (2H, d), 4.50 (2H, q), 7.04-7.11 (3H, m), 9.40 (1H, s (br)), 10.72 (1H, s (br)).
Пример 650: 4-[({[1-этил-4-(тетрагидро-2N-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)метил]бензойной кислоты натриевая соль
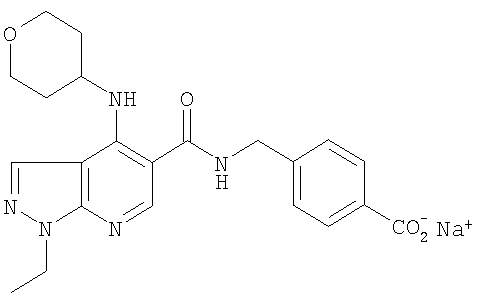
2 М Раствор гидроксида натрия (98 мкл, 0,196 ммоль) добавляли к перемешиваемому раствору Примера 593 (22 мг, 0,049 ммоль) в метаноле (104 мкл) и воде (6 мкл). Полученный в результате раствор перемешивали при 50°С в атмосфере азота. Через 16ч реакционную смесь разбавляли водой (0,5 мл) и доводили до рН 4 уксусной кислотой. Смесь экстрагировали этилацетатом (2×0,5 мл) и объединенные экстракты сушили (Na2SO4) и выпаривали в вакууме с получением твердого вещества (15 мг). Это твердое вещество суспендировали в воде и обрабатывали 2 М раствором гидроксида натрия (15 мкл). В результате выпаривания растворителя в вакууме получали Пример 650 в виде белого твердого вещества (11 мг). LCMS показала МН+=425; TRET=2,69 мин.
Пример 651: 3-[({[1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-ил]карбонил}амино)метил]бензойная кислота
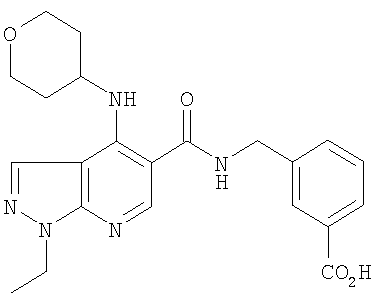
2 М Раствор гидроксида натрия (98 мкл, 0,196 ммоль) добавляли к перемешиваемому раствору Примера 558 (22 мг, 0,049 ммоль) в метаноле (104 мкл) и воде (6 мкл). Полученный в результате раствор перемешивали при 50°С в атмосфере азота. Через 16 ч реакционную смесь разбавляли водой (0,5 мл) и доводили до рН 4 уксусной кислотой. Выпавшее в осадок твердое вещество собирали фильтрацией и сушили в вакууме с получением Примера 651 в виде белого твердого вещества (15 мг). LCMS показала МН+=425; TRET=2,72 мин.
Пример 652: Этил-1-этил-4-{[4-(гидроксиимино)циклогексил]амино}-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
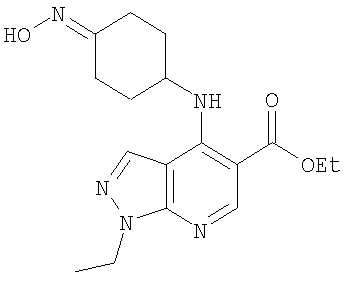
Смесь Примера 205 (200 мг), гидрохлорида гидроксиламина (50 мг) и безводного карбоната калия (420 мг) в ацетонитриле (10 мл) перемешивали и нагревали с обратным холодильником в течение 17 часов. Раствор охлаждали и концентрировали в вакууме. Остаток распределяли между EtOAc и водой. Органическую фазу отделяли, сушили над Na2SO4 и концентрировали в вакууме с получением Примера 652 в виде белого порошка (203 мг). LCMS показала МН+=346; ТRET=2,84 мин.
Пример 653: 1-Этил-4-{[4-(гидроксиимино)циклогексил]амино}-N-{[4-(метилокси)фенил]метил}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
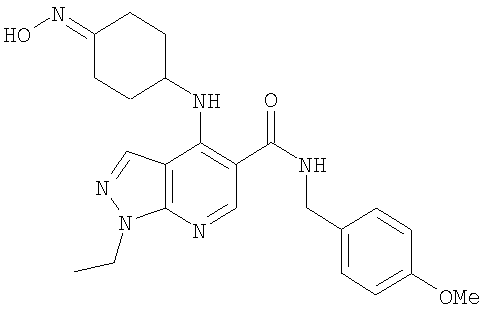
Смесь Примера 263 (217 мг), гидрохлорида гидроксиламина (43 мг) и безводного карбоната калия (355 мг) в ацетонитриле (10 мл) перемешивали и нагревали с обратным холодильником в течение 17 часов. Раствор охлаждали и концентрировали в вакууме. Остаток распределяли между EtOAc и водой. Органическую фазу отделяли, сушили над Na2SO4 и концентрировали в вакууме с получением Примера 653 в виде желтого твердого вещества (186 мг). LCMS показала MH+=437; TRET=2,82 мин. δн (CDCl3) 1.49 (3H, t), 1.80 (2H, m), 2.2-2.4 (4H, m), 2.54 (1H, m), 3.13 (1H, dt), 3.81 (3H, s), 4.13 (1H, m), 4.46 (2H, q), 4.54 (2Н, d), 6.28 (1H, t), 6.90+7.28 (4H, AA'BB'), 7.98 (1H, s), 8.36 (1H, s), 9.84 (1H, d). Гидроксильный протон не виден.
Приведенные ниже примеры получали аналогичным способом, например, используя такое же или аналогичное число молей реагентов и такие же или аналогичные объемы растворителей:
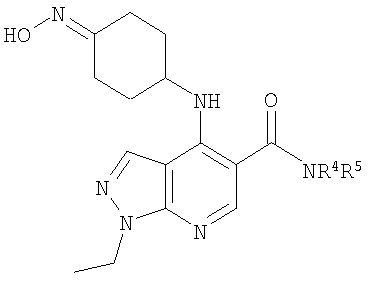
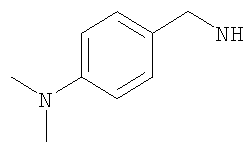
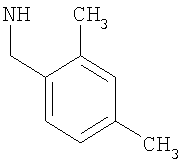
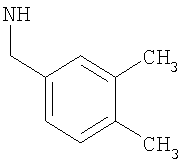
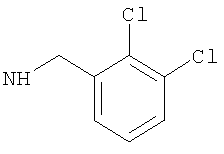
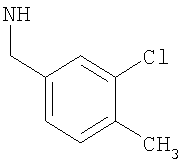
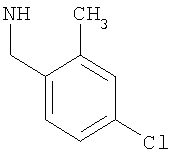
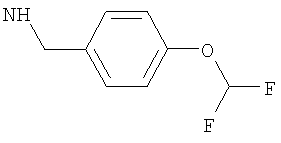
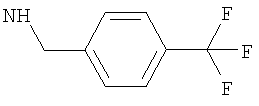
Альтернативное получение Примера 681 см. ниже.
Пример 655: 1-Этил-4-({4-1(этилокси)имино]циклогексил}амино)-N-{[4-(метилокси)фенил]метил}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
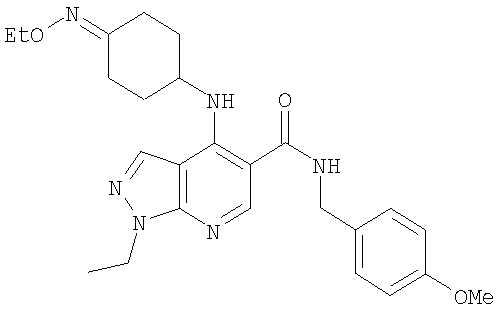
Смесь Примера 263 (25 мг), гидрохлорида этоксиамина (R26ONH2, где R26=Et, 20 мг) и диизопропилэтиламина (30 мг) в ацетонитриле (3 мл) перемешивали и нагревали с обратным холодильником в течение 3,25 часов. Раствор охлаждали и концентрировали в вакууме. Остаток наносили на SPE картридж (5 г). Картридж элюировали EtOAc. Фракции, содержащие нужный продукт, концентрировали в вакууме с получением Примера 655 в виде бесцветной смолы (20 мг). LCMS показала МН+=465; TRET=3,28 мин.
Приведенные ниже примеры получали аналогичным способом, например, используя такое же или аналогичное число молей реагентов и такие же или аналогичные объемы растворителей:
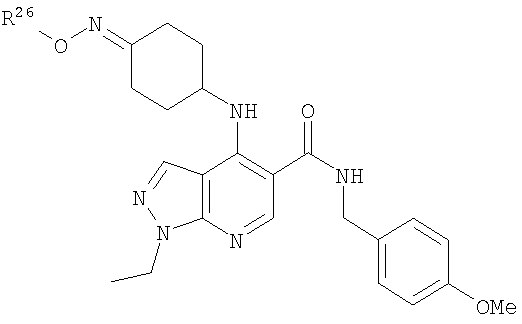
Пример 658: 1-Этил-N-{[4-(метилокси)фенил]метил}-4-[(7-оксогексагидро-1Н-азепин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
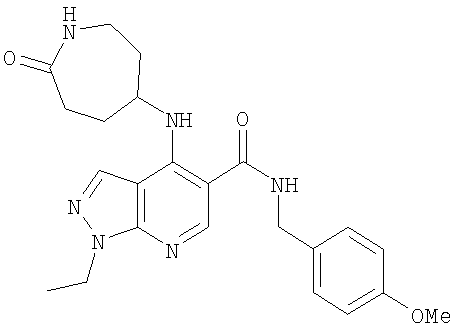
Суспензию цианурхлорида (2,4,6-трихлор-1,3,5-триазина) (150 мг) в DMF (0,2 мл) перемешивали в течение 30 минут при комнатной температуре. Эту суспензию разбавляли до 7 мл DMF при перемешивании. Порцию 1,0 мл полученной в результате суспензии отбирали и добавляли к Примеру 653 (52 мг). Полученный в результате раствор перемешивали в течение 90 часов при комнатной температуре, затем концентрировали в вакууме. Остаток распределяли между EtOAc и водой. Органическую фазу отделяли и промывали последовательно насыщенным карбонатом натрия, 10%-ной мас./об. лимонной кислотой и насыщенным рассолом, сушили над Na2SO4 и концентрировали в вакууме. Остаток наносили на SPE картридж (2 г). Картридж элюировали последовательно EtOAc:циклогексаном (1:1), EtOAc, а затем смесью (100:8:1) дихлорметана, этанола и аммиака. Фракции, содержащие нужный продукт (элюируемые аммиачным раствором), концентрировали в вакууме с получением Примера 658 в виде бесцветного масла (11 мг). LCMS показала МН+=437; TRET=2,50 мин.
Пример 659: Этил-1-этил-4-[(7-оксогексагидро-1Н-азепин-4-ил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
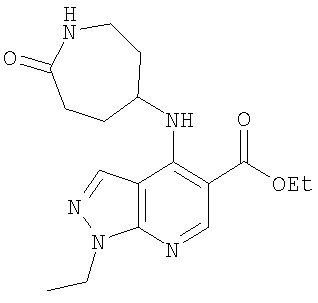
Пример 659 получали из Примера 652, используя методику, идентичную использованной для Примера 658. LCMS показала МН+=346; TRET=2,56 мин.
Пример 660: 4-{[цис-4-(Бутиламино)циклогексил]амино}-N-(2,3-дигидро-1Н-инден-2-ил)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид

Раствор Примера 258 (25 мг), бутиральдегида (5 мг) и ледяной уксусной кислоты (30 мг) в DCM (3 мл) перемешивали в течение 10 мин. Добавляли триацетоксиборгидрид натрия (21 мг). Эту реакционную смесь перемешивали в течение 1,5 часов. Бикарбонат натрия (1,0 молярный, 3 мл) добавляли по каплям при перемешивании. После перемешивания в течение 5 мин фазы разделяли. Органическую фазу сушили над Na2SO4 и наносили на SPE картридж (5 г). Картридж элюировали смесью (100:8:1) дихлорметана, этанола и аммиака. Фракции, содержащие нужный продукт, концентрировали в вакууме с получением Примера 660 в виде аморфного, кремового твердого вещества (19 мг). LCMS показала МН+=346; TRET=2,56 мин.
Примеры 661-664
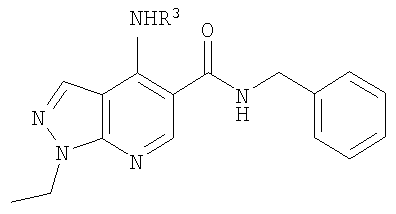
Общая методика
Промежуточное соединение 17 (0,16 ммоль) в ацетонитриле (1 мл) обрабатывали амином R3NH2 (0,8 ммоль) в ацетонитриле (1 мл) и N,N-диизопропилэтиламином (0,8 ммоль). Смесь нагревали при 50°С в течение 18 ч, затем концентрировали в вакууме. Остаток разбавляли водой (3 мл) и экстрагировали дихлорметаном (2×5 мл). Объединенные органические экстракты выпаривали и остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ с получением нужного продукта, содержащего муравьиную кислоту. Это вещество растворяли в смеси хлороформ - метанол (10/1, 5,5 мл) и промывали 5%-ным раствором гидрокарбоната натрия (1 мл) с получением после выпаривания растворителей чистого продукта.
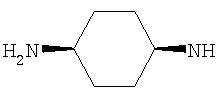
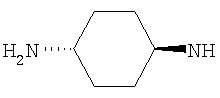
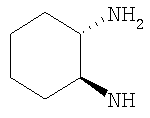
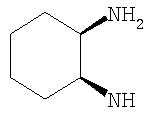
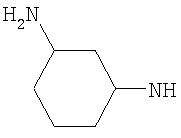
Пример 665: Этил-1-этил-4-{[(1SR,3RS)-3-гидроксициклогексил]амино}-1Н-пиразоло[3,4-b]пиридин-5-карбоксилат
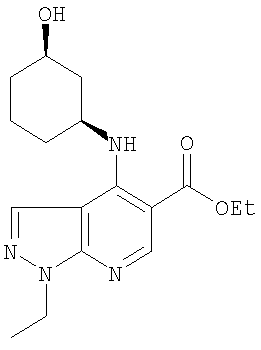
[цис-(3-гидроксициклогекс-1-ил)амино группа, рацемическая]
3-Аминоциклогексанол (0,677 г, 5,9 ммоль, как описано в J. Chem. Soc., Perkin Trans 1, 1994, 537) в ацетонитриле (10 мл) и этаноле (1 мл) добавляли при комнатной температуре к перемешиваемому раствору Промежуточного соединения 1 (1,24 г, 4,9 ммоль) и диизопропилэтиламина (4,26 мл, 24,5 ммоль) в ацетонитриле (25 мл). Полученную в результате смесь перемешивали при 85°С в течение 17 ч. Смесь концентрировали в вакууме и остаток распределяли между DCM (50 мл) и водой (10 мл). Фазы разделяли и органическую фазу сушили (Na2SO4) и выпаривали с получением оранжево-коричневого масла. Это масло очищали Biotage хроматографией (силикагель 100 г), элюируя 30-50%-ным EtOAc в циклогексане, с получением Примера 665 в виде белой пены (0,681 г). LCMS показала МН+=333; TRET=2,76 мин.
Примеры 666-676
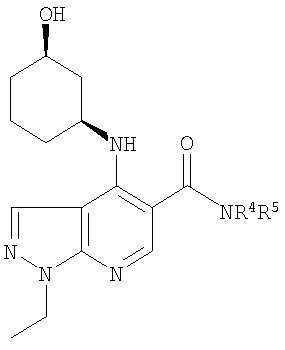
[цис-(3-гидроксициклогекс-1-ил)амино группа, рацемическая]
Общая методика
Смесь Промежуточного соединения 76 (0,1 ммоль), HATU (0,1 ммоль) и DIPEA (0,4 ммоль) в DMF (0,5 мл) встряхивали при комнатной температуре в течение 10 мин. Затем добавляли раствор амина HNR4R5 (0,12 ммоль) в DMF (0,5 мл) и смесь перемешивали в течение нескольких минут до получения раствора. Раствор выдерживали при комнатной температуре в течение 16 часов, затем концентрировали в вакууме. Остаток очищали регулируемой по массе автоматической препаративной ВЭЖХ.
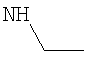
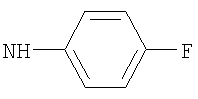
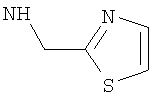
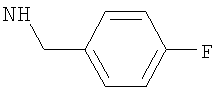
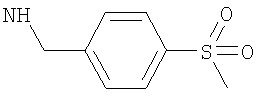
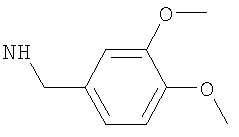
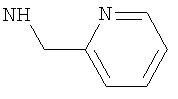
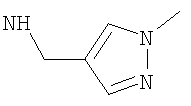
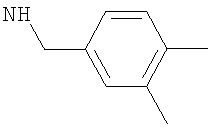
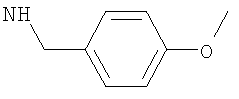
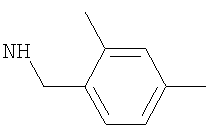
Пример 260 (Альтернативная методика)
N-[(2,4-Диметилфенил)метил]-1-этил-4-[(4-оксоциклогексил)амино]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
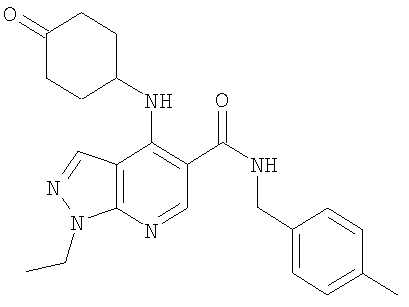
Альтернативная методика получения Примера 260:
Смесь Промежуточного соединения 58 (45 мг), HATU (63 мг) и DIPEA (39 мг) в ацетонитриле (5 мл) перемешивали в течение 10 мин. Затем добавляли раствор 2,4-диметилбензиламина (24 мг) (доступен от Salor; либо ICN Biomedicals; либо Synthesis, 1982, 12, 1036) в ацетонитриле (1 мл). Реакционную смесь перемешивали в течение 18 часов. Раствор концентрировали и остаток распределяли между этилацетатом (25 мл) и 0,5 М бикарбонатом натрия (20 мл). Органическую фазу отделяли, промывали водой (20 мл), сушили над Na2SO4 и концентрировали с получением смолы, которую наносили на SPE картридж (5 г). Картридж элюировали этилацетатом. Фракции, содержащие нужное соединение, объединяли и концентрировали в вакууме с получением Примера 260 (32 мг). LCMS показала MH+=420; TRET=3,16 мин. δн (CDCl3) 1.49 (3H, t), 2.11 (2Н, m), 2.33 (3H, s), 2.35 (3H, s), 2.40 (2H, m), 2.52 (2H, m), 2.61 (2H, m), 4.36 (1H, m), 4.47 (2H, q), 4.55 (2H, d), 6.14 (1H, t), 7.01 + 7.18 (2H, AA'BB'), 7.04 (1H, s), 8.01 (1H, s), 8.36 (1H, s), 9.96 (1H, d).
Приведенные ниже Примеры 677-679 получали аналогично Примеру 260 (приведенная выше альтернативная методика), например, используя такое же или аналогичное число молей реагентов и такие же или аналогичные объемы растворителей:
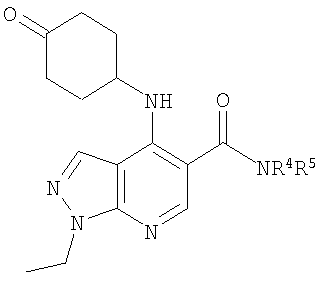
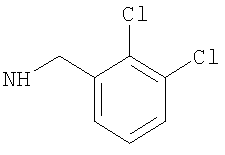
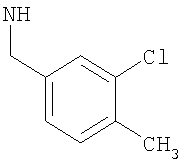
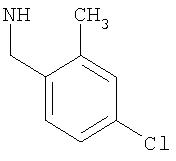
Примеры 680-686 и их получение показаны выше вместе с Примером 653.
Альтернативное получение Примера 681: N-[(3,4-Диметилфенил)метил]-1-этил-4-{[4-(гидроксиимино)циклогексил]амино}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид
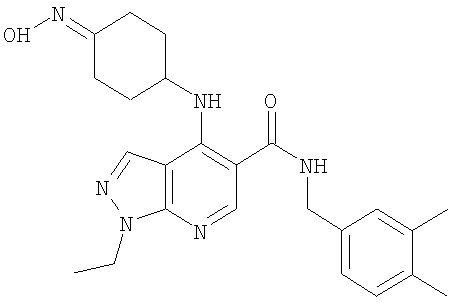
Смесь Примера 261 (35 мг), гидрохлорида гидроксиламина (10 мг) и диизопропилэтиламина (26 мг) в ацетонитриле (4 мл) перемешивали и нагревали с обратным холодильником в течение 2,5 часов. Раствор охлаждали и концентрировали в вакууме. Остаток распределяли между EtOAc и водой. Органическую фазу отделяли, сушили над Na2SO4 и концентрировали в вакууме. Остаток наносили на SPE картридж (10 г). Картридж элюировали смесью EtOAc:циклогексан (1:1) и затем EtOAc. Фракции, содержащие нужное соединение, объединяли и концентрировали в вакууме с получением Примера 681 в виде белого, аморфного твердого вещества (18 мг). LCMS показала МН+=435; TRET=3,08 мин. δн (CDCl3) 1.49 (3Н, t), 1.79 (2Н, m), 2.24 (6H, s), 2.19-2.38 (4H, m), 2.56 (2Н, dt), 4.13 (1H, m), 4.46 (2Н, q), 4.53 (2Н, d), 6.36 (1H, t), 7.09 (2Н, t), 7.12 (1H, s), 7.98 (1H, s), 8.38 (1H, s), 9.79 (1H, d). Гидроксильный протон не виден.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРАЗОЛО[3,4-b]ПИРИДИНОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗ | 2003 |
|
RU2348633C2 |
| ПРОИЗВОДНЫЕ ТИПА АЗАИНДАЗОЛА ИЛИ ДИАЗАИНДАЗОЛА ДЛЯ ЛЕЧЕНИЯ БОЛИ | 2013 |
|
RU2640046C2 |
| ПРОИЗВОДНОЕ ТИЕНОПИРАЗОЛА, ИМЕЮЩЕЕ ИНГИБИРУЮЩУЮ ФОСФОДИЭСТЕРАЗУ 7 (PDE 7) АКТИВНОСТЬ | 2005 |
|
RU2376309C2 |
| ПРОИЗВОДНЫЕ АЗАИНДАЗОЛА ИЛИ ДИАЗАИНДАЗОЛА В КАЧЕСТВЕ МЕДИКАМЕНТА | 2012 |
|
RU2600976C2 |
| ИНГИБИТОРЫ СЕРИН/ТРЕОНИН КИНАЗЫ ДЛЯ ЛЕЧЕНИЯ ГИПЕРПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2644947C2 |
| ИНГИБИТОРЫ СЕРИН/ТРЕОНИНОВЫХ КИНАЗ | 2013 |
|
RU2650501C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2827714C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ И ОЧИСТКИ ГЕТЕРОАРИЛЬНЫХ СОЕДИНЕНИЙ | 2010 |
|
RU2557242C2 |
| АМИНОТРИАЗОЛОПИРИДИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2009 |
|
RU2552642C2 |
| СОЕДИНЕНИЯ ПИРИДАЗИНАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ СЕЛЕЗЕНКИ (SYK) | 2013 |
|
RU2627661C2 |
Данное изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, где значения радикалов R1, R2, n1 и n2, Y и X представлены в описании, R3 представляет собой гетероциклическую группу подформулы (bb) (указанной ниже). Данные соединения являются ингибиторами фосфодиэстеразы (PDE), в частности ингибиторами PDE4. Также предложено получение фармацевтических композиций, содержащих в качестве активного ингредиента соединение формулы (I) или его фармацевтически приемлемой соли, и их применение в изготовлении лекарства для лечения и/или профилактики воспалительного и/или аллергического заболевания у млекопитающего, такого как человек, например астмы, хронической обструктивной болезни легких (COPD), атопического дерматита, аллергического ринита, ревматоидного артрита, рассеянного склероза, болезни Альцгеймера, депрессии или боли у млекопитающего, такого как человек. 3 н. и 17 з.п. ф-лы.
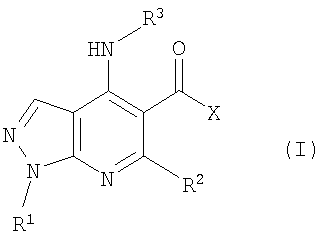
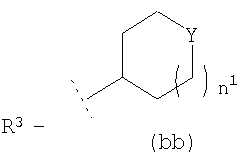
1. Соединение формулы (I) или его фармацевтически приемлемая соль

где R1 представляет собой этил;
R2 представляет собой атом водорода (Н);
R3 представляет собой гетероциклическую группу подформулы (bb);
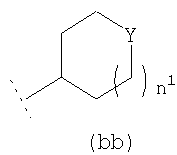
где n1 равно 1; и где Y представляет собой О, S, SO2 или NR10; где R10 представляет собой атом водорода (Н), C(O)NH2, С(О)-С1-2алкил или С(О)-С1фторалкил;
и X представляет собой NR4R5,
где R4 представляет собой атом водорода (Н); и
R5 представляет собой (4-С1-3алкил-фенил)метил; (4-С1фторалкил-фенил)метил;
(4-С1-2алкокси-фенил)метил; (4-С1фторалкокси-фенил)метил; (3,4-диметил-фенил)метил; (2,4-диметил-фенил)метил; (3,5-диметил-фенил)метил; (2,3-диметил-фенил)метил; (2,5-диметил-фенил)метил; (4-метил-3-хлор-фенил)метил; (3-метил-4-хлор-фенил)метил; (2-метил-4-хлор-фенил)метил; (2-хлор-4-фторфенил)метил; (2,4-дифтор-фенил)метил; (4-бром-2-фторфенил)метил; (4-хлор-2-фторфенил)метил; (3,4-дихлор-фенил)метил; (2,4-дихлор-фенил)метил; (2,6-дихлор-фенил)метил; (2,3-дихлор-фенил)метил; (2,4-дихлор-6-метил-фенил)метил или [2,3-дихлор-6-(гидроксиметил)-фенил]метил.
2. Соединение или его фармацевтически приемлемая соль по п.1, где R10 представляет собой атом водорода (Н) или С(О)метил.
3. Соединение или его фармацевтически приемлемая соль по п.1, где Y представляет собой О или NR10.
4. Соединение или его фармацевтически приемлемая соль по п.1, где R3 представляет собой тетрагидро-2Н-пиран-4-ил.
5. Соединение или его фармацевтически приемлемая соль по п.1, которое представляет собой:
1-Этил-N-(4-метоксибензил)-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-4-(тетрагидро-2Н-пиран-4-иламино)-N-[4-(трифторметил)бензил]-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетил-4-пиперидинил)амино]-N-[(3,4-дихлорфенил)метил]-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетил-4-пиперидинил)амино]-1-этил-N-{[4-(трифторметил)фенил]метил}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетил-4-пиперидинил)амино]-1-этил-N-{[4-(метилокси)фенил]метил}-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетил-4-пиперидинил)амино]-N-[(2,4-дихлорфенил)метил]-1-этил-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
4-[(1-Ацетил-4-пиперидинил)амино]-N-({4-[(дифторметил)окси]фенил}метил)-1-этил-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(3-Хлор-4-метилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(4-Хлор-2-метилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b] пиридин-5-карбоксамид,
N-[(3,4-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[2-(4-метилфенил)этил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-{[4-(1-метилэтил)фенил]метил}-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,4-Дихлорфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,4-Дифторфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2-Хлор-4-фторфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,4-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(3,4-Дихлорфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-({4-[(Дифторметил)окси]фенил}метил)-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(4-Хлор-2-фторфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(4-Бром-2-фторфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(3,5-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,3-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,3-Дихлорфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,6-Дихлорфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
1-Этил-N-[(4-этилфенил)метил]-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-{[2,3-Дихлор-6-(гидроксиметил)фенил]метил}-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1H-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,4-Дихлор-6-метилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
N-[(2,5-Диметилфенил)метил]-1-этил-4-(тетрагидро-2Н-пиран-4-иламино)-1Н-пиразоло[3,4-b]пиридин-5-карбоксамид,
6. Соединение или фармацевтически приемлемая соль по п.1, в форме с уменьшенным размером частиц, где размер частиц (значение D50) соединения или соли с уменьшенным размером частиц составляет от приблизительно 0,5 до приблизительно 10 мкм.
7. Соединение или фармацевтически приемлемая соль по любому из пп.1-6 для применения в качестве ингибитора PDE4 у млекопитающего, такого как человек.
8. Соединение или фармацевтически приемлемая соль по любому из пп.1-6 для применения в лечении и/или профилактике астмы, хронической обструктивной болезни легких (COPD), атопического дерматита, аллергического ринита, ревматоидного артрита, рассеянного склероза, болезни Альцгеймера, депрессии или боли у млекопитающего, такого как человек.
9. Соединение или фармацевтически приемлемая соль по п.8 для применения в лечении и/или профилактике хронической обструктивной болезни легких (COPD), астмы, ревматоидного артрита, аллергического ринита или атопического дерматита у млекопитающего, такого как человек.
10. Соединение или фармацевтически приемлемая соль по п.8 для применения в лечении и/или профилактике атопического дерматита у человека.
11. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении PDE4, содержащая в эффективном количестве соединение формулы (I), как определено в любом из пп.1-6, или его фармацевтически приемлемую соль, и один или более чем один фармацевтически приемлемый носитель и/или эксципиент.
12. Фармацевтическая композиция по п.11, которая пригодна и/или адаптирована для ингаляционного введения, в которой соединение или соль находится в форме с уменьшенным размером частиц, где размер частиц (значение D50) соединения или его фармацевтически приемлемой соли с уменьшенным размером частиц составляет от приблизительно 0,5 до приблизительно 10 мкм.
13. Фармацевтическая композиция по п.11 для лечения и/или профилактики астмы, хронической обструктивной болезни легких (COPD), атопического дерматита, аллергического ринита, ревматоидного артрита, рассеянного склероза, болезни Альцгеймера, депрессии или боли у млекопитающего, такого как человек.
14. Фармацевтическая композиция по п.11 для применения в лечении и/или профилактике хронической обструктивной болезни легких (COPD), астмы, ревматоидного артрита, аллергического ринита или атопического дерматита у млекопитающего, такого как человек.
15. Применение соединения формулы (I), как определено в любом из пп.1-6, или его фармацевтически приемлемой соли в изготовлении лекарства для лечения и/или профилактики астмы, хронической обструктивной болезни легких (COPD), атопического дерматита, аллергического ринита, ревматоидного артрита, рассеянного склероза, болезни Альцгеймера, депрессии или боли у млекопитающего, такого как человек.
16. Применение по п.15, где лекарство предназначено для лечения и/или профилактики хронической обструктивной болезни легких (COPD), астмы, ревматоидного артрита, аллергического ринита или атопического дерматита у млекопитающего, такого как человек.
17. Применение по п.15, где лекарство предназначено для лечения и/или профилактики хронической обструктивной болезни легких (COPD) у человека.
18. Применение по п.15, где лекарство предназначено для лечения и/или профилактики атопического дерматита у человека.
19. Применение по п.15, где лекарство предназначено для лечения и/или профилактики болезни Альцгеймера или депрессии у человека.
20. Применение по п.15, где лекарство предназначено для перорального или ингаляционного введения и представляет собой фармацевтическую композицию, как она определена в п.11.
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Daly J.W | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Medicinal Chemistry Research, 1994, vol.4, N5, p.293-306 | |||
| JP 2002020386 A, 23.01.2002 | |||
| ПИРАЗОЛО- И ПИРРОЛОПИРИДИНЫ | 1995 |
|
RU2135498C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛО(3,4-B)ПИРИДИНА | 1989 |
|
RU2022964C1 |
Авторы
Даты
2009-06-10—Публикация
2003-09-12—Подача