[0001] ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к соединениям, которые ингибируют серин/треонин киназы и могут использоваться для лечения гиперпролиферативных и неопластических заболеваний посредством ингибирования путей сигнальной трансдукции которые обычно демонстрируют чрезмерную активность или гиперэкспрессию в опухолевой ткани. Данные соединения представляют собой селективные ингибиторы ERK (киназы, регулируемой внеклеточными сигналами). Настоящее изобретение дополнительно относится к способам лечения рака или гиперпролиферативных заболеваний соединениями в пределах настоящего изобретения.
[0003] УРОВЕНЬ ТЕХНИКИ
[0004] Процессы, вовлеченные в рост, прогрессию и метастазирование опухоли, опосредуются сигнальными путями, которые активируются в опухолевых клетках. Пути ERK играют центральную роль в регулировании роста клеток млекопитающих посредством перенаправления внеклеточных сигналов от связанной с лигандом рецепторной тирозинкиназы (RTK) на поверхности клетки, такой как рецепторная тирозинкиназа семейства erbB, фактора роста тромбоцитов (PDGF), фактора роста фибробластов (FGF) и фактора роста эндотелия сосудов (VEGF). Активация RTK индуцирует каскад событий фосфорилирования, который начинается с активации Ras. Активация Ras ведет к рекрутингу и активации Raf, серин-треонин киназы. Далее активированный Raf фосфорилирует и активирует сигнальный путь MEK1/2, который затем фосфорилирует и активирует ERK1/2. Активированный ERK1/2 фосфорилирует некоторые мишени, лежащие ниже в сигнальном пути и вовлеченные во множество клеточных событий, включая цитоскелетные изменения и активацию транскрипции. Сигнальный путь ERK/MAPK представляет собой один из наиболее важных для клеточной пролиферации, и считается, что сигнальный путь ERK/MAPK часто активируется во многих опухолях. Гены Ras, регулирующие сигнальный каскад ERK1/2, являются мутантными при некоторых формах рака, включая колоректальный рак, меланому, опухоли молочной железы и поджелудочной железы. Высокая активность Ras сопровождается повышенной активностью ERK во многих опухолях человека. Кроме того, мутации BRAF, серин-треонин киназы семейства Raf, ассоциируются с повышенной активностью киназы. Мутации в BRAF идентифицированы при меланоме (60%), раке щитовидной железы (более 40%) и колоректальном раке. Такие наблюдения указывают на то, что сигнальный путь ERK1/2 представляется перспективным для противоопухолевой терапии при широком спектре опухолей у человека (М. Hohno and J. Pouyssegur, Prog. в Cell Cycle Res. 2003 5:219).
[0005] Таким образом, низкомолекулярные ингибиторы активности ERK (например, активности ERK1 и/или ERK2) могут быть полезными для лечения широкого спектра типов рака, таких как, например, меланома, рак поджелудочной железы, рак щитовидной железы, колоректальный рак, рак легкого, рак молочной железы и рак яичника. Такой вклад обеспечивается настоящим изобретением.
[0006] СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] В одном аспекте настоящего изобретения предлагается соединение в соответствии с формулой I

[0008] где: Х представляет собой СН или N;
[0009] Z представляет собой (i) NH(CH2)nCHR1Ar, где n равно 0 или 1 или (ii) 1-алкил-4-арил-пирролидин-3-иламин или 4-арил-пирролидин-3-иламин, где алкил представляет собой C1-3 алкил, необязательно замещенный фенильным кольцом, и арильный заместитель на пирролидине представляет собой необязательно замещенный фенил;
[0010] R1 представляет собой (а) водород, (б) C1-С6 алкил, необязательно замещенный одной или более гидроксильной или C1-6 алкокси-группами, (в) C1-С6 алкенил, необязательно замещенный одной или более гидроксильной или C1-6 алкокси-группами, (г) C1-С6 алкинил с одной или более гидроксильной или C1-6 алкокси-группами, (д) С3-С6 циклоалкил, необязательно замещенный одной или более группами, выбранными из группы, содержащей гидроксил, C1-6 алкокси, C1-6 алкила и галогена; (е) 4-6-членный гетероцикл, содержащий 1 или 2 гетероатома, выбранных из N или О, где гетероцикл необязательно замещен одной или более групп, выбранных из группы, состоящей из гидроксила, C1-6 алкокси, C1-6 алкила и галогена; или (ж) 5-6-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из N или О, где гетероарил необязательно замещен одной или более групп, выбранной из группы, состоящей из гидроксила, C1-6 алкокси, C1-6 алкила и галогена;
[0011] Ar представляет собой фенил, пиридинил или индолил, необязательно замещенный 1-3 группами, независимо выбранными из (а) C1-6 алкила, (б) C1-6 галогеналкила, (в) C1-6 алкокси, (г) С3-6 циклоалкила, (д) галогена, (е) C1-6 галогеналкокси, (ж) C1-6 алкилтио, (е) циано, (ж) бензила, (з) фенокси, где указанный бензил и фенокси необязательно замещены галогеном, C1-6 алкилом или C1-6 алкокси, (и) 4-метилпиперазин-1-ила или (й) гетероарила, выбранного из группы, состоящей из пиридинила, пиразинила, пиридазинила, пиримидинила и пиразолила, причем указанный гетероарил необязательно замещен одним или более C1-10 алкилом;
[0012] R2 выбран из группы, состоящей из (а) C1-10 алкила, (б) C1-10 гидроксиалкила, (в) C1-6 галогеналкила, (г) гетероциклила, где указанный гетероцикл выбран из группы, состоящей из тетрагидропиранила, тетрагидрофуранила, оксетанила, 2-окса-бицикло[2,2,1]гептан-5-ила, пиперидинила и пирролидинила, причем указанный гетероциклил или гетероциклил-C1-6 алкил необязательно замещен 1-3 группами, независимо выбранными из группы, состоящей из C1-6 алкила, C1-6 галогеналкила, С1-4 ацилокси-С1-2 алкила, галогена, гидроксила, фенила, C1-3 гидроксиалкила и оксо, (д) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила, причем указанный гетероарил необязательно замещен 1-3 C1-3 алкильными группами, и (е) С3-7 циклоалкила или С3-7 циклоалкил-C1-6 алкила, где указанный циклоалкил или С3-7 циклоалкил-C1-6 алкил необязательно замещен гидроксилом или галогеном; или
[0013] его стереоизомер, таутомер или фармацевтически приемлемая соль.
[0014] Настоящее изобретение также относится к способу лечения гиперпролиферативного расстройства посредством введения терапевтически эффективного количества соединения в соответствии с формулой I пациенту, который в этом нуждается. Соединение формулы I может быть введено в качестве монотерапии или введено по меньшей мере с еще одним анти-гиперпролиферативным или химиотерапевтическим препаратом.
[0015] Настоящее изобретение также относится к способу ингибирования активности протеинкиназы ERK в клетке, включающему обработку клетки соединением в соответствии с формулой I, в количестве, эффективном для ослабления или устранения активности киназы ERK.
[0016] Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение в соответствии с формулой I и по меньшей мере один фармацевтически приемлемый носитель, разбавитель или вспомогательное вещество.
[0017] ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0018] Элементы, указанные в данном документе в единственном числе, определены здесь как представляющие один или большее количество соответствующих элементов; например, соединение обозначает одно или более соединений или по меньшей мере одно соединение. Таким образом, в настоящем документе термины в единственном числе, «один или более» и «по меньшей мере один» взаимозаменяемы.
[0019] Выражение «как определено выше в настоящем документе» обозначает максимально широкое определение для каждой группы, как раскрыто в Сущности изобретения или наиболее широком пункте Формулы изобретения. Во всех других вариантах реализации, раскрытых ниже, для заместителей, которые могут присутствовать в каждом варианте и которые не определены явно, сохраняется наиболее широкое определение, предложенное в Сущности изобретения.
[0020] В настоящем документе, независимо от использования в переходной фразе или в основной части формулы изобретения, термины «содержит(ат) (включает(ют))» и «содержащий (включающий)» следует трактовать как имеющие неограничивающее значение. Это означает, что термины следует трактовать синонимически с выражениями «содержащий по меньшей мере» или «включающий по меньшей мере». При использовании в контексте способа, термин «включающий» означает, что способ включает по меньшей мере указанные стадии, но может включать дополнительные стадии. При использовании в контексте соединения или композиции, термин «содержащий» обозначает, что соединение или композиция обладает по меньшей мере указанными признаками или содержит по меньшей мере указанные компоненты, но также может обладать дополнительными признаками или содержать дополнительные компоненты.
[0021] Термин «независимо» используют в настоящем документе для указания на то, что переменная применяется в любом отдельном случае, без учета присутствия или отсутствия, переменной, имеющей такое же или другое определение, в пределах одного и того же соединения. Таким образом, в соединении, где R'' встречается дважды и определен как «независимо представляющий собой углерод или азот», оба R'' могут быть углеродом, оба R'' могут быть азотом, или один R'' может быть углеродом, а другой - азотом.
[0022] Если любая переменная (например, R1, R4a, Ar, X1 или Het) встречается более одного раза в любом проиллюстрированном фрагменте или формуле, и раскрытые соединения используются или заявляются в настоящем изобретении, ее определение в каждом случае является независимым от ее определения в каждом другом случае. Кроме того, комбинации заместителей и/или переменных разрешаются только в том случае, если такие комбинации приводят к стабильным соединениям.
[0023] Каждый из символов «*» на конце связи или «••••••», пересекающий связь, обозначает точку присоединения функциональной группы или другого химического фрагмента к остальной части молекулы, частью которой они являются. Таким образом, например:
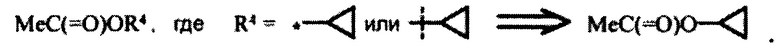
[0024] Связь, направленная в систему кольца (в противоположность соединяющей разные вершины), указывает на то, что связь может быть присоединена к любому из подходящих атомов кольца.
[0025] Термин «необязательный» или «необязательно» в настоящем документе означает, что описанное далее событие или обстоятельство может возникать, но не обязательно возникает, и что описание включает случаи, в которых событие или обстоятельство возникает, и случаи, в которых оно не возникает. Например, «необязательно замещенный» означает, что данный необязательно замещенный фрагмент может содержать водород или заместитель.
[0026] Термин «приблизительно» используют в настоящем документе в значении приблизительно, в области, грубо или около. Если термин «приблизительно» используют в сочетании с числовым интервалом, он меняет интервал посредством расширения границ выше и ниже указанных числовых значений. В общем, термин «приблизительно» используют в настоящем документе для модификации числового значения выше и ниже указанного значения с разбросом 20%.
[0027] В настоящем документе заявление численного интервала для переменной предназначено передавать, что изобретение может практиковаться с переменной, равной любому из значений в пределах указанного интервала. Таким образом, для переменной, которая по существу является дискретной, переменная может равняться любому целому числу в численном интервале, включая конечные точки интервала. Подобным образом, для переменной, которая по существу является непрерывной, переменная может равняться любому действительному числу в численном интервале, включая конечные точки интервала. В качестве примера, переменная, раскрытая как имеющая значения от 0 до 2, может равняться 0, 1 или 2 для переменных, которые по существу являются дискретными, и может равняться 0,0, 0,1, 0,01, 0,001 или любому другому действительному числу для переменных, которые по существу являются непрерывными.
[0028] Соединения формулы I проявляют таутомерию. Таутомерные соединения могут существовать как две или более взаимопревращающихся молекул. Прототропные таутомеры являются результатом миграции ковалентно присоединенного атома водорода между двумя атомами. Таутомеры в общем существуют в равновесии, и попытки выделить отдельные таутомеры обычно дают смесь, химические и физические свойства которой согласуются со смесью соединений. Равновесное состояние зависит от химических особенностей молекулы. Например, во многих алифатических альдегидах и кетонах, таких как ацетальдегид, преобладает кетоформа, тогда как в фенолах преобладает енольная форма. Общие прототропные таутомеры включают кетон/енол  амид/имидную кислоту
амид/имидную кислоту 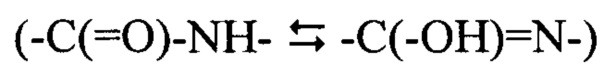 и таутомеры амидина
и таутомеры амидина 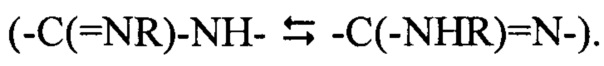 Два последних специфично распространены в гетероарильных и гетероциклических кольцах, и настоящее изобретение охватывает все таутомерные формы соединений.
Два последних специфично распространены в гетероарильных и гетероциклических кольцах, и настоящее изобретение охватывает все таутомерные формы соединений.
[0029] Квалифицированному специалисту будет понятно, что некоторые из соединений формулы I могут содержать один или более хиральных центров и, таким образом, существовать в двух или более стереоизомерных формах. Рацематы указанных изомеров, отдельные изомеры и смеси, обогащенные одним из энантиомеров, а также диастереомеры, если присутствуют два хиральных центра, и смеси, частично обогащенные конкретными диастереомерами, находятся в пределах настоящего изобретения. Настоящее изобретение включает все индивидуальные стереоизомеры (например, энантиомеры), рацемические смеси или частично разделенные смеси соединений формулы I, и если это уместно, их индивидуальные таутомерные формы.
[0030] Соединения формулы I могут содержать основный центр, причем подходящие кислотно-аддитивные соли образуются с кислотами, которые образуют нетоксичные соли. Примеры солей неорганических кислот включают гидрохлорид, гидробромид, гидройодид, хлорид, бромид, йодид, сульфат, бисульфат, нитрат, фосфат и гидрофосфат. Примеры солей органических кислот включают ацетат, фумарат, памоат, аспартат, безилат, карбонат, бикарбонат, камзилат, D- и L-лактат, D- и L-тартрат, эзилат, мезилат, малонат, оротат, глюцептат, метилсульфат, стеарат, глюкуронат, 2-напзилат, тозилат, гибензат, никотинат, изетионат, малат, малеат, цитрат, глюконат, сукцинат, сахарат, бензоат, эзилат и памоат. Обзор подходящих солей см. в Berge et al, J. Pharm. Sci., 1977 66:1-19 и G.S. Paulekuhn et al. J. Med. Chem. 2007 50:6665.
[0031] Определения, раскрытые в настоящем документе, могут применяться для образования химически релевантных комбинаций, таких как «гетероалкиларил», «галогеналкилгетероарил», «арилалкилгетероциклил», «алкилкарбонил», «алкоксиалкил» и т.п. Если термин «алкил» используется в качестве суффикса после другого термина, как в «фенилалкиле» или «гидроксиалкиле», он предназначен обозначать алкильную группу, как раскрыто выше, замещенную одним или двумя заместителями, выбранными из другой, конкретно указанной группы. Таким образом, например, «фенилалкил» обозначает алкильную группу, которая содержит от 1 до 2 фенильных заместителей и, таким образом, включает бензил и фенилэтил. «Алкиламиноалкил» представляет собой алкильную группу, которая содержит от 1 до 2 алкиламино заместителей. «Гидроксиалкил» включает 2-гидроксиэтил, 2-гидроксипропил, 1-(гидроксиметил)-2-метилпропил, 2-гидроксибутил, 2,3-дигидроксибутил, 2-(гидроксиметил), 3-гидроксипропил и т.д. Соответственно, в настоящем документе термин «гидроксиалкил» используется для определения подмножества гетероалкильных групп, определенных ниже. Термин -(ар)алкил обозначает незамещенный алкил или аралкильную группу. Термин (гетеро)арил или (гет)арил обозначает фрагмент, который является арилом или гетероарильной группой.
[0032] Термин «алкил» в настоящем документе, отдельно или в сочетании с другими группами, обозначает одновалентный остаток насыщенного углеводорода с неразветвленной или разветвленной цепью, содержащей от 1 до 10 атомов углерода. Термин «низший алкил» обозначает углеводородный остаток с неразветвленной или разветвленной цепью, содержащей от 1 до 6 атомов углерода. «C1-6 алкил» в настоящем документе обозначает алкил, состоящий из 1-6 атомов углерода. Примеры алкильных групп включают, без ограничения, метил, этил, пропил, изо-пропил, н-бутил, изо-бутил, трет-бутил, неопентил, гексил и октил.
[0033] Термин «алкенил» в настоящем документе обозначает радикал незамещенной углеводородной цепи, содержащий от 2 до 10 атомов углерода и 1 или 2 олефиновые двойные связи. «С2-10 алкенил» в настоящем документе обозначает алкенил, состоящий из 2-10 атомов углерода. Примерами являются винил, 1-пропенил, 2-пропенил (аллил) или 2-бутенил (кротил).
[0034] Термин «алкинил» в настоящем документе обозначает радикал неразветвленной или разветвленной углеводородной цепи, содержащий от 2 до 10 атомов углерода и 1 или, если это возможно, 2 тройные связи. «С2-10 алкенил» в настоящем документе обозначает алкенил, состоящий из 2-10 атомов углерода. Примерами являются этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил или 3-бутинил.
[0035] Термин «циклоалкил» обозначает одновалентную насыщенную моноциклическую или бициклическую углеводородную группу, содержащую 3-10 атомов углерода в кольце. Слитые циклоалкильные группы в общем могут содержать 1 (т.е. спироциклическая), 2 (т.е. бициклическая) или более (т.е. полициклическая) атомов углерода. Конкретные циклоалкильные группы являются моноциклическими. «С3-7 циклоалкил» в настоящем документе обозначает циклоалкил, состоящий из 3-7 атомов углерода в карбоциклическом кольце. Примерами моноциклического циклоалкила являются циклопропил, циклобутанил, циклопентил, циклогексил или циклогептил. Примерами бициклического циклоалкила являются бицикло[2,2,1]гептанил или бицикло[2,2,2]октанил.
[0036] Термин «циклоалкилалкил» в настоящем документе обозначает радикал R'R''-, где R' представляет собой циклоалкильный радикал, и R'' представляет собой алкиленовый радикал, как определено в настоящем документе, с пониманием того, что точка присоединения циклоалкилалкильного фрагмента будет находиться на алкиленовом радикале. Примеры циклоалкилалкильных радикалов включают, без ограничения, циклопропилметил, циклогексилметил, циклопентилэтил. С3-7 циклоалкил-C1-3 алкил обозначает радикал R'R'', где R' представляет собой С3-7 циклоалкил, и R'' представляет собой C1-3 алкилен, как определено в настоящем документе.
[0037] Термин «алкилен» в настоящем документе обозначает двухвалентный насыщенный линейный углеводородный радикал, содержащий 1-10 атомов углерода (например, (СН2)n) или разветвленный насыщенный двухвалентный углеводородный радикал, содержащий 2-10 атомов углерода (например, -СНМе- или -СН2СН(i-Pr)СН2-), если не указано иное. «С0-4 Алкилен» обозначает линейный или разветвленный насыщенный двухвалентный углеводородный радикал, содержащий 1-4 атома углерода или, в случае С0, алкиленовый радикал опущен. «(СН2)0-4» обозначает линейный насыщенный двухвалентный углеводородный радикал, содержащий 0-4 атома углерода или, в случае С0, алкиленовый радикал опущен. За исключением случая метилена, открытые валентности алкиленовой группы не присоединены к одному и тому же атому. Примеры алкиленовых радикалов включают, без ограничения, метилен, этилен, пропилен, 2-метил-пропилен, 1,1-диметил-этилен, бутилен, 2-этилбутилен.
[0038] Термин «алкокси» в настоящем документе обозначает -O-алкильную группу, где алкил является таким, как определено выше, например, метокси, этокси, н-пропилокси, изо-пропилокси, н-бутилокси, изо-бутилокси, трет-бутилокси, пентилокси, гексилокси, включая их изомеры. «Низший алкокси» в настоящем документе обозначает алкокси-группу с группой «низшего алкила», как было определено ранее. «C1-10 алкокси» в настоящем документе обозначает -O-алкил, где алкил представляет собой C1-10.
[0039] Термин «галогеналкил» в настоящем документе обозначает алкильную группу, как определено выше, где по меньшей мере один атом водорода заменен галогеном. Примерами являются 1-фторметил, 1-хлорметил, 1-бромметил, 1-йодметил, дифторметил, трифторметил, трихлорметил, 1-фторэтил, 1-хлорэтил, 2-фторэтил, 2-хлорэтил, 2-бромэтил, 2,2-дихлорэтил, 3-бромпропил или 2,2,2-трифторэтил.
[0040] Термин «галогеналкокси» в настоящем документе обозначает группу -OR, где R представляет собой галогеналкил, как определено в настоящем документе. Термин «галогеналкилтио» в настоящем документе обозначает группу -SR, где R представляет собой галогеналкил, как определено в настоящем документе.
[0041] Термин «галоген» или «гало» в настоящем документе обозначает фтор, хлор, бром или йод. В настоящем документе термины «гало», «галоген» и «галогенид» используются взаимозаменяемым образом и обозначают фтор, хлор, бром или йод.
[0042] Термин «алкилтио» или «алкилсульфанил» обозначает группу -S-алкил, где алкил является таким, как определено выше, например, метилтио, этилтио, н-пропилтио, изо-пропилтио, н-бутилтио, гексилтио, включая их изомеры. «Низший алкилтио» в настоящем документе обозначает группу алкилтио, содержащую группу «низшего алкила», как было определено ранее. «C1-10 алкилтио» в настоящем документе обозначает S-алкил, где алкил представляет собой C1-10.
[0043] Термин «ацилокси» в настоящем документе обозначает радикал -OC(O)R, где R представляет собой радикал низшего алкила, как определено в настоящем документе. Примеры радикалов ацилокси включают, без ограничения, ацетокси, пропионилокси. Ацилокси-С1-2 алкил в настоящем документе обозначает радикал R'R''-, где R' представляет собой радикал ацилокси, и R'' представляет собой метиленовый или этиленовый радикал, как определено в настоящем документе, исходя из предположения, что место присоединения ацилокси-С1-2 алкильного фрагмента будет находиться на алкильном радикале.
[0044] Термины «гидроксиалкил» и «алкоксиалкил» в настоящем документе обозначают алкильный радикал, как определено в настоящем документе, где 1-3 атома водорода при различных атомах углерода заменены гидрокси- или алкокси-группами, соответственно. C1-3 алкокси-C1-6 алкильный фрагмент обозначает C1-6 алкильный заместитель, где 1-3 атома водорода заменены C1-3 алкокси, и место присоединения алкокси представляет собой атом кислорода.
[0045] Термины «гетероцикл» и «гетероциклический» охватывают 4-7-членные насыщенные или частично ненасыщенные кольца, содержащие 1, 2 или 3 гетероатома, выбранных из группы, состоящей из О, N, S, S(=O) и S(=O)2. Указанные термины включают бициклические кольца, такие как 2-оксабицикло[2,2,1]гептан. В некоторых случаях, указанные термины могут быть дополнительно и конкретно ограничены, например, «5-6-членный гетероциклический» включает только 5-и 6-членные кольца.
[0046] Термин «гетероциклоалкил» (или «гетероциклилалкил») обозначает радикал формулы R'R'', где R' представляет собой гетероциклический радикал, как определено в настоящем документе, R'' представляет собой алкиленовый радикал, как определено в настоящем документе, и место присоединения гетероциклоалкильного радикала будет находиться на алкиленовом радикале. Примеры гетероциклоалкильных радикалов включают, без ограничения, 1-пиперазинилметил, 2-морфолинометил и т.п.
[0047] Термин «арил» в настоящем документе обозначает одновалентный ароматический карбоциклический радикал, содержащий 6-15 атомов углерода, который состоит из одного индивидуального кольца или одного или более сочлененных колец, где по меньшей мере одно кольцо по своей природе является ароматическим. Арильная группа необязательно может быть замещена одним или более, предпочтительно 1-3 заместителями. Альтернативно, два смежных атома арильного кольца могут быть замещены метилендиокси- или этилендиокси-группой. Примеры арильных радикалов включают фенил, нафтил, инданил, 3,4-метилендиоксифенил, 1,2,3,4-тетрагидрохинолин-7-ил, 1,2,3,4-тетрагидроизохинолин-7-ил и т.п.
[0048] Термин «арилокси» в настоящем документе обозначает O-арильную группу, где арил является таким, как определено выше. Группа арилокси может быть незамещенной или замещенной 1 или 3 подходящими заместителями. Термин «фенокси» обозначает группу арилокси, где арильный фрагмент является фенильным кольцом.
[0049] Термин «гетероарил» включает 5-6-членные ароматические кольца, содержащие 1, 2, 3 или 4 гетероатома, выбранных из группы, состоящей из О, N и S. В некоторых случаях, указанные термины могут быть конкретно и дополнительно ограничены, например, 5-6-членный гетероарил, где гетероарил содержит 1 или 2 гетероатомы азота. Как хорошо известно специалистам в данной области техники, гетероарильным кольцам присущ менее выраженный ароматический характер, чем их полностью углеродным двойникам. Таким образом, для целей изобретения, гетероарильная группа должна обладать только некоторой степенью выраженности ароматического характера.

[0050] Термин «1-алкил-4-арил-пирролидин-3-иламин» в настоящем документе обозначает фрагмент формулы II, где R3 представляет собой C1-3 алкил, необязательно замещенный фенильным кольцом, и Ar представляет собой необязательно замещенный фенил. 4-Арил-пирролидин-3-иламин обозначает фрагмент формулы II, где R3 представляет собой водород, и арил является таким, как определено выше.
[0051] Термины "лечить" и "лечение" обозначают терапевтическое лечение, при котором целью является замедление (облегчение) нежелательного физиологического изменения или расстройства, такого как распространение рака. Для целей данного изобретения, благоприятные или желательные клинические результаты включают, без ограничения, облегчение симптомов, ограничение протяженности заболевания, стабилизацию (т.е. отсутствие ухудшения) заболевания, отодвигание или замедление прогрессирования заболевания, облегчение или смягчение заболевания и ремиссию (частичную или полную), которые поддаются или не поддаются обнаружению. Кроме того, «лечение» может обозначать увеличение продолжительности жизни, по сравнению с ожидаемой продолжительностью жизни в отсутствие лечения.
[0052] Выражение "терапевтически эффективное количество" обозначает количество соединения по настоящему изобретению, которое (i) лечит конкретное заболевание, состояние или расстройство, (ii) ослабляет, облегчает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства или (iii) предупреждает или отодвигает возникновение одного или более симптомов конкретного заболевания, состояния или расстройства, раскрытого в настоящем документе. В случае рака терапевтически эффективное количество лекарственного средства может снижать количество раковых клеток, уменьшать размеры опухоли, подавлять (т.е. до некоторой степени замедлять и предпочтительно останавливать) инфильтрацию раковыми клетками периферических органов; подавлять (т.е. до некоторой степени замедлять и предпочтительно останавливать) метастазирование опухоли; подавлять, до некоторой степени, рост опухоли; и/или до некоторой степени облегчать один или более из симптомов, связанных с раком. В той степени, в которой лекарственное средство может предупреждать рост и/или вызывать гибель существующих раковых клеток, оно может быть цитостатическим и/или цитотоксическим. В случае лечения рака эффективность может быть измерена, например, посредством оценки периода до прогрессирования заболевания (ПДП) и/или определения частоты ответа (ЧО).
[0053] Термины «рак» и «раковый» обозначают или описывают физиологическое состояние у млекопитающих, которое типично характеризуется нерегулируемым ростом клеток. «Опухоль» содержит один или несколько типов раковых клеток. Примеры рака включают, без ограничения, карциному, лимфому, бластому, саркому и лейкоз или злокачественные опухоли лимфоидной ткани. Более конкретные примеры таких типов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого («НМКРЛ»), аденокарциному легкого и плоскоклеточную карциному легкого, рак брюшины, гепатоцеллюлярный рак, рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичника, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак ободочной кишки, рак прямой кишки, рак ободочной и прямой кишки, карциному эндометрия или матки, карциному слюнной железы, рак почки, рак предстательной железы, рак вульвы, рак щитовидной железы, карциному печени, анальную карциному, карциному пениса, а также рак головы и шеи.
[0054] «Химиотерапевтический агент» представляет собой химическое соединение, используемое для лечения рака. Примеры химиотерапевтических агентов включают эрлотиниб (TARCEVA®, Genentech/OSI Pharm.), бортезомиб (VELCADE®, Millennium Pharm.), фулвестрант (FASLODEX®, AstraZeneca), сунитиниб (SUTENT®, Pfizer/Sugen), летрозол (FEMARA®, Novartis), иматиниба мезилат (GLEEVEC®, Novartis), финазунат (VATALANIB®, Novartis), оксалиплатин (ELOXATIN®, Sanofi), 5-ФУ (5-фторурацил), лейковорин, рапамицин (Sirolimus, RAPAMUNE®, Wyeth), лапатиниб (TYKERB®, GSK572016, Glaxo Smith Kline), лонафамиб (SCH 66336), зорафениб (NEXAVAR®, Bayer Labs), гефитиниб (IRESSA®, AstraZeneca), AG1478, алкилирующие агенты, такие как тиотепа и CYTOXAN® циклофосфамид; алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбозон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилмеламин; ацетогенины (особенно буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекан); бриостатин; каллистатин; СС-1065 (включая его аналоги альдоселезин, карселезин и биселезин); криптофицины (конкретно, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и СВ1-ТМ1); элеутеробин; панкратистатин; саркодиктиин, спонгистатин; производные ипритного азота, такие как хлорамбуцил, хломафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлорэтамин, мехлорэтамина оксид гидрохлорид, мелфалан, новэмбихин, фенестерин, преднимустин, трофосфамид, ипритный азот урацила; производные нитрозомочевины, такие как кармустин, хлорзотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как эндииновые антибиотики (например, калихеамицин, особенно калихеамицин γ1I и калихеамицин ω1I (Angew Chem. Intl. Ed. Engl. 1994 33:183-186); динемицин, включая динемицин А; бисфосфонаты, такие как клодронат; эсперамицин; а также неокарциностатиновые хромофоры и родственные хромопротеиновые хромофоры эндииновых антибиотиков), аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, каминомицин, карцинофиллин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, ADRIAMYCIN® (доксорубицин), морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марселломицин, митомицины, такие как митомицин С, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, хеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, циностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-ФУ); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; пуриновые аналоги, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; пиримидиновые аналоги, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, дромостанолона пропионат, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функцию надпочечников, такие как аминоглутетимид, митотан, трилостан; пополнители фолиевой кислоты, такие как фолиновая кислота; ацеглатон; альдофосфамид гликозид; аминолевулиновая кислота; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазихон; эльфомитин; эллиптиния ацатат; эпотилон; этоглюцид; галлия нитрат; гидроксимочевина; лентинан; лонидайнин; майтанзиноиды, такие как майтанзин и анзамитоцины; митогуазон; митоксантрон; мопидамнол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; подофиллиновая кислота; 2-этилгидразид; прокарбазин; PSK® полисахаридный комплекс (JHS Natural Products, Юджин, Орегон); разоксан; ризоксин; сизофуран; спирогерманий; тенуазоновая кислота; триазихон; 2,2',2''-трихлортриэтиламин; трихотецены (особенно токсин Т-2, верракурин А, роридин А и ангидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Ara-С"); циклофосфамид; тиотепа; таксаны, например, TAXOL (паклитаксел; Bristol-Myers Squibb Oncology, Принстон, Нью-Джерси), ABRAXANE® (не содержащий Cremophor), препараты альбуминовых наночастиц паклитаксела (American Pharmaceutical Partners, Шомберг, Иллинойс) и TAXOTERE® (доцетаксал, доксетаксел; Sanofi-Aventis); хлорамбуцил; GEMZAR® (гемцитабин); 6-тиогуанин; меркаптопурин; метотрексат; платиновые аналоги, такие как цисплатин и карбоплатин; винбластин; этопозид (VP-16); ифосфамид; митоксантрон; винкристин; NAVELBINE® (винорельбин); новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; капецитабин (XELODA®); ибандронат; СРТ-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (ДФМО); ретиноиды, такие как ретиноевая кислота; а также фармацевтически приемлемые соли, кислоты и производные любого из перечисленного выше.
[0055] В определение "химиотерапевтического агента" дополнительно включены: (i) анти-гормональные агенты, действие которых состоит в регуляции или подавлении воздействия гормонов на опухоли, например, анти-эстрогены и селективные модуляторы рецепторов эстрогена (СМРЭ), включая, например, тамоксифен (в том числе NOLVADEX®; тамоксифена цитрат), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и FARESTON® (торемифена цитрат); (ii) ингибиторы ароматазы, которые ингибируют фермент ароматазу, регулирующий выработку эстрогена в надпочечниках, например, такие как, 4(5)-имидазолы, аминоглутетимид, MEGASE® (мегестрола ацетат), AROMASIN® (экземестан; Pfizer), форместан, адрозол, R1VISOR® (ворозол), FEMARA® (летрозол; Novartis) и AR1MIDEX® (анастрозол; AstraZeneca); (iii) анти-андрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и гозерелин; а также троксацитабин (1,3-диоксолановый аналог нуклеозида цитозина); (iv) ингибиторы протеинкиназы; (v) ингибиторы липидкиназы; (vi) антисмысловые олигонуклеотиды, конкретно такие, которые подавляют экспрессию генов в сигнальных путях, вовлеченных в аберрантную пролиферацию клеток, например, PKC-альфа, Raf и H-Ras; (vii) рибозимы, такие ингибиторы экспрессии фактора роста сосудистого эндотелия (VEGF) (например, ANGIOZYME®) и ингибиторы экспрессии HER2; (viii) вакцины, такие как вакцины для генной терапии, например, ALLOVECTIN®, LEUVECTIN® и VAXID®; PROLEUKIN®, rIL-2; ингибитор топоизомеразы 1, такой как LURTOTECAN®; ABARELIX® rmRH; (ix) антиангиогенные агенты, такие как бевацизумаб (AVASTIN®), Genentech); и (х) фармацевтически приемлемые соли, кислоты и производные любого из перечисленного выше.
[0056] В одном варианте реализации настоящего изобретения предлагается соединение формулы I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе. Термины «как определено выше» и "«как определено выше в настоящем документе», при обозначении переменной, включают посредством ссылки на наиболее широкое определение переменной, раскрытое в Сущности изобретения или наиболее широком пункте Формулы изобретения.
[0057] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N, и R1, R2, Ar и Z являются такими, как определено выше в настоящем документе.
[0058] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой СН, и R1, R2, Ar и Z являются такими, как определено выше в настоящем документе.
[0059] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, Z представляет собой NHCH2CHR1Ar и R1, R2 и Ar являются такими, как определено выше в настоящем документе.
[0060] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N, Z представляет собой NHCH2CHR1Ar и R1, R2 и Ar являются такими, как определено выше в настоящем документе.
[0061] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой СН, Z представляет собой NHCH2CHR1Ar и R1, R2 и Ar являются такими, как определено выше в настоящем документе.
[0062] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, R1 представляет собой (а) водород, (б) C1-6 алкил, необязательно замещенный 1-3 гидроксильными или C1-6 алкокси-группами, (в) пирролидинильную группу, необязательно замещенную галогеном, или (г) пиразолильный или имидазолильный фрагмент, необязательно замещенный 1-3 C1-6 алкильными фрагментами, и Ar представляет собой необязательно замещенный фенил.
[0063] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N, R1 представляет собой (а) водород, (б) C1-6 алкил, необязательно замещенный одной или более гидроксильных или C1-6 алкокси-групп, (в) пирролидинильную группу, необязательно замещенную галогеном, или (г) пиразолильный или имидазолильный фрагмент, необязательно замещенный 1-3 C1-6 алкильными фрагментами, и Ar представляет собой необязательно замещенный фенил.
[0064] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой СН, R1 представляет собой (а) водород, (б) C1-6 алкил, необязательно замещенный одной или более гидроксильных или C1-6 алкокси-групп, (в) пирролидинильную группу, необязательно замещенную галогеном, или (г) пиразолильный или имидазолильный фрагмент, необязательно замещенный 1-3 C1-6 алкильными фрагментами, Ar представляет собой необязательно замещенный фенил.
[0065] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, Z представляет собой NHCHR1Ar, R1 представляет собой (а) водород, (б) C1-6 алкил, необязательно замещенный одной или более гидроксильных или C1-6 алкокси-групп, (в) пирролидинильную группу, необязательно замещенную галогеном, или (г) пиразолильный или имидазолильный фрагмент, необязательно замещенный 1-3 C1-6 алкильными фрагментами; и Ar представляет собой необязательно замещенный фенил. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0066] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, Z представляет собой NHCHR1Ar, R1 представляет собой (а) C1-6 алкил, (б) C1-6 алкил, замещенный гидроксильной группой, или (в) пиразолил, необязательно замещенный 1 или 2 C1-6 алкильными фрагментами; и Ar представляет собой необязательно замещенный фенил. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0067] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, Z представляет собой NHCHR1Ar, R1 представляет собой (a) (R)-C1-6 алкил, (б) (S)-C1-6 гидроксиалкил или (в) (S)-1-C1-6 алкил-1Н-пиразол-4-ил; и Ar представляет собой необязательно замещенный фенил. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0068] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, Z представляет собой, R1 представляет собой (а) (R)-этил, (б) гидроксиметил или (в) (S)-1-метил-1Н-пиразол-4-ил; и Ar представляет собой необязательно замещенный фенил. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0069] В некоторых вариантах реализации R1 выбран из (а) водорода (б) C1-С6 алкила, необязательно замещенного одной или более гидроксильных или C1-6 алкокси-групп; (в) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен одной или более групп, выбранных из гидроксила, C1-6 алкокси, C1-6 алкила и галогена; и (г) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен одной или более групп, выбранных из гидроксила, C1-6 алкокси, C1-6 алкила и галогена. В некоторых вариантах реализации R1 выбран из (а) водорода; (б) C1-С6 алкила, необязательно замещенного 1 или 2 гидроксильными или C1-6 алкокси-группами; (в) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен 1 или 2 группами, выбранными из гидроксила, C1-6 алкокси, C1-6 алкила и галогена; и (г) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен 1 или 2 группами, выбранными из гидроксила, C1-6 алкокси, C1-6 алкила и галогена. В некоторых вариантах реализации R1 выбран из (а) водорода; (б) C1-С6 алкила, необязательно замещенного одной гидроксильной группой; (в) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен галогеном; и (г) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен C1-6 алкилом. В некоторых вариантах реализации R1 выбран из (а) водорода; (б) C1-С6 алкила, необязательно замещенного одной гидроксильной группой; (в) 4-6-членного гетероцикла, содержащего один гетероатом N, причем гетероцикл необязательно замещен галогеном; и (г) 5-6-членного гетероарила, содержащего два гетероатома N, причем гетероарил необязательно замещен C1-6 алкилом.
[0070] В некоторых вариантах реализации R1 выбран из водорода, гидроксиметила, (S)-гидроксиметила, (R)-гидроксиметила, этила, (S)-этила, (R)-этила, 2-гидроксиэтила, (R)-2-гидроксиэтила, (S)-2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, (R)-3-фторпирролидин-3-ила, (S)-3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, (S)-1-метил-1H-пиразол-4-ила, (R)-1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, (S)-1-метил-1Н-пиразол-5-ила, (R)-1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила, (S)-1-метил-1H-имидазол-5-ила, (R)-1-метил-1H-имидазол-5-ила, 1-метил-1H-пиразол-3-ила, (S)-1-метил-1H-пиразол-3-ила и (R)-1-метил-1H-пиразол-3-ила, В некоторых вариантах реализации R1 выбран из водорода, гидроксиметила, (S)-гидроксиметила, этила, (S)-этила, 2-гидроксиэтила, (R)-2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, (R)-3-фторпирролидин-3-ила, (S)-3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, (S)-1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, (S)-1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила, (S)-1-метил-1H-имидазол-5-ила, (R)-1-метил-1H-имидазол-5-ила, 1-метил-1H-пиразол-3-ила, (S)-1-метил-1H-пиразол-3-ила и (R)-1-метил-1Н-пиразол-3-ила. В некоторых вариантах реализации R1 выбран из водорода, гидроксиметила, этила, 2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила и 1-метил-1H-пиразол-3-ила.
[0071] В некоторых вариантах реализации R1 выбран из (а) C1-С6 алкила, необязательно замещенного одной или более гидроксильных или C1-6 алкокси-групп; (б) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен одной или более групп, выбранных из гидроксила, C1-6 алкокси, C1-6 алкила и галогена; и (в) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен одной или более групп, выбранных из гидроксила, C1-6 алкокси, C1-6 алкила и галогена. В некоторых вариантах реализации R1 выбран из (а) C1-C6 алкила, необязательно замещенного 1 или 2 гидроксильными или C1-6 алкокси-группами; (б) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен 1 или 2 группами, выбранными из гидроксила, C1-6 алкокси, C1-6 алкила и галогена; и (в) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен 1 или 2 группами, выбранными из гидроксила, C1-6 алкокси, C1-6 алкила и галогена. В некоторых вариантах реализации R1 выбран из (а) C1-C6 алкила, необязательно замещенного одной гидроксильной группой; (б) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен галогеном; и (в) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен C1-6 алкилом. В некоторых вариантах реализации R1 выбран из (а) C1-C6 алкила, необязательно замещенного одной гидроксильной группой; (б) 4-6-членного гетероцикла, содержащего один гетероатом N, причем гетероцикл необязательно замещен галогеном; и (в) 5-6-членного гетероарила, содержащего два гетероатома N, причем гетероарил необязательно замещен C1-6 алкилом.
[0072] В некоторых вариантах реализации R1 выбран из гидроксиметила, (S)-гидроксиметила, (R)-гидроксиметила, этила, (S)-этила, (R)-этила, 2-гидроксиэтила, (R)-2-гидроксиэтила, (S)-2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, (R)-3-фторпирролидин-3-ила, (S)-3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, (S)-1-метил-1H-пиразол-4-ила, (R)-1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, (S)-1-метил-1H-пиразол-5-ила, (R)-1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила, (S)-1-метил-1H-имидазол-5-ила, (R)-1-метил-1H-имидазол-5-ила, 1-метил-1H-пиразол-3-ила, (S)-1-метил-1H-пиразол-3-ила и (R)-1-метил-1H-пиразол-3-ила. В некоторых вариантах реализации R1 выбран из гидроксиметила, (S)-гидроксиметила, этила, (S)-этила, 2-гидроксиэтила, (R)-2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, (R)-3-фторпирролидин-3-ила, (S)-3-фторпирролидин-3-ила, 1-метил-1Н-пиразол-4-ила, (S)-1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, (S)-1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила, (S)-1-метил-1H-имидазол-5-ила, (R)-1-метил-1H-имидазол-5-ила, 1-метил-1H-пиразол-3-ила, (S)-1-метил-1H-пиразол-3-ила и (R)-1-метил-1H-пиразол-3-ила. В некоторых вариантах реализации R1 выбран из гидроксиметила, этила, 2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, 1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила и 1-метил-1H-пиразол-3-ила.
[0073] В некоторых вариантах реализации R2 выбран из (а) C1-10 гидроксиалкила; (б) C1-6 галогеналкила; (в) гетероциклила, где указанный гетероциклил выбран из группы, состоящей из тетрагидропиранила, тетрагидрофуранила, 2-оксабицикло[2,2,1]гептан-5-ила и пирролидинила, причем указанный гетероциклил необязательно замещен 1-3 группами, независимо выбранными из группы, состоящей из галогена, C1-3 гидроксиалкила и оксо; (г) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила, где указанный гетероарил необязательно замещен 1 или 2 C1-3 алкильными группами; и (д) С3-7 циклоалкил-C1-6 алкила, необязательно замещенного гидроксилом. В некоторых вариантах реализации R2 выбран из (а) C1-10 гидроксиалкила; (б) C1-6 галогеналкила; (в) гетероциклила, где указанный гетероциклил выбран из группы, состоящей из тетрагидропиранила, тетрагидрофуранила, 2-оксабицикло[2,2,1]гептан-5-ила и пирролидинила, причем указанный гетероциклил необязательно замещен 1-3 группами, независимо выбранными из группы, состоящей из галогена, C1-3 гидроксиалкила и оксо; (г) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила и, при этом. указанный гетероарил необязательно замещен 1 или 2 метальными группами; и (д) С3-7 циклоалкил-C1-6 алкила необязательно замещенного гидроксилом. В некоторых вариантах реализации R2 выбран из группы, состоящей из 1-гидроксипропан-2-ила, (S)-1-гидроксипропан-2-ила, 3-гидрокси-3-метилбутан-2-ила, (S)-3-гидрокси-3-метилбутан-2-ила, (R)-3-гидрокси-3-метилбутан-2-ила, 3-фторпропила, 5-оксопирролидин-3-ила, тетрагидропиран-4-ила, 3-фтортетрагидропиран-4-ила, (3S,4S)-3-фтортетрагидропиран-4-ила, (3R,4S)-3-фтортетрагидропиран-4-ила, 2-(гидроксиметил)тетрагидропиран-4-ила, (2S,4R)-2-(гидроксиметил)тетрагидропиран-4-ила, 2-оксабицикло[2,2,1]гептан-5-ила, тетрагидрофуран-3-ила, 1-метил-1H-пиразол-5-ила, 2-метилпиридин-4-ила, 1,3-диметил-1H-пиразол-5-ила, 1-(1-гидроксициклопропил)этила и (S)-1-(1-гидроксициклопропил)этила.
[0074] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и R2 представляет собой (а) C1-10 гидроксиалкил, (б) гетероциклил, где указанный гетероциклил представляет собой тетрагидропиранил или тетрагидрофуранил, необязательно замещенный 1-3 группами, независимо выбранными из C1-6 алкила, галогена или C1-6 гидроксиалкила, или (в) гетероарил, где указанный гетероарил представляет собой пиразолил или пиридинил, необязательно замещенный 1-3 C1-6 алкильными фрагментами. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН. В другом подварианте R2 представляет собой N-C1-3 алкил-пиразолил, необязательно замещенный 1-3 C1-6 алкильными фрагментами. Еще в другом подварианте R2 представляет собой N-метил-пиразолил, необязательно замещенный 1-3 C1-6 алкильными фрагментами.
[0075] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и R2 представляет собой 1-метил-1Н-пиразол-4-ил, 2-метил-2Н-пиразол-3-ил, 2,5-диметил-2Н-пиразол-3-ил, тетрагидропиран-4-ил, 3-фтор-тетрагидропиран-4-ил, тетрагидрофуран-3-ил или 2-гидрокси-1-метил-этил.
[0076] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН; R2 представляет собой 1-метил-1Н-пиразол-4-ил, 2-метил-2Н-пиразол-3-ил, 2,5-диметил-2Н-пиразол-3-ил, тетрагидропиран-4-ил, 3-фтор-тетрагидропиран-4-ил, тетрагидрофуран-3-ил или 2-гидрокси-1-метил-этил; и Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0077] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0078] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и R1 представляет собой (R)-этил, (S)-2-гидроксиметил или (S)-1-метил-1Н-пиразол-4-ил; R2 представляет собой 1-метил-1H-пиразол-4-ил, 2-H метил-2Н-пиразол-3-ил, 2,5-диметил-2Н-пиразол-3-ил, тетрагидропиран-4-ил, 3-фтор-тетрагидропиран-4-ил, тетрагидрофуран-3-ил или 2-гидрокси-1-метил-этил; и Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0079] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и R1 представляет собой (R)-этил, (S)-2-гидроксиметил или (S)-1-метил-1H-пиразол-4-ил; R2 представляет собой 1-метил-1H-пиразол-4-ил, 2-метил-2Н-пиразол-3-ил или 2,5-диметил-2Н-пиразол-3-ил; и Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0080] В некоторых вариантах реализации Ar выбран из фенила, 3-фторфенила, 3-фтор-4-метоксифенила, 4-хлор-3-фторфенила, 4-трифторметоксифенила, 3-хлор-4-цианофенила, 2-бромфенила, 4-бромфенила, 3-бромфенила, 4-(1-метил-1H-пиразол-4-ил)фенила, 4-(4-метилпиридин-3-ил)фенила, 3-(4-метилпиридин-3-ил)фенила, 3-(1-метил-1H-пиразол-4-ил)фенила, 3-бензилфенила, 4-(пиримидин-5-ил)фенила, 4-(пиразин-5-ил)фенила, 4-(пиридин-4-ил)фенила, 3-(пиридин-4-ил)фенила, 3-(пиразин-2-ил)фенила, 2-(1-метил-1H-пиразол-4-ил)фенила, 3-феноксифенила, 4-метоксифенила, 3-хлор-4-фторфенила, 4-(дифторметокси)фенила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, 5-бензилпиридин-3-ила, 4-бензилпиридин-2-ила, 4-(4-метилпиперазин1-ил)пиридин-2-ила, 4-феноксипиридин-2-ила, 2-бензилпиридин-3-ила, 4-(о-толил)пиридин-2-ила, 4-(2-хлорфенокси)пиридин-2-ила и 4-фтор-1H-индол-2-ила. В некоторых вариантах реализации Ar выбран из фенила, 3-фторфенила, 3-фтор-4-метоксифенила, 4-хлор-3-фторфенила, 4-трифторметоксифенила, 3-хлор-4-цианофенила, 2-бромфенила, 4-бромфенила, 3-бромфенила, 4-(1-метил-1H-пиразол-4-ил)фенила, 4-(4-метилпиридин-3-ил)фенила, 3-(4-метилпиридин-3-ил)фенила, 3-(1-метил-1H-пиразол-4-ил)фенила, 3-бензилфенила, 4-(пиримидин-5-ил)фенила, 4-(пиразин-5-ил)фенила, 4-(пиридин-4-ил)фенила, 3-(пиридин-4-ил)фенила, 3-(пиразин-2-ил)фенила, 2-(1-метил-1H-пиразол-4-ил)фенила, 3-феноксифенила, 4-метоксифенила, 3-хлор-4-фторфенила и 4-(дифторметокси)фенила. В некоторых вариантах реализации Ar выбран из пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, 5-бензилпиридин-3-ила, 4-бензилпиридин-2-ила, 4-(4-метилпиперазин-1-ил)пиридин-2-ила, 4-феноксипиридин-2-ила, 2-бензилпиридин-3-ила, 4-(о-толил)пиридин-2-ила и 4-(2-хлорфенокси)пиридин-2-ила. В некоторых вариантах реализации Ar выбран из 4-фтор-1H-индол-2-ила.
[0081] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Ar выбран из 3-фторфенила, 3-фтор-4-метокси-фенила, 4-хлор-3-фтор-фенила, 4-трифторметокси-фенила, 3-хлор-4-циано-фенила, 4-метокси-фенила и 4-дифторметокси-фенила.
[0082] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и R1 представляет собой (R)-этил, (S)-2-гидроксиметил или (S)-1-метил-1Н-пиразол-4-ил; R2 представляет собой 1-метил-1H-пиразол-4-ил, 2-метил-2Н-пиразол-3-ил или 2,5-диметил-2Н-пиразол-3-ил; и Ar представляет собой 3-фторфенил, 3-фтор-4-метокси-фенил, 4-хлор-3-фтор-фенил, 4-трифторметокси-фенил, 3-хлор-4-циано-фенил, 4-метокси-фенил или 4-дифторметокси-фенил. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0083] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где Х представляет собой N или СН, и Z представляет собой NH(СН2)nCHR1Ar, где n равно 0. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН.
[0084] В другом варианте реализации настоящего изобретения предлагается соединение в соответствии с формулой I, где R1 представляет собой 1-алкил-4-арил-пирролидин-3-иламин. В одном подварианте Х представляет собой N. В другом подварианте Х представляет собой СН. В другом подварианте Х представляет собой N, и алкил представляет собой метил. В другом подварианте Х представляет собой СН, и алкил представляет собой метил.
[0085] В некоторых вариантах реализации Z представляет собой NH(CH2)nCHR1Ar, n равно 1, и R1 представляет собой водород. В некоторых вариантах реализации Х представляет собой N, Z представляет собой NH(CH2)nCHR1Ar, n равно 1, и R1 представляет собой водород.
[0086] В некоторых вариантах реализации Х представляет собой СН, Z представляет собой (i) NH(CH2)nCHR1Ar, где n равно 0, или (ii) 1-алкил-4-арил-пирролидин-3-иламин или 4-арил-пирролидин-3-иламин, где алкил представляет собой С1-3 алкил, необязательно замещенный фенильным кольцом, и арил представляет собой необязательно замещенный фенил.
[0087] В некоторых вариантах реализации:
R1 выбран из (а) водорода; (б) C1-C6 алкила, необязательно замещенного одной гидроксильной группой; (в) 4-6-членного гетероцикла, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероцикл необязательно замещен галогеном; и (г) 5-6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранных из N и О, причем гетероарил необязательно замещен C1-6 алкилом
R2 выбран из (а) C1-10 гидроксиалкила; (б) C1-6 галогеналкила; (в) гетероциклила, где указанный гетероциклил выбран из группы, состоящей из тетрагидропиранила, тетрагидрофуранила, 2-оксабицикло[2,2,1]гептан-5-ила и пирролидинила, причем указанный гетероциклил необязательно замещен галогеном, C1-3 гидроксиалкилом или оксо; (г) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила, причем указанный гетероарил необязательно замещен 1 или 2 C1-3 алкильными группами; и (д) С3-7 циклоалкил-C1-6 алкила, необязательно замещенного гидроксилом.
[0088] В некоторых вариантах реализации:
R1 выбран из водорода, гидроксиметила, (S)-гидроксиметила, этила, (S)-этила, 2-гидроксиэтила, (R)-2-гидроксиэтила, 1-гидроксиэтила, 3-фторпирролидин-3-ила, (R)-3-фторпирролидин-3-ила, (S)-3-фторпирролидин-3-ила, 1-метил-1H-пиразол-4-ила, (S)-1-метил-1H-пиразол-4-ила, 1-метил-1Н-пиразол-5-ила, (S)-1-метил-1H-пиразол-5-ила, 1-метил-1H-имидазол-5-ила, (S)-1-метил-1H-имидазол-5-ила, (R)-1-метил-1H-имидазол-5-ила, 1-метил-1H-пиразол-3-ила, (S)-1-метил-1H-пиразол-3-ила и (R)-1-метил-1H-пиразол-3-ила;
R2 выбран из группы, состоящей из 1-гидроксипропан-2-ила, (S)-1-гидроксипропан-2-ила, 3-гидрокси-3-метилбутан-2-ила, (S)-3-гидрокси-3-метилбутан-2-ила, (R)-3-гидрокси-3-метилбутан-2-ила, 3-фторпропила, 5-оксопирролидин-3-ила, тетрагидропиран-4-ила, 3-фтортетрагидропиран-4-ила, (3S,4S)-3-фтортетрагидропиран-4-ила, (3R,4S)-3-фтортетрагидропиран-4-ила, 2-(гидроксиметил)тетрагидропиран-4-ила, (2S,4R)-2-(гидроксиметил)тетрагидропиран-4-ила, 2-оксабицикло[2,2,1]гептан-5-ила, тетрагидрофуран-3-ила, 1-метил-1H-пиразол-5-ила, 2-метилпиридин-4-ила, 1,3-диметил-1H-пиразол-5-ила, 1-(1-гидроксициклопропил)этила и (S)-1-(1-гидроксициклопропил)этила.
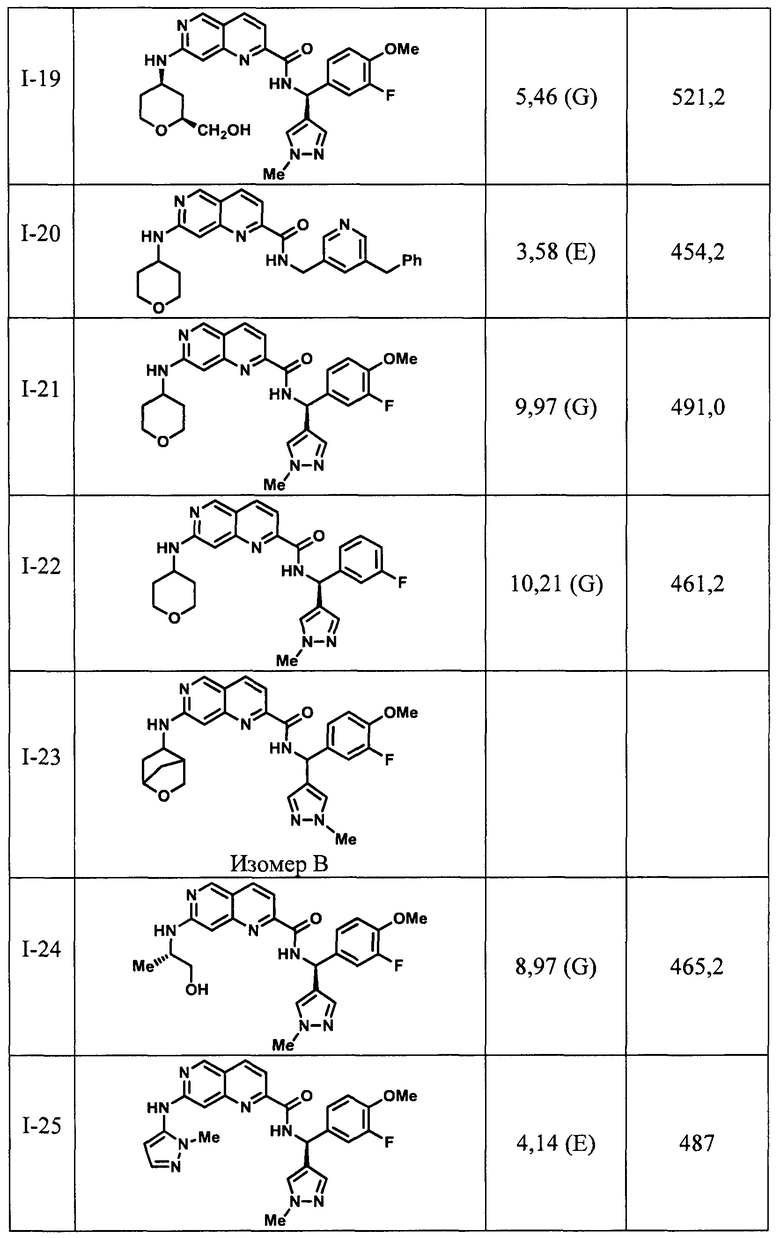
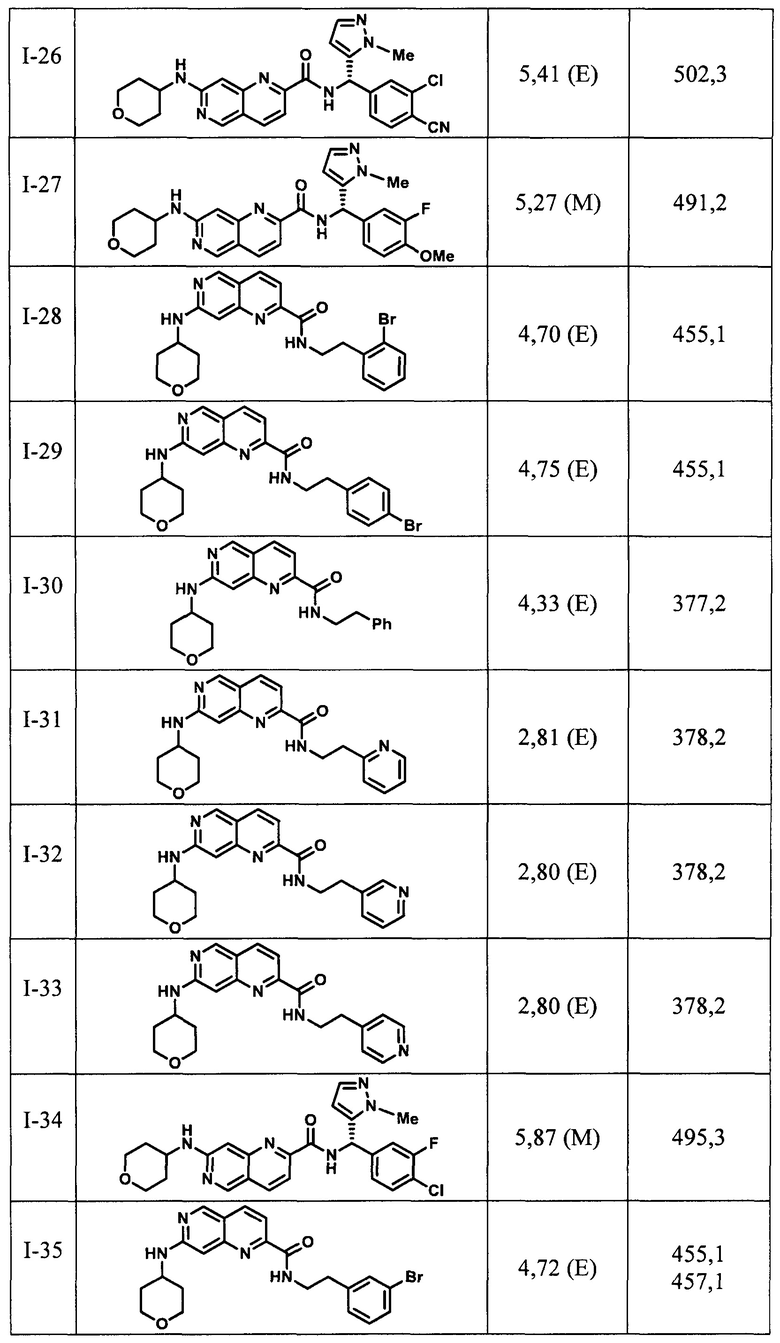
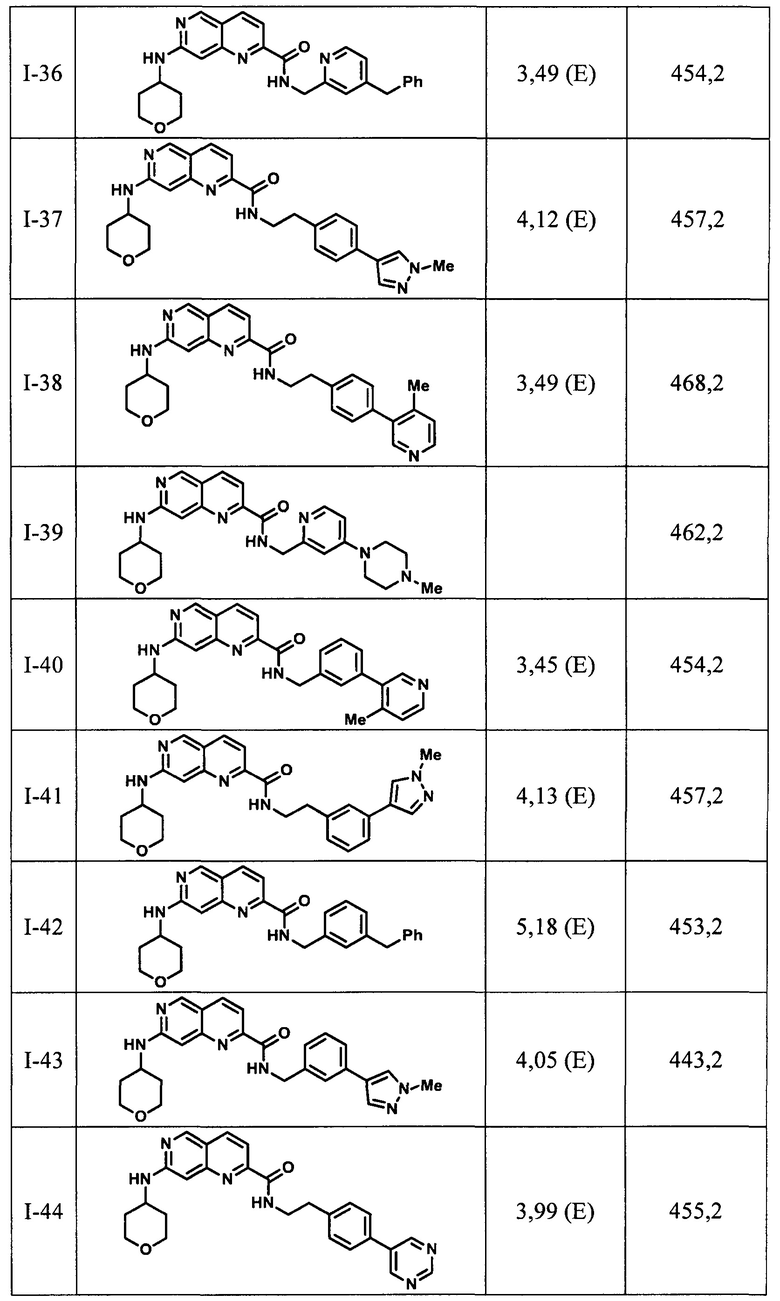
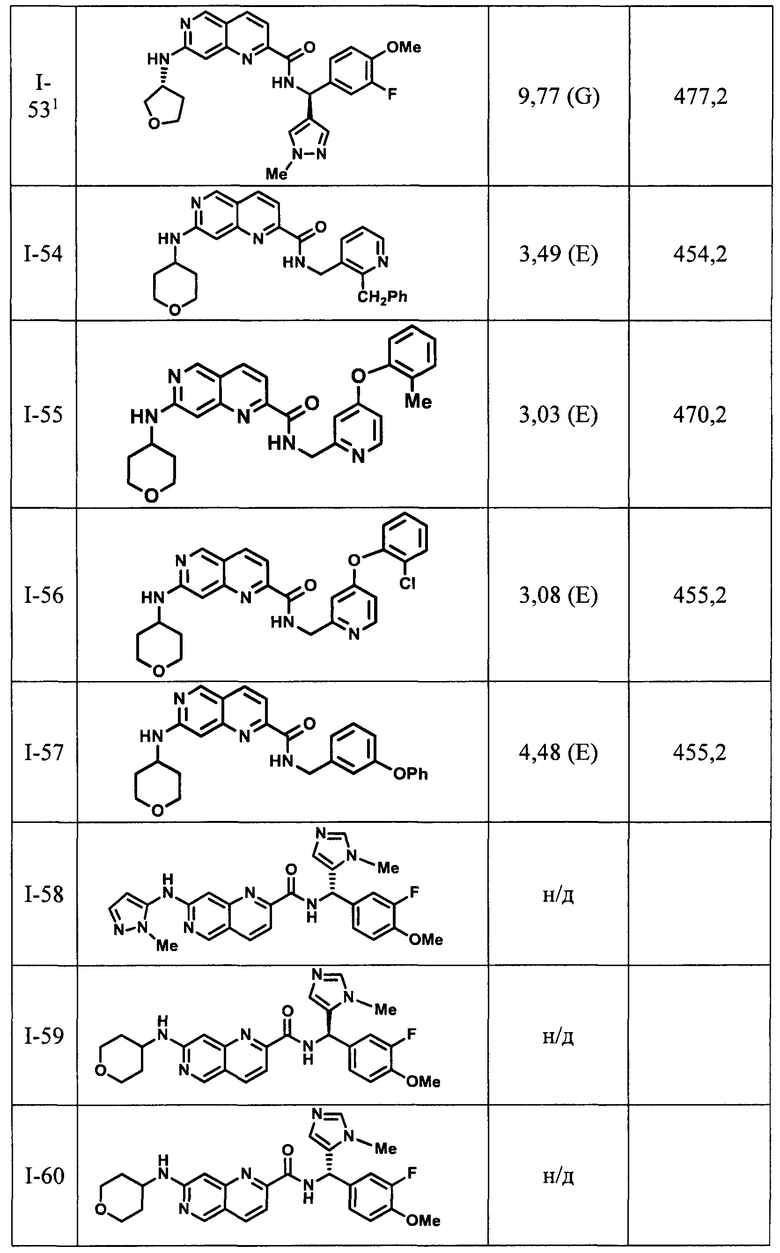
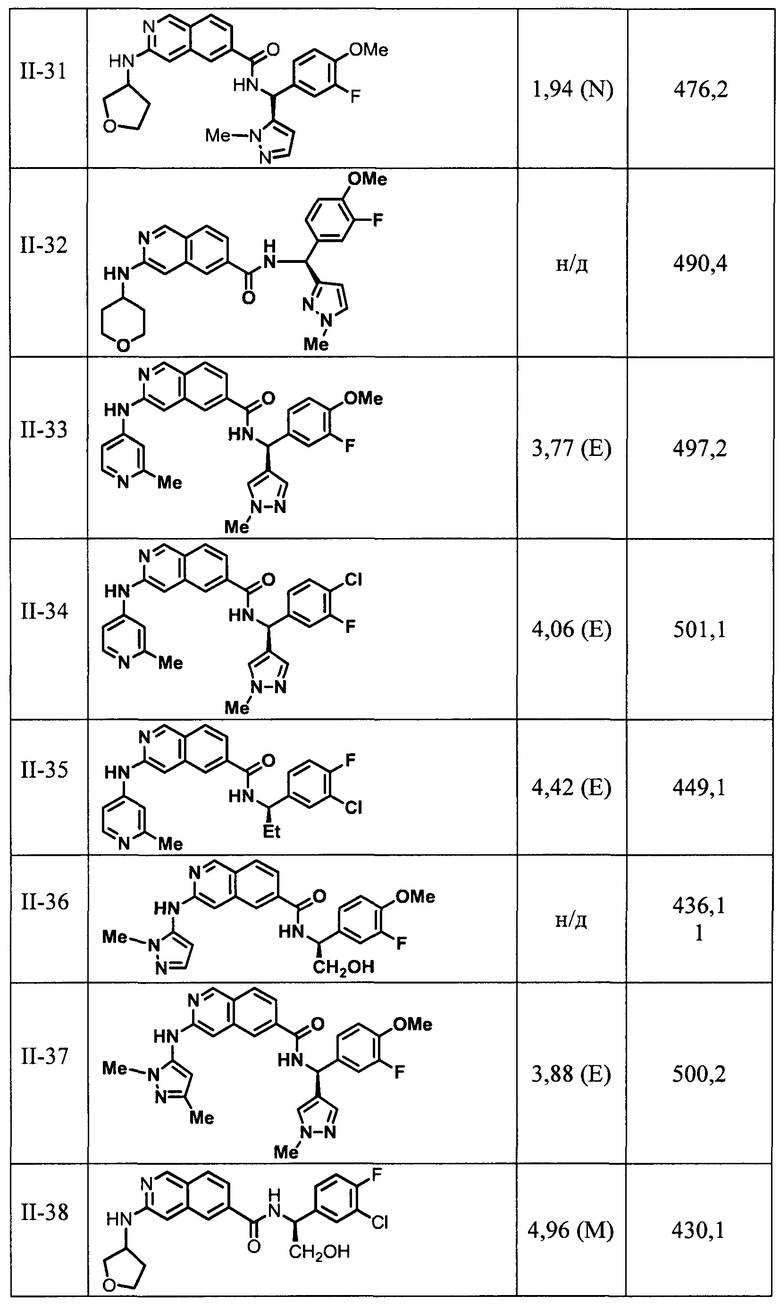
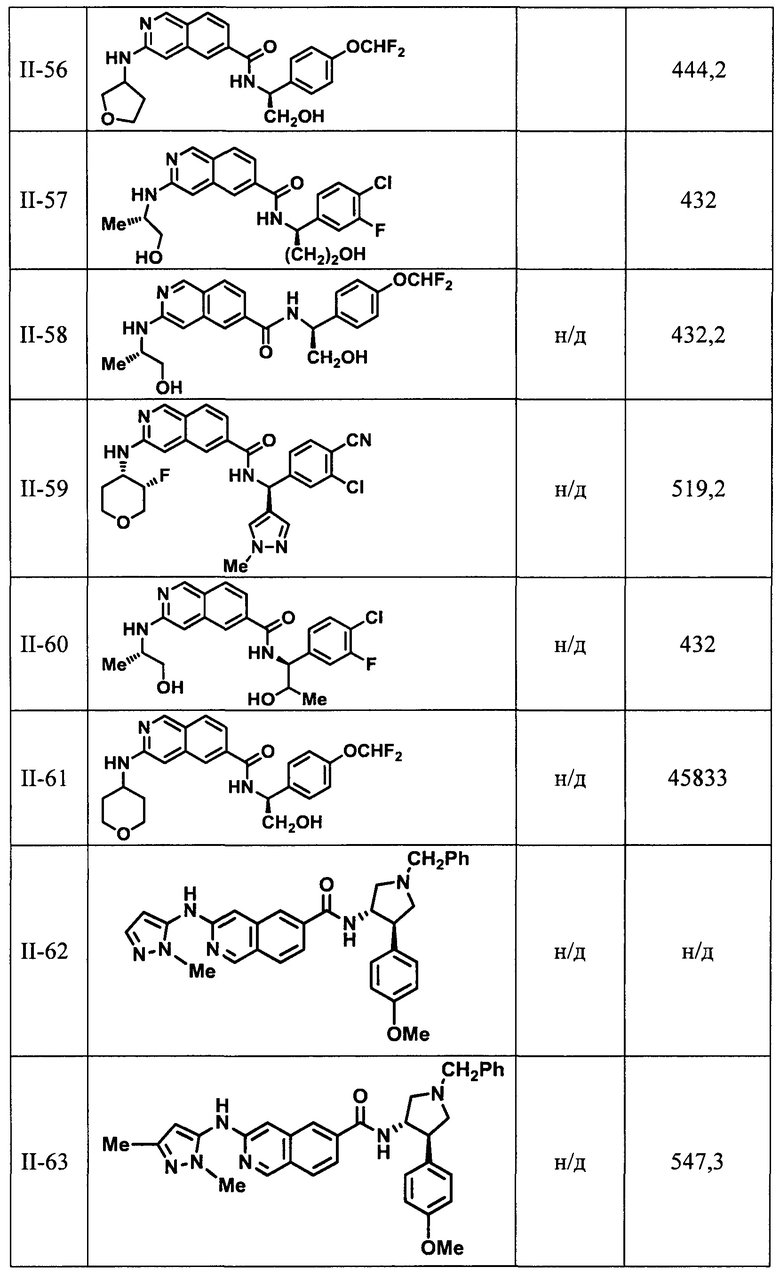
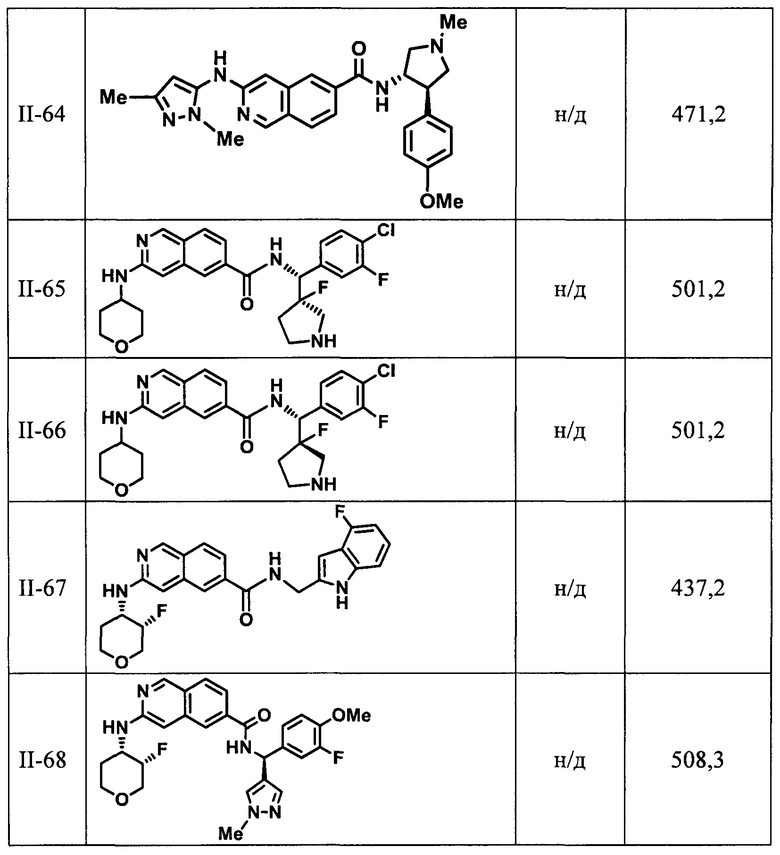
[0089] В другом варианте реализации настоящего изобретения предлагается соединение, выбранное из соединений с I-1 по I-61 в Табл. I и с II-1 по II-69 в Табл. II, или его фармацевтически приемлемая соль. В другом варианте реализации настоящего изобретения предлагается соединение, выбранное из соединений с I-1 по I-61 в Табл. I, или его фармацевтически приемлемая соль. В другом варианте реализации настоящего изобретения предлагается соединение, выбранное из соединений с II-1 по II-69 в Табл. II, или его фармацевтически приемлемая соль.
[0090] В другом варианте реализации настоящего изобретения предлагается фармацевтическая композиция, содержащая соединение в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере один фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель.
[0091] В другом варианте реализации настоящего изобретения предлагается способ ингибирования активности протеинкиназы ERK в клетке, включающий обработку клетки соединением в соответствии с формулой I, где R1, R2, Ar, Х и Z являются такими, как определено выше в настоящем документе, с по меньшей мере одним фармацевтически приемлемым носителем, вспомогательным веществом или разбавителем.
[0092] В другом варианте реализации настоящего изобретения предлагается способ ингибирования активности протеинкиназы ERK у пациента, нуждающегося в этом, причем способ включает введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, Х и Z являются такими, как определено выше в настоящем документе, и по меньшей мере одного фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя.
[0093] В другом варианте реализации настоящего изобретения предлагается способ лечения или уменьшения тяжести гиперпролиферативного расстройства у пациента, нуждающегося в этом, причем способ включает введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, Х и Z являются такими, как определено выше в настоящем документе, и по меньшей мере одного фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя.
[0094] В другом варианте реализации настоящего изобретения предлагается способ лечения или уменьшения тяжести гиперпролиферативного расстройства, выбранного из группы, состоящей из аденомы, рака мочевого пузыря, рака мозга, рака молочной железы, колоректального рака, эпидермальной карциномы, фолликулярной карциномы, рака мочеполовых путей, глиобластомы, болезни Ходжкинса, рака головы и шеи, гепатомы, кератоксантомы, рака почки, крупноклеточной карциномы, лейкозов, аденокарциномы легкого, рака легкого, лимфоидных расстройств, меланомы и немеланомного рака кожи, миелодиспластического синдрома, нейробластомы, неходжкинской лимфомы, рака яичника, папиллярной карциномы, рака поджелудочной железы, рака предстательной железы, рака прямой кишки, саркомы, мелкоклеточной карциномы, рака яичка, тетракарцином, рака щитовидной железы и недифференцированной карциномы, у пациента, нуждающегося в этом, причем способ включает введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере одного фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя.
[0095] В другом варианте реализации настоящего изобретения предлагается способ лечения или уменьшения тяжести гиперпролиферативного расстройства, выбранного из группы, состоящей из меланомы, рака поджелудочной железы, рака щитовидной железы, колоректального рака, рака легкого, рака молочной железы и рака яичника, у пациента, нуждающегося в этом, причем способ включает введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере одного фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя.
[0096] В другом варианте реализации настоящего изобретения предлагается способ лечения или уменьшения тяжести гиперпролиферативного расстройства, выбранного из группы, состоящей из острого миелогенного лейкоза, хронического миеломоноцитарного лейкоза, хронического миелогенного лейкоза, множественной миеломы и миелоидного лейкоза, у пациента, нуждающегося в этом, причем способ включает введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере одного фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя.
[0097] В другом варианте реализации настоящего изобретения предлагается способ лечения или уменьшения тяжести гиперпролиферативного расстройства у пациента, нуждающегося в этом, причем способ включает сопутствующее введение пациенту соединения в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере еще одного применяемого химиотерапевтического агента.
[0098] В другом варианте реализации настоящего изобретения предлагается применение соединения формулы I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, для производства лекарственного средства для лечения гиперпролиферативного заболевания.
[0099] В другом варианте реализации настоящего изобретения предлагается применение соединения формулы I, где R1, R2, Ar, X и Z являются лекарственным средством.
[00100] В другом варианте реализации настоящего изобретения предлагается применение соединения формулы I, где R1, R2, Ar, X и Z, в терапии.
[00101] В другом варианте реализации настоящего изобретения предлагается применение соединения формулы I, где R1, R2, Ar, X и Z, при лечении рака.
[00102] В другом варианте реализации настоящего изобретения предлагается фармацевтическая композиция для применения при лечении гиперпролиферативного заболевания, содержащая соединение в соответствии с формулой I, где R1, R2, Ar, X и Z являются такими, как определено выше в настоящем документе, и по меньшей мере один фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель.
[00103] Общеизвестные сокращения включают: ацетил (Ас), водный (водн.), атмосфера (атм.), 2,2'-бис(дифенилфосфино)-1,1'-бинафтил (БИНАФ), трет-бутоксикарбонил (Boc), ди-трет-бутил пирокарбонат или ангидрид boc (BOC2O), бензил (Bn), бутил-(Bu), регистрационный номер Chemical Abstracts (CASRN), бензилоксикарбонил (CBZ или Z), карбонилдиимидазол (КДИ), 1,5-диазабицикло[4,3,0]нон-5-ен (ДБН), 1,8-диазабицикло[5,4,0]ундец-7-ен (ДБУ), N,N'-дициклогексилкарбодиимид (ДЦК), 1,2-дихлорэтан (ДХЭ), дихлорметан (ДХМ), диэтилазодикарбоксилат (ДЭАД), диизопропилазодикарбоксилат (ДИАД), диизобутилалюминия гидрид (ДИБАЛ или ДИБАЛ-Г), диизопропилэтиламин (ДИПЭА), дифенилфосфорилазид (ДФФА), N,N-диметилацетамид (ДМА), 4-N,N-диметиламинопиридин (ДМАП), N,N-диметилформамид (ДМФА), диметилсульфоксид (ДМСО), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (ЭДКИ), этил (Et), этилацетат (EtOAc), этанол (EtOH), 2-этокси-2Н-хинолин-1-карбоновой кислоты этиловый эфир (ЭЭДХ), диэтиловый эфир (Et2O), O-(7-азабензотриазол-1-ил)-N,N,N'N'-тетраметилуроний гексафторфосфат уксусная кислота (ГУТУ), уксусная кислота (НОАс), 1-гидрокси-7-аза-бензотриазол (HOAt), 1-N-гидроксибензотриазол (HOBt), высокоэффективная жидкостная хроматография при высоком давлении (ВЭЖХ), изопропанол (ИПА), лития диизопропиламид (ЛДА), метанол (МеОН), температуру плавления (Тпл), MeSO2- (мезил или Ms), метил (Me), ацетонитрил (MeCN), м-хлорпербензойную кислоту (МХПБК), масс-спектр (МС), метил-трет-бутиловый эфир (МТБЭ), N-метилморфолин (НММ), N-метилпирролидон (НМП), недоступен (н/д), фенил (Ph), пропил (Pr) изопропил (i-Pr), фунты на квадратный дюйм (фунт/дюйм2), пиридин (pyr), комнатную температуру (rt или RT), насыщенный (насыщ.), трет-бутилдиметилсилил или трет-BuMe2Si (ТБДМС), тетрабутиламмония фторид (ТБАФ), триэтиламин (ТЭА или Et3N), трифлат или CF3SO2- (Tf), трифторуксусную кислоту (ТФУ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборат (ТБТУ), тонкослойную хроматографию (ТСХ), тетрагидрофуран (ТГФ), тетраметилэтилендиамин (ТМЭДА), триметилсилил или Me3Si (TMC), n-толуолсульфоновой кислоты моногидрат (TsOH или n-TsOH), 4-Ме-C6H4SO2- или тозил (Ts), N-уретан-N-карбоксиангидрид (УНКА). Традиционная номенклатура, включая приставки «нормальный» (н-), «изо» (изо-), «вторичный» (втор-), «третичный» (трет-) и нео- имеет общепринятое значение при использовании с алкильным фрагментом. (J. Rigaudy and D.P. Klesney, Nomenclature in Organic Chemistry, IUPAC 1979 Pergamon Press, Oxford.)
[00104] СОЕДИНЕНИЯ И ПРЕПАРАТИВНЫЕ ПРИМЕРЫ
[00105] Примеры характерных соединений в рамках изобретения раскрыты в следующих таблицах. Указанные примеры и препаративные примеры, приведенные ниже, предложены с целью обеспечения более четкого понимания и практики изобретения специалистами в данной области техники. Их не следует рассматривать как ограничивающие объем изобретения, а только как иллюстрирующие и характеризующие изобретение.
[00106] Если присутствует расхождение между изображенной структурой и присвоенным указанной структуре названием, предпочтение следует отдавать изображенной структуре. Кроме того, если стереохимия структуры или части структуры не изображена, например, жирными или пунктирными линиями, структуру или часть структуры следует интерпретировать как охватывающую все стереоизомеры данной структуры. Следующая система нумерации используется в настоящем документе.

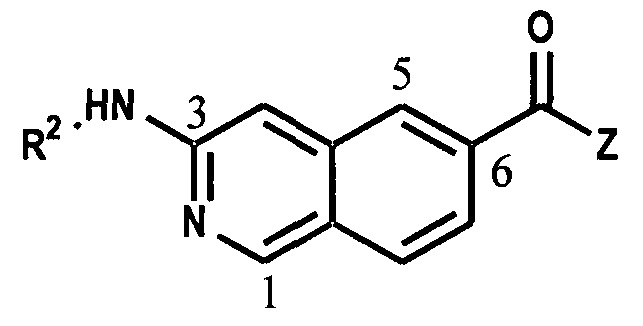
[00107] В Табл. I проиллюстрированы примеры нафтиридинов в рамках Формулы настоящего изобретения.




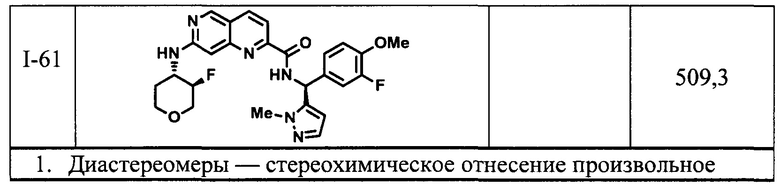
[00108] В табл. II проиллюстрированы примеры изохинолинов в рамках Формулы настоящего изобретения.

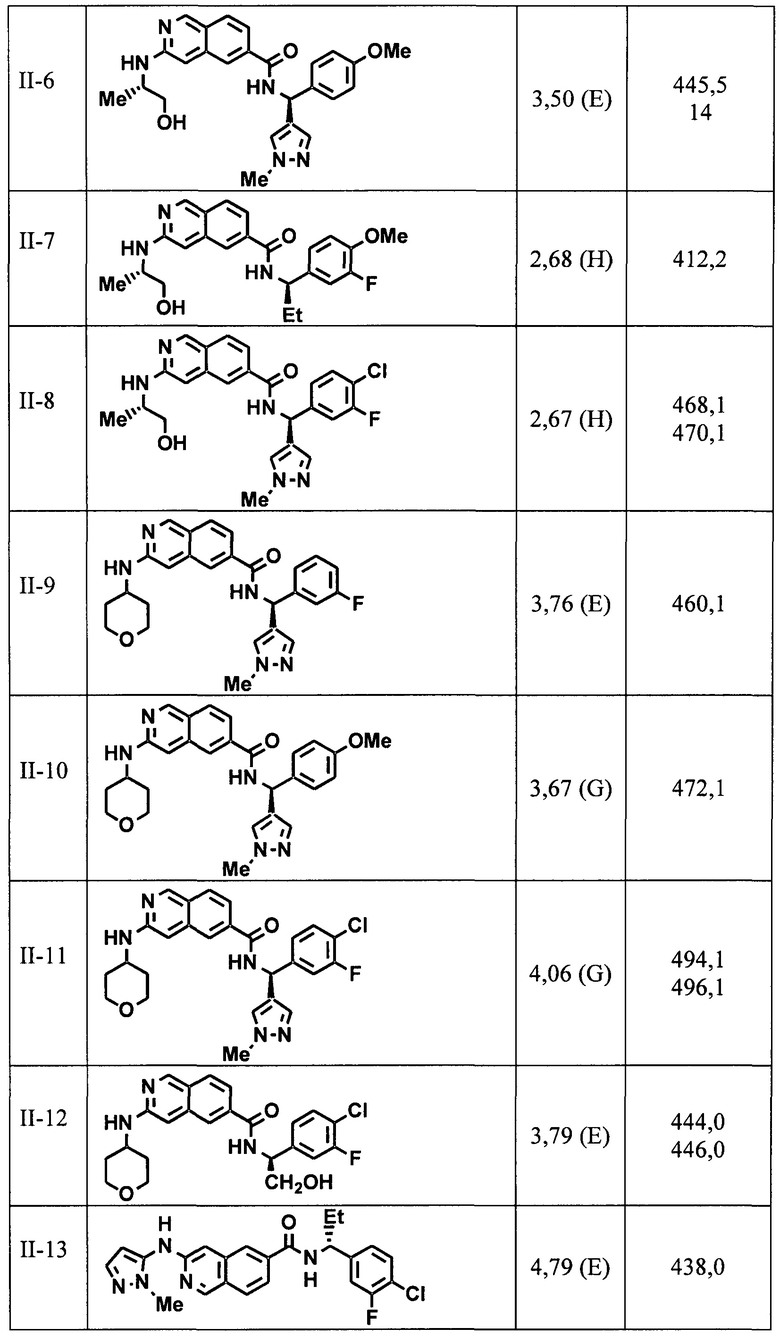
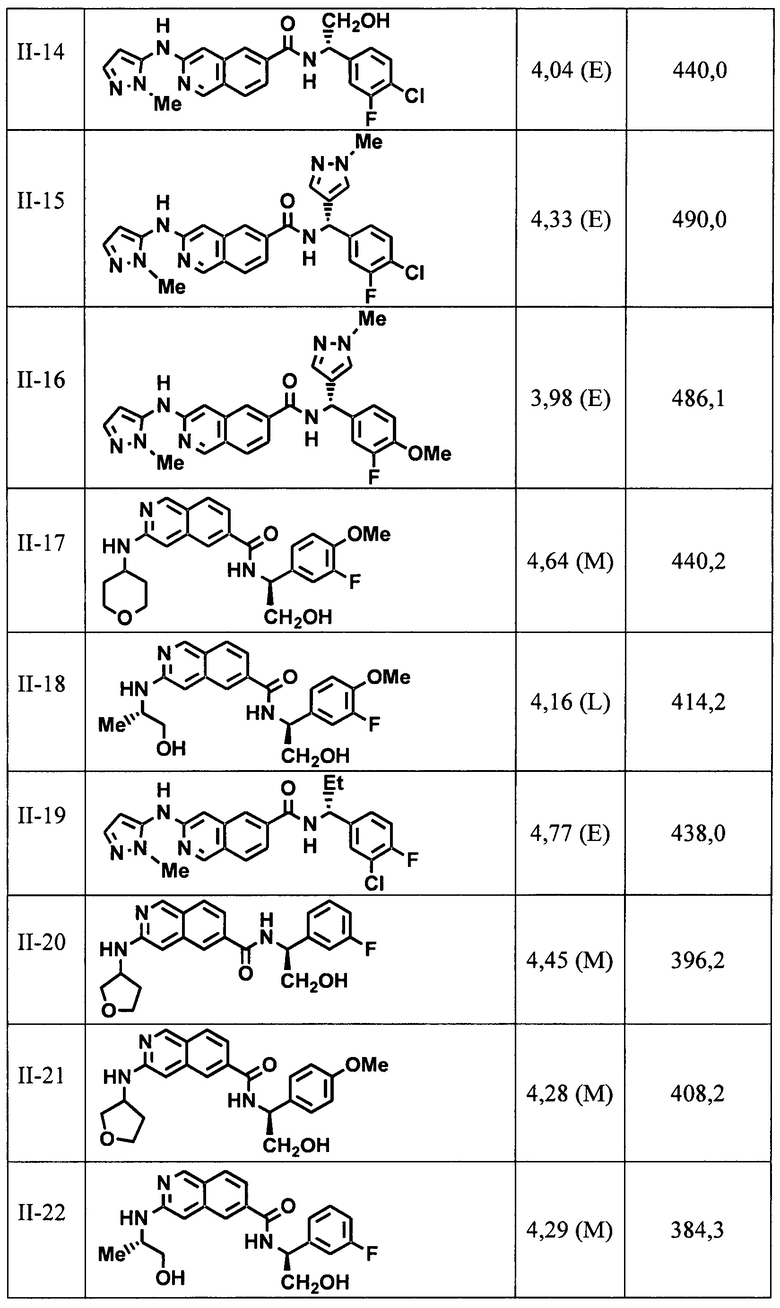
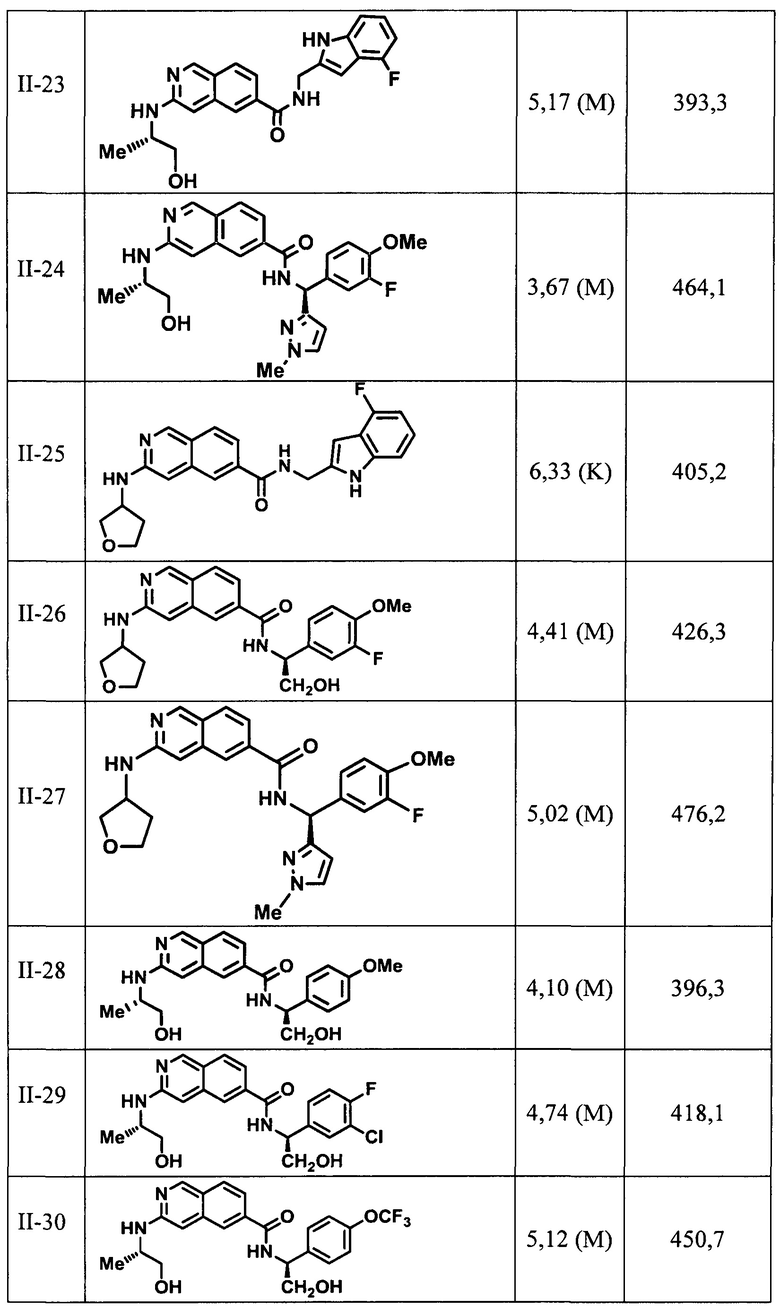


[00109] Соединения по настоящему изобретению могут быть получены разнообразными способами, проиллюстрированными на иллюстративных схемах реакций синтеза, которые представлены ниже. Исходные материалы и реагенты, используемые для получения этих соединений, в основном доступны от коммерческих поставщиков, таких как Sigma Aldrich Chemical Co., или их получают способами, известными специалистам в данной области техники. Общеприменимые методики синтеза описаны в трактатах, которые представлены в форме ссылок, таких как Fieser and Fieser's Reagents for Organic Synthesis; Wiley & Sons: New York, Volumes 1-21; R.C. LaRock, Comprehensive Organic Transformations, 2nd edition Wiley-VCH, New York 1999; Comprehensive Organic Synthesis, B. Trost and I. Fleming (Eds.) vol. 1-9 Pergamon, Oxford, 1991; Comprehensive Heterocyclic Chemistry, A.R. Katritzky and C.W. Rees (Eds) Pergamon, Oxford 1984, vol. 1-9; Comprehensive Heterocyclic Chemistry II, A.R. Katritzky and C.W. Rees (Eds) Pergamon, Oxford 1996, vol. 1-11; и Organic Reactions, Wiley & Sons: New York, 1991, Volumes 1-40. Следующие схемы реакций синтеза являются только иллюстрацией некоторых способов, которыми могут быть синтезированы соединения по настоящему изобретению, и различные модификации указанных схем реакций синтеза могут быть осуществлены и предусмотрены специалистом в данной области техники, который ознакомится со ссылками, содержащиеся в настоящм документе.
[00110] Исходные материалы и промежуточные соединения для схем реакций синтеза могут быть выделены и при желании очищены с применением традиционных методик. Специалист в данной области техники будет применять методики, которые с наибольшей вероятностью приведут к желаемому разделению. Обычно, такое разделение включает многофазную экстракцию, кристаллизацию из растворителя или смеси растворителей, дистилляцию, сублимацию или хроматографию. Хроматография может включать любое количество методов, в том числе, например: хиральную, обращенно-фазовую и нормально-фазовую; эксклюзионную; ионообменную хроматографию; методы и приборы для жидкостной хроматографии при высоком, среднем и низком давлении, аналитической в маленьком масштабе; имитацию движущегося слоя (ИДС) и препаративную толсто- или тонкослойную хроматографию, а также методики тонкослойной и флеш-хроматографии в маленьком масштабе. Такие материалы могут быть охарактеризованы с использованием традиционных величин, включая физические константы и спектральные данные.
[00111] Если не указано иное, реакции, раскрытые в настоящем документе, предпочтительно проводят в атмосфере инертного газа при атмосферном давлении и интервале температур реакции от приблизительно -78°С до около 150°С, более предпочтительно от приблизительно 0°С до около 125°С и наиболее предпочтительно и традиционно при приблизительно комнатной температуре (или температуре окружающей среды), например, около 20°С.
[00112] Диастереомерные смеси могут быть разделены на отдельные диастереомеры, на основе их физико-химических отличий, способами, хорошо известными специалистам в данной области техники, такими как хроматография и/или фракционная кристаллизация. Энантиомеры могут быть разделены путем превращения смеси энантиомеров в диастереомерную смесь, посредством реакции с использованием соответствующего оптически активного соединения (например, хирального вспомогательного вещества, такого как хиральный спирт или галогенангидрид кислоты Мошера), с разделением диастереомеров и превращением (например, посредством гидролиза) отдельных диастереомеров в соответствующие чистые энантиомеры. Кроме того, энантиомеры могут быть разделены с использованием хиральной ВЭЖХ колонки.
[00113] Одинарный стереоизомер, например, энантиомер, в значительной мере свободный от второго стереоизомера, может быть получен разделением рацемической смеси с применением способа, такого как образование диастереоизомеров, с использованием оптически активных разделяющих агентов (Eliel, E. and Wilen, S. "Stereochemistry of Organic Compounds," John Wiley & Sons, Inc., New York, 1994; Lochmuller, C.H., J. Chromatogr., 1975 113(3):283-302). Рацемические смеси могут быть разделены и выделены любым подходящим способом, включая: (1) образование ионных, диастереомерных солей с хиральными соединениями и разделение фракционной кристаллизацией или другими способами, (2) превращение смеси энантиомеров в диастереомерную смесь реакцией с использованием соответствующего оптически активного соединения (например, хирального вспомогательного вещества, такого как хиральный спирт или галогенангидрид кислоты Мошера), разделение диастереомеров и превращение (например, посредством гидролиза) отдельных диастереомеров в соответствующие чистые энантиомеры и (3) разделение в значительной мере чистых или обогащенных стереоизомеров непосредственно в хиральных условиях, (см., например, Drug Stereochemistry, Analytical Methods and Pharmacology, Irving W. Wainer, Ed., Marcel Dekker, Inc., New York 1993).
[00114] В соответствии со способом (1), диастереомерные соли могут быть образованы реакцией энантиомерно чистых хиральных оснований, таких как бруцин, хинин, эфедрин, стрихнин, α-метил-β-фенилэтиламин (амфетамин) и т.п., с асимметричными соединениями, несущими кислую функциональную группу, такую как карбоновая кислота и сульфоновая кислота. Диастереомерные соли могут быть разделены фракционной кристаллизацией или ионной хроматографией. В случае разделения оптических изомеров аминосоединений, добавление хиральных карбоновых или сульфоновых кислот, таких как камфорсульфоновая кислота, винная кислота, манделовая кислота или молочная кислота, может привести к образованию диастереомерных солей.
[00115] Альтернативно, в соответствии со способом (2), подлежащий разделению субстрат реагирует с одним энантиомером хирального соединения с образованием диастереомерной пары (Е. Eliel and S. Wilen, Stereochemistry of Organic Compounds, John Wiley & Sons, Inc., 1994, p.322). Диастереомерные соединения могут быть образованы реакцией асимметричного соединения с энантиомерно чистыми хиральными дериватизирующими реагентами, такими как ментиловые производные, с последующим разделением диастереомеров и гидролизом, с получением чистого или обогащенного энантиомера. Способ определения оптической чистоты включает получение хиральных сложных эфиров, таких как ментиловый сложный эфир, например, (-) ментилхлорформиат, в присутствии основания или эфира Мошера, α-метокси-α-(трифторметил)фенилацетата (Jacob III. J. Org. Chem., 1982 47:4165), из рацемической смеси и анализ 1Н ЯМР спектра на предмет присутствия двух атропизомерных энантиомеров или диастереомеров. Стабильные диастереомеры атропизомерных соединений могут быть разделены и выделены нормально- и обращенно-фазовой хроматографией в соответствии с методами разделения атропизомерных нафтил-изохинолинов (WO 96/15111). В соответствии со способом (3), рацемическая смесь двух энантиомеров может быть разделена хроматографией с использованием хиральной неподвижной фазы ("Chiral Liquid Chromatography" 1989 W.J. Lough, Ed., Chapman and Hall, New York; Okamoto, J. Chromatogr., 1990 513:375-378). Обогащенные или очищенные энантиомеры можно различить с помощью методов, применяемых для различения других хиральных молекул с асимметрическими атомами углерода, таких как оптическое вращение и круговой дихроизм.
[00116] Некоторые соединения проиллюстрированы на следующих схемах с обобщенными заместителями; однако, для специалиста в данной области техники будет очевидно, что природа групп R может варьировать с образованием различных соединений, охватываемых данным изобретением. Более того, условия реакции приведены в качестве примера, и альтернативные условия хорошо известны. Последовательности реакций в приведенных ниже примерах не являются ограничивающими объем изобретения, определенный Формулой изобретения.

[00117] 7-Бром-1Н-[1,6]нафтиридин-2-он (А-6) может быть получен двухстадийным аминированием 2,5-дибром-пиридина. Металлирование и охлаждение заливанием CO2 полученного литийорганического промежуточного соединения дает А-2. Превращение А-2 в соответствующий ацилазид с использованием дифенилфосфорилазида в трет-бутаноле и последующая перегруппировка Курциуса дают трет-бутил-(2,5-дибром-пиридин-4-ил)-карбамат А-3. Формилирование А-3 посредством металлирования и охлаждения заливанием ДМФА дает А-4, который обрабатывают литиевой солью трет-бутилацетата с получением А-5. Приведение А-5 в контакт с водным раствором кислоты приводит к удалению защитной группы с аминогруппы и внутримолекулярной циклизации и дегидратации с получением А-6.
[00118] Катализируемое палладием замещение бромида амином дает А-7. Желательный карбоксамид обрабатывают путем хлорирования лактама, который далее подвергают катализируемому палладием карбонилированию в МеОН, что дает соответствующий сложный эфир, который гидролизуют до соответствующей кислоты А-10, которую, в свою очередь, превращают в амид с использованием протоколов амидирования, разработанных для синтеза пептидов. Соединения, раскрытые в настоящем документе, где R2 представляет собой тетрагидропиран-4-ил, получены по методике, раскрытой на СХЕМЕ А.

[00119] В случаях, когда вытеснение бромида амином неэффективно, бромид превращают в соответствующий фторид В-2, который, в свою очередь, превращают в карбоксамид, по аналогии с последовательностью, раскрытой на СХЕМЕ А. Вытеснение фторида необходимым амином дает желательный амин В-7. Справочные примеры включают получение некоторых аминов в рамках настоящего изобретения. Другие амины, которые получают из коммерческих источников, включают: (3S)-3-амино-2-метил-бутанол (CASRN 74608-26-7), 3-амино-2-метил-бутанол (CASRN 6291-17-4), 1,3-диметил-1Н-пиразол-5-амин (CASRN 3524-32-1), 2-метил-пиридин-4-амин (CASRN18437-58-6), 1-метил-1H-пиразол-5-амин (CASRN 1192-21-8), тетрагидро-3-фуранамин (CASRN 88675-24-5), (3S)-тетрагидро-3-фуранамин (CASRN 104530-79-2), (3R)-тетрагидро-3-фуранамин (CASRN 111769-26-7) и 3-фтор-1-пропанамин (CASRN 462-41-9).

[00120] Изохинолины, охватываемые настоящим изобретением, могут быть получены, как раскрыто на СХЕМЕ С. 3-Амино-6-бром-изохинолин превращают в -6-бром-3-фтор-изохинолин, который подвергается вытеснению фтора амином с получением С-3. Карбоксиметилирование, омыление сложного эфира и конденсация с необходимым амином дают желательные изохинолинкарбоксамиды.
[00121] Необходимые амины могут быть получены, как раскрыто на СХЕМЕ D, на которой арил-гетероариламины (D-3; R=гетероарил) могут быть получены в стадиях 1-2. Добавление арила Гриньяра или ариллитиевого реагента к N-трет-бутилсульфинилиминам (D-2) дает амины (С-3) после гидролиза промежуточных сульфинамидных соединений. Хиральные амины получают добавлением арила Гриньяра или лития к хиральному сульфинамиду. (D.А. Cogan et al., Tetrahedron 1999 55:8883-8904). Сульфинилимины D-2, в свою очередь, доступны из большого пула альдегидов, которые могут быть с легкостью получены или приобретены.
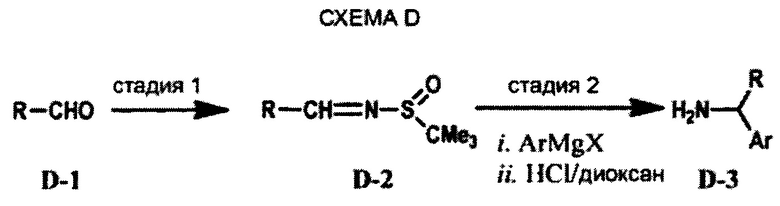
[00122] 4-Арил-1-бензил-пирролин-3-карбоновую кислоту получают из легко доступных замещенных бензальдегидов Е-1 конденсацией Кновенагеля с малоновой кислотой, с получением замещенной акриловой кислоты. Конденсация соответствующего галогенангидрида кислоты с (R)-4-фенилоксазолидин-2-оном вводит хиральное вспомогательное вещество, что дает хиральный Е-4 после 1,3-биполярного добавления азометин метилида. Гидролиз амида дает карбоновую кислоту, которая может быть превращена в изоцианат и конденсирована с амином, с последующим удалением защитной группы и получением соединения, находящегося в рамках настоящего изобретения.

[00123] Проиллюстрированные выше Схемы раскрывают общие методики, которые были применены к соединениям, охватываемым настоящим изобретением. Приведенные ниже примеры содержат дополнительные детали, полезные для введения различных структурных признаков, найденных в конкретных соединениях.
[00124] БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
[00125] Определение степени активности ERK у соединения формулы I может быть осуществлено многими методами прямого и непрямого определения. Некоторые характерные соединения, раскрытые в настоящем документе, анализировали в анализе ингибирования ERK (Пример 18). Интервал значений активности связывания ERK составлял от менее 1 нМ (наномолярный) до приблизительно 10 мкМ (микромолярный). Клеточный функциональный анализ (Пример 20) используют для определения воздействия ингибиторов ERK на нисходящее проведение сигнала в сигнальных путях с помощью исследования фосфорилирования P90RSK.
[00126] Цитотоксическую или цитостатическую активность характерных соединений формулы I определяют следующим образом: получение культуры пролиферирующих клеток опухоли млекопитающего в питательной среде для клеток, добавление соединения формулы I, выращивание клеток в течение периода от приблизительно 6 часов до около 5 дней; и измерение жизнеспособности клеток (Пример 19). Анализ клеток in vitro применяется для измерения выживаемости, т е. пролиферации (IC50), цитотоксичности (ЕС50).
[00127] ДОЗЫ И СПОСОБ ВВЕДЕНИЯ
[00128] В настоящем изобретении предлагаются фармацевтические композиции или лекарственные средства, содержащие соединения по изобретению и по меньшей мере один терапевтически инертный носитель, разбавитель или вспомогательное вещество, а также способы применения соединений по изобретению для получения таких композиций и лекарственных средств. В одном из примеров, соединения Формулы I с желательной степенью чистоты могут быть введены в препарат путем смешивания с физиологически приемлемыми носителями, т.е. носителями, которые являются нетоксичными для реципиентов в используемых в лекарственной форме дозах и концентрациях, при комнатной температуре и подходящем значении рН. рН состава будет зависеть от конкретно используемого соединения и его концентрации, но типично варьирует от приблизительно 3 до около 8. В одном из примеров, соединение Формулы I вводят в ацетатный буфер, при рН 5. В другом варианте реализации соединения Формулы I являются стерильными. Соединение может храниться, например, в форме твердого вещества или аморфной композиции, в форме лиофилизированного препарата или водного раствора.
[00129] Композиции получают, дозируют и вводят способом, согласующимся с Надлежащей медицинской практикой. Факторы, рассматриваемые в данном контексте, включают конкретное расстройство, подлежащее лечению, тяжесть расстройства, конкретного пациента, нуждающегося в лечении, клиническое состояние отдельного пациента, причину расстройства, место доставки агента, способ введения, схему введения и другие факторы, известные медицинским работникам. "Эффективное количество" соединения для введения будет определяться такими соображениями и представляет собой минимальное количество, необходимое для подавления активности ERK. Как правило, такое количество может быть ниже, чем количество, которое является токсичным для нормальных клеток или организма пациента в целом.
[00130] Фармацевтическая композиция (или препарат) для применения может быть упакована различными способами, в зависимости от способа, применяемого для введения лекарственного средства. В общем, промышленное изделие для дистрибьюции включает емкость, в которую помещен фармацевтический препарат в подходящей форме. Подходящие емкости хорошо известны специалистам в данной области и включают материалы, такие как бутыли (пластиковые и стеклянные), саше, ампулы, пластиковые пакеты, металлические цилиндры и т.п. Кроме того, емкость может включать элементы для контроля первого вскрытия, чтобы предупредить несанкционированный доступ к содержимому упаковки. Дополнительно, на емкости присутствует этикетка, где описано содержимое емкости. Этикетка может также содержать соответствующие предупреждения.
[00131] Могут быть получены препараты с пролонгированным высвобождением. Подходящие примеры препаратов с пролонгированным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие соединение Формулы I, причем матрицы находятся в форме профилированных изделий, например, пленок или микрокапсул. Примеры матриц для пролонгированного высвобождения включают полиэфиры, гидрогели (например, поли(2-гидроксиэтил-метакрилат) или поли(виниловый спирт)), полилактиды, сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамат, неразлагаемый этилен-винилацетат, разлагаемые сополимеры молочной кислоты-гликолевой кислоты, такие как LUPRON DEPOT™ (инъекционные микросферы, состоящие из сополимера молочной кислоты-гликолевой кислоты и лейпролида ацетата), а также поли-D-(-)-3-гидроксимасляную кислоту.
[00132] Доза для лечения пациентов может варьировать от приблизительно 0,1 мг до приблизительно 1000 мг соединения формулы I. Типичная доза может составлять от приблизительно 1 мг до около 300 мг соединения. Доза может вводиться 1 раз в день (QD), 2 раза в день (BID) или чаще, в зависимости от фармакокинетических и фармако динамических свойств, включая абсорбцию, распределение, метаболизм и экскрецию конкретного соединения. Кроме того, факторы токсичности могут влиять на дозы и схему введения. При пероральном введении, пилюля, капсула или таблетка может приниматься ежедневно или реже в течение указанного периода времени. Схема может быть повторена для нескольких циклов терапии.
[00133] Соединения данного изобретения могут быть введены любым подходящим способом, включая пероральное, местное (в том числе, буккальное и сублингвальное), ректальное, вагинальное, трансдермальное, парентеральное, подкожное, внутрибрюшинное, внутрилегочное, внутрикожное, интратекальное, эпидуральное и интраназальное введение, и, при необходимости, для местного лечения, внутриочагового введения. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение.
[00134] Соединения данного изобретения могут быть введены в любой традиционной форме для введения, например, таблетки, порошки, капсулы, растворы, дисперсии, суспензии, сиропы, спреи, суппозитории, гели, эмульсии, пластыри, и т.д. Такие композиции могут содержать компоненты, традиционные для фармацевтических препаратов, например, разбавители, носители, модификаторы рН, подсластители, наполнители и дополнительные активные агенты.
[00135] Типичный препарат готовят смешиванием соединения по настоящему изобретению и носителя или вспомогательного вещества. Подходящие носители и вспомогательные вещества хорошо известны специалистам в данной области техники и подробно описаны, например, в Ansel, Н.С., et al., Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems. Philadelphia: Lippincott, Williams & Wilkins, 2004; Gennaro, Alfbnso R., et al. Remington: The Science and Practice of Pharmacy. Philadelphia: Lippincott, Williams & Wilkins, 2000; and Rowe, R.C., Handbook of Pharmaceutical Excipients, Chicago, Pharmaceutical Press, 2005. Дополнительно, препараты могут содержать один или более буферных агентов, стабилизаторов, поверхностно-активных веществ, увлажняющих агентов, смазывающих агентов, эмульгаторов, суспендирующих агентов, консервантов, антиоксидантов, замутнителей, улучшающих скольжение агентов, облегчающих обработку средств, красителей, подсластителей, ароматизаторов, вкусовых добавок, разбавителей и других известных добавок, для достижения приятного внешнего вида лекарственного средства (т.е. соединения по настоящему изобретению или фармацевтической композиции на его основе) или содействия процессу производства фармацевтического продукта (т.е. лекарственного средства).
[00136] Для перорального введения, таблетки, содержащие различные вспомогательные вещества, такие как лимонная кислота, могут использоваться вместе с различными дезинтегрантами, такими как крахмал, альгиновая кислота и некоторые сложные силикаты, и связующими агентами, такими как сахароза, желатин и камедь. Кроме того, смазывающие агенты, такие как магния стеарат, натрия лаурилсульфат и тальк, часто являются пригодными для целей таблетирования. Дополнительно, твердые композиции подобного типа могут применяться в форме мягких и твердых заполненных желатиновых капсул. Предпочтительные материалы, таким образом, включают лактозу или молочный сахар и высокомолекулярный полиэтиленгликоль. Если для перорального введения желательными являются водные суспензии или эликсиры, активное соединение в них может быть объединено с различными подсластителями или вкусовыми добавками, окрашенными веществами или красителями, и, при желании, эмульгаторами или суспендирующими агентами, вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин или их комбинации.
[00137] Примером подходящей лекарственной формы для перорального применения является таблетка, содержащая приблизительно 25 мг, 50 мг, 100 мг, 250 мг или 500 мг соединения по изобретению в комбинации приблизительно с 90-30 мг безводной лактозы, приблизительно 5-40 мг натрий кроскармеллозы, приблизительно 5-30 мг поливинилпирролидона (ПВП) K30 и приблизительно 1-10 мг магния стеарата. Порошкообразные ингредиенты вначале перемешивают, и затем смешивают с раствором ПВП. Полученная композиция может быть высушена, гранулирована, смешана с магния стеаратом и спрессована в форме таблеток с использованием традиционного оборудования. Пример аэрозольного препарата может быть получен путем растворения соединения по изобретению, например, 5-400 мг, в подходящем буферном растворе, например, фосфатном буфере, и, при желании, добавления средства для повышения осмотического давления, например, соли, такой как натрия хлорид. Раствор может быть профильтрован, например, с использованием фильтра с размером пор 0,2 мкм, для удаления примесей и загрязняющих веществ.
[00138] В одном варианте реализации фармацевтическая композиция дополнительно содержит по меньшей мере один дополнительный антипролиферативный агент.
[00139] Вариант реализации, таким образом, включает фармацевтическую композицию, содержащую соединение Формулы I или его стереоизомер, таутомер или фармацевтически приемлемую соль. Дополнительный вариант включает фармацевтическую композицию, содержащую соединение Формулы I или его стереоизомер, таутомер или фармацевтически приемлемую соль, вместе с фармацевтически приемлемым носителем или вспомогательным веществом.
[00140] В изобретении дополнительно предлагаются ветеринарные композиции, содержащие по меньшей мере один активный ингредиент, как было определено выше, вместе с ветеринарным носителем. Ветеринарные носители представляют собой соединения, пригодные для цели введения, и могут представлять собой твердые, жидкие или газообразные материалы, которые в других отношениях являются инертными или приемлемыми для ветеринарии, а также совместимы с активным ингредиентом. Указанные ветеринарные композиции могут быть введены парентерально, перорально или любым другим желательным способом.
[00141] Комбинированная терапия
[00142] Соединения формулы I могут использоваться отдельно или в комбинации с другими терапевтическими агентами для лечения заболевания или расстройства, представленных в настоящем документе, таких как гиперпролиферативное расстройство (например, рак). В некоторых вариантах реализации соединение формулы I объединяют в комбинированном фармацевтическом препарате или схеме лечения в форме комбинированной терапии со вторым соединением, которое обладает анти-гиперпролиферативными свойствами или пригодно для лечения гиперпролиферативного расстройства (например, рака). Второе соединение в комбинированном фармацевтическом препарате или схеме лечения предпочтительно обладает дополняющей активностью к соединению формулы I, таким образом, что они не оказывают побочного действия друг на друга. Комбинированная терапия может обеспечивать "синергию" и оказывать "синергетическое" воздействие, т.е. эффект, достигаемый, если активные ингредиенты при совместном применении оказывают воздействие, превышающее сумму эффектов от применения соединений по отдельности.
[00143] Комбинированная терапия может вводиться в схеме совместно или последовательно. При последовательном введении, комбинация может вводиться в виде двух или более доз. Сочетанное введение включает одновременное введение с использованием отдельных препаратов или единого фармацевтического препарата и последовательное введение в любом порядке, при котором предпочтительно существует период времени, когда оба (или все) активные агенты одновременно проявляют свою биологическую активность.
[00144] Подходящие дозы для любого из перечисленных выше, совместно вводимых агентов являются такими, которые в настоящее время используются, и могут быть снижены благодаря сочетанному действию (синергии) вновь идентифицированного агента и других химиотерапевтических агентов или препаратов.
[00145] Комбинированная терапия в соответствии с настоящим изобретением, таким образом, включает введение по меньшей мере одного соединения формулы I или его стереоизомера, геометрического изомера, таутомера или фармацевтически приемлемой соли, а также применение по меньшей мере еще одного способа лечения рака. Количества соединения(й) формулы I и другого(их) фармацевтически активного(ых) химиотерапевтического(их) агента(ов), а также соответствующие схемы введения будут выбираться в порядке достижения желательного сочетанного терапевтического эффекта.
[00146] ПРОИЗВОДСТВЕННЫЕ ИЗДЕЛИЯ
[00147] В другом варианте реализации изобретения предлагается производственное изделие или "набор", содержащее материалы, пригодные для лечения заболеваний и расстройств, раскрытых выше. В одном варианте реализации набор включает емкость, содержащую соединение формулы I или его стереоизомер, таутомер или фармацевтически приемлемую соль. Набор может дополнительно включать этикетку или аннотацию на емкости или сопровождающий ее. Термин «аннотация» используют для обозначения инструкций, которые традиционно вкладывают в коммерческие упаковки терапевтических продуктов и которые содержат информацию о показаниях, применении, дозах, способе введения, противопоказаниях и/или предупреждения относительно применения таких терапевтических продуктов. Подходящие емкости включают, например, бутыли, флаконы, шприцы, блистерную упаковку и т.д. Емкость может быть изготовлена из различных материалов, таких как стекло или пластик. Емкость может содержать соединение формулы I или его препарат, которые эффективны при лечении состояния, и может быть оборудована стерильным портом доступа (например, емкость может представлять собой пакет для внутривенного раствора или флакон с пробкой, прокалываемой иглой для подкожных инъекций). По меньшей мере один активный агент в композиции представляет собой соединение формулы I. Альтернативно или дополнительно, промышленное изделие может включать вторую емкость, содержащую фармацевтический разбавитель, такой как бактериостатическая вода для инъекций (БВДИ), фосфатно-солевой буфер, раствор Рингера и раствор декстрозы. Оно может дополнительно включать другие материалы, желательные с коммерческой и потребительской точки зрения, включая другие буферные вещества, разбавители, фильтры, иглы и шприцы.
[00148] В другом варианте реализации наборы пригодны для доставки твердых лекарственных форм соединения формулы I для перорального применения, таких как таблетки или капсулы. Такой набор может включать несколько единиц лекарственной формы. Примером такого набора является «блистерная упаковка». Блистерные упаковки хорошо известны в упаковочной промышленности и широко используются для упаковки фармацевтических дозированных лекарственных форм.
[00149] В соответствии с одним вариантом реализации, набор может включать (а) первую емкость с соединением формулы I, содержащимся в ней; и необязательно (б) вторую емкость со вторым фармацевтическим препаратом, содержащимся в ней, причем фармацевтический препарат содержит второе соединение с анти-гиперпролиферативной активностью. Альтернативно или дополнительно, набор может дополнительно включать третью емкость, содержащую фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (БВДИ), фосфатно-солевой буфер, раствор Рингера и раствор декстрозы. Он может дополнительно может включать другие материалы, желательные с коммерческой и потребительской точки зрения, включая другие буферные вещества, разбавители, фильтры, иглы и шприцы.
[00150] Следующие примеры иллюстрируют получение и биологическую оценку соединений в объеме изобретения. Указанные примеры и препаративные примеры, приведенные ниже, предназначены для более четкого понимания и применения настоящего изобретения специалистами в данной области техники. Их не следует рассматривать как ограничивающие объем изобретения, но исключительно как иллюстративные и репрезентативные. Справочные примеры, приведенные ниже, иллюстрируют методики получения аминов, необходимых для сборки ингибиторов ERK, охватываемых настоящим изобретением.
[00151] Следующие хроматографические методы приведены со ссылкой на методики, перечисленные в Табл. I и II.
[00152] Метод А: Эксперименты проводят с использованием системы Agilent или Shimadzu, с источника ионизации ESI и колонки Xtimate С18 (3 мкм), 30×2,1 мм, при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 90% воды, содержащей 0,0375% ТФУ (растворитель А), и 10% ацетонитрила, содержащего 0,01875% ТФУ (растворитель В), с нарастанием до 20% растворителя А и до 80% растворителя В в течение 2 минут.
[00153] Метод В: Эксперименты проводят с использованием системы Agilent или Shimadzu, с применением ESI в качестве источника ионизации и колонки Xtimate С18 (3 мкм), 30×2,1 мм, при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 100% воды, содержащей 0,0375% ТФУ (растворитель А), и 0% ацетонитрила, содержащего 0,01875% ТФУ (растворитель В), с подъемом до 40% растворителя А и до 60% растворителя В в течение 2 минут.
[00154] Метод С: Эксперименты проводят с использованием системы Agilent или Shimadzu, с применением ESI в качестве источника ионизации и колонки Xtimate С18 (3 мкм), 30×2,1 мм, при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 100% воды, содержащей 0,0375% ТФУ (растворитель А), и 0% ацетонитрила, содержащего 0,01875% ТФУ (растворитель В), с подъемом до 70% растворителя А и до 30% растворителя В в течение 2 минут.
[00155] Метод D: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1100 и масс-спектрометра Agilent MCD с применением ESI в качестве источника ионизации, используя колонку Agilent ZORBAX SB-C18 100×3,0 мм и скорость потока 0,7 мл/мин. Система растворителей представляет собой градиент, начинающийся с 98% воды, содержащей 0,05% ТФУ (растворитель А), и 2% ацетонитрила, содержащего 0,05% ТФУ (растворитель В), с подъемом до 2% растворителя А и до 98% растворителя В в течение 25,5 минут. Конечный градиент растворителей удерживают постоянным еще в течение 2,5 минут.
[00156] Метод Е: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1100 и масс-спектрометра Agilent MCD с применением ESI в качестве источника ионизации, используя колонку Agilent ZORBAX SB-С18 30×2,1 мм и скорость потока 0,4 мл/мин. Система растворителей представляет собой градиент, начинающийся с 97% воды, содержащей 0,05% ТФУ (растворитель А), и 3% ацетонитрила, содержащего 0,05% ТФУ (растворитель В), с подъемом до 5% растворителя А и до 95% растворителя В в течение 7 минут. Конечный градиент растворителей удерживают постоянным еще в течение 1,5 мин.
[00157] Метод F: Эксперименты проводят с использованием системы жидкостной хроматографии со сверхвысоким давлением Waters Acquity с масс-спектрометром Waters-LCT Premier XE, с использованием ESI в качестве источника ионизации, используя колонку Acquity UPLC ВЕН С18, 1,7 мкм, 2,1*50 мм и скорость потока 0,6 мл/мин. Система растворителей представляет собой градиент, начинающийся с 98% воды, содержащей 0,05% ТФУ (растворитель А), и 2% ацетонитрила, содержащего 0,05% ТФУ (растворитель В), с подъемом до 2% растворителя А и до 98% растворителя В в течение 2,5 минут. Конечный градиент растворителей удерживают постоянным еще в течение 0,5 мин.
[00158] Метод G: Эксперименты проводят с использованием системы жидкостной хроматографии со сверхвысоким давлением Waters Acquity с масс-спектрометром Waters-LCT Premier XE, с применением ESI в качестве источника ионизации, используя колонку Acquity UPLC ВЕН С18, 1,7 мкм, 2,1*50 мм и скорость потока 0,6 мл/мин. Система растворителей представляет собой градиент, начинающийся с 98% воды, содержащей 0,05% ТФУ (растворитель А), и 2% ацетонитрила, содержащего 0,05% ТФУ (растворитель В), с подъемом до 2% растворителя А и до 98% растворителя В в течение 17 минут. Конечный градиент растворителей удерживают постоянным еще в течение 1,5 минут.
[00159] Метод Н: Эксперименты проводят с использованием системы жидкостной хроматографии со сверхвысоким давлением Waters Acquity UHPLC с масс-спектрометром Waters-LCT Premier XE, с применением ESI в качестве источника ионизации, используя колонку Acquity UPLC ВЕН С18, 1,7 мкм, 2,1*50 мм и скорость потока 0,6 мл/мин. Система растворителей представляет собой градиент, начинающийся с 98% воды, содержащей 0,05% ТФУ (растворитель А), и 2% ацетонитрила, содержащего 0,05% ТФУ (растворитель В), с подъемом до 2% растворителя А и до 98% растворителя В в течение 7,5 минут. Конечный градиент растворителей удерживают постоянным еще в течение 1,0 минуты.
[00160] Метод I: Эксперименты проводят с использованием системы Agilent или Shimadzu, ESI в качестве источника ионизации, используя колонку Xtimate С18 (3 мкм), 30×2,1 мм, при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 70% воды, содержащей 0,0375% ТФУ (растворитель А), и 30% ацетонитрила, содержащего 0,01875% ТФУ (растворитель В), с подъемом до 10% растворителя А и до 90% растворителя В в течение 2 минут.
[00161] Метод J: Эксперименты проводят с использованием системы Agilent или Shimadzu, с применением ESI в качестве источника ионизации, используя колонку Xtimate С18 (3 мкм), 30×2,1 мм, при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 90% воды, содержащей 0,0375% ТФУ (растворитель А), и 10% ацетонитрила, содержащего 0,01875% ТФУ (растворитель В), с подъемом до 20% растворителя А и до 80% растворителя В в течение 7 минут.
[00162] Метод К: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1200 и масс-спектрометра Agilent MCD, с применением ESI в качестве источника ионизации, используя колонку Waters Sunfire С18 4,6×50 мм (или Agilent Poroshell 120 SB C18 4,6×30 мм), при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 95% воды, содержащей 0,01% ТФУ (растворитель А), и 5% ацетонитрила, содержащего 0,01% ТФУ (растворитель В), с подъемом до 5% растворителя А и 95% растворителя В в течение 8,0 минут. Конечный градиент растворителей удерживают постоянным еще в течение 2,0 минут.
[00163] Метод L: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1200 и масс-спектрометра Agilent MCD, с применением ESI в качестве источника ионизации, используя колонку Waters Xbridge C18 4,6×50 мм (или YMC Triart C18 4,6×50 мм), при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 95% воды, содержащей 0,01% аммиака (растворитель А), и 5% ацетонитрила (растворитель В), с подъемом до 5% растворителя А и до 95% растворителя В в течение 8,0 минут. Конечный градиент растворителей удерживают постоянным еще в течение 2,0 минут
[00164] Метод М: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1200 и масс-спектрометра Agilent MCD, с применением ESI в качестве источника ионизации, используя колонку Waters Xbridge C18 4,6×50 мм (или YMC Triart C18 4,6×50 мм), при скорости потока 1,2 мл/мин. Система растворителей представляет собой градиент, начинающийся с 95% воды, содержащей 10 мМ аммония гидрокарбоната (растворитель А), и 5% ацетонитрила (растворитель В), с подъемом до 5% растворителя А и до 95% растворителя В в течение 8,0 минут. Конечный градиент растворителей удерживают постоянным еще в течение 2,0 минут.
[00165] Метод N: Эксперименты проводят с использованием системы ВЭЖХ Agilent 1200 и масс-спектрометра Agilent MCD, с применением ESI в качестве источника ионизации, используя колонку Waters Xbridge C18 4,6 ×50 мм (или YMC Triart С18 4,6×50 мм), при скорости потока 1,2 мл/минуту. Система растворителей представляет собой градиент, начинающийся с 95% воды, содержащей 10 мМ аммония гидрокарбоната (растворитель А), и 5% ацетонитрила (растворитель В), с подъемом до 5% растворителя А и до 95% растворителя В в течение 1,6 минут. Конечный градиент растворителей удерживают постоянным еще в течение 2,0 минут.
[00166] Справочный Пример 1
[00167] 2-Окса-бицикло[2,2,1]гептан-5-амина гидрохлорид

[00168] Стадия 1: К раствору 3-оксо-2-окса-бицикло[2,2,1]гептан-5-карбоновой кислоты (20а, 0,50 г, 3,2 ммоль) в толуоле (5,0 мл) добавляют ДФФА (0,97 г, 3,5 ммоль) и ТЭА (384 мг, 3,80 ммоль). Смесь перемешивают при 100°С в атмосфере N2, и затем добавляют фенилметанол (1,0 г, 10 ммоль). Полученную смесь перемешивают при 130°С еще в течение 2 часов. Реакцию гасят водой (1,0 мл) и разбавляют EtOAc (300 мл). Органическую фракцию промывают раствором соли (3×50 мл), сушат (Na2SO4), фильтруют и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc, с получением 600 мг (72%) 20b в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, CDCl3) δ 7,39-7,31 (м, 5Н), 5,08-5,00 (м, 3Н), 3,87 (с, 1Н), 2,78 (с, 1Н), 2,20 (м, 1Н), 2,14 (д, J=9 Гц, 1Н), 1,97 (т, J=20,5 Гц, 1Н), 1,71 (д, J=14 Гц, 1Н).
[00169] Стадия 2: К раствору 20b (1,0 г, 3,8 ммоль) и CaCl2 (0,85 г, 7,6 ммоль) в EtOH (50 мл) добавляют NaBH4 (0,58 г, 15 ммоль) при 0°С. Смесь перемешивают при комнатной температуре в течение 12 часов. Избыток реагента разлагают с помощью конц. HCl, и раствор упаривают. Остаток экстрагируют CHCl3 (3×100 мл), промывают водой (50 мл), раствором соли (50 мл), сушат (Na2SO4). После упаривания неочищенный продукт перекристаллизуют из петролейного эфира с получением 750 мг (75%) 22 в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 7,38-7,31 (м, 5Н), 7,25 (д, J=13,5 Гц, 1Н), 4,99 (с, 1Н), 4,53 (д, J=4,0 Гц, 1Н), 4,48 (т, J=10,0 Гц, 1Н), 4,09 (д, J=4,0 Гц, 1Н), 3,73 (т, J=15,5 Гц, 1Н), 3,44 (м, 1Н), 3,30 (м, 1Н), 1,99 (д, J=7,0 Гц, 1Н), 1,80-1,74 (м, 2Н), 1,57 (т, J=12,5 Гц, 1Н), 1,26 (с, 1Н).
[00170] Стадия 3: К раствору 22 (100 мг, 0,380 ммоль) и пиридина (3,0 мл) в толуоле (6,0 мл) при 0°С добавляют по каплям раствор TsCl (290 мг, 1,52 ммоль) в толуоле (3,0 мл). Смесь нагревают до комнатной температуры и перемешивают в течение 2 дней. Далее реакционную смесь нагревают до 120°С, выдерживая при этой температуре в течение 16 часов. Реакционную смесь охлаждают, и растворитель удаляют под вакуумом. Остаток очищают обращенно-фазовой комби-флеш хроматографией, элюируя MeCN/H2O (0,3% NH4HCO3) градиент (5-95% MeCN), с получением 58 мг (62%) 24а в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 7,37-7,31 (м, 5Н), 5,09 (с, 1Н), 4,33 (с, 1Н), 3,73 (д, J=5,5 Гц, 1Н), 3,63-3,61 (м, 2Н), 3,48 (д, J=7,5 Гц, 1Н), 2,53 (с, 1Н), 2,07-2,04 (м, 2Н), 1,72 (д, J=10,5 Гц, 1Н), 1,61 (д, J=11,0 Гц, 1Н), 1,42 (д, J=14 Гц, 1Н).
[00171] Стадия 4: Смесь 24а (0,50 г, 2,0 ммоль) и Pd/C (50 мг) в МеОН (20 мл) перемешивают в атмосфере водорода при комнатной температуре в течение 16 часов. рН смеси доводят приблизительно до 4 с помощью смеси 1 н HCl/метанола. Полученную смесь фильтруют сквозь Celite®, и фильтрат упаривают при сниженном давлении с получением 300 мг (100%) 24b в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 4,43 (с, 1Н), 3,72-3,70 (м, 2Н), 3,54 (д, J=7,5 Гц, 1Н), 3,50-3,48 (м, 2Н), 2,76 (с, 1Н), 2,20-2,15 (м, 2Н), 1,96 (д, J=11,0 Гц, 1Н), 1,78 (д, J=11,0 Гц, 1Н), 1,61 (д, J=11,0 Гц, 1Н).
[00172] Справочный Пример 2
[00173] (S)-1-(1-Аминоэтил)циклопропанол
[00174] Стадия 1: К раствору (S)-этил-2-аминопропаноата гидрохлорида (4,59 г, 30,0 ммоль) и K2CO3 (12,4 г, 90,0 ммоль) в MeCN добавляют (бромметил)бензол (12,9 г, 75,0 ммоль) при комнатной температуре. Смесь перемешивают при 70°С, выдерживая при этой температуре в течение 14 часов. Реакционную смесь гасят водн. NH4Cl. После упаривания, водную фракцию экстрагируют EtOAc. Объединенные органические фракции сушат (MgSO4), фильтруют и упаривают под вакуумом. Неочищенный продукт очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (100:1), с получением 8,8 г (98%) (S)-этил-2-(дибензиламино)пропаноата (26): ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 298,2 [М+Н]+.
[00175] Стадия 2: К раствору 26 (8,80 г, 29,5 ммоль) и титана тетраизопропоксида (1,28 г, 5,90 ммоль) в сухом ТГФ (100 мл) добавляют EtMgBr (30 мл, 90 ммоль, 3,0 н в ТГФ) при 0°С. После перемешивания при комнатной температуре в течение ночи смесь охлаждают до 0°С и гасят раствором NH4Cl. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc. Объединенные органические фракции сушат (MgSO4), фильтруют и упаривают под вакуумом. Неочищенный продукт очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (20:1), с получением 7,5 г (90%) 7,5 г (90%) (S)-1-(1-(дибензиламино)этил)циклопропанола (28). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 282,1 [М+Н]+.
[00176] 1761 Стадия 3: К раствору 28 (7,50 г, 26,6 ммоль) в МеОН (80 мл) при комнатной температуре добавляют Pd(OH)2/C (1,50 г). Смесь перемешивают в атмосфере Н2 (1 атм) при комнатной температуре в течение 15 часов. После фильтрации и упаривания остаток очищают хроматографией на SiO2, элюируя смесью ДХМ/МеОН (15:1), с получением 1,4 г (54%) (S)-1-(1-аминоэтил)циклопропанола (30). 1Н ЯМР (500 МГц, CDCl3) δ 2,58 (к, J=6,5 Гц, 1Н), 2,18 (с, 3Н), 1,17 (д, J=6,5 Гц, 3Н), 0,80-0,74 (м, 2Н), 0,70-0,51 (м, 2Н).
[00177] Справочный Пример 3
[00178] (4-Фтор-1Н-индол-2-ил)метанамин (38)
[00179] Стадия 1: Натрий (2,30 г, 100 ммоль) добавляют к безводному EtOH (80 мл) при 0-5°С, выдерживая при этой температуре в течение 10 минут, с получением свежеприготовленного раствора натрия этоксида. Раствор 1-фтор-2-метил-3-нитробензола (14,4 г, 93,0 ммоль) и диэтилоксалата (15,3 г, 105 ммоль) в EtOH (80 мл) добавляют к вышеописанному раствору, и полученную смесь далее кипятят с обратным холодильником в течение 45 минут. После охлаждения раствор темно-красного цвета разбавляют водой (100 мл). После удаления этанола остаток экстрагируют EtOAc. Водную фракцию подкисляют 2 н HCl до рН приблизительно 3-4 и экстрагируют ДХМ. Органические фракции промывают водой, сушат и упаривают с получением 4,5 г (21%) 3-(2-фтор-6-нитрофенил)-2-оксопропановой кислоты (32) в виде масла красного цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда:245,1 [M+NH4]+.
[00180] 1801 Стадия 2: Раствор 32 (4,8 г, 31 ммоль) в 4% растворе NH4OH (60 мл) добавляют к суспензии железа (II) гидроксида, приготовленной из железа (II) сульфата гептагидрата (52,45 г, 188,7 ммоль), и концентрированного раствора NH4OH (23 мл) в воде (200 мл). Смесь выдерживают при температуре кипения в течение 5 минут. Железа (II) гидроксид отделяют фильтрацией, затем повторно промывают разбавленным раствором NH4OH и водой. Фильтрат подкисляют разбавленной HCl. Полученное твердое вещество отделяют фильтрацией с получением 1,2 г (22%) 4-фтор-1H-индол-2-карбоновой кислоты (34) в виде твердого вещества белого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00181] Стадия 3: К раствору 34 (179 мг, 1,00 ммоль) в безводном ДМФА (2,0 мл) добавляют NH4Cl (160 мг, 3,00 ммоль), ЭДКИ (395 мг, 2,20 ммоль), HOBt (297 мг, 2,20 ммоль) и ТЭА (303 мг, 3,00 ммоль) при комнатной температуре. После перемешивания при комнатной температуре в течение 3 часов смесь гасят H2O (10 мл). Полученную смесь экстрагируют EtOAc (3×6 мл). Объединенные экстракты сушат и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (от 5:1 до 3:1), с получением 130 мг (73%) 4-фтор-1Н-индол-2-карбоксамида (36) в виде твердого вещества белого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 179,1 [М+Н]+.
[00182] 1821 Стадия 4: К раствору 36 (130 мг, 0,730 ммоль) в безводном ТГФ (5,0 мл) добавляют LiAlH4 (138 мг, 3,65 ммоль) при 0-5°С. Реакционную смесь нагревают до 80°С, выдерживая при этой температуре в течение ночи. После охлаждения до комнатной температуры смесь обрабатывают води. Na2SO4. Полученную смесь экстрагируют EtOAc (3×10 мл). Объединенные органические фракции сушат и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc/ТЭА (10:10:0,5), с получением 40 мг (33%) (4-фтор-1H-индол-2-ил)метанамина (38) в виде твердого вещества бледно-желтого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 11,22 (с, 1Н), 7,14 (д, J=8,0 Гц, 1Н), 6,97 (м, 1Н), 6,70 (м, 1Н), 6,28 (с, 1Н), 3,82 (с, 2Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 148,1 [М+Н-17]+.
[00183] Справочный Пример 4
[00184] (S)-4-(Амино(1-метил-1H-пиразол-4-ил)метил)-2-хлорбензонитрила гидрохлорид (44)
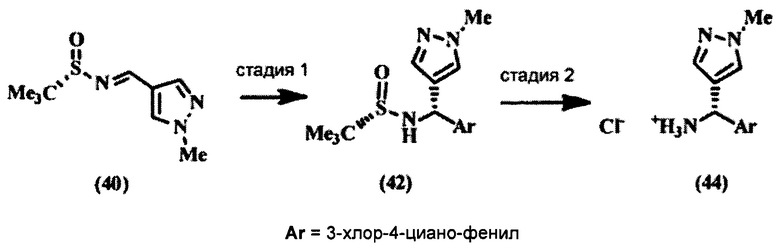
[00185] Стадия 1: К раствору 1-метил-1H-пиразол-4-карбальдегида (3,0 г, 27 ммоль) в ТГФ (100 мл) добавляют (S)-2-метилпропан-2-сульфинамид (6,6 г, 54 ммоль) и Ti(OEt)4 (22,3 г, 98,0 ммоль). Реакционную смесь нагревают до 65°С, выдерживая при этой температуре в течение 12 часов. После охлаждения смесь выливают в воду. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc (3×100 мл). Органическую фракцию промывают водой (3×50 мл), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (4:1), с получением 5,6 г (98%) (S,E)-2-метил-N-((1-метил-1H-пиразол-4-ил)метилен)пропан-2-сульфинамида 40 в виде бесцветного масла. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 214,1 [М+Н]+.
[00186] Стадия 2: К суспензии LiCl (920 мг, 22,0 ммоль) в ТГФ (20 мл) при комнатной температуре добавляют изопропилмагния хлорид (2,0 н в ТГФ, 11 мл, 22 ммоль). Полученную смесь перемешивают при 40°С в течение 30 минут. Смесь охлаждают до -78°С, и добавляют 4-бром-2-хлорбензонитрил (4,00 г, 18,5 ммоль) в ТГФ (50 мл). Полученную смесь перемешивают при 0°С в течение 1 часа, после чего охлаждают до -78°С. Далее добавляют 40 (2,8 г, 13 ммоль) в ТГФ (50 мл). Реакционную смесь перемешивают при 0°С в течение 4 часов, после чего гасят водой (50 мл). Полученную смесь экстрагируют EtOAc (3×100 мл). Органическую фракцию промывают насыщ. NaCl (3×50 мл), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя ДХМ/МеОН (100:1), с получением 1,0 г (19%) 42 в виде твердого вещества желтого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 351,2 [М+Н]+.
[00187] Стадия 3: К раствору 42 (1,0 г, 3,0 ммоль) в EtOAc (20 мл) при комнатной температуре добавляют 3 н HCl/EtOAc (2,2 мл). После перемешивания в течение 1 часа, твердое вещество отфильтровывают с получением 500 мг (68%) 44 в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, CD3OD) δ 7,96 (д, J=8,0 Гц, 1Н), 7,84-7,82 (м, 2Н), 7,67-7,64 (м, 2Н), 5,80 (с, 1Н), 3,93 (с, 3Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 247,1 [М+Н]+.
[00188] Справочный Пример 5
[00189] (S)-(4-Хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил) метанамина гидрохлорид (50а)
[00190] Стадия 1: К раствору 1-метил-1H-пиразол-4-карбальдегида (2,2 г, 20 ммоль) в ТГФ (50 мл) добавляют (R)-2-метилпропан-2-сульфинамид (4,8 г, 40 ммоль) и Ti(OEt)4 (9,2 г, 40 ммоль). Реакционную смесь нагревают до 65°С, выдерживая при этой температуре в течение 14 часов. После охлаждения смесь выливают в воду. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc. Органическую фракцию упаривают и очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (5:1), с получением 4,0 г (83%) (R,E)-2-метил-N-((1-метил-1H-пиразол-4-ил)метилен)пропан-2-сульфинамида (46). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 214,1 [М+Н]+.
[00191] Стадия 2: К смеси 4-бром-1-хлор-2-фторбензола (11,7 г, 56,0 ммоль) и магниевой стружки (2,1 г, 84 ммоль) в ТГФ (150 мл) при комнатной температуре добавляют несколько капель 1,2-дибромэтана (1,1 г, 5,6 ммоль). Смесь перемешивают при комнатной температуре в течение 1,5 часов. После охлаждения до -78°С добавляют (R,E)-2-метил-N-((1-метил-1H-пиразол-4-ил)метилен)пропан-2-сульфинамид (4,00 г, 18,7 ммоль) и перемешивают при -78°С в течение 6 часов. Реакцию гасят водн. раствором NH4Cl и экстрагируют EtOAc. Объединенные органические фракции сушат (MgSO4), фильтруют и упаривают.Неочищенный продукт очищают хроматографией на SiO2, элюируя смесью ДХМ/МеОН (150:1), с получением 2,9 г (45%) (R)-N-((S)-(4-хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метил)-2-метилпропан-2-сульфинамида (48). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 344,1 [М+Н]+.
[00192] Стадия 3: К раствору 48 (2,9 г, 8,4 ммоль) в МТБЭ (40 мл) добавляют 3 н HCl/метанол (6,0 мл, 18 ммоль). Смесь перемешивают в течение 2 часов при комнатной температуре. Полученное твердое вещество отфильтровывают и промывают МТБЭ с получением 650 мг (35%) 50а. 1Н ЯМР (500 МГц, CD3OD) δ 7,46-7,43 (м, 2Н), 7,38 (с, 1Н), 7,31 (дд, J=10,5, 2,0 Гц, 1Н), 7,21 (дд, J=8,5, 1,5 Гц, 1Н), 5,13 (с, 1Н), 3,85 (с, 3Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 240,0 [М+Н]+.
[00193] (S)-(1-Метил-1H-пиразол-4-ил)(4-(трифторметокси)фенил)метанамина гидрохлорид (50b) получают аналогичным образом, за исключением того, что на стадии 2 заменяют 4-бром-1-хлор-2-фторбензол на 4-трифторметокси-бромбензол. 1Н ЯМР (500 МГц, CD3OD) δ 7,74 (с, 1Н), 7,65-7,63 (м, 3Н), 7,42 (д, J=8,5 Гц, 2Н), 5,73 (с, 1Н), 3,94 (с, 3Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 272,1 [М+Н-17]+.
[00194] (S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлорид (50с) получают аналогичным образом, за исключением того, что на стадии 2 заменяют 4-бром-1-хлор-2-фторбензол на 4-метокси-3-фтор-1-бромбензол. 1Н ЯМР (500 МГц, CD3OD) δ 7,58 (д, J=1,5 Гц, 1Н), 7,24-7,17 (м, 3Н), 6,55 (д, J=2,0 Гц 1Н), 5,87 (с, 1Н), 3,92 (с, 3H), 3,68 (с, 3H). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 236,3 [М+Н]+.
[00195] (S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлорид (50d) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 1-метил-1H-пиразол-4-карбальдегид на 1-метил-1H-пиразол-3-карбальдегид, и на стадии 2 используют 4-метокси-3-фтор-1-бромбензол вместо 4-бром-1-хлор-2-фторбензола. 1Н ЯМР (500 МГц, CD3OD) δ 7,62 (с, 1Н), 7,26-7,15 (м, 3H), 6,15 (с, 1Н), 5,54 (с, 1Н), 3,93 (с, 3H), 3,91 (с, 3H). ЖХМС соотношение массы и заряда: 219,1 [М+Н-17]+.
[00196] (S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-5-ил)метанамина гидрохлорид (50е) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 1-метил-1H-пиразол-4-карбальдегид на 1-метил-1H-пиразол-5-карбальдегид, и на стадии используют 2 4-метокси-3-фтор-1-бромбензол вместо 4-бром-1-хлор-2-фторбензола.
[00197] (S)-(3-Фтор-фенил)(1-метил-1H-пиразол-5-ил)метанамина гидрохлорид (50f) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 1-метил-1H-пиразол-4-карбальдегид на 1-метил-1H-пиразол-5-карбальдегид, и на стадии 2 используют 4-метокси-3-фтор-1-бромбензол вместо 1-бром-3-фторбензола.
[00198] (S)-(4-Хлор-3-фторфенил)(1-метил-1H-пиразол-5-ил)метанамина гидрохлорид (50 г) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 1-метил-1H-пиразол-4-карбальдегид на 1-метил-1H-пиразол-5-карбальдегид.
[00199] (S)-(3-Фтор-фенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлорид (50h) получают аналогичным образом, за исключением того, что на стадии 2 используют 4-метокси-3-фтор-1-бромбензол вместо 1-бром-3-фторбензола.
[00200] (S)-(4-Метокси-фенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлорид (50i) получают аналогичным образом, за исключением того, что на стадии 2 используют 4-метокси-1-бромбензол вместо 1-бром-3-фторбензола.
[00201] Справочный Пример 6
[00202] (S)-2-Амино-2-(3-фторфенил)этанола гидрохлорид 62а (Ar=3-фторфенил)
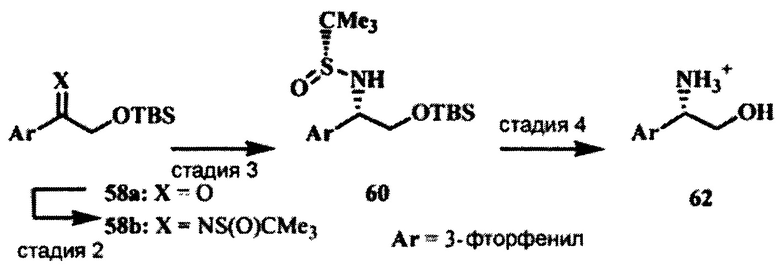
[00203] Стадия 1: К суспензии магниевых опилок (2,10 г, 85,7 ммоль) в безводном ТГФ (120 мл) при комнатной температуре медленно добавляют 1-бром-3-фторбензол (10,0 г, 57,2 ммоль) и 1,2-дибромэтан (0,10 мл). После перемешивания в течение 40 минут в атмосфере аргона смесь охлаждают до -78°С, и добавляют 2-(трет-бутилдиметилсилилокси)-N-метокси-N-метилацетамид (9,3 г, 40 ммоль). Полученную смесь нагревают до 0°С и перемешивают в течение 2 часов. Реакцию гасят насыщенным раствором NH4Cl (5,0 мл), и нерастворимый материал отфильтровывают. Фильтрат сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (20:1), с получением 10,3 г (93%) 2-(трет-бутилдиметилсилилокси)-1-(3-фторфенил)этанона (58а) в виде масла. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 268,0 [М+Н]+.
[00204] Стадия 2: К смеси 58а (11,3 г, 42,1 ммоль) и (R)-2-метилпропан-2-сульфинамида (6,60 г, 54,7 ммоль) в ТГФ (200 мл) при комнатной температуре добавляют Ti(Oi-Pr)4 (29,9 г, 105 ммоль). Реакционную смесь нагревают до кипения с обратным холодильником в атмосфере N2 на протяжении ночи. Смесь охлаждают, обрабатывают насыщенным раствором NH4Cl (5,0 мл), и нерастворимый материал отфильтровывают. Фильтрат сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc с градиентом (от 60:1 до 20:1), с получением 7,6 г (49%) (R,E)-N-(2-(трет-бутилдиметилсилилокси)-1-(3-фторфенил)этилиден)-2-метилпропан-2-сульфинамида (58b) в виде масла желтого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 372,2 [М+Н]+.
[00205] Стадия 3: К раствору 58b (7,60 г, 20,5 ммоль) в безводном ТГФ (250 мл) в атмосфере аргона при -78°С добавляют ДИБАЛ-Г (51,1 мл, 51,1 ммоль). После перемешивания при -78°С в течение 1 часа смесь обрабатывают раствором соли (16 мл) при -78°С, и затем нагревают до комнатной температуры. Нерастворимый материал отфильтровывают, фильтрат сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc с градиентом (от 20:1 до 6:1), с получением 6,5 г (86%) 60 в виде твердого вещества желтого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 374,2 [М+Н]+.
[00206] Стадия 4: К раствору 60 (3,0 г, 8,0 ммоль) в МеОН (100 мл) добавляют 3 н HCl/MeOH (8,0 мл, 24 ммоль). После перемешивания при комнатной температуре в течение 1 часа смесь упаривают под вакуумом и разбавляют EtOAc (30 мл). Твердое вещество отфильтровывают и промывают EtOAc (20 мл) с получением 880 мг (57%) 62а в виде твердого вещества белого цвета. 1Н ЯМР (500 МГц, CD3OD) δ 7,50 (м, 1Н), 7,32-7,28 (м, 2Н), 7,19 (м, 1Н), 7,41 (м, 1Н), 3,93 (м, 1Н), 3,82 (м, 1Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 156,1 [М+Н]+.
[00207] (S)-2-Амино-2-(4-(трифторметокси)фенил)этанола гидрохлорид (62b) (Ar=4-трифторметоксифенил) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 4-фторметокси-бромбензол. 1Н ЯМР (500 МГц, CD3OD) δ 7,44 (д, J=8,5 Гц, 2Н), 7,33 (д, J=8,5 Гц, 2Н), 4,44 (м, 1Н), 3,91-3,81 (м, 2Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 222,1 [М+Н]+.
[00208] (S)-2-Амино-2-(4-метоксифенил)этанола гидрохлорид (62с) (Ar=4-метоксифенил) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 4-метокси-бромбензолом. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,49 (с, 3H), 7,43 (д, J=8,5 Гц, 2Н), 6,97 (д, J=8,5 Гц, 2Н), 5,50 (шс, 1Н), 4,19 (м, 1Н), 3,76 (с, 3H), 3,68-3,67 (м, 2Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 151,3 [М+Н-17]+.
[00209] (S)-2-Амино-2-(3-фтор-4-метоксифенил)этанола гидрохлорид (62d) (Ar=3-фтор-4-метоксифенил) получают аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 3-фтор-4-метокси-бромбензол. 1Н ЯМР (500 МГц, CD3OD) δ 7,28-7,17 (м, 3H), 4,31 (м, 1Н), 3,91-3,87 (м, 4Н), 3,78 (м, 1Н). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 169,3 [М+Н-17]+.
[00210] (S)-2-Амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлорид (62е) (Ar=4-хлор-3-фтор-фенил) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 4-хлор-3-фтор-бромбензол.
[00211] (S)-2-Амино-2-(3-хлор-4-фтор-фенил)этанола гидрохлорид (62f) (Ar=3-хлор-4-фтор-4-фенил) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 3-хлор-4-фтор-бромбензол.
[00212] (S)-2-Амино-2-(4-фторфенил)этанол (62г) (Ar=4-фторфенил) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол зна 4-фтор-бромбензол.
[00213] (S)-2-Амино-2-(4-дифторметокси-фенил)этанол (62h) (Ar=4-дифторметокси-фенил) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-бромбензол на 4-дифторметокси-бромбензол.
[00214] Справочный Пример 7
[00215] (S)-4-(1-Амино-2-(трет-бутилдиметилсилилокси)этил)-2-хлорбензонитрила гидрохлорид (62i; Ar=3-хлор-4-циано-фенил)
[00216] Стадия 1: 4-(2-(трет-Бутилдиметилсилилокси)ацетил)-2-хлорбензонитрил - К раствору 4-бром-2-хлорбензонитрила (15 г, 69 ммоль) в ТГФ (150 мл) при -78°С добавляют LiCl (3,39 г, 81,0 ммоль) и изопропилмагния хлорид (1,3 н в ТГФ, 62 мл, 81 ммоль). После перемешивания при 0°С в течение 30 минут раствор охлаждают до -78°С, и добавляют раствор 2-(трет-бутилдиметилсилилокси)-N-метокси-N-метилацетамида (12 г, 57 ммоль) в ТГФ (150 мл). Реакционную смесь перемешивают при 0°С, выдерживая при этой температуре в течение 2 часов, затем гасят водой (50 мл), и полученную смесь экстрагируют EtOAc (3×100 мл). Органическую фракцию промывают насыщ. NaCl (3×50 мл), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (50:1), с получением 37 г (88%) 58 (Ar=3-хлор-4-цианофенил) в виде желтого масла. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 509,1 [М+Н]+.
[00217] Стадия 2: (R,Е)-N-(2-(трет-Бутилдиметилсилилокси)-1-(3-хлор-4-цианофенил)этилиден)-2-метилпропан-2-сульфинамид получают в соответствии с методикой со стадии 2 Справочного Примера 6, за исключением того, что в качестве реагента используют 58а (Ar=3-хлор-4-цианофенил). Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (20:1), с получением 4,9 г (25%) 58b (Ar=3-хлор-4-цианофенил) в виде твердого вещества желтого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 413,1 [М+Н]+.
[00218] Стадия 3: К раствору 58b (Ar=3-хлор-4-цианофенил) (4,90 г, 11,9 ммоль) в ТГФ (100 мл) добавляют NaBH4 (700 мг, 14,2 ммоль) при 0°С. После перемешивания в течение 30 минут реакционную смесь обрабатывают водой (50 мл) и экстрагируют EtOAc (2×100 мл). Органическую фракцию промывают насыщ. NaCl (50 мл), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (20:1) с получением 1 г (22%) 60 (Ar=3-хлор-4-цианофенил) в виде твердого вещества белого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 415,3 [М+Н]+.
[00219] Стадия 4: К раствору 60 (Ar=3-хлор-4-цианофенил) (500 мг, 1,20 ммоль) в EtOAc (10 мл) при комнатной температуре добавляют 3 н HCl/метанол (1,2 мл). После перемешивания в течение 1 часа твердое вещество отфильтровывают с получением 400 мг (100%) 62i (Ar=3-хлор-4-цианофенил) в виде твердого вещества белого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 311,3 [М+Н]+.
[00220] Справочный Пример 8
[00221] (R)-1-(3-Фтор-4-метоксифенил)пропан-1-амина гидрохлорид (70а)
[00222] Стадия 1: К раствору 3-фтор-4-метоксибензальдегида (2,0 г, 13 ммоль) в ТГФ (40 мл) добавляют (S)-2-метилпропан-2-сульфинамид (2,84 г, 23,4 ммоль) и Ti(OEt)4 (5,92 г, 26,0 ммоль). Реакционную смесь нагревают до 65°С, выдерживая при этой температуре в течение 12 часов. После охлаждения до комнатной температуры смесь выливают в воду. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc (3×100 мл). Фильтрат сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя EtOAc/петролейным эфиром (1:4), с получением 3,0 г (90%) (S,E)-N-(3-фтор-4-метоксибензилиден)-2-метилпропан-2-сульфинамида (66). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 258,1 [М+Н]+.
Стадия 2: К раствору 66 (3,0 г, 12 ммоль) в ТГФ (30 мл) при -78°С добавляют раствор этилмагния бромида в ТГФ (1 н, 18 мл, 18 ммоль). После перемешивания в течение 4 часов реакционную смесь нагревают до 25°С и перемешивают при комнатной температуре в течение ночи. Смесь обрабатывают NH4Cl и разбавляют EtOAc. Объединенные органические фракции сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью EtOAc/петролейного эфира (1:1), с получением 1,5 г (45%) (S)-N-((R)-1-(3-фтор-4-метоксифенил)пропил)-2-метилпропан-2-сульфинамида (68). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 288,1 [М+Н]+.
[00223] Стадия 3: К раствору 68 (1,5 г, 5,2 ммоль) в Et2O (20 мл) при 0°С добавляют 3 н HCl/MeOH (5,0 мл, 15 ммоль). После перемешивания в течение 1,5 часов твердое вещество отфильтровывают и сушат под вакуумом с получением 900 мг (80%) 70а. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,56 (с, 3H), 7,44 (дд, J=12,5, 2,0 Гц, 1Н), 7,29-7,20 (м, 2Н), 4,08 (м, 1Н), 3,84 (с, 3H), 1,97 (м, 1Н), 1,78 (м, 1Н), 0,73 (т, J=7,0 Гц, 3H). ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 167,1 [М+Н-17]+.
[00224] (R)-1-(4-Хлор-3-фтор-фенил)пропан-1-амина гидрохлорид (70b) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-4-метокси-бензальдегид на 4-хлор-3-фтор-бензальдегид.
[00225] (R)-1-(3-Хлор-4-фтор-фенил)пропан-1-амина гидрохлорид (70с) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-4-метокси-бензальдегид на 3-хлор-4-фтор-бензальдегид.
[00226] (R)-1-(4-Хлор-3-фторфенил)проп-2-ен-1-амина гидрохлорид (70d) может быть получен аналогичным образом, за исключением того, что на стадии 1 заменяют 3-фтор-4-метокси-бензальдегид на 3-хлор-4-фтор-бензальдегид. На стадии 2 используют этилмагния бромид вместо винилмагния бромида. 1Н ЯМР (500 МГц, МеОН-d4) δ 7,62 (т, J=7,0 Гц, 1Н), 7,40 (м, 1Н), 7,33 (дд, J=5,5, 2,5 Гц, 1Н), 6,13 (м, 1Н), 5,55-5,46 (м, 2Н), 5,04 (д, J=6,0 Гц, 1Н).
[00227] Справочный Пример 9
[00228] (3S,4S)-3-Фтортетрагидро-2H-пиран-4-амин (71с) и (3R,4R)-3-фтортетрагидро-2H-пиран-4-амин (71d)

[00229] Стадия 1: При перемешивании к раствору 1-хлорметил-4-фтор-1,4-диазониабицикло[2,2,2]октан бис-тетрафторбората (147 г, 414 ммоль, Selectfluor®) в смеси MeCN/H2O (1:1, 800 мл), охлажденному до 0°С в атмосфере азота в круглодонной колбе вместимостью 3 л, добавляют по каплям раствор 67 (45,0 г, 394 ммоль, CASRN 17327-22-9) в MeCN (120 мл). Реакционную смесь перемешивают в течение 30 минут на ледяной бане, после чего снимают с бани и перемешивают еще в течение 1 часа. Затем твердый NaCl (200 г) добавляют к реакционной смеси вместе с ДХМ (300 мл). Медленно добавляют насыщенный раствор Na2CO3 до тех пор, пока рН не достигнет 10. Смесь переносят в делительную воронку вместимостью 4 л и трижды экстрагируют ДХМ. Затем водную фракцию помещают в жидкость-жидкостный экстрактор непрерывного действия, содержащий ДХМ, и нагревают до 58°С, выдерживая при этой температуре в течение 18 часов. Объединенные органические экстракты сушат (MgSO4), фильтруют и упаривают при 20°С на роторном испарителе. Неочищенный продукт очищают хроматографией на SiO2, элюируя с градиентом смеси ДХМ/МеОН (ДХМ:МеОН от 500:3 до 500:5), с получением 30 г (64,4%) 3-фтордигидро-2Н-пиран-4(3H)-она (69).
[00230] Стадия 2: К раствору 69 (30 г, 254 мМ) и ДХЭ (800 мл), охлажденному до 0°С в атмосфере азота, добавляют фенилметанамин (29,8 мл, 267 ммоль), и раствор перемешивают в течение 10 минут. К реакционной смеси добавляют NaBH(OAc)3 (75,4 г, 356 ммоль), с последующим добавлением по каплям ледяной НОАс (14,5 мл, 254 ммоль). Реакционную смесь перемешивают в течение 2 часов, после чего выливают в 1 М раствор NaOH и экстрагируют ДХМ. Объединенные органические фракции сушат (MgSO4), фильтруют и упаривают. Неочищенный продукт очищают обращенно-фазовой колоночной хроматографией с использованием MeCN/H2O с градиентом (0-40% MeCN), с получением 39 г (73,4%) рацемического цис продукта [(3S,4S)- и (3R,4R)-N-бензил-3-фтортетрагидро-2Н-пиран-4-амина (71а) и (71b), соответственно].
[00231] Энантиомеры могут быть разделены хроматографией на колонке Chiralpak IC, 5×25 см, с элюацией 10% ИПА (0,1% NH4OH)/90% СО2 при скорости потока 300 мл/мин и температуре 40°С. Обратное давление составляет 100 Бар.
[00232] Стадия 3: К раствору 71а (3,7 г, 18 ммоль) и МеОН (40 мл) при комнатной температуре добавляют Pd/C (3,8 г, 1,8 ммоль), и полученную суспензию перемешивают в атмосфере H2 в течение 18 часов. Катализатор фильтруют и промывают метанолом. Растворитель упаривают с получением 2,1 г (100%) (3S,4S)-3-фтортетрагидро-2H-пиран-4-амина (71с). 1Н ЯМР (400 МГц, CDCl3) δ 4,58-4,44 (м, 1Н), 4,19-4,09 (м, 1Н), 4,05-3,95 (м, 1Н), 3,56-3,38 (м, 2H), 2,96-2,84 (м, 1Н), 1,88-1,77 (м, 1Н), 1,72-1,65 (м, 1Н). Энантиомер, (3R,4R)-3-фтортетрагидро-2Н-пиран-4-амин (71d), может быть получен аналогичным способом, с заменой 71а на 71b.
[00233] Справочный Пример 10
[00234] (3S,4R)-3-Фтортетрагидро-2H-пиран-4-амин (77а) и (3R,4S)-3-фтортетрагидро-2H-пиран-4-амин (77b)

[00235] Стадия 1: При перемешивании к раствору 73 (34,58 г, 292,8 ммоль) и ТГФ (350 мл), охлажденному до -78°С в атмосфере азота, добавляют по каплям L-селектрид (307,4 мл, 307,4 ммоль), и реакционную смесь перемешивают в течение 30 минут. Затем добавляют МеОН (35,58 мл, 878,4 ммоль) и 1 М NaOH (878,4 мл, 878,4 ммоль), и реакционной смеси дают нагреться до 0°С. К раствору осторожно добавляют по каплям H2O2 (99,59 мл, 1464 ммоль), и реакционную смесь перемешивают еще в течение 30 минут. После этого добавляют насыщенный раствор соли (50 мл), и реакционную смесь упаривают для удаления ТГФ. Раствор разбавляют ДХМ (500 мл) и переносят в жидкость-жидкостный экстрактор непрерывного действия, который нагревают до 58°С, выдерживая при этой температуре в течение 24 часов. Далее органическую фракцию отделяют, сушат (MgSO4), фильтруют и упаривают. Неочищенный продукт очищают хроматографией на SiO2, элюируя ДХМ/EtOAc с градиентом (от 5:1 до 3:1), с получением 21 г (60,2%) рацемического цис-продукта (3R,4S)- и (3S,4R)-3-фтортетрагидро-2H-пиран-4-ол ((75а) и (75b), соответственно).
[00236] Стадия 2: При перемешивании к раствору 75а и 75b (15,0 г, 125 ммоль), изоиндолин-1,3-диона (20,2 г, 137 ммоль) и 2-(дифенилфосфино)пиридина (42,7 г, 162 ммоль) в ТГФ (550 мл), охлажденному до 0°С в атмосфере азота, добавляют (E)-ди-трет-бутил-диазен-1,2-дикарбоксилат (37,4 г, 162 ммоль), и реакционную смесь перемешивают при комнатной температуре в течение 24 часов. К реакционной смеси добавляют 4 М HCl в диоксане (156 мл, 624 ммоль), и полученный раствор перемешивают в течение 2 часов, после чего упаривают до сухого состояния. Остаток растворяют в эфире и промывают 6 раз 4 М HCl. Твердое вещество, которое не растворилось в эфире, оставляют для дальнейшей очистки (серия 1). Затем органический раствор сушат (MgSO4), фильтруют и упаривают. Неочищенный материал суспендируют в ТГФ и фильтруют с получением продукта в виде твердого вещества (партия 2). Далее фильтрат упаривают, ресуспендируют в ДХМ и фильтруют. Твердое вещество отбрасывают. Фильтрат объединяют с первыми двумя партиями твердого вещества (серии 1 и 2), упаривают и очищают хроматографией на SiO2, элюируя ДХМ/МеОН с градиентом (от 500:2 до 500:5), с получением 14 г (45%) рацемического 2-((3S,4R)- и (3R,4S)-3-фтортетрагидро-2H-пиран-4-ил)изоиндолин-1,3-диона ((77а) и (77b), соответственно).
[00237] Энантиомеры разделяют хроматографически на колонке Chiralpak IA, 5×25 см, элюируя 10% МеОН:ДХМ (1:1)/90% CO2 при скорости потока 300 мл/мин и температуре 40°С. Обратное давление составляет 100 Бар.
[00238] Стадия 3: К раствору 77b (8,4 г, 34 мМ) и ТГФ/МеОН (1:1, 160 мл) добавляют гидразина моногидрат (17 г, 337 ммоль), реакционную смесь перемешивают при 50°С в течение 6 часов, и затем охлаждают до комнатной температуры, выдерживая при этой температуре в течение 24 часов. Полученную смесь фильтруют, и твердое вещество промывают ТГФ. Фильтрат упаривают, и неочищенный продукт очищают хроматографией на SiO2, элюируя смесью ДХМ:МеОН с градиентом (от 500:20 до 500:25), с получением 4,0 г (100%) (3R,4S)-3-фтортетрагидро-2H-пиран-4-амина (79а). 1Н ЯМР (400 МГц, CDCl3) δ 4,28-4,04 (м, 2Н), 3,94-3,85 (м, 1Н), 3,45-3,35 (м, 1Н), 3,30-3,20 (м, 1Н), 3,05-2,92 (м, 1Н), 1,97-1,88 (м, 1Н), 1,58-1,48 (м, 1Н). Другой энантиомер, (3R,4S)-3-фтортетрагидро-2H-пиран-4-амин (79b), получают аналогичным способом из 77а.
[00239] Справочный Пример 11
[00240] (2S,4R)-2-(трет-Бутил-диметил-силанилоксиметил)-тетрагидропиран-4-иламин

[00241] Стадия 1: К раствору (2S,4S)-2-((трет-бутилдиметилсилилокси)метил)-3,4-дигидро-2H-пиран-4-ола (79, 3,565 г, 14,59 ммоль) (получен из (2R,3S,4R)-2-(гидроксиметил)-3,4-дигидро-2H-пиран-3,4-диола в соответствии с методиками из L.A. Paquette and J.A. Oplinger, J. Org. Chem. 1988 53:2953-2959) и ДХМ (25 мл) добавляют молекулярные сита 4
[00242] Стадия 2: Суспензию 81 (3,097 г, 12,78 ммоль), Pd/C (0,5439 г, 0,2555 ммоль) и EtOAc (30 мл) перемешивают и выдерживают в атмосфере водорода из баллона в течение 18 часов. Реакционную смесь фильтруют сквозь слой Celite® и упаривают. Полученный остаток очищают хроматографией на SiO2, элюируя смесью 20% EtOAc/гексана, с получением 2,035 г (65,17%) 83.
[00243] Стадия 3: К раствору 83 (1,885 г, 7,713 ммоль), фенилметанамина (0,9470 мл, 8,484 ммоль) и ДХЭ (40 мл) добавляют NaBH(OAc)3 (2,288 г, 10,80 ммоль), и реакционную смесь перемешивают в течение 1 часа. Реакционную смесь выливают в воду и экстрагируют ДХМ. Объединенные органические экстракты промывают раствором NaHCO3, сушат (MgSO4), фильтруют и упаривают. Полученный остаток очищают на SiO2, элюируя смесью ДХМ/МеОН с градиентом (от 0 до 3% МеОН), с получением (2S,4R)-N-бензил-2-((трет-бутилдиметилсилилокси)метил)тетрагидро-2H-пиран-4-амина (87а, 1,686 г, выход 65,15%) и транс-(2S,4S)-N-бензил-2-((трет-бутилдиметилсилилокси)метил)тетрагидро-2H-пиран-4-амина (85а,1,04 г, выход 40,18%).
[00244] Стадия 4: К раствору 85а (1,04 г, 3,10 ммоль) и EtOH (20 мл) добавляют Pd/C (0,660 г, 0,310 ммоль), реакционную смесь перемешивают и выдерживают в атмосфере водорода из баллона в течение 18 часов. Смесь фильтруют сквозь мембранный фильтр ZapCap. Фильтрат упаривают с получением 664 мг (87,3%) 85b которое использовали без дополнительной очистки.
[00245] Превращение 87а в (2S,4R)-2-((трет-бутилдиметилсилилокси)метил)тетрагидро-2H-пиран-4-амин (87b) осуществляют аналогичным способом.
[00246] Справочный Пример 12
[00247] 7-(Тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоновая кислота (72) [А-10, Схема A, R1=тетрагидропиран-4-ил)]
[00248] Стадия 1: Четырехгорлую круглодонную колбу вместимостью 20 л продувают, и в атмосфере N2 в колбу помещают раствор диизопропиламина (582 г, 5,76 моль, 1,05 экв.) в ТГФ (4,2 л), с последующим добавлением по каплям на протяжении 30 минут н-BuLi (2,4 М, 2,4 л, 1,05 экв.), перемешивая при -30°С. Полученный раствор перемешивают при -30°С, выдерживая при этой температуре в течение 30 минут, затем охлаждают до -80°С. К раствору ЛДА при перемешивании добавляют по каплям на протяжении 1 часа раствор 2,5-дибромпиридина (1,3 кг, 5,49 моль, 1,00 экв.) в ТГФ (5,2 л). Полученный раствор перемешивают при -70°С, выдерживая при этой температуре в течение 30 минут. К смеси при -70°С добавляют CO2 (сухой лед) (1267 г, 28,80 моль, 5,00 экв.) в виде нескольких порций. Полученный раствор перемешивают при -70°С, выдерживая при этой температуре в течение 30 минут, гасят добавлением 5 л воды при -70°С, упаривают под вакуумом и экстрагируют 3×4 л EtOAc. Значение рН водной фракции доводят до 3-4 с помощью HCl (12 моль/л). Осадок отделяют фильтрацией с получением 2,5-дибромизоникотиновой кислоты (А-2) в виде твердого вещества белого цвета.
[00249] Стадия 2: Четырехгорлую круглодонную колбу вместимостью 20 л продувают, и в атмосфере N2 помещают в колбу 2,5-дибромизоникотиновую кислоту (1,030 кг, 3,67 моль, 1,00 экв.), ТЭА (484 г, 4,78 моль, 1,30 экв.) и трет-бутанол (10 л), с последующим добавлением ДФФА (1215 г, 4,41 моль, 1,20 экв.). Полученный раствор перемешивают в течение ночи при 80°С. Эту реакцию повторяют 5 раз. Полученную смесь упаривают под вакуумом, разбавляют 20 л воды и экстрагируют 3×15 л EtOAc. Органические фракции объединяют, промывают 2×15 л раствора соли, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью EtOAc/петролейного эфира с градиентом (от 1:30 до 1:15), с получением 3,2 кг (41%) трет-бутил-2,5-дибромпиридин-4-илкарбамата (А-3) в виде твердого вещества белого цвета.
[00250] Стадия 3: Четырехгорлую круглодонную колбу вместимостью 10 л продувают, и в атмосфере N2 помещают в колбу А-3 (420 г, 1,19 моль, 1,00 экв.), МТБЭ (3,2 л), ТГФ (1,4 л), после чего охлаждают до -80°С и при перемешивании добавляют по каплям н-BuLi (2,5 М, 52 мл, 2,40 экв.) на протяжении 30 минут. Полученный раствор перемешивают при -70°С в течение 30 минут, и затем при перемешивании добавляют по каплям ДМФА (1400 мл, 5,00 экв.) при -70°С. Полученный раствор перемешивают при -70°С в течение 30 минут. Значение рН раствора доводят до 5-6 с помощью НОАс. Полученный раствор экстрагируют 3×2,0 л EtOAc. Органические фракции объединяют, промывают 2×3,0 л раствора соли, сушат (MgSO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью EtOAc/петролейного эфира (от 1:30 до 1:10), с получением 200 г (56%) А-4 в виде твердого вещества белого цвета.
[00251] Стадия 4: Четырехгорлую круглодонную колбу вместимостью 2 л продувают, и в атмосфере N2 в колбу помещают раствор диизопропиламина (30,3 г, 299,44 ммоль, 2,00 экв.) в ТГФ (250 мл), после чего при перемешивании добавляют по каплям н-бутиллитий (125 мл, 2,00 экв.) при -60°С. Полученный раствор перемешивают при температуре от -20 до -30°С, выдерживая при этой температуре в течение 1 часа. При перемешивании к раствору, охлажденному до температуры от -60 до -70°, добавляют по каплям раствор трет-бутпацетата (34,8 г, 299,59 ммоль, 2,00 экв.) в ТГФ (100 мл). Полученный раствор перемешивают при -50°С, выдерживая при этой температуре в течение 1 часа. К смеси добавляют раствор А-4 (45 г, 149,43 ммоль, 1,00 экв.) в ТГФ (100 мл) при температуре от -60 до -70°С. Полученный раствор перемешивают при температуре от -50 до -60°С в течение 1 часа, гасят добавлением 300 мл насыщ. водн. NH4Cl, упаривают под вакуумом и экстрагируют 2×300 мл EtOAc. Органические фракции объединяют, промывают раствором соли (3×300 мл), сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением 60 г (96%) А-5 в виде желтого масла.
[00252] Стадия 5: Круглодонную колбу вместимостью 2 л продувают, и в атмосфере N2 в колбу помещают А-5 (60 г, 143,78 ммоль, 1,00 экв.), 6 н HCl (360 мл) и 1,4-диоксан (240 мл). Полученный раствор кипятят с обратным холодильником в течение ночи, охлаждают и упаривают под вакуумом. рН раствора доводят до 8~9 с помощью NaOH. Осадок отделяют фильтрацией и сушат в печи при сниженном давлении с получением 20 г (62%) А-6 в виде твердого вещества практически белого цвета. (Электрораспыление, соотношение массы и заряда): 225 [М+Н]+. Н ЯМР (ДМСО, 300 МГц, пропромилле): 12,09 (с, 1Н), 8,66 (с, 1Н), 7,97~8,01 (д, 1Н, J=9,6 Гц), 7,36 (с, 1Н), 6,60~6,64 (дд, 1Н, J=1,5, 9,6 Гц).
[00253] Стадия 6: Четырехгорлую круглодонную колбу вместимостью 5 л продувают, и в атмосфере N2 в колбу помещают А-6 (100 г, 444,36 ммоль, 1,00 экв.), Pd(OAc)2 (10 мг, 0,04 ммоль, 0,10 экв.), Xantphos (25,8 г, 44,56 ммоль, 0,10 экв.), тетрагидро-2H-пиран-4-амина гидрохлорид (67 г, 486,88 ммоль, 1,10 экв.) и ТГФ (1 л), и затем добавляют раствор LiHMDS (1 М в ТГФ) (2000 мл, 4,50 экв.). Полученный раствор кипятят с обратным холодильником на протяжении 2 часов, упаривают под вакуумом, разбавляют 4 л воды и экстрагируют EtOAc (2×2 л). Водные фракции объединяют, и рН доводят до 8~9 с помощью NaHCO3 (твердый). Порции осадка отделяют фильтрацией и сушат в печи под вакуумом с получением 81,7 г (75%) А-7 (R2=тетрагидро-2H-пиран-4-ил) в виде твердого вещества желтого цвета.
[00254] Стадия 7: В круглодонную колбу вместимостью 2 л помещают А-7 (R2=тетрагидро-2H-пиран-4-ил) (71,7 г, 289,94 мМ, 1,00 экв.) и POCl3 (360 мл). Полученный раствор кипятят с обратным холодильником в течение 1 часа, охлаждают до 0°С, гасят добавлением 5 л насыщ. водн. NaHCO3 и экстрагируют EtOAc (3×3 л). Органические фракции объединяют, промывают раствором соли (2×4 л), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc с градиентом (от 5:1 до 2:1), с получением 30 г (39%) А-8 (R2=тетрагидро-2H-пиран-4-ил) в виде твердого вещества желтого цвета.
[00255] Стадия 8: В корпусной реактор вместимостью 1 л, предназначенный для работы под давлением (20 атм.), помещают А-8 (R2=тетрагидро-2H-пиран-4-ил) (30 г, 113,76 ммоль, 1,00 экв.), Pd(dppf)Cl2 (12,5 г, 17,08 ммоль, 0,15 экв.), ТЭА (33,3 г, 329,08 ммоль, 3,00 экв.) и МеОН (500 мл). Вводят СО (избыток). Полученный раствор перемешивают при 80°С в течение 5 часов, и затем охлаждают до комнатной температуры. Твердое вещество отфильтровывают, и фильтрат упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc с градиентом (от 2:1 до 0:1), с получением 29,5 г (90%) А-9 (R2=тетрагидро-2H-пиран-4-ил) в виде твердого вещества желтого цвета.
[00256] Стадия 9: В круглодонную колбу вместимостью 500 мл помещают А-9 (R2=тетрагидро-2H-пиран-4-ил) (29,5 г, 102,68 ммоль, 1,00 экв.), LiOH (2,75 г, 114,82 ммоль, 1,10 экв.) и смесь ТГФ/воды (300/60 мл). Полученный раствор перемешивают при комнатной температуре в течение 1 часа, упаривают под вакуумом, разбавляют 500 мл воды и экстрагируют ДХМ (3×150 мл). Значение рН водной фракции доводят до 5 с помощью HCl (12 моль/л). Осадок отделяют фильтрацией и сушат в печи при сниженном давлении с получением 27,26 г (97%) А-10 (R2=тетрагидро-2H-пиран-4-ил) в виде твердого вещества красного цвета. (Электрораспыление, соотношение массы и заряда): 274 [М+Н]+. Н ЯМР (ДМСО, 300 МГц, пропромилле) δ 9,03 (с, 1Н), 8,36~8,39 (д, 1Н, J=8,4 Гц), 7,66~7,69 (д, 1Н, J=8,4 Гц), 7,03~7,06 (д, 1Н, J=7,8 Гц), 6,81 (с, 1Н), 3,88~3,92 (м, 3Н), 3,42~3,49 (м, 3Н), 1,91~1,94 (д, 2Н, J=10,8 Гц), 1,46~1,58 (м, 2Н).
[00257] Справочный Пример 13
[00258] 7-Фтор-1,6-нафтиридин-2-карбоновая кислота (74) (Схема В, В-5)
[00259] Стадия 1: В корпусный реактор вместимостью 2 л, предназначенный для работы под давлением, помещают А-6 (93,5 г, 415,48 ммоль, 1,00 экв.), аммиак (1 кг) и Cu (10,7 г, 167,19 ммоль, 0,40 экв.). Полученный раствор перемешивают при 120°С, выдерживая при этой температуре в течение ночи, и затем охлаждают до 25°С. Твердое вещество отделяют фильтрацией и промывают 2×350 мл аммиака, с получением 48,8 г (73%) В-1 в виде твердого вещества желтого цвета.
[00260] Стадия 2: Четырехгорлую круглодонную колбу вместимостью 1 л продувают, и в атмосфере N2 в колбу помещают В-1 (48,8 г, 302,80 ммоль, 1,00 экв.) и BMIM⋅BF4 (685 г, 3,03 моль, 10,00 экв.), с последующим добавлением NO⋅BF4 (53,2 г, 455,44 ммоль, 1,50 экв.) в виде нескольких порций. Полученный раствор перемешивают при комнатной температуре в течение 1,5 часов, и затем разбавляют водой (500 мл). Твердое вещество отделяют фильтрацией и промывают водой (2×200 мл). Фильтрат экстрагируют EtOAc (3×1,5 л). Объединенные органические фракции промывают раствором соли (2×1,5 л), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток объединяют с полученным ранее твердым веществом. Неочищенный продукт промывают H2O (2×20 мл) и сушат с получением 35 г (70%) В-2 в виде твердого вещества желтого цвета.
[00261] Стадия 3: В круглодонную колбу вместимостью 500 мл помещают В-2 (35 г, 213,24 ммоль, 1,00 экв.) и POCl3 (200 мл). Полученный раствор кипятят с обратным холодильником в течение 1 часа, охлаждают до 30°С, гасят холодным насыщ. водн. NaHCO3 (3 л) и экстрагируют EtOAc (3×2 л). Объединенные органические фракции промывают раствором соли (2×4 л), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью EtOAc/гексана с градиентом (от 20 до 25% EtOAc), с получением 24 г (62%) В-3 в виде твердого вещества практически белого цвета.
[00262] Стадия 4: В корпусной реактор вместимостью 1 л, предназначенный для работы под давлением (20 атм.), помещают В-3 (18 г, 98,59 ммоль, 1,00 экв.), МеОН (360 мл), ТЭА (28,4 г, 280,66 ммоль, 3,00 экв.) и Pd(dppf)Cl2⋅CH2Cl2 (13,4 г, 16,46 ммоль, 0,15 экв.). Вводят избыток СО, и полученный раствор перемешивают при 60°С в течение 2 часов, и затем при 70°С в течение ночи. Реакционную смесь охлаждают до 30°С и упаривают под вакуумом. Остаток очищают на SiO2, элюируя смесью петролейного эфира/EtOAc (3:1), с получением 15,8 г (78%) В-4 в виде твердого вещества практически белого цвета.
[00263] Стадия 5: В трехгорлую круглодонную колбу вместимостью 1 л помещают В-4 (16,2 г, 78,57 ммоль, 1,00 экв.) и ТГФ (230 г, 3,19 моль, 40,59 экв.), и затем при перемешивании по каплям добавляют раствор LiOH (2,1 г, 87,50 ммоль, 1,10 экв.) в воде (40 мл). Полученный раствор перемешивают при комнатной температуре в течение 1,5 часов, упаривают под вакуумом, разбавляют H2O (500 мл) и экстрагируют EtOAc (2×200 мл). рН водной фракции доводят до 3 с помощью водн. HCl (12 моль/л). Осадок отделяют фильтрацией, промывают H2O (2×50 мл) и сушат в вакуумной печи с получением 13,8 г (91%) В-5 в виде твердого вещества белого цвета. МС (электрораспыление, соотношение массы и заряда): 193 [М+Н]+. Н ЯМР (300 МГц, ДМСО) δ 13,88 (1Н, с), 9,35 (1Н, с), 8,84~8,81 (1Н, д, J=8,7 Гц), 8,20~8,17 (1Н, д, J=8,7 Гц), 7,81 (1H, с).
[00264] Справочный Пример 14
[00265] (R)-3-Амино-3-(3-фтор-4-(трифторметил)фенил)пропан-1-ол (91a) и (R)-3-амино-3-(4-хлор-3-фторфенил)пропан-1-ол (91b)
[00266] Стадия 1: Раствор 3-фтор-4-(трифторметил)бензальдегида (4,8 г, 25 ммоль), малоновой кислоты (2,6 г, 25 ммоль), аммония ацетата (0,85 г, 50 ммоль) и EtOH (30 мл) нагревают до 80°С, выдерживая при этой температуре в течение 18 часов. Реакционную смесь охлаждают, разбавляют Et2O (50 мл) и фильтруют с получением 2,0 г (16%) 3-амино-3-(3-фтор-4-(трифторметил)фенил)пропановой кислоты (93) в виде твердого вещества белого цвета, которое использовали без дополнительной очистки.
[00267] Стадия 2: При перемешивании к суспензии 93 (2,0 г, 8,0 ммоль) и ТГФ (25 мл) в атмосфере N2 при 0°С добавляют по каплям 1 М LiAlH4 в ТГФ (12 мл, 12 ммоль), и реакционную смесь перемешивают при 0°С на ледяной бане в течение 1,5 часов. Холодную реакционную смесь гасят осторожным добавлением реакционной смеси к насыщенному раствору виннокислого калия-натрия (50 мл), охлажденному на ледяной бане и хорошо продуваемому. Полученную смесь перемешивают в течение 18 часов при медленном нагревании до комнатной температуры, по мере таяния льда в ледяной бане. Смесь разбавляют EtOAc (50 мл) и фильтруют сквозь Celite® для удаления твердого вещества, которое несколько раз промывают EtOAc. Фракции разделяют, и водную фракцию снова экстрагируют EtOAc (30 мл). Объединенные органические экстракты промывают раствором соли (50 мл), сушат (MgSO4), фильтруют и упаривают под вакуумом. Неочищенный продукт очищают хроматографией на SiO2, элюируя смесью 5% 7 н NH3 в МеОН/ДХМ (500 мл на предварительно промытой колонке, и затем 500 мл элюента, после чего 500 мл 7,5% 7 н NH3 в МеОН/ДХМ) с получением 0,43 г (22%) 3-амино-3-(3-фтор-4-(трифторметил)фенил)пропан-1-ола (91а).
[00268] (R)-3-Амино-3-(4-хлор-3-фторфенил)пропан-1-ол (91b) получают аналогичным образом, за исключением того, что на стадии 1 3-фтор-4-трифторметилбензальдегид заменяют 4-хлор-3-фторбензальдегидом.
[00269] Пример 1
[00270] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-21) Способ А

[00271] Смесь 72 (720 мг, 2,63 ммоль), ГАТУ (1503 мг, 3,95 ммоль) и ДИПЭА (1,38 мл, 7,90 ммоль) в ДМФА (6,14 мл, 79,03 ммоль) перемешивают при комнатной температуре в течение 5 минут (раствор становится темно-коричневым). Через 5 минут добавляют 50с (859,0 мг, 3,16 ммоль) как твердое вещество, в виде одной порции, и реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь разбавляют EtOAc (200 мл) и промывают водой (200 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Неочищенный продукт очищают хроматографией на SiO2, элюируя смесью EtOAc/гептана с градиентом (от 0 до 100% EtOAc). Содержащие продукт фракции объединяют и упаривают под вакуумом с получением целевого продукта в виде желтой/оранжевой пены, которую дополнительно очищают сверхкритической флюидной хроматографией (СФХ) с получением 1,38 г (93%) I-21 в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (д, J=6,7 Гц, 2Н), 8,38 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,28 (дд, J=12,7, 1,9 Гц, 1Н), 7,19-7,14 (м, 1Н), 7,11 (т, J=8,6 Гц, 1Н), 6,98 (д, J=8,0 Гц, 1Н), 6,80 (с, 1Н), 5,07 (т, J=5,4 Гц, 1Н), 5,03 (м, 1Н), 3,95-3,83 (м, 3Н), 3,81 (с, 3Н), 3,79-3,71 (м, 2Н), 3,47 (м, 2Н), 1,93 (д, J=10,5 Гц, 2Н), 1,51 (м, 2Н); ЖХМС (Способ G): RT=9,97 минут, M+H+=491,0.
[00272] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-1-(4-хлор-3-фтор-фенил)-2-гидрокси-этил]-амид (I-5) получают аналогичным образом, за исключением того, что 50с заменяют (S)-2-амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлоридом (62е). 1Н ЯМР (400 МГц, ДМСО) δ 9,10 (д, J=8,1 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,4 Гц, 1Н), 7,71 (д, J=8,3 Гц, 1Н), 7,54 (т, J=8,1 Гц, 1Н), 7,47 (дд, J=10,6, 1,9 Гц, 1Н), 7,28 (дд, J=8,3, 1,9 Гц, 1Н), 6,97 (д, J=7,9 Гц, 1Н), 6,81 (с, 1Н), 5,14 (т, J=5,4 Гц, 1Н), 5,08 (м, 1Н), 3,91 (м, 2Н), 3,47 (м, 2Н), 1,94 (м, 2Н), 1,54 (м, 2Н).
[00273] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(R)-1-(3-фтор-4-метокси-фенил)-пропил]-амид (I-6) получают аналогичным образом, за исключением того, что 50с заменяют 70а. 1Н ЯМР (400 МГц, ДМСО) δ 8,99 (д, J=10,4 Гц, 2Н), 8,36 (д, J=8,3 Гц, 1Н), 7,70 (д, J=8,3 Гц, 1Н), 7,35 (дд, J=12,7, 2,0 Гц, 1Н), 7,20 (д, J=8,4 Гц, 1Н), 7,11 (т, J=8,7 Гц, 1Н), 6,97 (д, J=8,0 Гц, 1Н), 6,80 (с, 1Н), 4,89 (дд, J=15,5, 8,4 Гц, 1Н), 3,95-3,88 (м, 2Н), 3,85 (м, 1Н), 3,46 (м, 2Н), 2,03-1,80 (м, 4Н), 1,54 (м, 2Н). 0,87 (т, J=7,3 Гц, 3Н).
[00274] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(1-метил-1H-пиразол-4-ил)-(4-трифторметокси-фенил)-метил]-амид (I-9) получают аналогичным образом, за исключением того, что 50с заменяют 50b. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,27 (д, J=8,6 Гц, 1Н), 9,01 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,64 (с, 1Н), 7,56 (м, 2Н), 7,43 (с, 1Н), 7,35 (д, J=8,3 Гц, 2Н), 6,97 (д, J=8,0 Гц, 1Н), 6,78 (с, 1Н), 6,33 (д, J=8,5 Гц, 1Н), 3,93-3,87 (м, 2Н), 3,87-3,81 (м, 1Н), 3,45 (м, 2Н), 1,91 (д, J=12,1 Гц, 2Н), 1,52 (м, 2Н).
[00275] (S)-N-(2-Гидрокси-1-(4-(трифторметокси)фенил)этил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-10) получают аналогичным образом, за исключением того, что 50с заменяют 62b. 1Н ЯМР (400 МГц, ДМСО) δ 9,12 (д, J=8,2 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,53 (м, 2Н), 7,33 (д, J=8,2 Гц, 2Н), 6,99 (д, J=8,0 Гц, 1Н), 6,81 (с, 1Н), 5,13 (м, 2Н), 3,86 (м, 5Н), 3,47 (м, 2Н), 1,94 (д, J=10,5 Гц, 2Н), 1,54 (м, 2Н).
[00276] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты 4-хлор-3-фтор-бензиламид (I-11) получают аналогичным образом, за исключением того, что на стадии 2 50с заменяют 4-хлор-3-фтор-бензиламином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,46 (т, J=6,5 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,54 (т, J=8,0 Гц, 1Н), 7,37 (дд, J=10,4, 1,8 Гц, 1Н), 7,22 (д, J=8,3 Гц, 1Н), 7,01 (д, J=7,8 Гц, 1Н), 6,75 (с, 1Н), 4,52 (д, J=6,4 Гц, 2Н), 3,91 (м, 3H), 3,45 (м, 2Н), 1,93 (д, J=10,4 Гц, 2Н), 1,53 (м, 2Н).
[00277] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-1-(3-фтор-4-метокси-фенил)-2-гидрокси-этил]-амид (I-12) получают аналогичным образом, за исключением того, что 50с заменяют 62d. 1Н ЯМР (400 МГц, ДМСО) δ 9,01 (д, J=6,7 Гц, 2Н), 8,38 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,28 (дд, J=12,7, 1,9 Гц, 1Н), 7,19-7,14 (м, 1Н), 7,11 (т, J=8,6 Гц, 1Н), 6,98 (д, J=8,0 Гц, 1Н), 6,80 (с, 1Н), 5,07 (т, J=5,4 Гц, 1Н), 5,03 (м, 1Н), 3,95-3,83 (м, 3H), 3,81 (с, 3H), 3,79-3,71 (м, 2Н), 3,47 (м, 2Н), 1,93 (д, J=10,5 Гц, 2Н), 1,51 (м, 2Н).
[00278] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-4) получают аналогичным образом, за исключением того, что 50с заменяют 50а. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,30 (д, J=8,5 Гц, 1Н), 9,01 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,71 (д, J=8,3 Гц, 1Н), 7,64 (с, 1Н), 7,57 (т, J=8,1 Гц, 1Н), 7,52 (дд, J=10,6, 1,9 Гц, 1Н), 7,43 (с, 1Н), 7,32 (дд, J=8,4, 1,8 Гц, 1Н), 6,98 (д, J=8,0 Гц, 1Н), 6,78 (с, 1Н), 6,30 (д, J=8,5 Гц, 1Н), 3,93-3,87 (м, 2Н), 3,87-3,81 (м, 1Н), 3,80 (с, 3H), 3,45 (м, 2Н), 1,92 (м, 2Н), 1,59-1,46 (м, 2Н).
[00279] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-22) получают аналогичным образом, за исключением того, что 50с заменяют 50h. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,30 (д, J=8,5 Гц, 1Н), 9,01 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,71 (д, J=8,3 Гц, 1Н), 7,64 (с, 1Н), 7,57 (т, J=8,1 Гц, 1Н), 7,52 (дд, J=10,6, 1,9 Гц, 1Н), 7,43 (с, 1Н), 7,32 (дд, J=8,4, 1,8 Гц, 1Н), 6,98 (д, J=8,0 Гц, 1Н), 6,78 (с, 1Н), 6,30 (д, J=8,5 Гц, 1Н), 3,93-3,87 (м, 2Н), 3,87-3,81 (м, 1Н), 3,80 (с, 3H), 3,45 (м, 2Н), 1,92 (м, 2Н), 1,59-1,46 (м, 2Н).
[00280] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-хлор-4-циано-фенил)-(2-метил-2H-пиразол-3-ил)-метил]-амид (I-26) получают аналогичным образом, за исключением того, что 50с заменяют 44. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,77 (д, J=9,0 Гц, 1Н), 9,03 (с, 1Н), 8,39 (д, J=8,5 Гц, 1Н), 8,03 (д, J=8,0 Гц, 1Н), 7,96 (с, 1Н), 7,74-7,70 (м, 2Н), 7,36 (д, J=1,5, 1H), 7,05 (д, J=7,5 Гц, 1Н), 6,78 (с, 1Н), 6,69 (д, J=8,5 Гц, 1Н), 5,94 (д, J=1,5 Гц, 1Н), 3,89-3,80 (м, 6Н), 3,46-3,42 (м, 2Н), 1,92-1,90 (м, 2Н), 1,53-1,51 (м, 2Н).
[00281] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-5-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-27) получают аналогичным образом, за исключением того, что 50с заменяют 50е. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,48 (д, J=8,5, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,0 Гц, 1Н), 7,71 (д, J=8,0 Гц, 1Н), 7,42 (м, 1Н), 7,34 (д, J=1,5 Гц, 1Н), 7,27 (м, 1Н), 7,18 (м, 1Н), 7,00 (д, J=8,0 Гц, 1Н), 6,78 (с, 1Н), 6,50 (д, J=9,0 Гц, 1Н), 6,03 (д, J=2,0 Гц, 1Н), 3,90-3,84 (м, 6Н), 3,74 (с, 3H), 3,46-3,42 (м, 2Н), 1,92-1,90 (м, 2Н), 1,55-1,50 (м, 2Н).
[00282] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [2-(2-бром-фенил)-этил]-амид (I-28) получают аналогичным образом, за исключением того, что 50с заменяют 2-бром-бензолэтанамином (CASRN 65185-58-2). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,93 (т, J=6,0 Гц, 1Н), 8,36 (д. J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,60 (д, J=7,9 Гц, 1Н), 7,37 (д, J=6,3 Гц, 1Н), 7,32 (т, J=7,4 Гц, 1Н), 7,17 (т, J=7,6 Гц, 1Н), 6,99 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,81 (м, 1Н), 3,91 (д, J=11,7 Гц, 2Н), 3,60 (к, J=7,0 Гц, 2Н), 3,45 (т, J=10,8 Гц, 2Н), 3,04 (т, J=7,3 Гц, 2Н), 1,93 (д, J=11,1 Гц, 2Н), 1,53 (кд, J=11,8, 4,3 Гц, 2Н).
[00283] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [2-(4-бром-фенил)-этил]-амид (I-29) получают аналогичным образом, за исключением того, что 50с заменяют 4-бром-бензолэтанамином (CASRN 73918-56-6). 1Н ЯМР (400 МГц, ДМСО) δ 9,00 (с, 1Н), 8,87 (т, J=5,8 Гц, 1Н), 8,36 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,48 (д, J=8,3 Гц, 2Н), 7,23 (д, J=8,3 Гц, 2Н), 6,99 (д, J=7,8 Гц, 1Н), 6,73 (с, 1Н), 3,94-3,80 (м, 1Н), 3,91 (д, J=11,4 Гц, 2Н), 3,56 (к, J=7,0 Гц, 2Н), 3,45 (т, J=10,7 Гц, 2Н), 2,88 (т, J=7,3 Гц, 2Н), 1,93 (д, J=10,8 Гц, 2Н), 1,59-1,47 (м, 2Н).
[00284] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты фенэтил-амид бензолэтанамин (I-30) получают аналогичным образом, за исключением того, что 50с заменяют бензолэтанамином (CASRN 64-04-0). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,87 (т, J=6,0 Гц, 1Н), 8,37 (д. J=8,3 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,34-7,24 (м, 4Н), 7,21 (т, J=7,0 Гц, 1Н), 7,00 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,82 (м, 1Н), 3,91 (д, J=11,3 Гц, 3H), 3,57 (к, J=7,2 Гц, 2Н), 3,45 (т, J=10,8 Гц, 2Н), 2,90 (т, J=7,5 Гц, 2Н), 1,93 (д, J=10,8 Гц, 2Н), 1,53 (кд, J=11,8, 4,2 Гц, 2Н).
[00285] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты (2-пиридин-2-ил-этил)-амид (I-31) получают аналогичным образом, за исключением того, что 50с заменяют 2-пиридинэтанамином (CASRN 2706-56-1). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,02-8,97 (м, 2Н), 8,53 (д, J=4,7 Гц, 1Н), 8,36 (д, J=8,4 Гц, 1Н), 7,75-7,69 (м, 2Н), 7,31 (д, J=7,7 Гц, 1Н), 7,24 (дд, J=7,4, 5,0 Гц, 1Н), 6,99 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3.94-3,83 (м, 1Н), 3,91 (д, J=11,4 Гц, 2Н), 3,71 (к, J=6,9 Гц, 2Н), 3,46 (т, J=10,8 Гц, 2Н), 3,06 (т, J=7,3 Гц, 2Н), 1,93 (д, J=11,2 Гц, 2Н), 1,53 (кд, J=11,6, 4,4 Гц, 2Н).
[00286] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты (2-пиридин-3-ил-этил)-амид (I-32) получают аналогичным образом, за исключением того, что 50с заменяют 3-пиридинэтанамином (CASRN 20173-24-4). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,92 (т, J=6,0 Гц, 1Н), 8,47 (д, J=1,6 Гц, 1Н), 8,41 (д, J=4,1 Гц, 1Н), 8,36 (д, J=8,3 Гц, 1Н), 7,71 (д, J=8,3 Гц, 1Н), 7,68 (д, J=7,8 Гц, 1Н), 7,31 (дд, J=7,7, 4,8 Гц, 1Н), 7,00 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,81 (м, 1Н), 3,91 (д, J=11,6 Гц, 2Н), 3,60 (к, J=6,9 Гц, 2Н), 3,45 (т, J=10,8 Гц, 2Н), 2,93 (т, J=7,2 Гц, 2Н), 1,93 (д, J=10,9 Гц, 2Н), 1,53 (кд, J=11,8, 4,3 Гц, 2Н).
[00287] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты (2-пиридин-4-ил-этил)-амид (I-33) получают аналогичным образом, за исключением того, что 50с заменяют 4-пиридинэтанамином (CASRN 13258-63-4). 1Н ЯМР (400 МГц, ДМСО) δ 9,01 (с, 1Н), 8,92 (т, J=6,0 Гц, 1Н), 8,47 (д, J=5,8 Гц, 2Н), 8,36 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,29 (д, J=5,7 Гц, 2Н), 7,00 (д, J=7,8 Гц, 1Н), 6,73 (с, 1Н), 3,94-3,81 (м, 1Н), 3,91 (д, J=11,5 Гц, 3H), 3,61 (к, J=6,9 Гц, 2Н), 3,45 (дд, J=11,5, 10,0 Гц, 2Н), 2,93 (т, J=7,3 Гц, 2Н), 1,93 (д, J=10,8 Гц, 2Н), 1,53 (ддд, J=15,5, 11,9, 4,2 Гц, 2Н).
[00288] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(2-метил-2H-пиразол-5-ил)-метил]-амид (I-34) получают аналогичным образом, за исключением того, что 50с заменяют 50g. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,64 (д, J=8,5 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,0 Гц,1Н), 7,71 (д, J=8,0 Гц, 1Н), 7,64-7,61 (м, 2Н), 7,41 (д, J=8,5, 1Н), 7,35 (д, J=1,5 Гц, 1Н), 7,03 (д, J=8,0 Гц, 1Н), 6,78 (с, 1Н), 6,59 (д, J=9,0 Гц, 1Н), 5,98 (д, J=1,5 Гц, 1Н), 3,91-3,78 (м, 6Н), 3,46-3,42 (м, 2Н), 1,92-1,90 (м, 2Н), 1,53-1,51 (м, 2Н).
[00289] Пример 2
[00290] N-((S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-7-((S)-1-гидроксипропан-2-иламино)-1,6-нафтиридин-2-карбоксамид (I-24) Способ В
[00291] Стадия 1: Смесь 74 (45 мг, 0,234 ммоль), ГАТУ (133,57 мг, 0,351 ммоль) и ДИПЭА (0,123 мл, 0,703 ммоль) в ДМФА (0,546 мл, 7,03 ммоль) перемешивают при комнатной температуре в течение 5 минут. К раствору добавляют (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид (50с) (76,36 мг, 0,281 ммоль) в виде одной порции, и реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь разбавляют EtOAc (30 мл) и промывают водой (20 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью EtOAc/гептана с градиентом (от 0 до 100% EtOAc), с получением 80 мг (83%) (S)-7-фтор-N-((3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-1,6-нафтиридин-2-карбоксамида (76) в виде желтого масла (80 мг, 83%), которое использовали на следующей стадии без дополнительной очистки.
[00292] Стадия 2: Смесь 76 (80 мг, 0,195 ммоль), (S)-(+)-2-амино-1-пропанола (75 мг, 0,977 ммоль) и НМП (0,551 мл, 5,86 ммоль) перемешивают и нагревают до 110°С, выдерживая при этой температуре в течение 48 часов. Реакционную смесь разбавляют EtOAc (50 мл) и промывают водой (50 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают обращенно-фазовой ВЭЖХ, элюируя смесью MeCN/H2O (содержащей 0,1% NH4OH) с градиентом (от 5 до 85% MeCN) на протяжении 14 минут, с получением I-24 в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, ДМСО) δ 9,19 (д, J=8,7 Гц, 1Н), 8,99 (с, 1Н), 8,37 (д, J=8,3 Гц, 1Н), 7,70 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,39 (с, 1Н), 7,32 (д, J=12,4 Гц, 1Н), 7,21 (д, J=8,6 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,76 (с, 1Н), 6,67 (д, J=8,1 Гц, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,75 (т, J=5,5 Гц, 1Н), 3,83 (м, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,53 (м, 1Н), 3,41-3,34 (м, 1Н), 1,19 (д, J=6,5 Гц, 3Н). ЖХМС (Способ G): RT=8,97 минут, M+H+=465,2.
[00293] 7-((S)-2-Гидрокси-1-метил-этиламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-фенил)-(1-метил-1Н-пиразол-4-ил)-метил]-амид (I-1) получают аналогичным образом, за исключением того, что на стадии 1 50с заменяют (S)-(3-фтор-фенил)(1-метил-1H-пиразол-5-ил)метанамина гидрохлоридом (50f). 1Н ЯМР (400 МГц, ДМСО) δ 9,27 (д, J=8,6 Гц, 1Н), 9,00 (с, 1Н), 8,37 (д, J=8,3 Гц, 1Н), 7,70 (д, J=8,3 Гц, 1Н), 7,64 (с, 1Н), 7,42 (с, 1Н), 7,41-7,36 (м, 1Н), 7,33-7,26 (м, 2Н), 7,10 (м, 1Н), 6,77 (с, 1Н), 6,68 (д, J=8,1 Гц, 1Н), 6,30 (д, J=8,6 Гц, 1Н), 4,74 (т, J=5,6 Гц, 1Н), 3,83 (с, 1Н), 3,80 (с, 3H), 3,53 (м, 1Н), 3,42-3,31 (м, 1Н), 1,19 (д, J=6,5 Гц, 3H).
[00294] 7-(5-Оксо-пирролидин-3-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-2) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 4-амино-пирролидин-2-оном (CASRN88016-17-5, (S)-160806-40-6, (R)-1292324-66-3). 1Н ЯМР (400 МГц, ДМСО) δ 9,21 (д, J=8,7 Гц, 1Н), 9,04 (с, 1Н), 8,41 (д, J=8,4 Гц, 1Н), 7,75 (д, J=8,3 Гц, 1Н), 7,66 (с.1Н), 7,61 (с, 1Н), 7,39 (д, J=8,5 Гц, 1Н), 7,32 (дд, J=12,6, 2,0 Гц, 1Н), 7,21 (д, J=10,2 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,78 (с, 1Н), 6,72 (с, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,48 (м, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,68 (дд, J=9,9, 6,9 Гц, 1Н), 3,18 (дд, J=10,0, 4,1 Гц, 1Н), 2,64 (дд, J=16,7, 8,1 Гц, 1Н), 2,20 (дд, J=16,7, 5,1 Гц, 1Н).
[00295] 7-(3-Фтор-пропиламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-3) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 3-фтор-пропиламином. 1Н ЯМР (400 МГц, ДМСО) δ 9,20 (д, J=8,7 Гц, 1Н), 9,01 (с, 1Н), 8,39 (д, J=8,3 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,39 (с, 1Н), 7,32 (дд, J=12,6, 2,0 Гц, 1Н), 7,21 (д, J=8,5 Гц, 1Н), 7,16-7,07 (м, 2Н), 6,73 (с, 1Н), 6,23 (д, J=8,7 Гц, 1Н), 4,63 (т, J=5,9 Гц, 1Н), 4,52 (т, J=5,8 Гц, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,38 (м, 2Н), 2,07-1,91 (м, 2Н).
[00296] 7-(2-Гидрокси-1,2-диметил-пропиламино)-[1,6]нафтиридин-2-карбоновой кислоты [(3-фтор-4-метокси-фенил)-(1-метил-1Н-пиразол-4-ил)-метил]-амид (I-13 и I-14) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 3-амино-2-метил-бутан-2-олом.
[00297] Диастереомер 1 (I-13): 1Н ЯМР (400 МГц, ДМСО) δ 9,16 (д, J=8,6 Гц, 1Н), 8,98 (с, 1Н), 8,35 (д, J=8,3 Гц, 1Н), 7,69 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,38 (с, 1Н), 7,32 (д, J=12,5 Гц, 1Н), 7,21 (д, J=8,7 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,81 (с, 1Н), 6,43 (д, J=9,5 Гц, 1Н), 6,22 (д, J=8,6 Гц, 1Н), 4,45 (с, 1Н), 3,84 (м, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 1,15 (м, 9Н). Время удерживания 0,52 с.
[00298] Диастереомер 2 (I-14): 1Н ЯМР (400 МГц, ДМСО) δ 9,16 (д, J=8,6 Гц, 1Н), 8,98 (с, 1Н), 8,35 (д, J=8,3 Гц, 1Н), 7,68 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,39 (с, 1Н), 7,32 (д, J=12,6 Гц, 1Н), 7,21 (д, J=8,7 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,81 (с, 1Н), 6,43 (д, J=9,4 Гц, 1Н), 6,22 (д, J=8,6 Гц, 1Н), 4,45 (с, 1Н), 3,84 (м, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 1,15 (м, 9Н). Время удерживания 0,62 с.
[00299] 7-(2-Окса-бицикло[2,2,1]гепт-5-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-16 и I-23) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 24b. 1Н ЯМР (400 МГц, ДМСО) δ 9,23 (д, J=8,7 Гц, 1Н), 9,03 (с, 1Н), 8,40 (д, J=8,3 Гц, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,60 (с, 1Н), 7,39 (с, 1Н), 7,32 (д, J=14,2 Гц, 1Н), 7,21 (д, J=8,6 Гц, 1Н), 7,13 (м, 2Н), 6,72 (с, 1Н), 6,24 (д, J=8,6 Гц, 1Н), 4,30 (с, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,73 (м, 1Н), 3,57 (дд, J=7,2, 3,1 Гц, 1Н), 3,49 (д, J=7,2 Гц, 1Н), 2,59 (с, 1Н), 2,11-2,01 (м, 1Н), 1,79 (д, J=10,1 Гц, 1Н), 1,55 (м, 2Н).
[00300] 7-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-17) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 71 с. 1Н ЯМР (400 МГц, ДМСО) δ 9,18 (д, J=8,6 Гц, 1Н), 9,04 (с, 1Н), 8,41 (д, J=8,4 Гц, 1Н), 7,74 (д, J=8,3 Гц. 1Н), 7,60 (с, 1Н), 7,39 (с, 1Н), 7,32 (д, J=12,6 Гц, 1Н), 7,21 (д, J=8,7 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 7,04 (д, J=8,2 Гц, 1Н), 6,97 (с, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,78 (д, J=49,6 Гц, 1Н), 4,26 (м, 1Н), 4,01 (т, J=12,2 Гц, 1Н), 3,92 (м, 1Н), 3,82 (с, 3H), 3,80 (с, 3H), 3,63 (дд, J=39,3, 13,1 Гц, 1Н), 3,52 (т, J=11.3 Гц, 1Н), 1,91 (м, 1Н), 1,73 (м, 1Н).
[00301] 7- [(S)-1-(1-Гидрокси-циклопропил)-этиламино]-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-18) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 30. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,16 (д, J=8,6 Гц, 1Н), 8,98 (с, 1Н), 8,36 (д, J=8,3 Гц, 1Н), 7,70 (д, J=8,3 Гц, 1Н), 7,60 (с, 1Н), 7,39 (с, 1Н), 7,32 (дд, J=12,6, 1,7 Гц, 1Н), 7,21 (д, J=8,7 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,77 (с, 1Н), 6,64 (д, J=8,6 Гц, 1Н), 6,22 (д, J=8,6 Гц, 1Н), 5,38 (с, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,67 (м, 1Н), 1,28 (д, J=6,5 Гц, 3H), 0,62-0,42 (м, 4Н).
[00302] 7-((2S,4R)-2-Гидроксиметил-тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-19) получают аналогичным образом, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют 87b. 1Н ЯМР (400 МГц, ДМСО) δ 9,20 (д, J=8,6 Гц, 1Н), 9,01 (с, 1Н), 8,37 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,60 (с, 1Н), 7,39 (с, 1Н), 7,32 (д, J=12,5 Гц, 1Н), 7,21 (д, J=8,1 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,94 (д, J=8,1 Гц, 1Н), 6,78 (с, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,62 (т, J=5,6 Гц, 1Н), 3,95 (м, 1Н), 3,86 (м, 1Н), 3,82 (с, 3H), 3,80 (с, 3H), 3,54-3,33 (м, 4Н), 1,95 (дд, J=35,7, 11,6 Гц, 2Н), 1,47 (м, 1Н), 1,26-1,11(м, 1Н).
[00303] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [4-(4-метил-пиперазин-1-ил)-пиридин-2-илметил]-амид (I-39) получают аналогичным образом, за исключением того, что на стадии 1, 50с заменяют 4-(4-метил-1-пиперазинил)-2-пиридинметанамином. 1Н ЯМР (400 МГц, ДМСО) δ 9,23 (т, J=5,6 Гц, 1Н), 9,03 (с, 1Н), 8,39 (д, J=8,3 Гц, 1Н), 8,14 (д, J=5,9 Гц, 1Н), 7,76 (д. J=8,3 Гц, 1Н), 7,04 (д, J=7,8 Гц, 1Н), 6,85 (с, 1Н), 6,77 (м, 2Н), 4,52 (д, J=5,6 Гц, 2Н), 3,90 (д, J=11,3 Гц, 3H), 3,46 (т, J=11,4 Гц, 2Н), 3,31-3,24 (м, 4Н), 2,39 (м, 4Н), 2,20 (с, 3H), 1,93 (д, J=12,5 Гц, 2Н), 1,52 (м, 2Н).
[00304] Пример 3
[00305] N-((S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-7-((S)-тетрагидрофуран-3-иламино)-1,6-нафтиридин-2-карбоксамид и N-((S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-7-((R)-тетрагидрофуран-3-иламино)-1,6-нафтиридин-2-карбоксамид (I-52 и I-53)

[00306] Названные в заголовке соединения получают в виде рацемата согласно методике из Примера 2, за исключением того, что на стадии 2 (S)-(+)-2-амино-1-пропанол заменяют тетрагидрофуран-3-амином, и затем разделяют хиральной суперкритической флюидной хроматографией (отнесение диастереомеров осуществлено произвольным образом).
[00307] Диастереомер 1: 1Н ЯМР (400 МГц, ДМСО) δ 9,21 (д, J=8,7 Гц, 1Н), 9,03 (с, 1Н), 8,40 (д, J=8,3 Гц, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,39 (с, 1Н), 7,32 (дд, J=12,6, 1,9 Гц, 1Н), 7,21 (м, 2Н), 7,13 (т, J=8,6 Гц, 1Н), 6,76 (с, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,33 (м, 1Н), 3,94 (дд, J=8,8, 5,9 Гц, 1Н), 3,87 (дд, J=15,4, 7,4 Гц, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,78-3,71 (м, 1Н), 3,64 (дд, J=8,8, 3,8 Гц, 1Н), 2,24 (м, 1Н), 1,90 (м, 1Н). ЖХМС (Способ G): RT=9,82 минуты, M+H+=477,2. ERK IC50 1,27 нМ.
[00308] Диастереомер 2: 1Н ЯМР (400 МГц, ДМСО) δ 9,21 (д, J=8,7 Гц, 1Н), 9,03 (с, 1Н), 8,40 (д, J=8,3 Гц, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,61 (с, 1Н), 7,39 (с, 1Н), 7,32 (дд, J=12,6, 1,9 Гц, 1Н), 7,24-7,18 (м, 2Н), 7,13 (т, J=8,6 Гц, 1Н), 6,76 (с, 1Н), 6,23 (д, J=8,6 Гц, 1Н), 4,32 (м, 1Н), 3,94 (дд, J=8,8, 5,9 Гц, 1Н), 3,87 (дд, J=15,3, 7,4 Гц, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,76 (м, 1Н), 3,64 (дд, J=8,8, 3,8 Гц, 1Н), 2,24 (м, 1Н), 1,90 (м, 1Н). ЖХМС (Способ G): RT=9,77 минуты, M+H+=477,2. ERK IC50 2,75 нМ.
[00309] Пример 4
[00310] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-7-(1-метил-1H-пиразол-5-иламино)-1,6-нафтиридин-2-карбоксамид (I-25)
[00311] Стадия 1: Смесь 74 (300 мг, 1,56 ммоль), 2-метилпиразол-3-амина (182 мг, 1,874 ммоль) и натрия гидрида (60 масс./масс. % суспензия в минеральном масле, 312 мг, 7,81 ммоль) разбавляют ДМФА (3,64 мл, 46,84 ммоль) и нагревают до 100°С, выдерживая при этой температуре в течение 1 часа. Реакционную смесь разбавляют 10 мл воды, упаривают под вакуумом с получением твердого вещества черного цвета, и затем растворяют в воде (15 мл) и промывают ДХМ (2×40 мл). Водную фракцию отделяют, нейтрализуют добавлением водн. HCl (11,6 моль/л) в воде (0,81 мл, 9,37 ммоль), и полученный осадок отделяют фильтрацией под вакуумом с получением 300 мг (71%) 7-(1-метил-1H-пиразол-5-иламино)-1,6-нафтиридин-2-карбоновой кислоты (80) в виде твердого вещества красного/коричневого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00312] Стадия 2: Смесь 80 (50 мг, 0,186 ммоль), ГАТУ (212 мг, 0,557 ммоль) и ДИПЭА (0,162 мл, 0,928 ммоль) в ДМФА (0,72 мл) перемешивают при комнатной температуре в течение 5 минут (раствор становится темно-коричневым). Через 5 минут добавляют 50с (61 мг, 0,223 ммоль) как твердое вещество, в виде одной порции, и реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь разбавляют EtOAc (100 мл) и промывают водой (100 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью метанола/ДХМ с градиентом (от 0 до 10% МеОН), с получением продукта в виде пены желтого/оранжевого цвета, которую дополнительно очищают обращенно-фазовой ВЭЖХ, элюируя смесью MeCN/H2O (содержащей 0,1% NH4OH) с градиентом (от 5 до 85% MeCN, 14 минут), с получением I-25 в виде твердого вещества светло-желтого цвета. 1Н ЯМР (400 МГц, ДМСО) δ 9,36 (д, J=8,9 Гц, 1Н), 9,18 (с, 1Н), 9,10 (с, 1Н), 8,53 (д, J=8,4 Гц, 1Н), 7,89 (д, J=8,4 Гц, 1Н), 7,59 (с, 1Н), 7,46 (д, J=1,9 Гц, 1Н), 7,37 (с, 1Н), 7,32 (дд, J=12,7, 2,1 Гц, 1Н), 7,20 (д, J=10,3 Гц, 1Н), 7,12 (т, J=8,7 Гц, 1Н), 6,94 (с, 1Н), 6,27 (д, J=1,9 Гц, 1Н), 6,25 (д, J=8,9 Гц, 1Н), 3,81 (с, 3H), 3,78 (с, 3H), 3,69 (с, 3H). ЖХМС (Способ Е): RT=4,14 минуты, M+H+=487,1.
[00313] 7-(2-Метил-2H-пиразол-3-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (I-7) получают аналогичным образом, за исключением того, что на стадии 2 50с заменяют 50а. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,48 (д, J=8,7 Гц, 1Н), 9,18 (с, 1Н), 9,11 (с, 1Н), 8,53 (д, J=8,4 Гц, 1Н), 7,89 (д, J=8,4 Гц, 1Н), 7,62 (с, 1Н), 7,58-7,53 (т, J=8,7 Гц, 1Н), 7,50 (д, J=1,9 Гц, 1Н), 7,46 (д, J=1,9 Гц, 1Н), 7,41 (с, 1Н), 7,32 (дд, J=8,3, 1,8 Гц, 1Н), 6,93 (с, 1Н), 6,32 (д, J=8,7 Гц, 1Н), 6,27 (д, J=1,9 Гц, 1Н), 3,79 (с, 3H), 3,69 (с, 3H).
[00314] 7-(2-Метил-2H-пиразол-3-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-1-(4-хлор-3-фтор-фенил)-2-гидрокси-этил]-амид (I-8) получают аналогичным образом, за исключением того, что на стадии 2 50с заменяют 62е. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,22 (д, J=8,2 Гц, 1Н), 9,19 (с, 1Н), 9,13 (с, 1Н), 8,54 (д, J=8,4 Гц, 1Н), 7,88 (д, J=8,4 Гц, 1Н), 7,53 (т, J=8,1 Гц, 1Н), 7,47 (дд, J=11,2, 1,9 Гц, 2Н), 7,27 (дд, J=8,3, 1,7 Гц, 1Н), 6,94 (с, 1Н), 6,29 (д, J=1,9 Гц, 1Н), 5,08 (м, 2Н), 3,84-3,72 (м, 2Н), 3,70 (с, 3H).
[00315] 7-(2-Метил-2Н-пиразол-3-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [(S)-1-(3-фтор-4-метокси-фенил)-2-гидрокси-этил]-амид (I-15) получают аналогичным образом, за исключением того, что на стадии 2 50с заменяют 62d. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,19 (с, 1Н), 9,12 (д, J=6,5 Гц, 2Н), 8,53 (д, J=8,4 Гц, 1Н), 7,88 (д, J=8,4 Гц, 1Н), 7,48 (д, J=1,5 Гц, 1Н), 7,28 (д, J=12,6 Гц, 1Н), 7,16 (д, J=8,6 Гц, 1Н), 7,10 (т, J=8,6 Гц, 1Н), 6,94 (с, 1Н), 6,65 (с, 1Н), 6,29 (с, 1Н), 5,02 (м, 2Н), 3,80 (с, 3H), 3,78-3,72 (м, 1Н), 3,70 (с, 3H).
[00316] Пример 5
[00317] N-((S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-3-((S)-1-гидроксипропан-2-иламино)изохинолин-6-карбоксамид (II-4) Способ D
[00318] Стадия 1: К охлажденной (0°С) суспензии С-1 (6,018 г, 26,98 ммоль, 1,00 экв.) в BMIM⋅BF4 (50 мл, 0,26 моль, 9,7 экв.) при перемешивании добавляют NO⋅BF4 (3,90 г, 32,7 ммоль, 1,21 экв.) в виде нескольких порций на протяжении 3 минут. Цвет смеси быстро меняется со светлого желто-коричневого до желто-оранжевого, и смесь нагревается до комнатной температуры с выделением азота. Через 15 минут выделение газа прекращается, и образуется подвижная суспензия желто-оранжевого цвета. Через 60 минут при комнатной температуре смесь обрабатывают насыщ. водн. NaHCO3, разбавляют водой и экстрагируют EtOAc. Нижний из 3-х слоев отбрасывают, и верхнюю EtOAc фракцию отделяют. Средний слой оранжево-коричневого цвета разбавляют достаточным количеством воды до гомогенного состояния, и снова экстрагируют EtOAc. Объединенные EtOAc фракции промывают водой и раствором соли, сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением 6,792 г бледно-коричневого кристаллического твердого вещества. Неочищенный остаток абсорбируют на силикагеле и очищают хроматографией на SiO2, элюируя смесью EtOAc/гептана с градиентом (0-30% EtOAc), с получением 4,248 г (70%) 6-бром-3-фторизохинолина (С-2) в виде твердого вещества белого цвета. 1Н ЯМР (400 МГц, CDCl3) δ 8,94 (с, 1Н), 8,00 (с, 1Н), 7,86 (д, J=8,8 Гц, 1Н), 7,63 (дд, J=8,8, 1,6 Гц, 1Н), 7,17 (с, 1Н). ЖХМС: MH+ 226,1/228,2.
[00319] Стадия 2: Раствор С-2 (1,01 г, 4,47 ммоль, 1,00 экв.) в ДМА (3,0 мл) обрабатывают по каплям (S)-2-аминопропан-1-олом (403 мг, 5,37 ммоль, 1,20 экв.) и ДИПЭА (1,17 мл, 6,70 ммоль, 1,50 экв.), и смесь нагревают до 100°С, выдерживая при этой температуре в течение 22 часов. Анализ методом ЖХМС обнаруживает смесь целевого продукта (MH+ 281/283) и исходного материала (МН+ 226/228) в соотношении 1,5:1 (254 нм). Смесь нагревают до 120°С, выдерживая при этой температуре в течение 48 часов, и затем охлаждают до комнатной температуры. Анализ методом ЖХМС показывает смесь целевого продукта и исходного материала в соотношении 9:1 (254 нм), загрязненную некоторым количеством O-арилированного побочного продукта. Смесь темно-коричневого цвета упаривают под вакуумом с получением 1,56 г маслянистого твердого вещества желто-коричневого цвета. Неочищенный продукт обрабатывают EtOAc и дважды промывают водой, затем раствором соли, сушат (Na2SO4), фильтруют и упаривают под вакуумом. Полученное твердое вещество зелено-желтого цвета (1,08 г) по данным ЯМР является смесью целевого продукта и исходного материала 1:1,5. Неочищенное вещество очищают автоматизированной флеш-хроматографией на SiO2, элюируя смесью EtOAc/гептана с градиентом (от 0 до 100% EtOAc), с получением 388 мг (31%) (S)-2-(6-бромизохинолин-3-иламино)пропан-1-ола (С-3, R2=(S)-1-гидроксипропан-2-иламино). 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,84 (с, 1Н), 7,79 (с, 1Н), 7,73 (д, J=8,7 Гц, 1Н), 7,21 (дд, J=8,7, 1,7 Гц, 1Н), 6,57 (с, 1Н), 6,26 (д, J=8,1 Гц, 1Н), 4,73 (т, J=5,6 Гц, 1Н), 3,83 (септет, J=6 Гц, 1Н), 3,51 (дт, J=10,4, 5,1 Гц, 1Н), 3,45-3,3 (1Н, заслоненный), 1,16 (д, J=6,5 Гц, 3Н). ЖХМС: MH+ 281,2/283,2.
[00320] Стадия 3: В колбу, содержащую дегазированный ДМФА (5,0 мл), в атмосфере азота помещают С-3 (R2=(S)-1-гидроксипропан-2-иламино) (377 мг, 1,34 ммоль, 1,00 экв.), Pd(OAc)2 (31,9 мг, 0.142 ммоль, 0,106 экв.), 1,3-бис(дициклогексилфосфино)-пропан бис(тетрафторборат) (90,8 мг, 0,144 ммоль, 0,107 экв.) и K2CO3 (381 мг, 2,73 ммоль, 2,04 экв.) и обрабатывают метанолом (0,55 мл, 14 ммоль, 10 экв.). Полученную смесь желто-оранжевого цвета нагревают до 100°С при продувании СО. Анализ методом ЖХМС через 1 час показывает отсутствие исходного материала, и смесь представляет собой смесь (254 нм) желательного метилового эфира (MH+ 261) и карбоновой кислоты (MH+ 247) 3,3:1. Реакционную смесь охлаждают, разбавляют водой и дважды экстрагируют EtOAc. Объединенные органические фракции промывают раствором соли, сушат (Na2SO4), фильтруют сквозь слой Celite® и упаривают под вакуумом с получением 315 мг твердого вещества темного желто-коричневого цвета. Неочищенный остаток абсорбируют на SiO2 и очищают флеш-хроматографией, элюируя смесью EtOAc/гептана с градиентом (от 0 до 100% EtOAc), с получением 0,1582 г (45%) С-4 (R2=(S)-1-гидроксипропан-2-иламино). 1Н ЯМР (400 МГц, CDCl3) δ 8,89 (с, 1Н), 8,28 (с, 1Н), 7,80 (д, J=8,5 Гц, 1Н), 7,76 (д, J=8,6 Гц, 1Н), 6,71 (с, 1Н), 4,60 (д, J=7,5 Гц, 1Н), 4,02-3,91 (м, 1Н), 3,97 (с, 3H), 3,85-3,76 (м, 1Н), 3,68-3,61 (м, 1Н), 2,82 (т, J=5,2 Гц, 1Н), 1,31 (д, J=6,6 Гц, 3H).
[00321] Стадия 4: Раствор С-4 (R2=(S)-1-гидроксипропан-2-иламино) (158 мг, 0,606 ммоль, 1,00 экв.) в ТГФ (5,0 мл) обрабатывают 1,0 М водн. LiOH (0,73 мл, 0,73 ммоль, 1,2 экв.) при комнатной температуре. Когда не остается следов исходного материала, рН оставшегося раствора доводят до 4 с помощью 2 н водн. H2SO4 (400 мкл) и раствора соли и экстрагируют EtOAc, содержащим приблизительно 10% МеОН. Отделенную водную фракцию желтого цвета еще дважды экстрагируют EtOAc. Объединенные органические фракции сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением 108,8 мг (73%) С-5 (R2=(S)-1-гидроксипропан-2-иламино) в виде твердого вещества желтого цвета, которое использовали без дополнительной очистки. ЖХМС соотношение массы и заряда M+H+=247.
[00322] Стадия 5: Суспензию С-5 (R2=(S)-1-гидроксипропан-2-иламино) (36,2 мг, 0,147 ммоль, 1,00 экв.) и ГАТУ (57,3 мг, 0,151 ммоль, 1,03 экв.) в ДМФА (2,0 мл) обрабатывают ДИПЭА (78 мкл, 0,45 ммоль, 3,0 экв.) при комнатной температуре. Через 10 минут полученный раствор янтарного цвета добавляют в виде одной порции к раствору 50с (47,4 мг, 0,174 ммоль, 1,19 экв.) и ДИПЭА (78 мкл, 0,45 ммоль, 3,0 экв.) в ДМФА (1,0 мл) при комнатной температуре. После расходования исходного материала, смесь разбавляют EtOAc и промывают последовательно водой, насыщ. води. NaHCO3 и раствором соли, сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением 42,3 мг желтого масла (42,3 мг). Неочищенный остаток очищают С-18 обращенно-фазовой ВЭЖХ, элюируя смесью MeCN/H2O (содержащей 0,1% NH4OH) с градиентом, с получением 15,0 мг (22%) II-4. 1Н ЯМР (400 МГц, ДМСО) δ 9,17 (д, J=8,6 Гц, 1Н), 8,89 (с, 1Н), 8,07 (с, 1Н), 7,84 (д, J=8,6 Гц, 1Н), 7,54 (с, 1Н), 7,52 (д, J=9,8 Гц, 1Н), 7,33 (с, 1Н), 7,27 (д, J=12,7 Гц, 1Н), 7,20 (д, J=10,1 Гц, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,69 (с, 1Н), 6,26 (д, J=8,5 Гц, 1Н), 6,18 (д, J=7,9 Гц, 1Н), 4,71 (т, J=5,5 Гц, 1Н), 3,88-3,78 (м, 1Н), 3,82 (с, 3H), 3,79 (с, 3H), 3,57-3,48 (м, 1Н), 3,45-3,3 (заслоненный, 1Н), 1,18 (д, J=6,5 Гц, 3H).
[00323] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-1) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,20 (д, J=8,6 Гц, 1Н), 8,91 (с, 1Н), 8,08 (с, 1Н), 7,84 (д, J=8,6 Гц, 1Н), 7,56-7,50 (м, 2Н), 7,33 (с, 1Н), 7,28 (дд, J=12,6, 2,0 Гц, 1Н), 7,22-7,17 (м, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,72 (с, 1Н), 6,52 (д, J=8,0 Гц, 1Н), 6,26 (д, J =8,5 Гц, 1Н), 3,93-3,86 (м, 2Н), 3,82 (с, 3H), 3,86-3,76 (м, 1Н), 3,79 (с, 3H), 3,44 (м, 2Н), 1,91 (д, J=12,6 Гц, 2Н), 1,49 (м, 2Н).
[00324] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(R)-1-(4-хлор-3-фтор-фенил)-пропил]-амид (II-2) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (R)-1-(4-хлор-3-фтор-фенил)пропан-1-амина гидрохлоридом (70b). 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,87 (д, J=8,2 Гц, 1Н), 8,05 (с, 1Н), 7,85 (д, J=8,5 Гц, 1Н), 7,55 (т, J=8,1 Гц, 1Н), 7,51 (д, J=8,5 Гц, 1Н), 7,46 (дд, J=10,6, 1,5 Гц, 1Н), 7,29 (д, J=8,3 Гц, 1Н), 6,74 (с, 1Н), 6,51 (д, J=7,9 Гц, 1Н), 4,95 (дд, J=14,8, 8,3 Гц, 1Н), 3,90 (м, 2Н), 3,83 (м, 1Н), 3,45 (т, J=10,7 Гц, 2Н), 1,92 (м, 2Н), 1,89-1,73 (м, 2Н), 1,56-1,43 (м, 2Н), 0,92 (т, J=7,3 Гц, 3H).
[00325] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-хлор-3-фтор-фенил)-2-гидрокси-этил]-амид (II-3) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 62е. 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,90 (с, 1Н), 8,87 (д, J=8 Гц, 1Н), 8,09 (с, 1Н), 7,85 (д, J=8,5 Гц, 1Н), 7,54 (т, J=8,2 Гц, 1Н), 7,53 (д, J=8,8 Гц, 1Н), 7,46 (д, J=10,7 Гц, 1Н), 7,29 (д, J=9,2 Гц, 1Н), 6,71 (с, 1Н), 6,24 (д, J=7,9 Гц, 1Н), 5,09 (к, J=7 Гц, 1Н), 3,84 (септет, J=7 Гц, 1Н), 3,77-3,65 (м, 2Н), 3,53 (дд, J=10,6, 4,8 Гц, 1Н), 3,36 (дд, J=10,5, 6,2 Гц, 1Н), 1,18 (д, J=6,5 Гц, 3Н).
[00326] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-5) получают аналогичным образом, за исключением того, что на стадии 5 (S)-50с заменяют 50h. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,24 (д, J=8,5 Гц, 1Н), 8,89 (с, 1Н), 8,08 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,57 (с, 1Н), 7,53 (д, J=8,5 Гц, 1Н), 7,43-7,35 (м, 2Н), 7,28 (д, J=8 Гц, 1Н), 7,26 (д, J=10 Гц, 1Н), 7,09 (т, J=8,5 Гц, 1Н), 6,70 (с, 1Н), 6,33 (д, J=8,5 Гц, 1Н), 6,18 (д, J=8,0 Гц, 1Н), 4,71 (т, J=5,6 Гц, 1Н), 3,87-3,78 (м, 1Н), 3,79 (с, 3H), 3,56-3,49 (1Н), 3,45-3,35 (заслоненный, 1Н), 1,18 (д, J=6,5 Гц, 3Н).
[00327] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-(4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-6) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 50i. 1Н ЯМР (400 МГц, ДМСО) δ 9,15 (д, J=8,5 Гц, 1Н), 8,89 (с, 1Н), 8,07 (с, 1Н), 7,83 (д, J=8,5 Гц, 1Н), 7,53 (д, J=10 Гц, 2Н), 7,51 (с, 1Н), 7,35 (д, J=8,6 Гц, 2Н), 7,31 (с, 1Н), 6,91 (д, J=8,7 Гц, 2Н), 6,69 (с, 1Н), 6,26 (д, J=8,6 Гц, 1Н), 6,17 (д, J=7,9 Гц, 1Н), 4,71 (т, J=5,5 Гц, 1Н), 3,88-3,78 (м, 1Н), 3,79 (с, 3H), 3,74 (с, 3H), 3,57-3,49 (м, 1Н), 3,5-3,3 (заслоненный, 1Н), 1,18 (д, J=6,5 Гц, 3H).
[00328] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(R)-1-(3-фтор-4-метокси-фенил)-пропил]-амид (II-7) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 70а. 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,89 (с, 1Н), 8,76 (д, J=8,4 Гц, 1Н), 8,02 (с, 1Н), 7,83 (д, J=8,5 Гц, 1Н), 7,50 (дд, J=8,5, 1,4 Гц, 1Н), 7,26 (дд, J=12,7, 1,9 Гц, 1Н),7,17(дд, J=8,6, 1,9 Гц, 1Н), 7,11 (т, J=8,6 Гц, 1Н), 6,70 (с, 1Н), 6,18 (д, J=8,0 Гц, 1Н), 4,89 (к, J=8,0 Гц, 1Н), 4,69 (т, J=5,5 Гц, 1Н), 3,88-3,79 (м, 1Н), 3,81 (с, 3H), 3,57-3,49 (м, 1Н), 3,41-3,32 (м, 1Н), 1,92-1,72 (м, 2Н), 1,18 (д, J=6,5 Гц, 3H), 0,90 (т, J=7,3 Гц, 3H).
[00329] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-8) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 50а. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,24 (д, J=8,3 Гц, 1Н), 8,89 (с, 1Н), 8,08 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,57 (т, J=8,0 Гц, 1Н), 7,57 (с, 1Н), 7,52 (дд, J=8,6, 1,2 Гц, 1Н), 7,47 (дд, J=10,6, 1,6 Гц, 1Н), 7,37 (с, 1Н), 7,32 (дд, J=8,3, 1,6 Гц, 1Н), 6,70 (с, 1Н), 6,32 (д, J=8,3 Гц, 1Н), 6,19 (д, J=8,1 Гц, 1Н), 4,70 (т, J=5,5 Гц, 1Н), 3,87-3,77 (м, 1Н), 3,79 (с, 3H), 3,57-3,49 (м, 1Н), 3,40-3,33 (м, 1Н), 1,18 (д, J=6,5 Гц, 3H).
[00330] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-9) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-(3-фтор-фенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50h). 1Н ЯМР (400 МГц, ДМСО) δ 9,26 (д, J=8,5 Гц, 1Н), 8,91 (с, 1Н), 8,10 (с, 1Н), 7,84 (д, J=8,6 Гц, 1Н), 7,57 (с, 1Н), 7,54 (дд, J=8,5, 1,4 Гц, 1Н), 7,40 (тд, J=8,0, 6,1 Гц, 1Н), 7,36 (с, 1Н), 7,30-7,24 (м, 2Н), 7,09 (тд, J=8,6, 2,5 Гц, 1Н), 6,73 (с, 1Н), 6,51 (д, J=8,0 Гц, 1Н), 6,33 (д, J=8,5 Гц, 1Н), 3,92-3,86 (м, 2Н), 3,86-3,80 (м, 1Н), 3,79 (с, 3H), 3,44 (тд, J=11,8, 2,0 Гц, 2Н), 1,92 (д, J=10,5 Гц, 2Н), 1,49 (ддд, J=15,6, 12,0, 4,2 Гц, 2Н).
[00331] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-10) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-(4-метокси-фенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50i). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,17 (д, J=8,6 Гц, 1Н), 8,90 (с, 1Н), 8,08 (с, 1Н), 7.83 (д, J=8,6 Гц, 1Н), 7,54 (дд, J=8,5, 1,4 Гц, 1Н), 7,51 (с, 1Н), 7,35 (д, J=8,6 Гц, 2Н), 7,32 (с, 1Н), 6,91 (д, J=8,6 Гц, 2Н), 6,71 (с, 1Н), 6,50 (д, J=8,0 Гц, 1Н), 6,26 (д, J=8,6 Гц, 1Н), 3,93-3,86 (м, 2Н), 3,86-3,80 (м, 1Н), 3,79 (с, 3H), 3,74 (с, 3H), 3,44 (тд, J=11,5, 2,0 Гц, 2Н), 1,92 (д, J=10,6 Гц, 2Н), 1,49 (ддд, J=15,5, 12,0, 4,3 Гц, 2Н).
[00332] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-11) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-(4-хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50а). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,26 (д, J=8,4 Гц, 1Н), 8,91 (с, 1Н), 8,10 (с, 1Н), 7,84 (д, J=8,6 Гц, 1Н), 7,57 (т, J=8,4 Гц, 1Н), 7,57 (с, 1Н), 7,53 (дд, J=8,5, 1,4 Гц, 1Н). 7,48 (дд, J=10,6, 1,9 Гц, 1Н), 7,37 (с, 1Н), 7,32 (дд, J=8,4, 1,8 Гц, 1Н), 6,73 (с, 1Н), 6,52 (д, J=7,9 Гц, 1Н), 6,32 (д, J=8,3 Гц, 1Н), 3,93-3,86 (м, 2Н), 3,86-3,80 (м, 1Н), 3,79 (с, 3H), 3,44 (тд, J=11,5, 2,0 Гц, 2Н), 1,92 (д, J=10,4 Гц, 2Н), 1,49 (ддд, J=15,4, 12,0, 4,3 Гц, 2Н).
[00333] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-хлор-3-фтор-фенил)-2-гидрокси-этил]-амид (II-12) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-2-амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлоридом (62е). 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,83 (д, J=7,9 Гц, 1Н), 8,10 (с, 1Н), 7,85 (д, J=8,6 Гц, 1Н), 7,55 (т, J=8,1 Гц, 1Н), 7,53 (дд, J=8,6, 1,6 Гц, 1Н), 7,47 (дд, J=10,6, 1,8 Гц, 1Н), 7,29 (дд, J=8,3, 1,7 Гц, 1Н), 6,74 (с, 1Н), 6,53 (д, J=7,9 Гц, 1Н), 5,10 (к, J=7,1 Гц, 1Н), 5,03 (т, J=5,8 Гц, 1Н), 3,94-3,87 (м, 2Н), 3,87-3,78 (м, 1Н), 3,78-3,64 (м, 2Н), 3,45 (тд, J=11,5, 2,0 Гц, 2Н), 1,92 (д, J=12,4 Гц, 2Н), 1,56-1,43 (м, 2Н).
[00334] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-фтор-4-метокси-фенил)-2-гидрокси-этил]-амид (II-17) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-2-амино-2-(3-фтор-4-метоксифенил)этанола гидрохлоридом (62d). 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,76 (д, J=8,5 Гц, 1Н), 8,08 (с, 1Н), 7,85 (д, J=8,5 Гц, 1Н), 7,53 (д, J=9,0 Гц, 1Н), 7,27 (д, J=13,0 Гц, 1Н), 7,17 (д, J=8,5 Гц, 1Н), 7,11 (т, J=8,5 Гц, 1Н), 6,73 (с, 1Н), 6,55 (д, J=8,0 Гц, 1Н), 5,06-5,02 (м, 1Н), 4,96 (т, J=5,5 Гц, 1Н), 3,91-3,89 (м, 2Н), 3,81 (с, 3H), 3,70-3,61 (м, 2Н), 3,46-3,42 (м, 3H), 1,94-1,91 (м, 2Н), 1,52-1,45 (м, 2Н).
[00335] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-фтор-4-метокси-фенил)-2-гидрокси-этил]-амид (II-18) получают аналогичным образом, за исключением того, что на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-2-амино-2-(3-фтор-4-метоксифенил)этанола гидрохлоридом (62d). 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,90 (с, 1Н), 8,74 (д, J=8,2 Гц, 1Н), 8,07 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,52 (дд, J=8,5, 1,4 Гц, 1Н), 7,27 (дд, J=12,7, 1,9 Гц, 1Н), 7,17 (дд, J=8.6, 1,8 Гц, 1Н), 7,11 (т, J=8,6 Гц, 1Н), 6,70 (с, 1Н), 6,23 (д, J=8,0 Гц, 1Н), 5,04 (тд, J=7,9, 6,9 Гц, 1Н). 4,93 (т, J=5,8 Гц, 1Н), 4,72 (т, J=5,6 Гц, 1Н), 3,88-3,80 (м, 1Н), 3,81 (с, 3H), 3,74-3,60 (м, 2Н), 3,53 (дт, J=10,4, 5,2 Гц, 1Н), 3,36 (дт, J=10,6, 6,0 Гц, 1Н), 1,18 (д, J=6,5 Гц, 3H).
[00336] N-((S)-1-(3-Фторфенил)-2-гидроксиэтил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-20) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют (S)-2-амино-2-(3-фторфенил)этанола гидрохлоридом (62а). 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,94 (с, 1Н), 8,87 (д, J=8 Гц, 1Н), 8,13 (с, 1Н), 7,88 (д, J=8,5 Гц, 1Н), 7,56 (д, 7=8,5 Гц, 1Н), 7,38 (м, 1Н), 7,26 (д, J=8,0 Гц, 2Н), 7,08 (т, J=19.5 Гц, 1Н), 6,84 (д, J=6 Гц, 1Н), 6,72 (с, 1Н), 5,12 (м, 1Н), 5,02 (т, J=11,5 Гц, 1Н), 4,32 (т, J=6,0, 1Н), 3,96-3,93 (м, 1Н), 3,87 (м, 1Н), 3,78-3,67 (м, 3H), 3,61 (м, 1Н), 2,23 (м, 1Н), 1,98 (м, 1Н).
[00337] N-((S)-2-Гидрокси-1-(4-метоксифенил)этил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-21) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют 62 с. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,93 (с, 1Н), 8,78 (д, J=8 Гц, 1Н), 8,10 (с, 1Н), 7,86 (д. J=8,5 Гц, 1Н), 7,55 (дд, J=8,5, 1,5 Гц, 1Н), 7,33 (д, J=9,0 Гц, 2Н), 6,89 (д, J=9,0 Гц, 2Н), 6,82 (д, J=6,0 Гц, 1Н), 6,70 (с, 1Н), 5,04 (м, 1Н), 4,91 (т, J=6,0 Гц, 1Н), 4,30 (м, 1Н), 3,95 (м, 1Н), 3,86 (м, 1Н), 3,77-3,64 (м, 5Н), 3,62-3,60 (м, 2Н), 2,23 (м, 1Н), 1,87 (м, 1Н).
[00338] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-фтор-фенил)-2-гидрокси-этил]-амид (II-22) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 62а. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,86 (д, J=10,0 Гц, 1Н), 8,10 (с, 1Н), 7,85 (д, J=11,0 Гц, 1Н), 7,53 (дд, J=10,5, 2,0 Гц, 1Н), 7,37 (м, 1Н), 7,27-7,25 (м, 2Н), 7,07 (м, 1Н), 6,70 (с, 1Н), 6,29 (д, J=10,0 Гц, 1Н), 5,11 (м, 1Н), 5,03 (т, J=7,5 Гц, 1Н), 4,76 (т, J=7,5 Гц, 1Н), 3,83 (м, 1Н), 3,76-3,64 (м, 2Н), 3,53 (м, 1Н), 3,31 (м, 1Н), 1,18 (д, J=8,5 Гц, 3H).
[00339] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты (4-фтор-1H-индол-2-илметил)-амид (II-23) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 38. 1Н ЯМР (500 МГц, ДМСО-d6) δ 11,31 (с, 1Н), 9,14 (т, J=5,5 Гц, 1Н), 8,90 (с, 1Н), 8,06 (с, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,57 (м, 1Н), 7,20 (д, J=8,0 Гц, 1Н), 7,01 (м, 1Н), 6,75-6,70 (м, 2Н), 6,38 (с, 1Н), 6,26 (д, J=8,0 Гц, 1Н), 4,73 (дд, J=5,5, 6,0 Гц, 1Н), 4,65 (д, J=5,5 Гц, 2Н), 3,84 (м, 1Н), 3,52 (м, 1Н), 3,35 (м, 1Н), 1,17(д, J=6,5 Гц, 3H).
[00340] 3-(Тетрагидро-фуран-3-иламино)-изохинолин-6-карбоновой кислоты (4-фтор-1H-индол-2-илметил)-амид (II-25) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют 38. 1Н ЯМР (500 МГц, ДМСО-d6) δ 11,32 (с, 1Н), 9,16 (т, J=5,5 Гц, 1Н), 8,94 (с, 1Н), 8,12 (с, 1Н), 7,89 (д, J=8,5 Гц, 1Н), 7,59 (м, 1Н), 7,20 (д, J=8,0 Гц, 1Н), 7,01 (м, 1Н), 6,83 (д, J=6,5 Гц, 1Н), 6,75-6,70 (м, 2Н), 6,39(с, 1Н), 4,66 (д, J=5,5 Гц, 2Н), 4,32 (м, 1Н), 3,94 (м, 1Н), 3,85 (м, 1Н), 3,75 (м, 1Н), 3,59 (м, 1Н), 2,22 (м, 1Н), 1,87 (м, 1Н).
[00341] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-3-ил)-метил]-амид (II-24) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,25 (д, J=9,0 Гц, 1Н), 8,89 (с, 1Н), 8,09 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,62 (д, J=2,0 Гц, 1Н), 7,53 (дд, J=8,5, 1,5 Гц, 1Н), 7,27 (дд, J=12,5, 2,0 Гц, 1Н), 7,18 (д, J=9,0 Гц, 1Н), 7,12 (т, J=8,5 Гц, 1Н), 6,70 (с, 1Н), 6,32 (д, J=8,0 Гц, 1Н), 6,26 (д, J=8,5 Гц, 1Н), 6,20 (д, J=2,0 Гц, 1Н), 4,75 (т, J=5,5 Гц, 1Н), 3,85-3,78 (м, 8Н), 3,52 (м, 1Н), 1,17 (д, J=6,5 Гц, 3H).
[00342] N-((S)-1-(3-Фтор-4-метоксифенил)-2-гидроксиэтил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-26) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-2-амино-2-(3-фтор-4-метоксифенил)этанола гидрохлоридом (62d) 1H ЯМР (500 МГц, CD3OD) δ 8,89 (с, 1Н), 8,09 (с, 1Н), 7,89 (д, J=8,5 Гц, 1Н), 7,59 (д, J=6,5 Гц, 1Н), 7,22-7,19 (м, 2Н), 7,09 (т, J=8,5 Гц, 1Н), 6,80 (с, 1Н), 5,18 (м, 1Н), 4,42 (м, 1Н), 4,07-3,99 (м, 2Н), 3,92-3,85 (м, 6Н), 3,76 (м, 1Н), 2,38 (м, 1Н), 1,98 (м, 1Н).
[00343] N-((R)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-27) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют (R)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,26 (д, J=9 Гц, 1Н), 8,92 (с, 1Н), 8,45 (с, 0,4Н), 8,28 (с, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,62 (д, J=2 Гц, 1Н), 7,56 (дд, J=8,55, 1,5 Гц, 1Н), 7,26 (дд, J=12,5, 1,5 Гц, 1Н), 7,18 (д, J=9 Гц, 1Н), 7,12 (т, J=9 Гц, 1Н), 6,83 (д, J=6 Гц, 1Н), 6,70 (с, 1Н), 6,32 (д, J=9 Гц, 1Н), 6,20 (д, J=2 Гц, 1Н), 4,30 (м, 1Н), 3,94 (м, 1Н), 3,85 (к, J=7,5 Гц, 1Н), 3,81 (с, 3H), 3,80 (с.3H), 3,75 (м, 1Н), 3,59 (дд, J=8,5, 3,5 Гц, 1Н), 2,22 (м, 1Н), 1,87 (м, 1Н).
[00344] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-2-гидрокси-1-(4-метокси-фенил)-этил]-амид (II-28) получают аналогичным образом, за исключением того, что на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют 62 с. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,89 (с, 1Н), 8,77 (д, J=7,5 Гц, 1Н), 8,07 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,52 (д, J=9,0 Гц, 1Н), 7,33 (д, J=8,5 Гц, 2Н), 6,89 (д, J=9,0 Гц, 2Н), 6,97 (с, 1Н), 6,26 (д, J=8,0 Гц, 1Н), 5,03 (м, 1Н), 4,91 (т, J=5,5 Гц, 1Н), 4,75 (т, J=5,5 Гц, 1Н), 3,82 (м, 1Н), 3,72-3,68 (м, 4Н), 3,62 (м, 1Н), 3,53 (м, 1Н), 3,35 (м, 1Н), 1,17 (д, J=6,0 Гц, 3H).
[00345] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-хлор-4-фтор-фенил)-2-гидрокси-этил]-амид (II-29) получают аналогичным образом, за исключением того, что на стадии 5 50с заменяют 62f. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,90 (с, 1Н), 8,85 (д, J=8,0 Гц, 1Н), 8,08 (с, 1Н), 7,85 (д, J=8,5 Гц, 1Н), 7,64 (м, 1Н), 7,51 (д, J=8,5 Гц, 1Н), 7,44-7,36 (м, 2Н), 6,71 (с, 1Н), 6,28 (д, J=8,0 Гц, 1Н), 5,09-5,02 (м, 2Н), 4,75 (т, J=4,4 Гц, 1Н), 3,83 (т, J=6,3 Гц, 1Н), 3,74-3,65 (м, 2Н), 3,53 (дд, J=11, 5,5 Гц, 1Н), 3,36 (дд, J=12, 6,0 Гц, 1Н), 1,18 (д, J=6,0 Гц, 3H).
[00346] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-2-гидрокси-1-(4-трифторметокси-фенил)-этил]-амид (II-30) получают аналогичным образом, за исключением того, что на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют 62b. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,90 (с, 1Н), 8,78 (д, J=8,5 Гц, 1Н), 8,09 (с, 1Н), 7,55-7,52 (м, 3H), 7,33 (д, J=8,0 Гц, 2Н), 6,70 (с, 1Н), 6,27 (д, J=8,5, 1Н), 5,12 (м, 1Н), 5,01 (с, 1Н), 4,74 (т, J=6,5 Гц, 1Н), 3,83-3,67 (м, 3H), 3,52 (м, 1Н), 3,32 (м, 1Н), 1,78 (д, J=6,5 Гц, 3H).
[00347] N-((S)-(3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-5-ил)метил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-31) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-5-ил)метанамина гидрохлоридом (50f). 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,46 (с, J=6,5 Гц, 1Н), 8,93 (с, 1Н), 8,13 (с, 1Н), 7,87 (д, J=8,0 Гц, 1Н), 7,55 (д, J=7,5 Гц, 1Н). 7,34-7,17 (м, 4Н), 6,84 (д, J=6,0 Гц, 1Н), 6,70 (с, 1Н), 6,49 (д, J=8,5 Гц, 1Н), 5,95 (д, J=1,5 Гц, 1Н), 4,40 (м, 1Н), 3,94 (м, 1Н), 3,88-3,83 (м, 4Н), 3,76-3,74 (м, 4Н), 3,59 (м, 1Н), 2,20 (м, 1Н), 1,89 (м, 1Н).
[00348] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-3-ил)-метил]-амид (II-32) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидропираном, и на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,07 (с, 1Н), 8,84 (с, 1Н), 8,78 (д, J=8,1 Гц, 1Н), 8,23 (с, 1Н), 8,00 (д, J=8,6 Гц, 1Н), 7,70 (д, J=8,5 Гц, 1Н), 7,42 (д, J=1,7 Гц, 1Н), 7,26 (д, J=12,7 Гц, 1Н), 7,17 (д, J=8,6 Гц, 1Н), 7,11 (т, J=8,6 Гц, 1Н), 6,94 (с, 1Н), 6,24 (д, J=1,7 Гц, 1Н), 5,04 (дд, J=13,8, 7,7 Гц, 2Н), 3,81 (с, 3H), 3,73-3,60 (м, 5Н).
[00349] N-((S)-1-(3-Хлор-4-фторфенил)-2-гидроксиэтил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-38) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют (S)-1-амино-2-(3-хлор-4-фтор-фенил)этанола гидрохлоридом 62f. 1H ЯМР (500 МГц, ДМСО-d6) δ 8,93 (с, 1Н), 8.87 (д, J=8,5 Гц, 1Н), 8,12 (с, 1Н), 7,87 (д, J=8,5 Гц, 1Н), 7,64 (дд, J=7,0, 2,0 Гц, 1Н), 7,55 (д, J=8,5 Гц, 1Н), 7,44-7,36 (м, 2Н), 6,84 (д, J=6,5 Гц, 1Н), 6,71 (с, 1Н), 5,10-5,03 (м, 2Н), 4,31 (м, 1Н), 3,95 (м, 1Н), 3,86 (м, 1Н), 3,77-3,75 (м, 2Н), 3,73 (м, 1Н), 3,61 (м, 1Н), 2,23 (м, 1Н), 1,87 (м, 1Н).
[00350] N-((S)-1-(3-Хлор-4-цианофенил)-2-гидроксиэтил)-3-(тетрагидрофуран-3-иламино)изохинолин-6-карбоксамид (II-39) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют 62i. 1H ЯМР (500 МГц, ДМСО-d6) δ 8,96 (д, J=7,5 Гц, 1Н), 8,94 (с, 1Н), 8,14 (с, 1Н), 7,95 (д, J=8,0 Гц, 1Н), 7,89 (д, J=8,5 Гц, 1Н), 7,81 (с, 1Н), 7,60 (д, J=7,5 Гц, 1Н), 7,56 (д, J=8,5 Гц, 1Н), 6,86 (д, J=6,5 Гц, 1Н), 6,72 (с, 1Н), 5,17-5,13 (м, 2Н), 4,31 (т, J=2,8 Гц, 1Н), 3,95 (м, 1Н), 3,87 (дд, J=16,0, 8,0 Гц, 1Н), 3,78-3,73 (м, 3H), 3,61 (дд, J=8,5, 3,5 Гц, 1Н), 2,23 (м, 1Н), 1,89 (м, 1Н).
[00351] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-фтор-фенил)-2-гидрокси-этил]-амид (II-40) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидропираном. и на стадии 5 50с заменяют (S)-2-амино-2-(4-фторфенил)этанолом (62г). 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,84 (д, J=8,5 Гц, 1Н), 8,10 (с, 1Н), 7,85 (д, J=8,5 Гц, 1Н), 7,53 (д, J=8,5 Гц, 1Н), 7,37 (м, 1Н), 7,25 (д, J=7,5 Гц, 2Н), 7,07 (м, 1Н), 6,74 (с, 1Н), 6,56 (д, J=8,0 Гц, 1Н), 5,11 (м, 1Н), 5,01 (т, J=5,5 Гц, 1Н), 3,91-3,84 (м, 3H), 3,73-3,66 (м, 2Н), 3,47-3,42 (м, 2Н), 1,94-1,91 (м, 2Н), 1,50-1,48 (м, 2Н).
[00352] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-2-гидрокси-1-(4-метокси-фенил)-этил]-амид (II-41) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-l-амино-2-(4-фторфенил)этанолом 62с. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,76 (д, J=8 Гц, 1Н), 8,08 (с, 1Н), 7,84 (д, J=8,5 Гц, 1Н), 7,53 (д, J=8,5 Гц, 1Н), 7,33 (д, J=8,5 Гц, 2Н), 6,89 (д, J=8,0 Гц, 2Н), 6,73 (с, 1Н), 6,55 (д, J=8,5 Гц, 1Н), 5,05 (м, 1Н), 4,90 (т, J=5,5 Гц, 1Н), 3,91-3,83 (м, 3H), 3,73-3,68 (м, 4Н), 3,63 (м, 1Н), 3,47-3,42 (м, 2Н), 1,94-1,91 (м, 2Н), 1,51-1,48 (м, 2Н).
[00353] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-хлор-4-циано-фенил)-2-гидрокси-этил]-амид (II-42) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидропираном, и на стадии 5 50с заменяют 62i. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,95-8,92 (м, 2Н), 8,11 (с, 1Н), 7,96 (д, J=7,5 Гц, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,81 (с, 1Н), 7,60 (д, J=8,5 Гц, 1Н), 7,53 (д, J=8,5 Гц, 1Н), 6,74 (с, 1Н), 6,58 (д, J=7,5 Гц, 1Н), 5,15-5,11 (м, 2Н), 3,92-3,70 (м, 5Н), 3,47-3,42 (м, 2Н), 1,94-1,91 (м, 2Н), 1,51-1,48 (м, 2Н).
[00354] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-2-гидрокси-1-(4-метокси-фенил)-этил]-амид (II-43) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют (3S,4S)-3-фтортетрагидро-2Н-пиран-4-амином (71с), и на стадии 5 50с заменяют (S)-2-амино-2-(4-метоксифенил)этанола гидрохлоридом (62с). 1Н ЯМР (500 МГц, ДМСО-d6): δ 8,93 (с, 1Н), 8,80 (д, J=8,5 Гц, 1Н), 8,09 (с, 1Н), 7,87 (д, J=9,0 Гц, 1Н), 7,56 (д, J=9,0 Гц, 1Н), 7,33 (д, J=8,5 Гц, 2Н), 6,90 (с, 1Н), 6,89 (д, J=8,5 Гц, 2Н), 6,67 (д, J=8,5 Гц, 1Н), 5,07-5,02 (м, 1Н), 4,92 (т, J=11,5 Гц, 1Н), 4,78 (д, J=50,0 Гц, 1Н), 4,30-4,20 (м, 1Н), 4,05-3,99 (м, 1Н), 3,94-3,90 (м, 1Н), 3,73-3,50 (м, 7Н), 1,92-1,80 (м, 1Н), 1,75-1,70 (м, 1Н).
[00355] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(R)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-3-ил)-метил]-амид (II-50) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидропираном, и на стадии 5 50с заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (500 МГц, ДМСО-d6): δ 9,23 (д, J=8,5 Гц, 1Н), 8,91 (с, 1Н), 8,10 (с, 1Н), 7,84 (д, J=8,0 Гц, 1Н), 7,62 (д, J=2,0 Гц, 1Н), 7,54 (дд, J=8,5, 1,5 Гц, 1Н), 7,27 (д, J=12,5, 1,5 Гц, 1Н), 7,20-7,10 (м, 2Н), 6.54 (д, J=8,0 Гц, 1Н), 6,32 (д, J=8,5 Гц, 1Н), 6,20 (д, J=2,5 Гц, 1Н), 3,91-3,88 (м, 2Н), 3,82-3,80 (м, 7Н), 3,46-3,42 (м, 2Н), 1,93-1,90 (м, 2Н), 1,50-1,48 (м, 2Н).
[00356] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(R)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-3-ил)-метил]-амид (II-51) получают аналогичным образом, за исключением того, что на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (500 МГц, МеОН-d4): δ 8,86 (с, 1Н), 8,06 (с, 1Н), 7,87 (д, J=8,5 Гц, 1Н), 7,58-7,56 (м, 2Н), 7,18-7,10 (м, 2Н), 7,09-7,06 (м, 1Н), 6,81 (с, 1Н), 6,41 (с, 1Н), 6,20 (с, 1Н), 3,93-3,87 (м, 7Н), 3,68-3,65 (м, 2Н), 1,30 (с, 3H).
[00357] 3-(Тетрагидро-фуран-3-иламино)-изохинолин-6-карбоновой кислоты [(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-3-ил)-метил]-амид (II-52) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 3-амино-тетрагидрофураном, и на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-3-ил)метанамина гидрохлоридом (50d). 1Н ЯМР (500 МГц, ДМСО-d6): δ 9,26 (д, J=9,0 Гц, 1Н), 8,93 (с, 1Н), 8,28 (с, 0,4Н), 8,12 (с, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,63 (с, 1Н), 7,62-7,55 (м, 1Н), 7,47-7,25 (м, 1Н), 7,18 (д, J=9,0 Гц, 1Н), 7,14-7,10 (м, 1Н), 6,82 (д, J=6,0 Гц, 1Н), 6,70 (с, 1Н), 6,32 (д, J=9,0 Гц, 1Н), 6,20 (с, 1Н), 4,31-4,29 (м, 1Н), 3,95-3,92 (м, 1Н), 3,88-3,72 (м, 8Н), 3,61-3,58 (м, 1Н), 2,50-2,20 (м, 1Н), 1,84-1,76 (м, 1Н).
[00358] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-хлор-4-фтор-фенил)-2-гидрокси-этил]-амид (II-53) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют (3S,4S)-3-фтортетрагидро-2H-пиран-4-амином (71с), и на стадии 5 50с заменяют (S)-2-амино-2-(3-хлор-4-фтор-фенил)этанола гидрохлоридом (62f). 1H ЯМР (500 МГц, MeOH-d4): δ 8,90 (с, 1Н), 8,08 (с, 1Н), 7,90 (д, J=8,5 Гц, 1Н), 7,60-7,57 (м, 2Н), 7,43-7,30 (м, 1Н), 7,27-7,23 (м, 1Н), 6,93 (с, 1Н), 5,21-5,18 (м, 1Н), 4,86-4,73 (м, 1Н), 4,27-4,12 (м, 2Н), 4,05-4,02 (м, 1Н), 3,91-3,86 (м, 2Н), 3,75-3,62 (м, 2Н), 2,04-1,96 (м, 1Н), 1,90-1,87 (м, 1Н),
[00359] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-хлор-3-фтор-фенил)-2-гидрокси-этил]-амид (II-54) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют (3S,4S)-3-фтортетрагидро-2H-пиран-4-амином (71с), и на стадии 5 50с заменяют (S)-2-амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлоридом (62е). 1H ЯМР (500 МГц, МеОН-d4): δ 8,90 (с, 1Н), 8,09 (с, 1Н), 7,92-7,88 (м, 1Н), 7,61-7,59 (м, 1Н), 7,47-7,45 (м, 1Н), 7,38-7,33 (м, 1Н), 7,28-7,24 (м, 1Н), 6,91 (д, J=9,0 Гц, 1Н), 5,21 (т, J=6,5 Гц, 1Н), 4,84-4,73 (м, 1Н), 4,27-4,11 (м, 2Н), 4,05-4,02 (м, 1Н), 3,92-3,80 (м, 2Н), 3,75-3,60 (м, 2Н), 2,06-1,96 (м, 1Н), 1,93-1,88 (м, 1Н).
[00360] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(3-хлор-4-циано-фенил)-2-гидрокси-этил]-амид (II-55) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют (3S,4S)-3-фтортетрагидро-2H-пиран-4-амином (71с), и на стадии 5 50с заменяют 62i. 1Н ЯМР (500 МГц, MeOD-d4): δ 8,79 (с, 1Н), 7,98 (с, 1Н), 7,79 (д, J=8,5 Гц, 1Н), 7,70 (д, J=8,5 Гц, 1Н), 7,62 (с, 1Н), 7,49-7,45 (м, 2Н), 7,81 (с, 1Н), 5,12 (т, J=5,5 Гц, 1Н), 4,71-4,61 (м, 1Н), 4,16-4,00 (м, 2Н), 3,94-3,90 (м, 1Н), 3,80-3,79 (м, 2Н), 3,64-3,52 (м, 2Н), 1,92-1,85 (м, 1Н), 1,77-1,73 (м, 1Н).
[00361] 3-(Тетрагидро-фуран-3-иламино)-изохинолин-6-карбоновой кислоты [1-(4-дифторметокси-фенил)-2-гидрокси-этил]-амид (II-56) получают аналогичным образом, за исключением того, что на стадии 2 50с заменяют 3-амино-тетрагидрофураном, и на стадии 5 50с заменяют (S)-2-амино-2-(4-(трифторметокси)фенил)этанола гидрохлоридом (62h).
[00362] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-дифторметокси-фенил)-2-гидрокси-этил]-амид (II-58) получают аналогичным образом, за исключением того, что на стадии 5 58с заменяют (S)-2-амино-2-(4-(трифторметокси)фенил)этанола гидрохлоридом (62b). 1Н ЯМР (500 МГц, МеОН-d4): δ 8,84 (с, 1Н), 8,07 (с, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,57 (д, J=8,0 Гц, 1Н), 7,49 (д, J=8,5 Гц, 2Н), 7,15 (д, J=8,0 Гц, 2Н), 6,82-6,79 (м, 2Н), 5,26-5,22 (м, 1Н), 3,93-3,89 (м, 3H), 3,68-3,59 (м, 2Н), 1,24 (д, J=6,5 Гц. 3H).
[00363] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-хлор-4-циано-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-59) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют (3S,4S)-3-фтортетрагидро-2H-пиран-4-амином (71с), и на стадии 5 50с заменяют (S)-4-(амино(1-метил-1Н-пиразол-4-ил)метил)-2-хлорбензонитрила гидрохлоридом (44). 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,39 (д, J=8,0 Гц, 1Н), 8,94 (с, 1Н), 8,11 (с, 1Н), 7,99 (д, J=8,5 Гц, 1Н), 7,87 (д, J=9,0 Гц, 1Н), 7,81 (с, 1Н), 7,63-7,55 (м, 3H), 7,41 (с, 1Н), 6,89 (с, 1Н), 6,69 (д, J=8,0 Гц, 1Н), 6,38 (д, J=8,0 Гц, 1Н), 4,78 (д, J=49,5 Гц, 1Н), 4,25-4,19 (м, 1Н), 4,01 (т, J=13,0 Гц, 1Н), 3,93-3,90 (м, 1Н), 3,79 (с, 3H), 3,67-3,49 (м, 3H), 1,91-1,83 (м, 1Н), 1,73-1,70 (м, 1Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 519,2 [М+Н]+.
[00364] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-дифторметокси-фенил)-2-гидрокси-этил]-амид (II-61) получают аналогичным образом, за исключением того, что на стадии 2 (S)-2-аминопропан-1-ол заменяют 4-амино-тетрагидропираном, и на стадии 5 (S)-(3-фтор-4-метокси-фенил)-(1-метилпиразол-4-ил)метанамина гидрохлорид заменяют (S)-2-амино-2-(4дифторметокси-фенил)этанолом (62h).
[00365] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты (4-фтор-1H-индол-2-илметил)-амид (II-67) получают аналогичным образом, за исключением того, что на стадии 2 71с используют вместо (S)-2-аминопропан-1-ола, и на стадии 5 38 используют вместо 50с. 1Н ЯМР (500 МГц, ДМСО-d6) δ 11,33 (с, 1Н), 9,18 (т, J=5,5 Гц, 1Н), 8,94 (с, 1Н), 8,11 (с, 1Н), 7,89 (д, J=8,5 Гц, 1Н), 7,60 (д, J=10,5 Гц, 1Н), 7,19 (д, J=8,5 Гц, 1Н), 7,02-6,98 (м, 1Н), 6,89 (с, 1Н), 6,75-6,69 (м, 2Н), 6,38 (с, 1Н), 4,78 (д, J=49,5 Гц, 1Н), 4,66-4,65 (м, 2Н), 4,27-4,21 (м, 1Н), 4,03-3,90 (м, 2Н), 3,67-3,49 (м, 2Н), 1,91-1,81 (м, 1Н), 1,73-1,70 (м, 1Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 437,2 [М+Н]+.
[00366] 3-((3S,4S)-3-Фтор-тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-68) получают аналогичным образом, за исключением того, что на стадии 2 71с используют вместо (S)-2-аминопропан-1-ола. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,25 (д, J=8,5 Гц, 1Н), 8,93 (с, 1Н), 8,09 (с, 1Н), 7,86 (д, J=8,5 Гц, 1Н), 7,57-7,53 (м, 2Н), 7,33 (с, 1Н), 7,28 (д, J=12,5 Гц, 1Н), 7,20 (д, J=10 Гц, 1Н), 7,19-7,12 (м, 1Н), 6,88 (с, 1Н), 6,67 (д, J=8,5 Гц, 1Н), 6,26 (д, J=8,5 Гц, 1Н), 4,78 (д, J=49,5 Гц, 1Н), 4,25-4,19 (м, 1Н), 4,01 (т, J=12 Гц, 1Н), 3,93-3,90 (м, 1Н), 3,67 (с, 3H), 3,64 (с, 3H), 3,59-3,49 (м, 2Н), 1,91-1,83 (м, 1Н), 1,73-1,70 (м, 1Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 568,3 [М+Н]+.
[00367] Пример 6
[00368] (S)-3-(1,3-Диметил-1H-пиразол-5-иламино)-N-(1-(3-фтор-4-метоксифенил)-2-гидроксиэтил)изохинолин-6-карбоксамид (II-44)
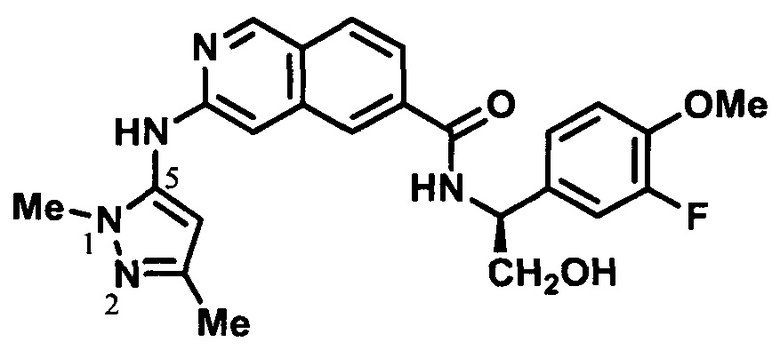
[00369] Стадия 1: Высушенную в печи круглодонную колбу вместимостью 100 мл, оборудованную мешалкой, охлаждают в атмосфере азота и помещают в колбу 1,3-диметил-1H-пиразол-5-амин (491,7 мг, 4,42 ммоль) и 45 мл безводного ТГФ (0,1 М). Раствор ТГФ обрабатывают твердым LiHMDS (1,481 г, 8,84 ммоль) и перемешивают при комнатной температуре в течение 5 минут, после чего образуется твердое вещество желтого цвета. Добавляют С-2 (500 мг, 2,21 ммоль) в виде одной порции. На колбу устанавливают обратный холодильник, и реакционную смесь нагревают до 80°С. Реакцию контролируют ЖХМС; через 2 часа при температуре 80°С реакция завершается на 90%. Реакционную смесь охлаждают до комнатной температуры, и ТГФ удаляют на роторном испарителе. Неочищенный остаток распределяют между ДХМ и водой. Фракцию ДХМ промывают раствором соли, сушат (MgSO4), фильтруют и упаривают. Неочищенный остаток абсорбируют на Celite® и очищают хроматографией на SiO2, элюируя смесью EtOAc/гептана с градиентом (от 50 до 100% EtOAc), с получением 328 мг (47%) 6-бром-N-(1,3-диметил-1H-пиразол-5-ил)-изохинолин-3-амина (82).
[00370] Стадия 2: Карбонилирование 82 (429 мг) осуществляют с помощью методики, раскрытой на стадии 3 Примера 5, с получением 350 мг (87%) метил-3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоксилата (84) в виде твердого вещества желтого/коричневого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00371] Стадия 3: Суспензию 84 (350 мг, 1,181 ммоль) и LiOH (62,2 мг, 2,60 ммоль) в смеси ТГФ (5,75 мл) и воды (0,85 мл) перемешивают при комнатной температуре в течение 24 часов. ТГФ удаляют на роторном испарителе. Реакционную смесь суспендируют в воде (6 мл) и обрабатывают 10 М HCl в воде (0,71 мл, 7,1 ммоль). Образуется осадок желто-коричневого цвета, который отделяют фильтрацией с получением 3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоновой кислоты (86), которую использовали на следующей стадии без дополнительной очистки.
[00372] Стадия 4: В пробирку для обработки микроволнами вместимостью 10 мл помещают 86 (29,7 мг, 0,105 ммоль, 62d (15 мг, 0,081) и ДМФА (1,0 мл) и обрабатывают ГАТУ (47,6 мг, 0,121 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 30 минут для предварительной активации, после чего обрабатывают ТЭА (0,046 мл, 0,324 ммоль). Реакционную смесь фильтруют, и затем очищают препаративной обращенно-фазовой ВЭЖХ (Varian HPLC с использованием Gemini-NX С-18 (3,0×100 см, 10 мкм) при скорости потока 60 мл/минут, NH4OH 5-50% MeCN в течение 10 минут) с получением 22,1 мг (60,7%) II-45 в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, ДМСО) δ 9,06 (с, 1Н), 8,86-8,69 (м, 2Н), 8,24 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,69 (д, J=8,5 Гц, 1Н), 7,33-7,22 (м, 1Н), 7,14 (дт, J=17,2, 8,6 Гц, 2Н), 6,93 (с, 1Н), 6,03 (с, 1Н), 5,04 (дд, J=13,8, 7,8 Гц 1Н), 4,94 (т, J=5,8 Гц, 1Н), 3,81 (с, 3H), 3,75-3,61 (м, 2Н), 3,61 (с, 3H), 2,15 (с, 3H). ЖХМС: MH+ 450,2.
[00373] (S)-3-(1,3-Диметил-1H-пиразол-5-иламино)-N-((3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)изохинолин-6-карбоксамид (II-37) получают аналогичным образом, за исключением того, что на стадии 4 62d заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50с). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,20 (д, J=8,5 Гц, 1Н), 9,05 (с, 1Н), 8,78 (с, 1Н), 8,24 (с, 1Н), 7,98 (д, J=8,6 Гц, 1Н), 7,70 (д, J=8,5 Гц, 1Н), 7,53 (с, 1Н), 7,32 (с, 1Н), 7,30-7,23 (м, 1Н), 7,16 (дт, J=17,2, 8,6 Гц, 2Н), 6,92 (с, 1Н), 6,26 (д, J=8,4 Гц, 1Н), 6,02 (с, 1Н), 3,80 (д, J=13,3 Гц, 6Н), 3,60 (с, 3H), 2,14 (с, 3H).
[00374] (S)-N-(1-(4-Хлор-3-фторфенил)-2-гидроксиэтил)-3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-45) получают аналогичным образом, за исключением того, что на стадии 4 62d заменяют (S)-2-амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлоридом (62е). 1Н ЯМР (400 МГц, ДМСО) δ 9,06 (с, 1Н), 8,85 (д, J=8,0 Гц, 1Н), 8,80 (с, 1Н), 8,26 (с, 1Н), 7,99 (д, J=8,5 Гц, 1Н), 7,69 (д, J=8,5 Гц, 1Н), 7,55 (т, J=8,0 Гц, 1Н), 7,47 (д, J=10,6 Гц, 1Н), 7,29 (д, J=8,3 Гц, 1Н), 6,94 (с, 1Н), 6,03 (с, 1Н), 5,10 (дд, J=13,8, 7,2 Гц, 1Н), 5,03 (т, J=5,8 Гц, 1Н), 3,78-3,63 (м, 2Н), 3,61 (с, 3H), 2,15 (с, 3H).
[00375] (R)-N-(1-(4-Хлор-3-фторфенил)пропил)-3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-46) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (R)-1-(4-хлор-3-фтор-фенил)пропан-1-амина гидрохлоридом (70b). 1Н ЯМР (400 МГц, ДМСО) δ 9,06 (с, 1Н), 8,89 (д, J=8,2 Гц, 1Н), 8,79 (с, 1Н), 8,21 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,67 (д, J=8,5 Гц, 1Н), 7,55 (т, J=8,0 Гц, 1Н), 7,49-7,40 (м, 1Н), 7,28 (д, J=8,3 Гц, 1Н), 6,94 (с, 1Н), 6,03 (с, 1Н), 4,95 (дд, J=14,8, 8,3 Гц, 1Н), 3,61 (с, 3H), 2,15 (с, 3H), 1,82 (м, J=20,8, 13,8, 6,7 Гц, 2Н), 0,92 (т, J=7,3 Гц, 3H).
[00376] (S)-N-((4-Хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метил)-3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-48) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (S)-(4-хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50а). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,28 (д, J=8,3 Гц, 1Н), 9,06 (с, 1Н), 8,79 (с, 1Н), 8,26 (с, 1Н), 7,98 (д, J=8,6 Гц, 1Н), 7,69 (д, J=8,5 Гц, 1Н), 7,63-7,53 (м, 2Н), 7,47 (д, J=10,6 Гц, 1Н), 7,36 (с, 1Н), 7,31 (д, J=8,3 Гц, 1Н), 6,93 (с, 1Н), 6,31 (д, J=8,2 Гц, 1Н), 6,02 (с, 1Н), 3,79 (с, 3H), 3,60 (с, 3H), 2,14 (с, 3H).
[00377] Пример 7
[00378] (S)-N-(1-(3-Фтор-4-метоксифенил)-2-гидроксиэтил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-36)
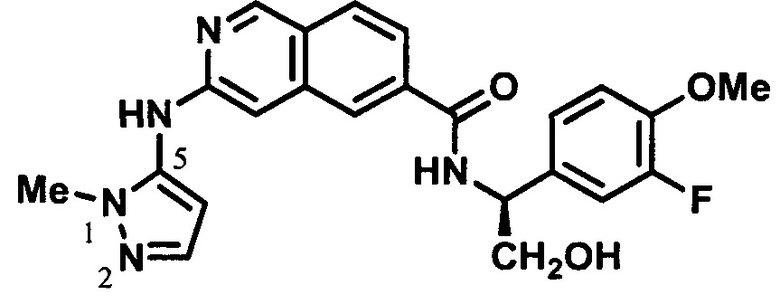
[00379] Стадия 1: Карбонилирование С-2 (500 мг, 2,12 мМ) осуществляют с применением методики, раскрытой на стадии 3 Примера 5, с получением 413 мг (91%) метил-3-фторизохинолин-6-карбоксилата (88) в виде твердого вещества белого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00380] Стадия 2: Суспензию 88 (413 мг, 2,013 ммоль) и LiOH (56 мг, 2,34 ммоль) в смеси ТГФ (9,8 мл) и воды (1,5 мл) перемешивают при комнатной температуре в течение 1,5 часов. Добавляют еще 50 мг LiOH (всего: 106 мг, 4,43 ммоль), и реакционную смесь перемешивают еще в течение 2 часов. ТГФ удаляют на роторном испарителе. Реакционную смесь суспендируют в воде (10 мл) и обрабатывают 10 М HCl в воде (0,604 мл, 6,04 ммоль). Белый замутненный осадок отделяют вакуумной фильтрацией. Осадок промывают водой (2×2 мл) и сушат под центральным вакуумом в течение ночи с получением 349 мг (100%) 3-фторизохинолин-6-карбоновой кислоты (90) в виде твердого вещества белого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00381] Стадия 3: В атмосфере азота 1-метил-1H-пиразол-5-амин (284,5 мг, 2,93 ммоль) растворяют в ТГФ (17,8 мл) при комнатной температуре и обрабатывают 1,0 М LiHMDS в ТГФ (5,86 мл, 5,86 ммоль). Реакционную смесь энергично перемешивают в течение 10 минут, и затем добавляют 90 (280 мг, 1,4647 ммоль) как твердое вещество в виде одной порции. На круглодонной реакционной колбе вместимостью 100 мл устанавливают холодильник с водяным охлаждением и нагревают до 80°С. Через 3,5 часа реакция завершается на 30%, поэтому добавляют дополнительное количество 1,0 М LiHMDS (8,86 мл, всего: 14,72 мл, 14,72 ммоль), и реакционную смесь нагревают до 80°С, выдерживая еще в течение 2,5 часов (общее время при 80°С=6 часов). Реакционную смесь разбавляют водой (20 мл), переносят в делительную воронку и промывают ДХМ (4×30 мл). Смывы ДХМ объединяют, и водную фракцию нейтрализуют путем добавления 1,26 мл 11,6 М водного HCl. Полученный осадок отделяют вакуумной фильтрацией с получением 373 мг (94%) 3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоновой кислоты (92), которую использовали без какой-либо дополнительной очистки.
[00382] Стадия 4: (S)-N-(1-(3-Фтор-4-метоксифенил)-2-гидроксиэтил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид получают из 92 (15 мг, 0,081 ммоль, 1,0 экв.) путем опосредованного ГАТУ сочетания, как раскрыто для стадии 4 Примера 7, с использованием (S)-2-амино-(3-фтор-4-метоксифенил)этанола гидрохлорида (62d) в качестве аминного соединения, с получением 8,3 мг (24%) II-37 в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, ДМСО) δ 9,07 (с, 1Н), 8,84 (с, 1Н), 8,23 (с, 1Н), 8,00 (д, J=8,6 Гц, 1Н), 7,70 (д, J=8,5 Гц, 1Н), 7,53 (с, 2Н), 7,42 (д, J=1,7 Гц, 1Н), 7,26 (д, J=12,7 Гц, 1Н), 7,17 (д, J=8,6 Гц, 1Н), 6,94 (с, 1Н), 6,24 (д, J=1,7 Гц, 1Н), 5,04 (дд, J=13,8, 7,7 Гц, 2Н), 3,81 (с, 3H), 3,73 (с, 3H), 3,66 (м, 2Н). ЖХМС: МН+ 436,1.
[00383] (R)-N-(4-Хлор-3-фторфенил)пропил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-13) получают аналогичным образом, за исключением того, что на стадии 4 62d заменяют (R)-1-(4-хлор-3-фтор-фенил)пропан-1-амина гидрохлоридом (70b). 1Н ЯМР (400 МГц, ДМСО) δ 9,07 (с, 1Н), 8,89 (д, J=8,1 Гц, 1Н), 8,83 (с, 1Н), 8,20 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,67 (дд, J=8,5, 1,5 Гц, 1Н), 7,54 (т, J=8,1 Гц, 1Н), 7,50-7,36 (м, 2Н), 7,28 (дд, J=8,3, 1,8 Гц, 1Н), 6,94 (с, 1Н), 6,23 (д, J=1,9 Гц, 1Н). 4,95 (дд, J=14,8, 8,4 Гц, 1Н), 3,69 (с, 3Н), 1,83 (м, J=20,7, 13,7, 6,9 Гц, 2Н), 0,92 (т, J=7,3 Гц, 3H).
[00384] (S)-N-(1-(4-Хлор-3-фторфенил)-2-гидроксиэтил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-14) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (S)-2-амино-2-(4-хлор-3-фтор-фенил)этанола гидрохлоридом (62е). 1Н ЯМР (400 МГц, ДМСО) δ 9,07 (с, 1Н), 8,83 (д, J=4,1 Гц, 2Н), 8,23 (д, J=12,1 Гц, 1Н), 8,00 (д, J=8,6 Гц, 1Н), 7,70 (дд, J=8,5, 1,4 Гц, 1Н), 7,54 (т, J=8,0 Гц, 1Н), 7,51-7,38 (м, 2Н), 7,29 (дд, J=8,3, 1,7 Гц, 1Н), 6,94 (с, 1Н), 6,24 (д, J=1,9 Гц, 1Н), 5,14-4,97 (м, 2Н), 3,69 (с, 3H), 3,82-3,60 (м, 2Н).
[00385] (S)-N-((4-Хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-15) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (S)-(4-хлор-3-фторфенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50а). 1Н ЯМР (400 МГц, ДМСО) δ 9,27(д, J=8,2 Гц, 1Н), 9,07 (с, 1Н), 8,83 (с, 1Н), 8,25 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,70 (дд, J=8,6, 1,5 Гц, 1Н), 7,62-7,52 (м, 2Н), 7,47 (дд, J=0,6, 1,9 Гц, 1Н), 7,41 (д, J=1,9 Гц, 1Н), 7,36 (с, 1Н), 7,31 (дд, J=8,3, 1,8 Гц, 1Н), 6,93 (с, 1Н), 6,31 (д, J=8,3 Гц, 1Н), 6,23 (д, J=1,9 Гц, 1Н), 3,79 (с, 3H), 3,69 (с, 3H).
[00386] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-16) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50с). 1H ЯМР (400 МГц, ДМСО) δ 9,20 (д, J=8,5 Гц, 1Н), 9,06 (с, 1Н), 8,82 (с, 1Н), 8,23 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,70 (дд, J=8,6, 1,4 Гц, 1Н), 7,53 (с, 1Н), 7,41 (д, J=1,9 Гц, 1Н), 7,32 (с, 1Н), 7,27 (дд, J=12,6, 2,0, 1Н), 7,27-7,17 (м, 1Н), 7,13 (т, J=8,6 Гц, 1Н), 6,93 (с, 1Н), 6,24 (дд, J=11,5, 5,2 Гц, 2Н), 3,82 (с, 3H), 3,79 (с, 3H), 2,49 (с, 3H).
[00387] (R)-N-(1-(3-Хлор-4-фторфенил)пропил)-3-(1-метил-1H-пиразол-5-иламино)изохинолин-6-карбоксамид (II-15) получают аналогичным образом, за исключением того, что на стадии 4 62 заменяют (R)-1-(3-хлор-4-фтор-фенил)пропан-1-амина гидрохлоридом (70с). 1Н ЯМР (400 МГц, ДМСО) δ 9,07 (с, 1Н), 8,88 (д, J=8,2 Гц, 1Н), 8,83 (с, 1Н), 8,19 (с, 1Н), 7,99 (д, J=8,6 Гц, 1Н), 7,67 (дд, J=8,6, 1,4 Гц, 1Н), 7,64 (дд, J=7,2, 2,0 Гц, 1Н), 7,45-7,33 (м, 3H), 6,94 (с, 1Н), 6,24 (д, J=1,9 Гц, 1Н), 4,94 (дд, J=14,9, 8,4 Гц, 1Н), 3,69 (с, 3H), 1,83 (м, 2Н), 0,91 (т, J=7,3 Гц, 3H).
[00388] Пример 8
[00389] (S)-N-(1-(4-Хлор-3-фторфенил)-2-гидроксиэтил)-3-(2-метилпиридин-4-иламино)изохинолин-6-карбоксамид (II-47)
[00390] Стадия 1: Сухой сцинтилляционный флакон вместимостью 40 мл, оборудованный навинчивающейся крышкой с тефлоновой вставкой, охлаждают в атмосфере азота, устанавливают мешалку, помещают в колбу 2-метилпиридин-4-амин (263 мг, 3,32 ммоль) и безводный ТГФ (27 мл) и выдерживают в атмосфере N2. Добавляют LiHMDS как твердое вещество (0,925 г, 5,53 ммоль). Реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 5 минут. К смеси добавляют 6-бром-3-фтор изохинолин (500 мг, 2,21 ммоль), флакон продувают N2, тщательно укупоривают и помещают на предварительно нагретую масляную баню с температурой 85°С. Через 4 часа при 85°С добавляют дополнительное количество 2-метилпиридин-4-амина (96 мг, всего: 359 мг, 3,32 ммоль) и LiHMDSi (185 мг, всего: 1,11 г, 6,64 ммоль), и реакционную смесь нагревают еще в течение 2 часов при 85°С. Реакционную смесь охлаждают, и ТГФ удаляют под вакуумом. Неочищенную реакционную смесь распределяют между водой и ДХМ, содержащим 10% МеОН. Органическую фракцию промывают раствором соли, сушат (Na2SO4), фильтруют и упаривают. Неочищенный остаток абсорбируют на Celite® и очищают хроматографией на SiO2, элюируя смесью метанола/ДХМ с градиентом (от 0 до 10% МеОН), с получением 196 мг (28%) 6-бром-N-(2-метилпиридин-4-ил)изохинолин-3-амина (94) в виде твердого вещества желтого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00391] Стадия 2: Карбонилирование 94 (196 мг, 0,624 мМ) осуществляют с применением методики, раскрытой на стадии 3 Примера 5, с получением 132 мг (72%) метил-3-(2-метилпиридин-4-иламино)изохинолин-6-карбоксилата (96) в виде твердого вещества желтого цвета, которое использовали на следующей стадии без дополнительной очистки.
[00392] Стадия 3: Суспензию 96 (132 мг, 0,45 ммоль) в смеси ТГФ (2,19 мл) и воды (0,324 мл) обрабатывают твердым LiOH (24 мг, 0,99 ммоль) и перемешивают в течение 3 часов. ТГФ удаляют под вакуумом, смесь суспендируют в воде (6,0 мл) и обрабатывают водным HCl (10 М, 0,27 мл). Осадок желто-коричневого цвета отделяют вакуумной фильтрацией с получением 3-(2-метилпиридин-4-иламино)изохинолин-6-карбоновой кислоты (98) в виде твердого вещества желтого цвета, которое использовали на следующих стадия без дополнительной очистки.
[00393] Стадия 4: (S)-N-(1-(4-Хлор-3-фторфенил)-2-гидроксиэтил)-3-(2-метилпиридин-4-иламино)изохинолин-6-карбоксамид получают из 92 (15 мг, 0,081 ммоль, 1,0 экв.) путем опосредованного ГАТУ сочетания, как раскрыто для стадии 4 Примера 6, с использованием (S)-2-амино-(4-хлор-3-фтор-фенил)этанола гидрохлорида (62е). Неочищенный продукт реакции сочетания и десилилирования очищают препаративной обращенно-фазовой ВЭЖХ (ВЭЖХ Waters под контролем масс-спектроскопии с использованием Gemini-NX С-18 (3,0×100 см, 10 мкм при скорости 60 мл/мин NH4OH, 20-60% MeCN в течение 10 минут)) с получением II-48 в виде твердого вещества желтого цвета (54 мг, 32%). 1Н ЯМР (400 МГц, ДМСО) δ 9,59 (с, 1Н), 9,21 (с, 1Н), 8,95 (д, J=7,9 Гц, 1Н), 8,34 (с, 1Н), 8,22-8,13 (м, 2Н), 8,08 (д, J=8,6 Гц, 1Н), 7,81 (д, J=8,5 Гц, 1Н), 7,56 (т, J=8,1 Гц, 1Н), 7,49 (д, J=10,6 Гц, 1Н), 7,44-7,34 (м, 3H), 7,31 (д, J=8,3 Гц, 1Н), 5,15-5,07 (м, 1Н), 3,77-3,66 (м, 2Н), 2,40 (с, 3H). ЖХМС [М+Н]+=451,1.
[00394] 3-(2-Метил-пиридин-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(3-фтор-4-метокси-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-33) получают аналогичным образом, за исключением того, что в реакции сочетания 62е заменяют (S)-(3-фтор-4-метоксифенил)(1-метил-1H-пиразол-4-ил)метанамина гидрохлоридом (50с). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,56 (с, 1Н), 9,30 (д, J=8,5 Гц, 1Н), 9,20 (с, 1Н), 8,33 (с, 1Н), 8,18 (д, J=5,6 Гц, 1Н), 8,06 (д, J=8,6 Гц, 1Н), 7,80 (д, J=8,5 Гц, 1Н), 7,55 (с, 1Н), 7,42-7,33 (м, 4Н), 7,29 (д, J=14,3 Гц, 1Н), 7,22 (д, J=8,7 Гц, 1Н), 7,14 (т, J=8,6 Гц, 1Н), 6,28 (д, J=8,4 Гц, 1Н), 3,81 (д, J=12,1 Гц, 6Н), 2,39 (с, 3H).
[00395] 3-(2-Метил-пиридин-4-иламино)-изохинолин-6-карбоновой кислоты [(S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метил]-амид (II-34) получают аналогичным образом, за исключением того, что 62е в реакции сочетания заменяют (S)-(4-хлор-3-фтор-фенил)-(1-метил-1H-пиразол-4-ил)-метанамина гидрохлоридом (50а). 1Н ЯМР (400 МГц, ДМСО) δ 9,57 (с, 1Н), 9,38 (д, J=8,3 Гц, 1Н), 9,20 (с, 1Н), 8,35 (с, 1Н), 8,18 (д, J=5,6 Гц, 1Н), 8,08 (т, J=8,7 Гц, 1Н), 7,80 (д, J=8,6 Гц, 1Н), 7,63-7,53 (м, 2Н), 7,50 (д, J=9,3 Гц, 1Н), 7,43-7,29 (м, 5Н), 6,34 (д, J=8,3 Гц, 1Н), 3,80 (с, 3H), 2,39 (с, 3H).
[00396] 3-(2-Метил-пиридин-4-иламино)-изохинолин-6-карбоновой кислоты [(R)-1-(3-хлор-4-фтор-фенил)-пропил]-амид (II-35) получают аналогичным образом, за исключением того, что 62е в реакции сочетания заменяют (R)-1-(3-хлор-4-фтор-фенил)пропан-1-амина гидрохлоридом (70с). 1Н ЯМР (400 МГц, ДМСО) δ 9,56 (с, 1Н), 9,20 (с, 1Н), 8,98 (д, J=8,2 Гц, 1Н), 8,29 (с, 1Н), 8,18 (д, J=5,6 Гц, 1Н), 8,07 (д, J=8,6 Гц, 1Н), 7,78 (д, J=8,6 Гц, 1Н), 7,65 (дд, J=7,2, 1,9 Гц, 1Н), 7,42 (м, J=14,1, 8,8, 5,0 Гц, 5Н), 4,96 (дд, J=14,9, 8,3 Гц, 1Н), 2,40 (с, 3H), 1,86 (м, J=27,7, 13,9, 7,1 Гц, 2Н), 0,93 (т, J=7,3 Гц, 3H).
[00397] Пример 9
[00398] N-((5-Бензилпиридин-3-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-20)
[00399] Стадия 1: N-((5-Бромпиридин-3-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (100) может быть получен в соответствии с методикой из Примера 1, с использованием (5-бромпиридин-3-ил)метанамина вместо 50с. Продукт используют на следующей стадии без дополнительной очистки.
[00400] Стадия 2: Смесь 100 (70 мг, 0,158 ммоль), бензилцинка бромида (0,5 моль/л) в ТГФ (0,9 мл, 0,475 ммоль) и бис(ди-трет-бутил(4-диметиламинофенил)фосфин)дихлорпалладия (II) (11,2 мг, 0,0158 ммоль) нагревают до 80°С, выдерживая при этой температуре в течение 3 часов. Реакционную смесь разбавляют EtOAc (50 мл) и промывают водой (50 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением остатка, который очищают обращенно-фазовой ВЭЖХ, элюируя смесью MeCN/H2O с градиентом (содержит 0,1% NH4OH, 14 минут), с получением 17,4 мг (24%) I-20 в виде твердого вещества желтого цвета. 1H ЯМР (400 МГц, ДМСО) δ 9,42 (т, J=6,3 Гц, 1Н), 9,01 (с, 1Н), 8,41 (д, J=2,0 Гц, 1Н), 8,38 (с, 1Н), 8,37 (д, J=5,3 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,60 (с, 1Н), 7,30-7,15 (м, 5Н), 7,01 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 4,50 (д, J=6,2 Гц, 2Н), 3,96 (с, 2Н), 3,94-3,87 (м, 2Н), 3,86 (с, 1Н), 3,44 (тд, J=11,5, 1,9 Гц, 2Н), 1,92 (д, J=12,5 Гц, 2Н), 1,59-1,46 (м, 2Н). ЖХМС (Способ Е): RT=3,58 минут, [М+Н]+=454,2.
[00401] N-((4-Бензилпиридин-2-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-36) получают аналогичным образом, за исключением того, что на стадии 1 (5-бромпиридин-3-ил)метанамин заменяют (4-бромпиридин-2-ил)метанамином. 1Н ЯМР (400 МГц, ДМСО) δ 9,33 (т, J=5,9 Гц, 1Н), 9,03 (с, 1Н), 8,42 (д, J=5,1 Гц, 1Н), 8,39 (д, J=8,3 Гц, 1Н), 7,75 (д, J=8,3 Гц, 1Н), 7,30-7,15 (м, 5Н), 7,13 (д, J=5,0 Гц, 1Н), 7,00 (д, J=7,8 Гц, 1Н), 6,77 (с, 1Н), 4,61 (д, J=6,0 Гц, 2Н), 3,95 (с, 2Н), 3,91 (м, 3H), 3,45 (т, J=10,9 Гц, 2Н), 1,93 (д, J=12,6 Гц, 2Н), 1,53 (тд, J=15,4, 4,2 Гц, 2Н).
[00402] N-(3-Бензилбензил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-42) получают аналогичным образом, за исключением того что 3-бром-бензиламин на стадии 1 используют вместо 50i. 1Н ЯМР (400 МГц, ДМСО) δ 9,33 (т, J=6,4 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,75 (д, J=8,3 Гц, 1Н), 7,29-7,01 (м, 10Н), 6,74 (с, 1Н), 4,49 (д, J=6,3 Гц, 2Н), 3,90 (д, J=12,7 Гц, 4Н), 3,87-3,79 (м, 1Н), 3,44 (т, J=11,1 Гц, 2Н), 1,92 (д, J=12,5 Гц, 2Н), 1,52 (ддд, J=15,2, 12,0, 4,2 Гц, 2Н).
[00403] N-((2-Бензилпиридин-3-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-54) получают аналогичным образом, за исключением того, что на стадии 1 (5-бромпиридин-3-ил)метанамин заменяют (2-бромпиридин-3-ил)метанамином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,34 (т, J=6,2 Гц, 1Н), 9,02 (с, 1Н), 8,43 (д, J=4,8 Гц, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,67 (д, J=7,7 Гц, 1Н), 7,30-7,21 (м, 5Н), 7,16 (м, 1Н), 7,05 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 4,56 (д, J=6,2 Гц, 2Н), 4,27 (с, 2Н), 3,90 (д, J=11,7 Гц, 2Н), 3,87-3,79 (м, 1Н), 3,44 (т, J=11,3 Гц, 2Н), 1,92 (д, J=13,2 Гц, 2Н), 1,52 (м, 2Н).
[00404] Пример 10
[00405] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты [2-(3-бром-фенил)-этил]-амид (I-35) и N-(3-(1-метил-1H-пиразол-4-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-41)
[00406] Стадия 1: N-[2-(3-Бромфенил)этил]-7-(тетрагидропиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-35) получают, как описано в Примере 1, с использованием 2-(3-бромфенил)этанамина вместо 50с. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,87 (т, J=5,9 Гц, 1Н), 8,37 (д, J=8,3 Гц, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,49 (с, 1Н), 7,43-7,38 (м, 1Н), 7,29-7,23 (м, 2Н), 7,00 (д, J=7,7 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,81 (м, 1Н), 3,91 (д, J=11,5 Гц, 2Н), 3,57 (к, J=6,9 Гц, 2Н), 3,45 (т, J=11,0 Гц, 2Н), 2,91 (т, J=7,3 Гц, 2Н), 1,93 (д, J=11,1 Гц, 2Н), 1,53 (кд, J=11,7, 4,2 Гц, 2Н).
[00407] Стадия 2: Суспензию I-35 (63,1 мг, 0,139 ммоль, 1,00 экв.), 1-метилпиразол-4-борной кислоты пинаколинового эфира (102, 120 мг, 0,550 ммоль, 3,97 экв.) и бис-(ди-трет-бутил(4-диметиламинофенил)-фосфин)дихлорпалладия (II) (20,8 мг, 0,029 ммоль, 0,212 экв.) в MeCN (3,0 мл) обрабатывают 1,0 М водн. Na2CO3 (1,0 мл, 1,0 ммоль, 7,2 экв.), и смесь облучают в микроволновом реакторе (СЕМ, 300 Вт) при 130°С, выдерживая при этой температуре в течение 20 минут. Охлажденную смесь разбавляют EtOAc, промывают водн. NaHCO3 и раствором соли, сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением 90,3 мг желтого масла. Неочищенный продукт очищают обращенно-фазовой ВЭЖХ (С18) с градиентом смеси MeCN/H2O (содержащей 0,1% аммония гидроксида), с получением 43,8 мг (69%) I-41 в виде твердого вещества светло-желтого цвета (43,8 мг, 69%). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,92 (т, J=6,0 Гц, 1Н), 8,37 (д, J=8,4 Гц, 1Н), 8,07 (с, 1Н), 7,81 (с, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,46 (с, 1Н), 7,40 (д, J=7,7 Гц, 1Н), 7,28 (т, J=7,6 Гц, 1Н), 7,09 (д, J=7,5 Гц, 1Н), 7,03 (д, J=7,8 Гц, 1Н), 6,72 (с, 1Н), 3,91 (д, J=11,6 Гц, 2Н), 3,93-3,80 (м, 1Н), 3,83 (с, 3H), 3,60 (дд, J=13,8, 6,8 Гц, 2Н), 3,45 (т, J=11,3 Гц, 2Н), 2,91 (т, J=7,3 Гц, 2Н), 1,92 (д, J=12,7 Гц, 2Н), 1,52 (кд, J=11,6, 4,2 Гц, 2Н). ЖХМС (способ Е): RT 4,13 минут, MH+ 457,2.
[00408] N-(3-(Пиридин-4-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-47) получают аналогичным образом, за исключением того, что 102 на стадии 2 заменяют 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином. 1Н ЯМР (400 МГц, ДМСО) δ 9,02 (с, 1Н), 8,95 (т, J=5,9 Гц, 1Н), 8,56 (д, J=5,6 Гц, 2Н), 8,37 (д, J=8,3 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,70-7,62 (м, 4Н), 7,46 (т, J=7,6 Гц, 1Н), 7,38 (д, J=7,5 Гц, 1Н), 7,04 (д, J=7,9 Гц, 1Н), 6,72 (с, 1Н), 3,94-3,79 (м, 1Н), 3,91 (д, J=11,6 Гц, 2Н), 3,65 (к, J=6,8 Гц, 2Н), 3,44 (т, J=11,0 Гц, 2Н), 3,00 (т, J=7,2 Гц, 2Н), 1,92 (д, J=11,8 Гц, 2Н), 1,52 (кд, J=11,2, 4,2 Гц, 2Н).
[00409] N-(3-(4-Метилпиридин-3-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-40) получают аналогичным образом, за исключением того, что 102 на стадии 2 заменяют 4-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином. 1Н ЯМР (400 МГц, ДМСО) δ 9,01 (с, 1Н), 8,90 (т, J=5,9 Гц, 1Н), 8,40 (д, J=4,9 Гц, 1Н), 8,36 (д, J=8,4 Гц, 1Н), 8,34 (с, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,42 (т, J=7,5 Гц, 1Н), 7,35-7,27 (м, 3H), 7,24 (д, J=7,5 Гц, 1Н), 7,02 (д, J=7,8 Гц, 1Н), 6,71 (с, 1Н), 3,94-3,80 (м, 1Н), 3,91 (д, J=11,6 Гц, 2Н), 3,63 (к, J=6,9 Гц, 2Н), 3,44 (т, J=11,4 Гц, 2Н), 2,98 (т, J=7,3 Гц, 2Н), 2,20 (с, 3H), 1,92 (д, J=12,9 Гц, 2Н), 1,52 (кд, J=11,1, 4,2 Гц, 2Н).
[00410] N-(3-(Пиразин-2-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-48) получают аналогичным образом, за исключением того, что 102 на стадии 2 заменяют 2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,24 (с, 1Н), 9,01 (с, 1Н), 8,96 (т, J=6,0 Гц, 1Н), 8,70 (с, 1Н), 8,60 (с, 1Н), 8,36 (д, J=8,4 Гц, 1Н), 8,06 (с, 1Н), 7,99 (д, J=7,7 Гц, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,48 (т, J=7,6 Гц, 1Н), 7,41 (д, J=7,5 Гц, 1Н), 7,02 (д, J=7,7 Гц, 1Н), 6,71 (с, 1Н), 3,94-3,79 (м, 1Н), 3,91 (д, J=11,5 Гц, 2Н), 3,64 (к, J=6,9 Гц, 2Н), 3,45 (т, J=11,4 Гц, 2Н), 3,01 (т, J=7,4 Гц, 2Н), 1,92 (д, J=12,9 Гц, 2Н), 1,52 (кд, J=11,2, 4,4 Гц, 2Н).
[00411] N-(2-(1-Метил-1H-пиразол-4-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-49) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-28. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,05-8,99 (м, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,4 Гц, 1Н), 8,06 (с, 1Н), 7,75 (д, J=8,3 Гц, 1Н), 7,71 (с, 1Н), 7,37-7,31 (м, 2Н), 7,27-7,21 (м, 2Н), 7,04 (д, J=7,8 Гц, 1Н), 6,75 (с, 1Н), 3,95-3,88 (м, 1Н), 3,94-3,80 (м, 1Н), 3,90 (с, 3H), 3,58-3,50 (м, 2Н), 3,46 (т, J=11,3 Гц, 2Н), 3,02-2,94 (м, 2Н), 1,93 (д, J=12,4 Гц, 2Н),1,53(кд, J=11,2, 4,1 Гц, 2Н).
[00412] N-(4-(1-Метил-1H-пиразол-4-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-37) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-29. 1H ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,87 (т, J=6,0 Гц, 1Н), 8,37 (д, J=8,3 Гц, 1Н), 8,07 (с, 1Н), 7,81 (с, 1Н), 7,73 (д, J=8,3 Гц, 1Н), 7,48 (д, J=8,0 Гц, 2Н), 7,24 (д, J=8,0 Гц, 2Н), 6,99 (д, J=7,8 Гц, 1Н), 6,73 (с, 1Н), 3,94-3,81 (м, 1Н), 3,90 (д, J=11,5 Гц, 2Н), 3,85 (с, 3H), 3,57 (к, J=7,0 Гц, 2Н), 3,45 (т, J=10,9 Гц, 2Н), 2,88 (т, J=7,4 Гц, 2Н), 1,92 (д, J=12,7 Гц, 2Н), 1,52 (кд, J=11,4, 4,2 Гц, 2Н).
[00413] N-(4-(4-Метилпиридин-3-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-38) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-29, и 1-метилпиразол-4-борной кислоты пинаколиновый эфир заменяют 4-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином. 1Н ЯМР (400 МГц, ДМСО) δ 9,01 (с, 1Н), 8,93 (т, J=5,8 Гц, 1Н), 8,41 (д, J=5,0 Гц, 1Н), 8,38 (д, J=8,4 Гц, 1Н), 8,36 (с, 1Н). 7,75 (д, J=8,3 Гц, 1Н), 7,39 (д, J=8,1 Гц, 2Н), 7,34 (д, J=8,1 Гц, 2Н), 7,32 (д, J=5,0 Гц, 1Н), 7,00 (д, J=7,7 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,80 (м, 1Н), 3,91 (д, J=11,7 Гц, 2Н), 3,63 (к, J=6,9 Гц, 2Н), 3,45 (т, J=11,0 Гц, 2Н), 2,97 (т, J=7,5 Гц, 2Н), 2,26 (с, 3H), 1,93 (д, J=12,5 Гц, 2Н), 1,53 (кд, J=11,4, 4,2 Гц, 2Н).
[00414] N-(4-(Пиразин-2-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-45) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-29, и 1-метилпиразол-4-борной кислоты пинаколиновый эфир заменяют 2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,24 (с, 1Н), 9,01 (с, 1Н), 8,95 (т, J=6,0 Гц, 1Н), 8,70 (с, 1Н), 8,59 (д, J=2,1 Гц, 1Н), 8,37 (д, J=8,4 Гц, 1Н), 8,09 (д, J=8,0 Гц, 2Н), 7,74 (д, J=8,3 Гц, 1Н), 7,44 (д, J=8,0 Гц, 2Н), 7,03 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,80 (м, 1Н), 3,90 (д, J=11,8 Гц, 2Н), 3,63 (к, J=6,8 Гц, 2Н), 3,44 (т, J=11,3 Гц, 2Н), 2,99 (т, J=7,3 Гц, 2Н), 1,92 (д, J=12,2 Гц, 2Н), 1,58-1,46 (м, 2Н).
[00415] N-(4-(Пиридин-4-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-46) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-29, и 1-метилпиразол-4-борной кислоты пинаколиновый эфир заменяют 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,95 (т, J=5,9 Гц, 1Н), 8,62 (д, J=5,0 Гц, 2Н), 8,37 (д, J=8,4 Гц, 1Н), 7,76 (д, J=8,5 Гц, 2Н), 7,74 (д, J=8 Гц, 1Н), 7,70 (д, J=5,0 Гц, 2Н), 7,42 (д, J=7,8 Гц, 2Н), 7,03 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,80 (м, 1Н), 3,90 (д, J=11,6 Гц, 2Н), 3,61 (к, J=6,8 Гц, 2Н), 3,44 (т, J=11,3 Гц, 2Н), 2,97 (т, J=7,4 Гц, 2Н), 1,92 (д, J=12,7 Гц, 2Н), 1,52 (кд, J=11,0, 4,2 Гц, 2Н).
[00416] N-(4-(Пиримидин-5-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-44) получают аналогичным образом, за исключением того, что I-35 на стадии 2 заменяют I-29, и 1-метилпиразол-4-борной кислоты пинаколиновый эфир заменяют 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиримидином. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,17 (с, 1Н), 9,14 (с, 2Н), 9,02 (с, 1Н), 8,95 (т, J=6,0 Гц, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,77 (д, J=7,9 Гц, 2Н), 7,74 (д, J=8,6 Гц, 1Н), 7,44 (д, J=7,9 Гц, 2Н), 7,04 (д, J=7,8 Гц, 1Н), 6,74 (с, 1Н), 3,94-3,79 (м, 1Н), 3,91 (д, J=11,9 Гц, 2Н), 3,62 (к, J=6,9 Гц, 2Н), 3,44 (т, J=11,3 Гц, 2Н), 2,98 (т, J=7,3 Гц, 2Н), 1,92 (д, J=12,4 Гц, 2Н), 1,52 (к, J=11,2, 4,2 Гц, 2Н).
[00417] N-(3-(1-Метил-1H-пиразол-4-ил)бензил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-43) получают аналогичным образом, за исключением того, что (2-бромфенил)метиламин используют на стадии 1 вместо 2-(3-бромфенил)этанамина. 1Н ЯМР (400 МГц, ДМСО) δ 9,35 (т, J=6,3 Гц, 1Н), 9,02 (с, 1Н), 8,39 (д, J=8,3 Гц, 1Н), 8,10 (с, 1Н), 7,82 (с, 1Н), 7,76 (д, J=8,3 Гц, 1Н), 7,54 (с, 1Н), 7,44 (д, J=7,6 Гц, 1Н), 7,31 (т, J=7,6 Гц, 1Н), 7,17 (д, J=7,6 Гц, 1Н), 7,03 (д, J=7,7 Гц, 1Н), 6,76 (с, 1Н), 4,54 (д, J=6,2 Гц, 2Н), 3,90 (д, J=11,5 Гц, 2Н), 3,85 (с, 4Н), 3,44 (т, J=11,2 Гц, 2Н), 1,92 (д. J=13,8 Гц, 2Н), 1,52 (кд, J=12,5, 4,4 Гц, 2Н).
[00418] N-(3-(4-Метилпиридин-3-ил)фенэтил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-50) получают аналогичным образом, за исключением того, что на стадии 2 используют 4-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-пиридин (CASRN 1171891-31-8) вместо 1-метилпиразол-4-борной кислоты пинаколинового эфира. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,01 (с, 1Н), 8,90 (т, J=5,9 Гц, 1Н), 8,40 (д, J=4,9 Гц, 1Н), 8,36 (д, J=8,4 Гц, 1Н), 8,34 (с, 1Н), 7,72 (д, J=8,3 Гц, 1Н), 7,42 (т, J=7,5 Гц, 1Н), 7,35-7,27 (м, 3H), 7,24 (д, J=7,5 Гц, 1Н), 7,02 (д, J=7,8 Гц, 1Н), 6,71 (с, 1Н), 3,94-3,80 (м, 1Н), 3,91 (д, J=11,6 Гц, 2Н), 3,63 (к, J=6,9 Гц, 2Н), 3,44 (т, J=11,4 Гц, 2Н), 2,98 (т, J=7,3 Гц, 2Н), 2,20 (с, 3H), 1,92 (д, J=12,9 Гц, 2Н), 1,52 (кд, J=11,1, 4,2 Гц, 2Н).
[00419] Пример 11
[00420] N-((4-Феноксипиридин-2-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-51)
[00421] Стадия 1: N-((4-Хлорпиридин-2-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (104) получают в соответствии с методикой из Примера 1, за исключением того, что 50с заменяют (5-бромпиридин-3-ил)метанамином. Продукт используют без дополнительной очистки.
[00422] Стадия 2: Смесь 104 (50 мг, 0,126 ммоль), фенола (17,8 мг, 0,189 ммоль), калия трет-бутоксида (43,6 мг, 0,377 ммоль) и НМП (0,25 мл) нагревают до 120°С, выдерживая при этой температуре в течение ночи. Охлажденную реакционную смесь разбавляют EtOAc (50 мл) и промывают водой (50 мл). Органическую фракцию отделяют, сушат (Na2SO4), фильтруют и упаривают под вакуумом с получением остатка, который очищают обращенно-фазовой ВЭЖХ с использованием смеси MeCN/H2O (содержащей 0,1% NH4OH) с градиентом (от 5 до 85%, 14 минут). Целевые фракции объединяют и упаривают под вакуумом с получением 17,6 мг (31%) I-51 в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,39 (т, J=6,0 Гц, 1Н), 9,03 (с, 1Н), 8,45-8,36 (м, 2Н), 7,73 (д, J=8,3 Гц, 1Н), 7,44 (т, J=7,7 Гц, 2Н), 7,24 (т, J=7,4 Гц, 1Н), 7,15 (д, J=8,1 Гц, 2Н), 7,05 (д, J=7,9 Гц, 1Н), 6,91 (с, 1Н), 6,77 (м, 2Н), 4,59 (д. J=6,0 Гц, 2Н), 3,91 (д, J=11,3 Гц, 3H). 3,46 (т, J=11,3 Гц, 2Н), 1,93(д, J=11,8 Гц, 2Н), 1,53 (м, 2Н).
[00423] 7-(Тетрагидро-2H-пиран-4-иламино)-N-((4-(о-толилокси)пиридин-2-ил)метил)-1,6-нафтиридин-2-карбоксамид (I-55) получают аналогичным образом, за исключением того, что на стадии 2 используют фенол вместо 2-метилфенола. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,38 (т, J=6,1 Гц, 1Н), 9,04 (с, 1Н), 8,42-8,36 (м, 2Н), 7,73 (д, J=8,2 Гц, 1Н), 7,32 (д, J=7,4 Гц, 1Н), 7,25 (т, J=7,7 Гц, 1Н), 7,16 (т, J=7,3 Гц, 1Н), 7,06 (дд, J=7,8, 3,4 Гц, 2Н), 6,81 (с, 1Н), 6,76 (с, 1Н), 6,66 (д, J=5,8 Гц, 1Н), 4,58 (д, J=6,0 Гц, 2Н), 3,91 (д, J=11,2 Гц, 3H), 3,46 (т, J=11,2 Гц, 2Н), 2,08 (с, 3H), 1,93 (д, J=12,6 Гц, 2Н), 1,53 (м, 2Н).
[00424] N-((4-(2-Хлорфенокси)пиридин-2-ил)метил)-7-(тетрагидро-2H-пиран-4-иламино)-1,6-нафтиридин-2-карбоксамид (I-56) получают аналогичным образом, за исключением того, что фенол на стадии 2 заменяют орто-хлорфенолом. 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,40 (с, 1Н), 9,03 (т, J=6,1 Гц, 1Н), 8,45-8,36 (м, 2Н), 7,73 (д, J=8,5 Гц, 1Н), 7,62 (д, J=8,1 Гц, 1Н), 7,48-7,38 (м, 1Н), 7,37-7,27 (м, 2Н), 7,05 (д, J=7,7 Гц, 1Н), 6,88 (с, 1Н), 6,76 (м, 1Н), 6,70 (с, 1Н), 4,60 (д, J=6,1 Гц, 2Н), 3,91 (д, J=11,6 Гц, 3H), 3,45 (т, J=11,0 Гц, 2Н), 1,93 (д, J=10,3 Гц, 2Н), 1,53 (м, 2Н).
[00425] 7-(Тетрагидро-пиран-4-иламино)-[1,6]нафтиридин-2-карбоновой кислоты 3-фенокси-бензиламид (I-57) получают аналогичным образом, за исключением того, что (5-бромпиридин-3-ил)метанамин на стадии 1 заменяют 3-фенокси-бензиламином, и стадию 2 пропускают. 1H ЯМР (400 МГц, ДМСО-d6) δ 9,41 (т, J=6,4 Гц, 1Н), 9,02 (с, 1Н), 8,38 (д, J=8,3 Гц, 1Н), 7,74 (д, J=8,3 Гц, 1Н), 7,40-7,30 (м, 3H), 7,15-6,96 (м, 6Н), 6,87 (д, J=8,1 Гц, 1Н), 6,74 (с, 1Н), 4,51 (д, J=6,3 Гц, 2Н), 3,90 (д, J=11,5 Гц, 2Н), 3,87-3,78 (м, 1Н), 3,44 (т, J=11,2 Гц, 2Н), 1,92 (д, J=12,8 Гц, 2Н), 1,52 (м, 2Н).
[00426] Пример 12
[00427] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(R)-1-(4-хлор-3-фтор-фенил)-3-гидрокси-пропил]-амид (II-57) и N-((1S)-1-(4-хлор-3-фторфенил)-2-гидроксипропил)-3-((S)-1-гидроксипропан-2-иламино)изохинолин-6-карбоксамид (II-60)
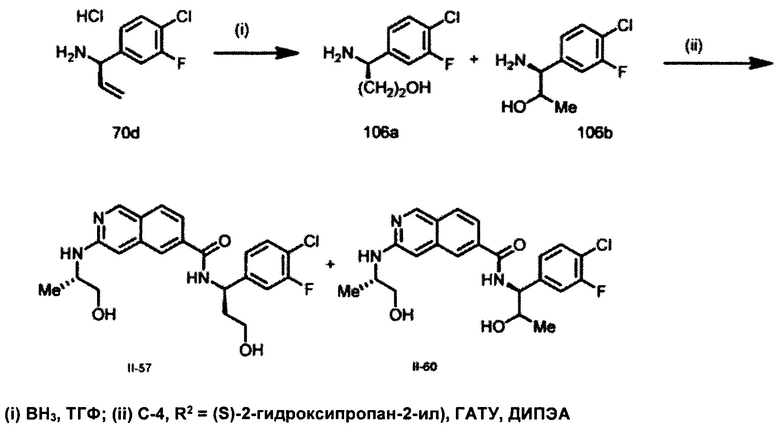
[00428] Стадия 1: К раствору 70d (50 мг, 0,27 ммоль) в ТГФ (1,0 мл) при -78°С добавляют ВН3⋅ТГФ (1 н, 1,0 мл). Далее смесь перемешивают при 0°С, выдерживая при этой температуре в течение 4 часов. Последовательно добавляют H2O2 (30%, 0,31 мл) и NaOH (2 н, 1,4 мл), и смесь дополнительно перемешивают в течение 1 часа. Смесь экстрагируют EtOAc, сушат и упаривают под вакуумом. Остаток очищают Combiflash (0,5% NH3 в смеси НСО3/CH3CN) с получением 25 мг (45%) смеси (R)-3-амино-3-(4-хлор-3-фторфенил)пропан-1-ола (106а) и (1S)-1-амино-1-(4-хлор-3-фторфенил)пропан-2-ола (106b): ЖХМС (ионизация электрораспылением): соотношение массы и заряда 204 [М+Н]+.
[00429] Стадия 2: К раствору смеси 106а и 106b, С-5 (R2=(S)-1-гидроксипропан-2-иламино) (60 мг, 0,25 ммоль), ГАТУ (93,6 мг, 0,25 ммоль) в ДМФА (2,0 мл) добавляют ТЭА (1,0 мл). Смесь перемешивают при комнатной температуре в течение 3 часов. Смесь разбавляют EtOAc (100 мл), промывают водой (3×20 мл), сушат (Na2SO4) и упаривают под вакуумом. Остаток очищают препаративной ВЭЖХ с получением 15 мг (14%) II-57 и 5 мг (4,6%) II-60.
[00430] N-((R)-1-(4-Хлор-3-фторфенил)-3-гидроксипропил)-3-((S)-1-гидроксипропан-2-иламино)изохинолин-6-карбоксамид (II-57): 1Н ЯМР (500 МГц, МеОН-d4) δ 8,86 (с, 1Н), 8,03 (с, 1Н), 7,86 (д, J=9,0 Гц, 1Н), 7,54 (дд, J=8,5, 1,5 Гц, 1Н), 7,47 (м, 1Н), 7,34 (дд, J=10,5, 2,5 Гц, 1Н), 7,26 (дд, J=8,5, 1,5 Гц, 1Н), 6,80 (с, 1Н), 5,31 (м, 1Н), 3,92 (м, 1Н), 3,96-3,59 (м, 4Н), 2,15-2,10 (м, 2Н), 1,29 (д, J=7,0 Гц, 3H); ЖХМС (ионизация электрораспылением): соотношение массы и заряда 432 [М+Н]+.
[00431] N-((1S)-1-(4-Хлор-3-фторфенил)-2-гидроксипропил)-3-((S)-1-гидроксипропан-2-иламино)изохинолин-6-карбоксамид (II-60): 1Н ЯМР (500 МГц, МеОН-d4) δ 8,74 (с, 1Н), 7,91 (с, 1Н), 7,76 (д, J=8,5 Гц, 1Н), 7,41 (м, 1Н), 7,34 (т, J=7,5 Гц, 1Н), 7,28 (дд, J=10, 1,5 Гц, 1Н), 7,17 (д, J=1,5 Гц, 1Н), 6,69 (с, 1Н), 4,87 (д, J=7,0 Гц, 1Н), 4,05 (м, 1Н), 3,80 (м, 1Н), 3,55-3,49 (м, 2Н), 1,20-1,14 (м, 6Н); ЖХМС (ионизация электрораспылением): соотношение массы и заряда 432 [М+Н]+.
[00432] Пример 13
[00433] 3-((S)-2-Гидрокси-1-метил-этиламино)-изохинолин-6-карбоновой кислоты [(S)-1-(4-дифторметокси-фенил)-2-гидрокси-этил]-амид (II-61)
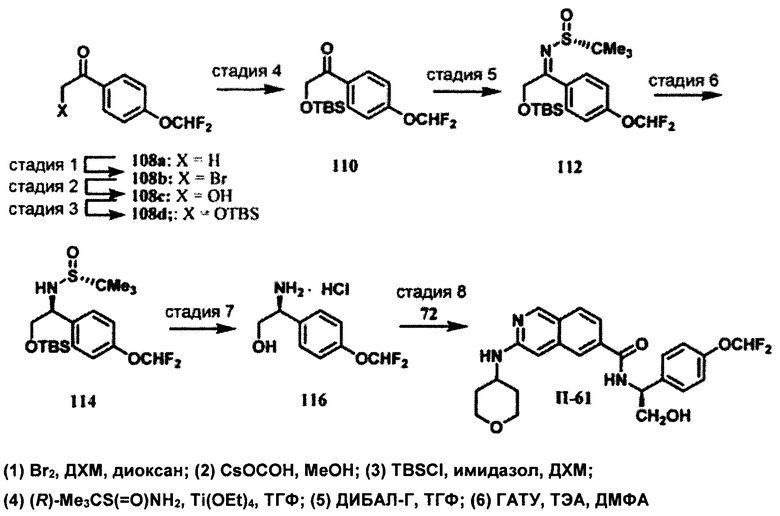
[00434] Стадия 1: К раствору 108а (1,0 г, 5,4 ммоль) в смеси диоксана (5 мл) и эфира (3 мл) при перемешивании по каплям добавляют бром (1,1 г, 7,0 ммоль) на протяжении 30 минут. После перемешивания при комнатной температуре еще в течение 30 минут, смесь выливают в воду. Органическую фракцию отделяют, промывают водой и сушат (Na2SO4). Растворитель выпаривают под вакуумом, и остаток перекристаллизуют из гексана с получением 1,2 г (выход 85%) 108b.
[00435] Стадия 2: Смесь 108b (1,8 г, 6,8 ммоль) и CsOCHO (3,6 г, 20 ммоль) в МеОН (10 мл) перемешивают при 80°С в течение 1 часа. Твердое вещество отфильтровывают, и фильтрат упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (1:3), с получением 0,90 г (65%) 108 с. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 203,1 [М+Н]+.
[00436] Стадия 3: К раствору 108с (850 мг, 4,20 ммоль) и имидазола (428 мг, 6,30 ммоль) в сухом ДХМ (10 мл) при 0°С добавляют по каплям раствор TBSCl (953 мг, 6,30 ммоль) в сухом ДХМ (4,0 мл). Смесь перемешивают при комнатной температуре в течение 4 часов. Реакционную смесь промывают насыщенным раствором Na2CO3, сушат (Na2SO4), фильтруют и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (100:6), с получением 850 мг (62%) 108d. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 317,3 [М+Н]+.
[00437] Стадия 4: Раствор 108d (1,6 г, 5,1 ммоль), Ti(OEt)4 (5,8 г, 20 ммоль) и (R)-2-метилпропан-2-сульфинамида (1,20 г, 10,2 ммоль) в сухом ТГФ (10 мл) перемешивают при 80°С в течение 4 часов. После удаления растворителя остаток разбавляют EtOAc, промывают раствором соли, сушат и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/этилацетата (100:15), с получением 0,80 г (42%) 110. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 420,2 [М+Н]+.
[00438] Стадия 5: К раствору 110 (100 мг, 0,240 ммоль) в сухом ТГФ (5,0 мл) при -78°С добавляют по каплям раствор ДИБАЛ-Г (0,60 мл, 0,60 ммоль) в сухом гексане. Смесь перемешивают при -78°С еще в течение 1 часа. МеОН добавляют по каплям при -78°С для гашения реакции. Смесь нагревают до комнатной температуры, фильтруют, сушат (Na2SO4), фильтруют и упаривают с получением 32 мг (32%) 112 в виде масла практически желтого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 422,2 [М+Н]+.
[00439] Стадия 6: Раствор 112 (100 мг, 0,24 ммоль) в 1 н HCl в метаноле (5,0 мл) перемешивают при комнатной температуре в течение 1 часа. После упаривания остаток разбавляют EtOAc (10 мл). Полученное твердое вещество отделяют с получением 40 мг (81%) 114. 1H ЯМР (500 МГц, ДМСО-d6) δ 7,40 (д, J=8,5 Гц, 2Н), 7,18 (т, J=74,5 Гц, 1Н), 7,10 (д, J=8,5 Гц, 2Н), 4,78 (шс, 1Н), 3,86 (м, 1Н), 3,42 (шс, 1Н), 3,33-3,25 (м, 2 Н), 2,04 (шс, 2Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 204,1 [М+Н]+.
[00440] Стадия 7: Смесь 72 (55 мг, 0,20 ммоль), 114 (40 мг, 0,20 ммоль), ГАТУ (76 мг, 0,20 ммоль) и ДИПЭА (0,50 мл) в ДМФА (1,5 мл) перемешивают при комнатной температуре в течение 3 часов. После разбавления EtOAc (100 мл) полученную смесь промывают водой (3×20 мл) и сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают препаративной ВЭЖХ с получением 3,5 мг (4%) II-61 в виде твердого вещества желтого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,91 (с, 1Н), 8,85 (д, J=8,5 Гц,1Н), 8,10 (с, 1Н), 7,84 (д, J=9,0 Гц, 1Н), 7,53 (м, 1Н), 7,46 (д, J=8,5 Гц, 2Н), 7,20 (т, J=74,0 Гц, 1Н), 7,15-7,12 (м, 2Н), 6,73 (с, 1Н), 6,57 (д. J=7,5 Гц, 1Н), 5,08 (м, 1Н), 4,99 (м, 1Н), 3,91-3,82 (м, 3H), 3,75-3,63 (м, 2Н), 3,46-3,42 (м, 2Н), 1,91 (д, J=13,5 Гц, 2Н), 1,53-1,45 (м, 2Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 458,3 [М+Н]+.
[00441] Пример 14
[00442] 3-(Тетрагидро-пиран-4-иламино)-изохинолин-6-карбоновой кислоты [(4-хлор-3-фтор-фенил)-(3-фтор-пирролидин-3-ил)-метил]-амид (II-65)

[00443] Стадия 1: терет-Бутил-3-(4-хлор-3-фторбензоил)-3-фторпирролидин-1-карбоксилат: К раствору 4-бром-1-хлор-2-фторбензола (12 г, 58 ммоль) в ТГФ (100 мл) добавляют магний (1,4 г, 58 ммоль). Смесь дегазируют азотом, и добавляют небольшое количество 1,2-дибромэтана. Реакционную смесь перемешивают в течение 1 часа, и раствор wpew-бутил-3-фтор-3-(метокси(метил)карбамоил)пирролидин-1-карбоксилата (8,0 г, 29 ммоль) в ТГФ (50 мл) добавляют к вышеописанной смеси при -78°С. Через 10 минут реакционной смеси дают нагреться до 0°С и перемешивают в течение 3 часов. Реакцию гасят NH4Cl, и полученную смесь экстрагируют EtOAc (3×100 мл). Объединенные органические фракции промывают раствором соли, сушат (Na2SO4), фильтруют и упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc с градиентом (от 20:1 до 8:1), с получением 8,8 г (88%) 118b. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 290 [М+Н-56]+.
[00444] Стадия 2: Смесь 118b (6,30 г, 18,3 ммоль), (S)-2-метилпропан-2-сульфинамида (3,31 г 27,4 ммоль) и Ti(OEt)4 (11 мл 46 ммоль) в ТГФ (100 мл) нагревают до 65°С, выдерживая при этой температуре в течение 12 часов. После охлаждения смесь выливают в воду. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc (3×100 мл). Органическую фракцию промывают водой (50 мл×3), сушат (Na2SO4), фильтруют и упаривают под вакуумом. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (5:1), с получением 5,6 г (68%) 120 в виде бесцветного масла.
[00445] Стадия 3: К раствору 120 (5,60 г, 12,5 ммоль) в сухом ТГФ (100 мл) при -65°С добавляют ДИБАЛ-Г (37,5 мл, 37,5 ммоль). После перемешивания в течение 1 часа при -65°С реакцию гасят водой (2,0 мл). Нерастворимый материал отфильтровывают, и фильтрат упаривают. Остаток очищают хроматографией на SiO2, элюируя смесью петролейного эфира/EtOAc (2:1), с получением 240 мг (4,3%) 124 (абсолютная конфигурация присвоена произвольно), 400 мг (7,1%) другого изомера и 1,8 г (32%) смеси двух изомеров. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 395,1 [М+Н-56]+.
[00446] Стадия 4: К раствору 124 (240 мг, 0,50 ммоль) в EtOAc (3,0 мл) при комнатной температуре добавляют 4 М HCl в метаноле (0,4 мл). После перемешивания в течение 30 минут твердое вещество отделяют фильтрацией с получением 130 мг (76%) 124 в виде твердого вещества белого цвета. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 291,1[M+H-56]+.
[00447] Стадия 5: Смесь 124 (70 мг, 0,20 ммоль), ГАТУ (152 мг, 0,400 ммоль), 72 (50 мг, 0,20 ммоль) и ТЭА (80 мг, 0,80 ммоль) в ДМФА (2,0 мл) перемешивают при комнатной температуре в течение 1 часа. Полученную смесь разбавляют EtOAc (2×20 мл), промывают раствором соли, сушат и упаривают с получением 120 мг (100%) 126а в виде желтого масла, которое использовали на следующей стадии без дополнительной очистки. ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 601,4 [М+Н]+.
[00448] Стадия 6: Раствор 126а (120 мг, 0,200 ммоль) в 4 М HCl в метаноле (2,0 мл) перемешивают в течение 30 минут при комнатной температуре. рН полученной смеси доводят приблизительно до 10 с помощью насыщ. NaHCO3, экстрагируют EtOAc (2×10 мл), промывают раствором соли, сушат и упаривают под вакуумом. Остаток очищают препаративной ВЭЖХ (0,5% NH4HCO3/MeCN) с получением 8,0 мг (8,0%) II-65 в виде твердого вещества желтого цвета. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,20 (д, J=9,0 Гц, 1Н), 8,91 (с, 1Н), 8,08 (с, 1Н), 7,84 (д, J=8,0 Гц, 1Н), 7,71 (д, J=11,0 Гц, 1Н), 7,58 (м, 1Н), 7,49-7,44 (м, 2Н), 6,75 (с, 1Н), 6,57 (д, J=7,5 Гц, 1Н), 5,50 (м, 1Н), 3,91-3,89 (м, 3H), 3,47-3,42 (м, 3H), 2,99-2,86 (м, 3H), 2,02-1,91 (м, 4Н), 1,59 (д, J=11,0 Гц, 2Н); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 501,2 [М+Н]+.
[00449] Другой диастереомер представлял собой II-66 и также может быть выделен. 1Н ЯМР (500 МГц, ДМСО-d6) δ 9,20 (д, J=9,0 Гц, 1Н), 8,91 (с, 1Н), 8,10 (с, 1Н), 7,86-7,83 (м, 1Н), 7,73 (д, J=10,5 Гц, 1Н), 7,61-7,58 (м, 1Н), 7,48-7,46 (м, 2Н), 6,76 (д, J=10,0 Гц, 1Н), 6,57 (д, J=8,0 Гц, 1Н), 5,53-5,45 (м, 1Н), 3,91-3,82 (м, 3H), 3,47-3,42 (м, 3H), 3,00-2,90 (м, 4Н), 1,93-1,91 (м, 3H), 1,53-1,46 (м, 3H); ЖХМС (ионизация электрораспылением) соотношение массы и заряда: 501,2 [М+Н]+.
[00450] Пример 15
[00451] N-((3S,4R)-1-Бензил-4-(4-метоксифенил)пирролидин-3-ил)-3-((1-метил-1H-пиразол-5-ил)амино)изохинолин-6-карбоксамид (II-62)
[00452] Во флакон для обработки микроволнами вместимостью 2-5 мл, оборудованный мешалкой, помещают 92 (94 мг, 0,3506 ммоль, 1,1 экв.), (3S,4R)-1-бензил-4-(4-метоксифенил)пирролидин-3-амин (90 мг, 0,3187 ммоль, 1,0 ммоль, CASRN 114616-86-5), ДМФА (2,0 мл) и ГАТУ (187,4 мг, 0,4780 ммоль, 1,5 экв.). Реакционную смесь перемешивают в течение 20 минут при комнатной температуре и обрабатывают ТЭА (0,1347 мл, 0,956 ммоль, 3,0 экв.). Флакон для обработки микроволнами закупоривают, и реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Диметилформамидный раствор распределяют между EtOAc и водой (120 мл/40 мл). Фракцию EtOAc дважды промывают раствором соли, сушат, фильтруют и упаривают с получением неочищенного масла. Порцию неочищенного продукта (20%) очищают обращенно-фазовой ВЭЖХ с получением 3,5 мг N-((3S,4R)-1-бензил-4-(4-метоксифенил)пирролидин-3-ил)-3-((1-метил-1H-пиразол-5-ил)амино)изохинолин-6-карбоксамида (чистота=100%, 254 нм). Остаток неочищенного продукта (80%) очищают на колонке SiO2 (ISCO), элюируя смесью метанола/ДХМ с градиентом (от 2 до 8% МеОН), с получением еще 48 мг (всего: 51,5 мг, 30%). 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,05 (с, 1Н), 8,87(с, 1Н), 8,80 (д, J=7,5 Гц, 1Н), 8,16 (с, 1Н), 7,96 (д, J=8,6 Гц, 1Н), 7,64 (д, J=8,4 Гц, 1Н), 7,42 (с, 1Н), 7,34 (к, J=7,7 Гц, 4Н), 7,26 (д, J=8,1 Гц, 3H), 6,92 (с, 1Н), 6,86 (д, J=8,4, 2Н), 6,23 (с, 1Н), 4,49-4,43 (м, 1Н), 3,76 (с, 3H), 3,70 (с, 3H), 3,62 (д, J=10,4 Гц, 1Н), 3,43 (к, J=7,5 Гц, 1Н), 3,04 (м, 2Н), 2,60 (м, 2Н). ЖХМС М+Н+=534.
[00453] Пример 16
[00454] N-((3S,4R)-1-Бензил-4-(4-метоксифенил)пирролидин-3-ил)-3-((1,3-диметил-1H-пиразол-5-ил)амино)изохинолин-6-карбоксамид (II-63) и 3-((1,3-диметил-1H-пиразол-5-ил)амино)-N-((3S,4R)-4-(4-метоксифенил)-1-метилпирролидин-3-ил)изохинолин-6-карбоксамид (II-64)
[00455] N-((3S,4R)-1-Бензил-4-(4-метоксифенил)пирролидин-3-ил)-3-((1,3-диметил-1H-пиразол-5-ил)амино)изохинолин-6-карбоксамид получают из 3-(1,3-диметил-1H-пиразол-5-иламино)изохинолин-6-карбоновой кислоты (99 мг, 0,3506 ммоль, 1,1 экв.) путем опосредованного ГАТУ сочетания с (3S,4R)-1-бензил-4-(4-метоксифенил)пирролидин-3-амином (90 мг, 0,3187 ммоль, 1,0 экв.) в качестве амина. Методики синтеза и очистки такие же, как применяются для получения N-((3S,4R)-1-бензил-4-(4-метоксифенил)пирролидин-3-ил)-3-((1-метил-1H-пиразол-5-ил)амино)изохинолин-6-карбоксамида. Часть неочищенного продукта (~30% материала) очищают препаративной обращенно-фазовой ВЭЖХ с получением 9,4 мг II-63 (чистота=100%, УФ 254 нм). Остаток неочищенного продукта используют без дополнительной очистки в реакции гидрогенизации для удаления N-бензила. 1H ЯМР (400 МГц, ДМСО) δ 9,04 (с, 1Н), 8,81 (с, 1Н), 8,79 (м, 1Н), 8,17 (с,1Н), 7,96 (д, J=8,6 Гц, 1Н), 7,64 (д, J=8,6 Гц, 1Н), 7,34 (к, J=8,0 Гц, 4Н), 7,26 (д, J=8,2 Гц, 3H), 6,92 (с, 1Н), 6,86 (д, J=8,4, 2Н), 6,03 (с, 1Н), 4,52-4,41 (м, 1Н), 3,70 (с, 3H), 3,70 (т, J=7,3 Гц, 1Н), 3,62 (д, J=10,4 Гц, 1Н), 3,60 (с, 3H), 3,43 (к, J=7,3 Гц, 1Н), 3,03 (м, 2Н), 2,57 (м, 2Н), 2,15 (с, 3H). ЖХМС M+H+=547,3.
[00456] Суспензию II-63 (48 мг, 0,0878 ммоль), 10% Pd/C (56 мг, 6,0 экв.) и МеОН (4 мл) трижды дегазируют и перемешивают в течение 24 часов в атмосфере водорода (баллон) с давлением 1 атм. N-бензильную группу отщепляют с получением TV-метилированного продукта. Реакционную смесь фильтруют сквозь слой Celite®, и слой Celite® промывают метанолом. Метанол выпаривают, и остаток очищают препаративной обращенно-фазовой ВЭЖХ с получением 2,4 мг (5,8%) II-64 (чистота=98% УФ на длине волны 254 нм). 1Н ЯМР (400 МГц, ДМСО) δ 9,05 (с, 1Н), 8,81 (с, 1Н), 8,79 (м, 1Н), 8,21 (д, J=18,7 Гц, 1Н), 7,96 (д, J=8,6 Гц, 1Н), 7,66 (д, J=8,5 Гц, 1Н), 7,25 (д, J=8,4 Гц, 2Н), 6,93 (с, 1Н), 6,86 (д, J=8,4, 2Н), 6,03 (с, 1Н), 4,49-4,42 (м, 1Н), 3,71 (с, 3H), 3,60 (с, 3H), 3,41 (к, J=7,3 Гц, 1Н), 3,02 (т, J=8,5 Гц, 2Н), 2,93 (т, J=8.5 Гц, 2Н), 2,60 (м, 1Н), 2,31 (с, 3H), 2,15 (с, 3H). ЖХМС М+Н+=471,2.
[00457] Пример 17
[00458] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-7-((тетрагидро-2H-пиран-4-ил)амино)-1,6-нафтиридин-2-карбоксамид (I-60)
[00459] Стадия 1: Раствор 1-метил-1H-имидазол-5-карбальдегида (1,46 г, 13,26 ммоль), (R)-2-метилпропан-2-сульфинамида (2,893 г, 23,87 ммоль) и тетраэтоксититана (10,89 г, 47,73 ммоль) в ТГФ (100 мл) нагревают до 65°С, выдерживая при этой температуре в течение 12 часов. Реакционную смесь охлаждают и выливают в воду. Твердое вещество отфильтровывают, и фильтрат экстрагируют EtOAc. Фракции разделяют, и органическую фракцию упаривают. Полученный остаток очищают на SiO2, элюируя смесью ДХМ/МеОН с градиентом (от 1,5 до 2% МеОН), с получением 1,444 г (51,1%) (R,E)-2-метил-N-((1-метил-1H-имидазол-5-ил)метилен)пропан-2-сульфинамида (128).
[00460] Стадия 2: Раствор 128 (1,444 г, 6,770 ммоль) и ТГФ (20 мл) охлаждают до -10°С, и добавляют (3-фтор-4-метоксифенил)магния бромид (2,717 г, 11,85 ммоль) с помощью воронки. Реакционную смесь перемешивают при -10°С, выдерживая при этой температуре в течение 1 часа. Добавляют воду, и смесь экстрагируют EtOAc. Органическую фракцию упаривают, и полученный остаток очищают обращенно-фазовой хроматографией (элюация смесью 0-65% MeCN/воды) с получением 0,203 г (8,83%) (R)-N-((R)-(3-фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-2-метилпропан-2-сульфинамида (130а) и 315 мг (13,71%) (R)-N-((S)-(3-фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-2-метилпропан-2-сульфинамида (130b).
[004611 Стадия 3: К раствору 130b (160 мг, 0,471 ммоль) в ДХМ (15 мл) добавляют 4 н HCl в диоксане (3 мл), и реакционную смесь перемешивают в течение 15 минут. К смеси добавляют эфир, и твердые вещества отфильтровывают с получением 106 мг (82,8%) (S)-(3-фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метанамина гидрохлорида (132).
[00462] Стадия 4: К раствору 132 (49,7 мг, 0,183 ммоль) и ДИПЭА (31,9 мкл, 0,183 ммоль) в ДМФА (5 мл) добавляют 72 (50 мг, 0,183 ммоль) и ГБТУ (76,3 мг, 0,201 ммоль), и реакционную смесь перемешивают при комнатной температуре в течение 18 часов. Реакционную смесь выливают в воду и экстрагируют EtOAc. Органическую фракцию упаривают, и полученный остаток очищают обращенно-фазовой хроматографией (SP4, элюация с градиентом 0-50% MeCN в H2O) с получением 62,1 мг (69,2%) I-61. 1Н ЯМР (400 МГц. CDCl3) δ 8,90 (с, 1Н), 8,79 (д, 1Н), 8,20 (д, 1Н), 7,98 (д, 1Н), 7,51 (с, 1Н), 7,16 (м, 2Н), 6,97 (м, 2Н), 6,81 (с, 1Н), 6,73 (с, 1Н), 6,43 (д, 2Н), 4,45 (д, 2Н), 4,06 (м, 2Н), 3,90 (с, 3H), 3,77 (м, 1Н), 3,62 (м, 2Н), 3,59 (с, 3H), 2,15 (м, 2Н), 1,65 (м, 2Н); соотношение массы и заряда (химическая ионизация при атмосферном давлении с положительным зарядом) М+1=491,1.
[00463] (R)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-7-((тетрагидро-2H-пиран-4-ил)амино)-1,6-нафтиридин-2-карбоксамид (I-59) получают аналогичным образом, за исключением того, что на стадии 3 130b заменяют (R)-N-((R)-(3-фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-2-метилпропан-2-сульфинамидом (130а), что в конечном счете дает 69 мг (77%) I-59 после сочетания с 72. 1Н ЯМР (400 МГц, CDCl3) δ 8,90 (с, 1Н), 8,79 (д, 1Н), 8,20 (д, 1Н), 7,98 (д, 1Н), 7,51 (с, 1Н), 7,16 (м, 2Н), 6,97 (м, 2Н), 6,81 (с, 1Н), 6,73 (с, 1Н), 6,43 (д, 2Н), 4,45 (д, 2Н), 4,06 (м, 2Н), 3,90 (с, 3H), 3,77 (м, 1Н), 3,62 (м, 2Н), 3,59 (с, 3H), 2,15 (м, 2Н), 1,65 (м, 2Н); соотношение массы и заряда (химическая ионизация при атмосферном давлении с положительным зарядом) М+1=491,1.
[00464] (S)-N-((3-Фтор-4-метоксифенил)(1-метил-1H-имидазол-5-ил)метил)-7-((1-метил-1H-пиразол-5-ил)амино)-1,6-нафтиридин-2-карбоксамид (I-58) получают аналогичным образом, за исключением того, что 72 на стадии 4 заменяют 80. 1Н ЯМР (400 МГц, CDCl3) δ 9,03 (с, 1Н), 8,61 (м, 1Н), 8,31 (д, 1Н), 8,12 (д, 1Н), 7,59 (м, 1Н), 7,48 (с, 1Н), 7,13 (м, 2Н), 6,96 (м, 1Н), 6,87 (с, 1Н), 6,80 (с, 1Н), 6,43 (м, 2Н), 6,29 (м, 1Н), 3,89 (с, 3H), 3,82 (с, 3H), 3,56 (с, 3H); соотношение массы и заряда (химическая ионизация при атмосферном давлении с положительным зарядом) М+1=487,2.
[00465] Биологический пример 1
[00466] Ферментная активность ERK-2
[00467] Соединения тестируют в ферментном анализе с использованием ERK-2 человека (митоген-активируемая киназа 1), рекомбинантно экспрессируемой в Е. coli как n-концевой 6-His гибридный белок и соответствующей аминокислотам (ак) 8-360. Используемый субстрат представляет собой флуоресцентный Омниа пептид S/T17 (Invitrogen, Карлсбад, Калифорния; кат. №KNZ1171C). Исследуемые соединения разбавляют в ДМСО, готовя 3-кратные серийные разведения в конечной концентрации 100х. Кроме соединения, анализ включает 50 мМ 4-(2-гидроксиэтил)-1-пиперазин этансульфоновой кислоты (ГЭПЭС) [рН 7,3], 10 мМ MgCl2, 2 мМ дитиотрейтола (ДТТ), 0,005% Тритона-Х100, 5 нМ фермента ERK-2, 6,25 мкМ пептидного субстрата S/T17 и 25 мкМ АТФ (в соответствии с наблюдаемой Km) до общего объема реакционной смеси 25 мкл. Анализ проводят при комнатной температуре в 384-лун очном белом полипропиленовом планшете (Nunc, Inc, Нейпервилл, Иллинойс; кат. №267462), собирая данные каждые 50секунд в течение приблизительно 30 минут на устройстве для считывания планшетов Envision (PerkinElmer, Inc., Уолтхэм, Массачусетс); возбуждение 340 нм/эмиссия 495 нм. Данные, собранные из каждой лунки, аппроксимируют к прямой, и полученную скорость используют для вычисления процента от контроля. Процент от контроля наносят на график против концентрации соединения, и значения IC50 определяют с использованием четырехпараметрической аппроксимации. Табл. 3 содержит характерные данные соединений, раскрытых в настоящем документе. Репрезентативные данные представлены в Табл. 3 (ниже).
[00468] Биологический пример 2
[00469] Клеточный анализ фосфорилирования P90RSK(Ser380)
[00470] Ингибирование стимулированного ФМА фосфорилирования P90RSK(Ser380) определяют с помощью следующего механистического клеточного анализа in vitro, который включает инкубацию клеток с соединением в течение 1,5 часов, количественное определение флуоресцентного сигнала pP90RSK(Ser380) на фиксированных клетках и нормализацию к сигналу глицеральдегид-3-фосфатдегидрогеназы (ГАФДГ).
[00471] Материалы и методы: Культура клеток HepG2 получена из Американской коллекции типовых культур (АКТК) и наращивалась в модифицированной Дульбекко среде Игла с добавлением 10% фетальной бычьей сыворотки. Клетки помещают на 96-луночные планшеты с плотностью 35000 клеток/лунку и дают прикрепиться в течение ночи при 37°С/5% CO2. После этого добавляют разбавленные соединения в конечной концентрации 0,5% в ДМСО. Через 1,5 часа инкубации с соединением клетки стимулируют добавлением ФМА (форбол-12-миристат-13-ацетат) в конечной концентрации 100 нг/мл; стимуляция ФМА осуществляется в форме 30-минутной инкубации при 37°С/5% CO2. После 30-минутной стимуляции ФМА, клетки промывают фосфатно-солевым буфером (ФСБ) и фиксируют 3,7% формальдегидом в ФСБ при комнатной температуре в течение 15-20 минут. Затем еще раз промывают ФСБ, и далее осуществляют пермеабилизацию в 100% МеОН при комнатной температуре в течение 10-15 минут. После пермеабилизационной инкубации клетки промывают ФСБ/0,05% Твина-20, с последующим блокированием в блокирующем буфере Odyssey (LI-COR Biosciences) по меньшей мере в течение 1 часа. Антитела к фосфорилированному P90RSK(Ser380) (Cell Signaling #9335, кроличье моноклональное) и ГАФДГ (Fitzgerald 10R-G109a, мышиное моноклональное) добавляют к клеткам и инкубируют в течение ночи при 4°С. Антитело pP90RSK(Ser380) используют в разведении 1:250; ГАФДГ используют в разведении 1:10000. После промывания ФСБ/0,05% Твина-20, клетки инкубируют с флуоресцентно мечеными вторичными антителами (антикроличье - Alexa Flour680, Invitrogen кат. №А21109; анти-мышиное - IRDye800CW, Rockland Inc., кат. №610-131-121) в течение 1 часа. Оба вторичных антитела используют в разведении 1:1000. Затем клетки промывают и анализируют на предмет флуоресценции на обеих длинах волн с использованием Odyssey Infrared Imaging System (LI-COR Biosciences). Сигнал фосфорилированного P90RSK(Ser380) нормализуют к сигналу ГАФДГ. Характерные данные приведены в Табл. III (ниже).
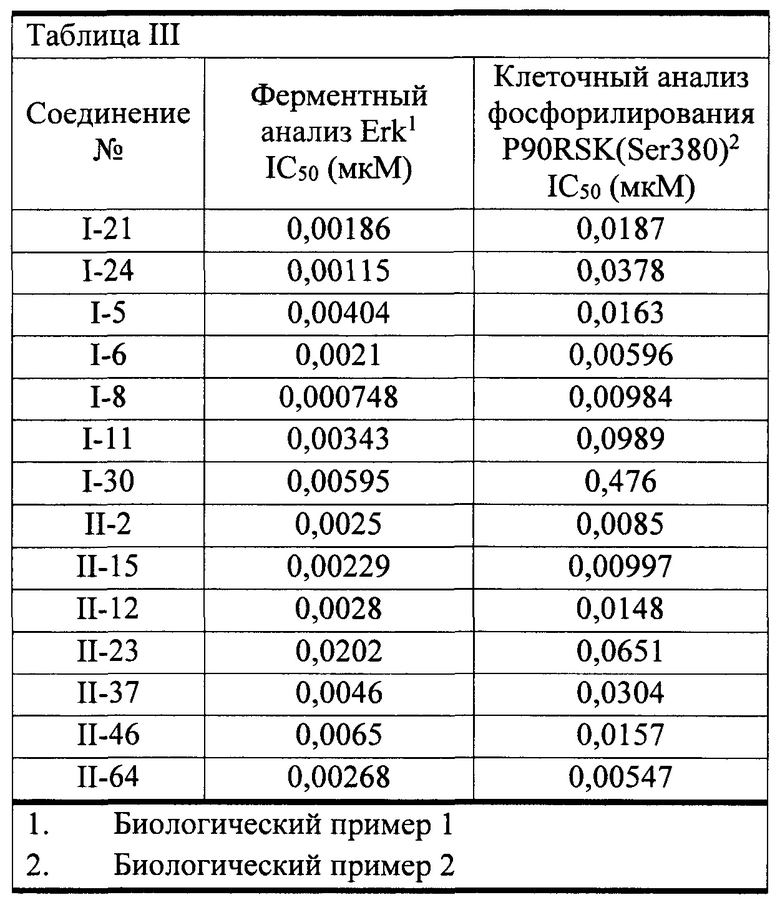
[00472] Пример препарата 21
[00473] Фармацевтические композиции исследуемых соединений для введения различными путями получают, как описано в настоящем Примере.
[00474] Композиция для перорального введения (А)

[00475] Ингредиенты смешивают и наполняют смесью капсулы, каждая из которых содержит приблизительно 100 мг.
[00476] Композиция для перорального введения (В)

[00477] Ингредиенты объединяют и гранулируют с использованием растворителя, такого как метанол. Далее препарат сушат и получают таблетки (содержащие приблизительно 20 мг активного соединения) с помощью подходящей таблетирующей машины.
[00478] Композиция для перорального введения (С)
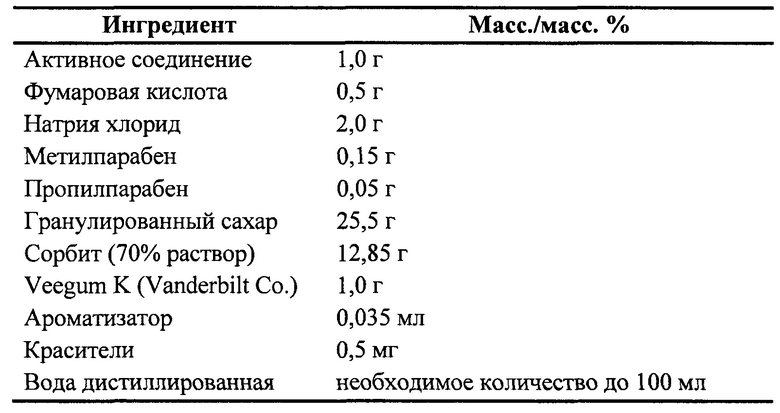
[00479] Ингредиенты смешивают для получения суспензии для перорального введения.
[00480] Препарат для парентерального введения (D)

[00481] Активный ингредиент растворяют в части воды для инъекций. Затем достаточное количество натрия хлорида добавляют при перемешивании, чтобы получить изотонический раствор. Доводят до необходимой массы оставшейся водой для инъекций, фильтруют сквозь мембранный фильтр с размером пор 0,2 мкм и фасуют в стерильных условиях.
[00482] Суппозиторный препарат (Е)

[00483] Ингредиенты плавят совместно, смешивают на паровой 10 бане и выливают в формы для получения общей массы 2,5 г.
[00484] Препарат для локального нанесения (F)
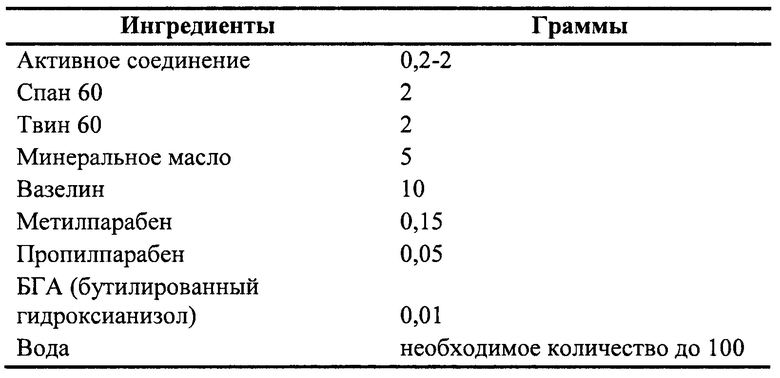
[00485] Все ингредиенты, за исключением воды, объединяют и нагревают приблизительно до 60°С при перемешивании. Затем добавляют достаточное количество воды приблизительно при 60°С, с энергичным перемешиванием для эмульгации ингредиентов, после чего добавляют необходимое количество воды приблизительно до 100 г.
[00486] Признаки, раскрытые в приведенном выше описании или последующей Формуле изобретения, выражены в конкретных формулах или в терминах значений для выполнения раскрытой функции или метода или способа для достижения раскрытого результата, сообразно обстоятельствам, и могут, по отдельности или в любой комбинации таких признаков, быть использованы для практики изобретения в его различных формах.
[00487] Раскрытое выше изобретение описано до некоторой степени подробности путем иллюстрации и примера, с целью прозрачности и понимания. Для специалиста в данной области техники будет очевидным, что изменения и модификации можно практиковать в объеме прилагаемой Формулы изобретения. Таким образом, необходимо понимать, что приведенное выше описание предназначено для иллюстрации и не является ограничивающим. Объем изобретения, таким образом, должен определяться не со ссылкой на приведенное выше описание, но, вместо этого, он должен определяться со ссылкой на прилагаемую Формулу изобретения, вместе с полным объемом эквивалентов, к которым применима Формула изобретения.
[00488] Патенты, опубликованные заявки и научная литература, процитированные в настоящем документе, определяют объем знаний специалистов в данной области техники и включены в настоящий документ посредством ссылки в полном объеме, в такой же степени, как если бы каждый из них был включен явно и индивидуально.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРИДОНОВЫЕ И АЗАПИРИДОНОВЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ПРИМЕНЕНИЯ | 2011 |
|
RU2617405C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2020 |
|
RU2840815C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ И ЗАМЕЩЕННЫЕ ПУРИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОЦЕССИРУЮЩЕЙ ПРОТЕАЗЫ 1 (USP1) | 2019 |
|
RU2833222C2 |
| НОВОЕ ПРОИЗВОДНОЕ ПУРИНИЛПИРИДИНИЛАМИНО-2,4-ДИФТОРФЕНИЛСУЛЬФОНАМИДА, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ RAF-КИНАЗЫ, СОДЕРЖАЩАЯ ДАННОЕ СОЕДИНЕНИЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2011 |
|
RU2550038C2 |
| МОДУЛЯТОРЫ КАЛЬПАИНА И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2773288C2 |
| ПРОИЗВОДНЫЕ АРИЛАМИДОВ В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2011 |
|
RU2535671C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ПУТИ JAK | 2011 |
|
RU2672100C2 |
| 2-АМИНОБЕНЗОКСАЗОЛКАРБОКСАМИДЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ 5-НТ3 | 2007 |
|
RU2448105C2 |
| 6,7-ДИГИДРО-5H-ПИРИДО[2,3-C]ПИРИДАЗИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ BCLXL И ПРОАПОПТОТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2832191C2 |
| ПИРАЗОЛОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2539568C2 |
Изобретение относится к области органической химии, а именно к гетероциклическому соединению формулы (I) или к его стереоизомеру или фармацевтически приемлемой соли, где X представляет собой CH или N; Z представляет собой (i) NH(CH2)nCHR1Ar, где n равно 0 или 1, или (ii) 1-алкил-4-арил-пирролидин-3-иламин, где алкил представляет собой C1 алкил, необязательно замещенный фенильным кольцом, и арил представляет собой фенил, замещенный метокси; R1 представляет собой (а) водород, (b) C1-C6 алкил, необязательно замещенный гидроксильной группой, (c) 4-5-членный гетероцикл, содержащий 1 гетероатом, выбранный из N, где гетероцикл необязательно замещен одной группой, выбранной из группы, состоящей из галогена, или (d) 5-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из N, где гетероарил необязательно замещен одной группой, выбранной из C1-6 алкила; Ar представляет собой фенил, пиридинил или индолил, необязательно замещенный 1-2 группами, независимо выбранными из (а) C1-6 алкокси, (b) галогена, (c) C1-6 галогеналкокси, (d) циано, (e) бензила, (f) фенокси, где указанный фенокси необязательно замещен галогеном или C1-6 алкилом, (g) 4-метилпиперазин-1-ила или (h) гетероарила, выбранного из группы, состоящей из пиридинила, пиразинила, пиримидинила и пиразолила, где указанный гетероарил необязательно замещен одним C1-10 алкилом; R2 выбран из группы, состоящей из (a) C1-5 гидроксиалкила, (b) C1-6 галогеналкила, (c) гетероциклила, где указанный гетероциклил выбран из группы, состоящей из тетрагидрoпиранила, тетрагидрoфуранила, 2-окса-бицикло[2,2,1]гептан-5-ила и пирролидинила, и где указанный гетероциклил необязательно замещен 1 группой, независимо выбранной из группы, состоящей из галогена, C1-3 гидроксиалкила или оксо, (d) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила, и где указанный гетероарил необязательно замещен 1-2 C1-3 алкильными группами, (е) C3 циклоалкил-C1-2 алкила, где указанный C3 циклоалкил-C1-2 алкил необязательно замещен гидроксилом. Также изобретение относится к фармацевтической композиции на основе соединения формулы (I), способу ингибирования активности протеинкиназы ERK, способу лечения или уменьшения тяжести гиперпролиферативного расстройства и применению соединения формулы (I). Технический результат: получены новые гетероциклические соединения, полезные при лечении гиперпролиферативного расстройства. 7 н. и 22 з.п. ф-лы, 3 табл., 34 пр.

1. Соединение в соответствии с формулой I

где X представляет собой CH или N;
Z представляет собой (i) NH(CH2)nCHR1Ar, где n равно 0 или 1, или (ii) 1-алкил-4-арил-пирролидин-3-иламин, где алкил представляет собой C1 алкил, необязательно замещенный фенильным кольцом, и арил представляет собой фенил, замещенный метокси;
R1 представляет собой (а) водород, (b) C1-C6 алкил, необязательно замещенный гидроксильной группой, (c) 4-5-членный гетероцикл, содержащий 1 гетероатом, выбранный из N, где гетероцикл необязательно замещен одной группой, выбранной из группы, состоящей из галогена, или (d) 5-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из N, где гетероарил необязательно замещен одной группой, выбранной из C1-6 алкила;
Ar представляет собой фенил, пиридинил или индолил, необязательно замещенный 1-2 группами, независимо выбранными из (а) C1-6 алкокси, (b) галогена, (c) C1-6 галогеналкокси, (d) циано, (e) бензила, (f) фенокси, где указанный фенокси необязательно замещен галогеном или C1-6 алкилом, (g) 4-метилпиперазин-1-ила или (h) гетероарила, выбранного из группы, состоящей из пиридинила, пиразинила, пиримидинила и пиразолила, где указанный гетероарил необязательно замещен одним C1-10 алкилом;
R2 выбран из группы, состоящей из (a) C1-5 гидроксиалкила, (b) C1-6 галогеналкила, (c) гетероциклила, где указанный гетероциклил выбран из группы, состоящей из тетрагидрoпиранила, тетрагидрoфуранила, 2-окса-бицикло[2,2,1]гептан-5-ила и пирролидинила, и где указанный гетероциклил необязательно замещен 1 группой, независимо выбранной из группы, состоящей из галогена, C1-3 гидроксиалкила или оксо, (d) гетероарила, где указанный гетероарил выбран из группы, состоящей из пиразолила и пиридинила, и где указанный гетероарил необязательно замещен 1-2 C1-3 алкильными группами, (е) C3 циклоалкил-C1-2 алкила, где указанный C3 циклоалкил-C1-2 алкил необязательно замещен гидроксилом; или
его стереоизомер или фармацевтически приемлемая соль.
2. Соединение по п.1, где X представляет собой N.
3. Соединение по п.1, где X представляет собой CH.
4. Соединение по любому из пп.2 или 3, где Z представляет собой NH(CH2)nCHR1Ar и n равно 1.
5. Соединение по любому из пп.2 или 3, где Z представляет собой NH(CH2)nCHR1Ar и n равно 0.
6. Соединение по любому из пп.2 или 3, где R1 представляет собой (а) водород, (b) C1-6 алкил, необязательно замещенный гидроксильной группой, (c) пирролидинильную группу, необязательно замещенную галогеном, или (d) пиразолильный или имидазолильный фрагмент, необязательно замещенный C1-6 алкильным фрагментом, и Ar представляет собой необязательно замещенный фенил.
7. Соединение по п.6, где R1 представляет собой (а) C1-6 алкил, (b) C1-6 алкил, замещенный гидроксильной группой, или (c) пиразолил, необязательно замещенный C1-6 алкильным фрагментом.
8. Соединение по п.7, где R1 представляет собой (а) (R)-C1-6 алкил, (b) (S)-C1-6 гидроксиалкил или (c) (S)-1-C1-6 алкил-1H-пиразол-4-ил.
9. Соединение по п.8, где R1 представляет собой (а) (R)-этил, (b) (S)-2-гидроксиметил или (c) (S)-1-метил-1H-пиразол-4-ил.
10. Соединение по п.1, где R2 представляет собой (а) C1-5 гидроксиалкил, (b) гетероциклил, где указанный гетероциклил представляет собой тетрагидрoпиранил или тетрагидрoфуранил, замещенный 1 группой, независимо выбранной из галогена или C1-3 гидроксиалкила, или (c) гетероарил, где указанный гетероарил представляет собой пиразолил, или пиридинил, где гетероарил необязательно замещен 1-2 C1-6 алкильными фрагментами, и N-алкил-пиразолил, необязательно замещенный 1 C1-6 алкильным фрагментом.
11. Соединение по п.10, где R2 представляет собой 1-метил-1H-пиразол-4-ил, 2-метил-2H-пиразол-3-ил, 2,5-диметил-2H-пиразол-3-ил, тетрагидрoпиран-4-ил, 3-фтор-тетрагидрoпиран-4-ил, тетрагидрoфуран-3-ил или 2-гидрокси-1-метил-этил.
12. Соединение по п.1, где Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано.
13. Соединение по пп.2 или 3, где R1 представляет собой (R)-этил, (S)-2-гидроксиметил или (S)-1-метил-1H-пиразол-4-ил; R2 представляет собой 1-метил-1H-пиразол-4-ил, 2-метил-2H-пиразол-3-ил, 2,5-диметил-2H-пиразол-3-ил, тетрагидрoпиран-4-ил, 3-фтор-тетрагидрoпиран-4-ил, тетрагидрoфуран-3-ил или 2-гидрокси-1-метил-этил; и Ar представляет собой фенил, необязательно замещенный 1 или 2 группами, независимо выбранными из C1-6 алкокси, галогена, C1-6 галогеналкокси или циано.
14. Соединение по п.13, где Ar представляет собой 3-фторфенил, 3-фтор-4-метокси-фенил, 4-хлор-3-фтор-фенил, 4-трифторметокси-фенил, 3-хлор-4-циано-фенил, 4-метокси-фенил или 4-дифторметокси-фенил.
15. Соединение по любому из пп.2 или 3, где Z представляет собой 1-алкил-4-арил-пирролидин-3-иламин, где алкил представляет собой C1 алкил, необязательно замещенный фенильным кольцом, и арил представляет собой фенил, замещенный метокси.
16. Соединение по п.1, выбранное из группы, состоящей из:
 ,
,  ,
, 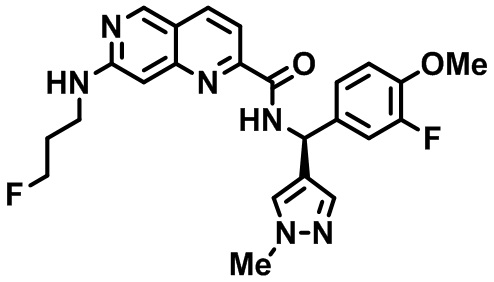 ,
,
 ,
,  ,
, 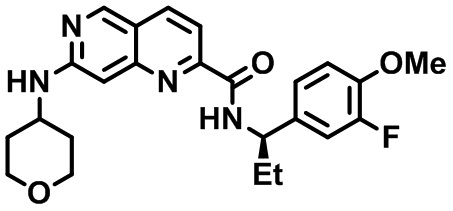 ,
,
 ,
,  ,
,  ,
,
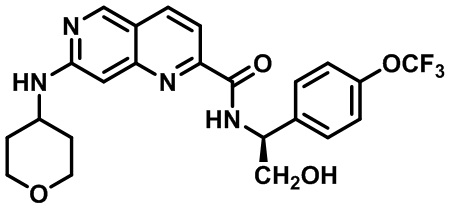 ,
,  ,
, 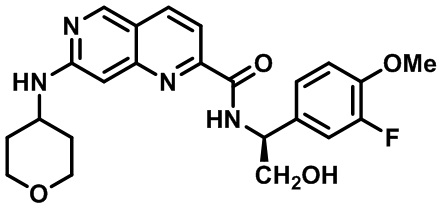 ,
,
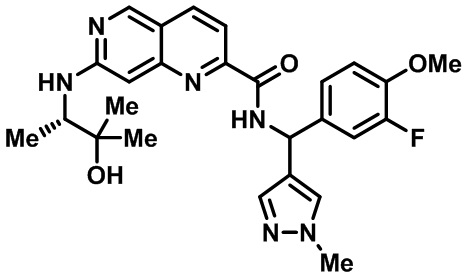 ,
,  ,
, 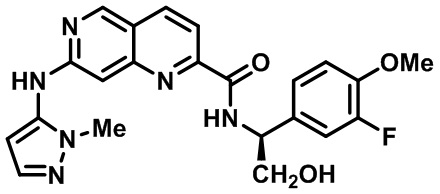 ,
,
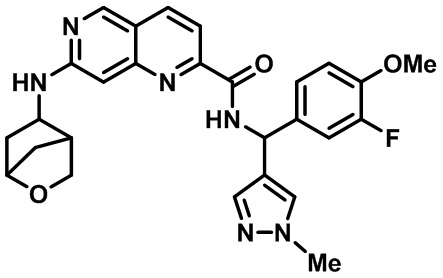 ,
, 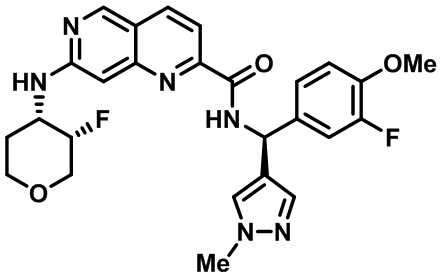 ,
, 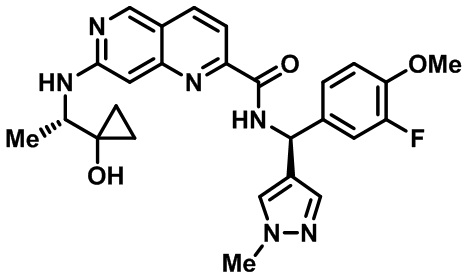 ,
,
 ,
, 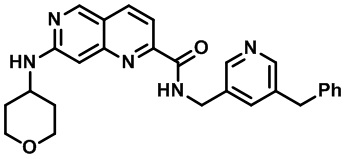 ,
, 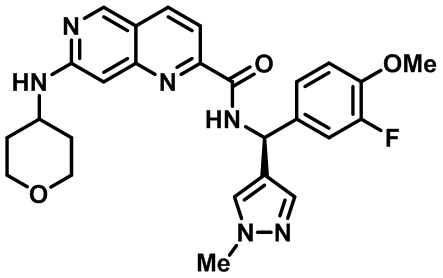 ,
,
 ,
,  ,
,  ,
, 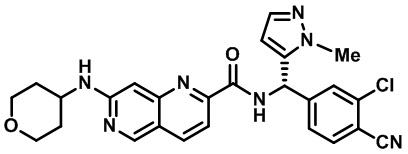 ,
, 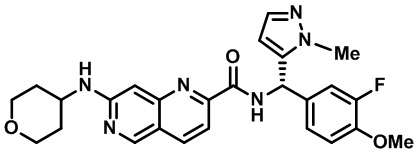 ,
, 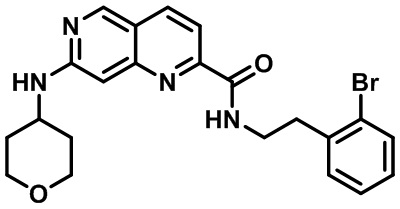 ,
,  ,
,  ,
,  ,
, 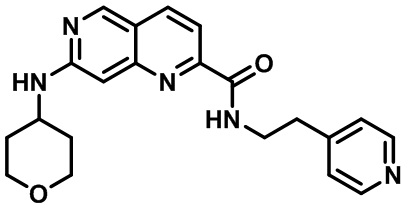 ,
, 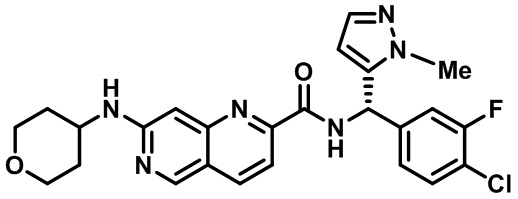 ,
, 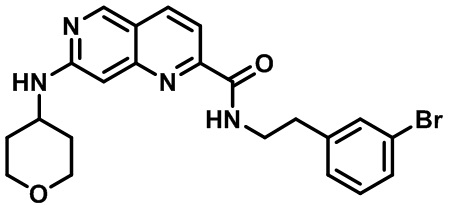 ,
,  ,
,  ,
,  ,
,  ,
, 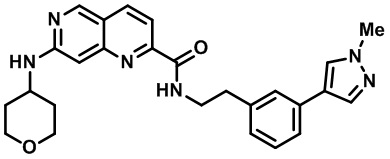 ,
,  ,
, 
 ,
,  ,
, 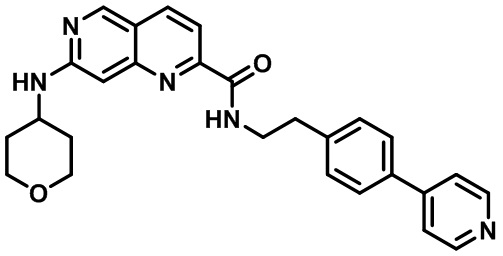 ,
,  ,
,  ,
, 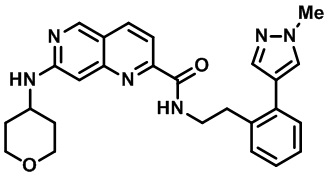 ,
,  ,
,  ,
, 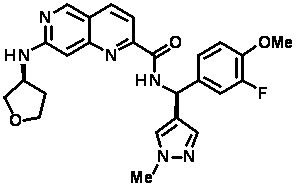 ,
,  ,
,  ,
, 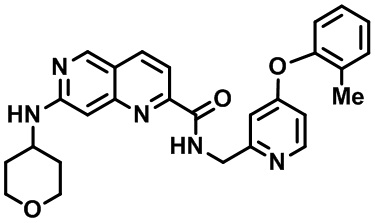 ,
,  ,
,  ,
, 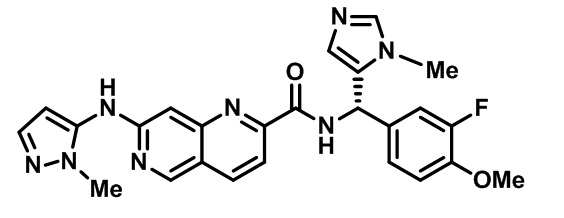 ,
, 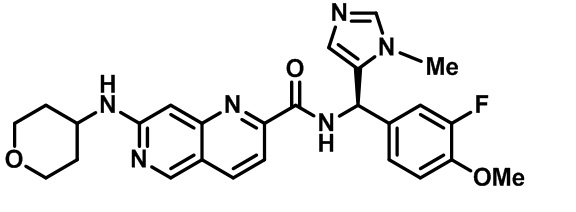 ,
,  ,
,  ,
,  ,
,  ,
, 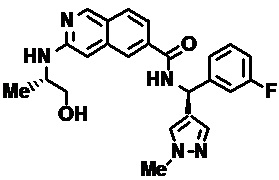 ,
, 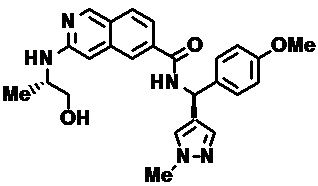 ,
, 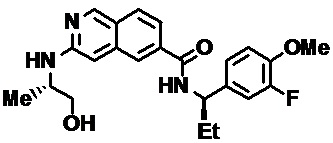 ,
, 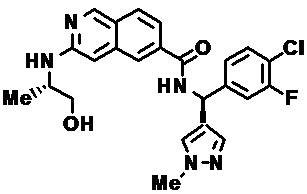 ,
,  ,
,  ,
, 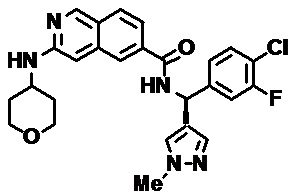 ,
,  ,
,  ,
, 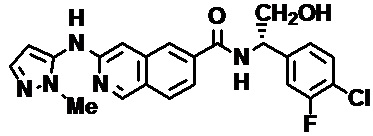 ,
, 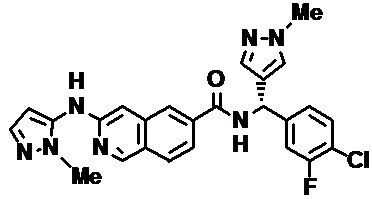 ,
, 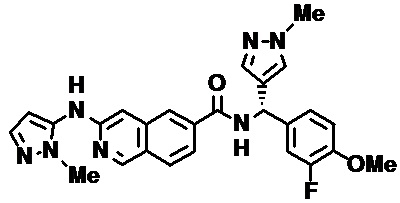 ,
, 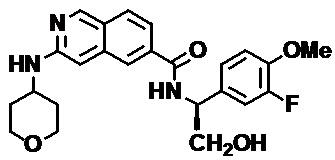 ,
, 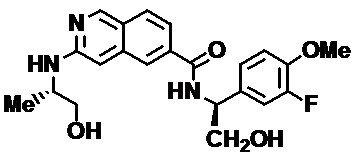 ,
,  ,
, 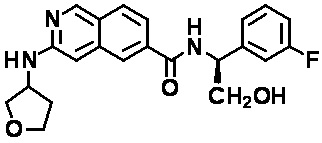 ,
, 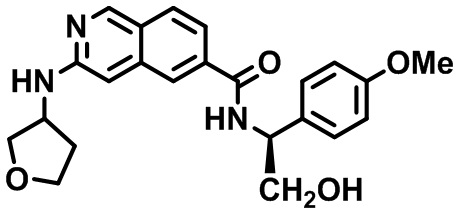 ,
,  ,
,  ,
, 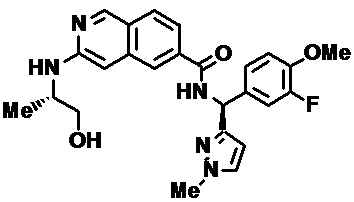 ,
, 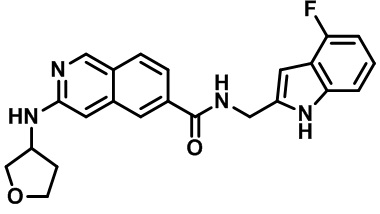 ,
, 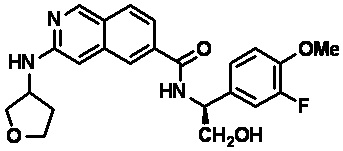 ,
, 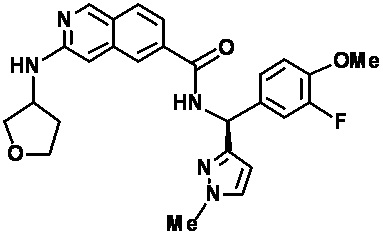 ,
, 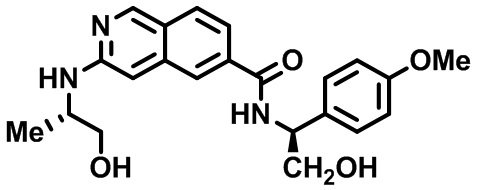 ,
,  ,
, 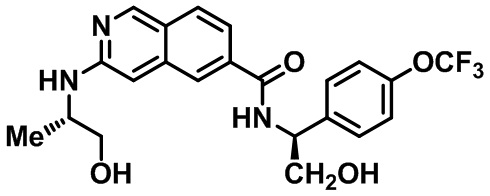 ,
,  ,
,  ,
, 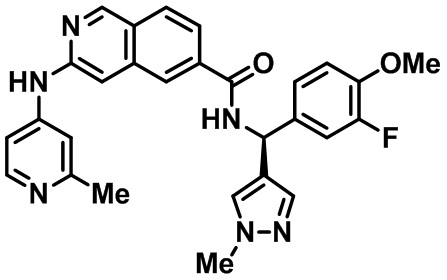 ,
, 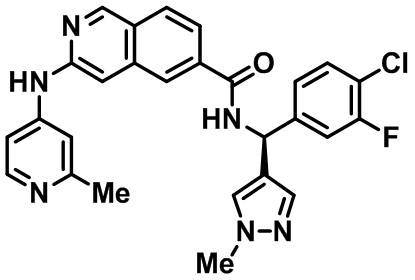 ,
, 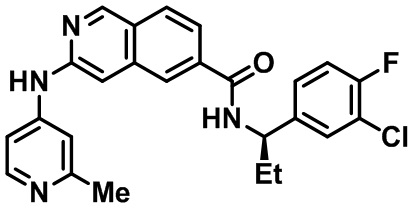 ,
,  ,
,  ,
, 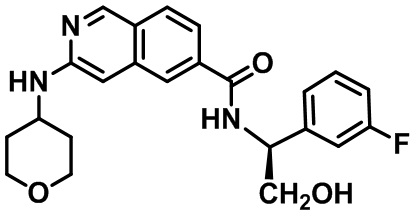 ,
, 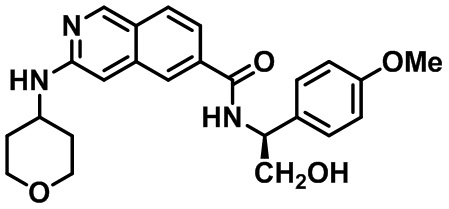 ,
,  ,
,  ,
, 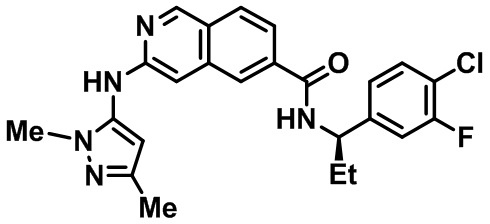 ,
,  ,
,  ,
, 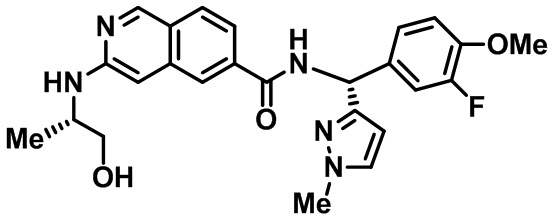 ,
,  ,
, 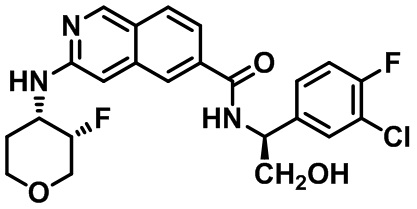 ,
, 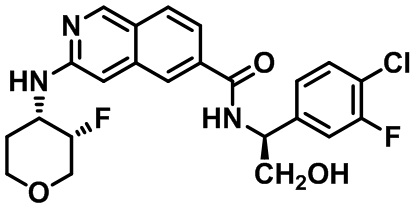 ,
, 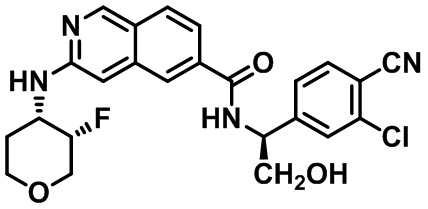 ,
,  ,
, 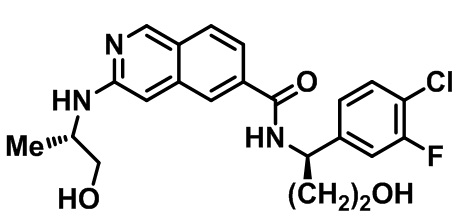 ,
, 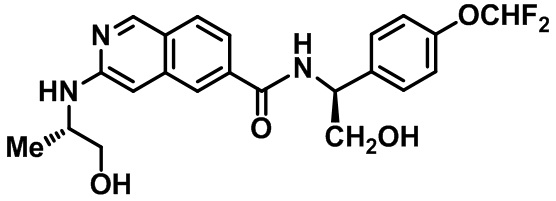 ,
, 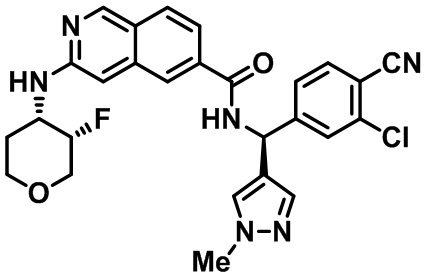 ,
, 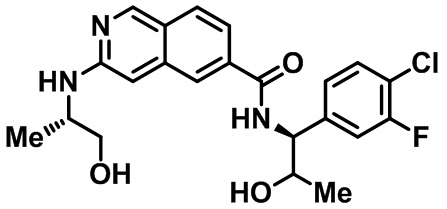 ,
,  ,
, 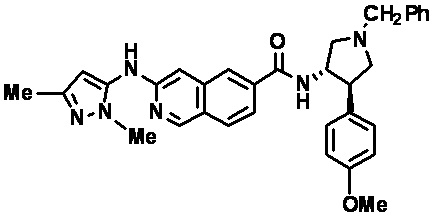 ,
, 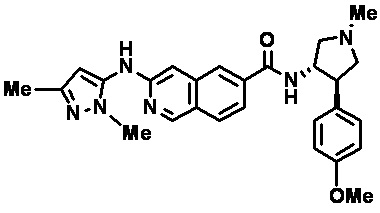 ,
,  ,
, 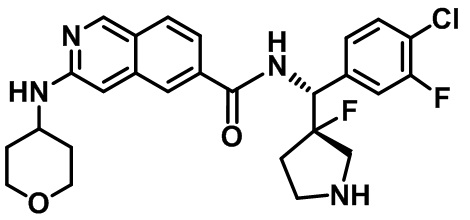 ,
, 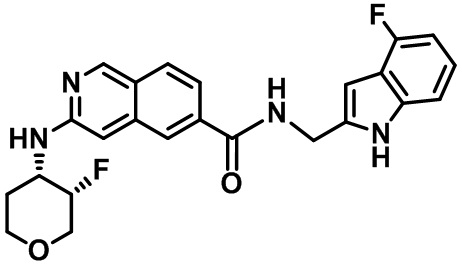 и
и 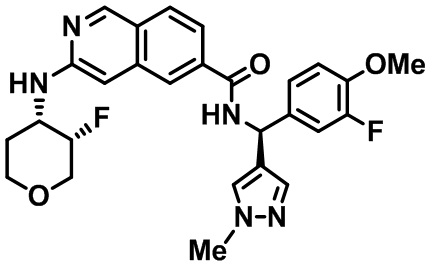
или его фармацевтически приемлемая соль.
17. Фармацевтическая композиция для лечения или уменьшения тяжести гиперпролиферативного расстройства, содержащая соединение по пп.1–16 и по меньшей мере один фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель.
18. Способ ингибирования активности протеинкиназы ERK в клетках, включающий обработку клеток соединением по п.1.
19. Способ ингибирования активности протеинкиназы ERK у пациента, нуждающегося в этом, включающий стадию введения указанному пациенту соединения по п.1.
20. Способ лечения или уменьшения тяжести гиперпролиферативного расстройства у пациента, нуждающегося в этом, причем способ включает введение указанному пациенту соединения по п.1.
21. Способ по п.20, отличающийся тем, что указанное гиперпролиферативное расстройство выбрано из группы, состоящей из аденомы, рака мочевого пузыря, рака мозга, рака молочной железы, колоректального рака, эпидермальной карциномы, фолликулярной карциномы, рака мочеполовых путей, глиобластомы, болезни Ходжкинса, рака головы и шеи, гепатомы, кератоксантомы, рака почки, крупноклеточной карциномы, лейкозов, аденокарциномы легкого, рака легкого, лимфоидных расстройств, меланомы и немеланомного рака кожи, миелодиспластического синдрома, нейробластомы, неходжкинской лимфомы, рака яичника, папиллярной карциномы, рака поджелудочной железы, рака предстательной железы, рака прямой кишки, саркомы, мелкоклеточной карциномы, рака яичка, тетракарцином, рака щитовидной железы и недифференцированной карциномы.
22. Способ по п.20, отличающийся тем, что указанное гиперпролиферативное расстройство выбрано из группы, состоящей из меланомы, рака поджелудочной железы, рака щитовидной железы, рака ободочной и прямой кишки, рака легкого, рака молочной железы и рака яичника.
23. Способ по п.20, отличающийся тем, что указанное гиперпролиферативное расстройство выбрано из группы, состоящей из острого миелогенного лейкоза, хронического миеломоноцитарного лейкоза, хронического миелогенного лейкоза, множественной миеломы и миелоидного лейкоза.
24. Способ по п.20, отличающийся тем, что соединение по п.1 вводят вместе с по меньшей мере еще одним химиотерапевтическим агентом, применяемым для лечения или облегчения гиперпролиферативного расстройства.
25. Применение соединения по п.1 в производстве лекарственного средства для лечения гиперпролиферативного заболевания.
26. Соединение по п.1 для применения в качестве лекарственного средства для лечения гиперпролиферативного заболевания.
27. Соединение по п.1 для применения в терапии для лечения гиперпролиферативного заболевания.
28. Соединение по п.1 для применения в лечении рака.
29. Фармацевтическая композиция, содержащая соединение по п.1, для применения в лечении гиперпролиферативного заболевания.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| АМИНОИЗОХИНОЛИНОВЫЙ ИНГИБИТОР ТРОМБИНА С УЛУЧШЕННОЙ БИОДОСТУПНОСТЬЮ | 2007 |
|
RU2437879C2 |
| EA 200100033 A1, 25.06.2001. | |||
Авторы
Даты
2018-02-15—Публикация
2013-08-27—Подача