Изобретение относится к области охраны окружающей среды, а именно к очистке отходящих газов предприятий цветной металлургии от диоксида серы с получением элементарной серы. Газы с высоким содержанием диоксида серы образуются при производстве меди, никеля, других металлов из сульфидных руд.
Прямое каталитическое восстановление диоксида серы до элементарной серы с помощью различных восстановителей, в частности сероводорода, монооксида углерода, метана и/или синтез-газа известно давно. Среди перечисленных газов-восстановителей наибольшее применение на практике нашел сероводород, используемый для восстановления диоксида серы в процессе Клауса. Однако процесс Клауса используется в основном на предприятиях по переработке нефти и природного газа (НПЗ и ГПЗ) прежде всего как способ утилизации сероводорода, а его применение на предприятиях металлургической промышленности ограничено ввиду необходимости создания производства сероводорода для целей очистки. Каталитические процессы с участием метана, монооксида углерода и водорода для извлечения серы широко исследуются в последние годы и рассматриваются как наиболее перспективные и технически приемлемые решения практической реализации процесса десульфуризации отходящих газов химических и металлургических производств.
Преимуществом процесса восстановления диоксида серы метаном является использование в качестве восстановителя доступного и дешевого сырья - природного газа, причем преимущества этого процесса возрастают с повышением концентрации
SO2. К недостаткам процесса восстановления диоксида серы метаном можно отнести высокие рабочие температуры, обычно 780-950°С, что обусловлено необходимостью активации метана, поэтому процесс требует больших энергозатрат на разогрев реакторов. В результате протекания при высоких температурах побочных реакций образуются С, CS и H2S, а в присутствии паров воды возможно также образование СО и COS. Эти и другие причины обусловливают низкий выход серы, не более 65%, и низкую эффективность очистки промышленных газов, что требует установки дополнительных стадий очистки, в том числе от H2S, или увеличения числа реакторов.
В отличие от восстановления диоксида серы метаном процесс восстановления диоксида серы монооксидом углерода и/или водородом можно проводить при низких рабочих температурах, 350-600°С, обеспечивая высокую степень извлечения серы (до 85-95%). Существенными недостатками данного процесса являются сильный экзотермический эффект и образование в результате взаимодействия образовавшейся серы с водородом и монооксидом углерода побочных продуктов: H2S и COS, последний из которых является более токсичным, чем SO2. Вместе с этим при определенных условиях проведения процесса, в частности температурах выше 400°С и мольном соотношении восстановителей и диоксида серы, близком к стехиометрическому значению, CO(H2)/SО2=2, можно снизить образование сероводорода и сульфида карбонила до минимума даже при конверсии диоксида серы на уровне 85-98%. Сульфид карбонила можно также возвращать в цикл, обеспечивая его взаимодействие с диоксидом серы с образованием элементной серы. Минимизировать образование побочных продуктов можно также оптимизацией состава и свойств катализатора.
Катализатор для процесса очистки металлургических газов от диоксида серы путем его восстановления монооксидом углерода и/или водородом должен обладать рядом свойств. Во-первых, иметь высокую активность и селективность по отношению к элементарной сере в широком интервале концентраций диоксида серы от 3,5 об.% (низкоконцентрированные) до 10-40 об.% (высококонцентрированные). Для практического применения катализатор должен обеспечивать высокую конверсию SO2, по крайней мере, 90% и селективность в отношении элементарной серы не менее 90% при температурах 400-500°С и объемных скоростях потока 500-5000 ч-1. Во-вторых, катализатор должен иметь низкую активность по отношению к побочным реакциям, приводящим к образованию H2S и COS при взаимодействии с парообразной серой. В-третьих, обладать устойчивостью к воздействию триоксида серы, кислорода и паров воды, присутствующих в отработанных газах металлургических производств.
Указанные соединения могут быть удалены из отработанных газов до их подачи на катализатор сорбционными методами. Триоксид серы можно также удалять термической деструкцией при высоких температурах (около 900°С). Однако описанные выше приемы существенно усложняет технологическое осуществление каталитического процесса очистки металлургических газов от диоксида серы.
В качестве катализаторов в процессах СКВ SO2 монооксидом углерода и/или водородом рассматривают активированный оксид алюминия [Khalafalla, S.E., Haas, L.A., J. Catal. 24 (1972) 115-120], смеси оксидов алюминия и железа, металлы группы железа, нанесенные на оксид алюминия [Doumani, Т.F., Ind. Eng. Chem. 36 (1944)
329-332], смешанные оксиды [Kim, Н., Appl. Catal. В: Env. 19 (1998) Р.233-243; Hibbert, D.B., Campbell, R.H., Appl.Catal. 41 (1988) 289-299] и др. Катализаторы на основе смешанных оксидов переходных металлов, нанесенные на оксид алюминия, являются наиболее активными в реакции восстановления диоксида серы среди изученных катализаторов.
В патентах US 3653833, B01D 53/50, С01В 17/04, 04.04.72, и US 4039650, B01D 53/50, С01В 17/04, 02.08.77, для проведения непрерывного процесса восстановления SO2, содержащегося в газовых потоках, в элементарную серу, восстановительным газом, выбранным из группы: СО, водород, углеводороды С1-С4 и их смеси, преимущественно метан или природный газ, предлагается использовать в качестве катализатора алюминат кальция, боксит, Al2O3, SiO2 V2O5. Описанный способ позволяет очищать газы с содержанием SO2 не менее 30 об.% (в расчете на сухой газ). Для увеличения эффективности очистки в US 3653833 и US 4039650 предлагается использовать последовательно три реактора, при этом на входе во второй и третий реакторы в газовую смесь дополнительно подается восстановительная смесь и возможно попеременное изменение потока (реверс потока), что позволяет исключить перегрев реакторов и снизить протекание побочных реакций. Добавление паров элементарной серы в первый реактор позволяет снизить температуру начала реакции и ускорить реакцию в первом реакторе. Недостатком данного процесса является то, что высокая эффективность катализатора достигается преимущественно при 510-1090°С.
В патенте US 4147763, F02M 7/22, 03.04.79, предложен катализатор со структурой шпинели: прямой (А[В]2О4), обращенной (В[АВ]О4) и разупорядоченной, проявляющий высокую активность и селективность в реакции восстановления SO2 монокосидом углерода или водородом из высококонцентрированных смесей (3-20 об.%) в присутствии кислорода и паров воды 450-700°С, скоростях потока
2000-36000 ч-1. Перед использованием проводят восстановительную обработку катализатора в СО или реакционной среде при 700°С в течение 15-45 мин. Катализатор на основе Со3О4 имеет высокую активность в отсутствие кислорода, а CoFe2О4, CoCr2О4 и CoV2O4 в присутствии кислорода.
В патенте US 5384301, B01D 53/86, B01J 23/10, 24.01.95, описаны катализаторы для процесса извлечения серы из промышленных газовых выбросов, содержащих 1-10 об.% SO2, путем каталитического восстановления SO2 газом-восстановителем: СО, водород, природный газ или их смеси. Предлагаемые катализаторы имеют общую формулу:
[(FO2)l-n(RO)n]1-kMk, либо [(FO2)l-n(RO1,5)n]1-kMk, либо [LnxZr1-xO2-0,5x]l-kMk, где F - Се, Th, Hf, Та, Zr; R - Be, Mg, Ca, Sr, Ba; M - Mn, Fe, Co, Ni, Cu, Zn, Mo, Rh, Pd, Ag и Pt. Катализаторы обладают высокой активностью при соотношении CO/SO2, близком к стехиометрическому (~2), температуре 300-800°С и скорости потока 500-100000 ч-1.
В патенте US 5494879, B01J 23/74, 37.02.96, предлагается оксидный катализатор сложного состава, содержащий оксиды Fe, Ni и Со с оксидами Мо, Mn или Cr, нанесенные на носители на основе SiO2, γ-Al2О3, молекулярные сита 5А и 13Х. Катализатор готовят методом пропитки растворами нитратов соответствующих солей с последующим прокаливанием при температурах 600-1000°С, что приводит к стабилизации активного компонента в кристаллических структурах типа шпинели или перовскита. Катализатор оптимального состава 30 мас.% Fe4CoNiMoCr2Mn2O18/γ-Al2О3 в широком интервале эксплуатационных параметров: 5000-15000 ч-1, 440-480°С и (H2+CO)/SO2=2 и Н2/СО=0,75, обеспечивает высокую конверсию SO2 (90-94%) и выход элементарной серы (до 93-96%). Для повышения эффективности процесса авторы предлагают первоначально нагревать катализатор до 700-800°С в течение 2 ч, а потом поддерживать температуру процесса в области 440-480°С. Для повышения эффективности очистки предлагается вводить H2S и COS обратно в реакционную среду.
Катализатор, описанный в US 5494879, является наиболее близким к заявляемому по технической сущности. К недостаткам известного катализатора можно отнести узкий диапазон температур (440-480°С), в которых катализатор обеспечивает высокую степень извлечения серы; необходимость высокотемпературной активации катализатора (700-800°С).
Задача, решаемая изобретением: достижение высокой эффективности очистки металлургических газов, содержащих не менее 15 об.% диоксида серы, путем восстановления на катализаторе диоксида серы в элементарную серу монооксидом углерода и/или водородом при варьировании соотношения СО/водород от 1/1 до 1/3 и при температурах от 350 до 550°С.
Поставленная задача решается следующим образом.
Катализатор для восстановления диоксида серы в металлургических газовых выбросах, в том числе предприятий цветной металлургии, включающий сульфид Cu1-xMxCr2S4+δ или смесь индивидуальных сульфидов CuS, Cr2S3 MS1+δ в количестве 2-20 мас.%, которые формируются при пропускании газовых смесей, содержащих сероводород, над нанесенным на носитель оксидом состава Cu1-xMxCr2O4 со структурой шпинели, где М - переходный металл, выбранный из группы: Fe, Со, Ni, значения х и δ изменяются от 0-0,5, и носитель, в качестве которого используют оксид алюминия, в том числе модифицированный добавкой оксида церия, при следующем соотношении компонентов, мас.%: Cr 3-12, Cu 0,1-5,0, металл переходной группы 0,01-2,50, церий 1-15, оксид алюминия - остальное.
Первоначальное формирование оксида Cu1-xMxCr2O4 со структурой шпинели при последующем пропускании сероводородсодержащей смеси обеспечивает формирование высокодисперсного рентгеноаморфного смешанного сульфида состава Cu1-xMxCr2S4+δ и/или смеси высокодисперсных индивидуальных сульфидов CuS, Cr2S3 MS1+δ, что обеспечивает высокую эффективность очистки от диоксида серы уже при температурах 350°С.
Превращение оксидной формы катализатора в сульфидную форму проводят при температуре 300-450°С в газовой смеси, изначально содержащей сероводород либо содержащей сероводород, образующийся в результате реакции. В качестве реакций, приводящих к образованию сероводорода, используют процесс разложения сераорганических соединений, преимущественно диметилдисульфида, или восстановления диоксида серы метаном или водородом, преимущественно водородом при соотношении водород/SO2>3.
Процесс СКВ SO2 смесью СО и Н2 проводят на катализаторе при температурах 350-550°С и скоростях газового потока 500-5000 ч-1, соотношениях Н2/СО в интервале 1-3 (синтез-газ, коксовый газ), обеспечивая выход элементной серы на уровне 85-95% при стехиометрическом соотношении CO+H2/SO2 (около 2).
Заявляемый катализатор готовят следующим образом.
Для приготовления катализатора используют гранулы из оксида алюминия, в том числе модифицированного оксидом церия, имеющие удельную поверхность 160-290 м2/г, объем пор 0,30-0,6 см3/г. Гранулы оксида алюминия могут иметь форму сфер, цилиндров, колец, блоков. Размер гранул 1,5-10 мм.
Модифицирование гранул оксида алюминия добавками оксида церия проводят методом пропитки по влагоемкости раствором нитрата церия заданной концентрации. Пропитанные гранулы сушат на воздухе при 70-120°С и прокаливают при 500°С в течение 4 ч. Содержание оксида церия в носителе варьируют в интервале от 1 до 15 мас.%. Оксид алюминия, модифицированный оксидом церия, имеет удельную поверхность 160-290 м2/г и объем пор 0,3-0,6 см3/г.
Далее на носитель наносят оксид состава Cu1-xMxCr2O4 со структурой шпинели одним из следующих способов.
Метод капиллярной пропитки по влагоемкости (метод 1)
Гранулы пористого алюмооксидного носителя, в том числе модифицированного добавкой оксида церия, пропитывают по влагоемкости раствором бихроматов меди и/или переходного металла из группы: Fe, Со, Ni, заданной концентрации. Пропитанные гранулы сушат на воздухе при 70-120°С и прокаливают при 700°С в течение 4 ч для формирования структуры шпинели. Содержание хромата меди в катализаторах, рассчитанное из данных атомно-эмиссионной спектроскопии с индуктивно-связанной плазмой (АЭС-ИСП), варьируют в интервале от 5 до 35 мас.%. Метод пропитки по влагоемкости является наиболее простым в технологическом исполнении и наиболее безотходным.
Метод последовательной капиллярной пропитки по влагоемкости (метод 2)
Гранулы пористого алюмооксидного носителя, в том числе модифицированного добавкой оксида церия, пропитывают по влагоемкости раствором хромовой кислоты, Н2Сr2О7, заданной концентрации. Пропитанные гранулы сушат на воздухе при 70-120°С и прокаливают при 400°С в течение 4 ч. Далее гранулы пропитывают раствором нитрата меди заданной концентрации; сушат и прокаливают при 700°С в течение 4 ч для формирования структуры шпинели. Содержание хромата меди в катализаторах, рассчитанное из данных АЭС-ИСП, варьируют в интервале от 5 до 20 мас.%.
Описанный метод позволяет готовить катализаторы с соотношением Cu/Cr в интервале 0,25-2,0.
Далее катализатор подвергают активированию одним из 3 способов.
В смеси сероводорода (способ 1)
Гранулы прокаленного катализатора загружают в стеклянный реактор и пропускают поток чистого сероводорода или смесь сероводорода и водорода при температуре 320-400°С. Скорость потока подбирают экспериментально так, чтобы в первый момент времени на выходе из реактора не фиксировался сероводород. Время активации рассчитывают таким образом, чтобы количество пропущенного сероводорода соответствовало 4 молям H2S на 1 моль оксида Cu1-xMxCr2O4 со структурой шпинели.
В смеси диметилдисулъфида (способ 2)
Гранулы прокаленного катализатора загружают в стеклянный реактор и пропускают поток диметилдисульфида или смесь диметилдисульфида и водорода при температуре 300-350°С. Скорость потока 500-1000 ч-1. Время активации рассчитывают таким образом, чтобы количество пропущенного диметидисульфида соответствовало 2 молям (СН3)2S2 на 1 моль оксида Cu1-xMxCr2O4 со структурой шпинели.
В смеси диоксида серы с восстановителем (способ 3)
Гранулы прокаленного катализатора загружают в проточный реактор и пропускают смесь диоксида серы с водородом с мольным соотношением H2/SO2>3 при температуре 300-450°С и скорости потока 500-1000 ч-1. Время активации рассчитывают таким образом, чтобы количество образующегося сероводорода соответствовало 4 молям H2S на 1 моль оксида Cu1-xMxCr2O4 со структурой шпинели.
Последний способ является предпочтительным, поскольку может быть проведен в реакторе восстановления диоксида серы монооксидом углерода и/или водородом перед началом эксплуатации. Кроме того, данный способ не требует снабжения производства сероводородом или диметилдисульфидом.
Каталитические свойства образцов изучали на лабораторной установке, оборудованной проточным реактором, в интервале температур от 300 до 600°С и объемной скорости потока 500-5000 ч-1. Реакционная газовая смесь содержала, об.%: SO2 15-30, монооксида углерода 15-54, водорода 15-54, пары воды до 15, СО2 до 15 и аргон, при соотношении SО2/(CO+H2), близком к 0,5. Загрузка катализатора составляла 180 см3, размер гранул 1,5-10 мм. Активность образцов характеризовали степенью превращения 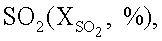 монооксида углерода (XCO, %) и водорода
монооксида углерода (XCO, %) и водорода 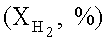 и выходом элементарной серы (YS, %), COS (YCOS, %) и сероводорода
и выходом элементарной серы (YS, %), COS (YCOS, %) и сероводорода 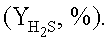
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. Катализатор готовят по методу 1, активирование по способу 1.
В качестве пористого алюмооксидного носителя используют сферический γ-Al2О3 с удельной поверхностью 180 м2/г, объемом пор 0,55 см3/г и диаметром гранул 1,5-1,8 мм. Носитель пропитывают раствором бихромата меди с концентрацией 431 г/л, сушат при 110°С и прокаливают при 700°С. Содержание Cu и Cr по данным АЭС-ИСП составляет 5,4 и 9,6 мас.% соответственно или 19,7 мас.% в расчете на CuCr2O4 и 1,1 мас.% в расчете на Cr2О3. Оксид алюминия, Al2O3, - остальное.
Для активирования катализатор в количестве 180 см3 загружают в проточный реактор диаметром 50 мм и подают поток сероводорода со скоростью 10 л/ч. Поднимают температуру в реакторе до 400°С. Выдерживают при указанных условиях в течение 2 часа. Охлаждают до 200°С. В процессе активирования по данным РФА и ДТА наблюдается формирование мелкодисперсных частиц CuS и Cr2S3. Содержание
Cu и Cr по данным АЭС-ИСП составляет 4,2 и 7,5 мас.%, соответственно. Содержание серы, определенное рентгеноспектральным флуоресцентным методом, составляет 4,2 мас.%. Расчетное содержание, мас.%, CuCr2S4 составляет 4,6; CuS 5; Cr2S3 1,1, т.е. суммарное содержание сульфидов составляет 10,7. Содержание CuCr2O4 10,5 мас.%, оксид алюминия, Al2O3 - остальное.
Для исследования активности на катализатор со скоростью 294 л/ч подают реакционную смесь, содержащую, об.%: SO2 28, СО 28 и Н2 54. Поднимают температуру на стенках реактора от 200 до 600°С, и при каждой температуре проводят хроматографический анализ газовой смеси. По данным хроматографического анализа с учетом изменения объема реагентов и продуктов реакции проводят расчет степени превращения 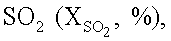 монооксида углерода (XCO, %) и водорода
монооксида углерода (XCO, %) и водорода 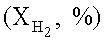 и выхода элементарной серы (YS, %), сульфида карбонила (YCOS, %) и сероводорода
и выхода элементарной серы (YS, %), сульфида карбонила (YCOS, %) и сероводорода 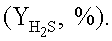 Кроме того, проводят измерение температуры в слое катализатора.
Кроме того, проводят измерение температуры в слое катализатора.
При 1630 ч-1 и составе газовой смеси, об.%: SO2 28, СО 18 и Н2 54, катализатор обеспечивает конверсию SO2 на уровне 85% при температуре 350°C и 99,5% при 400-600°С; выход серы составляет 78% при 350°С и 92-99% при 400-600°С; максимальный выход COS достигается при 300°С и составляет 2%, при 400°С и более высоких температурах образования COS и H2S не наблюдается.
Пример 2.
Аналогичен примеру 1, отличие заключается в том, что для приготовления катализатора используют носитель на основе γ-Al2О3, модифицированный оксидом церия. Содержание Cu, Cr и Се по данным АЭС-ИСП составляет 4,2; 7,8 и 12 мас.% соответственно или 15,4 мас.% в расчете на CuCr2O4 и 1,3 мас.% в расчете на Cr2О3. Оксид алюминия - остальное. Церий входит в состав катализатора в виде оксида СеO2.
Для активирования катализатор в количестве 180 см3 загружают в проточный реактор диаметром 50 мм и подают смесь сероводорода (10 об.%) в водороде со скоростью 80 л/ч. Поднимают температуру в реакторе до 320°С. Выдерживают при указанных условиях в течение 2 часов. Охлаждают до 200°С. В процессе активирования по данным РФА и ДТА наблюдается формирование мелкодисперсных частиц CuS, окристаллизованные частицы с параметрами решетки Cr2S3 и CuCr2S4 наблюдаются методом рентгеновской дифракции. Содержание Cu, Cr и Се по данным АЭС-ИСП составляет 3,7; 6,8 и 12 мас.% соответственно. Содержание серы, определенное рентгеноспектральным флуоресцентным методом, составляет 3,6 мас.%. Суммарное содержание сульфидов составляет 9 мас.%, из них CuCr2S4 4,9; CuS 3,3; Cr2S3 0,8. Содержание, мас.%, CuCr2O4 5,5; CeO2 14,7; оксид алюминия - остальное.
При 1630 ч-1 и составе газовой смеси, об.%: SO2 28, СО 18 и Н2 54(аналогичны примеру 1), катализатор обеспечивает конверсию SO2 на уровне 90% при температуре 350°С и 99,5% при 400-600°С; выход серы составляет 82% при 350°С и 92-99% при 400-600°С; максимальный выход COS достигается при 300°С и составляет 2%, при 400°С и более высоких температурах образования COS и H2S не наблюдается.
Примеры 3-7. Катализатор готовят по методу 1, активирование по способу 2.
Способ приготовления катализатора аналогичен примеру 2, отличие заключается в содержании оксида CuCr2O4 шпинельной структуры. Содержание оксида CuCr2O4 составляет 5, 10, 15, 25 и 30 мас.%. Содержание церия 5 мас.% (для примеров 3,4, 5) и 1 мас.% (для примеров 6 и 7).
Активирование катализатора проводят в смеси диметилдисульфида с водородом (5 об.% ДМДС) при 320°С в течение 1-3 ч. Для этого образец катализатора в количестве 180 см3 загружают в проточный реактор и пропускают смесь со скоростью 20-40 л/ч. Время активации и скорость потока указаны в таблице 1, определялись из содержания оксида CuCr2O4 шпинельной структуры, общее количество пропущенного диметилдисульфида составляло 2 моль (СН3)2S2 на 1 моль CuCr2O4. В процессе активирования по данным РФА не наблюдается формирование окристаллизованных фаз сульфидов переходных металлов, мелкодисперсные окристаллизованные частицы с параметрами решетки CuS, Cr2S3 и CuCr2S4 наблюдаются методом рентгеновской дифракции и по данным ДТА. Содержание серы определяют рентгеноспектральным флуоресцентным методом.
Активность катализатора определяли при условиях из примера 1. Химический состав катализатора и каталитические свойства приведены в таблице 1.
Пример 8. Катализатор готовят по методу 2, активирование по способу 3.
В качестве пористого алюмооксидного носителя используют кольцеобразный γ-Al2О3 с влагоемкостью 0,5 см3/г, который пропитывают раствором нитрата меди с концентрацией 105 мг Cu/см3, сушат и прокаливают при 400°С. Далее пропитывают раствором хромой кислоты, Н2Сr2О7, с концентрацией 170 мг Cr/см3, сушат и прокаливают при 700°С. Содержание Cu, Cr и Се по данным АЭС-ИСП составляет 5,2; 8,5 и 10 мас.% соответственно или 19,0 мас.% в расчете на CuCr2O4 и 12,3 мас.% в расчете на СеО2, оксид алюминия - остальное. Катализатор имеет форму колец с внешним диаметром 6-8 мм, внутренним диаметром 3-5 мм и длиной 5-7 мм.
Активирование катализатора проводят в смеси диоксида серы и водорода (10 oб.% SO2) при 450°С, образующийся в процессе реакции сероводород расходуется на осернение катализатора и формирование мелкодисперсных частиц сульфидов переходных металлов. Время активации 2 ч, скорость потока газовой смеси 80 л/ч. В процессе активирования по данным РФА не наблюдается формирование окристаллизованных фаз сульфидов переходных металлов, мелкодисперсные окристаллизованные частицы с параметрами решетки CuS и CuCr2S4 наблюдаются методом рентгеновской дифракции. Содержание серы, определенное рентгеноспектральным флуоресцентным методом, составляет 2,8 мас.%. Суммарное содержание сульфидов составляет 7 мас.%, из них CuCr2S4 4,7; CuS 2,3. Содержание, мас.%: CuCr2O4 5,7; СеО2 12,3; оксид алюминия - остальное.
Через 2 ч подают реакционную газовую смесь, имеющую состав, об.%: SO2 28, СО 18 и H2 54 (аналогично примеру 1). При 1630 ч-1 катализатор обеспечивает конверсию SO2 на уровне 90% при температуре 300°С и 99,5% при 400-600°С; выход серы составляет 80% при 300°С и 92-99% при 400-600°С; максимальный выход COS достигается при 300°С и составляет 2%, при 400°С и более высоких температурах образования COS и H2S не наблюдается.
Пример 9 (сравнительный).
Аналогичен примеру 2, отличие заключается в том, что катализатор испытывают без предварительной активации. Содержание Cu, Cr и Се по данным АЭС-ИСП составляет 4,2; 7,8 и 12 мас.% соответственно или 15,4 мас.% в расчете на CuCr2O4 и 1,3 мас.% в расчете на Cr2О3. Оксид алюминия - остальное. Церий входит в состав катализатора в виде оксида СеО2.
При условиях, указанных в примере 1, катализатор обеспечивает конверсию SO2 на уровне 99% при 450°С, выход серы на уровне 92-94% в интервале температур 400-500°С, помимо серы при 300°С в продуктах реакции фиксируется COS (YCOS=4%).
Пример 10-13.
Аналогичны примеру 1, отличие заключается в том, что для приготовления катализатора используют смешанный раствор бихромата меди и кобальта (или железа, или никеля). Катализатор содержит 18-21 мас.% Cu1-xMxCr2O4, где М - катион кобальта, железа или никеля; соотношение М/Сu составляет 0,05-0,50.
Активирование катализатора проводят по способу 2. Суммарное содержание сульфидов переходных металлов составляет 4,9-15,7 мас.%, из них CuCr2S4 4,5-4,9; индивидуальные сульфиды переходных металлов - остальное. Носитель - остальное. Химический состав и каталитические характеристики приведены в таблице 2.
При условиях, аналогичных примеру 1, катализатор обеспечивает в зависимости от природы катиона М (Со, Fe, Ni) конверсию SO2 на уровне 89-99% при 320°С, выход серы 75-85% при 300-350°С, карбоксида серы - не более 3% при 300°С и выход H2S не фиксируется при 300-600°С.
Из приведенных примеров 1-8 и 10-13 видно, что заявляемые составы катализаторов, содержащие в качестве соединения переходного металла сульфид Cu1-xMxCr2S4+δ или смесь индивидуальных сульфидов CuS, Cr2S3 MS1+δ, получающиеся в результате пропускания сероводорода над нанесенным на носитель оксидом состава Cu1-xMxCr2O4 со структурой шпинели, где М - катион переходного металла (Fe, Со, Ni), обеспечивают конверсию диоксида серы на уровне не ниже 75% и выход элементарной серы на уровне не ниже 68% уже при температуре 300-350°С из газовых смесей, содержащих до 33 об.% SO2. Оптимальный состав заявляемых катализаторов определяется требованиями технологического процесса восстановления диоксида серы из промышленных газов: температура и степень очистки. Катализатор может иметь различную геометрическую форму: сферические гранулы, черенки, кольца, блоки сотовой структуры.
Из примеров 2 и 9 (таблица 1) видно, что активирование катализатора путем пропускания сероводорода над нанесенным на носитель оксидом состава
Cu1-xMxCr2O4 со структурой шпинели (оксидная форма катализатора) приводит к существенному улучшению каталитических свойств, основным их которых является существенное снижение температуры процесса. При одинаковом составе и содержании оксида состава Cu1-xMxCr2O4 со структурой шпинели активирование приводит к снижению температуры 90%-ной конверсии с 450°С (пример 9) до 350°С (пример 2). Из примеров 2-8 видно, что способ активирования в сероводород содержащей смеси (сероводород, диметилдисульфид или смесь диоксида серы с водородом) оказывает незначительное влияние на каталитические характеристики. Предпочтительным с технологической точки зрения является активирование в смеси диоксида серы с водородом при температуре 300-450°С, образующийся в процессе реакции сероводород расходуется на осернение катализатора.
Из данных таблицы 1 видно, что степень превращения диоксида серы и выход серы возрастают с увеличением содержания сульфида Cu1-xMxCr2S4+δ или смеси индивидуальных сульфидов CuS, Cr2S3 MS1+δ, которые формируются при пропускании газовых смесей, содержащих сероводород, над нанесенным на носитель оксидом состава Cu1-xMxCr2O4 со структурой шпинели. Т.е. эти характеристики возрастают с увеличением содержания оксида CuCr2O4 до 15-20 мас.% и практически не изменяются при более высоких содержаниях. Метод формирования оксида состава Cu1-xMxCr2O4 со структурой шпинели не оказывает значительного влияния на каталитические характеристики (примеры 2 и 8). При температуре 300-350°С катализаторы обеспечивают конверсию диоксида серы на уровне 80-90%, выход серы составляет 78-82%. Максимальное образование COS наблюдается при температуре 300°С и существенно снижается при температурах выше 300°С.
Из примеров 1 и 2 (таблица 1) видно, что приготовление катализатора на пористом алюмооксидном носителе, модифицированном добавками оксидов РЗЭ, в основном церия, обеспечивает незначительное улучшение каталитических характеристик, а именно увеличение конверсии диоксида серы и выхода элементарной серы.
Из данных таблицы 2 видно, что введение второго катиона в шпинель (примеры 10-13) позволяет варьировать оптимальную рабочую температуру при эксплуатации катализатора без существенного снижения каталитических характеристик (конверсии диоксида серы и селективности по сере). Это позволяет снизить экзотермический эффект реакции и тем самым контролировать перегрев катализатора.
Преимуществом предлагаемых составов катализатора является их высокая активность и селективность при различном составе восстановительной смеси, в качестве которой могут быть использованы синтез-газ с соотношением Н2/СО,
1) равным 3 и характерным для парового риформинга метана (Н2/СО=3);
2) равным 2 и характерным для парциального окисления метана (Н2/СО=2);
3) равным 1 и характерным для паровой конверсии углей (Н2/СО=1).
Это иллюстрируется примерами 14-17 (таблица 3).
Пример 14. Состав оксидной формы катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм.
Катализатор активирован по способу 3, согласно которому сероводород образуется в результате реакции диоксида серы с водородом в условиях, аналогичных примеру 8. Для этого образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм и подают смесь диоксида серы и водорода (10 об.% SO2). При температуре 450°С проводят осернение катализатора и формирование мелкодисперсных частиц сульфидов переходных металлов. Время активации 2 ч, скорость потока газовой смеси 80 л/ч. Охлаждают реактор до температуры 200°С.
Отличие составляет условия испытаний образца катализатора.
Далее проводят испытание катализатора. Для этого на катализатор со скоростью 124 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 32,0; СО 16,0 и Н2 48,0 (СО/Н2=1/3), азот - остальное. Поднимают температуру на обмотке печи до 400°С, при этом температура в слое катализатора составляет 620°С, проводят хроматографический анализ газовой смеси. Разница между температурой в слое катализатора и в печи указывает на выделение тепла в результате экзотермической реакции.
Катализатор при температуре 400/620°С обеспечивает конверсию SO2 на уровне 98%, выход серы составляет 93%, в продуктах реакции не фиксирует COS и H2S.
Пример 15. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм.
Катализатор активирован по способу 3 в условиях, аналогичных примеру 14.
Отличие составляют условия испытаний образца катализатора. Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 124 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 7,9 и Н2 23,7 (СО/Н2=1/3), азот - остальное. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 505°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 400/505°С обеспечивает конверсию SO2 на уровне 94%, выход серы составляет 93%, в продуктах реакции не фиксируется COS и H2S.
Пример 16. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму цилиндров диаметром 4-5 мм и длиной 4-5 мм.
Катализатор активирован по способу 2, согласно которому сероводород образуется в результате реакции разложения диметилдисульфида в условиях, аналогичных примеру 5. Для этого образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм, со скоростью 40 л/ч подают смесь диметилдисульфида (5 об.%) в водороде, нагревают реактор до температуры 320°С и проводят осернение в течение 3 часов.
Далее проводят испытание катализатора. Со скоростью 115 л/ч (объемная скорость 525 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 10,5 и Н2 21,0 (СО/Н2=1/2), азот - остальное. Поднимают температуру на обмотке печи до 450°С, при этом температура в печи составляет 575°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 450/575°С обеспечивает конверсию SO2 на уровне 70%, выход серы составляет 68%, в продуктах реакции фиксируется COS и H2S в количестве не более 0,6 об.%.
Пример 17. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм.
Катализатор активируют в условиях, аналогичных примеру 16.
Отличие составляет условия испытаний образца катализатора.
Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 115 л/ч (объемная скорость 525 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8 ; СО 15,8 и Н2 15,8 (СО/Н2=1/1), азот - остальное. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 550°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 400/550°С обеспечивает конверсию SO2 на уровне 95%, выход серы составляет 95%, в продуктах реакции не фиксируется COS и H2S.
Пример 18. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Катализатор активируют в условиях, аналогичных примеру 14.
Условия испытаний катализатора аналогичны таковым из примера 17, отличие заключается в том, что газовую смесь подают на катализатор со скоростью 315 л/ч, т.е. объемная скорость потока составляет 1430 ч-1. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 650°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 400/650°С обеспечивает конверсию SO2 на уровне 80%, выход серы составляет 79%, в продуктах реакции не фиксируется COS и H2S.
Пример 19. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Катализатор предварительно активируют в условиях, аналогичных примеру 14.
Условия испытаний катализатора аналогичны таковым из примера 17, отличие заключается в том, что газовую смесь подают на катализатор со скоростью 1100 л/ч, т.е. объемная скорость потока составляет 5000 ч-1. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 420°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 400/420°С обеспечивает конверсию SO2 на уровне 60%, выход серы составляет 54%, в продуктах реакции не фиксируется COS и H2S.
Пример 20. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Катализатор предварительно активируют в условиях, аналогичных примеру 14.
Условия испытаний катализатора аналогичны таковым из примера 18, отличие заключается в составе газовой смеси, а именно в нее добавляют пары воды в количестве 2,3 об.%. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 650°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 400/650°С обеспечивает конверсию SO2 на уровне 85%, выход серы составляет 85%, в продуктах реакции не фиксируется COS и H2S.
Пример 21 (сравнительный).
Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм.
Отличие заключается в том, что образец не активируют (с помощью пропускания сероводорода над катализатором) перед измерением активности.
Условия испытаний образца катализатора аналогичны таковым их примера 15.
Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 124 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 7,9 и Н2 23,7 (СО/Н2=1/3), азот - остальное. Поднимают температуру на обмотке печи до 600°С, при этом температура в печи составляет 650°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 600/650°С обеспечивает конверсию SO2 на уровне 70%, выход серы составляет 70%, в продуктах реакции фиксируется образование COS в количестве не более 0,6 об.%.
Пример 21 (сравнительный). Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Условия активирования катализатора аналогичны таковым из примера 14.
Отличие заключается в условиях тестирования, а именно соотношение SО2/восстановитель отличается от стехиометрического значения (1/2, α=1).
Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 115 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 5,2, Н2 15,8 (СО/Н2=1/3, α=0,67), азот - остальное. Поднимают температуру на обмотке печи до 450°С, при этом температура в печи составляет 520°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 520/450°С обеспечивает конверсию SO2 на уровне 60%, выход серы составляет 52%, в продуктах реакции не фиксируется образование COS и H2S.
Пример 22. Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Активирование катализатора аналогично условиям примера 14.
Отличие заключается в условиях тестирования, а именно соотношение SO2/восстановитель отличается от стехиометрического значения (1/2, α=1).
Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 115 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 5,2, Н2 15,8 (СО/Н2=1/3, α=1,26), азот - остальное. Поднимают температуру на обмотке печи до 450°С, при этом температура в печи составляет 590°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 590/450°С обеспечивает конверсию SO2 на уровне 94%, выход серы составляет 93%, в продуктах реакции не фиксируется образование COS и H2S.
Пример 33 (сравнительный). Состав катализатора аналогичен примеру 2. Содержание Cu, Cr и Се составляет 4,2; 7,8 и 12 соответственно. Катализатор имеет форму сферических гранул диаметром 4-5 мм. Активирование катализатора аналогично таковым из примера 14.
Отличие заключается в условиях тестирования, а именно соотношение SО2/восстановитель отличается от стехиометрического значения (1/2, α=1).
Образец в количестве 220 см3 загружают в проточный реактор диаметром 60 мм. Со скоростью 115 л/ч (объемная скорость 565 ч-1) подают реакционную смесь, содержащую, об.%: SO2 15,8; СО 17,9, Н2 53,8 (СО/Н2=1/3, α=2,2), азот - остальное. Поднимают температуру на обмотке печи до 400°С, при этом температура в печи составляет 770°С, проводят хроматографический анализ газовой смеси.
Катализатор при температуре 770/400°С обеспечивает конверсию SO2 на уровне 99%, выход серы составляет 62%, в продуктах реакции фиксируется образование H2S в количестве 9 об.% на сухой газ.
Из примеров 14 и 15 видно, что разбавление реакционной газовой смеси позволяет снизить перегрев реактора, на что указывает пропорциональное снижение разницы температур между горячей точкой в реакторе и температурой задания на обмотке печи при разбавлении реакционной газовой смеси в 2 раза. Разбавление газовой смеси не оказывает влияния на конверсию диоксида серы и выход серы. Технически это позволяет упростить конструкцию реактора (исключить теплообменники), без изменения эффективности процесса и выхода серы.
Из примеров 15-17 видно, что использование в качестве восстановителя синтез-газа с соотношением монооксида углерода и водорода в пределах от 1/1 до 1/3 позволяет проводить процесс восстановления диоксида серы при температурах 300-600°С, при этом варьирование содержания монооксида углерода позволяет регулировать количество выделяющего тепла и выход серы. При соотношении СО и
Н2, равном 1:1, процесс при 525 ч-1 устойчиво «зажигается» при температуре 230°С, в то время как при соотношении СО и Н2, равном 1:3, «зажигание» происходит при температуре выше 270°С.
Из примеров 17-19 видно, что процесс восстановления диоксида серы на заявляемых катализаторах имеет удовлетворительные характеристики при скоростях потока до 5000 ч-1, в том числе в присутствии паров воды, хотя с увеличением скорости потока и наблюдается снижение выхода серы.
Из примеров 21-23 видно, что предпочтительными являются использование катализатора и проведение процесса при соотношениях восстановитель/SO2, близких к стехиометрическому значению, (CO+H2)/SO2=2, т.е. α=1. Незначительное уменьшение или увеличение коэффициента избытка восстановителя от α=1 (например, до 1,26 в примере 22) не влияет на конверсию диоксида серы и селективность процесса к элементарной сере, выход серы составляет около 93% (см. примеры 15 и 22). В то время как значительное уменьшение коэффициента избытка восстановителя от α=1 (например, до 0,67 в примере 21) приводит к существенному снижению конверсии диоксида серы, с 94% (примеры 15, 22) до 52% (пример 21) и, следовательно, к снижению эффективности процесса очистки металлургических газов от диоксида серы. Значительное увеличение коэффициента избытка восстановителя от α=1 (например, до 2,2 в примере 23) приводит к существенному снижению селективности процесса по отношению к элементарной сере, например с 93% (примеры 15, 22) до 62% (пример 23), и, следовательно, к снижению степени извлечения элементарной серы. Снижение селективности процесса восстановления диоксида серы приводит к образованию побочных серосодержащих соединений, таких как сероводород и сульфид карбонила, что требует дополнительных стадий очистки.
Заявляемый процесс восстановления диоксида серы синтез-газом различного состава на заявляемых составах катализатора, содержащего в качестве соединения переходного металла сульфид Cu1-xMxCr2S4+δ или смесь индивидуальных сульфидов CuS, Cr2S3 MS1+δ, получающихся при пропускании сероводорода над нанесенным на носитель оксидом состава Cu1-xMxCr2O4 со структурой шпинели, имеет следующие преимущества:
1) процесс протекает при температурах 300°С с высокой эффективностью и селективностью по сере, что делает заявляемый процесс привлекательным с точки зрения энергосбережения;
2) при оптимальных условиях процесс восстановления диоксида серы синтез-газом обеспечивает высокие выходы серы, более 90%, что не требует последующих стадий извлечения серы.
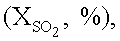 выхода серы (YS, %) и побочных продуктов реакции (YCOS,
выхода серы (YS, %) и побочных продуктов реакции (YCOS, 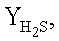 %) и температура их достижения
%) и температура их достижения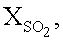 % (Т, °С)
% (Т, °С)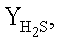 % (Т, °С)
% (Т, °С)
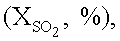 выхода серы (YS, %) и побочных продуктов реакции (YCOS,
выхода серы (YS, %) и побочных продуктов реакции (YCOS, 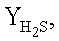 %) и температура их достижения
%) и температура их достижения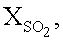 % (Т, °С)
% (Т, °С)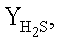 % (Т, °С)
% (Т, °С)
Горячая точка/задание
Расчет/по взвешиванию
α=1
α=1
α=0,67
α=1,26
α=2,20
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ОЧИСТКИ ГАЗОВЫХ ВЫБРОСОВ ОТ ДИОКСИДА СЕРЫ | 2008 |
|
RU2372986C1 |
| КАТАЛИЗАТОР И СПОСОБ ВОССТАНОВЛЕНИЯ ДИОКСИДА СЕРЫ | 2008 |
|
RU2369435C1 |
| СПОСОБ И КАТАЛИЗАТОР ДЛЯ ПРЯМОГО ОКИСЛЕНИЯ СЕРОВОДОРОДА ДО СЕРЫ | 1994 |
|
RU2107024C1 |
| КАТАЛИЗАТОР И СПОСОБ ГЛУБОКОЙ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ ОТ СЕРОВОДОРОДА В ЕГО ПРИСУТСТВИИ | 2008 |
|
RU2414298C2 |
| КАТАЛИЗАТОР (ВАРИАНТЫ) И СПОСОБ ВОССТАНОВЛЕНИЯ ДИОКСИДА СЕРЫ ИЗ СЕРОСОДЕРЖАЩИХ ГАЗОВ (ВАРИАНТЫ) | 2010 |
|
RU2445162C2 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРИГОДНАЯ ДЛЯ КАТАЛИТИЧЕСКОГО ВОССТАНОВЛЕНИЯ СЕРНИСТОГО СОЕДИНЕНИЯ, СОДЕРЖАЩЕГОСЯ В ГАЗОВОМ ПОТОКЕ, И СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ТАКОЙ КОМПОЗИЦИИ | 2008 |
|
RU2461424C2 |
| Каталитическая композиция на основе оксидных соединений титана и алюминия и ее применение | 2021 |
|
RU2775472C1 |
| РЕАКТИВИРОВАННЫЕ КАТАЛИЗАТОРЫ ГИДРООЧИСТКИ ДЛЯ ПРИМЕНЕНИЯ В СНИЖЕНИИ ВЫБРОСОВ СЕРЫ | 2020 |
|
RU2814491C2 |
| Катализатор гидрирования и гидролиза сернистых соединений в отходящих газах процесса Клауса и способ его применения | 2023 |
|
RU2812535C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА | 2008 |
|
RU2497588C2 |
Изобретение относится к области охраны окружающей среды, а именно к очистке отходящих газов предприятий цветной металлургии от диоксида серы с получением элементарной серы. Описан катализатор очистки газовых выбросов от диоксида серы в процессе восстановления диоксида серы до элементарной серы смесью монооксида углерода и водорода, включающий переходные металлы и носитель, в качестве соединения переходного металла он содержит сульфид
Cu1-xMxCr2S4+δ или смесь индивидуальных сульфидов CuS, Сr2S3 и MS1+δ количестве 2-20 мас.%, где М - переходный металл, выбранный из группы: Fe, Co, Ni, значения х и δ изменяются от 0-0,5, а в качестве носителя - оксид алюминия, в том числе модифицированный добавкой оксида церия, при следующем соотношении компонентов, мас.%: Cr 12, Сu 0,1-5,0, металл переходной группы 0,01-2,50, церий 1-15, оксид алюминия - остальное. Описан способ приготовления этого катализатора и его применение в процессе очистки газовых выбросов. Технический результат - процесс протекает при температурах 300°С с высокой эффективностью и селективностью по сере. 3 н. и 4 з.п. ф-лы, 3 табл.
1. Катализатор очистки газовых выбросов от диоксида серы в процессе восстановления диоксида серы до элементарной серы смесью монооксида углерода и водорода, включающий переходные металлы и носитель, отличающийся тем, что в качестве соединения переходного металла он содержит сульфид Сu1-xМхСr2S4+δ или смесь индивидуальных сульфидов CuS, Cr2S3 и MS1+δ в количестве 2-20 мас.%, где М - переходный металл, выбранный из группы: Fe, Co, Ni, значения х и δ изменяются от 0-0,5; а в качестве носителя - оксид алюминия, в том числе модифицированный добавкой оксида церия, при следующем соотношении компонентов, мас.%: Сr 3-12, Сu 0,1-5,0; металл переходной группы 0,01-2,50, церий 1-15, оксид алюминия -остальное.
2. Катализатор по п.1, отличающийся тем, что катализатор имеет форму сферических, кольцеобразных, цилиндрических гранул или блоков сотовой структуры.
3. Способ получения катализатора для восстановления диоксида серы до элементарной серы смесью монооксида углерода и водорода, включающий пропитку носителя растворами предшественника оксида, сушку и термообработку, отличающийся тем, что в качестве пропиточного раствора используют раствор бихроматов меди и/или переходного металла из группы Fe, Со, Ni; сушку проводят при температуре 70-120°С, а термообработку при 600-900°С в течение 3-4 ч для формирования шпинельной структуры, после чего проводят активирование катализатора при температуре 300-450°С в газовой смеси, содержащей сероводород, который содержится в ней изначально или образуется в результате протекания реакций; при этом получают катализатор, содержащий сульфид Cu1-xMxCr2S4+δ или смесь индивидуальных сульфидов CuS, Сr2S3 MS1+δ, в количестве 2-20 мас.%, где М - переходный металл, выбранный из группы: Fe, Co, Ni, значения х и δ изменяются от 0-0,5; а в качестве носителя - оксид алюминия, в том числе модифицированный добавкой оксида церия, при следующем соотношении компонентов, мас.%: Сr 3-12, Сu 0,1-5,0; металл переходной группы 0,01-2,50, церий 1-15, оксид алюминия - остальное.
4. Способ по п.3, отличающийся тем, что для активации катализатора используют органическое серосодержащее соединение в смеси с водородом или азотом, при этом сероводород образуется в результате разложения органического серосодержащего соединения, преимущественно диметилдисульфида.
5. Способ по п.3, отличающийся тем, что для активации катализатора используют сероводородсодержащую газовую смесь, образующуюся в результате восстановления диоксида серы, преимущественно в результате реакция восстановления диоксида серы водородом с соотношением водород/SО2=3-10.
6. Способ по п.3, отличающийся тем, что в смеси, используемой для активации катализатора, помимо сероводорода, присутствует газ-восстановитель, преимущественно водород или монооксид углерода.
7. Способ очистки газовых выбросов от диоксида серы в процессе восстановления диоксида серы до элементарной серы смесью монооксида углерода и водорода в присутствии катализатора, включающего в свой состав оксиды переходных металлов и носитель, отличающийся тем, что процесс используют для очистки промышленных газовых выбросов, содержащих 5-35 об.% диоксида серы, включая металлургические газы, процесс проводят при объемной скорости потока 500-5000 ч-1, соотношении восстановитель/SO2=1,8-2,25 и температуре 350-550°С, в качестве восстановителя используют смесь монооксида углерода и водорода с соотношением СО/Н2 в пределах 1/1-1/3, а в качестве катализатора используют катализатор по п.1.
| US 5494879 A, 27.02.1996 | |||
| US 4147763 A, 03.04.1979 | |||
| СПОСОБ ОЧИСТКИ ГАЗА ОТ ДИОКСИДА СЕРЫ | 1993 |
|
RU2088313C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТНОЙ СЕРЫ ИЗ ОТХОДЯЩИХ ГАЗОВ, СОДЕРЖАЩИХ ДИОКСИД СЕРЫ | 2002 |
|
RU2221742C2 |
| NL 7413164 A, 09.04.1976 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
Авторы
Даты
2009-10-10—Публикация
2008-08-14—Подача