Настоящее изобретение относится к конъюгатам гидроксиалкилкрахмала и белка фактора, стимулирующего колонии гранулоцитов (G-CSF), причем указанные конъюгаты образованы ковалентным связыванием между гидроксиалкилкрахмалом или производным гидроксиалкилкрахмала и белком. Настоящее изобретение также относится к способу получения этих конъюгатов и к применению этих конъюгатов.
В целом принято, что устойчивость белков можно улучшить и иммунный ответ против этих белков уменьшить, когда эти белки соединяются с полимерными молекулами. В документе WO 94/28024 описано, что физиологически активные белки, модифицированные полиэтиленгликолем (PEG), проявляют сниженную иммуногенность и антигенность и циркулируют в потоке крови значительно дольше, чем неконъюгированные белки, т.е. имеют сниженную скорость клиренса.
G-CSF представляет собой гликопротеид с молекулярной массой 21 кДа, стабилизированный двумя внутрицепочечными дисульфидными связями и содержащий одну связанную с О углеводородную часть. Зрелый G-CSF имеет 174 аминокислоты. В организме животного G-CSF синтезируется стромальными клетками костного мозга, макрофагами и фибробластами. Его основная функция заключается в том, что он представляет собой фактор роста и дифференциации для нейтрофилов и их клеток-предшественников. Однако в данной области также известно, что G-CSF активирует зрелые нейтрофилы. Кроме того, он стимулирует рост/дифференциацию различных других гематопоэтических клеток-предшественников (в синергии с дополнительными гематопоэтическими ростовыми факторами) и содействует пролиферации и миграции эндотелиальных клеток. Клинически G-CSF вводится для лечения недостаточности уровней нейтрофилов (вызванных, например, апластической анемией, миелодисплазией, СПИДом или химиотерапией).
В документе WO 02/09766, наряду с другими соединениями, описываются биологически совместимые белково-полимерные соединения, которые получают коньюгацией биологически активного белка с биологически совместимым полимерным производным. Используемые биологически совместимые полимеры представляют собой высоко реакционноспособные разветвленные полимеры, и полученные конъюгаты содержат длинный линкер между полимерным производным и белком. В качестве биологически совместимых полимеров описаны полимеры формулы (P-OCH2CO-NH-CHR-CO-)n-L-Qk-A, где P и Q представляют собой полимерные остатки, а k может быть равна 1 или 0. Для P и Q упоминаются полиэтиленгликоль, полипропиленгликоль, полиоксиэтилен, политриметиленгликоль, полимолочная кислота и ее производные, полиакриловая кислота и ее производные, полиаминокислота, полифиниловый спирт, полиуретан, полифосфазен, поли(L-лизин), полиалкиленоксид, полиакриламид и растворимые в воде полимеры, такие как декстран или полисахарид. В качестве белков, среди других, упоминаются альфа, бета и гамма интерфероны, факторы крови, цитокины, такие как интерлейкины, G-CSF, GM-CSF. В примерах документа WO 02/09766 раскрыты только производные моно-, ди- и три-полиэтиленгликоля, которые соединены исключительно с интерфероном и эпидермальным ростовым фактором и человеческим гормоном роста.
В документе WO 94/01483 описаны конъюгаты биологически совместимого полимера, которые образованы ковалентным связыванием биологически неактивного полимера или полимерного производного с фармацевтически чистым, синтетическим гидрофильным полимером посредством определенных типов химических связей. В качестве природных полимеров и их производных раскрываются полисахариды, такие как гиалуроновая кислота, протеогликаны, такие как хондроитинсульфаты А, В и С, хитин, гепарин, гепаринсульфат, декстраны, такие как циклодекстран, гидроксиэтилцеллюлоза, простой эфир целлюлозы и крахмала, липиды, такие как триглицериды и фосфолипиды. В качестве синтетических полимеров, наряду с другими, описаны полиэтилен и его производные, имеющие среднюю молекулярную массу от примерно 100 до примерно 100000. В качестве белков, связанных с полимером или полимерным производным, описаны цитокины и ростовые факторы, включая раскрытые интерфероны, факторы опухолевого некроза, интерлейкины, колониестимулирующие факторы, ростовые факторы, такие как экстракт остеогенного фактора, эпидермальный ростовой фактор, трансформирующий ростовой фактор, полученный из тромбоцитов ростовой фактор, кислотный фактор роста фибробластов и другие. Во всех рабочих примерах документа WO 94/01483 в качестве полимера используются производные полиэтиленгликолей.
В документе WO 96/11953 раскрыты химически модифицированные на N-конце белковые соединения и способы их получения. В частности, описаны композиции G-CSF, которые получены в результате присоединения растворимого в воде полимера по N-концу G-CSF. В контексте документа WO 96/11953 раскрыт также рекомбинантный интерферон типа 1, соединенный по N-концу с растворимыми в воде полимерами. Хотя в документе WO 96/11953 перечислено широкое разнообразие растворимых в воде полимеров (например, сополимеры этиленгликоля и пропиленгликоля, карбоксиметилцеллюлоза, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена/малеинового ангидрида, полиаминокислоты (или гомополимеры, или случайные сополимеры), поли(н-винилпирролидон)полиэтиленгликоль, гомополимеры полипропиленгликоля, сополимеры полипропиленоксида/этиленоксида или полиоксиэтилированные полиолы), в рабочих примерах документа WO 96/11953 описаны только композиции соединенного с PEG G-CSF или рекомбинантного IFN (интерферона) типа 1.
В патенте США № 6555660 В2 раскрыты полипептидные конъюгаты, включающие полипептид, проявляющий активность G-CSF и имеющий аминокислотную последовательность, которая отличается от аминокислотной последовательности, в которой конъюгат включает группу присоединения для не полипептидной части и, кроме того, включает, по меньшей мере, одну не полипептидную часть, присоединенную к группе присоединения полипептида. Не полипептидная часть может представлять собой полимер, такой как полиэтиленгликоль или олигосахарид. В патенте США № 6555660 В2 ясно и однозначно указано, что PEG пока является самой предпочтительной полимерной молекулой, поскольку у него есть лишь несколько реакционноспособных групп, способных к перекрестной сшивке, по сравнению с полисахаридами, такими как декстран.
В документе WO 97/30148 описываются полипептидные конъюгаты со сниженной аллергенностью, включающие молекулы полимерного носителя, имеющего 2 или более полипептидных молекул, связанных с ним. Эти конъюгаты представляют собой предпочтительно часть композиций, используемых на рынке продуктов для ухода. Указанные конъюгаты получают активацией молекулы полимерного носителя, взаимодействием двух или более полипептидных молекул с активированной молекулой полимерного носителя и блокировкой остаточных активных групп на конъюгате. В качестве молекулы полимерного носителя в документе WO 97/30148 перечислено их многочисленное разнообразие, включая такие различные группы соединений как натуральные или синтетические гомополимеры, такие как полиолы, полиамины, поликарбоновые кислоты и гетерополимеры, включающие, по меньшей мере, 2 различные группы присоединения. Приведены примеры, которые включают прямые PEG, разветвленные PEG, поливиниловые спирты, поликарбоксилаты, поливинилпирролидоны и поли-D,L-аминокислоты. Среди других соединений описаны также декстраны, такие как карбоксиметилдекстран, целлюлозы, такие как гидроксиэтилцеллюлоза или гидроксипропилцеллюлоза, гидролизаты хитосана, крахмалы, такие как гидроксиэтилкрахмалы или гидроксипропилкрахмалы, гликоген, агароза, гуаровая смола, инулин, пуллулан, ксантановая смола, каррагинин, пектин, альгиновая кислота и т.д. В качестве полипептидов ясно раскрыты только некоторые ферменты.
Baldwin, J.E. et al., Tetrahedron, vol. 27 (1981), pp. 1723-1726 описывают химическую модификацию декстрана и гидроксиэтилкрахмала для получения замещенных альдегидом полимеров, которые могут взаимодействовать с гемоглобином с получением растворимых, связанных с полимером гемоглобинов. Было показано, что они способны связывать кислород, но эксперименты с перфузией сердца ясно показали, что связанные с полимером гемоглобины не подходили для использования в качестве заменителей крови.
В документе WO 99/49897 описаны конъюгаты гемоглобина, образованные взаимодействием полисахаридов, таких как декстран или гидроксиэтилкрахмал, с аминогруппами гемоглобина. В качестве функциональных групп полисахарида используются альдегидные группы, полученные окислительным раскрытием сахаридного кольца. В качестве предпочтительного восстанавливающего агента раскрыт боран диметиламина. Более того, документ WO 99/49897 исключительно ограничен гемоглобином.
Документ WO 03/074087 относится к способу сочетания белков с полученным из крахмала модифицированным полисахаридом. Гидроксиалкилкрахмал, который оказывает соединяющее действие между белком и полисахаридом, представляет собой ковалентную связь, которая образована между концевой альдегидной группой или функциональной группой, полученной в результате химической модификации указанной концевой альдегидной группой молекулы гидроксиалкилкрахмал, и функциональной группой белка. В качестве реакционноспособной группы белка раскрыты тиогруппы и карбоксильные группы, а альдегидные группы белка не упомянуты. Более того, хотя приведено многочисленное разнообразие возможностей различных связей в виде многих перечней, включающих различные функциональные группы, теоретически подходящие различные линкерные молекулы и различные химические методики, рабочие примеры описывают только 2 альтернативы: во-первых, используется окисленный гидроксиэтилкрахмал и соединяется непосредственно с белками, используя активацию этилдиметиламинопропилкарбодиимидом (EDC), или используется неокисленный гидроксиэтилкрахмал и соединяется непосредственно с белком, образующим основание Шиффа, которое в последующем восстанавливается в соответствующий амин. Так, рабочие примеры документа WO 03/074087 не раскрывают индивидуальный конъюгат, соединенный через тиогруппу или карбоксигруппу белка, и не описывают конъюгат, включающий гидроксиэтилкрахмал, белок и одну или несколько линкерных молекул. Кроме того, в рабочих экспериментах не используется молекула G-CSF.
Поэтому целью настоящего изобретения является предоставление конъюгатов гидроксиалкилкрахмала, предпочтительно гидроксиэтилкрахмала, и G-CSF, которые еще не описаны в предшествующем уровне техники.
Еще одной целью настоящего исследования является предоставление способов получения этих конъюгатов.
Поэтому настоящее изобретение относится к способу получения конъюгата, включающего белок и полимер или его производное, причем полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), причем способ включает взаимодействие, по меньшей мере, одной функциональной группы А полимера или его производного, по меньшей мере, с одной функциональной группой Z белка и посредством этого образуя ковалентную связь, где Z выбрана из группы, состоящей из аминогруппы, тиоловой группы, альдегидной группы и кетогруппы, и
- где, в случае, если Z представляет собой альдегидную группу или кетогруппу, то А включает аминогруппу, образующую указанное соединение с Z, или
- где, в случае, если Z представляет собой аминогруппу, то А выбрана из группы, состоящей из реакционноспособной карбоксигруппы и альдегидной группы, кетогруппы или полуацетальной группы,
-- где, в случае, если А представляет собой альдегидную группу, кетогруппу или полуацетальную группу, то способ, кроме того, включает введение А в полимер для получения производного полимера,
--- взаимодействием полимера, по меньшей мере, с бифункциональным соединением, одна функциональная группа которого взаимодействует с полимером и, по меньшей мере, одной другой функциональной группой из которых является альдегидная группа, кетогруппа или полуацетальная группа, или представляет собой функциональную группу, которая, кроме того, химически модифицирована для получения альдегидной группы, кетогруппы или полуацетальной группы, или
--- окислением полимера для получения, по меньшей мере, одной, в частности, по меньшей мере, двух альдегидных групп, или
-- где, в случае, если А представляет собой реакционноспособную карбоксигруппу, способ, кроме того, включает введение А в полимер для получения производного полимера,
--- селективным окислением полимера на его восстанавливающем конце и активацией полученной карбоксигруппы, или
--- взаимодействием полимера по его неокисленному восстанавливающемуся концу со сложным карбоновым эфиром, или
- где в случае, если Z представляет собой тиоловую группу, то А включает
-- малеимидогруппу или
-- галогенацетильную группу,
образуя указанную связь с Z.
Соответственно, настоящее изобретение также относится к конъюгату, который можно получить описанным выше способом.
G-CSF можно получить химическими синтетическими способами, или он может быть получен из любого человеческого (см., например, Burgess, A.W. et al. 1977, Stimulation by human placental conditioned medium of hemopoietic colony formation by human marrow cells. Blood 49 (1977), 573-583; Shah, R.G. et al. 1977, Characterization of colony-stimulating activity produced by human monocytes and phytohemagglutinin-stimulated lymphocytes, Blood 50 (1977), 811) или из другого источника-млекопитающего, и его можно получить очисткой из природных источников, подобных плаценте человека, крови человека или мочи человека. Кроме того, множество эпителиальных карцином, клеток острого миелолейкоза и различных линий опухолевых клеток (карцином мочевого пузыря, медуллобластом) способны экспрессировать этот фактор.
Кроме того, экспрессия G-CSF охватывает также вариант G-CSF, в котором одна или несколько аминокислот (например, от 1 до 25, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, наиболее предпочтительно 1 или 2) были заменены другой аминокислотой, которая проявляет активность G-CSF (см., например, Riedhaar-Olson, J.F. et al. 1996, Identification of residues critical to the activity of human granulocyte colony-stimulating factor, Biochemistry 35:9034-9041 1996; патенты США 5581476; 5214132; 5362853; 4904584). Измерение активности G-CSF описано в данной области (измерение активности G-CSF in vitro см., например, Shirafuji, N. et al.1989, A new bioassay for human granulocyte colony-stimulating factor (hG-CSF) using murine myeloblastic NFS-60 cells as targets and estimation of its levels in sera from normal healthy persons and patients with infectious and hematological disorders, Exp. Hematol. 1989, 17, 116-119; измерение активности G-CSF in vivo см., например, Tanaka, H. et al. 1991, Pharmacokinetics of recombinant human granulocyte colony-stimulating factor conjugated to polyethylene glycol in rats, Cancer Research 51, 3710-3714, 1991). Другие публикации, где описаны тесты измерения активности G-CSF, представляют собой патент США № 6555660; Nohynek, G.J. et al.1997, Comparison of the potency of glycosylated and nonglycosylated recombinant human granulocyte colony-stimulating factors in neutropenic and nonneutropenic CD rats, Cancer Chemother Pharmacol (1997) 39; 259-266.
Предпочтительно G-CSF получен рекомбинантно. Это включает экспрессию последовательностей экзогенной ДНК прокариотического или эукариотического хозяина, полученных геномным или цДНК клонированием или синтезом ДНК. Подходящие прокариотические хозяева включают различные бактерии, такие как E. coli. Подходящие эукариотические хозяева включают дрожжи, такие как S. cerevisiae, и клетки млекопитающих, такие как клетки яичников китайского хомячка и клетки обезьян.
Рекомбинантное получение белка известно в данной области. В целом, это включает трансфекцию клеток хозяина соответствующим вектором экспрессии, культивацию клеток хозяина в условиях, которые обеспечивают возможность получения белка и очистки белка из клеток хозяина. Подробную информацию можно найти, например, в публикациях Souza, L. M. et al. 1986, Recombinant human granulocyte colony-stimulating factor: effects on normal and leukemic myeloid cells, Science 1986 232:61-65, 1986; Nagata, S. et.al. 1986, Molecular cloning and expression of cDNA for human granulocyte colony-stimulating factor, Nature 319:415-418, 1986; Komatsu, Y. et al. 1987, Cloning of granulocyte colony-stimulating factor cDNA from human macrophages and its expression in Escherichia coli, Jpn J Cancer Res. 1987 78(11):1179-1181.
В предпочтительном варианте осуществления G-CSF имеет аминокислотную последовательность человеческого зрелого G-CSF
(см., например, Nagata, S. et. al. 1986. Molecular cloning and expression of cDNA for human granulocyte colony-stimulating factor. Nature 319:415-418, 1986) и может, кроме того, содержать метионин на его амино-конце, который затем приводит к получению белка из 175 аминокислот. Кроме того, вместо метионина G-CSF может содержать сериновый или треониновый остаток.
G-CSF, используемый в способах настоящего изобретения, и конъюгаты в соответствии с настоящим изобретением могут включать одну углеводородную боковую цепь, присоединенную к G-CSF посредством связанного с О гликозилирования в положении Thr 133, т.е. G-CSF гликозилирован (V. Gervais et al., Eur. J. Biochem. 1997, 247, 386-395). Структура углеводородной боковой цепи может представлять собой NeuNAc(альфа2-3)Gal(бета-3)[NeuNAc(альфа2-6)]GalNAc и (альфа2-3)Gal(бета1-3)GalNAc (NeuNAc=N-ацетилнейраминовая кислота, GalNAc = N-ацетилгалактозамин).
Была предложена модификация G-CSF и других полипептидов с тем, чтобы ввести, по меньшей мере, одну дополнительную углеводородную цепь, по сравнению с нативным полипептидом (патент США № 5218092). В зависимости от используемого хозяина продукт экспрессии G-CSF может быть гликозилирован углеводородами млекопитающих или другими эукариотическими углеводородами. Обычно, когда G-CSF получают в эукариотических клетках, белок гликозилируется после трансляции. Следовательно, углеводородная боковая цепь может быть присоединена к G-CSF во время биосинтеза в клетках млекопитающего, особенно человека, насекомого или дрожжей.
Рекомбинантный человеческий G-CSF (rhG-CSF) в целом используется для лечения различных форм лейкопении. Так, в продаже препараты G-CSF имеются под названиями филграстим (Gran® и Neupogen®), ленограстим (Neutrogin® и Granocyte®) и нартограстим (Neu-up®). Gran® и Neupogen® являются негликозилированными и получены в рекомбинантных клетках E.coli. Neutrogin® и Granocyte® являются гликозилированными и получены в рекомбинантных клетках СНО и Neu-up® является негликозилированным с пятью аминокислотами, замещенными в N-концевой области интактного rhG-CSF, полученного в рекомбинантных клетках E.coli.
В качестве гликозилированного белка может использоваться любой гликозилированный G-CSF, такой как Granocyte®. В качестве не гликозилированного белка может использоваться любой негликозилированный G-CSF, такой как Neupogen® в способах и конъюгатах в соответствии с настоящим изобретением.
Кроме того, в положении -1 G-CSF может содержать метиониновый аминокислотный остаток, сериновый остаток или треониновый остаток.
В контексте настоящего изобретения термин «гидроксиалкилкрахмал» (HAS) относится к производному крахмала, которое было замещено, по меньшей мере, одной гидроксиалкильной группой. Предпочтительный гидроксиалкилкрахмал настоящего изобретения имеет строение в соответствии с формулой (I)
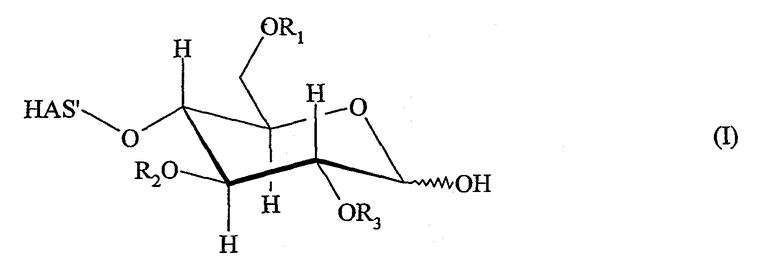
где восстанавливающий конец молекулы крахмала показан в неокисленной форме, а концевое сахаридное звено показано в ацетальной форме, который, в зависимости, например, от растворителя, может быть в равновесии с альдегидной формой.
Термин «гидроксиалкилкрахмал», используемый в настоящем изобретении, не ограничивается соединениями, где концевая углеводородная часть включает гидроксиалкильные группы R1, R2 и/или R3, как изображено для краткости в формуле (I), но также относится к соединениям, в которых, по меньшей мере, одна гидроксигруппа, которая присутствует или в концевой углеводородной части, и/или в остающейся части молекулы крахмала HAS', замещена гидроксиалкильной группой R1, R2 и/или R3.
Возможен также гидроксиалкилкрахмал, включающий две или более различные гидроксиалкильные группы.
По меньшей мере, одна гидроксиалкильная группа, включенная в HAS, может содержать две или более гидроксигруппы. В соответствии с предпочтительным вариантом осуществления, по меньшей мере, одна гидроксиалкильная группа, включенная в HAS, содержит одну гидроксигруппу.
Выражение «гидроксиалкилкрахмал» также включает производные, в которых алкильная группа является моно- или полизамещенной. В этом контексте предпочтительно, чтобы алкильная группа была замещена галогеном, особенно фтором. Или арильной группой. Кроме того, гидроксигруппа гидроксиалкильной группы может быть превращена в сложный или в простой эфир.
Кроме того, вместо алкила можно использовать линейные или разветвленные замещенные или незамещенные алкеновые группы.
Гидроксиалкилкрахмал представляет собой эфирное производное крахмала. Кроме указанных эфирных производных, также другие производные крахмала можно использовать в контексте настоящего изобретения. Например, могут использоваться производные, которые включают этерифицированные гидроксигруппы. Эти производные могут, например, представлять собой производные незамещенных моно- или дикарбоновых кислот с 2-12 атомами углерода или их замещенных производных. Особенно полезными являются производные незамещенных монокарбоновых кислот с 2-6 атомами углерода, особенно производные уксусной кислоты. В этом контексте предпочтительны ацетилкрахмал, бутилкрахмал и пропилкрахмал.
Кроме того, предпочтительны производные незамещенных дикарбоновых кислот с 2-6 атомами углерода.
В случае производных дикарбоновых кислот полезно, чтобы вторая карбоксигруппа дикарбоновой кислоты была также этерифицирована. Кроме того, производные сложных моноалкиловых эфиров дикарбоновых кислот также подходят в контексте настоящего изобретения.
Для замещенных моно- или дикарбоновых кислот замещающие группы могут быть предпочтительно такими же, как указано выше для замещенных алкильных остатков.
Методики этерификации крахмала известны в данной области (см., например, (Klemm D. et al, Comprehensive Cellulose Chemistry Vol. 2, 1998, Whiley-VCH, Weinheim, New York, в частности, глава 4.4, Esterification of Cellulose (ISBN 3-527-29489-9).
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, используется гидроксиалкилкрахмал в соответствии с формулой (I). В формуле (I) конкретно описанное сахаридное кольцо и остаток, обозначенный как HAS', вместе представляют предпочтительную молекулу гидроксиалкилкрахмала. Другие структуры сахаридного кольца, содержащиеся в HAS', могут быть такими же или отличными от конкретно описанного сахаридного кольца.
Что касается остатков R1, R2 и R3 в соответствии с формулой (I), то нет конкретных ограничений. В соответствии с предпочтительным вариантом осуществления, R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 2 до 10 атомов углерода в соответствующем алкильном остатке. Предпочтительны водород и гидроксиалкильные группы, имеющие от 2 до 10 атомов. Предпочтительнее гидроксиалкильная группа имеет от 2 до 6 атомов углерода, предпочтительнее от 2 до 4 атомов углерода, еще предпочтительнее от 2 до 4 атомов углерода. Поэтому «гидроксиалкилкрахмал» предпочтительно включает гидроксиэтилкрахмал, гидроксипропилкрахмал и гидроксибутилкрахмал, причем гидроксиэтилкрахмал и гидроксипропилкрахмал являются особенно предпочтительными, а гидроксиэтилкрахмал является особенно наиболее предпочтительным.
Алкильная, арильная, аралкильная и алкарильная группа может быть линейной или разветвленной и подходящим образом замещенной.
Поэтому настоящее изобретение также относится к способу, как описано выше, где R1, R2 и R3 представляют собой независимо водород или линейную или разветвленную гидроксиалкильную группу с 1-6 атомами углерода.
Таким образом, R1, R2 и R3 предпочтительно могут представлять собой гидроксигексил, гидроксипентил, гидроксибутил, гидроксипропил, такой как 2-гидроксипропил, 3-гидроксипропил, 2-гидроксиизопропил, гидроксиэтил, такой как 2-гидроксиэтил, причем водород и 2-гидроксиэтильная группа особенно предпочтительны.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где R1, R2 и R3 представляют собой независимо водород или 2-гидроксиэтильную группу, причем особенно предпочтителен вариант осуществления, где, по меньшей мере, один остаток R1, R2 и R3 представляет собой 2-гидроксиэтил.
Гидроксиэтилкрахмал (HES) наиболее предпочтителен для всех вариантов осуществления настоящего изобретения.
Поэтому настоящее изобретение относится к способу и конъюгату, как описано выше, где полимер представляет собой гидроксиэтилкрахмал и полимерное производное представляет собой производное гидроксиэтилкрахмала.
Гидроксиэтилкрахмал (HES) представляет собой производное природного амилопектина, и он разрушается альфа-амилазой в организме. HES представляет собой замещенное производное углеводородного полимера амилопектина, который присутствует в кукурузном крахмале в концентрации до 95% мас. HES проявляет преимущественные биологические свойства и используется в качестве средства для замещения объема крови и при гемодилюционной терапии в клиниках (Sommermeyer et al., 1987, Krankenhauspharmazie, 8(8), 271-278;. и Weidler et al., 1991, Arzneim.-Forschung/Drug Res., 41,494-498).
Амилопектин состоит из глюкозных частей, где в основной цепи присутствуют альфа-1,4-гликозидные связи, и в ответвляющихся участках обнаруживаются альфа-1,6-гликозидные связи. Физико-химические свойства этой молекулы определяются главным образом типом гликозидных связей. Вследствие альфа-1,4-гликозидной связи в виде «зарубки» получаются спиральные структуры примерно с шестью мономерами глюкозы на один виток. Физико-химические, а также биохимические свойства полимера можно модифицировать замещением. Введение гидроксиэтильной группы может быть достигнуто посредством щелочного гидроксиэтилирования. Подбором условий реакции можно использовать различную реакционную способность соответствующей гидроксигруппы у незамещенного мономера глюкозы в отношении гидроксиэтилирования. Благодаря этому факту специалист может в некоторой степени повлиять на тип замещения.
HES главным образом характеризуется распределением молекулярной массы и степенью замещения. Существуют две возможности описания степени замещения:
1. Степень можно описать относительно части замещенных мономеров глюкозы в отношении всех глюкозных частей.
2. Степень замещения можно описать в виде молярного замещения, где описывается количество гидроксиэтильных групп на одну глюкозную часть.
В контексте настоящего изобретения степень замещения, обозначенная как DS, относится к молярному замещению, как описано выше.
Растворы HES присутствуют в виде полидисперсных композиций, где каждая молекула отличается от другой в отношении степени полимеризации, количества и типа участков ответвления и типа замещения. Поэтому HES представляет собой смесь соединений с различной молекулярной массой. Следовательно, определенный раствор HES определяется средней молекулярной массой с помощью статистического средства. В этом контексте Mn рассчитывается в виде арифметической средней величины, зависящей от количества молекул. Альтернативно Mw (или MW), средняя величина массы, представляет единицу, которая зависит от массы HES.
В контексте настоящего изобретения гидроксиэтилкрахмал может предпочтительно иметь среднюю молекулярную массу (среднюю величину массы) от 1 до 300 кДа. Гидроксиэтилкрахмал может, кроме того, проявлять предпочтительную молярную степень замещения от 0,1 до 0,8 и предпочтительное соотношение между замещением
С2:С6 в диапазоне от 2 до 20 в отношении гидроксиэтильных групп.
Термин «средняя молекулярная масса», используемый в контексте настоящего изобретения, относится к массе, определенной в соответствии с Sommermeyer et al, 1987, Krankenhauspharmazie, 8(8), 271-278; и Weidler et al., 1991, Arzneim.-Forschung/Drug Res., 41,494-498.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, средняя молекулярная масса используемого гидроксиэтилкрахмала составляет от 1 до 300 кДа, предпочтительнее от 2 до 200 кДа, предпочтительнее от 4 до 130 кДа, предпочтительнее от 4 до 70 кДа.
Примером HES со средней молекулярной массой примерно 130 кДа является Voluven® от компании Fresenius. Voluven® представляет собой искусственный коллоид, используемый, например, для замещения объема, используемого при терапевтическом показании для лечения и профилактики гиповолемии. Характеристиками Voluven® являются средняя молекулярная масса 130000 +/- 20000 Да, молярное замещение 0,4 и соотношение С2 : С6 примерно 9:1.
Поэтому настоящее изобретение также относится к способу и конъюгатам, как описано выше, где гидроксиалкилкрахмал представляет собой гидроксиалкилкрахмал, имеющий среднюю молекулярную массу от 4 до 70 кДа.
Предпочтительными диапазонами средней молекулярной массы являются: от 4 до 70 кДа, или от 10 до 70 кДа, или от 12 до 70 кДа, или от 18 до 70 кДа, или от 50 до 70 кДа, или от 4 до 50 кДа, или от 10 до 50 кДа, или от 12 до 50 кДа, или от 18 до 50 кДа, или от 4 до 18 кДа, или от 10 до 18 кДа, или от 12 до 18 кДа, или от 4 до 12 кДа, или от 10 до 12 кДа или от 4 до 10 кДа.
В соответствии с особенно предпочтительными вариантами осуществления настоящего изобретения, средняя молекулярная масса используемого гидроксиэтилкрахмала находится в диапазоне от более чем 4 кДа и ниже 70 кДа, например, примерно 10 кДа, или в диапазоне от 9 до 10 кДа, или от 10 до 11 кДа, или от 9 до 11 кДа, или примерно 12 кДа, или в диапазоне от 11 до 12 кДа, или от 12 до 13 кДа, или от 11 до 13 кДа, или примерно 18 кДа, или в диапазоне от 17 до 18 кДа, или от 18 до 19 кДа, или от 17 до 19 кДа, или примерно 50 кДа, или в диапазоне от 49 до 50 кДа, или от 50 до 51 кДа, или от 49 до 51 кДа.
Что касается степени замещения (DS), то она составляет предпочтительно, по меньшей мере, 0,1, предпочтительнее, по меньшей мере, 0,2, и предпочтительнее, по меньшей мере, 0,4. Предпочтительными диапазонами DS являются от 0,1 до 0,8, предпочтительнее от 0,2 до 0,8, предпочтительнее от 0,3 до 0,8 и еще предпочтительнее от 0,4 до 0,8, еще более предпочтительно от 0,1 до 0,7, предпочтительнее от 0,2 до 0,7, предпочтительнее от 0,3 до 0,7 и предпочтительнее от 0,4 до 0,7. Особенно предпочтительными величинами DS являются, например, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7 или 0,8, причем более предпочтительными являются 0,2, 0,3, 0,4, 0,5 0,6, 0,7 или 0,8, еще более предпочтительными являются 0,3, 0,4, 0,5 0,6, 0,7 или 0,8, и особенно предпочтительными являются, например, 0,4 и 0,7.
Особенно предпочтительными комбинациями молекулярной массы гидроксиалкилкрахмала, предпочтительно, гидроксиэтилкрахмала, и степени его замещения DS являются, например, 10 кДа и 0,4, или 10 кДа и 0,7, или 12 кДа и 0,4, или 12 кДа и 0,7, или 18 кДа и 0,4, или 18 кДа и 0,7, или 50 кДа и 0,4, или 50 кДа и 0,7.
В другом предпочтительном варианте осуществления настоящего изобретения гидроксиэтилкрахмал (используемый, а также содержащийся в описанных здесь конъюгатах) имеет молекулярную массу от примерно 20 кДа до примерно 130 кДа (т.е. примерно 40 кДа, примерно 50 кДа, примерно 60 кДа, примерно 70 кДа, примерно 80 кДа, примерно 90 кДа, примерно 100 кДа, примерно 110 кДа, примерно 120 кДа, примерно 130 кДа), предпочтительно среднюю молекулярную массу от примерно 30 кДа до примерно 100 кДа, предпочтительнее от примерно 40 до примерно 70 кДа, и степень замещения от 0,4 до 0,8, предпочтительнее от 0,5 до 0,8.
В этом контексте термин «примерно 30 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 25 до 34 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 26, 27, 28, 29, 31, 32, 33 кДа или 34 кДа.
В этом контексте термин «примерно 40 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 35 до 44 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 36, 37, 38, 39, 41, 42, 43 кДа или 44 кДа.
В этом контексте термин «примерно 50 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 45 до 54 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 46, 47, 48, 49, 51, 52, 53 или 54 кДа.
В этом контексте термин «примерно 60 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 55 до 64 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 56, 57, 58, 59, 61, 62, 63 кДа или 64 кДа.
В этом контексте термин «примерно 70 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 65 до 74 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 66, 67, 68, 59, 71, 72, 73 кДа или 74 кДа.
В этом контексте термин «примерно 80 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 75 до 84 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 76, 77, 78, 79, 81, 82, 83 кДа или 84 кДа.
В этом контексте термин «примерно 90 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 85 до 94 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 86, 87, 88, 89, 41, 92, 93 кДа или 94 кДа.
В этом контексте термин «примерно 100 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 95 до 104 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 96, 97, 98, 99, 101, 102, 103 кДа или 104 кДа.
В этом контексте термин «примерно 110 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 105 до 114 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 106, 107, 108, 109, 111, 112, 113 кДа или 114 кДа.
В этом контексте термин «примерно 120 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 115 до 124 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 116, 117, 118, 119, 121, 122, 123 кДа или 124 кДа.
В этом контексте термин «примерно 130 кДа» подразумевается как относящийся к средней молекулярной массе в диапазоне от 125 до 134 кДа, т.е. включая также крахмалы, имеющие среднюю молекулярную массу 126, 127, 128, 129, 131, 132, 133 кДа или 134 кДа.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 30 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 40 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 50 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 60 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 70 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 80 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 90 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 100 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 110 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 120 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Соответственно, описанный выше вариант осуществления включает гидроксиэтилкрахмал (и описанные здесь конъюгаты, включающие гидроксилэтилкрахмал, а также описанные здесь способы, использующие гидроксилэтилкрахмал), который имеет среднюю молекулярную массу примерно 130 кДа и степень замещения 0,4, или 0,5, или 0,6, или 0,7, или 0,8, предпочтительно 0,6, 0,7 или 0,8.
Примером HES, имеющего среднюю молекулярную массу примерно 130 кДа, является HES со степенью замещения от 0,2 до 0,8, например 0,2, 0,3, 0,4, 0,5, 0,6, 0,7 или 0,8, предпочтительно от 0,4 до 0,7, например 0,4, 0,5, 0,6 или 0,7.
Что касается соотношения замещения С2:С6, то указанное замещение находится предпочтительно в диапазоне от 2 до 20, предпочтительнее в диапазоне от 2 до 15, а еще предпочтительнее в диапазоне от 3 до 12.
В соответствии с еще одним вариантом осуществления, можно также использовать смеси гидроксилэтилкрахмалов, имеющие средние молекулярные массы и/или различные степени замещения и/или различные соотношения замещения С2:С6. Поэтому можно использовать смеси гидроксилэтилкрахмалов, имеющие различные средние молекулярные массы и различные степени замещения и различные соотношения замещения С2:С6, или имеющие различные средние молекулярные массы и различные степени замещения и одинаковое или примерно одинаковое соотношение замещения С2:С6, или имеющие различные средние молекулярные массы и одинаковую или примерно одинаковую степень замещения и различные соотношения замещения С2:С6, или имеющие одинаковую или примерно одинаковую среднюю молекулярную массу и различные степени замещения и различные соотношения замещения С2:С6, или имеющие различные средние молекулярные массы и одинаковую или примерно одинаковую степень замещения и одинаковое или примерно одинаковое соотношение замещения С2:С6, или имеющие одинаковую или примерно одинаковую среднюю молекулярную массу и различные степени замещения и одинаковое или примерно одинаковое соотношение замещения С2:С6, или имеющие одинаковую или примерно одинаковую среднюю молекулярную массу и одинаковую или примерно одинаковую степень замещения и различные соотношения замещения С2:С6, или имеющие одинаковую или примерно одинаковую среднюю молекулярную массу и примерно одинаковую степень замещения и примерно одинаковое соотношение замещения С2:С6.
В различных конъюгатах и/или других способах в соответствии с настоящим изобретением можно использовать различные гидроксиалкилкрахмалы, предпочтительно различные гидроксиэтилкрахмалы и/или смеси различных гидроксиалкилкрахмалов.
В соответствии с вариантом осуществления настоящего изобретения, функциональная группа Z белка представляет собой альдегидную группу или кетогруппу. Поэтому, настоящее изобретение относится к способу и конъюгатам, как описано выше, где функциональная группа Z белка представляет собой альдегидную группу или кетогруппу.
Хотя нет общих ограничений в отношении положения альдегидной или кетогруппы внутри белка, альдегидная или кетогруппа, в соответствии с предпочтительным вариантом осуществления настоящего изобретения, расположена в углеводородной боковой цепи белка. Поэтому в контексте этого варианта осуществления используется гликозилированный белок.
В качестве гликозилированного белка можно использовать гликозилированный G-CSF, такой как Granocyte®.
В контексте настоящего изобретения термин «углеводородная боковая цепь» относится к гидроксиальдегидам или гидроксикетонам, а также к их химическим модификациям (см. публикацию Römpp Chemielexikon, Thieme Verlag Stuttgart, Germany, 9th edition 1990, Volume 9, pages 2281-2285 и приведенные в ней литературные ссылки). Кроме того, он также относится к природным производным углеводородов, подобных галактозе, N-ацетилнейрамовой кислоте и N-ацетилгалактозамину, и им подобным. В случае использования мутанта G-CSF, являющегося N-гликозилированным, углеводородная часть может представлять собой маннозу.
В еще более предпочтительном варианте осуществления альдегидная группа или кетогруппа представляет собой часть остатка галактозы углеводородной боковой цепи. Этот остаток галактозы может быть сделан доступным для взаимодействия с функциональной группой А, содержащейся в полимере или полимерном производном, удалением концевых сиаловых кислот с последующим окислением, как описано ниже в данном описании.
В еще одном предпочтительном варианте осуществления полимер или полимерное производное, включающее функциональную группу А, соединено с остатком сиаловой кислоты углеводородных боковых цепей, предпочтительно с концевым остатком сиаловой кислоты углеводородной боковой цепи.
Окисление концевых углеводородных частей может выполняться или химически, или ферментативно.
Способы химического окисления углеводородных частей полипептидов известны в данной области и включают обработку периодатом (Chamow et al., 1992, J. Biol. Chem., 267, 15916-15922).
Химическим окислением в принципе можно окислить любую углеводородную часть, расположенную или не расположенную на конце. Однако путем выбора мягких условий реакции можно предпочтительно окислить концевую сиаловую кислоту углеводородной боковой цепи для получения альдегидной группы или кетогруппы.
В соответствии с одним вариантом осуществления настоящего изобретения, указанные мягкие условия взаимодействия относятся к взаимодействию белка с подходящим водным раствором периодата, имеющим предпочтительную концентрацию периодата в диапазоне от 1 до 50 мМ, предпочтительнее от 1 до 25 мМ и особенно предпочтительно от 1 до 10 мМ, например примерно 1 мМ, и при предпочтительной температуре взаимодействия от 0 до 40°С и особенно предпочтительно от 0 до 21°С, например примерно 0°С, и в течение предпочтительного времени взаимодействия от 5 мин до 5 ч, предпочтительно от 10 мин до 2 ч и особенно предпочтительно от 10 мин до 1 ч, например примерно 1 ч. Предпочтительное молярное соотношение периодата: и белка составляет от 1:200 до 1:1, а предпочтительнее от 1:50 до 1:5, например примерно 15:1.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где перед взаимодействием белка и полимера или полимерного производного гликозилированный белок взаимодействует с раствором периодата для получения белка, имеющего альдегидную группу или кетогруппу, расположенную в окисленной углеводородной боковой цепи.
Альтернативно, углеводородная боковая цепь может быть окислена ферментативно. Ферменты для окисления отдельной углеводородной боковой цепи известны в данной области, например, в случае галактозы фермент представляет собой галактозо-оксидазу. Если имеется намерение окислить галактозные части, то, в конечном счете, потребуется удалить концевые сиаловые кислоты (частично или полностью), если полипептид был получен в клетках, способных присоединить сиаловые кислоты к углеводородным цепям, например. В клетках млекопитающих или в клетках, которые были генетически модифицированы для способности присоединения сиаловых кислот к углеводородным цепям. Химические или ферментные способы для удаления сиаловых кислот известны в данной области (Chaplin and Kennedy (eds.), 1996, Carbohydrate Analysis: a practical approach, especially Chapter 5 Montreuill, Glycoproteins, pages 175-177; IRL Press Practical approach series (ISBN 0-947946-44-3)).
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, альдегидная группа или кетогруппа может быть расположена на N конце белка и достижима подходящим окислением. Особенно в случае, когда содержащая гидроксигруппу аминокислота расположена на N-конце белка, такого как треонин или серин, можно осуществить окисление N-концевой аминокислоты, ведущее к получению указанной кетогруппы или альдегидной группы. Теронин представляет собой N-концевую аминокислоту в G-CSF человеческого происхождения. Дополнительный N-концевой серин или треонин могут быть внесены в любой белок, проявляющий активность, подобную G-CSF, молекулярно-биологическими способами. Этот белок или белок, экспрессирующий человеческую аминокислотную последовательность, может быть получен экспрессией в прокариотических или эукариотических клетках, таких как бактерии, клетки млекопитающих, насекомых или дрожжей, и которые могут быть или не быть гликозилированными. В качестве способа химического окисления подходящей N-концевой аминокислоты можно использовать любой возможный способ, причем предпочтительным является окисление периодатом.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, указанные мягкие условия взаимодействия относятся к взаимодействию белка с подходящим водным раствором периодата, имеющим предпочтительную концентрацию периодата в диапазоне от 1 до 50 мМ, предпочтительнее от 1 до 25 мМ и особенно предпочтительно от 1 до 10 мМ, например примерно 1 мМ, и при предпочтительной температуре взаимодействия от 0 до 40°С и особенно предпочтительно от 0 до 21°С, например примерно 0°С, и в течение предпочтительного времени взаимодействия от 5 мин до 5 ч, предпочтительно от 10 мин до 2 ч, и особенно предпочтительно от 10 мин до 1 ч, например примерно 1 ч. Предпочтительное молярное соотношение периодат:белок составляет от 1:200 до 1:1, а предпочтительнее от 1:50 до 1:5, например примерно 15:1.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где альдегидная группа или кетогруппа расположена в углеводородной боковой цепи белка и/или в N-концевой группе белка.
Тип олигосахарида белков, полученных в эукариотических клетках, подвергнутых посттрансляционному гликозилированию таким образом, не идентичен белкам, полученным у человека. Более того, многие гликозилированные белки не имеют желательного количества концевых остатков сиаловой кислоты, маскирующих другую углеводородную часть, такую как остаток галактозы. Однако те дополнительные углеводородные части, такие как остаток галактозы, если они не замаскированы, возможно ответственны за недостатки, такие как более короткий период полувыведения из плазмы белка при возможных способах применения белка в качестве лекарственного средства. К удивлению, было обнаружено, что путем предоставления белкового конъюгата, образованного полимером гидроксиалкилкрахмала, предпочтительно полимером гидроксиэтилкрахмала, который ковалентно соединен, например, через оксимную связь, как раскрыто ниже в настоящем описании, с углеводородной частью углеводородной боковой цепи белка, или непосредственно, или посредством, по меньшей мере, одного линкерного соединения, например, одного или двух линкерных соединений, можно преодолеть, по меньшей мере, указанные выше недостатки. Следовательно, считается, что путем сочетания полимера гидроксиалкилкрахмал или его производного, предпочтительно полимера гидроксиэтилкрахмала или его производного, по меньшей мере, с одной углеводородной боковой цепью гликозилированного белка, компенсируется отсутствие подходящих концевых углеводородных остатков в углеводородной боковой цепи. В соответствии с другим аспектом изобретения, предоставление соответствующего конъюгата с полимером гидроксиалкилкрахмала или его производного, предпочтительно полимера гидроксиэтилкрахмала или его производного, соединенного с окисленной углеводородной частью, как описано выше, не только компенсирует недостаток, но предоставляет конъюгат белка, имеющий лучшие характеристики в желательной области использования, чем соответствующий природный белок. Поэтому, соответствующие конъюгаты в соответствии с изобретением оказывают компенсаторное и даже синергическое влияние на белок. Возможно также, что даже белки, которые идентичны человеческим белкам, или которые представляют собой человеческие белки, не имеют желательного количества подходящих маскирующих концевых углеводородных остатков, таких как остатки сиаловой кислоты и природные углеводородные части. В таких случаях предоставление соответствующего конъюгата с полимером гидроксиалкилкрахмала или его производным, предпочтительно с полимером гидроксиэтилкрахмала или его производным, соединенным с окисленной углеводородной частью, как описано выше, не только преодолевает и компенсирует недостаток искусственно полученного белка, но и улучшает характеристики природного белка. Что касается функциональной группы гидроксиалкилкрахмала, предпочтительно гидроксиэтилкрахмала, или их производного, которое соединено с альдегидной группой или кетогруппой окисленной углеводородной части белка, делается ссылка на функциональные группы А, как раскрыто ниже в настоящем описании. Эта общая концепция не только применима к гликозилированному G-CSF, но в принципе ко всем гликозилированным соединениям, не имеющим концевые углеводородные остатки. Среди других можно упомянуть эритропоэтин (ЕРО), интерферон бета 1а (IFN бета 1а), АТIII, фактор VII, фактор VIII, фактор IX, альфа1-антитрипсин (А1АТ), htPA или GM-CSF.
Поэтому настоящее изобретение также относится к применению гидроксиалкилкрахмала, предпочтительно гидроксиэтилкрахмала, или его производного для компенсации отсутствия концевых углеводородных остатков, предпочтительно остатков сиаловой кислоты, в природных или посттрансляционно присоединенных углеводородных частях белка, ковалентным соединением крахмала или его производного, по меньшей мере, к одной окисленной углеводородной части белка, имеющего, по меньшей мере, одну кето или альдегидную группу.
Соответственно, настоящее изобретение также относится к способу компенсации отсутствия концевых углеводородных остатков, предпочтительно остатков сиаловой кислоты, в природных или посттрансляционно присоединенных углеводородных частях белка, ковалентным соединением гидроксиалкилкрахмала, предпочтительно гидроксиэтилкрахмала, или его производного, по меньшей мере, к одной окисленной углеводородной части белка, имеющего, по меньшей мере, одну кето или альдегидную группу, предпочтительно через оксимную связь.
Более того, настоящее изобретение также относится к конъюгату, образованному ковалентной связью гидроксиалкилкрахмала, предпочтительно гидроксиэтилкрахмала, или его производного, по меньшей мере, с одной окисленной углеводородной частью белка, причем указанный белок или выделен из естественных источников, или получен экспрессией в эукариотических клетках, таких как клетки млекопитающих, насекомых или дрожжей, причем указанная углеводородная часть имеет, по меньшей мере, одну кето или альдегидную группу, где конъюгат имеет желательную область применения, предпочтительно применение в качестве лекарственного средства, и такие же или лучшие характеристики, чем соответствующий не модифицированный белок.
В случае, когда функциональная группа Z белка представляет собой альдегидную группу, функциональная группа А полимера или его производного включает аминогруппу в соответствии со структурой -NH-.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа А, способная взаимодействовать с необязательно окисленным восстанавливающим концом полимера, включает аминогруппу в соответствии со структурой -NH-.
В соответствии с одним предпочтительным вариантом осуществления настоящего изобретения, эта функциональная группа А представляет собой группу, имеющую структуру R'-NH-, где R' представляет собой водород или алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток, где циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток может быть соединен непосредственно с группой NH или, в соответствии с другим вариантом осуществления, может быть соединен кислородным мостиком с группой NH. Алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остатки могут быть подходяще замещенными. В качестве предпочтительных заместителей можно упомянуть галогены, такие как F, Cl или Br. Особенно предпочтительными остатками R' являются водород, алкильная и алкоксигруппы, а еще предпочтительнее являются водород и незамещенные алкильная и алкоксигруппы.
Среди алкильных и алкоксигрупп предпочтительны группы с 1, 2, 3, 4, 5 или 6 атомами С. Более предпочтительными являются метильная, этильная, пропильная, изопропильная, метокси, этокси, пропокси и изопропоксигруппы. Особенно предпочтительными являются метил, этил, метокси, этокси, и особенное предпочтение отдается метилу или метокси.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где R' представляет собой водород или метильную или метосигруппу.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, функциональная группа А имеет структуру R'-NH-R”, где R” предпочтительно включает структурную единицу -NH- и/или структурную единицу -(C=G)-, где G представляет собой O или S и/или структурную единицу -SO2-. В соответствии с более предпочтительными вариантами осуществления, функциональная группа R” выбрана из группы, состоящей из
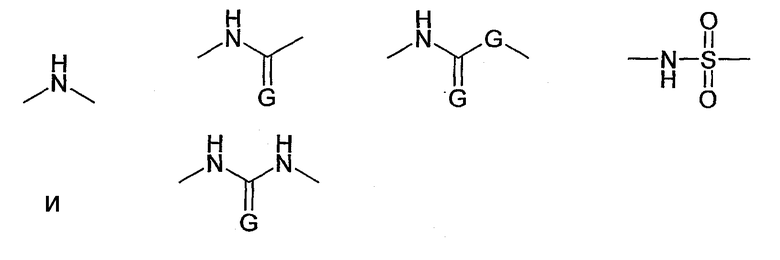
где, если G присутствует дважды, она представляет собой независимо O или S.
Поэтому предпочтительными функциональными группами А, включающими аминогруппу -NH2, являются, например,
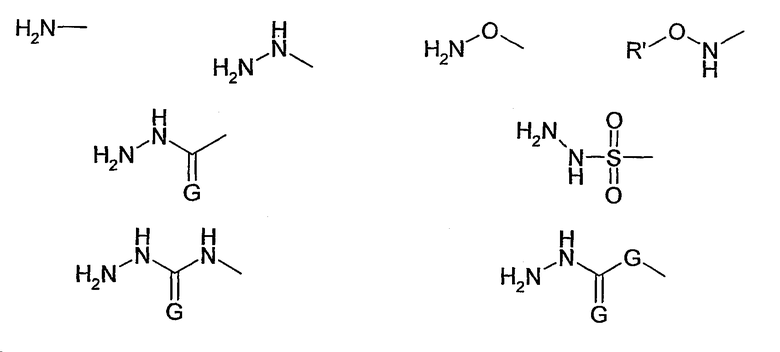
где G представляет собой O или S, и, если присутствует дважды, независимо O или S, и R' представляет собой метил.
Особенно предпочтительными функциональными группами А, включающими аминогруппу, являются аминооксигруппы

причем особенно предпочтительна H2N-O- и гидразидогруппа
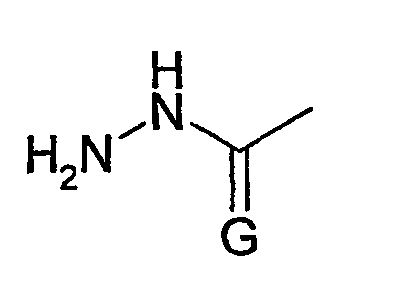
где G представляет собой предпочтительно O.
Поэтому настоящее изобретение также относится к описанному выше способу, где функциональная группа Z белка представляет собой альдегидную группу или кетогруппу, а функциональная группа А представляет собой аминооксигруппу или гидразидогруппу. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, А представляет собой аминооксигруппу.
Таким образом, настоящее изобретение также относится к конъюгату, как описано выше, где функциональная группа Z белка представляет собой альдегидную группу или кетогруппу, а функциональная группа А представляет собой аминооксигруппу или гидразидогруппу. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, А представляет собой аминооксигруппу.
При взаимодействии аминооксигруппы полимера или полимерного производного с альдегидной группой или кетогруппой белка образуется оксимная связь.
Поэтому, настоящее изобретение также относится к конъюгату, как описано выше, где ковалентная связь между белком и полимером или полимерным производным представляет собой оксимную связь, образованную взаимодействием функциональной группы Z белка, причем указанная функциональная группа Z представляет собой альдегидную группу или кетогруппу, и функциональной группы А полимера или полимерного производного, причем указанная функциональная группа А представляет собой аминооксигруппу.
При взаимодействии гидразидогруппы полимера или полимерного производного с альдегидной группой или кетогруппой белка образуется гидразоновая связь.
Поэтому, настоящее изобретение также относится к конъюгату, как описано выше, где ковалентная связь между белком и полимером или полимерным производным представляет собой гидразоновую связь, образованную взаимодействием функциональной группы Z белка, причем указанная функциональная группа Z представляет собой альдегидную группу или кетогруппу, и функциональной группы А полимера или полимерного производного, причем указанная функциональная группа А представляет собой гидразидогруппу.
Для введения функциональной группы А в полимер не существует определенных ограничений, если получается полимерное производное, включающее функциональную группу А.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, функциональная группа А вводится в полимер взаимодействием полимера, по меньшей мере, с бифункциональным соединением, причем одна функциональная группа из которых способна взаимодействовать, по меньшей мере, с одной функциональной группой полимера и, по меньшей мере, одной другой функциональной группой, по меньшей мере, бифунциональной группы, представляющей собой функциональную группу А или способную быть химически модифицированной для получения функциональной группы А.
В соответствии с еще одним предпочтительным вариантом осуществления, полимер взаимодействует, по меньшей мере, с бифункциональным соединением на его необязательно окисленном восстанавливающем конце.
В случае если полимер взаимодействует с его неокисленным восстанавливающим концом, полимер предпочтительно имеет строение
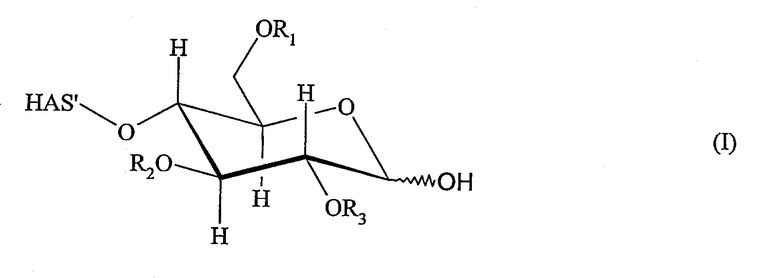
где в формулу (I) включена альдегидная форма неокисленного восстанавливающего конца.
В случае если полимер взаимодействует с его неокисленным восстанавливающим концом, полимер предпочтительно имеет строение в соответствии с формулой (IIa)
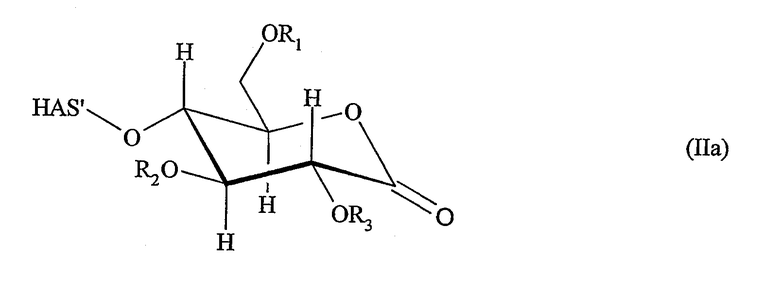
и/или в соответствии с формулой (IIb)
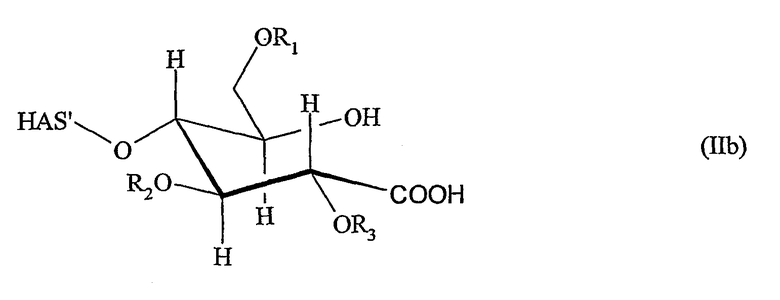
Окисление восстанавливающего конца полимера, предпочтительно гидроксиэтилкрахмала, можно проводить в соответствии с каждым способом или комбинацией способов, которые приводят к получению соединений, имеющих указанные выше структуры (IIa) и/или (IIb).
Хотя окисление можно проводить в соответствии с любым подходящим способом или способами, приводящими к получению окисленного восстанавливающего конца гидроксиалкилкрахмала, оно предпочтительно проводится с использованием щелочного раствора йода, как описано, например, в документе DE 196 28 705 A1, соответствующее содержание которого (пример А, колонка 9, строки 6-24) включено в настоящее описание в качестве ссылки.
В качестве функциональной группы, по меньшей мере, бифункциональной группы, которая способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, можно использовать каждую функциональную группу, которая способна образовывать химическую связь с необязательно окисленным восстанавливающим концом гидроксиалкилкрахмала.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, эта функциональная группа включает химическую структуру -NH-.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа, по меньшей мере, бифункциональной группы, причем указанная функциональная группа способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, включает структуру -NH-.
В соответствии с одним предпочтительным вариантом осуществления настоящего изобретения, эта функциональная группа, по меньшей мере, бифункционального соединения, представляет собой группу, имеющую структуру R'-NH-, где R' представляет собой водород или алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток, где циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток может быть соединен непосредственно с группой NH или, в соответствии с другим вариантом осуществления, может быть соединен кислородным мостиком с группой NH. Алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остатки могут быть подходяще замещенными. В качестве предпочтительных заместителей можно упомянуть галогены, такие как F, Cl или Br. Особенно предпочтительными остатками R' являются водород, алкильная и алкоксигруппы, а еще предпочтительнее являются водород и незамещенные алкильная и алкоксигруппы.
Среди алкильной и алкоксигруппы предпочтительны группы с 1, 2, 3, 4, 5 или 6 атомами С. Более предпочтительными являются метильная, этильная, пропильная, изопропильная, метокси, этокси, пропокси и изопропоксигруппы. Особенно предпочтительными являются метил, этил, метокси, этокси, и особенное предпочтение отдается метилу или метокси.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где R' представляет собой водород или метильную или метосигруппу.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, функциональная группа, по меньшей мере, бифункциональной группы имеет структуру R'-NH-R”, где R” предпочтительно включает структурную единицу -NH- и/или структурную единицу -(C=G)-, где G представляет собой O или S и/или структурную единицу -SO2-. В соответствии с более предпочтительными вариантами осуществления, функциональная группа R” выбрана из группы, состоящей из

где, если G присутствует дважды, она представляет собой независимо O или S.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, выбрана из группы, состоящей из

где, если G присутствует дважды, она представляет собой независимо O или S, а R' представляет собой метил.
В соответствии с еще более предпочтительным вариантом осуществления настоящего изобретения, функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, и включает аминогруппу, представляет собой аминооксигруппы

причем особенно предпочтительна H2N-O- или гидразидогруппа

где G представляет собой предпочтительно O.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа Z белка представляет собой альдегидную группу или кетогруппу, а функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, представляет собой аминооксигруппу или гидразидогруппу, предпочтительно аминооксигруппу.
Таким образом, настоящее изобретение также относится к конъюгату, как описано выше, где функциональная группа Z белка представляет собой альдегидную группу или кетогруппу, а функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, представляет собой аминооксигруппу или гидразидогруппу, предпочтительно аминооксигруппу.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, по меньшей мере, бифункциональное соединение взаимодействует с полимером на его неокисленном восстанавливающем конце.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, по меньшей мере, бифункциональное соединение, которое взаимодействует с необязательно окисленным восстанавливающим концом полимера, включает функциональную группу А.
По меньшей мере, бифункциональное соединение может сначала взаимодействовать с полимером для получения полимерного производного, которое в последующем взаимодействует с белком через функциональную группу А. Возможно также взаимодействие, по меньшей мере, бифункционального соединения через функциональную группу А сначала с белком для получения производного белка, которое в последующем взаимодействует с полимером через, по меньшей мере, одну функциональную группу, по меньшей мере, остатка бифункционального соединения, содержащегося в белковом производном.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, по меньшей мере, бифункциональное соединение сначала взаимодействует с полимером.
Поэтому настоящее изобретение относится к способу и конъюгату, как описано выше, причем указанный способ, кроме того, включает взаимодействие полимера на его неокисленном восстанавливающем конце, по меньшей мере, с бифункциональным связывающим соединением, включающим функциональную группу, способную взаимодействовать с неокисленным восстанавливающим соединением полимера и группой А перед взаимодействием полимерного производного, включающего А, и белка, включающего Z.
Функциональную группу, по меньшей мере, бифункционального связывающего соединения, которое взаимодействует с полимером. И функциональную группу А, по меньшей мере, бифункционального связывающего соединения, которое взаимодействует с функциональной группой Z, можно отделить любым подходящим промежуточным соединением. Среди других промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. В целом углеводородный остаток имеет до 60, предпочтительно до 40, предпочтительнее до 20, предпочтительнее до 10, предпочтительнее до 6 и особенно предпочтительно до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, предпочтительнее от 1 до 6, предпочтительнее от 1 до 4 и, в частности, от 1 до 2 гетероатомов. В качестве гетероатома предпочтительнее О. Углеводородный остаток может включать необязательно разветвленную алкильную цепь или арильную группу или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или может представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления настоящего изобретения, функциональные группы отделены линейной углеводородной цепью, имеющей 4 атома углерода. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, функциональные группы отделены линейной углеводородной цепью, имеющей 4 атома углерода, и, по меньшей мере, одним гетероатомом, особенно предпочтительно, атомом кислорода.
В соответствии с еще одним предпочтительным вариантом осуществления, по меньшей мере, бифункциональное связывающее соединение представляет собой гомобифункциональное связывающее соединение. Поэтому настоящее изобретение также относится к способу получения конъюгата, как описано выше, где, по меньшей мере, бифункциональное связывающее соединение представляет собой гомобифункциональное соединение.
Таким образом, в отношении указанных выше предпочтительных функциональных групп связывающего соединения, указанное гомобифункциональное связывающее соединение предпочтительно включает или 2 аминооксигруппы H2N-O-, или 2 аминооксигруппы R'-O-NH-, или 2 гидразидогруппы H2N-NH-(C=G)-, причем предпочтительны аминооксигруппы H2N-O- и гидразидогруппы H2N-NH-(C=O)-, и особенно предпочтительны аминооксигруппы H2N-O-.
Среди всех возможных гомобифункциональных соединений, включающих 2 гидразидогруппы H2N-NH-(C=O)-, предпочтительны гидразиды, где 2 гидразидогруппы отделены углеводородным остатком, имеющим до 60, предпочтительно до 40, предпочтительнее до 20, предпочтительнее до 10, предпочтительнее до 6 и особенно предпочтительно до 4 атомов углерода. Предпочтительнее углеводородный остаток имеет 1-4 атома углерода, например 1, 2, 3 или 4 атома углерода. Наиболее предпочтительно углеводородный остаток имеет 4 атома углерода. Поэтому предпочтительно гомобифункциональное соединение в соответствии с формулой
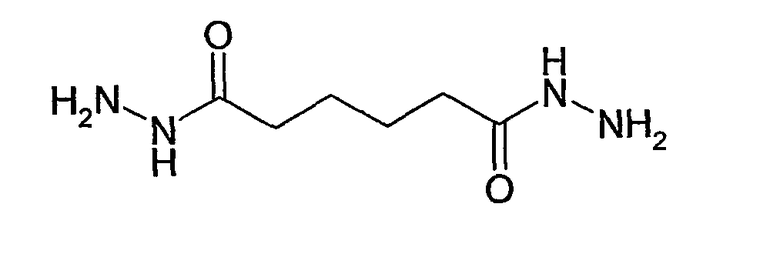
В соответствии с еще более предпочтительным вариантом осуществления настоящего изобретения, бифункциональное связывающее соединение представляет собой карбогидразид
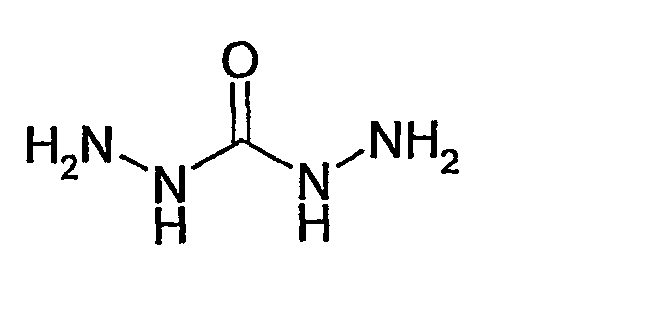
Как описано выше, настоящее изобретение также относится к способу и конъюгату, где, по меньшей мере, бифункциональное связывающее соединение представляет собой гомобифункциональное соединение и включает 2 аминооксигруппы. Следовательно, настоящее изобретение также относится к способу и конъюгату, как описано выше, где, по меньшей мере, бифункциональное связывающее соединение представляет собой гомобифункциональное соединение и включает 2 аминооксигруппы H2N-O-.
Как описано выше, полимер предпочтительно взаимодействует на его восстанавливающем конце, который не окислен перед взаимодействием с бифункциональным связывающим соединением. Поэтому взаимодействие предпочтительного гомобифункционального соединения, включающего 2 аминооксигруппы H2N-O-, с полимером приводит к полимерному производному, включающему оксимную связь.
Поэтому, поскольку функциональная группа Z белка представляет собой альдегидную или кетогруппу, которая предпочтительно взаимодействует с аминооксигруппой полимерного производного, настоящее изобретение также относится к конъюгату, как описано выше, причем указанный конъюгат включает полимер и белок, причем каждый ковалентно связан со связывающим соединением оксимной или циклической аминной связью.
Среди всех возможных гомобифункциональных соединений, включающих 2 аминооксигруппы H2N-O-, предпочтительны бифункциональные соединения, где 2 аминооксигруппы отделены углеводородным остатком, имеющим от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 1 до 10, предпочтительнее от 1 до 6, и особенно предпочтительно от 1 до 4 атомов углерода. Предпочтительнее углеводородный остаток имеет 1-4 атома углерода, например 1, 2, 3 или 4 атома углерода. Наиболее предпочтительно углеводородный остаток имеет 4 атома углерода. Еще предпочтительнее углеводородный остаток имеет, по меньшей мере, один гетероатом, а наиболее предпочтительно один атом кислорода. Особенно предпочтительно соединение O-[2-(2-аминооксиэтокси)этил]гидроксиламин в соответствии с формулой
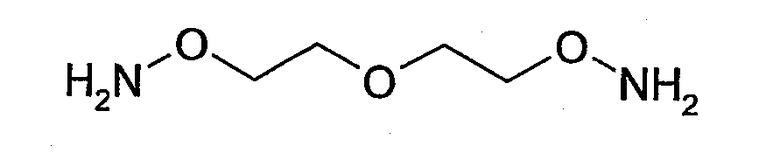
Поэтому настоящее соединение относится к конъюгату, как описано выше, причем указанный конъюгат имеет структуру в соответствии с формулой
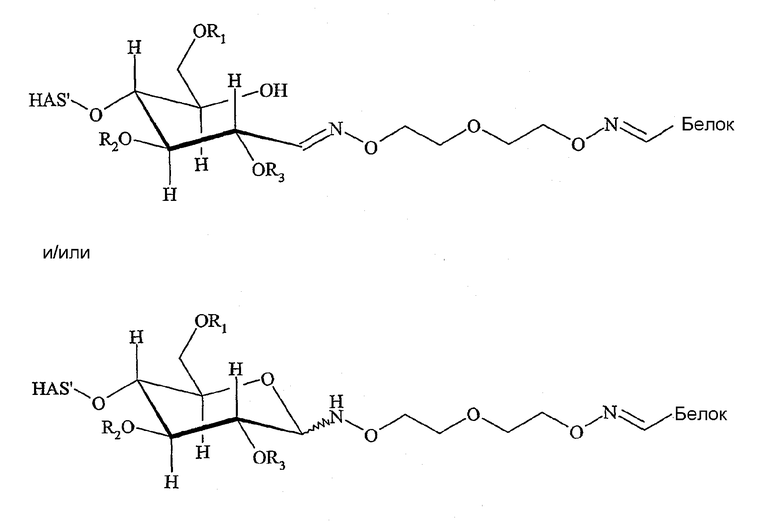
причем HAS' предпочтительно представляет собой HES'. Особенно предпочтительными гидроксиэтилкрахмалами являются, например, гидроксиэтилкрахмалы, имеющие среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7.
Взаимодействие полимера на его неокисленном восстанавливающем конце со связывающим соединением, особенно в случае, когда указанное связывающее соединение представляет собой гомобифункциональное связывающее соединение, включающее 2 аминооксигруппы H2N-O-, предпочтительно проводится в водной системе.
Термин «водная система», используемый в контексте настоящего изобретения, относится к растворителю или смеси растворителей, включающей воду, в диапазоне от, по меньшей мере, 10% мас., предпочтительно, по меньшей мере, 50% мас., предпочтительнее, по меньшей мере, 80% мас., еще предпочтительно, по меньшей мере, 90% мас., или до 100% мас., на основании массы включенных растворителей. Предпочтительной средой для реакции является вода.
В соответствии с другим вариантом осуществления можно использовать, по меньшей мере, один другой растворитель, в котором растворим HAS, предпочтительно HES. Примерами этих растворителей являются, например, DMF (диметилформамид), диметилацетамид или DMSO (диметисульфоксид).
Что касается температур, которые применяются во время реакции, то определенные ограничения не существуют при условии, что взаимодействие приводит к получению желательного полимерного производного.
В случае если полимер взаимодействует с гомобифункциональным связывающим соединением, включающим 2 аминооксигруппы H2N-O-, предпочтительно O-[2-(2-аминооксиэтокси)этил]гидроксиламин, температура предпочтительно находится в диапазоне от 0 до 45°С, предпочтительнее в диапазоне от 4 до 30°С, и особенно предпочтительно в диапазоне от 15 до 25°С.
Время взаимодействия для взаимодействия полимера с гомобифункциональным связывающим соединением, включающим 2 аминооксигруппы H2N-O-, предпочтительно O-[2-(2-аминооксиэтокси)этил]гидроксиламин, можно подобрать для конкретных нужд, и оно в целом находится в диапазоне от 1 ч до 7 дн, предпочтительно от 1 ч до 3 дн, а предпочтительнее от 2 ч до 48 ч.
Величину рН для взаимодействия полимера с гомобифункциональным связывающим соединением, включающим 2 аминооксигруппы H2N-O-, предпочтительно O-[2-(2-аминооксиэтокси)этил]гидроксиламин, можно подобрать для конкретных нужд, таких как химическая природа реагентов. Величина рН предпочтительно находится в диапазоне от 4,5 до 9,5, предпочтительнее в диапазоне от 4,5 до 6,5.
Конкретными примерами указанных выше условий взаимодействия являются, например, температура взаимодействия примерно 25°С и рН примерно 5,5.
Подходящую величину рН реакционной смеси можно регулировать добавлением, по меньшей мере, одного подходящего буфера. Среди предпочтительных буферов можно упомянуть буфер ацетата натрия, фосфатный или боратный буфер.
Когда образовано полимерное производное, включающее полимер и связанное с ним бифункциональное связывающее соединение, его можно выделить из реакционной смеси, по меньшей мере, одним подходящим способом. При необходимости полимерное производное может осаждаться перед выделением, по меньшей мере, одним подходящим способом.
Если полимерное производное сначала осаждается, можно, например, обеспечить контакт реакционной смеси, по меньшей мере, с одним растворителем или смесью растворителей, отличных от растворителя или смеси растворителей, присутствующих в реакционной смеси, при подходящих температурах. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, где водная среда, предпочтительно вода, используется в качестве растворителя, реакционная смесь контактирует с 2-пропанолом при температуре, предпочтительно в диапазоне от -20 до +50°С, а особенно предпочтительно от -20 до 25°С.
Выделение полимерного производного можно проводить подходящим способом, который может включать одну или больше стадий. В соответствии с предпочтительными вариантами осуществления настоящего изобретения, полимерное производное сначала отделяется от реакционной смеси или смеси реакционной смеси, например, водной смесью 2-пропанола, подходящим способом, таким как центрифугирование или фильтрация. На второй стадии отделенное полимерное производное может быть подвергнуто дальнейшей обработке, такой как диализ, подобный последующей обработке, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография в обращенной фазе, ВЭЖХ, ЖХСД (жидкостная хроматография под средним давлением), гель-фильтрация и/или лиофилизация. В соответствии с еще более предпочтительным вариантом реализации, отделенное полимерное производное сначала диализируется, предпочтительно против воды, а затем лиофилизируется до тех пор, пока содержание растворителя продукта взаимодействия не будет достаточно низким, в соответствии с желательными спецификациями продукта. Лиофилизацию можно проводить при температуре от 20 до 35°С, предпочтительно от 20 до 30°С.
Выделенное таким образом полимерное производное затем взаимодействует через функциональную группу А с функциональной группой Z белка, причем Z представляет собой альдегидную группу или кетогруппу. В особенно предпочтительном случае, при котором А представляет собой аминооксигруппу H2N-O- для предоставления оксимной связи между полимерным производным и белком, взаимодействие предпочтительно проводится в водной среде, предпочтительно воде, при предпочтительной температуре в диапазоне от 0 до 40°С, предпочтительнее от 4 до 25°С, и особенно предпочтительно от 15 до 25°С. Величина рН реакционной среды находится предпочтительно в диапазоне от 4 до 10, предпочтительнее в диапазоне от 5 до 9 и особенно предпочтительно в диапазоне от 5 до 7. Время реакции составляет предпочтительно в диапазоне от 1 до 72 ч, предпочтительнее в диапазоне от 1 до 48 ч, а предпочтительно в диапазоне от 4 до 24 ч.
Конъюгат может быть подвергнут дальнейшей обработке, такой как последующая обработка, подобная диализу, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография с обращенной фазой, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация.
В соответствии с другим вариантом осуществления настоящего изобретения, функциональная группа Z белка представляет собой аминогруппу. Поэтому настоящее изобретение относится к способу и конъюгату, как описано выше, где функциональная группа Z белка представляет собой аминогруппу.
В соответствии с еще одни предпочтительным вариантом осуществления настоящего изобретения, функциональная группа А, которой предстоит взаимодействие с функциональной группой Z, представляющей собой аминогруппу, представляет собой реакционноспособную карбоксигруппу. Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа Z представляет собой аминогруппу, а функциональная группа А полимера или полимерного производного представляет собой реакционноспособную карбоксигруппу.
В соответствии с первым предпочтительным вариантом осуществления настоящего изобретения, реакционноспособная карбоксигруппа вводится в полимер избирательным окислением полимера на его восстанавливающем конце.
Поэтому полимер, в который введена реакционноспособная карбоксигруппа, имеет структуру в соответствии с формулой (IIa)

и/или в соответствии с формулой (IIb)
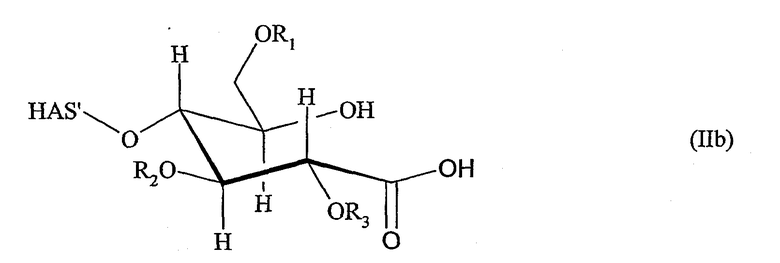
Окисление восстанавливающего конца полимера в соответствии с формулой (I)

предпочтительно гидроксиэтилкрахмала, можно проводить в соответствии с каждым способом или комбинацией способов, которые приводят к получению соединений, имеющих указанные выше структуры (IIa) и/или (IIb).
Хотя окисление можно производить в соответствии с подходящим способом или способами, приводящими к получению окисленного восстанавливающего конца гидроксиалкилкрахмала, его предпочтительно проводить с использованием щелочного раствора йода, как описано, например, в документе DE 196 28 705 A1, соответствующее содержание которого (пример А, колонка 9, строки 6-24) включено в настоящее описание в качестве ссылки.
Введение реакционноспособной карбоксигруппы в полимер, который селективно окислен на его восстанавливающем конце, можно провести всеми возможными способами.
Окисленный полимер можно использовать как таковой или в виде соли, такой как соль щелочного металла, предпочтительно в виде соли натрия и/или калия.
В соответствии с предпочтительным способом настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце, по меньшей мере, с одним спиртом, предпочтительно, по меньшей мере, с одним кислотным спиртом. Еще более предпочтительными являются кислотные спирты, имеющие величину pKA в диапазоне от 6 до 12, предпочтительнее от 7 до 11 при 25°С. Молекулярная масса кислотного спирта находится в диапазоне от 80 до 500 г/моль, предпочтительнее от 90 до 300 г/моль, и особенно предпочтительно от 100 до 200 г/моль.
Подходящими кислотными спиртами являются все спирты H-O-RA, имеющие кислотную часть и способны взаимодействовать с окисленным полимером, для получения соответствующего реакционноспособного сложного эфира полимера, предпочтительно в соответствии с формулой
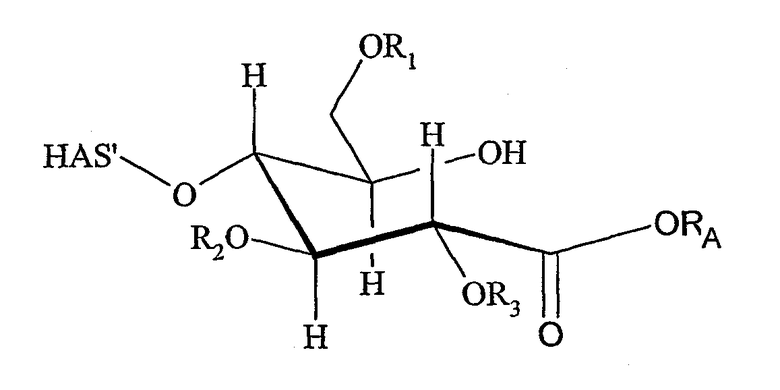
еще предпочтительнее в соответствии с формулой
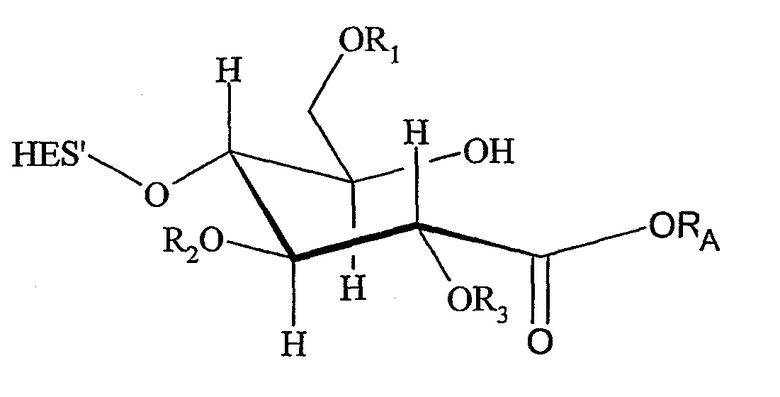
Предпочтительными спиртами являются N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол, 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N-гидроксисукцинимид, причем особенно предпочтительны N-гидроксисукцинимид и сульфо-N-гидроксисукцинимид. Все спирты можно использовать отдельно или в виде подходящей комбинации двух или более из них. В контексте настоящего изобретения можно также использовать соединение, которое высвобождает соответствующий спирт, например, добавлением сложных диэфиров карбоновой кислоты.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер, который селективно оксилен на его восстанавливающем конце, активирован взаимодействием окисленного полимера с кислотным спиртом, предпочтительно с N-гидроксисукцинимидом и/или сульфо-N-гидроксисукцинимидом.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце, по меньшей мере, с одним сложным карбоновым диэфиром RB-O-(C=O)-O-RC, где RB и RC могут быть одинаковыми или различными. Предпочтительно этот способ дает реакционноспособные полимеры в соответствии с формулой
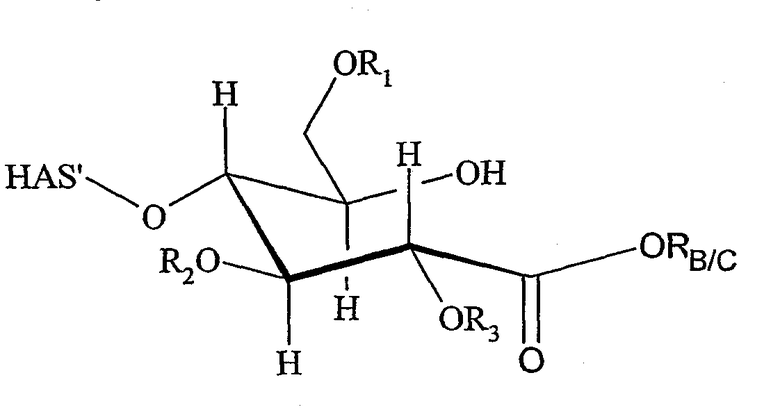
где HAS' представляет собой предпочтительно HES'.
В качестве соединений сложного карбонового диэфира могут использоваться соединения, спиртовые компоненты которых представляют собой независимо N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол, 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N,N'-дисукцинимидилкарбонат и сульфо-N,N'-дисукцинимидилкарбонат, причем особенно предпочтителен N,N'-дисукцинимидилкарбонат.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер, который селективно окислен на его восстанавливающем конце, активирован взаимодействием окисленного полимера с N,N'-дисукцинимидилкарбонатом.
Кислотный спирт взаимодействует с окисленным полимером или солью окисленного полимера при молярном соотношении кислотного спирта и полимера предпочтительно от 5:1 до 50:1, предпочтительнее от 8:1 до 20:1 при предпочтительной температуре взаимодействия от 2 до 40°С, предпочтительнее от 10 до 30°С, и особенно предпочтительно от 15 до 25°С. Время взаимодействия находится предпочтительно в диапазоне от 1 до 10 ч, предпочтительнее от 2 до 5 ч, предпочтительнее от 2 до 4 ч и, в частности, от 2 до 3 ч.
Соединение сложного карбонового диэфира взаимодействует с окисленным полимером или солью окисленного полимера при молярном соотношении сложного диэфира и полимера предпочтительно от 1:1 до 3:1, предпочтительнее от 1:1 до 1,5:1. Время взаимодействия находится предпочтительно в диапазоне от 0,1 до 12 ч, предпочтительнее от 0,2 до 6 ч, предпочтительнее от 0,5 до 2 ч и, в частности, от 0,75 до 1,25 ч.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие окисленного полимера с кислотным спиртом и/или сложным карбоновым диэфиром проводится, по меньшей мере, в одном апротонном растворителе, имеющем содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями, среди других, являются диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси двух или более из них. Температуры взаимодействия находятся предпочтительно в диапазоне от 2 до 40°С, предпочтительнее от 10 до 30°С.
Для взаимодействия окисленного полимера, по меньшей мере, с одним кислотным спиртом используется, по меньшей мере, один дополнительный активирующий агент.
Подходящими активирующими агентами являются, среди других, карбонилдиимидазол, карбодиимиды, такие как диизопропилкарбодиимид (DIC), дициклогексилкарбодиимиды (DCC), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), причем особенно предпочтительны дициклогексилкарбодиимиды (DCC) и 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC).
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер, который селективно окислен на его восстанавливающем конце, взаимодействует с кислотным спиртом в присутствии дополнительного активирующего агента для получения реакционноспособного сложного эфира полимера.
В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, взаимодействие окисленного полимера со сложным карбоновым диэфиром и/или кислотным спиртом проводится при низкой основной активности, которую можно определить добавлением реакционной смеси к воде при объемном соотношении между водой и реакционной смесью 10:1. Перед добавлением вода, которая по существу не включает буфер, имеет рН 7 при 25°С. После добавления реакционной смеси и измерения величины рН определяется основная активность реакционной смеси, имеющая величину предпочтительно не более чем 9,0, предпочтительнее не более чем 8,0, особенно предпочтительно не более чем 7,5.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, окисленный полимер взаимодействует с N-гидроксисукцинимидом в сухом DMA в отсутствие воды с EDC для селективного получения N-гидроксисукцинимидного сложного эфира полимера в соответствии с формулой
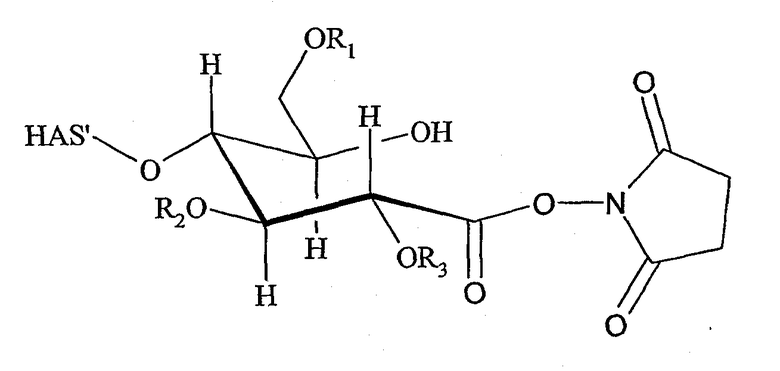
причем HAS' предпочтительно представляет собой HES'.
К удивлению, это взаимодействие не дает побочные продукты, полученные в результате взаимодействий EDC с группами ОН HES, и реакция перегруппировки О-ацилмочевины, образованной EDC и окисленным полимером в соответствующую N-ацилмочевину, к удивлению подавлена.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, окисленный полимер взаимодействует с N,N'-дисукцинимидилкарбонатом в безводном DMF и в отсутствие активирующего агента для селективного получения N-гидроксисукцинимидного сложного эфира полимера в соответствии с формулой

причем HAS' предпочтительно представляет собой HES'.
Реакционноспособный полимер, как описано выше, предпочтительно далее взаимодействует, по меньшей мере, с одной аминогруппой белка для получения амидной связи. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, реакционноспособный полимер взаимодействует с одной аминогруппой белка.
Поэтому настоящее изобретение относится к конъюгату, предпочтительно имеющему структуру в соответствии с формулой
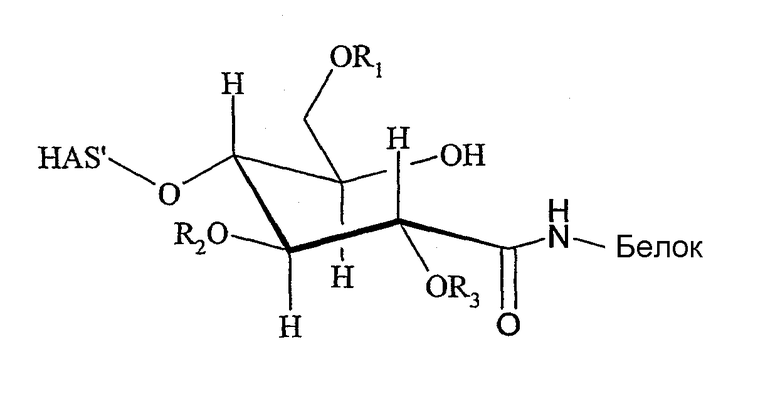
где атом N амидной связи получен из аминогруппы белка, предпочтительнее при HAS' представляющем собой HES', причем гидроксиэтилкрахмал представляет собой гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7.
Взаимодействие реакционноспособного полимера с белком можно проводить объединением реакционной смеси препарата реакционноспособного полимера, т.е. без выделения реакционноспособного полимера, включающего, по меньшей мере, 10, предпочтительнее, по меньшей мере, 30 и еще предпочтительнее, по меньшей мере, 50% мас. реакционноспособного полимера, с водным раствором бела. Предпочтительные водные растворы белка включают от 0,05 до 10, предпочтительнее от 0,5 до 5, и особенно предпочтительно от 0,5 до 2% мас. белка при предпочтительном рН от 5,0 до 9,0, предпочтительнее от 6,0 до 9,0 и особенно предпочтительно от 7,5 до 8,5.
В соответствии с настоящим изобретением, можно также очистить реакционноспособный полимер, по меньшей мере, одним, предпочтительно множественным осаждением, по меньшей мере, одним осаждающим агентом, таким как безводный этанол, изопропанол и/или ацетон, для получения твердого вещества, включающего, по меньшей мере, 10, предпочтительнее, по меньшей мере, 30 и еще предпочтительнее, по меньшей мере, 50% мас. реакционноспособного полимера.
Очищенный реакционноспособный полимер может добавляться в водный раствор белка. Можно также добавить раствор очищенного реакционноспособного полимера к водному раствору белка.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие реакционноспособного полимера с белком для получения амидной связи проводится при температуре от 2 до 40°С, предпочтительнее от 5 до 35°С и особенно предпочтительнее от 10 до 30°С и предпочтительном рН от 7,0 до 9,0, предпочтительно от 7,5 до 9,0 и особенно предпочтительно от 7,5 до 8,5 при предпочтительном времени взаимодействия от 0,1 до 12 ч, предпочтительнее от 0,5 до 5 ч, предпочтительнее от 0,5 до 3 ч, еще предпочтительнее от 0,5 до 72 ч, и особенно предпочтительно от 0,5 до 1 ч, причем молярное соотношение реакционноспособного сложного эфира полимера:белка составляет от 1:1 до 70:1, предпочтительнее от 5:1 до 50:1, и особенно предпочтительно от 10:1 до 50:1.
В соответствии с еще одним вариантом осуществления настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце с азолидом, таким как карбонилдиимидазол или карбонилдибензимидазол, для получения полимера, имеющего реакционноспособную карбоксигруппу. В случае карбонилдиимидазола получается реакционноспособное полимерное производное в соответствии с формулой
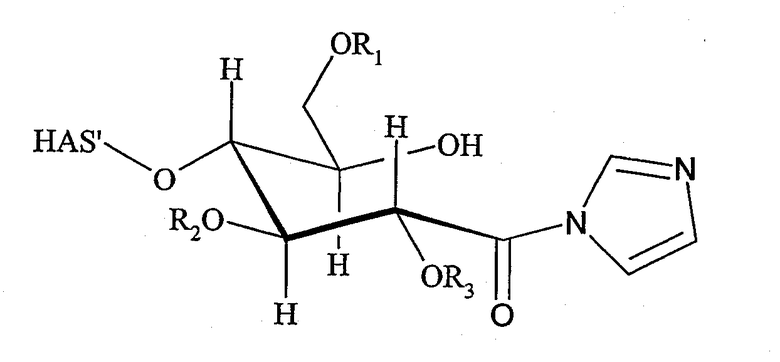
где HAS' предпочтительно представляет собой HES'. Имидазолид, полученный в результате взаимодействия полимера с азолидом, может предпочтительно взаимодействовать с аминогруппой белка для получения амидной связи. Также возможно взаимодействие, если оно присутствует, с гидроксигруппой белка для получения сложноэфирной связи, или с тиогруппой белка для получения тио-сложноэфирной связи, или, если она присутствует, с карбоксигруппой белка для получения связи -(C=O)-O-(C=))-.
В соответствии с еще одним вариантом осуществления настоящего изобретения, полимер, имеющий реакционноспособную карбоксигруппу А, полученную в результате взаимодействия селективно окисленного восстанавливающего конца полимера с одним из указанных выше соединений, предпочтительно, по меньшей мере, с одним из кислотных спиртов и/или, по меньшей мере, одним из соединений сложного карбонового диэфира, может быть соединен с функциональной группой Z белка, по меньшей мере, через одно линкерное соединение. В случае использования линкерного соединения, указанное соединение представляет собой, по меньшей мере, бифункциональное соединение, имеющее, по меньшей мере, одну функциональную группу F1, способную взаимодействовать с функциональной группой А полимерного производного и, по меньшей мере, одну функциональную группу F2, способную взаимодействовать с функциональной группой Z белка или функциональной группой
F2, способной быть химически модифицированной для взаимодействия с функциональной группой Z белка. Химическая модификация может представлять собой, например, взаимодействие функциональной группы F2 с функциональной группой F3 еще одного линкерного соединения или окисление или восстановление подходящей функциональной группы F2. В случае использования, по меньшей мере, одного линкерного соединения, взаимодействие не ограничивается аминогруппой белка, но, в зависимости от химической природы функциональных групп линкерного соединения или линкерных соединений, может использоваться для образования связи с каждой подходящей функциональной группой белка, такой как карбоксигруппа, реакционноспособная карбоксигруппа, альдегидная группа, кетогруппа, тиогруппа, аминогруппа или гидроксигруппа. В случае использования двух линкерных соединений, используется первое линкерное соединение, имеющее, по меньшей мере, одну функциональную группу F1, способную взаимодействовать с реакционноспособной карбоксигруппой А полимера, такой как аминогруппа, тиогруппа, гидроксигруппа, или карбоксигруппа. Более того, первое линкерное соединение имеет, по меньшей мере, одну другую функциональную группу F2, которая способна взаимодействовать, по меньшей мере, с одной функциональной группой F3 второго линкерного соединения. В качестве функциональной группы F2, следует упомянуть, среди других, следующие функциональные группы:
- С-С-двойные связи, или С-С-тройные связи, или ароматические С-С-связи;
- тиогруппа или гидроксигруппы;
- гидразид алкилсульфоновой кислоты, гидразид арилсульфоновой кислоты;
- 1,2-диолы;
- 1,2-аминоспирты;
- 1,2-аминотиоспирты;
- азиды;
- аминогруппа -NH2 или производные аминогрупп, включающие структурную единицу -NH-, такие как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы или алкариламиногруппы;
- гидроксиламиногруппа -O-NH2 или производные гидроксиламиногруппы, включающие структурную единицу -O-NH-, такие как гидроксиалкиламиногруппы, гидроксилариламиногруппы, гидроксиаралкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогруппы, арилоксиаминогруппы, аралкилоксиаминогруппы или алкарилоксиаминогруппы, каждая из которых включает структурную единицу -NH-O-;
- остатки, имеющие карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такое как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;
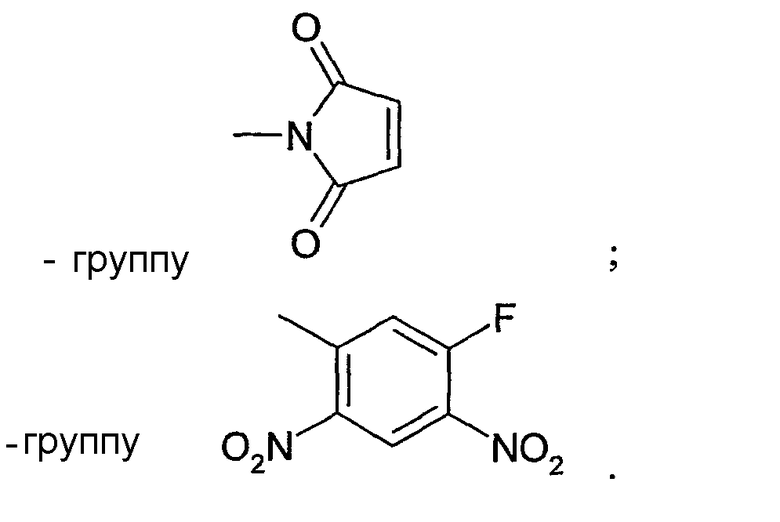
где F3 представляет собой группу, способную образовывать химическую связь с одной из указанных выше групп, и предпочтительно выбрана из указанных выше групп. Более того, второе линкерное соединение имеет, по меньшей мере, одну функциональную группу, которая способна взаимодействовать с функциональной группой Z белка, которая представляет собой, например, аминогруппу, тиогруппу, карбоксигруппу, реакционноспособную карбоксигруппу, альдегидную группу, кетогруппу или гидроксигруппу. В случае использования одной связывающей группы для ковалентного связывания с полимером и белком, полимер может взаимодействовать со связывающим соединением, и полученное полимерное производное взаимодействует с белком, или белок может взаимодействовать со связывающим соединением, и полученное производное белка взаимодействует с полимером. В случае использования двух связывающих соединений L1 и L2, можно обеспечить взаимодействие полимера с L1, взаимодействие полученного полимерного производного с L2 и взаимодействие полученного полимерного производного с белком, или взаимодействие белка с L2, взаимодействие полученного белкового производного с L1 и взаимодействие полученного белкового производного с полимером. Можно также обеспечить взаимодействие полимера с L1, взаимодействие белка с L2 и взаимодействие полимерного производного с белковым производным. Кроме того, можно обеспечить взаимодействие L1 с L2, взаимодействие полученного соединения с полимером и полученного полимерного производного с белком. Кроме того, можно обеспечить взаимодействие L1 с L2, взаимодействие полученного соединения с белком и полученного белкового производного с полимером.
В соответствии со вторым предпочтительным вариантом осуществления настоящего изобретения, относящимся к введению реакционноспособной карбоксигруппы в полимер, реакционноспособная карбоксигруппа вводится в полимер, восстанавливающий конец которого не окислен, взаимодействием, по меньшей мере, одной гидроксигруппы полимера со сложным карбоновым диэфиром.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где А представляет собой реакционноспособную карбоксигруппу и где А вводится в полимер, восстанавливающий конец которого не окислен, взаимодействием, по меньшей мере, одной гидроксигруппы полимера, по меньшей мере, с одним сложным карбоновым диэфиром RB-O-(C=O)-O-RC, где RB и RC могут одинаковыми или различными.
В соответствии с другим вариантом осуществления настоящего изобретения, полимер, восстанавливающий конец которого не окислен, взаимодействует, по меньшей мере, при одной гидроксигруппе с азолидом, таким как карбонилдиимидазол, карбонил-ди-(1,2,4-триазол) или карбонилдибензимидазол, для получения полимера, имеющего реакционноспособную карбоксигруппу.
В качестве соединений сложных карбоновых диэфиров могут использоваться соединения, спиртовые компоненты которых представляют собой независимо N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходяще замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол или 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол.
Особенно предпочтительными являются симметричные соединения сложных карбоновых диэфиров, причем RB и RC, таким образом, одинаковы. Спиртовой компонент сложного карбонового диэфира предпочтительно выбран из группы, состоящей из N-гидроксисукцинимида, сульфонированного N-гидроксисукцинимида, N-гидроксибензотриазола и нитро- и галоген-замещенных фенолов. Среди других, предпочтительны нитрофенол, динитрофенол, трихлорфенол, трифторфенол, пентахлорфенол и пентафторфенол. Особенно предпочтительными являются N,N'-дисукцинимидилкарбонат и сульфо-N,N'-дисукцинимидилкарбонат, причем особенно предпочтителен N,N'-дисукцинимидилкарбонат.
Поэтому настоящее изобретение также относится к производному гидроксиалкилкрахмала и к способу его получения, предпочтительно, производного гидроксиэтилкрахмала, где, по меньшей мере, одна гидроксигруппа, предпочтительно, по меньшей мере, 2 гидроксигруппы указанного крахмала, были подвергнуты взаимодействию с соединением сложного карбонового диэфира для получения соответствующего реакционноспособного сложного эфира.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие полимера, восстанавливающий конец которого не окислен, по меньшей мере, с одним соединением сложного карбонового диэфира проводится при температуре от 2 до 40°С, предпочтительнее от 10 до 30°С и, в частности, от 15 до 25°С, и при предпочтительном времени взаимодействия от 0,5 до 5 ч, предпочтительнее от 1 до 3 ч, а особенно предпочтительно от 2 до 3 ч.
Молярное соотношение между сложным карбоновым диэфиром и/или азолидом, предпочтительно сложного карбонового диэфира:полимера, зависит от степени замещения полимера в отношении количества гидроксигрупп, вступивших во взаимодействие с соединением сложного карбонового диэфира, относительно количества гидроксигрупп, присутствующих в не вступившем во взаимодействие полимере.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, молярное соотношение сложного карбонового диэфира и звеньев ангидроглюкозы находится в диапазоне от 1:2 до 1:1000, предпочтительно от 1:3 до 1:100, а особенно предпочтительно от 1:10 до 1:50, для получения степени замещения в диапазоне от 0,5 до 0,001, предпочтительно от 0,33 до 0,01 и особенно предпочтительно от 0,1 до 0,02. Степень замещения определяется посредством УФ спектроскопии.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие полимера, восстанавливающий конец которого не окислен, по меньшей мере, с одним соединением сложного карбонового диэфира проводится, по меньшей мере, в одном апротонном растворителе, особенно предпочтительно в безводном апротонном растворителе, имеющем содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями, среди других, являются диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смесь двух или более из них.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где взаимодействие, по меньшей мере, одной гидроксигруппы полимера, восстанавливающий конец которого не окислен, со сложным карбоновым диэфиром для получения реакционноспособной сложноэфирной группы А, проводится в безводном апротонном полярном растворителе, причем растворитель предпочтительно представляет собой диметилацетамид, диметилформамид или их смесь.
Взаимодействие реакционноспособного полимера, включающего, по меньшей мере, одну реакционноспособную сложноэфирную группу, предпочтительно, по меньшей мере, 2 реакционноспособные сложноэфирные группы, для получения, по меньшей мере, одной амидной связи, предпочтительно, по меньшей мере, двух амидных связей, можно проводить объединением реакционной смеси препарата реакционноспособного полимера, т.е. без выделения реакционноспособного полимера, включающего, по меньшей мере, 5, предпочтительнее, по меньшей мере, 10 и еще предпочтительнее, по меньшей мере, 15% мас. реакционноспособного полимера, с водным раствором белка. Предпочтительные водные растворы белка включают от 0,05 до 10, предпочтительнее от 0,5 до 5 и особенно предпочтительно от 0,5 до 2% мас. белка при предпочтительном рН от 7,0 до 9, предпочтительнее от 7,5 до 9, и особенно предпочтительно от 7,5 до 8,5.
В соответствии с настоящим изобретением, можно также очистить реакционноспособный полимер, по меньшей мере, одним, предпочтительно множественным, осаждением, по меньшей мере, одним осаждающим агентом, таким как безводный этанол, изопропанол и/или ацетон, для получения твердого вещества, включающего, по меньшей мере, 20, предпочтительнее, по меньшей мере, 50, а еще предпочтительнее, по меньшей мере, 80% мас. реакционноспособного полимера.
Очищенный реакционноспособный полимер можно добавить к водному раствору белка. Можно также добавить раствор очищенного реакционноспособного полимера к водному раствору белка.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие реакционноспособного полимера с белком для получения, по меньшей мере, одной, предпочтительно, по меньшей мере, двух амидных связей, можно проводить при температуре от 2 до 40°С, предпочтительнее от 5 до 35°С и, в частности, от 10 до 30°С и предпочтительном рН от 7,5 до 9,5, предпочтительно от 7,5 до 9 и особенно предпочтительно от 7,5 до 8,5, при предпочтительном времени взаимодействия от 0,5 до 5 ч, предпочтительнее от 0,5 до 3 ч, а особенно предпочтительно от 0,5 до 1 ч, причем молярное соотношение реакционноспособного сложного эфира полимера:белка составляет предпочтительно от 1:1 до 70:1, предпочтительнее от 5:1 до 50:1 и особенно предпочтительно от 10:1 до 50:1.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, получают полимеры с замещенными несколькими или множественными белками, где белковые молекулы связаны с полимером через амидную связь.
Степень замещения белковых молекул (PDS), используемая в контексте настоящего изобретения, относится к части глюкозных частей, связанных с белком, относительно всех глюкозных частей, содержащихся в HAS, предпочтительно HES.
PDS находится в диапазоне от 0,001 до 1, предпочтительно от 0,005 до 0,5, предпочтительнее от 0,005 до 0,2.
В соответствии с другим вариантом осуществления настоящего изобретения, полимер, имеющий реакционноспособную карбоксигруппу А, полученную в результате взаимодействия, по меньшей мере, одной гидроксигруппы полимера с одним из указанных выше соединений, предпочтительно, по меньшей мере, с одним из соединений сложного карбонового диэфира, может быть соединен с функциональной группой Z белка, по меньшей мере, через одно линкерное соединение. В случае использования линкерного соединения, указанное соединение представляет собой, по меньшей мере, бифункциональное соединение, имеющее, по меньшей мере, одну функциональную группу F1, способную взаимодействовать с функциональной группой А полимерного производного и, по меньшей мере, одну функциональную группу F2, способную взаимодействовать с функциональной группой Z белка или функциональной группой F2, способной быть химически модифицированной для взаимодействия с функциональной группой Z белка. Химическая модификация может представлять собой, например, взаимодействие функциональной группы F2 с функциональной группой F3 еще одного линкерного соединения или окисление или восстановление подходящей функциональной группы F2. В случае использования, по меньшей мере, одного линкерного соединения, взаимодействие не ограничивается аминогруппой белка, но, в зависимости от химической природы функциональных групп линкерного соединения или линкерных соединений, может использоваться для образования связи с каждой подходящей функциональной группой белка, такой как карбоксигруппа, реакционноспособная карбоксигруппа, альдегидная группа, кетогруппа, тиогруппа, аминогруппа или гидроксигруппа. В случае использования двух линкерных соединений используется первое линкерное соединение, имеющее, по меньшей мере, одну функциональную группу F1, способную взаимодействовать с реакционноспособной карбоксигруппой А полимера, такой как аминогруппа, тиогруппа, гидроксигруппа, или карбоксигруппа. Более того, первое линкерное соединение имеет, по меньшей мере, одну другую функциональную группу F2, которая способна взаимодействовать, по меньшей мере, с одной функциональной группой F3 второго линкерного соединения. В качестве функциональной группы F2 следует упомянуть, среди других, следующие функциональные группы:
- С-С-двойные связи или С-С-тройные связи, или ароматические С-С-связи;
- тиогруппа или гидроксигруппы;
- гидразид алкилсульфоновой кислоты, гидразид арилсульфоновой кислоты;
- 1,2-диолы;
- 1,2-амиоспирты;
- 1,2-аминотиоспирты;
- азиды;
- аминогруппа -NH2 или производные аминогрупп, включающие структурную единицу -NH-, такие как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы, или алкариламиногруппы;
- гидроксиламиногруппа -O-NH2, или производные гидроксиламиногруппы, включающие структурную единицу -O-NH-, такие как гидроксиалкиламиногруппы, гидроксилариламиногруппы, гидроксиаралкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогруппы, арилоксиаминогруппы, аралкилоксиаминогруппы или алкарилоксиаминогруппы, каждая из которых включает структурную единицу -NH-O-;
- остатки, имеющие карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такое как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;

где F3 представляет собой группу, способную образовывать химическую связь с одной из указанных выше групп, и предпочтительно выбрана из указанных выше групп. Более того, второе линкерное соединение имеет, по меньшей мере, одну функциональную группу, которая способна взаимодействовать с функциональной группой Z белка, которая представляет собой, например, аминогруппу, тиогруппу, карбоксигруппу, реакционноспособную карбоксигруппу, альдегидную группу, кетогруппу или гидроксигруппу. В случае использования одной связывающей группы для ковалентного связывания с полимером и белком, полимер может взаимодействовать со связывающим соединением, и полученное полимерное производное взаимодействует с белком, или белок может взаимодействовать со связывающим соединением, и полученное производное белка взаимодействует с полимером. В случае использования двух связывающих соединений L1 и L2, можно обеспечить взаимодействие полимера с L1, взаимодействие полученного полимерного производного с L2 и взаимодействие полученного полимерного производного с белком, или взаимодействие белка с L2, взаимодействие полученного белкового производного с L1 и взаимодействие полученного белкового производного с полимером. Можно также обеспечить взаимодействие полимера с L1, взаимодействие белка с L2 и взаимодействие полимерного производного с белковым производным. Кроме того, можно обеспечить взаимодействие L1 с L2, взаимодействие полученного соединения с полимером и полученного полимерного производного с белком. Кроме того, можно обеспечить взаимодействие L1 с L2, взаимодействие полученного соединения с белком и полученного белкового производного с полимером.
В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, функциональная группа Z белка представляет собой аминогруппу, а функциональная группа А полимера или его производное представляет собой альдегидную группу, кетогруппу или группу полуацеталя. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, функциональная группа Z и функциональная группа А взаимодействуют посредством реакции восстановительного аминирования.
Реакция восстановительного аминирования в соответствии с изобретением, где полимер или полимерное производное ковалентно связано, по меньшей мере, через альдегидную группу или кетогруппу, или группу полуацеталя, по меньшей мере, с одной аминогруппой белка, предпочтительно проводится при температуре от 0 до 40°С, предпочтительнее от 0 до 25°С и особенно предпочтительно от 4 до 21°С. Время взаимодействия предпочтительно находится в диапазоне от 0,5 до 72 ч, предпочтительнее от 2 до 48 ч и особенно предпочтительно от 4 до 7 ч. В качестве растворителя для взаимодействия предпочтительна водная среда.
Таким образом, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при температуре от 4 до 21°С.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится в водной среде.
Таким образом, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при температуре от 4 до 21°С в водной среде.
Термин «водная среда», используемый в контексте настоящего изобретения, относится к растворителю или смеси растворителей, включающей воду в диапазоне от, по меньшей мере, 10% мас., предпочтительнее, по меньшей мере, 20% мас., предпочтительнее, по меньшей мере, 30% мас., предпочтительнее, по меньшей мере, 40% мас., предпочтительнее, по меньшей мере, 50% мас., предпочтительнее, по меньшей мере, 60% мас., предпочтительнее, по меньшей мере, 70% мас., предпочтительнее, по меньшей мере, 80% мас., еще предпочтительнее, 90% мас. или до 100% мас. на основании массы используемого растворителя. Предпочтительной средой взаимодействия является вода.
Величина рН среды взаимодействия в целом находится в диапазоне от 4 до 9, или от 4 до 8, или от 4 до 7,3.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, рН, при котором проводится реакция восстановительного аминирования, составляет менее 7,3, предпочтительно меньше или равен 7, а наиболее предпочтительно менее 7, т.е. в кислотном диапазоне. Поэтому предпочтительные диапазоны составляют от 3 до менее 7, предпочтительнее от 3,5 до 6,5, еще предпочтительнее от 4 до 6, еще предпочтительнее от 4,5 до 5,5, а особенно предпочтительно примерно 5,0, т.е. 4,6, или 4,7, или 4,8, или 4,9, или 5,0, или 5,1, или 5,2, или 5,3, или 5,4. Предпочтительными диапазонами, среди других, являются от 3 до 6,9, или от 3 до 6,5, или от 3 до 6, или от 3 до 5,5, или от 3 до 5, или от 3 до 4,5, или от 3 до 4, или от 3 до 3,5, или от 3,5 до 6,9, или от 3,5 до 6,5, или от 3,5 до 6, или от 3,5 до 5,5, или 3,5 до 5, или от 3,5 до 4,5, или от 3,5 до 4, или от 4 до 6,9, или от 4 до 6,5, или от 4 до 6, или от 4 до 5,5, или от 4 до 5, или от 4 до 4,5, или от 4,5 до 6,9, или от 4,5 до 6,5, или от 4,5 до 6, или от 4,5 до 5,5, или от 4,5 до 5, или от 5 до 6,9, или от 5 до 6,5, или от 5 до 6, или от 5 до 5,5, или от 5,5 до 6,9, или от 5,5 до 6,5, или от 5,5 до 6, или от 6 до 6,9, или от 6 до 6,5, или от 6,5 до 6,9.
Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при рН 7 или менее, предпочтительно при рН 6 или менее.
Таким образом, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при температуре от 4 до 21°С при рН 7 или менее, предпочтительно 6 или менее.
Следовательно, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится в водной среде при рН 7 или менее, предпочтительно 6 или менее.
Соответственно, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при температуре от 4 до 21°С в водной среде при рН 7 или менее, предпочтительно 6 или менее.
Молярное соотношение полимерного производного и белка, используемое для взаимодействия, находится предпочтительно в диапазоне от 200:1 до 5:1, предпочтительнее от 100:1 до 10:1, а особенно предпочтительно от 75:1 до 20:1.
К удивлению, было обнаружено, что было возможно, особенно при предпочтительных диапазонах рН, указанных выше, особенно при рН ниже 7 и больше или равном 4, осуществлять взаимодействие полимерного производного преимущественно с аминогруппой, расположенной на N конце белка. Термин «преимущественно», используемый в контексте настоящего изобретения, относится варианту осуществления, где, по меньшей мере, 80%, предпочтительно, по меньшей мере, 85% имеющихся N-концевых аминогрупп взаимодействуют посредством восстановительного аминирования. Можно также осуществлять взаимодействие, по меньшей мере, 90% или, по меньшей мере, 95% или, по меньшей мере, 96%, или, по меньшей мере, 97%, или, по меньшей мере, 98%, или, по меньшей мере, 99% имеющихся N-концевых аминогрупп. Хотя нельзя полностью исключить соединение с аминогруппами, отличными от N-концевой аминогруппы, считается, что соединение посредством восстановительного аминирования в соответствии с настоящим изобретением при рН ниже 7, предпочтительно ниже 6, происходило по существу селективно у N-концевой аминогруппы.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где белок включает N-концевую аминогруппу и, по меньшей мере, еще одну аминогруппу, указанный конъюгат включает полимер, преимущественной связанный с N-концевой аминогруппой.
В соответствии с особенно предпочтительным вариантом осуществления, настоящее изобретение относится к способу сочетания гидроксиалкилкрахмала, функционализированного альдегидной или кетогруппой, или полуацеталем, или производного гидроксиалкилкрахмала, функционализированного альдегидной или кетогруппой, или полуацеталем, с N-концевой аминогруппой белка, причем указанный способ включает воздействие на указанный гидроксиалкилкрахмал или его производное реакции восстановительного аминирования при рН ниже 7, предпочтительно ниже 6, причем указанная реакция восстановительного аминирования проводится предпочтительно в водной среде.
В соответствии с настоящим изобретением, предпочтителен гидроксиалкилкрахмал, функционализированный альдегидом, или производное гидроксиалкилкрахмала, функционализированное альдегидом.
В соответствии с особенно предпочтительным вариантом осуществления, настоящее изобретение относится к способу соединения гидроксиалкилкрахмала, функционализированного альдегидной или кетогруппой, или полуацеталем, или производного гидроксиалкилкрахмала, функционализированного альдегидной или кетогруппой, или полуацеталем, с N-концевой аминогруппой белка, причем указанный способ включает воздействие на указанный гидроксиалкилкрахмал или его производное реакции восстановительного аминирования при рН ниже 7, предпочтительно ниже 6, причем указанная реакция восстановительного аминирования проводится предпочтительно в водной среде, причем используемый гидроксиэтилкрахмал предпочтительно представляет собой гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа, и DS примерно 0,7.
Реакция полимерного производного и белка между альдегидной группой или кетогруппой или полуацетальной группой и аминогруппой представляет собой восстановительное аминирование, где получается основание Шиффа. В последующем после взаимодействия это основание может быть восстановлено, по меньшей мере, одним восстановительным агентом для получения устойчивой связи между полимерным производным и белком. Также можно проводить реакцию в присутствии, по меньшей мере, одного восстановительного агента. В соответствии с предпочтительным вариантом осуществления, реакция окислительного аминирования проводится в присутствии, по меньшей мере, одного восстановительного агента.
Предпочтительными восстанавливающими агентами являются боргидрид натрия, цианоборгидрид, соединения комплекса органического борана, такого как комплекс 4-(диметиламин)пиридинборана, комплекс N-этилдиизопропиламинборана, комплекс N-этилморфолинборана, комплекс N-метилморфолинборана, комплекс N-фенилморфолинборана, комплекс лутидинборана, комплекс триэтиламинборана или комплекс триметиламинборана. Особенно предпочтительным является цианоборгидрид натрия.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится в присутствии NaCNBH3.
Следовательно, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится в водной среде при рН 7 или менее, предпочтительно 6 или менее, в присутствии восстановительного агента, предпочтительно NaCNBH3.
Соответственно, настоящее изобретение также относится к способу и конъюгату, как описано выше, где восстановительное аминирование проводится при температуре от 4 до 21°С в водной среде при рН 7 или менее, предпочтительно 6 или менее, в присутствии восстановительного агента, предпочтительно NaCNBH3.
Молярное соотношение полимерного производного и белка, используемое для взаимодействия, находится предпочтительно в диапазоне от 200:1 до 10:1, предпочтительнее от 100:1 до 10:1, а особенно предпочтительно от 75:1 до 20:1.
Поэтому, настоящее изобретение также относится к способу получения конъюгата, причем указанный способ включает взаимодействие полимера или полимерного производного, включающего альдегидную группу, в водной среде с аминогруппой белка в присутствии восстановительного агента, причем восстановительный агент предпочтительно представляет собой NaCNBH3.
В соответствии с первым предпочтительным вариантом осуществления настоящего изобретения, в соответствии с которым полимер включает, по меньшей мере, 2 альдегидные группы, которые вводятся в полимер открывающей кольцо реакцией окисления, полимер предпочтительно включает, по меньшей мере, одну структуру в соответствии с формулой
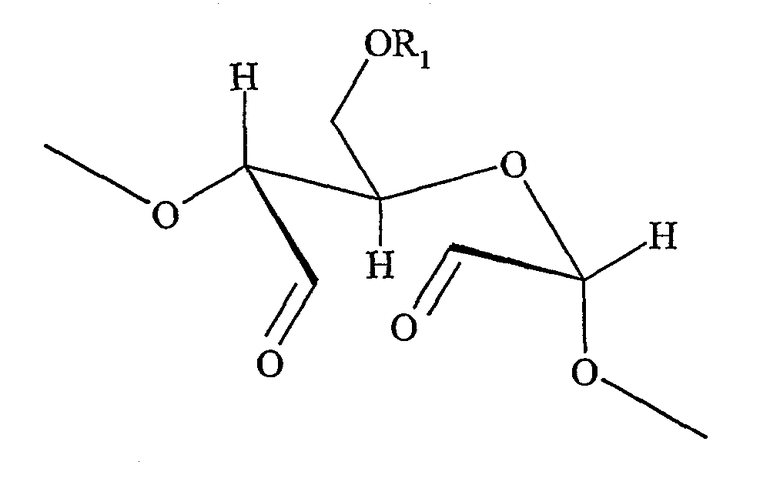
В соответствии с этим вариантом осуществления настоящего изобретения, может использоваться каждый агент окисления или комбинация агентов окисления, который способен к окислению, по меньшей мере, одного сахаридного кольца полимера для получения раскрытого сахаридного кольца, имеющего, по меньшей мере, одну, предпочтительно, по меньшей мере, 2 альдегидных группы. Эта реакция иллюстрируется следующей схемой взаимодействия, которая показывает сахаридное кольцо полимера, которое окисляется для получения открытого кольца, имеющего 2 альдегидных группы:
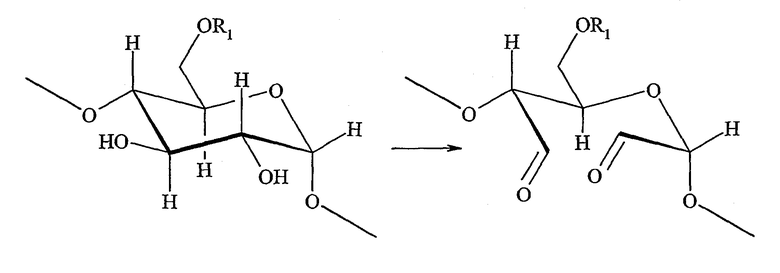
Подходящими окисляющими агентами, среди других, являются периодаты, такие как периодаты щелочных металлов или смеси двух или более из них, причем предпочтительны периодат натрия и периодат калия.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер подвергнут открывающей кольцо реакции окисления с использованием периодата для получения полимерного производного, имеющего, по меньшей мере, одну, предпочтительно, по меньшей мере, 2 альдегидных группы.
Для этой реакции окисления полимер может использоваться с его восстанавливающим концом или в окисленной, или в неокисленной форме, причем предпочтительна неокисленная форма.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер используется с его восстанавливающим концом в неокисленной форме.
Температура взаимодействия находится в предпочтительном диапазоне от 0 до 40°С, предпочтительнее от 0 до 25°С и особенно предпочтительно от 0 до 5°С. Время взаимодействия находится в предпочтительном диапазоне от 1 мин до 5 ч, а особенно предпочтительно от 10 мин до 4 ч. В зависимости от желательной степени окисления, т.е. количества альдегидных групп, полученных в результате реакции окисления, можно соответствующим образом выбрать молярное соотношение периодата и полимера.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где реакция окисления, приводящая к раскрытию кольца, проводится при температуре от 0 до 5°С.
Реакция окисления полимера периодатом предпочтительно проводится в водной среде, наиболее предпочтительно в воде.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где реакция окисления, приводящая к раскрытию кольца, проводится в водной среде. Подходящую величину рН реакционной смеси можно регулировать добавлением, по меньшей мере, одного подходящего буфера. Среди предпочтительных буферов можно упомянуть буфер ацетата натрия, фосфатный или боратный буферы.
Гидроксиэтилкрахмал, подвергнутый указанной реакции окисления с раскрытием кольца, представляет собой предпочтительно гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа, и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа, и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа, и DS примерно 0,7.
Полученное полимерное производное может быть очищено из реакционной смеси, по меньшей мере, одним подходящим способом. При необходимости полимерное производное может осаждаться перед выделением, по меньшей мере, одним подходящим способом.
Если полимерное производное сначала осаждается, можно, например, обеспечить контакт реакционной смеси, по меньшей мере, с одним растворителем или смесью растворителей, присутствующих в реакционной смеси, при подходящих температурах. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, где водная среда, предпочтительно вода, используется в качестве растворителя, реакционная смесь контактирует с 2-пропанолом или со смесью ацетона и этанола, предпочтительно смесью 1:1 (об./об.) при температуре, предпочтительно в диапазоне от -20 до +50°С, а особенно предпочтительно от -20 до 25°С.
Выделение полимерного производного можно проводить подходящим способом, который может включать одну или больше стадий. В соответствии с предпочтительными вариантами осуществления настоящего изобретения, полимерное производное сначала отделяется от реакционной смеси или смеси реакционной смеси, например водной смесью 2-пропанола, подходящим способом, таким как центрифугирование или фильтрация. На второй стадии отделенное полимерное производное может быть подвергнуто дальнейшей обработке, такой как диализ, подобный последующей обработке, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография с обращенной фазой, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация. В соответствии с еще более предпочтительным вариантом реализации, отделенное полимерное производное сначала диализируется, предпочтительно против воды, а затем лиофилизируется до тех пор, пока содержание растворителя продукта взаимодействия не будет достаточно низким, в соответствии с желательными спецификациями продукта. Лиофилизиацию можно проводить при температуре от 20 до 35°С, предпочтительно от 20 до 30°С.
В соответствии с предпочтительным вариантом осуществления, окисленный полимер, полученный в результате реакции окисления, очищается с использованием, по меньшей мере, одного подходящего способа, такого как ультрафильтрация и/или диализ, например, для удаления нежелательных солей с низкой молекулярной массой и полимерных компонентов, предоставляя посредством этого средства регуляции диапазона молекулярной массы окисленного полимера.
Окисленный полимер может использоваться непосредственно для взаимодействия с белком или подходяще выделяется на первой стадии, например, лиофилизацией, и растворяется в воде для конъюгации с белком на второй стадии. Что касается соединения, по меньшей мере, одной аминогруппы белка, по меньшей мере, с одной альдегидной группой полимера восстановительным аминированием, то делается ссылка на приведенное выше подробное описание, касающееся определенных параметров взаимодействия реакции восстановительного аминирования, таких как рН или температура.
В соответствии со вторым предпочтительным вариантом осуществления, полимер взаимодействует, по меньшей мере, с бифункциональным соединением, включающим, по меньшей мере, одну функциональную группу М, способную взаимодействовать с полимером, и, по меньшей мере, одну функциональную группу Q, которая представляет собой альдегидную группу или кетогруппу, или полуацетальную группу, и которая взаимодействует с аминогруппой белка восстановительным аминированием.
Окисленный полимер может использоваться непосредственно для взаимодействия с белком или подходяще выделяется на первой стадии, например, лиофилизацией, и повторно растворяется в воде для конъюгации с белком на второй стадии. Что касается соединения, по меньшей мере, одной аминогруппы белка, по меньшей мере, с одной альдегидной группой полимера восстановительным аминированием, то делается ссылка на приведенное выше подробное описание, касающееся определенных параметров взаимодействия реакции восстановительного аминирования, таких как рН или температура. В соответствии с особенно предпочтительными вариантами осуществления настоящего изобретения, восстановительное аминирование предпочтительно проводится при температуре от 0 до 5°С, например примерно 4°С, при рН примерно от 4,5 до 5,5, например примерно 5,0, и в течение времени взаимодействия примерно от 20 до 30 ч, например примерно 24 ч.
В соответствии со вторым предпочтительным вариантом осуществления, полимер взаимодействует, по меньшей мере, с бифункциональным соединением, включающим, по меньшей мере, одну функциональную группу М, способную взаимодействовать с полимером, и, по меньшей мере, одну функциональную группу Q, которая представляет собой альдегидную группу, кетогруппу или полуацетальную группу, и которая взаимодействует с аминогруппой белка восстановительным аминированием.
Предпочтительно использовать соединение, имеющее, кроме альдегидной группы или кетогруппы, или полуацетальной группы, по меньшей мере, одну карбоксигруппу или, по меньшей мере, одну реакционноспособную карбоксигруппу, предпочтительно одну карбоксигруппу или одну реакционноспособную карбоксигруппу. Альдегидная группа или кетогруппа, или полуацетальная группа и карбоксигруппа, или реакционноспособная карбоксигруппа может быть отделена подходящим промежуточным звеном. Среди других, промежуточное звено может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 2 до 10, предпочтительнее от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, и особенно предпочтительно от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь или арильную группу, или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или может представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой арильный остаток, имеющий от 5 до 7, а предпочтительно 6 атомов углерода. Наиболее предпочтительно углеводородный остаток представляет собой бензольный остаток. В соответствии с этим предпочтительным вариантом осуществления, карбоксигруппа и альдегидная группа может располагаться в бензольном кольце в 1,4-положении, 1,3-положении или 1,2-положении, причем предпочтительным является 1,4-положение.
В качестве реакционноспособной карбоксигруппы можно упомянуть реакционноспособный сложный эфир, изотиоцианаты или изоцианат. Предпочтительные реакционноспособные сложные эфиры получают из N-гидроксисукцинимидов, таких как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенных фенолов, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол или 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N-гидроксисукцинимиды, причем особенно предпочтительны N-гидроксисукцинимид и сульфо-N-гидроксисукцинимид. Все спирты могут использоваться отдельно или в виде подходящей комбинации двух или более из них. В качестве реакционноспособного сложного эфира особенно предпочтительными являются сложный пентафторфениловый эфир и сложный эфир N-гидроксисукцинимида.
Таким образом, в соответствии с предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимер взаимодействует с формилбензойной кислотой.
В соответствии с другим предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимер взаимодействует со сложным пентафторфениловым эфиром формилбензойной кислоты.
В соответствии с еще одним предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимер взаимодействует со сложным N-гидроксисукцинимидным эфиром формилбензойной кислоты.
В соответствии с еще одним предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимер взаимодействует с 4-(4-формил-3,5-диметоксифенокси)масляной кислотой.
Гидроксиэтилкрахмал, подвергнутый взаимодействию с соединением, включающим М, причем М предпочтительно представляет собой карбоксигруппу или реакционноспособную карбоксигруппу, а Q представляет собой альдегидную группу или кетогруппу, или полуацетальную группу, представляет собой наиболее предпочтительно гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7. Возможны также гидроксиэтилкрахмалы, имеющие среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7. Особенно предпочтительно гидроксиалкилкрахмал, а еще предпочтительнее гидроксиэтилкрахмал используется с его восстанавливающим концом в окисленной форме.
Полученное полимерное производное с альдегидной группой или кетогруппой, или полуацетальной группой в последующем взаимодействует с аминогруппой белка через восстановительное аминирование. Что касается соединения, по меньшей мере, одной аминогруппы белка, по меньшей мере, с одной альдегидной группой или кетогруппой, или полуацетальной группой полимера восстановительным аминированием, то делается ссылка на приведенное выше подробное описание, касающееся определенных параметров взаимодействия, таких как рН или температура. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, взаимодействие с аминогруппой белка предпочтительно проводится при температуре от 0 до 40°С, предпочтительнее от 0 до 25°С, и особенно предпочтительно от 4 до 21°С. Время взаимодействия предпочтительно находится в диапазоне от 30 мин до 72 ч, предпочтительнее от 2 до 48 ч и особенно предпочтительно от 4 до 17 ч. В качестве растворителя для взаимодействия предпочтительна водная среда. Величина рН реакционной среды находится предпочтительно в диапазоне от 4 до 9, предпочтительнее от 4 до 8 и особенно предпочтительно от 4,5 до 5,5.
В соответствии с третьим предпочтительным вариантом осуществления, полимер взаимодействует на его необязательно окисленном восстанавливающем конце, по меньшей мере, с бифункциональным соединением, включающим аминогруппу М и функциональную группу Q, где указанная аминогруппа М взаимодействует с необязательно окисленным восстанавливающим концом полимера, и где функциональная группа Q химически модифицирована для получения функционализированного альдегидом полимерного производного, которое взаимодействует с аминогруппой белка восстановительным аминированием.
Что касается функциональной группы Q, то, среди других, нужно указать следующие функциональные группы:
- С-С-двойные связи или С-С-тройные связи, или ароматические С-С-связи;
- тиогруппа или гидроксигруппы;
- гидразид алкилсульфоновой кислоты, гидразид арилсульфоновой кислоты;
- 1,2-диолы;
- 1,2-аминотиоспирты;
- азиды;
- 1,2-аминоспирты;
- аминогруппа -NH2 или производные аминогрупп, включающие структурную единицу -NH-, такие как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы, или алкариламиногруппы;
- гидроксиламиногруппа -O-NH2, или производные гидроксиламиногруппы, включающие структурную единицу -O-NH-, такие как гидроксиалкиламиногруппы, гидроксилариламиногруппы, гидроксиаралкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогруппы, арилоксиаминогруппы, аралкилоксиаминогруппы, или алкарилоксиаминогруппы, каждая из которых включает структурную единицу -NH-O-;
- остатки, имеющие карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такое как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;

В соответствии с предпочтительным вариантом осуществления настоящего изобретения, термин «функциональная группа Q» относится к функциональной группе Q, которая включает химическую структуру -NH-.
В соответствии с одним предпочтительным вариантом осуществления настоящего изобретения, эта функциональная группа М представляет собой группу, имеющую структуру R'-NH-, где R' представляет собой водород или алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток, где циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток может быть соединен непосредственно с группой NH или, в соответствии с другим вариантом осуществления, может быть соединен кислородным мостиком с группой NH. Алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остатки могут быть подходяще замещенными. В качестве предпочтительных заместителей можно упомянуть галогены, такие как F, Cl или Br. Особенно предпочтительными остатками R' являются водород, алкильная и алкоксигруппы, а еще предпочтительнее являются водород и незамещенные алкильная и алкоксигруппы.
Среди алкильной и алкоксигруппы предпочтительны группы с 1, 2, 3, 4, 5 или 6 атомами С. Более предпочтительными являются метильная, этильная, пропильная, озопропильная, метокси, этокси, пропокси и изопропоксигруппы. Особенно предпочтительными являются метил, этил, метокси, этокси, и особенное предпочтение отдается метилу или метокси.
В соответствии с другим вариантом осуществления настоящего изобретения, функциональная группа М имеет структуру R'-NH-R”, где R” предпочтительно включает структурную единицу -NH- и/или структурную единицу -(C=G)-, где G представляет собой O или S и/или структурную единицу -SO2-. Конкретными примерами функциональной группы R” являются

где, если G присутствует дважды, она представляет собой независимо O или S.
Поэтому настоящее изобретение также относится к способу и конъюгату, как указано выше, где функциональная группа М выбрана из группы, состоящей из

где G представляет собой O или S и, если присутствует дважды, независимо O или S, и R' представляет собой метил.
В соответствии с особенно предпочтительными вариантом осуществления настоящего изобретения, функциональная группа М представляет собой аминогруппу -NH2.
Термин «аминогруппа Q» относится к функциональной группе Q, которая включает химическую структуру -NH-.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, функциональная группа Q представляет собой группу, имеющую структуру R'-NH-, где R' представляет собой водород или алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток, где циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток может быть соединен непосредственно с группой NH или, в соответствии с другим вариантом осуществления, может быть соединен кислородным мостиком с группой NH. Алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остатки могут быть подходяще замещенными. В качестве предпочтительных заместителей можно упомянуть галогены, такие как F, Cl или Br. Особенно предпочтительными остатками R' являются водород, алкильная и алкоксигруппы, а еще предпочтительнее являются водород и незамещенные алкильная и алкоксигруппы.
Среди алкильной и алкоксигрупп предпочтительны группы с 1, 2, 3, 4, 5 или 6 атомами С. Более предпочтительными являются метильная, этильная, пропильная, изопропильная, метокси, этокси, пропокси и изопропоксигруппы. Особенно предпочтительными являются метил, этил, метокси, этокси, и особенное предпочтение отдается метилу или метокси.
В соответствии с другим вариантом осуществления настоящего изобретения, функциональная группа Q имеет структуру R'-NH-R”, где R” предпочтительно включает структурную единицу -NH- и/или структурную единицу -(C=G)-, где G представляет собой O или S и/или структурную единицу -SO2-. В соответствии с более предпочтительными вариантами осуществления, функциональная группа R” выбрана из группы, состоящей из

где, если G присутствует дважды, она представляет собой независимо O или S.
Поэтому настоящее изобретение также относится к способу и конъюгату, как указано выше, где функциональная группа Q выбрана из группы, состоящей из

где G представляет собой O или S и, если присутствует дважды, независимо O или S, и R' представляет собой метил.
В соответствии с особенно предпочтительными вариантом осуществления настоящего изобретения, функциональная группа Q представляет собой аминогруппу -NH2.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, и М, и Q группа включают аминогруппу -NH-. В соответствии с особенно предпочтительным вариантом осуществления, и М, и Q группа представляют собой аминогруппу -NH2.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, соединение, включающее М и Q, представляет собой гомобифункциональное соединение, предпочтительнее гомобифункциональное соединение, включающее в качестве функциональных групп М и Q, наиболее предпочтительно аминогруппу -NH2, или в соответствии с другими вариантами осуществления, гидроксиламиногруппу -O-NH2, или группу

причем G предпочтительно представляет собой О. Конкретными примерами для этих соединений, включающих M и Q, являются
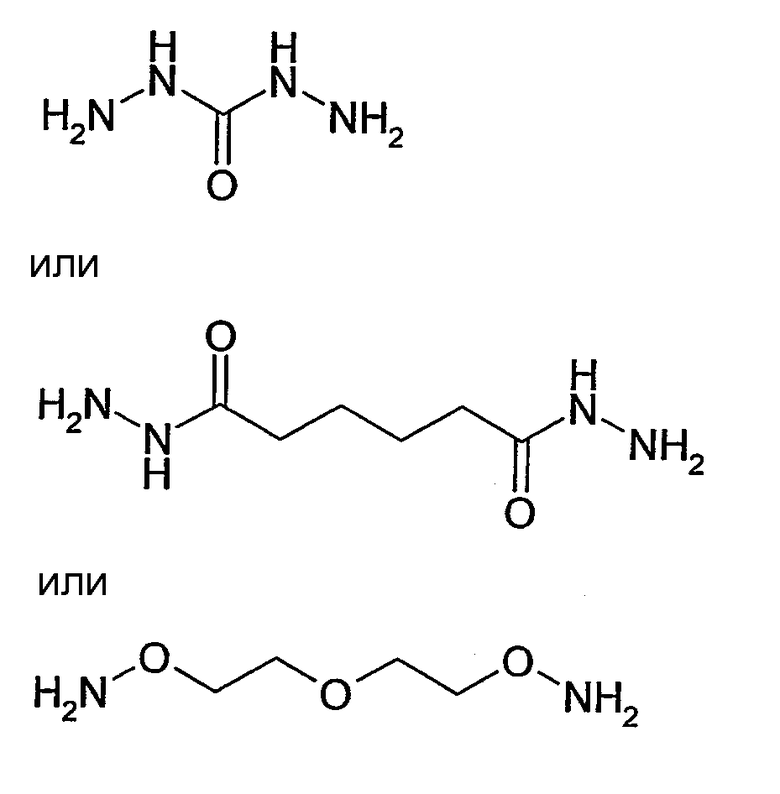
Гидроксиэтилкрахмал, подвергнутый взаимодействию с соединением, включающим М, причем М предпочтительно представляет собой аминогруппу -NH-, а предпочтительнее, представляет собой аминогруппу -NH2, еще предпочтительнее, и М, и Q, включающие аминогруппу -NH-, а особенно предпочтительно, и М, и Q, включающие аминогруппу -NH2, представляет собой предпочтительно гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7. Возможны также гидроксиэтилкрахмалы, имеющие среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7.
В случае, когда и М, и Q представляет собой аминогруппу -NH2, М и Q могут быть отделены любым подходящим промежуточным соединением. Среди других, промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно, от 1 до 40, предпочтительнее, от 1 до 20, предпочтительнее, от 2 до 10, предпочтительнее, от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно, от 1 до 8, а особенно предпочтительно, от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь или арильную группу или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или представлять собой аралкильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой алкильную цепь из 1 до 20, предпочтительно, от 2 до 10, предпочтительнее, от 2 до 6, а особенно предпочтительно, от 2 до 4 атомов углерода.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер взаимодействует с 1,4-диаминбутаном, 1,3-диаминпропаном или 1,2-диаминэтаном для получения полимерного производного.
Взаимодействие, по меньшей мере, бифункционального соединения, включающего М и Q, с полимером предпочтительно проводится при температуре от 0 до 100°С, предпочтительнее от 4 до 80°С, а особенно предпочтительно от 20 до 80°С; время взаимодействия предпочтительно находится в диапазоне от 4 ч до 7 сут, предпочтительнее от 10 ч до 5 сут и особенно предпочтительно от 17 ч до 4 сут. Молярное соотношение, по меньшей мере, бифункционального соединения и полимера находится предпочтительно в диапазоне от 10 до 200, в частности от 50 до 100.
В качестве растворителя для взаимодействия, по меньшей мере, бифункционального соединения с полимером, предпочтительнее, по меньшей мере, один апротонный растворитель, особенно предпочтительно безводный апротонный растворитель, имеющий содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями являются, среди других, диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси из двух или более из них.
В качестве растворителя для взаимодействия, по меньшей мере, бифункционального соединения с полимером можно также использовать водную среду.
В соответствии с предпочтительным вариантом осуществления, полимерное производное, включающее полимер и, по меньшей мере, бифункциональное соединение, химически модифицировано у свободной функциональной группы Q для получения полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу. В соответствии с этим вариантом осуществления, предпочтительно обеспечить взаимодействие полимерного производного, по меньшей мере, с одним бифункциональным соединением, которое включает функциональную группу, способную взаимодействовать с функциональной группой Q и альдегидной группой, или кетогруппой, или полуацетальной группой.
В качестве, по меньшей мере, бифункционального соединения подходит каждое соединение, которое имеет альдегидную группу или кетогруппу, или полуацетальную группу и, по меньшей мере, одну функциональную группу, которая способна образовывать связь с функциональной группой Q полимерного производного. По меньшей мере, одна функциональная группа выбрана из того же пула функциональных групп, что и Q, и выбрана для способности взаимодействовать с Q. В предпочтительном случае, когда Q представляет собой аминогруппу -NH2, предпочтительно использовать соединение, имеющее, кроме альдегидной группы или кетогруппы, или полуацетальной группы, по меньшей мере, одну карбоксигруппу или, по меньшей мере, одну реакционноспособную карбоксигруппу, предпочтительно одну карбоксигруппу или одну реакционноспособную карбоксигруппу. Альдегидная группа или кетогруппа, или полуацетальная группа и карбоксигруппа, или реакционноспособная карбоксигруппа может быть отделена любым подходящим промежуточным соединением. Среди других промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 2 до 10, предпочтительнее от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8 и особенно предпочтительно от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь или арильную группу, или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или может представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой арильный остаток, имеющий от 5 до 7, а предпочтительно 6 атомов углерода. Наиболее предпочтительно углеводородный остаток представляет собой бензольный остаток. В соответствии с этим предпочтительным вариантом осуществления, карбоксигруппа и альдегидная группа может располагаться в бензольном кольце в 1,4-положении, 1,3-положении или 1,2-положении, причем предпочтительным является 1,4-положение.
В качестве реакционноспособной карбоксигруппы можно упомянуть реакционноспособный сложный эфир, изотиоцианаты или изоцианат. Предпочтительные реакционноспособные сложные эфиры получают из N-гидроксисукцинимидов, таких как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенных фенолов, таких как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол или 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N-гидроксисукцинимиды, причем особенно предпочтительны N-гидроксисукцинимид и сульфо-N-гидроксисукцинимид. Все спирты могут использоваться отдельно или в виде подходящей комбинации двух или более из них. В качестве реакционноспособного сложного эфира, особенно предпочтительными являются сложный пентафторфениловый эфир и сложный эфир N-гидроксисукцинимида.
Таким образом, в соответствии с предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимерное производное, включающее Q, причем Q представляет собой аминогруппу -NH2, далее взаимодействует с формилбензойной кислотой.
В соответствии с другим предпочтительным вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимерное производное, включающее Q, причем Q представляет собой аминогруппу -NH2, далее взаимодействует со сложным пентафторфениловым эфиром формилбензойной кислоты.
В соответствии с еще одним вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимерное производное, включающее Q, причем Q представляет собой аминогруппу, далее взаимодействует со сложным N-гидроксисукцинимидным эфиром формилбензойной кислоты.
В соответствии с еще одним вариантом осуществления, настоящее изобретение относится к способу и конъюгату, как описано выше, где полимерное производное, включающее Q, причем Q представляет собой аминогруппу -NH2, далее взаимодействует с 4-(4-формил-3,5-диметоксифенокси)масляной кислотой.
В качестве растворителя для взаимодействия полимерного производного, включающего аминогруппу, например формилбензойную кислоту, предпочтителен, по меньшей мере, один апротонный растворитель, особенно предпочтительно безводный апротонный растворитель, имеющий содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями являются, среди других, диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси из двух или более из них.
Взаимодействие предпочтительно проводится при температуре от 0 до 40°С, предпочтительнее от 0 до 25°С и особенно предпочтительно от 15 до 25°С, в течение времени взаимодействия предпочтительно от 0,5 до 24 ч и особенно предпочтительно от 1 до 17 ч.
В соответствии с предпочтительным вариантом осуществления, взаимодействие проводится в присутствии активирующего агента. Подходящими активирующими агентами являются, среди других, карбодиимиды, такие как диизопропилкарбодиимид (DIC), дициклогексилкарбодиимиды (DCC), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), причем особенно предпочтителен диизопропилкарбодиимид (DIC).
Полученное полимерное производное можно очистить из реакционной смеси, по меньшей мере, одним подходящим способом. При необходимости полимерное производное можно осадить перед выделением, по меньшей мере, одним подходящим способом.
Если полимерное производное сначала осаждается, можно, например, обеспечить контакт реакционной смеси, по меньшей мере, с одним растворителем или смесью растворителей, отличных от растворителя или смеси растворителей, присутствующих в реакционной смеси, при подходящих температурах. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, где водная среда, предпочтительно вода, используется в качестве растворителя, реакционная смесь контактирует с 2-пропанолом или со смесью ацетона и этанола, предпочтительно смесью 1:1 (об./об.), указывающей на равные объемы указанных соединений, при температуре, предпочтительно в диапазоне от -20 до +50°С, а особенно предпочтительно от -20 до 25°С.
Выделение полимерного производного можно проводить подходящим способом, который может включать одну или более стадий. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, полимерное производное сначала отделяется от реакционной смеси или смеси реакционной смеси, например с водной смесью 2-пропанола, подходящим способом, таким как центрифугирование или фильтрация. На второй стадии отделенное полимерное производное может быть подвергнуто дальнейшей обработке, такой как диализ, подобный последующей обработке, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография в обращенной фазе, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация. В соответствии с еще более предпочтительным вариантом реализации, отделенное полимерное производное сначала диализируется, предпочтительно против воды, а затем лиофилизируется до тех пор, пока содержание растворителя продукта взаимодействия не будет достаточно низким, в соответствии с желательными спецификациями продукта. Лиофилизиацию можно проводить при температуре от 20 до 35°С, предпочтительно от 20 до 30°С.
Полученное полимерное производное с альдегидной группой или кетогруппой, или полуацетальной группой в последующем взаимодействует с аминогруппой белка через восстановительное аминирование. Что касается соединения, по меньшей мере, одной аминогруппы белка, по меньшей мере, с одной альдегидной группой или кетогруппой, или полуацетальной группой полимера восстановительным аминированием, то делается ссылка на приведенное выше подробное описание, касающееся определенных параметров взаимодействия, таких как рН или температура. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, восстановительное аминирование проводится при температуре от 0 до 10°С, например от 1 до 8°С или от 2 до 6°С , например примерно при 4°С при рН примерно от 4,5 до 5,5, например примерно при 5,0. Время взаимодействия составляет примерно от 10 до 20 ч, например от 12 до 19 ч, или от 14 до 18 ч, например примерно 17 ч, или примерно от 20 до 30 ч, например примерно 24 ч.
Таким образом, в соответствии с указанными выше предпочтительными вариантами осуществления, настоящее изобретение также относится, в случае взаимодействия полимера через его окисленный восстанавливающий конец, к конъюгату в соответствии с формулой
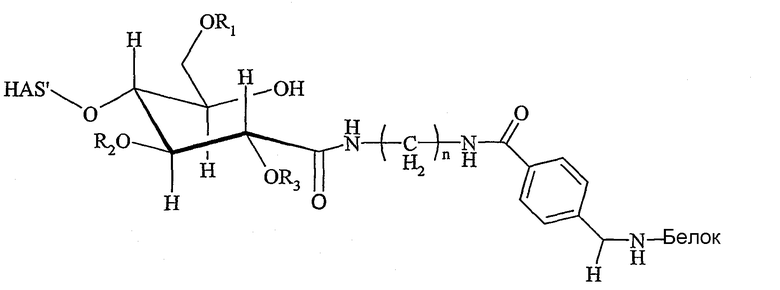
В соответствии с особенно предпочтительным вариантом осуществления, полимер представляет собой гидроксиэтилкрахмал, т.е. HAS' представляет собой HES', а n=2, 3 или 4, наиболее предпочтительно 4, как описано выше. Поэтому, в случае, когда полимер взаимодействовал через его окисленный восстанавливающий конец, настоящее изобретение также относится к конъюгату в соответствии с формулой
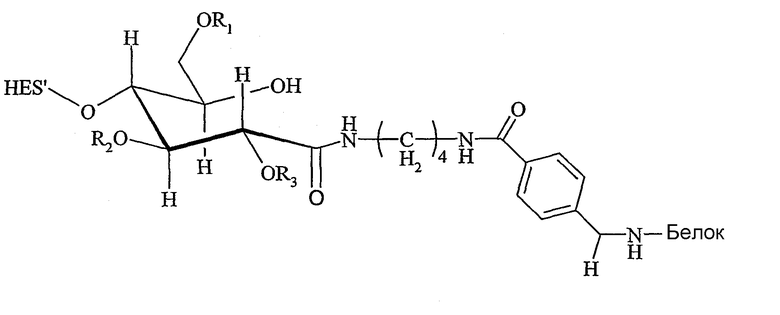
В соответствии с другим предпочтительным вариантом осуществления, настоящее изобретение также относится, в случае, когда полимер взаимодействовал через его окисленный восстанавливающий конец, к конъюгату в соответствии с формулой
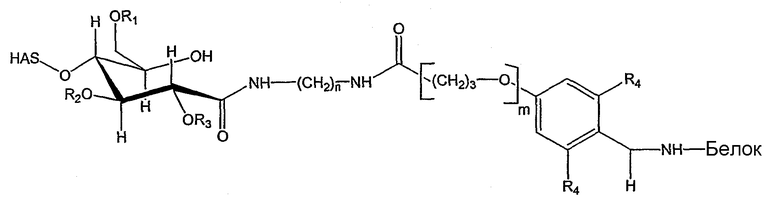
где n=2, 3 или 4, причем R4 представляет собой независимо водород или метоксигруппу, а m=0 в случае, когда R4 представляет собой водород, и m=1 в случае, когда R4 представляет собой метокси, причем HAS предпочтительно представляет собой HES'.
В каждой из приведенных выше формул азот, присоединенный к белку, происходит из аминогруппы белка, к которому полимерное производное присоединено через альдегидную группу.
В отношении указанных выше вариантов осуществления, в соответствии с которыми функциональные группы М и Q включают аминогруппу -NH2, возможно также, что М представляет собой аминогруппу -NH2, а Q включает бета-гидроксиаминогруппу -CH(OH)-CH2-NH2, а предпочтительно представляет собой бета-гидроксиаминогруппу.
Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где аминогруппа Q соединения, включающего 2 аминогруппы М и Q, представляет собой бета-гидроксиаминогруппу -CH(OH)-CH2-NH2.
В этом случае М и Q могут быть отделены любым подходящим промежуточным соединением. Среди других, промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 2 до 10, предпочтительнее от 1 до 6 и особенно предпочтительно от 1 до 2 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, а особенно предпочтительно от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь, или арильную группу, или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой алкильную цепь из 1 до 20, предпочтительно от 1 до 10, предпочтительнее от 1 до 6, предпочтительнее от 1 до 4 атомов углерода, а особенно предпочтительно от 1 до 2 атомов углерода. Еще предпочтительнее М и Q разделены метиленовой группой.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер взаимодействует с 1,3-диамин-2-гидроксипропаном.
В случае, когда полимер взаимодействует через окисленный восстанавливающий конец, получается полимерное производное, в соответствии с формулой
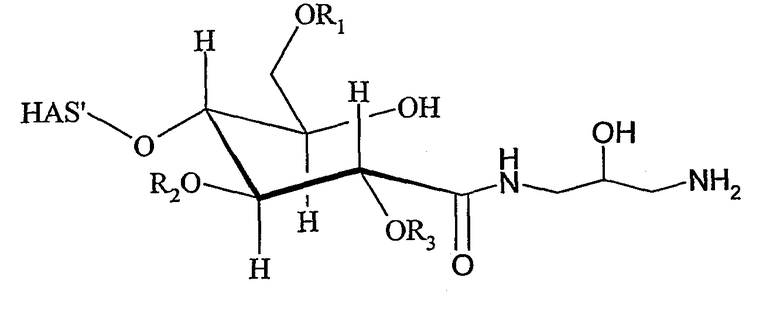
Особенно предпочтительно при HAS'=HES'
Взаимодействие, по меньшей мере, бифункционального соединения, включающего М и Q, особенно предпочтительно 1,3-диамино-2-гидроксипропан, с полимером предпочтительно проводится при температуре от 40 до 120°С, предпочтительнее от 40 до 90°С, а особенно предпочтительно от 60 до 80°С. Время взаимодействия предпочтительно находится в диапазоне от 17 ч до 168 ч, предпочтительнее от 17 до 96 ч и особенно предпочтительно от 48 до 96 ч. Молярное соотношение, по меньшей мере, бифункционального соединения и полимера находится предпочтительно в диапазоне от 200:1 до 10:1, в частности от 50:1 до 100:1.
В качестве растворителя для взаимодействия, по меньшей мере, бифункционального соединения с полимером, предпочтителен, по меньшей мере, один апротонный растворитель, особенно предпочтительно безводный апротонный растворитель, имеющий содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями являются, среди других, диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси из двух или более из них.
Бета-гидроксиаминогруппа Q полимерного производного в целом может взаимодействовать, по меньшей мере, с бифункциональным соединением, включающим, по меньшей мере, одну функциональную группу, способную взаимодействовать с Q, и, кроме того, включающим, по меньшей мере, одну функциональную группу, являющуюся альдегидной группой, или кетогруппой, или полуацетальной группой, или функциональную группу, являющуюся модифицированной, для получения альдегидной группы, или кетогруппы, или полуацетальной группы. В соответствии с другим вариантом осуществления настоящего изобретения, бета-гидроксиаминогруппа непосредственно химически модифицирована для получения альдегидной группы химическим окислением.
Это окисление можно проводить всеми подходящими агентами окисления, которые способны превращать бета-гидроксиаминогруппу в альдегидную группу. Предпочтительными реагентами окисления являются периодаты, такие как периодаты щелочных металлов. Особенно предпочтительным является периодат натрия, который предпочтительно используется в виде водного раствора. Этот раствор имеет предпочтительную концентрацию йодата от 1 до 50 мМ, предпочтительнее от 1 до 25 мМ и особенно предпочтительно от 1 до 10 мМ. Окисление проводится при температуре от 0 до 40°С, предпочтительно от 0 до 25°С и особенно предпочтительно от 4 до 20°С.
Полученное полимерное производное может быть очищено из реакционной смеси, по меньшей мере, одним подходящим способом. При необходимости полимерное производное может осаждаться перед выделением, по меньшей мере, одним подходящим способом.
Если полимерное производное сначала осаждается, можно, например, обеспечить контакт реакционной смеси, по меньшей мере, с одним растворителем или смесью растворителей, присутствующих в реакционной смеси, при подходящих температурах. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, где водная среда, предпочтительно вода, используется в качестве растворителя, реакционная смесь контактирует с 2-пропанолом или со смесью ацетона и этанола, предпочтительно смесью 1:1 (об./об.), указывающей на одинаковые объемы указанных соединений, при температуре, предпочтительно в диапазоне от -20 до +50°С, а особенно предпочтительно от -20 до 25°С.
Выделение полимерного производного можно проводить подходящим способом, который может включать одну или более стадий. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, полимерное производное сначала отделяется от реакционной смеси или смеси реакционной смеси, например с водной смесью 2-пропанола, подходящим способом, таким как центрифугирование или фильтрация. На второй стадии отделенное полимерное производное может быть подвергнуто дальнейшей обработке, такой как диализ, подобный последующей обработке, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография в обращенной фазе, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация. В соответствии с еще более предпочтительным вариантом реализации, отделенное полимерное производное сначала диализируется, предпочтительно против воды, а затем лиофилизируется до тех пор, пока содержание растворителя продукта взаимодействия не будет достаточно низким, в соответствии с желательными спецификациями продукта. Лиофилизацию можно проводить при температуре от 20 до 35°С, предпочтительно от 20 до 30°С.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где окисление бета-гидрокиаминогруппы Q проводится с использованием периодата.
Поэтому настоящее изобретение также относится к способу получения конъюгата, где, в случае использования полимера с окисленным восстанавливающим концом, полимерное производное, имеющее бета-гидрокиаминогруппу, особенно предпочтительно
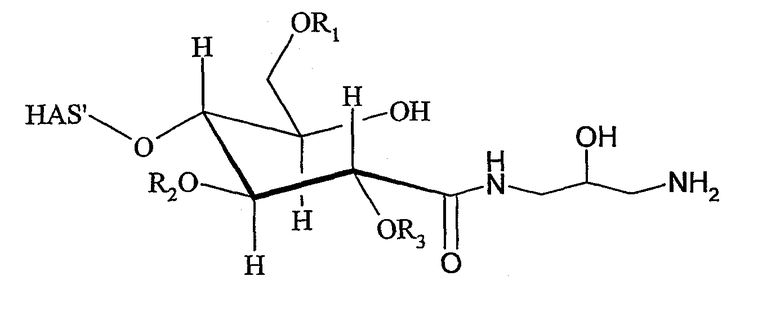
и особенно при HAS'=HES', окисляется предпочтительно периодатом в полимерное производное, имеющее альдегидную группу, особенно предпочтительно
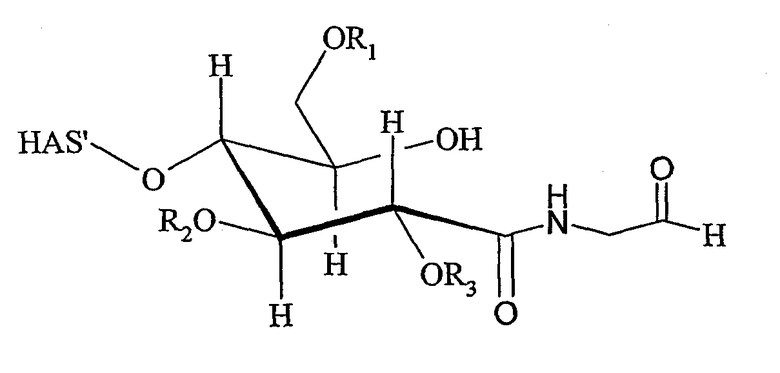
и особенно при HAS'=HES'.
Полученное полимерное производное с альдегидной группой А в последующем взаимодействует с белком. Поэтому настоящее изобретение также относится к способу получения конъюгата, причем указанный способ включает взаимодействие полимерного производного, имеющего бета-гидроксиаминогруппу, в случае использования полимера с окисленным восстанавливающим концом, особенно предпочтительно в соответствии с формулой
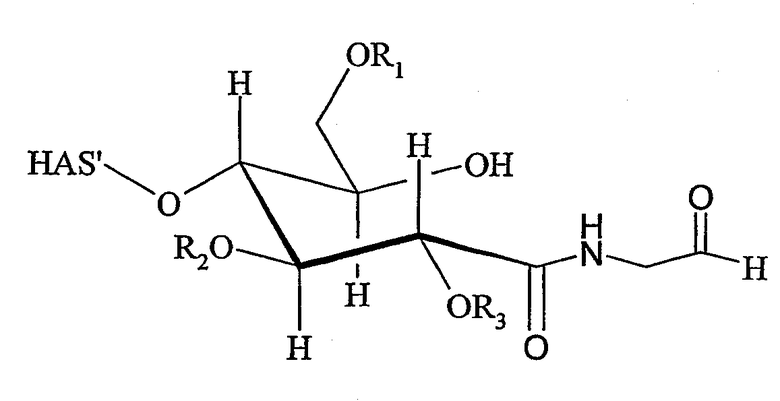
и особенно при HAS'=HES', с аминогруппой белка.
Полученное полимерное производное с альдегидной группой в последующем взаимодействует с аминогруппой белка через восстановительное аминирование. Что касается соединения, по меньшей мере, одной альдегидной группы восстановительным аминированием, то делается ссылка на представленное выше подробное описание.
Таким образом, в соответствии с указанным выше предпочтительным вариантом осуществления, настоящее изобретение также относится к конъюгату в соответствии с формулой
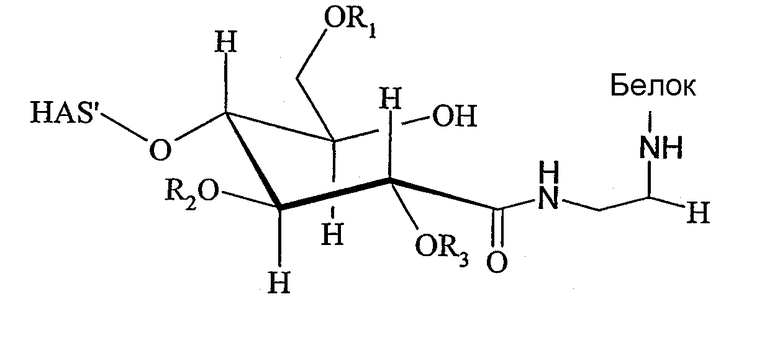
особенно при HAS'=HES', в случае использования полимера с окисленным восстанавливающим концом. В представленной выше формуле азот, присоединенный к белковому производному, происходит из аминогруппы белка, к которому полимерное производное присоединено через альдегидную группу.
В соответствии с еще одним вариантом осуществления настоящего изобретения, полимер сначала взаимодействует с подходящим соединением для получения первого полимерного производного, включающего, по меньшей мере, одну реакционноспособную карбоксигруппу. Это первое полимерное производное затем взаимодействует с еще одним, по меньшей мере, бифункциональным соединением, где, по меньшей мере, одна функциональная группа этого еще одного соединения взаимодействует, по меньшей мере, с одной реакционноспособной карбоксигруппой полимерного производного и, по меньшей мере, одна другая функциональная группа еще одного соединения представляет собой альдегидную группу, или кетогруппу, или полуацетальную группу, или представляет собой функциональную группу, которая химически модифицирована для получения альдегидной группы или кетогруппы, или полуацетальной группы, и где полученное полимерное производное, включающее указанную альдегидную группу, или кетогруппу, или полуацетальную группу, взаимодействует посредством восстановительного аминирования, как описано выше, по меньшей мере, с одной аминогруппой белка. Можно также изменить последовательность взаимодействия соответствующих соединений друг с другом.
В соответствии с первой альтернативой указанного еще одного варианта осуществления, полимер, включающий, по меньшей мере, одну реакционноспособную карбоксигруппу, получают селективным окислением полимера на его восстанавливающем конце и последующим взаимодействием окисленного полимера, представляющего собой лактон

и/или карбоновую кислоту

или подходящую соль карбоновой кислоты, такую как соль щелочного металла, предпочтительно в виде соли натрия и/или калия, а HAS' предпочтительно представляющего собой HES', с подходящим соединением для получения полимера, включающего, по меньшей мере, одну реакционноспособную карбоксигруппу.
Окисление полимера, предпочтительно гидроксиэтилкрахмала, можно проводить в соответствии с каждым способом или комбинацией способов, которые приводят к получению соединений, имеющих указанные выше структуры (IIa) и/или (IIb).
Хотя окисление можно проводить в соответствии с любым подходящим способом или способами, приводящими к получению окисленного восстанавливающего конца гидроксиалкилкрахмала, оно предпочтительно проводится с использованием щелочного раствора йода, как описано, например, в документе DE 196 28 705 A1, соответствующее содержание которого (пример А, колонка 9, строки 6-24) включено в настоящее описание в качестве ссылки.
Введение реакционноспособной карбоксигруппы в полимер, который селективно окислен на его восстанавливающем конце, можно провести всеми возможными способами и всеми подходящими соединениями.
В соответствии с определенным способом настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце, по меньшей мере, с одним спиртом, предпочтительно, по меньшей мере, с одним кислотным спиртом, таким как кислотные спирты, имеющие величину pKA в диапазоне от 6 до 12, предпочтительнее, от 7 до 11 при 25°С. Молекулярная масса кислотного спирта может быть в диапазоне от 80 до 500 г/моль, например от 90 до 300 г/моль или от 100 до 200 г/моль.
Подходящими кислотными спиртами являются все спирты H-O-RA, имеющие кислотную часть и способные взаимодействовать с окисленным полимером для получения соответствующего реакционноспособного сложного эфира полимера, предпочтительно в соответствии с формулой
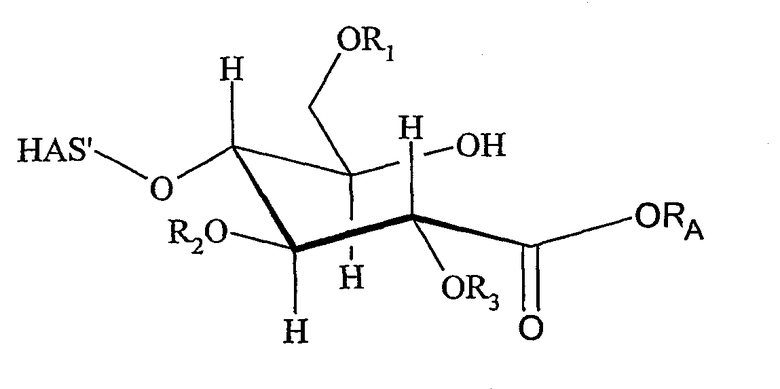
еще предпочтительнее в соответствии с формулой
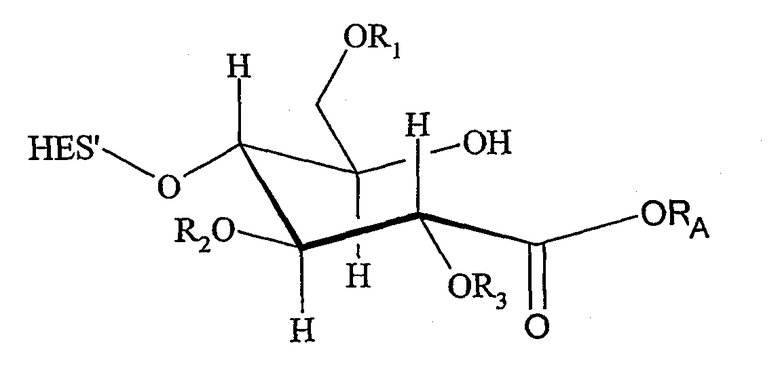
Предпочтительными спиртами являются N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол, 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N-гидроксисукцинимиды, причем особенно предпочтительны N-гидроксисукцинимид и сульфо-N-гидроксисукцинимид. Все спирты можно использовать отдельно или в виде подходящей комбинации двух или более из них. В контексте настоящего изобретения можно также использовать соединение, которое высвобождает соответствующий спирт, например добавлением сложного диэфира карбоновой кислоты.
Поэтому настоящее изобретение также относится к способу, как описано выше, где полимер, который селективно окислен на его восстанавливающем конце, активирован взаимодействием окисленного полимера с кислотным спиртом, предпочтительно с N-гидроксисукцинимидом и/или сульфо-N-гидроксисукцинимидом.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце, по меньшей мере, с одним сложным карбоновым диэфиром RB-O-(C=O)-O-RC, где RB и RC могут быть одинаковыми или различными. Предпочтительно, этот способ дает реакционноспособные полимеры в соответствии с формулой
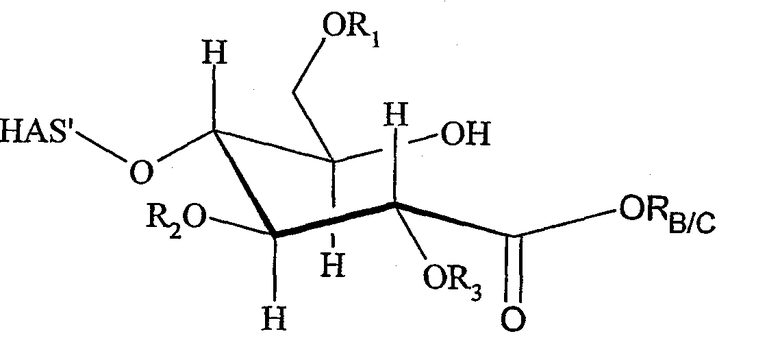
где HAS' представляет собой предпочтительно HES'.
В качестве подходящих соединений сложного карбонового диэфира, могут использоваться соединения, спиртовые компоненты которых представляют собой независимо N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходящим образом замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол, 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол. Особенно предпочтительными являются N,N'-дисукцинимидилкарбонат и сульфо-N,N'-дисукцинимидилкарбонат, причем особенно предпочтителен N,N'-дисукцинимидилкарбонат.
Поэтому настоящее изобретение также относится к способу, как описано выше, где полимер, который селективно окислен на его восстанавливающем конце, активирован взаимодействием окисленного полимера с N,N'-дисукцинимидилкарбонатом.
Кислотный спирт взаимодействует с окисленным полимером или солью окисленного полимера при молярном соотношении кислотного спирта и полимера предпочтительно от 5:1 до 50:1, предпочтительнее от 8:1 до 20:1 при предпочтительной температуре взаимодействия от 2 до 40°С, предпочтительнее от 10 до 30°С и особенно предпочтительно от 15 до 25°С. Время взаимодействия находится предпочтительно в диапазоне от 1 до 10 ч, предпочтительнее от 2 до 5 ч, предпочтительнее от 2 до 4 ч и, в частности, от 2 до 3 ч.
Соединение сложного карбонового диэфира взаимодействует с окисленным полимером или солью окисленного полимера при молярном соотношении соединения сложного диэфира и полимера в целом от 1:1 до 3:1, например от 1:1 до 1,5:1. Время взаимодействия находится в целом в диапазоне от 0,1 до 12 ч, например от 0,2 до 6 ч, или от 0,5 до 2 ч, или от 0,75 до 1,25 ч.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие окисленного полимера с кислотным спиртом и/или сложным карбоновым диэфиром проводится, по меньшей мере, в одном апротонном растворителе, таком как безводный апротонный растворитель, имеющий содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями, среди других, являются диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси двух или более из них. Температуры взаимодействия находятся предпочтительно в диапазоне от 2 до 40°С, предпочтительнее от 10 до 30°С.
Для взаимодействия окисленного полимера, по меньшей мере, с одним кислотным спиртом используется, по меньшей мере, один дополнительный активирующий агент.
Подходящими активирующими агентами являются, среди других, карбонилдиимидазол, карбодиимиды, такие как диизопропилкарбодиимид (DIC), дициклогексилкарбодиимиды (DCC), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), причем особенно предпочтительны дициклогексилкарбодиимиды (DCC) и 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC).
Поэтому настоящее изобретение также относится к способу, как описано выше, где полимер, который окислен на его восстанавливающем конце, взаимодействует с кислотным спиртом в присутствии дополнительного активирующего агента для получения реакционноспособного сложного эфира полимера.
В соответствии с одним вариантом осуществления настоящего изобретения, взаимодействие окисленного полимера со сложным карбоновым диэфиром и/или кислотным спиртом проводится при низкой основной активности, которую можно определить добавлением реакционной смеси к воде при объемном соотношении между водой и реакционной смесью 10:1. Перед добавлением вода, которая по существу не включает буфер, имеет рН 7 при 25°С. После добавления реакционной смеси и измерением величины рН определяется основная активность реакционной смеси, имеющая величину предпочтительно не более чем 9,0, предпочтительнее не более чем 8,0, особенно предпочтительно не более чем 7,5.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, окисленный полимер взаимодействует с N-гидроксисукцинимидом в сухом DMA в отсутствие воды с EDC для селективного получения N-гидроксисукцинимидного сложного эфира полимера в соответствии с формулой
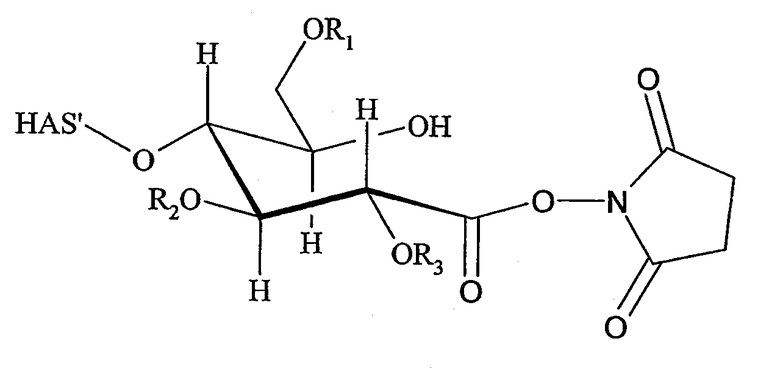
причем HAS' предпочтительно представляет собой HES'.
К удивлению, это взаимодействие не дает побочные продукты, полученные в результате взаимодействий EDC с группами ОН HES, и реакция перегруппировки О-ацилмочевины, образованной EDC и окисленным полимером в соответствующую N-ацилмочевину, к удивлению подавлена.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, окисленный полимер взаимодействует с N,N'-дисукцинимидилкарбонатом в сухом DMF в отсутствие воды и в отсутствие активирующего агента для селективного получения N-гидроксисукцинимидного сложного эфира полимера в соответствии с формулой
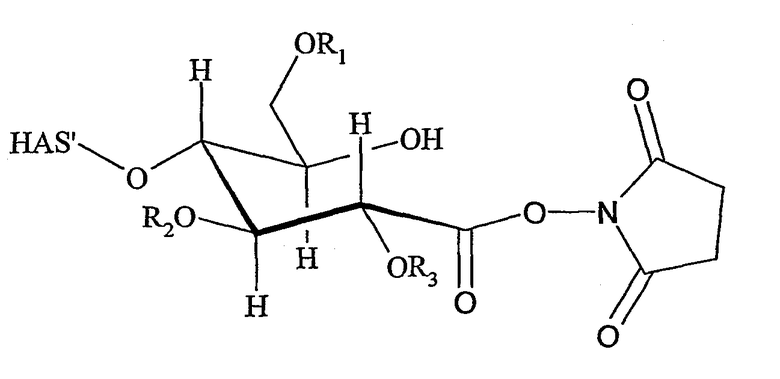
причем HAS' предпочтительнее представляет собой HES'.
В соответствии с еще одним вариантом осуществления настоящего изобретения, полимер, который селективно окислен на его восстанавливающем конце, взаимодействует на окисленном восстанавливающем конце с азолидом, таким как карбонилдиимидазол или карбонилдибензимидазол, для получения полимера, имеющего реакционноспособную карбоксигруппу. В случае карбонилдиимидазола, получается реакционноспособное имидазолидное полимерное производное в соответствии с формулой
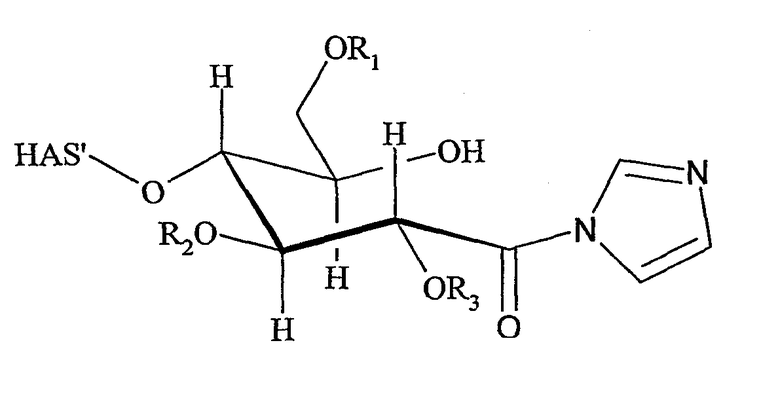
где HAS' предпочтительно представляет собой HES'.
В соответствии со второй альтернативой указанного еще одного варианта осуществления настоящего изобретения, относящегося к введению, по меньшей мере, одной реакционноспособной карбоксигруппы в полимер, реакционноспособная карбоксигруппа вводится в полимер, восстанавливающий конец которого не окислен, взаимодействием, по меньшей мере, одной гидроксигруппы полимера со сложным карбоновым диэфиром.
Поэтому настоящее изобретение также относится к способу и конъюгатам, где реакционноспособная карбоксигруппа введена в полимер, чей восстанавливающий конец не окислен, взаимодействием, по меньшей мере, одной гидроксигруппы полимера, по меньшей мере, с одним сложным карбоновым диэфиром
RB-O-(C=O)-O-RC, где RB и RC могут быть одинаковыми или различными.
В соответствии с другим вариантом осуществления настоящего изобретения, полимер, восстанавливающий конец которого не окислен, взаимодействует, по меньшей мере, при одной гидроксигруппе с азолидом, таким как карбонилдиимидазол, карбонил-ди-(1,2,4-триазол) или карбонилдибензимидазол, для получения полимера, имеющего реакционноспособную карбоксигруппу.
В качестве подходящих соединений сложных карбоновых диэфиров, могут использоваться соединения, спиртовые компоненты которых представляют собой независимо N-гидроксисукцинимиды, такие как N-гидроксисукцинимид или сульфо-N-гидроксисукцинимид, подходяще замещенные фенолы, такие как пара-нитрофенол, о,п-динитрофенол, о,о'-динитрофенол, трихлорфенол, такой как 2,4,6-трихлорфенол или 2,4,5-трихлорфенол, трифторфенол, такой как 2,4,6-трифторфенол или 2,4,5-трифторфенол, пентахлорфенол, пентафторфенол или гидроксиазолы, такие как гидроксибензотриазол.
Особенно предпочтительными являются симметричные соединения сложных карбоновых диэфиров, причем RB и RC, таким образом, одинаковы. Спиртовой компонент сложного карбонового диэфира предпочтительно выбран из группы, состоящей из N-гидроксисукцинимида, сульфонированного N-гидроксисукцинимида, N-гидроксибензотриазола и нитро- и галоген-замещенных фенолов. Среди других, предпочтительны нитрофенол, динитрофенол, трихлорфенол, трифторфенол, пентахлорфенол и пентафторфенол. Особенно предпочтительными являются N,N'-дисукцинимидилкарбонат и сульфо-N,N'-дисукцинимидилкарбонат, причем особенно предпочтителен N,N'-дисукцинимидилкарбонат.
Поэтому настоящее изобретение также относится к производному гидроксиалкилкрахмала, предпочтительно производному гидроксиэтилкрахмала, где, по меньшей мере, одна гидроксигруппа, предпочтительно, по меньшей мере, 2 гидроксигруппы указанного крахмала, были подвергнуты взаимодействию с соединением сложного карбонового диэфира для получения соответствующего реакционноспособного сложного эфира.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, взаимодействие полимера, восстанавливающий конец которого не окислен, по меньшей мере, с одним соединением сложного карбонового диэфира проводится при температуре от 2 до 40°С, предпочтительнее от 10 до 30°С и, в частности, от 15 до 25°С. Предпочтительное время взаимодействия находится в диапазоне от 0,5 до 5 ч, предпочтительнее от 1 до 3 ч, а особенно предпочтительно от 2 до 3 ч.
Молярное соотношение между сложным карбоновым диэфиром и полимером зависит от степени замещения полимера в отношении количества гидроксигрупп, вступивших во взаимодействие с соединением сложного карбонового диэфира, относительно количества гидроксигрупп, присутствующих в не вступившем во взаимодействие полимере.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, молярное соотношение сложного карбонового диэфира и единиц ангидроглюкозы полимера находится в диапазоне от 1:2 до 1:1000, предпочтительнее, от 1:3 до 1:100, а особенно предпочтительно от 1:10 до 1:50, для получения степени замещения в диапазоне от 0,5 до 0,001, предпочтительно от 0,33 до 0,01 и особенно предпочтительно от 0,1 до 0,02.
В соответствии с одним вариантом осуществления настоящего изобретения, взаимодействие полимера, восстанавливающий конец которого не окислен, по меньшей мере, со сложным карбоновым диэфиром проводится, по меньшей мере, в одном апротонном растворителе, особенно предпочтительно в безводном апротонном растворителе, имеющем содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями, среди других, являются диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид(DMF) и смесь двух или более из них.
Поэтому настоящее изобретение также относится к способу, как описано выше, где взаимодействие, по меньшей мере, одной гидроксигруппы полимера, восстанавливающий конец которого не окислен, со сложным карбоновым диэфиром для получения реакционноспособной карбоксигруппы, проводится в безводном апротонном полярном растворителе, причем растворитель предпочтительно представляет собой диметилацтамид, диметилформамид или их смесь.
Реакционноспособное полимерное производное, включающее, по меньшей мере, одну реакционноспособную карбоксигруппу, предпочтительно полученную в результате взаимодействия полимера с кислотным спиртом, карбонатом и/или азолидом, как описано выше, далее взаимодействует с еще одним, по меньшей мере, бифункциональным соединением, где, по меньшей мере, одна функциональная группа F1 этого еще одного соединения взаимодействует, по меньшей мере, с одной реакционноспособной карбоксигруппой полимерного производного. В отношении, по меньшей мере, одной функциональной группы F1 этого еще одного соединения не существуют определенные ограничения, при условии, что возможно взаимодействие, по меньшей мере, с одной реакционноспособной карбоксигруппой полимера. Предпочтительными функциональными группами F1 являются, например, аминогруппа, или гидроксигруппа, или тиогруппа, или карбоксигруппа.
Это еще одно, по меньшей мере, бифункциональное соединение включает, по меньшей мере, другую функциональную группу F2, представляющую собой альдегидную группу, или функциональную группу F2, которая способна быть химически модифицированной для получения альдегидной группы. Химической модификацией может быть, например, взаимодействие функциональной группы F2 с функциональной группой F3 еще одного линкерного соединения или окисление или восстановление подходящей функциональной группы F2.
В случае, когда F2 взаимодействует с функциональной группой F3 еще одного соединения, F2 может быть выбрана, среди других, из:
- С-С-двойных связей, или С-С-тройных связей, или ароматических С-С-связей;
- тиогруппы или гидроксигруппы;
- гидразида алкилсульфоновой кислоты, гидразида арилсульфоновой кислоты;
- 1,2-диолов;
- 1,2-аминоспиртов;
- 1,2-аминотиоспиртов;
- азидов;
- аминогруппы -NH2 или производных аминогрупп, включающих структурную единицу -NH-, таких как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы или алкариламиногруппы;
- гидроксиламиногруппы -O-NH2 или производных гидроксиламиногруппы, включающих структурную единицу -O-NH-, такую как гидроксиалкиламиногруппы, гидроксилариламиногруппы, гидроксиаралкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогрупп, арилоксиаминогрупп, аралкилоксиаминогрупп или алкарилоксиаминогрупп, каждая из которых включает структурную единицу -NH-O-;
- остатков, имеющих карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такое как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;

где F3 представляет собой группу, способную образовывать химическую связь с одной из указанных выше групп, и предпочтительно выбрана из указанных выше групп. Более того, второе линкерное соединение предпочтительно имеет, по меньшей мере, одну альдегидную группу, или кетогруппу, или полуацетальную группу, которая способна взаимодействовать с аминогруппой белка посредством восстановительного аминирования.
Функциональная группа F1 и альдегидная группа, или кетогруппа, или полуацетальная группа, по меньшей мере, бифункционального связывающего соединения, которое взаимодействует с полимером, и/или функциональные группы F1 и F2, по меньшей мере, бифункционального связывающего соединения, которое взаимодействует с полимером, и/или функциональная группа F3 и альдегидная группа, или кетогруппа, или полуацетальная группа этого еще одного, по меньшей мере, бифункционального связывающего соединения, могут быть независимо отделены любым подходящим промежуточным соединением. Среди других, промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический, алифатический и/или ароматический углеводородный остаток. В целом, углеводородный остаток имеет до 60, предпочтительно до 40, предпочтительнее до 20, предпочтительнее до 10 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, предпочтительнее от 1 до 6, предпочтительнее от 1 до 4 и особенно предпочтительно от 1 до 2 гетероатомов. В качестве гетероатома предпочтителен О. Углеводородный остаток может включать необязательно разветвленную алкильную цепь, или арильную руппу, или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или может представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу.
Примерами соединения с функциональными группами F1 и F2 являются, например, необязательно замещенный диаминоалкан, имеющий от 2 до 20 атомов углерода, особенно предпочтительно 1,2-диаминоэтан, 1,3-диаминопропан и 1,4-диаминобутан. Предпочтительными примерами соединения с функциональными группами F3 и альдегидной группой, или кетогруппой, или полуацетальной группой являются, например, формилбензойная кислота, сложный пентафторфениловый эфир 4-формилбензойной кислоты, сложный N-гидроксисукцинимидный эфир 4-формилбензойной кислоты и 4-(4-формил-3,5-диметоксифенокси)масляная кислота.
Поэтому настоящее изобретение также относится к способу получения конъюгата, причем указанный способ включает взаимодействие полимера, предпочтительно гидроксиэтилкрахмала, на его необязательно окисленном восстанавливающем конце с соединением, выбранным из группы, состоящей из кислотных спиртов, сложных карбоновых диэфиров и азолидов, для получения полимерного производного, включающего, по меньшей мере, одну реакционноспособную карбоксигруппу, взаимодействие указанного полимерного производного, по меньшей мере, с одним, по меньшей мере, бифункциональным соединением для получения полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, или функциональную группу, способную подвергаться химической модификации для получения альдегидной группы, или кетогруппы, или полуацетальной группы, необязательную химическую модификацию указанной функциональной группы для получения полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, и взаимодействие полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, с аминогруппой белка посредством восстановительного аминирования.
Соответственно, настоящее изобретение также относится к конъюгату, включающему полимер, предпочтительно гидроксиэтилкрахмал, и белок, ковалентно связанные друг с другом, который можно получить способом получения конъюгата, причем указанный способ включает взаимодействие полимера на его необязательно окисленном восстанавливающем конце с соединением, выбранным из группы, состоящей из кислотных спиртов, сложных карбоновых диэфиров и азолидов, для получения полимерного производного, включающего, по меньшей мере, одну реакционноспособную карбоксигруппу, взаимодействие указанного полимерного производного, по меньшей мере, с одним, по меньшей мере, бифункциональным соединением для получения полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, или функциональную группу, способную подвергаться химической модификации для получения альдегидной группы, или кетогруппы, или полуацетальной группы, необязательную химическую модификацию указанной функциональной группы для получения полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, и взаимодействие полимерного производного, включающего альдегидную группу, или кетогруппу, или полуацетальную группу, с аминогруппой белка посредством восстановительного аминирования.
Определенным примером соединения, имеющего функциональную группу F1 и функциональную группу F2, которая окислена для получения альдегидной группы, является, например, соединение, имеющее аминогруппу в качестве F1 и бета-гидроксиаминогруппу в качестве F2. Особенно предпочтительным примером является 1,3-диамино-2-гидроксипропан. Это окисление можно проводить всеми подходящими агентами окисления, которые способны превратить бета-гидроксиаминогруппу в альдегидную группу. Предпочтительными реагентами окисления являются периодаты, такие как периодаты щелочных металлов. Особенно предпочтителен периодат натрия, который предпочтительно используется в виде водного раствора. Этот раствор имеет предпочтительную концентрацию иодата от 1 до 50 мМ, предпочтительнее от 1 до 25 мМ, а особенно предпочтительно 1 до 10 мМ. Оксиление проводится при температуре от 0 до 40°С, предпочтительно от 0 до 25°С, а особенно предпочтительно от 4 до 20°С.
Полученное полимерное производное может быть очищено из реакционной смеси, по меньшей мере, одним подходящим способом. При необходимости полимерное производное может осаждаться перед выделением, по меньшей мере, одним подходящим способом.
Если полимерное производное сначала осаждается, можно, например, обеспечить контакт реакционной смеси, по меньшей мере, с одним растворителем или смесью растворителей, отличных от растворителя или смеси растворителей, присутствующих в реакционной смеси, при подходящих температурах. В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, где водная среда, предпочтительно вода, используется в качестве растворителя, реакционная смесь контактирует с 2-пропанолом или со смесью ацетона и этанола, предпочтительно смесью 1:1 (об./об.), указывающей на равные объемы указанных соединений, при температуре, предпочтительно в диапазоне от -20 до +50°С, а особенно предпочтительно от -20 до 25°С.
Выделение полимерного производного можно проводить подходящим способом, который может включать одну или больше стадий. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, полимерное производное сначала отделяется от реакционной смеси или смеси реакционной смеси, например водной смесью 2-пропанола, подходящим способом, таким как центрифугирование или фильтрация. На второй стадии отделенное полимерное производное может быть подвергнуто дальнейшей обработке, такой как диализ, подобный последующей обработке, центрифужная фильтрация или фильтрация под давлением, ионообменная хроматография, хроматография в обращенной фазе, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация. В соответствии с еще более предпочтительным вариантом реализации, отделенное полимерное производное сначала диализируется, предпочтительно против воды, а затем лиофилизируется до тех пор, пока содержание растворителя продукта взаимодействия не будет достаточно низким, в соответствии с желательными спецификациями продукта. Лиофилизиацию можно проводить при температуре от 20 до 35°С, предпочтительно, от 20 до 30°С.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, функциональная группа Z белка, подлежащая взаимодействию с функциональной группой А полимера или полимерного производного, представляет собой тиоловую группу.
Тиоловая группа может присутствовать в белке как таковая. Более того, можно ввести тиоловую группу в белок в соответствии с подходящим способом. Среди других, можно упомянуть химические способы. Если в белке присутствует дисульфидный мостик, можно восстановить структуру -S-S- для получения тиоловой группы. Можно также преобразовать аминогруппу, присутствующую в полипептиде, в группу SH взаимодействием полипептида через аминогруппу с соединением, которое имеет, по меньшей мере, 2 различные функциональные группы, одна из которых способна взаимодействовать с аминогруппой, а другая представляет собой группу SH или предшественник группы SH, например N-сукцинимидил-S-ацетилтиоацетат, N-сукцинимидил-S-ацетилтиопропинат или N-сукцинимидил-3-(пиридилдитио)пропионат. Можно также ввести группу SH мутацией белка, например введением дополнительного цистеина в белок, обменом аминокислоты на цистеин или, например, удалением цистеина из белка с тем, чтобы лишить другой цистеин в белке возможности образовывать дисульфидный мостик. Наиболее предпочтительно полимер соединен со свободным цистеином белка, особенно предпочтительно Cys 17 или Cys 18, причем Cys 17 присутствует, например, в Granocyte®, а Cys 18 присутствует, например, в Neupogen®.
В соответствии с первым вариантом осуществления, функциональная группа Z белка представляет собой тиоловую группу, а функциональная группа А полимера представляет собой галогенацетильную группу, и где А введена взаимодействием полимера на его необязательно окисленном восстанавливающем конце, по меньшей мере, с бифункциональным соединением, имеющим, по меньшей мере, 2 функциональные группы, каждая из которых включает аминогруппу, для получения полимерного производного, имеющего, по меньшей мере, одну функциональную группу, включающую аминогруппу, и взаимодействием полимерного производного с моногалоген-замещенной уксусной кислотой и/или реакционноспособным производным моногалоген-замещенной уксусной кислоты.
Что касается, по меньшей мере, бифункционального соединения, имеющего, по меньшей мере, 2 функциональные группы, каждая из которых включает аминогруппу, то возможны все соединения, которые способны взаимодействовать с полимером на его необязательно восстанавливающем конце для получения полимерного производного, включающего аминогруппу, которая может взаимодействовать с моногалоген-замещенной уксусной кислотой и/или реакционноспособным производным моногалоген-замещенной уксусной кислоты.
В соответствии с предпочтительным вариантом осуществления, одна функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа взаимодействует с необязательно окисленным восстанавливающим концом полимера, выбрана из группы, состоящей из
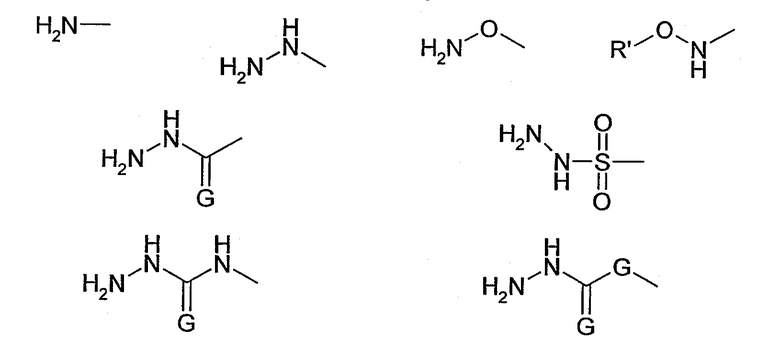
где G представляет собой O или S и, если они присутствует дважды, независимо O или S, и R' представляет собой метил.
В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа взаимодействует с необязательно окисленным восстанавливающим концом, представляет собой аминогруппу -NH2. В соответствии с еще одним предпочтительным вариантом осуществления, эта функциональная группа, наиболее предпочтительно аминогруппа, взаимодействует с окисленным восстанавливающим концом полимера.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, функциональная группа, по меньшей мере, бифункционального соединения, причем указанная функциональная группа взаимодействует с моногалоген-замещенной уксусной кислотой и/или реакционноспособным производным моногалоген-замещенной уксусной кислоты, представляет собой аминогруппу -NH2.
Функциональные группы, предпочтительно обе представляющие собой аминогруппу -NH2, по меньшей мере, бифункционального соединения, причем указанная функциональная группа взаимодействует с полимером на его необязательно окисленным восстанавливающим концом, предпочтительно окисленным восстанавливающим концом, и моногалоген-замещенной уксусной кислотой и/или реакционноспособным производным моногалоген-замещенной уксусной кислоты, могут быть отделены подходящим промежуточным соединением. Среди других, промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. Подходящими заместителями являются, среди других, группы алкил, арил, аралкил, алкарил, галоген, карбонил, ацил, карбокси, карбоксиэфир, гидрокси, тио, алкокси и/или алкилтио. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 2 до 10, предпочтительнее от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, а особенно предпочтительно от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь, или арильную группу, или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой алкильную цепь, имеющую от 1 до 20, предпочтительно от 2 до 10, и особенно предпочтительно от 2 до 8 атомов углерода. Таким образом, предпочтительными, по меньшей мере, бифункциональными соединениями являются бифункциональными амино соединениями, особенно предпочтительно 1,8-диаминооктан, 1,7-диаминогептан, 1,6-диаминогексан, 1,5-диаминопентан, 1,4-диаминобутан, 1,3-диаминопропан, и 1,2-диаминоэтан. В соответствии с еще одним предпочтительным вариантом осуществления, по меньшей мере, бифункциональное соединение представляет собой диаминополиэтиленгликоль, предпочтительно, диаминополиэтиленгликоль в соответствии с формулой
H2N-(CH2-CH2-O)m-CH2-CH2-NH2
где m представляет собой целое число, причем m предпочтительно равно 1, 2, 3 или 4.
Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер взаимодействует с 1,8-диаминооктаном, 1,7-диаминогептаном, 1,6-диаминогексаном, 1,5-диаминопентаном, 1,4-диаминобутаном, 1,3-диаминопропаном и 1,2-диаминоэтаном на его окисленном восстанавливающем конце для получения полимерного производного в соответствии с формулой
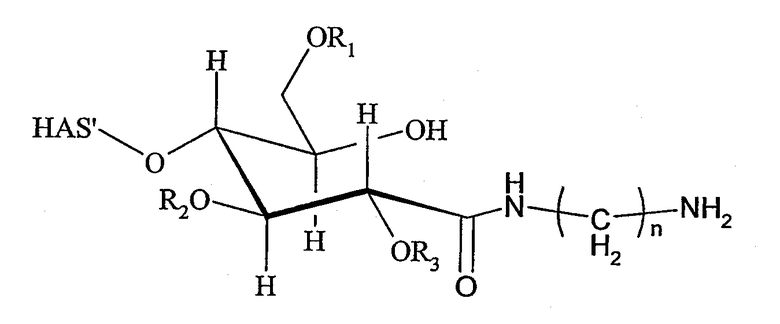
при n=2, 3, 4, 5, 6, 7 или 8, а полимер особенно предпочтительно представляет собой HES.
Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер взаимодействует с H2N-(CH2-CH2-O)m-CH2-CH2-NH2 на его окисленном восстанавливающем конце, где m представляет собой целое число, причем m предпочтительно равно 1, 2, 3 или 4, для получения полимерного производного в соответствии с формулой
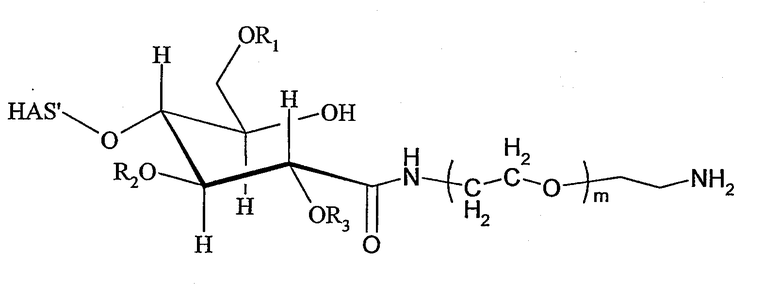
при m=1, 2, 3 или 4, а полимер особенно предпочтительно представляет собой HES.
Окисление восстанавливающего конца полимера, предпочтительно гидроксиэтилкрахмала, можно проводить в соответствии с каждым способом или комбинацией способов, которые приводят к получению соединений, имеющих структуры (IIa) и/или (IIb):
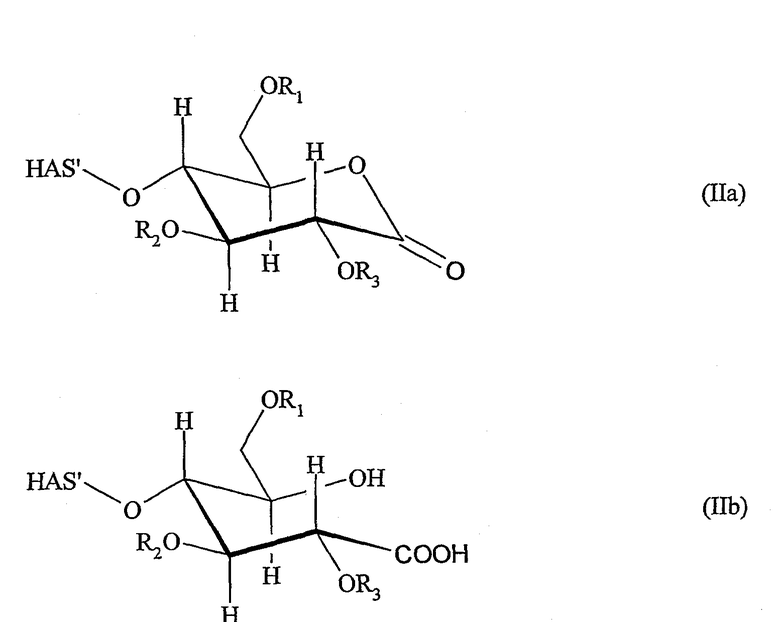
Хотя окисление можно проводить в соответствии с любым подходящим способом или способами, приводящими к получению окисленного восстанавливающего конца гидроксиалкилкрахмала, оно предпочтительно проводится с использованием щелочного раствора йода, как описано, например, в документе DE 196 28 705 А1, соответствующее содержание которого (пример А, колонка 9, строки 6-24) включено в настоящее описание в качестве ссылки.
Полимерное производное, полученное в результате взаимодействия полимера с, по меньшей мере, бифункциональным соединением, далее взаимодействует с моногалоген-замещенной уксусной кислотой и/или реакционноспособным производным моногалоген-замещенной уксусной кислоты.
В качестве моногалоген-замещенной уксусной кислоты или реакционноспособной кислоты предпочтительна Cl-замещенная, Br-замещенная и I-замещенная уксусная кислота, причем особенно предпочтителен хлорид уксусной кислоты.
Если галоген-замещенная кислота используется как таковая, то предпочтительно, чтобы кислота взаимодействовала с полимерным производным в присутствии активирующего агента. Подходящими активирующими агентами являются, среди других, карбодиимиды, такие как диизопропилкарбодиимид (DIC), дициклогексилкарбодиимиды (DCC), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), причем особенно предпочтительны дициклогексилкарбодиимиды (DCC) и 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC).
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер, предпочтительно HES, взаимодействует с диаминосоединением, предпочтительно диаминоалканом с 2-8 атомами углерода или H2N-(CH2-CH2-O)m-CH2-CH2-NH2 при m=1, 2, 3 или 4, и способ включает взаимодействие полученного полимерного производного с Br-замещенной и I-замещенной уксусной кислотой в присутствии активирующего агента, предпочтительно EDC.
Поэтому настоящее изобретение также относится к полимерному производному в соответствии с формулой
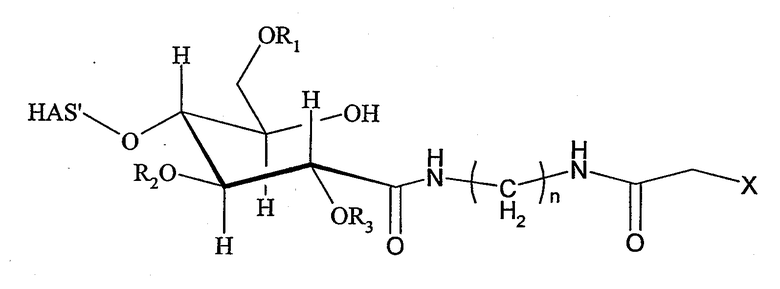
С Х=Cl, Br или I, n=2, 3, 4, 5, 6, 7 или 8 и полимер особенно предпочтительно представляет собой HES или полимерное производное в соответствии с формулой
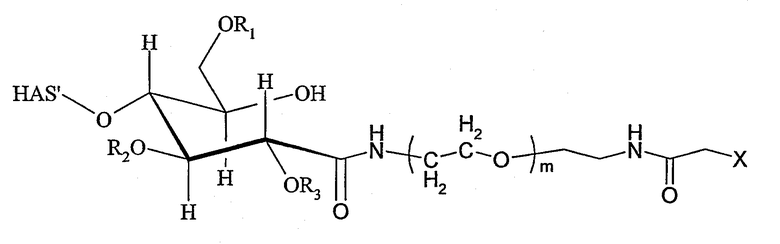
С Х=Cl, Br или I, m=1, 2, 3 или 4 и полимер особенно предпочтительно представляет собой HES.
Взаимодействие полимерного производного с галоген-замещенной уксусной кислотой предпочтительно проводится в водной системе, предпочтительно воде, при предпочтительном рН от 3,5 до 5,5, предпочтительнее от 4,0 до 5,0 и особенно предпочтительно от 4,5 до 5,0; и предпочтительной температуре взаимодействия от 4 до 30°С, предпочтительнее от 15 до 25 и особенно предпочтительно от 20 до 25°С; и в течение предпочтительного времени взаимодействия от 1 до 8 ч, предпочтительнее от 2 до 6 ч и особенно от 3 до 5 ч.
Реакционную смесь, включающую полимерное производное, которое включает полимер, по меньшей мере, бифункциональное соединение и галоген-замещенную уксусную кислоту, можно использовать для взаимодействия с белком как таковым. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, полимерное производное отделяется от реакционной смеси предпочтительно ультрафильтрацией, последующим осаждением, необязательным промыванием и сушкой в вакууме.
Взаимодействие полимерного производного с белком предпочтительно проводится в водной системе.
Взаимодействие полимерного производного с белком проводится при предпочтительном рН от 6,5 до 8,5, предпочтительнее от 7,0 до 8,5 и особенно предпочтительно от 7,5 до 8,5; и предпочтительной температуре взаимодействия от 4 до 30°С, предпочтительнее от 15 до 25 и особенно предпочтительно от 20 до 25°С; и в течение предпочтительного времени взаимодействия от 0,5 до 8 ч, предпочтительнее от 1 до 6 ч и особенно от 2 до 5 ч.
Взаимодействие полимерного производного с тиоловой группой белка приводит к тиоэфирной связи между полимерным производным и белком.
Поэтому, настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер, предпочтительно HES, взаимодействует с диаминосоединением, предпочтительно диаминоалканом с 2-8 атомами углерода или H2N-(CH2-CH2-O)m-CH2-CH2-NH2 при m=1, 2, 3 или 4, полученное полимерное производное взаимодействует с Br-замещенной и I-замещенной уксусной кислотой в присутствии активирующего агента, предпочтительно EDC, и полученное полимерное производное взаимодействует с тиоловой группой белка для получения конъюгата, включающего тиоэфирную связь между белком и полимерным производным.
Поэтому настоящее изобретение также относится к конъюгату в соответствии с формулой
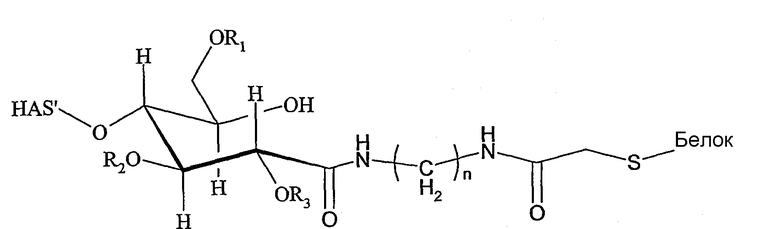
при n=2, 3, 4, 5, 6, 7 или 8 и полимер особенно предпочтительно представляет собой HES, или конъюгату в соответствии с формулой
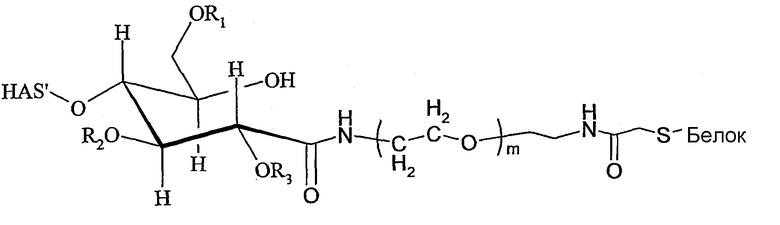
при m=1, 2, 3 или 4 и полимер предпочтительно представляет собой HES. Гидроксиэтилкрахмал представляет собой предпочтительно гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7.
В соответствии со вторым вариантом осуществления, функциональная группа Z белка представляет собой тиоловую группу, а функциональная группа А полимера включает малеимидогруппу.
В соответствии с этим вариантом осуществления, существуют несколько возможностей получить конъюгат. В целом, полимер взаимодействует на его необязательно окисленном восстанавливающем конце, по меньшей мере, с бифункциональным соединением, причем это, по меньшей мере, бифункциональное соединение включает одну функциональную группу, которая способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера, и, по меньшей мере, одну функциональную группу, которая или включает малеимидогруппу, или химически модифицирована для получения полимерного производного, которое включает малеимидогруппу. В соответствии с предпочтительным вариантом осуществления, указанная функциональная группа химически модифицирована для получения полимерного производного, которое включает малеимидогруппу.
Поэтому настоящее изобретение относится к способу и конъюгату, как описано выше, взаимодействием полимерного производного, включающего малеимидогруппу, с тиоловой группой белка, причем указанный способ включает взаимодействие полимера на его необязательно окисленном восстанавливающем конце, по меньшей мере, с бифункциональным соединением, включающим функциональную группу U, способную взаимодействовать с необязательно окисленным восстанавливающим концом, причем, по меньшей мере, бифункциональное соединение, кроме того, включает функциональную группу W, способную к химической модификации, для получения малеимидогруппы, причем способ, кроме того, включает химическую модификацию функциональной группы W для получения малеимидогруппы.
В качестве функциональной группы U возможна каждая функциональная группа, которая способна взаимодействовать с необязательно окисленным восстанавливающим концом полимера.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, функциональная группа U включает химическую структуру -NH-.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа U включает структуру -NH-.
В соответствии с одним предпочтительным вариантом осуществления настоящего изобретения, эта функциональная группа U представляет собой группу, имеющую структуру R'-NH-, где R' представляет собой водород или алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток, где циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остаток может быть соединен непосредственно с группой NH или, в соответствии с другим вариантом осуществления, может быть соединен кислородным мостиком с группой NH. Алкильный, циклоалкильный, арильный, аралкильный, арилциклоалкильный, алкарильный или циклоалкиларильный остатки могут быть подходяще замещенными. В качестве предпочтительных заместителей можно упомянуть галогены, такие как F, Cl или Br. Особенно предпочтительными остатками R' являются водород, алкильная и алкоксигруппы, а еще предпочтительнее являются водород и незамещенные алкильная и алкоксигруппы.
Среди алкильной и алкоксигрупп, предпочтительны группы с 1, 2, 3, 4, 5 или 6 атомами С. Более предпочтительными являются метильная, этильная, пропильная, изопропильная, метокси, этокси, пропокси и изопропоксигруппы. Особенно предпочтительными являются метил, этил, метокси, этокси, и особенное предпочтение отдается метилу или метокси.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где R' представляет собой водород или метильную или метоксигруппу.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, функциональная группа U имеет структуру R'-NH-R”, где R” предпочтительно включает структурную единицу -NH- и/или структурную единицу -(C=G)-, где G представляет собой O или S и/или структурную единицу -SO2-. В соответствии с более предпочтительными вариантами осуществления, функциональная группа R” выбрана из группы, состоящей из
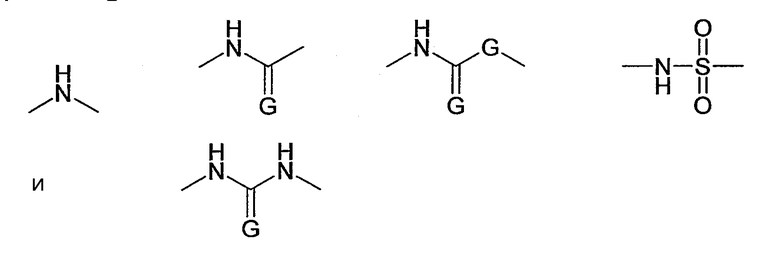
где, если G присутствует дважды, она представляет собой независимо O или S.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где функциональная группа U выбрана из группы, состоящей из
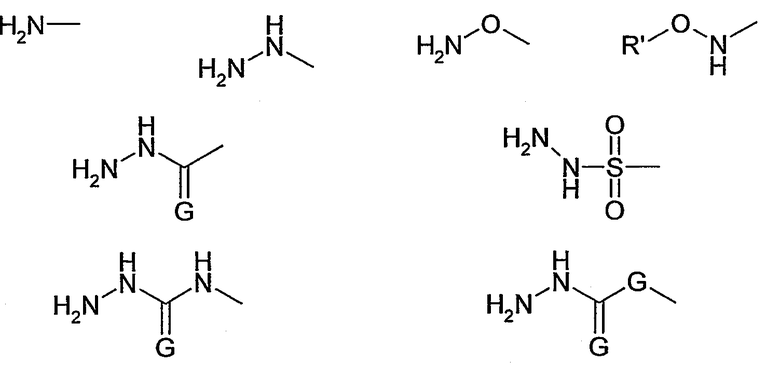
где G представляет собой O или S и, если присутствует дважды, независимо O или S, и R' представляет собой метил.
В соответствии с еще более предпочтительными вариантом осуществления настоящего изобретения, U включает аминогруппу -NH2.
В соответствии с вариантом осуществления настоящего изобретения, функциональная группа W, по меньшей мере, бифункционального соединения химически модифицирована взаимодействием полимерного производного, включающего W, с еще одним, по меньшей мере, бифункциональным соединением, включающим функциональную группу, способную взаимодействовать с W, и, кроме того, включающую малеимидогруппу.
Что касается функциональной группы W и функциональной группы указанного еще одного, по меньшей мере, бифункционального соединения, которое способно взаимодействовать с W, то следует, среди других, упомянуть следующие функциональные группы:
- С-С-двойные связи, или С-С-тройные связи, или ароматические С-С-связи;
- тиогруппа или гидроксигруппы;
- гидразид алкилсульфоновой кислоты, гидразид арилсульфоновой кислоты;
- 1,2-диолы;
- 1,2-аминоспирты;
- 1,2-аминотиоспирты;
- азиды;
- аминогруппа -NH2 или производные аминогрупп, включающие структурную единицу -NH-, такие как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы или алкариламиногруппы;
- гидроксиламиногруппа -O-NH2, или производные гидроксиламиногруппы, включающие структурную единицу -O-NH-, такие как гидроксилалкиламиногруппы, гидроксилариламиногруппы, гидроксиларалкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогруппы, арилоксиаминогруппы, аралкилоксиаминогруппы или алкарилоксиаминогруппы, каждая из которых включает структурную единицу -NH-O-;
- остатки, имеющие карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такое как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;

где соответственно W и функциональная группа еще одного, по меньшей мере, бифункционального соединения, представляет собой группу, способную образовывать химическую связь с одной из указанных выше групп.
В соответствии с еще более предпочтительным вариантом осуществления настоящего изобретения, W включает аминогруппу -NH2.
В соответствии с предпочтительными вариантами осуществления настоящего изобретения, и W, и другая функциональная группа представляют собой группы из приведенного выше перечня групп.
В соответствии с одним вариантом осуществления настоящего изобретения, одна из этих функциональных групп представляет собой тиогруппу. В этом конкретном случае другая функциональная группа предпочтительно выбрана из группы, состоящей из
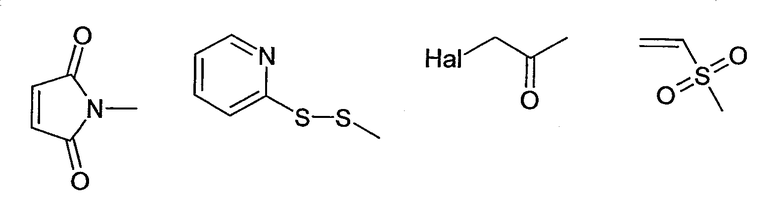
где Hal представляет собой Cl, Br, или I, предпочтительно Br или I.
В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, одна из этих функциональных групп выбрана из группы, состоящей из реакционноспособного сложного эфира, такого как сложный эфир гидроксиламинов, имеющих имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или такие как арилокси соединение с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил, или карбоксигруппа, которая необязательно трансформирована в реакционноспособный сложный эфир. В этом конкретном случае другая функциональная группа включает химическую структуру -NH-.
В соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения, W включает структуру -NH-, а еще одно, по меньшей мере, бифункциональное соединение включает реакционноспособный сложный эфир и малеимидогруппу.
Что касается функциональной группы W, включающей структуру -NH-, можно сделать ссылку на функциональную группу, как описано выше, где W может быть такой же или отличной от U. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, U и W являются одинаковыми. Предпочтительнее и U, и W включают аминогруппу. Особенно предпочтительно и U, и W представляют собой аминогруппу -NH2.
В соответствии с одним вариантом осуществления настоящего изобретения, полимер может взаимодействовать с, по меньшей мере, бифункциональным соединением, включающим U и W на его неокисленном восстанавливающем конце в водной среде. В соответствии с предпочтительным вариантом осуществления, где и U, и W представляют собой аминогруппу, взаимодействие проводится с использованием полимера с восстанавливающим концом в окисленной форме, по меньшей мере, в одном апротонном растворителе, особенно предпочтительно в безводном апротонном растворителе, имеющем содержание воды не более чем 0,5% мас., предпочтительно не более чем 0,1% мас. Подходящими растворителями, среди других, являются диметилсульфоксид (DMSO), N-метилпирролидон, диметилацетамид (DMA), диметилформамид (DMF) и смеси двух или более из них.
Особенно, в случае, когда и U, и W представляют собой аминогруппу -NH2, U и W могут быть отделены любым подходящим промежуточным соединением. Среди других, промежуточное соединение может представлять собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток. Подходящими заместителями являются, среди других, алкильная, арильная, аралкильная, алкарильная, галогеновая, карбонильная, ацильная, карбокси, карбоксиэфирная, гидрокси, тио, алкокси и/или алкилтиогруппы. В целом, углеводородный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 2 до 10, предпочтительнее, от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода. Если присутствуют гетероатомы, то отделяющая группа включает в целом от 1 до 20, предпочтительно от 1 до 8, а особенно предпочтительно от 1 до 4 гетероатомов. Углеводородный остаток может включать необязательно разветвленную алкильную цепь или арильную группу или циклоалкильную группу, имеющую, например, от 5 до 7 атомов углерода, или представлять собой аралкильную группу, алкарильную группу, где алкильная часть может представлять собой линейную и/или циклическую алкильную группу. В соответствии с еще более предпочтительным вариантом осуществления, углеводородный остаток представляет собой алкильную цепь из 1 до 20, предпочтительно от 2 до 10, предпочтительнее от 2 до 6, а особенно предпочтительно от 2 до 4 атомов углерода.
Поэтому настоящее изобретение также относится к способу и конъюгату, как описано выше, где полимер взаимодействует своим окисленным восстанавливающим концом с 1,4-диаминбутаном, 1,3-диаминпропаном или 1,2-диаминэтаном для получения полимерного производного в соответствии с формулой
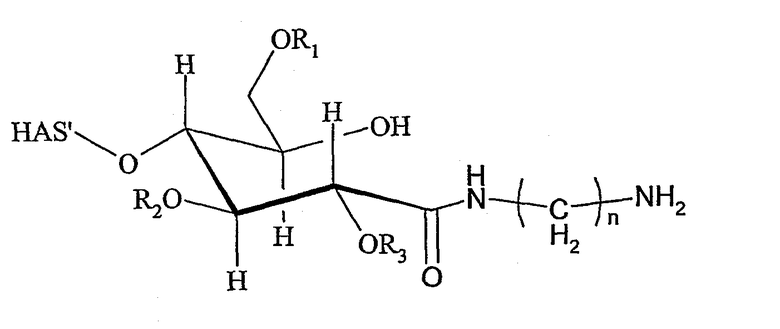
при n=2, 3 или 4, причем полимер предпочтительно представляет собой HES.
В соответствии с указанным выше предпочтительным вариантом осуществления, полимерное производное, включающее аминогруппу, далее взаимодействует с, по меньшей мере, бифункциональным соединением, включающим реакционноспособную сложноэфирную группу и малеимидогруппу. Реакционноспособная сложноэфирная группа и малеимидогруппа могут быть отделены подходящим промежуточным соединением. Что касается этого промежуточного соединения, то можно сослаться на промежуточное соединение между функциональными группами U и W. В соответствии с предпочтительным вариантом осуществления настоящего изобретения, реакционноспособная сложноэфирная группа и малеимидогруппа разделены углеводородной цепью, имеющей от 1 до 10, предпочтительно, от 1 до 8 предпочтительнее от 1 до 6, предпочтительнее от 1 до 4, предпочтительнее от 1 до 2 и особенно предпочтительно 1 атом углерода. В соответствии с еще одним предпочтительным вариантом осуществления, реакционноспособный сложный эфир представляет собой сложный эфир сукцинимида, а в соответствии с особенно предпочтительным вариантом осуществления, по меньшей мере, бифункциональное соединение, включающее малеимидогруппу и реакционноспособную сложноэфирную группу, представляет собой сложный эфир N-(альфа-малеимидоацетокси)сукцинимида.
Поэтому настоящее изобретение также относится к полимерному производному в соответствии с формулой
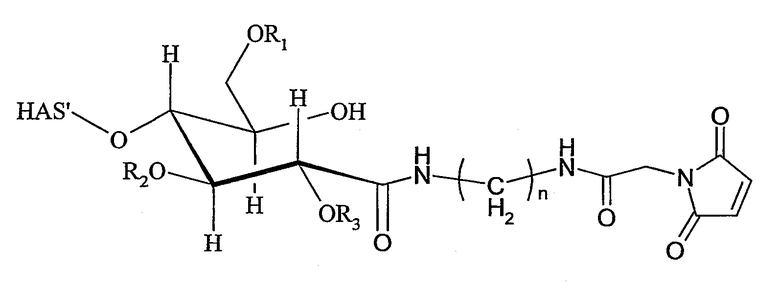
при n=2, 3 или 4, причем полимер предпочтительно представляет собой HES.
Полимерное производное, включающее малеимидогруппу, далее взаимодействует с тиоловой группой белка для получения конъюгата, включающего полимерное производное, соединенное с белком посредством тиоэфирной группы.
Поэтому настоящее изобретение также относится к конъюгату, включающему белок и полимер, в соответствии с формулой
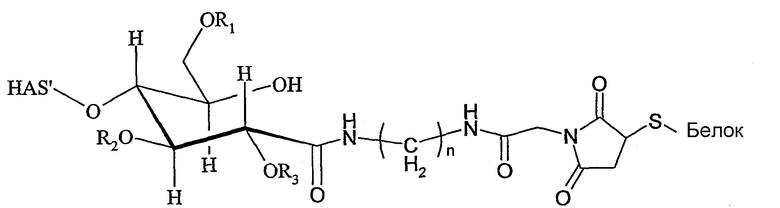
при n=2, 3 или 4, причем полимер предпочтительно представляет собой HES, и где атом S в представленной выше формуле происходит из Cys17 или Cys18 белка. Гидроксиэтилкрахмал представляет собой предпочтительно гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 10 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 12 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 18 кДа и DS примерно 0,7, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,4, или гидроксиэтилкрахмал, имеющий среднюю молекулярную массу примерно 50 кДа и DS примерно 0,7.
Взаимодействие полимерного производного, включающего малеимидогруппу, с тиоловой группой белка предпочтительно проводится в водной системе с приданными ей буферными свойствами при предпочтительно рН от 5,5 до 8,5, предпочтительнее от 6 до 8, а особенно предпочтительно от 6,5 до 7,5, и предпочтительной температуре взаимодействия от 0 до 40°С, предпочтительно от 0 до 25 и особенно предпочтительно от 4 до 21°С, и в течение предпочтительного времени взаимодействия от 0,5 до 24 ч, предпочтительнее от 1 до 20 ч и особенно от 2 до 17 ч. Подходящую величину рН реакционной смеси можно регулировать добавлением, по меньшей мере, одного подходящего буфера. Среди предпочтительных буферов можно упомянуть буфер ацетата натрия, фосфатный или боратный буферы, содержащие или мочевину в предпочтительной концентрации от 0 до 8 М, предпочтительнее от 2 до 8 М и особенно предпочтительно от 4 до 8 М, и/или содержащие SDS в предпочтительной концентрации от 0 до 1% (мас./об.), предпочтительнее, от 0,4 до 1% (мас./об.), и особенно предпочтительно, от 0,8 до 1% (мас./об.).
Конъюгат может быть подвергнут дальнейшей обработке, такой как последующая обработка, подобная диализу, центрифужная фильтрация или фильтрация давлением, ионообменная хроматография, хроматография в обращенной фазе, ВЭЖХ, ЖХСД, гель-фильтрация и/или лиофилизация.
Поэтому настоящее изобретение также относится к конъюгату, который можно получить способом, как описано выше.
Поэтому настоящее изобретение также относится к конъюгату, который можно получить способом, как описано выше, где А представляет собой реакционноспособную карбоксигруппу, и где А была введена в полимер, восстанавливающий конец которого не был окислен, взаимодействием, по меньшей мере, одной гидроксигруппы полимера со сложным карбоновым диэфиром, и где указанная, содержащая один полимер молекула и, по меньшей мере, одна, в частности, от 1 до 10 молекул белка, связаны с полимером через амидные связи.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
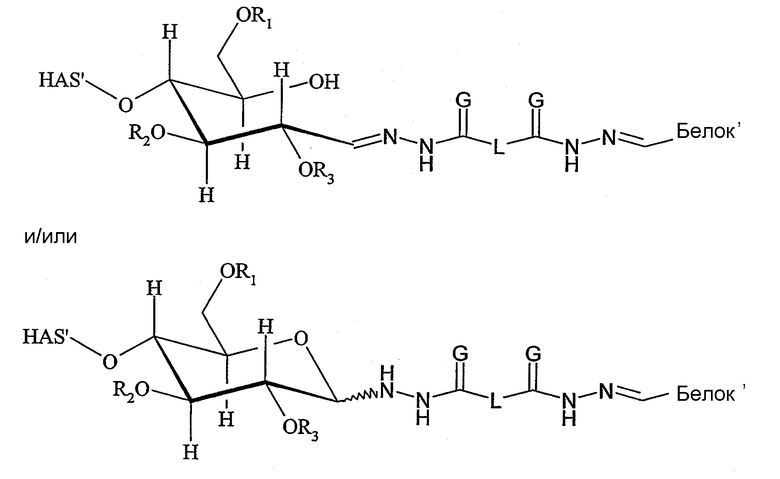
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу,
где G выбрана из группы, состоящей из O и S, предпочтительно О, и где L представляет собой необязательно подходящим образом замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, предпочтительно алкильный, арильный, аралкильный, гетероарильный, гетероаралкильный остаток, имеющий от 2 до 60 атомов углерода.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома углерода углеводородного соединения в двойной связи N=C.
Настоящее изобретение также относится к конъюгату, как описано выше, где -L- представляет собой -(CH2)n- при n=2, 3, 4, 5, 6, 7, 8, 9, 10, предпочтительно 2, 3, 4, 5, 6, предпочтительнее 2, 3, 4 и особенно предпочтительно 4.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
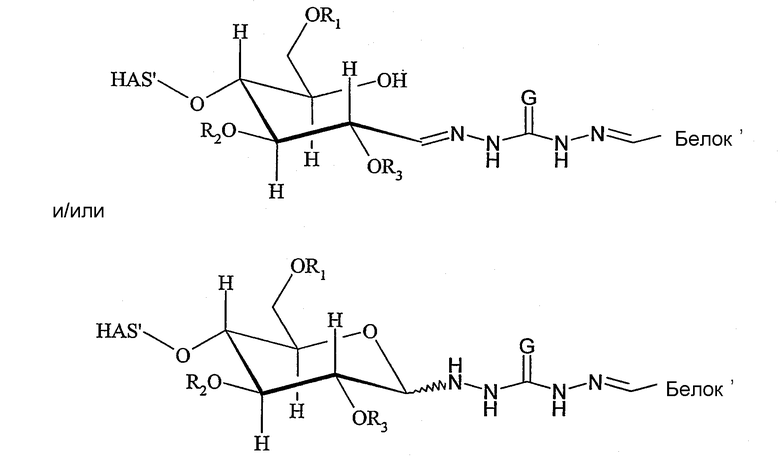
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где G выбрана из группы, состоящей из О и S, предпочтительно О.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома углерода углеводородной части, которая представляет собой часть оксимной связи в двойной связи N=C.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
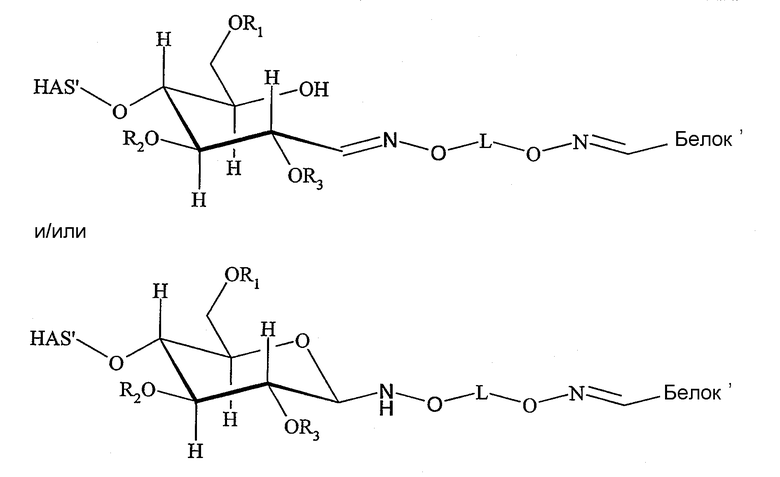
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где L представляет собой необязательно подходящим образом замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, предпочтительно алкильный, арильный, аралкильный, гетероарильный, гетероаралкильный остаток, имеющий от 2 до 60 атомов углерода.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома углерода углеводородной части, которая представляет собой часть оксимной связи в двойной связи N=C.
Указанные выше 2 структуры описывают структуру, где поперечно сшивающее соединение связанно через оксимную связь с восстанавливающим концом HAS, где концевая сахаридная единица HES присутствует в открытой форме, а структура в соответствующей циклической аминальной форме, где поперечно сшивающее соединение связано с восстанавливающим концом HES через оксиаминогруппу, и где концевая сахаридная единица HES присутствует в циклической форме. Обе структуры могут одновременно присутствовать в равновесии друг с другом.
Настоящее изобретение также относится к конъюгату, как описано выше, где -L- представляет собой
-[(CRaRb)mG]n[CRcRd]o-
где остатки Ra, Rb, Rc, Rd представляют собой независимо водород, алкил, арил, предпочтительно водород,
где G выбран из группы, состоящей из О и S, предпочтительно О,
и где
m=1, 2, 3 или 4, где Ra и Rb могут быть одинаковыми или различными в m группах СRaRb;
n=0-20, предпочтительно 0-10, предпочтительнее 1, 2, 3, 4, 5, наиболее предпочтительно 1 или 2;
о=0-20, предпочтительно 0-10, предпочтительнее 1, 2, 3, 4, 5, наиболее предпочтительно 1 или 2,
где остатки Rc и Rd могут быть одинаковыми или различными в о группах СRcRd.
Настоящее изобретение также относится к конъюгату, как описано выше, где Ra, Rb, Rc, Rd представляют собой водород, m=2, n=1 и о=2.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
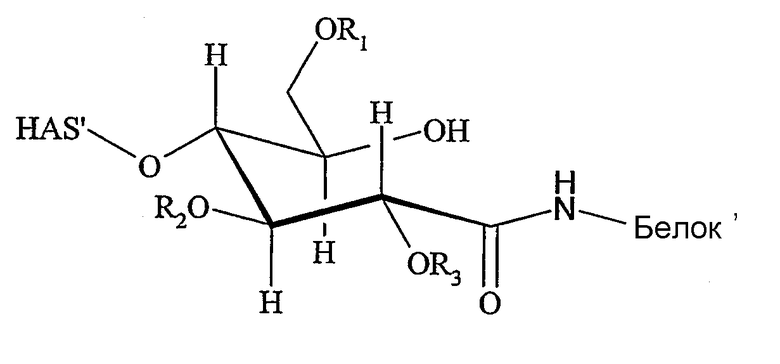
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома азота аминогруппы, которая представляет собой часть амидной связи.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
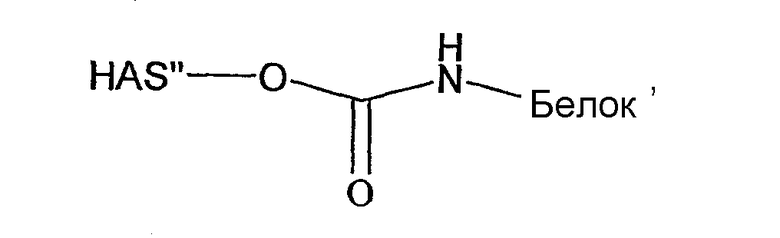
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где связь -О-(С=О)- была образована взаимодействием карбоксигруппы или реакционноспособной карбоксигруппы с гидроксигруппой молекулы HAS.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома азота аминогруппы, которая представляет собой часть амидной связи.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
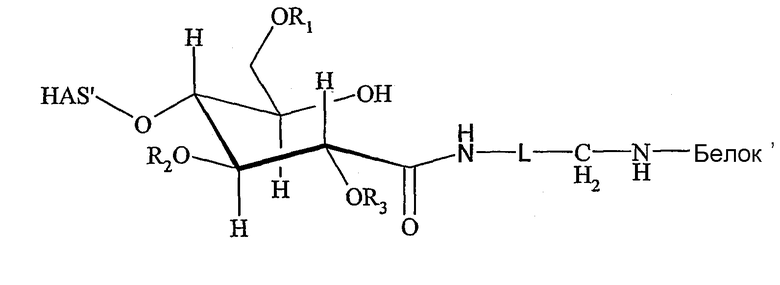
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее, водород или гидроксиэтильную группу, и
где L представляет собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, имеющий от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 1 до 10, предпочтительнее от 1 до 6, предпочтительнее от 1 до 2 атомов углерода, а особенно предпочтительно 1 атом углерода, причем L представляет собой в частности СН2.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома азота аминогруппы, которая представляет собой часть аминометиловой связи.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
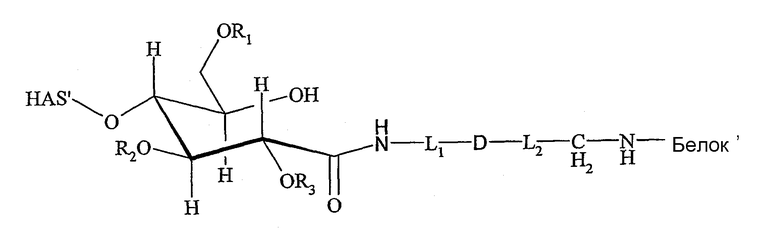
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где L1 и L2 представляют собой независимо необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, включающий алкильную, арильную, аралкильную, гетероалкильную и/или гетероаралкильную часть, причем указанный остаток имеет от 1 до 60, предпочтительно от 1 до 40, предпочтительнее от 1 до 20, предпочтительнее от 1 до 10 атомов углерода, и
где D представляет собой связь, предпочтительно ковалентную связь, которая образована подходящей функциональной группой F2, связанной с L1, и подходящей функциональной группой F3, связанной с L2.
Аббревиатура «Белок», используемая в приведенных выше формулах, относится к молекуле G-CSF, используемой для взаимодействия, без атома азота аминогруппы, которая представляет собой часть аминометиловой связи.
Настоящее изобретение также относится к конъюгату, как описано выше, где L1 представляет собой -(CH2)n- при n=2, 3, 4, 5, 6, 7, 8, 9, 10, предпочтительно 2, 3, 4, 5, 6, предпочтительнее 2, 3, 4 и особенно предпочтительно 4.
Настоящее изобретение также относится к конъюгату, как описано выше, где L2 включает необязательно подходящим образом замещенную арильную часть, предпочтительно арильную часть, содержащую 6 атомов углерода, причем L2 особенно предпочтительно представляет собой C6H4, или где L2 представляет собой -(CH2)n- при n=2, 3, 4, 5, 6, 7, 8, 9, 10, предпочтительно 2, 3, 4, 5, 6, предпочтительнее 2, 3, 4.
Настоящее изобретение также относится к конъюгату, как описано выше, где функциональная группа выбрана из
- С-С-двойных связей или С-С-тройных связей, или ароматических С-С-связей;
- тиогруппы или гидроксигруппы;
- гидразида алкилсульфоновой кислоты, гидразида арилсульфоновой кислоты;
- 1,2-диолов;
- 1,2-аминотиоспиртов;
- азидов;
- 1,2-аминоспиртов;
- аминогруппы -NH2 или производных аминогрупп, включающих структурную единицу -NH-, таких как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы или алкариламиногруппы;
- гидроксиламиногруппы -O-NH2 или производных гидроксиламиногруппы, включающих структурную единицу -O-NH-, такую как гидроксилалкиламиногруппы, гидроксилариламиногруппы, гидроксиларалкиламиногруппы или гидроксалалкариламиногруппы;
- алкоксиаминогрупп, арилоксиаминогрупп, аралкилоксиаминогрупп или алкарилоксиаминогрупп, каждая из которых включает структурную единицу -NH-O-;
- остатков, имеющих карбонильную группу, -Q-C(=G)-M, где G представляет собой O или S, а М представляет собой, например,
-- -ОН или -SH;
-- алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
-- алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
-- алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
-- активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такие как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или O;
- -NH-NH2 или -NH-NH-;
- -NO2;
- нитрильную группу;
- карбонильные группы, такие как альдегидная группа или кетогруппа;
- карбоксигруппу;
- группу -N=C=O или группу -N=C=S;
- группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
- -C≡C-H;
- -(C=NH2Cl)-OАлкил;
- группы -(C=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
- -CH=CH-SO2-;
- дисульфидную группу, включающую структуру -S-S-;

где F3 представляет собой функциональную группу, способную образовывать химическую связь с F2, и предпочтительно выбрана из указанных выше групп, причем F2 предпочтительно включает часть -NH-, предпочтительно включает аминогруппу, F3 предпочтительно включает часть -(C=G)-, предпочтительнее -(С=О)-, предпочтительнее часть -(C=G)-G-, еще предпочтительнее -(C=O)-G-, а особенно предпочтительно -(C=O)-O-, причем особенно предпочтительно D представляет собой амидную связь.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
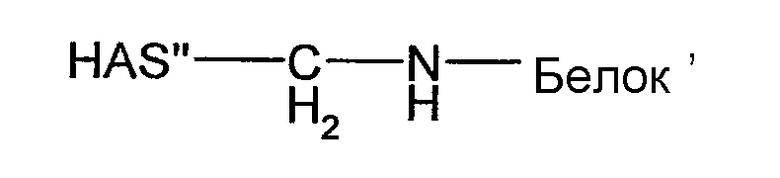
где атом углерода части -CH2-N2- получен из альдегидной группы, которая была введена в полимер раскрывающей кольцо реакцией окисления, где HAS” относится к молекуле гидроксиалкилкрахмала без альдегидной группы, полученной в результате раскрывающей кольцо реакции окисления, и взаимодействующей с аминогруппой белка, и где атом азота получен из аминогруппы белка.
Аббревиатура «Белок», используемая в приведенной выше формуле, относится к молекуле G-CSF, используемой для взаимодействия, без атома азота аминогруппы, которая представляет собой часть амидной связи.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
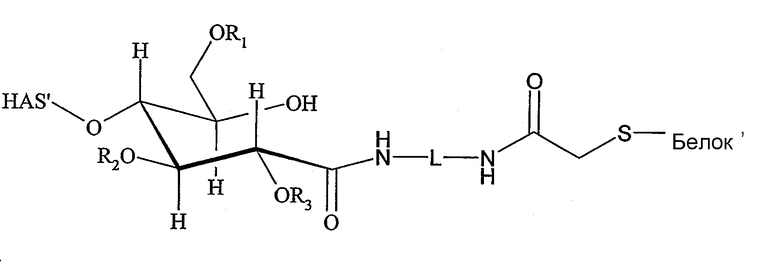
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где L представляет собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, включающий алкильную, арильную, аралкильную, гетероалкильную и/или гетероаралкильную часть, причем указанный остаток имеет от 2 до 60, предпочтительно от 2 до 40, предпочтительнее от 2 до 20, предпочтительнее от 2 до 10 атомов углерода, и где атом серы получен из цистеинового остатка или дисульфидной группы белка.
Настоящее изобретение также относится к конъюгату, как описано выше, где -L- представляет собой
-[(CRaRb)mG]n[CRcRd]o-
где Ra, Rb, Rc, Rd представляют собой независимо водород, алкил, арил, предпочтительно водород,
где G выбран из группы, состоящей из О и S, предпочтительно О,
и где
m=1, 2, 3 или 4, наиболее предпочтительно 2, где остатки Ra и Rb могут быть одинаковыми или различными в m группах СRaRb;
n=1-20, предпочтительно 1-10, предпочтительнее 1, 2, 3, или 4;
о=1-20, предпочтительно 1-10, предпочтительнее 1, 2, 3, 4, 5, наиболее предпочтительно 1 или 2, наиболее предпочтительно 1, где остатки Rc и Rd могут быть одинаковыми или различными в огруппах СRcRd;
или
где
n=0, и
о=2-20, предпочтительно 2-10, предпочтительнее 2, 3, 4, 5, 6, 7 или 8, где остатки Rc и Rd могут быть одинаковыми или различными в огруппах СRcRd.
Настоящее изобретение также относится к конъюгату, включающему белок и полимер или его производное, где полимер представляет собой гидроксиалкилкрахмал (HAS), а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой
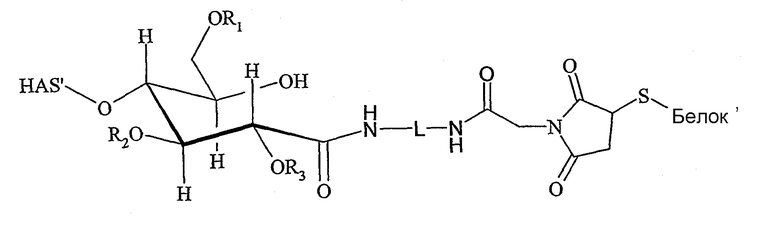
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, гидроксиарильную группу, гидроксиаралкильную группу или гидроксиалкарильную группу, имеющую от 1 до 10 атомов углерода, предпочтительно водород или гидроксиалкильную группу, предпочтительнее водород или гидроксиэтильную группу, и
где L представляет собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, включающий алкильную, арильную, аралкильную, гетероалкильную и/или гетероаралкильную часть, причем указанный остаток имеет от 2 до 60, предпочтительно от 2 до 40, предпочтительнее от 2 до 20, предпочтительнее от 2 до 10 атомов углерода, и
где атом серы получен из цистеинового остатка или дисульфидной группы белка.
Настоящее изобретение также относится к конъюгату, как описано выше, где -L- представляет собой
-[(CRaRb)mG]n[CRcRd]o-
где Ra, Rb, Rc, Rd представляют собой независимо водород, алкил, арил, предпочтительно водород,
где G выбран из группы, состоящей из О и S, предпочтительно О, и где
m=1, 2, 3 или 4, наиболее предпочтительно 2, где остатки Ra и Rb могут быть одинаковыми или различными в m группах СRaRb;
n=1-20, предпочтительно 1-10, предпочтительнее 1, 2, 3 или 4;
о=1-20, предпочтительно 1-10, предпочтительнее 1, 2, 3, 4, 5, предпочтительнее 1 или 2, наиболее предпочтительно 1, где остатки Rc и Rd могут быть одинаковыми или различными в огруппах СRcRd;
или
где
n=0, и
о=2-20, предпочтительно 2-10, предпочтительнее 2, 3, 4, 5, 6, 7 или 8, где остатки Rc и Rd могут быть одинаковыми или различными в огруппах СRcRd.
Настоящее изобретение также относится к любому конъюгату, как описано выше, где гидроксиалкилкрахмал представляет собой гидроксиэтилкрахмал.
Настоящее изобретение также относится к любому конъюгату, как описано выше, где гидроксиэтилкрахмал имеет молекулярную массу от 2 до 200 кДа, предпочтительно от 4 до 130 кДа, предпочтительнее от 4 до 70 кДа.
В соответствии с еще одним аспектом, настоящее изобретение относится к конъюгату, как описано выше, или к конъюгату, который можно получить способом, как описано выше, для применения в способе для лечения организма человека или животного.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей в терапевтически эффективном количестве конъюгат, как описано выше, или к конъюгату, который можно получить способом, как описано выше.
Термин «в терапевтически эффективном количестве», используемый в контексте настоящего изобретения, относится к тому количеству, которое обеспечивает терапевтический эффект для данного состояния и схемы введения. Введение предпочтительно проводится обычными путями. Определенный выбранный путь будет зависеть от подлежащего лечению состояния. Введение предпочтительно осуществляется в виде части состава, содержащего подходящий носитель, такой как полисорбат, подходящий разбавитель, такой как вода, и/или подходящий адъювант, такой как сорбит. Требуемая дозировка будет зависеть от тяжести состояния подлежащего лечению состояния, индивидуальной реакции пациента, способа введения и им подобных факторов.
Таким образом, в предпочтительном варианте осуществления фармацевтическая композиция, кроме того, включает, по меньшей мере, один фармацевтически приемлемый разбавитель, адъювант и/или носитель, особенно предпочтительно используемый при лечении G-CSF.
Фармацевтическая композиция предпочтительно используется для лечения расстройства, характеризуемого сниженной гематопоэтической или иммунной функцией или связанных с ней заболеваний.
Поэтому настоящее изобретение также относится к применению фармацевтической композиции, как описано выше, включающей конъюгат, как описано выше, или конъюгат, который можно получить способом, как описано выше, для изготовления лекарственного средства для лечения расстройства, характеризуемого сниженной гематопоэтической или иммунной функцией.
В соответствии с предпочтительным вариантом осуществления, расстройство, характеризуемое сниженной гематопоэтической или иммунной функцией, представляет собой результат химиотерапии, лучевой терапии, инфекционное заболевание, тяжелую хроническую нейтропению или лейкоз. Поэтому настоящее изобретение также относится к применению фармацевтической композиции, как описано выше, включающей конъюгат, как описано выше, или конъюгат, который можно получить способом, как описано выше, для изготовления лекарственного средства для лечения расстройства, характеризуемого сниженной гематопоэтической или иммунной функцией, причем расстройство, представляет собой результат химиотерапии, лучевой терапии, инфекционное заболевание, тяжелую хроническую нейтропению или лейкоз.
Объекту лечения фармацевтической композицией в соответствии с изобретением введение предпочтительно проводится внутривенным или подкожным путями. Для этого фармацевтическую композицию можно ввести в виде стерильного раствора.
Изобретение далее иллюстрируется следующими чертежами, таблицами и примерами, которые никоим образом не предназначены для ограничения объема настоящего изобретения.
Краткое описание чертежей
Фиг.1а
На фиг.1а показан анализ конъюгата HES-G-CSF SDS-PAGE (электрофорезом в полиакриламидном геле с додецилсульфатом натрия), полученного в соответствии с примером 2.1(а), Neupogen®. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS (3-(N-морфолино)пропансульфоновой кислотой - додецилсульфатом натрия) при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D) Молекулярная масса маркера сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт после конъюгации G-CSF (Neupogen®) с HES, как описано в примере 2.1(а).
Полоса С: Исходный материал G-CSF.
Фиг.1b
На фиг.1b показан анализ конъюгата HES-G-CSF SDS-PAGE, полученного в соответствии с примером 2.1(а), Granocyte®. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D) Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт после конъюгации G-CSF (Granocyte®) с HES, как описано в примере 2.1(а).
Полоса С: Исходный материал G-CSF.
Фиг.2
На фиг.2 показан анализ конъюгата HES-G-CSF SDS-PAGE, полученного в соответствии с примером 2.1(b), G-CSF от Strathmann Biotec AG, Hamburg, D. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт после конъюгации G-CSF с HES10/0,4 в буфере 0,1М NaOAc рН 5,0.
Полоса С: Неочищенный продукт после конъюгации G-CSF с HES10/0,7 в буфере 0,1М NaOAc рН 5,0.
Полоса D: Неочищенный продукт после конъюгации G-CSF с HES50/0,4 в буфере 0,1М NaOAc рН 5,0.
Полоса E: Неочищенный продукт после конъюгации G-CSF с HES50/0,7 в буфере 0,1М NaOAc рН 5,0.
Полоса F: Исходный материал G-CSF.
Фиг.3
На фиг.3 показан анализ конъюгатов HES-G-CSF SDS-PAGE, полученных в соответствии с примером 2.2, G-CSF от Strathmann Biotec AG, Hamburg, D. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт после конъюгации G-CSF с HES10/0,7 в буфере 0,1М NaOAc рН 5,0.
Полоса С: Неочищенный продукт после конъюгации G-CSF с HES50/0,4 в буфере 0,1М NaOAc рН 5,0.
Полоса D: Неочищенный продукт после конъюгации G-CSF с HES50/0,7 в буфере 0,1М NaOAc рН 5,0.
Полоса E: Исходный материал G-CSF.
Фиг.4
На фиг.4 показан анализ конъюгатов HES-G-CSF SDS-PAGE, полученных в соответствии с примером 2.3, G-CSF представляет собой Neupogen® или Granocyte®. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт (i-N) в соответствии с примером 2.3.
Полоса С: Неочищенный продукт (ii-N) в соответствии с примером 2.3.
Полоса D: Неочищенный продукт (iii-N) в соответствии с примером 2.3.
Полоса E: Неочищенный продукт (iv-N) в соответствии с примером 2.3.
Полоса F: Неочищенный продукт (i-G) в соответствии с примером 2.3.
Полоса G: Неочищенный продукт (ii-G) в соответствии с примером 2.3.
Полоса H: Неочищенный продукт (iii-G) в соответствии с примером 2.3.
Полоса I: Неочищенный продукт (iv-G) в соответствии с примером 2.3.
Полоса J: Neupogen®.
Фиг.5
На фиг.5 показан анализ конъюгатов HES-G-CSF SDS-PAGE, полученных в соответствии с примером 2.4, G-CSF от Strathmann Biotec AG, Hamburg, D. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Молекулярная масса маркера сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт (vi) в соответствии с примером 2.4.
Полоса С: Неочищенный продукт (v) в соответствии с примером 2.4.
Полоса D: Исходный материал G-CSF.
Полоса E: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса F: Неочищенный продукт (ix) в соответствии с примером 2.4.
Полоса G: Неочищенный продукт (viii) в соответствии с примером 2.4.
Полоса H: Неочищенный продукт (vii) в соответствии с примером 2.4.
Полоса I: Исходный материал G-CSF.
Фиг.6
На фиг.6 показан анализ конъюгатов HES-G-CSF SDS-PAGE, полученных в соответствии с примером 2.5, G-CSF от Strathmann Biotec AG, Hamburg, D. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 10% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт в соответствии с примером 2.5.
Полоса С: Исходный материал G-CSF.
Фиг.7
На фиг.7 показан анализ SDS-PAGE конъюгатов HES-G-CSF, полученных в соответствии с примером 3, G-CSF представляет собой Neupogen® или Granocyte®. Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер SeeBlue®Plus2 (Invitrogen GmbH, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 188, 98, 62, 49, 38, 28, 17, 14, 6, 3 кДа.
Полоса В: Неочищенный продукт (x) в соответствии с примером 3.
Полоса С: Неочищенный продукт (xi) в соответствии с примером 3.
Полоса D: Неочищенный продукт (xii) в соответствии с примером 3.
Полоса E: Неочищенный продукт (xiii) в соответствии с примером 3.
Полоса F: Неочищенный продукт (xiv) в соответствии с примером 3.
Полоса G: Неочищенный продукт (xv) в соответствии с примером 3.
Фиг.8
На фиг.8 показаны результаты in vitro примера 6.
На графике ось х показывает концентрацию в пкг/мл, ось у относится к количеству клеток/100000. На графике следующие аббревиатуры относятся к
Фиг.9
На фиг.9 показана хроматограмма ГПХВД (гель-проникающей хроматографии под высоким давлением) в отношении неочищенного продукта реакции конъюгации в соответствии с примером 4.1. Следующие параметры использовались при анализе ГПХВД:
А представляет результат, полученный детектором 1, В представляет результат, полученный детектором 2.
Фиг.10
На фиг.10 показана хроматограмма ГПХВД в отношении неочищенного продукта реакции конъюгации в соответствии с примером 4.1, где содержание смеси, относящейся к побочным продуктам реакции, таким как не вступивший во взаимодействие оксо-HES и свободный N-гидроксисукцинимид, а также растворитель, понижалось с использованием ультрафильтрационной мембраны 10 кДа в охлаждающей центрифуге.
Следующие параметры использовались при анализе ГПХВД:
А представляет результат, полученный детектором 1, В представляет результат, полученный детектором 2.
Фиг.11
Следующие параметры использовались при анализе ГПХВД:
А представляет результат, полученный детектором 1, В представляет результат, полученный детектором 2.
Фиг.12
Следующие параметры использовались при анализе ГПХВД:
А представляет результат, полученный детектором 1, В представляет результат, полученный детектором 2.
Фиг.13
На фиг.13 показан анализ SDS-PAGE проточной жидкости и элюата модифицированного HES G-CSF (A32) после хроматографии на DEAE (диэтиламиноэтил)-сефарозе CL-6D. 1,5% указанных фракций обессоливали ультрафильтрацией, сушили в SpeedVac и наносили на 12,5% полиакриламидный гель.
Фиг.14
На фиг.14 показан спектр MALDI/TOF исходного материала G-CSF (образец А33).
Фиг.15
На фиг.15 показан спектр MALDI/TOF G-CSF, модифицированного HES (образец А32).
Фиг.16
На фиг.16 показан спектр MALDI/TOF G-CSF, модифицированного HES (образец А60).
Фиг.17
На фиг.17 показан гель-электрофорез реакционных смесей примера 7.2(b). Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя. Гель окрашивали красителем Roti-Blue (Carl Roth GmbH + Co.KG, Karlsruhe, D) в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер Roti-Mark STANDARD (Carl Roth GmbH + Co.KG, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 200, 119, 66, 43, 29, 20, 14,3 кДа.
Полоса В: Неочищенный продукт после конъюгации hG-CSF с производным HES, полученным в примере 7.1(d).
Полоса C: Неочищенный продукт после конъюгации hG-CSF с производным HES, полученным в примере 7.1(b).
Полоса D: Неочищенный продукт после конъюгации hG-CSF с производным HES, полученным в примере 7.1(j).
Полоса Е: Контроль реакции: HES 50/07.
Фиг.18
На фиг.18 показан гель-электрофорез реакционных смесей примера 7.2(d). Для гель-электрофореза использовали XCell Sure Lock Mini Cell (Invitrogen GmbH, Karlsruhe, D) и Consort E143 питание (CONSORTnv, Turnhout, B). 12% гель Bis-Tris вместе с фракционирующим буфером MOPS SDS при восстанавливающих условиях (оба Invitrogen GmbH, Karlsruhe, D) использовали в соответствии с инструкцией изготовителя. Гель окрашивали красителем Roti-Blue (Carl Roth GmbH + Co.KG, Karlsruhe, D) в соответствии с инструкцией изготовителя.
Полоса А: Белковый маркер Roti-Mark STANDARD (Carl Roth GmbH + Co.KG, Karlsruhe, D). Маркер молекулярной массы сверху вниз: 200, 119, 66, 43, 29, 20, 14,3 кДа.
Полоса В: hG-CSF после обмена буфера, как описано в примере 7.2(с).
Полоса С: Неочищенный продукт после конъюгации hG-CSF с производным HES, полученным в примере 7.1(f).
Полоса D: Неочищенный продукт после конъюгации hG-CSF с производным HES, полученным в примере 7.1(h).
Фиг.19
На фиг.19 показана хроматограмма ГПХВД в отношении продукта реакции конъюгации в соответствии с примером 7.3 (детектор MALLS: верхняя диаграмма; УФ детектор: нижняя диаграмма). Следующие параметры использовались при анализе ГПХВД:
Фиг.20
На фиг.20 показаны результаты анализа митогенности в примере 7.4. Ось Y показывает количество NFS-60-клеток/мл, а ось Х - концентрацию в пкг/мл.
Фиг.21
На фиг.21 показаны результаты анализа in vivo в примере 7.5.
ПРИМЕРЫ
Пример 1: Синтез гидроксиэтилкрахмала, функционализированного альдегидом
Пример 1.1(а): Синтез окислением периодатом гидроксиэтилкрахмала, селективно окисленного на его восстанавливающем конце, и инкубацией при 0°С
100 мг Оксо-HES10/0.4 (молекулярная масса=10 кДа, DS=0,4, полученный Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1) растворяют в 5 мл 20 мМ буфера фосфата натрия, рН 7,2 и охлаждают до 0°С. 21,4 мг периодата натрия (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 5 мл того же буфера и охлаждают до 0°С. Оба раствора смешивают и после инкубации в течение 10 мин при 0°С добавляют 0,73 мл глицерина и реакционную смесь инкубируют при 21°С в течение 10 мин. Реакционную смесь диализируют в течение 24 ч против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.1(b): Синтез окислением периодатом гидроксиэтилкрахмала, селективно окисленного на его восстанавливающем конце, и инкубацией при 21°С
100 мг Оксо-HES10/0/4 (молекулярная масса=10 кДа, DS=0,4, полученный Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1) растворяют в 5 мл 20 мМ буфера фосфата натрия, рН 7,2 С. 21,4 мг периодата натрия (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 5 мл того же буфера. Оба раствора смешивают и после инкубации в течение 10 мин при 21°С добавляют 0,73 мл глицерина и реакционную смесь инкубируют при 21°С в течение 10 мин. Реакционную смесь диализируют в течение 24 ч против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.2(а): Синтез функционализированного альдегидом гидроксиэтилкрахмала окислением периодатом гидроксиэтилкрахмала с неокисленным восстанавливающим концом и инкубацией при 0°С
100 мг HES10/0.4 (молекулярная масса=10 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D) растворяют в 5 мл 20 мМ буфера фосфата натрия, рН 7,2 и охлаждают до 0°С. 21,4 мг периодата натрия (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 5 мл того же буфера и охлаждают до 0°С. Оба раствора смешивают и после инкубации в течение 10 мин при 0°С добавляют 0,73 мл глицерина и реакционную смесь инкубируют при 21°С в течение 10 мин. Реакционную смесь диализируют в течение 24 ч против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.2(b): Синтез функционализированного альдегидом гидроксиэтилкрахмала окислением периодатом гидроксиэтилкрахмала с неокисленным восстанавливающим концом и инкубацией при 21°С
100 мг HES10/0.4 (молекулярная масса=10 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D) растворяют в 5 мл 20 мМ буфера фосфата натрия, рН 7,2. 21,4 мг периодата натрия (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 5 мл того же буфера. Оба раствора смешивают и после инкубации в течение 10 мин при 21°С добавляют 0,73 мл глицерина и реакционную смесь инкубируют при 21°С в течение 10 мин. Реакционную смесь диализируют в течение 24 ч против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.3: Синтез функционализированного альдегидом гидроксиэтилкрахмала из амино функционализированного гидроксиэтилкрахмала и формилбензойной кислоты
Оксо-HES10/0.4 (молекулярная масса=10 кДа, DS=0,4) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
5,1 г (0,51 ммоль) оксо-HES10/0.4 растворяют в 15 мл безводного диметилсульфоксида (DMSO, Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют по каплям в атмосфере азота к раствору 5,1 мл (51 ммоль) 1,4-диаминобутана в 10 мл безводного диметилсульфоксида и перемешивают при 40°С в течение 19 ч. Реакционную смесь добавляют к смеси 80 мл этанола и 80 мл ацетона. Полученный осадок отделяют центрифугированием, промывают смесью 20 мл этанола и 20 мл ацетона и повторно растворяют в 80 мл воды. Раствор диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и в последующем лиофилизируют. Выход 67% (3,4 г) амино-HES10/0,4.
150 мг 4-формилбензойной кислоты и 230 мг 1-гидрокси-1Н-бензотриазола (оба Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 10 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 204 мкл N,N'-диизопропилкарбодиимида. После инкубации при 21°С в течение 30 мин добавляют 1 г амино-HES10/0,4. После встряхивания в течение 19 ч при 22°С реакционную смесь добавляют к 84 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в 50 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.4: Синтез функционализированного альдегидом гидроксиэтилкрахмала из гидроксиэтилкрахмала и формилбензойной кислоты
Оксо-HES10/0.7 (молекулярная масса=10 кДа, DS=0,7) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
83 мг 4-формилбензойной кислоты и 180 мг 1-гидрокси-1Н-бензотриазола (оба Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 5 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valkenswaard, NL) и добавляют 78 мкл N,N'-диизопропилкарбодиимида. После инкубации при 21°С в течение 30 мин добавляют 0,5 г оксо-HES10/0.7. После встряхивания в течение 19 ч при 22°С реакционную смесь добавляют к 37,5 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в смеси 2,5 мл воды и 2,5 мл DMF и снова осаждают, как описано выше. Продукт реакции собирают центрифугированием, как описано, повторно растворяют в 10 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.5: Синтез функционализированного альдегидом гидроксиэтилкрахмала из гидроксиэтилкрахмала и формилбензойной кислоты
HES10/0.7 (молекулярная масса=10 кДа, DS=0,7) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D.
50 мг 4-формилбензойной кислоты и 108 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 3 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valkenswaard, NL) и добавляют 47 мкл N,N'-диизопропилкарбодиимида. После инкубации при 21°С в течение 30 мин добавляют 0,3 г HES10/0.7. После встряхивания в течение 19 ч при 22°С реакционную смесь добавляют к 23 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в смеси 1,5 мл воды и 1,5 мл DMF и снова осаждают, как описано выше. Продукт реакции собирают центрифугированием, как описано, повторно растворяют в 10 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.6: Синтез функционализированного альдегидом гидроксиэтилкрахмала из амино функционализированного гидроксиэтилкрахмала и сложного пентафторфенилового эфира формилбензойной кислоты
Оксо-HES10/0,7 (молекулярная масса=10 кДа, DS=0,7) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
6,0 г (0,6 ммоль) оксо-HES10/0,7 растворяют в 20 мл безводного диметилсульфоксида (DMSO, Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют по каплям в атмосфере азота к раствору 6 мл (60 ммоль) 1,4-диаминобутана в 11 мл безводного диметилсульфоксида и перемешивают при 40°С в течение 19 ч. Реакционную смесь добавляют к смеси 80 мл этанола и 80 мл ацетона. Полученный осадок отделяют центрифугированием, промывают смесью 20 мл этанола и 20 мл ацетона и повторно растворяют в 80 мл воды. Раствор диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и в последующем лиофилизируют. Выход 52% (3,15 г) амино-HES10/0,7.
Сложный пентафторфениловый эфир 4-формилбензойной кислоты синтезировали, как описано в публикации J.S.Lindsey et al., Tetrahedron 50 (1994) pp.8941-68, в частности, p.8956. 50 мг амино-HES10/0,7 растворяют в 0,5 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valkenswaard, NL) и добавляют 15,3 мг сложного пентафторфенилового эфира 4-формилбензойной кислоты. После встряхивания в течение 22 ч при 22°С реакционную смесь добавляют к 3,5 мл ледяного 2-пропанола. Осажденный продукт собирают центрифугированием при 4°С, промывают 4 мл ледяного 2-пропанола, повторно растворяют в 50 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.7: Синтез функционализированного альдегидом гидроксиэтилкрахмала из гидроксиэтилкрахмала и сложного пентафторфенилового эфира формилбензойной кислоты
Оксо-HES10/0,7 (молекулярная масса=10 кДа, DS=0,7) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
Сложный пентафторфениловый эфир 4-формилбензойной кислоты синтезировали, как описано в публикации J.S.Lindsey et al., Tetrahedron 50 (1994) pp.8941-68, в частности, p.8956. 200 мг оксо-HES10/0,7 растворяют в 2 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valkenswaard, NL) и добавляют 61,2 мг сложного пентафторфенилового эфира 4-формилбензойной кислоты. После встряхивания в течение 22 ч при 22°С реакционную смесь добавляют к 15 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в смеси 1,4 мл воды и 0,7 мл DMF и снова осаждают, как описано выше. Продукт реакции собирают центрифугированием, как описано, повторно растворяют в 10 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 1.8: Синтез функционализированного альдегидом гидроксиэтилкрахмала из амино функционализированного гидроксиэтилкрахмала и 4-(4-формил-3,5-диметоксифенокси)масляной кислоты
Оксо-HES10/0,4 (молекулярная масса=10 кДа, DS=0,4) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
5,1 г (0,51 ммоль) оксо-HES10/0,4 растворяют в 15 мл безводного диметилсульфоксида (DMSO, Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют по каплям в атмосфере азота к раствору 5,1 мл (51 ммоль) 1,4-диаминобутана в 10 мл безводного диметилсульфоксида и перемешивают при 40°С в течение 19 ч. Реакционную смесь добавляют к смеси 80 мл этанола и 80 мл ацетона. Полученный осадок отделяют центрифугированием, промывают смесью 20 мл этанола и 20 мл ацетона и повторно растворяют в 80 мл воды. Раствор диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и в последующем лиофилизируют. Выход 67% (3,4 г) амино-HES10/0,4.
80,5 мг 4-(4-формил-3,5-диметоксифенокси)масляной кислоты (Calbiochem-Novabiochem, Läufelfingen, CH) и 61 мг 1-гидрокси-1Н-бензотриазола (Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 3 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valkenswaard, NL) и добавляют 45,4 мкл N,N'-диизопропилкарбодиимида. После инкубации при 21°С в течение 30 мин добавляют 0,3 г амино-HES10/0.4. После встряхивания в течение 22 ч при 22°С реакционную смесь добавляют к 23 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в смеси 2 мл воды и 1 мл DMF и снова осаждают, как описано выше. Продукт реакции собирают центрифугированием, как описано, повторно растворяют в 10 мл воды, диализируют в течение 1 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют.
Пример 2: Синтез конъюгатов G-CSF восстановительным аминированием
Пример 2.1(а): Синтез конъюгатов G-CSF восстановительным аминированием с гидроксиэтилкрахмалом с неокисленным восстанавливающим концом при рН 7,4 (сравнительный пример)
В примере 2.1 сделана попытка использования способа синтеза WO 03/074087 (пример 12, стр.22-23) для получения конъюгата HES-G-CSF.
К 3,33 мкл водного раствора G-CSF (Neupogen® от Amgen, München, D, или Granocyte® от Aventis Pharma AG, Zürich, CH соответственно 3 мг/мл) в 0,1 М буфере фосфата натрия с рН 7,4, добавляют 3,33 мкл раствора HES10/0,4 (молекулярная масса=10 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, 79 мг/мл) в том же буфере. К этой смеси добавляют 3,33 мкл 60 мМ раствора цианоборгидрида натрия в том же буфере, и полученную смесь инкубируют в течение 4 ч при 22°С. В последующем добавляют еще 3,33 мкл 60 мМ свежеприготовленного раствора цианоборгидрида натрия. В течение времени инкубации 30 ч добавляют всего 5 порций 3,33 мкл 60 мМ свежеприготовленного раствора цианоборгидрида натрия. Реакционную смесь анализируют гель-электрофорезом. Реакция не наблюдается.
Пример 2.1(b): Синтез конъюгатов G-CSF восстановительным аминированием с гидроксиэтилкрахмалом с неокисленным восстанавливающим концом при рН от 5,0 до 9,2
(Сравнительный пример)
К 3,33 мкл водного раствора G-CSF (G-CSF от Strathmann Biotec AG, Hamburg, D, 3 мг/мл) в данном буфере добавляют 3,33 мкл раствора HES (300 мг/мл) в том же буфере. Смесь охлаждают до 4°С и добавляют 3,33 мкл 60 мМ раствора цианоборгидрида натрия в том же буфере при 4°С, и полученную смесь инкубируют в течение 20 ч при 4°С.
Используют следующие препараты HES и буфер:
а) Буфер: буфер 0,1 М ацетата натрия рН 5,0
- HES10/0,4 (молекулярная масса=10 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
- HES50/0,4 (молекулярная масса=50 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
- HES50/0,7 (молекулярная масса=50 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
b) Буфер: буфер 0,1 М фосфата натрия рН 7,2
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
с) Буфер: буфер 0,1 М бората натрия рН 8,3
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
d) Буфер: буфер 0,2 М бората калия рН 9,2
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
Каждую реакционную смесь анализируют гель-электрофорезом. Конъюгация не наблюдается или ей можно пренебречь (сканы геля для реакций b)-d) не показаны).
Пример 2.2: Синтез конъюгатов G-CSF восстановительным аминированием с гидроксиэтилкрахмалом с окисленным восстанавливающим концом при рН от 5,0 до 9,2
(Сравнительный пример)
К 3,33 мкл водного раствора G-CSF (G-CSF от Strathmann Biotec AG, Hamburg, D, 3 мг/мл) в данном буфере добавляют 3,33 мкл раствора оксо-HES (300 мг/мл) в том же буфере. Смесь охлаждают до 4°С и добавляют 3,33 мкл 60 мМ раствора цианоборгидрида натрия в том же буфере при 4°С, и полученную смесь инкубируют в течение 17 ч при 4°С.
Используют следующие препараты HES и буфер:
а) Буфер: буфер 0,1 М ацетата натрия рН 5,0
- оксо-HES10/0,4 (молекулярная масса 10 кДа, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
- оксо-HES50/0,7 (молекулярная масса=50 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
- оксо-HES50/0,7 (молекулярная масса=50 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
b) Буфер: буфер 0,1 М фосфата натрия рН 7,2
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
с) Буфер: буфер 0,1 М бората натрия рН 8,3
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
d) Буфер: буфер 0,2 М бората калия рН 9,2
- HES10/0,7 (молекулярная масса=10 кДа, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D)
Каждую реакционную смесь анализируют гель-электрофорезом. Конъюгация не наблюдается или ей можно пренебречь (сканы геля для реакций b)-d) не показаны).
Окисление HES10/0,4 (молекулярная масса=10 кДа, DS=0,4) проводят Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, в соответствии с DE 196 28 705 А1.
Пример 2.3: Синтез конъюгатов G-CSF восстановительным аминированием с функционализированным альдегидом гидроксиэтилкрахмалом, синтезированным окислением периодатом
К 3,33 мкл водного раствора G-CSF (Granocyte® от Aventis Pharma AG, Zürich, CH и Neupogen® от Amgen, München, D, соответственно 3 мг/мл) в 0,1 М буфере ацетата натрия с рН 5,0, добавляют 3,33 мкл раствора альдегидо-HES (79 мг/мл) в том же буфере. К смеси добавляют 3,33 мкл 60 мМ раствора цианоборгидрида натрия в том же буфере, и смесь инкубируют в течение 25 ч при 21°С. Реакционную смесь анализируют гель-электрофорезом.
Используют следующие функционализированные альдегидом конъюгаты HES:
(i-N) полученный с Neupogen® в соответствии с примером 1.1(а), представленным выше;
(ii-N) полученный с Neupogen® в соответствии с примером 1.1(b), представленным выше;
(iii-N) полученный с Neupogen® в соответствии с примером 1.2(а), представленным выше;
(iv-N) полученный с Neupogen® в соответствии с примером 1.2(b), представленным выше;
(i-G) полученный с Granocyte® в соответствии с примером 1.1(а), представленным выше;
(ii-G) полученный с Granocyte® в соответствии с примером 1.1(b), представленным выше;
(iii-G) полученный с Granocyte® в соответствии с примером 1.2(а), представленным выше;
(iv-G) полученный с Granocyte® в соответствии с примером 1.2(b), представленным выше.
Пример 2.4: Синтез конъюгатов G-CSF восстановительным аминированием с функционализированным альдегидом гидроксиэтилкрахмалом, синтезированным конъюгацией гидроксиэтилкрахмала с формилкарбоновой кислотой
К 3,33 мкл водного раствора G-CSF (G-CSF от Strathmann Biotec AG, Hamburg, D, 3 мг/мл) в 0,1 М буфере ацетата натрия с рН 5,0, добавляют 3,33 мкл раствора альдегидо-HES (118,5 мг/мл) в том же буфере и охлаждают до 4°С. К смеси добавляют 3,33 мкл 60 мМ раствора цианоборгидрида натрия в том же буфере при 4°С, и смесь инкубируют в течение 17 ч при 4°С. Реакционную смесь анализируют гель-электрофорезом.
Используют следующие функционализированные альдегидом конъюгаты HES:
(v) полученный в соответствии с примером 1.4, представленным выше;
(vi) полученный в соответствии с примером 1.5, представленным выше;
(vii) полученный в соответствии с примером 1.6, представленным выше;
(viii) полученный в соответствии с примером 1.7, представленным выше;
(ix) полученный в соответствии с примером 1.8, представленным выше.
Пример 2.5: Синтез конъюгатов G-CSF восстановительным аминированием с функционализированным альдегидом гидроксиэтилкрахмалом, синтезированным конъюгацией гидроксиэтилкрахмала с формилкарбоновой кислотой
К 2,5 мл водного раствора G-CSF (G-CSF от Strathmann Biotec AG, Hamburg, D, 2,27 мг/мл) в 0,1 М буфере ацетата натрия с рН 5,0, добавляют 136 мг альдегидо-HES, полученного, как описано выше в примере 1.3, и раствор охлаждают до 0°С. К смеси добавляют 2,5 мл ледяного 40 мМ раствора цианоборгидрида натрия в том же буфере, и смесь инкубируют в течение 17 ч при 4°С. Реакционную смесь анализируют гель-электрофорезом.
Пример 3: Синтез конъюгатов G-CSF алкилированием SH
Оксо-HES10/0,7 (молекулярная масса=10 кДа, DS=0,7) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1.
6,0 г (0,6 ммоль) оксо-HES10/0,7 растворяют в 20 мл безводного диметилсульфоксида (DMSO, Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют по каплям в атмосфере азота к раствору 6 мл (60 ммоль) 1,4-диаминобутана в 11 мл безводного диметилсульфоксида и перемешивают при 40°С в течение 19 ч. Реакционную смесь добавляют к смеси 80 мл этанола и 80 мл ацетона. Полученный осадок отделяют центрифугированием, промывают смесью 20 мл этанола и 20 мл ацетона и повторно растворяют в 80 мл воды. Раствор диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и в последующем лиофилизируют. Выход 52% (3,15 г) амино-HES10/0,7.
К 132 мкг амино-HES10/0,7, растворенного в 100 мкл буфера фосфата натрия (0,1 М, 0,15 М NaCl, 50 мМ ЭДТА, рН 7,2), добавляют 10 мкл раствора 17,5 мг/мл сложного N-альфа(малеимидоацетокси)сукцинимидного эфира (AMAS) в сухом DMSO (оба Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D), и прозрачный раствор инкубируют в течение 80 мин при 25°С и в последующем в течение 20 мин при 40°С. Избыток AMAS удаляют центрифужной фильтрацией концентратором 0,5 мл VIVASPIN, 5 кДа MWCO (VIVASCIENCE, Hannover, D) при 13000 об/мин, промывают 2 раза в течение 30 мин 450 мкл фосфатного буфера и 1 раз 450 мкл буфера В. К остаточному раствору добавляют 10 мкг G-CSF (Neupogen® от Amgen, München, D, или Granocyte® от Aventis Pharma AG, Zürich, CH соответственно 3 мкг/мкл в 0,1 М фосфатном буфере), и смесь инкубируют в течение 16 ч при 25°С. Реакционную смесь анализируют гель-электрофорезом после концентрации в вакууме.
Выбирают следующие способы:
(x) G-CSF (Granocyte®), используя буфер фосфата натрия (0,1 М, 0,15 М NaCl, 50 мМ ЭДТА, рН 7,2) в качестве буфера В.
(xi) G-CSF (Neupogen®), используя буфер фосфата натрия (0,1 М, 0,15 М NaCl, 50 мМ ЭДТА, рН 7,2) в качестве буфера В.
(xii) G-CSF (Granocyte®), используя смесь 1:1 (об./об.) буфера фосфата натрия (0,1 М, 0,15 М NaCl, 50 мМ ЭДТА, рН 7,2) и 8 М мочевины, 1% SDS, рН 7,4 в качестве буфера В.
(xiii) G-CSF (Neupogen®), используя смесь 1:1 (об./об.) буфера фосфата натрия (0,1 М, 0,15 М NaCl, 50 мМ ЭДТА, рН 7,2) и 8 М мочевины, 1% SDS, рН 7,4 в качестве буфера В.
(xiv) G-CSF (Granocyte®), используя 8 М мочевинe, 1% SDS, рН 7,4 в качестве буфера В.
(xv) G-CSF (Neupogen®), используя 8 М мочевинe, 1% SDS, рН 7,4 в качестве буфера В.
Пример 4: Синтез конъюгатов G-CSF взаимодействием гидроксиэтилкрахмала, имеющего реакционноспособную сложноэфирную группу, с G-CSF
Пример 4.1:
Оксо-HES10/0,4 (молекулярная масса=10559 Д, DS=0,4) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1. Степень окисления оксо-HES составляет 95%.
66 мг оксо-HES10/0,4 растворяют в 0,5 мл безводного DMF. К этому раствору добавляют 3,4 мг карбоната N,N'-дисукцинимидила, и смесь перемешивают в течение 2 ч при комнатной температуре. Полученный раствор имеет концентрацию реакционноспособного HES 13% мас.
Раствор G-CSF (Strathmann Biotec AG, Hamburg, D), имеющий концентрацию примерно 0,5 мг G-CSF/мл, концентрируют до концентрации 10 мг/мл ультрацентрифугированием при отсечке 10 кДа, используя охлаждающую центрифугу.
К 0,5 мл этого концентрированного раствора G-CSF добавляют 180 мкл раствора бикарбоната натрия. В последующем к раствору белка добавляют по каплям 3 порции (100 мкл каждая) раствора реакционноспособного HES до тех пор, пока примерно через 30 мин не завершится взаимодействие. Таким образом, общее молярное соотношение реакционноспособного HES:G-CSF составляет 20:1. Затем рН смеси доводят до 4,0, используя 0,1 N HCl.
Анализ ГПХВД (гель-проникающей хроматографией под высоким давлением) дает выход примерно 70%. Этот результат показан на фиг.9.
Смесь можно хранить при 4°С при рН 4,0 в течение 4 сут, и, в соответствии с анализами ГПХВД, она остается стабильной, т.е. неизменной.
Понижение содержания смеси в отношении побочных продуктов взаимодействия, таких как не вступивший в реакцию оксо-HES и свободный N-гидроксисукцинимид, а также растворитель, при использовании мембраны ультрафильтрации 10 кДа в охлаждающей центрифуге было возможно без трудностей. Результаты этого понижающего эксперимента показаны на фиг.10.
Пример 4.2:
Оксо-HES10/0,4 (молекулярная масса=10559 Д, DS=0,4) был получен Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1. Степень окисления оксо-HES составляет 95%.
400 мг оксо-HES10/0,4 растворяют в 1 мл безводного DMF. К этому раствору добавляют 21 мг карбоната N,N'-дисукцинимидила, и смесь перемешивают в течение 2 ч при комнатной температуре. Полученный раствор имеет концентрацию реакционноспособного HES 40% мас.
Раствор G-CSF (Strathmann Biotec AG, Hamburg, D), имеющий концентрацию примерно 0,5 мг G-CSF/мл, концентрируют до концентрации 10 мг/мл ультрацентрифугированием при отсечке 10 кДа, используя охлаждающую центрифугу.
К 0,5 мл этого концентрированного раствора G-CSF добавляют 180 мкл раствора бикарбоната натрия. В последующем к раствору белка добавляют по каплям 3 порции (100 мкл каждая) раствора реакционноспособного HES до тех пор, пока примерно через 30 мин не завершится взаимодействие. Таким образом, общее молярное соотношение реакционноспособного HES:G-CSF составляет 50:1. Затем рН смеси доводят до 4,0, используя 0,1 N HCl.
Анализ ГПХВД (гель-проникающей хроматографией под высоким давлением) дает выход более чем 95%. Выявляется не вступивший во взаимодействие G-CSF. Этот результат показан на фиг.11.
Смесь очищают с использованием технологии ультрафильтрации без трудностей. Результаты этого понижения показаны на фиг.12.
Пример 5
5.1. Очистка
Получают очищенный G-CSF, имеющий по существу такие же характеристики как имеющийся в продаже продукт Neupogen® (Amgen), и одно аликвотное количество держат без изменений в качестве контроля.
5.2 Синтез конъюгатов HES и G-CSF
Конъюгаты синтезируют по существу, как описано в примере 4.2, но с Оксо-HES50/0.7 (код образца А60) или как описано в примере 2.5 (код образца А32) и используют для дальнейшего обмена буфера и очистки.
5.3 Обмен буфера образцов G-CSF и G-CSF, модифицированного HES, перед очисткой анионообменной хроматографией
Образцы G-CSF, модифицированного HES, или немодифицированного G-CSF (в качестве контроля) (0,5-5 мг белка) подвергают обмену буфера с использованием блоков концентратора Vivaspin 6 (10000 MWCO PES, Vivascience, каталожный № VS0602). Образцы концентрируют до 0,5-0,7 мл и разбавляют до 5 мл 10 мМ буфера фосфата Na рН 7,2. Каждый образец подвергают 3 раза этому циклу концентрации/буферного обмена.
5.4 Анионообменная хроматография G-CSF и его модифицированных HES форм на колонке DEAE-Sepharose
Образцы G-CSF после модификации HES и, для сравнения, образцы модифицированного G-CSF очищают и анализируют анионообменной хроматографией при комнатной температуре использованием устройства исследования 10 ÄKTA, как описано. Аликвотные количества G-CSF, или до или после HESилирования диализируют ультрафильтрацией против указанного буфера А (10 мМ Na-фосфата, рН 7,2) или разводят примерно 13 объемами буфера А. Колонку, содержащую 2 мл DEAE-Sepharose (CL-6B, Pharmacia Kat. Nr. 17-0710-01) регенерируют нанесением 5,0 колоночных объемов (CV) 6,5 М гуанидина/HCl, 5,0 CV буфера А, 5,0 CV буфера С (1,5 M NaCl в 10 мМ Na-фосфате, рН 7,2) и затем 10 CV буфера А. Затем образцы (0,8-4,5 мл в 10 мМ буфера Na-фосфата рН 7,2) инъецируют использованием скорости потока 0,6 мл/мин. После промывания петли образца 10 мл (петля образца 2 мл) или 20 мл (петля образца 5 мл) буфера А, в зависимости от нанесенного образца, колонку затем промывают 0-22 CV буфера А (скорость потока = 0,8 мл/мин). Элюирование выполняют нанесением линейного градиента от 0 до 100% буфера В по 5 CV и изократического цикла 2,5 CV 100% буфера В с использованием скорости потока 0,6 мл/мин. Колонку повторно уравновешивают 5 CV буфера А и регенерируют, как подробно описано выше, использованием скорости потока 1 мл/мин.
Если требуется, образцы концентрируют с использованием концентратора Vivaspin, и выполняют обмен буфера, как описано выше. Образцы хранят при 0-8°С в 10 мМ буфере ацетата Na рН 4,0 перед и после стерильной фильтрации с использованием 0,2 мкм фильтрационного блока, Corning, Cat. No. 431215). Для биологических анализов in vivo и для дальнейшего аналитического анализа готовят следующие образцы. Концентрацию белка определяют, как описано ниже в разделе 6.1:
I. 0401-15/А33, 0,44 мг/мл, объем=500 мкл
G-CSF (E.coli)
II. 0402-03/A60, 0,35 мг/мл, объем=600 мкл
H-G-CSF (G-CSF HES модифицированный, 10/0,4)
III. 0401-13/A32, 0,28 мг/мл, объем=900 мкл
G-CSF (E.coli)HES модифицированный, 10/0,4
IV. 0401-28/A58, 0,60 мг/мл, объем=350 мкл
Neupogen
V. 0401-28/A57, 0,50 мг/мл, объем=400 мкл
Neulasta
5.5. Дополнительный анализ образцов G-CSF
Аликвотные количества образцов анализируют на содержание белка и на наличие модификаций.
5.5(а) Количественный анализ белка в G-CSF RP-HPLC (ВЭЖХ в обращенной фазе)
Содержание белка в G-CSF образцов количественно анализируют с использованием немодифицированного белкового препарата (концентрация: 0,453 мг/мл) в качестве стандарта.
Используют устройство ВЭЖХ Dionex, состоящее из насоса P 680 A HPG, дегазирующего блока Degasys DG 1210, автосемплера и инжектора ASI-100, петли образца 250 мкл, термостатированного колоночного отдела ТСС 100 наряду с детектором УФ/видимого спектра UVD170U, оборудованного программным устройством управления хроматографией Chromeleon. Используют предварительную колонку СС 8/4 Nucleosil 120-5 C4, Machery-Nagel, Cat. No. 721889 и разделительную колонку 40 С-4 Nucleosil MPN, колонку 5 мкл, 125×4 мм обращенной фазы (Macherey-Nagel, № заказа 7200 45.20). Растворитель А представляет собой Н2О плюс 0,06% (об./об.) трифторуксусная кислота, а растворитель В представляет собой 90% ацетонитрил в Н2О, содержащий 0,06% (об./об.) трифторуксусную кислоту; скорость потока составляет 1 мл/мин. УФ выявление проводят при длине волн 214, 221, 260 и при 280 нм.
Образцы приблизительно 10-20 мкг инъецируют в колонку RP-ВЭЖХ. Используют следующий градиент:
Используют полученную площадь пика в положении элюирования стандартного препарата G-CSF и сравнивают с эталонным стандартом сравнением пика, появляющегося примерно через 29 мин при длине волн 280 нм.
5.5(b) Восстановление+карбоксамидометилирование белка G-CSF
Аликвотные количества образцов белка G-CSF восстанавливают и карбоксамидометилируют, как описано в другом документе (Guillermina Fomo, Mariela Bollati Fogolin, Marcos Oggero, Ricardo Kratje, Marina Etcheverrigaray, Harald S. Conradt, Manfred Nimtz (2004) N- and О-linked carbohydrates and glycosylation site occupancy in recombinant human granulocyte-macrophage colony-stimulating factor secreted by a Chinese hamster ovary cell line; European J. Biochem, 273(5), 907-919). Карбоксамидометилирование ведет к получению модифицированных цистеиновых остатков. Переваривание карбоксамидометилированного белка эндопротеиназой Glu-C выполняют в 25 мМ NH4HCO3, содержащем 1 М мочевину при рН 7,8 и используя соотношение фермент/субстрат 0,2:10, в течение 18-24 ч.
5.5(с) Отделение пептидов эндо-Glu-C ВЭЖХ в обращенной фазе
Пептиды, полученные перевариванием эндо-Glu-C, отделяют на системе ВЭЖХ Dionex, состоящей из насоса P 680 A HPG, дегазирующего блока Degasys DG 1210, автосемплера и инжектора ASI-100, петли образца 250 мкл, термостатированного колоночного отдела ТСС 100 наряду с детектором УФ/видимого спектра UVD170U, оборудованного программным устройством управления хроматографией Chromeleon. Используют предварительную колонку СС 8/4 Nucleosil 120-5 C4, Machery-Nagel, Cat. No. 721889 и разделительную колонку 40 С-4 Nucleosil MPN, колонку 5 мкл, 125×4 мм обращенной фазы (Macherey-Nagel, № заказа 7200 45.40). Растворитель А представляет собой Н2О плюс 0,06% (об./об.) трифторуксусная кислота, а растворитель В представляет собой 90% ацетонитрил в Н2О, содержащий 0,06% (об./об.) трифторуксусную кислоту; скорость потока составляет 1 мл/мин. Используют следующий градиент:
УФ выявление проводят при длине волн 214, 221, 260 и при 280 нм. Пептиды, полученные перевариванием эндо-Glu-C, отделяют (данные не показаны).
5.5(d) Анализ протеолитических пептидов поддерживаемой матрицей лазерной десорбцией/ионизационной масс-спектрометрией времени пролета (MALDI/TOF/TOF-MS)
Масс-спектрометрию используют для выявления интактного N-конца G-CSF в различных полученных образцах. Образцы (3-5 мкг), полученные перевариваниями эндопротеиназой Glu-C восстановленных и карбоксамидометилированных белковых образцов, используют непосредственно для масс-спектрометрического анализа (без ВЭЖХ в обращенной фазе стадии 6.3) и очищают, используя наконечники пипеток ZipTip, содержащие материал обращенной фазы С18, в соответствии с инструкциями изготовителя. После промывания 0,1% (об./об.) муравьиной кислотой, элюирование пептидов выполняют 10 мкл 0,1% (об./об.) муравьиной кислотой в 60% (об./об.) ацетонитриле.
Протеолитические (эндо-Glu-C) пептидные фрагменты анализируют прибором для определения времени пролета (TOF/TOF) Bruker ULTRAFLEX в линейном положительном ионном режиме с использованием матрицы из 22,4 мг 3,5-диметокси-4-гидроксициннамовой кислоты в 400 мкл ацетонитрила и 600 мкл 0,1% (об./об.) трифторуксусной кислоты в Н2О; (глико)-пептиды измеряют с использованием матрицы из 19 мг α-циано-4-гидроксициннамовой кислоты в той же смеси растворителей с использованием рефлектрона для усиленного разрешения. Растворы образцов по 1 мкл и приблизительную концентрацию 1-10 пкмоль/мкл смешивают с равными количествами соответствующей матрицы. Смесь наносят в виде пятна на мишень из нержавеющей стали и сушат при комнатной температуре перед анализом. Спектры регистрировали в диапазоне массы 900-5000 дальтон. В таблице коррелируются ожидаемые массы с соответствующими пептидами G-CSF.
Теоретические (моноизотопные) массы пептидов Эндо-Glu-C, полученных из ХМ02
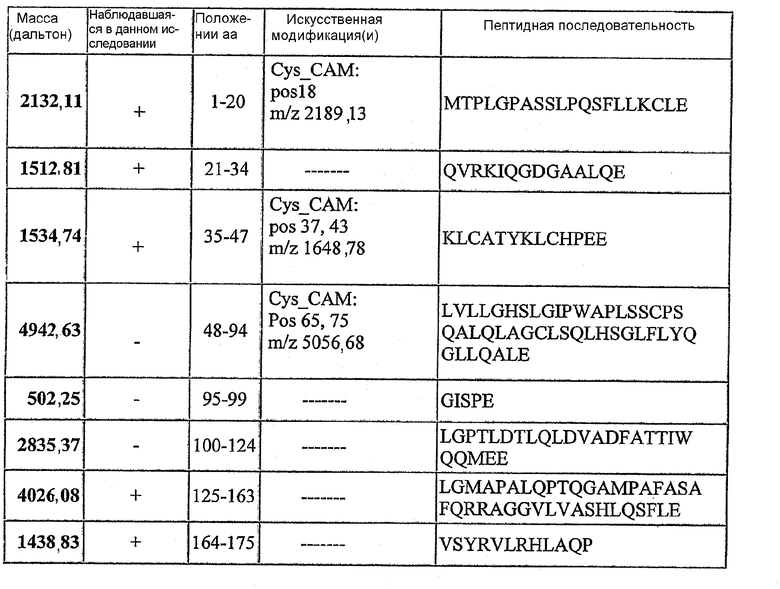
Цистеиновые остатки карбоксамидометилируют; пептиды, маркированные как жир, выявляют в спектре MALDI/TOF не модифицированного G-CSF.
N-концевой пептид Эндо-Glu-C (MTPLGPASSLPQSFLLKCLE; m/z 2189,1), включающий положение 1-20 белка, выявляют в спектрах MALDI/TOF-MS образцов после протеолитической обработки G-CSF эндопротеиназой Glu-C, как описано выше.
5.6. Результаты
5.6(а) Очистка G-CSF и модифицированных вариантов HES
А32, А60 и немодифицированный G-CSF подвергали очистке с использованием колонки DEAE-Sepharose CL-6B, как описано под А4.
В случае немодифицированного образца 0401-15/А33 не было выявлено значимое поглощение при 280 нм в протоке и белке, элюированном при концентрации буфера В 40-50% (0,16-0,20 М NaCl) в объеме 6 мл с площадью специфического пика 660 mAU × мл × мг-1 при 280 нм.
Образец 0401-15/А32 (полученный из 0401-15/А33; HESилирование альдегидоHES 10/0.4) элюировался в большом диапазоне градиента при концентрации буфера В 20-80% (0,08-0,32 М NaCl) в объеме 12 мл. Примерно 90% общей площади пика, выявленной при 280 нм, было обнаружено в протоке, содержащем примерно 50% общего количества белка с очевидно несколько более высокой молекулярной массой при сравнении с элюированным белком, по данным выявления анализом SDS-PAGE, как показано ниже на фиг.13.
Образец 0402-03/А60 (HESилированный HES 10/0.4, после общей процедуры примера 4.2) элюировали в объеме 10,5 мл в такой же концентрации буфера В 20-80%. В этом случае примерно 35% общей площади пика, выявленной при 280 нм, было обнаружено в протоке, однако, анализом SDS-PAGE несвязанный белок не был выявлен в этой фракции. При сравнении с площадью специфического пика образца 0401-15/А33, содержание белка в элюате образца 0402-03/А60 было на 45% выше, чем заявленное количество белка, которое наносилось на колонку.
Извлечение белков рассчитывали на основании площади пика (А280 нм) элюирующих фракций, по сравнению с немодифицированным белком G-CSF.
Сравнение площадей пиков при выявлении при 280 нм
5.6(b) Анализ белков пептидным картированием и MALDI/TOF MS после обработки эндопротеиназой Glu-C
N-концевой пептид, полученный в результате переваривания эндопротеиназой Glu-C и карбоксамидометилированного не модифицированного G-CSF (фиг.14), и имеющегося в продаже продукта Neupogen (данные не показаны) был отчетливо выявлен MALDI/TOF-MS (MTPLGPASSLPQSFLLKC*LE; m/z 2189,1; карбоксамидометилированный цистеином). Этот сигнал отсутствовал в образцах, подвергнутых модификацией HES, восстановительным аминированием (фиг.15) и при Nеulastа (данные не показаны), указывающие на модификацию этого пептида. В случае G-CSF, модифицированного HES, где модификация была проведена химией активированного сложного эфира, N-концевой пептид выявляли при относительной интенсивности сигнала, сравнимой с таковой немодифицированного исходного материала А32 (фиг.16), указывая на то, что модификация HES этих производных была достигнута в различных аминокислотных боковых цепях.
N-концевое секвенирование модифицированного HES G-CSF (образец А33 и имеющийся в продаже продукт Neulasta) выявило блокированный N-конец, свидетельствующий о том, что в действительности N-концевой метиониновый остаток этого белкового производного модифицирован производным HES. Поскольку, сигнал, соответствующий пептиду, включающему аминокислотные остатки положений 35-47 (KLCATYKLCHPEE; оба цистеиновых остатка карбоксамидометилированные m/z 1648,78), не был выявлен в образце А60, сделан вывод, что один или оба лизиновых остатка (в положении 35 и положении 41) могут быть модифицированы HES.
Ссылки:
Guillermina Forno, Mariela Bollati Fogolin, Marcos Oggero, Ricardo Kratje, Marina Etcheverrigaray, Harald S. Conradt, Manfred Nimtz (2004) N- and O-linked carbohydrates and glycosylation site occupancy in recombinant human granulocyte-macrophage colony-stimulating factor secreted by a Chinese hamster ovary cell line Eur. J. Biochem, 271 (5), 907-919
Nimtz, M., Grabenhorst, E., Conradt, H.S., Sanz, L. & Calvete, JJ. (1999) Structural characterization of the oligosaccharide chains of native and crystallized boar seminal plasma spermadhesin PSP-I and PSP-II glycoforms. Eur. J. Biochem. 265,703-718.
Nimtz, M., Martin, W., Wray, V., Kloppel, K.-D., Agustin, J. & Conradt, H.S. (1993) Structures of sialylated oligosaccharides of human erythropoietin expressed in recombinant BHK-21 cells. Eur. J. Biochem. 213, 39-56.
Nimtz, M., Noll G., Paques, E. & Conradt, H.S. (1990) Carbohydrate structures of human tissue plasminogen activator variant expressed in recombinant Chinese hamster ovary cells. FEBS Lett. 271, 14-18.
Schröter, S., Derr, P., Conradt, H.S., Nimtz, M., Hale, G. & Kirchhoff, C. (1999) Male-specific modification of human CD52. J. Biol. Chem. 274, 29862-29873.
E.Grabenhorst and H.S. Conradt (1999) The Cytoplasmic, Transmembrane and the Stem Regions of Glycosyltransferases specify their in vivo functional sublocalization and stability in the Golgi J. Biol. Chem., 274, 36107-36116.
E. Grabenhorst, A. Hoffmann, M. Nimtz, G. Zettlmeiβl and H. S.Conradt (1995) Construction of stable BHK-21 cells coexpressing human secretory glycoproteins and human Galβl-4GlcNAc-R □2,6-sialyltransferase: □2,6-linked NeuAc is preferably attached to the Galβl-4GlcNAcβl-2Manβl-3-branch of biantennary oligosaccharides from secreted recombinant. -trace protein. Eur.J.Biochem., 232, 718-725.
Пример 6: Результаты in vitro конъюгата G-CSF, полученного в примерах 2.5 и 4.2 и очищенного в соответствии с примером 5: митогенность вариантов G-CSF для мышиных клеток NSF-60
G-CSF известен своими специфическими эффектами на пролиферацию, дифференциацию и активацию гематопоэтических клеток нейтрофильной гранулоцитарной линии. Митогенную способность вариантов G-CSF тестировали с использованием мышиных клеток NFS-60 (N. Shirafuji et al., Exp. Hematol. 1989, 17, 16-119). Клетки, выращенные в среде RPMI с 10% фетальной телячьей сывороткой (Gibco INVITROGEN GmbH, Karlsruhe, D), содержащей кондиционированную среду 5-10% WEHI-3B (DSMZ, Braunschweig, D; культивированные, как описано DSMZ) в качестве источника экзогенного IL-3, собирали центрифугированием, промывали и делили на аликвотные количества при 100000 клетках на лунку в 24-луночные планшеты. Клеткам давали возможность адаптироваться в течение 1 ч при 37°С в среде RPMI без сред, кондиционированных WEHI-3B, перед добавлением образцов фактора роста G-CSF, разведенных в тех же средах. Клетки NFS-60 подвергали воздействию очищенных вариантов G-CSF в течение 3 сут при 37°С и затем клетки электронно подсчитывали (счетчик клеток Casy TT, Schärfe System, Reutlingen, D). Результаты сведены на фиг.12. Как видно на фиг.12, различные варианты G-CSF (0,5-50 пкг/мл) могли стимулировать увеличение количества клеток после 3 сут, по сравнению со средой, которая не содержала добавленные факторы роста.
Немодифицированные контрольные белки G-CSF/A33 и G-CSF/A58 стимулировали клетки в очень похожей степени (ED50=5-10 пкг/мл), тогда как конъюгаты G-CSF/A60 и G-CSF/A32 G-CSF/A57 проявили только небольшое уменьшение активности при сравнении с немодифицированным вариантом (ED50=10-25 пкг/мл).
(см. фиг.8)
Пример 7 Синтез конъюгатов G-CSF
Пример 7.1 Синтез производных альдегидо-HES
Пример 7.1(а) Синтез АминоHES10/0.4
5,12 г оксо HES10/0.4 (молекулярная масса=10000 Д, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, в соответствии с DE 196 28 705 A1) нагревают в течение ночи при 80°С в вакууме и растворяют в атмосфере азота в 25 мл сухого диметилсульфоксида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют 5,13 мл 1,4-диаминобутана. После перемешивания при 40°С в течение 17 ч реакционную смесь добавляют к 150 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, промывают 40 мл ледяной смеси 1:1 ацетона и этанола (об./об.) и собирают центрифугированием. Неочищенный продукт растворяют в 80 мл воды, диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 67%.
Пример 7.1(b) Синтез альдегидоHES10/0.4
105 мг 4-формилбензойной кислоты и 135 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 7 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 135 мкл N,N'-диизопропилкарбодиимида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D). После инкубации при 21°С в течение 30 мин добавляют 0,7 г амино-HES10/0,4 (синтезированного, как описано в 1.1). После встряхивания в течение 18 ч при 22°С реакционную смесь добавляют к 42 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в 5 мл DMF и осаждают 42 мл этанола/ацетона, как описано выше. После центрифугирования собранный осадок растворяют в воде, диализируют в течение 1 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 95%.
Пример 7.1(с) Синтез аминоHES10/0.7
6,02 г оксо-HES 10/0.7 (молекулярная масса=10000 дальтон, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, в соответствии с DE 196 28 705) растворяют в атмосфере азота в 32 мл сухого диметилсульфоксида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют 6,03 мл 1,4-диаминобутана. После перемешивания при 40°С в течение 17 ч реакционную смесь добавляют к 150 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, промывают 40 мл ледяной смеси 1:1 ацетона и этанола (об./об.) и собирают центрифугированием. Неочищенный продукт растворяют в 80 мл воды, диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 52%.
Пример 7.1(d) Синтез альдегидоHES10/0,7
150 мг 4-формилбензойной кислоты и 230 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 10 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 204 мкл N,N'-диизопропилкарбодиимида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D). После инкубации при 21°С в течение 30 мин добавляют 1 г амино-HES10/0,7 (синтезированного, как описано в 1.3). После встряхивания в течение 19 ч при 22°С реакционную смесь добавляют к 84 мл ледяного 2-пропанола. Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в 50 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 83%.
Пример 7.1(е) Синтез аминоHES30/0,4
5 г оксо-HES30/0.4 (молекулярная масса=30000 дальтон, DS=0,4, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, с использованием молярных соотношений ингредиентов, в соответствии с DE 196 28 705 А1) нагревают в течение ночи при 80°С в вакууме и затем растворяют в атмосфере азота в 28 мл сухого диметилсульфоксида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют 1,67 мл 1,4-диаминобутана. После перемешивания при 40°С в течение 17 ч реакционную смесь добавляют к 175 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С. Неочищенный продукт растворяют в 40 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта не определяют.
Пример 7.1(f) Синтез альдегидоHES30/0,4
130 мг 4-формилбензойной кислоты и 153 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 36 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 110 мкл N,N'-диизопропилкарбодиимида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D). После инкубации при 21°С в течение 30 мин добавляют 2,61 г аминоHES30/0,4 (синтезированного, как описано в 1.5). После встряхивания в течение 22,5 ч при 22°С реакционную смесь добавляют к 160 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, и промывают ледяной смесью 1:1 ацетона и этанола (об./об.). После центрифугирования осадок растворяют в 30 мл воды, диализируют в течение 1 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 81%.
Пример 7.1(g) Синтез аминоHES30/0,7
5 г оксо-HES30/0.7 (молекулярная масса=30000 дальтон, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, с использованием молярных соотношений ингредиентов, в соответствии с DE 196 28 705 А1) нагревают в течение ночи при 80°С в вакууме и затем растворяют в атмосфере азота в 28 мл сухого диметилсульфоксида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют 1,67 мл 1,4-диаминобутана. После перемешивания при 40°С в течение 17 ч реакционную смесь добавляют к 175 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С. Неочищенный продукт растворяют в 40 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта не определяют.
Пример 7.1(h) Синтез альдегидоHES30/0,7
122 мг 4-формилбензойной кислоты и 144 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 34 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 103 мкл N,N'-диизопропилкарбодиимида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D). После инкубации при 21°С в течение 30 мин добавляют 2,46 г аминоHES30/07 (синтезированного, как описано в 1.7). После встряхивания в течение 22,5 ч при 22°С реакционную смесь добавляют к 160 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, и промывают ледяной смесью 1:1 ацетона и этанола (об./об.). После центрифугирования осадок растворяют в 30 мл воды, диализируют в течение 1 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 87%.
Пример 7.1(i) Синтез аминоHES50/0,7
6,09 г оксо-HES 50/0.7 (молекулярная масса=50000 дальтон, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D, с использованием молярных соотношений ингредиентов, в соответствии с DE 196 28 705 А1) нагревают в течение ночи при 80°С в вакууме и затем растворяют в атмосфере азота в 32 мл сухого диметилсульфоксида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) и добавляют 1,22 мл 1,4-диаминобутана. После перемешивания при 40°С в течение 17 ч реакционную смесь добавляют к 150 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, промывают 40 мл ледяной смеси 1:1 ацетона и этанола (об./об.) и собирают центрифугированием. Неочищенный продукт растворяют в 80 мл воды, диализируют в течение 4 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 82%.
Пример 7.1(j) Синтез альдегидоHES50/0,7
125 мг 4-формилбензойной кислоты и 174 мг 1-гидрокси-1Н-бензотриазола (оба Aldrich, Sigma-Aldrich Chemie GmbH, Taufkirchen, D) растворяют в 38 мл N,N-диметилформамида (сорта пептидного синтеза, Biosolve, Valenswaard, NL) и добавляют 155 мкл N,N'-диизопропилкарбодиимида (Fluka, Sigma-Aldrich Chemie GmbH, Taufkirchen, D). После инкубации при 21°С в течение 30 мин добавляют 3,8 г аминоHES50/07 (синтезированного, как описано в 1.9). После встряхивания в течение 19 ч при 22°С реакционную смесь добавляют к 160 мл ледяной смеси 1:1 ацетона и этанола (об./об.). Осажденный продукт собирают центрифугированием при 4°С, повторно растворяют в 20 мл N,N-диметилформамида и осаждают 80 мл ледяной смеси 1:1 ацетона и этанола (об./об.), как описано выше. После центрифугирования осадок растворяют в 50 мл воды, диализируют в течение 2 сут против воды (диализная трубка SnakeSkin, отсечка 3,5 кДа, Perbio Sciences Deutschland GmbH, Bonn, D) и лиофилизируют. Выход выделенного продукта составляет 77%.
Пример 7.2 Синтез конъюгатов HES-G-CSF восстановительным аминированием
Пример 7.2(а) Обмен буфера А:
33 мл раствора 0,454 мг/мл hG-CSF (XM02, BioGeneriX AG, Mannheim, D) в 10 мМ ацетате натрия, 50 мг/мл сорбита и 0,004% Tween 80 при рН 4,0 концентрируют диафильтрацией при 0°С до 4 мл концентратором Vivaspin 15R (VS15RH11, 5 кДа MWCO, Vivascience AG, Hannover, D) и повторно разбавляют до 15 мл 0,1 М буфером ацетата натрия при рН 5,0. Эту диафильтрацию повторяют дважды. Конечная концентрация на последней стадии диафильтрации составляет 3 мг/мл.
Пример 7.2(b) Реакция hG-CSF с производными альдегидоHES примеров 7.1(b), 7.1(d) и 7.1(j)
К 1,67 мл раствора hG-CSF после обмена буфера на 0,1 М буфер ацетата натрия при рН 5,0 (как описано выше в 7.2(а)) добавляют 1,67 мл раствора производного HES и 1,67 мл 60 мМ раствора цианоборгидрида натрия, оба в том же буфере, и раствор инкубируют в течение 15 ч при 4°С. Все растворы охлаждают до 0°С перед смешиванием.
Используют следующие конечные концентрации HES:
39,4 мг/мл для производных HES, полученных в соответствии с примером 7.1(b) и 7.1(d).
197 мг/мл для производных HES, полученных в соответствии с примером 7.1(j)
197 мг/мл HES50/0.7 (молекулярная масса=50000 дальтон, DS=0,7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D) в качестве контроля реакции.
Реакционные смеси анализируют гель-электрофорезом (см. Фиг.17).
Пример 7.2(с) Обмен буфера В:
20 мл раствора 0,454 мг/мл hG-CSF (XM02, BioGeneriX AG, Mannheim, D) в 10 мМ ацетате натрия, 50 мг/мл сорбита и 0,004% Tween 80 при рН 4,0 концентрируют диафильтрацией при 15°С до 4 мл концентратором Vivaspin 15R (VS15RH11, 5 кДа MWCO, Vivascience AG, Hannover, D) и повторно разбавляют до 15 мл 0,1 М буфером ацетата натрия при рН 5,0. Эту диафильтрацию повторяют дважды. Конечная концентрация на последней стадии диафильтрации составляет 1,5 мг/мл.
Пример 7.2(d) Реакция hG-CSF с производными альдегидоHES примеров 7.1(f), 7.1(h)
К 3,3 мл раствора hG-CSF после обмена буфера на 0,1 М буфер ацетата натрия при рН 5,0 (как описано выше в 7.2(с)) добавляют 3,3 мл раствора 789 мг производного HES и 3,3 мл 60 мМ раствора цианоборгидрида натрия, оба в том же буфере, и раствор инкубируют в течение 30 ч при 4°С. Все растворы охлаждают до 0°С перед смешиванием.
Через 17 ч образцы удаляют для контроля реакции. Реакционные смеси анализируют гель-электрофорезом (см. Фиг.18).
Пример 7.3 Синтез конъюгатов HES-GCFS соединением карбоната N,N'-сукцинимидила
Пример 7.3(а) Синтез конъюгатов G-CFS взаимодействием гидроксиэтилкрахмала, имеющего реакционноспособную сложноэфирную группу, с G-CFS
400 мг Оксо-HES10/0,7 (полученный Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, D; в соответствии с DE 196 28 705 A1, степень окисления оксо-HES составляет 95%) растворяют в 1 мл безводного DMF. К этому раствору добавляют 21 мг карбоната N,N'-сукцинимидила, и смесь перемешивают в течение 2 ч при комнатной температуре. Полученный раствор имеет концентрацию реакционноспособного HES 40% мас.
Раствор G-CSF (Strathmann Biotec AG, Hamburg, D), имеющий концентрацию примерно 0,5 мг G-CSF/мл, концентрируют до концентрации 10 мг/мл ультрацентрифугированием при отсечке 100 кДа с использованием охлаждающей центрифуги.
К 0,5 мл этого концентрированного раствора G-CSF добавляют 180 мкл раствора бикарбоната натрия. В последующем 3 порции (100 мкл каждая) раствора реакционноспособного HES по каплям добавляют к раствору белка до тех пор, пока примерно через 30 мин не завершится реакция. Таким образом, общее молярное соотношение реакционноспособного HES:G-CSF составляет примерно 50:1. Затем рН смеси доводят до 4,0, используя 0,1 N HCl.
Анализ ГПХВД (гель-проникающей хроматографией под высоким давлением) дает выход более чем 95%. Можно выявить не вступивший во взаимодействие G-CSF. Этот результат показан на фиг.19.
Пример 7.4 Анализ in vitro
Митогенность вариантов G-CSF для мышиных клеток NFS-60
Известно, что G-CSF оказывает специфические воздействия на пролиферацию, дифференциацию и активацию гематопоэтических клеток линии нейтрофильных гранулоцитов. Митогенную способность вариантов G-CSF испытывают с использованием мышиных клеток NFS-60 (N. Shirafuji et al., Exp. Hematol. 1989, 17, 116-119). Клетки, выращенные в среде RPMI с 10% фетальной телячьей сывороткой (Gibco INVITROGEN GmbH, Karlsruhe, D), содержащей кондиционированную среду 5-10% WEHI-3B (DSMZ, Braunschweig, D; культивированные, как описано DSMZ) в качестве источника экзогенного IL-3, собирают центрифугированием, промывают и делят на аликвотные количества по 100000 клеток на лунку в 24-луночной планшете. Клеткам давали возможность адаптироваться в течение 1 ч при 37°С в среде RPMI без сред, кондиционированных WEHI-3B, перед добавлением образцов фактора роста G-CSF, разведенных в тех же средах. Клетки NFS-60 подвергали воздействию очищенных вариантов G-CSF (очистка в соответствии с примерами 5.3, 5.4, количественное определение белка в соответствии с примером 5.5(а)):
Neupogen® , Neulasta® оба от Amgen,
«Конъюгат HES-GCSF10/0,4», полученный в примере 7.2(b),
«Конъюгат HES-GCSF10/0,7», полученный в примере 7.2(b),
«Конъюгат HES-GCSF30/0,4», полученный в примере 7.2(d),
«Конъюгат HES-GCSF30/0,7», полученный в примере 7.2(d),
«Конъюгат HES-GCSF50/0,7», полученный в примере 7.2(b),
«Конъюгат HES-GCSF10/0,7 (Supramol)», полученный в соответствии с примером 7.3(а),
«Имитационная инкубация» (= контроль реакции, 197 мг/мл HES50/0.7, молекулярная масса 50000 дальтон, DS 7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, Germany),
в течение 3 сут при 37°С, и затем клетки электронно подсчитывают (счетчик клеток Casy TT, Schärfe System, Reutlingen, D). Результаты сведены в таблице 2 и на фиг.20. Во всех случаях количества белка, представленные в таблице 2 и на фиг.20, представляют содержание G-CSF только конъюгатов и основаны на концентрациях, определенных GlycoThera. Как видно на фиг.20, все различные варианты G-CSF (2,5-250 пкг/мл) были способны стимулировать увеличение количества клеток через 3 сут, по сравнению со средой, которая не содержала добавленные ростовые факторы. Все варианты достигли одинакового максимального уровня стимуляции при концентрации 250 пкг/мл.
Таблица 2
Пролиферация мышиных клеток NFS-60, вызванная вариантами G-CSF
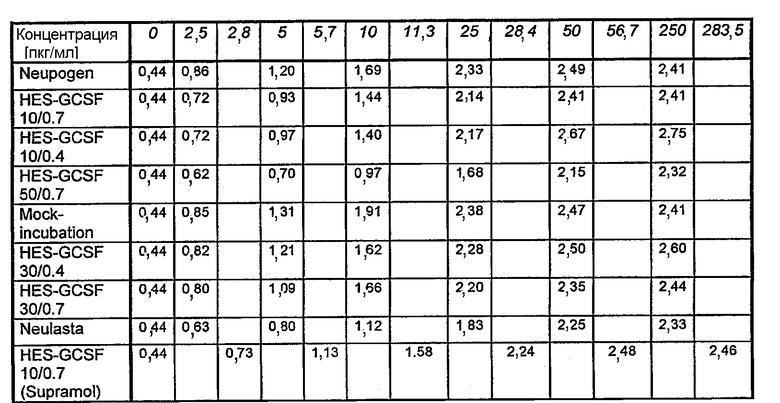
Пример 7.5 Биологические эффекты in vivo конъюгатов hG-CSF у крыс
При поступлении крыс [самцов крыс CRL:CD® (в возрасте 7 нед), Charles River Deutschland GmbH, Sanghofer Weg 7, D-97633 Sulzfeld)] методом случайной выборки распределяли в группы по 5 животных. Через 7 сут акклиматизации крыс в плохом состоянии исключали и заменяли запасными животными. Масса крыс при поступлении составляла 181-203 г.
Затем каждой группе выбранных случайным методом крыс внутривенно вводили 100 мкг на 1 кг массы тела (скорость инъекции 15 с/дозу, носитель: 5 мл PBS/кг массы тела) следующих неконъюгированных или конъюгированных образцов G-CSF (очищенных в соответствии с примерами 5.3, 5.4, количественное определение в соответствии с примером 5.5(а)):
Neupogen®, Neulasta® оба от Amgen,
«Конъюгат HES-GCSF10/0,4», полученный в примере 7.2(b),
«Конъюгат HES-GCSF10/0,7», полученный в примере 7.2(b),
«Конъюгат HES-GCSF30/0,4», полученный в примере 7.2(d),
«Конъюгат HES-GCSF30/0,7», полученный в примере 7.2(d),
«Конъюгат HES-GCSF50/0,7», полученный в примере 7.2(b),
«Конъюгат HES-GCSF10/0,7 (Supramol)», полученный в соответствии с примером 7.3(а),
«Имитационная инкубация» (= контроль реакции, 197 мг/мл HES50/0,7, молекулярная масса 50000 дальтон, DS 7, Supramol Parenteral Colloids GmbH, Rosbach-Rodheim, Germany) и контроль носителя.
У всех животных образцы цельной крови приблизительно 200 мкл ЭДТА брали из ретробульбарного венозного сплетения в условиях легкой эфирной анестезии. За 5 сут до тестирования кровь брали 1 раз утром у всех животных после голодания в течение ночи. На 1-8 сут теста кровь брали дважды в сутки с интервалом 12 ч. Первый образец крови в 1-й сут брали перед введением конъюгата G-CSF/GCSF.
Лейкоцитарную формулу (WBC) определяли с использованием Bayer ADVIATM 120 (Fernwald, Germany). Результаты показаны на фиг.21.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ГИДРОКСИАЛКИЛКРАХМАЛА | 2003 |
|
RU2329274C2 |
| КОНЪЮГАТЫ ГИДРОКСИАЛКИЛКРАХМАЛА И АЛЛЕРГЕНА | 2003 |
|
RU2325925C2 |
| КОНЪЮГАТ ГИДРОКСИАЛКИЛКРАХМАЛА И НИЗКОМОЛЕКУЛЯРНОГО ВЕЩЕСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2327702C2 |
| ПОЛИПЕПТИДЫ, ОБРАБОТАННЫЕ HAS, ОСОБЕННО ЭРИТРОПОЭТИН, ОБРАБОТАННЫЙ HAS | 2003 |
|
RU2328505C2 |
| ОПОСРЕДУЮЩИЕ ТРАНСПОРТ КОЛЛОИДНЫЕ ЛЕКАРСТВЕННЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2519225C2 |
| ПРОИЗВОДНЫЕ ГИДРОКСИАЛКИЛКРАХМАЛА | 2003 |
|
RU2326891C2 |
| СПОСОБ СИНТЕЗА КОНЪЮГАТОВ ГЛИКОЗАМИНОГЛИКАНОВ (GAG) С БИОЛОГИЧЕСКИ АКТИВНЫМИ МОЛЕКУЛАМИ, ПОЛИМЕРНЫЕ КОНЪЮГАТЫ И ИХ СООТВЕТСТВУЮЩИЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2530649C2 |
| КОНЪЮГАТЫ ГЕМОГЛОБИНА С ПОЛИСАХАРИДОМ | 1999 |
|
RU2225222C2 |
| ГЛИКОПЭГИЛИРОВАННЫЙ ГРАНУЛОЦИТАРНЫЙ КОЛОНИЕСТИМУЛИРУЮЩИЙ ФАКТОР | 2004 |
|
RU2400490C2 |
| НОВЫЙ СТАБИЛИЗАТОР ДЛЯ ФАРМАЦЕВТИЧЕСКИХ БЕЛКОВ | 2011 |
|
RU2571496C2 |


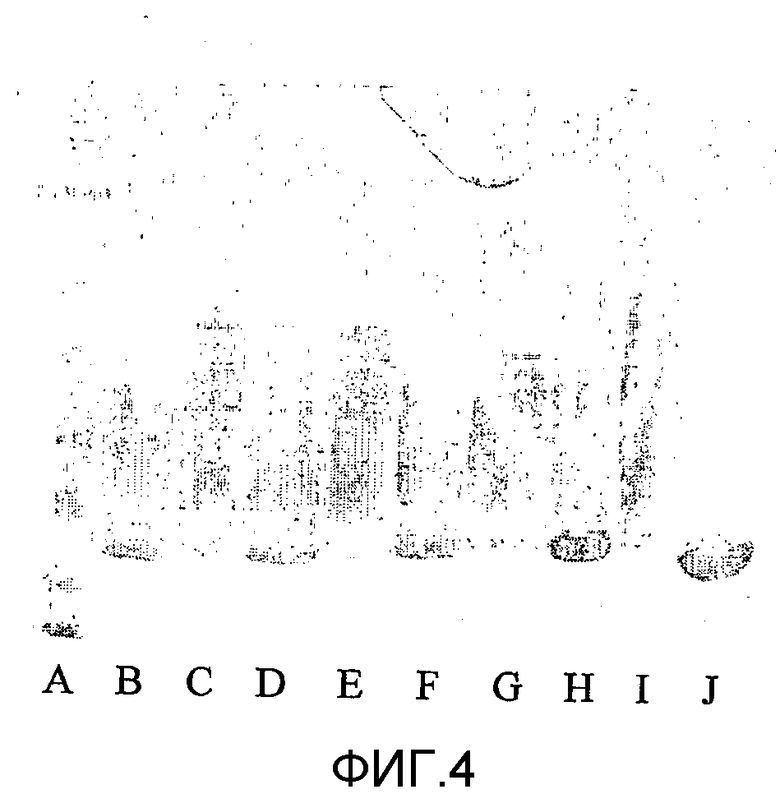
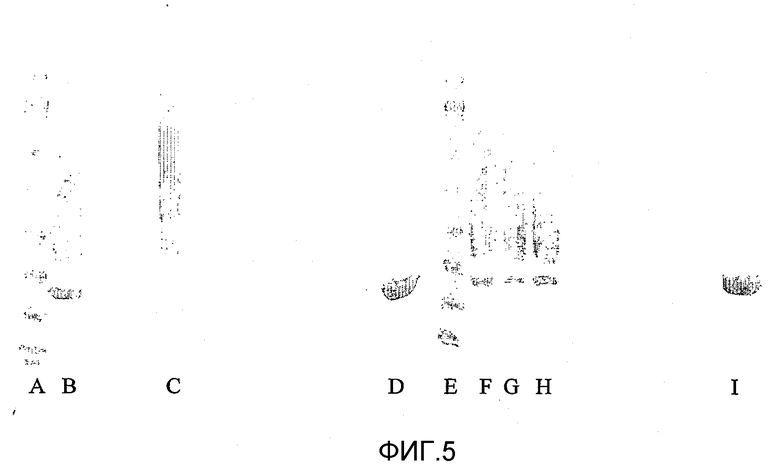


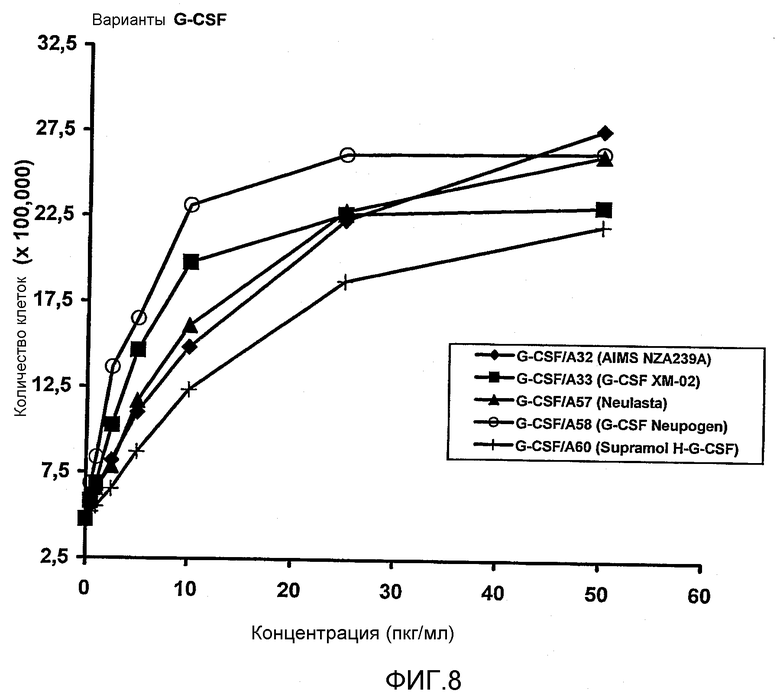
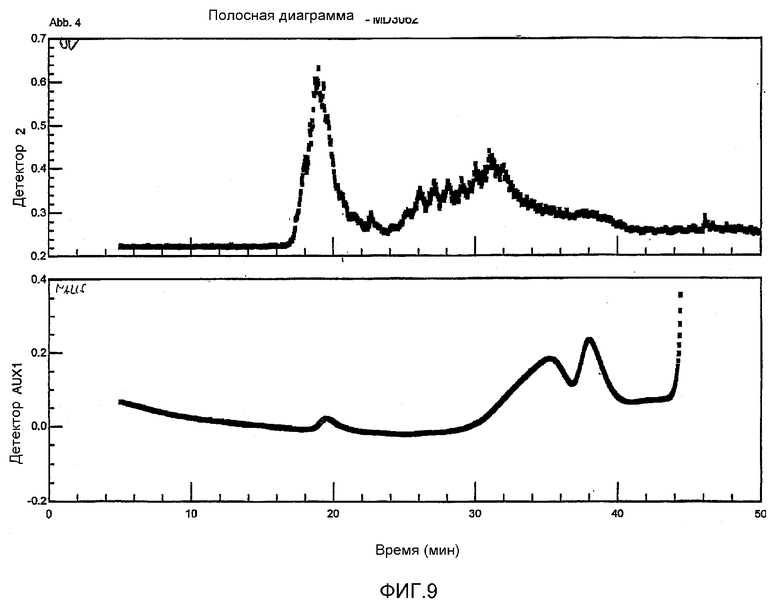
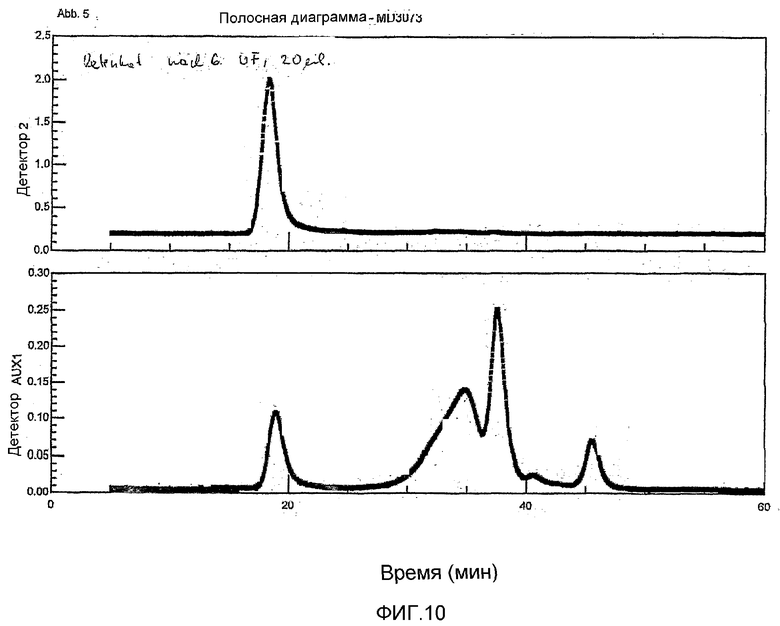
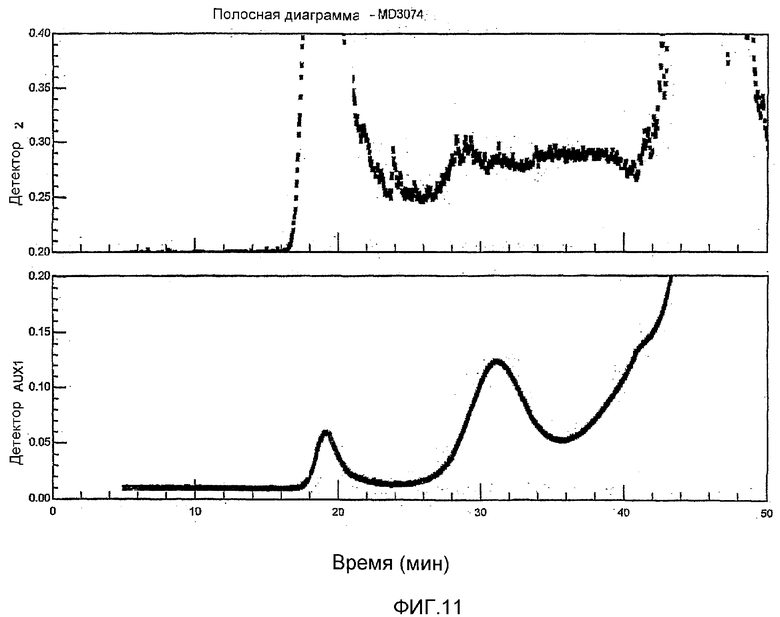
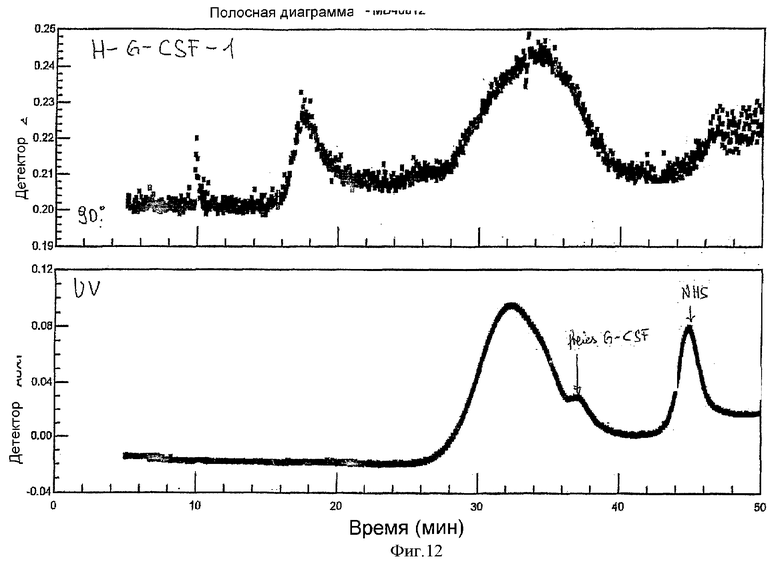
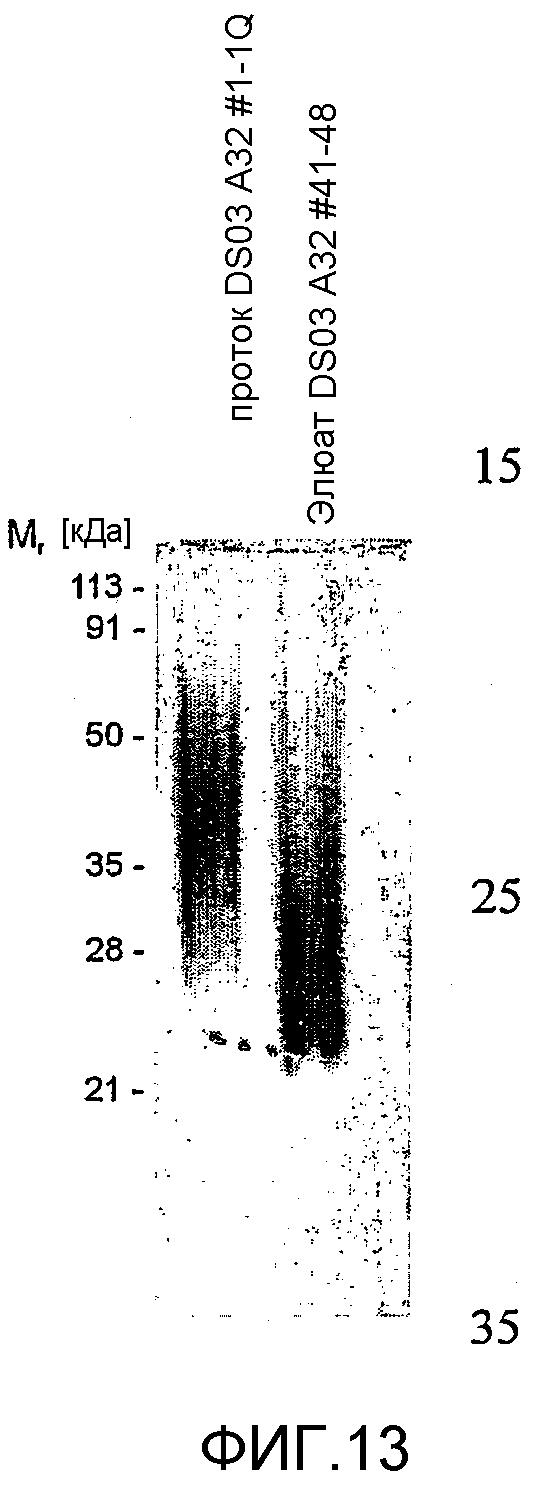
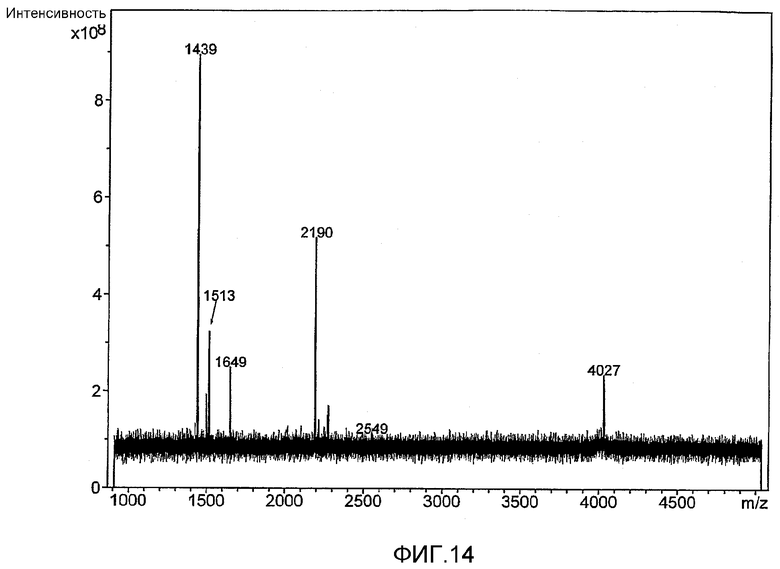
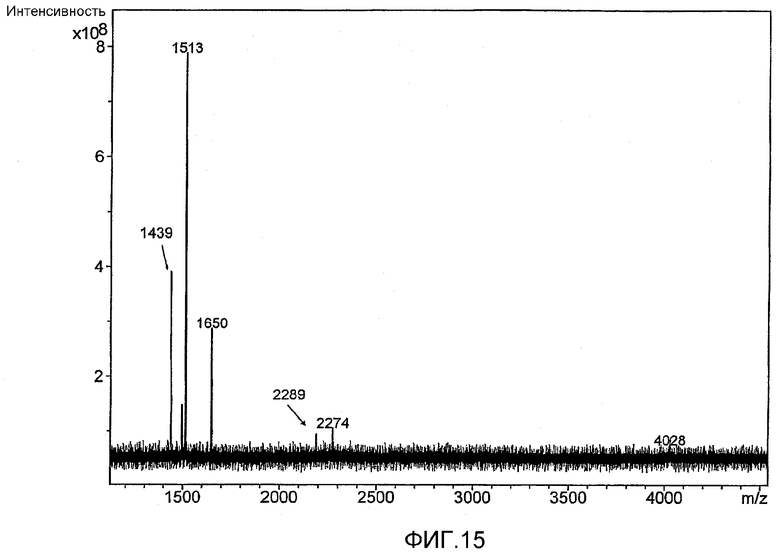
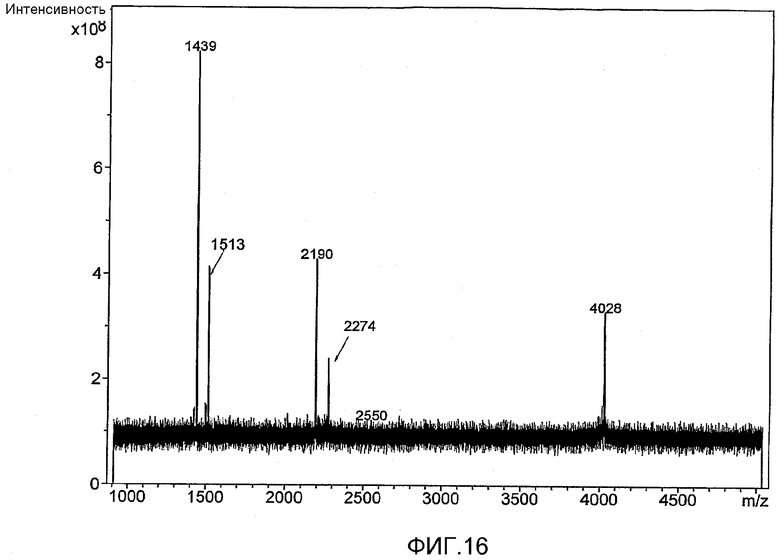


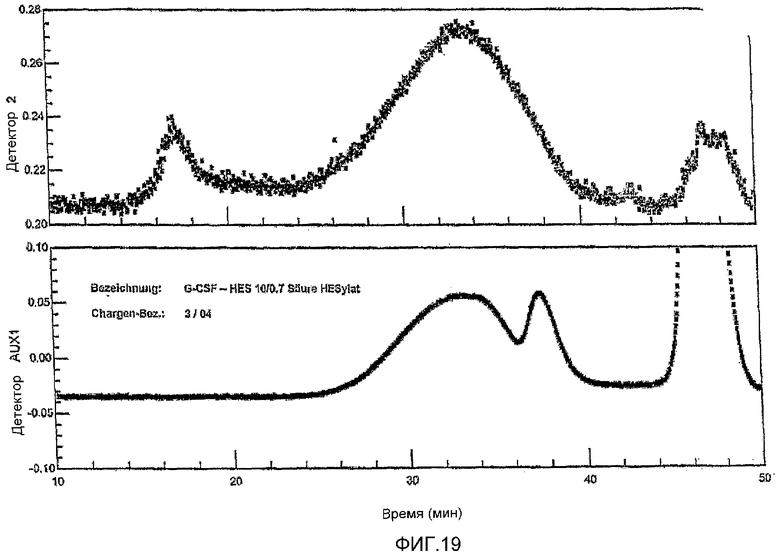
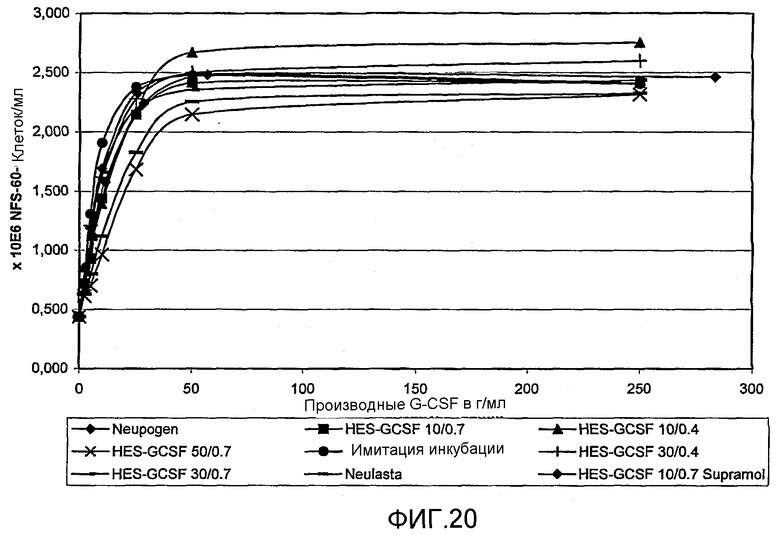
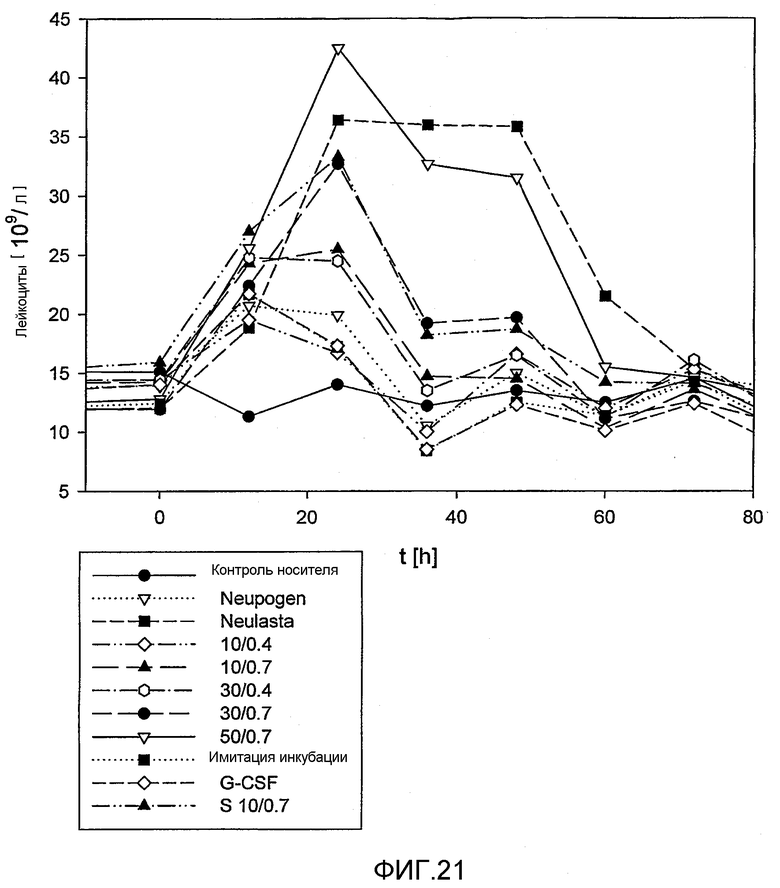
Изобретение относится к области биотехнологии и касается конъюгатов гидроксиалкилкрахмала и белка фактора, стимулирующего колонии гранулоцитов (G-CSF), причем указанные конъюгаты образованы ковалентным связыванием между гидроксиэтилкрахмалом или его производным с молекулярным весом от 2 до 200 кДа и белком. Настоящее изобретение также относится к способам получения этих конъюгатов и к применению этих конъюгатов. 6 н. и 20 з.п. ф-лы, 2 табл., 21 ил.
1. Способ получения конъюгата, включающего белок и производное полимера, причем полимер представляет собой гидроксиалкилкрахмал (HAS), который представляет собой гидроксиэтилкрахмал с молекулярным весом от 2 до 200 кДа, а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), причем способ включает взаимодействие, по меньшей мере, одной функциональной группы А производного полимера, по меньшей мере, с одной функциональной группой Z белка и, посредством этого, образуя ковалентную связь, где Z представляет собой аминогруппу, и
где А выбрана из группы, состоящей из альдегидной группы, кетогруппы или полуацетальной группы,
где способ, кроме того, включает введение А в полимер для получения производного полимера путем
взаимодействия полимера на его окисленном восстанавливающем конце с функциональной группой М, по меньшей мере, бифункционального соединения, где М включает аминогруппу, для получения полимерного производного, причем, по меньшей мере, бифункциональное соединение, кроме того, включает, по меньшей мере, одну другую функциональную группу Q, которая представляет собой альдегидную группу, кетогруппу или полуацетальную группу А, или
взаимодействия полимера на его окисленном восстанавливающем конце с функциональной группой M, по меньшей мере, бифункционального соединения, где M включает аминогруппу, для получения полимерного производного, причем, по меньшей мере, бифункциональное соединение, кроме того, включает, по меньшей мере, одну другую функциональную группу Q, которая не является альдегидной группой, кетогруппой или полуацетальной группой, и последующего взаимодействия группы Q с по крайней мере одним соединением, пригодным для получения полимерного производного, включающего альдегидную группу, кетогруппу или полуацетальную группу А,
где указанный коньюгат соответствует формуле
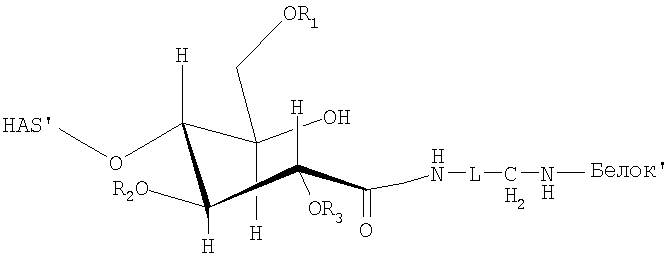
и/или
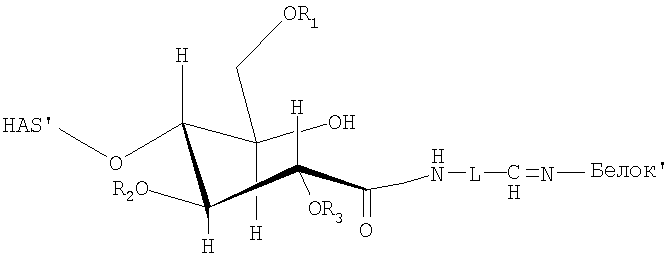
где R1, R2 и R3 представляют собой независимо водород или гидроксиэтильную группу, и
где L представляет собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, имеющий от 1 до 60, предпочтительно, от 1 до 40, предпочтительнее, от 1 до 20, предпочтительнее, от 1 до 10, предпочтительнее, от 1 до 6, предпочтительнее, от 1 до 2 атомов углерода, а особенно предпочтительно, 1 атом углерода, причем L представляет собой в частности CH2,
или коньюгат соответствует формуле
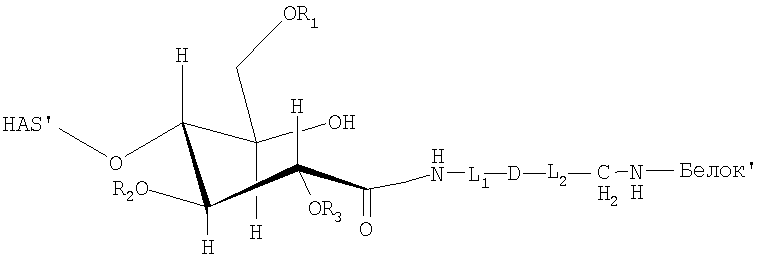
где R1, R2 и R3 представляют собой независимо водород или гидроксиэтильную группу, и
где L1 и L2 представляют собой независимо необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, включающий алкильную, арильную, аралкильную, гетероалкильную и/или гетероаралкильную часть, причем указанный остаток имеет от 1 до 60, предпочтительно, от 1 до 40, предпочтительнее, от 1 до 20, предпочтительнее, от 1 до 10 атомов углерода, и
где D представляет собой связь, предпочтительно, ковалентную связь, которая образована подходящей функциональной группой F2, связанной с L1, и подходящей функциональной группой F3, связанной с L3.
2. Способ по п.1, где гидроксиэтилкрахмал имеет молекулярную массу от 4 до 130 кДа, предпочтительнее, от 4 до 70 кДа.
3. Способ по п.1 или 2, где способ включает взаимодействие полимера с функциональной группой М, по меньшей мере, бифункционального соединения, где М включает аминогруппу, для получения полимерного производного, причем, по меньшей мере, бифункциональное соединение, кроме того, включает, по меньшей мере, одну другую функциональную группу Q, которая не является альдегидной группой, кетогруппой или полуацетальной группой, причем способ, кроме того, включает взаимодействие функциональной группы Q, по меньшей мере, с одним подходящим соединением для получения полимерного производного, включающего альдегидную группу, кетогруппу или полуацетальную группу А, где Q включает аминогруппу.
4. Способ по п.3, где, по меньшей мере, одно подходящее соединение включает карбоксигруппу и альдегидную группу, кетогруппу или полуацетальную группу.
5. Способ по п.4, где, по меньшей мере, одно подходящее соединение представляет собой формилбензойную кислоту или 4-(4-формил-3,5-диметоксифенокси)масляную кислоту.
6. Способ по п.3, где М включают аминогруппу, а Q включает бета-гидроксиаминогруппу.
7. Способ по п.6, кроме того, включающий окисление бета-гидроксиаминогруппы для получения альдегидной группы.
8. Способ по п.7, где реакция окисления проводится с использованием периодата.
9. Способ по п.1, где взаимодействие полимерного производного с белком представляет собой восстановительное аминирование.
10. Способ по п.9, где восстановительное аминирование проводится в присутствии NaCNBH3.
11. Способ по п.9, где восстановительное аминирование проводится при рН 7 или менее.
12. Способ по п.11, где рН составляет 6 или менее.
13. Способ по п.9, где восстановительное аминирование проводится при температуре от 0 до 25°С.
14. Способ по п.9, где восстановительное аминирование проводится в водной среде.
15. Конъюгат, который можно получить способом по любому из пп.1-14.
16. Конъюгат, включающий белок и производное полимера, где полимер представляет собой гидроксиалкилкрахмал (HAS), который представляет собой гидроксиэтилкрахмал с молекулярным весом от 2 до 200 кДа, а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой

и/или
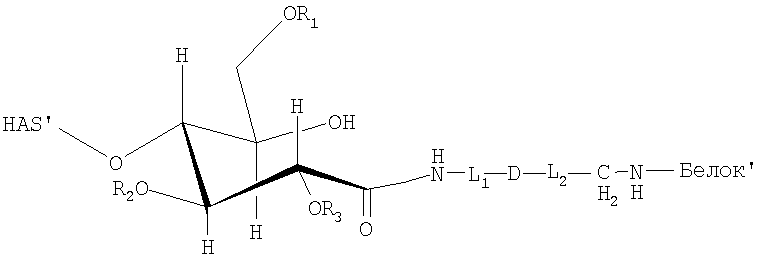
где R1, R2 и R3 представляют собой независимо водород или гидроксиалкильную группу, предпочтительнее, водород или гидроксиэтильную группу, и
где L представляет собой необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, имеющий от 1 до 60, предпочтительно, от 1 до 40, предпочтительнее, от 1 до 20, предпочтительнее, от 1 до 10, предпочтительнее, от 1 до 6, предпочтительнее, от 1 до 2 атомов углерода, а особенно предпочтительно, 1 атом углерода, причем L представляет собой в частности CH2.
17. Конъюгат, включающий белок и производное полимера, где полимер представляет собой гидроксиалкилкрахмал (HAS), который представляет собой гидроксиэтилкрахмал с молекулярным весом от 2 до 200 кДа, а белок представляет собой фактор, стимулирующий колонии гранулоцитов (G-CSF), имеющий структуру в соответствии с формулой

где R1, R2 и R3 представляют собой независимо водород или гидроксиэтильную группу, и
где L1 и L2 представляют собой независимо необязательно замещенный, линейный, разветвленный и/или циклический углеводородный остаток, необязательно включающий, по меньшей мере, один гетероатом, включающий алкильную, арильную, аралкильную, гетероалкильную и/или гетероаралкильную часть, причем указанный остаток имеет от 1 до 60, предпочтительно, от 1 до 40, предпочтительнее, от 1 до 20, предпочтительнее, от 1 до 10 атомов углерода, и
где D представляет собой связь, предпочтительно, ковалентную связь, которая образована подходящей функциональной группой F2, связанной с L1, и подходящей функциональной группой F3, связанной с L2.
18. Конъюгат по п.17, где L1 представляет собой -(CH2)n- при n=2, 3, 4, 5, 6, 7, 8, 9, 10, предпочтительно, 2, 3, 4, 5, 6, предпочтительнее, 2, 3, 4, и особенно предпочтительно, 4.
19. Конъюгат по п.17, где L2 включает необязательно подходящим образом замещенную арильную часть, предпочтительно, арильную часть, содержащую 6 атомов углерода, причем L2 особенно предпочтительно представляет собой С6Н4.
20. Конъюгат по п.17, где F2 выбрана из группы, состоящей из
C-C-двойных связей или C-C-тройных связей или ароматических С-С-связей;
тиогруппы или гидроксигруппы;
гидразида алкилсульфоновой кислоты, гидразида арилсульфоновой кислоты;
1,2-диолов;
1,2-аминотиоспиртов;
азидов;
1,2-аминоспиртов;
аминогруппы -NH2 или производных аминогрупп, включающих структурную единицу -NH-, таких как аминоалкильные группы, аминоарильные группы, аминоаралкильные группы, или алкариламиногруппы;
гидроксиламиногруппы -O-NH2, или производных гидроксиламиногруппы, включающих структурную единицу -O-NH-, такую как гидроксилалкиламиногруппы, гидроксилариламиногруппы, гидроксиларалкиламиногруппы или гидроксалалкариламиногруппы;
алкоксиаминогрупп, арилоксиаминогрупп, аралкилоксиаминогрупп, или алкарилоксиаминогрупп, каждая из которых включает структурную единицу -NH-O-;
остатков, имеющих карбонильную группу, -Q-C(=G)-M, где G представляет собой О или S, а М представляет собой, например,
-ОН или -SH;
алкоксигруппу, арилоксигруппу, аралкилоксигруппу или алкарилоксигруппу;
алкилтиогруппу, арилтиогруппу, аралкилтиогруппу или алкарилтиогруппу;
алкилкарбонилоксигруппу, арилкарбонилоксигруппу, аралкилкарбонилоксигруппу, алкарилкарбонилоксигруппу;
активированные сложные эфиры, такие как сложные эфиры гидроксиламинов, имеющие имидную структуру, такие как N-гидроксисукцинимид, или имеющие структурную единицу O-N, где N представляет собой часть гетероарильного соединения или с отсутствующими G=O и Q, такие как арилокси соединения с замещенным арильным остатком, такие как пентафторфенил, паранитрофенил или трихлорфенил;
где Q отсутствует или представляет собой NH или гетероатом, такой как S или О;
-NH-NH2, или -NH-NH-;
-NO2;
нитрильную группу;
карбонильные группы, такие как альдегидная группа или кетогруппа;
карбоксигруппу;
группу -N=C=O или группу -N=C=S;
группы винилгалогенидов, такие как группа винилиодида или винилбромида или трифлат;
-С≡С-Н;
-(С=NH2Cl)-ОАлкил;
группы - (С=O)-CH2-Hal, где Hal представляет собой Cl, Br или I;
-CH=CH-SO2-;
дисульфидную группу, включающую структуру -S-S-;
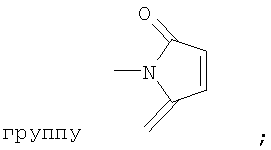
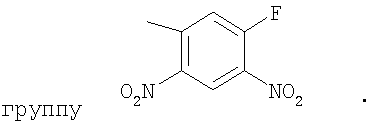
где F3 представляет собой функциональную группу, способную образовывать химическую связь с F2, и предпочтительно выбрана из указанных выше групп, причем F2 предпочтительно включает часть -NH-, предпочтительно включает аминогруппу, F3 предпочтительно включает часть -(C=G)-, предпочтительнее, -(С=O)-, предпочтительнее, часть -(C=G)-G-, еще предпочтительнее, -(C=O)-G-, а особенно предпочтительно, -(С=O)-O-, причем особенно предпочтительно, D представляет собой амидную связь.
21. Конъюгат по любому из пп.16-20, где гидроксиэтилкрахмал имеет молекулярную массу от 4 до 130 кДа, предпочтительнее, от 4 до 70 кДа.
22. Конъюгат по любому из пп.15-21 для применения в способе лечения организма человека или животного.
23. Фармацевтическая композиция, включающая в терапевтически эффективном количестве конъюгат по любому из пп.15-21.
24. Фармацевтическая композиция по п.23, кроме того, включающая, по меньшей мере, один фармацевтически приемлемый разбавитель, адъювант или носитель.
25. Применение конъюгата по любому из пп.15-21 для изготовления лекарственного средства для лечения расстройства, характеризуемого сниженной гематопоэтической или иммунной функцией.
26. Применение по п.25, где расстройство представляет собой результат химиотерапии, лучевой терапии, инфекционное заболевание, тяжелую хроническую нейтропению или лейкоз.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
Авторы
Даты
2009-10-20—Публикация
2004-08-06—Подача