ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области молекулярной биологии растений и, в частности, к способам увеличения экспрессии гетерологичных белков в семенах растений путем супрессии конкуренции за эндогенную экспрессию запасных белков семян в эндосперме однодольных растений.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Многие растения экспрессируют и запасают в эндосперме развивающихся семян большое количество белков, выполняющих различные функции, таких как разные виды запасных белков, метаболические ферменты, эндохитиназы, ингибиторы белкового синтеза, ингибиторы протеаз, амилазы, лектины и пероксидазы. Запасные белки в эндосперме могут составлять более 15% от сухого веса семени, что является обычным во многих видах однодольных зерновых культурах. Соответственно, на определенной стадии развития клеточный аппарат в эндосперме семени занят в основном продуцированием и запасанием этих специфических белков. Кроме того, большинство генов запасных белков обнаружено во множественных копиях, что отражает важность быстрого накопления этих белков в интервале от нескольких дней до нескольких недель.
Неотъемлемая биологическая способность семян культурных растений накапливать белки в развивающемся эндосперме подразумевает, что многие сельскохозяйственные культуры, особенно однодольные, имеют потенциал для того, чтобы быть практическим и эффективным носителем для крупномасштабного производства гетерологичных рекомбинантных белков, например, ценных полипептидов для фармацевтической промышленности; производственного процесса, часто упоминаемого как молекулярное фермерство. Кроме того, запасание гетерологичных полипептидов в семенах снижает стоимость технологии производства и выделения целевого продукта, так как эти семена могут храниться в течение нескольких лет без потери качества гетерологичного полипептида. Экспрессия таких белков осуществляется предпочтительно под контролем специфических для семян или специфических для эндосперма промоторов.
Для улучшения уровней экспрессии гетерологичного белка в конкретном растении, используемом для молекулярного фермерства, используют общие стратегии молекулярной биологии, такие как выбор подходящих промоторов и субклеточной локализации, хотя на уровень экспрессии также критически влияет природа экспрессируемого белка, его сложность и функция. Однако низкие уровни экспрессии гетерологичного белка (низкое процентное содержание общего растворимого белка или % ОРБ) представляли особый интерес даже при экспрессии в семенах. Требуется новый биотехнологический подход для того, чтобы дополнительно увеличить уровень экспрессии. Это является серьезной проблемой, особенно когда клеточные механизмы уже запрограммированы на их эндогенную роль, которая в развивающихся семенах предпочтительно заключается в накоплении запасных белков и общей подготовке к выживанию в состоянии покоя. Промоторы, наиболее часто используемые для запуска экспрессии интересующего гетерологичного гена в эндосперме или семенах однодольных растений, представляют собой в основном промоторы из генов запасных белков, такие как GluB-1, специфический для эндосперма промотор длиной 1,3 т.п.н. из риса (Patel et аl., 2000; регистрационный № в GenBank X54314), или D-гордеиновый промотор длиной 0,45 т.п.н. из ячменя (Sorensen et al., 1996; регистрационный № в GenBank Х84368). Хотя эти промоторы являются сильными в отношении запуска экспрессии интересующих гетерологичных белков, их активность во времени и в пространстве совпадает с активностью эндогенных промоторов, запускающих большинство распространенных запасных белков, вызывая конкуренцию за ограниченные ресурсы, такие как аминокислоты, сайты связывания рибосом и ансамбль ферментов, участвующих в трансляции и посттрансляционном процессинге. Эта конкуренция отрицательно влияет на уровни экспрессии интересующего гетерологичного полипептида.
Было бы особенно желательно иметь способ супрессии экспрессии эндогенных генов, таких как многие эндогенные гены запасных белков, которые активно конкурируют за ресурсы во времени и в пространстве с экспрессией интересующего гетерологичного белка. Поэтому супрессия запасных белков могла бы удовлетворять различные промышленные потребности, если бы был предложен практический способ супрессии. Это может быть задачей особой важности в молекулярном фермерстве, особенно если эндогенный ген является членом мультигенного семейства. В ячмене, например, основным потребителем ресурсов в эндосперме являются В-гордеиновые запасные белки, которые могут составлять до 50% общих белков эндосперма (Shewry 1993: in Barley; Chemistry and Technology).
Термины "сток", "гены стока" и "белки стока" относятся в данном изобретении к генам и генным продуктам, которые активно экспрессируются и поглощают значительное количество имеющихся в клетке ресурсов, т.е. сток "выкачивает" из клетки значительную часть ее ресурсов и, следовательно, ограничивает ресурсы, имеющиеся для экспрессии других генов и генных продуктов.
Антисмысловая технология возникла как эффективный способ уменьшения экспрессии специфических эндогенных генных продуктов в растительных клетках (см., например, патент США №5759829; Orvar et al., 1997; Coles et al., 1999). Однако эта технология не является практическим подходом к прямой супрессии экспрессии генов, которые являются членами семейства генов, что часто имеет место в случае запасных белков семян, таких как В-гордеиновые гены, которые насчитывают, по меньшей мере, 20 генов на гаплоидный геном (Shewry et al., 1985); эта технология лучше подходит для управления экспрессией генов, не принадлежащих семейству генов.
Другой способ уменьшения экспрессии эндогенных генов состоит в использовании двухцепочечной РНК (дцРНК) для посттранскрипционного сайленсинга (выключения) генов (PTGS). Этот РНК-индуцированный сайленсинг генов или РНК-интерференция, где как смысловая, так и ее комплементарная антисмысловая цепь РНК конкретного эндогенного гена объединяются в одну дцРНК, был впервые продемонстрирован в Caenorhabditis elegans (Fire et al., 1998). Hamilton и др. (1999) показали, что короткие нуклеотидные РНК (длиной 21-23 нуклеотида) представляют собой продукты распада дцРНК, которые регулируют расщепление эндогенной мРНК-мишени в PTGS в растениях. Более эффективным подходом к сайленсингу двухцепочечных генов в растениях стал способ, описанный Wesley и др. (2001), где ген, приводящий к сайленсингу генов, сконструирован таким образом, что после транскрипции он образует "шпилечную петлю" РНК (hpPHK). Одна форма hpPHK сайленсинга генов представляет собой интронсплайсированную hpPHK (ihpPHK), где спейсером в шпилечной петле является интрон; ihpPHK способна к очень сильному PTGS в растениях (см. также Waterhouse еt al., 2001 и Smith et al., 2000). Способы получения таких PTGS конструкций в специальном векторе описаны в патентной заявке США 2003-А-0049835.
Существует необходимость в новых способах улучшения экспрессии гетерологичных генов в молекулярном фермерстве и особенно в однодольных растениях, таких как ячмень. Способность уменьшать конкуренцию при экспрессии между интересующими гетерологичными генами и эндогенными генами "стока" с целью увеличения экспрессии интересующих фармацевтических белков в молекулярном фермерстве не была достигнута в данной области. Из предшествующего уровня техники также не известно, как сайленсинг генов-мишеней с использованием, например, hpPHK-индуцированного PTGS может в действительности увеличить уровни экспрессии интересующих гетерологичных генов в молекулярном фермерстве.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Главная задача настоящего изобретения состоит в обеспечении способов и конструкций нуклеиновых кислот для увеличения уровней накопления интересующих гетерологичных полипептидов в трансгенных семенах, используемых в качестве носителя продукции в молекулярном фермерстве. Главный подход состоит в том, чтобы ограничить конкуренцию за ресурсы для трансляции белка, определяемой эндогенной нежелательной мРНК, кодирующей специфические для эндосперма запасные белки в однодольных растениях, в пользу экспрессии в вышеуказанном эндосперме интересующего рекомбинантно продуцируемого гетерологичного полипептида.
Предыдущие способы супрессии экспрессии генов, которые являются членами семейства генов, нацелены на индивидуальный член или гомологичные участки внутри кодирующей последовательности членов генного семейства, которые являются типичными для всех них. Одна задача настоящего изобретения состоит в том, чтобы избежать недостатков этих ранее описанных способов путем ослабления экспрессии семейства генов посредством супрессии экспрессии регуляторов транскрипции одного гена, которые в координированной манере обеспечивают регуляцию экспрессии множества членов вышеуказанного семейства генов.
Другая задача настоящего изобретения состоит в том, чтобы использовать hрРНК-индуцированный PTGS (post-transcriptional gene silencing) регуляторов транскрипции для того, чтобы супрессировать экспрессию основных запасных белков в эндосперме однодольных растений и при этом избежать использования так называемой антисмысловой технологии, которая является более традиционной в данной области, или так называемой косупрессии для той же цели.
Если hpРНК-индуцированное PTGS регуляторов транскрипции генов основных запасных белков, таких как гордеины в ячмене, может быть достигнуто, не влияя при этом на уровни экспрессии регуляторов транскрипции конкретного промотора, запускающего трансген, кодирующий интересующий гетерологичный белок, то конкуренция за ограниченные ресурсы для трансляции может быть уменьшена в пользу мРНК, кодирующей интересующий гетерологичный белок, что приведет к повышенному накоплению конкретного интересующего гетерологичного белка.
Задача настоящего изобретения состоит в том, чтобы предложить способы супрессии экспрессии регуляторов транскрипции генов основных запасных белков и, таким образом, уменьшения уровней экспрессии указанных генов запасных белков, не влияя на активность конкретного промотора, запускающего экспрессию интересующего трансгена, кодирующего гетерологичный белок, продуцируемый в растении.
В первом аспекте изобретения предложен способ усиления экспрессии и накопления интересующего гетерологичного полипептида в семенах растений, включающий:
(а) трансформацию растительной клетки последовательностью ДНК для специфического для семян промотора, функциональным образом связанного с последовательностью ДНК, кодирующей один или более чем один регулятор транскрипции (TF) или его часть(и), включая химерную комбинацию различных TF, регулирующих транскрипцию одного или более эндогенных генов, кодирующих запасные белки семян, причем транскрибированная цепь последовательности ДНК TF способна образовывать "шпилечную" РНК, способную супрессировать, замедлять или иным образом уменьшать экспрессию одного или более запасных белков семян в растительной клетке, и
(б) выбор специфического для семян промотора, который не имеет никаких цис-действующих элементов, распознаваемых регуляторами транскрипции, описанными выше в (а), и
(в) трансформацию той же или другой растительной клетки, описанной в (а), последовательностью ДНК для промотора, описанного в (б), функциональным образом связанного с последовательностью ДНК, кодирующей интересующий гетерологичный полипептид;
(г) регенерацию растения из указанной(ых) трансформированной(ых) растительной(ых) хозяйской(их) клетки(ок), и выращивание растения в условиях, при которых последовательность(и) ДНК, кодирующая(ие) один или более TF или его(их) часть(и), транскрибируется, уменьшая при этом экспрессию эндогенной мРНК, уменьшая таким образом экспрессию запасных белков семян и усиливая таким образом экспрессию и накопление интересующего гетерологичного полипептида.
В полезном варианте осуществления последовательность(и) ДНК из стадии (а) и последовательность ДНК из стадии (в) внедряют в одну и ту же растительную клетку. В таких вариантах осуществления последовательность может быть функциональным образом связана в одну последовательность ДНК.
Однако в других представляющих интерес вариантах осуществления последовательность(и) ДНК из стадии (а) внедряют в геном первой растительной клетки-хозяина, а указанную последовательность ДНК из стадии (в) внедряют в геном второй растительной клетки-хозяина. Первое трансгенное растение затем регенерируют из первой растительной клетки-хозяина, а второе трансгенное растение получают из второй растительной клетки-хозяина, и популяцию потомства трансгенных растений получают из полового скрещивания между первым и вторым трансгенными растениями, причем популяция потомства этих растений имеет клетки, содержащие как последовательность(и) ДНК, кодирующую(ие) один или более TF, так и последовательности ДНК, кодирующие интересующий гетерологичный белок, так что эти растения способны экспрессировать и накапливать указанный гетерологичный белок.
В предпочтительных вариантах осуществления супрессированный запасной белок семян представляет собой гордеин ячменя, например, один или оба гордеина: В-гордеин и С-гордеин.
Последовательность ДНК, кодирующая интересующий гетерологичный полипептид, может представлять собой последовательность ДНК, кодирующую прокариотический или эукариотический белок, который может накапливаться в растительной клетке согласно изобретению. Примеры белков, которые могут быть выбраны для продукции согласно настоящему изобретению, представляют собой коллагены, коллагеназу, гомеобокс полипептиды, моноклональные антитела, секретируемые антитела, одноцепочечные антитела, маннозо-связывающий лектин, пепсин, химотрипсин, трипсин, казеин, гормон роста человека, человеческий сывороточный альбумин, человеческий инсулин, лактоферрин, лизоцимы, целлюлазы, пектиназы, гемицеллюлазы, фитазы, гидролазы, пероксидазы, фибриноген, фактор IX, фактор XIII, тромбин, белок С, ксиланазу, изоамилазу, глюкоамилазу, амилазы, лизоцим, бета-глюканазу, глюкоцереброзидазу, казеины, лактазу, уреазу, глюкозоизомеразу, инвертазу, стрептавидин, эстеразы, щелочную фосфатазу, ингибиторы протеаз, протеазы, папаин, киназы, фосфатазы, дезоксирибонуклеазы, рибонуклеазы, фосфолипазы, липазы, лакказу, белки паутины, антифризные белки, противомикробные пептиды или дефензины, ростовые факторы и цитокинины.
В некоторых вариантах осуществления последовательность ДНК кодирует желательный белок из термофильного организма, такой как, например, углевод-связывающий модуль (carbohydrate binding module, CBM). Примером подходящего СВМ является СВМ9-2 из Thermotoga maritima. Геномная последовательность ДНК, кодирующая СВМ9-2 доступна, имеет регистрационный № в GenBank Z46264 и принадлежит семейству IX СВМ. Согласно изобретению слитые белки, содержащие указанный СВМ или другой подходящий СВМ, также могут кодироваться последовательностью ДНК и сверхэкспрессироваться в семенах. Способы очистки таких СВМ и слитых белков СВМ описаны более подробно в находящихся на совместном рассмотрении международных патентных заявках заявителей настоящего изобретения "Неденатурирующий способ очистки рекомбинантных белков из растений" и "Способ протеолитического расщепления и очистки рекомбинантных белков", поданных одновременно с этой заявкой. Эти патентные документы включены в данное описание путем ссылки во всей их полноте.
В конкретном варианте осуществления указанная последовательность ДНК содержит гомеобокс В4 (НохВ4)-содержащий ген человека, кодирующий белок НохВ4. Белок НохВ4 человека предпочтительно имеет последовательность, обозначенную как SEQ ID NO:1, или последовательность, по существу идентичную последовательности SEQ ID NO:1, так что экспрессирующийся белок предпочтительно имеет все функциональные характеристики нативного белка НохВ4. По существу идентичная последовательность в контексте данного изобретения означает последовательность, идентичную, по меньшей мере, на 50% и более предпочтительно, по меньшей мере, на 60%, такую как последовательность, идентичная, по меньшей мере, на 70%, такую как последовательность, идентичная, по меньшей мере, на 80% и предпочтительно, по меньшей мере, на 90%, такую как последовательность, идентичная, по меньшей мере, на 95% или 99%.
Как изложено в данном изобретении, последовательность ДНК, кодирующая один или более TF или его часть(и), предпочтительно способна образовывать "шпилечную" РНК, способную супрессировать, замедлять или иным образом уменьшать экспрессию одного или более запасных белков семян. Последовательность ДНК может содержать полную последовательность TF, однако в некоторых случаях супрессия будет осуществляться, даже если присутствует только часть последовательности TF. Поэтому в этих вариантах осуществления требуется достаточно длинная часть одной или более последовательностей TF, такая, которая оказывает влияние на супрессию. В некоторых случаях достаточной является часть последовательности TF длиной 20 нуклеотидов, но предпочтительно используют часть, находящуюся в диапазоне, по меньшей мере, 20-500 нуклеотидов, включая примерно 20-200, например, в диапазоне 20-100 или в диапазоне 50-100 нуклеотидов.
В некоторых полезных вариантах осуществления последовательность ДНК, кодирующая один или более TF, представляет собой химерную последовательность ДНК, как определено в данном описании, состоящую из участков двух или более последовательностей ДНК, кодирующих TF или их части. В других полезных вариантах осуществления последовательность ДНК, кодирующая один или более TF в химерной последовательности ДНК, может также включать интронную последовательность, способную образовывать петлю в "шпилечной" РНК.
В предпочтительных вариантах осуществления используют последовательности ДНК, кодирующие TF или его часть, содержащую участок, кодирующий TF или его часть, из группы белков bZIP, более предпочтительно белков bZIP, выбранных из белков BLZ1 и BLZ2 ячменя (см. Onate et al., 1999). Последовательность ДНК может содержать часть последовательности, кодирующей такой белок, достаточной длины для того, чтобы влиять на супрессию, или комбинацию частей последовательностей, кодирующих указанные белки.
Последовательность ДНК предпочтительно содержит последовательность, определенную как SEQ ID NO:2, SEQ ID NO:3, или SEQ ID NO:4, или последовательность, кодирующую белок с последовательностью, по существу идентичной любой аминокислотной последовательности, кодируемой указанными последовательностями, или последовательность с частью последовательности SEQ ID NO:2 или SEQ ID NO:4, имеющей достаточную длину для того, чтобы вызывать супрессию согласно способу настоящего изобретения. Как указано выше, может быть полезна любая комбинация указанных последовательностей, такая как комбинация одной или более частей вышеуказанных последовательностей, пример такой комбинации представлен как SEQ ID NO:5, которая представляет собой химерную последовательность частей BLZ1 и BLZ2.
Другая задача настоящего изобретения состоит в том, чтобы предложить способы применения hpРНК-индуцированной PTGS технологии для супрессии экспрессии регуляторов транскрипции генов основных запасных белков. Поэтому в некоторых вариантах осуществления способов по изобретению используют hpРНК-индуцированную PTGS технологию супрессии экспрессии эндогенных запасных белков и, следовательно, увеличение доступности ресурсов, таких как аминокислоты, сайты связывания рибосом и ансамбль ферментов, участвующих в трансляции и посттрансляционном процессинге, для трансляции мРНК, кодирующей интересующий гетерологичный полипептид. Поэтому в предпочтительных вариантах осуществления последовательность ДНК, кодирующая один или более TF или его(их) часть(и) или их комбинацию, предпочтительно из группы белков bZIP, описанных выше, способных экспрессировать "шпилечную" РНК (hpPHK) в растительной клетке. Последовательность ДНК предпочтительно содержит последовательность, выбранную из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6 или SEQ ID NO:7, SEQ ID NO:8, и любой их части или комбинации, достаточной длины для того, чтобы вызывать супрессию согласно способам, описанным в данном изобретении, т.е. особенно в семенах и/или эндосперме, предпочтительно в таком, как эндосперм ячменя.
Поэтому задача настоящего изобретения состоит в том, чтобы предложить способы и средства в молекулярной биологии для уменьшения уровней В-гордеинов и С-гордеинов в эндосперме ячменя. Более конкретно, задача настоящего изобретения состоит в том, чтобы предложить генные конструкции, содержащие участки генов BLZ1 и BLZ2, способных образовывать hpPHK и, таким образом, позволяющих уменьшать экспрессию указанных генов эндосперма.
Более конкретно, в изобретении предложены генные конструкции участков генов BLZ1 и BLZ2, кодирующих транскрипт, образующий hpPHK, способную к PTGS в эндосперме ячменя.
В предпочтительном варианте осуществления настоящего изобретения способ получения трансгенных растений с пониженным уровнем запасных белков в эндосперме включает: (1) получение клетки однодольного растения, предпочтительно ячменя, способной регенерировать в плодоносящее растение; (2) трансформацию растительной клетки конструкцией нуклеиновой кислоты, содержащей экспрессионную кассету, считываемую в 5'-3'-направлении; специфический для семян, предпочтительно специфический для эндосперма, промотор; последовательность нуклеиновой кислоты, кодирующую регулятор транскрипции, регулирующий эндогенные запасные белки семян; другой специфический для семян, предпочтительно специфический для эндосперма, промотор, который не имеет никаких цис-действующих элементов, распознаваемых регулятором транскрипции, регулирующим ген(ы) запасного(ых) белка(ов), подлежащих супрессии; последовательность нуклеиновой кислоты, кодирующую интересующий гетерологичный полипептид и 3'-нетранслируемый участок; (3) регенерацию растительной клетки с получением первого трансгенного растения, имеющего пониженные уровни регуляторов транскрипции, регулирующих экспрессию запасных белков семян, и имеющего пониженные уровни эндогенных запасных белков.
В объем защиты настоящего изобретения также входят конструкции ДНК для высокоуровневой экспрессии интересующих гетерологичных полипептидов в семенах однодольных растений. Такие конструкции ДНК включают: промотор, который функционирует в данном семени однодольного растения и функциональным образом связан с последовательностью, кодирующей интересующий гетерологичный полипептид; химерную генную конструкцию участков генов BLZ1 и BLZ2, кодирующих транскрипт, способный образовывать hpРНК, способную к PTGS в эндосперме ячменя, функциональным образом связанный с промотором, который функционирует в данном семени однодольного растения.
В другом аспекте изобретения предусмотрены трансгенные растения, такие как, в частности, растения, описанные выше, полученные способами, описанными в данном изобретении. Указанные растения имеют вышеупомянутые желательные характеристики, т.е. супрессируют экспрессию выбранных основных ресурсных белков "стока" для того, чтобы увеличить экспрессию и накопление желательных рекомбинантно полученных белков. Предпочтительные растения согласно изобретению включают растения ячменя, например сорт Hordeum vulgaris, который может быть использован в соответствии с изобретением для экспрессии и накопления гетерологичных белков в семенах. Растения ячменя по настоящему изобретению предпочтительно имеют в своем геноме последовательности, кодирующие предпочтительные TF, описанные в настоящем изобретении, такие как TF или его часть из группы белков bZIP.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг.1 представлен электрофорез общего белка из Hordeum vulgaris, сорт Skegla в полиакриламиде с додецилсульфатом натрия (через 49 дней после опыления) с использованием водной экстракции (дорожка 1), солевой экстракции (дорожка 2) и EtOH экстракции (дорожка 3). Стрелки указывают на В- (нижний) и С-гордеины (верхний).
На Фиг.2 представлен анализ в агарозном геле продуктов ПЦР-амплификации с использованием а) праймеров SEQ ID NO: 9 и SEQ ID NO: 10 (см. Пример 2) и б) праймеров SEQ ID NO: 12 и SEQ ID NO: 13 (Пример 3). Продукты разделяли в 1,0%-ном агарозном геле, окрашивали бромистым этидием и фотографировали под УФ. Маркеры размера слева представляют собой лямбда, разрезанный EcoRI/HindIII. Стрелки указывают на амплифицированные продукты.
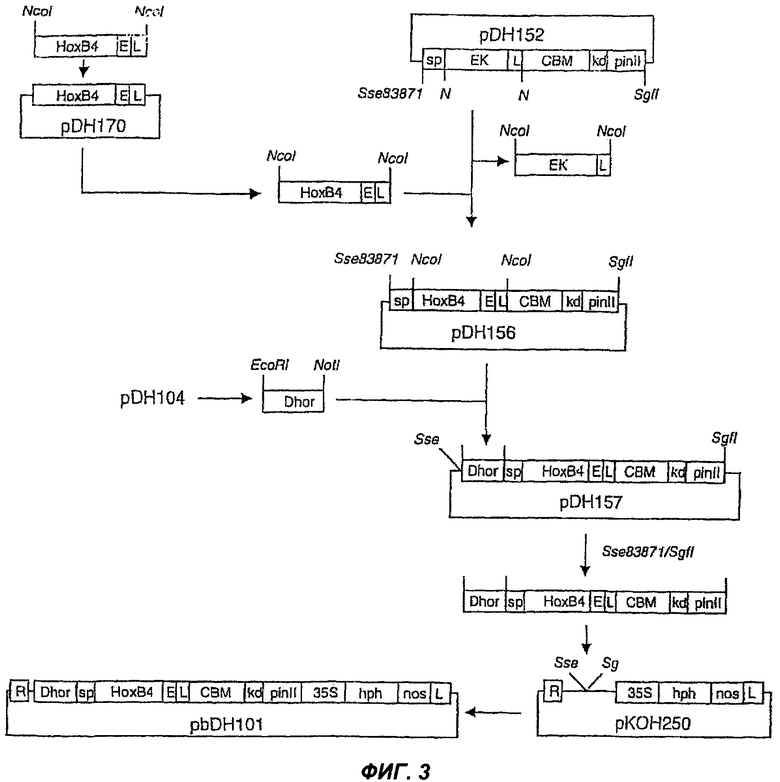
На Фиг.3 проиллюстрировано схематическое представление о клонировании бинарного вектора для трансформации растений pbDH101 для трансформации ячменя кодон-оптимизированным химерным геном НохВ4-СВМ для экспрессии в ткани эндосперма ячменя под контролем D-гордеинового промотора. Сокращения: D-hor, D-гордеиновый промотор; СВМ, кодон-оптимизированный ген, кодирующий углевод-связывающий домен из Thermatoga maritima; HoxB4, кодон-оптимизированный (SEQ ID NO:20); L, линкер (РТРТРТ; Р - пролин, Т - треонин); kd, KDEL последовательность; pinII, сигнал терминации гена ингибитора протеазы II картофеля; CaMV 35S, промотор 35S вируса мозаики цветной капусты; hph, гигромицинфосфотрансфераза из Е.coli (регистрационный № в Genebank K01193); Nos-ter, сигнал терминации гена нопалинсинтазы; R, правый край; L, левый край.
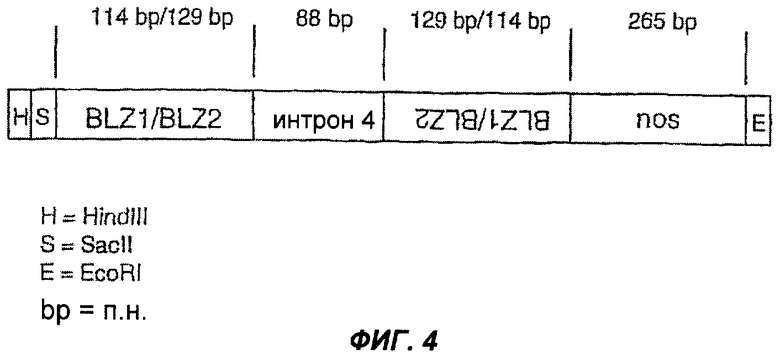
На Фиг.4 представлено схематическое изображение гена, сконструированного для индуцированной шпилечной РНК направленной супрессии BLZ1 и BLZ2 в ячмене под контролем D-гордеинового промотора. BLZ1/BLZ2 длиной 114 п.н. в смысловой ориентации и в антисмысловой ориентации, соответственно, способны образовывать стержневой участок, тогда как интрон 4 длиной 88 п.н. образует петлю в шпилечной петле.
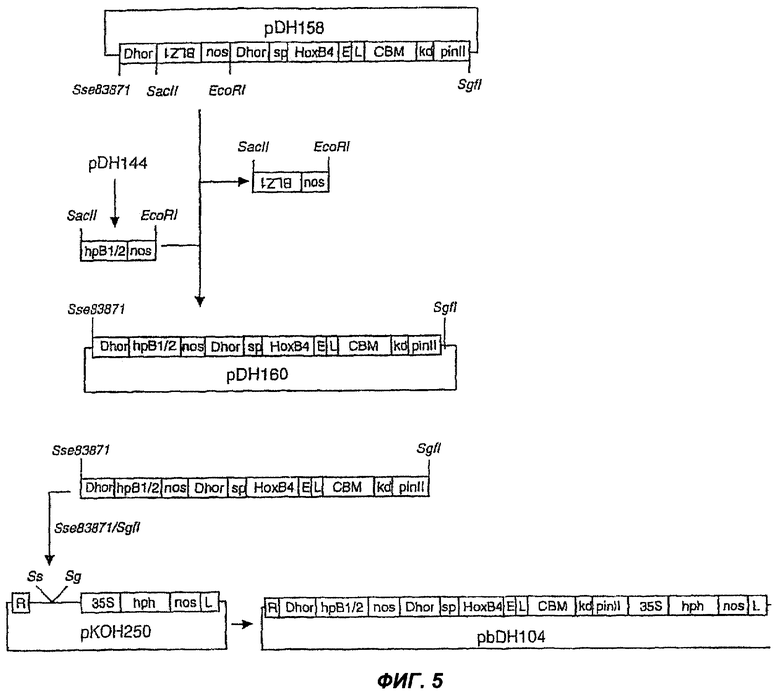
На Фиг.5 схематически проиллюстрировано клонирование бинарного вектора для трансформации растений pbDH104 для трансформации ячменя с hрРНК-индуцированной направленной супрессией BLZ1 и BLZ2 в ткани эндосперма ячменя под контролем D-гордеинового промотора. Сокращения: D-hor, D-гордеиновый промотор; hpВ1/2, супрессорный фрагмент длиной 620 п.н., состоящий из нуклеотидных последовательностей (SEQ ID NO:8), происходящих из BLZ1 и BLZ2; СВМ, кодон-оптимизированный ген, кодирующий углевод-связывающий домен из Thermatoga maritima; HoxB4, кодон-оптимизированный гомеобокс В4-содержащий ген (SEQ ID NO:20); L, линкер (РТРТРТ; Р - пролин, Т - треонин); pinII, сигнал терминации гена ингибитора протеазы II картофеля; CaMV 35S, промотор 35S вируса мозаики цветной капусты; hph, гигромицинфосфотрансфераза из Е.coli (регистрационный № в Genebank K01193); Nos-ter, сигнал терминации гена нопалинсинтазы; R, правый край; L, левый край.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Ниже настоящее изобретение будет описано более подробно.
Термин "белок" используется в данном описании взаимозаменяемо с терминами "полипептид" и "пептид".
Термин "гетерологичный" в данном описании может быть использован взаимозаменяемо с термином "ненативный" или "чужеродный", или "экзогенный", и относится к белкам и/или модифицированным in vitro последовательностям ДНК, которые в норме не обнаруживаются в организмах хозяев, которые не были подвергнуты генетической манипуляции, включающей технологию рекомбинантных ДНК. Используемый в данном описании термин "интересующий гетерологичный полипептид" или "интересующий полипептид" относится к любому полипептиду, предназначенному для экспрессии в организме хозяина с использованием способов или композиций по настоящему изобретению. В качестве неограничивающих примеров согласно настоящему изобретению могут быть получены фармакологические полипептиды (например, для медицинских применений) или промышленные полипептиды (например, ферменты).
Термин "кодирующая последовательность" относится к нуклеотидной последовательности, кодирующей специфическую аминокислотную последовательность.
"Промотор" определяется как совокупность контролирующих последовательностей нуклеиновой кислоты или сайтов связывания регуляторов транскрипции, которые направляют транскрипцию функциональным образом связанной нуклеиновой кислоты. Промотор относится к последовательности нуклеиновой кислоты, контролирующей экспрессию кодирующей последовательности или функциональной РНК. Термин "функциональным образом связанный" относится к функциональной связи между промотором (последовательностью, контролирующей экспрессию нуклеиновой кислоты, или совокупностью сайтов связывания факторов транскрипции) и второй последовательностью нуклеиновой кислоты, где промотор направляет транскрипцию нуклеиновой кислоты, соответствующей второй последовательности.
"Регуляторы транскрипции" или "факторы транскрипции" относятся к трансдействующим регуляторным белкам, которые могут связываться с цис-действующими элементами, также называемыми цис-действующими мотивами, которые представляют собой короткие последовательности ДНК, расположенные выше генов, или внутри интронов, или ниже стоп-кодона.
Термин "эндогенный ген" относится к нативному гену в его природном положении в геноме организма.
Термин "химерная комбинация", или "химерный ген", или "гибридный ген" относится к любым двум или более связанным последовательностям ДНК, образующим ген, который не является эндогенным геном, содержащий регуляторные и/или кодирующие последовательности, которые в норме не встречаются вместе в природе. Термин "генная конструкция", или "конструкция ДНК", или "конструкция нуклеиновой кислоты" относится к любым последовательностям ДНК или комбинации последовательностей ДНК, которые собраны вместе с помощью обычных стратегий молекулярной биологии.
Используемый в данном описании термин "экспрессия" относится к биосинтезу генного продукта, включая транскрипцию его смысловой (мРНК), антисмысловой РНК или других РНК-полимеров либо в одно-, либо в двухцепочечную форму, являющуюся результатом катализируемой РНК-полимеразой транскрипции последовательности ДНК. Экспрессия может также относиться к трансляции мРНК указанного гена в полипептид.
Термин "трансформация" относится к переносу молекулы нуклеиновой кислоты в геном организма-хозяина, приводящему к генетически стабильному наследованию. Организмы-хозяева, содержащие трансформированные фрагменты нуклеиновой кислоты, называются "трансгенными" организмами. Термин "трансгенный" подразумевает, что растительная клетка-хозяин по изобретению содержит, по меньшей мере, одну чужеродную, предпочтительно две чужеродные молекулы нуклеиновой кислоты, стабильно встроенные в геном. Примеры способов трансформации растений включают в себя трансформацию, опосредованную агробактериями (De Blaere et al., 1987), и технологию трансформации с использованием бомбардировки частицами или "генной пушки" ("gene gun") (Klein et al. (1987); патент США №4945050).
Термин "антисмысловое ингибирование" или "антисмысловой", или "антисмысловая супрессия" относится к антисмысловой цепи, достаточно комплементарной эндогенному продукту транскрипции или мРНК, так чтобы трансляция и экспрессия эндогенного продукта транскрипции ингибировалась или уменьшалась. Термин "направленная супрессия" относится к применению технологии рекомбинантных ДНК для конструирования и применения последовательностей ДНК, способных кодировать РНК-транскрипты, способные препятствовать и супрессировать экспрессию эндогенных генов, выбранных для супрессии в некоем заданном живом организме. Термин "супрессорный трансген" относится к любой гетерологичной последовательности ДНК, кодирующей РНК-транскрипты, способные препятствовать и супрессировать экспрессию эндогенных генов. Термин "косупрессия" относится к случаю, когда ген, внедренный в клетку с помощью трансформации и имеющий идентичную или похожую последовательность, как и эндогенный ген в той же клетке, вызывает супрессию как эндогенного гена, так и внедренного гена.
Используемые в данном описании белки "bZIP" относятся к регуляторным белкам, которые содержат домены, известные как основная спираль/лейциновый зиппер ("застежка-молния" от англ. zipper), которые вовлечены в связывание ДНК и димеризацию и которые, как правило, связываются с последовательностями ДНК, содержащими 5'ACGT'3 кор.
Используемый в данном описании термин "гордеины" относится к запасным белкам в ячмене, специфически синтезирующимся в эндосперме. Белки разделены на 4 группы: β-(бета, также названный как В-), D-, С- и гамма-гордеины.
Используемый в данном описании термин "молекулярное фермерство" относится к способу применения растений для производства ценных биологических соединений, таких как белки для дальнейшего процессинга.
В настоящем описании могут быть использованы однодольные растения, с которыми можно осуществлять генетические манипуляции. Предпочтительно, растение представляет собой однодольное растение, более предпочтительными являются ячмень, кукуруза, пшеница, овес и рис. Ячмень имеет много желательных характеристик, делающих его предпочтительным кандидатом для настоящего изобретения, особенно предпочтительным является вид ячменя Hordeum vulgarisis. Растение, которое может быть генетически трансформировано, представляет собой растение, в котором гетерологичная последовательность ДНК, включающая последовательность ДНК для кодирующего участка или последовательность ДНК, кодирующую РНК-транскрипт, способный образовывать hpРНК, может внедряться, экспрессироваться, стабильно поддерживаться и передаваться последующим поколениям потомства. Для производства растений ячменя были использованы способы генетической манипуляции и трансформации, в которых в качестве селективных маркеров используют гербициды, включая, например, биалафос или басту, или антибиотик, такой как гигромицин.
После выбора подходящего растения-хозяина выбирают промотор для запуска экспрессии интересующего гетерологичного гена. В литературе был описан целый ряд промоторов, которые активны в растительных клетках. Предпочтительно, чтобы промоторы, используемые в конструкции ДНК по настоящему изобретению, имели сильную активность в тканях, в которых желательно накопление интересующего гетерологичного полипептида, таких как эндосперм семян однодольных растений. Более предпочтительно, чтобы выбранный промотор не регулировался регуляторами транскрипции, которые являются мишенями для супрессии с помощью способа по изобретению, такими как регуляторы транскрипции, которые регулируют экспрессию генов эндогенных запасных белков, которые конкурируют за ресурсы с экспрессией интересующего гетерологичного гена. Такие промоторы могут быть получены из разного растительного генетического материала или из вирусов растений. Как описано ниже, предпочтительно, чтобы конкретный выбранный промотор был подходящим для экспрессии гетерологичного белка в семенах однодольных растений, более предпочтительно в ячмене и еще более предпочтительно в ткани эндосперма семени. Клонирование и анализ такого подходящего промотора, полезного для изобретения, описан в Примере 2.
Еще более предпочтительно, чтобы была проанализирована картина экспрессии белкового профиля в ткани-мишени, выбранной для накопления интересующего гетерологичного белка, и большинство распространенных запасных белков, идентифицированных для направленной супрессии согласно изобретению. Анализ может основываться на предшествующем уровне техники, например, данных, собранных на основе опубликованной литературы. Он может также включать одновременно мониторинг картин экспрессии тысяч генов с помощью подхода микромассивов (micro array approach) с использованием мРНК, экстрагированной из указанной ткани в моменты времени, которые перекрывают профиль временной экспрессии промотора, выбранного для запуска экспрессии гетерологичного белка, или с использованием Нозерн-блоттинга (Northern blot analysis), ОТ-ПЦР и/или Вестерн-блоттинга. На основании накопленной информации для направленной супрессии согласно изобретению выбирают кандидатные гены с высокой экспрессией, конкурирующие во времени и в пространстве с экспрессией интересующего гетерологичного гена.
Рекомбинантная плазмида по изобретению может быть получена путем лигирования (вставки) интересующей последовательности ДНК в подходящую плазмиду, которая реплицируется в бактериальном хозяине. Последовательности ДНК, такие как ген, кодирующий интересующий гетерологичный белок, или последовательности ДНК, сконструированные для направленной супрессии эндогенных генов, должны быть предпочтительно функциональным образом включены в плазмиду, которая может содержать помимо промотора для этой цели, и если желательно, дополнительные энхансерные последовательности ДНК, участки прикрепления к клеточному каркасу (scaffold), интроны, поли(А)-дополнительный сигнал, последовательность связывания рибосом и ген интересующего селективного маркера, такой как ген устойчивости к гигромицину, ген устойчивости к ампициллину, ген устойчивости к биалафосу или тому подобное.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Следующие примеры предназначены для того, чтобы лучше охарактеризовать настоящее изобретение и служить руководством для специалистов в данной области по осуществлению настоящего изобретения. Если не указано иначе, термины следует понимать в соответствии со стандартным их применением специалистами в релевантной области.
СПОСОБЫ
Экстракция РНК и Нозерн-блоттинг
Общую РНК выделяют, используя TRIzol (Gibco BRL) в соответствии с инструкциями производителя, и 10 мкг общей РНК на дорожку подвергают электрофорезу и переносят на мембрану Hybond N (Amersham) путем капиллярного действия. РНК сшивают с мембраной, используя Stratolinker (Stratagene), и этот фильтр подвергают гибридизации в строгих условиях и промывке, как описано (Davis et al., 1994). Зонды метят радиоактивным изотопом 32P с помощью случайного праймирования (Т7 QuickPrime Kit®; Pharmacia) в соответствии с инструкциями производителя. Негативные цифровые изображения EtBr-окрашенных блотов используют в качестве контролей нагрузки.
Трансформация ячменя
а) Растительный материал для генетической трансформации
Семена Hordeum vulgare сорта Golden Promise высевали на смесь 75% торфа из светлого сфагнума и 25% пемзы (средний размер гранул), и растения росли при 18°С днем (16 часов) и 12°С ночью (8 часов) и 70% относительной влажности под 250 мкмоль м-2 с-1 постоянного освещения в течение дня при холодной белой флуоресценции и орошении по мере необходимости водой. В этих условиях растения росли вегетативно в течение примерно 55-95 дней или до тех пор, пока незрелые семена не были подготовлены в качестве материала для трансформации, что составляло примерно 8-14 дней после опыления. Семена стерилизовали в 3%-ном гипохлорите натрия в течение 40 мин в ротационном шейкере и промывали пятью сменами стерильной воды.
б) Бактериальные штаммы и их получение для трансформации растений
Agrobacterium tumefaciens, содержащий бинарный вектор в транс с Ti-плазмидой, обладающей vir участком, используют для внедрения в ячмень участка Т-ДНК вместе с конструкцией ДНК, регулирующей экспрессию интересующего гетерологичного белка. Трансформацию бактерий, таких как Е.coli XL-Blue и Agrobacterium tumefaciens осуществляют путем электропорации, как описано Maniatis и др. в Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1982). Для трансформации растения одну колонию агробактериальной культуры инокулируют в 5 мл среды Agro (5 г/л триптона, 2,5 г/л дрожжевого экстракта, 5 г/л маннита, 1 г/л глутаминовой кислоты, 250 мг/л KH2PO4, 100 мг/л MgSO4·7H2O, 1 мкг/л биотина, рН 7,0, 25 мкг/мл рифампицина, 50 пг/мл спектиномицина) и выращивают в течение 24-40 часов при 27°С. В стерильных пробирках "эппендорф" 200 мкл культуры добавляют к 200 мкл 30%-ного водного глицерина (предварительно стерилизованного), и культуру хорошо встряхивают и оставляют на 2 часа перед дальнейшем хранением при -80°С. Для каждой трансформации одну пробирку извлекают из морозильной камеры на -80°С, оттаивают и приблизительно 200 мкл исходной массы агробактерий добавляют к 5 мл среды Agro без антибиотика. Культуру затем выращивают в течение 17-20 часов при 27°С перед тем, как использовать для инокуляции растительного материала (см. ниже).
в) Получение эксплантов ячменя для трансформации, индуцированной агробактериями
В первый день отбирают приблизительно 10 колосьев ячменя приблизительно через 8-14 дней после опыления, ости и семена удаляют и отбирают зародыши размером от 1,5 мм до 2 мм. Необходимо, чтобы исходный растительный материал был здоровым и зрелым и не содержал избытка воды, а семена должны быть зелеными без каких-либо признаков болезни или грибков. Семена помещали в 50 мл конусовидную пробирку (заполненную не более чем наполовину) и промывали 70%-ным этанолом, и этанол затем сливали. Затем добавляли 20% обесцвечивающего раствора (White King) и перемешивали в течение 20 минут. В ламинарном боксе обесцвечивающий раствор сливали, семена промывали стерильной водой (примерно 5-8 промывок), и пробирку выдерживали при 4°С в течение ночи. Во второй день семена помещали в стерильную чашку Петри на столик микроскопа. Определяли местоположение зародыша, отрезали конец семени и делали надрез сбоку семени. Затем семя крепко фиксировали пинцетом и надавливали на середину семени так, что зародыш выталкивался. Зародыш удерживали на месте пинцетом, и лезвие скальпеля вставляли в желобок между щитком и зародышевой осью, и эту ось медленно вырезали. Зародыш без оси помещали в регенерационную среду, разрезали сбоку, в центр чашки Петри с приблизительно 25 зародышами на планшет.
г) Полный бинарный вектор размножали в E.coli XI-Blue культуральной среде LB, содержащей 100 мкг/мл спектиномицина, при 37°С, и этот вектор затем очищали из 100 мл культуры, росшей в течение ночи, используя набор QIAGEN® Plasmid Midi Kit. Очищенный бинарный вектор внедряли в Agrobactehum tumefaciens путем электропорации, помещая 1 мкл (1 мкг) вектора в стерильную кювету с 0,1 см щелью (BioRad), промывая вектор 40 мкл электрокомпетентных клеток и устанавливая напряжение 2,5 кВ и емкость 21 мкФ для электропорации. Клетки распределялись на селекционных планшетах YEP, содержащих 100 мкг/мл спектиномицина и 20 мкг/мл рифампицина, росли при 28°С в течение 2 дней. Затем проводили рестрикционный анализ плазмиды из трансформантов A. tumefaciens, чтобы проверить интактность бинарного вектора.
д) Заражение эксплантов ячменя агробактериями
Приблизительно 20 мкл культуры агробактерий наносили пипеткой на каждый зародыш, обеспечивая контакт всех зародышей с раствором. Зародыши переворачивали (разрезанной стороной вниз) и медленно протаскивали через регенерационную среду за пределы планшета, удаляя избыток агробактерий. Затем зародыши переносили в планшеты со свежей регенерационной средой (разрезанной стороной вверх), располагая их равномерно относительно друг друга (25 на планшет), и помещали в темный шкаф при 24°С.
е) Регенерация и органогенез в тканевой культуре ячменя после заражения агробактериями
Через три дня зародыши переносили в свежую регенерационную среду с селективным маркером, таким как биалафос или гигромицин, и оставляли в ней на четыре-шесть недель, пересевая каждые две недели. Для регенерации побегов каллусы переносили в среду для индукции роста побегов (SIM), и выживший каллус и регенерирующие побеги переносили в свежую среду SIM каждые две недели до тех пор, пока не сформируются маленькие проростки. Затем проростки переносили в среду для индукции роста корней (RIM), и выжившие растения высаживали в почву для последующего скрининга.
Экстракция ДНК, ПЦР и клонирование
Геномную ДНК для ПЦР-амплификации экстрагировали из примерно 200 мг молодой листовой ткани с использованием набора NucleoSpin Plant Kit® от фирмы Clonetech и в соответствии с инструкциями производителя. Реакции ПЦР осуществляли в термоциклере Пельтье (MJ Research, PTC-200) с нагретой крышкой. Все праймеры были синтезированы химически с помощью полностью автоматизированного синтезатора ДНК (Perkin-Elmer). Все фрагменты ДНК разделяли по размеру в 1%-ном, окрашенном EtBr, агарозном геле под УФ светом и очищали, используя набор QIAquick® Gel Extration Kit (Qiagen). Рестрикционные ферменты получали от фирм New England Biolabs Inc (Beverly, Mass.) и Fermentas и использовали в соответствии с инструкциями производителя. Клонирование и другие манипуляции с ДНК осуществляли согласно стандартным процедурам, как описано у Maniatis и др. в Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1982), но во всех реакциях лигирования использовали следующие условия: Т4 ДНК-лигаза (2,5 ед.) в буфере [50 мМ Трис-HCl (рН 7,6), 5 мМ MgCl2, 1 мМ ДТТ, 0,5 мМ АТФ, 2,5% полиэтиленгликоль-8000] при 16°С в течение 16 часов. Компетентный штамм Escherichia coli XL-Blue использовали в качестве реципиента в экспериментах по трансформации для манипуляций с ДНК и конструирования плазмидных клонов. Весь миди-препарат плазмидной ДНК получали, используя набор Qiagen® Plasmid Midi Kit (Qiagen), и секвенирование фрагментов ДНК осуществляли с использованием автоматизированного секвенирования ДНК (ABI, Pharmacia).
Пример 1
Анализ белков "стока" в эндосперме Hordeum vulciaris
Анализ экспрессии белков в семенах Hordeum vulgahs сорта Skegia может быть осуществлен с использованием ПААГ с ДСН (полиакриламидного геля с додецилсульфатом натрия) белков, экстрагированных из семян, собранных на 49-й день после опыления (дпо), для идентификации тех экспрессирующихся в эндосперме белков, которые вносят основной вклад в общий уровень белка в эндосперме, и, следовательно, потенциального кандидата для направленной супрессии. Целые семена из пяти осей ячменя вручную тонко измельчали в жидком азоте перед добавлением подходящего экстрагирующего буфера. На обоих образцах использовали два вида экстрагирующих буферов, в дополнение к водной экстракции. Во-первых, экстракцию общих белков осуществляли в восстанавливающих условиях путем этанольной экстракции (70% ЕtOН) в присутствии 1% 2-меркаптоэтанола, 10 мМ Трис-HCl, рН 8,0, и 1% поливинилпирролидина (ММ 360000). Во-вторых, экстракцию общих белков осуществляли в восстанавливающих условиях в присутствии 170 мМ NaCl, 1% 2-меркаптоэтанола, 10 мМ Трис-HCl, рН 8,0, и 1% поливинилпирролидина (MM 360000). После измельчения образца в жидком азоте во флакон для экстракции добавляли 5 мл экстрагирующего буфера с последующим непрерывным измельчением в течение 3 мин. Экстракт осветляли центрифугированием при 4000 об/мин в течение 10 мин при 4°С, с последующим десятикратным цетробежным концентрированием в Ultrafree-4 концентраторах с отсечением молекул с молекулярной массой 5 кДа (UFV4BCC00-Millipore Corp. Bedford, MA, США). Образец 100 мкл осветленного, концентрированного экстракта добавляли к 100 мкл 2х буфера для образцов, и эту смесь помещали в кипящую водяную баню на 5 мин. После охлаждения 10 мкл образца наносили на 12%-ный разделяющий полиакриламидный гель (ПААГ с ДСН). После электрофореза в ПААГ с ДСН гель окрашивали с помощью кумасси голубого R250 и отмывали от красителя для визуализации белковых полос. Результаты показывают, что большинство широко распространенных белков в развивающемся эндосперме в H.vulgare сорта Skegia представляют собой В- и С-гордеины (Фиг.1).
Эти результаты показывают, что супрессия регуляторов транскрипции, которые регулируют гены, кодирующие В- и С-гордеины, является очень перспективной для снижения конкуренции за ресурсы и возможности увеличения накопления экспрессирующегося гетерологичного полипептида в соответствии с изобретением.
Пример 2
Выбор промотора для направленной супрессии В- и С-гордеинов в Hordeum vulgare, используемого в качестве экспрессионного носителя гетерологичных белков
Генные промоторы В-гордеинов (регистрационный № в GenBank X53690) и С-гордеинов (регистрационный № в GenBank M36941) содержат 100% индентичных цис-действующих элементов, идентифицированных в обоих из них, которые участвуют в регуляции их транскрипции (Muller and Knudsen, 1993; Vicente-Carbajosa et al., 1992). Эти цис-элементы находятся внутри так называемого эндосперм-бокса (ЕМ), расположенного примерно на 300 п.н. выше стартового кодона трансляции. ЕМ содержит два различных цис-действующих мотивов для связывания транскрипционных факторов: проламин-бокс (РВ) 5'-TGTAAAG-3' и GСN4-подобный мотив (GLM) 5'-(G/A)TGA(G/C)TCAT-3'. GLM распознается двумя транскрипционными факторами, BLZ1 (регистрационный № в GenBank X80068) и BLZ2 (регистрационный № в GenBank X80068). После связывания активируется транскрипция конкретного гена (см. Onate et al., 1999). Оба эти гена являются однокопийными генами и, следовательно, хорошими кандидатами для направленной супрессии, описанной в этом изобретении. Vicente-Carbajosa и др. (1998) исследовали их антисмысловую супрессию в системе временной экспрессии без изучения влияния на стабильно трансформированные растения или на накопление запасных белков. Кроме того, не исследовалось влияние такой супрессии на накопление гетерологичных белков в той же ткани. Важным критерием при конструировании направленной супрессии согласно изобретению является то, что промотор, запускающий трансген, кодирующий интересующий гетерологичный белок, не должен содержать цис-действующие мотивы, распознаваемые конкретным регулятором транскрипции, отвечающим за экспрессию запасных белков, подлежащих супрессии. Поскольку В- и С-гордеины содержат GLM, распознаваемый BLZ1 и BLZ2, В- и С-гордеиновые промоторы не могут быть использованы для запуска экспрессии гетерологичного трансгена, кодирующего желательный гетерологичный белок. Другим важным критерием является то, что промотор, запускающий супрессорный трансген, сам запускается тканеспецифическим, например эндосперм-специфическим, промотором, так что экспрессия регуляторов транскрипции в других тканях, где они могут быть необходимы, не должна затрагиваться. Это важно, так как многие транскрипционные факторы, такие как BLZ1 в ячмене, экспрессируются в более чем одной ткани. Еще один критерий состоит в том, чтобы избежать "аутосупрессии" супрессорного трансгена при использовании промотора для запуска супрессорного трансгена, который не имеет цис-действующих элементов, распознаваемых регуляторами транскрипции, подлежащими супрессии по изобретению.
На основании этих критериев был выбран кандидатный промотор для направленной супрессии В- и С-гордеинов.
Выделение, клонирование и анализ D-гордеинового промотора из Hordeum vulgare сорта Skegla
Для амплификации проксимального промоторного участка от -435 до -16 были сконструированы и синтезированы праймеры на основании сайта инициации трансляции D-гордеинового гена, описанного в GenBank последовательности под идентификационным номером Х84368, в качестве смыслового праймера,
5'GGAATTCCEcoRICTTCGAGTGCCCGCCGATTTGCCAGCAATGG (SEQ ID NO: 9), с сайтом рестрикции для EcoRI, введенным на 5'-конце, и в качестве антисмыслового праймера,
5'ATAAGAATGCGGCCGCNotIAATGAATTGATCTCTAGTTTTGTGG (SEQ ID NO: 10), с сайтом рестрикции для NotI, введенным на 5'-конце. Цель введения этих сайтов рестрикции в 5'-конец праймеров состояла в том, чтобы облегчить клонирование амплифицированного фрагмента. Состав реакционного раствора, используемого для амплификации фрагмента длиной 420 п.н., использующего геномную ДНК из Hordeum vulgare сорта Skegia в качестве матрицы, был следующим:
Реакционный раствор тщательно перемешивали, за исключением 9 мкл стерилизованной воды и Taq ДНК-полимеразы, и этот раствор нагревали до 94°С в течение 3 мин, затем охлаждали до 80°С в течение 30 с и добавляли Taq ДНК-полимеразу и 9 мкл стерилизованной воды. Первый цикл ПЦР осуществляли следующим образом: реакционную смесь нагревали до 94°С в течение 30 с, охлаждали до 57°С в течение 30 с для отжига и затем нагревали до 72°С в течение 45 с для удлинения. Последующие 30 циклов осуществляли следующим образом: тепловая денатурация при 94°С в течение 30 с, отжиг при 62°С в течение 30 с и удлинение при 72°С в течение 45 с. После завершения 30 циклов реакционную смесь нагревали до 72°С в течение 4 мин. Амплифицированный фрагмент длиной 420 п.н. (Фиг.2а) расщепляли с помощью EcoRI/NotI и затем лигировали в I сайт EcoRI/NotI вектора рКОН122 с получением рекомбинантной плазмиды pDH104. Затем определяли нуклеотидную последовательность ДНК-вставки длиной 420 п.н. (SEQ ID NO:11). Согласно последовательности D-гордеиновый промотор не содержит GLM и, следовательно, супрессия В- и С-гордеинов во время направленной супрессии либо BLZ1, либо BLZ2 (см. обсуждение выше) не будет влиять на активность D-гордеинового промотора и, следовательно, экспрессию интересующего гетерологичного белка. Кроме того, поскольку D-гордеиновый промотор является чрезвычайно специфическим для эндосперма, этот промотор полезен для запуска супрессорного трансгена, сконструированного для супрессии экспрессии BLZ1 и BLZ2.
Так как важно избежать "аутосупрессии" супрессорного трансгена путем использования промотора для запуска супрессорного трансгена, который не имеет цис-действующих элементов, распознаваемых регуляторами транскрипции, подлежащих супрессии согласно изобретению, использование D-гордеинового промотора, который теряет GLM, для запуска супрессорного гена, супрессирующего BLZ1 и BLZ2, не должно вызывать такую "аутосупрессию".
Пример 3
Клонирование участка, кодирующего D-гордеин. и анализ эндогенной экспрессии D-гордеинового гена на уровне мРНК
Смысловой праймер 5'GGAATTCCEcoRiATGGCTAAGCGGCTGGTCCTC (SEQ ID NO:12), и антисмысловой праймер
5'GGAATTCCEcoRiTTGCAATTGGATAGGTCTCTTG (SEQ ID NO:13) были сконструированы для амплификации фрагмента длиной 748 п.н. из кодирующего участка D-гордеинового гена, описанного в GenBank последовательности под идентификационным номером Х84368. Состав реакционного раствора, используемого для амплификации фрагмента длиной 748 п.н. с использованием геномной ДНК из Hordeum vulgare сорта Skegia в качестве матрицы, был следующий:
Реакционный раствор тщательно перемешивали, за исключением 9 мкл стерилизованной воды и Taq ДНК-полимеразы, и раствор нагревали до 94°С в течение 3 мин, затем охлаждали до 80°С в течение 30 с и добавляли Taq ДНК-полимеразу и 9 мкл стерилизованной воды. Первый цикл ПЦР осуществляли следующим образом: реакционную смесь нагревали до 94°С в течение 30 с, охлаждали до 60°С в течение 30 с для отжига и затем нагревали до 72°С в течение 45 с для удлинения. Последующие 30 циклов осуществляли следующим образом:
тепловая денатурация при 94°С в течение 30 с, отжиг при 65°С в течение 30 с и удлинение при 72°С в течение 45 с.После завершения 30 циклов реакционную смесь нагревали до 72°С в течение 4 мин. Амплифицированный фрагмент длиной 748 п.н. (Фиг.26) расщепляли с помощью EcoRI и затем лигировали в EcoRI сайт вектора рКОШ22 с получением рекомбинантной плазмиды pDH136. Затем определяли последовательность ДНК-вставки (SEQ ID NO:14).
Устойчивый уровень мРНК D-гордеинового гена в эндосперме 40 DAP, зародыше 40 DAP, листьях, стебле и корне соответственно анализируют с использованием Нозерн-блоттинга: тотальную РНК выделяют из 200-250 мг растительного материала из различных тканей или частей растения Hordeum vulgare сорта Skegia, разделяют в 1,2%-ном агарозно-формальдегидном геле и переносят посредством блоттинга на мембрану Zeta-Probe (Millipore, Bedford, Mass.) в соответствии с инструкциями поставщика. Блоттинг, гибридизацию и промывку осуществляют, как описано (Davis et al., 1994). Гибридизацию осуществляют с использованием меченного радиоактивным изотопом 32Р, случайно праймированного фрагмента D-гордеинового гена (SEQ ID NO:14) длиной 748 п.н. в качестве зонда.
Пример 4
Клонирование кодон-оптимизированного НохВ4 из эндосперма ячменя в векторе для трансформации растений pbDH101
Кодон-оптимизированный НохВ4 для экспрессии под контролем D-гордеинового промотора в ячмене синтезируют с помощью GeneArt GmbH (Германия), используя информацию об основной последовательности, описанной в GeneBank ID NM_024015, и информацию об использовании кодонов для кодон-оптимизированной экспрессии в эндосперме под контролем D-гордеинового промотора, как описано (см. находящуюся на совместном рассмотрении заявку заявителей настоящего изобретения "Способы высокоуровневой экспрессии полипептидов в растениях с использованием оптимизации кодонов"). Фрагмент длиной 791 п.н. (SEQ ID NO:15) фланкирован сайтами для Ncol (CCATGG) для клонирования и включает последовательность длиной 27 нуклеотидов, кодирующую линкерный сайт расщепления энтерокиназой DDDDKPTPTPT на 3'-конце. Фрагмент НохВ4 лигируют в Ncol/Ncol сайт рКОН122 с получением pDH170. Этот фрагмент затем высвобождают с помощью Ncol и лигируют в Ncol сайт в pDH152, замещая EK-L фрагмент в pDH152 с получением pDH156. Фрагмент D-гордеинового промотора из pDH104 затем лигируют в EcoRI/Notl сайт pDH156 с получением pDH157. Фрагмент D-пpомотор/SP/HoxB4-E-L/CBM/kd/pinll высвобождают с помощью Sse83871/Sfl и лигируют в Sse83871/Sfl сайт рКОН250 с получением вектора для трансформации растений pbDH101 (Фиг.3).
Пример 5
Конструирование вектора для трансформации растений pbDH104 с индуцированной шпилечной РНК направленной супрессией BLZ1 и BLZ2 под контролем D-гордеинового промотора
Ген для направленной супрессии BLZ1 и BLZ2. индуцированной шпилечной РНК, синтезировали с помощью GeneArt GmbH (Германия) как супрессорный фрагмент длиной 592 п.н. с последующим фрагментом nos-сигнала терминации длиной 265 п.н. (SEQ ID NO:8) и клонировали в HindIII/EcoRI сайт в pUC19 с получением pDH144. Фрагмент представляет собой химерную композицию нуклеотидных последовательностей из BLZI-гена (SEQ ID NO:2) и BLZ2-гeнa (SEQ ID NO:4), образующих смысловые и антисмысловые участки, и нуклеотидную последовательность длиной 88 п.н., представляющую собой интрон 4 из BLZ1 гена (последовательность в GenBank, идентификационный номер Х80068), сконструированную для образования шпилечной петли РНК после транскрипции (Фиг.4). Фрагмент 857 п.н. hpB1/2-nos высвобождали с помощью SacII/EcoRI и замещения антисмыслового BLZI-nos фрагмента в pDH158 с получением pDH160. Полную вставку в pDH160 высвобождали с помощью расщепления Sse83871/Sgfl и лигировали в Sse83871/Sgfl сайт рКОН250 с образованием бинарного вектора для трансформации растений pbDH104 (Фиг.5), способного к стабильной интеграции последовательности ДНК между левыми границами (L) и правыми границами (R) вектора в растительный геном.
Пример 6
Генетическая трансформация ячменя с помощью векторов pdDH101 и pDН104
Незрелое семя Hordeum vulgaris сорта Golden Promise получают примерно через 8-14 дней после опыления и хранят в течение ночи при 4°С в темноте. Выдержанное на холоду незрелое семя обрабатывают в 70%-ном EtOH в течение 1 мин и затем в 0,6%-ном гипохлориде натрия в течение 10 мин с последующей тщательной промывкой (5-8 раз) в стерильной дистиллированной воде и помещают в стерильную чашку Петри под препарирующий микроскоп в ламинарном боксе в стерильных условиях. Определяли местоположение зародыша, отрезали конец семени и делали надрез сбоку семени. Затем семя крепко фиксировали пинцетом и надавливали на середину семени так, что зародыш выталкивался. Зародыш удерживали на месте пинцетом, и лезвие скальпеля вставляли в желобок между щитком и зародышевой осью, и эту ось медленно вырезали. Щиток помещали в среду для индукции каллуса, разрезали сбоку и инокулировали 25-40 мкл концентрированной массы Agrobacterium tumefaciens, несущих вектор для трансформации растений, в течение 1-5 минут. После инокуляции щиток вытаскивали из чашки для того, чтобы уменьшить бактериальную нагрузку и снизить чрезмерный рост во время фазы сокультивирования. Инфицированный щиток переносили в новый планшет со средой для индукции каллуса, и этот планшет инкубировали при 24°С в темноте в течение 3 дней. Через 3 дня щиток переносили в новую среду для индукции каллуса, но с 100 мкг/мл тиментина для уничтожения агробактерий и 50 мкг/мл гигромицина для отбора трансформированных клеток, и инкубировали в течение 4 недель в темноте при 24°С, пересевая через 2 недели. Каллус затем переносили в среду для индукции побегов, содержащую 2,5 мг/л ВАР, 50 мкг/мл тиментина и 25 мкг/мл гигромицина, и инкубировали при ярком свете в течение 4-10 недель. Индивидуальные регенерирующие проростки переносили в среду для укоренения (50 мкг/мл тиментина и 25 мкг/мл гигромицина и без гормонов). После развития до приблизительно 5-7 см побегов с корнями трансгенные растения помещали в почву и выращивали в ней при ярком свете.
Пример 7
Накопление белка НохВ4-СВМ после направленной супрессии BLZ1 и BLZ2
Чтобы измерить накопление В- и С-гордеинов в трансгенных растениях, трансформированных либо pbDH101 (только hoxB4-cbm), либо pbDH104 (BLZ1/2 hpРНК экспрессируется с hoxB4-cbm), может быть использован способ с коллоидным красителем - кумасси бриллиантовым голубым G, как описано у Smith (в The Protein Protocols Handbook ed. Walker, 2nd ed., Humana Press, 2002). Растворимые белки из экстрактов семян затем разделяют с помощью ПААГ с ДСН вместе со стандартными белками, затем гель окрашивают в течение 1 часа окрашивающим раствором (0,04% (мас./об.) бриллиантового голубого G в 3,5% (мас./об.) хлорной кислоте), с последующей отмывкой красителя из геля в дистиллированной воде в течение 4 часов. Интенсивность соответствующих В- и С-гордеиновых полос анализируют с помощью сканирующей денситометрии и сравнивают относительную интенсивность полос в трансгенных растениях, трансформированных с помощью pbDH101 или pbDH104. Это дает оценку супрессии В- и С-гордеина, вызванной BLZ1/2 hрРНК. Идентичность и уровень экспрессии НохВ4-СВМ в растениях, трансформированных с помощью pbDH101 или pbDH104, могут быть подтверждены и измерены с помощью Вестерн-блоттинга фрагмента того же геля, содержащего дубликат образцов. Полосы могут быть перенесены посредством электроблоттинга из фрагмента геля на нитроцеллюлозную мембрану с использованием Biorad's Mini transblot Cell, но контуры фрагмента геля отмечали на фильтре до блоттинга. После блоттинга и разборки "сэндвича" гель/мембрана, нитроцеллюлозу гибридизуют с поликлональной антисывороткой против СВМ, и после многократных стадий промывки (2·5 мин, 2·15 мин, 1·5 мин), инкубируют в течение 45 мин со вторым антителом, конъюгированным с пероксидазой хрена (HRP). После дополнительных стадий промывки, описанных выше, и после добавления субстратов 5-бром-4-хлор-3-индолилфосфата и нитросинего тетразолия хлорида к мембране, цветная реакция с HRP положительно идентифицирует полосу как НохВ4-СВМ, а также дает оценку действия экспрессии BLZ1/2 hpРНК на уровень hохВ4-СВМ.
Несмотря на то, что конкретно проиллюстрированы лишь предпочтительные варианты осуществления изобретения, ожидается, что многочисленные модификации и вариации в изобретении, описанные в вышеупомянутых примерах, будут очевидны специалистам в данной области, без отклонения от сущности и обозначенного объема изобретения.
Литература
1. Coles et al. (1999) Plant J. 17:547-556.
2. Davis et al. (1994); In: Basic Methods in Molecular Biology. Norwalk. Connecticut: Appelton and Lenge:350-355.
3. De Blaere et al. (1987) Meth. Enzymol. 143:277.
4. Fire et al. (1998) Nature 391:806-811.
5. Klein et al. (1987) Nature 327:70-73.
6. Maniatis et al. (1982) Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.
7. Muller et al. (1993) Plant 3. 4:343-355.
8. Onate et al. (1999) J. Biol. Chem. 274:9175-9182.
9. Patel et al. (2000) Molecular Breeding 6:113-123.
10. Sanford et al. US Patent №4945050.
11. Shewmaker et al. US Patent №5759829.
12. Shewry et al. (1985) Biochem. Genet. 23:389-402.
13. Smith et al. (2000) Nature 40: 319-320.
14. Sorensen et al. (1996) Mol. Gen, Genet. 250:750-760.
15. Takaiwa et al. (2003) EP patent application EP 1327685 A1
16. Vicente-Carbajosa et al. (1992) Plant Mol. Biol. 18:453-458.
17. Vicente-Carbajosa et al. (2998) Plant J. 13(5):629-640.
18. Waterhouse et al. (1998) Proc. Natl. Acad. Sci. 95:13959-13964.
19. Wesley et al. (2001) Plant J. 27:581-590.
20. Örvar et al. (1997) Plant J. 11:1297-1305.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОМОТОР ЦЕЛОГО СЕМЕНИ | 2010 |
|
RU2561463C2 |
| РЕГУЛЯТОРНЫЕ ЭЛЕМЕНТЫ РАСТЕНИЙ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2639275C2 |
| ЭНХАНСЕР ПАЛОЧКОВИДНОГО ВИРУСА САХАРНОГО ТРОСТНИКА (SCBV) И ЕГО ПРИМЕНЕНИЕ В ФУНКЦИОНАЛЬНОЙ ГЕНОМИКЕ РАСТЕНИЙ | 2013 |
|
RU2639517C2 |
| СЕМЕНА ТРАНСГЕННЫХ РАСТЕНИЙ С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ ЛИЗИНА | 2006 |
|
RU2460281C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2013 |
|
RU2662672C2 |
| ЯЧМЕНЬ С НИЗКИМ СОДЕРЖАНИЕМ ГОРДЕИНОВ | 2008 |
|
RU2518241C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2016 |
|
RU2759224C2 |
| РЕГУЛЯТОРНЫЕ МОЛЕКУЛЫ НУКЛЕИНОВЫХ КИСЛОТ ДЛЯ УСИЛЕНИЯ СЕМЯ-СПЕЦИФИЧНОЙ И/ИЛИ СЕМЯ-ПРЕДПОЧТИТЕЛЬНОЙ ГЕННОЙ ЭКСПРЕССИИ В РАСТЕНИЯХ | 2010 |
|
RU2559534C2 |
| СПОСОБ И КОНСТРУКТ ДЛЯ СИНТЕТИЧЕСКОГО ДВУНАПРАВЛЕННОГО РАСТИТЕЛЬНОГО ПРОМОТОРА SCBV | 2012 |
|
RU2627595C2 |
| РЕГУЛЯТОРНЫЕ МОЛЕКУЛЫ НУКЛЕИНОВЫХ КИСЛОТ ДЛЯ УСИЛЕНИЯ СЕМЯ-СПЕЦИФИЧНОЙ И/ИЛИ СЕМЯ-ПРЕДПОЧТИТЕЛЬНОЙ ГЕННОЙ ЭКСПРЕССИИ В РАСТЕНИЯХ | 2010 |
|
RU2692924C2 |










Экспрессию эндогенных запасных белков в семенах растений подавляют посредством трансформации растительной клетки генетическим конструктом, содержащим семя-специфичный промотор, функционально связанный с последовательностью ДНК, кодирующей факторы транскрипции эндогенных генов или части этих факторов, включая их различные комбинации. Транскрибированная цепь упомянутой последовательности способна супрессировать, замедлять или иным образом уменьшать экспрессию запасных белков семян в растительной клетке. Далее эту или другую растительную клетку трансформируют конструктом, содержащим такой же самый семя-специфичный промотор, функционально связанный с последовательностью ДНК, кодирующей представляющий интерес гетерологичный полипептид. В регенерированном из указанной клетки растении уменьшается экспрессия эндогенной мРНК, что способствует накоплению в этом растении гетерологичного полипептида. 2 н. и 23 з.п. ф-лы, 5 ил.
1. Способ усиления экспрессии и накопления интересующего гетерологичного полипептида в семенах растений, включающий
(а) трансформацию растительной клетки последовательностью ДНК специфичного для семян промотора, функциональным образом связанного с последовательностью ДНК, кодирующей один или более регуляторов транскрипции (TF) или его (их) часть (части), включая химерную комбинацию различных TF, регулирующих транскрипцию одного или более эндогенных генов, кодирующих запасные белки семян, причем транскрибированная цепь указанной последовательности способна супрессировать, замедлять или иным образом уменьшать экспрессию одного или более запасных белков семян в растительной клетке, и
(б) выбор специфичного для семян промотора, который не имеет никаких цис-действующих элементов, распознаваемых регуляторами транскрипции, указанными на стадии (а), и
(в) трансформацию той же или другой растительной клетки, используемой на стадии (а), последовательностью ДНК указанного специфичного для семян промотора, выбранного на стадии (б), функциональным образом связанного с последовательностью ДНК, кодирующей интересующий гетерологичный полипептид;
(г) регенерацию растения из клетки-хозяина (клеток-хозяев) трансформированного растения и выращивание растения в условиях, при которых последовательность (последовательности) ДНК, кодирующая (кодирующие) один или более TF или его (их) часть (части), транскрибируется, уменьшая при этом экспрессию эндогенной мРНК, уменьшая таким образом экспрессию запасных белков семян и усиливая таким образом экспрессию и накопление интересующего гетерологичного полипептида.
2. Способ по п.1, отличающийся тем, что транскрибированная цепь последовательности, кодирующей один или более регуляторов транскрипции (TF) или его часть (части), способна образовывать "шпилечную" РНК, способную супрессировать, замедлять или иным образом уменьшать экспрессию одного или более запасных белков семян в растительной клетке.
3. Способ по п.1, отличающийся тем, что растительная клетка-хозяин выбрана из группы однодольных растений.
4. Способ по п.3, отличающийся тем, что растительная клетка-хозяин выбрана из группы однодольных растений, включающих ячмень, кукурузу, пшеницу, овес и рис.
5. Способ по п.1, отличающийся тем, что выбранный промотор представляет собой D-гордеиновый промотор ячменя.
6. Способ по п.1, отличающийся тем, что последовательность (последовательности) ДНК из стадии (а) и последовательность ДНК из стадии (б) функциональным образом связаны в одну последовательность ДНК.
7. Способ по п.1, отличающийся тем, что последовательность (последовательности) ДНК из стадии (а) и последовательности ДНК из стадии (б) вводят в одну и ту же растительную клетку.
8. Способ по п.1, отличающийся тем, что последовательность (последовательности) ДНК из стадии (а) вводят в геном первой растительной клетки-хозяина, а последовательность ДНК из стадии (б) вводят в геном второй растительной клетки-хозяина.
9. Способ по п.8, отличающийся тем, что первое трансгенное растение регенерируют из первой растительной клетки-хозяина, второе трансгенное растение получают из второй растительной клетки-хозяина, а популяцию потомства трансгенных растений получают в результате полового скрещивания между первым и вторым трансгенным растением.
10. Способ по п.1, отличающийся тем, что один или более чем один запасной белок семян представляют собой гордеин ячменя.
11. Способ по п.1, отличающийся тем, что последовательность ДНК, кодирующая интересующий гетерологичный полипептид, кодирует белок из группы прокариотических или эукариотических белков.
12. Способ по п.11, отличающийся тем, что последовательность ДНК, кодирующая интересующий гетерологичный полипептид, кодирует белок из термофильного организма.
13. Способ по п.11, отличающийся тем, что последовательность ДНК кодирует углевод-связывающий модуль (СВМ).
14. Способ по п.11, отличающийся тем, что последовательность ДНК, кодирующая прокариотический или эукариотический белок, выбрана из группы, состоящей из последовательностей ДНК, кодирующих коллагены, коллагеназу, гомеобокс-полипептиды, моноклональные антитела, секретируемые антитела, одноцепочечные антитела, маннозо-связывающий лектин, пепсин, химотрипсин, трипсин, казеин, гормон роста человека, человеческий сывороточный альбумин, человеческий инсулин, целлюлазы, пектиназы, гемицеллюлазы, фитазы, гидролазы, пероксидазы, фибриноген, фактор IX, фактор XIII, тромбин, белок С, ксиланазу, изоамилазу, глюкоамилазу, амилазы, лизоцим, бета-глюканазу, глюкоцереброзидазу, казенны, лактазу, уреазу, глюкозоизомеразу, инвертазу, стрептавидин, эстеразы, щелочную фосфатазу, ингибиторы протеаз, папаин, киназы, фосфатазы, дезоксирибонуклеазы, рибонуклеазы, фосфолипазы, липазы, лакказу, белки паутины, антифризные белки, противомикробные пептиды или дефензины, ростовые факторы и цитокинины.
15. Способ по п.14, отличающийся тем, что последовательность ДНК, кодирующая эукариотический белок, представляет собой гомеобокс В4 (НохВ4)-содержащий ген человека, кодирующий белок НохВ4.
16. Способ по п.15, отличающийся тем, что НохВ4 белок имеет последовательность, по меньшей мере, на 70% идентичную аминокислотной последовательности SEQ ID NO:1.
17. Способ по п.1, отличающийся тем, что последовательность ДНК, кодирующая один или более TF, представляет собой химерную последовательность ДНК, состоящую из участков двух или более последовательностей ДНК, кодирующих TF или его части.
18. Способ по п.1, отличающийся тем, что последовательность ДНК, кодирующая TF или его часть, содержит участок, кодирующий TF или его часть из группы bZIP белков.
19. Способ по п.18, отличающийся тем, что последовательность ДНК, кодирующая bZIP белок, содержит последовательность ДНК, выбранную из:
(а) последовательности ДНК, кодирующей BLZ1 белок ячменя или его часть;
(б) последовательности ДНК, кодирующей BLZ2 белок ячменя или его часть;
(в) комбинации (а) и (б).
20. Способ по п.19, отличающийся тем, что последовательность ДНК выбрана из SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5 и любой их части или комбинации.
21. Способ по п.1, отличающийся тем, что последовательность ДНК, кодирующая TF, способна экспрессировать шпилечную РНК (hpPHK) в растительной клетке.
22. Способ по п.21, отличающийся тем, что последовательность ДНК, кодирующая TF, содержит участок или его часть, кодирующий TF из группы bZIP белков.
23. Способ по п.22, отличающийся тем, что bZIP белок выбран из BLZ1, BLZ2 и химерной комбинации BLZ1 и BLZ2.
24. Способ по п.23, отличающийся тем, что последовательность ДНК содержит последовательность, выбранную из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, или SEQ ID NO:7, SEQ ID NO:8 и любой их части или комбинации.
25. Трансгенное растение ячменя, имеющее в своем геноме:
а) последовательность ДНК, кодирующую специфичный для семян промотор, функциональным образом связанный с последовательностью ДНК, кодирующей один или более регуляторов транскрипции (TF) или его (их) часть (части), включая химерную комбинацию различных TF, регулирующих транскрипцию одного или более эндогенных генов, кодирующих запасные белки семян,
б) специфичный для семян промотор, который не имеет никаких цис-действующих элементов, распознаваемых указанными регуляторами транскрипции, функциональным образом связанный с последовательностью ДНК, кодирующей интересующий гетерологичный белок,
причем растение экспрессирует в своих семенах гетерологичный белок и экспрессирует, по существу, меньше запасных белков семян, чем соответствующее нерекомбинантное растение.
| Узел соединения высокочастотных коаксиальных кабелей | 1985 |
|
SU1312672A1 |
| ЕР 1327685 А, 16.07.2003 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| WO 00/77174 A, 21.12.2000 | |||
| JOURNAL OF BIOLOGICAL CHEMISTRY, vol.274, no.14 (1999), p.9175-9182. | |||
Авторы
Даты
2009-11-20—Публикация
2004-08-27—Подача