Данное изобретение касается предоставления средств и способов экспрессии генов. В частности, изобретение касается полинуклеотида, содержащего контролирующую экспрессию последовательность, которая делает возможной семя-специфическую экспрессию представляющей интерес нуклеиновой кислоты, функционально связанной с ней, в растениях. Более того, предложены векторы, клетки-хозяева, трансгенные растения и способы экспрессии представляющих интерес нуклеиновых кислот, которые основаны на указанном полинуклеотиде.
Получение трансгенных растений является основной техникой в биотехнологии растений и, следовательно, необходимым условием для фундаментального исследования растений, а также для получения растений с улучшенными новыми качествами для сельского хозяйства, для улучшения качества продуктов питания человека, либо для производства определенных химических препаратов или лекарственных средств. Основным условием для трансгенной экспрессии определенных генов в растениях является предоставление специфических для растений промоторов. Известны различные промоторы растений. Конститутивные промоторы, преимущественно используемые в настоящее время в растениях, в основном, представляют собой вирусные промоторы или промоторы, изолированные от агробактерий, такие как промотор вируса мозаики цветной капусты CaMV355 (Odell et al. (1985) Nature 313:810-812). Так как концепции производства и трансгенные механизмы действия становятся все сложнее, конститутивная экспрессия больше не является оптимальным желаемым образцом экспрессии. Например, в то время как манипуляция стрессиндуцируемых генов может играть важную роль в увеличении устойчивости растений к стрессам, было показано, что конститутивная экспрессия стрессиндуцируемых генов оказывает сильное отрицательное воздействие на рост растения и его развитие, в случае отсутствия стресса (Kasuga et al, (1999) Nature Biotechnology 17(3): 287-291). Поэтому желательны промоторы, управляющие экспрессией, которая является временной и/или пространственно-дифференцированной.
В зерновых культурах агрономической важности образование семян является основной целью развития растения. Семена собирают для использования в пищу, корм, а также для промышленной продукции. Практичность и ценность данных семян определяется количеством и качеством содержащегося в них белка, масла и крахмала.
Семена однодольных растений могут рассматриваться, как содержащие две основных составляющих: зародыш или эмбрион, который содержит клетки-предшественники растения, которые будут развиваться из семени, и эндосперм, который служит вместилищем питательных компонентов (в частности, накопленные крахмал, белки и масло), которые потребляются во время прорастания семян и раннего развития ростков. Семена двудольных растений содержат, в основном, часть зародыша, так как питательную функцию в развитии двудольных растений выполняют питательные запасы дополнительных семян.
Были определены и охарактеризованы многие промоторы, которые способны управлять трансгенной экспрессией в различных комбинациях пространственных и временных наборов экспрессии. В данной области техники также известны некоторые промоторы, управляющие экспрессией в семенах растения. Известные промоторы управляют экспрессией в частях семян растения либо в целом семени. Например, было показано, что промоторы запасных белков семян управляют ключевой экспрессией в семени. К ним относятся промоторы фазеолинов (US 5,504,200, Bustos М.М. et al., Plant Cell. 1989, 2(9): 839-53), 2S альбумин (Joseffson L.G. et al., J. Biol. Chem. 1987, 262: 12196-12201), легумин (Shirsat A et al., Mol Gen Genet. 1989, 215(2): 326-331), USP (неизвестный белок семени; Bäumlein H, et al., Molecular & General Genetics 1991, 225(3): 459-67) напин (Stalberg K., et al., L. Planta 1996, 199: 515-519), сахароза-связывающий белок (WO 00/26388) или LeB4 (Bäumlein H. et al., Mol Gen Genet 1991, 225: 121-128). Криптический промотор со специфичностью для семенной коробочки был определен в табаке методом «Т-ДНК мечения» (Fobert P.R. et al., Plant Journal 1994, 6(4): 567-77; US 5,824,863; WO 99/53067).
Промоторы семян, которые направляют экспрессию в целом семени, то есть как эндосперм, так и зародыш, описаны только для двудольных растений, а не для однодольных. Единственными доступными промоторами для экспрессии целого семян в однодольных растениях являются конститутивные промоторы, которые выражаются в обеих основных составляющих семян, но также управляют трансгенной экспрессией в большинстве или во всех остальных тканях.
Однако средства и методы для надежно управляемой экспрессии представляющих интерес нуклеиновых кислот в целом семени однодольных растений еще не доступны, но весьма желательны.
Таким образом, техническая проблема, лежащая в основе данного изобретения, может рассматриваться как предоставление средств и методов, которые позволяют удовлетворить вышеуказанным требованиям. Техническая проблема решается вариантами осуществления изобретения, охарактеризованными в формуле изобретения и ниже в данном документе.
Поэтому, настоящее изобретение касается полинуклеотида, содержащего контролирующую экспрессию последовательность, которая делает возможной экспрессию семян представляющей интерес нуклеиновой кислоты в растениях, при этом указанную контролирующую экспрессию последовательность выбирают из группы, включающей:
(a) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, как показано в любой из SEQ ID NO: 1-3;
(b) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая, по меньшей мере, на 80% идентична последовательности нуклеиновой кислоты, показанной в любой из SEQ ID NO: 1-3;
(c) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая при жестких условиях гибридизирует к последовательности нуклеиновой кислоты, как показано в любой из SEQ ID NO: 1-3;
(d) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности, показанной в любой из SEQ ID NO: 4, 6 или 8;
(e) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности, кодирующей аминокислотную последовательность, как показано в любой из SEQ ID NO: 5, 7 или 9;
(f) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности, которая, по меньшей мере, на 80% идентична открытой рамке считывания последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8, где открытая рамка считывания кодирует белок семени;
(g) контролирующую экспрессию последовательность, имеющей последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности, кодирующей аминокислотную последовательность, которая, по меньшей мере, на 80% идентична аминокислотной последовательности, как показано в любой из SEQ ID NO: 5, 7 или 9, где открытая рамка считывания кодирует белок семени;
(h) контролирующую экспрессию последовательность, доступной с помощью 5′ прогулки по геному или термической асимметричной переплетенной полимеразной цепной реакции (TAIL-PCR) на геномной ДНК из первого экзона открытой рамки считывания последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8; и
(i) контролирующую экспрессию последовательность, доступной с помощью 5′ прогулки по геному или TAIL-PCR на геномной ДНК из первого экзона открытой рамки считывания последовательности, которая, по меньшей мере, на 80% идентична открытой рамке считывания последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8, где открытая рамка считывания кодирует белок семени; а также
(j) контролирующую экспрессию и последовательность, доступной с помощью 5′ прогулки по геному или TAIL-PCR на геномной ДНК из первого экзона открытой рамки считывания последовательности, кодирующей аминокислотную последовательность, которая, по меньшей мере, на 80% идентична аминокислотной последовательности, закодированной открытой рамкой считывания, как показано в любой из SEQ ID NO: 5, 7 или 9, где открытая рамка считывания кодирует белок семени;
Используемый в данном документе термин «полинуклеотид» относится к линейной или кольцевой молекуле нуклеиновой кислоты. Предпочтительно он охватывает молекулу ДНК. Полинуклеотид настоящего изобретения характеризуется тем, что он содержит контролирующую экспрессию последовательность, как указано в другом месте в данном описании. В дополнение к контролирующей экспрессии последовательности, полинуклеотид настоящего изобретения предпочтительно далее содержит, по меньшей мере, одну представляющую интерес нуклеиновую кислоту, функционально связанную с контролирующей экспрессию последовательностью и/или, по меньшей мере, один терминирующий кодон или транскрипцию. Поэтому полинуклеотид настоящего изобретения предпочтительно содержит кассету экспрессии для экспрессии, по меньшей мере, одной представляющей интерес нуклеиновой кислоты.
Вместо представляющей интерес нуклеиновой кислоты или в дополнение к представляющей интерес нуклеиновой кислоте, по меньшей мере, одна кассета экспрессии может также содержать сайт множественного клонирования и/или терминирующий кодон для транскрипции. В данном случае, сайт множественного клонирования, предпочтительно, расположенный таким образом, чтобы позволить введение функциональной связи нуклеиновой кислоты в сайт множественного клонирования с контролирующей экспрессию последовательностью. В дополнение к вышеуказанным компонентам, полинуклеотид настоящего изобретения, предпочтительно, может содержать компоненты, требуемые для гомологической рекомбинации, т.е. фланкирующей геномной последовательности из целевого локуса. Однако также рассматривается полинуклеотид, который в основном состоит из указанной контролирующей экспрессию последовательности.
Используемый в настоящем документе термин «контролирующая экспрессию последовательность» относится к нуклеиновой кислоте, способной управлять экспрессией другой нуклеиновой кислоты, функционально с ней связанной, например, представляющей интерес нуклеиновой кислотой, детально рассматриваемой в другом месте данного описания. Контролирующая экспрессию последовательность, как указано в соответствии с настоящим изобретением, предпочтительно содержит последовательность мотивов, которые распознаны и связаны полипептидами, т.е. факторами транскрипции. Указанные факторы транскрипции должны при связывании набирать РНК полимеразы, предпочтительно РНК полимеразу I, II или III, более предпочтительно РНК полимеразу II или III, наиболее предпочтительно РНК полимеразу II. Таким образом, будет инициирована экспрессия нуклеиновой кислоты, функционально связанная с контролирующей экспрессию последовательностью. Следует понимать, что в зависимости от типа подлежащей экспрессии нуклеиновой кислоты, т.е. представляющей интерес нуклеиновой кислоты, экспрессия, как подразумевается в данном документе, может содержать транскрипцию РНК полинуклеотидов из последовательности нуклеиновой кислоты (подходящей, например, для антисмысловых подходов или подходов РНК-интерференции), либо может содержать транскрипцию РНК полинуклеотидов, за которой следует трансляция указанных РНК полинуклеотидов в полипептиды (подходящие, например, для экспрессии генов и подходов производства рекомбинантных полипептидов. Для того чтобы управлять экспрессией нуклеиновой кислоты, контролирующая экспрессию последовательность может быть расположена в непосредственной близости от экспрессии нуклеиновой кислоты, т.е. физически связана с указанной нуклеиновой кислотой на ее 5′ конце. В противном случае, она может быть расположена в физической близости. В последнем случае, однако, последовательность должна располагаться так, чтобы позволить физическое взаимодействие с подлежащей экспрессии нуклеиновой кислотой. Контролирующая экспрессию последовательность, указанная в данном документе, предпочтительно содержит от 200 до 5000 нуклеотидов в длину. Более предпочтительно она содержит от 500 до 2500 нуклеотидов, и наиболее предпочтительно от 1000 до 1500 нуклеотидов. Как указано выше, контролирующая экспрессию последовательность, предпочтительно содержит множество мотивов последовательности, которые необходимы для связывания фактора транскрипции или для предоставления определенной структуры полинуклеотиду, содержащему экспрессию контрольной последовательности. Мотивы последовательности иногда также называют цис-регуляторными элементами и, как указано в данном документе, включают элементы промотора, а также элементы энхансера. Контролирующая экспрессию последовательность настоящего изобретения подходит для экспрессии семени, и таким образом содержит цис-регуляторные элементы, которые могут использовать РНК полимеразы в указанной ткани для функционального связывания транскрипции тканей нуклеиновых кислот с указанной контролирующей экспрессию последовательностью. Предпочтительная контролирующая экспрессию последовательность, включенная в полинуклеотид настоящего изобретения, имеет последовательность нуклеиновой кислоты, как показано в любой из SEQ ID NO: 1-3.
Далее предпочтительно контролирующая экспрессию последовательность, содержащаяся в полинуклеотиде настоящего изобретения, имеет последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8, т.е. является вариантом контролирующей экспрессию последовательности. Следует понимать, что контролирующие экспрессию последовательности могут незначительно различаться своими последовательностями из-за аллельных вариаций. Следовательно, настоящее изобретение также предполагает контролирующую экспрессию последовательность, которая может быть получена из контролирующей экспрессию последовательности, как показано в любой из SEQ ID NO: 1-3. Указанные контролирующие экспрессию последовательности, способны гибридизироваться, предпочтительно в жестких условиях, в расположенные выше последовательности открытых рамок считывания, как показано в любой из SEQ ID NO: 5, 6 или 8, т.е. в контролирующие экспрессию последовательности, как показано в любой из SEQ ID NO: 1-3. Строгие условия гибридизации, как указано в данном документе, предпочтительно представляют собой условия гибридизации в 6 натрий хлорид/цитрат натрия (SSC) при примерно 45°C, с последующим одним или несколькими этапами промывки в 0,2 SSC, 0,1% SDS от 53 до 65°C, предпочтительно при 55°C, 56°C, 57°C, 58°C, 59°C, 60°C, 61°C, 62°C, 63°C, 64°C или 65°C. Специалисту известно, что данные условия гибридизации различаются в зависимости от типа нуклеиновой кислоты и, например, если присутствуют органические растворители, относительно температуры и концентрации буферного раствора. Например, в «стандартных условиях гибридизации» температура различается в зависимости от типа нуклеиновой кислоты от 42°C до 58°C в водном буферном растворе с концентрацией от 0,1 до 5 SSC (pH 7,2). Если в вышеуказанном буферном растворе присутствует органический растворитель, например 50% формамид, температура в стандартных условиях составляет примерно 42°C. Условия гибридизации для ДНК: ДНК гибриды предпочтительно, например, 0,1 SSC и от 20°C до 45°C, предпочтительно от 30°C до 45°C. Условия гибридизации для ДНК: РНК гибриды предпочтительно, например, 0,1 SSC и от 30°C до 55°C, предпочтительно от 45°C до 55°C. Вышеуказанные температуры гибридизации определяются, например, для нуклеиновой кислоты с приблизительно 100 п.о. (пар оснований) в длину и G+С содержание в 50% при отсутствии формамида. Подобные гибридизирующие контролирующие экспрессию последовательности, более предпочтительно, по меньшей мере, на 70%, по меньшей мере, на 80%, по меньшей мере, на 90%, по меньшей мере, на 91%, по меньшей мере, на 92%, по меньшей мере, на 93%, по меньшей мере, на 94%, по меньшей мере, на 95%, по меньшей мере, на 96%, по меньшей мере, на 97%, по меньшей мере, на 98%, или, по меньшей мере, на 99% идентичны контролирующей экспрессии последовательности, как показано в любой из SEQ ID NO: 1-3. Значения процентной идентичности предпочтительно рассчитывают на протяжении всей области последовательности нуклеиновой кислоты. Специалисту доступна серия программ, основанных на различных алгоритмах, для сравнения различных последовательностей. В данном контексте, алгоритмы Нидлмана-Вунша или Смита-Ватермана дают особо достоверные результаты. Для проведения выравнивания последовательностей должна использоваться программа PileUp (J. Mol. Evolution., 25, 351-360, 1987, Higgins 1989, CABIOS, 5: 151-153) или программы Gap и BestFit (Needleman 1970 J. Mol. Biol. 48; 443-453 и Smith 1981, Adv. Appl. Math. 2; 482-489), которая является частью пакета программного обеспечения GCG (Genetics Computer Group, 575 Science Drive, Мэдисон, Висконсин, США 53711 версия 1991). Значения идентичности последовательности, перечисленные выше в процентах (%), должны определяться предпочтительно с использованием программы GAP, на протяжении всей области последовательности, со следующими настройками: Пробел Масса: 50, Длина Масса: 3, Среднее Соответствие: 10,000 и Среднее Несоответствие: 0,000, если не указано иначе, всегда будут использоваться в качестве стандартных настроек для выравнивания последовательности.
Более того, контролирующие экспрессию последовательности, которые предусматривают семя-специфическую экспрессию, могут быть расположены не только выше открытых рамок считывания, имеющих последовательность нуклеиновой кислоты, как показано в любой из SEQ ID NO: 4, 6 или 8. Точнее, контролирующие экспрессию последовательности, которые предусматривают семя-специфическую экспрессию, могут быть расположены не только выше генов ортологов, паралогов или гомологов (т.е. открытых рамок считывания). Таким образом, также предпочтителен вариант контролирующей экспрессию последовательности, содержащейся в полинуклеотиде настоящего изобретения, имеет последовательность нуклеиновой кислоты, которая гибридизирует к последовательностям нуклеиновой кислоты, расположенным выше открытой рамки считывания последовательности являясь, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 90%, по меньшей мере, 91%, по меньшей мере, 92%, по меньшей мере, 93%, по меньшей мере, 94% по меньшей мере, 95%, по меньшей мере, 96%, по меньшей мере, 97%, по меньшей мере, 98%, или, по меньшей мере, 99% идентичными к последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8. Указанный вариант открытого считывания должен кодировать полипептид, имеющий биологическую активность соответствующего полипептида, закодированного открытой рамкой считывания, как показано в любой из SEQ ID NO: 4, 6 или 8. В данном контексте необходимо отметить, что открытая рамка считывания, показанная в SEQ ID NO: 4, кодирует полипептид, имеющий аминокислотную последовательность, показанную в SEQ ID NO: 5, и предпочтительно кодирует белок семени. Открытая рамка считывания, показанная в SEQ ID NO: 6, кодирует полипептид, имеющий аминокислотную последовательность, показанную в SEQ ID NO: 7, и предпочтительно кодирует белок семени, точнее тонкопластный внутренний белок 3-1. Открытая рамка считывания, показанная в SEQ ID NO: 8, кодирует полипептид, имеющий аминокислотную последовательность, показанную в SEQ ID NO: 9, и предпочтительно кодирует белок семени.
Также предпочтителен вариант контролирующей экспрессию последовательности, содержащейся в полинуклеотиде настоящего изобретения (i), получаемый 5′ прогулкой по геному или TAIL PCR из открытой рамки считывания последовательности, как показано в любой из SEQ ID NO: 4, 6 или 8, или (ii) получаемый с помощью 5′ прогулки по геному из открытой рамки считывания последовательности, которая, по меньшей мере, на 80% идентична открытой рамке считывания, как показано в любой из SEQ ID NO: 4, 6 или 8. Вариант контролирующих экспрессию последовательностей, получаемых без дальнейших трудностей с помощью технологии прогулки по геному или термической ассиметричной переплетенной полимеразной цепной реакции (TAIL-PCR), которая может проводиться, как описано в сопутствующих примерах, с использованием, например, имеющихся в продаже наборов.
Вариант контролирующих экспрессию последовательностей, указанных в данном описании, для контролирующей экспрессию последовательности, показанной в SEQ ID NO: 1, предпочтительно содержит, по меньшей мере, 10, по меньшей мере, 20, по меньшей мере, 30, или все мотивы последовательностей, указанные в Таблице 4. Вариант контролирующих экспрессию последовательностей, указанных в данном описании, для контролирующей экспрессию последовательности, показанной в SEQ ID NO: 2, предпочтительно содержит, по меньшей мере, 10, по меньшей мере, 20, по меньшей мере, 30, по меньшей мере, 40, по меньшей мере, 50 или все мотивы последовательности, указанные в Таблице 9. Вариант контролирующих экспрессию последовательностей, указанных в данном описании, для контролирующей экспрессию последовательности, показанной в SEQ ID NO: 3, предпочтительно содержит, по меньшей мере, 10, по меньшей мере, 20, по меньшей мере, 30, по меньшей мере, 40, по меньшей мере, 50 или все мотивы последовательности, указанные в Таблице 10.
Примеры для предпочтительного варианта контролирующей экспрессию последовательности показаны в SEQ ID NO: 120, 121, и 122 (варианты SEQ ID NO: 3), в SEQ ID NO: 123 и 124 (варианты SEQ ID NO: 2), и в SEQ ID NO: 125, 126 и 127 (варианты SEQ ID NO: 1). По сравнению с соответствующей контролирующей экспрессию последовательностью, вышеуказанные варианты (как показано в SEQ ID NO от 120 до 127) не содержат инициирующие кодоны (ATG). Инициирующие кодоны заменяют либо BVH, либо BVH с терминирующим кодоном между двумя любыми инициирующими кодонами (в соответствии с номенклатурой IUPAC (Международного союза теоретической и прикладной химии)): В представляет собой C или G или T, V представляет собой A или C или G, и H представляет собой A или C или T). Таким образом, вариант контролирующей экспрессию последовательности можно получить путем мутирования предполагаемых инициирующих кодонов, как описано выше. Дальнейшие примеры варианта контролирующей экспрессию последовательности показаны в SEQ ID NO: 129, 130 и 131 (варианты SEQ ID NO: 1). Вышеупомянутая контролирующая экспрессию последовательность не содержит короткие открытые рамки считывания, указывающие на гомологию токсическим или аллергенным пептидам или полипептидам (см. Пример 3).
Будет понятно, что неосновные последовательности контролирующей экспрессию последовательности изобретения могут быть удалены без значительного ухудшения указанных свойств. Ограничение контролирующей экспрессию последовательности до определенных необходимых регуляторных областей может также происходить с помощью компьютерной программы, такой как программа PLACE («Растительные, действующие в цис-положении, регулирующие элементы ДНК») (Higo К et al. (1999) Nucleic Acids Res 27:1, 297-300) или база данных BIOBASE "Transfac" (Biologische Datenbanken GmbH, Braunschweig). Подобным образом вариант контролирующих экспрессию последовательностей, как указано выше, может быть искусственно генерирован. Более того, специалисту известны процессы мутагенеза последовательностей нуклеиновой кислоты, которые включают, например, использование олигонуклеотидов, имеющих одну или больше мутаций по сравнению с областью, которая будет мутирована (например, в рамках сайт-специфического мутагенеза). Праймеры, имеющие приблизительно от 15 до приблизительно 75 нуклеотидов или больше, обычно используют с, предпочтительно, от около 10 до около 25 или больше нуклеотидными остатками на обеих сторонах последовательности, которая будет модифицирована. Специалисту известны детали и процедура указанных процессов мутагенеза (Kunkel et al. (1987) Methods Enzymol 154:367-382; Tomic et al. (1990) Nucl Acids Res 12:1656; Upender et al. (1995) Biotechniques 18(1):29-30; патент США №4,237,224). Мутагенеза можно добиться путем обработки, например, векторов, содержащих экспрессию контрольной последовательности изобретения, с агентами мутагенеза, такими как гидроксиламин. В результате мутагенеза также получают вариант полинуклеотидов изобретения, как указано выше.
Контролирующая экспрессию последовательность, содержащаяся в полинуклеотиде настоящего изобретения предусматривает семя-сфецическую экспрессию. В частности, указанная контролирующая экспрессию последовательность предусматривает специфическую экспрессию, как в зародыше, так и в эндосперме, и, следовательно, в целом семени. Поэтому «семя», как используется в настоящем документе, относится, предпочтительно, к эндосперму и зародышевым тканям. Предпочтительно контролирующая экспрессию последовательность согласно настоящему изобретению предусматривает семя-сфецическую экспрессию на всех стадиях развития семени (например, в семенах кукурузы до 35-40 дней после опыления, см. Примеры). Более того, контролирующая экспрессию последовательность может также допускать экспрессию в пыльце (см. Примеры). «Специфический» в смысле изобретения означает, что представляющие интерес нуклеиновые кислоты, функционально связанные с контролирующей экспрессию последовательностью, указанной в данном документе, будут преимущественно (т.е. предпочтительно) экспрессированы в указанных тканях и клетках, когда они присутствуют в растении. Следует понимать, что особая экспрессия в тканях обычно не достигается тканеспецифическими промоторами. Скорее тканеспецифический промотор кажется, предпочтительно, включается в некоторые ткани, тем не менее, все еще имеет некоторую фоновую активность в других тканях. Данное явление известно как растекающаяся экспрессия. Однако под специфической экспрессией в данном изобретении подразумевают доминирующую экспрессию в тканях растения, как указано в данном документе. Доминирующая экспрессия, как указано в данном документе, характеризуется статистически значительно большим количеством выявляемой транскрипции в указанных тканях или клетках по отношению к другим тканям растения. Статистически значительно более высокий уровень экспрессии предпочтительно означает количество, которое, по меньшей мере, в два раза, три раза, четыре раза, пять раз, десять раз, сто раз, пятьсот раз или тысячу раз больше уровня, по меньшей мере, одной из других тканей с выявляемой транскрипцией. В противном случае, это экспрессия в указанной ткани или клетке, при этом уровень экспрессии в других тканях или клетках меньше, чем 1%, 2%, 3%, 4%, 5%, 10% или наиболее предпочтительно 15% от общего (всего растения) уровня экспрессии. Уровень экспрессии напрямую соотносится с количеством транскриптов (т.е. РНК) или полипептидов, закодированных транскриптами, находящимися в клетке или ткани. Специалистам известны подходящие техники измерения транскрипции, основанных либо на РНК или полипептидах. Специфичность ткани или клетки, кроме того, и предпочтительно в дополнение к вышесказанному означает, что экспрессия ограничена или почти ограничена до указанных тканей или клеток, т.е. в других тканях нет выявляемой транскрипции. Почти ограничена, как указано в данном документе, означает, что неспецифическая экспрессия, является выявляемой в менее, чем десяти, менее, чем в пяти, менее, чем в четырех, менее, чем в трех, менее, чем в двух или одной другой ткани(ях).
Семя-специфическая экспрессия может быть определена, например, путем сравнения экспрессии представляющей интерес нуклеиновой кислоты, например, гена-репортера, такого как [бета]-глюкуронидаза (GUS), функционально связанного с контролирующей экспрессию последовательностью в следующих тканях и на следующих стадиях развития: 1) корни и листья на стадии пяти листьев, 2) стебель на стадии V-7, 3) листья, шелуха и рыльца на стадии цветения, 4) колосок/кисть во время опыления, 5) початок или зерна на 5, 10, 15, 20 и 25 день после опыления (см. также Примеры). Предпочтительно, экспрессия представляющей интерес нуклеиновой кислоты может быть определена в початке или зернах на 5, 10, 15, 20 и 25 день после опыления в указанном образце, как показано на сопутствующих Фигурах. Экспрессия представляющей интерес нуклеиновой кислоты может быть определена с использованием различных хорошо известных техник, например, Нозерн-блоттинга или техник гибридизации in situ, как описано в WO 02/102970 и, предпочтительно, как описано в сопутствующих примерах. Трансгенные растения для анализа экспрессии семени могут быть также генерированы с помощью техник, хорошо известных специалистам в данной области техники и рассмотренных где-либо в другом месте в данном описании.
Термин «представляющая интерес нуклеиновая кислота» относится к нуклеиновой кислоте, которая будет экспрессирована под контролем контролирующей экспрессию последовательности, указанной в данном документе. Предпочтительно, представляющая интерес нуклеиновая кислота кодирует полипептид, наличие которого желательно в клетке или растении, как указано в данном документе и, в частности, в семени растения. Таким полипептидом может быть любой функционально активный или инертный белок, который накапливается в семени и/или дает положительный эффект растению или семени при его экспрессии. Необходимо понимать, что если представляющая интерес нуклеиновая кислота кодирует полипептид, может потребоваться транскрипция нуклеиновой кислоты в РНК и трансляция транскрибированной РНК в полипептид. Представляющая интерес нуклеиновая кислота также предпочтительно включает биологически активные молекулы РНК и, более предпочтительно, антисмысловые РНК, рибозимы, микро РНК или короткие интерферирующие РНК. Указанные биологически активные молекулы РНК могут использоваться для модификации количества целевого полипептида, находящегося в клетке или растении. Например, нежелательную энзимную активность в семени можно сократить благодаря экспрессии семени антисмысловых РНК, рибозимов, микро РНК или коротких интерферирующих РНК. Основные биологические принципы действия вышеуказанных биологически активных молекул РНК хорошо известны в технологии. Более того, специалисту известно, как получить нуклеиновые кислоты, которые кодируют подобные биологически активные молекулы РНК. Необходимо понимать, что биологически активные молекулы РНК можно напрямую получить при транскрипции представляющей интерес нуклеиновой кислоты, т.е. без трансляции в полипептид. Предпочтительно, по меньшей мере, одна представляющая интерес нуклеиновая кислота, которая будет выражена под контролем контролирующей экспрессию последовательности настоящего изобретения, является гетерогенной относительно указанной контролирующей экспрессию последовательности, т.е. не обязательно под ее контролем, но указанный контроль производится неестественным образом (например, с помощью технологий генной инженерии).
Термин «функционально связан», используемый в настоящем документе, означает, что контролирующая экспрессию последовательность настоящего изобретения и представляющая интерес нуклеиновая кислота связаны таким образом, что экспрессия может управляться указанной контролирующей экспрессию последовательностью, т.е. контролирующая экспрессию последовательность будет функционально связана с указанной последовательностью нуклеиновой кислоты, подлежащей экспрессии. Следовательно, контролирующая экспрессию последовательность и последовательность нуклеиновой кислоты, подлежащая экспрессии, могут быть функционально связаны друг с другом, например, путем вкладывания контролирующей экспрессию последовательности в 5′ конец последовательности нуклеиновой кислоты, подлежащей экспрессии. В противном случае, контролирующая экспрессию последовательность и нуклеиновая кислота, подлежащая экспрессии, могут находиться лишь в физической близости так, что контролирующая экспрессию последовательность способна управлять экспрессией, по меньшей мере, одной представляющей интерес последовательности нуклеиновой кислоты. Контролирующая экспрессию последовательность и нуклеиновая кислота, подлежащая экспрессии, предпочтительно, разделены не более, чем 700 п.о., 500 п.о., 300 п.о., 100 п.о., 80 п.о., 60 п.о., 40 п.о., 20 п.о., 10 п.о. или 5 п.о.
Предпочтительно, в ходе исследований, лежащих в основе настоящего изобретения, было установлено, что специфическая экспрессия (целого) семени представляющей интерес нуклеиновой кислоты может быть достоверно получена путем экспрессии указанных представляющих интерес нуклеиновых кислот под контролем контролирующей экспрессию последовательности из кукурузы или варианта контролирующей экспрессию последовательности, указанной выше (см. Таблицы 4A, 11 и 12). Благодаря настоящему изобретению возможно (i) особым образом управлять биохимическими процессами в тканях семени, например, путем экспрессии гетерогенных энзимов или биологически активных РНК, как указано выше, или (ii) путем производства гетерогенных белков в указанных тканях семени. По существу, настоящее изобретение предполагает использование полинуклеотида, вектора, клетки-хозяина или растения для экспрессии представляющей интерес нуклеиновой кислоты. Семя-специфические промоторы, описанные в известном уровне техники, только обеспечивают экспрессию в зародыше или эндосперме семени однодольного растения, нежели в целом семени.
Настоящее изобретение также относится к вектору, содержащему полинуклеотид настоящего изобретения.
Термин «вектор» предпочтительно включает плазмиды, векторы экспрессии, Т-ДНК векторы, а также искусственные хромосомы, такие как бактериальные или искусственные хромосомы дрожжей. Более того, данный термин также относится к целевым конструктам, которые допускают произвольную или сайт-направленную интеграцию целевого конструкта в геномную ДНК. Подобные целевые конструкты предпочтительно содержат ДНК достаточной длины либо для гомологичной, либо для гетерогенной рекомбинации, как детально описано ниже. Вектор, включающий полинуклеотиды настоящего изобретения, предпочтительно далее содержит селектируемые маркеры для размножения и/или селекции в хозяине. Вектор может быть включен в клетку-хозяина различными, известными в данной области техниками. При введении в клетку-хозяина вектор может находиться в цитоплазме или может быть включен в геном. В последнем случае необходимо понимать, что вектор может далее содержать последовательности нуклеиновой кислоты, которые допускают гомологическую рекомбинацию или гетерогенное включение. Векторы могут быть введены в прокариотические или эукариотические клетки путем обычной трансформации или техниками трансфекции. Предполагается, что термины «трансформация» и «трансфекция», конъюгация и трансдукция, использующиеся в данном контексте, содержат большое количество процессов известного уровня техники для введения чужеродной нуклеиновой кислоты (например, ДНК) в клетку-хозяина, включая соосаждение фосфата кальция, хлорида рубидия или хлорида кальция, диэтиламиноэтилдекстран-опосредованную трансфекцию, липофекцию, естественную компетенцию, основанные на угле кластеры, химически опосредованный перенос, электропорацию или бомбардировку частицами (например, «генная пушка»). Подходящие способы для трансформации или трансфекции клетки-хозяина, включая клетки растения, можно найти в Sambrook et al. (Молекулярное Клонирование: лабораторный справочник, 2-е изд., Cold Spring Harbor Laboratory, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989) и другие лабораторные справочники, такие как Methods in Molecular Biology, 1995, том 44, Agrobacterium protocols, Изд.: Gartland and Davey, Humana Press, Totowa, Нью-Джерси.
Предпочтительно, вектор, указанный в данном документе, подходит в качестве клонирующего вектора, т.е. воспроизводимого в системах микроорганизмов. Подобные векторы гарантируют эффективное клонирование в бактериях и, предпочтительно, дрожжах или грибах, а также позволяют стабильную трансформацию растений. «Клонирующие векторы» обычно содержат участок узнавания рестрикционной эндонуклеазы, в которую могут быть включены чужеродные последовательности ДНК определяемым способом без значительной биологической функции вектора, а также маркерный ген, подходящий для использования в идентификации и селекции клеток, трансформированных клонирующим вектором. Маркерные гены обычно включают гены, которые обеспечивают, например, устойчивость к канамицину, стрептомицину, спектиномицину, тетрациклину, гигромицину или ампицилину.
Теми векторными системами, которые должны быть упомянуты, в частности, являются различные бинарные и коинтегрированные векторные системы, подходящие для Т-ДНК опосредованной трансформации. Подобные векторные системы, как правило, характеризуются тем, что они содержат, по меньшей мере, vir-гены, которые необходимы для агробактерии-опосредованной трансформации, а также последовательности, которые разграничивают Т-ДНК (границы Т-ДНК). Векторные системы предпочтительно также содержат далее цис-регуляторные области, такие как промоторы и терминаторы и/или селективные маркеры, с которыми могут быть идентифицированы подходящие трансформированные клетки-хозяева или организмы. В то время как коинтегрированные векторные системы имеют vir-гены и последовательности Т-ДНК, размещенные на том же векторе, бинарные системы основаны, по меньшей мере, на двух векторах, один из которых несет vir-гены, но не Т-ДНК, в то время как второй несет Т-ДНК, но не vir-гены. В результате вышеупомянутые векторы сравнительно небольшие, легко манипулируемые и могут быть дублированы как в кишечной палочке, так и в агробактерии. Данные бинарные векторы включают векторы из серий pBIB-HYG, pPZP, pBecks, pGreen. Согласно данному изобретению предпочтительно используют pBinl9, pBI101, pBinAR, pGPTV, pSUN, pPZP и pCAMBIA. Обзор бинарных векторов и их использования можно найти в Hellens et al, Trends in Plant Science (2000) 5, 446-451. Более того, при использовании соответствующих клонирующих векторов, полинуклеотиды изобретения могут быть введены в клетки-хозяева и/или растения и, таким образом, использоваться в трансформации растений, таких как те, что были опубликованы и описаны в: Plant Molecular Biology and Biotechnology (CRC Press, Boca Raton, Florida), глава 6/7, стр.71-119 (1993); F.F. White, Vectors for Gene Transfer in Higher Plants; in: Transgenic Plants, том 1, Engineering and Utilization, Ed.: Kung and R. Wu, Academic Press, 1993, 15-38; B. Jenes et al., Techniques for Gene Transfer, в: Transgenic Plants, том 1, Engineering and Utilization, Ed.: Kung and R. Wu, Academic Press (1993), 128-143; Potrykus, Annu. Rev. Plant Physiol. Plant Molec. Biol. 42 (1991), 205-225.
Примеры векторов экспрессии растений включают те, что детально описаны у: Becker, D., Kemper, Е., Schell, J., и Masterson, R. (1992) "New plant binary vectors with selectable markers located proximal to the left border", Plant Mol. Biol. 20:1195-1197; и Bevan, M.W. (1984) "Binary Agrobacterium vectors for plant transformation", Nucl. Acids Res. 12:8711-8721; Vectors for Gene Transfer in Higher Plants; в: Transgenic Plants, том 1, Engineering and Utilization, Ed.: Kung and R. Wu, Academic Press, 1993, стр.15-38. Кассета экспрессии растения предпочтительно содержит регуляторные последовательности, которые способны контролировать экспрессию гена в растении и которые функционально связаны так, что каждая последовательность может выполнять свои функции, такие как транскрипционная терминация, например, сигналы полиаденилирования. Предпочтительными являются сигналы полиаденилирования, полученные от опухолеобразующей агробактерии Т-ДНК, такой как ген 3 Ti-плазмида pTiACH5, известный как октопин синтаза (Gielen et al., EMBO J. 3 (1984) 835 et seq.) или их функциональные эквиваленты, но все другие терминаторы, являющиеся функционально активными в растениях, также подходят. Так как экспрессия гена растения часто не ограничена транскрипционными уровнями, кассета экспрессии растения предпочтительно содержит другие функционально связанные последовательности, такие как усилители трансляции, например, ускоренная последовательность, которая содержит 5′ нетранслируемую лидерную последовательность вируса табачной мозаики, который увеличивает белки/отношение РНК (Gallie et al., 1987, Nucl. Acids Research 15:8693-8711). Другие предпочтительные последовательности для использования при функциональной связи в кассетах экспрессии генов растения это целевые последовательности, необходимые для нацеливания генного продукта представляющей интерес нуклеиновой кислоты в соответствующую ячейку клетки (для обзора, см. Kermode, Crit. Rev. Plant Sci. 15, 4 (1996) 285-423 и ссылки, указанные в данном документе), например, в вакуоль, ядро, все виды пластидов, такие как амилопласты, хромопласты, внеклеточное пространство, митохондрии, эндоплазматический ретикулум, консистентность масла, пероксисомы и другие составляющие клеток растения.
Необходимо понимать, что бинарные векторы и любые другие векторы могут быть модифицированы обычными техниками ДНК рекомбинации, размножены в кишечной палочке, введены в агробактерию с помощью, например, электропорации или других техник трансформации (Mozo and Hooykaas, Plant Mol. Biol. 16:917-918(1991)).
Настоящее изобретение также рассматривает клетку-хозяина, содержащую полинуклеотид или вектор настоящего изобретения.
Клетки-хозяева предпочтительно представляют собой трансгенные клетки или клеточные линии, полученные из растений. Более предпочтительно, указанные клетки-хозяева получены из однодольных растений. Предпочтительные однодольные растения описаны в данном документе. Клетки-хозяева, полученные из растений, включают клетки определенных тканей, органы и части растений во всех их фенотипических формах, таких как пыльники, волокна, коневые волоски, стебли, зародыши, каллюсы, котелидоны, черешки, собранный материал, ткань растения, репродуктивная ткань и клеточные культуры, полученные из реального трансгенного растения и/или может использоваться для получения трансгенного растения.
Необходимо понимать, что полинуклеотиды или векторы в соответствии с настоящим изобретением могут также присутствовать в прокариотическом и эукариотическом одноклеточном организме (также называемом микроорганизмом), в частности, в целях клонирования (например, в кишечной палочке) и для трансформации растений (например, в агробактерии). Таким образом, термин «клетка-хозяин» предпочтительно также включает прокариотические или эукариотические одноклеточные организмы (также называемые микроорганизмами). В частности, рассматриваемыми как прокариотические клетки-хозяева в контексте настоящего изобретения являются клетки Rhizobiaceae, в частности вид агробактерии. Предпочтительными клетками агробактерий являются опухолеобразующие агробактерии и клетки агробактерий ризогенов.
Агробактерия представляет собой рожденный в почве фитопатоген, который объединяет часть ДНК (Т-ДНК) в геном растения (Chilton, et al., 1977 Cell 11:263-271; Hoekema, et al., 1985 Nature 303:179-180; Bevan, 1984 Nucleic Acids Res. 12:8711-8721; Sheng and Citovsky, 1996 The Plant Cell, том 8. 1699-1710). Предпочтительно клетки/штаммы агробактерий обезврежены, т.е. лишены свойств, опосредующих корончатый галл, или лишены свойств, опосредующих корневой возбудитель, но в остальных случаях, предоставляющий функции для заражения растения. Клетки агробактерий в контексте настоящего изобретения предпочтительно выбраны из LBA4404, GV2260, GV3600, ЕНА101, ЕНА105, AGL-1, LBA9402, GV3101, COR341, COR356, UIA143, рСН32, BIBAC2, С58С1, рМР90 и AGT121. В предпочтительном варианте осуществления изобретения, клетку агробактерий выбирают из группы, включающей С58С1, ЕНА101, рМР90, и LBA4404.
Специалисту в данной области хорошо известно, как культивировать вышеуказанные виды агробактерий.
Настоящее изобретение также относится к трансгенному растению или его семенам, содержащим полинуклеотид или вектор настоящего изобретения.
Полинуклеотид или вектор могут присутствовать в цитоплазме клеток указанного растения или его семенах. Предпочтительно полинуклеотид или вектор устойчиво присоединяется к геному или клеткам указанного растения или семени растения. В данной области техники известно, как устойчиво присоединить полинуклеотид или вектор (в частности, вектор Т-ДНК) к геному клетки растения, что описано в данном документе. В контексте настоящего изобретения особо предусмотрено, что полинуклеотид или вектор должен быть устойчиво интегрирован в геном с помощью агробактерии-опосредованной трансформации.
Предпочтительные растения для использования для трансгенных растений настоящего изобретения представляют собой однодольные растения.
«Однодольное растение», как используется в данном документе, предпочтительно относится к цветущему растению с одной семядолей в семени. Особенно предпочтительными односемядольными растениями (также называемыми в данном документе однодольными) являются кукуруза, пшеница, рис, ячмень, овес, рожь, сорго, просо, трикалат, бананы, плевел или коикс. Термин «односемядольное растение» включает растения рода подсемейств Andropogonoideae (в частности, вид Saccharum, Sorghum или Zea), Arundineae (в частности, род Phragmites), Oryzoideae (в частности, род Oryza), Panicoideae, и, более предпочтительно, Pooideae (Festuciadeae) (в частности, род Роа, Festuca, Lolium, Trisetum, Agrostis, Phleum, Dactylis, Alopecurus, Avena, Triticum, Secale, and Hordeum). Предпочтительные односемядольные растения представляют собой Avena sativa (овес), Saccharum officinarum (сахарный тростник), Triticum dicoccum (пшеница двузернянка), Triticum monococcum (пшеница однозернянка), Triticum spelta (пшеница спельта), Triticum durum (пшеница), Triticum turgidum, Triticum aestivum (пшеница), Zea mays (маис/кукуруза), Panicum miliaceum (просо обыкновенное), Pennisetum thiphoides (просо тростниковое), Hordeum vulgare или H. sativum (ячмень), Oryza sativa (рис), Zizania aquatica (дикий рис), Secale cereale (рожь), Sorghum bicolor (S. vulgare) (сорго). Более предпочтительны пшеница (Triticum spp.), рис (Oryza spp.), ячмень (Hordeum spp.), овес (Avena spp.), рожь (Secale spp.), кукуруза (Zea mays), сорго и просо (Pennisettum spp).
Наиболее предпочтительным односемядольным растением является Zea mays.
Более того, настоящим изобретением предусмотрены определенные ткани, органы и части указанных односемядольных растений во всех их фенотипических формах, таких как пыльники, волокна, корневые волоски, стебли, зародыши, каллюсы, семядоли, черешки, собранный материал, ткань растения, репродуктивная ткань и клеточные культуры, полученные из реального трансгенного растения и/или может использоваться для осуществления трансгенного растения.
Трансгенные растения или трансгенные клетки-хозяева в соответствии с настоящим изобретением могут быть получены с помощью трансформационных техник, опубликованных и описанных в: Plant Molecular Biology and Biotechnology (CRC Press, Boca Raton, Florida), глава 6/7, стр.71-119 (1993); F.F. White, Vectors for Gene Transfer in Higher Plants; in: Transgenic Plants, том 1, Engineering and Utilization, Ed.: Kung and R. Wu, Academic Press, 1993, 15-38; B. Jenes et al., Techniques for Gene Transfer, в: Transgenic Plants, том 1, Engineering and Utilization, Ed.: Kung and R. Wu, Academic Press (1993), 128-143; Potrykus, Annu. Rev. Plant Physiol. Plant Molec. Biol. 42 (1991), 205-225; Transgenic Plants: Methods and Protocols Editor: Leandro Peca, Instituto Valenciano de Investigaciones Agrarias, Valencia Spain Series: Methods in Molecular Biology, том 286 (2004) или в WO 2006/133983. Предпочтительно, трансгенные растения могут быть получены путем Т-ДНК опосредованной трансформации. Подобные векторные системы, как правило, характеризуются тем, что они содержат, по меньшей мере, vir-гены, которые необходимы для агробактерии опосредованной трансформации, а также последовательности, которые разграничивают Т-ДНК (границы Т-ДНК). Подходящие векторы детально описаны в другом месте данной спецификации
Настоящее изобретение также относится к способу экспрессии представляющей интерес нуклеиновой кислоты в клетке-хозяине, содержащей
(a) введение полинуклеотида или вектора настоящего изобретения в клетку-хозяина; и
(b) экспрессию, по меньшей мере, одной представляющей интерес нуклеиновой кислоты в указанной клетке-хозяине.
Полинуклеотид или вектор настоящего изобретения может быть введен в клетку-хозяина с помощью подходящей трансфекции или трансформационных техник, как указано в другом месте данного описания. Представляющая интерес нуклеиновая кислота будет выражена в клетке-хозяине в подходящих условиях. Для этой цели, клетка-хозяин будет культивирована в условиях, которые, в общем, допускают транскрипцию нуклеиновых кислот. Более того, клетка-хозяин предпочтительно содержит экзогенно доставленные или эндогенно присутствующие механизмы транскрипции, необходимые для экспрессии представляющей интерес нуклеиновой кислоты контролирующей экспрессию последовательностью. Предпочтительно, указанная клетка-хозяин является клеткой односемядольного растения.
Более того, настоящее изобретение включает способ экспрессии представляющей интерес нуклеиновой кислоты в растении, содержащем
(a) введение полинуклеотида или вектора настоящего изобретения в растение; и
(b) экспрессию, по меньшей мере, одной представляющей интерес нуклеиновой кислоты в указанном растении.
Полинуклеотид или вектор настоящего изобретения может быть введен в растение с помощью подходящих техник, как указано в другом месте данного описания.
Также, настоящее изобретение относится к способу экспрессии семени представляющей интерес нуклеиновой кислоты, содержащей
(a) введение полинуклеотида или вектора настоящего изобретения в растение; и
(b) экспрессию, по меньшей мере, одной представляющей интерес нуклеиновой кислоты в указанном растении.
Далее некоторые предпочтительные примеры осуществления изобретения, относящиеся к настоящему изобретению, описаны более подробно.
В предпочтительном варианте осуществления изобретения, полинуклеотид настоящего изобретения также содержит дальнейшие генетические контрольные последовательности. Генетическая контрольная последовательность, как указано в соответствии с настоящим изобретением, должна пониматься в широком смысле и обозначает все последовательности, имеющие влияние на возникающую функцию трансгенной кассеты экспрессии изобретения. Генетические контрольные последовательности модифицируют, например, транскрипцию и трансляцию в эукариотических организмах. Кассеты экспрессии изобретения, предпочтительно, содержат в качестве дополнительной генетической контрольной последовательности один из промоторов изобретения 5" расположенный выше определенной последовательности нуклеиновой кислоты, подлежащей трансгенной экспрессии, и терминатор последовательности 3′ расположенный ниже и, при необходимости, дальнейшие обычные регуляторные элементы, в каждом случае функционально связанные с последовательностью нуклеиновой кислоты, подлежащей трансгенной экспрессии.
Генетические контрольные последовательности также содержат дальнейшие промоторы, элементы промотора или минимальные промоторы, которые способны модифицировать характеристики контроля экспрессии. Таким образом, возможно, например, через генетические контрольные последовательности для экспрессии тканей проводить дополнительно в зависимости от определенных факторов стресса. Соответствующие элементы описаны, например, для водного стресса, абсцизовой кислоты (Lam Е and Chua N Н, (1991) J Biol Chem 266(26):17131-17135) и теплового стресса (Schöffl F et al. (1989) Mol Gen Genetics 217(2-3):246-53). Другая возможность для дальнейших промоторов, которые делают возможной экспрессию в дальнейших тканях растения или других организмах, таких как, например, бактерии кишечной палочки, функционально связанные с последовательностью нуклеиновой кислоты, подлежащей экспрессии. Подходящими промоторами растений являются, в общем, все промоторы, описанные выше. Возможно, например, что определенная последовательность нуклеиновой кислоты описана промотором (например, одним из промоторов изобретения) в одной ткани растения в качестве смысловой РНК и транслирована в соответствующий белок, в то время как та же последовательность нуклеиновой кислоты транскрибируется другим промотором с различной специфичностью в различных тканях в антисмысловой РНК, а количество соответствующего белка снижается. Это можно осуществить с помощью кассеты экспрессии изобретения одним промотором, расположенным перед последовательностью нуклеиновой кислоты, подлежащей трансгенной экспрессии, и другим промотором позади.
Было показано, что нетранслируемые области могут иметь значительные функции при регулировании генной экспрессии. Таким образом, было показано, что 5"-нетранслируемые последовательности могут усиливать неустойчивую экспрессию гетерогенных генов. Это может, более того, содействовать тканевой специфичности (Rouster J et al. (1998) Plant J. 15:435-440.). С другой стороны, 5"-нетранслируемая область непрозрачного-2 гена сдерживает экспрессию. Удаление соответствующей области данного гена приводит к увеличению активности гена (Lohmer S et al. (1993) Plant Cell 5:65-73). Специалисту известны дальнейшие 5"-нетранслируемые последовательности и интроны с функцией стимулирования экспрессии. McElroy и коллеги (McElroy et al. (1991) Mol Gen Genet 231(1): 150-160) описали конструкт, основанный на промоторе актина риса 1 (Act1) для трансформации односемядольных растений. Использование интрона Act1 в комбинации с 35S промотором в клетках трансгенного риса привело к отношению экспрессии, которое увеличилось в десять раз, по сравнению с изолированным промотором 35S. Оптимизация среды последовательности сайта инициации трансляции гена-репортера [бета]-глюкуронидаза (GUS) привело к четырехкратному увеличению в GUS экспрессии в трансформированных клетках риса. Комбинация оптимизированного сайта инициации трансляции и интрона Act1 привело к увеличению в 40 раз в GUS экспрессии CaMV35S промотором в трансформированных клетках риса; такой же результат был получен у трансформированных клеток кукурузы. В общем, из вышеописанных исследований был сделан вывод, что векторы экспрессии, основанные на промоторе Act1 подходят для контроля достаточно сильной и конститутивной экспрессии чужеродной ДНК в трансформированных клетках односемядольных растений.
Более того, профиль экспрессии контрольной области экспрессии изобретения может быть усилен экспрессией, усиливающей интроны и/или транскрипции терминирующих кодонов.
Таким образом, в предпочтительном варианте осуществления изобретения полинуклеотид изобретения содержит, по меньшей мере, один дополнительный элемент из группы, состоящей из a) 5"-нетранслируемых областей, b) интрона, кодирующего последовательности, и c) транскрипции терминирующих кодонов.
«Интрон, кодирующий последовательность» предпочтительно представляет собой интрон, кодирующий экспрессию, усиливающую интрон из односемядольного растения. Более предпочтительно интрон, кодирующий последовательность, представляет собой интрон из убиквитина, актина или гена алкогольдегидрогеназы. Наиболее предпочтительно интрон, кодирующий последовательность, представляет собой первый интрон растительного гена, кодирующий полипептид металлотионина 1 (МЕТ1), металлотиониноподобный полипептид (MET-like) или его функциональный эквивалент или ортолог.
Предпочтительные первые интроны растительного гена, кодирующие металлотиониноподобный полипептид (или его функциональный эквивалент или гомолог) описаны в WO 2006/094976 и WO 2008/099013, которые включены в данный документ посредством ссылки. Предпочтительно, указанный первый интрон получается из МЕТ-подобного гена односемядольного растения. Более предпочтительно, указанный первый интрон получается из Oryza sativa (см. Примеры). Еще более предпочтительно, первый интрон получается из МЕТ-подобного гена, кодирующего полипептид, как показано в SEQ ID NO: 118. Более предпочтительно, первый интрон растительного гена, кодирующий металлотионинподобный ген 1, имеет последовательность, как показано в SEQ ID NO: 119.
Также предполагается, что интрон, кодирующий область, является вариантом первого интрона растительного гена, кодирующего металлотионинподобный белок, в частности, вариант первого интрона, имеющего последовательность, как показано в SEQ ID NO: 120. Подобный вариант, предпочтительно, по меньшей мере, на 70%, по меньшей мере, на 80%, по меньшей мере, на 90%, по меньшей мере, на 91%, по меньшей мере, на 92%, по меньшей мере, на 93%, по меньшей мере, на 94% по меньшей мере, на 95%, по меньшей мере, на 96%, по меньшей мере, на 97%, по меньшей мере, на 98%, или, по меньшей мере, на 99% идентичен указанному первому интрону. В других местах данного документа описано, как определить степень идентичности.
Предпочтительно, интрон, кодирующий последовательность, вводится в конструкт экспрессии в 5"-нетранслируемую область представляющей интерес нуклеиновой кислоты, подлежащей экспрессии (т.е. между контролирующей экспрессию последовательностью и белком, кодирующим последовательность (открытую рамку считывания) или представляющую интерес нуклеиновую кислоту).
Предпочтительно, в контексте настоящего изобретения было показано, что интрон Met1-1 усиливает экспрессию контролирующих экспрессию последовательностей, в соответствии с настоящим изобретением в ткани семени.
Кассета экспрессии может также содержать одну или больше так-называемых усиливающих последовательностей, функционально связанных с промотором, которые позволяют увеличить трансгенную экспрессию в нуклеиновой кислоте. Также существует возможность введения дополнительных предпочтительных последовательностей, таких как дальнейшие регуляторные элементы или терминаторы, на 3′ конце последовательностей нуклеиновой кислоты, подлежащих трансгенной экспрессии.
Контрольные последовательности дополнительно обозначают те, что дают возможность гомологической рекомбинации или введения в геном организма-хозяина, а также позволяют удаление из генома. При гомологической рекомбинации, например, существует возможность замены естественного промотора на один из промоторов изобретения. Способы, такие как технология cre/lox, позволяют ткане-специфическое удаление, индуцируемое в некоторых случаях, кассеты экспрессии из генома организма-хозяина (Sauer В. (1998) Methods. 4(4):381-92). В данном случае, особые фланкирующие последовательности присоединяются (lox-последовательности) к целевому гену и впоследствии делают возможным удаление путем cre-рекомбиназы. Промотор для введения может быть размещен путем гомологической рекомбинации перед целевым геном, подлежащим экспрессии с помощью связи промотора с последовательностями ДНК, которые, например, гомологичны эндогенным последовательностям, которые предшествуют рамке считывания целевого гена. Подобные последовательности должны считаться генетическими контрольными последовательностями. После трансформации клетки с соответствующим конструктом ДНК, две гомологичные последовательности могут взаимодействовать и, таким образом, помещают промотор последовательности в необходимое место перед целевым геном так, что последовательность промотора становится функционально связанной с целевым геном и образует кассету экспрессии изобретения. Селекция гомологичных последовательностей определяет место встраивания промотора. В данном случае существует возможность генерировать кассету экспрессии гомологической рекомбинацией путем одинарной или двойной обратной рекомбинации. При одинарной обратной рекомбинации используется только одна рекомбинационная последовательность, и вставляется полная введенная ДНК. При двойной обратной рекомбинации вводимая ДНК фланкируется двумя гомологичными последовательностями, и вставляется фланкирующая область. Последний процесс подходит для замены, как описано выше, естественного промотора определенного гена одним из промоторов изобретения и, таким образом, модифицируется местоположение и время генной экспрессии. Данная функциональная связь представляет собой кассету экспрессии изобретения. Для эффективной селекции гомологически рекомбинированных или трансформированных другими способами клеток, необходимо дополнительно ввести селектируемый маркер. Различные подходящие маркеры указаны ниже. Селективный маркер позволяет проводить селекцию трансформированных клеток из нетрансформированных. Гомологическая рекомбинация представляет собой относительно редкое явление в эукариотах, особенно в растениях. Преобладает произвольное введение в главный геном. Одна возможность удаления произвольно введенных последовательностей и, таким образом, усиления клеточных клонов, имеющих правильную гомологическую рекомбинацию, состоит в использовании системы рекомбинации последовательности, как описано в US 6,110,736.
Сигналы полиаденилирования, подходящие в качестве генетических контрольных последовательностей, представляют собой сигналы полиаденилирования и предпочтительно из опухолеобразующих агробактерий.
В особенно предпочтительном варианте осуществления изобретения кассета экспрессии содержит терминаторную последовательность, являющуюся функциональной в растениях. Терминаторные последовательности, являющиеся функциональными в растениях, обозначают, в общем, последовательности, способные производить терминацию транскрипции последовательности ДНК в растениях. Примерами подходящих терминаторных последовательностей являются OCS (октопин синтаза) терминатор и NOS (нопалин синтаза) терминатор. Тем не менее, особенно предпочтительны последовательности растительного терминатора. Последовательности растительного терминатора обозначают, в общем, последовательности, состоящие из естественного растительного гена. Особое предпочтение, в этой связи, отдается терминатору катепсина D картофеля ингибиторного гена (GenBank Acc. No.: Х74985) или терминатору гена запасного белка конских бобов VfLEIB3 (GenBank Acc. No.: Z26489). Данные терминаторы, по меньшей мере, эквивалентны вирусным или Т-ДНК терминаторам, описанным в науке.
Специалисту также известно большое количество нуклеиновых кислот и белков, чья рекомбинантная экспрессия находится, предпочтительно, под контролем кассет экспрессии или процессов изобретения. Некоторые примеры представляющих интерес нуклеиновых кислот, чья экспрессия предоставляет желаемый эффект, указаны ниже.
Специалисту известно большое количество генов, посредством репрессии или выключения которых с помощью экспрессии соответствующей антисмысловой РНК достигается предпочтительный эффект. Неограниченные примеры предпочтительных эффектов, которые могут быть указаны: способствующее производство трансгенного организма, например, посредством экспрессии селективных маркеров, достижение устойчивости к факторам абиотического стресса (тепло, холод, сухость, увеличенная влажность, засуха, средовые токсины, УФ-излучение), достижение устойчивости к факторам биотического стресса (патогены, вирусы, насекомые и заболевания), улучшение качеств человеческой или животной пищи, улучшение скорости роста урожая. Предпочтительно, фактором биотического стресса является болезнь, имеющая зародыш в семенах (в основном, микоз, например, твердая головня пшеницы (Tilletia tritici); полосатость листьев (Pyrenophora graminea), и пыльная головня (Ustilago nuda), в основном, в ячмене.
Более того, основное использование зерна, особенно, зерна кукурузы для корма или пищи. Введение генов, меняющих состав зерна, может значительно увеличить кормовую или питательную ценность. Первичными компонентами зерна являются крахмал, белок и масло. Каждый из первичных компонентов можно улучшить путем изменения его уровня или состава. Первичными компонентами зерна являются крахмал, белок и масло. Каждый из первичных компонентов может быть улучшен путем изменения его уровня или состава (имеется в виду питательная ценность структурных блоков каждого компонента, или, в противном случае, соответствующие структуры масел и крахмалов могут быть улучшены так, чтобы улучшалось их питательное содержание).
Белок многих зерен хлебных злаков является недостаточным для корма и пиши, особенно для корма свиней, домашней птицы, пищи людей. Мало белка содержится в нескольких аминокислотах, которые необходимы для диеты данных видов, поэтому необходимы дополнительные добавки в зерно. К ограниченным необходимым аминокислотам относятся лизин, метионин, триптофан, треонин, валин, аргинин и гистидин. Уровни данных необходимых аминокислот в семенах и зернах могут быть повышены с помощью механизмов, которые включают введение генов для увеличения биосинтеза аминокислот, уменьшение деструкции аминокислот, увеличение запаса аминокислот в белках, увеличение транспорта аминокислот в семена или зерна.
Одним механизмом увеличения биосинтеза аминокислот является введение генов, которые ослабляют аминокислотные биосинтетические пути так, что растение больше не может соответствующим образом контролировать производимые уровни. Это может быть сделано путем ослабления или пропуска шагов в аминокислотном биосинтетическом пути, который обычно регулируется уровнями аминокислотного конечного продукта пути. Примеры включают введение генов, кодирующих ослабленные версии энзимов аспартокиназы или синтеза дигидродипиколинициновой кослоты (DHDP) для увеличения производства лизина и треонина, и антранилат синтазы для увеличения производства триптофана. Сокращение диссимиляции аминокислот может быть завершено путем введения последовательностей ДНК, которые сокращают или исключают экспрессию генов, кодирующих энзимы, которые катализируют шаги в катаболических путях, таких как энзим лизин-кетоглутарат редуктаза.
Белковый состав зерна может меняться для улучшения баланса аминокислот различными способами, включая повышение экспрессии нативных белков, сокращение экспрессии белков, имеющих плохой состав, изменение состава нативных белков или введение генов, кодирующих полностью новые белки, имеющие лучший состав. Может быть введена ДНК, что уменьшит экспрессию членов семейства зеинов запасных белков. Данная ДНК может кодировать рибозимы или антисмысловые последовательности, направленные на ослабление экспрессии белков зеинов или экспрессии регуляторов экспрессии зеин, такой как генный продукт опак-2. Белковый состав зерна может быть модифицирован с помощью такого явления как косупрессия, т.е. подавление экспрессии эндогенного гена посредством экспрессии идентичного структурного гена или фрагмента гена, введенного путем трансформации. Кроме того, введенный ДНК может кодировать энзимы, которые ослабляют зеины. Достигнутое уменьшение экспрессии зеинов может сопровождаться увеличением белков с более желательным аминокислотным составом или увеличением других основных составляющих семени, таких как крахмал. В противном случае, может быть введен химерный ген, который содержит кодирующую последовательность для нативного белка соответствующего аминокислотного состава, такого как для одного из белков глобулина или 10 кД зеинов кукурузы и промотор или другой регуляторной последовательности, созданной для увеличения экспрессии указанного белка. Кодирующая последовательность указанного гена может включать дополнительные или замещающие кодоны для необходимых аминокислот. Кроме того, может использоваться кодирующая последовательность, полученная из другого вида, или частично или полностью синтетической последовательности, кодирующей совершенно уникальную пептидную последовательность, разработанную для усиления аминокислотного состава семени.
Введение генов, меняющих содержание масла в зерне, может иметь значение. Увеличение содержания масла может привести к увеличению содержания обменной энергии и плотности семян, использующихся в корме и пище. Введенные гены могут кодировать энзимы, которые убирают или сокращают ограничения скорости или регулируемые шаги в жирных кислотах или липидном биосинтезе. Подобные гены это, например, гены, которые кодируют ацетил-CoA-карбоксилазу, ACP-ацилтрансферазу, бета-кетоацил-ACP синтазу и другие хорошо известные биосинтетические действия жирной кислоты.
Гены могут быть введены для усиления питательной ценности крахмала зерна, например, путем увеличения уровня разветвления, приводящего к улучшению использования крахмала у коров посредством замедления их метаболизма.
Корм или пища, содержащая некоторые зерна хлебных злаков, обладает недостаточным количеством витаминов и должна быть дополнена, чтобы предоставлять соответствующую питательную ценность. Введение генов, усиливающих биосинтез витаминов в семенах, может быть представлен, включая, например, витамины A, E, B12, холин и подобные.
Свойства крахмала могут выгодно меняться путем изменения отношения амилозы к амилопектину, размера молекул крахмала или их схемы разветвления. Посредством данных изменений могут быть модифицированы многие свойства, включая, например, температура застудневания, подогрев застудневания, четкость пленок и пасты. Для проведения изменений в свойствах, гены, которые кодируют синтазную активность грануло-связанного или растворимого крахмала или активность ветвящего фермента, могут вводиться отдельно или в комбинации. ДНК, такие как антисмысловые конструкции, могут также использоваться для снижения уровней эндогенной активности данных энзимов.
Кроме того, некоторые зерна хлебных злаков, используемые в кормовых и пищевых добавках, обладают недостаточным количеством витаминов и должны быть дополнены для предоставления соответствующей питательной ценности; введение генов, усиливающих биосинтез витаминов в семенах, может быть представлен, включая, например, витамины A, E, B12, холин и подобные.
В дополнение, можно считать, что растение, используемое для производства или обработки полезных биологических соединений, которые либо вообще не были произведены, либо не производились на том же уровне, раньше в растениях. Новые растения, производящие данные соединения, стали возможными благодаря введению и экспрессии генов с помощью трансформационных способов. Данные возможности включают, например, любое биологическое соединение, которое в настоящее время производится любым организмом, такое как белки, нуклеиновые кислоты, первичные и промежуточные метаболиты, углеводные полимеры и т.д. Соединения могут производиться растением, полученным из урожая и/или обработки, и использоваться для любых признанных в настоящее время целей, таких как лекарственные препараты, ароматизаторы, промышленные энзимы и многие другие.
Полезные последовательности представляющей интерес нуклеиновой кислоты могут соединяться с контролирующей экспрессию последовательностью настоящего изобретения, включающей, предпочтительно, данные кодирующие запасные белки семени, энзимный путь жирной кислоты, токоферольные биосинтетические энзимы, аминокислотные биосинтетические энзимы и ветвящие энзимы крахмала.
В соответствии с настоящим изобретением, контролирующая экспрессию последовательность может использоваться для экспрессии метаболических энзимов для использования в кормовом и пищевом секторе, например, фетазы и целлюлазы. Особенно предпочтительны нуклеиновые кислоты, такие как искусственные кДНК, которые кодируют микробную фитазу (GenBank Асе. No.: A19451) или их функциональные эквиваленты. Экспрессия генов, которая вызывает накопление чистых химикатов, таких как токоферолы, токотриенолы или каротиноиды. Примером может служить фитоин десатураза. Предпочтительны нуклеиновые кислоты, которые кодируют фитоин десатуразу Narcissus pseudonarcissus (нарцисс ложный) (GenBank Acc. No.: X78815) или их функциональные эквиваленты.
В соответствии с настоящим изобретением, контролирующая экспрессию последовательность может использоваться для экспрессии представляющих интерес нуклеиновых кислот, которые модифицировали производство масел (US 6,444,876), производство высокого уровня масла (патенты США №№5,608,149 и 6,476,295), или модифицированный состав жирной кислоты (US 6,537,750). Предпочтительный энзимный путь жирной кислоты включает тиоэстеразы (патенты США №№5,512,482; 5,530,186; 5,945,585; 5,639,790; 5,807,893; 5,955,650; 5,955,329; 5,759,829; 5,147,792; 5,304,481; 5,298,421; 5,344,771; и 5,760,206), диацилглицерин ацилтрансферазу (Публикации патента США 200301 15632A1 и 20030028923A1), и десатуразы (патенты США №№5,689,050; 5,663,068; 5,614,393; 5,856,157; 6,117,677; 6,043,411; 6,194,167; 5,705,391; 5,663,068; 5,552,306; 6,075,183; 6,051,754; 5,689,050; 5,789,220; 5,057,419; 5,654,402; 5,659,645; 6,100,091; 5,760,206; 6,172,106; 5,952,544; 5,866,789; 5,443,974; и 5,093,249), которые все включены в настоящий документ посредством ссылки.
Производство нутрицевтиков, таких как, например, полиненасыщенные жирные кислоты, такие как, например, арахидоновая кислота или EP (эйкозапентаеновая кислота) или DHA (докозагексановая кислота) путем экспрессии жирной кислоты элонгазы и/или десатуразы или производства белков, имеющих улучшенную питательную ценность, такую как, например, имеющих высокое содержание незаменимых аминокислот (например, метионин-богатый 2S ген альбумина бразильского ореха). Предпочтительные нуклеиновые кислоты представляют собой кислоты, кодирующие метионин-богатый 2S альбумин из Bertholletia excelsa (GenBank Acc. No.: AB044391), [дельта] 6-ациллипид десатуразу из Physcomitrella patens (GenBank Acc. No.: AJ222980; Girke et al. (1998) Plant J 15:3948), [дельта]6-десатуразу из Mortierelia alpina (Sakuradani et al. (1999) Gene 238:445-453), [дельта] 5-десатуразу из Caenorhabditis elegans (Michaelson et al. 1998, FEBS Letters 439:215-218), [дельта]5-десатуразу жирной кислоты (des-5) из Caenorhabditis elegans (GenBank Acc. No.: AF078796), [дельта]5-десатуразу из Mortierelia alpina (Michaelson et al. J Biol Chem 273:19055-19059), [дельта]6-элонгазу из Caenorhabditis elegans (Beaudoin et al. (2000) Proc Natl. Acad Sci USA 97:6421-6426), [дельта]6-элонгазу из Physcomitrella patens (Zank et al. (2000) Biochemical Society Transactions 28:654-657) или их функциональные эквиваленты.
Достижение увеличенной способности запасания в клетках, которые обычно содержат небольшое количество запасных белков или липидов, с целью увеличения эффективности данных веществ, например, посредством экспрессии ацетил-CoA-карбоксилазы. Предпочтительные нуклеиновые кислоты представляют собой кислоты, кодирующие ацетил-CoA-карбоксилазу (акказу) из Medicago sativa (GenBank Acc. No.: L25042) или их функциональные эквиваленты. Дальнейшие примеры предпочтительных генов указаны, например, в Dunwel1 J М (2000) J Exp Bot. 51 Spec No:487-96. В противном случае, увеличенный запас белкового состава может быть предпочтительным для производства высокобелковой продукции. Предпочтительные запасные белки семени включают зеины.
Представляющая интерес нуклеиновая кислота может также предоставлять устойчивость к связанным с семенами болезням, вызванным вирусами, бактериями, грибами, насекомыми (например, путем экспрессии подходящего Bt гена) и нематодами.
Например, представляющая интерес нуклеиновая кислота может придавать устойчивость к грибам, влияющим на запасные семена, таким как грибы рода Aspergillus, Penicilium или Fusarium (в частности Fusarium moniliformere). Устойчивость к Fusarium может быть предпочтительно получена посредством функциональной связи контролирующей экспрессию последовательности, в соответствии с настоящим изобретением, с последовательностью нуклеиновой кислоты, кодирующей Cry-1A(b) или любой другой вариант Cry, который дает устойчивость к Fusarium.
Более того, представляющая интерес нуклеиновая кислота может дать устойчивость к нематоде Anguina tritici, которая может вызвать значительную потерю урожая пшеницы двузернянки (Triticum monococcum), ржи (Secale cereale), пшеницы спельта (Т. spelta) и пшеницы (Т. aestivum).
Также представляющая интерес нуклеиновая кислота может придавать устойчивость к виду Cnephasia, в частности, к зерновой листовертке (Cnephasia pumicana) и трубковертам, таким как Cnephasia longana.
Также предполагается, что представляющая интерес нуклеиновая кислота может придать устойчивость к серым полевым слизням, таким как Deroceras reticulatum или Deroceras agreste.
Устойчивость к вирусам может быть получена посредством экспрессии новых генов. Например, было показано, что экспрессия белка вирусной оболочки в трансгенном растении может передавать устойчивость к инфекции растения с помощью данного вируса и, возможно, других тесно связанных вирусов. Предполагается, что экспрессия антисмысловых генов, направленных на основные вирусные функции, может передавать устойчивость к указанному вирусу. Например, антисмысловой ген, направленный на ген, ответственный за редупликацию вирусной нуклеиновой кислоты, может ингибировать указанную редупликацию и привести к устойчивости к вирусу. Считается, что интерференция с другими вирусными функциями посредством использования антисмысловых генов может увеличить устойчивость к вирусам.
Экспрессия нуклеиновых кислот под контролем промоторов изобретения возможна в любом желаемом клеточном элементе, таком как, например, эндомембранная система, вакуоли и хлоропласты. Желаемые гликозилированные реакции, особенно фолдинги и им подобные, возможны при использовании секреторного пути. Также возможна секреция целевого белка на клеточной поверхности или секреция в среду культивирования, например, образец суспензионно-культивируемых клеток или протопластов. Целевые последовательности, необходимые для данной цели, могут, таким образом, учитываться в отдельных вариантах вектора и вводиться вместе с целевым геном, подлежащим клонированию, в вектор, с помощью подходящей стратегии клонирования. Возможно использовать целевые последовательности как подлинно-генные, в случае их присутствия, или гетерологические последовательности. Дополнительные гетерологические последовательности, предпочтительные для функциональной связи, но не ограниченные этим, являются далее целевыми последовательностями для обеспечения субклеточной локализации в апопластах, в вакуоле, в пластидах, в митохондрии, в эндоплазматическом ретикулуме (ER), в ядре клетки, в элайопластах или других элементах; и усилителях трансляции, таких как 5" лидерная последовательность из вируса табачной мозаики (Gallie et al. (1987) Nucl Acids Res 15 8693-8711) и подобных. Процесс транспортировки белков, не локализованных самих по себе в пластидах в целевом образце, в пластиды описан (Klosgen R В & Weil J Н (1991) Mol Gen Genet 225(2):297-304; Van Breusegem F et al. (1998) Plant Mol Biol 38(3):491-496).
Предпочтительные последовательности представляют собой
a) малые субъединицы (SSU) рибулезобисфосфатоксигеназы (Rubisco ssu) гороха, кукурузы, подсолнечника
b) транзитные пептиды, полученные из генов биосинтеза растительной жирной кислоты, такие как транзитные пептиды пластидного ацилпереносящего белка (АСР), стеариловая ACP десатуразы, [бета]-кетоацил-ACP синтаза или ацил-ACP тиоэстераза.
c) транзитный пептид для GBSSI (синтаза 1 крахмального зерна связанного крахмала)
d) LHCP II гены.
Целевые последовательности могут быть связаны с другими целевыми последовательностями, которые отличаются от транзитного пептида, кодирующего последовательности для обеспечения субклеточной локализации в апопластах, в вакуоле, в пластидах, в митохондрии, в эндоплазматическом ретикулуме (ER), в ядре клетки, в элайопластах или других элементах. Также возможно использование усилителей трансляции, таких как 5" лидерная последовательность вируса табачной мозаики (Gallie et al. (1987) Nucl Acids Res 15:8693-8711) и подобных.
Специалисту известно, что ему не нужно производить экспрессию генов, описанных выше, напрямую с помощью последовательностей нуклеиновой кислоты, кодирующих данные гены, или репрессировать их, например, антисмысловым способом. Он также может использовать, например, факторы искусственной транскрипции типа белков «цинковые пальцы» (Beerli R R et al. (2000) Proc Natl Acad Sci USA 97(4):1495-500). Данные факторы связывают регулирующие области эндогенных генов, которые подлежат экспрессии или репрессии и приводят, в зависимости от структуры фактора, к экспрессии или репрессии эндогенного гена. Таким образом, желаемого эффекта можно добиться посредством экспрессии соответствующего фактора транскрипции «цинковых пальцев» под контролем одного из промоторов изобретения.
Кассеты экспрессии изобретения могут, кроме того, использоваться для супрессии семени или редукции редупликации или/и трансляции целевых генов путем сайленсинга генов.
Кассеты экспрессии изобретения могут также использоваться для экспрессии семени нуклеиновых кислот, которые содействуют так - называемым антисмысловым эффектам и, таким образом, способны, например, сокращать экспрессию целевого белка.
Предпочтительные гены и белки, чья супрессия является условием для предпочтительного фенотипа, содержат, на примере, но не ограничены:
a) редукцией в экспрессии аллергенных белков, как описано, например, в Tada Y et al. (1996) FEBS Lett 391(3):341-345 или Nakamura R (1996) Biosci Biotechnol Biochem 60(8):1215-1221.
b) перемещением амилозного/амилопектинового содержания в крахмал путем супрессии ветвящего фермента Q, ответственного за [альфа]-1,6-гликозидную связь. Соответствующие процедуры описаны (например, в Schwall G Р et al. (2000) Nat Biotechnol 18(5):551-554). Для данных целей предпочтительно использование последовательностей нуклеиновой кислоты, подобно последовательностям крахмала ветвящего фермента II в картофеле (GenBank Acc. No.: AR123356; патент США №6,169,226) или его гомологах из другого рода или вида.
«Антисмысловая» нуклеиновая кислота обозначает, в первую очередь, последовательность нуклеиновой кислоты, которая является полностью или частично комплементарной, по меньшей мере, к части кодирующей нити указанного целевого белка. Специалисту известно, что он может, в противном случае, использовать кДНК или соответствующий ген в качестве начальной матрицы для соответствующих антисмысловых конструктов. Антисмысловая нуклеиновая кислота является, предпочтительно, комплементарной к кодирующей области целевого белка или его части. Антисмысловая нуклеиновая может, однако, также быть комплементарной к некодирующей области его части. Начиная с последовательности информации для целевого белка, антисмысловая нуклеиновая кислота может быть разработана известным специалисту способом, с учетом правила пар оснований Ватсона и Крика. Антисмысловая нуклеиновая кислота может быть комплементарной к целой или части последовательности нуклеиновой кислоты целевого белка. В предпочтительном варианте осуществления изобретения, антисмысловая нуклеиновая кислота является олигонуклеотидом, длиной, например, 15, 20, 25, 30, 35, 40, 45 или 50 нуклеотидов.
Антисмысловая нуклеиновая кислота содержит в предпочтительном варианте осуществления изобретения [альфа]-аномерные молекулы нуклеиновой кислоты. [альфа]-Аномерные молекулы нуклеиновой кислоты образуют в определенных двухспиральных гибридах с комплементарной РНК, в которой спирали находятся параллельно друг другу, в отличие от обычных [бета] единиц (Gaultier et al. (1987) Nucleic Acids Res 15:6625-6641). Использование последовательностей, описанных выше, в смысловой ориентации, кроме того, осуществляется и может, как известно специалисту, привести к косупрессии. Экспрессия смысловой РНК в эндогенный ген может сократить или отключить экспрессию, подобную той, которая описана в антисмысловых подходах (Goring et al. (1991) Proc Natl Acad Sci USA 88:1770-1774; Smith et al. (1990) Mol Gen Genet 224:447-481; Napoli et al. (1990) Plant Cell 2:279-289; Van der Krol et al. (1990) Plant Cell 2:291-299). Более того, введенный конструкт представляет собой ген, подлежащий сокращению полностью или частично. Возможность трансляции не является необходимой.
Также предпочтительно использовать процессы, такие как генная регуляция посредством двухспиральной PHK (интерференция двухспиральной PHK). Специалисту известны соответствующие процессы, которые подробно описанны (например, Matzke М A et al. (2000) Plant Mol Biol 43:401-415; Fire A. et al (1998) Nature 391:806-811; WO 99/32619; WO 99/53050; WO 00/68374; WO 00/44914; WO 00/44895; WO 00/49035; WO 00/63364). Прямое указание сделано на процессы и способы, описанные в указанных ссылках. Высокоэффективная супрессия нативных генов вызывается посредством одновременного введения спирали и дополнительной спирали.
Возможно и предпочтительно соединять антисмысловую стратегию с рибозимным процессом. Рибозимы являются каталитически активными последовательностями PHK, которые при соединении с антисмысловыми последовательностями, каталитически расщепляют целевые последовательности (Tanner N К. FEMS Microbiol Rev. 1999; 23 (3):257-75). Это может увеличить эффективность антисмысловой стратегии. Экспрессия рибозимов для сокращения определенных белков известна специалисту и описана, например, в EP-A1 0 291 533, EP-A1 0 321 201 и EP-A1 0 360 257. Подходящие целевые последовательности и рибозимы могут определяться, как описано Steinecke (Ribozymes, Methods in Cell Biology 50, Galbraith et al. eds. Academic Press, Inc. (1995), 449-460) расчетами вторичной структуры рибозима PHK и целевого PHK и путем их взаимодействия (Bayley С С et al., Plant Mol Biol. 1992; 18(2):353-361; Lloyd A M and Davis R W et al., Mol Gen Genet. 1994 March; 242(6):653-657). Примерами, которые необходимо отметить, являются рибозимы в виде головки молотка (Haselhoff and Gerlach (1988) Nature 334:585-591). Предпочтительные рибозимы основаны на производных от РНК тетрагимена L-19 IVS (патент США №4,987,071; патент США №5,116,742). Могут быть выбраны дальнейшие рибозимы, имеющие избирательность для L119 mRNA, (Bartel D and Szostak J W (1993) Science 261:1411-1418).
В дальнейшем варианте осуществления изобретения целевая экспрессия белка может быть сокращена с помощью последовательностей нуклеиновой кислоты, которые являются комплементарными к регуляторным элементам генов целевого белка, формироваться с тройной спиральной структурой и, таким образом, предотвратить транскрипцию гена (Helene С (1991) Anticancer Drug Des. 6(6):569-84; Helene С et al. (1992) Ann NY Acad Sci 660:27-36; Maher L J (1992) Bioassays 14(12):807-815).
Кассеты экспрессии изобретения и векторы, полученные из них, могут содержать дальнейшие функциональные элементы. Термин функциональный элемент должен пониматься широко, и обозначает все элементы, которые имеют влияние на производство, увеличение или функцию кассет экспрессии изобретения или векторов или организмов, полученных из них. Не ограничивающими примерами, которые можно отметить, являются:
a) Гены-репортеры или белки, кодирующие для легко измеримых белков, которые обеспечивают посредством собственной окраски или энзимной активности оценку эффективности трансформации или местоположения или времени экспрессии (Schenborn Е, Groskreutz D (1999) Mol Biotechnol 13(1):2944). Примерами, которые можно отметить, являются:
зеленые флуоресцентные белки (GFP) (Chui W L et al., Curr Biol 1996, 6:325-330; Leffel S M et al., Biotechniques. 23(5):912-8, 1997; Sheen et al. (1995) Plant Journal 8(5):777-784; Haseloff et al. (1997) Proc Natl Acad Sci USA 94(6):2122-2127; Reichel et al. (1996) Proc Natl Acad Sci USA 93(12):5888-5893; Tian et al. (1997) Plant Cell Rep 16:267-271; WO 97/41228), хлоромицетиновая трансфераза (Fromm et al. (1985) Proc Natl Acad Sci USA 82:5824-5828), люцифераза (Millar et al. (1992) Plant Mol Biol Rep 10:324-414; Ow et al. (1986) Science, 234:856-859); позволяет определять биолюминесценцию, [бета]-галактозидазу, кодирует для энзима, для которого доступны различные хромогенные субстраты, [бета]-глюкуронидаза (GUS) (Jefferson et al. (1987) EMBO J 6:3901-3907) или ген uidA, который кодирует энзим для различных хромогенных субстратов, R-локус генный белковый продукт, регулирующий производство антоцианиновых пигментов (окрашивание красным) в тканях растения и, таким образом, делает возможным прямой анализ деятельности промотора без добавления дополнительных вспомогательных или хромогенных субстратов (Dellaporta et al., In: Структура и функция хромосомы: Влияние новых концепций, 18-й Генетический симпозиум Сдэдлера 11:263-282, 1988), [бета]-лактамаза (Sutcliffe (1978) Proc Natl Acad Sci USA 75:3737-3741), энзим для различных хромогенных субстратов (например, PADAC, хромогенный цефалоспорин), xyIE генный продукт (Zukowsky et al. (1983) Proc Natl Acad Sci USA 80:1101-1105), катехол диоксигеназа, который может преобразовывать хромогенные катехолы, альфа-амилазу (Ikuta et al. (1990) Biol Technol. 8:241-242, тирозиназу (Katz et al. (1983) J Gen Microbiol 129:2703-2714), энзим, который окисляет тирозин до DOPA и допахинона, который впоследствии образует легко определяемый меланин, экворин (Prasher et al. (1985) Biochem Biophys Res Commun 126(3):1259-1268), может использоваться в кальций-чувствительном биолюминесцентном определении.
b) Источники редупликации, которые обеспечивают умножение кассет экспрессии или векторов изобретения в, например, кишечной палочке. Примерами, которые можно отметить, являются ORI (источник ДНК редупликации), pBR322 ori или P15A ori (Sambrook et al.: Molecular Cloning. A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989)
c) Элементы, например, «пограничные последовательности», которые делают возможным агробактерии-опосредованный перенос в растительные клетки для переноса и интеграции в растительный геном, такой как, например, правая или левая граница Т-ДНК или vir область.
d) Многочисленные области клонирования (MCS) позволяют и усиливают введение одной или больше последовательностей нуклеиновой кислоты.
Специалисту известны различные способы получения кассеты экспрессии изобретения. Получение кассеты экспрессии изобретения происходит, например, посредством слияния одной из контролирующих экспрессию последовательностей изобретения с представляющей интерес последовательностью нуклеиновой кислоты, подлежащей экспрессии, при необходимости с последовательностью, кодирующей транзитный пептид, который, предпочтительно, находится между промотором и соответствующей последовательностью нуклеиновой кислоты, с терминатором или сигналом полиаденилирования. Для данных целей используются обычные техники рекомбинации и клонирования (как описано выше).
Также возможно, по аналогии, произвести трансгенно экспрессию последовательности, например, путем гомологической рекомбинации, и разместить за эндогенным естественным промотором, что приведет к образованию кассеты экспрессии изобретения, которая контролирует экспрессию последовательности нуклеиновой кислоты, подлежащей трансгенной экспрессии.
В принципе, изобретение также предполагает клетки, клеточные культуры, части, такие как, например, корни, листья, семена и т.д. в случае организмов трансгенных растений, и трансгенный материал для размножения, такой как, семена или плоды, полученные из вышеописанных трансгенных организмов.
Генетические модифицированные растения изобретения, которые могут потребляться людьми и животными, могут также использоваться в качестве человеческой или животной пищи, например, в сыром виде или после обработки, способом, известным самим по себе.
Дальнейший аспект изобретения, таким образом, относится к использованию вышеописанных трансгенных организмов и клеток, клеточных культур, частей, таких как, например, корни, листья, семена и т.д. в случае организмов трансгенных растений, и трансгенный материал для размножения, такой как, семена или плоды, полученные из них, для производства человеческой или животной пищи, лекарственных препаратов или чистых химикатов.
Предпочтение, кроме того, отдается процессу для рекомбинантного производства лекарственных препаратов или чистых химикатов в организмах-хозяинах, где организм-хозяин трансформируется с одной из кассет экспрессии или векторов, описанных выше, а данная кассета экспрессии содержит один или больше структурных генов, которые кодируют для желаемого чистого химиката или катализирует биосинтез желаемого чистого химиката, культивируется трансформированный организм-хозяин, и желаемый чистый химикат отделяется от культурной среды. Данный процесс широко применяется для чистых химикатов, таких как, энзимы, витамины, аминокислоты, сахара, жирные кислоты, естественные и синтетические ароматизирующие вещества, ароматизаторы и красители. Особенно предпочтительно производство токоферолов, токотриенолов и каротеноидов. Культивирование трансформированных организмов-хозяев и отделение от организмов-хозяев или от культурной среды происходит посредством процессов, известных специалисту. Производство лекарственных препаратов, таких как, например, антитела или вакцины, описано в Hood Е Е, Jilka J М (1999). Curr Opin Biotechnol 10(4):382-6; Ma J K, Vine N D (1999). Curr Top Microbiol Immunol 236:275-92.
Все ссылки, указанные в данной спецификации настоящим объединены по ссылке, относительного полного раскрытия содержания и раскрытие содержания, в частности, указанного в данной спецификации.
ФИГУРЫ
Фигура 1. Последовательность KG_Фрагмент 86 (SEQ ID NO: 10)
Фигура 2. Последовательность 62260557.f_o13_1 кукурузы (SEQ ID NO: 11)
Фигура 3. q-RT-PCR результаты показывают целую экспрессию семени 62260557.f_o13_1 кукурузы. [Корень_dv: смесь корней на 5, 15, 30 день после опыления (DAP); Лист_dv: смесь листьев на 5, 15, 30 день DAP; Початок: смесь початка на 5 и 10 DAP; целые семена: смесь целых семян на 15, 20, 30 DAP; Эндосперм: смесь эндосперма на 15, 20, 30 DAP; Зародыш: смесь зародыша на 15, 20, 30 DAP; Корень_V2+V4: смесь корня на стадиях V2 и V4; Побег/лист_V2+V4: смесь побега V2 и листьев V4; Цветок_GS: смесь цветка и удвоенных семян]
Фигура 4. Соответствующая CDS последовательность KG_Фрагмента 86 (SEQ ID NO:4)
Фигура 5. Аминокислотная последовательность расшифрованного белка соответствующего гена KG_Фрагмента 86 (SEQ ID NO: 5)
Фигура 6. Последовательность AZM5 7833 (SEQ ID NO: 128), содержащая рассчитанную последовательность и верхнюю область промотора. 5′ нетранслируемая область UTR (127 п.о.) была определена путем сравнения геномной последовательности с EST последовательностью кукурузы и обозначена курсивом, предсказанная рамка открытого считывания подчеркнута, праймеры, использующиеся для изолирования области промотора выделены жирным шрифтом.
Фигура 7. Последовательность промотора KG86 (p-KG86) (SEQ ID NO: 1)
Фигура 8. Диаграмма вектора RKF126
Фигура 9. Последовательность RKF126 (SEQ ID NO: 56)
Фигура 10. GUS экспрессия в различных тканях на разных стадиях развития, получена с помощью p-KG86 в трансгенной кукурузе с RKF126
Фигура 11. A) Последовательности ZM1s61973481 (SEQ ID NO: 57), B) ZM1s61221800 (SEQ ID NO: 58 и C) ZM1s62042561 (SEQ ID NO: 59)
Фигура 12. q-RT-PCR результаты показывают целую экспрессию семени MAWS42 [Корень_dv: смесь корней на 5, 15, 30 день после опыления (DAP); Лист_dv: смесь листьев на 5, 15, 30 день DAP; Початок: смесь початка на 5 и 10 DAP; целые семена: смесь целых семян на 15, 20, 30 DAP; Эндосперм: смесь эндосперма на 15, 20, 30 DAP; Зародыш: смесь зародыша на 15, 20, 30 DAP; Корень_V2+V4: смесь корня на стадиях V2 и V4; Побег/лист_V2+V4: смесь побега V2 и листьев V4; Цветок_GS: смесь цветка и удвоенных семян.]
Фигура 13. q-RT-PCR результаты показывают целую экспрессию семени MAWS45 [Корень_dv: смесь корней на 5, 15, 30 день после опыления (DAP); Лист_dv: смесь листьев на 5, 15, 30 день DAP; Початок: смесь початка на 5 и 10 DAP; целые семена: смесь целых семян на 15, 20, 30 DAP; Эндосперм: смесь эндосперма на 15, 20, 30 DAP; Зародыш: смесь зародыша на 15, 20, 30 DAP; Корень_V2+V4: смесь корня на стадиях V2 и V4; Побег/лист_V2+V4: смесь побега V2 и листьев V4; Цветок_GS: смесь цветка и удвоенных семян.]
Фигура 14. Соответствующая CDS последовательность MAWS42 (SEQ ID NO: 6)
Фигура 15. Аминокислотная последовательность ZmTIP3-1 соответствующего гена MAWS42 (SEQ ID NO: 7)
Фигура 16. Соответствующая CDS последовательность MAWS45 (SEQ ID NO: 8)
Фигура 17. Аминокислотная последовательность соответствующего гена MAWS45 (SEQ ID NO: 9)
Фигура 18. Последовательность AZM5_17960 (SEQ ID NO: 70) и AZM5_6324 (SEQ ID NO: 71), содержащая предсказанную CDS последовательность (ATG выделена жирным шрифтом и подчеркнута), предпочтительный 5′-UTR (выделен курсивом), и предполагаемая промоторная последовательность. 5′ UTR последовательности были определены с помощью сравнения геномной последовательности с кукурузой EST.
Фигура 19. Последовательность промотора MAWS42 (p-MAWS42), SEQ ID NO: 2 и промотор MAWS45 (p-MAWS45), SEQ ID NO: 3
Фигура 20. Диаграмма RTP1052
Фигура 21. Последовательность RTP1052 (SEQ ID NO: 116)
Фигура 22. Диаграмма RTP1057
Фигура 23. Последовательность RTP1057 (SEQ ID NO: 117)
Фигура 24. GUS экспрессия в различных тканях на разных стадиях развития, получена с помощью p-MAWS42 в трансгенной кукурузе с RTP1052
Фигура 25. GUS экспрессия в различных тканях на разных стадиях развития, получена с помощью p-MAWS45 в трансгенной кукурузе с RTP1057
ПРИМЕРЫ
Изобретение сейчас будет проиллюстрировано следующими Примерами, которые, что бы ни было, не направлены на ограничение сферы применения.
Пример 1: Определение и подтверждение промотора KG86 всего семени кукурузы
Определение транскрипта KG86
Профильный анализ генной экспрессии кукурузы был проведен с использованием частного поставщика технологии сравнительной экспрессии (Keygene N.V., P.O.Box 216, 6700 АЕ Wageningen, The Netherlands), с помощью батареи образцов РНК из 23 тканей кукурузы, генерированных BASF (Таблица 1). Среди AFLP дисков, определенных как имеющие экспрессию целого семени, был фрагмент 231 п.о., обозначенный «KG_Фрагмент 86». Последовательность KG_Фрагмента 86 показана на Фигуре 1.
Определение гена, соответствующего KG_Фрагменту 86
Последовательность KG_Фрагмента 86 использовалась в качестве вопроса для поиска BLASTN по сравнению с внутренней базой данных BASF, HySeq All EST. Доступ, 62260557.f_o13_1 кукуруза, показывающий 97% совпадений с KG_Фрагментом 86 был определен, как имеющий самое большое сходство с KG_Фрагментом 86. Последовательность 62260557.f_o13_1 кукурузы показана на Фигуре 2.
Подтверждение схемы экспрессии 62260557.f_o13_1 кукурузы с использованием количественной полимеразной цепной реакции с обратной транскриптазой (q-RT-PCR)
Для подтверждения схемы нативной экспрессии 62260557.f_o13_1 кукурузы, количественная обратная транскрипция PCR (q-RT-PCR) проводилась с использованием целой РНК, изолированной от тех же материалов, которые использовали для профилирования экспрессии AFLP (Таблица 1).
Праймеры для q-RT-PCR были разработаны, основываясь на последовательностях 62260557.f_o13_1 кукурузы и KG_Фрагменте 86 с использованием программного пакета Вектор NTI (Invitrogen, Carlsbad, СА, США). Два комплекта праймеров использовали для амплификации 62260557.f_o13_1 кукурузы (Таблица 2). Ген глицеральдегида-3-фосфата дегидрогеназы (GAPDH) служил в качестве контроля за целями нормализации.

q-RT-PCR проводили с использованием обратной траскриптазы Superscript III (Invitrogen, Carlsbad, СА, США) и SYBR Green QPCRMaster Mix (Eurogentec, San Diego, СА, США) в системе обнаружения последовательности ABI Prism 7000. кДНК синтезировали с помощью 2-3 мкг целой РНК и 1 мкл обратной транскриптазы в 20 мкл объема. кДНК разбавляли до ряда концентраций (15-20 нг/мкл). От 30 до 40 нг кДНК использовали для количественной ПЦР (кПЦР) в 30 мкл объема с SYBR Green Q PCR Master Mix, согласно инструкции производителя. Условия термоциклирования были следующими: инкубирование при 50°C в течение 2 минут, денатурирование при 95°C в течение 10 минут, прохождение 40 циклов при 95°C в течение 15 секунд и 60°C в течение 1 минуты для амплификации. После последнего цикла амплификации проводили анализ диссоциации кривой для проверки того, что амплификация прошла специфически, и во время процесса амплификации не был генерирован димерный продукт праймера. Конститутивный ген глицеральдегид-3-фосфат-дегидрогеназа (GAPDH, последовательности праймера в Таблице 2) использовали в качестве эндогенного эталонного гена для нормализации расчета с использованием метода оценки Сравнительного Ct (пороговый цикл). Значение ΔCT было получено путем вычитания значения Ct гена GAPDH от значения гена-«кандидата» (62260557.f_o13_1 кукурузы), и относительное количество транскрипции (уровень экспрессии) гена-«кандидата» было выражено как 2-ΔСТ. Результаты q-RT-PCR обобщены на Фигуре 3. Оба набора праймеров дали подобные схемы экспрессии, которые эквивалентны схемам экспрессии, полученным из данных AFLP.
Аннотация KG_Фрагмента 86
Кодирующая последовательность KG_Фрагмента 86 аннотировалась, основываясь на результаты кремния, полученным как при поиске BLASTX последовательности кукурузы EST 62260557.f_o13_1, по сравнению с базой данных белков GenBank (nr), так и результатов трансляции кремния последовательности, с использованием пакета программ Вектор NTI. Последовательность кукурузы 62260557.f_o13_1 кодирует неполноценный белок с самой высокой гомологией к гену риса, аннотированному как гипотетический белок OsI_025737 (GenBank Accession: EAZ04505.1). 15 верхних гомологических последовательностей, определенные в запросе BlastX, представлены в Таблице 3.
Последовательность CDS KG_Фрагмента 86 показана на Фигуре 4, а расшифрованная амонокислотная последовательность показана на Фигуре 5.
Определение области промотора
Для определения промотора, последовательность, расположенная выше инициирующего кодона ожидаемого KG_Фрагмента 86 гена, была определена как промотор p-KG86. Чтобы определить данную область промотора, последовательность 62260557.f_ol3_l была нанесена на карту патентованной прикладной ботаникой базы данных последовательности геномной ДНК, PUB_tigr_maize_genomic_partial_5.0.nt. Была определена одна последовательность геномной ДНК кукурузы AZM5 7833 (5084 п.о.). Последовательность 5084 п.о., содержала CDS KG_Фрагмента 86 и больше, чем 2 т.н. выше последовательности ATG инициирующего кодона данного гена (Фигура 6).
Изолирование области промотора посредством PCR амплификации
Область путативного промотора была изолирована с помощью геномного PCR, с использованием следующих праймеров последовательности:
Прямой праймер: tcccgtgtccgtcaatgtgata (SEQ ID NO: 18)
Обратный праймер: Ggactcacgagctgaggctcgg (SEQ ID NO: 19)
Ожидаемый фрагмент 1198 п.о. был амплифицирован из геномной ДНК кукурузы и определен как промотор KG86 (p-KG86). Последовательность p-KG86 показана на Фигуре 7.
PLACE анализ промотора KG86
Мотив, действующий в цис-положении, в области промотора 1198 п.о. KG86, был определен с помощью PLACE (база данных растительных, действующих в цис-положении, регулирующих ДНК элементов), посредством набора базы данных Genomatix. Результаты перечислены в Таблице 4. Несмотря на определение предполагаемого согласования TATA бокса в идущей вперед нити, был обнаружен мотив бокса ЦААТ в позиции нуклеотида 701-705 в идущей вперед нити.
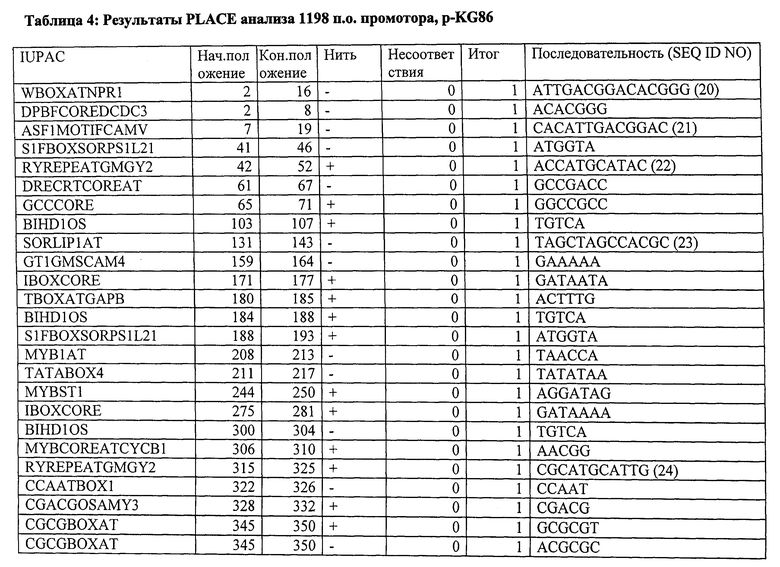
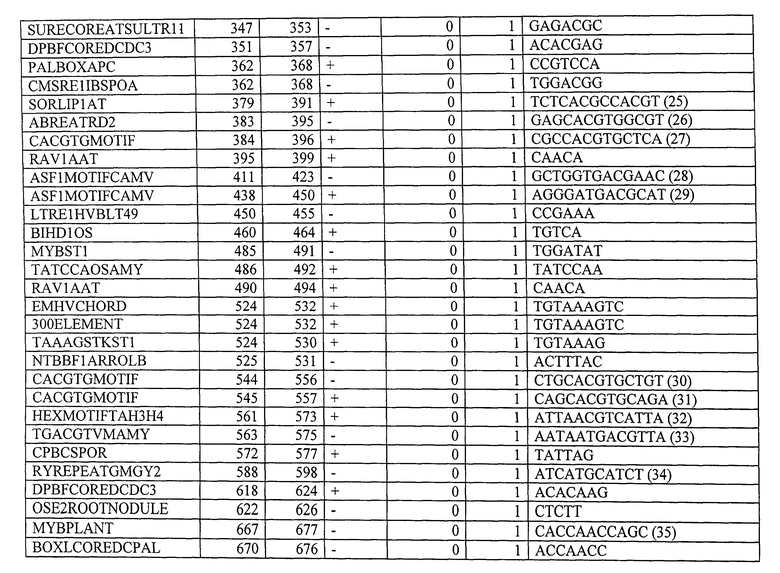
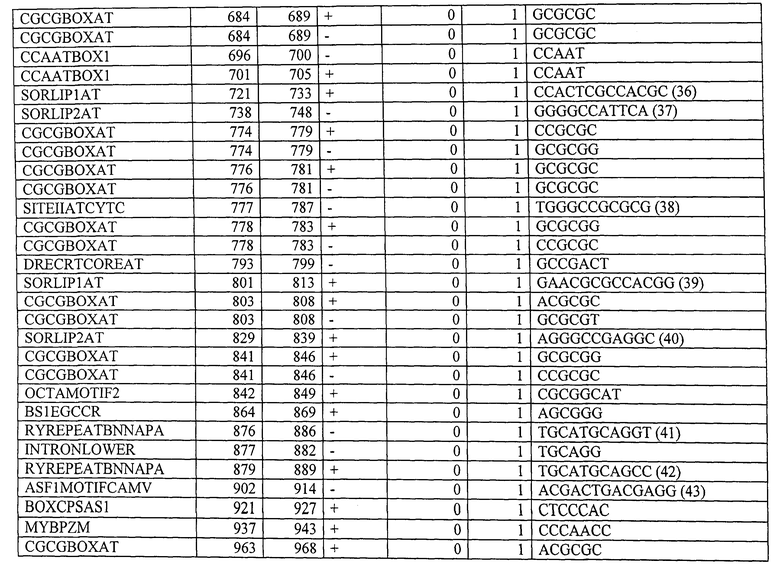
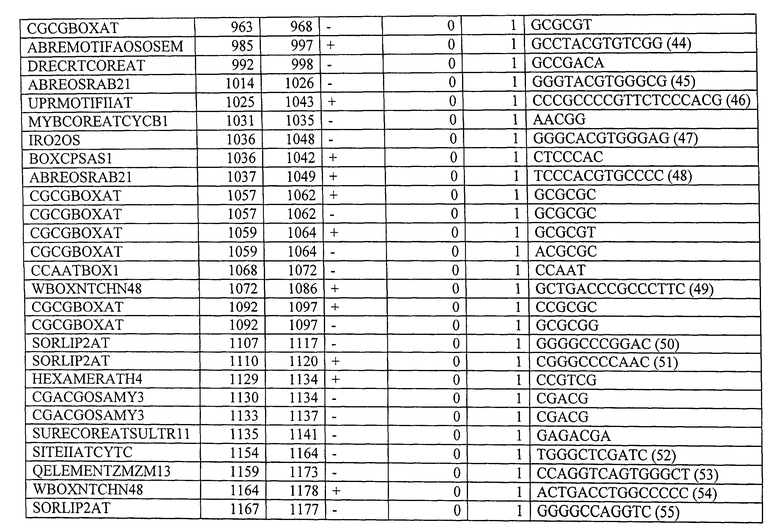
Конструкция бинарного вектора для трансформации кукурузы для оценки функции p-KG86
Для усиления субклонирования, фрагмент промотора 1198 п.о. был модифицирован путем добавления сайта рестриктивного фермента на 5′ конец и BsiWI сайта на 3′ конец. Фрагмент промотора PacI-pKG86-BsiWI был расщеплен и привязан к PacI и BsiWI, расщепленному BPS основным бинарным вектором HF84. HF84 содержит растительный селектируемый маркер кассеты экспрессии (p-Ubi::c-EcEsdA::t-NOS), а также промоторную оценочную кассету, которая состоит из многочисленных сайтов встраивиния для введения путативных промоторов посредством PacI и BsiWI, интрона MET1-1 риса для поставки интрон-опосредованного усиления в клетки однодольного растения, ген-репортер GUS и терминатор NOS. Получившийся бинарный вектор, содержащий кассету экспрессии p-KG86::i-MET1::GUS::t-NOS был назван RKF126 и использовался для оценки схемы экспрессии, управляемой промотором p-KG86. Фигура 8 представляет собой диаграмму RKF126. Последовательность бинарного вектора RKF126 показана на Фигуре 9.
Оценка промотора в трансгенной кукурузе с RKF126
Схемы экспрессии и уровни, управляемые промотором p-KG86 были измерены с использованием гистохимического анализа с соблюдением протокола в науке (Jefferson 1987). Траснформация кукурузы проводилась с использованием агробактерии-опосредованной трансформационной системы. Десять и пять событий уникальной копии для растений Т0 и Т1 были выбраны для анализа промотора. Экспрессия GUS измерялась на различных стадиях развития:
1) Корни и листья на 5-стадии листа
2) Стебель на V-7 стадии
2) Листья, оболочка и «рыльца» на стадии цветения (первое появление рыльца)
3) Колоски/кисточки (при опылении)
5) Початок и зерна на 5, 10, 15, 20 и 25 день после опыления (DAP)
Результаты указывают, что промотор p-KG86 RKF126, выраженный специфично в пыльце и целых семенах (Фигура 10).

Пример 2: Определение и подтверждение промотора всего семени кукурузы MAWS42 и MAWS45
Определение транскрипта MAWS42 и MAWS45
Было проведено микроматричное исследование для определения транскриптов с целой экспрессией семени в кукурузе, с использованием той же панели образцов РНК кукурузы, показанных в Таблице 1. 23 маркированные РНК данных тканей кукурузы были скрещены отдельно от наших 23, сконструированных по заказу, аффиметрических чипов BPS кукурузы, маркированных с флуоресцентными стрептавидиновыми антителами, промытыми, окрашенными и просканированными, как указано в Техническом руководстве аффимитрического анализа экспрессии.
Данные гибридизации чипа анализировали с использованием программного обеспечения Genedata Specialist, а относительный уровень экспрессии определяли, основываясь на интенсивности сигнала гибридизации каждой ткани.
Три из пробных наборов чипов кукурузы BPS были выбраны в качестве кандидатов транскриптов, показывающих 3-8 раз более высокая экспрессия в целых семенах, по сравнению с другими тканями: ZM1s61973481_at, ZM1s61221800_s_at и ZM1s62042561_at. Консенсусные последовательности ZM1s61973481_at, ZM1s61221800_s_at и ZM1s62042561_at показаны на Фигуре 11.
Предварительный анализ последовательности, указывает, что ZM1s61221800 включена в ZM1s62042561, поэтому, мы считаем, что ZM1s61221800 и ZM1s62042561 представляют собой тот же ген; дальнейшие исследования данного гена проводили на основе ZM1s62042561. Для удобства презентации, мы назвали ZM1s61973481 в качестве кандидата MAWS42 и ZM1s62042561 как MAWS45.
Подтверждение схемы экспрессии MAWS42 и MAWS45 с помощью количественной полимеразной цепной реакции с обратной транскриптазой (qRT-PCR)
Подтверждение схем нативной экспрессии MAWS42 и MAWS45 проводилось посредством количественной обратной транскрипции PCR (q-RT-PCR) с использованием целой РНК, изолированной от тех же материалов, которые использовали для исследования чипа (Таблица 1).
Праймеры для q-RT-PCR были разработаны, основываясь на последовательностях ZM1s61973481 для MAWS42 и ZM1s62042561 для MAWS45 с использованием программного пакета Вектор NTI. Два комплекта праймеров использовали для PCR амплификации каждого гена. Последовательности праймеров указаны в Таблице 5. Ген глицеральдегида-3-фосфата дегидрогеназы (GAPDH) служил в качестве контроля за целями нормализации.

q-RT-PCR проводили с использованием обратной траскриптазы Superscript III (Invitrogen, Carlsbad, CA, США) и SYBR Green QPCRMaster Mix (Eurogentec, San Diego, CA, США) в системе обнаружения последовательности ABI Prism 7000. кДНК синтезировали с помощью 2-3 мкг целой РНК и 1 мкл обратной транскриптазы в 20 мкл объема. кДНК разбавляли до ряда концентраций (15-20 нг/мкл). От 30 до 40 нг кДНК использовали для количественной ПЦР (кПЦР) в 30 мкл объема с SYBR Green QPCR Master Mix, согласно инструкции производителя.
Условия термоциклирования были следующими: инкубирование при 50°C в течение 2 минут, денатурирование при 95°C в течение 10 минут, прохождение 40 циклов при 95°C в течение 15 секунд и 60°C в течение 1 минуты для амплификации. После последнего цикла амплификации проводили анализ диссоциации кривой для проверки того, что амплификация прошла специфически, и во время процесса амплификации не был генерирован димерный продукт праймера. Конститутивный ген глицеральдегид-3-фосфат-дегидрогеназа (GAPDH, последовательности праймера в Таблице 2) использовали в качестве эндогенного эталонного гена для нормализации расчета с использованием метода оценки Сравнительного Ct (пороговый цикл). Значение ΔCT было получено путем вычитания значения Ct гена GAPDH от значения генов-«кандидатов». Относительное количество транскрипции (уровень экспрессии) гена-«кандидата» было выражено как 2-ΔCT. Результаты q-RT-PCR обобщены на Фигуре 12 и Фигуре 13. Оба набора праймеров дают подобные схемы экспрессии, которые были получены при микроматричном исследовании.
Аннотация MAWS42 и MAWS45
Кодирующую последовательность, соответствующую генам MAWS42 и MAWS45 аннотировали, основываясь на результатах кремния, полученных как при BLASTX чипа консенсусной последовательности ZM1s61973481 и ZM1s62042561, по сравнению с базой данных белков GenBank (nr), так и результатов трансляционной программы с использованием пакета программ Вектор NTI. ZM1s61973481 кодирует частично внутренний белок тонопласт кукурузы 3-1(ZmTIP3). CDS ZmTIP3-1 (GenBank Accession:NP_0011050321) показано на Фигуре 14, транслированная аминокислотная последовательность и 15 верхних гомологичных последовательностей из запроса BLASTX представлены в Таблице 6.
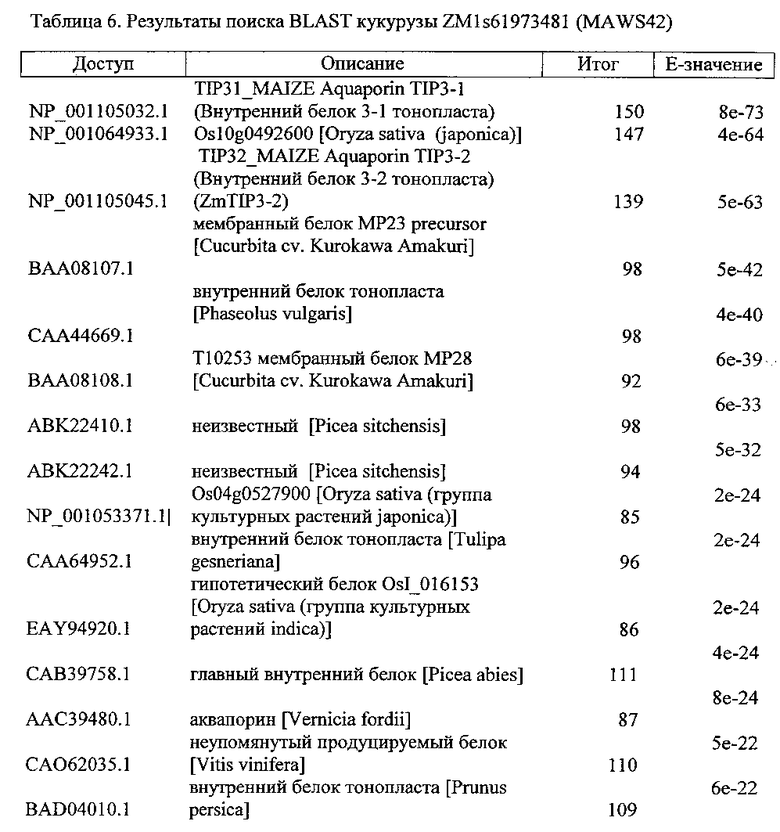
ZM1s62042561(MAWS45) кодирует неполноценный белок, имеющий самую высокую гомологию с неизвестным белком кукурузы (GenBank Accession: ACF84237.1), CDS данного гена показан на Фигуре 16, транслированная аминокислотная последовательность показана на Фигуре 17, 15 верхних гомологичных последовательностей из запроса BLASTX представлены в Таблице 7.
Определение области промотора
Последовательности выше инициирующих кодонов соответствующих генов MAWS42 и MAWS45 были определены как путативные промоторы р-MAWS42 и p-MAWS45. Чтобы определить данные путативные области промотора, последовательности ZM1s61973481 и ZM1s62042561 были нанесены на карту BASF патентованной прикладной ботаникой базы данных последовательности геномной ДНК, PUB_tigr_maize_genomic_partial_5.0 nt. Две последовательности геномной ДНК кукурузы были определены AZM5_17960 (3985 п.о.) и AZM5_6324 (4565 п.о.), соответственно. Последовательность AZM5_17960 имеет около 1 т.н. последовательности выше ожидаемого CDS соответствующего гена MAWS42 и AZM5_6324 имеет около 1,5 т.н. последовательности выше ожидаемого CDS соответствующего гена MAWS45. Данные последовательности, расположенные выше, считались путативным промотором MAWS42 (p-MAWS42) и промотором MAWS45 (p-MAWS45). На Фигуре 18 показаны последовательности AZM5_17960 и последовательность AZM5_6324.
Изолирование области промотора посредством PCR амплификации
Последовательности путативного промотора были изолированы геномной PCR, с использованием праймеров последовательности, указанных в Таблице 8. Фрагмент 1008 п.о. AZM5_17960 и фрагмент 1492 п.о. AZM5_6324 были амплифицированы из геномной ДНК кукурузы. Данные фрагменты были названы промотором MAWS42 (p-MAWS42) и промотором MAWS45 (p-MAWS45), соответственно. Последовательности p-MAWS42 и p-MAWS45 показаны на Фигуре 19.
PLACE анализ промоторов MAWS42 и MAWS45
Мотив, действующий в цис-положении, в областях промотора 1008 п.о. P-MAWS42 и 1492 п.о. p-MAWS45, был определен с помощью PLACE (база данных растительных, действующих в цис-положении, регулирующих ДНК элементов), посредством набора базы данных Genomatix. Результаты перечислены в Таблице 9 и Таблице 10.
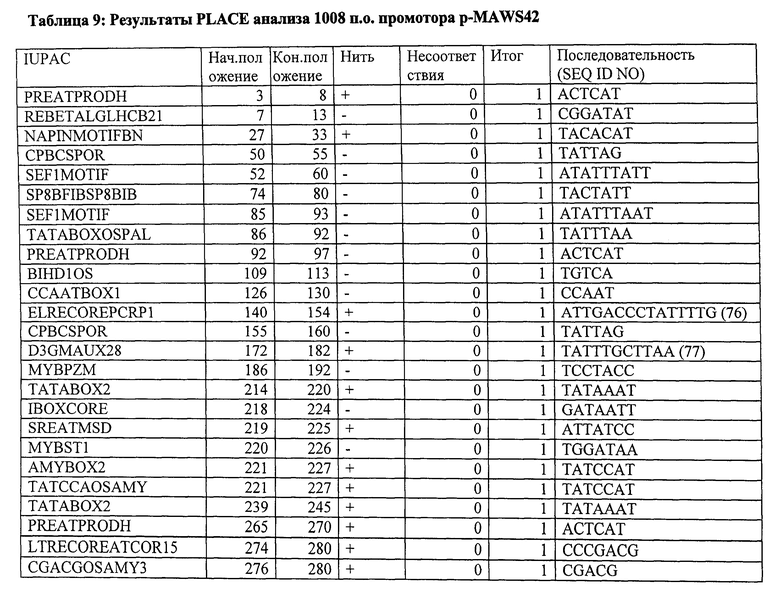
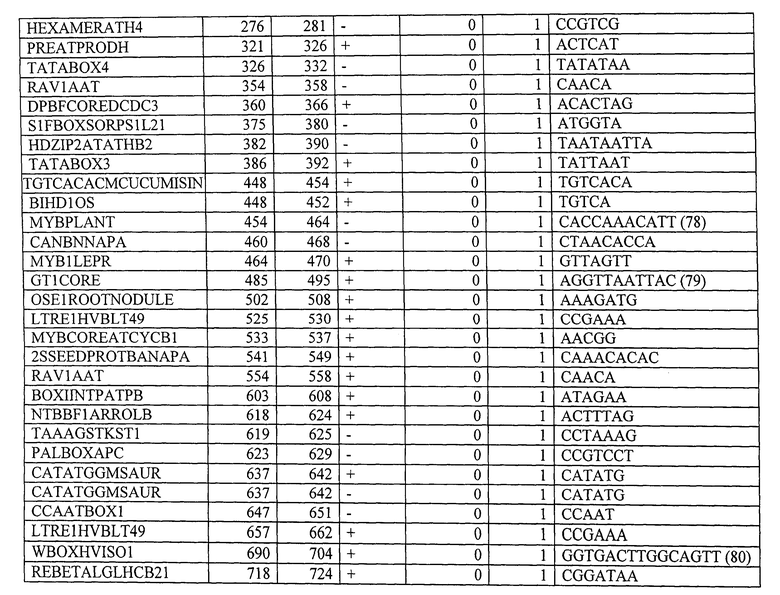
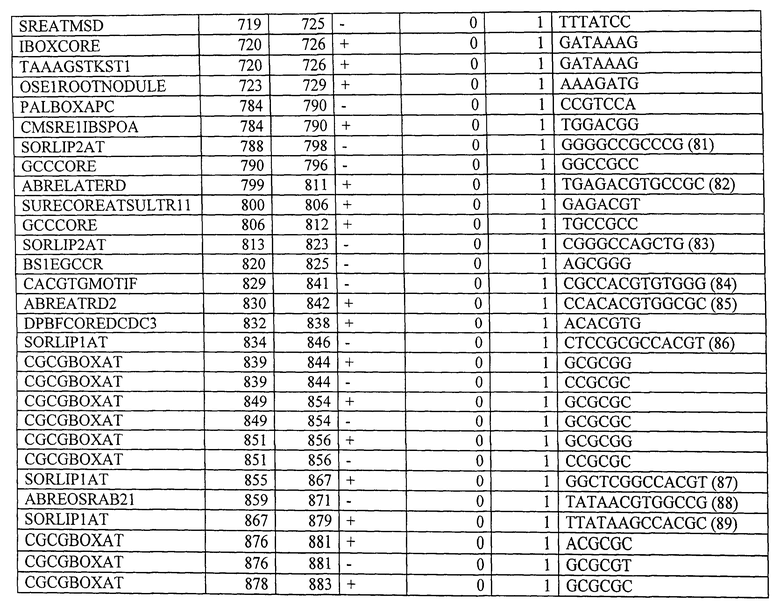
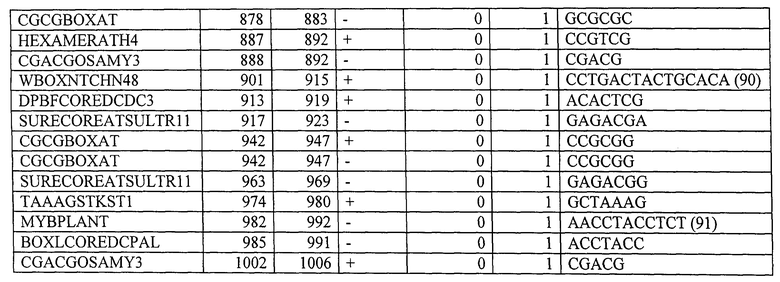
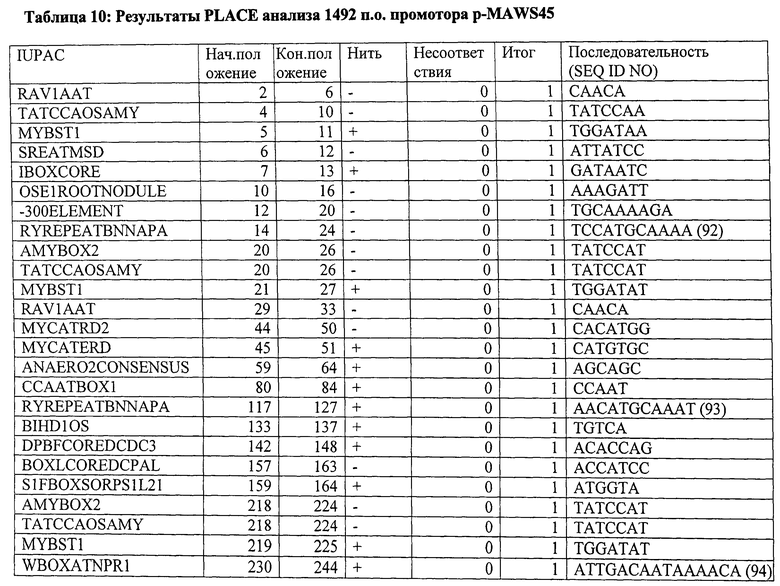
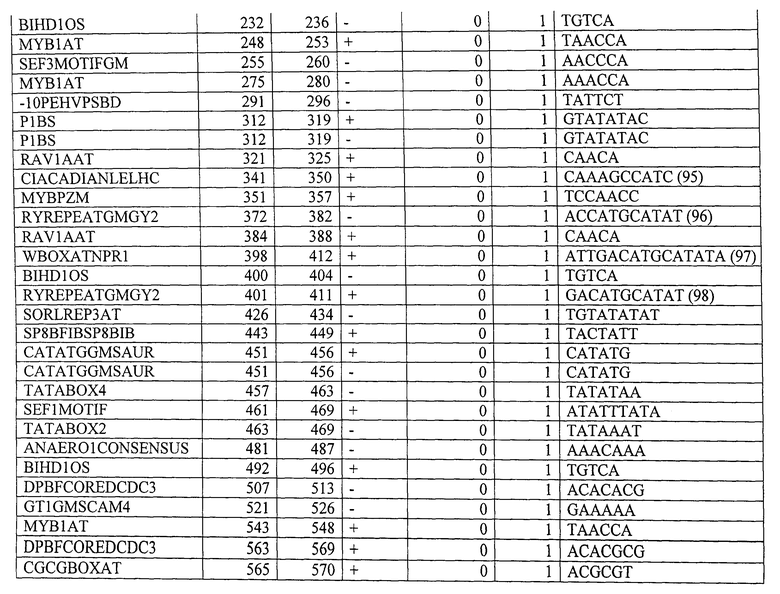
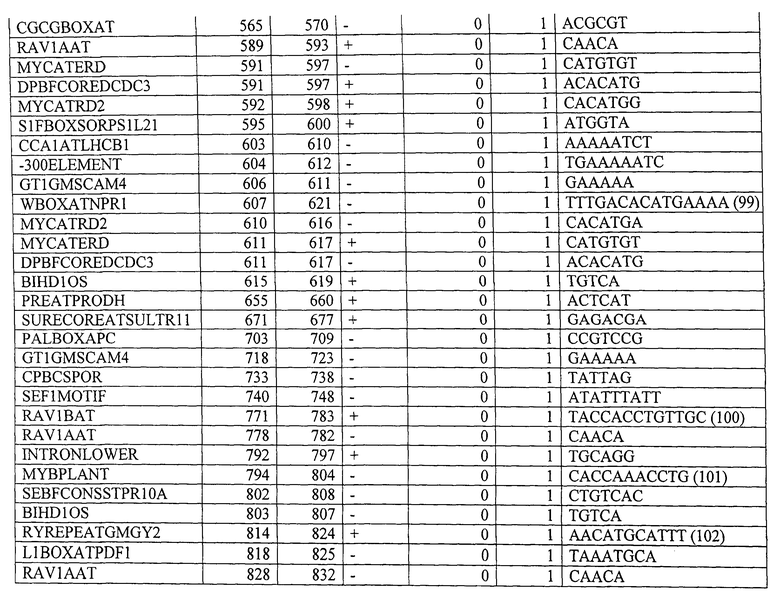
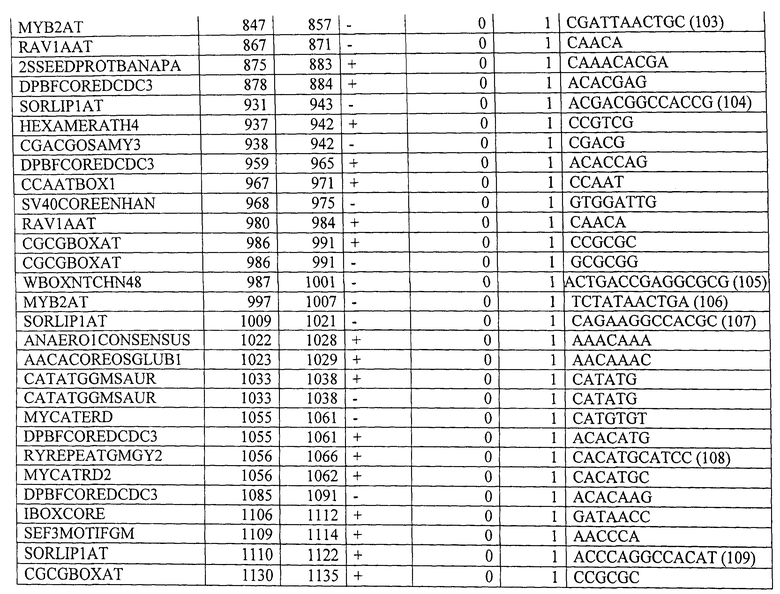
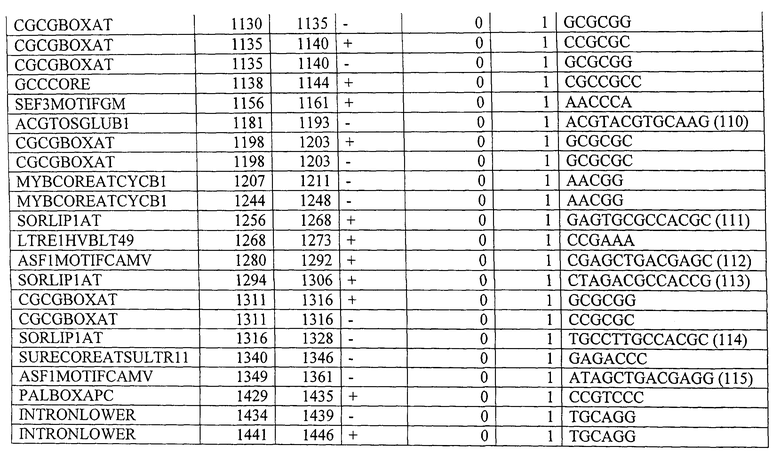
Конструкция бинарного вектора для трансформации кукурузы для оценки функции p-MAWS42 и p-MAWS45
Фрагмент промотора 1008 п.о. p-MAWS42 был амплифицирован PCR, включая сайт рестриктивного фермента Swal на 5′ конце и BsiWI сайт на 3′ конце. Полученный фрагмент был расщеплен и привязан к SwaI и BsiWI, расщепленному BPS основным бинарным вектором СВ1006. Плазмида СВ1006 является растительным трансформационным вектором, который содержит растительный селектируемый маркер кассеты экспрессии (p-Ubi::c-ZmAHASL2::t-NOS), а также промоторную оценочную кассету, которая состоит из многочисленных сайтов встраивиния для введения путативных промоторов посредством сайтов SwaI и BsiWI, интрона MET1-l риса для поставки интрон-опосредованного усиления в клетки однодольного растения, ген-репортер GUS и терминатор NOS. Получившийся бинарный вектор, содержащий кассету экспрессии p-MAWS42::i-MET1::GUS::t-NOS назвали RTP1052 и использовали для оценки схемы экспрессии, управляемой промотором p-MAWS42. Фигура 20 представляет собой диаграмму RTP1052. Последовательность бинарного вектора RTP1052 показана на Фигуре 21.
Фрагмент промотора 1492 п.о. p-MAWS45 был амплифицирован PCR, включая сайт рестриктивного фермента SwaI на 5′ конце и BsiWI сайт на 3′ конце. Полученный фрагмент был расщеплен и привязан к SwaI и BsiWI, расщепленному BPS основным бинарным вектором СВ1006. Плазмида СВ1006 является растительным трансформационным вектором, который содержит растительный селектируемый маркер кассеты экспрессии (p-Ubi::c-ZmAHASL2::t-NOS), а также промоторную оценочную кассету, которая состоит из многочисленных сайтов встраивиния для введения путативных промоторов посредством сайтов SwaI и BsiWI, интрона МЕТ1-1 риса для поставки интрон-опосредованного усиления в клетки однодольного растения, ген-репортер GUS и терминатор NOS. Получившийся бинарный вектор, содержащий кассету экспрессии p-MAWS42::i-MET1::GUS::t-NOS назвали RTP1057 и использовали для оценки схемы экспрессии, управляемой промотором p-MAWS45. Фигура 22 представляет собой диаграмму RTP1052. Последовательность бинарного вектора RTP1057 показана на Фигуре 23.
Оценка промотора в трансгенной кукурузе с RTP1052 или RTP1057
Схемы экспрессии и уровни, управляемые промоторами p-MAWS42 или p-MAWS45, были измерены с использованием гистохимического анализа с соблюдением протокола в науке (Jefferson 1987). Траснформацию кукурузы проводили с использованием агробактерия-опосредованной трансформационной системы. Десять и пять событий уникальной копии для растений Т0 и Т1 были выбраны для анализа промотора. Экспрессию GUS измеряли на различных стадиях развития:
1) Корни и листья на 5-стадии листа
2) Стебель на V-7 стадии
2) Листья, оболочка и «рыльца» на стадии цветения (первое появление рыльца)
3) Колоски/кисточки (при опылении)
5) Початок и зерна на 5, 10, 15, 20 и 25 день после опыления (DAP)
Результаты показали, что как промотор p-MAWS42 RTP1052, так и промотор p-MAWS45 RTP1057 экспрессировали специфично в пыльце и целых семенах (Фигуры 24 и 25).

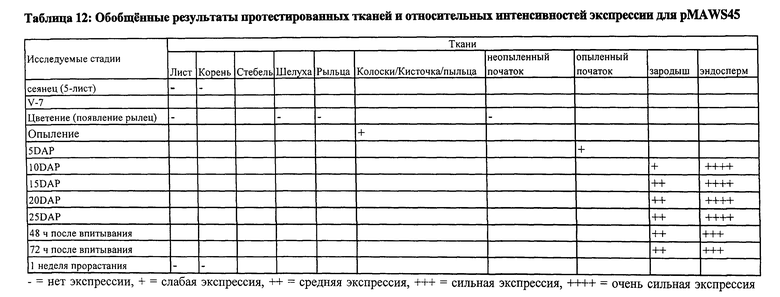
Пример 3:
Последовательность промотора pKG86 (SEQ ID NO: 1) исследовали на короткие открытые рамки считывания, которые могут придавать аллергенность или токсичность, с использованием базы данных, содержащей аллергенные и токсичные пептиды и полипептиды. Было определено, что короткие открытые рамки считывания проявляют гомологию к пептидам или полипептидам, содержащимся в указанной базе данных. Во избежание экспрессии пептидов, которые могут быть токсичными или аллергенными, последовательность pKG86 была модифицирована. Получившиеся промоторы pKG86_12A (SEQ ID NO: 129), pKG86_14A (SEQ ID NO: 130) и pKG86_15A (SEQ ID NO:131) были функционально связаны с геном-репортером и трансформированы в кукурузу обыкновенную для анализа экспрессии.
































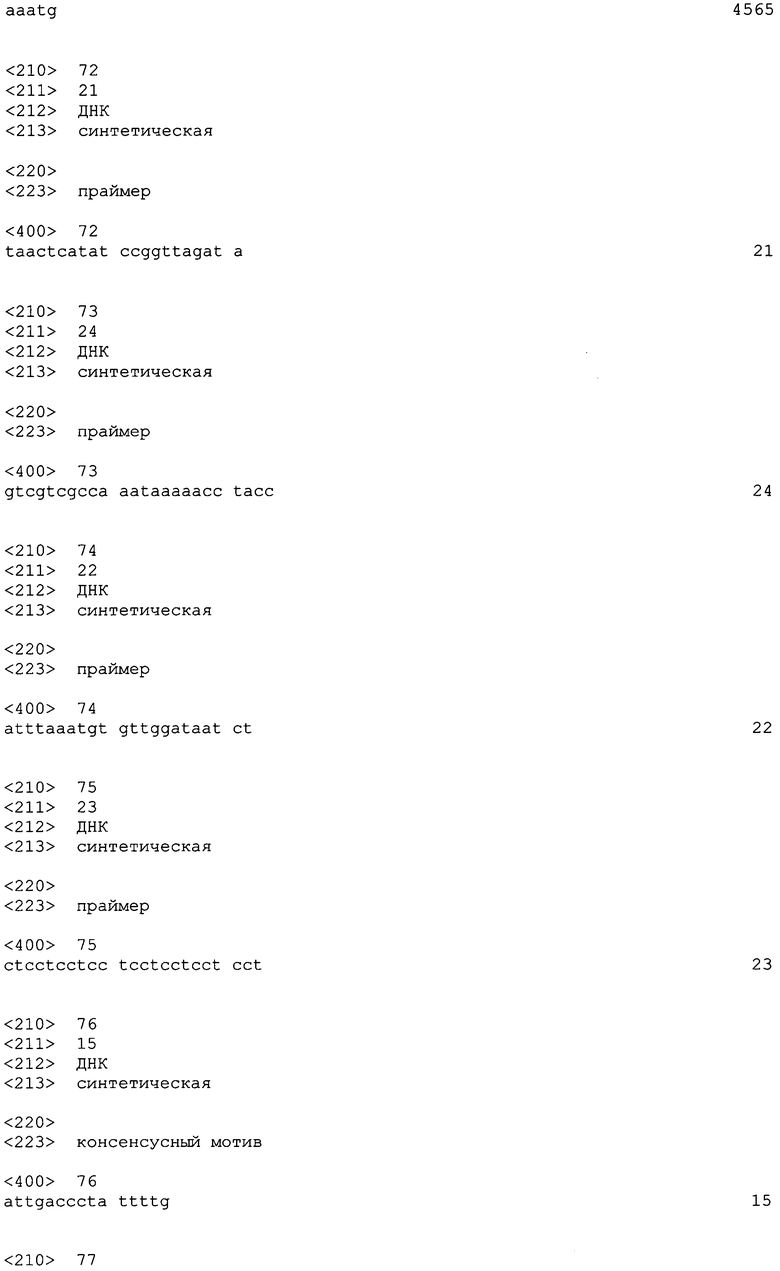





































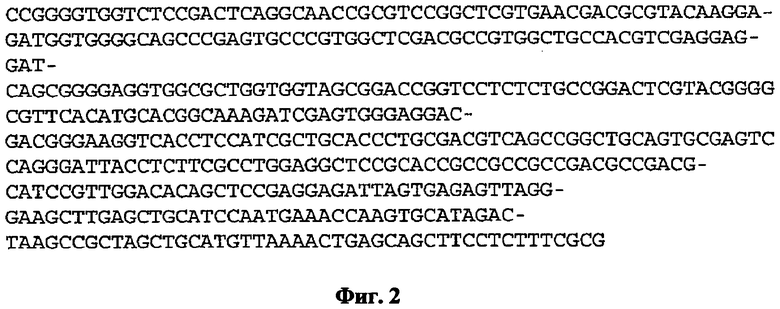
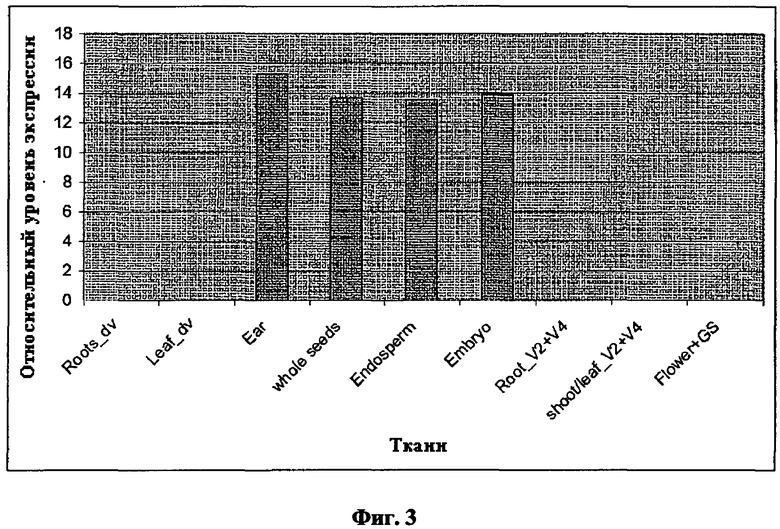






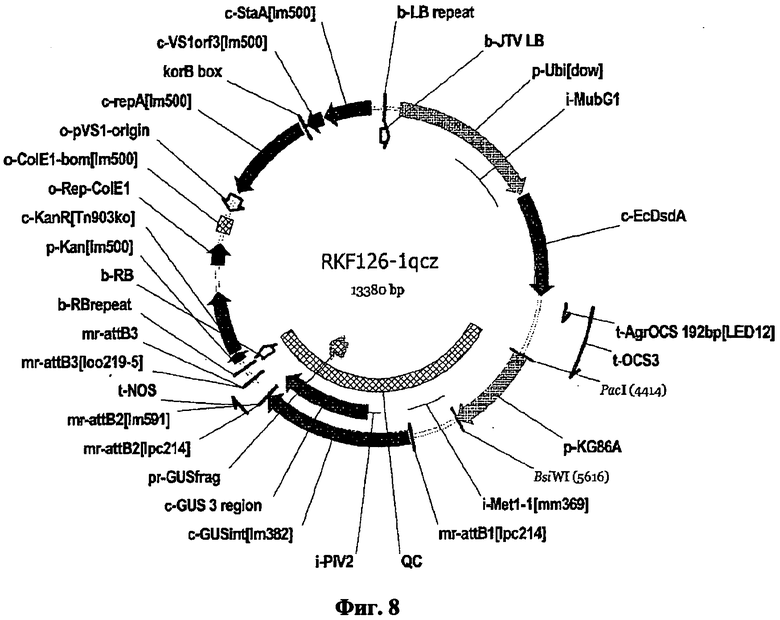






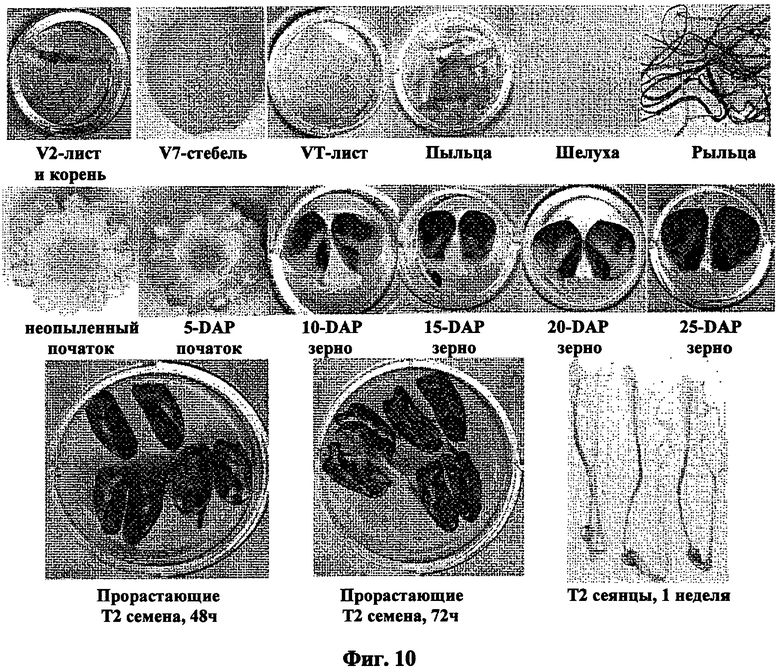

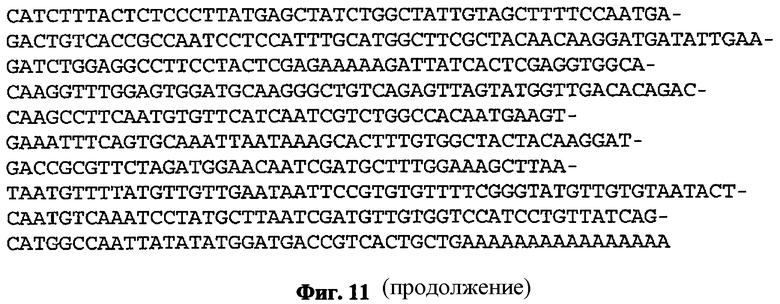
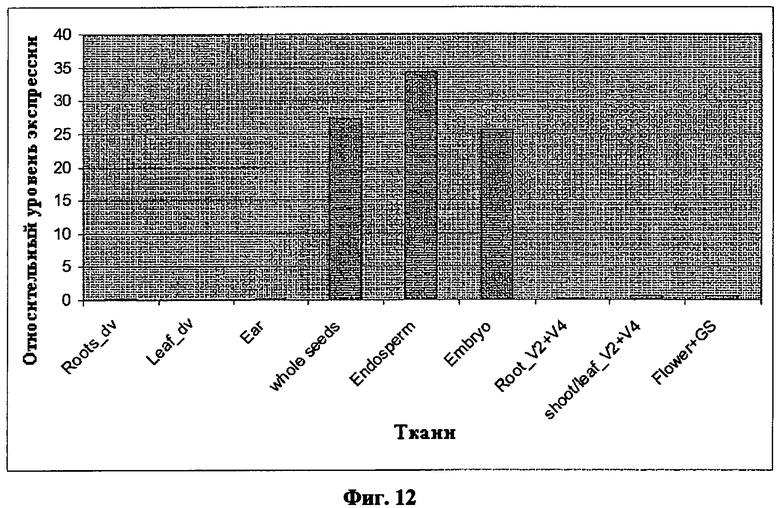
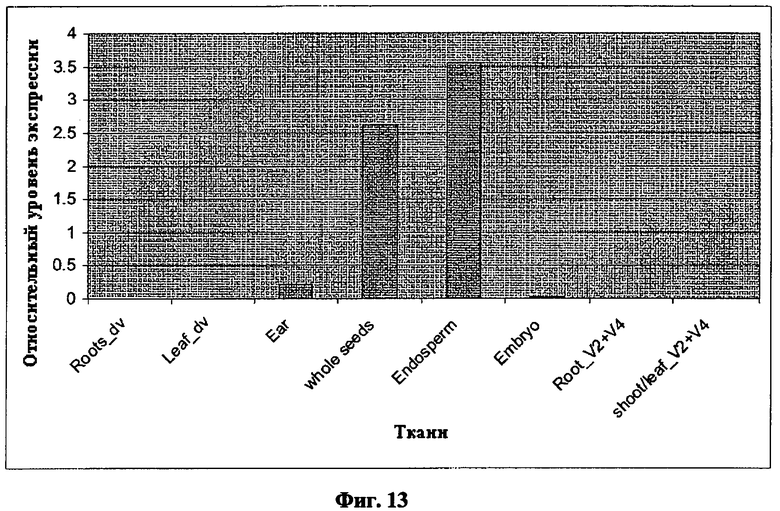
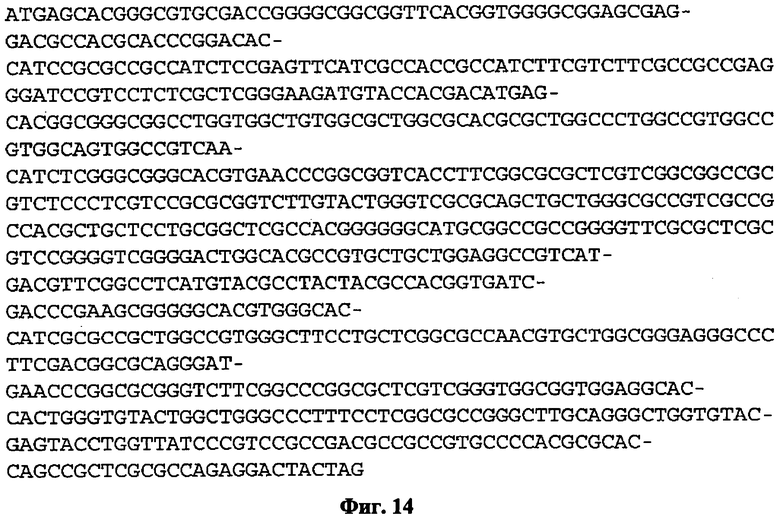

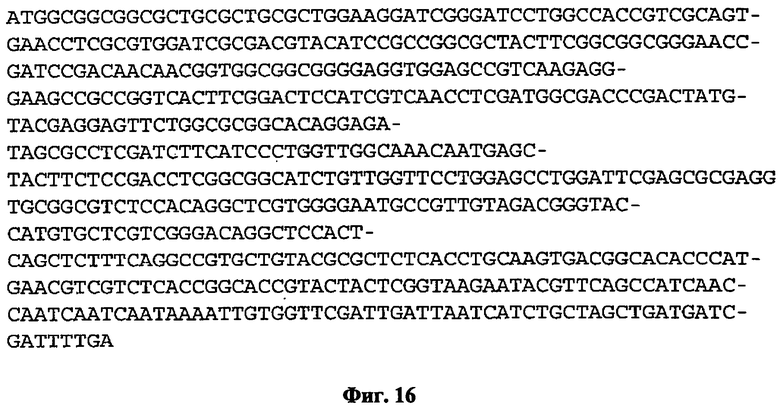






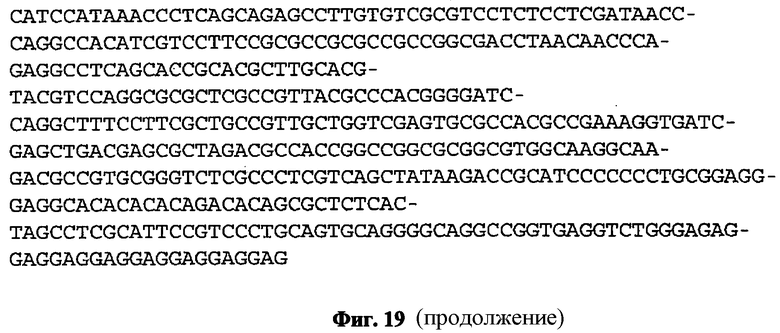
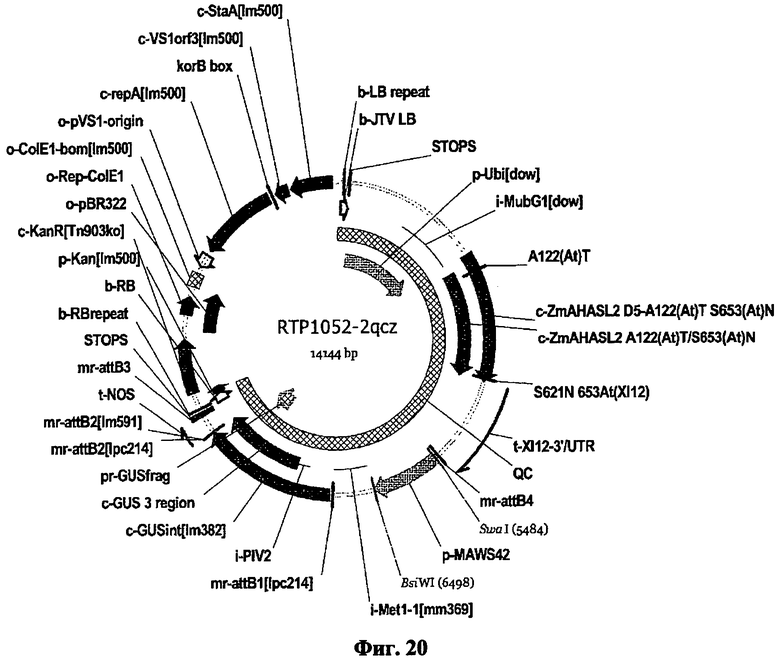






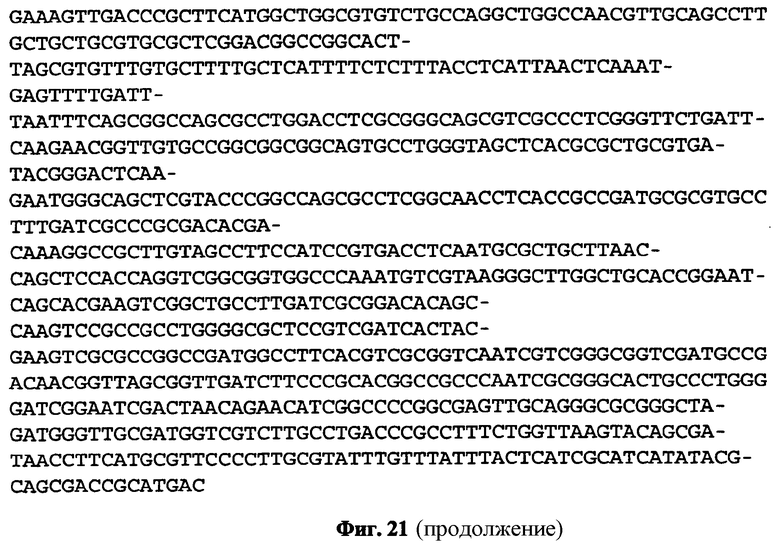
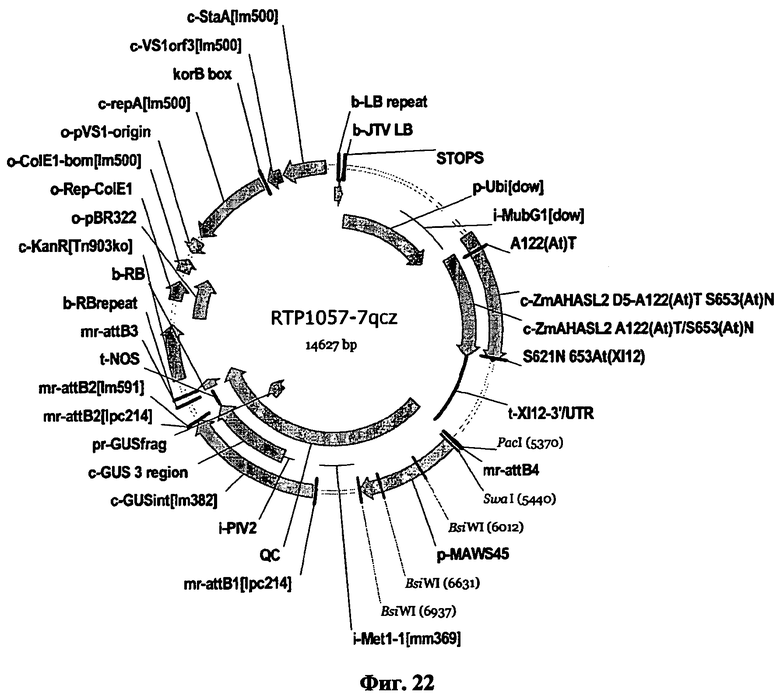







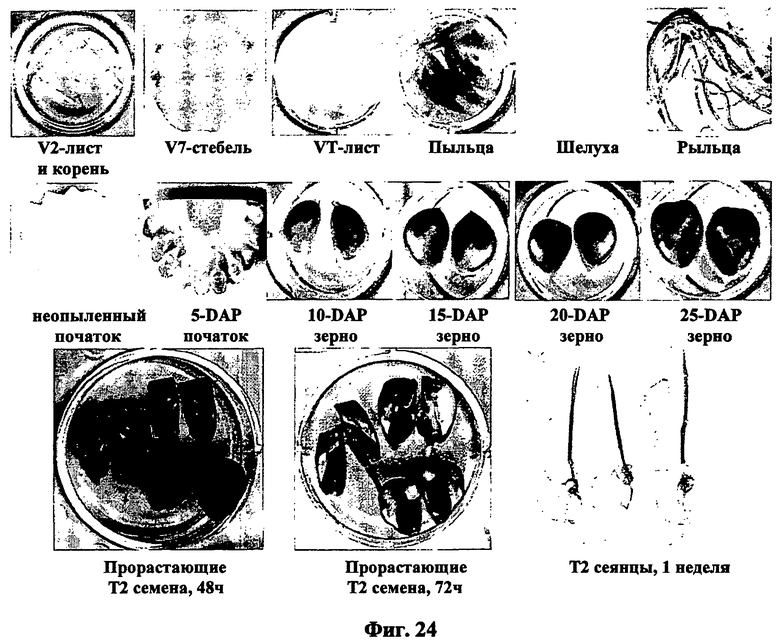
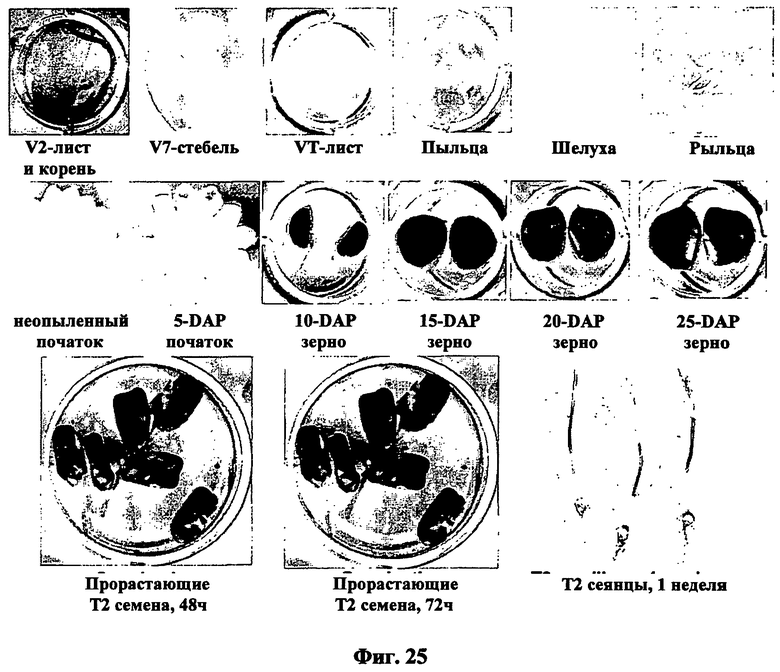
Изобретение относится к генной инженерии. Описан полинуклеотид, обладающий свойствами специфического промотора семян, содержащий контролирующую экспрессию последовательность, которая делает возможной семя-специфическую экспрессию представляющей интерес нуклеиновой кислоты, функционально связанной с ней, в растениях. Предоставлены векторы, клетки-хозяева, трансгенные растения и способы экспрессии представляющих интерес нуклеиновых кислот, которые основаны на указанном полинуклеотиде. 7 н. и 13 з.п. ф-лы, 25 ил., 12 табл., 3 пр.
1. Полинуклеотид, обладающий свойствами специфического промотора семян, содержащий контролирующую экспрессию последовательность, которая делает возможной семя-специфическую экспрессию представляющей интерес нуклеиновой кислоты, функционально связанной с ней, в растениях, при этом указанную контролирующую экспрессию последовательность выбирают из группы, включающей:
(a) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, как показано в любой из SEQ ID NO: 1-3; и
(b) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, которая, по меньшей мере, на 90% идентична последовательности нуклеиновой кислоты, показанной в любой из SEQ ID NO: 1-3, или имеющую последовательность нуклеиновой кислоты, показанной в любой из SEQ IDNO: 129-131.
2. Полинуклеотид по п. 1, где указанная контролирующая экспрессию последовательность представляет собой (а) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, как показано в любой из SEQ ID NO: 1-3.
3. Полинуклеотид по п. 1, где указанная контролирующая экспрессию последовательность представляет собой (b) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, которая, по меньшей мере, на 90% идентична последовательности нуклеиновой кислоты, показанной в любой из SEQ ID NO: 1-3.
4. Полинуклеотид по п. 1, где указанная контролирующая экспрессию последовательность представляет собой (b) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, которая, по меньшей мере, на 95% идентична последовательности нуклеиновой кислоты, показанной в любой из SEQ ID NO: 1-3.
5. Полинуклеотид по п. 1, где указанная контролирующая экспрессию последовательность представляет собой (b) контролирующую экспрессию последовательность, имеющую последовательность нуклеиновой кислоты, показанной в любой из SEQ ID NO: 129-131.
6. Полинуклеотид по п. 1, где указанный полинуклеотид содержит, по меньшей мере, одну представляющую интерес нуклеиновую кислоту, функционально связанную с контролирующей экспрессию последовательностью.
7. Полинуклеотид по п. 1, где указанная представляющая интерес нуклеиновая кислота является гетерогенной относительно контролирующей экспрессию последовательности.
8. Полинуклеотид по любому из пп. 1-7, где указанный полинуклеотид содержит первый интрон гена растения, кодирующего металлотионин 1 полипептид.
9. Вектор экспрессии, содержащий полинуклеотид по любому из пп. 1-8.
10. Вектор по п. 9, где указанный вектор является Т-ДНК вектором.
11. Клетка-хозяин для экспрессии представляющей интерес нуклеиновой кислоты, содержащая полинуклеотид по любому из пп. 1-8 или вектор по п. 9 или 10, причем клетка-хозяин выбрана из растительной клетки и микроорганизма.
12. Клетка-хозяин по п. 11, где указанная клетка-хозяин является растительной клеткой.
13. Трансгенное растение для экспрессии представляющей интерес нуклеиновой кислоты, содержащее полинуклеотид по любому из пп. 1-8 или вектор по п. 9 или 10.
14. Трансгенное растение по п. 13, где указанное трансгенное растение является однодольным растением.
15. Семя растения для экспрессии представляющей интерес нуклеиновой кислоты, содержащее полинуклеотид по любому из пп. 1-8 или вектор по п. 9 или 10.
16. Семя растения по п. 15, где указанное семя растения является семенем однодольного растения.
17. Способ экспрессии представляющей интерес нуклеиновой кислоты в клетке-хозяине, включающий
(a) введение полинуклеотида по любому из пп. 1-8 или вектора по п. 9 или 10 в клетку-хозяин; и
(b) экспрессию, по меньшей мере, одной представляющей интерес нуклеиновой кислоты в указанной клетке-хозяине,
причем клетку-хозяин выбрирают из растительной клетки и микроорганизма.
18. Способ по п. 17, где указанная клетка-хозяин является растительной клеткой.
19. Способ экспрессии представляющей интерес нуклеиновой кислоты в растении или его семени, включающий
(a) введение полинуклеотида по любому из пп. 1-8 или вектора по п. 9 или 10 в указанное растение или его семя; и
(b) экспрессию, по меньшей мере, одной представляющей интерес нуклеиновой кислоты в указанном растении или его семени.
20. Способ по п. 19, где указанное растение является однодольным растением.
| US 20120090049 A1, 12.04.2012 | |||
| RU 94046161 A1, 10.05.1997 |
Авторы
Даты
2015-08-27—Публикация
2010-04-22—Подача