Изобретение относится к области медицины, в частности хирургии, комбустиологии, дерматологии, и может быть использовано при лечении ран кожи субдермального уровня, ожоговых и донорских ран, пролежней и потертостей.
Известен способ лечения ожоговой раны, включающий хирургическую обработку и закрытие раны трансплантатом, содержащим фетальные фибробласты человека первичной культуры на гидрофильном основании, покрытом коллагеном (авт. свид. №1699047 СССР, А61К 35/48, 1989 г.).
Недостатком этого способа является использование первичных культур аллогенных фибробластов без надлежащего обследования и без указаний критериев отбора абортированного материала, из которого получают фибробласты, что не позволяет исключить наличия вирусных и микоплазменных контаминаций культур, способных инфицировать пациента. В процессе культивирования соматические клетки человека, в том числе фибробласты, способны претерпевать спонтанную трансформацию к неограниченному росту, что определяет необходимость изучения кариотипа клеток в процессе культивирования для оценки стабильности их генома.
Гидрофильная природа основания, использованного в прототипе, способствует прочной фиксации на раневой поверхности, что сопровождается крайне болезненной процедурой ее удаления при перевязке. Кроме того, при удалении полимерного основания происходит травматизация вновь образованного эпителия.
Приведенные в прототипе клинические примеры позволяют полагать, что трансплантация фибробластов проводилась на «старые ожоговые раны», требующие тщательной подготовки поверхности раны перед трансплантацией для снижения уровня микробного обсеменения. Указывается, что при использовании клеточных трансплантатов микробное обсеменение тканей раны не должно превышать 102-103 микробных тел/г. Это свидетельствует о применении аллофибробластов в отдаленные от травмы сроки.
Задачей предложенного способа лечения является сокращение сроков заживления ожоговых ран кожи субдермального уровня за счет применения охарактеризованной клеточной линии аллогенных фибробластов, гарантирующей биологическую безопасность клеточного материала.
Поставленная задача решается тем, что в 1-2 сутки после травмы на ожоговую рану после выполнения ее туалета накладывают биологическую повязку, состоящую из перфорированного гидрофобного кремнийорганического полимерного основания, покрытого человеческим коллагеном типа I, и аллогенных диплоидных фибробластов клеточной линии М-22 на уровне пассажей №15-25.
Для стимуляции ранозаживления применяется детально охарактеризованная линия аллогенных фибробластов М-22, трансплантация которых выполняется в период «биологической стерильности» раны (не позднее 1-2 суток после травмы).
Характеристики диплоидных фибробластов человека линии М-22 приведены в паспорте.
Паспорт диплоидной клеточной линии М-22
I. Наименование линии: М-22
II. Видовая принадлежность: человек
III. История получения:
1. кем и когда выделена культура: ГУ ИПиВЭ им. М.П.Чумакова РАМН, 1986 г., лицензирована ГИСК и разрешена для изготовления любых видов иммунобиологических препаратов
2. генеалогия:
а) женщина 32 лет; онкологических, венерических заболеваний, гепатита, туберкулеза в анамнезе не обнаружено, генетических и врожденных заболеваний в семье не обнаружено
3. источник материала: ткани, полученные при выполнении аборта по медицинским показаниям
IV. Культуральные свойства:
1. тип роста: фибробластоподобный
2. жизненный цикл (количество удвоений): - 70
3. фазы роста: I - 1-3 пассажа; II - 4-39 пассажей; III - 40-70 пассажей
4. способ культивирования: стационарный, перевивки 2 в неделю
5. условия культивирования:
а) среда Игла MEM с α-глутамином
б) сыворотка крупного рогатого скота или эмбриональная сыворотка коров 15%
в) температура 37°С
г) метод снятия - 0,25% раствор трипсина с раствором Версена
6. условия хранения:
а) среда хранения: Игла-МЕМ 80% + сыворотка коров 10% + глицерин 10%
б) режим замораживания: до -30°С 1 градус/минута;
в) режим хранения: -196°С
V. Восстановление культур после криоконсервации: среда для культивирования та же, жизнеспособность клеток не менее 75%±5%
VI. Кариологическая характеристика: кариотип человека
VII. Контроль контаминации:
1. бактерии - не обнаружено
2. грибы - не обнаружено
3. микоплазмы - не обнаружено методами посева на специальные питательные среды; на куриные эмбрионы; методом электронной микроскопии
4. вирусы - не выявлено в исследованиях на животных, в клеточных культурах, на куриных эмбрионах, методами электронной микроскопии
VIII. Онкогенная безопасность:
In vivo
мыши СВА
В числе количество животных из числа взятых в опыт, * недостающие животные погибли по неспецифическим причинам
In vitro - не обнаружено
Из клеток ранних пассажей линии диплоидных фибробластов человека М-22 сформирован Банк, в котором ампулы с клеточными суспензиями (10-15·106 клеток) хранятся в жидком азоте при температуре минус 196°С.
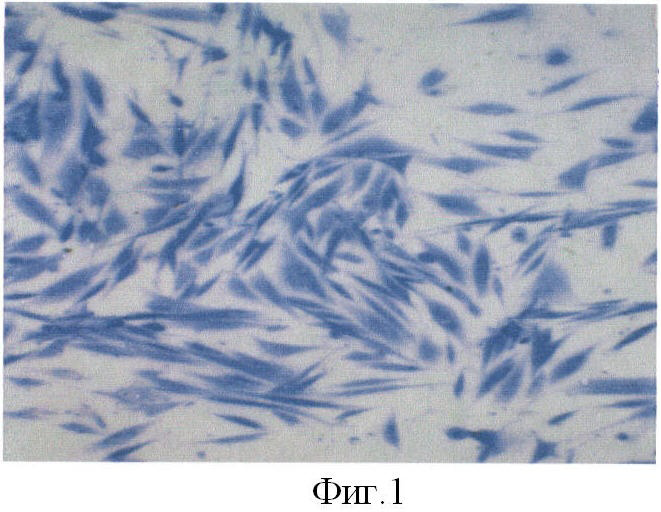
Способ осуществляется следующим образом: на расположенную на дне чашки Петри гидрофобную прозрачную перфорированную для оттока излишков экссудата кремнийорганическую пленку «Карбосил-П», покрытую слоем коллагена I-го типа человека (основа повязки), переносятся фибробласты линии М-22 пассажа №15-25. Плотность посева составляет 5-7,5·104 клеток на 1 см2. Культивирование проводят при 37°С в атмосфере, содержащей 5% CO2 и 100% влажности. Через 3-4 часа клетки закрепляются на поверхности основания и распластываются. В качестве культуральной среды используется среда Игла MEM, содержащая 15% сыворотки эмбрионов коров и α-глутамин. Для предупреждения у пациентов местных аллергических реакций, обусловленных непереносимостью, антибиотики на этом этапе не применяются. Прозрачная кремнийорганическая пленка «Карбосил-П», которая используется в качестве основания, позволяет контролировать характер роста и формирование клеточного монослоя микроскопически. В течение 18-24 часов на поверхности полимерного основания фибробласты формируют монослой (70-80% конфлюэнтность). На фиг.1 представлены фибробласты повязки, растущие на основание из «Карбосил-П» (окраска толуидиновым синим, х200).
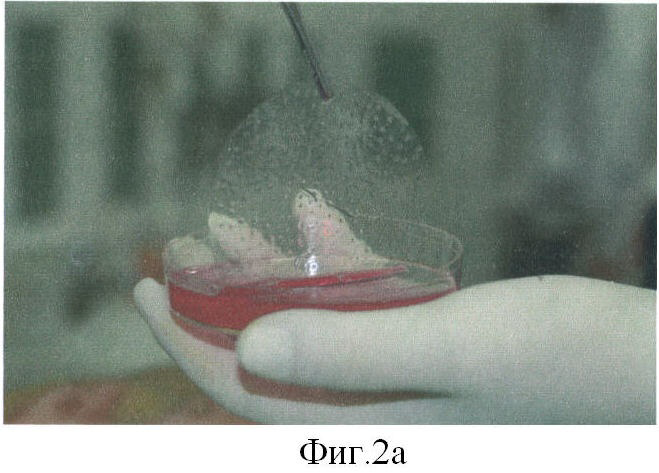
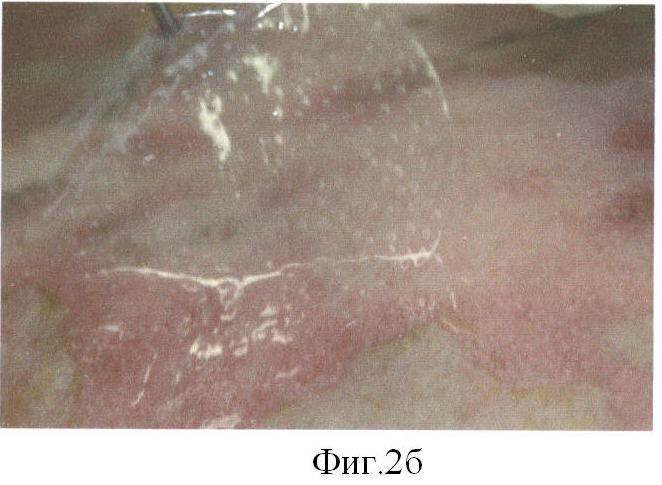
Подготовленный таким образом трансплантат доставляется в клинику в герметичном термоконтейнере. С помощью тампонов, смоченных 1% раствором хлоргексидина, выполняют туалет ожоговой раны, который включает удаление с раневой поверхности мертвых тканей, продуктов горения и загрязнений. На подготовленную таким образом поверхность раны клетками вниз накладывают подготовленную биологическую повязку (фиг.2а, б), которую фиксируют влажно-высыхающей марлевой повязкой. Повязку применяют с 1-2 суток после ожоговой травмы. Следующую перевязку выполняют через 2-3 дня.
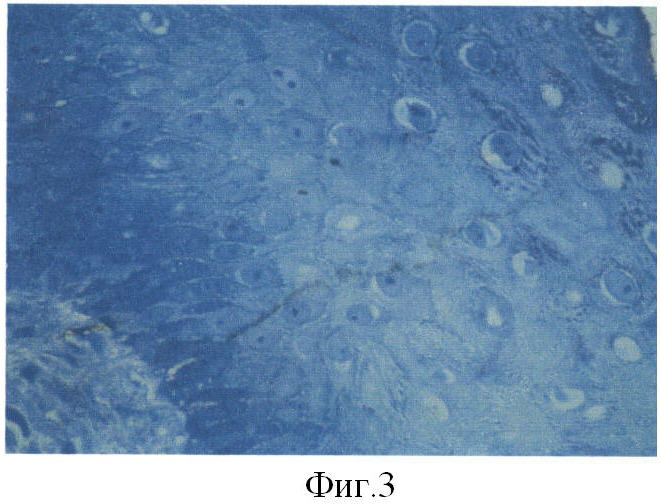
Прозрачность кремнийорганического полимерного основания позволяет наблюдать за состоянием раны и контролировать ее заживление, а газопроницаемость пленки, сравнимая с показателями здоровой кожи, обеспечивает метаболический комфорт в ране. Гидрофобная природа пленки способствует легкому, безболезненному ее удалению при перевязке без повреждения сформировавшегося на поверхности раны регенерировавшего слоя неоэпителия. На этом этапе (2-3 сутки) на поверхности раны формируется слой неоэпителия, состоящий из 1-3 слоев кератиноцитов. К 6-10 суткам после трансплантации у 70-80% пациентов, в зависимости от глубины ожога, формируется полнослойный эпителий, о чем свидетельствует морфологическое исследование биоптатов, полученных из зоны применения аллофибробластов на 7 сутки. На фиг.3 представлен пример, иллюстрирующий восстановление эпителия на ожоговой ране IIIA степени, окраска гематоксилином и эозином, увеличение х630. Наблюдение за больными в течение последующих 2-3 месяцев свидетельствует о формировании полноценного кожного покрова с нормальной эластичностью, пигментацией и ростом волос. При контрольном осмотре через 3-6 месяцев кожа в зоне применения аллофибробластов гладкая, эластичная, нормального цвета с наличием волос.
Предложенный способ позволяет сократить срок заживления ожогов II-IIIA степени до 5-7 суток. Кроме того, раннее применение аллотрансплантатов из живых фибробластов с 1-2 суток после травмы стимулирует не только эпителизацию раны, но и предотвращает развитие местных гнойно-некротических осложнений в ране, что проиллюстрировано следующим клиническим наблюдением.
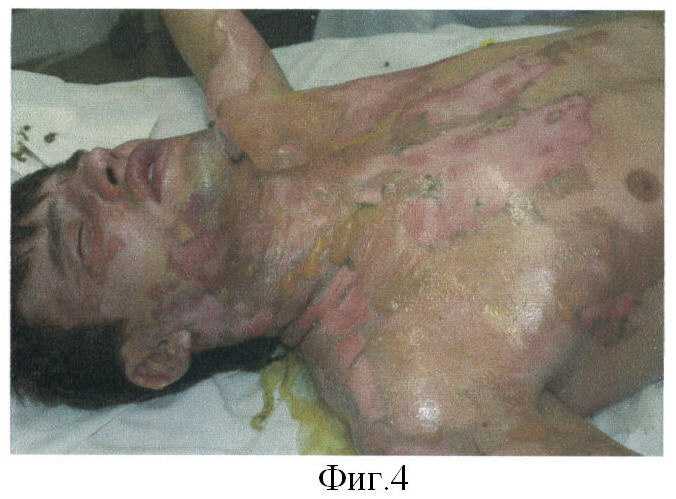
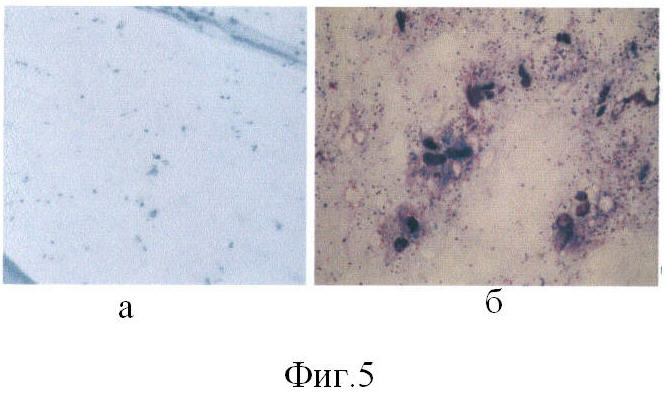
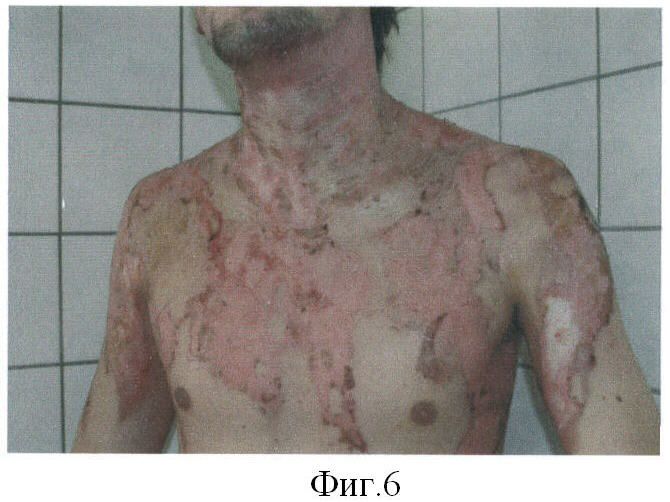
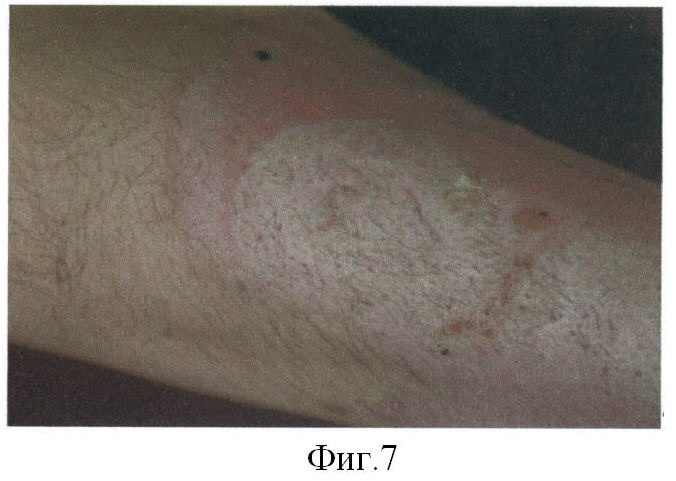
Больной В., 24 лет. Диагноз: ожог пламенем II-IIIA степени 17% поверхности тела. Через 20 часов после травмы проведен туалет ожоговой раны и наложены биологические повязки на основе живых аллогенных фибробластов линии М-22 (фиг.4). На 4-е сутки после наложения биологической повязки на всей раневой поверхности сформирован слой неоэпидермиса. Мазки-отпечатки с поверхности неоэпителия свидетельствуют о наличии микрофлоры, типичной для нормальной кожи (фиг.5а), в то время как на ране под повязкой с мазью «Левомиколь» выявляется нейтрофильная инфильтрация (фиг.5б). На 6-е сутки в местах наложения биологических повязок наблюдается полная эпителизация всей раневой поверхности без признаков гипертрофии эпидермиса (фиг.6). На 10 сутки в зоне трансплантата восстановилась пигментация, появились нормальные волосы (фиг.7).
В табл.№1 представлены основные свойства полимерных пленок из кремнийорганического полимера «Карбосил-П», физико-химические свойства которого обеспечивают «метаболический комфорт» раны и безболезненное удаление основы повязки при выполнении перевязки.
Использование для клинических нужд в составе биологической повязки всесторонне обследованной клеточной линии живых диплоидных аллогенных фибробластов М-22 гарантирует биологическую безопасность клеточного материала. Организация Банка из детально охарактеризованных клеточных линий позволяет своевременно и в полном объеме обеспечивать потребности клиники.
Применение биологической повязки на основе живых аллофибробластов в 1-2 сутки после травмы позволяет добиться полноценного восстановления эпителия по всей поверхности кожной раны субдермального уровня (ожоги IIIA степени, донорские раны, пролежни, мацерации, потертости и пр.) с хорошим функциональным и косметическим результатом в течение 6-10 суток.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МЕСТНОГО ЛЕЧЕНИЯ РАН С ПОМОЩЬЮ БИОЛОГИЧЕСКОЙ ПОВЯЗКИ, СОДЕРЖАЩЕЙ ЖИВЫЕ КЛЕТКИ ЛИНИИ ДИПЛОИДНЫХ ФИБРОБЛАСТОВ ЧЕЛОВЕКА | 2013 |
|
RU2526811C1 |
| КОМБИНИРОВАННЫЙ ТРАНСПЛАНТАТ ДЕРМАЛЬНОГО МАТРИКСА С МЕЗЕНХИМАЛЬНЫМИ МУЛЬТИПОТЕНТНЫМИ СТРОМАЛЬНЫМИ КЛЕТКАМИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ РАН С ЕГО ИСПОЛЬЗОВАНИЕМ | 2013 |
|
RU2526813C1 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 2006 |
|
RU2320349C1 |
| БИОЛОГИЧЕСКАЯ ПОВЯЗКА ДЛЯ ЛЕЧЕНИЯ ОЖОГОВ | 2006 |
|
RU2314129C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ ОЖОГОВЫХ РАН IIIA СТЕПЕНИ | 2010 |
|
RU2455997C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОЖНОГО ПОКРОВА У ПАЦИЕНТОВ С ОБШИРНЫМИ РАНАМИ С ДЕФЕКТОМ МЯГКИХ ТКАНЕЙ (ВАРИАНТЫ) | 2013 |
|
RU2526814C1 |
| Способ подготовки аутологичных моноцитов человека для терапии ожоговых ран | 2017 |
|
RU2685472C2 |
| СПОСОБ ПОВЫШЕНИЯ ПРОЛИФЕРАТИВНЫХ СВОЙСТВ ДИПЛОИДНЫХ КЛЕТОК ФИБРОБЛАСТОВ ЧЕЛОВЕКА | 2013 |
|
RU2536992C1 |
| СПОСОБ ОПЕРАТИВНОГО ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 2018 |
|
RU2673806C1 |
| ПЛЕНКООБРАЗУЮЩИЙ АЭРОЗОЛЬ ДЛЯ ЗАЩИТЫ РАН ПРИ ЛЕЧЕНИИ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2312658C1 |
Изобретение относится к медицине, а именно к хирургии и комбустиологии, и может быть использовано при лечении пациентов с ожоговыми ранами. Для этого проводят туалет раны. Начиная с 1-2 суток после травмы на поверхность раны накладывают повязку, основание которой выполнено из гидрофобной перфорированной кремнийорганической пленки «Карбосил-П», покрытой слоем человеческого коллагена типа I и аллогенными фибробластами человека. При этом в качестве аллогенных фибробластов используют охарактеризованные клетки линии диплоидных фибробластов человека М-22 на уровне пассажей №15-25. Способ позволяет обеспечить быстрое полноценное восстановление эпителия по всей поверхности раны с хорошим функциональным и косметическим результатом, в том числе и при ожогах II-IIIA степени, а также предотвратить развитее местных гнойно-некротических осложнений. 7 ил., 3 табл.
Способ лечения ожоговых ран, включающий туалет раны и наложение на ее поверхность биологической повязки, состоящей из полимерного основания, покрытого коллагеном, и живых аллогенных фибробластов человека, отличающийся тем, что основание повязки выполнено из гидрофобной перфорированной кремнийорганической пленки «Карбосил-П», покрытой слоем человеческого коллагена типа I, а в качестве аллогенных фибробластов используют охарактеризованные клетки линии диплоидных фибробластов человека М-22 на уровне пассажей №15-25, причем повязку применяют с 1-2 суток после ожоговой травмы.
| СПОСОБ ЛЕЧЕНИЯ РАНЫ | 1993 |
|
RU2023424C1 |
| КОМПОЗИЦИОННЫЙ ЭКВИВАЛЕНТ ЖИВОЙ КОЖИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ТЕСТ-НАБОР | 1991 |
|
RU2135191C1 |
| US 6039760 A, 21.03.2000, реферат | |||
| АЛЕИНИК Д.Я | |||
| и др | |||
| Опыт получения и использования культивированных аллофибробластов при лечении ожоговых ран у детей | |||
| Травматология и ортопедия, №1, 1996, с.19-22 | |||
| ВАСИЛЬЕВ А.В | |||
| и др | |||
| Применение выращенных аллогенных эпидермальных пластов для | |||
Авторы
Даты
2009-11-27—Публикация
2008-06-23—Подача