Изобретение относится к области биотехнологии.
Известно, что для скрининга биологически активных веществ используют генетически модифицированные дрожжи, которые гетерологично экспрессируют белок-мишень, который должен ингибироваться испытуемым веществом. Гетерологичная экспрессия обозначает в рамках настоящего изобретения экспрессию чуждого организму гена или экспрессию собственного гена организма с модифицированной картиной экспрессии, в частности усиленную или уменьшенную экспрессию, и/или измененную во времени и/или пространственно (например, в других компартментах, в случае высших организмов, например, в других тканях) экспрессию. В простейшем случае гетерологичная экспрессия приводит к обнаружимому измененному фенотипу, в большинстве случаев к ингибированию роста дрожжей.
Ингибирование роста обозначает в рамках предлагаемого изобретения уменьшенную скорость пролиферации и/или уменьшенный рост и включает в себя также смерть клеток (апоптотическую или некротическую). Тип возникающего ингибирования роста зависит также от организма, так, у дрожжей можно наблюдать скорее задержку пролиферации или лизис, у эукариотических клеток, которые первоначально происходят из многоклеточных организмов, напротив, можно наблюдать отчасти также апоптоз. Если гетерологичная экспрессия приводит к заметному извне изменению поведения и/или морфологии организма (следовательно, к измененному фенотипу), то этот модифицированный генетически организм может быть простым образом использован для скрининга биологически активных веществ, причем эффективность испытуемых веществ может быть установлена на основе их способности элиминировать или уменьшать этот фенотип (например, ингибирование роста). Это осуществляется в случае дрожжевой системы с ингибированием роста в качестве измененного фенотипа предпочтительно при помощи простых анализов, которые пригодны также для высокопроизводительного скрининга (HTS).
Измененным фенотипом называют любое заметное извне изменение генетически модифицированного организма (формы, размера и т.д.) или его поведения (роста, скорости деления клеток) и т.д. в сравнении с немодифицированным генетически или не экспрессирующим гетерологичный белок (гетерологичные белки) или фрагменты организмом. Фенотипирование обозначает, следовательно, достижение (вызывание) такого изменения. Однако этот способ существующего уровня техники обнаруживает недостаток, заключающийся в том, что только небольшая часть экспрессирующихся генов вызывает применимый для скрининга биологически активных веществ фенотип генетически модифицированного организма. Так, предполагается, что, например, только приблизительно 20-30% всех гетерологично экспрессируемых киназ вызывают пригодное для скрининга биологически активных веществ ингибирование роста в дрожжах. В случае остальных 70-80% ингибирование роста является настолько малым, что оно является непригодным для скрининга (приводит к небольшому различию в сравнении с контролем, к высокому фону и, следовательно, к большому числу ложноположительных результатов) или вообще отсутствует.
Поэтому существует потребность в способе создания генетически модифицированного организма для скрининга биологически активных веществ, который не обнаруживает недостатков существующего уровня техники и, в частности, применим для того, чтобы добавить также такие гетерологично экспрессируемые гены к скринингу биологически активных веществ, которые в гетерологично экспрессирующем их организме не индуцируют никакой полезный или не индуцируют никакой полезный для скрининга, в частности для высокопроизводительного скрининга (HTS), фенотип.
Эта задача решается в соответствии с изобретением при помощи способа генерирования генетически модифицированного организма для скрининга биологически активных веществ, включающего следующие стадии:
a) достижение гетерологичной экспрессии по меньшей мере одного белка или фрагмента белка при помощи генетически модифицированного организма,
b) предпочтительно эта стадия сочетается с определением фенотипа этого генетически модифицированного организма,
c) анализ модифицированной картины экспрессии и идентификацию компенсаторно дифференциально регулируемых генов,
d) фенотипирование организма (предпочтительно посредством делеции, мутагенеза или сверхэкспрессии компенсаторно регулируемых генов для усиления или генерирования фенотипа в комбинации с гетерологично экспрессируемым белком или фрагментом белка).
Изобретение основывается на знании авторов изобретения, что отсутствие детектируемого фенотипа при гетерологичной экспрессии большинства генов основано на том, что генетически модифицированный организм регулирует экспрессию собственных генов в ответ на экспрессию гетерологично экспрессируемого белка или фрагмента белка повышающим или понижающим образом (т.е. регулирует компенсаторно дифференциально). В этом случае термин «регулирует дифференциально» обозначает "регулирует по-другому, чем в генетически не модифицированном организме", или без гетерологичной экспрессии гетерологично экспрессируемого белка или фрагмента белка. Термин "компенсаторно" обозначает, что эта дифференциальная регуляция генов является ответом на гетерологичную экспрессию белка или фрагмента белка.
Изобретение делает возможной развитие платформной технологии в клеточной, в противоположность просто биохимической модели, например, в дрожжах. С этой системой анализа могут быть идентифицированы ингибиторы, например, из химических библиотек, из комбинированных химических библиотек и из экстрактов природных веществ. Эта система анализа может быть приспособлена к 96-, 384- или 1536-луночным планшетам или другим общепринятым для клеточных анализов форматам. Выбираемый формат зависит отчасти также от выбранного организма, причем этот выбор находится в пределах компетенции специалистов в данной области.
Способ по изобретению применим, в частности, к генам или белкам или фрагментам белков, гетерологичная экспрессия которых в желаемом организме не приводит к детектируемому изменению фенотипа в сравнении с генетически немодифицированным или не экспрессирующим гетерологично белок или фрагмент белка организмом. Могут испытываться, например, протеинкиназы, а также другие генные продукты, которые вызывают транскрипционную ответную реакцию. Однако он применим также при детектируемо измененном фенотипе, в частности, тогда, когда измененный фенотип, хотя и является детектируемым, но по определенным причинам является непригодным или нецелесообразным для применения в скрининге биологически активных веществ. Он может усиливаться фенотипированием или быть изменен таким образом, что он становится полезным для скрининга биологически активных веществ. Фенотипирование обозначает в рамках изобретения достижение или усиление фенотипа, отличающегося от неэкспрессирующего гетерологично белки или фрагменты или от генетически немодифицированного организма, в гетерологично экспрессирующем белки или фрагменты, генетически модифицированном организме.
В качестве организмов пригодны предпочтительно клетки как эукариотические, так и прокариотические, а также многоклеточные, не являющиеся человеком организмы, которые пригодны для скрининга биологически активных веществ, например Drosophila и, предпочтительно, С.elegans. В качестве эукариотических клеток пригодны предпочтительно культивируемые клеточные линии, которые первоначально были получены из многоклеточных организмов, например 3Т3, СНО, Hela, но также другие, или эукариотические одноклеточные организмы, в частности дрожжи. Среди дрожжей пригодны, в свою очередь, особенно штаммы S. cerevisiae или S. pombe. Специалисту достаточно хорошо известны подходящие лабораторные штаммы дрожжевых клеток или подходящие эукариотические клеточные линии.
В качестве белков и фрагментов белков рассматриваются в основном все белки и фрагменты белков, гетерологичная экспрессия которых в организме приводит к изменению картины экспрессии собственных генов. Предпочтительными являются все белки и фрагменты белков, которые представляют интерес для нахождения новых биологически активных веществ, в рамках изобретения особенно предпочтительными являются киназы, фосфатазы, GPCR (связанные с G-белком рецепторы), (особенно малые) ГТФ-азы, протеазы и ионные каналы.
Понятие скрининг биологически активных веществ охватывает в рамках изобретения любой вид поиска веществ, которые действуют на активность одного или нескольких определенных рассматриваемых генов и/или рассматриваемых белков, с использованием по меньшей мере одного генетически модифицированного организма. При этом рассматриваются в основном все виды веществ, например все виды природных веществ (т.е. природно встречающихся молекул, в частности биомолекул), а также не встречающихся в природе, синтетически полученных химикалиев и природных веществ, в частности произведенных из биологических молекул веществ/производных (например, модифицированных пептидов или олигонуклеотидов).
Гетерологичная экспрессия может включать в себя введение чужеродного гена, но также измененную экспрессию собственного гена организма, например, введением соответствующего экспрессирующего вектора. Необходимая для этого генетическая модификация может при этом относиться к изменению генома организма (например, посредством стабильных, интегрируемых в геном векторов или посредством различных типов мутагенеза), быть эписомной или включать в себя просто введение подходящих векторов, которые для дальнейшего пребывания в организме требуют постоянного отбора с использованием одного или нескольких маркеров отбора. Наиболее подходящий тип зависит от различных факторов, в том числе также от вида организма, и может быть простым способом определен компетентным специалистом.
Гетерологичная экспрессия относится при этом по меньшей мере к одному белку или фрагменту белка, но может относиться также к нескольким белкам или фрагментам белков. Может быть целесообразным подтверждение экспрессии гетерологичного белка/фрагмента при помощи подходящих способов (ПЦР, Нозерн-, Вестерн-блоттинг и т.д.), перед сравнением и, следовательно, анализом картины экспрессии генов генетически модифицированного организма, с организмом без экспрессии гетерологичного белка. Этот анализ выполняют при помощи подходящих мероприятий, которые достаточно хорошо известны специалисту, в частности, для этого пригодным является применение систем массивов (например, микромассивов ДНК/РНК или белков) или чипов. Посредством сравнения картины экспрессии контрольного организма (например, организма дикого типа или организма, в который включен только пустой вектор, или при индуцируемых системах генетически модифицированного организма, у которого экспрессиия гетерологичного гена не индуцирована) и генетически модифицированного, экспрессирующего гетерологичный ген организма, такие генные продукты, которые в картине экспрессии генетически модифицированного организма в отличие от картины экспрессии контрольного организма увеличиваются/уменьшаются или вообще не обнаруживаются, рассматриваются, следовательно, как компенсаторно дифференциально регулируемые гены и могут использоваться для фенотипирования генетически модифицированного организма.
Фенотипированием называют вызывание или усиление отличимого от организма дикого типа фенотипа в генетически измененном организме (или, в случае индуцируемых систем, фенотипа, который образуется только при гетерологичной экспрессии белка или белков или фрагментов генетически модифицированным организмом и не образуется в неиндуцированном состоянии организма, если не экспрессируются этот белок или эти белки или фрагменты), предпочтительно речь идет при этом о фенотипе, подходящем для оценки в высокопроизводительном скрининге (HTS) биологически активных веществ. Это достижение или усиление может выполняться, например, на уменьшении или прекращении экспрессии одного или нескольких компенсаторно положительно регулируемых генов (это может, например, выполняться посредством геномного нокаута одного или нескольких компенсаторно дифференциально регулируемых генов или посредством мутагенеза) или усиленной экспрессии одного или нескольких компенсаторно дифференциально отрицательно регулируемых генов (это может, например, выполняться посредством гетерологичной экспрессии одного или нескольких компенсаторно дифференциально отрицательно регулируемых генов с подходящими экспрессирующими векторами). Таким образом может стать очевидным присущий организму индуцированный гетерологично экспрессируемым геном фенотип, который был запрещен компенсаторной дифференциальной регуляцией одного или нескольких генов (предпочтительно, здесь рассматривается ингибирование роста, в частности, у многоклеточных организмов, но также и другие фенотипы).
Следующей возможностью является также мечение одного или нескольких генов, которые компенсаторно положительно регулируются, с использованием подходящего маркера/метки (который связан, например, с продуктом гена) или с использованием репортера, который находится под контролем энхансера и/или промотора компенсаторно положительно регулируемого гена и вводится в этот организм. Подходящие репортеры известны компетентному специалисту, и здесь пригодны, в частности, все виды самопроизвольно светящихся белков (например, GFP, BFP и т.д.), но также другие репортеры, с которыми может быть получен детектируемый сигнал (например, люцифераза, β-галактозидазы), а также маркеры роста для ауксотрофных штаммов, такие как, например, HIS3, URA3, LEU2, TRP1, и гены устойчивости к антибиотикам, такие как, например, гены устойчивости к канамицину или G418. Возможны также другие виды фенотипирования.
Сразу же после фенотипирования целесообразно проверить успешность фенотипирования при помощи подходящих способов (например, измерением скорости пролиферации, счетом клеток или определением величины или морфологии и т.д., и сравнением с фенотипом при неосуществленной гетерологичной экспрессии).
Согласно предпочтительному варианту осуществления способа по изобретению фенотипирование выполняют с использованием делеции, мутагенеза или сверхэкспрессии по меньшей мере одного компенсаторно регулируемого гена.
Согласно предпочтительному варианту осуществления способа по изобретению фенотипирование выполняют уменьшением/увеличением компенсаторно дифференциальной экспрессии или мечением по меньшей мере одного компенсаторно дифференциально регулируемого гена. При этом гетерологичная экспрессия может приводить к компенсаторной повышающей регуляции, а также понижающей регуляции по меньшей мере одного собственного гена организма, но также к тому, что один или несколько генов положительно регулируются, и один или несколько других генов отрицательно регулируются.
Особенно практично также, если гетерологичная экспрессия белка или фрагмента белка является индуцируемой. Подходящие системы известны компетентному специалисту; так, пригодны, например, регулируемые галактозой или медью промоторы, система Tet-On - Tet-Off и т.д. При этом может индуцируемо включаться экспрессия либо чужеродного для организма гена, либо собственного гена (индуцируемое включение гена (knock-in)), или экспрессия собственного гена организма индуцируемо уменьшается или полностью выключается (индуцируемая элиминация гена (knock-out)). При этом генетическая модификация включает в себя введение подходящим образом вектора, который делает возможной индуцируемую экспрессию белка или фрагмента белка, предпочтительно белка или фрагмента с регулируемыми галактозой (GAL1/GAL10) или медью (CUP1) промоторами, индуцируемого тетрациклином вектора или тканеспецифически индуцируемых промоторов, таких как, например, hspl6-2, unc-119, unc-54, mec-7 или myo-3 в С.elegans.
Согласно предпочтительному варианту осуществления предпочтительным организмом является С.elegans, прокариотическая или эукариотическая клетка и, особенно предпочтительно, дрожжевая клетка, предпочтительно дрожжевая клетка штамма S. cerevisiae.
Анализ модифицированной экспрессии генов выполняют предпочтительно при помощи анализа профиля ДНК/РНК с использованием микромассивов кДНК или олигонуклеотидов, но может включать в себя по существу все изменения мРНК или белка стационарного состояния (транскрипцию, трансляцию, стабилизирование и т.д.) и, следовательно, также при помощи анализа профиля белков, а также при помощи массивов белков.
В одном предпочтительном варианте осуществления этого способа фенотипирование выполняют посредством уменьшения или прекращения компенсаторно дифференциальной регуляции. Если компенсаторно дифференциально регулируемый ген экспрессируется сильнее, чем в контрольных организмах, выполняют уменьшение или прекращение посредством полного или частичного ингибирования усиленной экспрессии. Предпочтительно, это выполняется скрещиванием с делеционным штаммом и последующим отбором двойных мутантов (что удобно, в частности, с дрожжами в качестве организма), геномным нокаутом с подходящими векторами (они известны специалисту и также хорошо пригодны в дрожжах, здесь прежде всего Saccharomyces cerevisiae), с использованием мутагенеза посредством облучения и/или мутагенных веществ или включения антисмысловых векторов или других, которые ингибируют образование белка рассматриваемого гена. При этом особенно предпочтительно, если нокаут компенсаторно дифференциально регулируемого гена включает в себя «удар» в репортерном гене, таком как, например, β-галактозидаза, люцифераза или маркер роста, такой как HIS3, ADE2, URA3 или маркере устойчивости, например, в отношении канамицина. Затем этот репортерный ген в последующем анализе может быть использован в качестве сигнала, чтобы детектировать и определить количественно эффективность испытуемых биологически активных веществ. При этом происходит предпочтительно обмен по меньшей мере одной части кодирующей последовательности дифферециально регулируемого гена на кодирующую последовательность (которая включает в себя также части этой последовательности, которые являются достаточными для того, чтобы быть детектируемыми) репортерного гена (например, люциферазы, β-галактозидазы и т.д.). Если компенсаторно дифференциально регулируемый ген является менее сильно экспрессируемым, чем в контрольном организме, проводят уменьшение или прекращение посредством усиления экспрессии, предпочтительно посредством скрещивания, включения эписомного или другого способного к отбору экспрессирующего вектора или посредством геномного введения (knock-in) (вышеупомянутые способы особенно хорошо пригодны для применения дрожжей в качестве организма). Предпочтительно, понижение или прекращение компенсаторно дифференциальной регуляции приводит к ингибированию роста измененного генной инженерией организма, но другие фенотипы могут быть также предпочтительными.
Следующий аспект изобретения относится к генетически модифицированному, фенотипированному организму, который был получен способом по изобретению.
В частности, изобретение относится к генетически модифицированному организму с генетически модифицированной экспрессией по меньшей мере одного собственного или чужого гена, которая приводит к компенсаторно дифференциальной регуляции по меньшей мере одного другого собственного гена организма и таким образом предпочтительно элиминирует или ингибирует появление оцениваемого/детектируемого/полезного фенотипа и с компенсаторно дифференциальной (посредством понижения/прекращения) экспрессией гена или индуцированным (посредством мечения компенсаторно дифференциально регулируемого генного продукта) фенотипом.
Следующий аспект изобретения относится к применению полученного в соответствии с изобретением генетически модифицированного организма для скрининга на вещества, обладающие действием на функцию гетерологичного белка или фрагмента белка, а также к способу идентификации веществ, обладающих действием на функцию гетерологичного белка или фрагмента белка.
Согласно следующему аспекту изобретение относится также к анализу для скрининга биологически активных веществ с использованием фенотипированного организма по изобретению посредством установления фенотипа (например, ингибирования роста вследствие индуцированной гетерологичной сверхэкспрессии белка), приведения в контакт испытуемого вещества с этим организмом и наблюдения возможного изменения фенотипа, предпочтительно его по меньшей мере частичного возврата к поведению или к морфологии организма дикого типа (следовательно, по меньшей мере частичного обратного возникновения фенотипа исходного организма, например прекращения ингибирования роста). Далее, этот аспект относится к веществам, которые посредством способа по изобретению или анализа по изобретению идентифицируются как эффективные.
Далее, изобретение объясняется более подробно при помощи примеров.
Пример 1. Развитие платформной технологии для идентификации биологически активных веществ, которые влияют на активность киназ, на основе дрожжей в качестве организма. Вызываемым фенотипом является в этом случае ингибирование роста. Принцип теста основан, следовательно, на ингибировании роста дрожжей, которые используют в качестве живого "реакционного стакана".
Под ингибированием роста подразумевают в данном контексте, например, задержку клеточного цикла или лизис рассматриваемых клеток. Дрожжи используют, так как они на основе их генетической манипулируемости являются идеально подходящими для этого. Киназы человека (или другие экзогенные киназы) сверхэкспрессируют в дрожжах под контролем индуцируемого галактозой промотора (GAL1/10). Трансформацию и культивирование дрожжей выполняют при этом в соответствии со стандартными способами. В качестве вектора используют, например, векторы серии p41x-GALl или р42х-GAL11.
В приблизительно 30% всех подлежащих испытанию киназах сверхэкспрессия будет уже приводить к ингибированию роста в дрожжах (Tugendreich et al., (2001)). Этот образ действия документируется на чертеже стадиями 1,3,5. Киназы, сверхэкспрессия которых приводит к ингибированию роста, интегрируют в подходящий штамм дрожжей и сразу после этого переносят в высокопроизводительный скрининг (HTS). В этом примере используются штаммы дрожжей штамма-фона "МАТ а his3□l
leu2□0 metl5□0 ura3DO" (BY4741 EUROSCARF).
Во время равития анализа для HTS условия оптимизируют испытанием различных "делеционных мутантов-транспортеров лекарственного средства" в вышеописанном штамме-фоне. Для всех подлежащих испытанию в этом примере протеинкиназ испытывают следующие комбинации делеций: 1. YRWS21 (МАТ а pdrl□::KanMX pdr3□::KanMX his3□1 leu2□0 met15□0 lys2□0 ura3□0) 2. YRWS39 (МАТ а pdr5□::KanMX yor1□::KanMX his3□1 leu2□0 MET15 lys2□0 ura3□0) 3. YRWS14 (МАТа pdr5□::KanMX snq2□::KanMX his3□1 leu2□0 MET15 lys2□0 ura3□0)4. YRWS13 (МАТа snq2□::KanMX yor1□::KanMX his3□l leu2□0 MET15 lys2□0 ura3□0) 5. YRWS44 (МАТ а pdr5□::KanMX snq2□::KanMX yor1□::KanMX his3□1 leu2□0 met15□0 lys2□0 ura3□0).
Затем в высокопроизводительном скрининге может проводиться поиск на биологические и химические молекулы, которые понижают или прекращают ингибирование роста, т.е. которые приводят к росту культур дрожжей. Все описанные до сих пор способы известны компетентному специалисту.
Как описано выше, приблизительно 30% всех экзогенных киназ вызывают ингибирование роста в дрожжах. Поэтому приблизительно 70% всех сверхэкспрессируемых киназ не вызывают никакого ингибирования роста или вызывают лишь небольшое ингибирование роста. Чтобы использовать принцип ингибирования роста дрожжей в качестве платформного способа для скрининга соединений всех протеинкиназ, должны также и остальные 70% протеинкиназ вызывать ингибирование роста. Для этого было необходимо настоящее изобретение.
Желаемые протеинкиназы клонируют в выбранный экспрессирующий вектор дрожжей, в данном случае р413 GALl (D. Mumberg et al. (1994) при полной длине и с С-концевой меткой, например MYC-Tag). После трансформации по способу с ацетатом лития согласно стандартному протоколу (см. Methods in Yeast Genetics) и культивирования в подходящей среде индуцируют сверхэкспрессию экзогенных киназ в дрожжах добавлением галактозы согласно стандартному протоколу (20 г/мл среды) в течение 4-6 часов при 30°С. Экспрессию киназ контролируют при помощи иммуноблотов согласно стандартному протоколу с использованием антител против выбранной метки (например, анти-Мус-антител: АВ1364 (Chemikon) или М5546 (Sigma); анти-НА-антител: НА-11-А (Biotrend) или 55138 (ICN)).
После иммунологического обнаружения экспрессии в дрожжах исследуют изменения экспрессии генов - индуцированные экспрессией экзогенных киназ - в дрожжах (компенсаторно дифференциальную регуляцию) при помощи ДНК-микромассивов. ДНК-микромассивы являются материалами-носителями, с которыми связаны химически специфические олигонуклеотиды. Отдельные олигонуклеотиды представляют здесь индивидуальные гены. ДНК-микромассивы используются в качестве инструментов, которые могут раскрывать существующую в данный момент картину экспрессии всего генома дрожжей. Для такого эксперимента трансформированные киназой дрожжи сравнивают с ложно трансформированными (пустой плазмидой) дрожжами в качестве контроля. Из обоих штаммов получают общую (тотальную) РНК с использованием стандартных способов. Затем эту РНК гибридизуют со связанными на чипе олигонуклеотидами (на микромассивах) при 45°С в течение 16 часов. Прямое сравнение РНК трансформированных киназой дрожжей с РНК ложно трансформированных дрожжей раскрывает гены дрожжей, которые компенсаторно дифференциально регулируются сверхэкспрессируемой протеинкиназой. Исследования авторов изобретения показали, что посредством генетического вмешательства, например, при сверхэкспрессии экзогенной протеинкиназы определенное количество РНК для генов дрожжей положительно регулируется, а определенное количество РНК отрицательно регулируется (таблица 1). Это проводили на примере киназы человека РАК1.
Таблица 1. 2 гена положительно регулируются, 11 генов отрицательно регулируются. Кроме того, авторы изобретения смогли впервые показать, что многие из положительно регулируемых генов регулируются положительно вследствие компенсаторных причин. В этом случае штамм дикого типа S. cerevisiae (W303-1a (штамм-фон или источник получения)) сравнивали со штаммом, который имеет делецию в гене cla4 (□cla4) (YEL252) Saccharomyces cerevisiae. До делеции в этом гене для CLA4 оба штамма являются изогенными, т.е. идентичными. При прямом сравнении препаратов РНК из этих двух различных штаммов (W303-1a и YEL252) появлялись 110 различных РНК из генома дрожжей в виде положительно регулируемых (таблица 2).
Таблица 2. 56 генов отрицательно регулировались (данные не показаны). Повышение РНК-копийности для определенных генов могло при этом возникать, возможно, вследствие компенсаторных причин. Компенсаторно обозначает в этом конкретном примере, что обусловленный делецией гена CLA4 дефект в генетически модифицированном штамме должен ослабляться увеличенной экспрессией генов, которые могут полностью или частично взять на себя функцию CLA4. Для доказательства этого положения были выбраны несколько из положительно регулируемых генов для дальнейших экспериментов (см. «2-ая делеция» в таблице 3).
Таблица 3. Для этого подбирали штаммы дрожжей MAT□ (могут быть куплены, например, в EUROSCARF или Research Genetics), которые в каждом отдельном случае несут делеции в положительно регулируемых генах. Эти делеции помечены маркерными генами, т.е. в соответствующий геном дрожжей интегрированы маркерные гены, например, для устойчивости к антибиотикам или для необходимых факторов роста, например определенные аминокислоты. Выбранные делеционные штаммы скрещивали в соответствии со стандартными генетическими способами для дрожжей (Methods in Yeast Genetics: A Cold Spring Harbor Course Manual (1994)) с CLА4-делеционным штаммом (YEL252, МАТа).
После скрещивания отбирали диплоидные дрожжи. Вызывали у них спорообразование. При этом из одной диплоидной клетки образовывались 4 гаплоидные споры, которые могли быть разделены для прорастания в 4 гаплоидных клона дрожжей. В соответствии с этим происходит перераспределение генов из диплоидного штамма. В 25% всех случаев 2 делеции различных исходных штаммов объединяются в новом гаплоидном клоне. Это можно проследить простым образом с использованием различных селективных маркеров.
С использованием этого стандартного способа пытались получить 13 различных двойных делеции. Только в 10 случаях эти двойные делеции были жизнеспособными, в 3 случаях никогда не получали двойную делецию (таблица 3, «летальный»). Во всех 3 случаях испытывали 40 асков. Поэтому ясно, что комбинация обеих делеций приводит к гибели соответствующие споры. Они являются также синтетически летальными. Удалось показать, что во всех 13 случаях двойные делеции были либо синтетически летальными, либо имели иные синтетические фенотипы (таблица 3). Это исследование подтверждает положение, что рассматриваемые гены положительно регулировались, чтобы компенсировать дефекты, возникающие в результате отсутствия CLA4. Для изобретения важно, что в исследуемых случаях (13 двойных мутаций) 3 комбинации и, следовательно, 23% всех возможных двойных мутаций обнаружили синтетическую летальность (таблица 3). В эксперименте со штаммом □с1а4 положительно регулировались 110 генов (таблица 2). Подобным образом в вышеописанном подходе посредством сверхэкспрессии РАК1 человека положительно регулировались мРНК для 2 генов (таблица 1). Следовательно, эти гены также положительно регулируются вследствие компенсаторных причин. По причине малого числа положительно регулируемых генов и связанной с этим низкой степени успеха для синтетически летальных комбинаций, авторы изобретения отказались от последующего эксперимента для идентификации штаммов, которые в комбинации из делеций в положительно регулируемых генах (с YMR096W или HIS3 из таблицы 1) и экспрессии РАК1 человека показали синтетически летальный фенотип. Напротив, получили гиперактивный мутант РАК1 человека, а именно PAK1□CRIB. Этот мутант трансформировали опять с использованием стандартных способов в дрожжи. На основе высокой киназной активности этот белок вызывал ингибирование роста в дрожжах. Был идентифицирован подходящий штамм для испытания низкомолекулярных веществ. Эта цель была достигнута. Несмотря на это, также и для этого случая получали дифференциальный профиль экспрессии с ДНК-микромассивами для обоснования валидности изобретения (таблица 4).
Таблица 4. 55 различных генов дрожжей на основе высокой киназной активности положительно регулировались компенсаторно, 3 гена отрицательно регулировались (не показано). На тот случай, если высокая активность PAKl-мутанта не была достаточной для вызывания ингибирования роста в дрожжах, смогли испытать делеционные штаммы для положительно регулируемых генов. РАК1-мутант должен был экспрессироваться в соответствующих штаммах. При взятии за основу показатель 23%-ного шанса на успех для синтетического фенотипа, в приблизительно 13 штаммах дрожжей экспрессия PAKl-мутанта человека вызывала бы ингибирование роста. Тем самым был бы идентифицирован штамм для испытания потенциальных ингибиторов киназ. В случае испытания киназ человека в дрожжах исходные штаммы не должны скрещиваться, так как киназы человека экспрессируются зависимым от галактозы образом из плазмиды. Эта плазмида должна только трансформироваться в соответствующий делеционный штамм, и должна индуцироваться экспрессия киназы. В 23% всех случаев испытуемых штаммов удалось наблюдать ингибирование роста (летальность). Штаммы с ингибированным ростом из-за соответствующих делеций не могли более компенсировать экспрессию кодируемой плазмидой протеинкиназы. Поэтому эти системы не могут переноситься в высокопроизводительный скрининг (HTS). Если сверхэкспрессия определенных киназ дикого типа в комбинации с ДНК-микромассив-экспериментом является недостаточной (как описано выше для РАК1 дикого типа, см. таблицу 2), чтобы вызвать ингибирование роста, тогда получают мутанты соответствующей киназы и используют вместо киназ дикого типа (также для экспериментов по сверхэкспрессии генов с ДНК-микромассивами). Эти мутанты могут быть получены по принципу случайного (ненаправленного) мутагенеза с целью получения гиперактивных мутантов. Для мутагенеза используют конструкции киназ с С-концевой меткой в соответствии со способом Tugendreich et al. (2001). Таким образом, авторами изобретения было впервые и неожиданно показано, что делеция компенсаторно дифференциально регулируемых генов может приводить к ингибированию роста, и на основе этих данных может быть создан стандартизованный платформный массив для протеинкиназ. В этих проведенных экспериментах было доказано ингибирование роста с частотой встречаемости 23%. Делеционные штаммы, которые после трансформации кодируемой плазмидой протеинкиназой, обнаруживают ингибирование роста, могут, как описано выше, только посредством оптимизации (на основании тестов различных "нокаутов транспортеров лекарственных средств") переводиться в HTS. На чертеже данное изобретение представлено при помощи пунктов 1, 4, 6-10.
Кроме скрещивания делений, компенсаторно дифференциально регулируемые гены могли получать их делеции также с использованием других способов, таких как геномный нокаут экспрессирующих киназу дрожжей. Однако в случае дрожжей выключение компенсаторно дифференциально регулируемых генов посредством скрещивания делеции или геномного нокаута на основе простоты образа действий является особенно предпочтительным. В противоположность этому, у других организмов могут быть пригодными скорее другие способы. Так, в примере эукариотических клеточных линий и в случае многоклеточных организмов, таких как Drosophila или С.elegans, предпочтительным является скорее применение антисмыслового способа, такого как способ с RNAi. Выбор в каждом случае способов, подходящих для отдельных организмов, находится в пределах компетенции специалиста в данной области.
Платформный способ по изобретению делает возможным высокопроизводительный скрининг (HTS) всех протеинкиназ (как описано на примере РАК1 человека) в гомогенных и поэтому требующих меньших затрат системах анализа. Эта система пригодна также для определения IС50-показателей в скрининге соединений.
Эксперименты по экспрессии генов, такие как описанные в примере, приводят также к идентификации РНК генов, которые репрессируются посредством экспрессии экзогенных киназ. Промоторы этих репрессированных генов могут служить в HTS в качестве репортера. Для этого промоторы дрожжей сливают с так называемыми репортерными генами, такими как гены β-галактозидазы, люциферазы, маркеров роста, таких как HIS3, URA3, LEU2 или TRP1, и т.д. Эти конструкции трансформируют в штамм дрожжей для HTS. Там они служат в качестве маркера роста для соединений, которые элиминируют ингибирование роста в рассматриваемом штамме.
Пример 2. Платформный анализ может использоваться также в виде так называемой мультиплексной системы. Под мультиплексной системой имеют в виду, что различные белки или фрагменты белков, например киназы, в одном и том же анализе в одно и то же время испытываются в одной реакционной смеси. Для этого сначала конструируют индивидуальные фенотипированные штаммы дрожжей. Экзогенные протеинкиназы интегрируют стандартными способами (см. выше). Затем эти штаммы дрожжей смешивают в одну гомогенную культуру. Экспрессия протеинкиназ в этой гомогенной смеси штамма дрожжей приводит к ингибированию роста, так как экспрессия каждой отдельной киназы сама по себе также вызывает ингибирование роста в фенотипированном штамме дрожжей. В высокопроизводительном скрининге (HTS) идентифицируют соединения, которые приводят к росту по меньшей мере одного штамма дрожжей. Необходимо приписать этим соединениям соответствующую киназу. Это достигается с использованием так называемого способа «ПЦР колоний» (A.J.P. Brown and M.Tuite (1998)). Для этого несколько микролитров (небольшое количество) из растущих культур дрожжей лизируют в соответствии с руководством (A.J.P. Brown and M.Tuite (1998)). Из (смеси) геномных ДНК (включающей в себя интегрированные протеинкиназы) безупречно идентифицируют со специфическими праймерами для различных протеинкиназ рассматриваемую (рассматриваемые)/ингибируемую (ингибируемые) киназу (киназы) при помощи ОТ-ПЦР. Таким образом посредством смешивания различных дрожжевых штаммов в равных частях в одном едином скрининге испытывают различные киназы. Преимуществом является огромная экономия расходов и времени.
Эта технология применима не только к протеинкиназам, но и ко всем белкам или веществам, которые вызывают транскрипционную ответную реакцию в дрожжах. Этот платформный способ, в противоположность анализам существующего уровня техники, делает возможным, например, высокопроизводительный скрининг (HTS) всех протеинкиназ (не только таких, которые вызывают фенотип уже с первого раза при гетерологичной экспрессии) в гомогенных и поэтому не вызывающих больших затрат в системах анализа.
Эта технология применима не только к протеинкиназам, но и ко всем белкам или веществам, которые вызывают транскрипционную ответную реакцию в дрожжах.
Способы
Для генетических манипуляций использовали стандартные способы в соответствии с Sambrook et al. (1989) Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, pp.545.
Условия выращивания, условия скрещивания и генетические манипуляции на дрожжах (Saccharomyces cerevisiae) выполняли в соответствии с Guthrie, С. and G.R. Fink (1991) Guide to Yeast Genetics and Molecular Biology, Volume 194, J.N. Abelson and M.I. Simon, eds. (San Diego, CA: Academic Press Inc.). Affymetrix-эксперименты («анализ экспрессии генов») проводили точно в соответствии с Klebl et al. (2001) Biochem. Biophys. Res. Commun. 286, 714-720.
глюкан-1,4-□-глюкозидазы
Литература
1. Brown, A.J.P. and M. Tuite (1998). PCR-Based Gene Targeting in Saccharomyces cerevisiae. Methods Microbiol. 26, 67-81.
2. Methods in Yeast Genetics; A Cold Spring Harbor Course Manual; 1994 Edition; Kaiser, C., Michaelis, S., and A. Mitchell; Cold Spring Harbor Laboratory Press.
3. Mumberg, D., Muller, R. and M. Funk (1994). Regulatable promoters of Saccharomyces cerevisiae: comparison of transcriptional activity and their use for heterologous expression. Nucl. Acids Res. 22, 5767-5768.
4. Tugendreich, S., Perkins, E., Couto, J., Barthmaier, P., Sun, D., Tang, S., Tulac, S., Nguyen, A., Yeh, E., Mays, A., Wallace, E., Lila, Т., Shivak, D., Prichard, M., Andrejka, L, Kim, R. and T. Melese (2001). A streamlined process to phenotypically profile heterologous cDNAs in parallel using yeast cell-based assays. Genome Res. 11, 1899-1912.
Изобретение относится к области биотехнологии, конкретно к способу получения генетически модифицированного организма для скрининга биологически активных веществ. Получают генетически измененную клетку дрожжей либо введением чужеродного гена, либо изменением экспрессии собственного гена. Для компенсации влияния этих генов в клетке изменяется повышающим (ап-регуляция) или понижающим (даун-регуляция) образом экспрессия ряда генов. С помощью микроматриц (микромассивов) ДНК идентифицируют компенсаторно экспрессирующиеся гены. Воздействуют на компенсаторные гены, что приводит к уменьшению или прекращению экспрессии ап-регулируемых генов или усилению экспрессии даун-регулируемых генов. В результате в клетке возникает фенотип, проявляющийся в виде ингибирования ее роста. Изобретение позволяет получить организм для скрининга биологически активных веществ, влияющих на гены, изменение экспрессии которых не проявляется фенотипически. 8 з.п. ф-лы, 1 ил., 4 табл.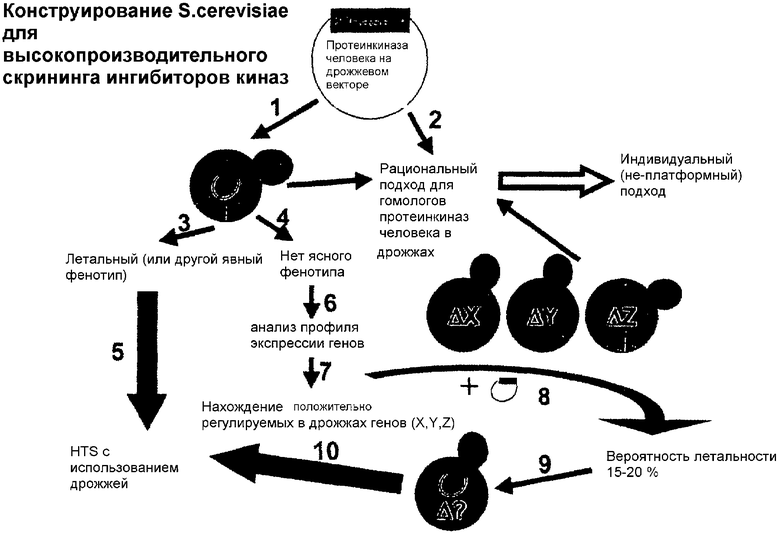
1. Способ создания измененной генной инженерией клетки дрожжей для скрининга на активные вещества, при котором;
a) ген или фрагмент гена, экспрессия которого приводит к компенсаторной экспрессии одного собственного гена клетки дрожжей, встраивают в клетку дрожжей и экспрессируют в измененной генной инженерией клетке дрожжей, или экспрессию собственного гена клетки дрожжей изменяют генной инженерией, что приводит к компенсаторной экспрессии одного собственного гена клетки дрожжей,
b) измененную посредством этого картину экспрессии генов клетки дрожжей анализируют сравнением с картиной экспрессии генов контрольного организма, который не был изменен генной инженерией, при помощи микроматриц (микромассивов) ДНК или белков,
c) идентифицируют гены, у которых повышающая регуляция (ап-регуляция) или понижающая регуляция (даун-регуляция) экспрессии компенсирует влияния экспрессии гена или фрагмента гена, экспрессия которого приводит к компенсаторной экспрессии одного собственного гена клетки дрожжей, или одного собственного гена клетки дрожжей, экспрессия которого была изменена генной инженерией, и
d) посредством уменьшения или прекращения экспрессии компенсаторного гена полным или частичным ингибированием ап-регулируемой экспрессии или усилением экспрессии компенсаторного гена усиленной экспрессией даун-регулируемого гена индуцируется некий фенотип в измененной генной инженерией клетке дрожжей, причем этот фенотип является ингибированием роста клетки дрожжей.
2. Способ по п.1, отличающийся тем, что генно-инженерное изменение экспрессии влияет на экспрессию по меньшей мере одного собственного для организма и/или чужеродного для организма гена или фрагмента гена.
3. Способ по одному из пп.1 или 2, отличающийся тем, что обусловленная генно-инженерным изменением компенсаторная экспрессия одного собственного гена клетки-дрожжей является уменьшением или выключением экспрессии по меньшей мере одного собственного гена этого организма.
4. Способ по одному из пп.1-3, отличающийся тем, что измененная вследствие генно-инженерного изменения экспрессия гена или фрагмента гена, экспрессия которого приводит к компенсаторной экспрессии одного собственного гена клетки дрожжей, является индуцируемой.
5. Способ по п.4, отличающийся тем, что генно-инженерное изменение включает в себя введение вектора, который делает возможной индуцируемую экспрессию гена или фрагмента гена, экспрессия которого приводит к компенсаторной экспрессии одного собственного гена клетки дрожжей.
6. Способ по п.5, отличающийся тем, что этот вектор является индуцируемым галактозой, медью или тетрациклином вектором.
7. Способ по пп.1-6, отличающийся тем, что генно-инженерное изменение гена или фрагмента гена включает в себя нокаут.
8. Способ по п.1, отличающийся тем, что ингибирование ап-регулируемой экспрессии компенсаторного гена проводится посредством нокаута.
9. Способ по п.8, отличающийся тем, что нокаут компенсаторного гена осуществляется посредством замены по меньшей мере части кодирующей последовательности компенсаторного гена кодирующей последовательностью репортерного гена или частями последовательности репортерного гена, которые являются достаточными для возможности детекции.
| TUGENDREICH S | |||
| ET AL.: "A streamlined process to phenotypically profile heterologous cDNAs in parallel using yeast cell-based assays", Genome research, 2001, v.l 1, n.l 1, p.1899-1912 | |||
| CAUMONT A.B | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2009-12-20—Публикация
2003-11-18—Подача