Изобретение относится к химии липидов, принадлежащих классу бесфосфорных катионных глицеролипидов с простой эфирной связью.
Как известно из литературных источников [Helmut К., Mangold H.K. Synthesis of biologically active ether lipids. // In: Prog. Biochem. Pharmacol. / Ed. Braquet P. Basel etc. Karger. - 1988. - V.22. - P.1] данные соединения способны проявлять антинеопластическое действие в экспериментах in vitro, кроме того, по своей природе они немутагенны. То есть, они не взаимодействуют с ДНК, а значит их использование в терапевтических целях в медицинской практике безопасно с точки зрения генной инженерии. Эти соединения могут быть рассмотрены как потенциальные агенты для противоопухолевой терапии. За аналог для представленного в заявке соединения был выбран эдельфозин (1-O-октадецил-2-O-метил-rac-глицеро-3-фосфохолин, ЕТ-18-ОМе).
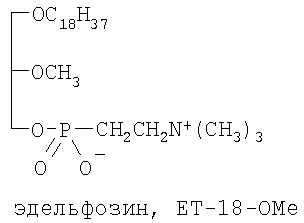
В настоящее время это коммерческий препарат, известный своей биологической полиактивностью. Так, например, он проявляет анти-ВИЧ-1 и ФАТ-антагонистическую активности, обладает антинеопластическими свойствами. Кроме того, характеризуется высокой избирательностью действия, вызывая цитостатический и цитотоксический эффекты преимущественно раковых клеток, не затрагивая при этом нормальные клетки человека. Эдельфозин прошел первую и вторую стадии биологических исследований. Выявлено, что он также способен проявлять антилейкемическую, противогрибковую, противоопухолевую и противовирусную активность, а также выступать в роли ингибитора протеинкиназы С.
Существенным недостатком эдельфозина является сложность его обнаружения в клетке, что является необходимым условием для изучения противоопухолевого действия. Так, не представляется возможным проследить динамику накопления препарата в клетке и его распределение во внутриклеточных компартментах. Из литературных источников известно, что он легко проникает в неопластические клетки за счет рецептор-зависимого эндоцитоза, вызывая клеточный апоптоз, при этом, однако, механизм действия препарата остается до сих пор неясным.
Многие проблемы, связанные с обнаружением вещества в клетках, решил прототип указанного в заявке соединения - РТЕ-эдельфозин (1-O-[15-фенилпентадека-(8E,10E,12Е,14Е)-тетраенил]-2-O-метил-rac-глицеро-3-фосфохолин, РТЕ-18-ОСН3).
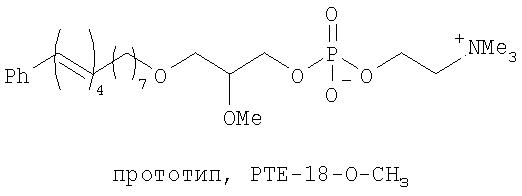
Благодаря наличию в структуре прототипа флуоресцентной составляющей стал доступным мониторинг за поведением липида в клетке. В качестве флуоресцентного зонда РТЕ-18-О-СНЗ можно использовать для полного биохимического анализа клеточных процессов. Кроме того, при введении метки вещество сохранило свою изначальную биологическую активность и селективность действия, что говорит о равноценности в получении результатов в сопоставлении с исходным эдельфозином.
К недостаткам представленного прототипа относится его нестабильность. Время жизни соединения ограничено его высокой реакционной способностью. Неустойчивая конъюгированная тетраеновая группа легко гидролизуется, что диктует использование особых условий при работе с соединением, а также необходимость применения экспесс-методов анализа, что не всегда технически осуществимо.
Техническим результатом предлагаемого изобретения является создание алкильного катионного глицеролипида с высокой биологической активностью, обладающего при этом избирательным действием в отношении неопластических клеток и содержащего стабильную флуоресцентную метку.
Для достижения указанного технического результата получено соединение, принадлежащее классу алкильных глицеролипидов, обладающее селективным цитотоксическим эффектом по отношению к опухолевым клеткам, содержащее в своей структуре стабильную флуоресцентную метку в виде дансильной группы.
Реализация данного изобретения подтверждается примером.
К раствору 0.290 г (2 ммоль) rac-1-октадецил-2-метилглицерина (1) в 1 мл безводного хлороформа при 0°С добавляли 0.5 мл безводного пиридина и по каплям, при перемешивании раствор 0.22 мл (1.2 ммоль) 5-бромпентаноилхлорида в 1.5 мл безводного хлороформа; смесь перемешивали 30 мин при 20°С, добавляли 20 мл хлороформа, промывали 1% HCl (3×20 мл), водой (2×20 мл) и сушили Na2SO4, упаривали. Остаток хроматографировали на колонке с силикагелем (элюент - хлороформ), получая 0.379 г (91.2%) целевого продукта, Rf 0.66 (петролейный эфир: эфир, 2:1). Полученные 0.379 г (0.73 ммоль) rac-2-метил-1-октадецил-3-(5-бромпентаноил)глицерина (2) растворяли в 1.6 мл DMSO, добавляли 0.09 мл (0.08 г; 0.87 ммоль) N,N-диметилэтаноламина и 0.33 г (2.2 ммоль) NaI. Смесь перемешивали 4.5 ч при 55°С, затем добавляли 20 мл хлороформа, промывали 1% раствором HCl (2×25 мл) до pH<7, водой (5×30 мл) до рН 7. Водный слой промывали хлороформом (1×15 мл). Объединенную органическую фазу сушили Na2SO4, упаривали. Остаток хроматографировали на силикагеле, элюируя системой хлороформ: метанол, 6:1. Выход 0.300 г (82.7%). Rf 0.56 (хлороформ: метанол, 3:1).
Схема синтеза флуоресцентно-меченого липида
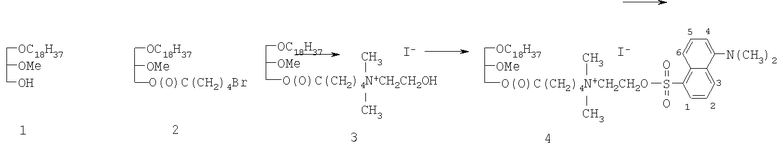
Дансильную флуоресцентную метку в полярную область молекулы вводили согласно методике [Синтез флуоресцентно-меченых гликозилдиглицеридов. М.К.Ангуладзе, А.П.Каплун, В.И.Швец. / Журнал Органической химии, том XVII, вып.11, 1981].
0,030 г (0.046 ммоль) rac-N-{4-[(2-метокси-3-октадецилокси)пропил]-оксикарбонилбутил}-N,N-диметил-N-(2-гидроксиэтил)аммоний иодида (3) растворяли в 6 мл безводного ацетона и добавляли по каплям 0.5 мл триэтиламина. Синтез проводили при перемешивании при комнатной температуре в течение 1.5 ч, добавляя при этом по каплям раствор
0.012 г (0.044 ммоль) дансилхлорида (dh) в 3 мл ацетона. Смесь выдерживали еще 6 ч в тех же условиях. Растворитель отгоняли в вакууме. Остаток хроматографировали (элюент - хлороформ:метанол, 7:1), получали 0.012 г целевого продукта (40%). Rf 0.46 (хлороформ:метанол, 9:4), обнаружение - УФ. Чистота и индивидуальность полученного соединения подтверждена данными 1H-ЯМР-спектроскопии.
Спектр 1H-ЯМР (δ, м.д.):: 0.86 (3 Н, т, J 6.8, ((CH2)15СН 3); 1.24 (30 Н, уш.с, (СН 2)15СН3); 1.48-1.53 (2 Н, м, ОСН2СН 2); 1.54-1.70 (4Н, м, ОСОСН2(СН 2)); 2.43 (2 Н, т, J6.9, OCOCH 2); 2.89 (6 Н, с, N(CH 3)2); 3.21 (6 Н, с, N+(CH 3)2); 3.36 (3 Н, с, СНОСН 3); 3.40-3.57 (4 Н, м, CH 2OCH 2CH2, СНОМе); 3.75-3.81 (2 Н, м, CH 2CH 2N+); 4.09 3.97-4.02 (1 Н, дд, J 5.9, J 11.8, CHH aOCO); 4.13-4.22 (2 Н, м, N+CH 2CH2O); 4.22 (1 Н, дд, J 4.2, J 11.8, CHH bOCO); 4.33 (2 Н, м, +NCH2CH 2O); 7.22-7.24 (1 Н, м, 2-CHAr); 7.50-7.59 (1 Н, м, 4-CHAr); 7.62-7.70 (1 Н, м, 5-CHAr); 8.32-8.35 (1 Н, м, 1-CHAr); 8.42-8.48 (1 Н, м, 6-CHAr); 8.70-8.76 (1 Н, м, 3-CHAr).
Таким образом, полученный нами флуоресцентный глицеролипид не уступает по своим биологическим параметрам прототипу. При этом эффективность изобретения может быть охарактеризована приведенными ниже данными.
Полученное нами соединение, во-первых, обладает высокой цитотоксической активностью по отношению к опухолевым клеткам. Так, при оценке биологического эффекта на клеточной линии К562 (лейкоз человека) показано, что введение флуоресцентной составляющей не снизило цитотоксические показатели соединения:
IC50 для соединения (3, см. схему) составила 4.8 ммоль, для прототипа - 6.2 ммоль и для дансильного производного - 9.3 ммоль. С точки зрения биологической значимости полученные результаты представляют собой величины одного порядка, которые статистически неразличимы.
Во-вторых, изучение гемолитической активности показало, что синтезированный флуоресцентный липид в рамках рассматриваемых концентраций не вызывает клеточного гемолиза, то есть его использование не затрагивает нормальные клетки крови. Вычисленный процент клеточной гибели для изобретения составляет 12,1%, что достоверно не превышает установленный порог активности для растворителя (33,2%, DMSO).
В-третьих, в структуре синтезированного соединения содержится функциональная флуоресцентная метка, позволяющая, например, использовать изобретение для избирательного мечения опухолевых метастаз. При этом устойчивость структуры полученного агента в 1,8 раза по физико-химическим расчетам выше по сравнению с прототипом.
Совокупность перечисленных свойств делает изобретение более привлекательным на фоне конкурирующих веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛИПОФИЛЬНЫЕ ПОЛИАМИНЫ С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2618393C1 |
| Применение rac-N-{ 4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил} -N-метил-имидазолинийиодида в качестве мультикиназного ингибитора | 2015 |
|
RU2625749C2 |
| 1-ГЕКСАДЕЦИЛ-5-(1-ПИРЕНБУТИЛ)-N-(L-ОРНИТИЛ)-L-ГЛУТАМАТ БИСХЛОРИД | 2009 |
|
RU2409587C2 |
| N-(2-(2-(2-азидоэтокси)этокси)этил)-4,6-ди(азиридин-1-ил)-1,3,5-триазин-2-амин, обладающий цитотоксическим действием | 2023 |
|
RU2825828C1 |
| ПРОИЗВОДНЫЕ ФЕНОТИАЗИНСОДЕРЖАЩИХ 1,2,3,4-ТЕТРАГИДРОПИРИДО[4,3-b]ИНДОЛОВ В КАЧЕСТВЕ СРЕДСТВА ДЛЯ СНИЖЕНИЯ НЕКОНТРОЛИРУЕМОЙ АГРЕГАЦИИ БЕЛКОВ В НЕРВНОЙ СИСТЕМЕ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ СНИЖЕНИЯ НЕКОНТРОЛИРУЕМОЙ АГРЕГАЦИИ БЕЛКОВ В НЕРВНОЙ СИСТЕМЕ | 2013 |
|
RU2529899C1 |
| 1-Сульфонил-2-(дифенилфосфорил)пирролидины, обладающие цитотоксичностью в отношении раковых клеток шейки матки, и способ их получения | 2020 |
|
RU2736205C1 |
| N-Ацильные производные 1-метиломино-1-дезоксиполиолов,проявляющие противоопухолевую активность | 1977 |
|
SU677290A1 |
| N-2 @ -Аминобензилиден-(1)-2-(S-алкилизотиосемикарбазонометил-(1)-анилин-N,N @ ,N @ ,N @ -никель (II) | 1989 |
|
SU1708813A1 |
| N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2654201C1 |
| N-НИТРОЗО-N-[(2-ХЛОРЭТИЛ)КАРБАМОИЛ]-L-ОРНИТИН | 2012 |
|
RU2503657C1 |
Изобретение относится к биологически активному катионному глицеролипиду алкильного типа, содержащему флуоресцентную метку в своей структуре, а именно к Rac-N,N-диметил-N-[2-(5-N',N'-диметиламинонафтален-1-сульфонилокси)
этил]-N-{4-[(2-метокси-3-октадецилокси)проп-1-илоксикарбонил]бутил}аммонийиодиду. Технический результат - получение нового соединения, которое может применяться в медицине в качестве противоопухолевого агента.
Rac-N,N-диметил-N-[2-(5-N',N'-диметиламинонафтален-1-сульфонилокси)этил]-N-{4-[(2-метокси-3-октадецилокси)проп-1-илоксикарбонил]бутил}аммонийиодид
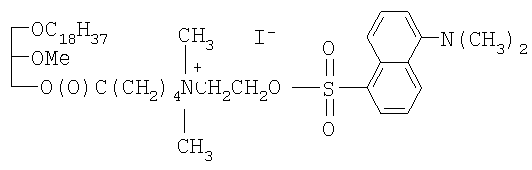
как противоопухолевый агент.
| WO 9959599 A1, 25.11.1999 | |||
| Способ получения трифенилметильных производных S @ -глицеро-3-фосфохолина и S @ -глицеро-3-фосфоэтаноламина | 1985 |
|
SU1422999A3 |
Авторы
Даты
2010-02-27—Публикация
2008-10-24—Подача