Изобретение относится к физиологически активным соединениям и может быть использовано в медицинской практике для лечения онкологических заболеваний как в качестве самостоятельного лекарственного средства, так и в композиции с известными препаратами.
Известно, что цисплатин (Цис-Диаминдихлорплатина (2+)) (коммерческие синонимы: Платидиам, Platidiam, Platinol) широко используется на практике для химиотерапии онкологических больных. Цисплатин представляет собой кристаллический порошок от желтого до желто-оранжевого цвета, который медленно и очень мало растворим в воде и изотоническом растворе хлорида натрия (Машковский М.Д. Лекарственные средства, изд. 12-е. - М.: Медицина, 1992, стр.523-524).
Несмотря на плохую растворимость соединения в воде и водных растворах, основной способ применения цисплатина при терапии - внутривенно. Для этого препарат растворяют из расчета 10 мг сухого вещества на 10 мл стерильной воды для инъекций, и этот раствор разводят в 1 л изотонического раствора натрия хлорида или 5% раствора глюкозы. Для увеличения растворимости цисплатина перед введением раствор рекомендуется предварительно подогреть до температуры 30-36 градусов Цельсия. Раствор вводят струйно (медленно) или в виде длительных инфузий (в течение 6-48 ч).
Известен способ получения цис-диаминдихлордигидроксоплатины (4+) из цис-диаминдихлорплатины (2+) путем обработки суспензии цисплатина 30%-ной перекисью водорода при 60-80°С с последующим отделением твердого остатка (SU 1137698 А1, Желиговская Н.Н. и др., 17.10.1983). Показано, что при проведении химических превращений встраиваемые гидроксигруппы не затрагивают стерического размещения хлор- и аминогрупп.
Также известны производные цисплатина, где один из лигандов замещен на другой биогенный лиганд с целью понижения общей токсичности цисплатина (US6548541, Shaw, 15.04.2003; US7160908, Shaw, 09.01.2007) и создания его растворимой формы (RU2151740 С1, Желиговская Н.Н. и др., 27.06.2000).
Задачей настоящего изобретения является разработка ранее неизвестного комплексного соединения цисплатина (двухвалентной платины), а именно комплекса цис-диаминдихлорплатины (2+) с гидразидом изоникотиновой кислоты (изониазид), отличающегося более высокой растворимостью и пониженной токсичностью, что позволяет отказаться от стадии лиофилизации в процессе получения лекарственной формы и облегчает ее использование, и способа его получения.
Новое комплексное соединение является производным цисплатина (цис-диаминдихлорплатина) формулы: Pt(NH3)2Cl2·2L, где L=INH (изониазид, гидразид изоникотиновой кислоты).
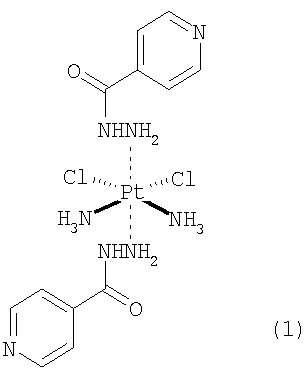
Для получения соединения (1) одну часть цисплатина смешивают с 2 частями изониазида, находящегося в растворе, при температуре раствора в диапазоне 50-80°С при постоянном перемешивании в течение 48 часов до образования гомогенного раствора. Полученное соединение фильтруют через стандартный микробиологический фильтр с размерами пор 0.22 мкм для очистки от нерастворимых фракций.
Патентуемое комплексное соединение является новым, в литературе не описано, не известен и способ его получения.
Ниже приводится детальное описание способа получения патентуемого соединения - комплексного соединения цис-диаминдихлорплатины (2+) с гидразидом изоникотиновой кислоты.
Приготовили раствор 0.274 г (0.002 моль) гидразида изоникотиновой кислоты в 5 мл воды. Полученный раствор нагревали до температуры 50°С и добавили к нему 0.300 г (0.001 моль) цис-диаминдихлороплатины (2+). После смешения реагентов реакционную смесь перемешивали 48 часов при 50°С. Полученный раствор фильтровали через стандартный микробиологический фильтр с размерами пор 0.22 мкм (фирмы Миллипоре). Полученный фильтрат концентрировали в вакууме. Получено 0.563 г (98%) вещества в виде стеклообразной пленки светло-желтого цвета. Комплекс растворим в воде, что значительно упрощает работу с ним на биообъектах, и это является техническим результатом группы изобретений.
Строение и состав полученного комплексного соединения были доказаны методами УФ- и ЯМР-спектроскопии и элементного анализа, а полученные спектры приведены на фиг.1-6:
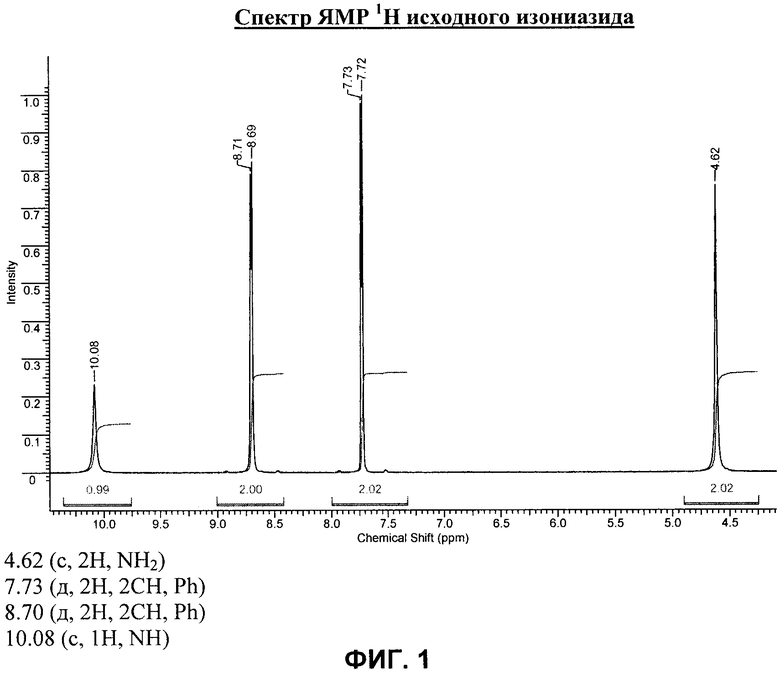
на фиг.1 представлен спектр ЯМР 1Н исходного изониазида;
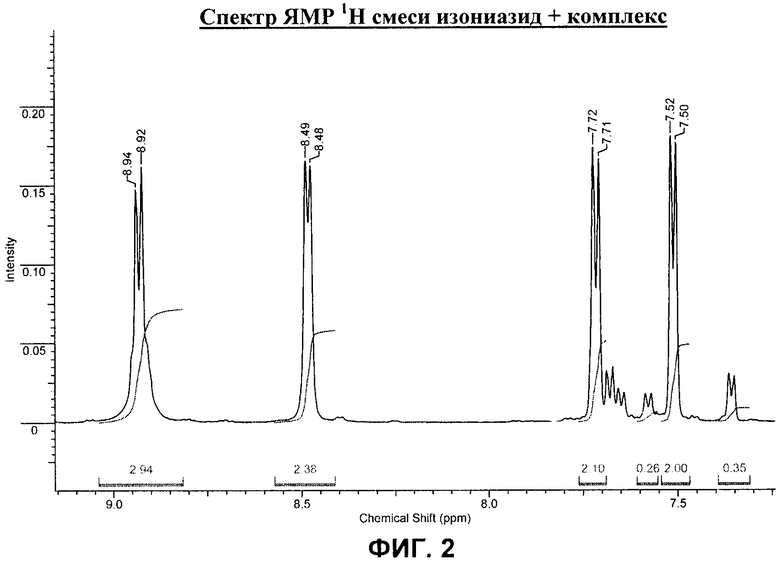
на фиг.2 - спектр ЯМР 1Н смеси изониазид + комплекс;
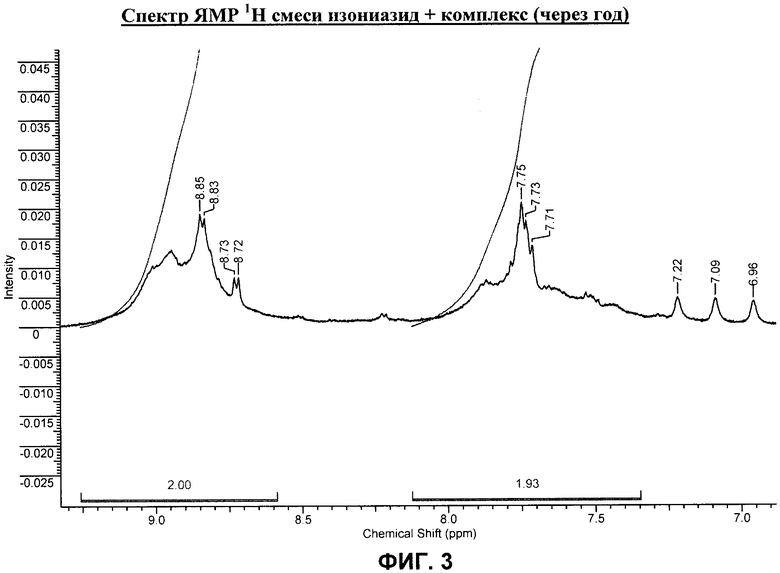
на фиг.3 - спектр ЯМР 1Н смеси изониазид + комплекс (через год);
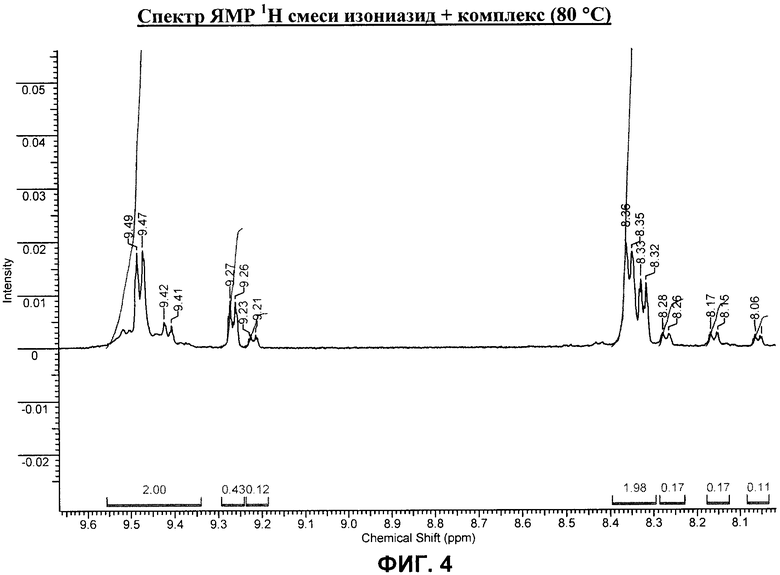
на фиг.4 - спектр ЯМР 1Н смеси изониазид + комплекс (80°С);
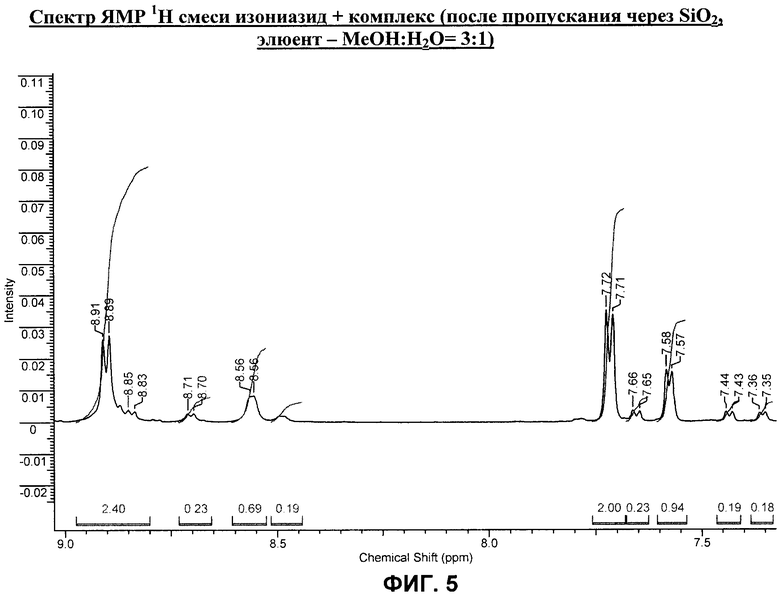
на фиг.5 - спектр ЯМР 1Н смеси изониазид + комплекс (после пропускания через SiO2, элюент - МеОН:Н2O 3:1);
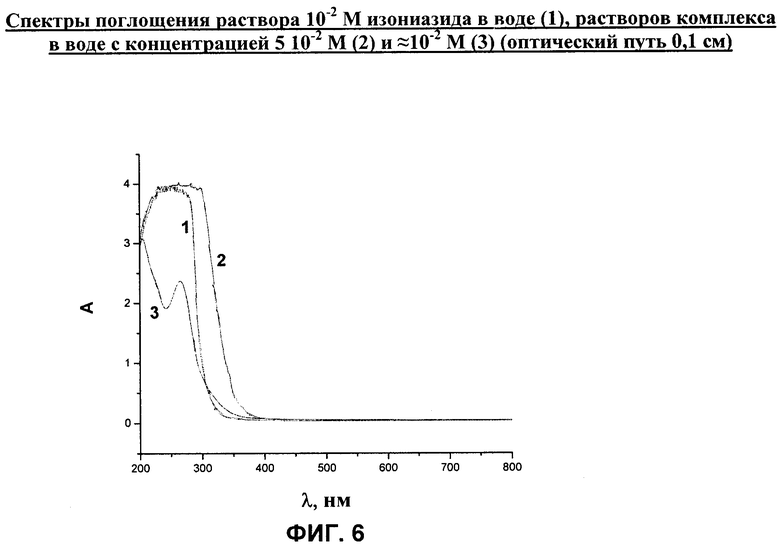
на фиг.6 - спектры поглощения раствора 10-2 М изониазида в воде (кривая 1), растворов комплекса в воде с концентрацией 5·10-2 М (кривая 2) и ≈10-2 М (кривая 3) (оптический путь 0,1 см).
Видно, что в спектре ЯМР 1Н полученного комплекса по сравнению со спектром исходного изониазида наблюдается смещение сигналов ароматических протонов в более слабое поле, что указывает на образование нового соединения. Величина константы спин-спинового взаимодействия составляет 6.3 Гц, что на 1 Гц больше, чем у исходного лиганда.
Стабильность комплекса была подтверждена сохранением ЯМР-спектра после выдерживания раствора комплекса в течение года, нагревания раствора с комплексом до 80°С и после пропускания раствора комплекса через колонку с селикагелем (SiO2), элюент - СН3OН:Н2O=3:1. Последнее показывает возможность дополнительной очистки получаемого комплекса.
Элементный анализ.
C12H20Cl2N8O2Pt
Найдено 1(%): С 25.48; Н 3.96; Сl 16.13; N 12.80; Pt 32.29;.
Найдено 2(%): С 25.18; Н 3.70; Сl 14.00; N 14.86; Pt 33.01;.
Вычислено (%): С 25.09; Н 3.48; Сl 12.37; N 19.51; Pt 33.97.
Таким образом, предлагаемый способ получения соединения формулы (1) позволяет достичь цели изобретения и получить ранее неизвестное водорастворимое комплексное соединение цисплатина, а именно комплекс цис-диаминдихлорплатины (2+) с гидразидом изоникотиновой кислоты. Полученное соединение может быть использовано в медицинской практике как в качестве самостоятельного противоопухолевого и антиметастатического лекарственного средства, так и в композиции с уже известными препаратами.
Испытания на острую токсичность проводили путем внутрибрюшинного введения раствора препарата мышам линии BDFi. В качестве препарата сравнения использовался исходный цисплатин. Испытания показали, что заявляемый комплекс при расчете на количество введенной платины обладает в несколько раз меньшей токсичностью по сравнению с исходным цисплатином, при этом активность в отношении всех видов испытанных опухолей, на которые действует цисплатин, сохраняется такой же или возрастает.
Эти данные доказывают, что физиологическая активность цисплатина, связанного в комплекс, в отношении опухолевых процессов практически не изменилась, острая токсичность снизилась, а удобство использования при терапии значительно возросло.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ТЕТРАХЛОРИДА ПЛАТИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2245328C1 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИС-ДИАМИНОПЛАТИНЫ (II) С СОПОЛИМЕРОМ NA-СОЛИ МАЛЕИНОВОЙ КИСЛОТЫ И ФУРАНА, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ, С ШИРОКИМ ИНТЕРВАЛОМ ТЕРАПЕВТИЧЕСКИХ ДОЗ ПРИ НИЗКОЙ НЕФРОТОКСИЧНОСТИ | 1990 |
|
RU2033998C1 |
| НОВЫЙ КОМПЛЕКС ПЛАТИНЫ (IV) | 2016 |
|
RU2695357C1 |
| ПИРИДИНОИЛГИДРАЗОНЫ ДИАЛКИЛ(2-МЕТИЛ-4-ОКСОПЕНТ-2-ИЛ) ФОСФИНОКСИДОВ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2498990C1 |
| ИЗОНИКОТИНОИЛГИДРАЗИД ЦИТРАКОНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ | 2000 |
|
RU2183625C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТОВ ГЕПАРИНА | 2005 |
|
RU2298406C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТОВ АЛЬГИНОВОЙ КИСЛОТЫ | 2005 |
|
RU2283848C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО КОНЪЮГАТА ГИДРАЗОНА ИЗОНИКОТИНОВОЙ КИСЛОТЫ | 2010 |
|
RU2454226C1 |
| ОКСОВАНАДИЕВЫЙ КОМПЛЕКС С ГЛИЦИНОМ, ПРОЯВЛЯЮЩИЙ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ | 2007 |
|
RU2341528C1 |
| ИЗОНИКОТИНОИЛГИДРАЗИД ФТАЛЕВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ | 2002 |
|
RU2228753C2 |
Изобретение относится к получению физиологически активных соединений, в частности к новому водорастворимому комплексу цис-диаминодихлорплатины (2+) с гидразидом изоникотиновой кислоты формулы Pt(NH3)2Cl2·2L, где L=INH - изониазид, гидразид изоникотиновой кислоты. Способ получения указанного комплекса заключается во взаимодействии цис-диаминодихлорплатины (2+) с гидразидом изоникотиновой кислоты с последующим выделением целевого продукта. Предложенное соединение может быть использовано в медицинской практике как аналог цисплатина по терапевтическому действию, но в более удобной для применения форме вследствие его повышенной растворимости и пониженной токсичности. Кроме того, предложенное соединение расширяет ассортимент водорастворимых противоопухолевых и антиметастатических препаратов. 2 н. и 1 з.п. ф-лы, 6 ил.
1. Водорастворимый комплекс цис-[диаминодихлорплатины (2+)] с гидразидом изоникотиновой кислоты формулы (1)
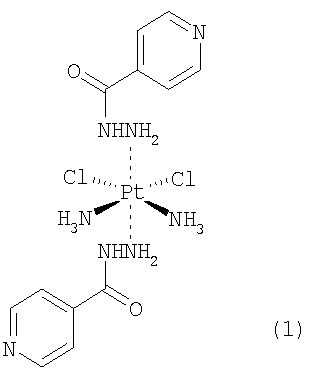
2. Способ получения водорастворимого комплекса общей формулы 1 по п.1, характеризующийся тем, что обработку цис-диаминодихлорплатины (2+) проводят при температуре 50-80°С раствором гидразида изоникотиновой кислоты при мольном соотношении цис-диаминодихлорплатина (2+) / гидразид изоникотиновой кислоты, равном 1:2, с последующим отделением нерастворимого остатка и выделением целевого продукта.
3. Способ по п.2, характеризующийся тем, что сначала готовят 0,4 молярный водный раствор гидразида изоникотиновой кислоты, нагревают его до температуры 50°С и добавляют 0,001 моля цис-диаминодихлорплатины (2+) с получением реакционной смеси, затем реакционную смесь перемешивают при температуре 50-80°С в течение 48 ч и фильтруют, а полученный фильтрат концентрируют в вакууме с выделением целевого продукта.
Авторы
Даты
2010-06-10—Публикация
2008-05-19—Подача