Изобретение относится к медицинской технике.
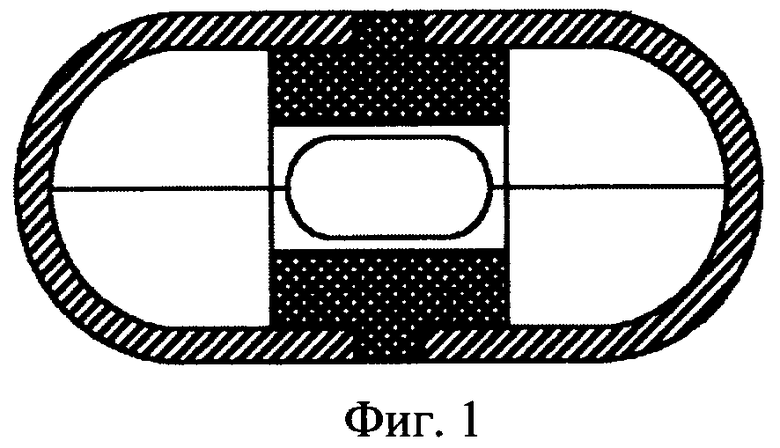
Достижения науки и техники множат лечебные возможности медицины. Одним из примеров, подтверждающих такую взаимосвязь, является терапия желудочно-кишечного тракта (ЖКТ) путем электрической стимуляции его моторно-эвакуационного механизма. Техника такой терапии известна с конца 19-го века, однако не имела широкого признания до 80-х годов 20-го века, когда был изобретен автономный электронный стимулятор желудочно-кишечного тракта (АЭС ЖКТ), получивший неофициальное название «кремлевская таблетка» [АС №936931, СССР, кл. A61N 1/36. Заявлено 25.01.1980]. Известный АЭС ЖКТ (далее для сокращения - стимулятор) выполнен в виде обтекаемой травмобезопасной капсулы, состоящей из проводящих половин корпуса, разделенных и изолированных друг от друга диэлектрической втулкой (фиг.1). Активный элемент стимулятора - автономный полупроводниковый генератор прямоугольных видео - или радиоимпульсов расположен в корпусе и соединен биполярно с его половинами, являющимися, таким образом, электродами. Автономность устройству обеспечивает расположенный в корпусе же источник питания - гальванический элемент. Размеры, форма и состояние поверхности стимулятора соответствуют условию незатруднительного проглатывания и самостоятельного передвижения его в ЖКТ естественным образом.
Устройство начинает работать после его проглатывания и погружения в кислотно-щелочную среду ЖКТ. При этом межэлектродный промежуток шунтируется проводимостью окружающей электролитной среды желудка - кишечника, автоматически подсоединяя источник питания и включая, тем самым, генератор импульсов. Импульсное электрическое поле межэлектродного промежутка воздействует на стенку кишечника, стимулируя или восстанавливая биопотенциалы управления режима бегущей волны перистальтики. Перистальтическое сокращение гладкой мускулатуры кишечника продвигает пищевой ком и стимулятор в дистальном направлении, к новому участку ЖКТ. На участках патологического сужения просвета кишки, например, вследствие пареза стимулятор замедляет движение, увеличивая время восстановительного воздействия. Электрический ресурс устройства согласован с временем его пребывания в ЖКТ, которое в норме всего процесса пищеварения составляет 20-24 часа.
Известно усовершенствованное устройство, с большей эффективностью и спектром лечебного воздействия [Патент РФ №2212257]. Имея в своей основе вышеуказанный аналог (АЭС ЖКТ), оно дополнительно снабжено объемными элементами из проницаемо-пористого никелида титана, распределенными в виде покрытия корпуса или локализованными в углублениях, заподлицо с поверхностью. Последние служат в качестве депо длительной резорбции помещаемых в них лекарственных средств. Перед работой объемы пропитывают показанным лекарственным средством и вводят в действие перорально. При продвижении по ЖКТ стимулятор действует штатно, а резорбируемые лекарственные средства усиливают лечебный эффект либо расширяют функции устройства за счет лечения сочетанной патологии. Скорость резорбции лекарственных средств определяется структурой пористого никелида титана, депонирующего жидкость: пористостью и размером сквозных пор, вязкостью жидкости, капиллярными силами. Практически процесс резорбции для данной жидкости неуправляем: неуправляема скорость резорбции и, следовательно, время действия и длина обслуживаемого участка ЖКТ. С точки зрения широты функциональных возможностей данное свойство является недостатком устройства, которое по наибольшему сходству технической сущности выбрано в качестве прототипа предлагаемого изобретения.
Технический результат предлагаемого изобретения - пролонгация и регулирование скорости резорбции лекарственных средств.
Указанный технический результат достигается тем, что в устройстве для лечения соматических заболеваний, содержащем автономный электростимулятор желудочно-кишечного тракта с размещенными на его поверхности депо лекарственных средств, указанные депо выполнены в виде углублений в корпусе автономного электростимулятора, прикрытых, каждое, гидропроницаемой диафрагмой из никелида титана.
Предпочтительно выполнение гидропроницаемой диафрагмы из проницаемо-пористого никелида титана.
Предпочтительно выполнение гидропроницаемой диафрагмы из проволочной никелид-титановой сетки.
Достижимость технического результата обусловлена наличием препятствия для транспорта лекарственного средства из объема депо наружу - в кишку. К имеющимся факторам, определяющим интенсивность резорбции в устройстве-прототипе, добавляется еще один - диффузия через гидропроницаемую диафрагму. Скорость диффузии зависит от проницаемости диафрагмы, которая определяется интегральной площадью просветов: пор в пористо-проницаемом материале или ячеек плетеной сетки. Подбирая эти параметры для конкретного лекарственного средства и необходимого времени резорбции, можно варьировать лекарственное действие вплоть до пролонгации его на все время пребывания устройства в ЖКТ. При этом лекарственная форма депонируемого средства может быть любая из существующих: жидкая, гелеобразная, твердая.
Возможен дополнительный регулирующий фактор - заполнение депо пористым никелидом титана в виде агрегатированного объема, как это имеет место в устройстве-прототипе, или разрозненных гранул. Армирование лекарственного средства инородными включениями снижает скорость резорбции, пролонгирует синергическую химиотерапию стимулятора.
Выбор материала диафрагмы - никелид титана - существенно важен благодаря высокой биосовместимости и необходимыми для данной ситуации капиллярными свойствами, обеспечивающими заданную скорость и время резорбции. Технологическая возможность варьирования пористостью и размером пор никелида титана позволяет подбирать структуру материала под резорбционные свойства используемого препарата при условии пролонгации его действия на нужной длине ЖКТ. Частным примером структуры гидропроницаемой диафрагмы может быть текстильная сетка, технология и производство которой к настоящему времени освоены. Сетка имеет преимущество по сравнению с листовым пористо-проницаемым никелид-титановым материалом в строгой заданности просветов отдельных ячеек и, следовательно, в большей контролируемости резорбции. Вариация плотности текстуры сетки позволяет изменять гидропроницаемость ее в широком диапазоне.
Форма гидропроницаемой диафрагмы соответствует форме депо лекарственных средств и может варьироваться от пространных оболочек по поверхности распределенного депо до локализованных укрытий сосредоточенных объемов. Конструктивные возможности проницаемых листовых никелид-титановых материалов достаточны для широкого выбора проектов этой детали.
Указанные приемы управления пролонгацией резорбции лекарственных средств неизвестны из уровня данной техники, что свидетельствует о соответствии предложения критерию «изобретательский уровень».
На иллюстрациях представлено:
Фиг.1. Автономный электронный стимулятор желудочно-кишечного тракта. Схема разреза.
Фиг.2. Автономный электронный стимулятор желудочно-кишечного тракта, снабженный депо лекарственных препаратов. Внешний вид.
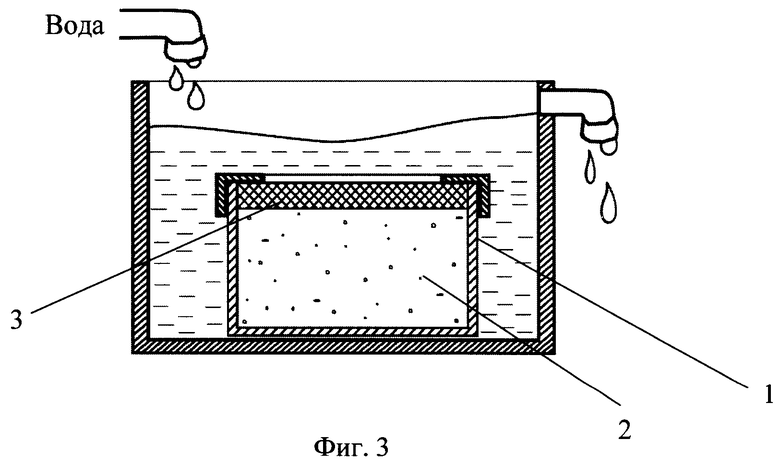
Фиг.3. Лабораторный макет устройства для проверки эффекта пролонгации резорбции лекарственных средств:
1 - контейнер, 2 - депо лекарственных средств, 3 - гидропроницаемая диафрагма.
Фиг.4. График насыщения депо лекарственным средством.
Фиг.5. График резорбции лекарственных средств:
4 - резорбция из незакрытого депо,
5 - резорбция с однослойной сетчатой диафрагмой,
6 - резорбция с трехслойной сетчатой диафрагмой.
Доказательством достижимости технического результата служит экспериментальная проверка эффекта управления скоростью резорбции, выполненная на макете депо лекарственных средств из проницаемо-пористого никелида титана (фиг.3). Устройство представляет собой цилиндрический уплощенный широкодонный контейнер 1, заполненный проницаемо-пористым никелидом титана 2 с рандомизированной пористостью около 50% и размерами пор, распределенными в интервале 10-500 мкм. В качестве химического резорбируемого препарата, моделирующего лекарственное средство, выбран, по ряду технических причин, химически чистый СаСО3 (известняк). Контейнер 1 для полупроницаемой гидроизоляции закрыт съемной диафрагмой 3, выполненной из тканой никелид-титановой сетки с размером ячейки 180 мкм. Модель предлагаемого устройства по ходу двухэтапного эксперимента действует следующим образом.
1. Смоделированное депо заполняют известняком путем окунания в раствор соли до полного пропитывания пор и последующего активного испарения влаги при подогреве всего макета. Процесс повторяют до насыщения, что фиксируют взвешиванием образца и анализом формы (пологий участок) графика (фиг.4). В эксперименте заполнение пор солью завершено к 9-10 циклу указанных действий.
2. Устройство с загруженным депо помещают в растворитель, в данном эксперименте - проточную воду, и фиксируют резорбцию соли по факту снижения веса всего образца через фиксированные промежутки времени. Резорбцию наблюдают до заметного снижения веса.
Скорость уменьшения веса образца характеризует рабочую длительность резорбции - основной критерий эксперимента. Для подтверждения технического результата произведено сравнение уменьшения веса в макетах с одно- и трехслойной сетчатой диафрагмами (кривые 5 и 6) и с непрекрытым депо (кривая 4). Константой эксперимента выбрано время резорбции - 47 часов. Результаты эксперимента свидетельствуют о снижении скорости уменьшения веса образца, т.е. о пролонгации процесса резорбции депонированной соли и управляемости им путем введения защиты депо диафрагмой (кривые 5, 6 по сравнению с кривой 4). Достигнутое время резорбции - около 2-х суток - конкретизировано для выбранного резорбируемого препарата - известняка и указанных характеристик депо и диафрагм.
Вариацией структуры материала и толщиной диафрагмы можно изменять время резорбции, подбирая его необходимое значение по медицинским показаниям, по резорбционным свойствам лекарственного средства в любом его состоянии: жидком, гелеобразном, твердом. Конструктивные особенности гидропроницаемой диафрагмы диктуются конструкцией депо используемого стимулятора, характеристиками лекарственного средства и должны подбираться при подготовке устройства к действию. В рамках заявленной общности устройство готово к «промышленной применимости».
| название | год | авторы | номер документа |
|---|---|---|---|
| СТИМУЛЯТОР ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2001 |
|
RU2212257C2 |
| КРИОАППЛИКАТОР | 2013 |
|
RU2580037C2 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЗАБОЛЕВАНИЙ | 2004 |
|
RU2285548C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ КАРКАСА ГРУДИНЫ ПРИ СТЕРНОМЕДИАСТИНИТАХ | 2012 |
|
RU2489097C1 |
| РЕГУЛЯТОР РОСТА КЛЕТОК IN VITRO И СПОСОБ РЕГУЛЯЦИИ РОСТА КЛЕТОК IN VITRO | 2000 |
|
RU2179578C2 |
| СРЕДСТВО ДЛЯ ФИКСАЦИИ СОЕДИНЯЕМЫХ В ХОДЕ ХИРУРГИЧЕСКОГО ВМЕШАТЕЛЬСТВА ТКАНЕЙ ОРГАНИЗМА | 2015 |
|
RU2614211C2 |
| ВНУТРИКОСТНЫЙ ШТИФТ | 2015 |
|
RU2604390C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОВЕРХНОСТНЫХ РАНЕНИЙ СЕЛЕЗЕНКИ | 2007 |
|
RU2337632C1 |
| СПОСОБ ФОРМИРОВАНИЯ КОМПРЕССИОННО-КЛАПАННОГО ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА | 2005 |
|
RU2296518C1 |
| ШОВНЫЙ МАТЕРИАЛ | 2015 |
|
RU2614212C2 |



Изобретение относится к медицинской технике, а именно к устройствам для терапии желудочно-кишечного тракта. Устройство содержит автономный электронный стимулятор желудочно-кишечного тракта с размещенным на его поверхности депо лекарственных средств в виде углублений в корпусе стимулятора. Дополнительно углубления прикрыты гидропроницаемой диафрагмой из никелида титана. Использование изобретения позволяет регулировать скорость резорбции лекарственных средств. 2 з.п. ф-лы, 5 ил.
1. Устройство для лечения соматических заболеваний, содержащее автономный электронный стимулятор желудочно-кишечного тракта с размещенным на его поверхности депо лекарственных средств, отличающееся тем, что депо лекарственных средств выполнено в виде углублений в корпусе стимулятора, прикрытых гидропроницаемой диафрагмой из никелида титана.
2. Устройство по 1, отличающееся тем, что гидропроницаемая диафрагма выполнена из проницаемо-пористого никелида титана.
3. Устройство по 1, отличающееся тем, что гидропроницаемая диафрагма выполнена из проволочной никелид-титановой сетки.
| СТИМУЛЯТОР ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2001 |
|
RU2212257C2 |
| Устройство для резки известковых камней | 1937 |
|
SU53161A1 |
| RU 2005127045 A, 27.02.2006 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| US 5170801 A, 15.12.1992. | |||
Авторы
Даты
2010-07-10—Публикация
2008-09-30—Подача